Modelowanie molekularne
|
|
|
- Dorota Socha
- 5 lat temu
- Przeglądów:
Transkrypt
1 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 7
2 Podstawowe idee i metody chemii kwantowej: Funkcja falowa, gęstość elektronowa; równanie Schrodingera; Teoria Funkcjonałów Gęstości (DFT); przyblienie Borna-Oppenheimera, zasada wariacyjna w mechanice kwantowej i w DFT, przyblienie jednoelektronowe; metoda HF; korelacja elektronowa; metody korelacyjne oparte na funkcji falowej; metoda Kohna-Shama Dane do obliczeń kwantowo-chemicznych; GAMESS: Geometria czasteczki; macierz Z; bazy funkcyjne w obliczeniach ab initio ; input/output programu GAMESS Struktura geometryczna układów molekularnych: Optymalizacja geometrii; optymalizacja z wiazami; analiza konformacyjna; problem minimum globalnego Struktura elektronowa układów molekularnych: Orbitale molekularne, orbitale KS; wiazanie chemiczne; gęstość różnicowa; orbitale zlokalizowane; analiza populacyjna; analiza rzędów wiązań Analiza wibracyjna; Wielkości termodynamiczne; Reaktywność chemiczna: Analiza wibracyjna; wielkosci termodynamiczne; modelowanie reakcji chemicznych; optymalizacja geometrii stanu przejściowego, IRC; indeksy reaktywności chemicznej, molekularny potencjał elektrostatyczny, funkcja Fukui ego i teoria orbitali granicznych; jedno- i dwu-reagentowe indeksy reaktywności Inne zagadnienia: Metody hybrydowe QM/MM; modelowanie wielkich układów; efety rozpuszczalnika; modelowanie w katalizie homo- i heterogenicznej; oddziaływania międzycząsteczkowe, i. in.
3 Struktura elektronowa
4 Ładunki atomów w i rzędy wiąza zań nawiązują do tradycyjnie używanych w chemii pojeć nie są obserwablami rożne metody obliczania ładunków na atomach i rzędów wiązań zależność uzyskanych wartości od metody i bazy funkcyjnej
5 Ładunki atomów w i rzędy wiąza zań Intuicyjne definicje : ładunek atomu = ładunek jądra - populacja elektronowa atomu ( ilość elektronów na atomie ) rząd wiązania = ilość par elektronowych wiążących dwa wybrane atomy [jak we wzorach strukturalnych cząsteczek]; ilość par elektronowych w obszarach pomiędzy atomami H C H 1 2 C H H H 1 C 3 C H
6 Ładunki atomów w i rzędy wiąza zań niejednoznaczność podziału gęstości cząsteczki pomiędzy tworzące ją atomy i wiązania chemiczne wynika z niejednoznaczności definicji atomu w cząsteczce
7 Ładunki atomów i rzędy wiązań niejednoznaczność podziału gęstości cząsteczki pomiędzy tworzące ją atomy i wiązania chemiczne wynika z niejednoznaczności definicji atomu w cząsteczce Gęstość elektronowa w benzenie
8 Ładunki atomów i rzędy wiązań alternatywne definicje atomów w cząsteczce oparte na podziale cząsteczki na atomy w przestrzeni fizycznej lub w przestrzeni funkcyjnej (poprzez funkcje bazy) N A = ρ (r )dr A ρ (r ) = ρ[χ A, χ B,...](r ) Gęstość elektronowa w benzenie
9 Analiza populacyjna Analiza populacyjna Mullikena (baza nieortogonalna)
10 Analiza populacyjna Analiza populacyjna Analiza populacyjna Löwdina (baza ortogonalizowana) ( ) q p q p s p s p s p q q p p p s p s q q p P P P P r N,, 1 p 1,, 1 1, ) ( 1/2 PS 1/2 S = = + = = = = = = = ρ = α α α p Z Q p
11 Analiza populacyjna Analiza populacyjna Analiza populacyjna Mullikena
12 Teoria AIM Badera (Atoms in Molecules) podział gęstości elektronowej w przestrzeni fizycznej w oparciu o pochodne i punkty krytyczne gęstości elektronowej. R.F.W. Bader, Theory of Atoms in Molecules
13 Teoria AIM Badera (Atoms in Molecules) R.F.W. Bader, Theory of Atoms in Molecules
14 Analiza populacyjna Analiza populacyjna Analiza Hirshfelda w przestrzeni fizycznej, ale bez podziału przestrzeni pomiędzy poszczególne atomy każdy punkt przestrzeni należy po cześci do każdego atomu pojecie promolekuły: molekuła złożona z nieoodziaływających atomów umieszczonych w pozycjach takich jak w molekule
15 Analiza populacyjna Analiza Hirshfelda w przestrzeni fizycznej, ale bez podziału przestrzeni pomiędzy poszczególne atomy każdy punkt przestrzeni należy po cześci do każdego atomu pojecie promolekuły: molekuła złożona z nieoodziaływających atomów umieszczonych w pozycjach takich jak w molekule r A B
16 Analiza populacyjna Analiza Hirshfelda w przestrzeni fizycznej, ale bez podziału przestrzeni pomiędzy poszczególne atomy każdy punkt przestrzeni należy po cześci do każdego atomu pojecie promolekuły: molekuła złożona z nieoodziaływających atomów umieszczonych w pozycjach takich jak w molekule r ρ Α 0 (r) ρ Β 0 (r) A B
17 Analiza populacyjna Analiza Hirshfelda w przestrzeni fizycznej, ale bez podziału przestrzeni pomiędzy poszczególne atomy każdy punkt przestrzeni należy po cześci do każdego atomu pojecie promolekuły: molekuła złożona z nieoodziaływających atomów umieszczonych w pozycjach takich jak w molekule r ρ 0 (r) = ρ Α 0 (r) + ρ Β 0 (r) ρ Α 0 (r) ρ Β 0 (r) A B
18 Analiza populacyjna Analiza Hirshfelda w przestrzeni fizycznej, ale bez podziału przestrzeni pomiędzy poszczególne atomy każdy punkt przestrzeni należy po cześci do każdego atomu pojecie promolekuły: molekuła złożona z nieoodziaływających atomów umieszczonych w pozycjach takich jak w molekule r ρ 0 (r) = ρ Α 0 (r) + ρ Β 0 (r) ρ Α 0 (r) ρ Β 0 (r) A B Udział atomu X w gestości promolekuły: w X (r) = ρ X 0 (r) / ρ 0 (r)
19 Analiza populacyjna Analiza Hirshfelda w przestrzeni fizycznej, ale bez podziału przestrzeni pomiędzy poszczególne atomy każdy punkt przestrzeni należy po cześci do każdego atomu pojecie promolekuły: molekuła złożona z nieoodziaływających atomów umieszczonych w pozycjach takich jak w molekule ρ Α 0 (r) A r ρ 0 (r) = ρ Α 0 (r) + ρ Β 0 (r) ρ Β 0 (r) B Molekularna gęstość el. ρ(r) w kazdym punkcie dzielona pomiędzy atomy n X (r) = w X (r) ρ(r) Udział atomu X w gestości promolekuły: w X (r) = ρ X 0 (r) / ρ 0 (r)
20 Analiza populacyjna Analiza Hirshfelda w przestrzeni fizycznej, ale bez podziału przestrzeni pomiędzy poszczególne atomy każdy punkt przestrzeni należy po cześci do każdego atomu pojecie promolekuły: molekuła złożona z nieoodziaływających atomów umieszczonych w pozycjach takich jak w molekule r ρ 0 (r) = ρ Α 0 (r) + ρ Β 0 (r) ρ Α 0 (r) A ρ Β 0 (r) B Molekularna gęstość el. ρ(r) w kazdym punkcie dzielona pomiędzy atomy n X (r) = w X (r) ρ(r) Udział atomu X w gestości promolekuły: w X (r) = ρ X 0 (r) / ρ 0 (r)
21 Analiza populacyjna Analiza Hirshfelda Molekularna gęstość el. ρ(r) w kazdym punkcie dzielona pomiędzy atomy: n X (r) = w X (r) ρ(r); N X = w X (r) ρ(r) dr
22 Analiza populacyjna Analiza Hirshfelda Molekularna gęstość el. ρ(r) w kazdym punkcie dzielona pomiędzy atomy: n X (r) = w X (r) ρ(r); N X = w X (r) ρ(r) dr Zwiazki z teorią informacji: Roman F. Nalewajski i Elżbieta Broniatowska
23 Rzędy wiąza zań nawiązują do tradycyjnie używanych w chemii pojeć (wiązanie pojedyncze, podwójne, itd.) rząd wiązania nie jest obserwablą rożne metody obliczania indeksów krotności wiązań zależność uzyskanych wartości od metody i bazy funkcyjnej H H C C H H H C C H
24 Rzędy wiąza zań intuicyjna definicja w ramach teorii MO b = (n (n n*)/2 n --liczba elektronów na na orbitalach wiążących; n* n* --liczba elektronów na na orb. antywiążących
25 Cząsteczka O 2 z σ 2pz2pz b = 2 2p O1 π 2px2px π 2py2py 2p O2 π 2px2px π 2py2py σ 2pz2pz σ 2s2s 2s O1 2s O2 σ 2s2s σ 1s1s 1s O1 1s O2 σ 1s1s
26 Rzędy wiąza zań intuicyjna definicja w ramach teorii MO b = (n (n n*)/2 n --liczba elektronów na na orbitalach wiążących; n* n* --liczba elektronów na na orb. antywiążących trudna do do stosowania w cząsteczkach wieloatomowych z silnie zdelokalizowanymi orbitalami molekularnymi
27 Rzędy wiąza zań elementy macierzy P (tzw. macierz rzedów wiązań i ładunków ( charge and bond-order-matrix, CBO matrix) T P = CnC Uzyskane wartości nie odpowiadają intuicyjnym (wiązanie pojedyncze, podwójne, itp.) Coulson, 1939
28 Rzędy wiąza zań definicja Wiberga kwadraty P ( ) b AB = P ab a A b B 2 Wiberg. K. Tetrahedron, 1968, 24, 1093.
29 Rzędy wiąza zań definicja Wiberga kwadraty P ( ) b AB = P ab a A b B 2 - metody półempirtyczne - kwadraty P - wagi przy przyczynkach do energiii wymiennej ex 1 EAB = P 2 abγ ab 2 a A b B Wiberg. K. Tetrahedron, 1968, 24, 1093.
30 Rzędy wiąza zań definicja Wiberga kwadraty P CNDO: ( ) b AB = P ab a A b B 2
31 Rzędy wiąza zań definicja Gopinathana i Juga (G-J) ( ) b AB = P ab a A b C ( S 1/2 PS 1/2 ) p q P p, q =, 2 - metody ab initio - definicja pokrewna do Wiberga- w ortogonalizowanej bazie AO Gopinathan M.S.; Jug, K. Theoret. Chim. Acta 1983, 63, 497.
32 Rzędy wiąza zań Mayer bab = ( PS) ( ) ab PS a A b C ba - metody ab initio - definicja pokrewna do Wiberga- w nieortogonalnej bazie Mayer, I. Chem. Phys. Lett. 1984, 97, 270.
33 Rzędy wiąza zań Wiberg, Gopinathan-Jug, Mayer - atom określony przez zbiór funkcji bazy scentrowanych na tym atomie - silna zalezność od bazy funkcyjnej (jak dla analizy populacyjnej) - problemy z układami opartymi na metalach przejściowych (wymagajacymi duzych baz)
34 Rzędy wiąza zań Teoria wartosciowości chemicznej Nalewajskiego i Mrozka Nalewajski, R.F.; Koster, A. M.; Jug K. Theor. Chim. Acta 1993, 85, 463. Nalewajski, R.F.; Mrozek, J.; Formosinho, S. J.; Varandas, A. J. C. International Journal of Quantum Chemistry 1994, 52, Nalewajski, R.F.; Mrozek, J. International Journal of Quantum Chemistry 1994, 51, 187. Nalewajski, R.F.; Mrozek, J. International Journal of Quantum Chemistry 1996, 57, 377. Nalewajski, R.F.; Mrozek, J.; Mazur, G. Can. J. Chem. 1996, 74, Nalewajski, R.F.; Mrozek, J.; Michalak, A. International Journal of Quantum Chemistry 1997, 61, 589. Nalewajski, R.F.; Mrozek, J.; Michalak, A. Polish J. Chem 1998, 72, R.F. Nalewajski Podstawy i metody chemii kwantowej. PWN 2001.
35 Rzędy wiąza zań Nalewajski i Mrozek (IJQC, 1994, 51, 187)
36 Rzędy wiąza zań (N-M) Wartościowość chemiczna wielkość różnicowa; okreslająca zmiany w przyczynkach kwadratowych do elementów diagonalnych w parach dwu-elektronowej w molekule w stosunku do promolekuły Γ (2) = Γ({ 2 P νµ }) Nalewajski, R.F.; Mrozek, J. International Journal of Quantum Chemistry 1994, 51, 187
37 Rzędy wiąza zań (N-M) Wartościowość chemiczna wielkość różnicowa; okreslająca zmiany w przyczynkach kwadratowych do elementów diagonalnych w parach dwu-elektronowej w molekule w stosunku do promolekuły
38 Rzędy wiąza zań (N-M) Indeksy wartościowości: V V i A c A = A A 2 a = { } 2 1 β aa aa 2 ( ) ( α ) 2 n + P + ( P ) A A [ ( ) ( ) ] α 2 β 2 P aa' + P aa' a< a' V V i AB c AB = = n A A a B b n b [( ) ( ) ] α 2 β 2 P + P ab ab Nalewajski, R.F.; Mrozek, J. International Journal of Quantum Chemistry 1994, 51, 187
39 Rzędy wiąza zań (N-M) Indeksy wartościowości: V V i A c A = A A 2 a = { } 2 1 β aa aa 2 ( ) ( α ) 2 n + P + ( P ) A A [ ( ) ( ) ] α 2 β 2 P aa' + P aa' a< a' V V i AB c AB = = n A A a B b n b [( ) ( ) ] α 2 β 2 P + P ab ab Całkowita wartościowośc: V = A V A + V A B AB Nalewajski, R.F.; Mrozek, J. International Journal of Quantum Chemistry 1994, 51, 187
40 Rzędy wiąza zań (N-M) V V i A c A = A A 2 a = { aa aa } 1 β 2 α 2 2 ( n ) + ( P ) + ( P ) A A α 2 β 2 [ ( P aa' ) + ( P aa ' ) ] a< a' V V i AB c AB = = n A n b A B α 2 β 2 [( Pab ) + ( Pab ) ] a b Rzędy wiązań z indeksów wartościowości: V = A B b AB Nalewajski, R.F.; Mrozek, J.; Mazur, G. Can. J. Chem. 1996, 74, Nalewajski, R.F.; Mrozek, J.; Michalak, A. International Journal of Quantum Chemistry 1997, 61, 589. Nalewajski, R.F.; Mrozek, J.; Michalak, A. Polish J. Chem 1998, 72, 1779.
41 Rzędy wiąza zań (N-M) V V i A c A = A A 2 a = { aa aa } 1 β 2 α 2 2 ( n ) + ( P ) + ( P ) A A α 2 β 2 [ ( P aa' ) + ( P aa ' ) ] a< a' V V i AB c AB = = n A n b A B α 2 β 2 [( Pab ) + ( Pab ) ] a b Rzędy wiązań z indeksów wartościowości: V = A B b AB b AB c i AB c i AB c = V + V + wa ( V + V ) + wb ( VB + V AB AB A A i B ) Nalewajski, R.F.; Mrozek, J.; Mazur, G. Can. J. Chem. 1996, 74, Nalewajski, R.F.; Mrozek, J.; Michalak, A. International Journal of Quantum Chemistry 1997, 61, 589. Nalewajski, R.F.; Mrozek, J.; Michalak, A. Polish J. Chem 1998, 72, 1779.
42 Rzędy wiąza zań (N-M) V V i A c A = A A 2 a = { aa aa } 1 β 2 α 2 2 ( n ) + ( P ) + ( P ) A A α 2 β 2 [ ( P aa' ) + ( P aa ' ) ] a< a' V V i AB c AB = = n A n b A B α 2 β 2 [( Pab ) + ( Pab ) ] a b Rzędy wiązań z indeksów wartościowości: V = A B b AB b AB c i AB c i AB c = V + V + wa ( V + V ) + wb ( VB + V AB AB A A Nalewajski, R.F.; Mrozek, J.; Mazur, G. Can. J. Chem. 1996, 74, Nalewajski, R.F.; Mrozek, J.; Michalak, A. International Journal of Quantum Chemistry 1997, 61, 589. Nalewajski, R.F.; Mrozek, J.; Michalak, A. Polish J. Chem 1998, 72, ) i B c XY XY w = V / X Z V c XZ
43 Rzędy wiąza zań (N-M) związane z prawdopodobieństwami dwulektronowymi podejście róznicowe dobrze zdefiniowany atomowy układ odniesienia uwzględniają przyczynki kowalencyjne i i jonowe wymagają obliczeń dla izolowanych atomów (( dla promolekuły)
44 Rzędy wiąza zań (N-M) Molekuła / baza C 2 H 2 SZ B C-C 2.98 B C-H 0.99 DZP, frozen core C 2 H 4 SZ DZP, frozen core C 2 H 6 SZ DZP, frozen core
45 Rzędy wiąza zań (N-M) Molecule/Basis C 2 H 2 SZ B C-C 2.98 (2.99) B C-H 0.99 (0.99) DZP, frozen core C 2 H 4 SZ 2.02 (2.02) 0.98 (0.97) DZP, frozen core C 2 H 6 SZ 1.03 (1.01) 0.99 (0.98) DZP, frozen core N-M b.o (Mayer b.o.)
46 Rzędy wiąza zań (N-M) Molecule/Basis C 2 H 2 SZ B C-C 2.98 (2.99) B C-H 0.99 (0.99) DZP, frozen core 2.83 (2.23) 1.04 (1.04) C 2 H 4 SZ 2.02 (2.02) 0.98 (0.97) DZP, frozen core 1.89 (1.67) 0.98 (1.01) C 2 H 6 SZ 1.03 (1.01) 0.99 (0.98) DZP, frozen core 1.01 (0.91) 0.96 (0.99) N-M b.o (Mayer b.o.)
47 Rzędy wiąza zań (N-M) Molecule/Basis C 2 H 2 SZ B C-C 2.98 (2.99) B C-H 0.99 (0.99) DZP, frozen core 2.83 (2.23) 1.04 (1.04) C 2 H 4 SZ 2.02 (2.02) 0.98 (0.97) DZP, frozen core 1.89 (1.67) 0.98 (1.01) C 2 H 6 SZ 1.03 (1.01) 0.99 (0.98) DZP, frozen core 1.01 (0.91) 0.96 (0.99) N-M: słabszy wpływ bazy N-M b.o (Mayer b.o.)
48 Rzędy wiąza zań (N-M) Molecule/Basis C 6 H 6 SZ B C-C 1.44 (1.43) B C-H 0.97 (0.96) DZP, frozen core 1.38 (1.24) 0.97 (1.04) N-M b.o (Mayer b.o.)
49 Rzędy wiąza zań (N-M) NaCl :
50 Rzędy wiąza zań (N-M) NaCl : N-M: 1.10 G-J: 0.36 Mayer: 0.54
51 Rzędy wiąza zań (N-M) H-Kr-C C-H: L. Kriatchev et al. JACS, 2003,125, 6875.
52 Rzędy wiąza zań (N-M) H-Kr-C C-H: N-M Mayer H-Kr: Kr-C: C-C: C-H:
53 Tlenek węgla: CO N-M: G-J: Mayer: 2.162
54 Tlenek wegla Układ Konfiguracja v CO Rząd wiązania CO CO + CO* (5σ) (5σ) (5σ) (2π 1 ) 1489,
55 Monokarbonylki metali przejściowych Zhou, M; Andrews, L.; Bauschlicher, C.W., Chem. Rev. 2001, 101, 1931.
56 Monokarbonylki metali przejściowych 2,8 2,7 MCO + C-O bond order 2,6 2,5 2,4 2,3 2,2 MCO MCO - 2,1 Sc Ti V Cr Mn Fe Co Ni Cu
57 Monokarbonylki metali przejściowych 2,8 2,7 MCO + C-O bond order 2,6 2,5 2,4 2,3 2,2 MCO MCO - 2,1 Sc Ti V Cr Mn Fe Co Ni Cu
58 Karbonylki metali przejściowych Kompleks v CO Rząd wiązania CO d 10 Ni(CO) [Co(CO) 4 ] [Fe(CO) 4 ]
59 Karbonylki metali przejściowych Kompleks v CO Rząd wiązania CO d 10 d 6 Ni(CO) [Co(CO) 4 ] [Fe(CO) 4 ] [Mn(CO) 6 ] Mo(CO) Cr(CO) [V(CO) 6 ]
60 Karbonylki metali przejściowych CO Bond Order 2,7 2,6 2,5 2,4 2,3 2,2 2,1 V(CO) 6 - Fe(CO) 4 2- Co(CO) 4 - Mo(CO) 6 Cr(CO) 6 Mn(CO) 6 + Ni(CO) v CO [cm -1 ]
61 Karbonylki metali przejściowych Fosfiny, Ni(CO) 3 R R Rzad wiązania CO P(CH 3 ) P(C 6 H 5 ) P(OCH 3 ) P(OC 6 H 5 ) P(Cl) P(F) CO 2.520
62 Wpływ trans ligandu Cl Cl NH 3 Ni NH 3 NH 3 Ni Cl Cl NH 3
63 NH 3 R 2+ Ni R NH 3 trans - influence R H CN Cl OH CO Rząd wiązania Ni-N
64 Kompleksy CrO n Cl 4-n wiązanie Cr-O Complex v (Cr-O) b (Cr-O) [CrO 4 ] 2-846, [CrO 3 Cl] - 907, [CrO 2 Cl 2 ] 984, [CrOCl 3 ] * 2.14 * Cr(O)Cl (TPP) value 2,3 [CrOCl 3 ] + M-O bond order 2,1 1,9 1,7 [CrO 4 ] 2- [CrO 3 Cl] - [CrO 2 Cl 2 ] 1, v M-O [1/cm]
65 O Powierzchnia (010) - MoO A Mo O 1.73A O O 1.68A 1.94 A Dł wiązania 1.94 A 2.33A O O Model klastrowy Mo 7 O 30 H 18 BALSAC plot A. Michalak, K. Hermann, M. Witko, Surf. Sci., 366 (1996) K. Hermann, A. Michalak, M. Witko, Catalysis Today, 32 (1996), K. Hermann, M. Witko, A. Michalak, Catalysis Today, 50 (1999)
66 O Powierzchnia (010) - MoO A Mo O 1.73A O Dł wiązań O 1.68A 1.94 A 1.94 A 2.33A O O 0.26 O O Rz. wiązań O O Mo O O Model klastrowy Mo 7 O 30 H 18 A. Michalak, K. Hermann, M. Witko, Surf. Sci., 366 (1996) K. Hermann, A. Michalak, M. Witko, Catalysis Today, 32 (1996), K. Hermann, M. Witko, A. Michalak, Catalysis Today, 50 (1999)
67 Cr2
68 Cr2 - wiązanie sześciokrotne σ Contour 0.3 Contour 0.05 π π MO δ δ σ
69 Cr2 - wiązanie sześciokrotne σ π π MO δ Contour 0.3 Rząd wiązania: N-M: 6.01 δ σ
70 cdn
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne
 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 10 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 10 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Rzędy wiązań chemicznych
 Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Modelowanie molekularne
 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 2 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 2 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Modelowanie molekularne
 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 13 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 13 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Cząsteczki. 1.Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? Jakie sąs. typy wiąza
 Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
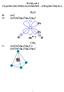 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Dotyczy to zarówno istniejących już związków, jak i związków, których jeszcze dotąd nie otrzymano.
 Chemia teoretyczna to dział chemii zaliczany do chemii fizycznej, zajmujący się zagadnieniami związanymi z wiedzą chemiczną od strony teoretycznej, tj. bez wykonywania eksperymentów na stole laboratoryjnym.
Chemia teoretyczna to dział chemii zaliczany do chemii fizycznej, zajmujący się zagadnieniami związanymi z wiedzą chemiczną od strony teoretycznej, tj. bez wykonywania eksperymentów na stole laboratoryjnym.
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Spis treści. Metoda VSEPR. Reguły określania struktury cząsteczek. Ustalanie struktury przestrzennej
 Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej jedną z dwóch metod (teorii): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Inżynieria Biomedyczna. Wykład XII
 Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Analizy populacyjne i rzedy
 Rzedy Analizy populacyjne i rzedy Kraków, 30 listopada 2005 Analizy populacyjne i rzedy O czym mówimy? Analizy populacyjne Rzedy Informacje wst epne Podzia l populacji mi edzy orbitale atomowe Rozk lad
Rzedy Analizy populacyjne i rzedy Kraków, 30 listopada 2005 Analizy populacyjne i rzedy O czym mówimy? Analizy populacyjne Rzedy Informacje wst epne Podzia l populacji mi edzy orbitale atomowe Rozk lad
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450
 Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
TEORIA ORBITALI MOLEKULARNYCH (MO) dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Wykład 16: Atomy wieloelektronowe
 Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Entropowe indeksy wiązań chemicznych na gruncie teorii informacji
 UNIWERSYTET JAGIELLOŃSKI WYDZIAŁ CHEMII PRACA MAGISTERSKA Entropowe indeksy wiązań chemicznych na gruncie teorii informacji Dariusz Szczepanik Praca wykonana w Zakładzie Metod Obliczeniowych Chemii pod
UNIWERSYTET JAGIELLOŃSKI WYDZIAŁ CHEMII PRACA MAGISTERSKA Entropowe indeksy wiązań chemicznych na gruncie teorii informacji Dariusz Szczepanik Praca wykonana w Zakładzie Metod Obliczeniowych Chemii pod
Ligand to cząsteczka albo jon, który związany jest z jonem albo atomem centralnym.
 138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 5 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 5 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Wiązania. w świetle teorii kwantów fenomenologicznie
 Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Kierunek i poziom studiów: Chemia. Drugi. Sylabus modułu: Chemia kwantowa i modelowanie molekularne (0310-CH-S2-B-062)
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia. Drugi. Sylabus modułu: Chemia kwantowa i modelowanie molekularne (0310-CH-S2-B-062) 1. Informacje ogólne koordynator modułu dr
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia. Drugi. Sylabus modułu: Chemia kwantowa i modelowanie molekularne (0310-CH-S2-B-062) 1. Informacje ogólne koordynator modułu dr
Analizy populacyjne, ªadunki atomowe
 Dodatek do w. # 3 i # 4 Šadunki atomowe, analizy populacyjne Q A = Z A N A Q A efektywny ªadunek atomu A, Z A N A liczba porz dkowa dla atomu A (czyli ªadunek j dra) efektywna liczba elektronów przypisana
Dodatek do w. # 3 i # 4 Šadunki atomowe, analizy populacyjne Q A = Z A N A Q A efektywny ªadunek atomu A, Z A N A liczba porz dkowa dla atomu A (czyli ªadunek j dra) efektywna liczba elektronów przypisana
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Wykład 3: Atomy wieloelektronowe
 Wykład 3: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 3: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
CZ STECZKA. Do opisu wi za chemicznych stosuje si najcz ciej jedn z dwóch metod (teorii): metoda wi za walencyjnych (VB)
 CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Wiązania kowalencyjne
 Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Ocena aromatyczności cząsteczek w oparciu o orbitale rzędów wiązań
 Seminarium Zakładu Chemii Teoretycznej i Zakładu Metod Obliczeniowych Chemii Ocena aromatyczności cząsteczek w oparciu o orbitale rzędów wiązań dr Dariusz Szczepanik Zakład Chemii Teoretycznej Kraków 2015
Seminarium Zakładu Chemii Teoretycznej i Zakładu Metod Obliczeniowych Chemii Ocena aromatyczności cząsteczek w oparciu o orbitale rzędów wiązań dr Dariusz Szczepanik Zakład Chemii Teoretycznej Kraków 2015
Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały
 WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
Wiązania chemiczne z teorii informacji Fishera
 praca magisterska Wiązania chemiczne z teorii informacji Fishera Piotr de Silva Praca wykonana w Zakładzie Metod Obliczeniowych Chemii pod kierunkiem dr hab. Janusza Mrozka 2008 Panu dr hab. Januszowi
praca magisterska Wiązania chemiczne z teorii informacji Fishera Piotr de Silva Praca wykonana w Zakładzie Metod Obliczeniowych Chemii pod kierunkiem dr hab. Janusza Mrozka 2008 Panu dr hab. Januszowi
Teoria funkcjonału gęstości
 Teoria funkcjonału gęstości Łukasz Rajchel Interdyscyplinarne Centrum Modelowania Matematycznego i Komputerowego Uniwersytet Warszawski lrajchel1981@gmail.com Wykład dostępny w sieci: http://tiger.chem.uw.edu.pl/staff/lrajchel/
Teoria funkcjonału gęstości Łukasz Rajchel Interdyscyplinarne Centrum Modelowania Matematycznego i Komputerowego Uniwersytet Warszawski lrajchel1981@gmail.com Wykład dostępny w sieci: http://tiger.chem.uw.edu.pl/staff/lrajchel/
Lokalizacja Orbitali Molekularnych
 Lokalizacja Orbitali Molekularnych Regionalnie Zlokalizowane Orbitale Molekularne Marek Giebułtowski Seminarium magisterskie w Zakładzie Chemii Teoretycznej UJ Spis Treści 1 Przegład Metod Lokalizacyjnych
Lokalizacja Orbitali Molekularnych Regionalnie Zlokalizowane Orbitale Molekularne Marek Giebułtowski Seminarium magisterskie w Zakładzie Chemii Teoretycznej UJ Spis Treści 1 Przegład Metod Lokalizacyjnych
Podstawy teoretyczne i moŝliwości aplikacyjne kwantowej teorii atomów w cząsteczkach - QTAIM
 Podstawy teoretyczne i moŝliwości aplikacyjne kwantowej teorii atomów w cząsteczkach - QTAIM 7..15 Wrocławskie Centrum Sieciowo-Superkomputerowe Chemia klasyczna wstęp molekuła = atomy + wiązania Chemia
Podstawy teoretyczne i moŝliwości aplikacyjne kwantowej teorii atomów w cząsteczkach - QTAIM 7..15 Wrocławskie Centrum Sieciowo-Superkomputerowe Chemia klasyczna wstęp molekuła = atomy + wiązania Chemia
Teoria VSEPR. Jak przewidywac strukturę cząsteczki?
 Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Struktura elektronowa czasteczek. przybliżenie Borna-Oppenheimera. równania Schrödingera dla elektronów przy ustalonym po lożeniu jader
 Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych
 1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Chemia I Semestr I (1 )
 1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
zaprezentowana w 1940 roku (Sidgwick i Powell). O budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu
 Teoria VSEPR (Valence Shell Electron Pair Repulsion) zaprezentowana w 1940 roku (Sidgwick i Powell). budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu centralnego
Teoria VSEPR (Valence Shell Electron Pair Repulsion) zaprezentowana w 1940 roku (Sidgwick i Powell). budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu centralnego
Przybli»one metody uwzgl dniania rozpuszczalnika. Šadunki atomowe
 Przybli»one metody uwzgl dniania rozpuszczalnika. Šadunki atomowe Dodatek do w. # 4 14 kwietnia 2015 Przybli»one metody uwzgl dniania rozpuszczalnika Dotychczasowe obliczenia kwantowochemiczne przeprowadzali±my
Przybli»one metody uwzgl dniania rozpuszczalnika. Šadunki atomowe Dodatek do w. # 4 14 kwietnia 2015 Przybli»one metody uwzgl dniania rozpuszczalnika Dotychczasowe obliczenia kwantowochemiczne przeprowadzali±my
H H 2.5 < H H CH 3 N O O H C N ŁADUNEK FORMALNY. 2.5 dla atomu węgla C C 2.5 H 2.1. Li 1.0. liczba e - walencyjnych w atomie wolnym C 2.5 H 2.
 .5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
.5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
( ) ρ ( ) ( ) ( ) ( ) ( ) Rozkład ładunku i momenty dipolowe cząsteczek. woda H 2 O. aceton (CH 3 ) 2 CO
 Rozkład ładunku i momenty dipolowe cząsteczek W fizyce klasycznej moment dipolowy układu ładunków oblicza się tak: i i i ( ) ρ ( ) µ = q r lub µ = ρ x, y, z r dxdydz = x, y, z r dv W teorii kwantowej moment
Rozkład ładunku i momenty dipolowe cząsteczek W fizyce klasycznej moment dipolowy układu ładunków oblicza się tak: i i i ( ) ρ ( ) µ = q r lub µ = ρ x, y, z r dxdydz = x, y, z r dv W teorii kwantowej moment
Elementy teorii powierzchni metali
 prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
Elektroujemność w konwencji Sandersona. mgr Magdalena Chrzan
 Elektroujemność w konwencji Sandersona mgr Magdalena Chrzan Elektroujemność Siła atomu w cząsteczce do przyciągania elektronów do siebie. Pauling 1932, 1960 Zdolność atomu do przyciągania gęstości elektronowej
Elektroujemność w konwencji Sandersona mgr Magdalena Chrzan Elektroujemność Siła atomu w cząsteczce do przyciągania elektronów do siebie. Pauling 1932, 1960 Zdolność atomu do przyciągania gęstości elektronowej
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Budowa atomu. Wiązania chemiczne
 strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
Chemia Ogólna wykład 1
 Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Chemia teoretyczna I Semestr V (1 )
 1/ 6 Chemia Chemia teoretyczna I Semestr V (1 ) Osoba odpowiedzialna za przedmiot: dr hab. inż. Aleksander Herman. 2/ 6 Wykład Program Podstawy mechaniki kwantowej Ważne problemy modelowe Charakterystyka
1/ 6 Chemia Chemia teoretyczna I Semestr V (1 ) Osoba odpowiedzialna za przedmiot: dr hab. inż. Aleksander Herman. 2/ 6 Wykład Program Podstawy mechaniki kwantowej Ważne problemy modelowe Charakterystyka
1. Przesłanki doświadczalne mechaniki kwantowej.
 1 Pytania egzaminacyjne: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny- interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest liczba wybijanych elektronów
1 Pytania egzaminacyjne: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny- interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest liczba wybijanych elektronów
Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
Załącznik Nr 5 do Zarz. Nr 33/11/12
 Załącznik Nr 5 do Zarz. Nr 33/11/12 Z1-PU7 WYDANIE N1 Strona 1 z 5 (pieczęć wydziału) KARTA PRZEDMIOTU 1. Nazwa przedmiotu: CHEMIA TEORETYCZNA 2. Kod przedmiotu: - 3. Karta przedmiotu ważna od roku akademickiego:
Załącznik Nr 5 do Zarz. Nr 33/11/12 Z1-PU7 WYDANIE N1 Strona 1 z 5 (pieczęć wydziału) KARTA PRZEDMIOTU 1. Nazwa przedmiotu: CHEMIA TEORETYCZNA 2. Kod przedmiotu: - 3. Karta przedmiotu ważna od roku akademickiego:
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oarciu o koncecję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncecja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oarciu o koncecję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncecja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
1,2 1,2. WYMAGANIA WSTĘPNE W ZAKRESIE WIEDZY, UMIEJĘTNOŚCI I INNYCH KOMPETENCJI 1. Brak
 Zał. nr 4 do ZW 33/01 WYDZIAŁ Podstawowych Problemów Techniki KARTA PRZEDMIOTU Nazwa w języku polskim Podstawy Chemii Ogólnej Nazwa w języku angielskim General Chemistry Kierunek studiów (jeśli dotyczy):
Zał. nr 4 do ZW 33/01 WYDZIAŁ Podstawowych Problemów Techniki KARTA PRZEDMIOTU Nazwa w języku polskim Podstawy Chemii Ogólnej Nazwa w języku angielskim General Chemistry Kierunek studiów (jeśli dotyczy):
Fizyka atomowa r. akad. 2012/2013
 r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru
 1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru 2. Na podstawie struktury cząsteczek wyjaśnij dlaczego N 2 jest bierny a Cl 2 aktywny chemicznie? 3. Które substancje posiadają budowę
1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru 2. Na podstawie struktury cząsteczek wyjaśnij dlaczego N 2 jest bierny a Cl 2 aktywny chemicznie? 3. Które substancje posiadają budowę
Struktura elektronowa
 Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Chemia Grudzień Styczeń
 Chemia Grudzień Styczeń Klasa VII IV. Łączenie się atomów. Równania reakcji chemicznych 1. Wiązania kowalencyjne 2. Wiązania jonowe 3. Wpływ rodzaju wiązania na właściwości substancji 4. Elektroujemność
Chemia Grudzień Styczeń Klasa VII IV. Łączenie się atomów. Równania reakcji chemicznych 1. Wiązania kowalencyjne 2. Wiązania jonowe 3. Wpływ rodzaju wiązania na właściwości substancji 4. Elektroujemność
UKŁAD OKRESOWY PIERWIASTKÓW
 UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
Konwersatorium 1. Zagadnienia na konwersatorium
 Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
ZWIĄZKI KOMPLEKSOWE. dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE Sole podwójne - to sole zawierające więcej niż jeden rodzaj kationów lub więcej niż jeden rodzaj anionów. Należą do nich m. in. ałuny, np. siarczan amonowo-żelazowy(ii),
ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE Sole podwójne - to sole zawierające więcej niż jeden rodzaj kationów lub więcej niż jeden rodzaj anionów. Należą do nich m. in. ałuny, np. siarczan amonowo-żelazowy(ii),
ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE
 ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE Sole podwójne - to sole zawierające więcej niż jeden rodzaj kationów lub więcej niż jeden rodzaj anionów. Należą do nich m. in. ałuny, np. ałun glinowo-potasowy K 2 Al
ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE Sole podwójne - to sole zawierające więcej niż jeden rodzaj kationów lub więcej niż jeden rodzaj anionów. Należą do nich m. in. ałuny, np. ałun glinowo-potasowy K 2 Al
Wewnętrzna budowa materii - zadania
 Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
1. Budowa atomu. Układ okresowy pierwiastków chemicznych
 Wymagania programowe z chemii na poszczególne oceny IV etap edukacyjny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 1. podręcznika dla liceum ogólnokształcącego
Wymagania programowe z chemii na poszczególne oceny IV etap edukacyjny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 1. podręcznika dla liceum ogólnokształcącego
S. Baran - Podstawy fizyki materii skondensowanej Wiązania chemiczne w ciałach stałych. Wiązania chemiczne w ciałach stałych
 Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
MARATON WIEDZY CHEMIA CZ. II
 MARATON WIEDZY CHEMIA CZ. II 1. Podaj liczbę elektronów, nukleonów, protonów i neuronów zawartych w następujących atomach: a), b) 2. Podaj liczbę elektronów, nukleonów, protonów i neutronów zawartych w
MARATON WIEDZY CHEMIA CZ. II 1. Podaj liczbę elektronów, nukleonów, protonów i neuronów zawartych w następujących atomach: a), b) 2. Podaj liczbę elektronów, nukleonów, protonów i neutronów zawartych w
TEORIA FUNKCJONA LÓW. (Density Functional Theory - DFT) Monika Musia l
 TEORIA FUNKCJONA LÓW GȨSTOŚCI (Density Functional Theory - DFT) Monika Musia l PRZEDMIOT BADAŃ Uk lad N elektronów + K j ader atomowych Przybliżenie Borna-Oppenheimera Zamiast funkcji falowej Ψ(r 1,σ 1,r
TEORIA FUNKCJONA LÓW GȨSTOŚCI (Density Functional Theory - DFT) Monika Musia l PRZEDMIOT BADAŃ Uk lad N elektronów + K j ader atomowych Przybliżenie Borna-Oppenheimera Zamiast funkcji falowej Ψ(r 1,σ 1,r
Chemia kwantowa. Pytania egzaminacyjne. 2010/2011: 1. Przesłanki doświadczalne mechaniki kwantowej.
 1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Świat chemii cz. 1, rok szkolny 2016/17 Opis założonych osiągnięć ucznia
 Świat chemii cz. 1, rok szkolny 2016/17 Opis założonych osiągnięć ucznia Osiągnięcia podstawowe Rodzaje i przemiany materii wymienia powtarzające się elementy podręcznika i wskazuje rolę, jaką odgrywają;
Świat chemii cz. 1, rok szkolny 2016/17 Opis założonych osiągnięć ucznia Osiągnięcia podstawowe Rodzaje i przemiany materii wymienia powtarzające się elementy podręcznika i wskazuje rolę, jaką odgrywają;
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 3 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy Poziom przedmiotu Symbole efektów kształcenia Symbole efektów dla obszaru kształcenia Symbole efektów kierunkowych
1 3 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy Poziom przedmiotu Symbole efektów kształcenia Symbole efektów dla obszaru kształcenia Symbole efektów kierunkowych
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia. Monika Musia l
 STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia Monika Musia l Uk lad zamkniȩtopow lokowy: N elektronów; N 2 elektronowa: Ψ = 1 N! orbitali. Funkcja falowa N- φ 1 (1)α(1)
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia Monika Musia l Uk lad zamkniȩtopow lokowy: N elektronów; N 2 elektronowa: Ψ = 1 N! orbitali. Funkcja falowa N- φ 1 (1)α(1)
SPIS TREŚCI 1. PODSTAWOWE POJĘCIA CHEMII. MASA ATOMOWA I CZĄSTECZKOWA... 3
 PRZEDMOWA DO WYDANIA PIĄTEGO.................................. 1 PRZEDMOWA DO WYDANIA SZÓSTEGO................................ 2 1. PODSTAWOWE POJĘCIA CHEMII. MASA ATOMOWA I CZĄSTECZKOWA... 3 1.1. Zadania
PRZEDMOWA DO WYDANIA PIĄTEGO.................................. 1 PRZEDMOWA DO WYDANIA SZÓSTEGO................................ 2 1. PODSTAWOWE POJĘCIA CHEMII. MASA ATOMOWA I CZĄSTECZKOWA... 3 1.1. Zadania
