Wyniki procedur na mocy art. 20 rozporządzenia (WE) nr 726/2004 oraz art. 31 dyrektywy 2001/83/WE
|
|
|
- Edward Sowiński
- 7 lat temu
- Przeglądów:
Transkrypt
1 28 lutego 2013 r. EMA/136606/2013 wer.1 EMEA/H/A-31/1333 EMEA/H/C/000604/A20/45 EMEA/H/C/000622/A20/60 EMEA/H/C/000674/A20/52 Pytania i odpowiedzi dotyczące ponownej oceny monowalentnych i poliwalentnych szczepionek przeciwko odrze, nagminnemu zapaleniu przyusznic, różyczce i/lub ospie Wyniki procedur na mocy art. 20 rozporządzenia (WE) nr 726/2004 oraz art. 31 dyrektywy 2001/83/WE W dniu 13 grudnia 2012 r. Europejska Agencja Leków dokonała ponownej oceny stosowania mono- i poliwalentnych (MMRV) w czasie ciąży oraz u pacjentów z niedoborami odporności (osłabieniem układu odpornościowego). Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) działający przy Agencji uznał, że w dalszym ciągu należy unikać stosowania tych szczepionek w czasie ciąży, ale przypadkowe zaszczepienie kobiety w ciąży przy użyciu szczepionki przeciwko odrze, nagminnemu zapaleniu przyusznic i/lub różyczce nie powinno stanowić wskazania do przerwania ciąży. Dodatkowo stosowania szczepionek MMRV należy w dalszym ciągu unikać w przypadku pacjentów z najcięższymi typami osłabienia układu odpornościowego, ale ich stosowanie można rozważyć w przypadku mniej poważnych niedoborów odporności. Komitet zalecił również wprowadzenie pewnych zmian do informacji o produkcie w celu objaśnienia zagrożeń i koniecznych środków ostrożności. Co to są szczepionki MMRV? Szczepionki MMRV są pomocne w ochronie organizmu przed zakażeniami wirusami odry, nagminnego zapalenia przyusznic, różyczki, a także ospy (który może wywołać ospę wietrzną lub półpasiec). Zawierają one żywe, atenuowane (osłabione) postaci wirusów wywołujących te choroby. Szczepionki MMRV mogą być dostępne jako osobne szczepionki przeciwko poszczególnym chorobom (monowalentne) lub jako szczepionki skojarzone (poliwalentne). Poliwalentne szczepionki M-M-RVAXPRO i ProQuad oraz monowalentna szczepionka przeciwko półpaścowi Zostavax zostały dopuszczone do obrotu na terenie Unii Europejskiej (UE) w drodze 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom Telephone +44 (0) Facsimile +44 (0) info@ema.europa.eu Website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 procedury scentralizowanej. Inne mono- i poliwalentne szczepionki przeciwko odrze, nagminnemu zapaleniu przyusznic, różyczce oraz ospie są dostępne od wielu lat i zostały zatwierdzone w drodze procedur krajowych na terenie państw członkowskich UE pod innymi nazwami handlowymi, w tym jako Amunovax, Priorix, Priorix Tetra, Provarivax, R.O.R. Vax, Rouvax, Trivivac, Varilrix, Varivax i nazwy produktów związanych. Dlaczego dokonano ponownej oceny szczepionek MMRV? Niektóre wirusy u kobiet w ciąży mogą przenikać przez łożysko i zakażać ich nienarodzone dzieci. W szczególności wirus różyczki może powodować wady rozwojowe i problemy głównie z uszami, oczami oraz sercem (znane jako zespół różyczki wrodzonej ), a wirus ospy może powodować wady rozwojowe kończyn (znane jako zespół wrodzonej ospy ) u dzieci, których matki uległy zakażeniu we wczesnej ciąży. Szczepionki MMRV zawierają osłabione, ale żywe wirusy. Choć są one zbyt słabe, aby spowodować problemy zdrowotne u zdrowych osób dorosłych, nie zatwierdzono ich do stosowania u kobiet w ciąży z uwagi na potencjalne ryzyko dla nienarodzonego dziecka, a szczepionym kobietom zaleca się unikanie zajścia w ciążę przez trzy miesiące od momentu szczepienia. Szczepionki MMRV są również przeciwwskazane w przypadku pacjentów z niedoborami odporności, u których szczepionka może nie działać prawidłowo i istnieje potencjalne ryzyko rozwoju poważnej lub rozległej choroby. Jednak od czasu zatwierdzenia tych szczepionek dostępne stały się nowe dane zebrane po wprowadzeniu produktu do obrotu i pochodzące z opublikowanego piśmiennictwa, dotyczące bezpieczeństwa stosowania szczepionek u kobiet w ciąży i pacjentów z niedoborami odporności. W wyniku tego belgijska agencja nadzorująca leki wystąpiła do CHMP z wnioskiem o przeprowadzenie oceny stosunku korzyści do ryzyka stosowania szczepień u tych grup pacjentów i wydanie opinii, czy należy zmienić czy utrzymać przyznane pozwolenia na dopuszczenie do obrotu. W tym samym czasie Komisja Europejska zwróciła się do CHMP z prośbą o rozszerzenie zakresu oceny o produkty dopuszczone do obrotu w drodze procedury scentralizowanej i zbadanie, czy należy zmienić czy utrzymać przyznane tym produktom pozwolenia na dopuszczenie do obrotu. Oceny jakich danych dokonał komitet CHMP? CHMP dokonał ponownej oceny dostępnych danych dotyczących bezpieczeństwa stosowania szczepionek MMRV, uzyskanych po wprowadzeniu produktów do obrotu, a także dostępnych w opublikowanym piśmiennictwie, skupiając się na ryzyku wystąpienia poronienia samoistnego, wewnątrzmacicznego obumarcia płodu, wad rozwojowych, niedojrzałości i niskiej wagi urodzeniowej. Ocena objęła zgłoszenia dotyczące ponad 3500 kobiet, którym we wczesnej ciąży przypadkowo podano szczepionkę przeciwko różyczce, oraz ponad 1800 kobiet, którym w czasie ciąży podano szczepionkę przeciwko ospie. CHMP uwzględnił również dostępne wytyczne Światowej Organizacji Zdrowia. W przypadku pacjentów z niedoborami odporności Komitet ocenił wyniki badań klinicznych oraz zgłoszenia zebrane po wprowadzeniu produktu do obrotu. Jakie są wnioski CHMP? Choć ryzyko nie może zostać całkowicie wykluczone, wśród ponad 5300 zgłoszeń dotyczących kobiet, którym w czasie ciąży przypadkowo podano szczepionkę MMRV, nie wykryto żadnych przypadków zespołu różyczki wrodzonej ani zespołu wrodzonej ospy. Częstość występowania wad wrodzonych lub poronienia samoistnego u kobiet po narażeniu na szczepionki MMRV w czasie ciąży nie EMA/136606/2013 rev1 Strona 2/5
3 była wyższa niż w przypadku kobiet niepoddanych szczepieniu. Jednak dane te, w tym dane z badań kontrolnych niektórych przypadków, nie były dla Komitetu wystarczającym dowodem braku związku zdarzeń niepożądanych ze szczepieniami. Uzyskane dane sugerują natomiast, że nie ma potrzeby opóźniania zajścia w ciążę dłużej niż jeden miesiąc od momentu szczepienia. U pacjentów z poważnymi niedoborami odporności w przypadku podania szczepionek zawierających żywe wirusy istniało ryzyko wystąpienia poważnych działań niepożądanych, ale wg uzyskanych danych u pacjentów z łagodnymi niedoborami odporności, w tym pacjentów zarażonych wirusem HIV z wystarczającą liczbą komórek CD4 (typu białych krwinek pełniących ważną rolę w zwalczaniu zakażeń) we krwi, szczepionki MMRV mogłyby być bezpiecznie stosowane z korzystnym rezultatem. Na podstawie oceny dostępnych danych i dyskusji naukowej Komitet CHMP uznał, że korzyści ze stosowania szczepionek MMRV u kobiet w ciąży oraz pacjentów z poważnymi niedoborami odporności nie przewyższają ryzyka i zalecił utrzymanie przeciwwskazania do stosowania wspomnianych szczepionek u tych grup pacjentów. Jednak kobiety starające się o dziecko muszą opóźnić zajście w ciążę tylko o jeden miesiąc od momentu szczepienia, a przypadkowe zaszczepienie kobiety w ciąży przeciwko różyczce nie stanowi wskazania do przerwania ciąży. Szczepienie może być rozważane u pacjentów z łagodnymi niedoborami odporności, jeśli korzyści ze szczepienia przewyższają ryzyko. (Nie dotyczy to produktu Zostavax, który charakteryzuje się inną mocą dawki i wskazaniami). Należy zaktualizować informacje o produkcie w celu uwzględnienia powyższych zmian. Pełne zmiany dokonane w informacji dla lekarzy i pacjentów dotyczące produktu M-M-RVAXPRO są dostępne tutaj, produktu ProQuad tutaj, produktu Zostavax tutaj, a zmiany dotyczące produktów dopuszczonych do obrotu w drodze procedur krajowych są dostępne tutaj. Jakie są zalecenia dla pacjentów? Kobiety nie powinny otrzymywać mono- ani poliwalentnych szczepionek MMRV w czasie ciąży. Jeśli kobieta jest lub podejrzewa, że jest w ciąży, powinna poinformować o tym lekarza lub pielęgniarkę przed otrzymaniem którejkolwiek z tych szczepionek. Kobiety otrzymujące jedną z tych szczepionek powinny stosować skuteczne środki antykoncepcyjne i unikać zajścia w ciążę przez jeden miesiąc od momentu szczepienia. Jeśli kobieta zajdzie w ciążę w ciągu jednego miesiąca od momentu otrzymania jednej z tych szczepionek, nie oznacza to, że dziecko jest z całą pewnością narażone na ryzyko ani że ciąża powinna zostać przerwana. Nie należy podawać tych szczepionek pacjentom z poważnym osłabieniem układu odpornościowego. W przypadku pacjentów z łagodniejszym osłabieniem odporności szczepienie może być rozważanie, choć nie zawsze pozwoli ono uzyskać taki sam poziom ochrony, jak u osób posiadających w pełni sprawny układ odpornościowy. Z wszelkimi pytaniami należy zgłosić się do lekarza lub farmaceuty. Jakie są zalecenia dla lekarzy przepisujących lek? Stosowanie szczepionek MMRV pozostaje przeciwwskazane u kobiet w ciąży i pacjentów z poważnym niedoborem humoralnej lub komórkowej odpowiedzi odpornościowej (jak w przypadku ciężkich złożonych niedoborów odporności, agammaglobulinemii lub AIDS). EMA/136606/2013 rev1 Strona 3/5
4 Kobietom zaleca się unikanie zajścia w ciążę przez jeden miesiąc od momentu otrzymania szczepionki MMRV. Przypadkowe zaszczepienie z użyciem szczepionki przeciwko różyczce w czasie ciąży nie stanowi wskazania do przerwania ciąży. W przypadku dzieci zakażonych wirusem HIV szczepienie jest przeciwwskazane u pacjentów w wieku poniżej 12 miesięcy, u których odsetek limfocytów CD4+ związany wiekiem wynosi poniżej 25%, u pacjentów w wieku od 12 do 35 miesięcy, u których odsetek limfocytów CD4+ związany wiekiem wynosi poniżej 20%, a także u pacjentów w wieku od 36 do 59 miesięcy, u których odsetek limfocytów CD4+ związany wiekiem wynosi poniżej 15%. Szczepienie może być rozważane u pacjentów z wybranymi niedoborami odporności (np. bezobjawowym zakażeniem wirusem HIV, selektywnymi niedoborami podklasy przeciwciał IgG, wrodzoną neutropenią, przewlekłą ziarniniakowatością oraz niedoborami układu dopełniacza), jeśli korzyści ze szczepienia przewyższają ryzyko. U pacjentów z niedoborami odporności po zaszczepieniu może nie dojść do wykształcenia wystarczającego poziomu odporności i należy ich monitorować pod kątem późniejszego zachorowania na odrę, zapalenie przyusznic, różyczkę lub ospę wietrzną po ekspozycji na te choroby. EMA/136606/2013 rev1 Strona 4/5
5 Dnia 28 lutego 2013 r. Komisja Europejska wydała decyzję na mocy art. 31, dotyczącą szczepionek MMRV. Dnia 27 czerwca 2013 r. Komisja Europejska wydała decyzję w sprawie sprostowania decyzji na mocy art. 31, dotyczącej szczepionek MMRV. Dnia 20 lutego 2013 r. Komisja Europejska wydała decyzję na mocy art. 20, dotyczącą produktu M-M- RVAXPRO. Dnia 18 lutego 2013 r. Komisja Europejska wydała decyzję na mocy art. 20, dotyczącą produktu ProQuad. Dnia 13 lutego 2013 r. Komisja Europejska wydała decyzję na mocy art. 20, dotyczącą produktu Zostavax. Aktualna treść Europejskiego Publicznego Sprawozdania Oceniającego dotyczącego produktu M-M- RVAXPRO znajduje się na stronie internetowej Agencji pod adresem: ema.europa.eu/find medicine/human medicines/european Public Assessment Reports Aktualna treść Europejskiego Publicznego Sprawozdania Oceniającego dotyczącego produktu ProQuad znajduje się na stronie internetowej Agencji pod adresem: ema.europa.eu/find medicine/human medicines/european Public Assessment Reports Aktualna treść Europejskiego Publicznego Sprawozdania Oceniającego dotyczącego produktu Zostavax znajduje się na stronie internetowej Agencji pod adresem: ema.europa.eu/find medicine/human medicines/european Public Assessment Reports EMA/136606/2013 rev1 Strona 5/5
szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana)
 EMA/90006/2015 EMEA/H/C/001104 Streszczenie EPAR dla ogółu społeczeństwa szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana) Niniejszy dokument jest streszczeniem
EMA/90006/2015 EMEA/H/C/001104 Streszczenie EPAR dla ogółu społeczeństwa szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana) Niniejszy dokument jest streszczeniem
czerniak (nowotwór skóry), który rozprzestrzenił się lub którego nie można usunąć chirurgicznie;
 EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Pradaxa jest lekiem zawierającym substancję czynną eteksylan dabigatranu. Lek jest dostępny w postaci kapsułek (75, 110 i 150 mg).
 EMA/47517/2015 EMEA/H/C/000829 Streszczenie EPAR dla ogółu społeczeństwa eteksylan dabigatranu Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego
EMA/47517/2015 EMEA/H/C/000829 Streszczenie EPAR dla ogółu społeczeństwa eteksylan dabigatranu Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego
Simponi jest lekiem o działaniu przeciwzapalnym. Preparat stosuje się w leczeniu następujących chorób u osób dorosłych:
 EMA/411054/2015 EMEA/H/C/000992 Streszczenie EPAR dla ogółu społeczeństwa golimumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
EMA/411054/2015 EMEA/H/C/000992 Streszczenie EPAR dla ogółu społeczeństwa golimumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
zaawansowanym rakiem nerkowokomórkowym, rodzajem raka nerki, u pacjentów, którzy byli wcześniej leczeni lekami przeciwnowotworowymi;
 EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
Poradnik dotyczący interpretacji spontanicznych zgłoszeń przypadków podejrzewanych działań niepożądanych leków
 30 styczeń 2017 r. Wydział ds. inspekcji, nadzoru nad bezpieczeństwem stosowania produktów leczniczych u ludzi i komisji EMA/749446/2016 Zmiana nr 1* Poradnik dotyczący interpretacji spontanicznych zgłoszeń
30 styczeń 2017 r. Wydział ds. inspekcji, nadzoru nad bezpieczeństwem stosowania produktów leczniczych u ludzi i komisji EMA/749446/2016 Zmiana nr 1* Poradnik dotyczący interpretacji spontanicznych zgłoszeń
EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri
 25/04/2016 EMA/266665/2016 EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri U pacjentów z grupy zwiększonego
25/04/2016 EMA/266665/2016 EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri U pacjentów z grupy zwiększonego
Często zadawane pytania (FAQ)
 4 listopada 2011 r. EMA/527628/2011 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków Jeśli nie znajdą tu Państwo odpowiedzi
4 listopada 2011 r. EMA/527628/2011 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków Jeśli nie znajdą tu Państwo odpowiedzi
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
W szpiczaku mnogim, nowotworze pewnego typu białych krwinek zwanych komórkami plazmatycznymi, Revlimid stosuje się:
 EMA/113870/2017 EMEA/H/C/000717 Streszczenie EPAR dla ogółu społeczeństwa lenalidomid Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/113870/2017 EMEA/H/C/000717 Streszczenie EPAR dla ogółu społeczeństwa lenalidomid Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Ograniczenia stosowania leków zawierających domperidon
 1 września 2014 r. EMA/465179/2014 W dniu 23 kwietnia 2014 r. grupa koordynacyjna ds. procedur wzajemnego uznania i zdecentralizowanej produkty stosowane u ludzi (CMDh) zatwierdziła nowe zalecenia o ograniczeniu
1 września 2014 r. EMA/465179/2014 W dniu 23 kwietnia 2014 r. grupa koordynacyjna ds. procedur wzajemnego uznania i zdecentralizowanej produkty stosowane u ludzi (CMDh) zatwierdziła nowe zalecenia o ograniczeniu
Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek przeciwcukrzycowy Suliqua
 19 stycznia 2017 r. EMA/747766/2016 Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek Środki mające na celu zmniejszenie ryzyka pomylenia dwóch wstrzykiwaczy o różnej mocy
19 stycznia 2017 r. EMA/747766/2016 Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek Środki mające na celu zmniejszenie ryzyka pomylenia dwóch wstrzykiwaczy o różnej mocy
Często zadawane pytania (FAQ)
 13 lutego 2017 r. EMA/527628/2011 Rev. 1 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków (EMA). W przypadku nieznalezienia
13 lutego 2017 r. EMA/527628/2011 Rev. 1 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków (EMA). W przypadku nieznalezienia
Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
20 września 2013 r. EMA/564255/2013. 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom
 20 września 2013 r. EMA/564255/2013 Zawieszenie pozwolenia na dopuszczenie do obrotu produktu leczniczego Numeta G13%E i wprowadzenie nowych działań służących zminimalizowaniu ryzyka stosowania produktu
20 września 2013 r. EMA/564255/2013 Zawieszenie pozwolenia na dopuszczenie do obrotu produktu leczniczego Numeta G13%E i wprowadzenie nowych działań służących zminimalizowaniu ryzyka stosowania produktu
Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu
 Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu Zmiany mają przede wszystkim na celu zmniejszenie ryzyka neurologicznych działań niepożądanych Komitet ds. Produktów Leczniczych Stosowanych
Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu Zmiany mają przede wszystkim na celu zmniejszenie ryzyka neurologicznych działań niepożądanych Komitet ds. Produktów Leczniczych Stosowanych
Revolade. eltrombopag. Co to jest Revolade? W jakim celu stosuje się produkt Revolade? Streszczenie EPAR dla ogółu społeczeństwa
 EMA/33466/2016 EMEA/H/C/001110 Streszczenie EPAR dla ogółu społeczeństwa eltrombopag Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/33466/2016 EMEA/H/C/001110 Streszczenie EPAR dla ogółu społeczeństwa eltrombopag Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 25 January 2018 EMA/PRAC/35597/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
25 January 2018 EMA/PRAC/35597/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Przewodnik użytkownika raportu internetowego
 Ochrona zdrowia pacjentów zawiera informacje dotyczące elementów składowych danych, układu, interpretacji i funkcji w raporcie internetowym. 1. Elementy składowe danych... 2 2. Dodatkowe informacje dotyczące
Ochrona zdrowia pacjentów zawiera informacje dotyczące elementów składowych danych, układu, interpretacji i funkcji w raporcie internetowym. 1. Elementy składowe danych... 2 2. Dodatkowe informacje dotyczące
Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie
 22 stycznia 2015 r. EMA/PRAC/63315/2015 Komitet ds. Oceny Ryzyka w ramach Nadzoru nad Bezpieczeństwem Farmakoterapii Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte
22 stycznia 2015 r. EMA/PRAC/63315/2015 Komitet ds. Oceny Ryzyka w ramach Nadzoru nad Bezpieczeństwem Farmakoterapii Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
zaawansowany rak nerki lub rak nerki z przerzutami, w skojarzeniu z interferonem alfa-2a;
 EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
21.04.2016 r., OZiPZ PSSE Opole Lubelskie
 24-30 kwietnia 2016 r. ph DOMKNIJMY LUKĘ W SZCZEPIENIACH! Główny cel inicjatywy: zwiększenie liczby osób zaszczepionych poprzez podniesienie wiedzy i świadomości społeczeństwa na temat znaczenia szczepień
24-30 kwietnia 2016 r. ph DOMKNIJMY LUKĘ W SZCZEPIENIACH! Główny cel inicjatywy: zwiększenie liczby osób zaszczepionych poprzez podniesienie wiedzy i świadomości społeczeństwa na temat znaczenia szczepień
ostrym reumatoidalnym zapaleniem stawów (choroba powodująca stan zapalny stawów), gdzie produkt MabThera podaje się dożylnie z metotreksatem;
 EMA/614203/2010 EMEA/H/C/000165 Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/614203/2010 EMEA/H/C/000165 Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie
 23 April 2015 EMA/PRAC/273915/2015 Pharmacovigilance Risk Assessment Committee Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte na posiedzeniu PRAC w dniach 7 10 kwietnia
23 April 2015 EMA/PRAC/273915/2015 Pharmacovigilance Risk Assessment Committee Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte na posiedzeniu PRAC w dniach 7 10 kwietnia
Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/481361/2018 EMEA/H/C/002392 Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Eylea i w jakim celu się go stosuje Eylea jest lekiem
EMA/481361/2018 EMEA/H/C/002392 Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Eylea i w jakim celu się go stosuje Eylea jest lekiem
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 17 December 2015 EMA/PRAC/835763/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęto w dniach od 30 listopada
17 December 2015 EMA/PRAC/835763/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęto w dniach od 30 listopada
Lek Avastin stosuje się u osób dorosłych w leczeniu następujących rodzajów nowotworów w skojarzeniu z innymi lekami przeciwnowotworowymi:
 EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
 18 października 2012 EMA/653433/2012 EMEA/H/A-5(3)/1319 Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
18 października 2012 EMA/653433/2012 EMEA/H/A-5(3)/1319 Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
PROFILAKTYKA PRZECIW GRYPIE
 PROFILAKTYKA PRZECIW GRYPIE Koordynator profilaktyki : mgr piel. Anna Karczewska CELE: zwiększanie świadomości pacjenta na temat szczepionek przeciwko grypie zapobieganie zachorowań na grypę zapobieganie
PROFILAKTYKA PRZECIW GRYPIE Koordynator profilaktyki : mgr piel. Anna Karczewska CELE: zwiększanie świadomości pacjenta na temat szczepionek przeciwko grypie zapobieganie zachorowań na grypę zapobieganie
EMA potwierdza zalecenia mające na celu zminimalizowanie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri
 26 lutego 2016 EMA/137488/2016 EMA potwierdza zalecenia mające na celu zminimalizowanie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri W przypadku pacjentów narażonych na większe
26 lutego 2016 EMA/137488/2016 EMA potwierdza zalecenia mające na celu zminimalizowanie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri W przypadku pacjentów narażonych na większe
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 15 September 2016 EMA/PRAC/603539/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
15 September 2016 EMA/PRAC/603539/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Keytruda (pembrolizumab)
 EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
zaburzeniem widzenia spowodowanym obrzękiem plamki wywołanym cukrzycą;
 EMA/677928/2015 EMEA/H/C/002392 Streszczenie EPAR dla ogółu społeczeństwa aflibercept Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/677928/2015 EMEA/H/C/002392 Streszczenie EPAR dla ogółu społeczeństwa aflibercept Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Aneks IV. Wnioski naukowe i podstawy do zmiany warunków pozwoleń na dopuszczenie do obrotu
 Aneks IV Wnioski naukowe i podstawy do zmiany warunków pozwoleń na dopuszczenie do obrotu 137 Wnioski naukowe CHMP rozważył poniższe zalecenie PRAC z dnia 5 grudnia 2013 r. odnoszące się do procedury zgodnej
Aneks IV Wnioski naukowe i podstawy do zmiany warunków pozwoleń na dopuszczenie do obrotu 137 Wnioski naukowe CHMP rozważył poniższe zalecenie PRAC z dnia 5 grudnia 2013 r. odnoszące się do procedury zgodnej
Bezpośredni komunikat do fachowych pracowników ochrony zdrowia
 Bezpośredni komunikat do fachowych pracowników ochrony zdrowia Wersja 2, data zatwierdzenia przez URPL: 07.11.2016 Strona 1/7 Acytretyna (Neotigason): poważne ryzyko działania teratogennego oraz ryzyko
Bezpośredni komunikat do fachowych pracowników ochrony zdrowia Wersja 2, data zatwierdzenia przez URPL: 07.11.2016 Strona 1/7 Acytretyna (Neotigason): poważne ryzyko działania teratogennego oraz ryzyko
Szczepienia ochronne. Dr hab. med. Agnieszka Szypowska Dr med. Anna Taczanowska Lek. Katarzyna Piechowiak
 Szczepienia ochronne Dr hab. med. Agnieszka Szypowska Dr med. Anna Taczanowska Lek. Katarzyna Piechowiak Klinika Pediatrii Warszawski Uniwersytet Medyczny Szczepienie (profilaktyka czynna) Podanie całego
Szczepienia ochronne Dr hab. med. Agnieszka Szypowska Dr med. Anna Taczanowska Lek. Katarzyna Piechowiak Klinika Pediatrii Warszawski Uniwersytet Medyczny Szczepienie (profilaktyka czynna) Podanie całego
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Aneks III. Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aspekty prawne w kontekście zagrożenia funkcjonariuszy i pracowników SW ekspozycją na wirusa HIV
 Aspekty prawne w kontekście zagrożenia funkcjonariuszy i pracowników SW ekspozycją na wirusa HIV Zespół Służby Medycyny Pracy i Bezpieczeństwa i Higieny Pracy Centralny Zarząd Służby Więziennej Ustawa
Aspekty prawne w kontekście zagrożenia funkcjonariuszy i pracowników SW ekspozycją na wirusa HIV Zespół Służby Medycyny Pracy i Bezpieczeństwa i Higieny Pracy Centralny Zarząd Służby Więziennej Ustawa
Ogólne podsumowanie oceny naukowej produktu leczniczego Mifepristone Linepharma i nazw produktów związanych (patrz aneks I)
 Aneks II Wnioski naukowe i podstawy pozytywnej opinii zgodnie z warunkiem pozwolenia na dopuszczenie do obrotu i warunkiem zmiany charakterystyki produktu leczniczego i ulotki dla pacjenta przedstawione
Aneks II Wnioski naukowe i podstawy pozytywnej opinii zgodnie z warunkiem pozwolenia na dopuszczenie do obrotu i warunkiem zmiany charakterystyki produktu leczniczego i ulotki dla pacjenta przedstawione
Aneks III. Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Anna Skop. Zachęcam do zapoznania się z prezentacja na temat szczepień.
 W ostatnim tygodniu kwietnia obchodziliśmy Europejski Tydzień Szczepień. Jest to inicjatywa Światowej Organizacji Zdrowia, WHO. W związku z tą inicjatywą w naszej szkole w maju prowadzona jest kampania,
W ostatnim tygodniu kwietnia obchodziliśmy Europejski Tydzień Szczepień. Jest to inicjatywa Światowej Organizacji Zdrowia, WHO. W związku z tą inicjatywą w naszej szkole w maju prowadzona jest kampania,
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 10 November 2016 EMA/PRAC/730052/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
10 November 2016 EMA/PRAC/730052/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
 SZCZEPIENIA OCHRONNE U DOROSŁYCH lek. Kamil Chudziński Klinika Anestezjologii i Intensywnej Terapii CSK MSW w Warszawie 10.11.2015 Szczepionki Zabite lub żywe, ale odzjadliwione drobnoustroje/toksyny +
SZCZEPIENIA OCHRONNE U DOROSŁYCH lek. Kamil Chudziński Klinika Anestezjologii i Intensywnej Terapii CSK MSW w Warszawie 10.11.2015 Szczepionki Zabite lub żywe, ale odzjadliwione drobnoustroje/toksyny +
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków
 Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
Podmiot odpowiedzialny Nazwa Moc Postać farmaceutyczna. Leflunomide Actavis 10 mg, filmomhulde tabletten
 Aneks I Wykaz nazw, postaci farmaceutycznych, mocy produktów leczniczych, droga podania, podmiot odpowiedzialny posiadający pozwolenie na dopuszczenie do obrotu w państwach członkowskich 1 Państwo Członkowskie
Aneks I Wykaz nazw, postaci farmaceutycznych, mocy produktów leczniczych, droga podania, podmiot odpowiedzialny posiadający pozwolenie na dopuszczenie do obrotu w państwach członkowskich 1 Państwo Członkowskie
Annex I. Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia
 Annex I Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia Podsumowanie naukowe Biorąc pod uwagę Raport oceniający komitetu PRAC dotyczący Okresowego Raportu o Bezpieczeństwie
Annex I Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia Podsumowanie naukowe Biorąc pod uwagę Raport oceniający komitetu PRAC dotyczący Okresowego Raportu o Bezpieczeństwie
Ogólne podsumowanie oceny naukowej szczepionki Priorix i produktów z nią związanych pod różnymi nazwami(patrz aneks I)
 Aneks II Wnioski naukowe i podstawy do zmiany charakterystyki produktu leczniczego, oznakowania opakowań i ulotki dla pacjenta przedstawione przez Europejską Agencję Leków 9 Wnioski naukowe Ogólne podsumowanie
Aneks II Wnioski naukowe i podstawy do zmiany charakterystyki produktu leczniczego, oznakowania opakowań i ulotki dla pacjenta przedstawione przez Europejską Agencję Leków 9 Wnioski naukowe Ogólne podsumowanie
Obowiązkowe szczepienia ochronne. Dz.U t.j. z dnia Status: Akt obowiązujący Wersja od: 1 stycznia 2017 r.
 Obowiązkowe szczepienia ochronne. Dz.U.2016.849 t.j. z dnia 2016.06.15 Status: Akt obowiązujący Wersja od: 1 stycznia 2017 r. Wejście w życie: 1 października 2011 r. ROZPORZĄDZENIE MINISTRA ZDROWIA 1 z
Obowiązkowe szczepienia ochronne. Dz.U.2016.849 t.j. z dnia 2016.06.15 Status: Akt obowiązujący Wersja od: 1 stycznia 2017 r. Wejście w życie: 1 października 2011 r. ROZPORZĄDZENIE MINISTRA ZDROWIA 1 z
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
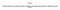 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Chronimy Ciebie i Twoje dziecko
 Chronimy Ciebie i Twoje dziecko Badania krwi podczas Twojej pierwszej wizyty przedporodowej Polish (Protecting you and your baby) Niniejsza ulotka opisuje badania krwi, które są zazwyczaj oferowane i zalecane
Chronimy Ciebie i Twoje dziecko Badania krwi podczas Twojej pierwszej wizyty przedporodowej Polish (Protecting you and your baby) Niniejsza ulotka opisuje badania krwi, które są zazwyczaj oferowane i zalecane
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Ospa wietrzna czy na pewno łagodna choroba zakaźna? Katedra i Zakład Profilaktyki Zdrowotnej UM w Poznaniu SZOZ nad Matką i Dzieckiem w Poznaniu
 Ospa wietrzna czy na pewno łagodna choroba zakaźna? Prof. dr hab. med. Jacek Wysocki dr med. Ilona Małecka Katedra i Zakład Profilaktyki Zdrowotnej UM w Poznaniu SZOZ nad Matką i Dzieckiem w Poznaniu Epidemiologia
Ospa wietrzna czy na pewno łagodna choroba zakaźna? Prof. dr hab. med. Jacek Wysocki dr med. Ilona Małecka Katedra i Zakład Profilaktyki Zdrowotnej UM w Poznaniu SZOZ nad Matką i Dzieckiem w Poznaniu Epidemiologia
WNIOSKI NAUKOWE I PODSTAWY ZMIANY POZWOLENIA NA DOPUSZCZENIE DO OBROTU DLA HBVAXPRO PRZEDSTAWIONE PRZEZ EMEA
 WNIOSKI NAUKOWE I PODSTAWY ZMIANY POZWOLENIA NA DOPUSZCZENIE DO OBROTU DLA HBVAXPRO PRZEDSTAWIONE PRZEZ EMEA WPROWADZENIE HBVAXPRO jest monowalentną szczepionką opracowaną w celu czynnego uodporniania
WNIOSKI NAUKOWE I PODSTAWY ZMIANY POZWOLENIA NA DOPUSZCZENIE DO OBROTU DLA HBVAXPRO PRZEDSTAWIONE PRZEZ EMEA WPROWADZENIE HBVAXPRO jest monowalentną szczepionką opracowaną w celu czynnego uodporniania
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
Mifepriston Linepharma. Mifepristone Linepharma. Mifepristone Linepharma 200 mg comprimé. Mifepristone Linepharma 200 mg Tafla
 Aneks I Wykaz nazw, postać farmaceutyczna, moc produktu leczniczego, droga podania, wnioskodawcy / podmioty odpowiedzialne posiadające pozwolenie na dopuszczenie do obrotu w państwach członkowskich 1 Podmiot
Aneks I Wykaz nazw, postać farmaceutyczna, moc produktu leczniczego, droga podania, wnioskodawcy / podmioty odpowiedzialne posiadające pozwolenie na dopuszczenie do obrotu w państwach członkowskich 1 Podmiot
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 4 January 2019 1 EMA/PRAC/854990/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
4 January 2019 1 EMA/PRAC/854990/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Co robię, aby nie zachorować na AIDS? Mateusz Hurko kl. III AG
 Co robię, aby nie zachorować na AIDS? Mateusz Hurko kl. III AG -Czym jest HIV? -HIV jest wirusem. Jego nazwa pochodzi od: H human I immunodeficiency ludzki upośledzenia odporności V virus wirus -To czym
Co robię, aby nie zachorować na AIDS? Mateusz Hurko kl. III AG -Czym jest HIV? -HIV jest wirusem. Jego nazwa pochodzi od: H human I immunodeficiency ludzki upośledzenia odporności V virus wirus -To czym
Informacja nt. sytuacji epidemiologicznej odry
 Łódź, dnia 28.01.2019 r. Informacja nt. sytuacji epidemiologicznej odry 23.01.2019 Rocznie rejestrowanych było w Polsce średnio 100 przypadków odry. W 2017 r. zarejestrowano 63 przypadki, zaś w 2018 r.
Łódź, dnia 28.01.2019 r. Informacja nt. sytuacji epidemiologicznej odry 23.01.2019 Rocznie rejestrowanych było w Polsce średnio 100 przypadków odry. W 2017 r. zarejestrowano 63 przypadki, zaś w 2018 r.
BROSZURA INFORMACYJNA DLA PACJENTA. PROGRAM ZAPOBIEGANIA CIĄŻY TOCTINO (Alitretynoina)
 BROSZURA INFORMACYJNA DLA PACJENTA PROGRAM ZAPOBIEGANIA CIĄŻY TOCTINO (Alitretynoina) Podmiot odpowiedzialny Stiefel Laboratories (Ireland) Ltd Finisklin Business Park, Sligo Irlandia Przedstawiciel podmiotu
BROSZURA INFORMACYJNA DLA PACJENTA PROGRAM ZAPOBIEGANIA CIĄŻY TOCTINO (Alitretynoina) Podmiot odpowiedzialny Stiefel Laboratories (Ireland) Ltd Finisklin Business Park, Sligo Irlandia Przedstawiciel podmiotu
Sprawozdanie roczne główne działania 2009
 4 października 2010 r. EMA/615494/2010 Biuro dyrektora zarządzającego Sprawozdanie roczne główne działania 2009 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom Telephone +44 (0)20 7418 8400
4 października 2010 r. EMA/615494/2010 Biuro dyrektora zarządzającego Sprawozdanie roczne główne działania 2009 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom Telephone +44 (0)20 7418 8400
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Dobierając optymalny program szczepień, jesteśmy w stanie zapobiec chorobom, które mogą być zagrożeniem dla zdrowia Państwa pupila.
 SZCZEPIENIA KOTÓW Działamy według zasady: Lepiej zapobiegać niż leczyć Wychodząc naprzeciw Państwa oczekiwaniom oraz dbając o dobro Waszych pupili opisaliśmy program profilaktyczny chorób zakaźnych psów,
SZCZEPIENIA KOTÓW Działamy według zasady: Lepiej zapobiegać niż leczyć Wychodząc naprzeciw Państwa oczekiwaniom oraz dbając o dobro Waszych pupili opisaliśmy program profilaktyczny chorób zakaźnych psów,
VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości
 VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Szacuje się, że wysokie ciśnienie krwi jest przyczyną
VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Szacuje się, że wysokie ciśnienie krwi jest przyczyną
Aneks I. Wnioski naukowe oraz podstawy zmian warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu.
 Aneks I Wnioski naukowe oraz podstawy zmian warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu. 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe oraz podstawy zmian warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu. 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
1. NAZWA PRODUKTU LECZNICZEGO PRIORIX. 1 dawka (0,5 ml) szczepionki po rekonstytucji zawiera: CCID 50. szczepu Jeryl Lynn) hodowli komórkowej
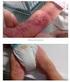 1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, 2. 1 dawka (0,5 ml) szczepionki po rekonstytucji zawiera: 1 (szczep Schwarz) 3,0 3 CCID 50 1 3,7 3 CCID 50 szczepu Jeryl Lynn) 2 (szczep Wistar RA 27/3) 3,0 3 CCID
1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, 2. 1 dawka (0,5 ml) szczepionki po rekonstytucji zawiera: 1 (szczep Schwarz) 3,0 3 CCID 50 1 3,7 3 CCID 50 szczepu Jeryl Lynn) 2 (szczep Wistar RA 27/3) 3,0 3 CCID
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 25 February 2016 EMA/PRAC/137769/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
25 February 2016 EMA/PRAC/137769/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
ANEKS WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO I SKUTECZNEGO UŻYWANIA PRODUKTÓW LECZNICZYCH DO SPEŁNIENIA PRZEZ PAŃSTWA CZŁONKOWSKIE
 ANEKS WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO I SKUTECZNEGO UŻYWANIA PRODUKTÓW LECZNICZYCH DO SPEŁNIENIA PRZEZ PAŃSTWA CZŁONKOWSKIE 1/5 WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO
ANEKS WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO I SKUTECZNEGO UŻYWANIA PRODUKTÓW LECZNICZYCH DO SPEŁNIENIA PRZEZ PAŃSTWA CZŁONKOWSKIE 1/5 WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO
Aneks I. Wnioski naukowe i podstawy do zmiany charakterystyki produktu leczniczego i ulotki informacyjnej
 Aneks I Wnioski naukowe i podstawy do zmiany charakterystyki produktu leczniczego i ulotki informacyjnej Ogólne podsumowanie oceny naukowej weterynaryjnych produktów leczniczych zawierających (fluoro)chinolony
Aneks I Wnioski naukowe i podstawy do zmiany charakterystyki produktu leczniczego i ulotki informacyjnej Ogólne podsumowanie oceny naukowej weterynaryjnych produktów leczniczych zawierających (fluoro)chinolony
Aneks II. Wnioski naukowe
 Aneks II Wnioski naukowe 205 Wnioski naukowe W następstwie rozpoczętej w styczniu 2012 r. oceny tworzonego w ramach procedury podziału pracy okresowego raportu o bezpieczeństwie dotyczącego produktów leczniczych
Aneks II Wnioski naukowe 205 Wnioski naukowe W następstwie rozpoczętej w styczniu 2012 r. oceny tworzonego w ramach procedury podziału pracy okresowego raportu o bezpieczeństwie dotyczącego produktów leczniczych
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 12 October 2017 EMA/PRAC/662548/2017 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
12 October 2017 EMA/PRAC/662548/2017 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Aneks II. Wnioski naukowe
 Aneks II Wnioski naukowe 8 Wnioski naukowe Solu-Medrol 40 mg, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań (zwany dalej Solu-Medrol ) zawiera metyloprednisolon i (jako substancję pomocniczą)
Aneks II Wnioski naukowe 8 Wnioski naukowe Solu-Medrol 40 mg, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań (zwany dalej Solu-Medrol ) zawiera metyloprednisolon i (jako substancję pomocniczą)
Lipophoral Tablets 150mg. Mediator 150 mg Tabletka Podanie doustne. Benfluorex Qualimed. Mediator 150mg Tabletka Podanie doustne
 ANEKS I WYKAZ NAZW WŁASNYCH, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTÓW LECZNICZYCH, DROGA PODANIA, PODMIOTY ODPOWIEDZIALNE POSIADAJĄCE POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH (EOG) 1
ANEKS I WYKAZ NAZW WŁASNYCH, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTÓW LECZNICZYCH, DROGA PODANIA, PODMIOTY ODPOWIEDZIALNE POSIADAJĄCE POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH (EOG) 1
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Priorix-Tetra, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince, różyczce i ospie wietrznej,
Ulotka dołączona do opakowania: informacja dla użytkownika Priorix-Tetra, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince, różyczce i ospie wietrznej,
Zaktualizowane zalecenia dotyczące stosowania wysokich dawek ibuprofenu
 22 maja 2015 r. EMA/325007/2015 Zaktualizowane zalecenia dotyczące stosowania wysokich dawek ibuprofenu Wyniki oceny potwierdziły występowanie niewielkiego ryzyka sercowonaczyniowego w przypadku przyjmowania
22 maja 2015 r. EMA/325007/2015 Zaktualizowane zalecenia dotyczące stosowania wysokich dawek ibuprofenu Wyniki oceny potwierdziły występowanie niewielkiego ryzyka sercowonaczyniowego w przypadku przyjmowania
Igantet j.m./ml, roztwór do wstrzykiwań, Immunoglobulina ludzka przeciwtężcowa
 ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA PACJENTA Igantet 250 250 j.m./ml, roztwór do wstrzykiwań, Immunoglobulina ludzka przeciwtężcowa Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA PACJENTA Igantet 250 250 j.m./ml, roztwór do wstrzykiwań, Immunoglobulina ludzka przeciwtężcowa Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
UCHWAŁA NR XXV/290/16 RADY GMINY MIELNO. z dnia 2 września 2016 r.
 UCHWAŁA NR XXV/290/16 RADY GMINY MIELNO z dnia 2 września 2016 r. w sprawie przyjęcia programu polityki zdrowotnej w zakresie szczepienia dzieci przeciwko ospie wietrznej Na podstawie art. 7 ust. 1 pkt
UCHWAŁA NR XXV/290/16 RADY GMINY MIELNO z dnia 2 września 2016 r. w sprawie przyjęcia programu polityki zdrowotnej w zakresie szczepienia dzieci przeciwko ospie wietrznej Na podstawie art. 7 ust. 1 pkt
Aneks II. Wnioski naukowe i podstawy do cofnięcia pozwoleń na dopuszczenie do obrotu
 Aneks II Wnioski naukowe i podstawy do cofnięcia pozwoleń na dopuszczenie do obrotu 4 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej produktów Caustinerf arsenical, Yranicid arsenical i
Aneks II Wnioski naukowe i podstawy do cofnięcia pozwoleń na dopuszczenie do obrotu 4 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej produktów Caustinerf arsenical, Yranicid arsenical i
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
WARUNKI LUB OGRANICZENIA DOTYCZĄCE BEZPIECZNEGO I SKUTECZNEGO STOSOWANIA PRODUKTU LECZNICZEGO DO WDROŻENIA PRZEZ KRAJE CZŁONKOWSKIE
 ANEKS 1 WARUNKI LUB OGRANICZENIA DOTYCZĄCE BEZPIECZNEGO I SKUTECZNEGO STOSOWANIA PRODUKTU LECZNICZEGO DO WDROŻENIA PRZEZ KRAJE CZŁONKOWSKIE Kraj członkowski musi upewnić się ze wszystkie warunki lub ograniczenia
ANEKS 1 WARUNKI LUB OGRANICZENIA DOTYCZĄCE BEZPIECZNEGO I SKUTECZNEGO STOSOWANIA PRODUKTU LECZNICZEGO DO WDROŻENIA PRZEZ KRAJE CZŁONKOWSKIE Kraj członkowski musi upewnić się ze wszystkie warunki lub ograniczenia
Podmiot odpowiedzialny Nazwa Moc Postać farmaceutyczna. FENOFIBRATO PENSA 160 mg comprimidos recubiertos con película EFG
 Aneks I Wykaz nazw, postaci farmaceutycznych, mocy produktów leczniczych, droga podania, podmiot odpowiedzialny posiadający pozwolenie na dopuszczenie do obrotu w państwach członkowskich 1 Państwo Członkowskie
Aneks I Wykaz nazw, postaci farmaceutycznych, mocy produktów leczniczych, droga podania, podmiot odpowiedzialny posiadający pozwolenie na dopuszczenie do obrotu w państwach członkowskich 1 Państwo Członkowskie
PROFIALKTYKA GRYPY W GMINIE CZAPLINEK W LATACH
 PROFIALKTYKA GRYPY W GMINIE CZAPLINEK W LATACH 2010-2016 CO WARTO WIEDZIEĆ O GRYPIE Każdego roku na całym świecie zaraża się 5-10% populacji osób dorosłych i 20-30%dzieci Wirusy grypy ludzkiej łatwiej
PROFIALKTYKA GRYPY W GMINIE CZAPLINEK W LATACH 2010-2016 CO WARTO WIEDZIEĆ O GRYPIE Każdego roku na całym świecie zaraża się 5-10% populacji osób dorosłych i 20-30%dzieci Wirusy grypy ludzkiej łatwiej
Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon
 VI.2 VI.2.1 Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon Omówienie rozpowszechnienia choroby Deksametazonu sodu fosforan w postaci roztworu do wstrzykiwań stosowany jest
VI.2 VI.2.1 Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon Omówienie rozpowszechnienia choroby Deksametazonu sodu fosforan w postaci roztworu do wstrzykiwań stosowany jest
Przedstawiona ulotka nie zastępuje informacji zawartej w Charakterystyce Produktu Leczniczego Leflunomide Sandoz.
 Aneks 8: Ulotka dla lekarza Informacja dotycząca bezpieczeństwa Leflunomide Sandoz 20 mg, tabletki powlekane leflunomid Leflunomide Sandoz, jako lek przeciwreumatyczny modyfikujący przebieg choroby (ang.
Aneks 8: Ulotka dla lekarza Informacja dotycząca bezpieczeństwa Leflunomide Sandoz 20 mg, tabletki powlekane leflunomid Leflunomide Sandoz, jako lek przeciwreumatyczny modyfikujący przebieg choroby (ang.
Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie
 brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
VARILRIX (Vaccinum varicellae vivum) Liofilizat i rozpuszczalnik do sporządzenia roztworu do wstrzykiwań podskórnych.
 INFORMACJA O LEKU DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem VARILRIX (Vaccinum varicellae vivum) Liofilizat i rozpuszczalnik do sporządzenia roztworu do wstrzykiwań podskórnych.
INFORMACJA O LEKU DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem VARILRIX (Vaccinum varicellae vivum) Liofilizat i rozpuszczalnik do sporządzenia roztworu do wstrzykiwań podskórnych.
Ulotka dołączona do opakowania: informacja dla użytkownika. Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji
 Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
