zaburzeniem widzenia spowodowanym obrzękiem plamki wywołanym cukrzycą;
|
|
|
- Wacława Sadowska
- 9 lat temu
- Przeglądów:
Transkrypt
1 EMA/677928/2015 EMEA/H/C/ Streszczenie EPAR dla ogółu społeczeństwa aflibercept Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia, jak Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) ocenił lek w celu ustalenia opinii, na podstawie której przyznano pozwolenie na dopuszczenie produktu do obrotu, oraz zaleceń w sprawie warunków stosowania leku. Co to jest? jest lekiem, który zawiera substancję czynną aflibercept. Produkt jest dostępny w postaci roztworu do wstrzykiwania do oka w napełnianych fabrycznie strzykawkach lub fiolkach. W jakim celu stosuje się produkt? Lek stosuje się w leczeniu osób dorosłych z: wysiękową postacią zwyrodnienia plamki żółtej związanego z wiekiem (AMD), chorobą obejmującą centralną część siatkówki (zwaną plamką żółtą) w tylnej części oka. Wysiękowa postać AMD jest spowodowana neowaskularyzacją podsiatkówkową (nieprawidłowy wzrost naczyń krwionośnych pod plamką żółtą), która może prowadzić do wysięku płynu, krwawienia i obrzęku; zaburzeniem widzenia spowodowanym obrzękiem (opuchnięciem) plamki żółtej spowodowanym zablokowaniem głównej żyły odprowadzającej krew z siatkówki (znanym jako zakrzep żyły środkowej siatkówki, CRVO) lub mniejszych odgałęzień tej żyły (znanym jako zakrzep gałęzi żyły środkowej siatkówki, BRVO); zaburzeniem widzenia spowodowanym obrzękiem plamki wywołanym cukrzycą; zaburzeniem widzenia spowodowanym neowaskularyzacją podsiatkówkową występującą w przebiegu patologicznej krótkowzroczności (poważna odmiana krótkowzroczności, w której następuje nadmierne wydłużenie gałki ocznej). 30 Churchill Place Canary Wharf London E14 5EU United Kingdom Telephone +44 (0) Facsimile +44 (0) Send a question via our website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 Plamka żółta odpowiada za widzenie środkowe i jest niezbędna do szczegółowego widzenia podczas wykonywania codziennych czynności, takich jak prowadzenie pojazdów, czytanie i rozpoznawanie twarzy. Choroba przyczynia się do stopniowej utraty wzroku w centralnej części pola widzenia. Lek wydaje się wyłącznie z przepisu lekarza. Jak stosować produkt? Lek musi być podawany we wstrzyknięciu do ciała szklistego (galaretowaty płyn wewnątrz oka) przez lekarza mającego doświadczenie w wykonywaniu wstrzyknięć do ciała szklistego. W przypadku wysiękowej postaci AMD wykonuje się jedno wstrzyknięcie w dawce 2 mg do chorego oka co miesiąc przez trzy kolejne miesiące, po czym wykonuje się jedno wstrzyknięcie co dwa miesiące. Po roku leczenia wstrzyknięcia można wykonywać rzadziej, w zależności od odpowiedzi na leczenie. W przypadku obrzęku plamki spowodowanego CRVO lub BRVO leczenie rozpoczyna się od wstrzyknięć w dawce 2 mg do chorego oka wykonywanych co miesiąc, ale w zależności od odpowiedzi pacjenta przerwę między podaniami można przedłużyć. Jeżeli u pacjenta nie wystąpi odpowiedź, leczenia nie należy kontynuować. W przypadku obrzęku plamki na tle cukrzycy wykonuje się jedno wstrzyknięcie w dawce 2 mg do chorego oka co miesiąc przez pięć kolejnych miesięcy, po czym wykonuje się jedno wstrzyknięcie co dwa miesiące. Po roku leczenia wstrzyknięcia można wykonywać rzadziej, w zależności od odpowiedzi na leczenie. Jeżeli u pacjenta nie wystąpi odpowiedź, leczenie należy przerwać. W przypadku neowaskularyzacji podsiatkówkowej występującej w przebiegu patologicznej krótkowzroczności wykonuje się jedno wstrzyknięcie w dawce 2 mg do chorego oka. Jeżeli choroba nie ustępuje, można wykonać dodatkowe wstrzyknięcia, przy czym przerwa pomiędzy wstrzyknięciami powinna wynosić co najmniej miesiąc. Procedurę należy przeprowadzać w sterylnych warunkach. Strzykawka i fiolka są przeznaczone wyłącznie do jednorazowego użytku. Fabrycznie napełniona strzykawka zawiera więcej leku, niż wynosi zalecana dawka, dlatego podczas przygotowywania zastrzyku lekarz musi usunąć nadmiarową objętość i dokonać wstrzyknięcia odpowiedniej dawki leku. Po wykonaniu zastrzyku należy zmierzyć ciśnienie w oku. Jak działa produkt? Aflibercept jest produktem inżynierii białkowej mającym na celu wiązanie i blokowanie działania substancji zwanej czynnikiem wzrostu śródbłonka naczyniowego A (VEGF-A). Produkt ten może także przyłączać się do innych białek, takich jak łożyskowy czynnik wzrostu (PlGF). Czynniki VEGF-A i PlGF biorą udział w stymulacji nieprawidłowego wzrostu naczyń krwionośnych u pacjentów z AMD, niektórymi odmianami obrzęku plamki i neowaskularyzacją podsiatkówkową występującą w przebiegu patologicznej krótkowzroczności. Blokując aktywność tych czynników, aflibercept zmniejsza intensywność wzrostu naczyń krwionośnych i umożliwia kontrolę wycieku płynów oraz obrzęku. Jak badano produkt? Lek oceniano w dwóch badaniach głównych z udziałem łącznej liczby około 2400 pacjentów z wysiękową postacią AMD. W badaniach lek (podawany w dawce 0,5 mg co cztery tygodnie, 2 mg co cztery tygodnie lub 2 mg co osiem tygodni, w każdym przypadku po trzech comiesięcznych dawkach EMA/677928/2015 Strona 2/5
3 początkowych) porównywano z ranibizumabem, innym lekiem stosowanym w AMD, podawanym w postaci wstrzyknięcia do oka co cztery tygodnie. Głównym kryterium oceny skuteczności był odsetek pacjentów, którzy zachowali zdolność widzenia (określaną jako obniżenie ostrości wzroku wynoszące mniej niż 15 liter w standardowym badaniu wzroku) po pierwszym roku leczenia. W obu badaniach oceniano także utrzymanie działania w drugim roku leczenia, w trakcie którego liczbę wstrzykiwań i przerwę między nimi dostosowano w zależności od zdolności widzenia i zmian w oku. Lek oceniano również w dwóch innych badaniach głównych z udziałem 366 pacjentów z obrzękiem plamki spowodowanym przez CRVO. W badaniach tych comiesięczne wstrzyknięcie leku w dawce 2 mg porównywano z pozorowanym wstrzyknięciem, wykonywanym za pomocą strzykawki bez igły. W innym badaniu głównym z udziałem 181 pacjentów z obrzękiem plamki spowodowanym przez BRVO comiesięczne wstrzyknięcie leku w dawce 2 mg porównano z leczeniem laserem. We wszystkich badaniach głównym kryterium oceny skuteczności był odsetek pacjentów, u których wystąpiła odpowiedź i których wzrok poprawił się o przynajmniej 15 liter w badaniu wzroku 24 tygodnie po leczeniu. W badaniach u pacjentów z obrzękiem plamki spowodowanym przez CRVO oceniano również efekty leczenia w zależności od zapotrzebowania po 24 tygodniach. W dwóch kolejnych badaniach głównych z udziałem 872 pacjentów z obrzękiem plamki na tle cukrzycy oceniano działanie produktu w porównaniu z leczeniem laserem. Produkt podawano raz na miesiąc lub raz na dwa miesiące po pierwszych pięciu comiesięcznych wstrzyknięciach. Głównym kryterium oceny skuteczności w obu badaniach była zmiana w liczbie liter, które dało się przeczytać w badaniu wzroku po roku leczenia. W neowaskularyzacji podsiatkówkowej występującej w przebiegu patologicznej krótkowzroczności lek oceniano w badaniu głównym z udziałem 122 pacjentów, w którym lek porównano z wstrzyknięciem pozorowanym. Głównym kryterium oceny skuteczności była zmiana w liczbie liter, które dało się przeczytać w badaniu wzroku po 24 tygodniach leczenia. Jakie korzyści ze stosowania produktu zaobserwowano w badaniach? Wykazano, że lek był tak samo skuteczny jak ranibizumab w utrzymaniu zdolności widzenia u pacjentów z wysiękową postacią AMD: na podstawie łącznych wyników obu badań odsetek pacjentów z zachowaną zdolnością widzenia wyniósł 96,1% (517 z 538 pacjentów), 95,4% (533 z 559 pacjentów) oraz 95,3% (510 z 535 pacjentów), odpowiednio w przypadku dawki 0,5 mg leku podawanej co cztery tygodnie, dawki 2 mg leku podawanej co cztery tygodnie i dawki 2 mg leku podawanej co osiem tygodni, w porównaniu z wynikiem 94,4% (508 z 538 pacjentów) w przypadku pacjentów, którym co cztery tygodnie podawano ranibizumab. W trakcie drugiego roku leczenia skuteczność leku została ogólnie zachowana, przy czym większość pacjentów otrzymywała zastrzyk z przerwą między podaniami przedłużoną do 10 tygodni, a niewielka liczba pacjentów sporadycznie wymagała częstszych wstrzykiwań (np. raz w miesiącu). Lek powodował również znaczną poprawę zdolności widzenia u pacjentów z obrzękiem plamki na tle CRVO i BRVO. W przypadku CRVO poprawa o przynajmniej 15 liter w badaniu wzroku w 24. tygodniu badania wystąpiła ogółem u około 60% pacjentów, którym podawano lek, w porównaniu z 17% pacjentów, u których wykonywano pozorowane wstrzyknięcia. Korzyści z leczenia w znacznym stopniu utrzymały się przez okres do 52 tygodni z leczeniem dostosowanym do potrzeb, chociaż wydaje się, że część korzyści utracono, kiedy pacjenci byli leczeni i obserwowani przez okres przekraczający 52 tygodnie. W przypadku BRVO poprawa o przynajmniej 15 liter w badaniu wzroku w 24. tygodniu badania wystąpiła u około 53% pacjentów, którym podawano lek, w porównaniu z EMA/677928/2015 Strona 3/5
4 27% pacjentów, których poddano leczeniu laserem. Działanie to utrzymało się w 52. tygodniu mimo rzadszego podawania produktu pomiędzy 24. a 52. tygodniem. U pacjentów z obrzękiem plamki na tle cukrzycy średnia liczba liter, które byli oni w stanie odczytać w badaniu wzroku przed leczeniem, wynosiła około 59 do 60; u pacjentów, którym comiesięcznie podawano produkt, liczba ta wzrosła o ok. 12 liter, a u osób, którym podawano produkt raz na dwa miesiące o ok. 11 liter. Natomiast u pacjentów, u których zastosowano leczenie laserowe, poprawa po roku wynosiła jedynie w przybliżeniu 1 literę. W badaniu dotyczącym neowaskularyzacji podsiatkówkowej występującej w przebiegu patologicznej krótkowzroczności średnia liczba liter, które pacjenci byli w stanie odczytać w badaniu wzroku przed leczeniem, wynosiła około 56; po 24 tygodniach leczenia pacjenci, którym podawano lek, byli w stanie odczytać średnio 12 liter więcej, natomiast pacjenci, u których wykonywano wstrzyknięcia pozorowane, byli w stanie odczytać średnio 2 litery mniej. Jakie ryzyko wiąże się ze stosowaniem produktu? Najczęstsze działania niepożądane (występujące u co najmniej 1 pacjenta na 20) związane ze stosowaniem leku to: wylew spojówkowy (krwawienie z drobnych naczyń krwionośnych na powierzchni oka w miejscu wstrzyknięcia), zmniejszenie widzenia, ból oka, odłączenie ciała szklistego (oddzielenie się galaretowatej substancji wewnątrz oka), zaćma (zmętnienie soczewki), męty ciała szklistego (drobne cząsteczki lub plamki w polu widzenia) oraz podwyższone ciśnienie wewnątrzgałkowe (zwiększone ciśnienie wewnątrz oka). Poważne działania niepożądane związane z wstrzyknięciem (które wystąpiły przy mniej niż 1 wstrzyknięciu na 2200) obejmują ślepotę, wewnątrzgałkowe zapalenie oka (zapalenie wewnątrz oka), zaćmę, podwyższone ciśnienie wewnątrzgałkowe, krwotok do ciała szklistego (krwotok do galaretowatej substancji wewnątrz oka, powodujący przejściową utratę zdolności widzenia) i odłączenie ciała szklistego lub odwarstwienie siatkówki. Pełny wykaz działań niepożądanych związanych ze stosowaniem leku znajduje się w ulotce dla pacjenta. Leku nie wolno stosować u pacjentów z infekcjami gałki ocznej lub jej okolicy (zakażenia oczu lub wokół oczu) lub u których istnieje podejrzenie takiej infekcji, a także u pacjentów z poważnym stanem zapalnym wewnątrz oka. Pełny wykaz ograniczeń związanych ze stosowaniem produktu znajduje się w ulotce dla pacjenta. Na jakiej podstawie zatwierdzono produkt? CHMP zauważył, że lek był równie skuteczny jak ranibizumab w utrzymaniu zdolności widzenia u pacjentów po pierwszym roku leczenia wysiękowej postaci AMD. Ponadto CHMP uznał, że lek miał korzystne działanie w polepszaniu widzenia u pacjentów z obrzękiem plamki wywołanym przez CRVO, BRVO lub cukrzycę oraz u pacjentów z neowaskularyzacją podsiatkówkową występującą w przebiegu patologicznej krótkowzroczności. CHMP zauważył też, że nie wystąpiły żadne poważne lub nieoczekiwane wątpliwości co do bezpieczeństwa stosowania leku. Dlatego też CHMP uznał, że korzyści ze stosowania produktu przewyższają ryzyko, i zalecił przyznanie pozwolenia na dopuszczenie produktu do obrotu. EMA/677928/2015 Strona 4/5
5 Jakie środki są podejmowane w celu zapewnienia bezpiecznego stosowania produktu? W celu zapewnienia możliwie najbezpieczniejszego stosowania produktu opracowano plan zarządzania ryzykiem. W oparciu o ten plan w charakterystyce produktu leczniczego i ulotce dla pacjenta dotyczących leku zawarto informacje dotyczące bezpieczeństwa, w tym odpowiednie środki ostrożności obowiązujące personel medyczny i pacjentów. Firma produkująca lek dostarczy materiały edukacyjne dla lekarzy (w celu minimalizacji zagrożeń związanych ze wstrzykiwaniem produktu do oka) i pacjentów (aby potrafili rozpoznać wszelkie poważne działania niepożądane i wiedzieli, kiedy należy pilnie zgłosić się do lekarza). Ponadto firma przeprowadzi badanie analizujące stosowanie dłuższych przerw w podawaniu produktu w obrzęku plamki na tle cukrzycy, a także badanie dotyczące skutków leczenia produktem w zależności od zapotrzebowania w wysiękowej postaci AMD. Inne informacje dotyczące produktu : W dniu 22 listopada 2012 r. Komisja Europejska przyznała pozwolenie na dopuszczenie produktu do obrotu ważne w całej Unii Europejskiej. Pełne sprawozdanie EPAR dotyczące produktu znajduje się na stronie internetowej Agencji pod adresem: ema.europa.eu/find medicine/human medicines/european public assessment reports. W celu uzyskania dodatkowych informacji dotyczących leczenia produktem należy zapoznać się z ulotką dla pacjenta (także część EPAR) bądź skontaktować się z lekarzem lub farmaceutą. Data ostatniej aktualizacji: EMA/677928/2015 Strona 5/5
Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/481361/2018 EMEA/H/C/002392 Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Eylea i w jakim celu się go stosuje Eylea jest lekiem
EMA/481361/2018 EMEA/H/C/002392 Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Eylea i w jakim celu się go stosuje Eylea jest lekiem
Simponi jest lekiem o działaniu przeciwzapalnym. Preparat stosuje się w leczeniu następujących chorób u osób dorosłych:
 EMA/411054/2015 EMEA/H/C/000992 Streszczenie EPAR dla ogółu społeczeństwa golimumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
EMA/411054/2015 EMEA/H/C/000992 Streszczenie EPAR dla ogółu społeczeństwa golimumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
Pradaxa jest lekiem zawierającym substancję czynną eteksylan dabigatranu. Lek jest dostępny w postaci kapsułek (75, 110 i 150 mg).
 EMA/47517/2015 EMEA/H/C/000829 Streszczenie EPAR dla ogółu społeczeństwa eteksylan dabigatranu Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego
EMA/47517/2015 EMEA/H/C/000829 Streszczenie EPAR dla ogółu społeczeństwa eteksylan dabigatranu Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego
Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek przeciwcukrzycowy Suliqua
 19 stycznia 2017 r. EMA/747766/2016 Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek Środki mające na celu zmniejszenie ryzyka pomylenia dwóch wstrzykiwaczy o różnej mocy
19 stycznia 2017 r. EMA/747766/2016 Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek Środki mające na celu zmniejszenie ryzyka pomylenia dwóch wstrzykiwaczy o różnej mocy
Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
czerniak (nowotwór skóry), który rozprzestrzenił się lub którego nie można usunąć chirurgicznie;
 EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana)
 EMA/90006/2015 EMEA/H/C/001104 Streszczenie EPAR dla ogółu społeczeństwa szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana) Niniejszy dokument jest streszczeniem
EMA/90006/2015 EMEA/H/C/001104 Streszczenie EPAR dla ogółu społeczeństwa szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana) Niniejszy dokument jest streszczeniem
Lek Avastin stosuje się u osób dorosłych w leczeniu następujących rodzajów nowotworów w skojarzeniu z innymi lekami przeciwnowotworowymi:
 EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Revolade. eltrombopag. Co to jest Revolade? W jakim celu stosuje się produkt Revolade? Streszczenie EPAR dla ogółu społeczeństwa
 EMA/33466/2016 EMEA/H/C/001110 Streszczenie EPAR dla ogółu społeczeństwa eltrombopag Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/33466/2016 EMEA/H/C/001110 Streszczenie EPAR dla ogółu społeczeństwa eltrombopag Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
zaawansowany rak nerki lub rak nerki z przerzutami, w skojarzeniu z interferonem alfa-2a;
 EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
zaawansowanym rakiem nerkowokomórkowym, rodzajem raka nerki, u pacjentów, którzy byli wcześniej leczeni lekami przeciwnowotworowymi;
 EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
W szpiczaku mnogim, nowotworze pewnego typu białych krwinek zwanych komórkami plazmatycznymi, Revlimid stosuje się:
 EMA/113870/2017 EMEA/H/C/000717 Streszczenie EPAR dla ogółu społeczeństwa lenalidomid Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/113870/2017 EMEA/H/C/000717 Streszczenie EPAR dla ogółu społeczeństwa lenalidomid Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
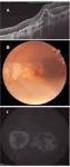 Dziennik Urzędowy Ministra Zdrowia 882 Poz. 79 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Dziennik Urzędowy Ministra Zdrowia 882 Poz. 79 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
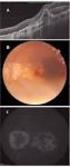 Dziennik Urzędowy Ministra Zdrowia 761 Poz. 48 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY afliberceptem
Dziennik Urzędowy Ministra Zdrowia 761 Poz. 48 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY afliberceptem
Keytruda (pembrolizumab)
 EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
ostrym reumatoidalnym zapaleniem stawów (choroba powodująca stan zapalny stawów), gdzie produkt MabThera podaje się dożylnie z metotreksatem;
 EMA/614203/2010 EMEA/H/C/000165 Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/614203/2010 EMEA/H/C/000165 Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 17 December 2015 EMA/PRAC/835763/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęto w dniach od 30 listopada
17 December 2015 EMA/PRAC/835763/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęto w dniach od 30 listopada
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej (wysiękowej) postaci afliberceptem
Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej (wysiękowej) postaci afliberceptem
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
 Dziennik Urzędowy Ministra Zdrowia 904 Poz. 133 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie
Dziennik Urzędowy Ministra Zdrowia 904 Poz. 133 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie
Ograniczenia stosowania leków zawierających domperidon
 1 września 2014 r. EMA/465179/2014 W dniu 23 kwietnia 2014 r. grupa koordynacyjna ds. procedur wzajemnego uznania i zdecentralizowanej produkty stosowane u ludzi (CMDh) zatwierdziła nowe zalecenia o ograniczeniu
1 września 2014 r. EMA/465179/2014 W dniu 23 kwietnia 2014 r. grupa koordynacyjna ds. procedur wzajemnego uznania i zdecentralizowanej produkty stosowane u ludzi (CMDh) zatwierdziła nowe zalecenia o ograniczeniu
6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej
 6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej 6.2.1. Podsumowanie korzyści wynikających z leczenia Co to jest T2488? T2488
6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej 6.2.1. Podsumowanie korzyści wynikających z leczenia Co to jest T2488? T2488
EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri
 25/04/2016 EMA/266665/2016 EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri U pacjentów z grupy zwiększonego
25/04/2016 EMA/266665/2016 EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri U pacjentów z grupy zwiększonego
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 25 January 2018 EMA/PRAC/35597/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
25 January 2018 EMA/PRAC/35597/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 10 November 2016 EMA/PRAC/730052/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
10 November 2016 EMA/PRAC/730052/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r.
 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r. ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r. ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Przewodnik użytkownika raportu internetowego
 Ochrona zdrowia pacjentów zawiera informacje dotyczące elementów składowych danych, układu, interpretacji i funkcji w raporcie internetowym. 1. Elementy składowe danych... 2 2. Dodatkowe informacje dotyczące
Ochrona zdrowia pacjentów zawiera informacje dotyczące elementów składowych danych, układu, interpretacji i funkcji w raporcie internetowym. 1. Elementy składowe danych... 2 2. Dodatkowe informacje dotyczące
Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie
 23 April 2015 EMA/PRAC/273915/2015 Pharmacovigilance Risk Assessment Committee Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte na posiedzeniu PRAC w dniach 7 10 kwietnia
23 April 2015 EMA/PRAC/273915/2015 Pharmacovigilance Risk Assessment Committee Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte na posiedzeniu PRAC w dniach 7 10 kwietnia
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 15 September 2016 EMA/PRAC/603539/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
15 September 2016 EMA/PRAC/603539/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie
 22 stycznia 2015 r. EMA/PRAC/63315/2015 Komitet ds. Oceny Ryzyka w ramach Nadzoru nad Bezpieczeństwem Farmakoterapii Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte
22 stycznia 2015 r. EMA/PRAC/63315/2015 Komitet ds. Oceny Ryzyka w ramach Nadzoru nad Bezpieczeństwem Farmakoterapii Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta
 Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta:informacja dla użytkownika Medivitan iv ampułko-strzykawka 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta:informacja dla użytkownika Medivitan iv ampułko-strzykawka 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Wyniki procedur na mocy art. 20 rozporządzenia (WE) nr 726/2004 oraz art. 31 dyrektywy 2001/83/WE
 28 lutego 2013 r. EMA/136606/2013 wer.1 EMEA/H/A-31/1333 EMEA/H/C/000604/A20/45 EMEA/H/C/000622/A20/60 EMEA/H/C/000674/A20/52 Pytania i odpowiedzi dotyczące ponownej oceny monowalentnych i poliwalentnych
28 lutego 2013 r. EMA/136606/2013 wer.1 EMEA/H/A-31/1333 EMEA/H/C/000604/A20/45 EMEA/H/C/000622/A20/60 EMEA/H/C/000674/A20/52 Pytania i odpowiedzi dotyczące ponownej oceny monowalentnych i poliwalentnych
Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu
 Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu Zmiany mają przede wszystkim na celu zmniejszenie ryzyka neurologicznych działań niepożądanych Komitet ds. Produktów Leczniczych Stosowanych
Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu Zmiany mają przede wszystkim na celu zmniejszenie ryzyka neurologicznych działań niepożądanych Komitet ds. Produktów Leczniczych Stosowanych
Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie
 brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
Aneks III. Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Prosta i skuteczna, nowa metoda leczenia jaskry
 Implant XEN Nowa skuteczna metoda leczenia jaskry Dla osób, u których ciśnienie w gałce ocznej jest zbyt wysokie pomimo stosowania kropli przeciwjaskrowych Obniża ciśnienie wewnątrz gałki ocznej, aby zapobiec
Implant XEN Nowa skuteczna metoda leczenia jaskry Dla osób, u których ciśnienie w gałce ocznej jest zbyt wysokie pomimo stosowania kropli przeciwjaskrowych Obniża ciśnienie wewnątrz gałki ocznej, aby zapobiec
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
EMA potwierdza zalecenia mające na celu zminimalizowanie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri
 26 lutego 2016 EMA/137488/2016 EMA potwierdza zalecenia mające na celu zminimalizowanie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri W przypadku pacjentów narażonych na większe
26 lutego 2016 EMA/137488/2016 EMA potwierdza zalecenia mające na celu zminimalizowanie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri W przypadku pacjentów narażonych na większe
Zaktualizowane zalecenia dotyczące stosowania wysokich dawek ibuprofenu
 22 maja 2015 r. EMA/325007/2015 Zaktualizowane zalecenia dotyczące stosowania wysokich dawek ibuprofenu Wyniki oceny potwierdziły występowanie niewielkiego ryzyka sercowonaczyniowego w przypadku przyjmowania
22 maja 2015 r. EMA/325007/2015 Zaktualizowane zalecenia dotyczące stosowania wysokich dawek ibuprofenu Wyniki oceny potwierdziły występowanie niewielkiego ryzyka sercowonaczyniowego w przypadku przyjmowania
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 25 February 2016 EMA/PRAC/137769/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
25 February 2016 EMA/PRAC/137769/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Metacam. meloksykam. Co to jest produkt Metacam i w jakim celu się go stosuje? Streszczenie EPAR dla ogółu społeczeństwa
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Streszczenie EPAR dla ogółu społeczeństwa meloksykam Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
EMA/CVMP/259397/2006 EMEA/V/C/000033 Streszczenie EPAR dla ogółu społeczeństwa meloksykam Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
Przegląd wiedzy na temat leku Metacam i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Przegląd wiedzy na temat leku Metacam i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Metacam i w jakim celu się go stosuje? Metacam
EMA/CVMP/259397/2006 EMEA/V/C/000033 Przegląd wiedzy na temat leku Metacam i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Metacam i w jakim celu się go stosuje? Metacam
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta
 Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Medivitan iv ampułki 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny chlorowodorek
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Medivitan iv ampułki 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny chlorowodorek
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
Często zadawane pytania (FAQ)
 4 listopada 2011 r. EMA/527628/2011 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków Jeśli nie znajdą tu Państwo odpowiedzi
4 listopada 2011 r. EMA/527628/2011 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków Jeśli nie znajdą tu Państwo odpowiedzi
Często zadawane pytania (FAQ)
 13 lutego 2017 r. EMA/527628/2011 Rev. 1 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków (EMA). W przypadku nieznalezienia
13 lutego 2017 r. EMA/527628/2011 Rev. 1 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków (EMA). W przypadku nieznalezienia
Annex I. Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia
 Annex I Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia Podsumowanie naukowe Biorąc pod uwagę Raport oceniający komitetu PRAC dotyczący Okresowego Raportu o Bezpieczeństwie
Annex I Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia Podsumowanie naukowe Biorąc pod uwagę Raport oceniający komitetu PRAC dotyczący Okresowego Raportu o Bezpieczeństwie
Aneks III. Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA
 ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA Poprawki do CHPL oraz ulotki dla pacjenta są ważne od momentu zatwierdzenia Decyzji Komisji. Po zatwierdzeniu Decyzji Komisji,
ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA Poprawki do CHPL oraz ulotki dla pacjenta są ważne od momentu zatwierdzenia Decyzji Komisji. Po zatwierdzeniu Decyzji Komisji,
Zaobserwowano częstsze przypadki stosowania produktu leczniczego Vistide w niezatwierdzonych wskazaniach i (lub) drogach podawania.
 Komunikat skierowany do fachowych pracowników ochrony zdrowia dotyczący występowania ciężkich działań niepożądanych związanych z stosowaniem produktu leczniczego Vistide (cydofowir) niezgodnie z zapisami
Komunikat skierowany do fachowych pracowników ochrony zdrowia dotyczący występowania ciężkich działań niepożądanych związanych z stosowaniem produktu leczniczego Vistide (cydofowir) niezgodnie z zapisami
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Poradnik dotyczący interpretacji spontanicznych zgłoszeń przypadków podejrzewanych działań niepożądanych leków
 30 styczeń 2017 r. Wydział ds. inspekcji, nadzoru nad bezpieczeństwem stosowania produktów leczniczych u ludzi i komisji EMA/749446/2016 Zmiana nr 1* Poradnik dotyczący interpretacji spontanicznych zgłoszeń
30 styczeń 2017 r. Wydział ds. inspekcji, nadzoru nad bezpieczeństwem stosowania produktów leczniczych u ludzi i komisji EMA/749446/2016 Zmiana nr 1* Poradnik dotyczący interpretacji spontanicznych zgłoszeń
Leki, zarejestrowane i stosowane aktualnie w krajach UE do leczenia onkologicznego i Stwardnienia Guzowatego.
 Leki, zarejestrowane i stosowane aktualnie w krajach UE do leczenia onkologicznego i Stwardnienia Guzowatego. Afinitor Ewerolumis Streszczenie EPAR dla ogółu społeczeństwa Niniejszy dokument stanowi streszczenie
Leki, zarejestrowane i stosowane aktualnie w krajach UE do leczenia onkologicznego i Stwardnienia Guzowatego. Afinitor Ewerolumis Streszczenie EPAR dla ogółu społeczeństwa Niniejszy dokument stanowi streszczenie
Czerwcowe spotkania ze specjalistami. Profilaktyka jaskry. Marek Rzendkowski Pryzmat-Okulistyka, Gliwice
 Czerwcowe spotkania ze specjalistami Profilaktyka jaskry Marek Rzendkowski Pryzmat-Okulistyka, Gliwice Gliwice, czerwiec 2018 Co robić żeby czegoś nie przeoczyć?... - Wada wzroku - okulary - Jaskra ważna
Czerwcowe spotkania ze specjalistami Profilaktyka jaskry Marek Rzendkowski Pryzmat-Okulistyka, Gliwice Gliwice, czerwiec 2018 Co robić żeby czegoś nie przeoczyć?... - Wada wzroku - okulary - Jaskra ważna
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta tabletki powlekane 100 mg Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Ulotka dołączona do opakowania: informacja dla pacjenta tabletki powlekane 100 mg Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Kiedy rozpocząć przyjmowanie dawki Jak przyjmować lek Uptravi? Jak zwiększać dawkę leku? Pominięcie przyjęcia leku...6
 PORADNIK DOTYCZĄCY DOBIERANIA DAWKI - PAKIET DOBIERANIA DAWKI Strona 1 Uptravi tabletki powlekane seleksypag Poradnik dobierania dawki Rozpoczynanie leczenia lekiem Uptravi Przed rozpoczęciem leczenia
PORADNIK DOTYCZĄCY DOBIERANIA DAWKI - PAKIET DOBIERANIA DAWKI Strona 1 Uptravi tabletki powlekane seleksypag Poradnik dobierania dawki Rozpoczynanie leczenia lekiem Uptravi Przed rozpoczęciem leczenia
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Ważne informacje nie wyrzucać! Agolek. w leczeniu dużych epizodów depresyjnych u dorosłych. Broszura dla Pacjenta
 Ważne informacje nie wyrzucać! Agolek w leczeniu dużych epizodów depresyjnych u dorosłych Broszura dla Pacjenta 1 Agolek jest lekiem przeciwdepresyjnym, który pomaga leczyć depresję. Aby zoptymalizować
Ważne informacje nie wyrzucać! Agolek w leczeniu dużych epizodów depresyjnych u dorosłych Broszura dla Pacjenta 1 Agolek jest lekiem przeciwdepresyjnym, który pomaga leczyć depresję. Aby zoptymalizować
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
Zawiadomienie Prezesa UR z dnia 19.03.2015 CCDS March 2014
 Ulotka dołączona do opakowania: informacja dla pacjenta PEVISONE, (10 mg + 1,1 mg)/g, krem Econazoli nitras + Triamcinoloni acetonidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta PEVISONE, (10 mg + 1,1 mg)/g, krem Econazoli nitras + Triamcinoloni acetonidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Bezpośredni komunikat do fachowych pracowników ochrony zdrowia
 Bezpośredni komunikat do fachowych pracowników ochrony zdrowia Wersja 2, data zatwierdzenia przez URPL: 07.11.2016 Strona 1/7 Acytretyna (Neotigason): poważne ryzyko działania teratogennego oraz ryzyko
Bezpośredni komunikat do fachowych pracowników ochrony zdrowia Wersja 2, data zatwierdzenia przez URPL: 07.11.2016 Strona 1/7 Acytretyna (Neotigason): poważne ryzyko działania teratogennego oraz ryzyko
Retinopatia cukrzycowa
 Retinopatia cukrzycowa Retinopatia cukrzycowa jest w krajach rozwiniętych jedną z głównych przyczyn ślepoty. Rozwija się u znacznej liczby pacjentów długo chorujących na cukrzycę, która może być przyczyną
Retinopatia cukrzycowa Retinopatia cukrzycowa jest w krajach rozwiniętych jedną z głównych przyczyn ślepoty. Rozwija się u znacznej liczby pacjentów długo chorujących na cukrzycę, która może być przyczyną
Choroba cukrzycowa oczu
 Choroba cukrzycowa oczu W języku medycznym cukrzyca w oczach to retinopatia cukrzycowa. Zwykle takie rozpoznanie stawia okulista i kieruje pacjenta na odpowiednie leczenie. Leczeniem cukrzycy w oczach
Choroba cukrzycowa oczu W języku medycznym cukrzyca w oczach to retinopatia cukrzycowa. Zwykle takie rozpoznanie stawia okulista i kieruje pacjenta na odpowiednie leczenie. Leczeniem cukrzycy w oczach
Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną hydroksyzynę.
 Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną hydroksyzynę. Aneks III Poprawki do odpowiednich punktów Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta
Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną hydroksyzynę. Aneks III Poprawki do odpowiednich punktów Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków
 Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
Agomelatyna. Broszura dla pacjenta
 Istotne informacje Nie wyrzucaj! Agomelatyna w leczeniu dużych epizodów depresyjnych u dorosłych Broszura dla pacjenta Informacje dotyczące leku Agomelatyna jest lekiem przeciwdepresyjnym, który pomoże
Istotne informacje Nie wyrzucaj! Agomelatyna w leczeniu dużych epizodów depresyjnych u dorosłych Broszura dla pacjenta Informacje dotyczące leku Agomelatyna jest lekiem przeciwdepresyjnym, który pomoże
POUFNE. Wersja ostateczna nr 1 z dnia 5 grudnia 2013 r. Numer ośrodka. Numer pacjenta. Numer wizyty. Badane oko
 POUFNE KARTA OBSERWACJI PACJENTA Rejestr pacjentów leczonych preparatem Lucentis (ranibizumab) we wszystkich zarejestrowanych wskazaniach w Polsce (Rejestr PRIME) Wersja ostateczna nr 1 z dnia 5 grudnia
POUFNE KARTA OBSERWACJI PACJENTA Rejestr pacjentów leczonych preparatem Lucentis (ranibizumab) we wszystkich zarejestrowanych wskazaniach w Polsce (Rejestr PRIME) Wersja ostateczna nr 1 z dnia 5 grudnia
NIEDROŻNOŚĆ ŻYŁY ŚRODKOWEJ SIATKÓWKI (CRVO)
 Przewodnik informacyjny Informacje naukowe na temat CRVO www.scienceofcrvo.org NIEDROŻNOŚĆ ŻYŁY ŚRODKOWEJ SIATKÓWKI (CRVO) W niniejszej broszurze przedstawione zostały informacje na temat CRVO oraz dostępnych
Przewodnik informacyjny Informacje naukowe na temat CRVO www.scienceofcrvo.org NIEDROŻNOŚĆ ŻYŁY ŚRODKOWEJ SIATKÓWKI (CRVO) W niniejszej broszurze przedstawione zostały informacje na temat CRVO oraz dostępnych
20 września 2013 r. EMA/564255/2013. 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom
 20 września 2013 r. EMA/564255/2013 Zawieszenie pozwolenia na dopuszczenie do obrotu produktu leczniczego Numeta G13%E i wprowadzenie nowych działań służących zminimalizowaniu ryzyka stosowania produktu
20 września 2013 r. EMA/564255/2013 Zawieszenie pozwolenia na dopuszczenie do obrotu produktu leczniczego Numeta G13%E i wprowadzenie nowych działań służących zminimalizowaniu ryzyka stosowania produktu
Ze względu na brak potwierdzenia w badaniu przeprowadzonym wśród młodzieży (opisanym poniżej) wyniki zostały uznane za niedostatecznie przekonujące.
 ZAŁĄCZNIK II WNIOSKI NAUKOWE I PODSTAWY DO WYDANIA POZYTYWNEJ OPINII ORAZ ZMIANY CHARAKTERYSTYKI PRODUKTU LECZNICZEGO, OZNAKOWANIA OPAKOWAŃ I ULOTKI DLA PACJENTA PRZEDSTAWIONE PRZEZ EUROPEJSKĄ AGENCJĘ
ZAŁĄCZNIK II WNIOSKI NAUKOWE I PODSTAWY DO WYDANIA POZYTYWNEJ OPINII ORAZ ZMIANY CHARAKTERYSTYKI PRODUKTU LECZNICZEGO, OZNAKOWANIA OPAKOWAŃ I ULOTKI DLA PACJENTA PRZEDSTAWIONE PRZEZ EUROPEJSKĄ AGENCJĘ
Lek BI w porównaniu z lekiem Humira u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą
 Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
BROSZURA INFORMACYJNA DLA PACJENTA
 BROSZURA INFORMACYJNA DLA PACJENTA Zastosowanie produktu BOTOX /Vistabel 4 jednostki Allergan/0,1 ml toksyna botulinowa typu A w leczeniu zmarszczek pionowych gładzizny czoła Spis treści Co to są zmarszczki
BROSZURA INFORMACYJNA DLA PACJENTA Zastosowanie produktu BOTOX /Vistabel 4 jednostki Allergan/0,1 ml toksyna botulinowa typu A w leczeniu zmarszczek pionowych gładzizny czoła Spis treści Co to są zmarszczki
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Należy zapoznać się z treścią ulotki przed zastosowaniem leku.
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA KAMAGRA 100 mg, tabletki powlekane Sildenafil w postaci cytrynianu Należy zapoznać się z treścią ulotki przed zastosowaniem leku. 1- Należy zachować tę ulotkę,
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA KAMAGRA 100 mg, tabletki powlekane Sildenafil w postaci cytrynianu Należy zapoznać się z treścią ulotki przed zastosowaniem leku. 1- Należy zachować tę ulotkę,
Aneks III. Zmiany do odpowiednich części Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta.
 Aneks III Zmiany do odpowiednich części Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta. Uwaga: Poszczególne punkty Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta są wynikiem zakończenia
Aneks III Zmiany do odpowiednich części Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta. Uwaga: Poszczególne punkty Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta są wynikiem zakończenia
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika D - Szczepionka błonicza adsorbowana zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Nie mniej niż 30 j.m. toksoidu błoniczego/0,5
Ulotka dołączona do opakowania: informacja dla użytkownika D - Szczepionka błonicza adsorbowana zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Nie mniej niż 30 j.m. toksoidu błoniczego/0,5
VI.2 Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego Bimican przeznaczone do publicznej wiadomości
 VI.2 Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego Bimican przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby jest stosowany w celu zmniejszenia
VI.2 Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego Bimican przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby jest stosowany w celu zmniejszenia
1. NAZWA PRODUKTU LECZNICZEGO. Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka zawiera 2,3 mg ranibizumabu w 0,23 ml roztworu.
1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka zawiera 2,3 mg ranibizumabu w 0,23 ml roztworu.
1. NAZWA PRODUKTU LECZNICZEGO. Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka zawiera 2,3 mg ranibizumabu w 0,23 ml roztworu.
1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka zawiera 2,3 mg ranibizumabu w 0,23 ml roztworu.
B. ULOTKA DLA PACJENTA
 B. ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla pacjenta Lucentis 10 mg/ml roztwór do wstrzykiwań ranibizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
B. ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla pacjenta Lucentis 10 mg/ml roztwór do wstrzykiwań ranibizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL
 PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO Szanowny Farmaceuto, Należy
PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO Szanowny Farmaceuto, Należy
B. ULOTKA DLA PACJENTA
 B. ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla pacjenta Lucentis 10 mg/ml roztwór do wstrzykiwań w ampułko-strzykawce ranibizumab Należy uważnie zapoznać się z treścią ulotki przed
B. ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla pacjenta Lucentis 10 mg/ml roztwór do wstrzykiwań w ampułko-strzykawce ranibizumab Należy uważnie zapoznać się z treścią ulotki przed
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
Ulotka dla pacjenta: Informacja dla użytkownika. Fladios, 1000 mg, tabletki Diosminum
 Ulotka dla pacjenta: Informacja dla użytkownika Fladios, 1000 mg, tabletki Diosminum Należy uważnie zapoznać się z treścią ulotki przed zastosowanie leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Ulotka dla pacjenta: Informacja dla użytkownika Fladios, 1000 mg, tabletki Diosminum Należy uważnie zapoznać się z treścią ulotki przed zastosowanie leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 60 Wnioski naukowe W dniu 7 czerwca 2017 r. Komisja Europejska (KE) otrzymała informację o śmiertelnym przypadku piorunującej niewydolności wątroby u pacjenta po zastosowaniu leczenia
Aneks IV Wnioski naukowe 60 Wnioski naukowe W dniu 7 czerwca 2017 r. Komisja Europejska (KE) otrzymała informację o śmiertelnym przypadku piorunującej niewydolności wątroby u pacjenta po zastosowaniu leczenia
Ulotka dołączona do opakowania: Informacja dla opiekunów dzieci urodzonych przedwcześnie. Lucentis 10 mg/ml roztwór do wstrzykiwań ranibizumab
 Ulotka dołączona do opakowania: Informacja dla opiekunów dzieci urodzonych przedwcześnie DZIECI URODZONE PRZEDWCZEŚNIE Lucentis 10 mg/ml roztwór do wstrzykiwań ranibizumab Informacja dotycząca pacjentów
Ulotka dołączona do opakowania: Informacja dla opiekunów dzieci urodzonych przedwcześnie DZIECI URODZONE PRZEDWCZEŚNIE Lucentis 10 mg/ml roztwór do wstrzykiwań ranibizumab Informacja dotycząca pacjentów
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
