Marcin Wróblewski, Renata Kołodziejska, Renata Studzińska, Aleksandra Karczmarska-Wódzka, Marcin Dramiński
|
|
|
- Urszula Kowalewska
- 7 lat temu
- Przeglądów:
Transkrypt
1 2013, 67, 9-10 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. BISYNTEZA PRLINY. WEWNĄTRZCZĄSTECZKWA KNDENSACJA ALDLWA PRLINE AS A CMMN AMIN ACID AND AN EXCEPTINAL CATALYST. PART I. PRLINE BISYNTHESIS. INTRAMLECULAR ALDL REACTIN Marcin Wróblewski, Renata Kołodziejska, Renata Studzińska, Aleksandra Karczmarska-Wódzka, Marcin Dramiński Katedra i Zakład Chemii gólnej Uniwersytetu Mikołaja Kopernika, Collegium Medicum w Bydgoszczy ul. Dębowa 3, Bydgoszcz marcin.wroblewski@cm.umk.pl Spis treści Abstract Wprowadzenie 1. Synteza i biosynteza proliny 2. Funkcje proliny 3. Mechanizm reakcji kondensacji aldolowej 4. Wewnątrzcząsteczkowa kondensacja aldolowa Uwagi końcowe Piśmiennictwo cytowane
2 802 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI Mgr Aleksandra Karczmarska-Wódzka, ukończyła chemię na Uniwersytecie Mikołaja Kopernika w Toruniu. Pracę magisterską wykonała w Zakładzie Chemii rganicznej. becnie pracuje w Katedrze i Zakładzie Chemii gólnej Collegium Medicum w Bydgoszczy Uniwersytetu Mikołaja Kopernika w Toruniu. W ramach pracy doktorskiej zajmuje się enancjoselektywną redukcją analogów nukleozydowych. Dr Renata Kołodziejska, pracownik Katedry i Zakładu Chemii gólnej Collegium Medicum w Bydgoszczy Uniwersytetu Mikołaja Kopernika w Toruniu. Zainteresowania naukowe Autorki związane są z badaniami nad regio- i stereoselektywnymi właściwościami biokatalizatorów oraz modyfikacją analogów nukleozydów pirymidynowych. Dr Renata Studzińska, pracownik Katedry i Zakładu Chemii gólnej Collegium Medicum w Bydgoszczy Uniwersytetu Mikołaja Kopernika w Toruniu. Zainteresowania naukowe Autorki związane są z badaniami nad syntezą zmodyfikowanych analogów nukleozydów pirymidynowych. Dr Marcin Wróblewski, pracownik Katedry i Zakładu Chemii gólnej Collegium Medicum w Bydgoszczy Uniwersytetu Mikołaja Kopernika w Toruniu. Zainteresowania naukowe Autora obejmują syntezę organiczną z wykorzystaniem enzymów jak również syntezę modyfikowanych nukleozydów pirymidynowych. Prof. dr hab. Marcin Dramiński, kieruje pracą w Zakładzie Chemii gólnej Collegium Medicum. Interesuje się chemią i stereochemią syntez związanych z analogami nukleozydów pirymidynowych i dydaktyką przedkliniczną dla studentów medycyny i kierunków pokrewnych.
3 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. 803 ABSTRACT In asymmetric synthesis of organic compounds more effective solutions are being looked for which will result in higher yield(s) of product(s) and their high enantioselectivity [1]. ne of such solutions is an use of a multilevel and cheap catalyst. Proline used as a catalyst is a substance of natural origin which was synthetically obtained by Willstätter who was carrying out research on hygric acid (Scheme 1) [10]. The cells of many organisms have a suitable enzymatic system essential for proline biosynthesis [15]. So far, three proline biosynthesis pathways have been described: from glutamate (Scheme 3 and 4), ornithine (Scheme 5 and 6), and arginine (Scheme 7) [16 28]. Proline which is obtained as a result of biosynthesis or supplementation is a substrate for many proteins. Characteristic and significant content (about 23%) of this amino acid was observed in collage. In cells proline can play an important role of osmoregulator [31 35] a protective substance regulating the activity of such enzymes as catalase and peroxidase [36]. Proline as a secondary amine shows exceptional nucleophilicity facilitating imine and enamine formation. Used as a catalyst in aldol reaction makes with substrates like imine or enamine transition state imitating the activity of naturally occurring enzymes for this type of reaction, that is aldolases. In their research Hajos and Parrish, and Eder, Sauer and Wiechert used proline in intramolecular aldol reaction obtaining proper enones (Scheme 9) [60 62]. The process of intramolecular aldol reaction was used for a separation of racemic mixture of diketones (Scheme 10) [63, 64], cyclization of ortho-substituted aromatic aldehydes and ketones (Scheme 11) [65], synthesis of cyclic diketones (Scheme 13) [68] and domino reaction to obtain substituted cyclohexanones from beta-diketones and unsaturated ketones (Scheme 14) [69]. Keywords: proline biosynthesis, mechanism of aldol reaction, intramolecular aldol reaction Słowa kluczowe: biosynteza proliny, mechanizm kondensacji aldolowej, wewnątrzcząsteczkowa reakcja aldolowa
4 804 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI WPRWADZENIE W ostatnim dziesięcioleciu zaobserwowano wzrost zainteresowania małocząstecz kowymi katalizatorami organicznymi organokatalizatorami. Katalizatory tego typu ogólnie dzieli się na dwie klasy. Pierwsza z nich zawiera związki, których działanie katalityczne opiera się na tworzeniu wiązań kowalencyjnych z reagentami. W drugiej grupie znalazły się związki wykorzystujące w akcie katalitycznym wiązania wodorowe i oddziaływania jonowe. Zadaniem badaczy jest poszukiwanie takich katalizatorów spośród obu tych klas, dzięki którym będzie można otrzymywać wysokie wydajności produktów, jak również wysoką enancjoselektywność. Występująca pow szechnie w organizmach żywych prolina okazała się skutecznym katalizatorem wielu typów reakcji (np.: kondensacji aldolowej, Mannicha, Michaela). Większość orga nokatalizatorów, w tym prolina, stanowią cząsteczki dwufunkcyjne, zawierające centra aktywne w postaci kwasu Brönsteda jak i zasady Lewisa. Takie cząsteczki akty wują zarówno donor jak i akceptor, co stanowi siłę napędową zachodzących proce sów syntezy. We wszystkich reakcjach katalizowanych proliną, transfer protonu z części aminowej lub grupy karboksylowej proliny powoduje utworzenie imidu lub alko ksydu, niezbędnych do stabilizacji ładunku i utworzenia wiązania węgiel węgiel w stanie przejściowym. Prolina stanowi wydajny, asymetryczny katalizator różnych reak cji zachodzących według mechanizmu enaminowego, jak również iminowego [1 5]. 1. SYNTEZA I BISYNTEZA PRLINY Spośród 21, naturalnie występujących i kodowanych przez odpowiednią trójkę zasad w DNA, aminokwasów tylko enancjomer L-proliny (1) posiada unikalną strukturę. Tworzy ją pięcioczłonowy pierścień pirolidynowy zawierający atom azotu w postaci drugorzędowej grupy aminowej. W punkcie izoelektrycznym (pk i = 6,3) prolina występuje jako jon obojnaczy (2) (Rys. 1). Podobną strukturę ma fragment cząsteczki pirolizyny (3) (Rys. 2) kodowanej przez kodon stop UAG, jednak kwalifikacja pirolizyny jako 22 naturalnie występującego aminokwasu wciąż pozostaje dyskusyjna [6 8]. Rysunek 1. Figure 1. Struktura proliny Structure of proline
5 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. 805 Rysunek 2. Figure 2. Struktura pirolizyny Structure of pyrrolysine L-prolina należy również do grupy aminokwasów endogennych, których obecność w substancjach odżywczych dla organizmów nie jest niezbędna. Jest to drugi aminokwas [9], po tyrozynie, otrzymany syntetycznie. Dokonał tego Will stätter w 1900 roku. Willstättera interesowało położenie grupy karboksylowej w kwasie higrynowym, otrzymanym przez utlenienie naturalnie występujących, halucynogennych alkaloidów: higryny i kuskohigryny [10]. pierając się na fakcie zbadanym przez Liebermana i Cybulskiego [11], że podczas suchej destylacji kwasu higrynowego wydziela się łatwo dwutlenek węgla, skłonił się do stwierdzenia obecności α grupy karboksylowej w stosunku do atomu azotu pierścienia pirolidynowego. Willstätter poddał kondensacji sól sodową malonianu dietylu (4) z 1,3-dibromopropanem (5) otrzymując bromopropylomalonian dietylu (6). Następnie potraktował ten produkt bromem przekształcając go w 1,4-dibromopropylomalo nian dietylu (7). Przy udziale amoniakalnego roztworu alkoholu metylowego przekształcił ester w amid, który następnie poddał zmydlaniu z wodorotlenkiem baru otrzymując kwas a-pirolidynokarboksylowy (8) (Schemat 1) [9]. Schemat 1. Scheme 1. Schemat otrzymywania kwasu α-pirolidynokarboksylowego wg Willstättera Synthesis of α-pyrrolydinecarboxylic acid (according to Willstätter) W roku 1901 Fischer, jako pierwszy, wyizolował prolinę z hydrolizatu kazeiny [12]. W 1911 roku razem z Londonem określił, że prolina jest pierwszym produktem hydrolizy białek, zarówno kwasowej (z zastosowaniem kwasu chlorowodorowego), jak i enzymatycznej (z zastosowaniem soków trawiennych). Fischer, również jako pierwszy zasugerował używanie nazwy prolina dla określenia kwasu α-pirolidynokarboksylowego [13]. Racemiczną prolinę otrzymywano w latach
6 806 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI czterdziestych dwudziestego wieku wykorzystując reakcję addycji Michaela akrylonitrylu (9) do malonianu dietylu (10) (Schemat 2) [8]. Schemat 2. Scheme 2. Schemat syntezy proliny w reakcji addycji Michaela Michael addition reaction for the synthesis of proline Komórki różnych organizmów posiadają szlaki enzymatyczne pozwalające zarówno na biosyntezę proliny, jak również jej katabolizm. W zależności od rodzaju organizmu odkryto trzy szlaki metaboliczne. rganizmy odżywiające się cudzożywnie (m.in. ludzie, zwierzęta) dostarczają wraz z pożywieniem odpowiednie ilości tego aminokwasu. Tym samym, przy odpowiedniej suplementacji, nie występuje konieczność wykorzystywania szlaków metabolicznych do biosyntezy proliny jako substratu do biosyntezy białek [14, 15]. Dotychczas opisane trzy szlaki biosyntezy proliny opierają się na trzech substratach: kwasie glutaminowym, ornitynie i argininie. W 1987 roku Leisinger w swojej pracy opisał szlak biosyntezy proliny u bakterii wykorzystujący kwas glutaminowy (11). Pierwszy etap biosyntezy proliny obejmuje fosforylację grupy γ-karboksylowej przy udziale kinazy γ-glutaminianowej (γ-gk, EC ) do γ-fosforanu kwasu glutaminowego (γ-gp, 12). Następnie produkt ten ulega redukcji do γ-semialdehydu kwasu glutaminowego (GSA, 13) przy udziale dehydrogenazy γ-semialdehydu kwasu glutaminowego (GSADH, EC ). GSA spontanicznie cyklizuje do pirolino-5-karboksylanu (P5C, 14), który dalej przy udziale reduktazy pirolino-5-karboksylanowej (P5CR, EC ) zostaje przekształcony do L-proliny (1) (Schemat 3) [16, 17].
7 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. 807 Schemat 3. Scheme 3. Szlak glutaminianowy syntezy proliny w komórkach bakterii i drożdży Proline biosynthesis pathway from glutamate in bacteria and yeasts Dehydrogenaza γ-semialdehydu kwasu glutaminowego, kinaza γ-glutaminianowa i reduktaza pirolino-5-karboksylanowa kodowane są przez trzy geny: odpowiednio proa, prob i proc wyizolowane po raz pierwszy z mutantów Escherichia coli [17]. Prace Stewarta z 1981 roku oraz Hu i in. z 1992 roku pokazały różnice w syntezie proliny w komórkach roślin w porównaniu do komórek bakterii i drożdży. Badania wykazały istnienie u roślin dwufunkcyjnego enzymu, syntetazy pirolino-5-karboksylanowej (P5CS), skupiającego aktywność kinazy γ-gk i dehydrogenazy GSADH (Schemat 4) [18, 19]. Schemat 4. Scheme 4. Szlak glutaminianowy syntezy proliny w komórkach roślinnych Proline biosynthesis pathway from glutamate in plant
8 808 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI Gen kodujący P5CS, który został wyizolowany z fasoli Vigna aconitifolia [19] oraz rzodkiewnika pospolitego Arabidopsis thaliana [19, 20] zawiera dwie domeny białkowe P5CS1 i P5CS2 analogiczne z białkami prob, proa bakterii E. coli. Turchetto-Zolet i in. [21] zbadali i opisali sekwencje genów, odpowiedzialnych za powstawanie tego kluczowego enzymu w biosyntezie proliny, dla wielu różnych gatunków roślin m.in.: Schizolobium parahyba, Bombacopsis quinata, Ceiba pentandra (Puchowiec pięciopręcikowy), Cedrela odorata (Cedrówka wonna). Biosynteza proliny odbywa się w cytoplazmie lub w plastydach; w przypadku roślin zielonych są to chloroplasty [22, 23]. Rośliny wykorzystują do syntezy proliny również drugi szlak oparty na ornitynie, której przemiana w prolinę odbywać się może w dwojaki sposób. Pierwszy polega na transaminacji grupy a-aminowej z ornityny (15) w obecności α-aminotransferazy ornitynowej (α-at) dając w produktach kwas α-okso-δ-aminowalerianowy (16). Kwas ten ulega spontanicznej cyklizacji do pirolino-2-karboksylanu (P2C, 17), który po reakcji redukcji przy udziale reduktazy pirolino-2-karboksylanowej (P2CR), przekształcony zostaje do L-proliny. Alternatywna transaminacja grupy δ-aminowej przy udziale δ-amino transferazy ornitynowej (d-at) przekształca ornitynę w GSA (13). GSA jako jeden z substratów w szlaku glutaminianowym zostaje przekształcony również do L-proliny (Schemat 5) [16, 24]. Schemat 5. Scheme 5. Dwie drogi szlaku ornitynowego syntezy proliny Two routes of proline biosynthesis pathway from ornithine Procesy, w których ornityna jest prekursorem proliny, odkryto również w komórkach: pierwotniaka Tetrahymena pyriformis [25], HeLa wywodzących się z komórek raka szyjki macicy [26]. W komórkach laseczki Clostridium sticklandii zaobserwowano przemianę ornityny bezpośrednio w prolinę, przy udziale enzymu cyklodeaminazy ornitynowej (CD, EC ) (Schemat 6) [27].
9 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. 809 CH NH 2 CH NH NH 2 15 CD cytoplazma 1 Schemat 6. Scheme 6. Bezpośrednia przemiana ornityny w prolinę u C. sticklandii Direct synthesis of proline from ornithine Trzeci rodzaj przemian zachodzących w komórkach, prowadzący do otrzymania proliny, polega na biochemicznym przekształceniu cząsteczek aminokwasu argininy (18). Istnieje kilka sposobów przemiany argininy w prolinę. Jeden z nich polega na wykorzystaniu deiminazy argininowej (EC ), która przekształca ją w cytrulinę (19). Cytrulina w reakcji z nieorganicznym fosforanem daje w produktach karbamoilofosforan i ornitynę (20) [27]. CH CH karbamoilofosforan CH NH 2 NH 2 P i NH 2 HN NH deiminaza argininowa HN transferaza ornityna-karbamoilofosforan NH 2 NH 2 NH arginaza Schemat 7. Scheme 7. Przemiana argininy w komórkach Transformation of arginine in cell W komórkach bakterii Staphylococcus aureus, Bacillus subtilis, Bacillus licheniformis oraz w komórkach grzybów Aspergillus nidulans, Saccharomyces cerevisiae i Neurospora crassa arginina (18) przy udziale arginazy (EC ) ulega biotransformacji bezpośrednio do ornityny (20) (Schemat 7). Następnie ornityna zostaje włączona w szlak przemian prowadzący do proliny (szlak ornitynowy). U wymienionych bakterii i grzybów, arginina, a nie kwas glutaminowy jest kluczowym substratem do syntezy proliny [28].
10 810 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI 2. FUNKCJE PRLINY Wysoka zawartość proliny występuje w głównym białku tkanki łącznej kolagenie. Charakterystyczną cechą struktury kolagenu jest występowanie triad aminokwasowych zawierających glicynę oraz dwa inne aminokwasy w układzie -Gly-X-Y-. Aminokwas X to najczęściej prolina, natomiast Y to 4-hydroksyprolina. Występowanie regularnie powtarzających się triad wpływa na przyjmowanie ściśle określonej konformacji kolagenu, gdzie trzy cząsteczki tworzą tropokolagen w strukturze α-helisy. Należy zwrócić uwagę na fakt, że 4-hydroksyprolina powstaje z proliny w enzymatycznym procesie posttranslacyjnym do cząsteczki kolagenu. Na różnorodność typów kolagenu ma wpływ częstość występowania proliny w pozycji X i Y, oraz 4-hydroksyproliny w pozycji Y triad aminokwasowych. Zawartość proliny i 4-hydroksyproliny w kolagenie oscyluje na poziomie 23% [29, 30]. W komórkach roślin, bakterii, protistów i grzybów prolina nagromadza się w cytoplazmie i pełni funkcje osmoregulatora. Charakter osmoregulacyjny przejawia się u roślin podczas stresu osmotycznego, jakim jest susza lub wysokie zasolenie wód i gleby. Aminokwas ten również pełni rolę regulatora zmian środowiskowych, typu: niska temperatura, promieniowanie UV, występowanie metali ciężkich (kadm) i patogenów roślinnych (wirusy, bakterie), stres metaboliczny związany ze zmianami zawartości składników odżywczych [17, 31 35]. Prolina pełni też funkcje ochronne w komórkach, przejawiające się poprzez regulację aktywności enzymów, do których należą katalaza, peroksydaza czy oksydaza polifenolowa [36]. Znaczącą rolę aminokwas ten pełni jako składnik nektaru kwiatowego. Badania wykazały, że nektar zawierający wysokie stężenie proliny (2 mm) był bardziej atrakcyjny dla pszczół. Pszczoły wykorzystują prolinę jako substrat bioenergetyczny w początkowej fazie lotu [37]. Pomimo odkrycia licznych, metabolicznych i regulatorowych funkcji proliny w organizmach ludzi, zwierząt, roślin, grzybów i bakterii, dotychczas nie poznano szczegółowo mechanizmów jej działania [38]. 3. MECHANIZM REAKCJI KNDENSACJI ALDLWEJ Jedną z ważniejszych reakcji syntezy wiązania C C jest kondensacja aldolowa. Jest to reakcja pomiędzy wygenerowanym w układzie enolem lub enolanem (donorem) a cząsteczką elektrofilową (akceptorem) z utworzeniem aldolu [8, 39 58]. W organizmie żywym tego typu reakcje z utworzeniem wiązania C C są przeprowadzane w obecności biokatalizatora. W reakcji enzymatycznej aldolazy synergicznie aktywują oba reagenty: donor i akceptor. Dodatkowo stereogeniczna struktura białka katalitycznego zapewnia kontrolę stereochemiczną reakcji poprzez odpowiednią orientację przestrzenną substratów. Znanych jest około 30 aldolaz, które ze względu na mechanizm reakcji można najogólniej podzielić na dwie klasy: aldolazy typu I i aldolazy typu II.
11 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. 811 Aldolazy typu I katalizują reakcję kondensacji aldolowej poprzez utworzenie enaminowego produktu pośredniego. Kluczowy związek przejściowy zasada Schiffa powstaje w reakcji enolizującego związku karbonylowego z lizyną, która znajduje się w centrum aktywnym aldolazy. Atak cząsteczki elektrofilowej na tak zaktywowany donor (enamina) prowadzi do powstania iminy, która hydrolizując uwalnia ketodiol [48, 54, 55]. Natomiast aldolazy typu II posiadają w centrum aktywnym kofaktor cynkowy. W procesie katalitycznym jon cynku wiąże się z cząsteczką donora tworząc przejściowy związek kompleksowy. Utworzony enolan jest podatny na atak cząsteczki elektrofilowej. statecznie jak w przypadku aldolazy typu I, tworzy się ketodiol [48, 54, 55]. Aldolazy zarówno typu I jak i typu II skutecznie katalizują enancjoselektywną reakcję syntezy wiązania C C w układzie fizjologicznym, nie mają jednak zastosowania w warunkach laboratoryjnych. W celu przeprowadzenia stereoselektywnej kondensacji aldolowej w laboratorium wykorzystuje się małe cząsteczki organiczne, które swoją budową imitują centra aktywne katalizatorów białkowych. Aldolazy typu II jako pierwsze udało się zastąpić katalizatorami metaloorganicznymi. Do najczęściej stosowanych metaloorganicznych związków kompleksowych należą cząsteczki zawierające jony cynku, baru i lantanowców. Jednym z przykładów katalizatora działającego jak aldolazy typu I jest prolina tzw. mikroaldolaza typu I. W porównaniu z innymi aminokwasami prolina jako amina II rzędowa wykazuje wyjątkową nukleofilowość, która ułatwia formowanie imin i enamin. W reakcji kondensacji aldolowej prolina synergicznie aktywuje substraty karbonylowe (donor i akceptor), tworząc w kluczowym etapie enaminę jako produkt przejściowy (Schemat 8). Kataliza mikroenzymem (1) rozpoczyna się od ataku grupy aminowej L-proliny na atom węgla grupy karbonylowej ketonu (aceton). Dehydratacja otrzymanego połączenia prowadzi do jonu iminowego (21). Jon iminowy ulega deprotonacji, co powoduje utworzenie enaminy (22). Następny etap jest wynikiem reakcji pomiędzy elektrofilem a enaminą z utworzeniem wiązania C C (23). Na tym etapie istotną rolę odgrywa grupa karboksylowa proliny. Grupa karboksylowa ułatwia aminokatalizę działając jako kokatalizator typu kwas Brönsteda przez protonowanie akceptorowej grupy karbonylowej aldehydu. W wyniku ataku lica re aldehydu na lico si (E)-enaminy powstaje produkt pośredni o strukturze odpowiadającej konformacji krzesłowej cykloheksanu. Dwustopniowa hydroliza produktów pośrednich (23 i 25) umożliwia otrzymanie aldolu (26) i zregenerowanego katalizatora (1). W reakcji kondensacji katalizowanej L-proliną preferencyjnie otrzymuje się aldol o konfiguracji anti [43, 45, 47 58].
12 812 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI R H 26 H 2 C 1 N H R H H N H 25 C 2 - H 2 N 21 C 2 - N C 2 - N C 2 H R 24 H R H 22 N H RCH 23 Schemat 8. Scheme 8. Mechanizm kondensacji aldolowej katalizowanej L-proliną Mechanism of proline-catalyzed aldol reaction 4. WEWNĄTRZCZĄSTECZKWA REAKCJA ALDLWA W latach siedemdziesiątych po raz pierwszy L-prolina została użyta jako katalizator w wewnątrzcząsteczkowej reakcji aldolowej Hajos-Parrish-Eder-Sauer-Wiechert [59 61]. W dwóch niezależnych ośrodkach w wyniku kondensacji triketonów, otrzymano enony z wysokim nadmiarem enancjomerycznym (Schemat 9). Metoda II przez wiele lat była stosowana w przemyśle, w syntezie bicyklicznych ketoli i α-, β-nienasyconych ketonów.
13 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. 813 Schemat 9. Scheme 9. Wewnątrzcząsteczkowa kondensacja aldolowa Hajos-Parrish-Ender-Sauer-Wiechert Hajos-Parrish-Ender-Sauer-Wiechert intramolecular aldol reaction Innym przykładem wewnątrzcząsteczkowej reakcji katalizowanej L-proliną jest reakcja rozdziału kinetycznego mieszaniny racemicznej diketonów. W zależności od zastosowanych warunków i struktury substratów, obok cyklicznego aldolu, otrzymano czyste optycznie diketony o konfiguracji R lub S (Schemat 10) [62, 63]. CH 3 CH 3 R L-prolina (65 mol%) DMF H 43% ee + H (R) R-CH 3, H + 46% ee (S) Schemat 10. Rozdział kinetyczny mieszaniny racemicznej diketonów Scheme 10. Kinetic separation of racemic mixture of diketones L-prolina umożliwia przeprowadzenie reakcji cyklizacji orto-podstawionych aromatycznych aldehydów lub ketonów, prowadząc do otrzymania chiralnych 2,3-dihydro-3-hydroksybenzofuranów. Reakcja charakteryzuje się wysoką diastereoselektywnością. W wyniku reakcji uzyskuje się w przewadze cis-izomer (dr = (93:7) (>99:1). Czystość optyczna otrzymanych aldoli wynosiła 76 87% ee (Schemat 11) [64].
14 814 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI R 1 L-prolina (30 mol%) H R 1 R 3 R 2 DMF R 3 74% - 96%; R 2 R 1 - H, CH 3 ; R 2 = CH 3, C 2 H 5 ; R 3 - H, CH 3 Schemat 11. Cyklizacja orto-podstawionych związków dikarbonylowych Scheme 11. Cyclization of ortho-substituted dicarbonyl compounds becność dwóch grup karbonylowych w cząsteczce umożliwia przeprowadzenie wewnątrzcząsteczkowej aldolizacji enolegzo. Na przykład w reakcji alifatycznych związków dikarbonylowych otrzymano anti pochodne cykloheksanolu o wysokiej czystości optycznej (Tab. 1) [65]. Tabela 1. Table 1. Cykloaldolizacja enolegzo związków dikarbonylowych Enolexo cyclo-aldolization of dicarbonyl compounds H HC CH HC Me m L-prolina (10 mol%) CH 2 Cl 2 Me m Numer 1 m = 0-2 Produkty H HC Wydajność (%) dr (%) ee (%) 95 10:1 99 H 2 HC 74 >20:1 98 H 3 HC 75 >20:1 97
15 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. 815 H HC CH HC Me m L-prolina (10 mol%) CH 2 Cl 2 Me m Numer 4 m = 0-2 Produkty H HC Wydajność (%) dr (%) ee (%) 76 22:5:5:1 75,89,95,8 H 5 HC 88 1: HC H 92 2:1 99 Natomiast w reakcji dialdehydów pochodnych kwasu winowego wewnątrzcząsteczkowa 6-enolegzo cykloaldolizacja prowadzi do powstania imino cukru o przeciwnej konfiguracji syn (dr > 10:1) (Schemat 12) [46]. NTs 1. L-prolina (15 mol%) CHCl 3 /DMS(3:1) 2. NaBH 4, MeH H NTs 70%; dr (syn:anti) 10:1 H Schemat enolegzo cykloaldolizacja pochodnych kwasu winowego Scheme enolexo cyclo-aldolization of tartaric acid derivatives Cykliczne diketony można zsyntetyzować w dwuetapowej reakcji aldolowej. W pierwszym etapie otrzymuje się triketony z cykloalkano-1,3-dionów i but-1-en- 3-onu, które w następnym etapie ulegają wewnątrzcząsteczkowej reakcji cyklizacji (Schemat 13) [67].
16 816 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI + L-prolina DMS -H 2 (S) 49%; 76% ee H Schemat 13. Dwuetapowa synteza związków dikarbonylowych Scheme 13. Two-step synthesis of dicarbonyl compounds R 1 R 2 + R 1 R 2 NMP - 1-metylo-2-pirolidon L-prolina NMP H + R 1 R R 1 = C 6 H 5 ; R 2 = C 6 H 5 14% 63%; 58% ee R 1 = p-ch 3 C 6 H 4 ; R 2 = p-ch 3 C 6 H 4 39% 39%; 43% ee R 1 = p-clc 6 H 4 ; R 2 = p-clc 6 H 4 7% 82%; 53% ee R 1 = p-brc 6 H 4 ; R 2 = p-brc 6 H 4 7% 85%; 63% ee R 1 = p-clc 6 H 4 ; R 2 = p-ch 3 C 6 H 4 26% 57%; 67% ee R 1 = C 4 H 3 S; R 2 = C 4 H 3 S 52% 47%; 67% ee R 1 = C 4 H 3 ; R 2 = C 4 H 3 35% 52%; 47% ee R 1 = C 5 H 4 N; R 2 = C 5 H 4 N 0% 81%; 80% ee R 1 = C 5 H 4 N; R 2 = p-ch 3 C 6 H 4 0% 93%; 50% ee Schemat 14. Dwuetapowa synteza pochodnych cykloheksanonu Scheme 14. Two-step synthesis of cyclohexanone derivatives W reakcji aldolowej domino Michaela otrzymuje się podstawione cykloheksanony. W obecności L-proliny β-diketony reagują z but-1-en-3-onem dając triketony (Schemat 14, związek 1), które cyklizują do chiralnych 3-hydroksycykloheksanonów (Schemat 14, związek 2) [68].
17 PRLINA PSPLITY AMINKWAS WYJĄTKWY KATALIZATR. CZĘŚĆ I. 817 UWAGI KŃCWE Prolina to aminokwas występujący powszechnie w organizmach flory i fauny. Powszechność proliny związana jest z różnorodnością szlaków jej biosyntezy. Wieloletnie badania pokazują wiele właściwości proliny m.in. budulcowe, ochronne, regulacyjne i energetyczne. Dzięki specyficznej budowie, z powodzeniem zastępuje enzymy z klasy aldolaz. dkrycie jej katalitycznych właściwości spowodowało lawinowe badania nad ich wykorzystaniem do syntezy wiązania węgiel węgiel w reakcji wewnątrzcząsteczkowej kondensacji aldolowej. Reakcje te charakteryzują się wysoką stereoselektywnością. trzymane z dużymi wydajnościami produkty charakteryzują się wysoką czystością optyczną. PIŚMIENNICTW CYTWANE [1] P. Dalko, L. Moisan, Angew. Chem. Int. Ed., 2004, 43, [2] A. Erkkilä, I. Majander, P. Pihko, Chem. Rev., 2007, 107, [3] P. Ha-Yeon Cheong, C. Legault, J. Um, N. Çelebi-Ölçüm, K. Houk, Chem. Rev., 2011, 111, [4] S. Mukherjee, J. Woon Yang, S. Hoffmann, B. List, Chem. Rev., 2007, 107, [5] A. Doyle, E. Jacobsen, Chem. Rev., 2007, 107, [6] G. Drewa, T. Ferenc, Genetyka medyczna. Podręcznik dla studentów, Elsevier Urban & Partner, Wrocław, [7] S. Lehmann, D. Funck, L. Szbados, D. Rentsch, Amino acids, 2010, 39, 949. [8] S. Panday, Tetrahedron: Asymmetry, 2011, 22, [9] H. Vickery, C. Schmidt, Chem. Rev., 1931, 9, 169. [10] R. Willstätter, Ber., 1900, 33, [11] C. Liebermann, G. Cybulski, Ber., 1895, 28, 578. [12] E. Fischer, Z. Physiol. Chem., 1901, 33, 151. [13] E. Fischer, U. Suzuki, Ber., 1904, 37, [14] T. Wyse, C. Netto, Metab. Brain Dis., 2011, 26, 159. [15] A. Beaudet, W. Sly, D. Valle, The metabolic and molecular bases of inherited disease, McGraw- Hill, New York, [16] A. Jaiswal, N. Singh, G. Shekhawat, M. Aktar, J. Jaiswal, Int. Trans. Appl. Sci., 2010, 2, 651. [17] M. Trovato, R. Mattioli, P. Costantino, Rend. Lincei, 2008, 19, 325. [18] L. Paleg, D. Aspinall, Physiology and Biochemistry of Drought Resistance in Plants, Academic Press, Sydney, [19] C. Hu, A. Delauney, D. Verma, Proc. Natl. Acad. Sci., 1992, 89, [20] P. Verslues, S. Sharma, The Arabidopsis Book, 2010, 8, e0140. [21] A. Zurchetto-Zolet, M. Margis-Pinheiro, R. Margis, Mol. Genet. Genomics, 2009, 281, 87. [22] N. Verbruggen, C. Hermans, Amino Acids, 2008, 35, 753. [23] E. Sanchez, L. Lopez-Lefebre, P. Garcia, R. Rivero, J. Ruiz, L. Romero, J. Plant. Physiol., 2001, 158, 593. [24] M. Graupner, R. White, J. Bacteriol., 2001, 183, [25] D. Hill, P. Chambers, Biochim. Biophys. Acta, 1967, 148, 435. [26] H. Eagle, J. Biol. Chem., 1965, 240, [27] J. Kenklies, R. Ziehn, K. Fritsche, A. Pich, R. Andreesen, Microbiology, 1999, 145, 819. [28] D. Townsend, A. Kaenjak, R. Jayaswal, B. Wilkinson, Microbiology, 1996, 142, 1491.
18 818 M. WRÓBLEWSKI, R. KŁDZIEJSKA, R. STUDZIŃSKA, A. KARCZMARSKA-WÓDZKA, M. DRAMIŃSKI [29] S. Krane, Amino Acids, 2008, 35, 703. [30] A. Barbul, J. Nutr., 2008, 138, 2021S. [31] I. Perez-Arellano, F. Carmona-Alvarez, A. Martinez, J. Rodriguez-Diaz, J. Cervera, Protein Sci., 2010, 19, 372. [32] J. Ambikapathy, J. Marshall, C. Hocart, A. Hardham, Fungal Genet. Biol., 2002, 35, 287. [33] V. Rai, Biol. Plant., 2002, 45, 481. [34] J. Xu, H. Yin, X. Li, Plant Cell Rep., 2009, 28, 325. [35] E. Vendruscolo I. Schuster M. Pileggi C. Scapim C. Molinari C. Marur L. Vieira, J. Plant Physiol., 2007, 164, [36] L. Öztürk, Y. Demir, Plant Growth Regul., 2002, 38, 259. [37] C. Carter, S. Shafir, L. Yehonatan, R. Palmer, R. Thornburg, Naturwissenschaften, 2006, 93, 72. [38] J. Phang, S. Donald, J. Pandhare, Y. Liu, Amino Acids, 2008, 35, 681. [39] S.G. Zlotin, A.S. Kucherenko, I.P. Beletskaya, Russian Chemical Reviews, 2009, 78, 737. [40] B. List, Tetrahedron, 2002, 58, [41] B. List, Acc. Chem. Res., 2004, 4, 548. [42] P.I. Dalko, Enantioselective rganocatalysis: Reactions and Experimental Procedures, Wiley-VCH Verlag GmbH & Co. KgaA, Weinheim, [43] J. Gawroński, K. Gawrońska, K. Kacprzak, M. Kwit, Współczesna synteza organiczna, PWN Warszawa, [44] M.J. Gaunt, C.C.C. Johansson, A. McNally, N.T. Vo, Drug Discovery Today, 2007, 12, 8. [45] M. Movassaghi, E.N. Jacobsen, Science, 2002, 298, [46] M. Stodulski, J. Młynarski, Wiad. Chem., 2010, 64, 5. [47] S. Bahmanyar, K.N. Houk, J. Am. Chem. Soc., 2001, 123, [48] H. Gröger, J. Wilken, Angew. Chem. Int. Ed., 2001, 40, 529. [49] L. Hoang, S. Bahmanyar, K.N. Houk, B. List, J. Am. Chem. Soc., 2003, 125, 16. [50] S. Bahmanyar, K.N. Houk, H.J. Martin, B. List, J. Am. Chem. Soc., 2003, 125, [51] B. List, L. Hoang, H.J. Martin, PNAS, 2004, 101, [52] B. List, Chem. Commun., 2006, 819. [53] D.A. Bock, Ch.W. Lehmann, B. List, PNAS, 2010, 107, [54] B. Alcaide, P. Almendros, Eur. J. rg. Chem., 2002, [55] T.D. Machajewski, Ch.-H Wong, Angew. Chem. Int. Ed., 2000, 39, [56] W. Notz, F. Tanaka, C.F. Barbas III, Acc. Chem. Res., 2004, 37, 580. [57] C. Palomo, M. iarbide, J. M. García, Chem. Eur. J., 2002, 8, 37. [58] J. Seayad, B. List, rg. Biomol. Chem., 2005, 3, 719. [59] U. Eder, G. Sauer, R. Wiechert, Angew. Chem. Int. Ed. Engl., 1971, 10, 496. [60] BRD P ; Chem. Abstr., 1972, 76, [61] BRD P ; Chem. Abstr., 1972, 76, [62] C. Agami, J. Levisalles, H. Sevestre, J. Chem. Soc., Chem. Commun., 1984, 418. [63] C. Agami, N. Platzer, C. Puchot, H. Sevestre, Tetrahedron, 1987, 43, [64] D. Enders,. Niemeier, L. Straver, Synlett, 2006, [65] C. Pidathala, L. Hoang, N. Vignola, B. List, Angew. Chem. Int. Ed., 2003, 42, [66] I. Kumar, Ch. V. Rode, Tetrahedron: Asymmetry, 2010, 21, [67] T. Bui, C. F. Barbas III, Tetrahedron Letters, 2000, 41, [68] D. Gryko, Tetrahedron: Asymmetry, 2005, 16, Praca wpłynęła do Redakcji 24 kwietnia 2013
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku
 Streszczenie pracy doktorskiej Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku mgr Agata Dudek Promotor: prof. dr hab. Jacek Młynarski Praca została wykonana w Zespole Stereokotrolowanej
Streszczenie pracy doktorskiej Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku mgr Agata Dudek Promotor: prof. dr hab. Jacek Młynarski Praca została wykonana w Zespole Stereokotrolowanej
Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej
 Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej Zespół VI Opiekun: dr hab. Jacek Młynarski, prof. nadzw. Oskar Popik Wstęp Początki organokatalizy Pierwszy przykład organokatalitycznej
Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej Zespół VI Opiekun: dr hab. Jacek Młynarski, prof. nadzw. Oskar Popik Wstęp Początki organokatalizy Pierwszy przykład organokatalitycznej
Aleksandra Karczmarska-Wódzka*, Renata Studzińska, Renata Kołodziejska, Marcin Wróblewski, Marcin Dramiński
 2014, 68, 1-2 PROLINA POSPOLITY AMINOKWAS WYJĄTKOWY KATALIZATOR. CZĘŚĆ IV. REAKCJA MICHAELA PROLINE AS A COMMON AMINO ACID AND AN EXCEPTIONAL CATALYST. PART IV. MICHAEL REACTION Aleksandra Karczmarska-Wódzka*,
2014, 68, 1-2 PROLINA POSPOLITY AMINOKWAS WYJĄTKOWY KATALIZATOR. CZĘŚĆ IV. REAKCJA MICHAELA PROLINE AS A COMMON AMINO ACID AND AN EXCEPTIONAL CATALYST. PART IV. MICHAEL REACTION Aleksandra Karczmarska-Wódzka*,
Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady
 Synteza i wykorzystanie -aminoketonów (zasad Mannicha) Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady i-pr Falicain środek zneczulający 2 Tramadol środek przeciwbólowy snervan choroba
Synteza i wykorzystanie -aminoketonów (zasad Mannicha) Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady i-pr Falicain środek zneczulający 2 Tramadol środek przeciwbólowy snervan choroba
Renata Studzińska*, Aleksandra Karczmarska-Wódzka, Marcin Wróblewski, Renata Kołodziejska, Marcin Dramiński
 2013, 67, 9-10 PROLINA POSPOLITY AMINOKWAS WYJĄTKOWY KATALIZATOR. CZĘŚĆ III. REAKCJA MANNICHA PROLINE AS A COMMON AMINO ACID AND AN EXCEPTIONAL CATALYST. PART III. MANNICH REACTION Renata Studzińska*,
2013, 67, 9-10 PROLINA POSPOLITY AMINOKWAS WYJĄTKOWY KATALIZATOR. CZĘŚĆ III. REAKCJA MANNICHA PROLINE AS A COMMON AMINO ACID AND AN EXCEPTIONAL CATALYST. PART III. MANNICH REACTION Renata Studzińska*,
b. Rozdział mieszaniny racemicznej na CHIRALNEJ kolumnie (Y. Okamoto, T. Ikai, Chem. Soc. Rev., 2008, 37, )
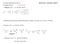 Jak otrzymać związki optycznie czynne??? ławomir Jarosz stereochemia- wykład VII Ze związków chiralnych 1. ozdział racematu a. Klasyczny : A (rac) 50% A() 50%A() b. ozdział mieszaniny racemicznej na CIAEJ
Jak otrzymać związki optycznie czynne??? ławomir Jarosz stereochemia- wykład VII Ze związków chiralnych 1. ozdział racematu a. Klasyczny : A (rac) 50% A() 50%A() b. ozdział mieszaniny racemicznej na CIAEJ
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Metabolizm białek. Ogólny schemat metabolizmu bialek
 Metabolizm białek Ogólny schemat metabolizmu bialek Trawienie białek i absorpcja aminokwasów w przewodzie pokarmowym w żołądku (niskie ph ~2, rola HCl)- hydratacja, homogenizacja, denaturacja białek i
Metabolizm białek Ogólny schemat metabolizmu bialek Trawienie białek i absorpcja aminokwasów w przewodzie pokarmowym w żołądku (niskie ph ~2, rola HCl)- hydratacja, homogenizacja, denaturacja białek i
Aminotransferazy. Dehydrogenaza glutaminianowa. Szczawiooctan. Argininobursztynian. Inne aminokwasy. asparaginian. fumaran. Arginina.
 Inne aminokwasy Szczawiooctan Aminotransferazy asparaginian Cytrulina Argininobursztynian Cykl mocznikowy Arginina fumaran Ornityna Aminotransferazy -ketoglutaran karbamoilofosforan Mocznik kwas glutaminowy
Inne aminokwasy Szczawiooctan Aminotransferazy asparaginian Cytrulina Argininobursztynian Cykl mocznikowy Arginina fumaran Ornityna Aminotransferazy -ketoglutaran karbamoilofosforan Mocznik kwas glutaminowy
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
CHIRALNE KWASY FOSFOROWE WŁAŚCIWOŚCI I ZASTOSOWANIE. Anna Kozioł Zespół II
 CHIRALNE KWASY FSFRWE WŁAŚCIWŚCI I ZASTSWANIE Anna Kozioł Zespół II STATNIE ZASTSWANIA KWASÓW W FSFRWYCH PARTYCH NA BINLU KWASY BRØNSTEDA JAK KATALIZATRY Model aktywacji kwasami Brønsteda Rozwój enancjoselektywnych,
CHIRALNE KWASY FSFRWE WŁAŚCIWŚCI I ZASTSWANIE Anna Kozioł Zespół II STATNIE ZASTSWANIA KWASÓW W FSFRWYCH PARTYCH NA BINLU KWASY BRØNSTEDA JAK KATALIZATRY Model aktywacji kwasami Brønsteda Rozwój enancjoselektywnych,
STEREOCHEMIA ORGANICZNA Wykład 6
 STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne 1.5 1.0 0 +3.0 1.0 +0.5-0.5 +2.5-10.5-9.1-10.9-9.0-9.1-8.2-9.5-8.5 Me x (-8.5 ev) (+2.5 ev) x+n y (~0 ev) y+m (-10.9 ev) Me x x+n
STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne 1.5 1.0 0 +3.0 1.0 +0.5-0.5 +2.5-10.5-9.1-10.9-9.0-9.1-8.2-9.5-8.5 Me x (-8.5 ev) (+2.5 ev) x+n y (~0 ev) y+m (-10.9 ev) Me x x+n
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Organokataliza mechanizmy, katalizatory, reakcje. Maria Rogozińska Zespół VI
 rganokataliza mechanizmy, katalizatory, reakcje Maria ogozińska Zespół VI rganokataliza Katalizowanie reakcji chemicznych małymi cząsteczkami organicznymi, zbudowanymi z węgla, wodoru, fosforu, azotu,
rganokataliza mechanizmy, katalizatory, reakcje Maria ogozińska Zespół VI rganokataliza Katalizowanie reakcji chemicznych małymi cząsteczkami organicznymi, zbudowanymi z węgla, wodoru, fosforu, azotu,
Otrzymywanie -aminokwasów
 trzymywanie -aminokwasów Przykłady -aminokwasów o znaczeniu praktycznym Cl Cl 2 C 2 Melaphalan (lek przeciwnowotworowy) 2 C 2 Levodopa (stosowana w chorobie Parkinsona) 1 1 2 2 3 C środowisko wodne reakcja
trzymywanie -aminokwasów Przykłady -aminokwasów o znaczeniu praktycznym Cl Cl 2 C 2 Melaphalan (lek przeciwnowotworowy) 2 C 2 Levodopa (stosowana w chorobie Parkinsona) 1 1 2 2 3 C środowisko wodne reakcja
STEREOCHEMIA ORGANICZNA
 STEECEMIA GANICZNA Sławomir Jarosz Wykład 6 Typowe energie (ev) i współczynniki orbitalne X LUM 1.5 1.0 C 0 Z +3.0 M -10.5-9.1 C -10.9 Z -9.0 X Typowe energie (ev) i współczynniki orbitalne X LUM 1.0 +0.5
STEECEMIA GANICZNA Sławomir Jarosz Wykład 6 Typowe energie (ev) i współczynniki orbitalne X LUM 1.5 1.0 C 0 Z +3.0 M -10.5-9.1 C -10.9 Z -9.0 X Typowe energie (ev) i współczynniki orbitalne X LUM 1.0 +0.5
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
Renata Kołodziejska, Marcin Wróblewski, Aleksandra Karczmarska-Wódzka, Renata Studzińska, Marcin Dramiński
 2013, 67, 11-12 PROLINA POSPOLITY AMINOKWAS WYJĄTKOWY KATALIZATOR. CZĘŚĆ II. MIĘDZYCZĄSTECZKOWA KONDENSACJA ALDOLOWA PROLINE AS A COMMON AMINO ACID AND AN EXCEPTIONAL CATALYST. PART II. INTERMOLECULAR
2013, 67, 11-12 PROLINA POSPOLITY AMINOKWAS WYJĄTKOWY KATALIZATOR. CZĘŚĆ II. MIĘDZYCZĄSTECZKOWA KONDENSACJA ALDOLOWA PROLINE AS A COMMON AMINO ACID AND AN EXCEPTIONAL CATALYST. PART II. INTERMOLECULAR
Biochemiczne i chemiczne metody syntezy nukleozydów
 Biochemiczne i chemiczne metody syntezy nukleozydów Biosynteza nukleozydów pirymidynowych i purynowych przebiega w komórkach w sposób ciągły. Jest to spowodowane koniecznością ciągłego dostarczania nukleozydów
Biochemiczne i chemiczne metody syntezy nukleozydów Biosynteza nukleozydów pirymidynowych i purynowych przebiega w komórkach w sposób ciągły. Jest to spowodowane koniecznością ciągłego dostarczania nukleozydów
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Przemiana materii i energii - Biologia.net.pl
 Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
Ćwiczenie 6 Aminokwasy
 Ćwiczenie 6 Aminokwasy Aminokwasy są to związki dwufunkcyjne, których cząsteczki zawierają grupy karboksylowe i aminowe: grupa aminowa:nh 2 grupa karboksylowa COOH Nomenklatura aminokwasów: Naturalne aminokwasy
Ćwiczenie 6 Aminokwasy Aminokwasy są to związki dwufunkcyjne, których cząsteczki zawierają grupy karboksylowe i aminowe: grupa aminowa:nh 2 grupa karboksylowa COOH Nomenklatura aminokwasów: Naturalne aminokwasy
Scenariusz lekcji pokazowej z chemii
 Scenariusz lekcji pokazowej z chemii 28.03.2008r. klasa II b prowadząca: Ewa Siennicka dział: Wielofunkcyjne pochodne węglowodorów. TEMAT: BUDOWA I WŁAŚCIWO CIWOŚCI AMINOKWASÓW. 1. Cele edukacyjne a) kształcenia:
Scenariusz lekcji pokazowej z chemii 28.03.2008r. klasa II b prowadząca: Ewa Siennicka dział: Wielofunkcyjne pochodne węglowodorów. TEMAT: BUDOWA I WŁAŚCIWO CIWOŚCI AMINOKWASÓW. 1. Cele edukacyjne a) kształcenia:
Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
 Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego. Schem. 1. Ogólny schemat reakcji odwodnienia enolu.
 TLENEK MEZYTYLU ZADANIE 7B Aldole (związki β-hydrokykarbonylowe), otrzymane na przykład w wyniku reakcji kondensacji aldolowej, są często związkami nietrwałymi. Pod wpływem śladów kwasów 1 (nawet tak słabych
TLENEK MEZYTYLU ZADANIE 7B Aldole (związki β-hydrokykarbonylowe), otrzymane na przykład w wyniku reakcji kondensacji aldolowej, są często związkami nietrwałymi. Pod wpływem śladów kwasów 1 (nawet tak słabych
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
LNA i metody jego syntezy
 LNA i metody jego syntezy LNA (Locked Nucleic Acids) nazwa ta obejmuje jeden z typów modyfikowanych kwasów nukleinowych, w których pentofuranozowy fragment cukrowy ma utrwaloną konformację pierścienia
LNA i metody jego syntezy LNA (Locked Nucleic Acids) nazwa ta obejmuje jeden z typów modyfikowanych kwasów nukleinowych, w których pentofuranozowy fragment cukrowy ma utrwaloną konformację pierścienia
SEMINARIUM 8:
 SEMINARIUM 8: 24.11. 2016 Mikroelementy i pierwiastki śladowe, definicje, udział w metabolizmie ustroju reakcje biochemiczne zależne od aktywacji/inhibicji przy udziale mikroelementów i pierwiastków śladowych,
SEMINARIUM 8: 24.11. 2016 Mikroelementy i pierwiastki śladowe, definicje, udział w metabolizmie ustroju reakcje biochemiczne zależne od aktywacji/inhibicji przy udziale mikroelementów i pierwiastków śladowych,
ENZYMY W CHEMII. Michał Rachwalski. Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii Organicznej i Stosowanej
 ENZYMY W CHEMII Michał Rachwalski Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii rganicznej i Stosowanej Czym są enzymy? Enzymy są białkami zawierającymi od 60 do 1000 reszt aminokwasów; Enzymy są
ENZYMY W CHEMII Michał Rachwalski Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii rganicznej i Stosowanej Czym są enzymy? Enzymy są białkami zawierającymi od 60 do 1000 reszt aminokwasów; Enzymy są
STEREOCHEMIA ORGANICZNA
 STERECEMIA RGANICZNA Sławomir Jarosz Wykład 6 Jak otrzymać związki optycznie czynne??? 1. Ze związków chiralnych a. Klasyczny : A (rac) b. Rozdział mieszaniny racemicznej na CIRALNEJ kolumnie (Y. kamoto,
STERECEMIA RGANICZNA Sławomir Jarosz Wykład 6 Jak otrzymać związki optycznie czynne??? 1. Ze związków chiralnych a. Klasyczny : A (rac) b. Rozdział mieszaniny racemicznej na CIRALNEJ kolumnie (Y. kamoto,
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
Reakcje charakterystyczne aminokwasów
 KATEDRA BIOCHEMII Wydział Biologii i Ochrony Środowiska Reakcje charakterystyczne aminokwasów BIOCHEMIA STRUKTURALNA ĆWICZENIE 1 REAKCJE CHARAKTERYSTYCZNE AMINOKWASÓW A) REAKCJE OGÓLNE ZADANIE 1 WYKRYWANIE
KATEDRA BIOCHEMII Wydział Biologii i Ochrony Środowiska Reakcje charakterystyczne aminokwasów BIOCHEMIA STRUKTURALNA ĆWICZENIE 1 REAKCJE CHARAKTERYSTYCZNE AMINOKWASÓW A) REAKCJE OGÓLNE ZADANIE 1 WYKRYWANIE
CHEMIA ORGANICZNA (II)
 CHEMIA ORGANICZNA (II) Plan 1) Selektywność i selektywne przekształcanie grup funkcyjnych; a) chemo-, regio- i stereoselektywność; b) kontrola kinetyczna i termodynamiczna. 2) Selektywne reakcje utleniania
CHEMIA ORGANICZNA (II) Plan 1) Selektywność i selektywne przekształcanie grup funkcyjnych; a) chemo-, regio- i stereoselektywność; b) kontrola kinetyczna i termodynamiczna. 2) Selektywne reakcje utleniania
Aminokwasy, peptydy i białka. Związki wielofunkcyjne
 Aminokwasy, peptydy i białka Związki wielofunkcyjne Aminokwasy, peptydy i białka Aminokwasy, peptydy i białka: - wiadomości ogólne Aminokwasy: - ogólna charakterystyka - budowa i nazewnictwo - właściwości
Aminokwasy, peptydy i białka Związki wielofunkcyjne Aminokwasy, peptydy i białka Aminokwasy, peptydy i białka: - wiadomości ogólne Aminokwasy: - ogólna charakterystyka - budowa i nazewnictwo - właściwości
Właściwości chemiczne nukleozydów pirymidynowych i purynowych
 Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
Chemiczne składniki komórek
 Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD
 Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD Aleksandra Kotynia PRACA DOKTORSKA
Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD Aleksandra Kotynia PRACA DOKTORSKA
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
CHEMIA ORGANICZNA (II)
 CHEMIA ORGANICZNA (II) Pracownia Stereochemii Organicznej Nagroda Nobla w dziedzinie chemii Jean-Pierre Sauvage, Bernard L. Feringa, J. Fraser Stoddart Plan 1) Selektywność i selektywne przekształcanie
CHEMIA ORGANICZNA (II) Pracownia Stereochemii Organicznej Nagroda Nobla w dziedzinie chemii Jean-Pierre Sauvage, Bernard L. Feringa, J. Fraser Stoddart Plan 1) Selektywność i selektywne przekształcanie
Bioinformatyka wykład 9
 Bioinformatyka wykład 9 14.XII.21 białkowa bioinformatyka strukturalna krzysztof_pawlowski@sggw.pl 211-1-17 1 Plan wykładu struktury białek dlaczego? struktury białek geometria i fizyka modyfikacje kowalencyjne
Bioinformatyka wykład 9 14.XII.21 białkowa bioinformatyka strukturalna krzysztof_pawlowski@sggw.pl 211-1-17 1 Plan wykładu struktury białek dlaczego? struktury białek geometria i fizyka modyfikacje kowalencyjne
X / \ Y Y Y Z / \ W W ... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Rys. 1. C-nukleozydy występujące w trna
 C-Nukleozydy Z próbek transferowego kwasu rybonukleinowego (trna) w roku 1957 wydzielono związek, zawierający w swej strukturze pierścień uracylowy i cukrowy, połączone odmiennie niż w klasycznych nukleozydach.
C-Nukleozydy Z próbek transferowego kwasu rybonukleinowego (trna) w roku 1957 wydzielono związek, zawierający w swej strukturze pierścień uracylowy i cukrowy, połączone odmiennie niż w klasycznych nukleozydach.
21. Wstęp do chemii a-aminokwasów
 21. Wstęp do chemii a-aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2016/2017 1 21.1. Budowa ogólna a-aminokwasów i klasyfikacja peptydów H 2 N H kwas 2-aminooctowy
21. Wstęp do chemii a-aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2016/2017 1 21.1. Budowa ogólna a-aminokwasów i klasyfikacja peptydów H 2 N H kwas 2-aminooctowy
Substytucje Nukleofilowe w Pochodnych Karbonylowych
 J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
Enzymy katalizatory biologiczne
 Enzymy katalizatory biologiczne Kataliza zjawisko polegające na obniżeniu energii aktywacji reakcji i zwiększeniu szybkości reakcji chemicznej i/lub skierowaniu reakcji na jedną z termodynamicznie możliwych
Enzymy katalizatory biologiczne Kataliza zjawisko polegające na obniżeniu energii aktywacji reakcji i zwiększeniu szybkości reakcji chemicznej i/lub skierowaniu reakcji na jedną z termodynamicznie możliwych
BIOPOLIMERY. Rodzaj zajęć: Grupa: WIMiC I-III r. Termin: poniedziałek Sala: Prowadzący: KONSULTACJE. POK. 106a A3. seminarium 105 A3/A4
 BIOPOLIMERY Rodzaj zajęć: seminarium Grupa: WIMiC I-III r. Termin: poniedziałek 15.00-16.30 Sala: Prowadzący: 105 A3/A4 dr hab. inż. Jadwiga Laska KONSULTACJE CZWARTEK 11.00-12.00 POK. 106a A3 Kontakt
BIOPOLIMERY Rodzaj zajęć: seminarium Grupa: WIMiC I-III r. Termin: poniedziałek 15.00-16.30 Sala: Prowadzący: 105 A3/A4 dr hab. inż. Jadwiga Laska KONSULTACJE CZWARTEK 11.00-12.00 POK. 106a A3 Kontakt
STEREOCHEMIA ORGANICZNA Wykład 6
 STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne Reakcja Dielsa Aldera - Regioselektywność w reakcjach DA LUM M 1.5-10.5 M 1.0-9.1 LUM 0-10.9 +3.0-9.0 Me M (-8.5 ev) LUM (+2.5 ev)
STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne Reakcja Dielsa Aldera - Regioselektywność w reakcjach DA LUM M 1.5-10.5 M 1.0-9.1 LUM 0-10.9 +3.0-9.0 Me M (-8.5 ev) LUM (+2.5 ev)
Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl
 Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl Wszelkie treści i zasoby edukacyjne publikowane na łamach Portalu www.szkolnictwo.pl mogą byd wykorzystywane przez jego Użytkowników
Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl Wszelkie treści i zasoby edukacyjne publikowane na łamach Portalu www.szkolnictwo.pl mogą byd wykorzystywane przez jego Użytkowników
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Charakterystyka izoenzymów aminotransferazy asparaginianowej z siewek pszenicy zwyczajnej (Triticum aestivum L.)
 Charakterystyka izoenzymów aminotransferazy asparaginianowej z siewek pszenicy zwyczajnej (Triticum aestivum L.) Marcin Maciąga & Andrzej Paszkowski Katedra Biochemii, Wydział Rolnictwa i Biologii, SGGW
Charakterystyka izoenzymów aminotransferazy asparaginianowej z siewek pszenicy zwyczajnej (Triticum aestivum L.) Marcin Maciąga & Andrzej Paszkowski Katedra Biochemii, Wydział Rolnictwa i Biologii, SGGW
Substancje o Znaczeniu Biologicznym
 Substancje o Znaczeniu Biologicznym Tłuszcze Jadalne są to tłuszcze, które może spożywać człowiek. Stanowią ważny, wysokoenergetyczny składnik diety. Z chemicznego punktu widzenia głównym składnikiem tłuszczów
Substancje o Znaczeniu Biologicznym Tłuszcze Jadalne są to tłuszcze, które może spożywać człowiek. Stanowią ważny, wysokoenergetyczny składnik diety. Z chemicznego punktu widzenia głównym składnikiem tłuszczów
Bliskie spotkania z biologią METABOLIZM. dr hab. Joanna Moraczewska, prof. UKW. Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki
 Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
46 i 47. Wstęp do chemii -aminokwasów
 46 i 47. Wstęp do chemii -aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 21.1. Budowa ogólna -aminokwasów i klasyfikacja peptydów H 2 H H 2 R H R R 1 H
46 i 47. Wstęp do chemii -aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 21.1. Budowa ogólna -aminokwasów i klasyfikacja peptydów H 2 H H 2 R H R R 1 H
Ćwiczenie 4. Reakcja aminokwasów z ninhydryną. Opisz typy reakcji przebiegających w tym procesie i zaznacz ich miejsca przebiegu.
 azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
PRZYKŁADOWE ZADANIA ORGANICZNE ZWIĄZKI ZAWIERAJĄCE AZOT
 PRZYKŁADOWE ZADANIA ORGANICZNE ZWIĄZKI ZAWIERAJĄCE AZOT Zadanie 1127 (1 pkt) Uszereguj podane związki według rosnącego ph w roztworze wodnym. Właściwy porządek podaj zapisując go wzorami półstrukturalnymi.
PRZYKŁADOWE ZADANIA ORGANICZNE ZWIĄZKI ZAWIERAJĄCE AZOT Zadanie 1127 (1 pkt) Uszereguj podane związki według rosnącego ph w roztworze wodnym. Właściwy porządek podaj zapisując go wzorami półstrukturalnymi.
Kierunek i poziom studiów: Biotechnologia, pierwszy. Nazwa wariantu modułu (opcjonalnie): nie dotyczy
 Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Czy żywność GMO jest bezpieczna?
 Instytut Żywności i Żywienia dr n. med. Lucjan Szponar Czy żywność GMO jest bezpieczna? Warszawa, 21 marca 2005 r. Od ponad połowy ubiegłego wieku, jedną z rozpoznanych tajemnic życia biologicznego wszystkich
Instytut Żywności i Żywienia dr n. med. Lucjan Szponar Czy żywność GMO jest bezpieczna? Warszawa, 21 marca 2005 r. Od ponad połowy ubiegłego wieku, jedną z rozpoznanych tajemnic życia biologicznego wszystkich
We wstępie autorka pracy zaprezentowała cel pracy opracowanie syntezy trzech optycznie czynnych kwasów aminofosfonowych, zawierających w swojej
 dr hab. Jacek Ścianowski, prof. UMK Toruń, 29 października 2016r. Katedra Chemii Organicznej, Wydział Chemii, Uniwersytet Mikołaja Kopernika w Toruniu 87-100 Toruń, ul. Gagarina 7 Recenzja rozprawy doktorskiej
dr hab. Jacek Ścianowski, prof. UMK Toruń, 29 października 2016r. Katedra Chemii Organicznej, Wydział Chemii, Uniwersytet Mikołaja Kopernika w Toruniu 87-100 Toruń, ul. Gagarina 7 Recenzja rozprawy doktorskiej
Przegląd budowy i funkcji białek
 Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
REAKCJE JONÓW ENOLANOWYCH
 REKCJE JNÓW ENLNWYC Część II MTERIŁY PRZYGTWUJĄCE D CLLQUIUM KŃCWEG PRCWNI ZWNSWN CEMI RGNICZN Dr artosz Trzewik Kraków, 12 listopada 2013 r. 25 Spis treści części I i II 1. Kwasowość atomów wodoru α,
REKCJE JNÓW ENLNWYC Część II MTERIŁY PRZYGTWUJĄCE D CLLQUIUM KŃCWEG PRCWNI ZWNSWN CEMI RGNICZN Dr artosz Trzewik Kraków, 12 listopada 2013 r. 25 Spis treści części I i II 1. Kwasowość atomów wodoru α,
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII
 ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII Zadanie 1. Na rysunku przedstawiono fragment układu okresowego pierwiastków. Dokoocz zdania tak aby były prawdziwe. Wiązanie jonowe występuje w związku chemicznym
ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII Zadanie 1. Na rysunku przedstawiono fragment układu okresowego pierwiastków. Dokoocz zdania tak aby były prawdziwe. Wiązanie jonowe występuje w związku chemicznym
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Mg I. I Mg. Nie można ich jednak otrzymać ze związków, które posiadają grupy chlorowcowe w tak zwanym ustawieniu wicynalnym.
 nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
Nazwa przedmiotu (w języku. CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot
 Nazwa pola Komentarz Nazwa (w języku CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot CBMiM PAN Liczba punktów ECTS 5 Sposób zaliczenia Egzamin Język wykładowy
Nazwa pola Komentarz Nazwa (w języku CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot CBMiM PAN Liczba punktów ECTS 5 Sposób zaliczenia Egzamin Język wykładowy
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Rys. 1. Podstawowy koncept nukleozydów acyklicznych. a-podstawienie nukleofilowe grupy nukleofugowej w czynniku alkilującycm
 Nukleozydy acykliczne Jak już wspomniano nukleozydy acykliczne formalnie są N-alkilowymi pochodnymi nukleozasad. Fragment acykliczny najczęściej zawiera atom tlenu naśladujący tlen pierścieniowy jak również
Nukleozydy acykliczne Jak już wspomniano nukleozydy acykliczne formalnie są N-alkilowymi pochodnymi nukleozasad. Fragment acykliczny najczęściej zawiera atom tlenu naśladujący tlen pierścieniowy jak również
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
I KSZTAŁCENIA PRAKTYCZNEGO. Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
Slajd 1. Slajd 2. Proteiny. Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) Kwas α-aminokarboksylowy aminokwas
 Slajd 1 Proteiny Slajd 2 Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) wiązanie amidowe Kwas α-aminokarboksylowy aminokwas Slajd 3 Aminokwasy z alifatycznym łańcuchem
Slajd 1 Proteiny Slajd 2 Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) wiązanie amidowe Kwas α-aminokarboksylowy aminokwas Slajd 3 Aminokwasy z alifatycznym łańcuchem
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
PL B1. Kwasy α-hydroksymetylofosfonowe pochodne 2-azanorbornanu i sposób ich wytwarzania. POLITECHNIKA WROCŁAWSKA, Wrocław, PL
 PL 223370 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 223370 (13) B1 (21) Numer zgłoszenia: 407598 (51) Int.Cl. C07D 471/08 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22) Data zgłoszenia:
PL 223370 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 223370 (13) B1 (21) Numer zgłoszenia: 407598 (51) Int.Cl. C07D 471/08 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22) Data zgłoszenia:
Z a d a n i a t e o r e t y c z n e
 O L I M P I A D A 45 1954 1998 Z a d a n i a t e o r e t y c z n e C H EM I C Z N A zmiana ph roztworów ZADANIE 1 Jak zmieni się stężenie jonów wodorotlenowych przy przejściu od roztworu A do roztworu
O L I M P I A D A 45 1954 1998 Z a d a n i a t e o r e t y c z n e C H EM I C Z N A zmiana ph roztworów ZADANIE 1 Jak zmieni się stężenie jonów wodorotlenowych przy przejściu od roztworu A do roztworu
Wykład 2. Kinetyka reakcji enzymatycznych.
 Wykład 2 Kinetyka reakcji enzymatycznych. Kofaktory enzymów wd_2 2 Ryboflawina witamina B 2 Ryboflawina wit. B 2 FAD dinukleotyd flawinoadeninowy wd_2 3 Niacyna witamina PP (B 3 ) NAD + dinukleotyd nikotynamidoadeninowy
Wykład 2 Kinetyka reakcji enzymatycznych. Kofaktory enzymów wd_2 2 Ryboflawina witamina B 2 Ryboflawina wit. B 2 FAD dinukleotyd flawinoadeninowy wd_2 3 Niacyna witamina PP (B 3 ) NAD + dinukleotyd nikotynamidoadeninowy
Chemia ogólna nieorganiczna Wykład XII Kinetyka i statyka chemiczna
 Chemia ogólna nieorganiczna Wykład 10 14 XII 2016 Kinetyka i statyka chemiczna Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od
Chemia ogólna nieorganiczna Wykład 10 14 XII 2016 Kinetyka i statyka chemiczna Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od
Nowoczesne systemy ekspresji genów
 Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA
 Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
PRÓBNY EGZAMIN MATURALNY Z CHEMII
 Wpisuje zdający przed rozpoczęciem pracy PESEL ZDAJĄ CEGO Miejsce na nalepkę z kodem szkoły Instrukcja dla zdającego PRÓBNY EGZAMIN MATURALNY Z CHEMII Arkusz II (dla poziomu rozszerzonego) Czas pracy 120
Wpisuje zdający przed rozpoczęciem pracy PESEL ZDAJĄ CEGO Miejsce na nalepkę z kodem szkoły Instrukcja dla zdającego PRÓBNY EGZAMIN MATURALNY Z CHEMII Arkusz II (dla poziomu rozszerzonego) Czas pracy 120
Lek od pomysłu do wdrożenia
 Lek od pomysłu do wdrożenia Lek od pomysłu do wdrożenia KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU
Lek od pomysłu do wdrożenia Lek od pomysłu do wdrożenia KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
Mechanizmy działania i regulacji enzymów
 Mechanizmy działania i regulacji enzymów Enzymy: są katalizatorami, które zmieniają szybkość reakcji, same nie ulegając zmianie są wysoce specyficzne ich aktywność może być regulowana m.in. przez modyfikacje
Mechanizmy działania i regulacji enzymów Enzymy: są katalizatorami, które zmieniają szybkość reakcji, same nie ulegając zmianie są wysoce specyficzne ich aktywność może być regulowana m.in. przez modyfikacje
protos (gr.) pierwszy protein/proteins (ang.)
 Białka 1 protos (gr.) pierwszy protein/proteins (ang.) cząsteczki życia materiał budulcowy materii ożywionej oraz wirusów wielkocząsteczkowe biopolimery o masie od kilku tysięcy do kilku milionów jednostek
Białka 1 protos (gr.) pierwszy protein/proteins (ang.) cząsteczki życia materiał budulcowy materii ożywionej oraz wirusów wielkocząsteczkowe biopolimery o masie od kilku tysięcy do kilku milionów jednostek
WARSZTATY olimpijskie. Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna Kinetyka
 WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
Widma UV charakterystyczne cechy ułatwiające określanie struktury pirydyny i pochodnych
 Pirydyna i pochodne 1 Pirydyna Tw 115 o C ; temperatura topnienia -41,6 0 C Miesza się w każdym stosunku z wodą tworząc mieszaninę azeotropowa o Tw 92,6 o C; Energia delokalizacji 133 kj/mol ( benzen 150.5
Pirydyna i pochodne 1 Pirydyna Tw 115 o C ; temperatura topnienia -41,6 0 C Miesza się w każdym stosunku z wodą tworząc mieszaninę azeotropowa o Tw 92,6 o C; Energia delokalizacji 133 kj/mol ( benzen 150.5
II Podkarpacki Konkurs Chemiczny 2009/10. ETAP II r. Godz Zadanie 1 (10 pkt.)
 II Podkarpacki Konkurs Chemiczny 2009/10 ETAP II 19.12.2009 r. Godz. 10.00-12.00 KPKCh Zadanie 1 (10 pkt.) 1. Gęstość 22% roztworu kwasu chlorowodorowego o stężeniu 6,69 mol/dm 3 wynosi: a) 1,19 g/cm 3
II Podkarpacki Konkurs Chemiczny 2009/10 ETAP II 19.12.2009 r. Godz. 10.00-12.00 KPKCh Zadanie 1 (10 pkt.) 1. Gęstość 22% roztworu kwasu chlorowodorowego o stężeniu 6,69 mol/dm 3 wynosi: a) 1,19 g/cm 3
Tytuł pracy w języku angielskim: Physical properties of liquid crystal mixtures of chiral and achiral compounds for use in LCDs
 Dr inż. Jan Czerwiec Kierownik pracy: dr hab. Monika Marzec Tytuł pracy w języku polskim: Właściwości fizyczne mieszanin ciekłokrystalicznych związków chiralnych i achiralnych w odniesieniu do zastosowań
Dr inż. Jan Czerwiec Kierownik pracy: dr hab. Monika Marzec Tytuł pracy w języku polskim: Właściwości fizyczne mieszanin ciekłokrystalicznych związków chiralnych i achiralnych w odniesieniu do zastosowań
Wykład z Chemii Ogólnej i Nieorganicznej
 Wykład z Chemii Ogólnej i Nieorganicznej Część 5 ELEMENTY STATYKI CHEMICZNEJ Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika w Toruniu Prof. dr hab. n.chem.
Wykład z Chemii Ogólnej i Nieorganicznej Część 5 ELEMENTY STATYKI CHEMICZNEJ Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika w Toruniu Prof. dr hab. n.chem.
Węglowodory poziom podstawowy
 Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
EGZAMIN MATURALNY Z CHEMII
 Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO MCH-W1D1P-021 EGZAMIN MATURALNY Z CHEMII Instrukcja dla zdającego Czas pracy 90 minut 1. Proszę sprawdzić, czy arkusz
Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO MCH-W1D1P-021 EGZAMIN MATURALNY Z CHEMII Instrukcja dla zdającego Czas pracy 90 minut 1. Proszę sprawdzić, czy arkusz
Prof. dr hab. Inż. Jacek Skarżewski
 Prof. dr hab. Inż. Jacek Skarżewski Zakład Chemii Organicznej, Wydział Chemiczny Politechnika Wrocławska, Wyb. Wyspiańskiego 27 50-370 Wrocław Tel.: (071) 320 2464, fax.: (071) 328 4064 E-mail: jacek.skarzewski@pwr.wroc.pl
Prof. dr hab. Inż. Jacek Skarżewski Zakład Chemii Organicznej, Wydział Chemiczny Politechnika Wrocławska, Wyb. Wyspiańskiego 27 50-370 Wrocław Tel.: (071) 320 2464, fax.: (071) 328 4064 E-mail: jacek.skarzewski@pwr.wroc.pl
KINETYKA INWERSJI SACHAROZY
 Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Komputerowe wspomaganie projektowanie leków
 Komputerowe wspomaganie projektowanie leków wykład V Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków wykład V Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
