kod epigenetyczny metylacja DNA modyfikacje histonów H3 i H4
|
|
|
- Kornelia Nowakowska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Postepy Hig Med Dosw. (online), 2009; 63: e-issn Review Received: Accepted: Published: Drugi kod, czyli co determinuje regiony aktywności transkrypcyjnej oraz miejsca inicjacji replikacji Second code, or what determines actively transcribed regions and replication origins Konrad Winnicki Katedra Cytofi zjologii, Wydział Biologii i Ochrony Środowiska, Uniwersytet Łódzki Streszczenie Komórki poszczególnych tkanek, chociaż zawierają identyczny materiał genetyczny, różnią się jednak kodami epigenetycznymi odpowiedzialnymi za odmienne wzorce ekspresji genów. Kody takie, poprzez wpływ na strukturę chromatyny, wyznaczają regiony aktywne transkrypcyjnie oraz mają pośredni wpływ na czas replikacji poszczególnych sekwencji. Metylacja cytozyny oraz modyfikacje histonów, np. deacetylacja oraz metylacja Lys9 w histonie H3 odgrywają rolę podczas tworzenia i przekazywania kodów epigenetycznych komórkom potomnym. Poprawne dziedziczenie takich modyfikacji jest ważne dla rozwoju embrionalnego, histogenezy oraz funkcji całego organizmu, a każde zaburzenie tego dziedziczenia może prowadzić do niewłaściwego rozwoju oraz chorób, takich jak np. nowotwory. Słowa kluczowe: kod epigenetyczny metylacja DNA modyfikacje histonów H3 i H4 Summary Although each cell of a complex organism is governed by the same genome, cells which form different tissues vary in epigenetic codes that are responsible for various gene expression. These codes, through their influence on chromatin structure, determine actively transcribed regions and have indirect impact on replication timing. Cytosine methylation and histone modifications, for example the deacetylation and methylation of Lys9 in histone H3, play important roles in forming and transferring epigenetic codes to the next cell generation. The correct copying of such modifications is important for embryonic development, histogenesis, and future functions of the whole organism, and any disturbance can cause abnormal development or disease, such as cancer. Key words: epigenetic code DNA methylation H3 and H4 histone modifications Full-text PDF: Word count: 3073 Tables: Figures: 2 References: 43 Adres autora: mgr Konrad Winnicki, Katedra Cytofi zjologii, Instytutu Fizjologii, Cytologii i Cytogenetyki, Wydział Biologii i Ochrony Środowiska, Uniwersytet Łódzki, ul. Pilarskiego 14, Łódź; winnicki@biol.uni.lodz.pl 169
2 Postepy Hig Med Dosw (online), 2009; tom 63: WSTĘP W procesie ewolucji życia istotne znaczenie miało początkowo szybkie tempo replikacji. Ze względu na ograniczone zasoby dostępnych substratów, dobór naturalny faworyzował te z samopowielających się kompleksów makrocząsteczek, które charakteryzowały się dużą dynamiką reprodukcji. Założenie to potwierdziły badania w warunkach in vitro, wskazujące na istnienie presji selekcyjnej prowadzącej do powstawania krótszych, a co za tym idzie szybciej replikujących cząsteczek kwasów nukleinowych [30,32]. Nieustannie postępujące zmiany środowiska oraz konieczność zasiedlania nowych nisz ekologicznych prowadziły jednocześnie do tworzenia bardziej zorganizowanych struktur, lepiej przystosowanych do niekorzystnych warunków. Kamieniem milowym na szlaku ewolucji coraz bardziej złożonych form materii ożywionej było pojawienie się komórek pro- i eukariotycznych, umożliwiających kolonizację nowych środowisk [6,26]. Jeszcze bardziej efektywną ekspansję umożliwiło powstanie organizmów wielokomórkowych. Dzięki temu wykształciły się różnorodne formy, odznaczające się odmiennymi strategiami przetrwania szybkim bądź wolnym tempem namnażania, w zależności od stopnia złożoności struktury oraz działającej presji środowiska. Organizmy wielokomórkowe charakteryzują się zróżnicowanymi fenotypowo komórkami, mimo obecności tego samego genotypu. Wydaje się jednak, że już we wczesnych etapach ewolucji informacja zapisana w sekwencji nukleotydów okazała się niewystarczająca do realizacji skomplikowanych procesów morfogenetycznych. W wytworzeniu grup komórek, wykazujących wspólne pochodzenie, lecz różniących się budową oraz funkcją, uczestniczyć musiały zatem dodatkowe mechanizmy, różnicujące możliwości wykorzystania informacji zapisanej w identycznych sekwencjach nukleotydów. Za powstanie morfologicznego i funkcjonalnego zróżnicowania komórek w obrębie organizmu odpowiadają różne wzorce ekspresji genów, które leżą u podstaw morfogenezy. Zróżnicowana ekspresja informacji genetycznej jest wynikiem funkcjonowania różnych kodów epigenetycznych pojawiających się w trakcie rozwoju [18]. DEFINICJA KODU EPIGENETYCZNEGO Jenuwein i Allis [19] źródeł różnych stanów epigenetycznych dopatrują się w informacji zapisanej w postaci kodu histonowego. Sugerują oni, że kod taki tworzą modyfikacje aminokwasów w N-terminalnych końcach histonów H3 i H4, do których zalicza się m.in. acetylację, metylację oraz fosforylację. Odczyt kodu histonowego w tym przypadku możliwy jest dzięki obecności białek, które zawierają bromodomeny (sekwencje rozpoznające acetylowane lizyny) oraz chromodomeny (chromodomain CD; sekwencje rozpoznające metylowane lizyny). Tworzenie miejsc aktywnych transkrypcyjnie oraz nieaktywnych regionów heterochromatynowych determinowane jest zatem przez przyłączanie określonych grup chemicznych do aminokwasów histonowych. 170 Turner [38] uważa jednak, że modyfikacje histonów, mimo wpływu na strukturę chromatyny, a przez to na aktywność transkrypcyjną, nie powinny być określane mianem kodu epigenetycznego. Sugeruje on, że termin ten definiuje potencjał przyszłej ekspresji genów, zapewniony przez modyfikacje w obrębie chromatyny, który pozwala na włączanie lub wyłączanie aktywności transkrypcyjnej w poszczególnych fazach morfogenezy. W określonym typie komórek modyfikacje takie ustanawiane są podczas wcześniejszego etapu różnicowania i prowadzą w efekcie do zmiany stopnia upakowania chromatyny. Modyfikacje histonów same w sobie nie tworzą jednak kodu epigenetycznego, a są jedynie częścią złożonego aparatu biochemicznego, który razem z metylacją DNA oraz innymi mechanizmami wpływającymi na strukturę chromatyny uczestniczą w tworzeniu kodu charakterystycznego dla danego typu komórek [38]. Kody epigenetyczne reprezentują więc różne epigenotypy, które nie tylko charakteryzują się odmienną ekspresją genów, ale co najważniejsze, dziedziczone są podczas mitozy i mejozy [18]. Niezależnie od dywagacji Turnera [38] dotyczących znaczenia słowa kod, w niniejszej pracy pojęcie zmian epigenetycznych równoznaczne jest z terminem kodu epigenetycznego, rozumianego jako źródło zróżnicowanej ekspresji genów oraz zmian w organizacji struktury chromatyny interfazowej. Chromatynę dzielimy na heterochromatynę (określaną niekiedy mianem heterochromatyny konstytutywnej) oraz euchromatynę. Heterochromatyna, która wykazuje znaczny stopień kondensacji, występuje głównie w centromerowych oraz telomerowych obszarach chromosomów i przeważnie charakteryzuje się niemal całkowitym brakiem sekwencji genowych. Większość genów znajduje się w regionach euchromatynowych, odznaczających się zdolnością do przyjmowania luźnej struktury. W euchromatynie, ze względu na występowanie regionów wyciszonych genetycznie, obecne są także obszary o znacznym stopniu kondensacji [31]. Zmiana struktury chromatyny interfazowej pociąga za sobą określoną sekwencję zdarzeń w przebiegu replikacji DNA podczas fazy S. Regiony aktywne transkrypcyjnie (euchromatyna) replikują bowiem wcześniej w porównaniu z regionami nieaktywnymi heterochromatyną konstytutywną i fakultatywną [por. 4,31]. Skoro niski stopień upakowania DNA jest strukturalnym czynnikiem warunkującym aktywność transkrypcyjną, nasuwa się pytanie: w jaki sposób determinowane są zmiany w stopniu kondensacji chromatyny interfazowej oraz jaki jest mechanizm ich przekazywania z pokolenia na pokolenie. Wydaje się, że niektóre z nich mogą być dziedziczone m.in. dzięki metylacji cytozyny. Taka modyfikacja w obrębie nukleotydów DNA pozwala nie tylko na zróżnicowanie stopnia upakowania nici polinukleotydowych w określonych obszarach, ale także na przekazywanie powstałego wzorca komórkom potomnym [18]. Jednak sama metylacja, mimo że u pewnych organizmów może uczestniczyć w dziedziczeniu powstałych kodów epigenetycznych, nie jest wystarczająca do tworzenia regionów heterochromatynowych oraz wyciszania genów. Zmiany o charakterze strukturalnym wymagają zaangażowania zarówno białek histonowych jak i niehistonowych, wiążących się z helisą DNA [28]. METYLACJA CYTOZYNY JAKO JEDEN Z MECHANIZMÓW TWORZENIA KODÓW EPIGENETYCZNYCH Wydaje się, że podczas replikacji DNA dochodzi nie tylko do wiernego powielenia sekwencji nukleotydów,
3 Winnicki K. Drugi kod, czyli co determinuje regiony aktywności transkrypcyjnej ale także do przekazania kolejnym pokoleniom zmian epigenetycznych, związanych z metylacją cytozyny. Modyfikacji takiej podlegają najczęściej dinukleotydy CpG, a jej dziedziczenie zapewnia obecność metylotransferaz wykazujących duże powinowactwo do hemimetylowanego DNA, kumulujących się w pobliżu widełek replikacyjnych dzięki interakcji z PCNA (proliferating cell nuclear antigen) białkiem wspomagającym funkcję polimeraz DNA d oraz e [35,36]. Właściwości takie u ssaków wykazuje metylotransferaza DNMT1 (DNA methyltransferase 1), która ma także zdolność metylacji de novo. U ssaków zidentyfikowano jak dotąd jeszcze 3 inne metylotransferazy: DNMT2 kontrolującą regiony centromerowe oraz DNMT3A i DNMT3B metylujące cytozyny, które nie podlegały wcześniej takiej modyfikacji [29]. Metylacja cytozyny następuje nie tylko w krótkich symetrycznych sekwencjach (CpG: GpC). U myszy DNMT3A zaangażowana jest np. w przyłączanie grup metylowych do asymetrycznych miejsc podatnych na metylację [35]. Okazuje się, że metylacja DNA ma istotne znaczenie dla wszelkich przemian zachodzących w organizmach wielokomórkowych. Prawidłowe dziedziczenie wzoru kodów epigenetycznych jest niezbędne do właściwego przebiegu embriogenezy oraz późniejszego funkcjonowania organizmów. Zmniejszenie poziomu ekspresji metylotransferazy DNMT1 u myszy, Xenopus oraz Danio rerio (danio pręgowany) prowadzi do śmierci już we wczesnym stadium rozwoju embrionalnego [5,10]. Dowodem świadczącym o korelacji między metylacją DNA i aktywnością transkrypcyjną mogą być doświadczenia polegające na zastępowaniu cytozyny jej analogiem 5-azacytydyną. Takie podstawienie uniemożliwia przyłączenie grupy metylowej i prowadzi do aktywacji wyciszonych genów, nawet w nieaktywnym chromosomie X [17]. U Drosophila melanogaster metylacja cytozyny prawdopodobnie nie odgrywa istotnej roli podczas rozwoju embrionalnego [25]. Weissmann i wsp. [40] wskazują jednak na obecność u Drosophila potencjalnej zależności metylacji Lys9 w histonie H3 od metylacji DNA. Nadekspresja metylotransferazy DNMT3A (pochodzącej od myszy) prowadzi bowiem do hipermetylacji DNA, zwiększając w konsekwencji poziom metylacji Lys9. Wpływ metylacji cytozyny na strukturę chromatyny pozostaje jednak do wyjaśnienia. Gilbert i wsp. [14] dowodzą, że utrata metylacji DNA w pierwotnych komórkach zarodkowych u myszy, prowadząca do redukcji metylacji oraz wzrostu acetylacji Lys9 w histonie H3, nie powoduje zmian stopnia upakowania chromatyny, a zwłaszcza obszarów heterochromatyny. Do wyjaśnienia pozostaje również mechanizm działania samych metylotransferaz. Chociaż u myszy biologiczna funkcja metylotransferazy DNMT1 (pośrednio związana z regulacją ekspresji genów) wymaga jej aktywności katalitycznej [5], to wyciszenie transkrypcji u Xenopus, przed stadium środkowej blastuli (midblastula transition MBT), wydaje się niezależne od enzymatycznej aktywności, natomiast uwarunkowane samą obecnością DNMT1. W tym przypadku metylotransferaza lokalizuje się w regionach promotorowych, funkcjonując jako bezpośredni represor aktywności transkrypcyjnej [10]. ROLA MODYFIKACJI AMINOKWASÓW HISTONOWYCH W REGULACJI EKSPRESJI GENETYCZNEJ I W TWORZENIU DOMEN HETEROCHROMATYNY KONSTYTUTYWNEJ Sama modyfikacja cytozyny prawdopodobnie nie jest czynnikiem bezpośrednio wpływającym na strukturę chromatyny i funkcjonuje raczej jako znacznik miejsc jej przyszłej rearanżacji. Mechanizmy odgrywające istotną rolę w tworzeniu domen heterochromatyny konstytutywnej zaangażowane są także w proces wyciszania genów w euchromatynie. Obejmują one przyłączanie do DNA różnych białek uczestniczących w późniejszej modyfikacji określonych aminokwasów histonowych. U kręgowców odkryto dwa niezależne mechanizmy łączące metylację cytozyny z modyfikacjami histonów [35]. Pierwszy z nich zakłada rekrutację do miejsc metylacji DNA białka MeCP2 (methylcytosine-binding protein), które zawiera domenę TRD (transcriptional repressor domain). Oddziałuje ona bezpośrednio z korepresorem msin3a, do którego przyłączone są dwie deacetylazy histonowe: HDAC1 oraz HDAC2 (histone deacetylase 1,2), biorące udział w procesie rearanżacji chromatyny (ryc. 1) [34,42]. Drugi mechanizm, odkryty u ssaków, wiąże się z bezpośrednim oddziaływaniem między metylotransferazą DNMT1 oraz histonowymi deacetylazami [35]. Podczas tworzenia struktur heterochromatynowych oraz w procesie wyciszania genów istotną rolę pełni metylacja Lys9 w N-terminalnym ogonie histonu H3, możliwa jedynie po wcześniejszej deacetylacji Lys9 oraz Lys14. U ssaków metylację histonu H3 w pozycji Lys9 prowadzi swoista metylotransferaza SUV39H1 (suppressor of variegation 3-9 homolog 1) (ryc. 1). Dowodem ogromnego znaczenia metylacji w tej pozycji mogą być mutanty Sacharomyces pombe pozbawione aktywności genu clr4 (homolog SUV39H1 u S. pombe), które wykazują: (i) nieprawidłowości podczas tworzenia heterochromatyny w rejonach okołocentromerowych, (ii) wzrost liczby pogubionych chromosomów, (iii) ograniczenie wyciszenia pewnych genów [35]. Ponadto, geny reporterowe wstawiane w rejony telomerowe u drożdży ulegają wyciszeniu, a stan taki utrzymuje się przez wiele pokoleń komórek [27]. Dla domen heterochromatynowych oraz regionów nieaktywnych transkrypcyjnie charakterystyczna jest także deacetylacja Lys16 i metylacja Lys20 w histonie H4. Przyłączenie grupy metylowej do aminokwasów histonowych może wyznaczać również miejsca aktywne transkrypcyjnie, czego przykładem jest metylacja Lys4 w histonie H3. Innym rodzajem potranslacyjnej modyfikacji decydującej o aktywności transkrypcyjnej jest fosforylacja Ser10 w histonie H3, która uniemożliwia metylację Lys9 [35,31]. Podczas formowania heterochromatyny u Metazoa istotną rolę odgrywa białko HP1 (heterochromatin protein 1). Zawiera ono w aminoterminalnym końcu motyw CD, wiążący się swoiście z metylowaną Lys9 w histonie H3. Z kolei w karboksyloterminalnym końcu znajduje się motyw CSD (chromo shadow domain), który może oddziaływać z różnymi białkami, np. metylotransferazą SUV39H1. Białko HP1 skoncentrowane jest w heterochromatynie okołocentromerowej i telomerach, a także uczestniczy w wycisza- 171
4 Postepy Hig Med Dosw (online), 2009; tom 63: Ryc. 1. Etapy jednego z potencjalnych mechanizmów tworzenia skondensowanych regionów heterochromatynowych, bogatych w sekwencje zmetylowanego DNA; metylacja Lys9 w histonie H3 jest efektem działania metylotransferazy SUV39H1, po wcześniejszym usunięciu reszt acetylowych przez deacetylazy histonowe HDAC1/HDAC2. Obecność zmetylowanej Lys9 umożliwia przyłączenie białka HP1 [na podstawie: 34,35,42 zmodyfikowano]; ack acetylacja Lys9, mk metylacja Lys9 niu pewnych genów umiejscowionych w euchromatynie. Dzięki HP1 deacetylacja i metylacja rozprzestrzenia się na kolejne nukleosomy [35]. W tworzeniu heterochromatyny oraz wyciszaniu genów u drożdży pączkujących (Saccharomyces cervisiae) uczestniczy kompleks SIR zawierający białka: Sir2, Sir3 i Sir4. Do telomerów kompleks Sir2/Sir4 rekrutowany jest przez białko Rap1 oraz białka Ku70 i Ku80. Dochodzi wówczas do lokalnej deacetylacji histonu H3 prowadzonej przez Sir2, która w konsekwencji umożliwia przyłączenie do nukleosomów białka Sir3. Multimeryzacja białek Sir3 i Sir4 oraz enzymatyczna aktywność Sir2 pozwala na rozprzestrzenienie się fali modyfikacji wzdłuż nukleosomów [27]. Mimo że u poszczególnych grup organizmów w rearanżacji chromatyny mogą uczestniczyć odmienne białka, to ogólny mechanizm wydaje się konserwatywny. Nadal do wyjaśnienie pozostaje jednak kwestia, czy podczas tworzenie kodów epigenetycznych informacja przepływa z 5mC na histony, czy odwrotnie. Przepisywanie informacji zapisanych w modyfikacjach histonów na metylację cytozyny możliwe jest u roślin kwiatowych dzięki obecności metylotransferaz DNA, które zawierają chromodomeny mogące łączyć się z metylowaną Lys9 w histonie H3, tzw. CMTs ( chromo methyltransferases ). Dowodem 172 na taki kierunek transferu informacji może być mutacja w genie dim-5 u Nerospora crassa (odpowiadającym za syntezę metylotransferazy histonu H3), która prowadzi do zablokowania metylacji wszystkich cytozyn. Mało prawdopodobne wydaje się jednak, aby same CMTs uczestniczyły w tłumaczeniu kodów histonowych na kod reprezentowany przez modyfikacje w obrębie cytozyny. [35]. Z kolei przepływ informacji w drugą stronę mógłby być zapewniony np. przez oddziaływanie kompleksu białek HP1 oraz SUV39H1 z białkiem MBD1. Podobnie jak MeCP2 należy ono do białek, które zawierają domeny wiążące metylowane regiony CpG (MBD proteins; methyl-cpg binding domain proteins) [13]. Mechanizm tworzenia regionów heterochromatynowych z udziałem białek zawierających domeny MBD nadal nie jest wyjaśniony. Chociaż pewne badania wskazują, że heterochromatynowa lokalizacja białka MBD1 jest zaburzona w komórkach wykazujących brak metylotransferazy DNMT1 [20], to inne sugerują, że białka MeCP2 oraz MBD1 mogą wiązać się zarówno z metylowanymi jak i niemetylowanymi wyspami CpG [21,42]. Ze względu na losową dystrybucję starych histonów do powstałych w czasie replikacji cząsteczek DNA [35] oraz acetylację nowo syntetyzowanych histonów [11], konieczne wydaje się rozważenie dwustronnego przepływu informacji oraz zaangażowania innych mechanizmów w tworzenie
5 Winnicki K. Drugi kod, czyli co determinuje regiony aktywności transkrypcyjnej Ryc. 2. Umiejscowienie punktów TDP i ODP w cyklu komórkowym u ssaków [na podstawie: 7,9 zmodyfikowano] różnych stanów epigenetycznych. Wydaje się mało prawdopodobne, aby kody epigenetyczne dziedziczone były jedynie na podstawie modyfikacji aminokwasów histonowych. Innym mechanizmem uczestniczącym w ich powstawaniu oraz dziedziczeniu wydaje się szlak zaangażowany w tworzenie małego interferującego RNA (sirna). Hipotezę taką potwierdzają badania dotyczące mutacji genu dicer- 2 (kodującego endonukleazę odpowiedzialną za tworzenie sirna u D. melanogaster), która prowadzi do utraty metylacji Lys9 histonu H3 w rdna [33]. Okazuje się, że sirna może powodować wyciszenie genów na poziomie transkrypcji przez regulację modyfikacji w obrębie DNA oraz histonów, powodując w konsekwencji wzrost poziomu upakowania chromatyny [39]. Badania na modelu C. elegans dowodzą z kolei, że zmiany ekspresji genów, w których uczestniczy szlak RNAi podlegają procesowi dziedziczenia [15]. Wpływ interferującego RNA na tworzenie heterochromatyny oraz przekazywanie zmian epigenetycznych opisano w wielu publikacjach [16,39,22]. W ustanawianiu oraz dziedziczeniu kodów epigenetycznych uczestniczy zatem wiele mechanizmów decydujących o strukturze chromatyny, które nie ograniczają się jedynie do modyfikacji w obrębie histonów oraz metylacji DNA (u organizmów, u których ona występuje), ale także angażują inne szlaki, których udział nadal pozostaje do wyjaśnienia. KODY EPIGENETYCZNE JAKO DETERMINANTY MIEJSC INICJACJI ORAZ CZASU REPLIKACJI DNA Czas replikacji poszczególnych sekwencji genomowego DNA zależy od lokalizacji wewnątrzjądrowej oraz struktury i aktywności chromatyny. Od dawna wiadomo, że miejsca aktywne transkrypcyjnie, o mniejszym stopniu kondensacji, replikują wcześniej, natomiast zwarte regiony heterochromatynowe później. Ponieważ o strukturze chromatyny decydują określone kody epigenetyczne, wydaje się, że mogą one mieć pośredni wpływ na czas oraz miejsca inicjacji replikacji (OR lub ori; origins of replication). Zależność między stopniem kondensacji chromatyny a czasem replikacji pewnych obszarów potwierdzają badania dotyczące efektu mutacji w genie Sir3. Prowadzi ona do wcześniejszej replikacji regionów telomerowych, co zapewne jest związane z aktywnością niewykorzystywanych wcześniej miejsc inicjacji replikacji. Z kolei wstawienie sekwencji odpowiedzialnych za wyciszenie genów w miejsca wcześnie replikujące prowadzi do opóźnienia syntezy DNA [43]. Replikacja inicjowana jest w miejscu przyłączenia kompleksów prereplikacyjnych, tworzonych przez białka ORC, Cdc6, Cdt1 oraz Mcm (2-7), montowanych już podczas poprzedniego cyklu komórkowego. U ssaków ORC(origin recognition complex) składa się z 6 podjednostek, spośród których 5 ORC (2-6) pozostaje trwale związanych z chromatyną. Pod koniec mitozy do DNA wiąże się kompleks Orc1/Cdc6, co w konsekwencji pozwala na przyłączenie się białka Cdt1. Jego związanie z chromatyną umożliwia rekrutację kompleksu Mcm (2-7), funkcjonującego jako helikaza DNA. Po rozpoczęciu replikacji białko Cdc6 oddysocjowuje w wyniku fosforylacji prowadzonej przez kompleksy Cdk2-cyklina A. Aktywność Cdt1 hamowana jest z kolei przez gemininę, pojawiającą się podczas fazy S. Zapobiega to stabilnemu wiązaniu się kompleksu Mcm (2-7) do chromatyny oraz uniemożliwia tworzenie nowych kompleksów prereplikacyjnych przed ukończeniem mitozy, gwarantując tylko jedną rundę replikacji na każdy cykl komórkowy [7]. Dimitrova i Gilbert [9] wyznaczają w fazie G1 dwa punkty determinujące przyszłą lokalizację miejsc inicjacji replikacji (ryc. 2). Pierwszym z nich jest punkt TDP (timing decision point), zlokalizowany we wczesnej fazie G1, decydujący o czasie w jakim będą replikowane określone sekwencje w nadchodzącej fazie S. Z kolei drugi punkt ODP (origin decision point) zlokalizowany w późnej fazie G1, wyznacza swoiste miejsca inicjacji replikacji. Wydaje się, że struktura chromatyny jest czynnikiem, który decyduje o czasie replikacji poszczególnych jej obszarów. Możliwe, że kompleksy prereplikacyjne w regionach heterochromatynowych są tylko częściowo zmontowane, ze względu na utrudniony dostęp białek do chromatyny, w przeciwieństwie do miejsc aktywnych transkrypcyjnie, gdzie kompleksy prereplikacyjne mogą być kompletnie zmontowane. Ponieważ białka kompleksów, w których nastąpi inicjacja replikacji wiążą się z chromatyną już na przełomie fazy M i G1 (ryc. 2) [7], bardziej prawdopodobne wydaje się 173
6 Postepy Hig Med Dosw (online), 2009; tom 63: jednak, że struktura chromatyny utrudnia dostęp białkom bezpośrednio inicjującym replikację, np. dla kompleksów cykliny A oraz kinazy Cdk2. Tezę o roli struktury chromatyny wydają się potwierdzać badania, w których komórki drożdży pozbawione aktywności deacetylazy histonowej wykazują wczesną aktywację późno replikujących sekwencji ori znajdujących się w wewnętrznych loci chromosomowych. Z kolei ektopowa lokalizacja sekwencji HMR- E (pochodzącej z wyciszonego locus MAT) prowadzi do opóźnienia syntezy DNA w miejscach wcześnie replikujących, przy czym opóźnienie to wymaga obecności kompleksu białek SIR [2,37,43]. Pewne badania wskazują, że struktura chromatyny bezpośrednio determinuje jedynie czas replikacji poszczególnych jej domen, decydując tym samym w jakiej kolejności będą powielane poszczególne regiony genomu (punkt TDP) [23]. Jednym z możliwych mechanizmów łączących aktywność transkrypcyjną oraz replikację może być wspomniany już szlak związany z postaciami interferującego RNA [8,22]. Wyjaśnienia wymaga jednak sposób w jaki wyznaczane są swoiste miejsca inicjacji replikacji w punkcie ODP. Sugeruje się, że aktywność transkrypcyjna może być jednym z czynników decydującym o miejscu zapoczątkowania syntezy DNA [1,8]. Blokowanie transkrypcji uniemożliwia bowiem wyznaczenie tych miejsc w jądrach pre-odp (replikacja inicjuje w miejscach przypadkowych), natomiast tylko nieznacznie zmienia ich lokalizację w jądrach post- ODP. Wskazuje to, że utrzymanie właściwych miejsc inicjacji replikacji podczas późnej fazy G1 jest w mniejszym stopniu uzależnione od przebiegu procesów transkrypcyjnych, niż proces ich wyznaczania we wczesnej fazie G1 [8]. Okazuje się, że problem wyznaczania swoistych miejsc startu replikacji jest bardziej złożony. U ssaków ustalone w określonym typie komórek miejsca inicjacji syntezy DNA nie ulegają zmianie w kolejnych rundach replikacji [24]. Z kolei najnowsze badania na modelu Xenopus sugerują, że swoiste miejsca inicjacji replikacji na poziomie replikonów wyznaczane są u tego gatunku w sposób przypadkowy [23]. Ponadto, nie do końca jest pewny wpływ samej transkrypcji na wyznaczanie miejsc inicjacji replikacji. Pewne obserwacje wskazują jednak, że wzorzec, według którego przebiega replikacja zależy raczej od sekwencji DNA i struktury chromatyny, a więc czynników wpływających także na transkrypcję, niż od transkrypcji jako takiej. Dowiedziono również, że na wyznaczanie swoistych miejsc inicjacji replikacji mogą mieć wpływ sekwencje, które są odpowiedzialne za regulację transkrypcji. Na przykład utrata promotora w genie DHFR u chomika chińskiego prowadzi do rozpoczęcia replikacji DNA w miejscach wewnątrzgenowych, w których ona nie zachodzi, gdy struktura genu jest prawidłowa. Zmiany miejsc inicjacji replikacji pojawiają się również w locus ludzkiej b-globiny w wyniku utraty regionu LCR (locus control region) [1]. PIŚMIENNICTWO [1] Aladjem M.I.: Replication in context: dynamic regulation of DNA replication patterns in metazoans. Nat. Rev. Genet., 2007; 8: [2] Aparicio J.G., Viggiani C.J., Gibson D.G., Aparicio O.M.: The Rpd3- Sin3 histone deacetylase regulates replication timing and enables intra-s origin control in Saccharomyces cerevisiae. Mol. Cell. Biol., 2004; 24: Wydaje się, że transkrypcja może odgrywać rolę w wyznaczaniu wcześnie oraz późno replikujących regionów w punkcie TDP. Badania dotyczące czasu replikacji poszczególnych sekwencji ludzkiego genomu wykonane techniką mikromacierzy wskazują, że transkrypcja może wpływać na sekwencję zdarzeń podczas replikacji [41]. Z kolei rola transkrypcji w wyznaczaniu swoistych miejsc inicjacji replikacji w punkcie ODP nadal pozostaje do wyjaśnienia. Możliwe, że zmiany epigenetyczne wpływają nie tylko na aktywność transkrypcyjną komórek, ale uczestniczą także w wyznaczaniu wczesnych i późnych miejsc inicjacji replikacji. Jednym z dowodów na taki związek może być wiązanie przez Orc1 białka Sir1 [3] lub białka HP1 [12], zaangażowanych w proces wyciszania genów. Udokumentowano także bezpośrednie interakcje między białkiem Orc2 oraz białkami regulującymi transkrypcję [37]. Dokładny mechanizm składania kompleksów prereplikacyjnych oraz wybór swoistych miejsc inicjacji replikacji w zależności od stopnia kondensacji chromatyny i aktywności transkrypcyjnej nadal pozostają do wyjaśnienia. WNIOSKI W strukturze DNA zapisana jest nie tylko informacja o sekwencji aminokwasów w białkach, ale także informacja o ekspresji genów, co ma szczególne znaczenie dla procesów morfogenezy. Swoiste kody epigenetyczne prawdopodobnie nie tylko wyznaczają aktywne transkrypcyjnie regiony, ale także determinują czas replikacji określonych obszarów chromatyny. Dlatego informacja zapisana we wzorcu metylacji cytozyny, modyfikacje aminokwasów histonowych oraz inne mechanizmy uczestniczące w rearanżacji chromatyny, np. RNAi, mają istotne znaczenie dla funkcjonowania komórek. Wierne odtwarzanie określonych kodów epigenetycznych wydaje się podstawowe dla rozwoju całego organizmu. Zaburzenie dziedziczenia kodu epigenetycznego we wczesnych etapach rozwoju embrionalnego może prowadzić do śmierci [5,10], natomiast w dalszych etapach ontogenezy może powodować wystąpienie chorób nowotworowych [29]. Dlatego istotne jest podejmowanie działań zmierzających do ustalenia wzorca metylacji w poszczególnych komórkach organizmu. W tym celu wprowadzony został projekt mający za zadanie rozszyfrowanie kodu zapisanego w metylacji cytozyny, który określono mianem HEP (human epigenome project) [29]. PODZIĘKOWANIA Wyrazy podziękowania składam prof. dr hab. Januszowi Maszewskiemu za opiekę naukową, krytyczne uwagi oraz pomoc w nadaniu pracy ostatecznego kształtu. [3] Bose M.E., McConnell K.H., Gardner-Aukema K.A., Müller U., Weinreich M., Keck J.L., Fox C.A.: The origin recognition complex and Sir4 protein recruit Sir1p to yeast silent chromatin through independent interactions requiring a common Sir1p domain. Mol. Cell. Biol., 2004; 24: [4] Cimbora D.M., Groudine M.: The control of mammalian DNA replication: A brief history of space and timing. Cell, 2001; 104:
7 Winnicki K. Drugi kod, czyli co determinuje regiony aktywności transkrypcyjnej [5] Damelin M., Bestor T.H.: Biological functions of DNA methyltransferase 1 require its methyltransferase activity. Mol. Cell. Biol., 2007; 27: [6] Dawkins R.: Samolubny gen. Prószyński i S-ka, 2007; [7] DePamphilis M.L.: The ORC cycle : a novel pathway for regulating eukaryotic DNA replication. Gene, 2003; 310: 1 15 [8] Dimitrova D.S.: Nuclear transcription is essential for specification of mammalian replication origins. Genes Cells, 2006; 11: [9] Dimitrova D.S., Gilbert D.M.: The spatial position and replication timing of chromosomal domains are both established in early G1 phase. Mol. Cell, 1999; 4: [10] Dunican D.S., Ruzov A., Hackett J.A., Meehan R.R.: xdnmt1 regulates transcriptional silencing in pre-mbt Xenopus embryos independently of its catalytic function. Development, 2008; 135: [11] Ehrenhofer-Murray A.E.: Chromatin dynamics at DNA replication, transcription and repair. Eur. J. Biochem., 2004; 271: [12] Eissenberg J.C., Elgin S.C.: The HP1 protein family: getting a grip on chromatin. Curr. Opin. Genet. Dev., 2000; 10: [13] Fujita N., Watanabe S., Ichimura T., Tsuruzoe S., Shinkai Y., Tachibana M., Chiba T., Nakao M.: Methyl-CpG binding domain 1 (MBD1) interacts with the Suv39h1-HP1 heterochromatic complex for DNA methylation-based transcriptional repression. J. Biol. Chem., 2003; 278: [14] Gilbert N., Thomson I., Boyle S., Allan J., Ramsahoye B., Bickmore W.A.: DNA methylation affects nuclear organization, histone modifi cations, and linker histone binding but not chromatin compaction. J. Cell Biol., 2007; 177: [15] Grishok A.: RNAi mechanisms in Caenorhabditis elegans. FEBS Lett., 2005; 579: [16] Guil S., Esteller M.: DNA methylomes, histone codes and mirnas: Tying it all together. Int. J. Biochem. Cell. Biol., 2009; 41: [17] Holliday R.: Epigenetics. A historical overview. Epigenetics, 2006; 1: [18] Holliday R.: DNA methylation and epigenotypes. Biochemistry (Mosc.), 2005; 70: [19] Jenuwein T., Allis D.C.: Translating histone code. Science, 2001; 293: [20] Jørgensen H.F., Adie K., Chaubert P., Bird A.P.: Engineering a high-affinity methyl-cpg-binding protein. Nucleic Acids Res., 2006; 34: e96 [21] Jørgensen H.F., Ben-Porath I., Bird A.P.: Mbd1 is recruited to both methylated and nonmethylated CpGs via distinct DNA binding domains. Mol. Cell. Biol., 2004; 24: [22] Kloc A., Martienssen R.: RNAi, heterochromatin and the cell cycle. Trends Genet., 2008; 24: [23] Labit H., Perewoska I., Germe T., Hyrien O., Marheineke K.: DNA replication timing is deterministic at the level of chromosomal domains but stochastic at the level of replicons in Xenopus egg extracts. Nucleic Acids Res., 2008; 36: [24] Li F., Chen J., Solessio E., Gilbert D.M.: Spatial distribution and specification of mammalian replication origins during G1 phase. J. Cell Biol., 2003; 161: [25] Mandrioli M.: A new synthesis in epigenetics: towards a unified function of DNA methylation from invertebrates to vertebrates. Cell. Mol. Life Sci., 2007; 64: [26] Martin W., Russell M.J.: On the origins of cells: a hypothesis for the evolutionary transitions from abiotic geochemistry to chemoautotrophic prokaryotes, and from prokaryotes to nucleated cells. Philos. Trans. R. Soc. Lond. B Biol. Sci., 2003; 358: [27] Moazed D.: Common themes in mechanisms of gene silencing. Mol. Cell, 2001; 8: [28] Morales V., Giamarchi C., Chailleux C., Moro F., Marsaud V., Le Ricousse S., Richard-Foy H.: Chromatin structure and dynamics: Functional implications. Biochimie, 2001; 83: [29] Novik K.L., Nimmrich I., Genc B., Maier S., Piepenbrock C., Olek A., Beck S.: Epigenomics: genome-wide study of methylation phenomena. Curr. Issues Mol. Biol., 2002; 4: [30] Oehlenschläger F., Eigen M.: 30 years later A new approach to Sol Spiegelman s and Leslie Orgel s in vitro evolutionary studies. Orig. Life Evol. Biosph., 1997; 27: [31] Olszewska M.J.: Heterochromatyna i heterochromatynizacja. Post. Biol. Kom., 2007; 34: [32] Orgel L.E.: Selection in vitro. Philos. Trans. R. Soc. Lond. B Biol. Sci., 1979; 205: [33] Peng J.C., Karpen G.H.: H3K9 methylation and RNA interference regulate nucleolar organization and repeated DNA stability. Nat. Cell Biol., 2007; 9: [34] Razin A.: CpG methylation, chromatin structure and gene silencing a three-way connection. EMBO J., 1998; 17: [35] Richards E.J., Elgin S.C.: Epigenetic codes for heterochromatin formation and silencing: Rounding up the usual suspects., Cell, 2002; 108: [36] Schermelleh L., Haemmer A., Spada F., Rösing N., Meilinger D., Rothbauer U., Cardoso M.C., Leonhardt H.: Dynamics of Dnmt1 interaction with the replication machinery and its role in postreplicative maintenance of DNA methylation. Nucleic Acids Res., 2007; 35: [37] Schwaiger M., Schübeler D.: A question of timing: emerging links between transcription and replication. Curr. Opin. Genet. Dev., 2006; 16: [38] Turner B.M.: Defining an epigenetic code. Nat. Cell Biol., 2007; 9: 2 6 [39] Verdel A., Moazed D.: RNAi-directed assembly of heterochromatin in fission yeast. FEBS Lett., 2005; 579: [40] Weissmann F., Muyrers-Chen I., Musch T., Stach D., Wiessler M., Paro R., Lyko F.: DNA hypermethylation in Drosophila melanogaster causes irregular chromosome condensation and dysregulation of epigenetic histone modifications. Mol. Cell Biol., 2003; 23: [41] Woodfine K., Fiegler H., Beare D.M., Collins J.E., McCann O.T., Young B.D., Debernardi S., Mott R., Dunham I., Carter N.P.: Replication timing of the human genome. Hum. Mol. Genet., 2004; 13: [42] Yakabe S., Soejima H., Yatsuki H., Tominaga H., Zhao W., Higashimoto K., Joh K., Kudo S., Miyazaki K., Mukai T.: MeCP2 knockdown reveals DNA methylation-independent gene repression of target genes in living cells and a bias in the cellular location of target gene products. Genes Genet. Syst., 2008; 83: [43] Zappulla D.C., Sternglanz R., Leatherwood J.: Control of replication timing by a transcriptional silencer. Curr. Biol., 2002; 12: Autor deklaruje brak potencjalnych konfliktów interesów. 175
Wykład 5. Remodeling chromatyny
 Wykład 5 Remodeling chromatyny 1 Plan wykładu: 1. Przebudowa chromatyny 2. Struktura, funkcje oraz mechanizm działania kompleksów remodelujących chromatynę 3. Charakterystyka kompleksów typu SWI/SNF 4.
Wykład 5 Remodeling chromatyny 1 Plan wykładu: 1. Przebudowa chromatyny 2. Struktura, funkcje oraz mechanizm działania kompleksów remodelujących chromatynę 3. Charakterystyka kompleksów typu SWI/SNF 4.
TRANSLACJA II etap ekspresji genów
 TRANSLACJA II etap ekspresji genów Tłumaczenie informacji genetycznej zawartej w mrna (po transkrypcji z DNA) na aminokwasy budujące konkretne białko. trna Operon (wg. Jacob i Monod) Zgrupowane w jednym
TRANSLACJA II etap ekspresji genów Tłumaczenie informacji genetycznej zawartej w mrna (po transkrypcji z DNA) na aminokwasy budujące konkretne białko. trna Operon (wg. Jacob i Monod) Zgrupowane w jednym
Wykład 3. Organizacja jądra komórkowego struktura chromatyny
 Wykład 3 Organizacja jądra komórkowego struktura chromatyny Struktura jądra komórkowego Matriks jądrowa - jądro komórkowe pozbawione chromatyny Nukleoplazma Heterochromatyna Euchromatyna Jąderko Otoczka
Wykład 3 Organizacja jądra komórkowego struktura chromatyny Struktura jądra komórkowego Matriks jądrowa - jądro komórkowe pozbawione chromatyny Nukleoplazma Heterochromatyna Euchromatyna Jąderko Otoczka
Dr. habil. Anna Salek International Bio-Consulting 1 Germany
 1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
INICJACJA ELONGACJA TERMINACJA
 INICJACJA ELONGACJA TERMINACJA 2007 by National Academy of Sciences Kornberg R D PNAS 2007;104:12955-12961 Struktura chromatyny pozwala na różny sposób odczytania informacji zawartej w DNA. Możliwe staje
INICJACJA ELONGACJA TERMINACJA 2007 by National Academy of Sciences Kornberg R D PNAS 2007;104:12955-12961 Struktura chromatyny pozwala na różny sposób odczytania informacji zawartej w DNA. Możliwe staje
października 2013: Elementarz biologii molekularnej. Wykład nr 2 BIOINFORMATYKA rok II
 10 października 2013: Elementarz biologii molekularnej www.bioalgorithms.info Wykład nr 2 BIOINFORMATYKA rok II Komórka: strukturalna i funkcjonalne jednostka organizmu żywego Jądro komórkowe: chroniona
10 października 2013: Elementarz biologii molekularnej www.bioalgorithms.info Wykład nr 2 BIOINFORMATYKA rok II Komórka: strukturalna i funkcjonalne jednostka organizmu żywego Jądro komórkowe: chroniona
Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej
 Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej PRAKTIKUM Z BIOLOGII KOMÓRKI () ćwiczenie prowadzone we współpracy z Pracownią Biofizyki Komórki Badanie dynamiki białek
Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej PRAKTIKUM Z BIOLOGII KOMÓRKI () ćwiczenie prowadzone we współpracy z Pracownią Biofizyki Komórki Badanie dynamiki białek
Komórka eukariotyczna
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
TRANSKRYPCJA - I etap ekspresji genów
 Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Metylacja DNA. Anna Fogtman Pracownia Analiz Mikromacierzy Uniwersytet Warszawski Polska Akademia Nauk
 Metylacja DNA Anna Fogtman Pracownia Analiz Mikromacierzy Uniwersytet Warszawski Polska Akademia Nauk Przykład symfoniczny Przykład symfoniczny Metylacja DNA O SAM-CH SAM NH 3 5 2 6 1 H DNMT Cytozyna
Metylacja DNA Anna Fogtman Pracownia Analiz Mikromacierzy Uniwersytet Warszawski Polska Akademia Nauk Przykład symfoniczny Przykład symfoniczny Metylacja DNA O SAM-CH SAM NH 3 5 2 6 1 H DNMT Cytozyna
Epigenetyczna regulacja ekspresji genów w trakcie rozwoju zwierząt i roślin
 Epigenetyczna regulacja ekspresji genów w trakcie rozwoju zwierząt i roślin Rozwój jest z natury epigenetyczny te same geny w różnych tkankach i komórkach utrzymywane są w stanie aktywnym lub wyciszonym
Epigenetyczna regulacja ekspresji genów w trakcie rozwoju zwierząt i roślin Rozwój jest z natury epigenetyczny te same geny w różnych tkankach i komórkach utrzymywane są w stanie aktywnym lub wyciszonym
TATA box. Enhancery. CGCG ekson intron ekson intron ekson CZĘŚĆ KODUJĄCA GENU TERMINATOR. Elementy regulatorowe
 Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
Budowa histonów rdzeniowych
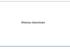 Histony rdzeniowe Budowa histonów rdzeniowych Histon H4 Silnie dodatnio naładowany N-koniec białka Globularna hydrofobowa domena odpowiedzialna za oddziaływania histon-histon oraz histon-dna Domena histonowa
Histony rdzeniowe Budowa histonów rdzeniowych Histon H4 Silnie dodatnio naładowany N-koniec białka Globularna hydrofobowa domena odpowiedzialna za oddziaływania histon-histon oraz histon-dna Domena histonowa
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
ODKRYCIE POLIMERAZY RNA IV
 ODKRYCIE POLIMERAZY RNA IV Ewa Róg-ZieliR Zielińska POLIMERAZY RNA U eukariota występuj pują trzy podstawowe rodzaje polimeraz RNA zależnych od DNA Wszystkie te polimerazy są złożone one z około o 12-17
ODKRYCIE POLIMERAZY RNA IV Ewa Róg-ZieliR Zielińska POLIMERAZY RNA U eukariota występuj pują trzy podstawowe rodzaje polimeraz RNA zależnych od DNA Wszystkie te polimerazy są złożone one z około o 12-17
Transport makrocząsteczek
 Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Modyfikacje epigenetyczne w czasie wzrostu oocytów związane z rozszerzeniem rozwoju partenogenetycznego u myszy. Małgorzata Karney
 Modyfikacje epigenetyczne w czasie wzrostu oocytów związane z rozszerzeniem rozwoju partenogenetycznego u myszy. Małgorzata Karney Epigenetyka Epigenetyka zwykle definiowana jest jako nauka o dziedzicznych
Modyfikacje epigenetyczne w czasie wzrostu oocytów związane z rozszerzeniem rozwoju partenogenetycznego u myszy. Małgorzata Karney Epigenetyka Epigenetyka zwykle definiowana jest jako nauka o dziedzicznych
Komórka stuktura i funkcje. Bogusław Nedoszytko. WSZPIZU Wydział w Gdyni
 Komórka stuktura i funkcje Bogusław Nedoszytko WSZPIZU Wydział w Gdyni Jądro komórkowe Struktura i funkcje Podziały komórkowe Jądro komórkowe 46 chromosomów 2,6 metra DNA 3 miliardy par nukleotydów (A,T,G,C)
Komórka stuktura i funkcje Bogusław Nedoszytko WSZPIZU Wydział w Gdyni Jądro komórkowe Struktura i funkcje Podziały komórkowe Jądro komórkowe 46 chromosomów 2,6 metra DNA 3 miliardy par nukleotydów (A,T,G,C)
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu w porównaniu z analizą trankryptomu:
Zarówno u organizmów eukariotycznych, jak i prokariotycznych proces replikacji ma charakter semikonserwatywny.
 HIPTEZY WYJAŚIAJĄCE MECHAIZM REPLIKACJI C. Model replikacji semikonserwatywnej zakłada on, że obie nici macierzystej cząsteczki DA są matrycą dla nowych, dosyntetyzowywanych nici REPLIKACJA każda z dwóch
HIPTEZY WYJAŚIAJĄCE MECHAIZM REPLIKACJI C. Model replikacji semikonserwatywnej zakłada on, że obie nici macierzystej cząsteczki DA są matrycą dla nowych, dosyntetyzowywanych nici REPLIKACJA każda z dwóch
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Mechanizm metylacji i demetylacji DNA znaczenie w kontroli ekspresji genów
 Mechanizm metylacji i demetylacji DNA znaczenie w kontroli ekspresji genów STRESZCZENIE Metylacja cytozyny do 5-metylocytozyny jest poreplikacyjną modyfikacją DNA, odgrywającą istotną rolę w transkrypcyjnym
Mechanizm metylacji i demetylacji DNA znaczenie w kontroli ekspresji genów STRESZCZENIE Metylacja cytozyny do 5-metylocytozyny jest poreplikacyjną modyfikacją DNA, odgrywającą istotną rolę w transkrypcyjnym
Plan wykładu: Budowa chromatyny - nukleosomy. Wpływ nukleosomów na replikację i transkrypcję
 Nukleosomy 1 Plan wykładu: Budowa chromatyny - nukleosomy Wpływ nukleosomów na replikację i transkrypcję Metody pozwalające na wyznaczanie miejsc wiązania nukleosomów Charakterystyka obsadzenia nukleosomów
Nukleosomy 1 Plan wykładu: Budowa chromatyny - nukleosomy Wpływ nukleosomów na replikację i transkrypcję Metody pozwalające na wyznaczanie miejsc wiązania nukleosomów Charakterystyka obsadzenia nukleosomów
Mechanizmy kontroli rozwoju roślin. Rafał Archacki
 Mechanizmy kontroli rozwoju roślin Rafał Archacki Drzewo życia pozycja roślin i zwierząt http://5e.plantphys.net/article.php?ch=t&id=399 Ewolucja roślin ewolucja procesu rozmnażania i rozwoju http://5e.plantphys.net/article.php?ch=t&id=399
Mechanizmy kontroli rozwoju roślin Rafał Archacki Drzewo życia pozycja roślin i zwierząt http://5e.plantphys.net/article.php?ch=t&id=399 Ewolucja roślin ewolucja procesu rozmnażania i rozwoju http://5e.plantphys.net/article.php?ch=t&id=399
Analizy wielkoskalowe w badaniach chromatyny
 Analizy wielkoskalowe w badaniach chromatyny Analizy wielkoskalowe wykorzystujące mikromacierze DNA Genotypowanie: zróżnicowane wewnątrz genów RNA Komórka eukariotyczna Ekspresja genów: Które geny? Poziom
Analizy wielkoskalowe w badaniach chromatyny Analizy wielkoskalowe wykorzystujące mikromacierze DNA Genotypowanie: zróżnicowane wewnątrz genów RNA Komórka eukariotyczna Ekspresja genów: Które geny? Poziom
Alchemia epigenetycznej regulacji pluripotencji
 Alchemia epigenetycznej regulacji pluripotencji Joanna Bem Iwona Grabowska * Zakład Cytologii, Wydział Biologii, Uniwersytet Warszawski, Warszawa * Zakład Cytologii, Wydział Biologii, Uniwersytet Warszawski,
Alchemia epigenetycznej regulacji pluripotencji Joanna Bem Iwona Grabowska * Zakład Cytologii, Wydział Biologii, Uniwersytet Warszawski, Warszawa * Zakład Cytologii, Wydział Biologii, Uniwersytet Warszawski,
Informacje dotyczące pracy kontrolnej
 Informacje dotyczące pracy kontrolnej Słuchacze, którzy z przyczyn usprawiedliwionych nie przystąpili do pracy kontrolnej lub otrzymali z niej ocenę negatywną zobowiązani są do dnia 06 grudnia 2015 r.
Informacje dotyczące pracy kontrolnej Słuchacze, którzy z przyczyn usprawiedliwionych nie przystąpili do pracy kontrolnej lub otrzymali z niej ocenę negatywną zobowiązani są do dnia 06 grudnia 2015 r.
Rola chromatyny w regulacji ekspresji genów. Monika Zakrzewska-Płaczek
 Rola chromatyny w regulacji ekspresji genów Monika Zakrzewska-Płaczek monika.z@ibb.waw.pl Co oznacza epigenetyka? Epigenetyczna regulacja ekspresji genów = zmiana ekspresji genu, która zachodzi bez zmiany
Rola chromatyny w regulacji ekspresji genów Monika Zakrzewska-Płaczek monika.z@ibb.waw.pl Co oznacza epigenetyka? Epigenetyczna regulacja ekspresji genów = zmiana ekspresji genu, która zachodzi bez zmiany
Wykład 14 Biosynteza białek
 BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
Rola chromatyny w regulacji ekspresji genów. Monika Zakrzewska-Płaczek
 Rola chromatyny w regulacji ekspresji genów Monika Zakrzewska-Płaczek monika.z@ibb.waw.pl Epigenetyczna etyczna regulacja ekspresji genów zmiana ekspresji genu, która zachodzi bez zmiany sekwencji DNA
Rola chromatyny w regulacji ekspresji genów Monika Zakrzewska-Płaczek monika.z@ibb.waw.pl Epigenetyczna etyczna regulacja ekspresji genów zmiana ekspresji genu, która zachodzi bez zmiany sekwencji DNA
The Maternal Nucleolus Is Essential for Early Embryonic Development in Mammals
 The Maternal Nucleolus Is Essential for Early Embryonic Development in Mammals autorstwa Sugako Ogushi Science vol 319, luty 2008 Prezentacja Kamil Kowalski Jąderko pochodzenia matczynego jest konieczne
The Maternal Nucleolus Is Essential for Early Embryonic Development in Mammals autorstwa Sugako Ogushi Science vol 319, luty 2008 Prezentacja Kamil Kowalski Jąderko pochodzenia matczynego jest konieczne
ANDRZEJ T. WIERZBICKI Zakład Biologii Molekularnej Roślin Uniwersytet Warszawski Pawińskiego 5a, Warszawa
 Tom 53, 2004 Numer 3 4 (264 265) Strony 271 280 ANDRZEJ T. WIERZBICKI Zakład Biologii Molekularnej Roślin Uniwersytet Warszawski Pawińskiego 5a, 02-106 Warszawa e-mail: andw@ibb.waw.pl DZIEDZICZENIE EPIGENETYCZNE
Tom 53, 2004 Numer 3 4 (264 265) Strony 271 280 ANDRZEJ T. WIERZBICKI Zakład Biologii Molekularnej Roślin Uniwersytet Warszawski Pawińskiego 5a, 02-106 Warszawa e-mail: andw@ibb.waw.pl DZIEDZICZENIE EPIGENETYCZNE
GENOM I JEGO STRUKTURA
 GENOM I JEGO STRUKTURA GENOM Ogół materiału genetycznego (kwasu nukleinowego niosącego informację genetyczną) zawartego w pojedynczej części składowej (komórce, cząstce wirusa) organizmu 1 Genom eukariotyczny
GENOM I JEGO STRUKTURA GENOM Ogół materiału genetycznego (kwasu nukleinowego niosącego informację genetyczną) zawartego w pojedynczej części składowej (komórce, cząstce wirusa) organizmu 1 Genom eukariotyczny
cytoplazma + jądro komórkowe = protoplazma Jądro komórkowe
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
NUTRIGENOMIKA na co mają geny apetyt. Ewa Róg - Zielińska
 NUTRIGENOMIKA na co mają geny apetyt Ewa Róg - Zielińska NUTRIGENOMIKA badanie zależności między żywieniem a odpowiedzią organizmu na poziomie ekspresji genów dieta ma wpływ na każdy etap ekspresji - na
NUTRIGENOMIKA na co mają geny apetyt Ewa Róg - Zielińska NUTRIGENOMIKA badanie zależności między żywieniem a odpowiedzią organizmu na poziomie ekspresji genów dieta ma wpływ na każdy etap ekspresji - na
WPROWADZENIE DO GENETYKI MOLEKULARNEJ
 WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
BUDOWA I FUNKCJA GENOMU LUDZKIEGO
 BUDOWA I FUNKCJA GENOMU LUDZKIEGO Magdalena Mayer Katedra i Zakład Genetyki Medycznej UM w Poznaniu 1. Projekt poznania genomu człowieka: Cele programu: - skonstruowanie szczegółowych map fizycznych i
BUDOWA I FUNKCJA GENOMU LUDZKIEGO Magdalena Mayer Katedra i Zakład Genetyki Medycznej UM w Poznaniu 1. Projekt poznania genomu człowieka: Cele programu: - skonstruowanie szczegółowych map fizycznych i
mikrosatelitarne, minisatelitarne i polimorfizm liczby kopii
 Zawartość 139371 1. Wstęp zarys historii genetyki, czyli od genetyki klasycznej do genomiki 2. Chromosomy i podziały jądra komórkowego 2.1. Budowa chromosomu 2.2. Barwienie prążkowe chromosomów 2.3. Mitoza
Zawartość 139371 1. Wstęp zarys historii genetyki, czyli od genetyki klasycznej do genomiki 2. Chromosomy i podziały jądra komórkowego 2.1. Budowa chromosomu 2.2. Barwienie prążkowe chromosomów 2.3. Mitoza
Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją).
 Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją). Czym jest życie? metabolizm + informacja (replikacja) 2 Cząsteczki organiczne mog y powstać w atmosferze pierwotnej
Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją). Czym jest życie? metabolizm + informacja (replikacja) 2 Cząsteczki organiczne mog y powstać w atmosferze pierwotnej
Składniki diety a stabilność struktury DNA
 Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Toruń, dnia r.
 dr hab. Dariusz Jan Smoliński Zakład Biologii Komórki Wydział Biologii i Ochrony Środowiska Uniwersytetu Mikołaja Kopernika w Toruniu Toruń, dnia 24.06.2013 r. RECENZJA rozprawy doktorskiej Pana magistra
dr hab. Dariusz Jan Smoliński Zakład Biologii Komórki Wydział Biologii i Ochrony Środowiska Uniwersytetu Mikołaja Kopernika w Toruniu Toruń, dnia 24.06.2013 r. RECENZJA rozprawy doktorskiej Pana magistra
transkrypcja chromatyny
 transkrypcja chromatyny problem: Jak to może e działać: dysocjacja histonów? kompleks pol II RNA >500 kd skip: split: nukleosom: 145 bp DNA = 100 kd rdzeń histonowy = 100 kd strip: + Skip czy Split czy
transkrypcja chromatyny problem: Jak to może e działać: dysocjacja histonów? kompleks pol II RNA >500 kd skip: split: nukleosom: 145 bp DNA = 100 kd rdzeń histonowy = 100 kd strip: + Skip czy Split czy
Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii
 Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii 1. Technologia rekombinowanego DNA jest podstawą uzyskiwania genetycznie zmodyfikowanych organizmów 2. Medycyna i ochrona zdrowia
Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii 1. Technologia rekombinowanego DNA jest podstawą uzyskiwania genetycznie zmodyfikowanych organizmów 2. Medycyna i ochrona zdrowia
Spis treści 1 Komórki i wirusy Budowa komórki Budowa k
 Spis treści 1 Komórki i wirusy.......................................... 1 1.1 Budowa komórki........................................ 1 1.1.1 Budowa komórki prokariotycznej.................... 2 1.1.2
Spis treści 1 Komórki i wirusy.......................................... 1 1.1 Budowa komórki........................................ 1 1.1.1 Budowa komórki prokariotycznej.................... 2 1.1.2
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 5 Droga od genu do
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 5 Droga od genu do
Dr hab. Anna Bębenek Warszawa,
 Dr hab. Anna Bębenek Warszawa, 14.01. 2018 Instytut Biochemii i Biofizyki PAN Ul. Pawińskiego 5a 02-106 Warszawa Recenzja pracy doktorskiej Pana mgr Michała Płachty Pod Tytułem Regulacja funkcjonowania
Dr hab. Anna Bębenek Warszawa, 14.01. 2018 Instytut Biochemii i Biofizyki PAN Ul. Pawińskiego 5a 02-106 Warszawa Recenzja pracy doktorskiej Pana mgr Michała Płachty Pod Tytułem Regulacja funkcjonowania
Chromatyna struktura i funkcja
 Chromatyna struktura i funkcja dr hab. Marta Koblowska dr Rafał Archacki http://www.accessexcellence.org/ab/gg/nucleosome.html GENETYKA FRIEDRICH MIESCHER (1844-1895) W 1869 roku wyizolował z jąder komórkowych
Chromatyna struktura i funkcja dr hab. Marta Koblowska dr Rafał Archacki http://www.accessexcellence.org/ab/gg/nucleosome.html GENETYKA FRIEDRICH MIESCHER (1844-1895) W 1869 roku wyizolował z jąder komórkowych
Regulacja ekspresji genów. Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego.
 Regulacja ekspresji genów Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego. Problem: jak sprawić aby z jednej komórki powstał wielokomórkowy
Regulacja ekspresji genów Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego. Problem: jak sprawić aby z jednej komórki powstał wielokomórkowy
Zawartość. Wstęp 1. Historia wirusologii. 2. Klasyfikacja wirusów
 Zawartość 139585 Wstęp 1. Historia wirusologii 2. Klasyfikacja wirusów 3. Struktura cząstek wirusowych 3.1. Metody określania struktury cząstek wirusowych 3.2. Budowa cząstek wirusowych o strukturze helikalnej
Zawartość 139585 Wstęp 1. Historia wirusologii 2. Klasyfikacja wirusów 3. Struktura cząstek wirusowych 3.1. Metody określania struktury cząstek wirusowych 3.2. Budowa cząstek wirusowych o strukturze helikalnej
EPIGENETYKA. genetyka XXI wieku? HUMAN GENOME PROJECT HUMAN GENOME PROJECT. CELE: 1. Identyfikacja - około 25 tys.
 EPIGENETYKA genetyka XXI wieku? HUMAN GENOME PROJECT CELE: 1. Identyfikacja - około 25 tys. genów 2. Oznaczenie sekwencji - 3 miliardów par zasad 3. Zgromadzenie informacji w formie bazy danych. Planowany
EPIGENETYKA genetyka XXI wieku? HUMAN GENOME PROJECT CELE: 1. Identyfikacja - około 25 tys. genów 2. Oznaczenie sekwencji - 3 miliardów par zasad 3. Zgromadzenie informacji w formie bazy danych. Planowany
Teoria ewolucji. Podstawowe pojęcia. Wspólne pochodzenie.
 Teoria ewolucji Podstawowe pojęcia. Wspólne pochodzenie. Informacje Kontakt: Paweł Golik Instytut Genetyki i Biotechnologii, Pawińskiego 5A pgolik@igib.uw.edu.pl Informacje, materiały: http://www.igib.uw.edu.pl/
Teoria ewolucji Podstawowe pojęcia. Wspólne pochodzenie. Informacje Kontakt: Paweł Golik Instytut Genetyki i Biotechnologii, Pawińskiego 5A pgolik@igib.uw.edu.pl Informacje, materiały: http://www.igib.uw.edu.pl/
Modyfikacje histonów rdzeniowych
 Modyfikacje histonów rdzeniowych Fosforylacja (seryna, treonina) Acetylacja (lizyna) Modyfikacje histonów rdzeniowych Metylacja (lizyna, arginina) ADP-rybozylacja Ubikwitynylacja (lizyna) Sumoilacja (lizyna)
Modyfikacje histonów rdzeniowych Fosforylacja (seryna, treonina) Acetylacja (lizyna) Modyfikacje histonów rdzeniowych Metylacja (lizyna, arginina) ADP-rybozylacja Ubikwitynylacja (lizyna) Sumoilacja (lizyna)
WPROWADZENIE DO GENETYKI MOLEKULARNEJ
 WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
białka wiążące specyficzne sekwencje DNA czynniki transkrypcyjne
 białka wiążące specyficzne sekwencje DNA czynniki transkrypcyjne http://www.umass.edu/molvis/bme3d/materials/jtat_080510/exploringdna/ch_flex/chapter.htm czynniki transkrypcyjne (aktywatory/represory)
białka wiążące specyficzne sekwencje DNA czynniki transkrypcyjne http://www.umass.edu/molvis/bme3d/materials/jtat_080510/exploringdna/ch_flex/chapter.htm czynniki transkrypcyjne (aktywatory/represory)
Dominika Stelmach Gr. 10B2
 Dominika Stelmach Gr. 10B2 Czym jest DNA? Wielkocząsteczkowy organiczny związek chemiczny z grupy kwasów nukleinowych Zawiera kwas deoksyrybonukleoinowy U organizmów eukariotycznych zlokalizowany w jądrze
Dominika Stelmach Gr. 10B2 Czym jest DNA? Wielkocząsteczkowy organiczny związek chemiczny z grupy kwasów nukleinowych Zawiera kwas deoksyrybonukleoinowy U organizmów eukariotycznych zlokalizowany w jądrze
Fragment cząsteczki DNA stanowiący matrycę dla syntezy cząsteczki lub podjednostki białka nazywamy GENEM
 KONTROLA EKSPRESJI GENU PRZEKAZYWANIE INFORMACJI GENETYCZNEJ Informacja genetyczna - instrukcje kierujące wszystkimi funkcjami komórki lub organizmu zapisane jako określone, swoiste sekwencje nukleotydów
KONTROLA EKSPRESJI GENU PRZEKAZYWANIE INFORMACJI GENETYCZNEJ Informacja genetyczna - instrukcje kierujące wszystkimi funkcjami komórki lub organizmu zapisane jako określone, swoiste sekwencje nukleotydów
Regulacja Ekspresji Genów
 Regulacja Ekspresji Genów Wprowadzenie o Ekspresja genu jest to złożony proces jego transkrypcji do mrna, o Obróbki tego mrna, a następnie o Translacji do białka. 4/17/2019 2 4/17/2019 3 E 1 GEN 3 Promotor
Regulacja Ekspresji Genów Wprowadzenie o Ekspresja genu jest to złożony proces jego transkrypcji do mrna, o Obróbki tego mrna, a następnie o Translacji do białka. 4/17/2019 2 4/17/2019 3 E 1 GEN 3 Promotor
WARUNKI ZALICZENIA PRZEDMIOTU- 5 ECTS
 WARUNKI ZALICZENIA PRZEDMIOTU- 5 ECTS KOLOKWIA; 15% KOLOKWIA-MIN; 21% WEJŚCIÓWKI; 6% WEJŚCIÓWKI-MIN; 5% EGZAMIN; 27% EGZAMIN-MIN; 26% WARUNKI ZALICZENIA PRZEDMIOTU- 5 ECTS kolokwium I 12% poprawa kolokwium
WARUNKI ZALICZENIA PRZEDMIOTU- 5 ECTS KOLOKWIA; 15% KOLOKWIA-MIN; 21% WEJŚCIÓWKI; 6% WEJŚCIÓWKI-MIN; 5% EGZAMIN; 27% EGZAMIN-MIN; 26% WARUNKI ZALICZENIA PRZEDMIOTU- 5 ECTS kolokwium I 12% poprawa kolokwium
Podstawy genetyki molekularnej
 Podstawy genetyki molekularnej Materiał genetyczny Materiałem genetycznym są kwasy nukleinowe Materiałem genetycznym organizmów komórkowych jest kwas deoksyrybonukleinowy (DNA) 5 DNA zbudowany jest z nukleotydów
Podstawy genetyki molekularnej Materiał genetyczny Materiałem genetycznym są kwasy nukleinowe Materiałem genetycznym organizmów komórkowych jest kwas deoksyrybonukleinowy (DNA) 5 DNA zbudowany jest z nukleotydów
DNA superhelikalny eukariota DNA kolisty bakterie plazmidy mitochondria DNA liniowy wirusy otrzymywany in vitro
 DNA- kwas deoksyrybonukleinowy: DNA superhelikalny eukariota DNA kolisty bakterie plazmidy mitochondria DNA liniowy wirusy otrzymywany in vitro RNA- kwasy rybonukleinowe: RNA matrycowy (mrna) transkrybowany
DNA- kwas deoksyrybonukleinowy: DNA superhelikalny eukariota DNA kolisty bakterie plazmidy mitochondria DNA liniowy wirusy otrzymywany in vitro RNA- kwasy rybonukleinowe: RNA matrycowy (mrna) transkrybowany
ROZPORZĄDZENIE KOMISJI (UE) / z dnia r.
 KOMISJA EUROPEJSKA Bruksela, dnia 29.5.2018 C(2018) 3193 final ROZPORZĄDZENIE KOMISJI (UE) / z dnia 29.5.2018 r. zmieniające rozporządzenie (WE) nr 847/2000 w odniesieniu do definicji pojęcia podobnego
KOMISJA EUROPEJSKA Bruksela, dnia 29.5.2018 C(2018) 3193 final ROZPORZĄDZENIE KOMISJI (UE) / z dnia 29.5.2018 r. zmieniające rozporządzenie (WE) nr 847/2000 w odniesieniu do definicji pojęcia podobnego
Pamiętając o komplementarności zasad azotowych, dopisz sekwencję nukleotydów brakującej nici DNA. A C C G T G C C A A T C G A...
 1. Zadanie (0 2 p. ) Porównaj mitozę i mejozę, wpisując do tabeli podane określenia oraz cyfry. ta sama co w komórce macierzystej, o połowę mniejsza niż w komórce macierzystej, gamety, komórki budujące
1. Zadanie (0 2 p. ) Porównaj mitozę i mejozę, wpisując do tabeli podane określenia oraz cyfry. ta sama co w komórce macierzystej, o połowę mniejsza niż w komórce macierzystej, gamety, komórki budujące
Analizy DNA in silico - czyli czego można szukać i co można znaleźć w sekwencjach nukleotydowych???
 Analizy DNA in silico - czyli czego można szukać i co można znaleźć w sekwencjach nukleotydowych??? Alfabet kwasów nukleinowych jest stosunkowo ubogi!!! Dla sekwencji DNA (RNA) stosuje się zasadniczo*
Analizy DNA in silico - czyli czego można szukać i co można znaleźć w sekwencjach nukleotydowych??? Alfabet kwasów nukleinowych jest stosunkowo ubogi!!! Dla sekwencji DNA (RNA) stosuje się zasadniczo*
Nowoczesne systemy ekspresji genów
 Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Transport makrocząsteczek (białek)
 Transport makrocząsteczek (białek) Transport makrocząsteczek sortowanie białek - sekwencje sygnałowe lata 70-te XX w. - Günter Blobel - hipoteza sygnałowa; 1999r - nagroda Nobla Sekwencja sygnałowa: A
Transport makrocząsteczek (białek) Transport makrocząsteczek sortowanie białek - sekwencje sygnałowe lata 70-te XX w. - Günter Blobel - hipoteza sygnałowa; 1999r - nagroda Nobla Sekwencja sygnałowa: A
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Ekspresja genów jest regulowana
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Ekspresja genów jest regulowana
Prokariota i Eukariota
 Prokariota i Eukariota W komórkach organizmów żywych ilość DNA jest zazwyczaj stała i charakterystyczna dla danego gatunku. ILOŚĆ DNA PRZYPADAJĄCA NA APARAT GENETYCZNY WZRASTA WRAZ Z BARDZIEJ FILOGENETYCZNIE
Prokariota i Eukariota W komórkach organizmów żywych ilość DNA jest zazwyczaj stała i charakterystyczna dla danego gatunku. ILOŚĆ DNA PRZYPADAJĄCA NA APARAT GENETYCZNY WZRASTA WRAZ Z BARDZIEJ FILOGENETYCZNIE
Zjawiska epigenetyczne w patogenezie nowotworów Nowe możliwości profilaktyki i terapii?
 Zjawiska epigenetyczne w patogenezie nowotworów Nowe możliwości profilaktyki i terapii? Jarosław Paluszczak Wanda Baer-Dubowska * Katedra Biochemii Farmaceutycznej Akademii Medycznej im. K. Marcinkowskiego,
Zjawiska epigenetyczne w patogenezie nowotworów Nowe możliwości profilaktyki i terapii? Jarosław Paluszczak Wanda Baer-Dubowska * Katedra Biochemii Farmaceutycznej Akademii Medycznej im. K. Marcinkowskiego,
O ROZUMIENIU POJĘCIA ''INFORMACJA'' W BIOLOGII WSPÓŁCZESNEJ. Radosław Siedliński
 O ROZUMIENIU POJĘCIA ''INFORMACJA'' W BIOLOGII WSPÓŁCZESNEJ Radosław Siedliński Dyskusja nad znaczeniem i rolą pojęcia ''informacji'' w biologii koncentruje się na opisie relacji zachodzących między genami
O ROZUMIENIU POJĘCIA ''INFORMACJA'' W BIOLOGII WSPÓŁCZESNEJ Radosław Siedliński Dyskusja nad znaczeniem i rolą pojęcia ''informacji'' w biologii koncentruje się na opisie relacji zachodzących między genami
Jak działają geny. Podstawy biologii molekularnej genu
 Jak działają geny Podstawy biologii molekularnej genu Uniwersalność życia Podstawowe mechanizmy są takie same u wszystkich znanych organizmów budowa DNA i RNA kod genetyczny repertuar aminokwasów budujących
Jak działają geny Podstawy biologii molekularnej genu Uniwersalność życia Podstawowe mechanizmy są takie same u wszystkich znanych organizmów budowa DNA i RNA kod genetyczny repertuar aminokwasów budujących
Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych
 Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych Zalety w porównaniu z analizą trankryptomu: analiza transkryptomu komórki identyfikacja mrna nie musi jeszcze oznaczać
Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych Zalety w porównaniu z analizą trankryptomu: analiza transkryptomu komórki identyfikacja mrna nie musi jeszcze oznaczać
Zgodnie z tzw. modelem interpunkcji trna, cząsteczki mt-trna wyznaczają miejsca
 Tytuł pracy: Autor: Promotor rozprawy: Recenzenci: Funkcje białek ELAC2 i SUV3 u ssaków i ryb Danio rerio. Praca doktorska wykonana w Instytucie Genetyki i Biotechnologii, Wydział Biologii UW Lien Brzeźniak
Tytuł pracy: Autor: Promotor rozprawy: Recenzenci: Funkcje białek ELAC2 i SUV3 u ssaków i ryb Danio rerio. Praca doktorska wykonana w Instytucie Genetyki i Biotechnologii, Wydział Biologii UW Lien Brzeźniak
Zmiany epigenetyczne a dieta
 GENO-centryczne teorie mają ograniczony zasięg Klasyczna genetyka nie może wytłumaczyć na przykład : Zmiany epigenetyczne a dieta 1. różnorodności fenotypowej w obrębie populacji; 2. dlaczego bliźniaki
GENO-centryczne teorie mają ograniczony zasięg Klasyczna genetyka nie może wytłumaczyć na przykład : Zmiany epigenetyczne a dieta 1. różnorodności fenotypowej w obrębie populacji; 2. dlaczego bliźniaki
Metody bioinformatyki. Ekspresja genów. prof. dr hab. Jan Mulawka
 Metody bioinformatyki Ekspresja genów prof. dr hab. Jan Mulawka Genetyczny skład prawie wszystkich komórek somatycznych organizmów wielokomórkowych jest identyczny. Fenotyp (swoistość tkankowa lub komórkowa)
Metody bioinformatyki Ekspresja genów prof. dr hab. Jan Mulawka Genetyczny skład prawie wszystkich komórek somatycznych organizmów wielokomórkowych jest identyczny. Fenotyp (swoistość tkankowa lub komórkowa)
The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna
 Streszczenie rozprawy doktorskiej pt. The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna mgr Tomasz Turowski, promotor prof. dr hab.
Streszczenie rozprawy doktorskiej pt. The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna mgr Tomasz Turowski, promotor prof. dr hab.
Regulacja transkrypcji genów eukariotycznych
 Regulacja transkrypcji genów eukariotycznych Klasyczne wyobrażenie genu fragment DNA, który koduje mrna Definicja genu GEN- podstawowa jednostka dziedziczenia Region DNA, który określa charakterystyczną
Regulacja transkrypcji genów eukariotycznych Klasyczne wyobrażenie genu fragment DNA, który koduje mrna Definicja genu GEN- podstawowa jednostka dziedziczenia Region DNA, który określa charakterystyczną
Zmiany epigenetyczne a dieta
 Zmiany epigenetyczne a dieta Prof. dr hab. n. med. Małgorzata Milkiewicz Zmiany epigenetyczne a dieta 1 Chromatyna ulega kondensacji i dekondensacji podczas cyklu komórkowego stopień jej kondensacji wpływa
Zmiany epigenetyczne a dieta Prof. dr hab. n. med. Małgorzata Milkiewicz Zmiany epigenetyczne a dieta 1 Chromatyna ulega kondensacji i dekondensacji podczas cyklu komórkowego stopień jej kondensacji wpływa
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Budowa rybosomu Translacja
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Budowa rybosomu Translacja
Podstawy biologii. Informacja genetyczna. Co to jest ewolucja.
 Podstawy biologii Informacja genetyczna. Co to jest ewolucja. Materiał genetyczny Materiałem genetycznym są kwasy nukleinowe Materiałem genetycznym organizmów komórkowych jest kwas deoksyrybonukleinowy
Podstawy biologii Informacja genetyczna. Co to jest ewolucja. Materiał genetyczny Materiałem genetycznym są kwasy nukleinowe Materiałem genetycznym organizmów komórkowych jest kwas deoksyrybonukleinowy
Epigenetic modifications during oocyte growth correlates with extended parthenogenetic developement in the mouse
 Epigenetic modifications during oocyte growth correlates with extended parthenogenetic developement in the mouse Tomohiro Kono, Yayoi Obata, Tomomi Yoshimzu, Tatsuo Nakahara & John Carroll Rozwój partenogenetyczny
Epigenetic modifications during oocyte growth correlates with extended parthenogenetic developement in the mouse Tomohiro Kono, Yayoi Obata, Tomomi Yoshimzu, Tatsuo Nakahara & John Carroll Rozwój partenogenetyczny
Rzęski, wici - budowa Mikrotubule. rozmieszczenie organelli. Stabilne mikrotubule szkielet rzęsek i wici
 Mikrotubule dynamiczna niestabilność - stabilizacja rozmieszczenie organelli ER Golgi organizują wnętrze komórki - polaryzacja komórki Mt Mt organizacja ER, aparatu Golgiego przemieszczanie mitochondriów
Mikrotubule dynamiczna niestabilność - stabilizacja rozmieszczenie organelli ER Golgi organizują wnętrze komórki - polaryzacja komórki Mt Mt organizacja ER, aparatu Golgiego przemieszczanie mitochondriów
Interfaza to niemal 90% cyklu komórkowego. Dzieli się na 3 fazy: G1, S i G2.
 W wyniku podziału komórki powstaje komórka potomna, która ma o połowę mniej DNA od komórki macierzystej i jest o połowę mniejsza. Aby komórka potomna była zdolna do kolejnego podziału musi osiągnąć rozmiary
W wyniku podziału komórki powstaje komórka potomna, która ma o połowę mniej DNA od komórki macierzystej i jest o połowę mniejsza. Aby komórka potomna była zdolna do kolejnego podziału musi osiągnąć rozmiary
DNA musi współdziałać z białkami!
 DNA musi współdziałać z białkami! Specyficzność oddziaływań między DNA a białkami wiążącymi DNA zależy od: zmian konformacyjnych wzdłuż cząsteczki DNA zróżnicowania struktury DNA wynikającego z sekwencji
DNA musi współdziałać z białkami! Specyficzność oddziaływań między DNA a białkami wiążącymi DNA zależy od: zmian konformacyjnych wzdłuż cząsteczki DNA zróżnicowania struktury DNA wynikającego z sekwencji
Wielofunkcyjne bialko CBC dynamika wiazania konca 5 mrna
 Wielofunkcyjne bialko CBC dynamika wiazania konca 5 mrna Ryszard Stolarski UNIWERSYTET WARSZAWSKI Wydzial Fizyki, Instytut Fizyki Doswiadczalnej, Zaklad Biofizyki ul. Zwirki i Wigury 93, 02-089 Warszawa
Wielofunkcyjne bialko CBC dynamika wiazania konca 5 mrna Ryszard Stolarski UNIWERSYTET WARSZAWSKI Wydzial Fizyki, Instytut Fizyki Doswiadczalnej, Zaklad Biofizyki ul. Zwirki i Wigury 93, 02-089 Warszawa
Epigenome - 'above the genome'
 e - 'above the genome' Wydziaª Matematyki i Informatyki UJ Instytut Informatyki 14 stycznia 2013 e Rysunek: ¹ródªo: http://learn.genetics.utah.edu/content/epigenetics/nutrition/ e Plan Genom 1 Genom e
e - 'above the genome' Wydziaª Matematyki i Informatyki UJ Instytut Informatyki 14 stycznia 2013 e Rysunek: ¹ródªo: http://learn.genetics.utah.edu/content/epigenetics/nutrition/ e Plan Genom 1 Genom e
THE UNFOLDED PROTEIN RESPONSE
 THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
Spis treści. 1 Budowa genomu jądrowego (M.J. Olszewska, J. Małuszyńska) 13. Przedmowa 10
 Spis treści Przedmowa 10 1 Budowa genomu jądrowego (M.J. Olszewska, J. Małuszyńska) 13 1.1. Organizacja DNA jądrowego 13 1.1.1. Rodzaje sekwencji powtarzalnych i ich lokalizacja 14 1.1.1.1. Sekwencje rozproszone
Spis treści Przedmowa 10 1 Budowa genomu jądrowego (M.J. Olszewska, J. Małuszyńska) 13 1.1. Organizacja DNA jądrowego 13 1.1.1. Rodzaje sekwencji powtarzalnych i ich lokalizacja 14 1.1.1.1. Sekwencje rozproszone
Wykład 13. Regulacja cyklu komórkowego w odpowiedzi na uszkodzenia DNA. Mechanizmy powstawania nowotworów
 Wykład 13 Regulacja cyklu komórkowego w odpowiedzi na uszkodzenia DNA Mechanizmy powstawania nowotworów Uszkodzenie DNA Wykrycie uszkodzenia Naprawa DNA Zatrzymanie cyklu kom. Apoptoza Źródła uszkodzeń
Wykład 13 Regulacja cyklu komórkowego w odpowiedzi na uszkodzenia DNA Mechanizmy powstawania nowotworów Uszkodzenie DNA Wykrycie uszkodzenia Naprawa DNA Zatrzymanie cyklu kom. Apoptoza Źródła uszkodzeń
Imię i nazwisko...kl...
 Gimnazjum nr 4 im. Ojca Świętego Jana Pawła II we Wrocławiu SPRAWDZIAN GENETYKA GR. A Imię i nazwisko...kl.... 1. Nauka o regułach i mechanizmach dziedziczenia to: (0-1pkt) a) cytologia b) biochemia c)
Gimnazjum nr 4 im. Ojca Świętego Jana Pawła II we Wrocławiu SPRAWDZIAN GENETYKA GR. A Imię i nazwisko...kl.... 1. Nauka o regułach i mechanizmach dziedziczenia to: (0-1pkt) a) cytologia b) biochemia c)
Cykl komórkowy. Rozmnażanie komórek G 1, S, G 2. (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza)
 Rozmnażanie komórek (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza) G 1, S, G 2 podział komórki (faza M) Obejmuje: podwojenie zawartości komórki (skopiowanie
Rozmnażanie komórek (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza) G 1, S, G 2 podział komórki (faza M) Obejmuje: podwojenie zawartości komórki (skopiowanie
Geny i działania na nich
 Metody bioinformatyki Geny i działania na nich prof. dr hab. Jan Mulawka Trzy królestwa w biologii Prokaryota organizmy, których komórki nie zawierają jądra, np. bakterie Eukaryota - organizmy, których
Metody bioinformatyki Geny i działania na nich prof. dr hab. Jan Mulawka Trzy królestwa w biologii Prokaryota organizmy, których komórki nie zawierają jądra, np. bakterie Eukaryota - organizmy, których
Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych. źródło: (3)
 Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych źródło: (3) Interakcje białko-białko Ze względu na zadanie: strukturalne lub funkcjonalne. Ze względu na właściwości fizyczne: stałe lub
Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych źródło: (3) Interakcje białko-białko Ze względu na zadanie: strukturalne lub funkcjonalne. Ze względu na właściwości fizyczne: stałe lub
Zagrożenia i ochrona przyrody
 Wymagania podstawowe Uczeń: Wymagania ponadpodstawowe Uczeń: Zagrożenia i ochrona przyrody wskazuje zagrożenia atmosfery powstałe w wyniku działalności człowieka, omawia wpływ zanieczyszczeń atmosfery
Wymagania podstawowe Uczeń: Wymagania ponadpodstawowe Uczeń: Zagrożenia i ochrona przyrody wskazuje zagrożenia atmosfery powstałe w wyniku działalności człowieka, omawia wpływ zanieczyszczeń atmosfery
Regulacja transkrypcji genów eukariotycznych
 Regulacja transkrypcji genów eukariotycznych Definicja genu Region DNA, który określa dziedziczoną cechę organizmu; zwykle koduje pojedyncze białko lub RNA. Zawiera całą funkcjonalną podjednostkę wraz
Regulacja transkrypcji genów eukariotycznych Definicja genu Region DNA, który określa dziedziczoną cechę organizmu; zwykle koduje pojedyncze białko lub RNA. Zawiera całą funkcjonalną podjednostkę wraz
Rozkład materiału z biologii dla klasy III AD. 7 godz / tyg rok szkolny 2016/17
 Rozkład materiału z biologii dla klasy III AD zakres rozszerzony LO 7 godz / tyg rok szkolny 2016/17 Biologia na czasie 2 zakres rozszerzony nr dopuszczenia 564/2/2012 Biologia na czasie 3 zakres rozszerzony
Rozkład materiału z biologii dla klasy III AD zakres rozszerzony LO 7 godz / tyg rok szkolny 2016/17 Biologia na czasie 2 zakres rozszerzony nr dopuszczenia 564/2/2012 Biologia na czasie 3 zakres rozszerzony
Replikacja DNA. Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego.
 Replikacja DNA Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego. Replikacja DNA jest bardzo złożonym procesem, w którym biorą udział setki
Replikacja DNA Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego. Replikacja DNA jest bardzo złożonym procesem, w którym biorą udział setki
Laboratoria.net Innowacje Nauka Technologie
 Akceptuję W ramach naszej witryny stosujemy pliki cookies w celu świadczenia państwu usług na najwyższym poziomie, w tym w sposób dostosowany do indywidualnych potrzeb. Korzystanie z witryny bez zmiany
Akceptuję W ramach naszej witryny stosujemy pliki cookies w celu świadczenia państwu usług na najwyższym poziomie, w tym w sposób dostosowany do indywidualnych potrzeb. Korzystanie z witryny bez zmiany
Biologia molekularna genu - replikacja
 Biologia molekularna genu - replikacja Funkcje informacji genetycznej Replikacja powielanie genomu, utrzymywanie stabilności genomu Ekspresja Odczytywanie informacji, niezbędne do funkcjonowania komórki
Biologia molekularna genu - replikacja Funkcje informacji genetycznej Replikacja powielanie genomu, utrzymywanie stabilności genomu Ekspresja Odczytywanie informacji, niezbędne do funkcjonowania komórki
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA
 SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
Badanie funkcji genu
 Badanie funkcji genu Funkcję genu można zbadać różnymi sposobami Przypadkowa analizy funkcji genu MUTACJA FENOTYP GEN Strategia ukierunkowanej analizy funkcji genu GEN 1. wprowadzenie mutacji w genie 2.
Badanie funkcji genu Funkcję genu można zbadać różnymi sposobami Przypadkowa analizy funkcji genu MUTACJA FENOTYP GEN Strategia ukierunkowanej analizy funkcji genu GEN 1. wprowadzenie mutacji w genie 2.
