WYKAZ BADAŃ KLINICZNYCH PRODUKTÓW LECZNICZNYCH/WYROBÓW MEDYCZNYCH PROWADZONYCH W WOJSKOWYM INSTYTUCIE MEDYCZNYM
|
|
|
- Wacława Marek
- 7 lat temu
- Przeglądów:
Transkrypt
1 Wykaz dotyczy tylko badań klinicznych, których Sponsor badania wyraził zgodę na umieszczenie tytułu na stronie internetowej Wojskowego Instytutu Medycznego. KOMÓRKA ORGANIZACYJNA TYTUŁ BADANIA Klinka Okulistyki 1 Prospektywne, wieloośrodkowe badanie kliniczne mające na celu ocenę bezpieczeństwa I skuteczności implantów Cypass u pacjentów z jaskrą z otwartym kątem przesączania odporną na terapię miejscową jednym lub wieloma środkami 2 Ocena kliniczna implantu AqueSys 3 Badanie kliniczne implantu Hydrus III- Prospektywne, wieloośrodkowe, randomizowane porównanie implantu Hydrus z istentem przy obniżaniu ciśnienia śródgałkowego u pacjentów z jaskrą poddanych operacji zaćmy 4 Bezpieczeństwo i skuteczność implantu drenującego ciecz wodnistą Hydrus w obniżaniu ciśnienia śródgałkowego u pacjentów poddawanych operacji ekstrakcji zaćmy. Prospektywne, wieloośrodkowe, randomizowane badanie kliniczne z grupa kontrolną (Badanie Hydrus 4) 5 Prospektywne, wieloośrodkowe, randomizowane porównanie implantu Hydrus z wyrobem istent przy obniżaniu ciśnienia śródgałkowego w jaskrze pierwotnej z otwartym kątem przesączania (badanie Hydrus 5) 6 Ocena skuteczności i bezpieczeństwa leku T4020 w porównaniu do nieaktywnego nośnika leku u pacjentów z przewlekłym neurotroficznym zapaleniem rogówki lub owrzodzeniem rogówki. Badanie kliniczne fazy III, międzynarodowe, wieloośrodkowe, randomizowane, podwójnie ślepe, w 2 grupach równoległych w porównaniu do nieaktywnego nośnika leku u 124 pacjentów leczonych przez 28 dni 7 Wieloośrodkowe badania porejestracyjne implantu AueSys XEN stosowanego u pacjentów z umiarkowaną jaskrą pierwotną z otwartym kątem przesączania 8 LUMINOUS: badanie skuteczności i bezpieczeństwa produktu LUCENTIS w zindywidualizowanym postępowaniu z chorym oraz rezultatów powiązanych 9 Ocena wyników klinicznych dotyczących stosowania akomodujących soczewek wewnątrzgałkowych (AIOL) FluidVision TM przy użyciu ulepszonego iniektora PowerJect. Klinika Kardiologii 1 Prospektywne, wieloośrodkowe, międzynarodowe badanie rejestrowe i Chorób obejmujące kobiety i mężczyzn ze świeżo rozpoznanym migotaniem Wewnętrznych przedsionków 2 Zapobieganie nagłej śmierci przy pomocy urządzenia VEST (VEST) oraz badanie urządzenia VEST 3 WIELOOŚRODKOWE, RANDOMIZOWANE, PROWADZONE METODĄ PODWÓJNIE ŚLEPEJ PRÓBY W GRUPACH RÓWNOLEGŁYCH BADANIE FAZY III KONTROLOWANE PLACEBO, MAJĄCE NA CELU OCENĘ SKUTECZNOŚCI, BEZPIECZEŃSTWA ORAZ TOLERANCJI BOCOCIZUMABU (PF ) W ZMNIEJSZANIU CZĘSTOTLIWOŚCI WYSTĘPOWANIA CIĘŻKICH ZDARZEŃ SERCOWO-NACZYNIOWYCH U UCZESTNIKÓW Z GRUPY WYSOKIEGO RYZYKA 4 RANDOMIZOWANE, PROWADZONE METODĄ PODWÓJNIE ŚLEPEJ PRÓBY W GRUPACH RÓWNOLEGŁYCH BADANIE FAZY III KONTROLOWANE PLACEBO, MAJĄCE NA CELU OCENĘ SKUTECZNOŚCI, BEZPIECZEŃSTWA ORAZ TOLERANCJI BOCOCIZUMABU (PF ) W ZMNIEJSZANIU CZĘSTOTLIWOŚCI WYSTĘPOWANIA CIĘŻKICH ZDARZEŃ SERCOWO- NACZYNIOWYCH U UCZESTNIKÓW Z GRUPY WYSOKIEGO RYZYKA 5 REAL Registry 1
2 Klinika Onkologii 1 Randomizowane, prowadzone metodą podwójnie ślepej próby, kontrolowane placebo badanie fazy 3 z sunitynibem jako leczenie adjuwantowe w raku nerki u pacjentów z wysokim ryzkiem wznowy 2 Otwarte, randomizowane badanie kliniczne fazy IIIB porównujące bewacizumab (AVASTIN) w skojarzeniu z temsyrolimusem (TORISEL) z bewacizumabem (AVASTIN) w skojarzeniu z interferonem (ROFERON) w pierwszej linii leczenia chorych na zaawansowanego raka nerwowo komórkowego 3 Otwarte, randomizowane, wieloośrodkowe badania kliniczne III fazy oceniające skuteczność i bezpieczeństwo TKI258 w porównaniu z sorafenibem u pacjentów z rozsianym rakiem nerkowokomórkowym po niepowodzeniu terapii antyangiogennych (anty-vegf i inhibitor mtor) 4 A Phase 3, Multicenter, Randomized, double-blind, Placebo Conteolled of AMG 479 or Placebo in Combination with Gemcitabine as First line Therapy of Metastatic Adenocarcinoma of the Pancreas 5 Otwarte, randomizowane badanie III fazy BIBW 2992 i winorelbiny w porównaniu z trastuzumabem i winorelbiną u pacjentek z przerzutowym HER2-nadreaktywnym rakiem piersi, u których zawiodła poprzednia terapia trastuzumabem 6 Badanie otwarte, nierandomizowane, 2 fazy oceniające leczenie przeciwciałem monoklonalnym anty-cd19 związanym z mayatansyną (SAR314), podawanym dozylnie jako jedyny lek pacjentom z nawrotowym lub opornym na leczenie rozlanym chłoniakiem z duzych limfocytów B z ekspansją CD19 7 Badanie III fazy. randomizowane, aktywnie kontrolowane, z zaślepieniem danych dla personelu oceniającego, sprawdzające bezpieczeństwo i skuteczność Pegylowanego Apo-Filgrastim w porównaniu do licencjonowanych postaci US Neulasta oraz EU Neulasta u pacjentów z nowotworem piersi w stadium IIa, IIb lub IIIa otrzymujących przeciwnowotworową chemioterapię TAC w leczeniu adjuwantowym 8 A Phase 3 study to Evaluate the Efficacy and Safety of Induction and Maintenance Regimens of Brodalumab Compared With Placebo and Ustekinumab in Subjects With Moderate to Severe Plaque Psoriasis 9 A Randomized, open-label, Phase 3 Study of BMS vs. Everolimus in subjects with Advanced or Metastatic Clear -Cell Renal Cell Carcinoma Who Have Received Prior Anti-Angiogenic Therapy 10 Randomizowane, kontrolowane badanie fazy 3 z zastosowaniem kabozantynibu (XL184) versus ewerolimus u pacjentów z przerzutowym rakiem nerkowokomórkowym, u których stwierdzono progresję po wcześniejszej terapii inhibitorem receptora kinazy tyrozynowej naczyniowo śródbłonkowego czynnika wzrostu (VEGFR) 11 Wieloośrodkowe, podwójnie zaślepione, randomizowane badanie III fazy prowadzone w grupach równoległych oceniające skuteczność i bezpieczeństwo Hercules porównawczo do Herceptyny u pacjentek HER2+ z przerzutowym rakiem piersi 12 Randomizowane, wieloośrodkowe, podwójnie zaślepione badanie III fazy zwiąku PD (doustnego inhibitora kinazy cyklino-zależnej 4/6 plus Letrozol w porównaniu do placebo plus Letrozol stsowanych w leczeniu kobiet po menopauzie chorujących na raka piersi ER (+), HER2 (-), którym nie podawano wcześniej żadnego systemowego leczenia przeciw-nowotworowego z powodu zaawansowanej choroby nowotworowej 2
3 Klinika Endokrynologii i Terapii Izotopowej Klinika Ginekologii i Ginekologii Onkologicznej 13 Randomizowane, prowadzone metodą podwójnie ślepej próby w grupach równoległych, wieloośrodkowe badanie III fazy prowadzone w celu porównania skuteczności, bezpieczeństwa, farmakokinetyki i immunogenności preparatu SB3 (proponowany lek biopodobny do trastuzumabu) i produktu Herceptin u kobiet z nowo zdiagnozowanym HER2 dodatnim rakiem piersi we wczesnym lub lokalnie zaawansowanym stadium rozwoju, stosowanych w leczeniu neoadjuwantowym 14 Randomizowane, kontrolowane placebo, prowadzone na zasadzie podwójnie ślepej próby badanie fazy III b oceniające skuteczność i bezpieczeństwo kontynuowania terapii enzalutamidem u pacjentów z przerzutowym rakiem gruczołu krokowego, opornym na terapię kastracyjną, niepoddawanych wcześniej chemioterapii, leczonych docetakselem i prednizolonem, u których doszło do progresji choroby podczas monoterapii enzalutamidem 15 Badanie MILO (Inhibitor MEK w surowiczym raku jajnika o niskim stopniu złośliwości histologicznej): Międzynarodowe, randomizowane badanie III fazy prowadzone zgodnie z otwartą próbą dotyczące stosowania MEK162 w porównaniu z chemioterapią wybraną przez lekarza u pacjentek z nawracającym lub przewlekłym surowiczym rakiem jajnika, jajowodu lub pierwotnym rakiem otrzewnej o niskim stopniu złośliwości histologicznej 1 Randomizowane, prowadzone metodą podwójnie ślepej próby badanie kliniczne fazy III oceniające skuteczność i bezpieczeństwo stosowania preparatu sorafenib w porównaniu do placebo u pacjentów z rozpoznaniem miejscowo zaawansowanego / z przerzutami, opornego na leczenie jodem radioaktywnym, zróżnicowanego raka tarczycy 2 Wielośrodkowe, randomizowane badanie III fazy prowadzone metodą podwójnie ślepej próby, mające na celu ocenę skuteczności i bezpieczeństwa pasyreotydu LAR u pacjentów z chorobą Cushinga 3 Badanie kliniczne wieloośrodkowe, międzynarodowe, randomizowane, prowadzone w grupach równoległych, kontrolowane placebo (podwójnie zaślepione) i z substancją czynną (otwarte) porównujące skuteczność i bezpieczeństwo leczenia podawanego raz w tygodniu lekiem NNC lub placebo z Norditropin FlexPro stosowanym codziennie u osób dorosłych z niedoborem hormonu wzrostu przez okres 35 tygodni z 53-tygodniowym okresem obserwacji. 4 Wieloośrodkowe, randomizowane, otwarte badanie fazy IV, oceniające leczenie hiperglikemii indukowanej pasyreotydem za pomocą terapii opartej na inkretynach lub insulinie, u dorosłych pacjentów z chorobą Cushinga lub akromegalią 5 An open label, multi-center pasireotide roll-over protocol for patients who have completed a previous Novartis-sponsored pasireotide study and are judged by the investigator to benefit from continued pasireotide treatment 1 Badanie kliniczne fazy IIb prowadzone w 2 ch etapach, z randomizacją, kontrolowane przy użyciu placebo i aktywnego komparatora (Tolterodyna), mające na celu ocenę skuteczności i bezpieczeństwa stosowania leku MK-4618 u pacjentów cierpiących z powodu nadreaktywności pęcherza moczowego 2 Randomizowane, podwójnie zaślepione, kontrolowane placebo badanie mające na celu ocenę bezpieczeństwa i skuteczności elagoliksu u pacjentek z umiarkowanym lub ciężkim bólem związanym z endometriozą 3 Phase 3, double-blind, extension studyevaluating the safety and efficacyof longterm treatment with elagolix in the management of moderate to severe endometriosis-associated pain in adult premenopausal female subjects who participated in Study M
4 Klinika Chorób Wewnętrznych i Reumatologii Klinika Neurologiczna 4 Randomizowane, wieloośrodkowe badanie kliniczne prowadzone metodą podwójnie ślepej próby w grupach równoległych z grupą kontrolną otrzymującą substancję czynną oraz grupą kontrolną otrzymującą placebo, mające na celu ocenę skuteczności, bezpieczeństwa i tolerancji leczenia skojarzonego bursztynianem solifenacyny i mirabegronem w porównaniu do monoterapii bursztynianem solifenacyny i mirabegronem w leczeniu zespołu pęcherza nadreaktywnego 5 Badanie prowadzone w grupach równoległych metodą podwójnie ślepej próby z randomizacją, z użyciem placebo i aktywnych leków w grupach kontrolnych, celem oceny skuteczności przeciwbólowej i bezpieczeństwa stosowania doustnego preparatu łączącego trometamol deksketoprofenu oraz chlorowodorek tramadolu w opanowaniu ostrego bólu o nasileniu umiarkowanym do ciężkiego występującego po histerektomii z dostępu brzusznego 1 Randomizowane, wieloośrodkowe badanie fazy III, prowadzone metodą podwójnie ślepej próby w grupach równoległych, kontrolowane przy użyciu placebo, oceniające bezpieczeństwo i skuteczność dwóch dawek apremilastu (CC-10004) u chorych z aktywną postacią łuszczycowego zapalenia stawów 2 A Phase III randomized, double-blind, placebo-controlled multicenter study of subcutaneous secukinumab in prefilled syringes to demonstrate the efficacy at 24 weeks and to asses the long term efficacy, safety and tolerability up to 5 years in pateints with Active Psoriatic Arthritis 3 A mulicenter, Ramdomized, Double-blind, Placebo controled, paralel Group Study of CNTO 136 (sirukumab), a human anti-il-6 Moinoclonal Antibody, Administered Subcutaneously in Subject with Active Rheumatoid Arthrists Despite DMARD 4 Wieloośrodkowe badanie kliniczne prowadzone w grupach równoległych, oceniające długoterminowe bezpieczeństwo i skuteczność zastosowania preparatu CNTO136 (sirukumab) w leczeniu reumatoidalnego zapalenia stawów u chorych, którzy zakończyli udział w badaniach CNTO136ARA3002 (SIRROUND- D) i CNTO136ARA3003 (SIRROUND-T). 5 6 Wieloośrodkowe, randomizowane badanie, prowadzone metodą podwójnie ślepej próby w grupach równoległych, dotyczące preparatu CNTO 136 (sirukumab) podawanego podskórnie w monoterapii w porównaniu z adalimumabem w monoterapii u pacjentów z aktywnym reumatoidalnym zapaleniem stawów 7 Podwójnie zaślepione, randomizowane, kontrolowane placebo badania oceniające bezpieczeństwo, farmakokinetykę, farmakodynamikę i skuteczność stosowania wielokrotnych dawek UCB4940 jako terapii dodatkowej do terapii certolizumabem pegol u pacjentów z umiarkowanym do ciężkiego reumatoidalnym zapaleniem stawów 1 Międzynarodowe, wieloośrodkowe, randomizowane, podwójnie ślepe, kontrolowane placebo, prowadzone w grupach równoległych badanie oceniające skuteczność i bezpieczeństwo dwuletniej terapii teriflunomidem w dawce 7 mg raz dziennie i 14 mg raz dziennie w porównaniu z placebo, u pacjentów z pierwszymi klinicznymi objawami sugerującymi stwardnienie rozsiane 2 Międzynarodowe, wieloośrodkowe, prowadzone w grupach równoległych, podwójne zaślepione, kontrolowane placebo, badanie oceniające skuteczność i bezpieczeństwo teriflunomidu stosowanego raz dziennie doustnie w dawkach 7 mg i 14 mg w porównaniu do placebo, u pacjentów z rzutową postacią stwardnienia rozsianego leczonych interferonem beta-1a (Rebif) jako kalibratorem, stosowanym w próbie otwartej 4
5 Klinika Chorób Infekcyjnych i Alergologii Zakład Immunologii i Alergologii Klinicznej Pracownia Badań Naczyniowych i Radiologii Interwencyjnej 3 Przedłużenie 24-miesiecznego, wieloośrodkowego, randomizowanego badania prowadzonego metodą podwójnie ślepej próby z grupą kontrolną placebo i grupami równoległymi, oceniającego skuteczność i bezpieczeństwo preparatu FTY720 w dawce 1,25 mg i 0,5 mg, podawanego doustnie raz dziennie u pacjentów ze stwardnieniem rozsianym przebiegającym z okresami zaostrzeń 4 Wieloośrodkowe, zaślepione pod względem częstotliwości dawkowania przedłużenie badania klinicznego, mające na celu długoterminową ocenę bezpieczeństwa i skuteczności PEGylowanego interferonu beta-1a (BIIB017) u pacjentów ze stwardnieniem rozsianym w postaci rzutowo-remisyjnej 5 Wieloośrodkowe, otwarte badanie kliniczne z jednym ramieniem terapeutycznym, oceniające długoterminowe bezpieczeństwo i tolerancję preparatu fingolimod (FTY720) w dawce 0,5 mg, podawanego raz dziennie doustnie, u pacjentów z nawracającą postacią stwardnienia rozsianego 6 Wieloośrodkowe, randomizowane, podwójnie zaślepione, prowadzone w grupach równoległych, kontrolowane za p0omocą placebo badanie mająca na celu ocenę skuteczności i bezpieczeństwa PEGylated interferon Beta 1a u pacjentów ze stwardnieniem rozsianym 7 Wieloośrodkowe, randomizowane badanie, prowadzone metodą podwójnie ślepej próby, kontrolowane placebo, oceniające skuteczność natalizumabu w redukowaniu progresji niepełnosprawności u pacjentów z wtórnie postępującym stwardnieniem rozsianym 8 Wieloośrodkowe, randomizowane badanie fazy 2, prowadzone w grupach równoległych, metodą podwójnie ślepej próby, z grupą kontrolną otrzymującą placebo oceniające skuteczność i bezpieczeństwo stosowania produktu RPC1063 podawanego doustnie u pacjentów chorych na rzutowe postacie stwardnienia rozsianego 9 Randomizowane, podwójnie zaślepione badanie dotyczące zakresu dawek, prowadzone w grupach równoległych, z grupą kontrolną otrzymująco placebo, celem oceny skuteczności, bezpieczeństwa, tolerancji i farmakokinetyki BIIB033 u pacjentów chorych na nawracające postacie stwardnienia rozsianego leczonych jednocześnie Avonexem 10 Wieloośrodkowe, randomizowane badanie, prowadzone metoda podwójnie ślepej próby, kontrolowane placebo, oceniające skuteczność natalizumabu w redukowaniu progresji niepełnosprawności u pacjentów z wtórnie postępującym stwardnieniem rozsianym Randomizowane, podwójnie zaślepione badanie, porównujące skuteczność i bezpieczeństwo doustnego inhibitora trombiny w postaci eteksylanu dabigatranu (110 mg lub 150 mg, doustnie dwa razy na dobę), w porównaniu do kwasu acetylosalicylowego (100 mg doustnie raz na dobę) w prewencji wtórnej udaru u pacjentów z udarem zatorowo pochodnym o nieustalonym źródle (RESPECT ESUS) 1 A multicentre randomised placebo-controlled double-blind pivotal clinical trial for the evaluation of safety and efficacy of specific immunotherapy with an aluminium hydroxide-adsorbed recombinat hypoallergenic derivative of the major birch pollen allerge, rbet v1-fv 1 A multicentre randomised placebo-controlled double-blind pivotal clinical trial for the evaluation of safety and efficacy of specific immunotherapy with an aluminium hydroxide-adsorbed recombinat hypoallergenic derivative of the major birch pollen allergen, rbet v1-fv 1 Sorafenib w skojarzeniu z lokalną mikroterapią pod kontrolą MRI z kontrastem Gd-EOB-DTPA u pacjentów z nieoperacyjnym rakiem wątroby 5
6 Klinika Dermatologiczna 1 Badanie wykonalności oceniające bezpieczeństwo i wstępną skuteczność Systemu Leczenia Trądziku Sebacia stosowanego w leczeniu trądziku pospolitego 2 Wieloośrodkowe, randomizowane, podwójnie zaślepione, kontrolowane placebo, prowadzone w grupach równoległych badanie 3 fazy mające na celu ocenę skuteczności i bezpieczeństwa 2 doustnych dawek preparatu CP-690,550 u pacjentów z umiarkowaną lub ciężką przewlekłą łuszczycą plackowatą 3 Wieloośrodkowe. otwarte badanie 3 fazy oceniające bezpieczeństwo i tolerancję długoterminowego przyjmowania 2 dawek doustnych preparatu CP-690,550 u pacjentów z umiarkowaną lub ciężką przewlekłą łuszczycą plackowatą 4 Wieloośrodkowe, randomizowane, prowadzone metodą podwójnie ślepej próby w grupach równoległych, z zastosowaniem jedynie podłoża w grupie kontrolnej badanie fazy 2 b dotyczące skuteczności bezpieczeństwa, miejscowej tolerancji oraz farmakokinetyki dwóch mocy dawek i dwóch schematów dawkowania tofacitinibu w postaci maści u osób z przewlekłą postacią łuszczycy plackowatej 5 Wieloośrodkowe, randomizowane, prowadzone metodą podwójnie ślepej próby w grupach równoległych, z zastosowaniem jedynie podłoża w grupie kontrolnej badanie fazy 2b dotyczące skuteczności, bezpieczeństwa, miejscowej tolerancji oraz farmakokinetyki dwóch mocy dawek i dwóch schematów dawkowania tofacitinibu w postaci maści u osób z przewlekłą postacią łuszczycy plackowatej 6 Podwójnie zaślepione, kontrolowane placebo, randomizowane, trzyramienne w grupach równoległych badanie III fazy oceniające skuteczność i bezpieczeństwo podawanej przez 4 miesiące diosminy w leczeniu pajączków kończyn dolnych oraz lipodystrofii typu kobiecego (obrzękowo-włókniejącego zwyrodnienia tkanki podskórnej, powszechnie znane jako cellulit) 7 Badanie fazy 3 trwające 52 tygodnie, prowadzone w grupach równoległych, z zastosowaniem randomizacji, z użyciem aktywnego leku i placebo w grupach kontrolnych, celem oceny skuteczności i bezpieczeństwa stosowania / tolerancji podawanego podskórnie preparatu SCH / MK-3222 u chorych na przewlekłą łuszczycę plackowatą o nasileniu umiarkowanym do ciężkiego, z uzupełniającą nieobowiązkową kontynuacją celem długoterminowej oceny bezpieczeństwa 8 A Phase 2 Multi-center, Randomized, Double-blind, Vehiclecontrolled, Four-arm, Parallel Group Study to Assess the Safety, Tolerability, and Efficacy of Topical OPA Ointment, in Subjects With Mild/Moderate Atopic Dermatitis 6
WYKAZ BADAŃ KLINICZNYCH PRODUKTÓW LECZNICZNYCH/WYROBÓW MEDYCZNYCH PROWADZONYCH W WOJSKOWYM INSTYTUCIE MEDYCZNYM
 Wykaz dotyczy tylko badań klinicznych, których Sponsor badania wyraził zgodę na umieszczenie tytułu na stronie internetowej Wojskowego Instytutu Medycznego. KOMÓRKA ORGANIZACYJNA TYTUŁ BADANIA Klinka Okulistyki
Wykaz dotyczy tylko badań klinicznych, których Sponsor badania wyraził zgodę na umieszczenie tytułu na stronie internetowej Wojskowego Instytutu Medycznego. KOMÓRKA ORGANIZACYJNA TYTUŁ BADANIA Klinka Okulistyki
WYKAZ BADAŃ KLINICZNYCH PRODUKTÓW LECZNICZNYCH/WYROBÓW MEDYCZNYCH PROWADZONYCH W WOJSKOWYM INSTYTUCIE MEDYCZNYM
 Wykaz dotyczy tylko badań klinicznych, których Sponsor badania wyraził zgodę na umieszczenie tytułu na stronie internetowej Wojskowego Instytutu Medycznego. KOMÓRKA ORGANIZACYJNA TYTUŁ BADANIA Klinka Okulistyki
Wykaz dotyczy tylko badań klinicznych, których Sponsor badania wyraził zgodę na umieszczenie tytułu na stronie internetowej Wojskowego Instytutu Medycznego. KOMÓRKA ORGANIZACYJNA TYTUŁ BADANIA Klinka Okulistyki
Nowotwór złośliwy piersi
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy piersi Lapatinib Refundacja z ograniczeniami Lapatinib jest wskazany do leczenia dorosłych pacjentów z rakiem piersi, u których nowotwór
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy piersi Lapatinib Refundacja z ograniczeniami Lapatinib jest wskazany do leczenia dorosłych pacjentów z rakiem piersi, u których nowotwór
Lek BI w porównaniu z lekiem Humira u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą
 Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Badania laboratoryjne (i inne) są wykonywane w jednych z najlepszych na świecie laboratoriów.
 {jcomments off} BADANIA KLINICZNE 1. W badaniach klinicznych testuje się nowe leki. 2. Badania kliniczne są często jedyną okazją do podjęcia leczenia w przypadku nieskuteczności lub niskiej sktutecznosći
{jcomments off} BADANIA KLINICZNE 1. W badaniach klinicznych testuje się nowe leki. 2. Badania kliniczne są często jedyną okazją do podjęcia leczenia w przypadku nieskuteczności lub niskiej sktutecznosći
Leczenie systemowe raka nie-jasnokomórkowego
 Leczenie systemowe raka nie-jasnokomórkowego Piotr Tomczak Uniwersytet Medyczny w Poznaniu Klinika Onkologii Jastrzębia Góra Nie-jasnokomórkowy rak nerki (ncc RCC) niejednorodna grupa o zróżnicowanej histologii
Leczenie systemowe raka nie-jasnokomórkowego Piotr Tomczak Uniwersytet Medyczny w Poznaniu Klinika Onkologii Jastrzębia Góra Nie-jasnokomórkowy rak nerki (ncc RCC) niejednorodna grupa o zróżnicowanej histologii
Data zakończenia badania klinicznego
 Lp. Numer protokołu badania Nazwa sponsora/cro Skład zespołu badawczego Data rozpoczęcia badania klinicznego w ośrodku Data zakończenia badania klinicznego 1 2 3 6 6 12 1. NR001-03 Faza III rejestracyjna
Lp. Numer protokołu badania Nazwa sponsora/cro Skład zespołu badawczego Data rozpoczęcia badania klinicznego w ośrodku Data zakończenia badania klinicznego 1 2 3 6 6 12 1. NR001-03 Faza III rejestracyjna
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Data zakończenia badania klinicznego
 Lp. Numer protokołu badania Nazwa sponsora/cro Skład zespołu badawczego Data rozpoczęcia badania klinicznego w ośrodku Data zakończenia badania klinicznego 1 2 3 6 6 12 1. EMRII200037-014 Otwarte, randomizowane,
Lp. Numer protokołu badania Nazwa sponsora/cro Skład zespołu badawczego Data rozpoczęcia badania klinicznego w ośrodku Data zakończenia badania klinicznego 1 2 3 6 6 12 1. EMRII200037-014 Otwarte, randomizowane,
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Katalog ryczałtów za diagnostykę w programach lekowych
 Katalog ryczałtów za diagnostykę w programach lekowych Lp. Kod Nazwa świadczenia Ryczałt roczny (punkty) Uwagi 1 2 3 4 5 1 5.08.08.0000001 Diagnostyka w programie leczenia przewlekłego WZW typu B lamiwudyną
Katalog ryczałtów za diagnostykę w programach lekowych Lp. Kod Nazwa świadczenia Ryczałt roczny (punkty) Uwagi 1 2 3 4 5 1 5.08.08.0000001 Diagnostyka w programie leczenia przewlekłego WZW typu B lamiwudyną
Katalog ryczałtów za diagnostykę w programach lekowych
 Katalog ryczałtów za diagnostykę w programach lekowych Lp. Kod Nazwa świadczenia Ryczałt roczny (punkty) Uwagi 1 2 3 4 5 1 5.08.08.0000001 Diagnostyka w programie leczenia przewlekłego WZW typu B lamiwudyną
Katalog ryczałtów za diagnostykę w programach lekowych Lp. Kod Nazwa świadczenia Ryczałt roczny (punkty) Uwagi 1 2 3 4 5 1 5.08.08.0000001 Diagnostyka w programie leczenia przewlekłego WZW typu B lamiwudyną
Rak piersi. Doniesienia roku Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie
 Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzid Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzid Skład zespołu badawczego rozpoczęcia
dr n. med. Paweł Nurzyński, prof. dr hab. n. med. Andrzej Deptała Klinika Onkologii i Hematologii, Centralny Szpital Kliniczny MSW w Warszawie
 Ewerolimus w codziennej praktyce klinicznej. Omówienie niemieckiego nieinterwencyjnego badania ewerolimusu w terapii przerzutowego raka nerki po niepowodzeniu leczenia inhibitorami kinaz tyrozynowych Everolimus
Ewerolimus w codziennej praktyce klinicznej. Omówienie niemieckiego nieinterwencyjnego badania ewerolimusu w terapii przerzutowego raka nerki po niepowodzeniu leczenia inhibitorami kinaz tyrozynowych Everolimus
Personalizacja leczenia rozsianego raka nerki.
 RAFAŁ STEC Personalizacja leczenia rozsianego raka nerki. Warszawa, 13 października 2018 roku Opis przypadku nr 1. Rozpoznanie Data rozpoznania: 07.11.2007 r. Pacjent: 65 lat, K Dane na temat guza: - Stopień
RAFAŁ STEC Personalizacja leczenia rozsianego raka nerki. Warszawa, 13 października 2018 roku Opis przypadku nr 1. Rozpoznanie Data rozpoznania: 07.11.2007 r. Pacjent: 65 lat, K Dane na temat guza: - Stopień
Aktualne na dzień:
 Aktualne na dzień: 20-12-2018 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Wieloośrodkowe otwarte badanie
Aktualne na dzień: 20-12-2018 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Wieloośrodkowe otwarte badanie
Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od 01.07.2012 r. Cena Oczekiwana 03.0000.301.
 Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od 01.07.2012 r. Kod Zakresu Nazwa Zakresu Cena Oczekiwana 03.0000.301.02 PROGRAM LECZENIA PRZEWLEKŁEGO WZW TYPU
Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od 01.07.2012 r. Kod Zakresu Nazwa Zakresu Cena Oczekiwana 03.0000.301.02 PROGRAM LECZENIA PRZEWLEKŁEGO WZW TYPU
L.p. Nazwa badania Numer protokołu. Główny Badacz. prowadząca badanie. Badania z aktywną rekrutacją
 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Randomizowane kontrolowane placebo z zastosowaniem podwójnie
L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Randomizowane kontrolowane placebo z zastosowaniem podwójnie
Katarzyna Pogoda Warszawa, 23 marca 2017 roku
 Chemioterapia doustna i podskórne metody podawania leków w raku piersi. Lepsza jakość życia pacjentek Katarzyna Pogoda Warszawa, 23 marca 2017 roku Rak piersi - heterogenna choroba Stopień zaawansowania
Chemioterapia doustna i podskórne metody podawania leków w raku piersi. Lepsza jakość życia pacjentek Katarzyna Pogoda Warszawa, 23 marca 2017 roku Rak piersi - heterogenna choroba Stopień zaawansowania
 W badaniu 4S (ang. Scandinavian Simvastatin Survivat Study), oceniano wpływ symwastatyny na całkowitą śmiertelność u 4444 pacjentów z chorobą wieńcową i z wyjściowym stężeniem cholesterolu całkowitego
W badaniu 4S (ang. Scandinavian Simvastatin Survivat Study), oceniano wpływ symwastatyny na całkowitą śmiertelność u 4444 pacjentów z chorobą wieńcową i z wyjściowym stężeniem cholesterolu całkowitego
Nowotwór złośliwy oskrzela i płuca
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy oskrzela i płuca Bevacizumab Bewacyzumab w skojarzeniu z chemioterapią opartą na pochodnych platyny jest wskazany w leczeniu pierwszego
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy oskrzela i płuca Bevacizumab Bewacyzumab w skojarzeniu z chemioterapią opartą na pochodnych platyny jest wskazany w leczeniu pierwszego
Wykaz aktualnie prowadzonych badań klinicznych i nieinterwencyjnych w Białostockim Centrum Onkologii im. Marii Skłodowskiej-Curie w Białymstoku
 Aktualne na dzień 10-05-2019 Wykaz aktualnie prowadzonych badań klinicznych i nieinterwencyjnych w Białostockim Centrum Onkologii im. Marii Skłodowskiej-Curie w Białymstoku L.p. Nazwa badania Numer Protokołu
Aktualne na dzień 10-05-2019 Wykaz aktualnie prowadzonych badań klinicznych i nieinterwencyjnych w Białostockim Centrum Onkologii im. Marii Skłodowskiej-Curie w Białymstoku L.p. Nazwa badania Numer Protokołu
Wykaz aktualnie prowadzonych badań klinicznych i nieinterwencyjnych w Białostockim Centrum Onkologii im. Marii Skłodowskiej-Curie w Białymstoku
 Aktualne na dzień 17-05-2019 Wykaz aktualnie prowadzonych badań klinicznych i nieinterwencyjnych w Białostockim Centrum Onkologii im. Marii Skłodowskiej-Curie w Białymstoku L.p. Nazwa badania Numer Protokołu
Aktualne na dzień 17-05-2019 Wykaz aktualnie prowadzonych badań klinicznych i nieinterwencyjnych w Białostockim Centrum Onkologii im. Marii Skłodowskiej-Curie w Białymstoku L.p. Nazwa badania Numer Protokołu
Wydłużenie życia chorych z rakiem płuca - nowe możliwości
 Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Białaczka limfatyczna
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od r. Cena Oczekiwana
 Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od 01.07.2012 r. Kod Zakresu Nazwa Zakresu Cena Oczekiwana 03.0000.301.02 PROGRAM LECZENIA PRZEWLEKŁEGO WZW TYPU
Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od 01.07.2012 r. Kod Zakresu Nazwa Zakresu Cena Oczekiwana 03.0000.301.02 PROGRAM LECZENIA PRZEWLEKŁEGO WZW TYPU
Badania z aktywną rekrutacją PCR CL-0201 KCP
 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Randomizowane kontrolowane placebo z zastosowaniem podwójnie
L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Randomizowane kontrolowane placebo z zastosowaniem podwójnie
Dlaczego potrzebne było badanie?
 Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z łagodną postacią choroby Alzheimera oraz trudności z funkcjonowaniem psychicznym Jest to podsumowanie badania klinicznego
Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z łagodną postacią choroby Alzheimera oraz trudności z funkcjonowaniem psychicznym Jest to podsumowanie badania klinicznego
Dlaczego potrzebne było badanie?
 Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z chorobą Alzheimera we wczesnym stadium Jest to podsumowanie badania klinicznego przeprowadzonego z udziałem pacjentów
Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z chorobą Alzheimera we wczesnym stadium Jest to podsumowanie badania klinicznego przeprowadzonego z udziałem pacjentów
LECZENIE RAKA NERKI (ICD-10 C 64)
 Załącznik B.10. LECZENIE RAKA NERKI (ICD-10 C 64) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1 2 3 1. Leczenie
Załącznik B.10. LECZENIE RAKA NERKI (ICD-10 C 64) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1 2 3 1. Leczenie
Spis treści. Przedmowa Barbara Czerska... 11 Autorzy... 17 Wykaz skrótów... 19
 Przedmowa Barbara Czerska.................................. 11 Autorzy.................................................... 17 Wykaz skrótów.............................................. 19 Rozdział I.
Przedmowa Barbara Czerska.................................. 11 Autorzy.................................................... 17 Wykaz skrótów.............................................. 19 Rozdział I.
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
Keytruda (pembrolizumab)
 EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
Wykaz programów zdrowotnych (lekowych)
 Wykaz programów zdrowotnych (lekowych) Część A Programy lekowe Lp. KOD NUMER ZAŁĄCZNIKA z Obw. MZ ROZPOZNANIE KLINICZNE ICD-10 NAZWA PROGRAMU SUBSTANCJE CZYNNE 1 2 3 4 5 6 1 03.0000.301.02 B.1. B 18.1
Wykaz programów zdrowotnych (lekowych) Część A Programy lekowe Lp. KOD NUMER ZAŁĄCZNIKA z Obw. MZ ROZPOZNANIE KLINICZNE ICD-10 NAZWA PROGRAMU SUBSTANCJE CZYNNE 1 2 3 4 5 6 1 03.0000.301.02 B.1. B 18.1
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
Główny Badacz. L.p. Nazwa badania Numer protokołu. prowadząca badanie. Badania z aktywną rekrutacją
 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 "Randomizowane, prowadzone metodą podwójnie ślepej próby
L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 "Randomizowane, prowadzone metodą podwójnie ślepej próby
INNOWACJE W LECZENIU RAKA NERKI- OCENA DOSTĘPNOŚCI W POLSCE. Prof. Cezary Szczylik Lek. Przemysław Langiewicz CSK WIM
 INNOWACJE W LECZENIU RAKA NERKI- OCENA DOSTĘPNOŚCI W POLSCE Prof. Cezary Szczylik Lek. Przemysław Langiewicz CSK WIM I/II linia leczenia rozsianego raka nerki Pazopanib - Produkt Votrient jest wskazany
INNOWACJE W LECZENIU RAKA NERKI- OCENA DOSTĘPNOŚCI W POLSCE Prof. Cezary Szczylik Lek. Przemysław Langiewicz CSK WIM I/II linia leczenia rozsianego raka nerki Pazopanib - Produkt Votrient jest wskazany
Aktualnie prowadzone badania kliniczne w Oddziałach Klinicznych Szpitala Uniwersyteckiego w Krakowie - stan na dzień 01.10.
 KLINIKA/ Numer kontaktowy TYTUŁ BADAŃ REKRUTACJA Wieloośrodkowe, międzynarodowe, randomizowane, prowadzone metodą podwójnie ślepej próby Oddział Kliniczny Alergii i Immunologii tel.12 430-53-14 Aktualnie
KLINIKA/ Numer kontaktowy TYTUŁ BADAŃ REKRUTACJA Wieloośrodkowe, międzynarodowe, randomizowane, prowadzone metodą podwójnie ślepej próby Oddział Kliniczny Alergii i Immunologii tel.12 430-53-14 Aktualnie
Rak jajnika. Prof. Mariusz Bidziński. Klinika Ginekologii Onkologicznej
 Rak jajnika Prof. Mariusz Bidziński Klinika Ginekologii Onkologicznej Współpraca z firmami: Roche, Astra Zeneca, MSD, Olympus Mutacje w genach BRCA1 i BRCA2 Materiały edukacyjne Astra Zeneca Mutacje w
Rak jajnika Prof. Mariusz Bidziński Klinika Ginekologii Onkologicznej Współpraca z firmami: Roche, Astra Zeneca, MSD, Olympus Mutacje w genach BRCA1 i BRCA2 Materiały edukacyjne Astra Zeneca Mutacje w
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Aktualne na dzień:
 Aktualne na dzień: 22-11-2018 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Badanie kliniczne oceniające
Aktualne na dzień: 22-11-2018 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Badanie kliniczne oceniające
Typ histopatologiczny
 Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Lek Avastin stosuje się u osób dorosłych w leczeniu następujących rodzajów nowotworów w skojarzeniu z innymi lekami przeciwnowotworowymi:
 EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Aneks II. Niniejsza Charakterystyka Produktu Leczniczego oraz ulotka dla pacjenta stanowią wynik procedury arbitrażowej.
 Aneks II Zmiany dotyczące odpowiednich punktów Charakterystyki Produktu Leczniczego oraz ulotki dla pacjenta przedstawione przez Europejską Agencję Leków (EMA) Niniejsza Charakterystyka Produktu Leczniczego
Aneks II Zmiany dotyczące odpowiednich punktów Charakterystyki Produktu Leczniczego oraz ulotki dla pacjenta przedstawione przez Europejską Agencję Leków (EMA) Niniejsza Charakterystyka Produktu Leczniczego
Leczenie łuszczycowego zapalenia stawów biologicznymi lekami modyfikującymi
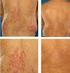 PRACA POGLĄDOWA Forum Reumatol. 2015, tom 1, nr 1, 25 29 Copyright 2015 Via Medica ISSN 2450 3088 Marcin Milchert, Marek Brzosko www.fr.viamedica.pl Klinika Reumatologii i Chorób Wewnętrznych, Pomorski
PRACA POGLĄDOWA Forum Reumatol. 2015, tom 1, nr 1, 25 29 Copyright 2015 Via Medica ISSN 2450 3088 Marcin Milchert, Marek Brzosko www.fr.viamedica.pl Klinika Reumatologii i Chorób Wewnętrznych, Pomorski
Aktualnie prowadzone badania kliniczne w Oddziałach Klinicznych Szpitala Uniwersyteckiego w Krakowie - stan na dzień 01.01.
 Aktualnie prowadzone badania kliniczne w Oddziałach Klinicznych Szpitala Uniwersyteckiego w Krakowie - stan na dzień 01.01.2016 roku KLINIKA/ Numer kontaktowy TYTUŁ BADAŃ REKRUTACJA Oddział Kliniczny Alergii
Aktualnie prowadzone badania kliniczne w Oddziałach Klinicznych Szpitala Uniwersyteckiego w Krakowie - stan na dzień 01.01.2016 roku KLINIKA/ Numer kontaktowy TYTUŁ BADAŃ REKRUTACJA Oddział Kliniczny Alergii
NOWE ZWIĄZKI PRZECIWNOWOTWOROWE Z GRUPY INHIBITORÓW KINAZY TYROZYNOWEJ EGFR STOSOWANE W TERAPII CELOWANEJ. Joanna Rozegnał
 NOWE ZWIĄZKI PRZECIWNOWOTWOROWE Z GRUPY INHIBITORÓW KINAZY TYROZYNOWEJ EGFR STOSOWANE W TERAPII CELOWANEJ Joanna Rozegnał TERAPIA CELOWANA: Jedna z najbardziej nowoczesnych metod leczenia nowotworów Skierowana
NOWE ZWIĄZKI PRZECIWNOWOTWOROWE Z GRUPY INHIBITORÓW KINAZY TYROZYNOWEJ EGFR STOSOWANE W TERAPII CELOWANEJ Joanna Rozegnał TERAPIA CELOWANA: Jedna z najbardziej nowoczesnych metod leczenia nowotworów Skierowana
Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od r. Cena Oczekiwana
 Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od 01.07.2012 r. Kod Zakresu Nazwa Zakresu Cena Oczekiwana 03.0000.301.02 PROGRAM LECZENIA PRZEWLEKŁEGO WZW TYPU
Ceny oczekiwane w rodzaju: leczenie szpitalne - programy zdrowotne (lekowe) obowiązujące od 01.07.2012 r. Kod Zakresu Nazwa Zakresu Cena Oczekiwana 03.0000.301.02 PROGRAM LECZENIA PRZEWLEKŁEGO WZW TYPU
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 139/2014 z dnia 2 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Giotrif,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 139/2014 z dnia 2 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Giotrif,
LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48)
 Dziennik Urzędowy Ministra Zdrowia 492 Poz. 66 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Dziennik Urzędowy Ministra Zdrowia 492 Poz. 66 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r.
 Dziennik Ustaw Nr 269 15687 Poz. 1597 1597 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na
Dziennik Ustaw Nr 269 15687 Poz. 1597 1597 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
Aktualne na dzień:
 Aktualne na dzień: 06-03-2019 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Wieloośrodkowe otwarte badanie
Aktualne na dzień: 06-03-2019 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Wieloośrodkowe otwarte badanie
Długoterminowa skuteczność golimumabu u pacjentów z zapalnymi spondyloartropatiami wtorek, 03 lutego :06
 Skuteczność leczenia zapalnych chorób reumatycznych poprawiła się istotnie w ostatnich latach. Złożyło się na to wiele czynników, do których można zaliczyć wczesną diagnostykę i szybkie rozpoczynanie odpowiedniej
Skuteczność leczenia zapalnych chorób reumatycznych poprawiła się istotnie w ostatnich latach. Złożyło się na to wiele czynników, do których można zaliczyć wczesną diagnostykę i szybkie rozpoczynanie odpowiedniej
Wyniki zasadniczego badania fazy III u pacjentów z rakiem jelita grubego z przerzutami:
 Informacja prasowa Bayer HealthCare Public Relations Al.Jerozolimskie 158 02-326 Warszawa Polska Wyniki zasadniczego badania fazy III u pacjentów z rakiem jelita grubego z przerzutami: Pozytywne dane z
Informacja prasowa Bayer HealthCare Public Relations Al.Jerozolimskie 158 02-326 Warszawa Polska Wyniki zasadniczego badania fazy III u pacjentów z rakiem jelita grubego z przerzutami: Pozytywne dane z
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego. Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa
 Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ
 FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ Prof. dr hab. med. Halina Bartosik - Psujek Katedra i Klinika Neurologii Uniwersytet Medyczny w Lublinie LEKI I RZUTU PREPARATY INTERFERONU
FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ Prof. dr hab. med. Halina Bartosik - Psujek Katedra i Klinika Neurologii Uniwersytet Medyczny w Lublinie LEKI I RZUTU PREPARATY INTERFERONU
Leczenie szpitalne ceny oczekiwane 2011
 Leczenie szpitalne ceny oczekiwane 2011 Zakres-kod Zakres-nazwa Cena 03.0000.103.02 teleradioterapia 03.0000.104.02 brachyterapia 03.0000.105.02 terapia izotopowa 03.3300.008.03 świadczenia w szpitalnym
Leczenie szpitalne ceny oczekiwane 2011 Zakres-kod Zakres-nazwa Cena 03.0000.103.02 teleradioterapia 03.0000.104.02 brachyterapia 03.0000.105.02 terapia izotopowa 03.3300.008.03 świadczenia w szpitalnym
Wykaz programów zdrowotnych (lekowych)
 Wykaz programów zdrowotnych (lekowych) Część A Programy lekowe Lp. KOD NUMER ZAŁĄCZNIKA ROZPOZNANIE KLINICZNE NAZWA PROGRAMU SUBSTANCJE CZYNNE z Obw. MZ ICD-10 1 2 3 4 5 6 1 03.0000.301.02 B.1. B 18.1
Wykaz programów zdrowotnych (lekowych) Część A Programy lekowe Lp. KOD NUMER ZAŁĄCZNIKA ROZPOZNANIE KLINICZNE NAZWA PROGRAMU SUBSTANCJE CZYNNE z Obw. MZ ICD-10 1 2 3 4 5 6 1 03.0000.301.02 B.1. B 18.1
LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48)
 Dziennik Urzędowy Ministra Zdrowia 546 Poz. 71 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Dziennik Urzędowy Ministra Zdrowia 546 Poz. 71 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Katalog ryczałtów za diagnostykę w programach lekowych
 Katalog ryczałtów za diagnostykę w programach lekowych Lp. Kod Nazwa świadczenia Ryczałt roczny (punkty) Uwagi 1 2 3 4 5 1 5.08.08.0000001 Diagnostyka w programie leczenia przewlekłego WZW typu B lamiwudyną
Katalog ryczałtów za diagnostykę w programach lekowych Lp. Kod Nazwa świadczenia Ryczałt roczny (punkty) Uwagi 1 2 3 4 5 1 5.08.08.0000001 Diagnostyka w programie leczenia przewlekłego WZW typu B lamiwudyną
zaawansowanym rakiem nerkowokomórkowym, rodzajem raka nerki, u pacjentów, którzy byli wcześniej leczeni lekami przeciwnowotworowymi;
 EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Piotr Potemski. Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi
 Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Obserwowane są samoistne regresje zmian przerzutowych
Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Obserwowane są samoistne regresje zmian przerzutowych
S T R E S Z C Z E N I E
 STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
Katalog ryczałtów za diagnostykę w programach lekowych
 Katalog ryczałtów za diagnostykę w programach lekowych Lp. Kod Nazwa świadczenia*** Ryczałt roczny (punkty) Uwagi 1 2 3 4 5 1 5.08.08.0000001 Diagnostyka w programie leczenia przewlekłego WZW typu B lamiwudyną
Katalog ryczałtów za diagnostykę w programach lekowych Lp. Kod Nazwa świadczenia*** Ryczałt roczny (punkty) Uwagi 1 2 3 4 5 1 5.08.08.0000001 Diagnostyka w programie leczenia przewlekłego WZW typu B lamiwudyną
zaawansowany rak nerki lub rak nerki z przerzutami, w skojarzeniu z interferonem alfa-2a;
 EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
I.J.G.C. 2013 -rak jajnika. Paweł Blecharz Klinika Ginekologii Onkologicznej Centrum Onkologii, Instytut, Oddział Kraków
 I.J.G.C. 2013 -rak jajnika Paweł Blecharz Klinika Ginekologii Onkologicznej Centrum Onkologii, Instytut, Oddział Kraków Kliniczne znaczenie STIC Utajone raki jajowodu są znajdowane częściej po RRSO niż
I.J.G.C. 2013 -rak jajnika Paweł Blecharz Klinika Ginekologii Onkologicznej Centrum Onkologii, Instytut, Oddział Kraków Kliniczne znaczenie STIC Utajone raki jajowodu są znajdowane częściej po RRSO niż
Centrum Onkologii-Instytut im. Marii Skłodowskiej-Curie w Warszawie ul. Wawelska 15B, Warszawa, Polska
 C ertyfikat N r: 2 5 8 756-2018-AQ-POL-RvA Data pierws zej c ertyfikacji: 0 6 kwietnia 2 012 Ważnoś ć c ertyfikatu: 2 7 maja 2 0 1 9-0 5 kwietnia 2 021 Niniejszym potwierdza się, że system zarządzania
C ertyfikat N r: 2 5 8 756-2018-AQ-POL-RvA Data pierws zej c ertyfikacji: 0 6 kwietnia 2 012 Ważnoś ć c ertyfikatu: 2 7 maja 2 0 1 9-0 5 kwietnia 2 021 Niniejszym potwierdza się, że system zarządzania
Immunoterapia w praktyce rak nerki
 Immunoterapia w praktyce rak nerki VII Letnia Akademia Onkologiczna dla Dziennikarzy Warszawa 09 sierpień 2018 Piotr Tomczak Uniwersytet Medyczny Poznań Katedra i Klinika Onkologii Leczenie mrcc - zalecenia
Immunoterapia w praktyce rak nerki VII Letnia Akademia Onkologiczna dla Dziennikarzy Warszawa 09 sierpień 2018 Piotr Tomczak Uniwersytet Medyczny Poznań Katedra i Klinika Onkologii Leczenie mrcc - zalecenia
Aktualne na dzień:
 Aktualne na dzień: 16-05-2019 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Randomizowane, prowadzone metodą
Aktualne na dzień: 16-05-2019 L.p. Nazwa badania Numer protokołu Nazwa Sponsora Komórka organizacyjna prowadząca badanie Główny Badacz Badania z aktywną rekrutacją Projekt 1 Randomizowane, prowadzone metodą
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Terapeutyczne Programy Zdrowotne 2009 Leczenie nowotworów podścieliska przewodu pokarmowego (GIST) Załącznik nr 9
 Załącznik nr 9 Nazwa programu: do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) ICD 10 grupa rozpoznań obejmująca nowotwory
Załącznik nr 9 Nazwa programu: do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) ICD 10 grupa rozpoznań obejmująca nowotwory
Forum Organizacji Pacjentów Onkologicznych. Problemy dostępu do leczenia
 Forum Organizacji Pacjentów Onkologicznych Problemy dostępu do leczenia Warszawa, 26 kwietnia 2012 1. CIĄGŁOŚĆ LECZENIA ONKOLOGICZNEGO 2. REGULACJA DOSTĘPU DO LECZENIA NA POZIOMIE ROZPORZĄDZEŃ/ZARZĄDZEŃ
Forum Organizacji Pacjentów Onkologicznych Problemy dostępu do leczenia Warszawa, 26 kwietnia 2012 1. CIĄGŁOŚĆ LECZENIA ONKOLOGICZNEGO 2. REGULACJA DOSTĘPU DO LECZENIA NA POZIOMIE ROZPORZĄDZEŃ/ZARZĄDZEŃ
Immunoterapia niedrobnokomórkowego raka płuca. dr n. med. Adam Płużański. Klinika Nowotworów Płuca i Klatki Piersiowej
 Immunoterapia niedrobnokomórkowego raka płuca dr n. med. Adam Płużański Klinika Nowotworów Płuca i Klatki Piersiowej Centrum Onkologii-Instytut im.m Skłodowskiej-Curie w Warszawie Historia prób immunoterapii
Immunoterapia niedrobnokomórkowego raka płuca dr n. med. Adam Płużański Klinika Nowotworów Płuca i Klatki Piersiowej Centrum Onkologii-Instytut im.m Skłodowskiej-Curie w Warszawie Historia prób immunoterapii
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Piotr Potemski. Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi
 Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Konferencje naukowe a praktyka kliniczna Podstawowe
Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Konferencje naukowe a praktyka kliniczna Podstawowe
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
PROPOZYCJE ZMIAN W PROGRAMIE II LINII. Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK
 PROPOZYCJE ZMIAN W PROGRAMIE II LINII Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK PROGRAM II LINII P R O B L E M Y Z G Ł A S Z A N E W 2 0 1 7 r o k u Brak możliwości
PROPOZYCJE ZMIAN W PROGRAMIE II LINII Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK PROGRAM II LINII P R O B L E M Y Z G Ł A S Z A N E W 2 0 1 7 r o k u Brak możliwości
Terapeutyczne Programy Zdrowotne 2012 Leczenie nowotworów podścieliska przewodu pokarmowego (GIST) Załącznik nr 8
 Załącznik nr 8 Nazwa programu: do Zarządzenia 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) ICD 10 grupa rozpoznań obejmująca nowotwory
Załącznik nr 8 Nazwa programu: do Zarządzenia 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) ICD 10 grupa rozpoznań obejmująca nowotwory
Leczenie zaawansowanych (nieresekcyjnych i/lub przerzutowych) GIST Nieoperacyjny lub rozsiany GIST jest oporny na konwencjonalną chemioterapię.
 Leczenie zaawansowanych (nieresekcyjnych i/lub przerzutowych) GIST Nieoperacyjny lub rozsiany GIST jest oporny na konwencjonalną chemioterapię. Rola radioterapii nie jest ostatecznie ustalona. Dotychczasowe
Leczenie zaawansowanych (nieresekcyjnych i/lub przerzutowych) GIST Nieoperacyjny lub rozsiany GIST jest oporny na konwencjonalną chemioterapię. Rola radioterapii nie jest ostatecznie ustalona. Dotychczasowe
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 130/2013 z dnia 22 lipca 2013 w sprawie oceny leku Afinitor (ewerolimus), tabletki, 5 mg, 30 tabl., kod EAN 5909990711567
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 130/2013 z dnia 22 lipca 2013 w sprawie oceny leku Afinitor (ewerolimus), tabletki, 5 mg, 30 tabl., kod EAN 5909990711567
LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4)
 Załącznik B.53. LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Załącznik B.53. LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Stosowanie preparatu BioCardine900 u chorych. z chorobą wieńcową leczonych angioplastyką naczyń
 Jan Z. Peruga, Stosowanie preparatu BioCardine900 u chorych z chorobą wieńcową leczonych angioplastyką naczyń wieńcowych II Katedra Kardiologii Klinika Kardiologii Uniwersytetu Medycznego w Łodzi 1 Jednym
Jan Z. Peruga, Stosowanie preparatu BioCardine900 u chorych z chorobą wieńcową leczonych angioplastyką naczyń wieńcowych II Katedra Kardiologii Klinika Kardiologii Uniwersytetu Medycznego w Łodzi 1 Jednym
Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008.
 załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
Porównanie skuteczności leków adiuwantowych. w neuropatycznym bólu nowotworowym1
 Porównanie skuteczności leków adiuwantowych w neuropatycznym bólu nowotworowym1 Badanie1 New Delhi Cel Metoda Porównanie pregabaliny z amitryptyliną* i gabapentyną pod względem skuteczności klinicznej
Porównanie skuteczności leków adiuwantowych w neuropatycznym bólu nowotworowym1 Badanie1 New Delhi Cel Metoda Porównanie pregabaliny z amitryptyliną* i gabapentyną pod względem skuteczności klinicznej
Leczenie systemowe raka piersi
 Leczenie systemowe raka piersi Marcin Napierała specjalista onkologii klinicznej Oddział Onkologii Ogólnej SP ZOZ Szpital Wojewódzki Zielona Góra Leczenie systemowe raka piersi Leczenie systemowe raka
Leczenie systemowe raka piersi Marcin Napierała specjalista onkologii klinicznej Oddział Onkologii Ogólnej SP ZOZ Szpital Wojewódzki Zielona Góra Leczenie systemowe raka piersi Leczenie systemowe raka
Nowe wytyczne w diagnostyce i leczeniu raka piersi w oparciu o doniesienia ESMO z 2007 roku
 Nowe wytyczne w diagnostyce i leczeniu raka piersi w oparciu o doniesienia ESMO z 2007 roku Tegoroczna konferencja ESMO zaowocowała nowo przedstawionymi wytycznymi, dotyczącymi zarówno diagnostyki, jak
Nowe wytyczne w diagnostyce i leczeniu raka piersi w oparciu o doniesienia ESMO z 2007 roku Tegoroczna konferencja ESMO zaowocowała nowo przedstawionymi wytycznymi, dotyczącymi zarówno diagnostyki, jak
Terapeutyczne Programy Zdrowotne 2012 Leczenie glejaków mózgu Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r.
 Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
RAK NERKOWO-KOMÓRKOWY UOGÓLNIONE STADIUM PRZEWLEKŁA CHOROBA // DŁUGOŚĆ LECZENIA
 RAK NERKOWO-KOMÓRKOWY PRZEWLEKŁA CHOROBA // DŁUGOŚĆ LECZENIA Maciej Krzakowski Centrum Onkologii-Instytut im. Marii Skłodowskiej-Curie Warszawa 1 SYGNAŁOWE SZLAKI // TERAPEUTYCZNE CELE * Oudard i wsp.
RAK NERKOWO-KOMÓRKOWY PRZEWLEKŁA CHOROBA // DŁUGOŚĆ LECZENIA Maciej Krzakowski Centrum Onkologii-Instytut im. Marii Skłodowskiej-Curie Warszawa 1 SYGNAŁOWE SZLAKI // TERAPEUTYCZNE CELE * Oudard i wsp.
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4)
 Załącznik B.53..docx LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Załącznik B.53..docx LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
