Wiązania chemiczne. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
|
|
|
- Alina Kowalska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Wiązania chemiczne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
2 oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku uwspólnienia dwóch elektronów o spinie przeciwnym, po jednym od każdego atomu wiązanie jonowe powstaje w wyniku przyciągania elektrostatycznego odmiennych ładunków siły Van der Waalsa - mają one głównie charakter elektrostatyczny wiązanie wodorowe wiązanie koordynacyjne 2
3 Wiązanie koordynacyjne tworząca je para elektronów pochodzi od jednego atomu donoru akceptor uzupełnia ostatnią powłokę elektronową do konfiguracji najbliższego gazu szlachetnego donor uzyskuje ładunek dodatni, akceptor uzyskuje ładunek ujemny donorami elektronów są atomy lub jony z przynajmniej jedną wolną parą elektronów, np. azot, tlen siarka, jon chlorkowy akceptorami zazwyczaj są jony wodoru oraz atomy mające lukę oktetową. 3
4 Związki kompleksowe zewnętrzna sfera wewnętrzna K 4 [Fe-(CN) 6 ] jon centralny ligandy wiązanie koordynacyjne 4
5 zewnętrzna sfera wewnętrzna Związki kompleksowe K 4 [Fe (CN) 6 ] Jon centralny: jon centralny ligandy najczęściej kationy metali takich jak żelazo, kobalt, nikiel, mangan oraz platynowce, miedziowce i cynkowce niemetale [SO 4 ] 2-, [PO 4 ] 3-,[BH 4 ] -, [SiF 6 ] 2- Ligandy: koordynowane z atomem centralnym podstawniki: atomy, grupy atomów lub jony ujemne otaczają one atomy centralne i dostarczają przynajmniej jedną wolną parę elektronów ligandy są połączone z jonem centralnym za pomocą wiązania koordynacyjnego w ligandach dawcami elektronów najczęściej są atomy azotu, tlenu, siarki i węgla O: H 2 0, OH -, O 2-, CO 3 2-, RO -, R 2 0 N: H 3 N, H 2 N -, RC:NOH, RNH 2 S: H 2 S, S 2-, S 2 O 3 2-, SCN - 5
6 zewnętrzna sfera wewnętrzna K 4 [Fe(CN) 6 ] jon centralny ligandy Jon kompleksowy może być kationem - [Cu(NH 3 ) 4 ] 2+ anionem [Fe(CN) 6 ] 4- cząsteczką obojętną Ni(CO) 4 Jeżeli część związku kompleksowego złożonego z jonu centralnego i ligandu jest obdarzona ładunkiem, to sferę zewnętrzną tworzą proste jony o przeciwnym znaku. 6
7 Związki kompleksowe - liczba koordynacyjna Liczbę przyłączonych par elektronowych, która najczęściej odpowiada liczbie podstawników przypadających na jon centralny nazywamy liczbą koordynacyjną 7
8 Liczba koordynacyjna Wartość liczby koordynacyjnej zależy od: stosunków przestrzennych możliwości jonu centralnego do przyjęcia par elektronowych na wolne wewnętrzne podpowłoki d (p) Liczba koordynacyjna przyjmuje najczęściej wartości 2, 4 lub 6 Reguła Lamberta - liczba koordynacyjna bardziej zależy od okresu niż grupy; często dla okresu: drugiego LK = 4 trzeciego i czwartego LK = 6 piątego i szóstego LK = 8 8
9 Liczba koordynacyjna 4 spotykana w przypadku: kompleksów metali przejściowych, zawierających dużą liczbę elektronów d. najczęstsza liczba koordynacyjna (dla kompleksów kationów metali grup głównych) związki o tej liczbie kompleksowej mogą wykazywać strukturę: tetraedryczną [BF 4 ] -, [AlH 4 ] - [AlCl 4 ] - płaską kwadratową [Ni(CN) 4 ] 2-, [Pt(H 2 O) 4 ] 2+ charakterystyczna dla kationów zawierających 8 elektronów d (Ni 2+, Pt 2+, Rh +, Pd 2+, r + ) 9
10 Liczba koordynacyjna 6, 7, 8 kompleksy o liczbie koordynacyjnej 6: najczęstsze kompleksy metali przejściowych. maja kształt regularnego ośmiościanu (kompleksy oktaedryczne). odchylenia od idealnego ośmiościanu wynikają: ze struktury elektronowej atomu centralnego (efekt Jahna-Tellera) z oddziaływania kompleksu z jego otoczeniem. liczby koordynacyjne 7, 8 i 9 spotykane są w przypadku, gdy atomy centralne mają duże rozmiary, np. Mo(V) lub W(V). budowa przestrzenna jest skomplikowana, np.bipiramida pentagonalna lub pryzmat trygonalny Efekt Jahna-Tellera: Każdy nieliniowy układ, w którym występuje degeneracja orbitali, wykazuje sposób oscylacji obniżający zarówno symetrię jak i energię układu. Dowolny kompleks oktaedryczny mający zdegenerowane orbitale będzie się odkształcał tak, aby obniżyć swoją symetrię i energię. 10
11 Synteza związków kompleksowych reakcje przyłączania (addycji) wzrasta liczba koordynacyjna metalu Ni + 4CO Ni(CO) 4 tetrakarbonylonikiel(0) reakcje podstawiania (substytucji) nie zmienia się liczba koordynacyjna metalu 4 [Cu(H 2 O) 4 ] NH 3 jony: tetraaquamiedzi() 0 [Cu(NH 3 ) 4 ] H 2 O tetraaminamiedzi() reakcje dysocjacji (eliminacji) maleje liczba koordynacyjna metalu 4 4 reakcje mogą zachodzić ze zmianą stopnia utlenienia +2 chlorek heksaaquakobaltu() 2[Co(H 2 O) 6 ]Cl 2 + 2NH 4 Cl + 10NH 3 + H 2 O 2 +3 chlorek heksaaminakobaltu() 2[Co(NH 3 ) 6 ]Cl H 2 O 9 11
12 zomeria związków kompleksowych Rozróżniamy dwa rodzaje izomerii związków kompleksowych: izomerię strukturalną ten sam sumaryczny skład chemiczny odmienny skład jonów kompleksowych stereoizomerię atom centralny otoczony jest we wszystkich izomerach takimi samymi ligandami, ligandy są położone względem siebie w różny sposób. 12
13 zomeria strukturalna zomeria jonowa: siarczan pentaaminabromokobaltu() - ciemnofioletowy [Co(NH 3 ) 5 Br]SO 4 ligand samodzielny jon bromek pentaaminasiarczanokobaltu czerwony. [Co(NH 3 ) 5 SO 4 ]Br Różnice w reaktywności chemicznej. Pierwszy tworzy osad z roztworem chlorku baru, drugi z azotanem srebra. [Co(NH 3 ) 5 Br]SO 4 + BaCl 2 -> [Co(NH 3 ) 5 Br]Cl 2 + BaSO 4 [Co(NH 3 ) 5 SO 4 ]Br + AgNO 3 -> [Co(NH 3 ) 5 SO 4 ]NO 3 + AgBr 13
14 zomeria strukturalna zomeria hydratacyjna Jednym z ligandów (samodzielnym jonem) jest cząsteczka wody. [Cr(H 2 O) 6 ]Cl 3 fioletowy chlorek heksaakwachromu() [Cr(H 2 O) 5 Cl]Cl 2x H 2 O niebieskozielony chlorek pentaakwachlorochromu() [Cr(H 2 O) 4 Cl 2 ]Cl x H 2 O zielony chlorek tetraakwadichlorochromu() 14
15 zomeria strukturalna zomeria koordynacyjna zomeria koordynacyjna - strefa wewnętrzna i zewnętrzna związku koordynacyjnego są kompleksami. heksacyjanochromian() heksaaminakobaltu() [Co(NH 3 ) 6 ] 3+ [Cr(CN) 6 ] 3- heksacyjanokobaltan() heksaaminachromu() [Cr(NH 3 ) 6 ] 3+ [Co(CN) 6 ] 3-15
16 Stereoizomeria Ligandy rozmieszczone są wokół atomu centralnego w różny sposób Liczba koordynacyjna 4 zomeria optyczna: izomery skręcają płaszczyznę światła spolaryzowanego: o ten sam kąt o przeciwnym znaku izomery nie mają płaszczyzny symetrii środka symetrii zomeria geometryczna (cis-trans): izomery mają płaszczyzny symetrii (przynajmniej jedną) środek symetrii nie wykazują czynności optycznej 16
17 Związki kompleksowe w przyrodzie Do najważniejszych z nich zaliczamy kompleks żelazo porfirynowy. Jest on obecny w hemie hemoglobiny i mioglobiny łańcuch polipeptydowy hemoglobina kompleks żelazo-porfirynowy 17
18 Budowa hemu Wiązania koordynacyjne w hemoglobinie: 4 wiązania łączące żelazo z azotami pierścieni pirolowych wiązanie żelazo azot pierścienia imidazolowego histydyny łączące kompleks żelazo-porfirynowy z łańcuchami wiązanie żelazo cząsteczka tlenu, gdy hemoglobina jest w formie oxy imidazolowy łańcuch boczny histydyny reszta histydyny 18
19 Związki kompleksowe w przyrodzie witamina B12 jon centralny kobalt chlorofil jon centralny magnez 19
20 Związki kompleksowe w przyrodzie białka transportujące metale ceruloplazmina (miedź), transferyna (żelazo). 20
21 Związki kompleksowe w medycynie MB (sestamibi, kardiolit) [Tc(CNR) 6 ] + heksakis(2-metoksyizobutylizonitryl) technet (99mTc) badanie: mięśnia sercowego (scyntygrafia) diagnostyka niektórych nowotworów gruczolaków przytarczyc RNC RNC CNR Tc CNR CNR CNR CH 3 R= CH 2 -C-OCH 3 CH 3 21
22 Związki kompleksowe w medycynie MB (sestamibi, kardiolit) [Tc(CNR) 6 ] + heksakis(2-metoksyizobutylizonitryl) technet (99mTc) badanie: mięśnia sercowego (scyntygrafia) diagnostyka niektórych nowotworów gruczolaków przytarczyc RNC RNC CNR Tc CNR CNR CNR CH 3 R= CH 2 -C-OCH 3 CH 3 zotop, przepływając wraz z krwią przez tętnice wieńcowe, jest wychwytywany przez serce. Miejsca, w których znacznik nie zgromadził się, to miejsca upośledzonego przepływu krwi (perfuzji) i upośledzonej żywotności (obszary żywego, ale niekurczącego się mięśnia). 22
23 Związki kompleksowe w medycynie MB (sestamibi, kardiolit) [Tc(CNR) 6 ] + heksakis(2-metoksyizobutylizonitryl) technet (99mTc) badanie: mięśnia sercowego (scyntygrafia) diagnostyka niektórych nowotworów gruczolaków przytarczyc RNC RNC CNR Tc CNR CNR CNR CH 3 R= CH 2 -C-OCH 3 CH 3 Pacjent z gruczolakiem przytarczyc. Po 10 minutach od podania sestamibi radionuklid jest obecny zarówno w tarczycy, jak i w przytarczycach W ciągu 2 godzin, radionuklid jest wypłukiwany z tarczycy i pozostaje tylko w prawym gruczole przytarczycznym. Strzałka wskazuje gruczolak przytarczycy o masie 794 mg 23
24 Związki kompleksowe w medycynie auranofina [Au(PEt 3 )(ttag)] + ttag = tetra-o-acetylotioglukoza lek przeciwreumatyczny niszczący wirusy HV deponowane w limfocytach T tetraacetylotioglukoza trietylofosfina złoto jon centralny 24
25 Związki kompleksowe w medycynie cis-platyna cis-diaminadichloroplatyna() Cl H 3 N Pt Cl NH 3 cis-[pt(nh 3 ) 2 Cl 2 ] (lek przeciwnowotworowy) Stosowana w leczeniu: raka jądra nowotworów piersi BRCA1 raka płuca raka pęcherza moczowego raka jajnika raka szyjki i macicy nowotworów w obrębie głowy i szyi czerniaka złośliwy mięsaków raka kory nadnerczy Dla prawidłowego funkcjonowania konieczna jest obecność: dwóch ligandów aktywnych chemicznie, będących względem siebie w położeniu cis (atomy chloru), dwóch ligandów niereaktywnych, obojętnych elektrycznie (grupy aminowe). Reaktywne atomy chloru są wymieniane (substytucja nukleofilowa) na atomy azotu zasad guanylowych w łańcuchu DNA 25
26 Związki kompleksowe w medycynie cis-platyna Cl H 3 N Pt Cl NH 3 trans-platyna stereoizomer cis-platyny nie jest aktywny biologicznie! Cl H 3 N Pt Cl H 3 N H 2 O Cl - Cl H 3 N Pt Cl NH 3 dyfuzja pasywna przez błonę komórkową + 2+ Cl H 2 O Cl - H 2 O H + OH H 3 N Pt H 2 O H 3 N Pt H 2 O H 3 N Pt H 2 O NH 3 NH 3 NH 3 aktywne formy cis-platyny addukty cis-platyna-dna krew żylna cytoplazma + DNA komórki nowotworowej + 26
27 Związki kompleksowe chelaty Ligandy zawierające więcej niż jedną parę elektronów, występujących w różnych atomach tej samej cząsteczki nazywamy ligandami chelatującymi związki organiczne zawierające tlen, azot lub siarkę ligandy mogą być cząsteczkami obojętnymi lub anionami ligandy tworzą z kationem centralnym związki pierścieniowe najtrwalsze są kompleksy pięcio- lub sześcioczłonowe w chelatach mogą występować także wiązania jonowe i kowalencyjne szczawian etylenodiamina * - donor o-fenantrolina 27
28 Związki kompleksowe - EDTA kwas etylenodiaminotetraoctowy 28
29 Związki kompleksowe - EDTA 29
30 30
Wiązania chemiczne w układach biologicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Wiązania chemiczne w układach biologicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje
Wiązania chemiczne w układach biologicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje
Chemia ogólna i nieorganiczna
 Chemia ogólna i nieorganiczna Wiązania chemiczne, związki kompleksowe Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli
Chemia ogólna i nieorganiczna Wiązania chemiczne, związki kompleksowe Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli
Wiązania chemiczne, związki kompleksowe. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Wiązania chemiczne, związki kompleksowe Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku
Wiązania chemiczne, związki kompleksowe Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku
Wiązania chemiczne. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Wiązania chemiczne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Wiązania chemiczne Wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku uwspólnienia dwóch elektronów o spinie przeciwnym,
Wiązania chemiczne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Wiązania chemiczne Wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku uwspólnienia dwóch elektronów o spinie przeciwnym,
Wiązania chemiczne Wiązanie koordynacyjne. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Wiązania chemiczne Wiązanie koordynacyjne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Wiązania chemiczne Wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku uwspólnienia dwóch elektronów
Wiązania chemiczne Wiązanie koordynacyjne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Wiązania chemiczne Wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku uwspólnienia dwóch elektronów
Wiązania chemiczne Wiązanie koordynacyjne. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Wiązania chemiczne Wiązanie koordynacyjne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje w
Wiązania chemiczne Wiązanie koordynacyjne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje w
ZWIĄZKI KOMPLEKSOWE. dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE Sole podwójne - to sole zawierające więcej niż jeden rodzaj kationów lub więcej niż jeden rodzaj anionów. Należą do nich m. in. ałuny, np. siarczan amonowo-żelazowy(ii),
ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE Sole podwójne - to sole zawierające więcej niż jeden rodzaj kationów lub więcej niż jeden rodzaj anionów. Należą do nich m. in. ałuny, np. siarczan amonowo-żelazowy(ii),
ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE
 ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE Sole podwójne - to sole zawierające więcej niż jeden rodzaj kationów lub więcej niż jeden rodzaj anionów. Należą do nich m. in. ałuny, np. ałun glinowo-potasowy K 2 Al
ZWIĄZKI KOMPLEKSOWE SOLE PODWÓJNE Sole podwójne - to sole zawierające więcej niż jeden rodzaj kationów lub więcej niż jeden rodzaj anionów. Należą do nich m. in. ałuny, np. ałun glinowo-potasowy K 2 Al
Kompleksy. Stała (nie)trwałości kompleksu (jonu kompleksowego) K 2 [HgI 4 ] 2K + + [HgI 4 ] 2- Budowa związku kompleksowego ... [HgI4] ...
![Kompleksy. Stała (nie)trwałości kompleksu (jonu kompleksowego) K 2 [HgI 4 ] 2K + + [HgI 4 ] 2- Budowa związku kompleksowego ... [HgI4] ... Kompleksy. Stała (nie)trwałości kompleksu (jonu kompleksowego) K 2 [HgI 4 ] 2K + + [HgI 4 ] 2- Budowa związku kompleksowego ... [HgI4] ...](/thumbs/66/54460939.jpg) Kompleksy a) Sole podwójne a związki kompleksowe b) Stałe (nie)trwałości kompleksów c) Ogólna budowa związków kompleksowych rozszczepienie energii orbitali d w kompleksach szereg spektrochemiczny ligandów
Kompleksy a) Sole podwójne a związki kompleksowe b) Stałe (nie)trwałości kompleksów c) Ogólna budowa związków kompleksowych rozszczepienie energii orbitali d w kompleksach szereg spektrochemiczny ligandów
Spis treści. Wstęp. Struktura związków kompleksowych
 Spis treści 1 Wstęp 1.1 Struktura związków kompleksowych 1.1.1 Nomenklatura związków kompleksowych 1.1.1.1 Przykłady: 1.2 Izomeria związków kompleksowych 1.3 Równowagi kompleksowania 2 Część doświadczalna
Spis treści 1 Wstęp 1.1 Struktura związków kompleksowych 1.1.1 Nomenklatura związków kompleksowych 1.1.1.1 Przykłady: 1.2 Izomeria związków kompleksowych 1.3 Równowagi kompleksowania 2 Część doświadczalna
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
4. Związki kompleksowe.
 4. Związki kompleksowe. Jeżeli bezbarwny, bezwodny siarczan(vi) miedzi(ii) CuSO4 rozpuścimy w wodzie, jon miedzi Cu ulega hydratacji przyłączając czasteczki wody. Jon [Cu(H2O)4] przyjmuje barwę niebieską.
4. Związki kompleksowe. Jeżeli bezbarwny, bezwodny siarczan(vi) miedzi(ii) CuSO4 rozpuścimy w wodzie, jon miedzi Cu ulega hydratacji przyłączając czasteczki wody. Jon [Cu(H2O)4] przyjmuje barwę niebieską.
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Związki kompleksowe pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor?
 pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? 1 1 1 H 3 Li 11 Na 19 K 37 Rb 55 Cs 87 Fr 4 Be 12 Mg 20 Ca 38 Sr 56 Ba 88 Ra Układ okresowy 2 13 14 15 16
pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? 1 1 1 H 3 Li 11 Na 19 K 37 Rb 55 Cs 87 Fr 4 Be 12 Mg 20 Ca 38 Sr 56 Ba 88 Ra Układ okresowy 2 13 14 15 16
Związki kompleksowe. pigmenty i barwniki. co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? Pierwiastki
 pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? 1 07_117 Układ okresowy Pierwiastki 1 1 H 3 Li 11 Na 19 K 37 Rb 55 Cs 87 Fr metale niemetale 2 13 14 15 16
pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? 1 07_117 Układ okresowy Pierwiastki 1 1 H 3 Li 11 Na 19 K 37 Rb 55 Cs 87 Fr metale niemetale 2 13 14 15 16
Większość metali bloku d wykazuje tendencje do tworzenia związków kompleksowych.
 Spis treści 1 Ogólna charakterystyka 2 Właściwości fizyczne 3 Związki kompleksowe metali bloku d 4 Wiązanie w związkach kompleksowych 5 Zależność struktury kompleksu od liczby koordynacyjnej (LK) 6 Równowagi
Spis treści 1 Ogólna charakterystyka 2 Właściwości fizyczne 3 Związki kompleksowe metali bloku d 4 Wiązanie w związkach kompleksowych 5 Zależność struktury kompleksu od liczby koordynacyjnej (LK) 6 Równowagi
Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
Wiązania jonowe występują w układach złożonych z atomów skrajnie różniących się elektroujemnością.
 105 Elektronowa teoria wiązania chemicznego Cząsteczki powstają w wyniku połączenia się dwóch lub więcej atomów. Już w początkowym okresie rozwoju chemii podejmowano wysiłki zmierzające do wyjaśnienia
105 Elektronowa teoria wiązania chemicznego Cząsteczki powstają w wyniku połączenia się dwóch lub więcej atomów. Już w początkowym okresie rozwoju chemii podejmowano wysiłki zmierzające do wyjaśnienia
Reakcje chemiczne, związki kompleksowe
 201-11-15, związki kompleksowe Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów
201-11-15, związki kompleksowe Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów
O kompleksach bez kompleksów
 O kompleksach bez kompleksów dr Paweł Urbaniak Łódź, 10.04.2013 Układ okresowy pierwiastków 2 1 Związki kompleksowe - definicja CrCl 3 jest trwałym związkiem, podobnie jak amoniak NH 3. Oba związki mogą
O kompleksach bez kompleksów dr Paweł Urbaniak Łódź, 10.04.2013 Układ okresowy pierwiastków 2 1 Związki kompleksowe - definicja CrCl 3 jest trwałym związkiem, podobnie jak amoniak NH 3. Oba związki mogą
Wiązania chemiczne. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Wiązania chemiczne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku uwspólnienia dwóch
Wiązania chemiczne Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego oddziaływania międzycząstczkowe Wiązania chemiczne wiązanie atomowe, czyli kowalencyjne, powstaje w wyniku uwspólnienia dwóch
1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru
 1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru 2. Na podstawie struktury cząsteczek wyjaśnij dlaczego N 2 jest bierny a Cl 2 aktywny chemicznie? 3. Które substancje posiadają budowę
1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru 2. Na podstawie struktury cząsteczek wyjaśnij dlaczego N 2 jest bierny a Cl 2 aktywny chemicznie? 3. Które substancje posiadają budowę
CHEMIA WARTA POZNANIA
 Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część III Podstawowe pojęcia chemii koordynacyjnej Atom centralny [Cr(H 2 O) 6 ]Cl 3 Ligand Związek
Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część III Podstawowe pojęcia chemii koordynacyjnej Atom centralny [Cr(H 2 O) 6 ]Cl 3 Ligand Związek
Spis treści. Metoda VSEPR. Reguły określania struktury cząsteczek. Ustalanie struktury przestrzennej
 Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Temat 1: Budowa atomu zadania
 Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej jedną z dwóch metod (teorii): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Reakcje chemiczne. Typ reakcji Schemat Przykłady Reakcja syntezy
 Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Chemia Nieorganiczna II (3.3.PBN.CHE109), konwersatorium Chemia, I stopień, III r., semestr 5. Lista 1.
 Lista 1. 1. Określ zależność pomiędzy właściwościami magnetycznymi (wartością momentu magnetycznego µ B, wyrażonego w magnetonach Bohra) a przynależnością do typu kompleksów wewnątrz- i zewnątrz-orbitalowych,
Lista 1. 1. Określ zależność pomiędzy właściwościami magnetycznymi (wartością momentu magnetycznego µ B, wyrażonego w magnetonach Bohra) a przynależnością do typu kompleksów wewnątrz- i zewnątrz-orbitalowych,
CZ STECZKA. Do opisu wi za chemicznych stosuje si najcz ciej jedn z dwóch metod (teorii): metoda wi za walencyjnych (VB)
 CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
III Podkarpacki Konkurs Chemiczny 2010/2011. ETAP I r. Godz Zadanie 1
 III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
Nazwy pierwiastków: ...
 Zadanie 1. [ 3 pkt.] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Atom pierwiastka X w reakcjach chemicznych może tworzyć jon zawierający 20
Zadanie 1. [ 3 pkt.] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Atom pierwiastka X w reakcjach chemicznych może tworzyć jon zawierający 20
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Ligand to cząsteczka albo jon, który związany jest z jonem albo atomem centralnym.
 138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Budowa atomu. Wiązania chemiczne
 strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
Chemia organiczna. Stereochemia. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami
Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami
Projekt Era inżyniera pewna lokata na przyszłość jest współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego
 TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
czyli reakcje wymiany ligandów i ich zastosowanie Mateusz Bożejko Edmund Pelc Liceum Ogólnokształcące nr III we Wrocławiu
 czyli reakcje wymiany ligandów i ich zastosowanie Mateusz Bożejko Edmund Pelc Liceum Ogólnokształcące nr III we Wrocławiu Podstawowe pojęcia Podstawowe pojęcia Związek kompleksowy Sfera koordynacyjna Ligand
czyli reakcje wymiany ligandów i ich zastosowanie Mateusz Bożejko Edmund Pelc Liceum Ogólnokształcące nr III we Wrocławiu Podstawowe pojęcia Podstawowe pojęcia Związek kompleksowy Sfera koordynacyjna Ligand
V KONKURS CHEMICZNY 23.X. 2007r. DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚWIĘTOKRZYSKIEGO Etap I ... ... czas trwania: 90 min Nazwa szkoły
 V KONKURS CHEMICZNY 23.X. 2007r. DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚWIĘTOKRZYSKIEGO Etap I...... Imię i nazwisko ucznia ilość pkt.... czas trwania: 90 min Nazwa szkoły... maksymalna ilość punk. 33 Imię
V KONKURS CHEMICZNY 23.X. 2007r. DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚWIĘTOKRZYSKIEGO Etap I...... Imię i nazwisko ucznia ilość pkt.... czas trwania: 90 min Nazwa szkoły... maksymalna ilość punk. 33 Imię
KOMPLEKSY. Wzory strukturalne kompleksów Ni 2+ oraz Cu 2+ z dimetyloglioksymem.
 KOMPLEKSY Kompleksem nazywamy układ złożony z centralnego atomu lub jonu metalu otoczonego ligandami. Ligandy łączą się z atomem centralnym za pomocą wiązań koordynacyjnych, w których atom/jon centralny
KOMPLEKSY Kompleksem nazywamy układ złożony z centralnego atomu lub jonu metalu otoczonego ligandami. Ligandy łączą się z atomem centralnym za pomocą wiązań koordynacyjnych, w których atom/jon centralny
Chemia I Semestr I (1 )
 1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Anna Grych Test z budowy atomu i wiązań chemicznych
 Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Wewnętrzna budowa materii
 Atom i układ okresowy Wewnętrzna budowa materii Atom jest zbudowany z jądra atomowego oraz krążących wokół niego elektronów. Na jądro atomowe składają się protony oraz neutrony, zwane wspólnie nukleonami.
Atom i układ okresowy Wewnętrzna budowa materii Atom jest zbudowany z jądra atomowego oraz krążących wokół niego elektronów. Na jądro atomowe składają się protony oraz neutrony, zwane wspólnie nukleonami.
8. Trwałość termodynamiczna i kinetyczna związków kompleksowych
 8. Trwałość termodynamiczna i kinetyczna związków kompleksowych Tworzenie związku kompleksowego w roztworze wodnym następuje poprzez wymianę cząsteczek wody w akwakompleksie [M(H 2 O) n ] m+ na inne ligandy,
8. Trwałość termodynamiczna i kinetyczna związków kompleksowych Tworzenie związku kompleksowego w roztworze wodnym następuje poprzez wymianę cząsteczek wody w akwakompleksie [M(H 2 O) n ] m+ na inne ligandy,
11) Stan energetyczny elektronu w atomie kwantowanym jest zespołem : a dwóch liczb kwantowych b + czterech liczb kwantowych c nie jest kwantowany
 PYTANIA EGZAMINACYJNE Z CHEMII OGÓLNEJ I Podstawowe pojęcia chemiczne 1) Pierwiastkiem nazywamy : a zbiór atomów o tej samej liczbie masowej b + zbiór atomów o tej samej liczbie atomowej c zbiór atomów
PYTANIA EGZAMINACYJNE Z CHEMII OGÓLNEJ I Podstawowe pojęcia chemiczne 1) Pierwiastkiem nazywamy : a zbiór atomów o tej samej liczbie masowej b + zbiór atomów o tej samej liczbie atomowej c zbiór atomów
O kompleksach bez kompleksów. dr Paweł Urbaniak Łódź,
 O kompleksach bez kompleksów dr Paweł Urbaniak Łódź, 24.04.2019 Plan prezentacji 1. Czym są związki kompleksowe? 2. Trwałość związków kompleksowych. 3. Gdzie znajduje zastosowanie wiedza o trwałości związków
O kompleksach bez kompleksów dr Paweł Urbaniak Łódź, 24.04.2019 Plan prezentacji 1. Czym są związki kompleksowe? 2. Trwałość związków kompleksowych. 3. Gdzie znajduje zastosowanie wiedza o trwałości związków
Związki chemiczne, wiązania chemiczne, reakcje
 Związki chemiczne, wiązania chemiczne, reakcje Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna
Związki chemiczne, wiązania chemiczne, reakcje Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 01/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 01/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Wewnętrzna budowa materii - zadania
 Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Jeśli teraz nasz związek, chlorek glinu, ulegnie dysocjacji elektrolitycznej, rozpadnie się na jony według równania:
 Wiązania chemiczne powstają między atomami wówczas, gdy dwa atomy zbliżą się do siebie na tak bliska odległość, że orbital jednego z nich znajdzie się w obrębie orbitala drugiego atomu. Jeśli na każdym
Wiązania chemiczne powstają między atomami wówczas, gdy dwa atomy zbliżą się do siebie na tak bliska odległość, że orbital jednego z nich znajdzie się w obrębie orbitala drugiego atomu. Jeśli na każdym
ligandu (donora elektronów) atomu centralnego (akceptora elektronów)
 Związki kompleksowe Podstawy chemii kompleksów stworzył Alfred Werner na początku XX wieku, gdy zajmował się grupą bardzo trwałych związków, jakie tworzy amoniak z CoCl 3. - Zaproponował dla nich poprawne
Związki kompleksowe Podstawy chemii kompleksów stworzył Alfred Werner na początku XX wieku, gdy zajmował się grupą bardzo trwałych związków, jakie tworzy amoniak z CoCl 3. - Zaproponował dla nich poprawne
Związki chemiczne, wiązania chemiczne, reakcje
 Związki chemiczne, wiązania chemiczne, reakcje Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna
Związki chemiczne, wiązania chemiczne, reakcje Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna
Konfiguracja elektronowa atomu
 Konfiguracja elektronowa atomu ANALIZA CHEMICZNA BADANIE WŁAŚCIWOŚCI SUBSTANCJI KONTROLA I STEROWANIE PROCESAMI TECHNOLOGICZNYMI Właściwości pierwiastków - Układ okresowy Prawo okresowości Mendelejewa
Konfiguracja elektronowa atomu ANALIZA CHEMICZNA BADANIE WŁAŚCIWOŚCI SUBSTANCJI KONTROLA I STEROWANIE PROCESAMI TECHNOLOGICZNYMI Właściwości pierwiastków - Układ okresowy Prawo okresowości Mendelejewa
Spis treści. Właściwości fizyczne. Wodorki berylowców. Berylowce
 Berylowce Spis treści 1 Właściwości fizyczne 2 Wodorki berylowców 3 Tlenki berylowców 4 Nadtlenki 5 Wodorotlenki 6 Iloczyn rozpuszczalności 7 Chlorki, fluorki, węglany 8 Siarczany 9 Twardość wody 10 Analiza
Berylowce Spis treści 1 Właściwości fizyczne 2 Wodorki berylowców 3 Tlenki berylowców 4 Nadtlenki 5 Wodorotlenki 6 Iloczyn rozpuszczalności 7 Chlorki, fluorki, węglany 8 Siarczany 9 Twardość wody 10 Analiza
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Zadanie 1. (1 pkt). Informacja do zada 2. i 3. Zadanie 2. (1 pkt) { Zadania 2., 3. i 4 s dla poziomu rozszerzonego} zania zania Zadanie 3.
 2. ELEKTRONY W ATOMACH I CZĄSTECZKACH. A1 - POZIOM PODSTAWOWY. Zadanie 1. (1 pkt). Konfigurację elektronową 1s 2 2s 2 2p 6 3s 2 3p 6 mają atomy i jony: A. Mg 2+, Cl -, K +, B. Ar, S 2-, K +, C. Ar, Na
2. ELEKTRONY W ATOMACH I CZĄSTECZKACH. A1 - POZIOM PODSTAWOWY. Zadanie 1. (1 pkt). Konfigurację elektronową 1s 2 2s 2 2p 6 3s 2 3p 6 mają atomy i jony: A. Mg 2+, Cl -, K +, B. Ar, S 2-, K +, C. Ar, Na
MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA
 Z am K or Copyright by ZamKor P. Sagnowski i Wspólnicy spółka jawna, Kraków 0 MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA Poziom rozszerzony Zadanie Odpowiedzi Uwagi za prawidłowe uzupełnienie schematu: Punktacja
Z am K or Copyright by ZamKor P. Sagnowski i Wspólnicy spółka jawna, Kraków 0 MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA Poziom rozszerzony Zadanie Odpowiedzi Uwagi za prawidłowe uzupełnienie schematu: Punktacja
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Związki chemiczne, wiązania chemiczne, reakcje
 Związki chemiczne, wiązania chemiczne, reakcje Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna
Związki chemiczne, wiązania chemiczne, reakcje Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu
KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW 2008/2009
 ...... kod pracy ucznia pieczątka nagłówkowa szkoły Drogi Uczniu, KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW 2008/2009 Witaj na I etapie konkursu chemicznego. Przeczytaj uważnie instrukcję i postaraj
...... kod pracy ucznia pieczątka nagłówkowa szkoły Drogi Uczniu, KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW 2008/2009 Witaj na I etapie konkursu chemicznego. Przeczytaj uważnie instrukcję i postaraj
Związki koordynacyjne
 Związki koordynacyjne. Cele lekcji a) Wiadomości Uczeń zna: pojęcia: związek koordynacyjny, ligand, atom centralny, centrum koordynacji, liczba koordynacyjna, budowę związków kompleksowych, podział kompleksów
Związki koordynacyjne. Cele lekcji a) Wiadomości Uczeń zna: pojęcia: związek koordynacyjny, ligand, atom centralny, centrum koordynacji, liczba koordynacyjna, budowę związków kompleksowych, podział kompleksów
WARSZTATY olimpijskie. Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna Kinetyka
 WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
ZWIĄZKI METALI PRZEJŚCIOWYCH. Jak powstaje jon kompleksowy? K 3 FeF 6 3K + + (FeF 6 ) 3-
 WYKŁAD 4 ZWIĄZKI METALI PRZEJŚCIOWYCH Jak powstaje jon kompleksowy? K 3 FeF 6 3K (FeF 6 ) 3 Fe 3 (1s) 2 (2s) 2 (2p) 6 (3s) 2 (3p) 6 (3d) 5 OKTAEDR F F F 3 Fe F F F jon centralny ligand Energia elektronów
WYKŁAD 4 ZWIĄZKI METALI PRZEJŚCIOWYCH Jak powstaje jon kompleksowy? K 3 FeF 6 3K (FeF 6 ) 3 Fe 3 (1s) 2 (2s) 2 (2p) 6 (3s) 2 (3p) 6 (3d) 5 OKTAEDR F F F 3 Fe F F F jon centralny ligand Energia elektronów
Związki kompleksowe (związki koordynacyjne) (opracowanie: dr Katarzyna Makyła-Juzak, dr Anna Chachaj-Brekiesz)
 Związki kompleksowe (związki koordynacyjne) (opracowanie: dr Katarzyna Makyła-Juzak, dr Anna Chachaj-Brekiesz) 1. Budowa związków kompleksowych W wyniku reakcji rozpuszczania osadu AgCl w nadmiarze wodnego
Związki kompleksowe (związki koordynacyjne) (opracowanie: dr Katarzyna Makyła-Juzak, dr Anna Chachaj-Brekiesz) 1. Budowa związków kompleksowych W wyniku reakcji rozpuszczania osadu AgCl w nadmiarze wodnego
1. Budowa atomu. Układ okresowy pierwiastków chemicznych
 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej (załącznik nr 1 do rozporządzenia, Dz.U. z 2018 r., poz. 467), programie nauczania oraz w części
Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej (załącznik nr 1 do rozporządzenia, Dz.U. z 2018 r., poz. 467), programie nauczania oraz w części
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
I. Substancje i ich przemiany
 NaCoBeZU z chemii dla klasy 1 I. Substancje i ich przemiany 1. Pracownia chemiczna podstawowe szkło i sprzęt laboratoryjny. Przepisy BHP i regulamin pracowni chemicznej zaliczam chemię do nauk przyrodniczych
NaCoBeZU z chemii dla klasy 1 I. Substancje i ich przemiany 1. Pracownia chemiczna podstawowe szkło i sprzęt laboratoryjny. Przepisy BHP i regulamin pracowni chemicznej zaliczam chemię do nauk przyrodniczych
Wiązania kowalencyjne
 Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne
 Anna Grych Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne Informacja do zadań -7 75 Dany jest pierwiastek 33 As. Zadanie. ( pkt) Uzupełnij poniższą tabelkę.
Anna Grych Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne Informacja do zadań -7 75 Dany jest pierwiastek 33 As. Zadanie. ( pkt) Uzupełnij poniższą tabelkę.
TYPY REAKCJI CHEMICZNYCH
 1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
( ) ρ ( ) ( ) ( ) ( ) ( ) Rozkład ładunku i momenty dipolowe cząsteczek. woda H 2 O. aceton (CH 3 ) 2 CO
 Rozkład ładunku i momenty dipolowe cząsteczek W fizyce klasycznej moment dipolowy układu ładunków oblicza się tak: i i i ( ) ρ ( ) µ = q r lub µ = ρ x, y, z r dxdydz = x, y, z r dv W teorii kwantowej moment
Rozkład ładunku i momenty dipolowe cząsteczek W fizyce klasycznej moment dipolowy układu ładunków oblicza się tak: i i i ( ) ρ ( ) µ = q r lub µ = ρ x, y, z r dxdydz = x, y, z r dv W teorii kwantowej moment
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA. Wykład 2
 PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
Obliczenia stechiometryczne, bilansowanie równań reakcji redoks
 Obliczenia stechiometryczne, bilansowanie równań reakcji redoks Materiały pomocnicze do zajęć wspomagających z chemii opracował: dr Błażej Gierczyk Wydział Chemii UAM Obliczenia stechiometryczne Podstawą
Obliczenia stechiometryczne, bilansowanie równań reakcji redoks Materiały pomocnicze do zajęć wspomagających z chemii opracował: dr Błażej Gierczyk Wydział Chemii UAM Obliczenia stechiometryczne Podstawą
1919 Irving Langmuir wyjaśnia wiązalność pierwiastków za pomocą procesów zachodzących w powłokach elektronowych - elektronowa teoria walencyjności
 WIĄZANIA CHEMICZNE To takie wzajemne oddziaływania, które powodują, Ŝe atomy są ze sobą związane trwale tzn. utrzymują się w określonych odległościach od siebie i tworzą układ, który ma nowe jakościowo
WIĄZANIA CHEMICZNE To takie wzajemne oddziaływania, które powodują, Ŝe atomy są ze sobą związane trwale tzn. utrzymują się w określonych odległościach od siebie i tworzą układ, który ma nowe jakościowo
pobrano z
 ODPOWIEDZI Zadanie 1. (2 pkt) 1. promienia atomowego, promienia jonowego 2. najwyższego stopnia utlenienia Zadanie 2. (1 pkt) 1. Pierwiastek I jest aktywnym metalem. Tworzy wodorek, w którym wodór przyjmuje
ODPOWIEDZI Zadanie 1. (2 pkt) 1. promienia atomowego, promienia jonowego 2. najwyższego stopnia utlenienia Zadanie 2. (1 pkt) 1. Pierwiastek I jest aktywnym metalem. Tworzy wodorek, w którym wodór przyjmuje
 PRACA KONTROLNA Z CHEMII NR 1 - Semestr I 1. (6 pkt) - Krótko napisz, jak rozumiesz następujące pojęcia: a/ liczba atomowa, b/ nuklid, c/ pierwiastek d/ dualizm korpuskularno- falowy e/promieniotwórczość
PRACA KONTROLNA Z CHEMII NR 1 - Semestr I 1. (6 pkt) - Krótko napisz, jak rozumiesz następujące pojęcia: a/ liczba atomowa, b/ nuklid, c/ pierwiastek d/ dualizm korpuskularno- falowy e/promieniotwórczość
Chemia Wydział SiMR, kierunek IPEiH I rok I stopnia studiów, semestr I. Chemia nieorganiczna. Stopień utlenienia. Stopień utlenienia.
 -- Chemia Wydział SiMR, kierunek IPEiH I rok I stopnia studiów, semestr I dr inż. Leszek Niedzicki Chemia nieorganiczna Drobina Drobiną nazywamy proste układy atomów tj.: atom (zwykle metalu np. Cu, Na,
-- Chemia Wydział SiMR, kierunek IPEiH I rok I stopnia studiów, semestr I dr inż. Leszek Niedzicki Chemia nieorganiczna Drobina Drobiną nazywamy proste układy atomów tj.: atom (zwykle metalu np. Cu, Na,
7-9. Stereoizomeria. izomery. konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych
 7-9. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
7-9. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
Zadanie 4. Mrówczan metylu ma taki sam wzór sumaryczny jak: A. octan etylu. C. kwas mrówkowy. B. octan metylu. D. kwas octowy.
 Pieczęć KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 3 marca 2011 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
Pieczęć KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 3 marca 2011 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
Stereochemia Ułożenie atomów w przestrzeni
 Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Z m.a. I. SUBSTANCJE CHEMICZNE BUDOWA I WŁAŚCIWOŚCI H, 2 1 H, 3 1 GC.I.(5) 1 WAŻNE POJĘCIA W CHEMII:
 pitagoras.d2.pl I. SUBSTANCJE CHEMICZNE BUDOWA I WŁAŚCIWOŚCI WAŻNE POJĘCIA W CHEMII: Pierwiastek chemiczny składnik prosty substancji, nie ulegający dalszemu rozkładowi w jakichkolwiek przemianach chemicznych.
pitagoras.d2.pl I. SUBSTANCJE CHEMICZNE BUDOWA I WŁAŚCIWOŚCI WAŻNE POJĘCIA W CHEMII: Pierwiastek chemiczny składnik prosty substancji, nie ulegający dalszemu rozkładowi w jakichkolwiek przemianach chemicznych.
Sprawdzian 2. CHEMIA. Przed próbną maturą. (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 34. Imię i nazwisko ...
 CHEMIA Przed próbną maturą Sprawdzian 2. (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 34 Imię i nazwisko... Liczba punktów Procent 2 Informacja do zadań 1 i 2. Naturalny chlor występuje
CHEMIA Przed próbną maturą Sprawdzian 2. (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 34 Imię i nazwisko... Liczba punktów Procent 2 Informacja do zadań 1 i 2. Naturalny chlor występuje
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
4. Stereoizomeria. izomery. konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych
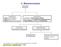 4. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
4. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Krystalografia. Typowe struktury pierwiastków i związków chemicznych
 Krystalografia Typowe struktury pierwiastków i związków chemicznych Wiązania w kryształach jonowe silne, bezkierunkowe kowalencyjne silne, kierunkowe metaliczne słabe lub silne, bezkierunkowe van der Waalsa
Krystalografia Typowe struktury pierwiastków i związków chemicznych Wiązania w kryształach jonowe silne, bezkierunkowe kowalencyjne silne, kierunkowe metaliczne słabe lub silne, bezkierunkowe van der Waalsa
Dlaczego sacharoza (cukier trzcinowy) topi się w temperaturze 185 C, podczas
 1 Wiązania chemiczne i zjawisko izomerii Dlaczego sacharoza (cukier trzcinowy) topi się w temperaturze 185 C, podczas gdy chlorek sodowy (sól kuchenna) topi się w znacznie wyższej temperaturze, bo w 801
1 Wiązania chemiczne i zjawisko izomerii Dlaczego sacharoza (cukier trzcinowy) topi się w temperaturze 185 C, podczas gdy chlorek sodowy (sól kuchenna) topi się w znacznie wyższej temperaturze, bo w 801
