Michał Bijak*, Michał Błażej Ponczek, Joanna Saluk, Marta Chabielska, Julita Stępniak, Paweł Nowak
|
|
|
- Stefan Czech
- 6 lat temu
- Przeglądów:
Transkrypt
1 2012, 66, 7-8 NADTLENOAZOTYN SILNY BIOLOGICZNY UTLENIACZ PEROXYNITRITE A STRONG BIOLOGICAL OXIDANT Michał Bijak*, Michał Błażej Ponczek, Joanna Saluk, Marta Chabielska, Julita Stępniak, Paweł Nowak Katedra Biochemii Ogólnej, Uniwersytet Łódzki, ul. Pomorska 141/143, Łódź * mbijak@biol.uni.lodz.pl Abstract Wstęp 1. Powstawanie i ogólna charakterystyka nadtlenoazotynu 2. Prekursory nadtlenoazotynu 3. Reaktywność nadtlenoazotynu 4. Biologiczne działanie nadtlenoazotynu Piśmiennictwo cytowane
2 624 M. BIJAK, M.B. PONCZEK, J. SALUK, M. CHABIELSKA, J. STĘPNIAK, P. NOWAK mgr Michał Bijak w 2010 roku ukończył studia na Wydziale Biologii i Ochrony Środowiska Uniwersytetu Łódzkiego. Badania prowadzone w ramach przygotowywania pracy magisterskiej zatytułowanej: Ocena działania polifenolowych ekstraktów roślinnych na aktywność koagulacyjną osocza i trombiny stały się podstawa jego dalszej działalności naukowej. Od 2010 roku jest doktorantem Studium Doktoranckiego Biochemiczno-Biofizycznego Uniwersytetu Łódzkiego. Pracę doktorską wykonuje w Katedrze Biochemii Ogólnej UŁ. Celem jego pracy jest zbadanie oddziaływania związków polifenolowych z enzymami kaskady krzepnięcia krwi. dr Michał Ponczek urodzony w 1975 roku w Łodzi biochemik, bioinformatyk, obecnie adiunkt zatrudniony od 2008 w Katedrze Biochemii Ogólnej Uniwersytetu Łódzkiego. Finalista 39 i 40 Olimpiady Chemicznej w 1994 i 1995 roku. Studiował Medycynę. Ukończył studia magisterskie z biologii na Wydziale Biologii i Ochrony Środowiska Uniwersytetu Łódzkiego, a następnie Podyplomowe Studium z Informatyki oraz Doktoranckie Studium Biochemiczno-Biofizyczne na Uniwersytecie Łódzkim. Obronił doktorat z biochemii w 2007 roku. Przebywał w 2008 roku na 3 miesięcznym stażu podoktorskim na Uniwersytecie Kalifornijskim San Diego, ufundowanym przez Europejską Organizację Biologii Molekularnej. Jest autorem i współautorem 13 artykułów naukowych w języku angielskim i 5 prac poglądowych w języku polskim obejmujących zagadnienia związane z bioinformatyką, filogenetyką molekularną i biochemią układu hemostazy oraz stresem oksydacyjnym. Jego zainteresowania badawcze obejmują szczególnie zagadnienia związane z ewolucją białek. dr Joanna Saluk od roku 2000 jest zatrudniona w Katedrze Biochemii Ogólnej Uniwersytetu Łódzkiego, gdzie obecnie pracuje na stanowisku adiunkta. W roku 2001 uzyskała stopień doktora na podstawie rozprawy zatytułowanej: Zmiany aktywności biologicznej płytek krwi wywołane działaniem lipopolisacharydów Proteus mirabilis. Jej naukowe zainteresowania koncentrują się wokół zagadnień związanych z rolą płytek krwi w rozwoju reakcji zapalnych, głównie na oddziaływaniu płytek z toksyną bakterii Gramujemnych. Drugi nurt prowadzonych przez nią badań to poszukiwanie aktywnych biologicznie związków naturalnych dostępnych w diecie, które mogłyby funkcjonować jako naturalne antyoksydanty egzogenne o właściwościach przeciwpłytkowych. W roku 2010 została laureatką konkursu na stypendium habilitacyjne L Oréal Polska dla Kobiet i Nauki przyznawane przy wsparciu Polskiego Komitetu ds. UNESCO. Marta Chabielska, studentka dwuletnich uzupełniających studiów magisterskich na Wydziale Biologii i Ochrony Środowiska, na kieruneku biologia, specjalność: biochemia. Obecnie wykonuje prace magisterską w Katedrze Biochemii Ogólnej UŁ, której celem jest zbadanie wybranych ekstraktów roślinnych (Asteraceae) jako potencjalnych antyoksydantów, chroniących układ hemostazy przed działaniem reaktywnych form tlenu i azotu. mgr Julita Stępniak ukończyła studia na wydziale Biologii i Ochrony Środowiska Uniwersytetu Łódzkiego; kierunek biologia (specjalność biochemia). Celem jej pracy magisterskiej było zbadanie wpływu nadtlenoazotynu na strukturę i lizę włóknika. dr hab. Paweł Nowak, prof. nadzw. UŁ, biochemik, specjalista w zakresie biochemii krzepnięcia krwi. Jest współautorem 48 prac doświadczalnych opublikowanych w czasopismach indeksowanych przez filadelfijski Instytut Informacji Naukowej, 1 podręcznika akademickiego i 5 prac przeglądowych. Rezultaty swoich badań prezentował na ponad 50 konferencjach krajowych i zagranicznych. W ciągu ostatnich 10 lat zasadniczy nurt Jego aktywności naukowej związany jest z wyjaśnieniem molekularnych mechanizmów zaburzeń w układzie hemostazy spowodowanych przez reaktywne formy tlenu i azotu, a w szczególności z badaniami zaburzeń funkcji płytek krwi, plazminogenu i fibrynogenu wywołanych przez nadtlenoazotyn.
3 NADTLENOAZOTYN SILNY BIOLOGICZNY UTLENIACZ 625 ABSTRACT As demonstrated in recent years, one of the major factors of oxidative stress, generated in the circulatory system, in both acute and chronic pathological conditions, is peroxynitrite (ONOO ) [4]. Peroxynitrite is a strong biological oxidant and nitrating compound, generated in vivo from a rapid reaction of two relatively less reactive, but commonly found, of free radicals: nitrogen monoxide (NO) and superoxide (O2 ) [8]. This reaction occurs spontaneously and is not catalyzed by any enzyme. A fundamental reaction of ONOO in biological systems is its fast reaction with carbon dioxide (k = 5, M 1 s 1 ) and yields a short-lived intermediate, nitrosoperoxycarbonate (ONOOCO 2 ), which homolyzes leads to the formation of carbonate (CO 3 ) and nitrogen dioxide (NO 2 ) radicals (yield ~35%) [29, 30] (Fig. 1), which are one-electron oxidants. ONOO is responsible for oxidative modifications in a wide variety of biomolecules and is capable to induce of nitrative changes in sulfur and aromatic amino acids, especially 3-nitrotyrosine and dityrosine formation [17] (Fig. 2). This article describes the formation, reactivity and biological action of peroxynitrite. Keywords: peroxynitrite, oxidative stress, 3-nitrotyrosine Słowa kluczowe: nadtlenoazotyn, stres oksydacyjny, 3-nitrotyrozyna
4 626 M. BIJAK, M.B. PONCZEK, J. SALUK, M. CHABIELSKA, J. STĘPNIAK, P. NOWAK WSTĘP Jednym z nieodłącznych elementów tlenowego metabolizmu komórki jest generowanie reaktywnych form tlenu (RFT) i reaktywnych form azotu (RFA). Mogą to być zarówno jony, jak i związki bez ładunku elektrycznego, ze sparowanymi elektronami, jak również wolne rodniki, których cechą wspólną jest duża reaktywność. Źródłem RFT/RFA są produkty pośrednie utleniania przenośników elektronów, związki generowane w czasie rozwoju reakcji zapalnych, peroksydacja lipidów oraz reakcje katalizowane przez oksydazy i jony metali (Fe 3+, Cu 2+ ) [1]. RFT i RFA stanowią ważny element procesów związanych z odpowiedzią immunologiczną, działają jako bezpośrednie czynniki bakteriobójcze (wybuch tlenowy fagocytów), a także uczestniczą w szlakach przekazywania sygnałów w komórkach [2]. Stan, w którym zostaje zaburzona równowaga pomiędzy szybkością powstawania RFT i RFA, a biologiczną zdolnością do szybkiej detekcji i unieczynnienia reaktywnych produktów pośrednich i/lub naprawy powstałych uszkodzeń przez układy antyoksydacyjne nosi nazwę stresu oksydacyjnego, który w skrajnych przypadkach może powodować nieodwracalne uszkodzenia komórek. Istotne znaczenie zaburzonej równowagi statusu oksydacyjnego zaobserwowano w wielu jednostkach chorobowych związanych z układem krążenia: między innymi w nadciśnieniu tętniczym, miażdżycy czy restenozie po zabiegach angioplastyki [3]. Wolnorodnikowe uszkodzenia białek, lipidów, węglowodanów oraz DNA stanowią jeden z głównych czynników etiopatologii wielu chorób [4]. Jak wykazano w ostatnich latach, jednym z głównych czynników stresu oksydacyjnego powstających w układzie krążenia w ostrych i przewlekłych stanach zapalnych oraz niedokrwienno-reperfuzyjnych jest nadtlenoazotyn [5,6]. Nadtlenoazotyn (ONOO ) jest silnym związkiem utleniającym i nitrującym, tworzonym przez komórki śródbłonka, aktywowane makrofagii oraz neutrofile [7]. W ciągu ostatnich lat bardzo szybko wzrasta liczba publikacji związanych z określeniem fizjologicznej i patofizjologicznej roli nadtlenoazotynu w organizmie, co świadczy o dużym zainteresowaniu tym czynnikiem stresu oksydacyjnego. 1. POWSTAWANIE I OGÓLNA CHARAKTERYSTYKA NADTLENOAZOTYNU Beckman i in. [8] w 1990 roku opisali reakcje powstawania nadtlenoazotynu w warunkach in vivo. W układach biologicznych ONOO jest tworzony w wyniku reakcji dwóch stosunkowo mało reaktywnych, lecz powszechnie występujących wolnych rodników: anionorodnika ponadtlenkowego (O 2 ) i tlenku azotu (NO ). Reakcja ta zachodzi spontanicznie i nie jest katalizowana przez żaden enzym. Stała szybkości reakcji powstawania nadtlenoazotynu jest około 3 8 razy większa niż rozkład anionorodnika ponadtlenkowego katalizowany przez dysmutazę ponadtlenkową (SOD) i wynosi k = 6, mol/l s [9, 10]. W związku z tym, że obydwa prekursory nadtlenoazotynu mają bardzo krótki okres półtrwania (NO 1 30 sekund; O 2
5 NADTLENOAZOTYN SILNY BIOLOGICZNY UTLENIACZ 627 milisekundy), nadlenoazotyn może powstawać w tym samym przedziale komórkowym przy jednoczesnym generowaniu jego prekursorów. Wewnątrz komórek stężenie rodnika tlenku azotu i anionorodnika ponadtlenkowego wynosi odpowiednio nm i 0,1 1 nm, co jest niewystarczające, aby mogła zajść synteza nadtlenoazotynu. Zupełnie odmienne warunki panują w pobliżu komórek generujących rodniki (np. komórki śródbłonka, aktywowane makrofagi, neutrofile), wtedy ich lokalne stężenie wzrasta aż do 1 10 µm [11]. Hydrofobowy tlenek azotu może przenikać swobodnie przez błony komórkowe, natomiast posiadający ładunek O 2 jest zdolny przemieszczać się jedynie poprzez kanały jonowe. Dlatego powstawanie nadtlenoazotynu w głównej mierze zależne jest od miejsca generowania anionorodnika ponadtlenkowego. Czas półtrwania nadtlenoazotynu w warunkach biologicznych wynosi nieco mniej niż 1 s. Czas ten jest jednak na tyle wystarczająco długi aby związek ten mógł przenikać przez błony komórkowe, dyfundując na odległość jednej do dwóch średnic komórkowych (~5 20 μm), co oznacza, że wytwarzany w jednej komórce może mieć wpływ na inne, sąsiadujące komórki [7, 12, 13]. Ponadto nadtlenoazotyn może przenikać przez błony biologiczne za pośrednictwem kanałów anionowych. ONOO znajduje się w stanie równowagi ze swoją uprotonowaną formą kwasem nadtlenoazotawym (ONOOH). W biologicznych warunkach stosunek ten zależny jest od lokalnego ph (w ph = 7,4 80% nadtlenoazotynu występować będzie w formie anionowej) [14]. Istnieje kilka laboratoryjnych metod syntezy nadtlenoazotynu. Związek ten można otrzymać w reakcji tlenku azotu z nadtlenkiem tetrametyloamonowym lub nadtlenkiem potasu, jak również poprzez fotolizę i radiolizę azotanu, utlenianie hydroksyloaminy oraz utlenianie organicznych azotanów [15]. Do badań chemicznych powszechnie wykorzystuje się metodę szybkiej reakcji azotynu z nadtlenkiem wodoru w kwaśnym ph, gdzie medium jest zakwaszane kwasem solnym, azotowym lub siarkowym, a następnie szybko uzasadawiane [16]. Ten rodzaj syntezy jest bardzo szybki, wydajny i niekłopotliwy do przeprowadzenia, jednak pewien problem stanowi pozostałość H 2 O 2 i efektywność jego usuwania z medium reakcyjnego. Do badań biologicznych powszechnie stosowaną jest metoda ozonowania roztworu azydku sodu opisana w 1995 roku przez Pryora i in. [17]. Metoda ta pozwala na uzyskiwanie preparatu nadtlenoazotynu o niskiej sile jonowej, bez zanieczyszczeń nadtlenkiem wodoru, ze śladową ilością pozostałego azydku i o stosunkowo wysokim stężeniu (do 80 mm). Nadtlenoazotyn, zaliczany do reaktywnych form azotu, nie jest wolnym rodnikiem. Niesparowane elektrony, które pochodzą od dwóch rodników tlenku azotu i anionorodnika ponadtlenkowego formują w cząsteczce ONOO nowe wiązanie [18]. Nadtlenoazotyn posiada dwa stany konformacyjne: cis i trans, a forma cis uważana jest za formę bardziej stabilną. Ma ona zdolność do przechodzenia w formę trans podczas rozpadu ONOO do azotanu [19].
6 628 M. BIJAK, M.B. PONCZEK, J. SALUK, M. CHABIELSKA, J. STĘPNIAK, P. NOWAK 2. PREKURSORY NADTLENOAZOTYNU W warunkach fizjologicznych pewna część O 2 (ok. 1 5%) ulega w mitochondrialnym łańcuchu oddechowym nie czteroelektronowej, a jednoelektronowej redukcji. W wyniku takiej redukcji powstaje anionorodnik ponadtlenkowy (O 2 ). Przemiana ta polega na przyłączeniu elektronu do cząsteczki tlenu i przekształceniu jej w wolny rodnik. Enzymami, które biorą udział w tej reakcji są dehydrogenaza NADH i koenzym Q [20]. Duże ilości O 2 są wytwarzane także przy udziale oksydazy NAD(P)H fagocytów, oksydazy ksantynowej czy lipooksygenazy 12/15 leukocytów enzymu odpowiadającego za powstawanie kwasu 12(S)-hydroksyeikozatetraenowego (12(S) HETE) oraz kwasu 15(S)-hydroksyeikozatetraenowego (15(S)HETE) [2]. Anionorodnik ponadtlenkowy może także powstawać podczas metabolizmu ksenobiotyków w mikrosomach, w reakcji utleniania ksantyny do kwasu moczowego katalizowanej przez oksydazę ksantynową przy udziale reduktazy NADPH i cytochromu P-450. W wyniku zachodzącej w erytrocytach autooksydacji hemoglobiny do methemoglobiny powstaje cząsteczek anionorodnika ponadtlenkowego w ciągu doby [21, 22]. Źródłem O 2 mogą także być płytki krwi, w których obecna jest jedna z izoform oksydazy NAD(P)H, a także oksydaza ksantynowa czy cyklooksygenaza [23]. Anionorodnik ponadtlenkowy może zachowywać się zarówno jako utleniacz jak i reduktor, w zależności od charakteru substancji z jaką reaguje. Niskie stężenie anionorodnika ponadtlenkowego utrzymywane jest w układach biologicznych przez dysmutazę ponadtlenkową (SOD), która obecna jest w mitochondriach, cytoplazmie i przestrzeni międzykomórkowej. Enzym ten powoduje przemianę O 2 w mniej szkodliwy nadtlenek wodoru, który następnie ulega rozkładowi przez katalazę i peroksydazę [18, 24]. Tlenek azotu w temperaturze pokojowej jest bezbarwnym, trującym gazem [25]. Posiada jeden niesparowany elektron na atomie tlenu, stąd jego niestabilność i wysoka reaktywność. W powietrzu samorzutnie reaguje z tlenem tworząc ditlenek azotu (NO 2 ). Czas półtrwania (t 1/2 ) cząsteczki NO wynosi 1 30 s [18, 24]. Tlenek azotu okazał się być bardzo ważną cząsteczką sygnałową w układach biologicznych. Furchgott i Zawadzki zaobserwowali w 1980 roku nieznany wcześniej czynnik rozszerzający naczynia krwionośne, który nazwali śródbłonkowym czynnikiem relaksującym (EDRF) [26]. Siedem lat później odkryto, że opisywany jako EDRF, czynnik rozszerzający naczynia krwionośne, to właśnie tlenek azotu [27]. Odkrycie faktu, że tlenku azotu jest cząsteczką powodującą rozluźnianie ściany naczyń krwionośnych zaowocowało w 1998 roku przyznania w Nobla z dziedziny medycyny i fizjologii trzem naukowcom (Furchgott, Ignarro, Murad). Tlenek azotu powstaje z L-argininy przy udziale syntazy tlenku azotu (E.C , ang. nitric oxide synthase, NOS) enzymu o aktywności NADPH-zależnej dioksygenazy wprowadzającej dwa atomy tlenu do cząsteczki L-argininy. Reakcja przebiega dwuetapowo, związkiem pośrednim jest N ω -hydroksy-l-arginina (NOH-L-Arg), a produk-
7 NADTLENOAZOTYN SILNY BIOLOGICZNY UTLENIACZ 629 tami końcowymi NO i L-cytrulina. Dodatkowo do zajścia reakcji konieczna jest obecność kofaktorów, tj.: FAD, FMN, tetrahydrobiopteryny oraz hemu [13, 28]. W ludzkim organizmie istnieją 3 izoformy syntazy tlenku azotu: neuronalna nnos (typ I), indukowalna inos (typ II) i endotelialna (śródbłonkowa) enos (typ III). Izoformy NOS różnią się między sobą masą cząsteczkową, strukturą, miejscem występowania w komórce oraz kinetyką reakcji. Neuronalna i endotelialna NOS uważane są za enzymy konstytutywne, a jako kafaktorów wymagają jonów wapnia i kalmoduliny. Indukowalna NOS ulega ekspresji w makrofagach, neutrofilach, komórkach śródbłonka, fibroblastach, mięśniach gładkich naczyń krwionośnych, miocytach oraz hepatocytach, w odpowiedzi na cytokiny lub inne czynniki zapalne. Jej aktywność nie zależy od poziomu jonów wapnia. inos wytwarza tlenek azotu w krotnie wyższych ilościach niż formy konstytutywne [18, 22]. Tlenek azotu produkowany w komórkach śródbłonka w wyniku działania różnych bodźców (stres, trombina, ADP, serotonina, bradykinina, histamina) powoduje rozszerzanie naczyń krwionośnych i reguluje ciśnienie krwi. NO hamuje nadmierną aktywację i agregację płytek krwi, co związane jest z jego działalnością przeciwzakrzepową i przeciwmiażdżycową. W mózgu i obwodowym układzie ner wowym, tlenek azotu pełni rolę neuroprzekaźnika. Uczestniczy on w procesie uczenia się i zapamiętywania, a także reguluje wydzielanie hormonów przysadki mózgowej [10, 29]. 3. REAKTYWNOŚĆ NADTLENOAZOTYNU Reakcje, w których uczestniczy nadtlenoazotyn można podzielić na: bezpośrednie reakcje redoks, reakcje z udziałem ditlenku węgla oraz reakcje związane z rozpadem sprzężonego z nadtlenoazotynem słabego kwasu ONOOH. W tych pierwszych nadtlenoazotyn bierze udział w reakcjach jedno- lub dwu-elektronowego utleniania. Reakcja CO 2 z nadtlenoazotynem zachodzi z dużą szybkością (k = 4, , M 1 s 1 ; ph = 7,4, temp. 37 C) [30]. W wyniku tej przemiany powstaje nietrwały produkt pośredni nitrozonadtlenowęglan (ONOOCO 2 ) (t 1/2 = 1 µs), który ulega homolitycznemu rozpadowi dając ditlenek azotu (NO 2 ) i rodnik węglanowy (CO 3 ). Nitrozonadtlenowęglan może ulegać także izomeryzacji do O 2 ONCO 2, a to prowadzi do odtworzenia ditlenku węgla oraz powstania azotanu (NO 3 ). Wtórne wolne rodniki (NO 2 i CO 3 ), które powstają w reakcji między ditlenkiem węgla a nadtlenoazotynem przyczyniają się do aż 4-krotnego zwiększenia potencjału nitrującego ONOO [31]. Wydajność tworzenia rodników podczas rozpadu ONOOCO 2 wydaje się być dyskusyjna. Większość autorów podaje, że addukt nadtlenoazotynu z CO 2 w około 65% rozpada się bezpośrednio do NO 3 i CO 2, natomiast w 35% do rodników CO 3 i NO 2 [7, 32, 33]. Trzeci rodzaj reakcji związany jest z powstawaniem rodnika hydroksylowego i rodnika ditlenku azotu podczas rozpadu kwasu nadtlenoazotawego [15]. Nadtlenoazotyn może ulegać protonacji (pk a = 6,8), dając kwas nadtlenoazotawy [34, 35].
8 630 M. BIJAK, M.B. PONCZEK, J. SALUK, M. CHABIELSKA, J. STĘPNIAK, P. NOWAK Uważa się, że cząsteczka ONOOH ulega homolizie z rozerwaniem wiązania O O tworząc parę rodników rodnik hydroksylowy ( OH) i ditlenek azotu ( NO 2 ) [7, 33, 36]. Wcześniej uważano, że ditlenek azotu obecny jest w organizmie jedynie po ekspozycji na dym papierosowy lub zanieczyszczenia powietrza [18]. Powstająca para rodnikowa OH/ NO 2 zamknięta jest w swoistej klatce, otoczonej cząsteczkami wody i może dyfundować na zewnątrz klatki (zachodzi to w ok. 30% przypadków) lub rekombinować bezpośrednio do NO 3 (takiej reakcji ulega około 70% par rodnikowych) [18, 33, 37]. Ze względu na wysokie stężenie ditlenku węgla w komórkach i płynach pozakomórkowych (1,3 1,5 mm, tj. około razy większe niż stężenie jonów wodorowych), jest on jednym z najważniejszych substratów dla nadtlenoazotynu [38]. Zatem najbardziej prawdopodobne jest, że nadtlenoazotyn w warunkach in vivo przereaguje właśnie z ditlenkiem węgla, niż ulegnie przekształceniu do HONOO, dając z kolei rodniki hydroksylowe. Rysunek 1. Figure 1. Reakcje nadtlenoazotynu Reaction of peroxynitrite 4. BIOLOGICZNE DZIAŁANIE NADTLENOAZOTYNU Nadtlenoazotyn jest czynnikiem o szerokim spektrum działania w stosunku do biomolekuł. Biologiczne skutki modyfikacji oksydacyjnych wywołanych przez ONOO są liczne, ale ważne jest, aby pamiętać, że w dużym stopniu zależą one od stężenia tworzonego nadtlenoazotynu i jego komórkowej lokalizacji. Związek
9 NADTLENOAZOTYN SILNY BIOLOGICZNY UTLENIACZ 631 ten i jego pochodne reagują zarówno z aminokwasami (m.in. tyrozyną, cysteiną, metioniną, tryptofanem), lipidami (fosfolipidy błon, lipoproteiny frakcji LDL), kwasami nukleinowymi, a także różnymi antyoksydantami. Nadtlenoazotyn powoduje tworzenie grup karbonylowych, dimeryzację, nitrowanie i nitrozylację aminokwasów, alkoholi, węglowodanów i związków tiolowych. Może działać jako jedno- lub dwuelektronowy utleniacz, z istotną rolą jonów metali przejściowych, spełniających funkcję katalizatorów. Jego aktywność, z jednej strony prowadzi do negatywnych następstw, takich jak utrata funkcji białek, a z drugiej, do powstawania związków będących donorami tlenku azotu, odgrywających rolę w rozkurczaniu naczyń krwionośnych [15]. Liczne badania dowodzą, że powstający w naczyniach krwionośnych nadtlenoazotyn jest zarówno silnym oksydantem jak i czynnikiem nitrującym. Modyfikacje białek spowodowane działaniem nadtlenoazotynu powodują zmiany w strukturze i funkcji tych biomolekuł, których występowanie stwierdzono w wielu stanach chorobowych [39]. Nadtlenoazotyn wywołuje nitrowanie reszt aminokwasów alifatycznych takich jak: cysteina, metionina oraz aminokwasów aromatycznych: tryptofan i tyrozyna. Najbardziej podatne na utlenianie są aminokwasy siarkowe (cysteina, metionina), a także tyrozyna, tryptofan, fenyloalanina i histydyna [40]. Działanie nadtlenoazotynu na białka ma bardzo istotne znaczenie w modulowaniu funkcjonowania enzymów. Szczególnie narażone na działanie ONOO są grupy prostetyczne zawierające jony metali przejściowych bądź hem. W wyniku ich utleniania dochodzi do zahamowania aktywności enzymatycznej m.in. mieloperoksydazy, ceruloplazminy, dysmutazy ponadtlenkowej [38]. Wolne rodniki powstające w wyniku homolizy nadtlenoazotynu, bądź podczas jego reakcji z CO 2 (NO 2, OH, NO 2, CO 3 ), również mają zdolność do oddziaływania z białkami, co prowadzi do ich modyfikacji. Utlenianie przez ONOO wolnych grup tiolowych prowadzi m.in. do zaburzenia funkcji enzymów zaangażowanych w metabolizm energetyczny komórki (dehydrogenazy bursztynianowej, reduktazy fumaranu) [10]. Szczególną uwagę należy zwrócić na udział nadtlenoazotynu w procesie nitrowania tyrozyny (Rys. 2). Nitrowanie tyrozyny prowadzi do kowalencyjnej modyfikacji białka w wyniku dodania grupy nitrowej (-NO 2 ) w sąsiedztwie grupy hydroksylowej w pierścieniu aromatycznym reszt tyrozynowych. Choć nadtlenoazotyn bezpośrednio nie może reagować z grupą fenolową, to produkty jego rozpadu rodnik hydroksylowy i ditlenek azotu wykazują taką aktywność. Dodatkowo, nietrwały nitrozonadtlenowęglan (ONOOCO 2 ), powstający w reakcji ONOO z CO 2, jest źródłem silnie reaktywnego rodnika węglanowego, który podobnie jak OH może powodować tworzenie rodników tyrozylowych reagujących dalej z NO 2. ONOOCO 2 ma czas półtrwania krótszy niż 3 ms i reaguje z tyrozyną ze stałą reakcji większą od M 1 s 1 [41, 42]. Rodniki CO 3 reagują z resztą tyrozyny poprzez oderwanie wodoru od grupy hydroksylowej, natomiast w odróżnieniu od rodników OH, nie przyłączają się do pierścienia aromatycznego. Dzięki temu, może powstawać więcej rodników tyrozylowych, oddziałujących następnie z NO 2 do postaci
10 632 M. BIJAK, M.B. PONCZEK, J. SALUK, M. CHABIELSKA, J. STĘPNIAK, P. NOWAK 3-nitrotyrozyny. Co prawda rodniki NO 2 również reagują z resztą tyrozyny poprzez oderwanie atomu wodoru z grupy hydroksylowej, jednak stała szybkości tej reakcji jest 2 3 rzędy wielkości mniejsza od stałej szybkości reakcji rodników OH czy CO 3 [43 45]. Wielu autorów uważa, że markerem działania nadtlenoazotynu w organizmie jest obecność znitrowanej tyrozyny w białkach. W osoczu osób zdrowych poziom 3-nitrotyrozyny jest stosunkowo niski (< 0,1 nmol/mg białka), ale znacząco wzrasta w przebiegu wielu chorób związanych z ostrym lub przewlekłym stanem zapalnym (posocznica, zespół ostrej niewydolności płuc, choroba niedokrwienna serca, chroniczna niewydolność nerek, reumatoidalne zapalenie stawów, cukrzyca, nowotwory płuc), a także u osób palących [46 49]. Rysunek 2. Figure 2. Powstawanie nitrotyrozyny i dityrozyny przy udziale nadtlenoazotynu Formation of nitrotyrosine and dityrosine by peroxynitrite Nadtlenoazotyn nie tylko silnie działa na tyrozynę, ale również na aminokwasy siarkowe (cysteinę i metioninę) [50]. W przypadku Cys ONOO jest odpowiedzialny za proces dwuelektronowego utleniania prowadzący do wytworzenia wiązań disiarczkowych, co może być ważnym mechanizmem inaktywacji wielu enzymów. W temperaturze pokojowej, w ph fizjologicznym nadtlenoazotyn utlenia grupy SH około 1000 razy szybciej niż nadtlenek wodoru. Reakcja ONOO z grupami tiolowymi przebiega z wytworzeniem produktów pośrednich, głównie S-nitrotioli
11 NADTLENOAZOTYN SILNY BIOLOGICZNY UTLENIACZ 633 (RSNO 2 ) oraz niewielkich ilości S-nitrozotioli (RSNO). Te drugie są ważnym składnikiem metabolizmu tlenku azotu i odgrywają istotną rolę w przekształcaniu toksycznego ONOO do tlenku azotu [51]. Metionina jest utleniana przez nadtlenoazotyn [52], jak również przez inne reaktywne formy tlenu, takie jak nadtlenek wodoru, ozon, kwas chlorowy(i), do sulfotlenku metioniny (MeSOX) i dalej do sulfonu metioniny (Me2SOX) (Rys. 3). In vivo działanie nadtlenoazotynu na metioninę ograniczone jest prawdopodobnie do dwuelektronowego utleniania jej do MeSOX. Powyższa reakcja zachodzi, jeśli w jej środowisku nie występuje ditlenek węgla. Utlenianie metioniny hamowane jest więc przez obecność ditlenku węgla, niezależnie od ph roztworu w przeciwieństwie do reakcji nitrowania tyrozyny. Nitrowanie tyrozyny i utlenianie metioniny, są zatem reakcjami konkurencyjnymi i zależą od dostępności ditlenku węgla [53, 54]. Rysunek 3. Figure 3. Proces wywołanego przez nadtlenoazotyn utleniania metioniny The process of peroxynitrite-induced oxidation of methionine Nadtlenoazotyn powoduje także modyfikację związków lipidowych: fosfolipidów błon, liposomów i lipoprotein [34]. Peroksydacja lipidów z udziałem ONOO polega na odłączeniu atomu wodoru od nienasyconych kwasów tłuszczowych. Nie jest przy tym wymagana obecność jonów metali przejściowych jako katalizatorów reakcji. Produktami utleniania lipidów są wodoronadtlenki lipidów, skoniugowane dieny i aldehydy. Produkty pośrednie peroksydacji (wodoronadtlenki lipidów, dialdehyd malonowy, izoprostany, 4-hydroksynonenal) mogą prowadzić do dalszych uszkodzeń oksydacyjnych w komórce. Utlenianie fosfolipidów oraz cholesterolu jest przyczyną zmian płynności i przepuszczalności błon komórkowych, co ma poważne konsekwencje dla prawidłowego funkcjonowania komórki. Utlenianie lipidów tworzących otoczkę mielinową neuronów prowadzi do demielinizacji i rozwoju chorób układu nerwowego [13, 18, 55]. Nitrowanie fosfolipidów błon wpływa na zaburzenie transdukcji sygnału w komórce [7]. Lipoproteiny o niskiej gęstości (LDL) są szczególnie podatne na utleniające i nitrujące działanie nadtlenoazotynu. Akumulacja utlenionego cholesterolu i LDL jest przyczyną rozwoju miażdżycy [56]. Nadtlenoazotyn jako silny związek utleniający i nitrujący jest w stanie wywoływać modyfikacje zasad azotowych. Spośród 4 zasad azotowych nukleotydów największą wrażliwość na jego toksyczne działanie wykazuje guanina. W wyniku
12 634 M. BIJAK, M.B. PONCZEK, J. SALUK, M. CHABIELSKA, J. STĘPNIAK, P. NOWAK jej utleniania powstaje 8-oksoguanina, która następnie może zostać przekształcona do kwasu cyjanurowego i oksazolonu. W konsekwencji dochodzi do rozerwania pierście nia imidazolowego guaniny i powstania trwałej mutacji. Nadtlenoazotyn powoduje również nitrowanie guaniny, czego produktem jest 8-nitroguanina, traktowana jako specyficzny marker uszkodzeń DNA wywołanych przez ONOO [57, 58]. Nadtlenoazotyn poprzez swoje toksyczne działanie przyczynia się do powstawania jedno- i dwuniciowych pęknięć DNA. W wyniku odłączenia atomu wodoru od deoksyrybozy dochodzi do rozerwania pierścienia cukrowego i przerwania nici DNA. Powstawanie jednoniciowych pęknięć DNA spowodowanych działaniem ONOO obserwuje się głównie w ph zasadowym, podczas gdy liczba uszkodzeń w ph kwaśnym i obojętnym jest dużo niższa. Jednoniciowe pęknięcia DNA powstające na skutek uszkadzającego wpływu nadtlenoazotynu mogą nadmiernie aktywować jądrowy enzym polimerazę poli(adp-rybozy) (PARP), co w konsekwencji prowadzi do nekrotycznej śmierci komórki w warunkach stresu oksydacyjnego [59 61]. PIŚMIENNICTWO CYTOWANE [1] E.R. Stadtman, R.L. Levine, Ann. N. Y. Acad. Sci., 2000, 899, 191. [2] N.R. Madamanchi, A. Vendrov, M.S. Runge, Arterioscler. Thromb. Vasc. Biol, 2005, 25, 29. [3] K.K. Griendling, G.A. FitzGerald, Circulation, 2003, 108, [4] R. Radi, Proc. Natl. Acad. Sci. U.S.A, 2004, 101, [5] H. Ischiropoulos, L. Zhu, J.S. Beckman, Arch. Biochem. Biophys., 1992, 298, 446. [6] D. Salvemini, S. Cuzzocrea, Free Radic. Biol. Med., 2002, 33, [7] C. Szabo, H. Ischiropoulos, R. Radi, Nat. Rev. Drug Discov., 2007, 6, 662. [8] J.S. Beckman, T.W. Beckman, J. Chen, P.A. Marshall, B.A. Freeman, Proc. Natl. Acad. Sci. U.S.A, 1990, 87, [9] P.C. Dedon, S.R. Tannenbaum, Arch. Biochem. Biophys., 2004, 423, 12. [10] J.P. Kamat, Indian J. Exp. Biol, 2006, 44, 436. [11] J.T. Groves, Curr. Opin. Chem. Biol, 1999, 3, 226. [12] L. Liaudet, G. Vassalli, P. Pacher, Front Biosci., 2009, 14, [13] A. Denicola, R. Radi, Toxicology, 2005, 208, 273. [14] R. Radi, G. Peluffo, M.N. Alvarez, M. Naviliat, A. Cayota, Free Radic. Biol. Med., 2001, 30, 463. [15] C. Ducrocq, B. Blanchard, B. Pignatelli, H. Ohshima, Cell Mol.Life Sci., 1999, 55, [16] J.S. Beckman, J. Chen, H. Ischiropoulos, J.P. Crow, Methods Enzymol., 1994, 233, 229. [17] W.A. Pryor, G.L. Squadrito, Am. J. Physiol, 1995, 268, 699. [18] P. Pacher, J.S. Beckman, L. Liaudet, Physiol. Rev., 2007, 87, 315. [19] M.C. Symons, J. Inorg. Biochem., 2000, 78, 299. [20] E. Potargowicz, E. Szerszenowicz, M. Staniszewska, D. Nowak, Postepy Hig. Med. Dosw., 2005, 59, 259. [21] A. Gendzwill, Pol. Merkur. Lekarski, 2007, 23, 280. [22] R. Rutkowski, S.A. Pancewicz, K. Rutkowski, J. Rutkowska, Pol. Merkur. Lekarski, 2007, 23, 131. [23] F. Krotz, H.Y. Sohn, U. Pohl, Arterioscler. Thromb. Vasc. Biol, 2004, 24, [24] R.P. Patel, J. McAndrew, H. Sellak, C.R. White, H. Jo, B.A. Freeman, V.M. Darley-Usmar, Biochim. Biophys. Acta, 1999, 1411, 385. [25] H. Puzanowska-Tarasiewicz, L. Kuzmicka, M. Tarasiewicz, Pol. Merkur. Lekarski, 2009, 27, 338.
13 NADTLENOAZOTYN SILNY BIOLOGICZNY UTLENIACZ 635 [26] R.F. Furchgott, J.V. Zawadzki, Nature, 1980, 288, 373. [27] R.M. Palmer, A.G. Ferrige, S. Moncada, Nature, 1987, 327, 524. [28] M.C. Carreras, J.J. Poderoso, Am. J. Physiol. Cell Physiol., 2007, 292, [29] M. Mielczarek-Puta, A. Chrzanowska, W. Grabon, A. Baranczyk-Kuzma, Postepy Hig. Med. Dosw., 2008, 62, 214. [30] B. Alvarez, R. Radi, Amino. Acids, 2003, 25, 295. [31] R. Meli, T. Nauser, P. Latal, W.H. Koppenol, J. Biol. Inorg. Chem., 2002, 7, 31. [32] O. Augusto, M.G. Bonini, A.M. Amanso, E. Linares, C.C. Santos, S.L. De Menezes, Free Radic. Biol. Med., 2002, 32, 841. [33] J. Zielonka, A. Sikora, J. Joseph, B. Kalyanaraman, J. Biol. Chem., 2010, 285, [34] R. Radi, J.S. Beckman, K.M. Bush, B.A. Freeman, Arch. Biochem. Biophys., 1991, 288, 481. [35] H. Gunaydin, K.N. Houk, Chem. Res. Toxicol., 2009, 22, 894. [36] M.P. Jensen, D.P. Riley, Inorg. Chem., 2002, 41, [37] A. Korkmaz, S. Oter, M. Seyrek, T. Topal, Interdiscip. Toxicol., 2009, 2, 219. [38] G. Ferrer-Sueta, R. Radi, ACS Chem. Biol, 2009, 4, 161. [39] P. Nowak, B. Olas, B. Wachowicz, Postepy Biochem., 2010, 56, 239. [40] C. Szabo, Toxicol. Lett., 2003, , 105. [41] S.V. Lymar, Q. Jiang, J.K. Hurst, Biochemistry, 1996, 35, [42] S. Zhu, K.F. Basiouny, J.P. Crow, S. Matalon, Am. J. Physiol. Lung. Cell Mol. Physiol, 2000, 278, [43] J.M. Souza, G. Peluffo, R. Radi, Free Radic. Biol. Med., 2008, 45, 357. [44] L. Gebicka, J. Didik, Postępy Biochem., 2010, 56, 103. [45] S. Bartesaghi, G. Ferrer-Sueta, G. Peluffo, V. Valez, H. Zhang, B. Kalyanaraman, R. Radi, Amino. Acids, 2007, 32, 501. [46] C. Vadseth, J.M. Souza, L. Thomson, A. Seagraves, C. Nagaswami, T. Scheiner, J. Torbet, G. Vilaire, J.S. Bennett, J.C. Murciano, V. Muzykantov, M.S. Penn, S.L. Hazen, J.W. Weisel, H. Ischiropoulos, J. Biol. Chem., 2004, 279, [47] B. Pignatelli, C.Q. Li, P. Boffetta, Q. Chen, W. Ahrens, F. Nyberg, A. Mukeria, I. Bruske-Hohlfeld, C. Fortes, V. Constantinescu, H. Ischiropoulos, H. Ohshima, Cancer Res., 2001, 61, 778. [48] N.W. Kooy, J.A. Royall, Y.Z. Ye, D.R. Kelly, J.S. Beckman, Am. J. Respir. Crit. Care Med., 1995, 151, [49] B. Lipinski, J. Diabetes Complications, 2001, 15, 203. [50] B. Alvarez, G. Ferrer-Sueta, B.A. Freeman, R. Radi, J. Biol. Chem., 1999, 274, 842. [51] A. van der Vliet, P.A. Hoen, P.S. Wong, A. Bast, C.E. Cross, J. Biol. Chem., 1998, 273, [52] W.A. Pryor, X. Jin, G.L. Squadrito, Proc. Natl. Acad. Sci. U.S.A, 1994, 91, [53] B.S. Berlett, R.L. Levine, E.R. Stadtman, Proc. Natl. Acad. Sci. U.S.A, 1998, 95, [54] M. Tien, B.S. Berlett, R.L. Levine, P.B. Chock, E.R. Stadtman, Proc. Natl. Acad. Sci. U.S.A, 1999, 96, [55] R.G. Brannan, E.A. Decker, J. Agric. Food Chem., 2001, 49, [56] H. Botti, A. Trostchansky, C. Batthyany, H. Rubbo, IUBMB. Life, 2005, 57, 407. [57] T. Douki, J. Cadet, Free Radic. Res., 1996, 24, 369. [58] V. Yermilov, J. Rubio, H. Ohshima, FEBS Lett., 1995, 376, 207. [59] H. Ohshima, L. Virag, J. Souza, V. Yermilov, B. Pignatelli, M. Masuda, C. Szabo, Methods Mol. Biol, 2002, 186, 77. [60] C. Szabo, H. Ohshima, Nitric. Oxide., 1997, 1, 373. [61] C. Szabo, Free Radic. Biol. Med., 1996, 21, 855. Praca wpłynęła do Redakcji 26 kwietnia 2012
Antyoksydanty pokarmowe a korzyści zdrowotne. dr hab. Agata Wawrzyniak, prof. SGGW Katedra Żywienia Człowieka SGGW
 Antyoksydanty pokarmowe a korzyści zdrowotne dr hab. Agata Wawrzyniak, prof. SGGW Katedra Żywienia Człowieka SGGW Warszawa, dn. 14.12.2016 wolne rodniki uszkodzone cząsteczki chemiczne w postaci wysoce
Antyoksydanty pokarmowe a korzyści zdrowotne dr hab. Agata Wawrzyniak, prof. SGGW Katedra Żywienia Człowieka SGGW Warszawa, dn. 14.12.2016 wolne rodniki uszkodzone cząsteczki chemiczne w postaci wysoce
Wolne rodniki w komórkach SYLABUS A. Informacje ogólne
 Wolne rodniki w komórkach A. Informacje ogólne Elementy sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Rodzaj Rok studiów /semestr
Wolne rodniki w komórkach A. Informacje ogólne Elementy sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Rodzaj Rok studiów /semestr
Do moich badań wybrałam przede wszystkim linię kostniakomięsaka 143B ze względu na jej wysoki potencjał przerzutowania. Do wykonania pracy
 Streszczenie Choroby nowotworowe stanowią bardzo ważny problem zdrowotny na świecie. Dlatego, medycyna dąży do znalezienia nowych skutecznych leków, ale również rozwiązań do walki z nowotworami. Głównym
Streszczenie Choroby nowotworowe stanowią bardzo ważny problem zdrowotny na świecie. Dlatego, medycyna dąży do znalezienia nowych skutecznych leków, ale również rozwiązań do walki z nowotworami. Głównym
Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD
 Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD Aleksandra Kotynia PRACA DOKTORSKA
Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD Aleksandra Kotynia PRACA DOKTORSKA
STRES OKSYDACYJNY WYSIŁKU FIZYCZNYM
 Agnieszka Zembroń-Łacny Joanna Ostapiuk-Karolczuk STRES OKSYDACYJNY W WYSIŁKU FIZYCZNYM STRES OKSYDACYJNY zaburzenie równowagi między wytwarzaniem a usuwaniem/redukcją reaktywnych form tlenu i azotu RONS
Agnieszka Zembroń-Łacny Joanna Ostapiuk-Karolczuk STRES OKSYDACYJNY W WYSIŁKU FIZYCZNYM STRES OKSYDACYJNY zaburzenie równowagi między wytwarzaniem a usuwaniem/redukcją reaktywnych form tlenu i azotu RONS
CHARAKTERYSTYKI SPEKTRALNE UTLENIONEJ I ZREDUKOWANEJ FORMY CYTOCHROMU C
 Ćwiczenie 4 CHARAKTERYSTYKI SPEKTRALNE UTLENIONEJ I ZREDUKOWANEJ FORMY CYTOCHROMU C REAKTYWNE FORMY TLENU DEGRADACJA NUKLEOTYDÓW PURYNOWYCH TWORZENIE ANIONORODNIKA PONADTLENKOWEGO W REAKCJI KATALIZOWANEJ
Ćwiczenie 4 CHARAKTERYSTYKI SPEKTRALNE UTLENIONEJ I ZREDUKOWANEJ FORMY CYTOCHROMU C REAKTYWNE FORMY TLENU DEGRADACJA NUKLEOTYDÓW PURYNOWYCH TWORZENIE ANIONORODNIKA PONADTLENKOWEGO W REAKCJI KATALIZOWANEJ
Nukleotydy w układach biologicznych
 Nukleotydy w układach biologicznych Schemat 1. Dinukleotyd nikotynoamidoadeninowy Schemat 2. Dinukleotyd NADP + Dinukleotydy NAD +, NADP + i FAD uczestniczą w procesach biochemicznych, w trakcie których
Nukleotydy w układach biologicznych Schemat 1. Dinukleotyd nikotynoamidoadeninowy Schemat 2. Dinukleotyd NADP + Dinukleotydy NAD +, NADP + i FAD uczestniczą w procesach biochemicznych, w trakcie których
Wolne rodniki :WR. O 2 - tlen singletowy NO - tlenek azotu. HO 2 - rodnik wodoronadtlenkowy H 2 O 2 - nadtlenek wodoru O 2 anionorodnik ponadtlenkowy
 Wolne rodniki :WR ROS = RFT RNS= RFA 1 O 2 - tlen singletowy NO - tlenek azotu O 3 - ozon OH- rodnik hydroksylowy HO 2 - rodnik wodoronadtlenkowy H 2 O 2 - nadtlenek wodoru O 2 anionorodnik ponadtlenkowy
Wolne rodniki :WR ROS = RFT RNS= RFA 1 O 2 - tlen singletowy NO - tlenek azotu O 3 - ozon OH- rodnik hydroksylowy HO 2 - rodnik wodoronadtlenkowy H 2 O 2 - nadtlenek wodoru O 2 anionorodnik ponadtlenkowy
Przemiana materii i energii - Biologia.net.pl
 Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Ćwiczenie nr 5 - Reaktywne formy tlenu
 Ćwiczenie nr 5 - Reaktywne formy tlenu I. Oznaczenie ilościowe glutationu (GSH) metodą Ellmana II. Pomiar całkowitej zdolności antyoksydacyjnej substancji metodą redukcji rodnika DPPH Celem ćwiczeń jest:
Ćwiczenie nr 5 - Reaktywne formy tlenu I. Oznaczenie ilościowe glutationu (GSH) metodą Ellmana II. Pomiar całkowitej zdolności antyoksydacyjnej substancji metodą redukcji rodnika DPPH Celem ćwiczeń jest:
Biochemia zadymionych komórek
 Biochemia zadymionych komórek Dariusz Latowski Uniwersytet Jagielloński Wydział Biochemii, Biofizyki i Biotechnologii Zakład Fizjologii i Biochemii Roślin Biochemia zadymionych komórek hemia życia zadymionych
Biochemia zadymionych komórek Dariusz Latowski Uniwersytet Jagielloński Wydział Biochemii, Biofizyki i Biotechnologii Zakład Fizjologii i Biochemii Roślin Biochemia zadymionych komórek hemia życia zadymionych
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Bliskie spotkania z biologią METABOLIZM. dr hab. Joanna Moraczewska, prof. UKW. Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki
 Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
CHEMIA. Wymagania szczegółowe. Wymagania ogólne
 CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
Układ pracy. Wstęp i cel pracy. Wyniki. 1. Ekspresja i supresja Peroksyredoksyny III w stabilnie transfekowanej. linii komórkowej RINm5F
 The influence of an altered Prx III-expression to RINm5F cells Marta Michalska Praca magisterska wykonana W Zakładzie Medycyny Molekularnej Katedry Biochemii Klinicznej Akademii Medycznej w Gdańsku Przy
The influence of an altered Prx III-expression to RINm5F cells Marta Michalska Praca magisterska wykonana W Zakładzie Medycyny Molekularnej Katedry Biochemii Klinicznej Akademii Medycznej w Gdańsku Przy
Transport przez błony
 Transport przez błony Transport bierny Nie wymaga nakładu energii Transport aktywny Wymaga nakładu energii Dyfuzja prosta Dyfuzja ułatwiona Przenośniki Kanały jonowe Transport przez pory w błonie jądrowej
Transport przez błony Transport bierny Nie wymaga nakładu energii Transport aktywny Wymaga nakładu energii Dyfuzja prosta Dyfuzja ułatwiona Przenośniki Kanały jonowe Transport przez pory w błonie jądrowej
SEMINARIUM 8:
 SEMINARIUM 8: 24.11. 2016 Mikroelementy i pierwiastki śladowe, definicje, udział w metabolizmie ustroju reakcje biochemiczne zależne od aktywacji/inhibicji przy udziale mikroelementów i pierwiastków śladowych,
SEMINARIUM 8: 24.11. 2016 Mikroelementy i pierwiastki śladowe, definicje, udział w metabolizmie ustroju reakcje biochemiczne zależne od aktywacji/inhibicji przy udziale mikroelementów i pierwiastków śladowych,
Mechanizmy działania i regulacji enzymów
 Mechanizmy działania i regulacji enzymów Enzymy: są katalizatorami, które zmieniają szybkość reakcji, same nie ulegając zmianie są wysoce specyficzne ich aktywność może być regulowana m.in. przez modyfikacje
Mechanizmy działania i regulacji enzymów Enzymy: są katalizatorami, które zmieniają szybkość reakcji, same nie ulegając zmianie są wysoce specyficzne ich aktywność może być regulowana m.in. przez modyfikacje
Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko. Syllabus przedmiotowy 2016/ /2019
 Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko Syllabus przedmiotowy 2016/2017-2018/2019 Wydział Fizjoterapii Kierunek studiów Fizjoterapia Specjalność ----------- Forma studiów Stacjonarne / Niestacjonarne
Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko Syllabus przedmiotowy 2016/2017-2018/2019 Wydział Fizjoterapii Kierunek studiów Fizjoterapia Specjalność ----------- Forma studiów Stacjonarne / Niestacjonarne
TIENS L-Karnityna Plus
 TIENS L-Karnityna Plus Zawartość jednej kapsułki Winian L-Karnityny w proszku 400 mg L-Arginina 100 mg Niacyna (witamina PP) 16 mg Witamina B6 (pirydoksyna) 2.1 mg Stearynian magnezu pochodzenia roślinnego
TIENS L-Karnityna Plus Zawartość jednej kapsułki Winian L-Karnityny w proszku 400 mg L-Arginina 100 mg Niacyna (witamina PP) 16 mg Witamina B6 (pirydoksyna) 2.1 mg Stearynian magnezu pochodzenia roślinnego
Cukry. C x H 2y O y lub C x (H 2 O) y
 Cukry Cukry organiczne związki chemiczne składające się z atomów węgla oraz wodoru i tlenu, zazwyczaj w stosunku H:O = 2:1. Zawierają liczne grupy hydroksylowe, karbonylowe a czasami mostki półacetalowe.
Cukry Cukry organiczne związki chemiczne składające się z atomów węgla oraz wodoru i tlenu, zazwyczaj w stosunku H:O = 2:1. Zawierają liczne grupy hydroksylowe, karbonylowe a czasami mostki półacetalowe.
Metabolizm białek. Ogólny schemat metabolizmu bialek
 Metabolizm białek Ogólny schemat metabolizmu bialek Trawienie białek i absorpcja aminokwasów w przewodzie pokarmowym w żołądku (niskie ph ~2, rola HCl)- hydratacja, homogenizacja, denaturacja białek i
Metabolizm białek Ogólny schemat metabolizmu bialek Trawienie białek i absorpcja aminokwasów w przewodzie pokarmowym w żołądku (niskie ph ~2, rola HCl)- hydratacja, homogenizacja, denaturacja białek i
Kryteria oceniania z chemii kl VII
 Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Bliskie spotkania z biologią. METABOLIZM część II. dr hab. Joanna Moraczewska, prof. UKW
 Bliskie spotkania z biologią METABOLIZM część II dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki METABOLIZM KATABOLIZM - rozkład związków chemicznych
Bliskie spotkania z biologią METABOLIZM część II dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki METABOLIZM KATABOLIZM - rozkład związków chemicznych
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA
 SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
Reakcje zachodzące w komórkach
 Reakcje zachodzące w komórkach W każdej sekundzie we wszystkich organizmach żywych zachodzi niezliczona ilość reakcji metabolicznych. Metabolizm (gr. metabole - przemiana) to przemiany materii i energii
Reakcje zachodzące w komórkach W każdej sekundzie we wszystkich organizmach żywych zachodzi niezliczona ilość reakcji metabolicznych. Metabolizm (gr. metabole - przemiana) to przemiany materii i energii
Oddychanie komórkowe. Pozyskiwanie i przetwarzanie energii w komórkach roślinnych. Oddychanie zachodzi w mitochondriach Wykład 7.
 Wykład 7. Pozyskiwanie i przetwarzanie energii w komórkach roślinnych Literatura dodatkowa: Oddychanie to wielostopniowy proces utleniania substratów związany z wytwarzaniem w komórce metabolicznie użytecznej
Wykład 7. Pozyskiwanie i przetwarzanie energii w komórkach roślinnych Literatura dodatkowa: Oddychanie to wielostopniowy proces utleniania substratów związany z wytwarzaniem w komórce metabolicznie użytecznej
Ćwiczenie VII. Reaktywne formy tlenu (RFT)
 Ćwiczenie VII Reaktywne formy tlenu (RFT) (1) Porównanie widm absorpcyjnych utlenionej i zredukowanej formy cytochromu c (2) Wytwarzanie i usuwanie anionorodnika ponadtlenkowego ZAGADIEIA D PRZYGTWAIA:
Ćwiczenie VII Reaktywne formy tlenu (RFT) (1) Porównanie widm absorpcyjnych utlenionej i zredukowanej formy cytochromu c (2) Wytwarzanie i usuwanie anionorodnika ponadtlenkowego ZAGADIEIA D PRZYGTWAIA:
PRZEWODNIK DYDAKTYCZNY PRZEDMIOTU
 PRZEWODNIK DYDAKTYCZNY PRZEDMIOTU (SYLABUS) NAZWA JEDNOSTKI PROWADZĄCEJ KIERUNEK: Zakład Biologii Molekularnej NAZWA KIERUNKU: Biotechnologia PROFIL KSZTAŁCENIA: ogólnoakademicki SPECJALNOŚĆ: Biotechnologia
PRZEWODNIK DYDAKTYCZNY PRZEDMIOTU (SYLABUS) NAZWA JEDNOSTKI PROWADZĄCEJ KIERUNEK: Zakład Biologii Molekularnej NAZWA KIERUNKU: Biotechnologia PROFIL KSZTAŁCENIA: ogólnoakademicki SPECJALNOŚĆ: Biotechnologia
Źródła energii dla mięśni. mgr. Joanna Misiorowska
 Źródła energii dla mięśni mgr. Joanna Misiorowska Skąd ta energia? Skurcz włókna mięśniowego wymaga nakładu energii w postaci ATP W zależności od czasu pracy mięśni, ATP może być uzyskiwany z różnych źródeł
Źródła energii dla mięśni mgr. Joanna Misiorowska Skąd ta energia? Skurcz włókna mięśniowego wymaga nakładu energii w postaci ATP W zależności od czasu pracy mięśni, ATP może być uzyskiwany z różnych źródeł
ROLA WAPNIA W FIZJOLOGII KOMÓRKI
 ROLA WAPNIA W FIZJOLOGII KOMÓRKI Michał M. Dyzma PLAN REFERATU Historia badań nad wapniem Domeny białek wiążące wapń Homeostaza wapniowa w komórce Komórkowe rezerwuary wapnia Białka buforujące Pompy wapniowe
ROLA WAPNIA W FIZJOLOGII KOMÓRKI Michał M. Dyzma PLAN REFERATU Historia badań nad wapniem Domeny białek wiążące wapń Homeostaza wapniowa w komórce Komórkowe rezerwuary wapnia Białka buforujące Pompy wapniowe
Ćwiczenie 4. Reakcja aminokwasów z ninhydryną. Opisz typy reakcji przebiegających w tym procesie i zaznacz ich miejsca przebiegu.
 azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 01/1 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 01/1 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Ważne pojęcia. Stopień utlenienia. Utleniacz. Reduktor. Utlenianie (dezelektronacja)
 Ważne pojęcia Stopień utlenienia Utleniacz Reduktor Utlenianie (dezelektronacja) Stopień utlenienia pierwiastka w dowolnym połączeniu chemicznym jest pojęciem umownym i określa ładunek, który istniałby
Ważne pojęcia Stopień utlenienia Utleniacz Reduktor Utlenianie (dezelektronacja) Stopień utlenienia pierwiastka w dowolnym połączeniu chemicznym jest pojęciem umownym i określa ładunek, który istniałby
Program zajęć z biochemii dla studentów kierunku weterynaria I roku studiów na Wydziale Lekarskim UJ CM w roku akademickim 2013/2014
 Program zajęć z biochemii dla studentów kierunku weterynaria I roku studiów na Wydziale Lekarskim UJ CM w roku akademickim 2013/2014 S E M E S T R II Tydzień 1 24.02-28.02 2 03.03-07.03 3 10.03-14.03 Wykłady
Program zajęć z biochemii dla studentów kierunku weterynaria I roku studiów na Wydziale Lekarskim UJ CM w roku akademickim 2013/2014 S E M E S T R II Tydzień 1 24.02-28.02 2 03.03-07.03 3 10.03-14.03 Wykłady
Biochemia Oddychanie wewnątrzkomórkowe
 Państwowa Wyższa Szkoła Zawodowa w Krośnie Biochemia Oddychanie wewnątrzkomórkowe Dr n. biol. Henryk Różański Laboratorium Biologii Przemysłowej i Eksperymentalnej Oddychanie Glikoliza beztlenowy, wewnątrzkomórkowy
Państwowa Wyższa Szkoła Zawodowa w Krośnie Biochemia Oddychanie wewnątrzkomórkowe Dr n. biol. Henryk Różański Laboratorium Biologii Przemysłowej i Eksperymentalnej Oddychanie Glikoliza beztlenowy, wewnątrzkomórkowy
ORP - jeden z parametrów określających jakość wody
 ORP - jeden z parametrów określających jakość wody Woda wodzie nierówna. I choć na pierwszy rzut oka nie widać różnicy między wodą mineralną, z kranu czy jonizowaną, to nie pozostaje to bez znaczenia dla
ORP - jeden z parametrów określających jakość wody Woda wodzie nierówna. I choć na pierwszy rzut oka nie widać różnicy między wodą mineralną, z kranu czy jonizowaną, to nie pozostaje to bez znaczenia dla
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Enzymy katalizatory biologiczne
 Enzymy katalizatory biologiczne Kataliza zjawisko polegające na obniżeniu energii aktywacji reakcji i zwiększeniu szybkości reakcji chemicznej i/lub skierowaniu reakcji na jedną z termodynamicznie możliwych
Enzymy katalizatory biologiczne Kataliza zjawisko polegające na obniżeniu energii aktywacji reakcji i zwiększeniu szybkości reakcji chemicznej i/lub skierowaniu reakcji na jedną z termodynamicznie możliwych
Aminotransferazy. Dehydrogenaza glutaminianowa. Szczawiooctan. Argininobursztynian. Inne aminokwasy. asparaginian. fumaran. Arginina.
 Inne aminokwasy Szczawiooctan Aminotransferazy asparaginian Cytrulina Argininobursztynian Cykl mocznikowy Arginina fumaran Ornityna Aminotransferazy -ketoglutaran karbamoilofosforan Mocznik kwas glutaminowy
Inne aminokwasy Szczawiooctan Aminotransferazy asparaginian Cytrulina Argininobursztynian Cykl mocznikowy Arginina fumaran Ornityna Aminotransferazy -ketoglutaran karbamoilofosforan Mocznik kwas glutaminowy
Reaktywne formy tlenu. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Reaktywne formy tlenu Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Tlen pierwiastek chorób i śmierci Negatywne działanie tlenu na organizm ludzki: uszkodzenie płuc prowadzące do ich zwłóknienia:
Reaktywne formy tlenu Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Tlen pierwiastek chorób i śmierci Negatywne działanie tlenu na organizm ludzki: uszkodzenie płuc prowadzące do ich zwłóknienia:
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Uniwersytet Łódzki, Instytut Biochemii
 Życie jest procesem chemicznym. Jego podstawą są dwa rodzaje cząsteczek kwasy nukleinowe, jako nośniki informacji oraz białka, które tę informację wyrażają w postaci struktury i funkcji komórek. http://www.nobelprize.org/nobel_prizes/medicine/laureates/1959/press.html?print=1
Życie jest procesem chemicznym. Jego podstawą są dwa rodzaje cząsteczek kwasy nukleinowe, jako nośniki informacji oraz białka, które tę informację wyrażają w postaci struktury i funkcji komórek. http://www.nobelprize.org/nobel_prizes/medicine/laureates/1959/press.html?print=1
Wykazanie obecności oksydoreduktaz w materiale biologicznym
 KATEDRA BIOCHEMII Wydział Biologii i Ochrony Środowiska Wykazanie obecności oksydoreduktaz w materiale biologicznym ĆWICZENIE 9 ZADANIE 1 OTRZYMYWANIE PREPARATU ENZYMATYCZNEGO 1. Umyty ziemniak utrzeć
KATEDRA BIOCHEMII Wydział Biologii i Ochrony Środowiska Wykazanie obecności oksydoreduktaz w materiale biologicznym ĆWICZENIE 9 ZADANIE 1 OTRZYMYWANIE PREPARATU ENZYMATYCZNEGO 1. Umyty ziemniak utrzeć
CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A. imię i nazwisko :. klasa :.. ilość punktów :.
 CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A imię i nazwisko :. klasa :.. ilość punktów :. Zadanie 1 Przeanalizuj schemat i wykonaj polecenia. a. Wymień cztery struktury występujące zarówno w komórce roślinnej,
CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A imię i nazwisko :. klasa :.. ilość punktów :. Zadanie 1 Przeanalizuj schemat i wykonaj polecenia. a. Wymień cztery struktury występujące zarówno w komórce roślinnej,
Beata Mendak fakultety z chemii II tura PYTANIA Z KLASY PIERWSZEJ
 Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Informacje. W sprawach organizacyjnych Slajdy z wykładów
 Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Równowaga kwasowo-zasadowa. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowaga kwasowozasadowa Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Krytyka pojęcia ph ph = log [H + ] ph [H+] 1 100 mmol/l D = 90 mmol/l 2 10 mmol/l D = 9 mmol/l 3 1 mmol/l 2 Krytyka pojęcia
Równowaga kwasowozasadowa Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Krytyka pojęcia ph ph = log [H + ] ph [H+] 1 100 mmol/l D = 90 mmol/l 2 10 mmol/l D = 9 mmol/l 3 1 mmol/l 2 Krytyka pojęcia
TYPY REAKCJI CHEMICZNYCH
 1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
11. Związki heterocykliczne w codziennym życiu
 11. Związki heterocykliczne w codziennym życiu a podstawie: J. A. Joule, K. Mills eterocyclic chemistry at a glace, 2nd ed., Wiley 2013. S. Rolski Chemia środków leczniczych, wyd. III, PZWL 1968. Związki
11. Związki heterocykliczne w codziennym życiu a podstawie: J. A. Joule, K. Mills eterocyclic chemistry at a glace, 2nd ed., Wiley 2013. S. Rolski Chemia środków leczniczych, wyd. III, PZWL 1968. Związki
CHOLESTONE NATURALNA OCHRONA PRZED MIAŻDŻYCĄ. www.california-fitness.pl www.calivita.com
 CHOLESTONE NATURALNA OCHRONA PRZED MIAŻDŻYCĄ Co to jest cholesterol? Nierozpuszczalna w wodzie substancja, która: jest składnikiem strukturalnym wszystkich błon komórkowych i śródkomórkowych wchodzi w
CHOLESTONE NATURALNA OCHRONA PRZED MIAŻDŻYCĄ Co to jest cholesterol? Nierozpuszczalna w wodzie substancja, która: jest składnikiem strukturalnym wszystkich błon komórkowych i śródkomórkowych wchodzi w
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Chemiczne składniki komórek
 Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
WYBRANE SKŁADNIKI POKARMOWE A GENY
 WYBRANE SKŁADNIKI POKARMOWE A GENY d r i n ż. Magdalena Górnicka Zakład Oceny Żywienia Katedra Żywienia Człowieka WitaminyA, E i C oraz karotenoidy Selen Flawonoidy AKRYLOAMID Powstaje podczas przetwarzania
WYBRANE SKŁADNIKI POKARMOWE A GENY d r i n ż. Magdalena Górnicka Zakład Oceny Żywienia Katedra Żywienia Człowieka WitaminyA, E i C oraz karotenoidy Selen Flawonoidy AKRYLOAMID Powstaje podczas przetwarzania
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
Poznań, dnia 28 maja 2018
 Wydział Chemii Prof. dr hab. Bronisław Marciniak Zakład Fizyki Chemicznej ul. Umultowska 89b 60-780 Poznań marcinia@amu.edu.pl Poznań, dnia 28 maja 2018 Recenzja rozprawy doktorskiej mgr inż. Ewy Gapys
Wydział Chemii Prof. dr hab. Bronisław Marciniak Zakład Fizyki Chemicznej ul. Umultowska 89b 60-780 Poznań marcinia@amu.edu.pl Poznań, dnia 28 maja 2018 Recenzja rozprawy doktorskiej mgr inż. Ewy Gapys
Obliczenia stechiometryczne, bilansowanie równań reakcji redoks
 Obliczenia stechiometryczne, bilansowanie równań reakcji redoks Materiały pomocnicze do zajęć wspomagających z chemii opracował: dr Błażej Gierczyk Wydział Chemii UAM Obliczenia stechiometryczne Podstawą
Obliczenia stechiometryczne, bilansowanie równań reakcji redoks Materiały pomocnicze do zajęć wspomagających z chemii opracował: dr Błażej Gierczyk Wydział Chemii UAM Obliczenia stechiometryczne Podstawą
Co może zniszczyć nerki? Jak żyć, aby je chronić?
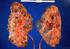 Co może zniszczyć nerki? Jak żyć, aby je chronić? Co zawdzięczamy nerkom? Działanie nerki można sprowadzić do działania jej podstawowego elementu funkcjonalnego, czyli nefronu. Pod wpływem ciśnienia hydrostatycznego
Co może zniszczyć nerki? Jak żyć, aby je chronić? Co zawdzięczamy nerkom? Działanie nerki można sprowadzić do działania jej podstawowego elementu funkcjonalnego, czyli nefronu. Pod wpływem ciśnienia hydrostatycznego
Elektrochemia - szereg elektrochemiczny metali. Zadania
 Elektrochemia - szereg elektrochemiczny metali Zadania Czym jest szereg elektrochemiczny metali? Szereg elektrochemiczny metali jest to zestawienie metali według wzrastających potencjałów normalnych. Wartości
Elektrochemia - szereg elektrochemiczny metali Zadania Czym jest szereg elektrochemiczny metali? Szereg elektrochemiczny metali jest to zestawienie metali według wzrastających potencjałów normalnych. Wartości
pobrano z
 ODPOWIEDZI Zadanie 1. (2 pkt) 1. promienia atomowego, promienia jonowego 2. najwyższego stopnia utlenienia Zadanie 2. (1 pkt) 1. Pierwiastek I jest aktywnym metalem. Tworzy wodorek, w którym wodór przyjmuje
ODPOWIEDZI Zadanie 1. (2 pkt) 1. promienia atomowego, promienia jonowego 2. najwyższego stopnia utlenienia Zadanie 2. (1 pkt) 1. Pierwiastek I jest aktywnym metalem. Tworzy wodorek, w którym wodór przyjmuje
Projekt Era inżyniera pewna lokata na przyszłość jest współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego
 TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
Prof. dr hab. Krzysztof Bobrowski Instytut Chemii i Techniki Jądrowej Dorodna 16, Warszawa
 Prof. dr hab. Krzysztof Bobrowski Instytut Chemii i Techniki Jądrowej Dorodna 16, 03-195 Warszawa Recenzja rozprawy doktorskiej mgr. inż. DAWIDA DĘBSKIEGO Mechanistyczne aspekty oksydatywnej konwersji
Prof. dr hab. Krzysztof Bobrowski Instytut Chemii i Techniki Jądrowej Dorodna 16, 03-195 Warszawa Recenzja rozprawy doktorskiej mgr. inż. DAWIDA DĘBSKIEGO Mechanistyczne aspekty oksydatywnej konwersji
liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2
![liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2 liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2](/thumbs/65/54124071.jpg) Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami.
![Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami.](/thumbs/100/143872318.jpg) Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. I. Gęstość propanu w warunkach normalnych wynosi II. Jeżeli stężenie procentowe nasyconego roztworu pewnej
Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. I. Gęstość propanu w warunkach normalnych wynosi II. Jeżeli stężenie procentowe nasyconego roztworu pewnej
2. Podczas spalania 2 objętości pewnego gazu z 4 objętościami H 2 otrzymano 1 objętość N 2 i 4 objętości H 2O. Jaki gaz uległ spalaniu?
 1. Oblicz, ilu moli HCl należy użyć, aby poniższe związki przeprowadzić w sole: a) 0,2 mola KOH b) 3 mole NH 3 H 2O c) 0,2 mola Ca(OH) 2 d) 0,5 mola Al(OH) 3 2. Podczas spalania 2 objętości pewnego gazu
1. Oblicz, ilu moli HCl należy użyć, aby poniższe związki przeprowadzić w sole: a) 0,2 mola KOH b) 3 mole NH 3 H 2O c) 0,2 mola Ca(OH) 2 d) 0,5 mola Al(OH) 3 2. Podczas spalania 2 objętości pewnego gazu
Równowaga kwasowo-zasadowa. Zakład Chemii Medycznej PUM
 Równowaga kwasowozasadowa Zakład Chemii Medycznej PUM Teorie kwasów i zasad Teoria dysocjacji elektrolitycznej Arheniusa: podczas rozpuszczania w wodzie wodzie kwas: dysocjuje z odszczepieniem kationu
Równowaga kwasowozasadowa Zakład Chemii Medycznej PUM Teorie kwasów i zasad Teoria dysocjacji elektrolitycznej Arheniusa: podczas rozpuszczania w wodzie wodzie kwas: dysocjuje z odszczepieniem kationu
relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
 1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
Aminokwasy, peptydy i białka. Związki wielofunkcyjne
 Aminokwasy, peptydy i białka Związki wielofunkcyjne Aminokwasy, peptydy i białka Aminokwasy, peptydy i białka: - wiadomości ogólne Aminokwasy: - ogólna charakterystyka - budowa i nazewnictwo - właściwości
Aminokwasy, peptydy i białka Związki wielofunkcyjne Aminokwasy, peptydy i białka Aminokwasy, peptydy i białka: - wiadomości ogólne Aminokwasy: - ogólna charakterystyka - budowa i nazewnictwo - właściwości
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
wielkość, kształt, typy
 Mitochondria 0,5-1µm wielkość, kształt, typy 1-7µm (10µm) Filmowanie poklatkowe (w mikroskopie fluorescencyjnym) sieci mitochondrialnej w komórkach droŝdŝy (krok czasowy 3 min) Mitochondria liczebność,
Mitochondria 0,5-1µm wielkość, kształt, typy 1-7µm (10µm) Filmowanie poklatkowe (w mikroskopie fluorescencyjnym) sieci mitochondrialnej w komórkach droŝdŝy (krok czasowy 3 min) Mitochondria liczebność,
uczeń opanował wszystkie wymagania podstawowe i ponadpodstawowe
 1 Agnieszka Wróbel nauczyciel biologii i chemii Plan pracy dydaktycznej na chemii w klasach pierwszych w roku szkolnym 2015/2016 Poziom wymagań Ocena Opis wymagań podstawowe niedostateczna uczeń nie opanował
1 Agnieszka Wróbel nauczyciel biologii i chemii Plan pracy dydaktycznej na chemii w klasach pierwszych w roku szkolnym 2015/2016 Poziom wymagań Ocena Opis wymagań podstawowe niedostateczna uczeń nie opanował
CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU.
 CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU. Projekt zrealizowany w ramach Mazowieckiego programu stypendialnego dla uczniów szczególnie uzdolnionych
CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU. Projekt zrealizowany w ramach Mazowieckiego programu stypendialnego dla uczniów szczególnie uzdolnionych
Konkurs Chemiczny dla uczniów szkół ponadgimnazjalnych rok szkolny 2013/2014
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Konkurs Chemiczny dla uczniów szkół ponadgimnazjalnych rok szkolny 2013/2014 Imię i nazwisko uczestnika Szkoła Klasa Nauczyciel Imię
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Konkurs Chemiczny dla uczniów szkół ponadgimnazjalnych rok szkolny 2013/2014 Imię i nazwisko uczestnika Szkoła Klasa Nauczyciel Imię
Wykład 1. Od atomów do komórek
 Wykład 1. Od atomów do komórek Skład chemiczny komórek roślinnych Składniki mineralne (nieorganiczne) - popiół Substancje organiczne (sucha masa) - węglowodany - lipidy - kwasy nukleinowe - białka Woda
Wykład 1. Od atomów do komórek Skład chemiczny komórek roślinnych Składniki mineralne (nieorganiczne) - popiół Substancje organiczne (sucha masa) - węglowodany - lipidy - kwasy nukleinowe - białka Woda
Uniwersytet Łódzki Wydział Biologii i Ochrony Środowiska Katedra Biofizyki Skażeń Środowiska ul. Pomorska 141/143, Łódź
 Uniwersytet Łódzki Wydział Biologii i Ochrony Środowiska Katedra Biofizyki Skażeń Środowiska ul. Pomorska 141/143, 90-236 Łódź Dr hab. Bożena Bukowska, prof. nadzw. UŁ Łódź, 09-07-2013 Katedra Biofizyki
Uniwersytet Łódzki Wydział Biologii i Ochrony Środowiska Katedra Biofizyki Skażeń Środowiska ul. Pomorska 141/143, 90-236 Łódź Dr hab. Bożena Bukowska, prof. nadzw. UŁ Łódź, 09-07-2013 Katedra Biofizyki
Witaminy rozpuszczalne w tłuszczach
 Jaką rolę pełnią witaminy w organizmie? I dlaczego są niezbędnymi składnikami w żywieniu świń? Dowiedz się o roli poszczególnych witamin w żywieniu trzody chlewnej. Witaminy są niezbędne do prawidłowego
Jaką rolę pełnią witaminy w organizmie? I dlaczego są niezbędnymi składnikami w żywieniu świń? Dowiedz się o roli poszczególnych witamin w żywieniu trzody chlewnej. Witaminy są niezbędne do prawidłowego
Część 1: Strategia ataku 15
 Wstęp 13 Część 1: Strategia ataku 15 1.1. Tlen: pierwiastek życia i śmierci 15 1.1.1. Tlen pierwiastek życia 15 1.1.2. Tlen pierwiastek chorób i śmierci 16 1.2. Co to są reaktywne formy tlenu? 19 1.3.
Wstęp 13 Część 1: Strategia ataku 15 1.1. Tlen: pierwiastek życia i śmierci 15 1.1.1. Tlen pierwiastek życia 15 1.1.2. Tlen pierwiastek chorób i śmierci 16 1.2. Co to są reaktywne formy tlenu? 19 1.3.
WSPÓŁCZESNE TECHNIKI ZAMRAŻANIA
 WSPÓŁCZESNE TECHNIKI ZAMRAŻANIA Temat: Denaturacja białek oraz przemiany tłuszczów i węglowodorów, jako typowe przemiany chemiczne i biochemiczne zachodzące w żywności mrożonej. Łukasz Tryc SUChiKL Sem.
WSPÓŁCZESNE TECHNIKI ZAMRAŻANIA Temat: Denaturacja białek oraz przemiany tłuszczów i węglowodorów, jako typowe przemiany chemiczne i biochemiczne zachodzące w żywności mrożonej. Łukasz Tryc SUChiKL Sem.
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
In vino veritas, in RESVERATROLUM sanitas
 In vino veritas, in RESVERATROLUM sanitas - w winie prawda, w resweratrolu zdrowie dr hab. n. farm. Ilona Kaczmarczyk-Sedlak Specjalista farmakolog Śląski Uniwersytet Medyczny FRANCUSKI PARADOKS WINO
In vino veritas, in RESVERATROLUM sanitas - w winie prawda, w resweratrolu zdrowie dr hab. n. farm. Ilona Kaczmarczyk-Sedlak Specjalista farmakolog Śląski Uniwersytet Medyczny FRANCUSKI PARADOKS WINO
Maksymalne wydzielanie potu w czasie wysiłku fizycznego może osiągać 2-3 litrów na godzinę zastanów się jakie mogą być tego konsekwencje?
 Ćwiczenia IV I. Termoregulacja wysiłkowa. Utrzymanie stałej temperatury ciała jest skomplikowanym procesem. Choć temperatura różnych części ciała może być różna, ważne jest utrzymanie temperatury wewnętrznej
Ćwiczenia IV I. Termoregulacja wysiłkowa. Utrzymanie stałej temperatury ciała jest skomplikowanym procesem. Choć temperatura różnych części ciała może być różna, ważne jest utrzymanie temperatury wewnętrznej
Prof. dr hab. Mirosław Soszyński Łódź, 29 lipca 2013 r. Katedra Biofizyki Molekularnej UŁ Uniwersytet Łódzki ul. Banacha 12/ Łódź
 Prof. dr hab. Mirosław Soszyński Łódź, 29 lipca 2013 r. Katedra Biofizyki Molekularnej UŁ Uniwersytet Łódzki ul. Banacha 12/16 90-237 Łódź OCENA Rozprawy doktorskiej Pani mgr Pauliny Kleniewskiej pt. Udział
Prof. dr hab. Mirosław Soszyński Łódź, 29 lipca 2013 r. Katedra Biofizyki Molekularnej UŁ Uniwersytet Łódzki ul. Banacha 12/16 90-237 Łódź OCENA Rozprawy doktorskiej Pani mgr Pauliny Kleniewskiej pt. Udział
KREW: 1. Oznaczenie stężenia Hb. Metoda cyjanmethemoglobinowa: Zasada metody:
 KREW: 1. Oznaczenie stężenia Hb Metoda cyjanmethemoglobinowa: Hemoglobina i niektóre jej pochodne są utleniane przez K3 [Fe(CN)6]do methemoglobiny, a następnie przekształcane pod wpływem KCN w trwały związek
KREW: 1. Oznaczenie stężenia Hb Metoda cyjanmethemoglobinowa: Hemoglobina i niektóre jej pochodne są utleniane przez K3 [Fe(CN)6]do methemoglobiny, a następnie przekształcane pod wpływem KCN w trwały związek
REAKTYWNE FORMY TLENU
 BROMAT. CHEM. TOKSYKOL. XLI, 2008, 4, str. 1007 1015 Helena Puzanowska-Tarasiewicz, Barbara Starczewska, Ludmiła Kuźmicka REAKTYWNE FORMY TLENU Zakład Chemii Ogólnej i Nieorganicznej Instytutu Chemii Uniwersytetu
BROMAT. CHEM. TOKSYKOL. XLI, 2008, 4, str. 1007 1015 Helena Puzanowska-Tarasiewicz, Barbara Starczewska, Ludmiła Kuźmicka REAKTYWNE FORMY TLENU Zakład Chemii Ogólnej i Nieorganicznej Instytutu Chemii Uniwersytetu
Spektrofotometryczna metoda oznaczania aktywności peroksydazy
 Spektrofotometryczna metoda oznaczania aktywności peroksydazy Cel ćwiczenia: Ćwiczenie poświęcone jest zapoznaniu się z metodą oznaczania aktywności peroksydazy chrzanowej jako jednego z enzymów z klasy
Spektrofotometryczna metoda oznaczania aktywności peroksydazy Cel ćwiczenia: Ćwiczenie poświęcone jest zapoznaniu się z metodą oznaczania aktywności peroksydazy chrzanowej jako jednego z enzymów z klasy
W tej reakcji stopień utleniania żelaza wzrasta od 0 do III. Odwrotnie tlen zmniejszył stopień utlenienia z 0 na II.
 8 Utlenianie i redukcja Początkowo termin utlenianie odnosił się do reakcji pierwiastków lub związków chemicznych z tlenem, a termin redukcja stosowano do określenia usunięcia tlenu ze związku. Później,
8 Utlenianie i redukcja Początkowo termin utlenianie odnosił się do reakcji pierwiastków lub związków chemicznych z tlenem, a termin redukcja stosowano do określenia usunięcia tlenu ze związku. Później,
Składniki diety a stabilność struktury DNA
 Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
TEORIA KOMÓRKI (dlaczego istnieją osobniki?)
 Wstęp do biologii 2. TEORIA KOMÓRKI (dlaczego istnieją osobniki?) Jerzy Dzik Instytut Paleobiologii PAN Instytut Zoologii UW 2015 WSPÓLNE WŁAŚCIWOŚCI dzisiejszych organizmów procesy życiowe katalizowane
Wstęp do biologii 2. TEORIA KOMÓRKI (dlaczego istnieją osobniki?) Jerzy Dzik Instytut Paleobiologii PAN Instytut Zoologii UW 2015 WSPÓLNE WŁAŚCIWOŚCI dzisiejszych organizmów procesy życiowe katalizowane
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab
 SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab CZĄSTECZKA I RÓWNANIE REKCJI CHEMICZNEJ potrafi powiedzieć co to jest: wiązanie chemiczne, wiązanie jonowe, wiązanie
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab CZĄSTECZKA I RÓWNANIE REKCJI CHEMICZNEJ potrafi powiedzieć co to jest: wiązanie chemiczne, wiązanie jonowe, wiązanie
Wymagania przedmiotowe do podstawy programowej - chemia klasa 7
 Wymagania przedmiotowe do podstawy programowej - chemia klasa 7 I. Substancje i ich właściwości opisuje cechy mieszanin jednorodnych i niejednorodnych, klasyfikuje pierwiastki na metale i niemetale, posługuje
Wymagania przedmiotowe do podstawy programowej - chemia klasa 7 I. Substancje i ich właściwości opisuje cechy mieszanin jednorodnych i niejednorodnych, klasyfikuje pierwiastki na metale i niemetale, posługuje
Nazwy pierwiastków: ...
 Zadanie 1. [ 3 pkt.] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Atom pierwiastka X w reakcjach chemicznych może tworzyć jon zawierający 20
Zadanie 1. [ 3 pkt.] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Atom pierwiastka X w reakcjach chemicznych może tworzyć jon zawierający 20
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Odwracalność przemiany chemicznej
 Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
(węglowodanów i tłuszczów) Podstawowym produktem (nośnikiem energii) - ATP
 śycie - wymaga nakładu energii źródłem - promienie świetlne - wykorzystywane do fotosyntezy - magazynowanie energii w wiązaniach chemicznych Wszystkie organizmy (a zwierzęce wyłącznie) pozyskują energię
śycie - wymaga nakładu energii źródłem - promienie świetlne - wykorzystywane do fotosyntezy - magazynowanie energii w wiązaniach chemicznych Wszystkie organizmy (a zwierzęce wyłącznie) pozyskują energię
 PRACA KONTROLNA Z CHEMII NR 1 - Semestr I 1. (6 pkt) - Krótko napisz, jak rozumiesz następujące pojęcia: a/ liczba atomowa, b/ nuklid, c/ pierwiastek d/ dualizm korpuskularno- falowy e/promieniotwórczość
PRACA KONTROLNA Z CHEMII NR 1 - Semestr I 1. (6 pkt) - Krótko napisz, jak rozumiesz następujące pojęcia: a/ liczba atomowa, b/ nuklid, c/ pierwiastek d/ dualizm korpuskularno- falowy e/promieniotwórczość
