Związki karbonylowe: aldehydy i ketony
|
|
|
- Patryk Kaczmarek
- 7 lat temu
- Przeglądów:
Transkrypt
1 Związki karbonylowe: aldehydy i ketony grupa Karbonylowa (C=O) płaska alkanal Nazewnictwo zwyczajowe Aldehydy (i kwasy) Ketony aldehyd mrówkowy aldehyd octowy aldehyd propionowy aldehyd masłowy aldehyd walerianowy aldehyd kapronowy Nazwy zwyczajowe grup dipol alkanon aldehyd benzoesowy kwas alkanowy Właściwości fizyczne aldehydów i ketonów polarne, do C 5 rozpuszczalne w wodzie temperatura wrzenia: wyŝsza niŝ alkanów niŝsza niŝ alkoholi (brak wiązań wodorowych) heptan 98 C eter metylowo-pentylowy 100 C heksanal 131 C 2-heksanon 150 C heksanol 157 C Właściwości grupy karbonylowej Addycja nukleofilowa do grupy karbonylowej Odczynniki nukleofilowe z ładunkiem ujemnym Nuobojętne bez wydzielenia wody z wydzieleniem wody pochodne amoniaku NuH 2 Redukcja aldehydów i ketonów redukcja wodorkami (NaBH 4, LiAlH 4 ) addycja Nu Addycja nukleofilowa związków Grignarda do aldehydów i ketonów synteza alkoholi 1, 2 i 3 rozkład pod wpływem: wody, kwasów, w, alkoholi, amin redukcja wodorem addycja katalityczna O C δ- δ+ podatne na atak kwasów i odczynnikow elektrofilowych cyklopent-3-enon aldehydy alkohole 1 ketony alkohole 2
2 reakcja formaldehydu 1 alkohole Reakcje Grignarda Addycja nukleofilowa HCN do aldehydów i ketonów synteza cyjanohydryn = hydroksynitryli reakcja innych aldehydów 2 alkohole Addycja nukleofilowa pochodnych amoniaku (z wydzieleniem wody) reakcja ketonów 3 alkohole reakcja CO 2 kwasy karboksylowe Właściwości aldehydów i ketonów Addycja nukleofilowa alkoholi acetale aldehydów i ketonów addycja nukleofilowa amin 1 (z wydzieleniem wody) R C=NHR C=C NR 2 Mechanizm syntezy acetali zasada Schiffa katalizator hemiacetal acetal Acetale Addycja nukleofilowa do aldehydów i ketonów z glikolami acetale cykliczne Właściwości acetali hydroliza kwasowa w środowisku zasadowym i obojętnym trwałe
3 Właściwości aldehydów i ketonów reakcje utleniania alkohol [H] [H] [O] = KMnO 4, H + Na 2 Cr 2 O 7, H + Cr 2 O 3, H + Reakcje utleniania aldehydów reakcja z odczynnikiem Tollensa lustro srebrowe aldehyd reakcja z odczynnikami: keton brak reakcji Fehlinga Cu 2+ + winian sodu Benedicta Cu 2+ + cytrynian sodu czerwony osad Cu 2 O oznaczanie jakościowe i ilościowe aldehydów reakcje charakterystyczne dla aldehydów ketony nie reagują! Reakcja Cannizzaro: utlenienie redukcja wybranych aldehydów Halogenowanie w połoŝeniu α aldehydy bez at. H na α at. C Mechanizm Reakcja haloformowa H 2 O - OH - aldehyd mrówkowy = formaldehyd = matanal reduktor oznaczanie aldehydu octowego, metyloketonów i alkoholi tworzących je po utlenieniu, np. etanolu Reakcja kondensacji aldolowej Mechanizm kondensacji aldolowej warunek konieczny: obecność atomu wodoru przy α atomie węgla, tzw. kwasowego H addycja nukleofilowa karboanion α atom węgla α atom wodoru β-hydroksyaldehydy β-hydroksyketony
4 Kkondensacja aldolowa krzyŝowa Kwasy karboksylowe i ich pochodne kwas alkanowy A alkan alkan (o) B alkan A A B B A B B A alkanan (R) alkilowy (R ) Nitryl alkano -nitryl Nazwy zwyczajowe Kwasy karboksylowe Kwasy karboksylowe Budowa izomasłowy walerianowy kapronowy C 8, C 10, C 12, C 14, C 16, C 18, C 20 benzoesowy Właściwości fizyczne Kwasy dikarboksylowe (alkanodiowe) ftalowy wiązania wodorowe polarne, do C 6 rozpuszczalne w wodzie temperatura wrzenia: wyŝsza niŝ aldehydów i alkoholi formaldehyd -21 C kwas mrówkowy 101 C acetaldehyd 21 C kwas octowy 118 C benzaldehyd 178 C kwas benzoesowy 249 C (temp. topn. 122 C) Kwasowość kwasów karboksylowych kwasowość Kwasy karboksylowe kwasowość HCl > CH 3 COOH > CH 3 CH 2 OH pk a ok ok. 3-5 CCl 3 COOH > CH 2 ClCOOH > HCOOH > C 6 H 5 COOH > CH3COOH > > CH 3 CH 2 COOH > (CH 3 ) 2 CHCOOH podstawnik dezaktywujący mocniejszy kwas podstawnik aktywujący słabszy kwas charakterystyczna próba jakościowa
5 Reakcje kwasów karboksylowych tworzenie soli z zasadami, metalami, węglanami Na i K Reakcje kwasów karboksylowych redukcja LiAlH 4 (NaBH 4 nie nadaje się) cis-oktadec-9-en-1-ol podstawienie w połoŝeniu α halogenowanie kwas α-bromoenantowy Reakcje substytucji nukleofilowej grupy acylowej kwasów karboksylowych Reakcje substytucji nukleofilowej w grupie acylowej kwasów karboksylowych otrzymywanie pochodnych kwasowych grupa opuszczająca Nu grupa wchodząca Y grupa opuszczająca grupy wchodzące aldehydy, ketony addycja nukleofilowa!!! Otrzymywanie halogenków kwasowych=acylowych chlorki kwasowe/acylowe bromki kwasowe/acylowe Otrzymywanie bezwodników kwasowych bezwodniki symetryczne i mieszane bezwodniki cykliczne kwasów dikarboksylowych halogenek alkanoilu
6 Otrzymywanie estrów - reakcja estryfikacji Równowaga reakcji odwracalnej estry Mechanizm reakcji estryfikacji alkohol acetale kwas - karbokation - przesuwanie rónowagi reakcji odwracalnej: nadmiar jednego z substratów usuwanie jednego lub obu produktów ester Otrzymywanie estrów acylowanie alkoholi acylowanie kwasem karboksylowym w obecności katalizatora: estryfikacja Otrzymywanie estrów S N w 1 halogenkach alkilowych acylowanie bezwodnikiem kwasowym metoda najlepsza 2 O bezwodnik octowy acylowanie halogenkiem kwasowym Transestryfikacja właściwość i metoda otrzymywania estrów 2 reaktywność alkoholi: CH 3 OH>1 > 2 >(3 ) 1 Inne reakcje halogenków i bezwodników kwasowych hydroliza do kwasów Reakcje estrów hydroliza kwasowa i zasadowa (zmydlanie) reakcja odwracalna amonoliza reakcja z amoniakiem (amidy) aminoliza reakcja z aminami 1 i 2 (N-podstawione/N,N-dipodstawione amidy) alkoholiza transestryfikacja synteza estrów CH 3 CH 2 COOCH 2 CH 3 +(CH 3 ) 2 CHOH H + CH 3 CH 2 COOCH(CH 3 ) 2 +CH 3 CH 2 OH
7 amonoliza Reakcje estrów Reakcje estrów analogiczne do halogenków i bezwodników kwasowych alkoholiza redukcja: do alkoholi R OH do aldehydów hydroliza aminoliza redukcja Laktony estry wewnętrzne γ- i δ-hydroksykwasy Pochodne kwasów karboksylowych Amidy halogenek lub bezwodnik kwasowy 4-alkilo butyrolakton (lakton kwasu γ- hydroksymasłowego) 5-alkilo walerolakton N-alkiloalkanoamid N,N-dialkiloalkanoamid amidów nie da się otrzymać bezpośrednio z kwasów Amidy Reakcje amidów hydroliza kwasowa i zasadowa Pochodne kwasów karboksylowych Reakcje substytucji nukleofilowej grupy acylowej redukcja do amin addycja nukleofila Nu powoli eliminacja grupy opuszczającej Y szybko dehydratacja do nitryli alkanonitryl Szybkość reakcji: reaktywność Czynnik steryczny: budowa R CH 3 C=O > RCH 2 C=O > R 2 CHC=O > R 3 CC=O Czynnik elektronowy: budowa Y Cl > OCOR > OH > OR > NH 2
8 Pochodne kwasów karboksylowych Reakcje substytucji nukleofilowej grupy acylowej Reaktywność pochodnych łatwe przemiany Pochodne kwasów karboksylowych Reakcje substytucji nukleofilowej grupy acylowej Hydroliza reakcja z wodą RCOX, (RCO) 2 O kwas reakcja z wodą i H + /OH - RCOOR, RCONH 2 kwas/sól kwasu Alkoholiza reakcja z alkoholem i H + /OH - Aminoliza reakcja z amoniakiem lub aminą ester amid nietrwałe H 2 O trwałe występują w przyrodzie Redukcja reakcja z czynnikiem redukującym (wodór, wodorki) aldehyd lub alkohol Reakcja Grignarda reakcja ze związkiem magnezoorganicznym keton lub alkohol Reakcje nitryli hydroliza kwasowa i zasadowa Lipidy biocząsteczki ekstrahowane z tkanek i komórek rozpuszczalnikami niepolarnymi redukcja: woski tłuszcze sterole do aminy estry hydrolizują nie hydrolizują do aldehydu Woski estry wysokocząsteczkowych kwasów i alkoholi Tłuszcze Tłuszcze estry gliceryny i kwasów tłuszczowych triacyloglicerole = triglicerydy kwas C 16 i alkohol C 30 tłuszcze zwierzęce oleje roślinne pochodzenie: zwierzęce roślinne stan skupienia: stałe ciekłe budowa chemiczna: nasycone nienasycone kwasy tłuszczowe
9 Tłuszcze Tłuszcze waŝniejsze kwasy tłuszczowe kwas nasycony kwas nienasycony kwasy nienasycone naturalne wszystkie C=C cis kwasy trans szkodliwe polinienasycone kwasy tłuszczowe Tłuszcze Reakcja zmydlania tłuszczów mydła mydło część niepolarna część polarna Reakcja transestryfikacji tłuszczów analiza kwasów tłuszczowych i biopaliwa Klasyfikacja amin alifatyczne aromatyczne Reakcja uwodornienia tłuszczów utwardzanie produkcja margaryn z olejów częściowa redukcja katalityczna wiązań podwójnych w resztach nienasyconych kwasów tłuszczowych reakcja z H 2 /Pt 1 i 2 wiązania wodorowe Właściwości fizyczne amin polarne do C 5 rozpuszczalne w wodzie temperatura wrzenia: dietyloamina 56, pntan 36 C
10 Właściwości zasadowe amin NH 3 + HCl NH 4 Cl RNH 2 + HCl RNH 3 Cl = RNH 3+ Cl - Właściwości zasadowe amin pk a jonów amoniowych amoniak 9.26 metyloamina dimetyloamina trimetyloamina 9.81 anilina 4.63 pirolidyna pirydyna 5.25 Otrzymywanie i właściwości amin alkilowanie amoniaku i amin 1, 2 i 3 reakcja S N 2 Reakcje amin metylowanie i degradacja Hofmanna amoniak 1 amina 1 amina 2 amina E2 eliminacja niezgodna z regułą Zajcewa 2 amina 3 amina 3 amina 4 sól amoniowa określanie budowy grup alkilowych Reakcje amin acylowanie amin 1 i 2 czynniki acylujące: chlorki i bezwodniki kwasowe aminy 1 N-podstawionyamid 1 aminy alifatyczne Reakcje amin rozróŝnianie rzędowości amin reakcja z HNO 2 1 aminy aromatyczne aminy 2 N,N-dipodstawionyamid 2 aminy alifatyczne i aromatyczne aminy 3 brak reakcji 3 aminy aromatyczne
11 Reakcje amin aromatycznych tworzenie soli diazoniowych Reakcje soli diazoniowych podstawienie grupy N 2+ nukleofilem aminy alifatyczne właściwości soli diazoniowych z fenolami Reakcje soli diazoniowych Reakcja sprzęgania - synteza barwików diazowych słaby elektrofil silnie zaktywowany pierścień Reakcje amin aromatycznych substytucja elektrofilowa z 3 aminami aromatycznymi reakcja substytucji elektrofilowej w pierścieniu aromatycznym * Aminokwasy (α-) * Aminokwasy klasyfikacja budowa chemiczna połoŝenie grupy NH 2 :α, β, γ, δ... ω rzędowość grupy NH 2 : 1, 2 ilość grup COOH i NH 2 COOH = NH 2 : obojętne COOH > NH 2 : kwasowe NH 2 >COOH : zasadowe inne pierwiastki: siarka inne grupy funkcyjne: OH, pierścień aromatyczny klasyfikacja znaczenie biologiczne aldehyd L-glicerynowy (S) L-seryna (S) białkowe (20) / niebiałkowe podstawowe (10) (egzogenne, niesyntezowane, dostarczane) / pozostałe (10) (endogenne, syntezowane)
12 Aminokwasy Aminokwasy klasyfikacja, budowa chemiczna klasyfikacja, budowa chemiczna glicyna leucyna seryna fenyloalanina H i-bu alanina Me izoleucyna s-bu treonina tyrozyna walina i-pr R H lub grupa alkilowa grupa OH i/lub Ph Aaminokwasy klasyfikacja, budowa chemiczna cysteina prolina Aminokwasy klasyfikacja, budowa chemiczna kwas asparaginowy asparagina metionina tryptofan kwas glutaminowy glutamina siarkowe z pierścieniem pirolidyny kwasowe obojętne amidy kwasowych lizyna Aminokwasy klasyfikacja, budowa chemiczna histydyna Aminokwasy Właściwości fizykochemiczne nielotne, krystaliczne, wysokie temperatury topnienia nierozpuszczalne w rozpuszczalnikach organicznych rozpuszczalne w wodzie duŝy moment dipolowy w roztworach wodnych bardzo niskie stałe kwasowości i zasadowości w porównaniu z kwasami i aminami arginina zasadowe
13 Aminokwasy Właściwości amfoteryczne centrum zasadowe jon obojnaczy jon dipolowy sól wewnętrzna Aminokwasy jako kwasy i zasady glicyna K a = 1.6 x kwasy k. K a = 10-5 zasada mocniejsza kwas mocniejszy kwas słabszy zasada słabsza K b = 2.5 x aminy K b = 10-4 centrum kwasowe Właściwości amfoteryczne aminokwasów punkt izoelektryczny lizyna Rozdzielanie aminokwasów glicyna kwas asparaginowy ph = pi = 9.74 ph = pi = 5.97 ph = pi = 2.77 punkt izoelektryczny (pi) = wartość ph, przy której aminokwas jest w roztworze w postaci jonów obojnaczych ph = 5.97 < pi (kwasowe) ph = pi = 5.97 (obojętne) ph = 5.97 > pi (zasadowe) aminokwasy obojętne pi = aminokwasy zasadowe pi = aminokwasy kwasowe pi = kation jon obojnaczy anion Elektroforeza aminokwasów i białek rozdział aminokwasów w polu elektrycznym WaŜne reakcje aminokwasów Reakcja z ninhydryną - wykrywanie aminokwasów katoda anoda fioletowa barwa Reakcja z HNO 2 - dezaminacja aminokwasów, peptydów i białek pomiar azotu N 2 + kation anion kation tert-pentylowy mieszanina alkenów i alkoholu jon obojnaczy
14 Właściwości chemiczne aminokwasów Właściwości grupy karboksylowej: tworzenie soli z zasadami tworzenie chlorków kwasowych z SOCl 2 tworzenie estrów z alkoholami i H + tworzenie amidów (z chlorków kwasowych) sole wewn. Właściwości grupy aminowej: tworzenie soli z kwasami reakcja z HNO 2 tworzenie amidów (z chlorkami kwasowymi lub bezwodnikami) - H 2 O tworzenie wiązań peptydowych, taka reakcja nie zachodzi NH wiązania amidowe płaskie peptydy białka glicyna Gly alanina Ala walina Val leucyna Leu izoleucyna Ile seryna Ser fenyloalanina Phe G A V L I S F Aminokwasy treonina Thr tyrozyna Tyr cysteina Cys metionina Met prolina Pro tryptofan Trp T Y C M P W kwas asparaginowy Asp D kwas glutaminowy Glu E asparagina Asn N glutamina Gln Q lizyna Lys K arginina Arg R histydyna His H n = 2 2 dipeptydy n = 3 6 tripeptydów n = 8 > 4000 oktapeptydów Peptydy Budowa: polimery aminokwasów glutation Glu - Cys - Gly polipeptydy M < białka M > Peptydy Rodzaje wiązań wiązanie amidowe = peptydowe wiązanie disulfidowe N-C = nm (0.147 nm) trwałe hydroliza 35% HCl Peptydy Określanie struktury peptydów jakie aminokwasy wchodzą w skład peptydu? ile jest jednostek kaŝdego z nich? peptyd + 35% HCl hydroliza wszystkich wiązań amidowych redukcja wszystkich wiązań disulfidowych ANALIZATOR AMINOKWASÓW chromatografia rozdział na kolumnie, wymywanie buforami Peptydy Określanie struktury peptydów w jakiej kolejności występują w łańcuchu? Sekwencjonowanie peptydów Metody chemiczne: oznaczanie reszty N-końcowej metoda Edmana metoda Sangera przyłączenie ragenta hydroliza wiązań peptydowych - odrywanie aminokwasu N-terminalnego identyfikacja Metoda enzymatyczna: oznaczanie reszty C-końcowej
15 Synteza peptydów - H 2 O NH, 1. zablokowanie grupy NH 2 2. zablokowanie grupy COOH 3. połączenie aminokwasów (aktywacja grupy COOH) 4. usunięcie grup blokujących cukry Węglowodany C n (H 2 O) m = cukry = sacharydy polihydroksylowane aldehydy i ketony CO 2 + H 2 O cukry proste: chlorofil C n (H 2 O) m proste: monosacharydy (monocukry) złoŝone: dwa lub więcej cukrów prostych: disacharydy (dwucukry) trisacharydy, tetra..., polisacharydy (wielocukry) aldozy ketozy C 4 tetroza tetruloza C 5 pentoza pentuloza C 6 heksoza heksuloza C 7 heptoza heptuloza heksoza Węglowodany = cukry czynność optyczna Węglowodany: szereg D cukrów aldehyd D-glicerynowy aldehyd glicerynowy ilość izomerów = 2 n n = ilość C* n =4 32 erytroza treoza wzór Fischera aldehyd D i L-glicerynowy ryboza arabinoza ksyloza liksoza alloza glukoza guloza galaktoza altroza mannoza idoza taloza Węglowodany: szereg D cukrów aldehyd D-(+)-glicerynowy Węglowodany D-(-)-erytroza D-(-)-treoza ryboza arabinoza glukoza mannoza galaktoza fruktoza D-(-)-ryboza D-(-)-arabinoza D-(+)-ksyloza D-(-)-liksoza D-(+)-alloza D-(+)-glukoza D-(-)- guloza D-(+)-galaktoza D-(+)- altroza D-(+)- mannoza D-(-)- idoza D-(+)- taloza
16 D-erytroza Węglowodany D(-)- i L(+)-erytroza Właściwości aldehydów i ketonów addycja nukleofilowa alkoholu do grupy karbonylowej hemiacetal γ- i δ-hydroksykwasy laktony = estry wewnętrzne α β enancjomery γ- i δ-hydroksyaldehydy i ketony wewnętrzne hemiacetale lub acetale * * α-d-erytrofuranoza i β -D-erytrofuranoza 4-hydroksybutanal 5-hydroksypentanal anomery diastereoizomeryczne hemiacetalowe formy cukrów α i β o róŝnej konfiguracji tylko na anomerycznym = hemiacetalowym at. C furan * hemiacetalowy = anomeryczny atom C piran Hemiacetalowe formy cukrów D-glukoza Hemiacetalowe formy cukrów równowaga w roztworze wodnym wzory konformacyjne β-d-glukopiranoza i α-d-glukopiranoza wzory Hawortha = taflowe α-d-glukopiranoza (EtOH) tt 146 C [α] D forma łańcuchowa D-glukozy w równowadze [α] D β-d-glukopiranoza (EtOH-H 2 O) tt [α] D anomer β trwalszy anomer α mniej trwały 36% 0.02% 64% MUTAROTACJA forma bardziej trwała Hemiacetalowe formy cukrów równowaga w roztworze wodnym Mutarotacja MUTAROTACJA zmiana skręcalności właściwej roztworu kaŝdej z anomerycznych form cukru do wartości odpowiadającej stanowi równowagi między: anomerami α i β (formy hemiacetalowe) oraz formą łańcuchową (forma aldehydowa) następuje dzięki otwarciu pierścienia wzory konformacyjne β-d-glukopiranoza bardziej trwała niŝ α-d-glukopiranoza ale β-d-mannopiranoza mniej trwała niŝ α-d-mannopiranoza
17 Ketozy Reakcje cukrów Reakcje formy łańcuchowej grupy karbonylowej Reakcje formy hemiacetalowej grupy hydroksylowej hemiacetalowej rybuloza ksyluloza fruktoza = lewuloza α-d-fruktofuranoza Deoksycukry Aminocukry Cukry o rozgałęzionych łańcuchach Reakcje formy hemiacetalowej grup hydroksylowych alkoholowych 2-deoxy- D-ryboza L-daunozamina D-apioza Reakcje formy łańcuchowej cukrów grupy karbonylowej Redukcja cukrów [aldoza alditol] mannoza α-d-mannopiranoza mannitol β-d-mannopiranoza Reakcje formy łańcuchowej cukrów grupy karbonylowej Utlenianie cukrów HNO 3 aldoza kwas aldarowy galaktoza α-d-galaktopiranoza β-d-galaktopiranoza galakcytol Br 2 aldoza kwas aldonowy glukoza kwas alduronowy kwas glutarowy glukoza glucytol = sorbitol fruktoza glucytol + mannitol ksyloza kwas ksylonowy forma hemiacetalowa Reakcje formy łańcuchowej cukrów Utlenianie cukrów odczynnik Benedicta lub Fehlinga odczynnik Tollensa Reakcje formy łańcuchowej cukrów utlenianie fruktozy i innych ketoz odczynnikami Benedicta, odczynnik Tollensa aldoza α-d-aldopiranoza β-d-aldopiranoza α-d-aldofuranoza β-d-aldofuranoza Ag pozytywna próba Benedicta (czerwony osad Cu 2 O) pozytywna próba Tollensa (lustro srebrowe) enolizacja ketoza endiol aldoza Ag fruktoza: pozytywna próba Benedicta (czerwony osad Cu 2 O) oraz Tollensa (lustro srebrowe) aldoza kwas aldonowy aldoza ketoza dwa kwasy aldonowe dwa kwasy aldonowe
18 Epimeryzacja cukrów ustalanie się równowagi w roztworach zasadowych aldoz lub ketoz między: dwiema epimerycznymi (diastereoizomerycznymi) aldozami, ketozą i odpowiednią formą enolową Reakcje formy łańcuchowej cukrów Tworzenie pochodnych krystalicznych z pochodnymi amoniaku Reakcja z hydroksyloaminą oksym D-galaktozy glukoza forma enolowa mannoza fruktoza glukoza i mannoza - epimery Reakcja z hydrazyną i fenylohydrazyną fenylohydrazon D-rybozy Reakcje formy łańcuchowej cukrów Reakcje cukrów z pochodnymi amoniaku Reakcja z nadmiarem hydrazyny i fenylohydrazyny jedna cząsteczka fenylohydrazyny jest utleniaczem Reakcje formy łańcuchowej cukrów Tworzenie cyjanohydryn przedłuŝanie łańcucha synteza Kilianiego-Fischera nowe centrum asymetrii D-arabinoza D-ryboza difenylohydrazon D-rybozy = D-arabinozy = D-rybulozy arabinoza dwie cyjanohydryny D-glukoza i D-mannoza D-rybuloza difenylohydrazon D-glukozy = D-mannozy = D-fruktozy dwie iminy dwie epimeryczne aldozy i odpowiadająca im ketoza tworzą ten sam osazon Reakcje hemiacetalowej grupy hydroksylowej w cukrach Glikozydy = Acetale cukrów O-Glikozydy = Acetale cukrów Glikozydy N-Glikozydy hemiacetal reakcja spontaniczna acetal reakcja katalizowana α β linamaryna (maniok) S-Glikozydy adenozyna (nukleozyd) D-glukoza α-d-glukopiranoza β-d-glukopiranoza α-d-glukozyd metylowy metylo-α-d- glukopiranozyd β-d-glukozyd metylowy metylo- β-d- glukopiranozyd synigryna (gorczyca) aglikon niecukrowa część glikozydu
19 Reakcje formy hemiacetalowej formy cukrów grupy hydroksylowe Tworzenie eterów Reakcje cukrów Reakcje formy hemiacetalowej grupy hydroksylowe Tworzenie estrów = acetylowanie cukrów D-glukoza α-d-glukopiranoza β-d-glukopiranoza ZnCl 2 α metylo-α-dglukopiranozyd metylo-2,3,4,6-tetra-o-metylo-α-dglukopiranozyd trwałe wiązania eterowe Fosforany AcONa β 1,2,3,4,6-penta-O-acetylo- α/β-d-lukopiranoza nietrwałe wiązanie acetalowe 2,3,4,6-tetra-O-metylo-D-glukoza Właściwości estrów trwałe w środowisku obojętnym hydrolizują w środowisku kwaśnym i zasadowy Właściwości acetali trwałe w środowisku zasadowym i obojętnym hydrolizują w środowisku kwaśnym Właściwości eterów trwałe w środowisku kwaśnym, zasadowym i obojętnym Reakcje cukrów Właściwości fruktozy Reakcje formy łańcuchowej grupa C=O C2!!! z H 2,Pt lub LiAlH 4 alditole z NH 2 OH oksym z NH 2 NH 2 osazon (fenyloosazon) ulega epimeryzacji z HCN rozgałęzienie łańcucha Reakcje formy łańcuchowej grupy -CH 2 OH z HNO 3 kwas ketoaldarowy Fruktoza: nie reaguje z Br 2 α-d-fruktofuranoza Reakcje cukrów Właściwości fruktozy 2 ulega mutarotacji β-d-fruktofuranoza Reakcje formy hemiacetalowej grupy hydroksylowej hemiacetalowej glikozydy Reakcje formy hemiacetalowej grup hydroksylowych alkoholowych etery i estry 2 2 Reakcje cukrów - podsumowanie Reakcje formy łańcuchowej grupy karbonylowej (aldozy i 2-ketozy- cukry redukujące) właściwości redukujące: reakcja z odczynnikami: Tollensa, Fehlinga, Benedicta ulegają mutarotacji tworzą oksymy i fenyloosazony oraz glikozydy Reakcje formy hemiacetalowej grupy hydroksylowej hemiacetalowej glikozydy (acetale) Reakcje formy hemiacetalowej grup hydroksylowych alkoholowych etery, estry
20 Podsumowanie reakcji cukrów Glikozydy = Acetale cukrów mieszanina anomerów α+β (CH 3 ) 2 SO 4, NaOH cukry nieredukujące nie reagują z odczynnikami: Tollensa, Fehlinga, Benedicta nie ulegają mutarotacji nie tworzą oksymów ani fenyloosazonów poniewaŝ pierścień nie moŝe się otworzyć + pochodne krystaliczne (+)-Maltoza Disacharydy C 12 H 22 O 11 (+)-Celobioza Disacharydy C 12 H 22 O 11 Właściwości chemiczne maltozy i celobiozy po hydrolizie tworzą glukozę ulegają mutarotacji: maltoza α (168 ), β (112 ) tworzą osazony maltaza, distaza wiązanie α- glikozydowe emulsyna wiązanie β- glikozydowe wykazują właściwości redukujące (redukują odczynniki: Tollensa, Fehlinga, Benedicta) utleniają się do kwasów bionowych tworzą pochodne: oktametylową (CH 3 J, Ag 2 O) i oktaacetylową (CH 3 COCl) dwa mole glukozy trawiona przez ludzi fermentowana przez bakterie nietrawiona przez ludzi niefermentowana przez bakterie Disacharydy Laktoza cukier mleczny Disacharydy Sacharoza (buraki cukrowe 15%, trzcina cukrowa 20%) właściwości chemiczne: cukier nieredukujący, nie redukuje odczynników T. i B., nie ulega mutarotacji, nie tworzy osazonu, oksymu, glikozydów rozszczepiana przez inwertazę na glukozę i fruktozę (zmiana skręcalności z (+66.5 ) na (-22 ): cukier inwertowany tworzy pochodne oktametylową (CH 3 J, Ag 2 O) i oktaacetylową (CH 3 COCl) właściwości chemiczne podobne jak maltoza i celobioza wiązanie C1-C2 rozszczepiana przez emulsynę (wiązanie β-glikozydowe) na glukozę i galaktozę właściwości redukujące w cząsteczce glukozy β-d-fruktofuranozylo-α-d-glukopiranozyd α-d-glukopiranozylo-β-d-fruktofuranozyd
21 Polisacharydy Polisacharydy Skrobia - Materiał zapasowy roślin Amyloza Amylopektyna celobioza maltoza częściowa hydroliza: celuloza skrobia całkowita hydroliza: glukoza celuloza materiał budulcowy roślin 20%, rozpuszczalna w wodzie 80%, nierozpuszczalna w wodzie azotan celulozy nitroceluloza octan celulozy-jedwab hydroliza skrobi (H +, enzymy) dekstryny maltoza glukoza ( ) Polisacharydy Amylopektyna Sacharydy Słodkość Glikogen Związki heterocykliczne Związki heterocykliczne pięcioczłonowe - aromatyczność _ + tlenek etylenu prolina N, O, S heteroatomy piran Związki heterocykliczne sześcioczłonowe pirydyna nie aromatyczny aromatyczny + _
22 Zasadowość amin heterocyklicznych piperydyna pirolidyna pirydyna pirol piran Inne aminy heterocykliczne pk a = ok. 11 pk a = 5.3 pk a = 0.4 Inne aminy heterocykliczne pk a jonów amoniowych alkaloidy związki biologicznie czynne, np. morfina, kodeina, kofeina, nikotyna zasady nukleinowe Kwasy nukleinowe hν parowanie zasad podwójna helisa * wiązania wodorowe N-H, O-H tekst tekst
Aminokwasy (α-) Aminokwasy. Aminokwasy. Aminokwasy. Aaminokwasy. klasyfikacja, budowa chemiczna. klasyfikacja, budowa chemiczna
 (α-) * * aldehyd L-glicerynowy (S) L-seryna (S) klasyfikacja budowa chemiczna położenie grupy NH 2 :α, β, γ, δ... ω rzędowość grupy NH 2 : 1, 2 ilość grup COOH i NH 2 COOH = NH 2 : obojętne COOH > NH 2
(α-) * * aldehyd L-glicerynowy (S) L-seryna (S) klasyfikacja budowa chemiczna położenie grupy NH 2 :α, β, γ, δ... ω rzędowość grupy NH 2 : 1, 2 ilość grup COOH i NH 2 COOH = NH 2 : obojętne COOH > NH 2
Aminy właściwości fizyczne
 Klasyfikacja amin 1 2 3 alifatyczne aromatyczne Budowa przestrzenna amin wiązanie wodorowe Aminy właściwości fizyczne polarne do C 5 rozpuszczalne w wodzie temperatura wrzenia Właściwości zasadowe amin
Klasyfikacja amin 1 2 3 alifatyczne aromatyczne Budowa przestrzenna amin wiązanie wodorowe Aminy właściwości fizyczne polarne do C 5 rozpuszczalne w wodzie temperatura wrzenia Właściwości zasadowe amin
Wykład 23 I 2019 Żywienie
 Wykład 23 I 2019 Żywienie Witold Bekas SGGW Węglowodany - cukrowce Nazwa pochodzi od wzoru sumarycznego: C x (H 2 O) y wodziany węgla Ogólnie definiuje się je jako: polihydroksyaldehydy i polihydroksyketony
Wykład 23 I 2019 Żywienie Witold Bekas SGGW Węglowodany - cukrowce Nazwa pochodzi od wzoru sumarycznego: C x (H 2 O) y wodziany węgla Ogólnie definiuje się je jako: polihydroksyaldehydy i polihydroksyketony
Aminokwasy (α-) L-seryna (S) aldehyd L-glicerynowy (S)
 Aminokwasy (α-) * * aldehyd L-glicerynowy (S) L-seryna (S) Aminokwasy klasyfikacja budowa chemiczna położenie grupy NH 2 :α, β, γ, δ... ω rzędowość grupy NH 2 : 1, 2 ilość grup COOH i NH 2 COOH = NH 2
Aminokwasy (α-) * * aldehyd L-glicerynowy (S) L-seryna (S) Aminokwasy klasyfikacja budowa chemiczna położenie grupy NH 2 :α, β, γ, δ... ω rzędowość grupy NH 2 : 1, 2 ilość grup COOH i NH 2 COOH = NH 2
Weglowodany. Nazwa pochodzi od wzoru sumarycznego: C x (H 2. O) y
 Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
IZOMERIA Izomery - związki o takim samym składzie lecz różniące się budową
 IZMERIA Izomery - związki o takim samym składzie lecz różniące się budową TAK zy atomy są tak samo połączone? NIE izomery konstytucyjne stereoizomery zy odbicie lustrzane daje się nałożyć na cząsteczkę?
IZMERIA Izomery - związki o takim samym składzie lecz różniące się budową TAK zy atomy są tak samo połączone? NIE izomery konstytucyjne stereoizomery zy odbicie lustrzane daje się nałożyć na cząsteczkę?
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Makrocząsteczki. Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe
 Makrocząsteczki Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe Syntetyczne: -Elastomery bardzo duża elastyczność charakterystyczna dla gumy -Włókna długie,
Makrocząsteczki Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe Syntetyczne: -Elastomery bardzo duża elastyczność charakterystyczna dla gumy -Włókna długie,
Aminy właściwości fizyczne
 alifatyczne aromatyczne Klasyfikacja amin 1 2 3 wiązanie wodorowe Aminy właściwości fizyczne polarne do C 5 rozpuszczalne w wodzie Budowa przestrzenna amin temperatura wrzenia Właściwości zasadowe amin
alifatyczne aromatyczne Klasyfikacja amin 1 2 3 wiązanie wodorowe Aminy właściwości fizyczne polarne do C 5 rozpuszczalne w wodzie Budowa przestrzenna amin temperatura wrzenia Właściwości zasadowe amin
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
CHEMIA 12. Wzorcem konfiguracji względnej H C * OH HO C * H (odmiany L i D) jest aldehyd glicerynowy CH 2 OH CH 2 OH
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 12 SACHARYDY. AMINOKWASY I BIAŁKA. IZOMERIA OPTYCZNA. IZOMERIA OPTYCZNA
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 12 SACHARYDY. AMINOKWASY I BIAŁKA. IZOMERIA OPTYCZNA. IZOMERIA OPTYCZNA
Materiały dodatkowe węglowodany
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe węglowodany 1. Mutarotacja Cukry występują głównie w formie pierścieniowej zawartość formy łańcuchowej w stanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe węglowodany 1. Mutarotacja Cukry występują głównie w formie pierścieniowej zawartość formy łańcuchowej w stanie
Kwasy nasycone. Wykład 10 2
 Związki pochodzenia naturalnego biomolekuły. 1. Lipidy związki pochodzenia naturalnego, nierozpuszczalne w wodzie, łatwo rozpuszczalne w organicznych rozpuszczalnikach niepolarnych i słabo polarnych. Dzielą
Związki pochodzenia naturalnego biomolekuły. 1. Lipidy związki pochodzenia naturalnego, nierozpuszczalne w wodzie, łatwo rozpuszczalne w organicznych rozpuszczalnikach niepolarnych i słabo polarnych. Dzielą
II ROK CHEMII GRUPA C1 Zadania na 17 stycznia 2011 r. Cukry odpowiedzi. 1. Zapisz wzory Fischera produktów reakcji D-glukozy z: a.
 16 stycznia 2011 roku II RK EMII GRUPA 1 Zadania na 17 stycznia 2011 r. ukry odpowiedzi 1. Zapisz wzory Fischera produktów reakcji D-glukozy z: a. Br 2 2 kwas D-glukonowy (ogólnie: kwas aldonowy) b. stęż.
16 stycznia 2011 roku II RK EMII GRUPA 1 Zadania na 17 stycznia 2011 r. ukry odpowiedzi 1. Zapisz wzory Fischera produktów reakcji D-glukozy z: a. Br 2 2 kwas D-glukonowy (ogólnie: kwas aldonowy) b. stęż.
Węglowodany. Monosacharydy Oligosacharydy Polisacharydy. Skrobia Celuloza Glikogen. Aldopentozy (ryboza) Disacharydy. Ketopentozy (rybuloza)
 Cz. XXVIII-a Węglowodany - cukry - sacharydy: klasyfikacja, budowa, nazewnictwo i izomeria I. Definicja i klasyfikacja Węglowodany to polihydroksylowe aldehydy i ketony oraz ich pochodne Węglowodany Monosacharydy
Cz. XXVIII-a Węglowodany - cukry - sacharydy: klasyfikacja, budowa, nazewnictwo i izomeria I. Definicja i klasyfikacja Węglowodany to polihydroksylowe aldehydy i ketony oraz ich pochodne Węglowodany Monosacharydy
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Podział związków organicznych
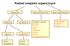 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Wstęp Wybrane zagadnienia z chemii związków naturalnych
 Wstęp Wybrane zagadnienia z chemii związków naturalnych wykład 15 h zaliczenie test otwarty Literatura: 1. Natural Products hemistry Raymound ooper, George Nicola, Taylor&Francis Group, 2015 2. Selected
Wstęp Wybrane zagadnienia z chemii związków naturalnych wykład 15 h zaliczenie test otwarty Literatura: 1. Natural Products hemistry Raymound ooper, George Nicola, Taylor&Francis Group, 2015 2. Selected
21. Wstęp do chemii a-aminokwasów
 21. Wstęp do chemii a-aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2016/2017 1 21.1. Budowa ogólna a-aminokwasów i klasyfikacja peptydów H 2 N H kwas 2-aminooctowy
21. Wstęp do chemii a-aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2016/2017 1 21.1. Budowa ogólna a-aminokwasów i klasyfikacja peptydów H 2 N H kwas 2-aminooctowy
46 i 47. Wstęp do chemii -aminokwasów
 46 i 47. Wstęp do chemii -aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 21.1. Budowa ogólna -aminokwasów i klasyfikacja peptydów H 2 H H 2 R H R R 1 H
46 i 47. Wstęp do chemii -aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 21.1. Budowa ogólna -aminokwasów i klasyfikacja peptydów H 2 H H 2 R H R R 1 H
Slajd 1. Slajd 2. Proteiny. Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) Kwas α-aminokarboksylowy aminokwas
 Slajd 1 Proteiny Slajd 2 Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) wiązanie amidowe Kwas α-aminokarboksylowy aminokwas Slajd 3 Aminokwasy z alifatycznym łańcuchem
Slajd 1 Proteiny Slajd 2 Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) wiązanie amidowe Kwas α-aminokarboksylowy aminokwas Slajd 3 Aminokwasy z alifatycznym łańcuchem
WĘGLOWODANY. 2n C 6 H 12 O 6. n C 12 H 22 O 11. [C 12 H 20 O 10 ] n 1 CH 2 OH C O CHOH O C 5 CH 2 OH 5 CHOH CHOH H O. Chiralność monosacharydów.
![WĘGLOWODANY. 2n C 6 H 12 O 6. n C 12 H 22 O 11. [C 12 H 20 O 10 ] n 1 CH 2 OH C O CHOH O C 5 CH 2 OH 5 CHOH CHOH H O. Chiralność monosacharydów. WĘGLOWODANY. 2n C 6 H 12 O 6. n C 12 H 22 O 11. [C 12 H 20 O 10 ] n 1 CH 2 OH C O CHOH O C 5 CH 2 OH 5 CHOH CHOH H O. Chiralność monosacharydów.](/thumbs/74/69994408.jpg) WĘGLWDANY WĘGLWDANY [ 0 0 ] n n n n n skrobia maltoza glukoza polisacharyd disacharyd monosacharyd ALDZA aldehyd glicerynowy KETZA dihydroksyaceton hydrolizuje do n cząsteczek monosacharydów ALDZY hydrolizuje
WĘGLWDANY WĘGLWDANY [ 0 0 ] n n n n n skrobia maltoza glukoza polisacharyd disacharyd monosacharyd ALDZA aldehyd glicerynowy KETZA dihydroksyaceton hydrolizuje do n cząsteczek monosacharydów ALDZY hydrolizuje
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Węglowodany (Cukry) Część 2. Związki wielofunkcyjne
 Węglowodany (Cukry) Część 2 Związki wielofunkcyjne Monosacharydy Glukoza, Fruktoza: - wzory łańcuchowe, wzory Fishera, - właściwości fizyczne i chemiczne (zależności między budową a właściwościami) - funkcje
Węglowodany (Cukry) Część 2 Związki wielofunkcyjne Monosacharydy Glukoza, Fruktoza: - wzory łańcuchowe, wzory Fishera, - właściwości fizyczne i chemiczne (zależności między budową a właściwościami) - funkcje
Slajd 1. Slajd 2. Węglowodany. Węglowodany. Wzór sumaryczny C n (H 2 O) n
 Slajd 1 Węglowodany Slajd 2 Wzór sumaryczny C n (H 2 O) n Węglowodany D-glukoza polihydroksy aldehyd D-fruktoza polihydroksy keton Związki, które hydrolizują do polihydroksy aldehydów lub ketonów są również
Slajd 1 Węglowodany Slajd 2 Wzór sumaryczny C n (H 2 O) n Węglowodany D-glukoza polihydroksy aldehyd D-fruktoza polihydroksy keton Związki, które hydrolizują do polihydroksy aldehydów lub ketonów są również
Skala słodkości cukrów Laktoza < maltoza < glukoza < sacharoza < fruktoza najsłodsza
 Źródła cukrów (węglowodanów) w produktach spożywczych: Warzywa i owoce (winogrona cukier gronowy glukoza) Produkty zbożowe: pieczywo, kasze, płatki śniadaniowe Funkcja węglowodanów w organizmie: Energetyczna:
Źródła cukrów (węglowodanów) w produktach spożywczych: Warzywa i owoce (winogrona cukier gronowy glukoza) Produkty zbożowe: pieczywo, kasze, płatki śniadaniowe Funkcja węglowodanów w organizmie: Energetyczna:
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Chemiczne składniki komórek
 Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
CHO H OH CH 2. D-(-)-ryboza H H OH HO. D-(+)-alloza D-(+)-altroza D-(+)-glukoza D-(+)-mannoza D-(+)-guloza D-(-)-idoza D-(+)-galaktoza D-(+)-taloza
 aldehyd D-()-glicerynowy U K Y D-(-)-ryboza D-(-)-erytroza D-(-)-arabinoza ryby arabski książe łyka. D-()-ksyloza D-(-)-treoza D-(-)-liksoza aluzyjny altruista gluchy mandaryn gulgocze idąc galerią talentów
aldehyd D-()-glicerynowy U K Y D-(-)-ryboza D-(-)-erytroza D-(-)-arabinoza ryby arabski książe łyka. D-()-ksyloza D-(-)-treoza D-(-)-liksoza aluzyjny altruista gluchy mandaryn gulgocze idąc galerią talentów
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/67/57994710.jpg) Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
Weglowodany. wodziany węgla Ogólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony. O) y
 Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
mie i sz s an a in i a rac r e ac miczn ic a /rac /r e ac mat/ E ime m ry
 Wzór sumaryczny Węglowodany C n H 2n O n Aldehydowe lub ketonowe pochodne alkoholi wielowodorotlenowych Węglowodany - podział CUKRY PROSTE Monosacharydy CUKRY ZŁOŻONE Oligosacharydy (kilka reszt cukrów
Wzór sumaryczny Węglowodany C n H 2n O n Aldehydowe lub ketonowe pochodne alkoholi wielowodorotlenowych Węglowodany - podział CUKRY PROSTE Monosacharydy CUKRY ZŁOŻONE Oligosacharydy (kilka reszt cukrów
Cukry. C x H 2y O y lub C x (H 2 O) y
 Cukry Cukry organiczne związki chemiczne składające się z atomów węgla oraz wodoru i tlenu, zazwyczaj w stosunku H:O = 2:1. Zawierają liczne grupy hydroksylowe, karbonylowe a czasami mostki półacetalowe.
Cukry Cukry organiczne związki chemiczne składające się z atomów węgla oraz wodoru i tlenu, zazwyczaj w stosunku H:O = 2:1. Zawierają liczne grupy hydroksylowe, karbonylowe a czasami mostki półacetalowe.
11. ALDEHYDY, KETONY CH 2. hydroksyloamina. hydrazyna fenylohydrazyna SO 4. semikarbazyd
 11. ALDEYDY, KETY 1. Podać nazwy następujących związków uwzględniając izomerię. C e. f. C g. h. C i. j. k. l. 2. kreślić typ hybrydyzacji atomów węgla, podać rodzaje wiązań chemicznych, kąty między wiązaniami,
11. ALDEYDY, KETY 1. Podać nazwy następujących związków uwzględniając izomerię. C e. f. C g. h. C i. j. k. l. 2. kreślić typ hybrydyzacji atomów węgla, podać rodzaje wiązań chemicznych, kąty między wiązaniami,
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna
 Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
1. Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Przegląd budowy i funkcji białek
 Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
I. Część teoretyczna aldozy ketozy
 I. Część teoretyczna Sacharydy (inaczej cukry) są to polihydroksyaldehydy i polihydroksyketony oraz niektóre ich pochodne (aminosacharydy, deoksysacharydy, kwasy uronowe). Nazwa sacharydy wywodzi się od
I. Część teoretyczna Sacharydy (inaczej cukry) są to polihydroksyaldehydy i polihydroksyketony oraz niektóre ich pochodne (aminosacharydy, deoksysacharydy, kwasy uronowe). Nazwa sacharydy wywodzi się od
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA
 CHEMIA KLASA III 2016-09-01 LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA Treści nauczania Tom III podręcznika Ciekawi świata wyd. Operon I. WĘGLOWODORY 1. Chemia organiczna jako chemia związków
CHEMIA KLASA III 2016-09-01 LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA Treści nauczania Tom III podręcznika Ciekawi świata wyd. Operon I. WĘGLOWODORY 1. Chemia organiczna jako chemia związków
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/55/35935976.jpg) KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Wymagania edukacyjne z chemii w klasie II
 Wymagania edukacyjne z chemii w klasie II kształcenie ogólne w zakresie podstawowym i rozszerzonym Program nauczania: DKOS-4015-88/02 Podręcznik: Chemia organiczna. Kształcenie ogólne w zakresie podstawowym
Wymagania edukacyjne z chemii w klasie II kształcenie ogólne w zakresie podstawowym i rozszerzonym Program nauczania: DKOS-4015-88/02 Podręcznik: Chemia organiczna. Kształcenie ogólne w zakresie podstawowym
Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1.
 1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ
 FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony.
 WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
I. Węgiel i jego związki z wodorem
 NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
WĘGLOWODORY. Uczeń: Przykłady wymagań nadobowiązkowych Uczeń:
 WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
ZWIĄZKI NATURALNE SACHARYDY
 ZWIĄZKI NATURALNE SACHARYDY 2 Związki naturalne Etap 0. i 1. ZADANIE 1. Identyfikacja węglowodanów Aldoheksoza szeregu D (związek A) w wyniku utleniania rozcieńczonym kwasem azotowym(v) tworzy kwas aldarowy
ZWIĄZKI NATURALNE SACHARYDY 2 Związki naturalne Etap 0. i 1. ZADANIE 1. Identyfikacja węglowodanów Aldoheksoza szeregu D (związek A) w wyniku utleniania rozcieńczonym kwasem azotowym(v) tworzy kwas aldarowy
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 2
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności
 Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności Kwasy Wymagania edukacyjne z podstawy programowej - klasa VIII Uczeń: definiuje pojęcie kwasy zgodnie z teorią Arrheniusa opisuje
Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności Kwasy Wymagania edukacyjne z podstawy programowej - klasa VIII Uczeń: definiuje pojęcie kwasy zgodnie z teorią Arrheniusa opisuje
Slajd 1. Slajd 2. Aminy. trietyloamina. amoniak. chlorofil
 Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY
 WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Aminokwasy, peptydy, białka
 Aminokwasy, peptydy, białka Aminokwasy KWAS 1-AMINOCYKLOPROPANOKARBOKSYLOWY α AMINOKWAS KWAS 3-AMINOPROPANOWY β AMINOKWAS KWAS 4-AMINOPROPANOWY γ AMINOKWAS KWAS 2-AMINOETANOSULFONOWY β AMINOKWAS Aminokwasy
Aminokwasy, peptydy, białka Aminokwasy KWAS 1-AMINOCYKLOPROPANOKARBOKSYLOWY α AMINOKWAS KWAS 3-AMINOPROPANOWY β AMINOKWAS KWAS 4-AMINOPROPANOWY γ AMINOKWAS KWAS 2-AMINOETANOSULFONOWY β AMINOKWAS Aminokwasy
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony
 CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
Monosacharydy Schemat konfiguracyjny
 B I T E N L EMIA G RGANIZNA I A Monosacharydy Schemat konfiguracyjny Aldozy szeregu D ustawia się w schemat wg dwu poniższych reguł: 1. Aldozy zawierające n atomów węgla otrzymuje się z aldoz zawierających
B I T E N L EMIA G RGANIZNA I A Monosacharydy Schemat konfiguracyjny Aldozy szeregu D ustawia się w schemat wg dwu poniższych reguł: 1. Aldozy zawierające n atomów węgla otrzymuje się z aldoz zawierających
WYKRYWANIE WIĄZAŃ WIELOKROTNYCH WYKRYWANIE WIĄZAŃ WIELOKROTNYCH
 WYKRYWANIE WIĄZAŃ WIELOKROTNYCH Odbarwienie wody bromowej Woda bromowa roztwór Br 2 w wodzie - Br 2 (aq): brunatna, brązowa lub ciemnoczerwona ciecz. Gdy brom przyłącza się związku nienasyconego barwa
WYKRYWANIE WIĄZAŃ WIELOKROTNYCH Odbarwienie wody bromowej Woda bromowa roztwór Br 2 w wodzie - Br 2 (aq): brunatna, brązowa lub ciemnoczerwona ciecz. Gdy brom przyłącza się związku nienasyconego barwa
Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, Spis treści
 Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, 2010 Spis treści Część II. Zagadnienia wybrane 25. Halogenki arylów. Substytucja nukleofilowa w pierścieniu
Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, 2010 Spis treści Część II. Zagadnienia wybrane 25. Halogenki arylów. Substytucja nukleofilowa w pierścieniu
Plan pracy dydaktycznej na chemii w klasach trzecich w roku szkolnym 2015/2016
 1 Agnieszka Wróbel nauczyciel biologii i chemii Wrocław,01.09.2015r. Plan pracy dydaktycznej na chemii w klasach trzecich w roku szkolnym 2015/2016 Poziom wymagań Ocena Opis wymagań podstawowe niedostateczna
1 Agnieszka Wróbel nauczyciel biologii i chemii Wrocław,01.09.2015r. Plan pracy dydaktycznej na chemii w klasach trzecich w roku szkolnym 2015/2016 Poziom wymagań Ocena Opis wymagań podstawowe niedostateczna
Umiejętności ponadpodstawowe Ocena bardzo dobra. Temat. Ocena celująca. Ocena dobra. Ocena dopuszczająca. Ocena dostateczna KWASY
 Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII, opracowane na podstawie programu nauczania chemii w szkole podstawowej
Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII, opracowane na podstawie programu nauczania chemii w szkole podstawowej
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII
 Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII Temat 1.Wzory i nazwy kwasów. dopuszczająca - zna zasady bezpiecznego posługiwania
Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII Temat 1.Wzory i nazwy kwasów. dopuszczająca - zna zasady bezpiecznego posługiwania
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
17. DODATKI Tabela 1. Symbole okre laj ce wielokrotno ci i podwielokrotno ci ułamków dziesi tnych Symbol Okre lenie Wielokrotno Tabela 2.
 17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
Cz. XXVIII - c Węglowodany - cukry - sacharydy: disacharydy i polisacharydy
 Cz. XXVIII - c Węglowodany - cukry - sacharydy: disacharydy i polisacharydy I. Budowa i właściwości disacharydów Wiązanie między monosacharydami powstaje z udziałem dwóch grup hydroksylowych pochodzących
Cz. XXVIII - c Węglowodany - cukry - sacharydy: disacharydy i polisacharydy I. Budowa i właściwości disacharydów Wiązanie między monosacharydami powstaje z udziałem dwóch grup hydroksylowych pochodzących
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery.
 CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
REAKCJE CHARAKTERYSTYCZNE CUKRÓW
 REAKCJE CHARAKTERYSTYCZNE CUKRÓW Grupa związków organicznych nazywanych węglowodanami, cukrami lub sacharydami obejmuje polihydroksylowe aldehydy i ketony oraz ich pochodne. Nazwa węglowodany pochodzi
REAKCJE CHARAKTERYSTYCZNE CUKRÓW Grupa związków organicznych nazywanych węglowodanami, cukrami lub sacharydami obejmuje polihydroksylowe aldehydy i ketony oraz ich pochodne. Nazwa węglowodany pochodzi
Informacje. W sprawach organizacyjnych Slajdy z wykładów
 Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Weglowodany. wodziany węgla Ogólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony. O) y
 Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wymagania programowe na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
ALDEHYDY, KETONY. 1. Podać nazwy systematyczne i zwyczajowe następujących związków, uwzględnić izomerię:
 ALDEYDY, KETY 1. Podać nazwy systematyczne i zwyczajowe następujących związków, uwzględnić izomerię: C 3 C b. C 3 CC 3 d. e. f. g. h. C i. C *j. k. C C 2 *l. ł. 2. Uzasadnić, dlaczego związki karbonylowe
ALDEYDY, KETY 1. Podać nazwy systematyczne i zwyczajowe następujących związków, uwzględnić izomerię: C 3 C b. C 3 CC 3 d. e. f. g. h. C i. C *j. k. C C 2 *l. ł. 2. Uzasadnić, dlaczego związki karbonylowe
WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej
 Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Protokół: Reakcje charakterystyczne cukrowców
 Protokół: Reakcje charakterystyczne cukrowców 1. Rekcja na obecność cukrów: próba Molischa z -naftolem Jest to najbardziej ogólna reakcja na cukrowce, tak wolne jak i związane. Ujemny jej wynik wyklucza
Protokół: Reakcje charakterystyczne cukrowców 1. Rekcja na obecność cukrów: próba Molischa z -naftolem Jest to najbardziej ogólna reakcja na cukrowce, tak wolne jak i związane. Ujemny jej wynik wyklucza
Węglowodany (Cukry) Część 3. Związki wielofunkcyjne
 Węglowodany (Cukry) Część 3 Związki wielofunkcyjne Glikozydy Monosacharydy Ryboza, Deoksyryboza: - wzory - funkcje biologiczne, pochodne Disacharydy Sacharoza, Celobioza, Maltoza,Laktoza - wzór - właściwości
Węglowodany (Cukry) Część 3 Związki wielofunkcyjne Glikozydy Monosacharydy Ryboza, Deoksyryboza: - wzory - funkcje biologiczne, pochodne Disacharydy Sacharoza, Celobioza, Maltoza,Laktoza - wzór - właściwości
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
WYMAGANIA EDUKACYJNE KLASA 3A - CHEMIA rok szkolny2018/19. Węglowodory
 WYMAGANIA EDUKACYJNE KLASA 3A - CHEMIA rok szkolny2018/19 Jarosław Kuśnierz Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje
WYMAGANIA EDUKACYJNE KLASA 3A - CHEMIA rok szkolny2018/19 Jarosław Kuśnierz Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje
spektroskopia elektronowa (UV-vis)
 spektroskopia elektronowa (UV-vis) rodzaje przejść elektronowych Energia σ* π* 3 n 3 π σ σ σ* daleki nadfiolet (λ max < 200 nm) π π* bliski nadfiolet jednostki energii atomowa jednostka energii = energia
spektroskopia elektronowa (UV-vis) rodzaje przejść elektronowych Energia σ* π* 3 n 3 π σ σ σ* daleki nadfiolet (λ max < 200 nm) π π* bliski nadfiolet jednostki energii atomowa jednostka energii = energia
WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19. Chemia organiczna jako chemia związków węgla
 Jarosław Kuśnierz WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19 Chemia organiczna jako chemia związków węgla Ocena dopuszczająca [1] pojęcie chemii organicznej pierwiastki chemiczne wchodzące w skład
Jarosław Kuśnierz WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19 Chemia organiczna jako chemia związków węgla Ocena dopuszczająca [1] pojęcie chemii organicznej pierwiastki chemiczne wchodzące w skład
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
Przedmiotowy system oceniania z CHEMII Zakres rozszerzony- klasa 3
 Przedmiotowy system oceniania z CHEMII Zakres rozszerzony- klasa 3 I Liceum Ogólnokształcące w Turku I. Wstęp Sprawdzaniu podlegają umiejętności i wiedza. W szczególności: - umiejętne stosowanie terminów,
Przedmiotowy system oceniania z CHEMII Zakres rozszerzony- klasa 3 I Liceum Ogólnokształcące w Turku I. Wstęp Sprawdzaniu podlegają umiejętności i wiedza. W szczególności: - umiejętne stosowanie terminów,
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne:
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Ocena dobra [ ]
![Ocena dobra [ ] Ocena dobra [ ]](/thumbs/51/27931734.jpg) Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
Wymagania programowe na poszczególne oceny
 Przedmiot: chemia Klasa: IIIa, IIIb Nauczyciel: Agata SROKA Wymagania programowe na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną
Przedmiot: chemia Klasa: IIIa, IIIb Nauczyciel: Agata SROKA Wymagania programowe na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną
