Aminokwasy (α-) Aminokwasy. Aminokwasy. Aminokwasy. Aaminokwasy. klasyfikacja, budowa chemiczna. klasyfikacja, budowa chemiczna
|
|
|
- Amelia Olszewska
- 6 lat temu
- Przeglądów:
Transkrypt
1 (α-) * * aldehyd L-glicerynowy (S) L-seryna (S) klasyfikacja budowa chemiczna położenie grupy NH 2 :α, β, γ, δ... ω rzędowość grupy NH 2 : 1, 2 ilość grup COOH i NH 2 COOH = NH 2 : obojętne COOH > NH 2 : kwasowe NH 2 >COOH : zasadowe inne pierwiastki: siarka inne grupy funkcyjne: OH, pierścień aromatyczny klasyfikacja znaczenie biologiczne białkowe (20) / niebiałkowe podstawowe (10) (egzogenne, niesyntezowane, dostarczane) / pozostałe (10) (endogenne, syntezowane) klasyfikacja, budowa chemiczna glicyna leucyna H i-bu klasyfikacja, budowa chemiczna fenyloalanina seryna alanina Me izoleucyna s-bu treonina tyrozyna walina i-pr R H lub grupa alkilowa grupa OH i/lub Ph Aaminokwasy klasyfikacja, budowa chemiczna cysteina prolina klasyfikacja, budowa chemiczna kwas asparaginowy asparagina metionina tryptofan kwas glutaminowy glutamina siarkowe z pierścieniem pirolidyny kwasowe obojętne amidy kwasowych 1
2 klasyfikacja, budowa chemiczna lizyna histydyna Właściwości nielotne, krystaliczne, wysokie temperatury topnienia nierozpuszczalne w rozpuszczalnikach organicznych rozpuszczalne w wodzie duży moment dipolowy w roztworach wodnych bardzo niskie stałe kwasowości i zasadowości w porównaniu z kwasami i aminami arginina zasadowe Właściwości amfoteryczne jon obojnaczy jon dipolowy Właściwości glicyna sól wewnętrzna K a = 1.6 x kwasy k. K a = 10-5 centrum zasadowe zasada mocniejsza kwas słabszy K b = 2.5 x kwas mocniejszy zasada słabsza aminy K b = 10-4 centrum kwasowe Właściwości amfoteryczne, punkt izoelektryczny Właściwości amfoteryczne lizyna glicyna kwas asparaginowy ph = pi = 9.74 ph = pi = 5.97 ph = pi = 2.77 punkt izoelektryczny (pi) = wartość ph, przy której aminokwas jest w roztworze w postaci jonów obojnaczych ph = 5.97 < pi (kwasowe) ph = pi = 5.97 (obojętne) ph = 5.97 > pi (zasadowe) aminokwasy obojętne pi = aminokwasy zasadowe pi = aminokwasy kwasowe pi = kation jon obojnaczy anion 2
3 Elektroforeza rozdział aminokwasów w polu elektrycznym Otrzymywanie aminokwasów reakcja Hella-Volharda-Zielinskiego katoda anoda reakcja Streckera kation jon obojnaczy anion reakcja Gabriela aminowanie ftalimidkiem potasowym Właściwości aminokwasów Właściwości grupy karboksylowej: tworzenie soli z zasadami tworzenie chlorków kwasowych z SOCl 2 tworzenie estrów z alkoholami i H + tworzenie amidów (z chlorków kwasowych) sole wewn. Właściwości aminokwasów Właściwości grupy karboksylowej: tworzenie estrów z alkoholami w obecności H + dezaktywacja grupy karboksylowej Właściwości grupy aminowej: tworzenie soli z kwasami reakcja z HNO 2 tworzenie amidów (z chlorkami kwasowymi lub bezwodnikami) peptydy białka Właściwości aminokwasów Właściwości grupy aminowej acylowanie - tworzenie amidów dezaktywacja grupy karboksylowej Wykrywanie aminokwasów reakcja z ninhydryną dezaminacja: reakcja z HNO 2 fioletowa barwa Właściwości aminokwasów tworzenie wiązań amidowych mieszanina alkenów i alkoholu NH kation tert-pentylowy - H 2O, taka reakcja nie zachodzi wiązania amidowe płaskie 3
4 Amidy Pochodne kwasów karboksylowych i amin wiązanie amidowe lub bezwodnik kwasowy N, N- dipodstawiony amid glicyna Gly alanina Ala walina Val leucyna Leu izoleucyna Ile seryna Ser fenyloalanina Phe G A V L I S F treonina Thr tyrozyna Tyr cysteina Cys metionina Met prolina Pro tryptofan Trp T Y C M P W kwas asparaginowy Asp D kwas glutaminowy Glu E asparagina Asn N glutamina Gln Q lizyna Lys K arginina Arg R histydyna His H amidy: nie mają właściwości kwasowych ani zasadowych hydrolizują w obecności kwasów i zasad n = 2 2 dipeptydy n = 3 6 tripeptydów Peptydy Budowa: polimery aminokwasów n = 8 > 4000 oktapeptydów glutation Glu - Cys - Gly polipeptydy M < białka M > Peptydy Rodzaje wiązań wiązanie amidowe = peptydowe wiązanie disulfidowe N-C = nm (0.147 nm) trwałe hydroliza 35% HCl Peptydy Określanie struktury peptydów jakie aminokwasy wchodzą w skład peptydu? ile jest jednostek każdego z nich? peptyd + 35% HCl hydroliza wszystkich wiązań amidowych redukcja wszystkich wiązań disulfidowych ANALIZATOR AMINOKWASÓW chromatografia rozdział na kolumnie, wymywanie buforami Peptydy Określanie struktury peptydów w jakiej kolejności występują w łańcuchu? Sekwencjonowanie peptydów Metody chemiczne: oznaczanie reszty N-końcowej metoda Edmana metoda Sangera przyłączenie ragenta hydroliza wiązań peptydowych - odrywanie aminokwasu N-terminalnego identyfikacja Metoda enzymatyczna: oznaczanie reszty C-końcowej 4
5 - H 2 O Synteza peptydów Węglowodany C n (H 2 O) m = cukry = sacharydy polihydroksylowane aldehydy i ketony NH, 1. zablokowanie grupy NH 2 2. zablokowanie grupy COOH 3. połączenie aminokwasów (aktywacja grupy COOH) 4. usunięcie grup blokujących cukry CO 2 + H 2 O cukry proste: chlorofil C n (H 2 O) m proste: monosacharydy (monocukry) złożone: dwa lub więcej cukrów prostych: disacharydy (dwucukry) trisacharydy, tetra..., polisacharydy (wielocukry) aldozy ketozy C 4 tetroza tetruloza C 5 pentoza pentuloza C 6 heksoza heksuloza C 7 heptoza heptuloza Węglowodany = cukry Węglowodany: szereg D cukrów heksoza czynność optyczna aldehyd D-glicerynowy aldehyd glicerynowy ilość izomerów = 2 n n = ilość C* n =4 32 erytroza treoza wzór Fischera aldehyd D i L-glicerynowy ryboza arabinoza ksyloza liksoza alloza glukoza guloza galaktoza altroza mannoza idoza taloza Węglowodany: szereg D cukrów aldehyd D-(+)-glicerynowy Węglowodany D-(-)-erytroza D-(-)-treoza ryboza arabinoza glukoza mannoza galaktoza fruktoza D-(-)-ryboza D-(-)-arabinoza D-(+)-ksyloza D-(-)-liksoza D-(+)-alloza D-(+)-glukoza D-(-)- guloza D-(+)-galaktoza D-(+)- altroza D-(+)- mannoza D-(-)- idoza D-(+)- taloza 5
6 D-erytroza Węglowodany D(-)- i L(+)-erytroza Właściwości aldehydów i ketonów addycja nukleofilowa alkoholi do grupy karbonylowej hemiacetal = półacetal α β enancjomery γ- i δ-hydroksykwasy laktony = estry wewnętrzne γ- i δ-hydroksyaldehydy i ketony wewnętrzne hemiacetale lub acetale α-d-erytrofuranoza i β -D-erytrofuranoza anomery 4-hydroksybutanal * 5-hydroksypentanal * diastereoizomeryczne hemiacetalowe formy cukrów α i β o różnej konfiguracji tylko na anomerycznym = hemiacetalowym at. C furan * hemiacetalowy = anomeryczny atom C piran Hemiacetalowe formy cukrów D-glukoza Hemiacetalowe formy cukrów równowaga w roztworze wodnym wzory konformacyjne β-d-glukopiranoza i α-d-glukopiranoza wzory Hawortha = taflowe α-d-glukopiranoza (EtOH) tt 146 C [α] D forma łańcuchowa D-glukozy w równowadze [α] D β-d-glukopiranoza (EtOH-H 2 O) tt [α] D anomer β trwalszy anomer α mniej trwały 36% 0.02% 64% MUTAROTACJA forma bardziej trwała Hemiacetalowe formy cukrów równowaga w roztworze wodnym Mutarotacja MUTAROTACJA zmiana skręcalności właściwej roztworu każdej z anomerycznych form cukru do wartości odpowiadającej stanowi równowagi między: anomerami α i β (formy hemiacetalowe) oraz formą łańcuchową (forma aldehydowa) następuje dzięki otwarciu pierścienia wzory konformacyjne β-d-glukopiranoza bardziej trwała niż α-d-glukopiranoza ale β-d-mannopiranoza mniej trwała niż α-d-mannopiranoza 6
7 Ketozy Reakcje formy łańcuchowej grupy karbonylowej Reakcje formy hemiacetalowej grupy hydroksylowej hemiacetalowej rybuloza ksyluloza fruktoza = lewuloza α-d-fruktofuranoza Deoksycukry Aminocukry Cukry o rozgałęzionych łańcuchach Reakcje formy hemiacetalowej grup hydroksylowych alkoholowych 2-deoxy- D-ryboza L-daunozamina D-apioza Reakcje formy łańcuchowej grupy karbonylowej Redukcja cukrów [aldoza alditol] mannoza α-d-mannopiranoza mannitol β-d-mannopiranoza Reakcje formy łańcuchowej grupy karbonylowej Utlenianie cukrów HNO 3 aldoza kwas aldarowy galaktoza α-d-galaktopiranoza β-d-galaktopiranoza galakcytol Br 2 aldoza kwas aldonowy glukoza kwas alduronowy kwas glutarowy glukoza glucytol = sorbitol fruktoza glucytol + mannitol ksyloza kwas ksylonowy forma hemiacetalowa Reakcje formy łańcuchowej grupy karbonylowej Utlenianie cukrów odczynnik Benedicta lub Fehlinga odczynnik Tollensa Reakcje formy łańcuchowej grupy karbonylowej Utlenianie cukrów odczynnik Benedicta, odczynnik Tollensa co z fruktozą i innymi ketozami? aldoza α-d-aldopiranoza β-d-aldopiranoza α-d-aldofuranoza β-d-aldofuranoza Ag pozytywna próba Benedicta (czerwony osad Cu 2 O) pozytywna próba Tollensa (lustro srebrowe) enolizacja ketoza endiol aldoza Ag fruktoza: pozytywna próba Benedicta (czerwony osad Cu 2 O) oraz Tollensa (lustro srebrowe) aldoza kwas aldonowy aldoza ketoza dwa kwasy aldonowe dwa kwasy aldonowe 7
8 Epimeryzacja cukrów ustalanie się równowagi w roztworach zasadowych aldoz lub ketoz między: dwiema epimerycznymi (diastereoizomerycznymi) aldozami, ketozą i odpowiednią formą enolową Reakcje formy łańcuchowej grupy karbonylowej Tworzenie pochodnych krystalicznych z pochodnymi amoniaku Reakcja z hydroksyloaminą oksym D-galaktozy glukoza forma enolowa mannoza fruktoza glukoza i mannoza - epimery Reakcja z hydrazyną i fenylohydrazyną fenylohydrazon D-rybozy Reakcje formy łańcuchowej grupy karbonylowej z pochodnymi amoniaku Reakcja z nadmiarem hydrazyny i fenylohydrazyny jedna cząsteczka fenylohydrazyny jest utleniaczem Tworzenie cyjanohydryn przedłużanie łańcucha synteza Kilianiego-Fischera nowe centrum asymetrii D-arabinoza D-ryboza difenylohydrazon D-rybozy = D-arabinozy = D-rybulozy arabinoza dwie cyjanohydryny D-glukoza i D-mannoza D-rybuloza difenylohydrazon D-glukozy = D-mannozy = D-fruktozy dwie iminy dwie epimeryczne aldozy i odpowiadająca im ketoza tworzą ten sam osazon Skracanie łańcucha degradacja Wohla Ustalanie budowy cukrów Utlenianie kwasem nadjodowym rozszczepienie wiązań C C D-galaktoza oksym cyjanohydryna D-galaktozy Skracanie łańcucha degradacja Ruffa COO - ) 2Ca 2+ D-liksoza rozszczepienie dioli wicynalnych rozszczepienie związków hydroksy-karbonylowych dwa związki karbonylowe kwas + związek kaarbonylowy CaCO 3 H 2O 2, Fe 3+ rozszczepienie trioli D-ksyloza kwas sól D-treoza kwas mrówkowy + dwa związki karbonylowe 8
9 Reakcje formy łańcuchowej grupy karbonylowej Reakcje formy hemiacetalowej grupy hydroksylowej hemiacetalowej Tworzenie glikozydów Reakcje formy hemiacetalowej grup hydroksylowych alkoholowych Reakcje hemiacetalowej grupy hydroksylowej Glikozydy = Acetale cukrów hemiacetal reakcja spontaniczna acetal reakcja katalizowana α β D-glukoza α-d-glukopiranoza β-d-glukopiranoza α-d-glukozyd metylowy metylo-α-d- glukopiranozyd β-d-glukozyd metylowy metylo-β-d- glukopiranozyd O-Glikozydy = Acetale cukrów Glikozydy N-Glikozydy Reakcje formy hemiacetalowej grupy hydroksylowe Tworzenie eterów linamaryna (maniok) metylo-α-dglukopiranozyd metylo-2,3,4,6-tetra-o-metylo-α-dglukopiranozyd S-Glikozydy adenozyna (nukleozyd) trwałe wiązania eterowe synigryna (gorczyca) aglikon niecukrowa część glikozydu nietrwałe wiązanie acetalowe 2,3,4,6-tetra-O-metylo-D-glukoza hydroliza kwasowa Właściwości acetali w środowisku zasadowym i obojętnym trwałe Reakcje formy hemiacetalowej grupy hydroksylowe Tworzenie estrów = acetylowanie cukrów D-glukoza α-d-glukopiranoza β-d-glukopiranoza ZnCl 2 α Właściwości eterów trwałe w środowisku kwaśnym, zasadowym i obojętnym Fosforany AcONa β 1,2,3,4,6-penta-O-acetylo- α/β-d-lukopiranoza 9
10 Właściwości fruktozy Reakcje formy łańcuchowej grupa C=O C2!!! z H 2,Pt lub LiAlH 4 alditole z NH 2 OH oksym z NH 2 NH 2 osazon (fenyloosazon) ulega epimeryzacji z HCN rozgałęzienie łańcucha Właściwości fruktozy 2 ulega mutarotacji 2 2 Reakcje formy łańcuchowej grupy -CH 2 OH z HNO 3 kwas ketoaldarowy Fruktoza: nie reaguje z Br 2 nie ulega degradacji Wohla i Ruffa α-d-fruktofuranoza β-d-fruktofuranoza Reakcje formy hemiacetalowej grupy hydroksylowej hemiacetalowej glikozydy Reakcje formy hemiacetalowej grup hydroksylowych alkoholowych etery i estry - podsumowanie Reakcje formy łańcuchowej grupy karbonylowej (aldozy i 2-ketozy- cukry redukujące) właściwości redukujące: reakcja z odczynnikami: Tollensa, Fehlinga, Benedicta ulegają mutarotacji tworzą oksymy i fenyloosazony oraz glikozydy Reakcje formy hemiacetalowej grupy hydroksylowej hemiacetalowej glikozydy (acetale) Reakcje formy hemiacetalowej grup hydroksylowych alkoholowych etery, estry Podsumowanie reakcji cukrów + pochodne krystaliczne mieszanina anomerów α+β (CH 3) 2SO 4, NaOH Glikozydy = Acetale cukrów Disacharydy C 12 H 22 O 11 (+)-Maltoza (+)-Celobioza cukry nieredukujące nie reagują z odczynnikami: Tollensa, Fehlinga, Benedicta nie ulegają mutarotacji nie tworzą oksymów ani fenyloosazonów ponieważ pierścień nie może się otworzyć trawiona przez ludzi fermentowana przez bakterie maltaza, distaza wiązanie α- glikozydowe dwa mole glukozy nietrawiona przez ludzi emulsyna wiązanie β- glikozydowe niefermentowana przez bakterie 10
11 Disacharydy C 12 H 22 O 11 Właściwości chemiczne maltozy i celobiozy Disacharydy C 12 H 22 O 11 Dowody budowy maltozy po hydrolizie tworzą glukozę ulegają mutarotacji: maltoza α (168 ), β (112 ) tworzą osazony wykazują właściwości redukujące (redukują odczynniki: Tollensa, Fehlinga, Benedicta) utleniają się do kwasów bionowych tworzą pochodne: oktametylową (CH 3 J, Ag 2 O) i oktaacetylową (CH 3 COCl) α + β celobioza reaguje analogicznie Disacharydy Laktoza cukier mleczny Disacharydy Dowody budowy laktozy C 6H 5NHNH 2 Br 2/H 2O właściwości chemiczne podobne jak maltoza i celobioza hydroliza hydroliza rozszczepiana przez emulsynę (wiązanie β-glikozydowe) na glukozę i galaktozę właściwości redukujące w cząsteczce glukozy α + β α + β Disacharydy Polisacharydy Sacharoza (buraki cukrowe 15%, trzcina cukrowa 20%) właściwości chemiczne: cukier nieredukujący, nie redukuje odczynników T. i B., nie ulega mutarotacji, nie tworzy osazonu, oksymu, glikozydów rozszczepiana przez inwertazę na glukozę i fruktozę (zmiana skręcalności z (+66.5 ) na (-22 ): cukier inwertowany tworzy pochodne oktametylową (CH 3 J, Ag 2 O) i oktaacetylową (CH 3 COCl) celobioza maltoza częściowa hydroliza: celuloza skrobia całkowita hydroliza: glukoza wiązanie C1-C2 celuloza materiał budulcowy roślin β-d-fruktofuranozylo-α-d-glukopiranozyd α-d-glukopiranozylo-β-d-fruktofuranozyd azotan celulozy nitroceluloza octan celulozy-jedwab 11
12 Polisacharydy Skrobia - Materiał zapasowy roślin Amyloza Amylopektyna Polisacharydy Amylopektyna 20%, rozpuszczalna w wodzie 80%, nierozpuszczalna w wodzie hydroliza skrobi (H +, enzymy) dekstryny maltoza glukoza ( ) Glikogen Sacharydy Słodkość Związki heterocykliczne tlenek etylenu prolina N, O, S heteroatomy Związki heterocykliczne pięcioczłonowe - aromatyczność _ + podstawienie elektrofilowe łatwiej niż w benzenie piran Związki heterocykliczne sześcioczłonowe pirydyna Podstawienie elektrofilowe w aromatycznych związkach heterocyklicznych halogenowanie nie aromatyczny aromatyczny + _ nitrowanie podstawienie elektrofilowe trudniej niż w benzenie acylowanie Friedla-Craftsa Związki heterocykliczne pięcioczłonowe nasycone THF cenny rozpuszczalnik 12
13 Zasadowość amin heterocyklicznych piperydyna pirolidyna pirydyna pirol piran Inne aminy heterocykliczne pk a = ok. 11 pk a = 5.3 pk a = 0.4 Inne aminy heterocykliczne pk a jonów amoniowych alkaloidy związki biologicznie czynne, np. morfina, kodeina, kofeina, nikotyna zasady nukleinowe Kwasy nukleinowe parowanie zasad podwójna helisa wiązania wodorowe N-H, O-H 13
Aminy właściwości fizyczne
 Klasyfikacja amin 1 2 3 alifatyczne aromatyczne Budowa przestrzenna amin wiązanie wodorowe Aminy właściwości fizyczne polarne do C 5 rozpuszczalne w wodzie temperatura wrzenia Właściwości zasadowe amin
Klasyfikacja amin 1 2 3 alifatyczne aromatyczne Budowa przestrzenna amin wiązanie wodorowe Aminy właściwości fizyczne polarne do C 5 rozpuszczalne w wodzie temperatura wrzenia Właściwości zasadowe amin
Aminokwasy (α-) L-seryna (S) aldehyd L-glicerynowy (S)
 Aminokwasy (α-) * * aldehyd L-glicerynowy (S) L-seryna (S) Aminokwasy klasyfikacja budowa chemiczna położenie grupy NH 2 :α, β, γ, δ... ω rzędowość grupy NH 2 : 1, 2 ilość grup COOH i NH 2 COOH = NH 2
Aminokwasy (α-) * * aldehyd L-glicerynowy (S) L-seryna (S) Aminokwasy klasyfikacja budowa chemiczna położenie grupy NH 2 :α, β, γ, δ... ω rzędowość grupy NH 2 : 1, 2 ilość grup COOH i NH 2 COOH = NH 2
Związki karbonylowe: aldehydy i ketony
 Związki karbonylowe: aldehydy i ketony grupa Karbonylowa (C=O) płaska alkanal Nazewnictwo zwyczajowe Aldehydy (i kwasy) Ketony aldehyd mrówkowy aldehyd octowy aldehyd propionowy aldehyd masłowy aldehyd
Związki karbonylowe: aldehydy i ketony grupa Karbonylowa (C=O) płaska alkanal Nazewnictwo zwyczajowe Aldehydy (i kwasy) Ketony aldehyd mrówkowy aldehyd octowy aldehyd propionowy aldehyd masłowy aldehyd
Aminy właściwości fizyczne
 alifatyczne aromatyczne Klasyfikacja amin 1 2 3 wiązanie wodorowe Aminy właściwości fizyczne polarne do C 5 rozpuszczalne w wodzie Budowa przestrzenna amin temperatura wrzenia Właściwości zasadowe amin
alifatyczne aromatyczne Klasyfikacja amin 1 2 3 wiązanie wodorowe Aminy właściwości fizyczne polarne do C 5 rozpuszczalne w wodzie Budowa przestrzenna amin temperatura wrzenia Właściwości zasadowe amin
Weglowodany. Nazwa pochodzi od wzoru sumarycznego: C x (H 2. O) y
 Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Wykład 23 I 2019 Żywienie
 Wykład 23 I 2019 Żywienie Witold Bekas SGGW Węglowodany - cukrowce Nazwa pochodzi od wzoru sumarycznego: C x (H 2 O) y wodziany węgla Ogólnie definiuje się je jako: polihydroksyaldehydy i polihydroksyketony
Wykład 23 I 2019 Żywienie Witold Bekas SGGW Węglowodany - cukrowce Nazwa pochodzi od wzoru sumarycznego: C x (H 2 O) y wodziany węgla Ogólnie definiuje się je jako: polihydroksyaldehydy i polihydroksyketony
IZOMERIA Izomery - związki o takim samym składzie lecz różniące się budową
 IZMERIA Izomery - związki o takim samym składzie lecz różniące się budową TAK zy atomy są tak samo połączone? NIE izomery konstytucyjne stereoizomery zy odbicie lustrzane daje się nałożyć na cząsteczkę?
IZMERIA Izomery - związki o takim samym składzie lecz różniące się budową TAK zy atomy są tak samo połączone? NIE izomery konstytucyjne stereoizomery zy odbicie lustrzane daje się nałożyć na cząsteczkę?
Makrocząsteczki. Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe
 Makrocząsteczki Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe Syntetyczne: -Elastomery bardzo duża elastyczność charakterystyczna dla gumy -Włókna długie,
Makrocząsteczki Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe Syntetyczne: -Elastomery bardzo duża elastyczność charakterystyczna dla gumy -Włókna długie,
II ROK CHEMII GRUPA C1 Zadania na 17 stycznia 2011 r. Cukry odpowiedzi. 1. Zapisz wzory Fischera produktów reakcji D-glukozy z: a.
 16 stycznia 2011 roku II RK EMII GRUPA 1 Zadania na 17 stycznia 2011 r. ukry odpowiedzi 1. Zapisz wzory Fischera produktów reakcji D-glukozy z: a. Br 2 2 kwas D-glukonowy (ogólnie: kwas aldonowy) b. stęż.
16 stycznia 2011 roku II RK EMII GRUPA 1 Zadania na 17 stycznia 2011 r. ukry odpowiedzi 1. Zapisz wzory Fischera produktów reakcji D-glukozy z: a. Br 2 2 kwas D-glukonowy (ogólnie: kwas aldonowy) b. stęż.
CHEMIA 12. Wzorcem konfiguracji względnej H C * OH HO C * H (odmiany L i D) jest aldehyd glicerynowy CH 2 OH CH 2 OH
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 12 SACHARYDY. AMINOKWASY I BIAŁKA. IZOMERIA OPTYCZNA. IZOMERIA OPTYCZNA
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 12 SACHARYDY. AMINOKWASY I BIAŁKA. IZOMERIA OPTYCZNA. IZOMERIA OPTYCZNA
Węglowodany. Monosacharydy Oligosacharydy Polisacharydy. Skrobia Celuloza Glikogen. Aldopentozy (ryboza) Disacharydy. Ketopentozy (rybuloza)
 Cz. XXVIII-a Węglowodany - cukry - sacharydy: klasyfikacja, budowa, nazewnictwo i izomeria I. Definicja i klasyfikacja Węglowodany to polihydroksylowe aldehydy i ketony oraz ich pochodne Węglowodany Monosacharydy
Cz. XXVIII-a Węglowodany - cukry - sacharydy: klasyfikacja, budowa, nazewnictwo i izomeria I. Definicja i klasyfikacja Węglowodany to polihydroksylowe aldehydy i ketony oraz ich pochodne Węglowodany Monosacharydy
21. Wstęp do chemii a-aminokwasów
 21. Wstęp do chemii a-aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2016/2017 1 21.1. Budowa ogólna a-aminokwasów i klasyfikacja peptydów H 2 N H kwas 2-aminooctowy
21. Wstęp do chemii a-aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2016/2017 1 21.1. Budowa ogólna a-aminokwasów i klasyfikacja peptydów H 2 N H kwas 2-aminooctowy
46 i 47. Wstęp do chemii -aminokwasów
 46 i 47. Wstęp do chemii -aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 21.1. Budowa ogólna -aminokwasów i klasyfikacja peptydów H 2 H H 2 R H R R 1 H
46 i 47. Wstęp do chemii -aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 21.1. Budowa ogólna -aminokwasów i klasyfikacja peptydów H 2 H H 2 R H R R 1 H
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Wstęp Wybrane zagadnienia z chemii związków naturalnych
 Wstęp Wybrane zagadnienia z chemii związków naturalnych wykład 15 h zaliczenie test otwarty Literatura: 1. Natural Products hemistry Raymound ooper, George Nicola, Taylor&Francis Group, 2015 2. Selected
Wstęp Wybrane zagadnienia z chemii związków naturalnych wykład 15 h zaliczenie test otwarty Literatura: 1. Natural Products hemistry Raymound ooper, George Nicola, Taylor&Francis Group, 2015 2. Selected
CHO H OH CH 2. D-(-)-ryboza H H OH HO. D-(+)-alloza D-(+)-altroza D-(+)-glukoza D-(+)-mannoza D-(+)-guloza D-(-)-idoza D-(+)-galaktoza D-(+)-taloza
 aldehyd D-()-glicerynowy U K Y D-(-)-ryboza D-(-)-erytroza D-(-)-arabinoza ryby arabski książe łyka. D-()-ksyloza D-(-)-treoza D-(-)-liksoza aluzyjny altruista gluchy mandaryn gulgocze idąc galerią talentów
aldehyd D-()-glicerynowy U K Y D-(-)-ryboza D-(-)-erytroza D-(-)-arabinoza ryby arabski książe łyka. D-()-ksyloza D-(-)-treoza D-(-)-liksoza aluzyjny altruista gluchy mandaryn gulgocze idąc galerią talentów
Kwasy nasycone. Wykład 10 2
 Związki pochodzenia naturalnego biomolekuły. 1. Lipidy związki pochodzenia naturalnego, nierozpuszczalne w wodzie, łatwo rozpuszczalne w organicznych rozpuszczalnikach niepolarnych i słabo polarnych. Dzielą
Związki pochodzenia naturalnego biomolekuły. 1. Lipidy związki pochodzenia naturalnego, nierozpuszczalne w wodzie, łatwo rozpuszczalne w organicznych rozpuszczalnikach niepolarnych i słabo polarnych. Dzielą
Materiały dodatkowe węglowodany
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe węglowodany 1. Mutarotacja Cukry występują głównie w formie pierścieniowej zawartość formy łańcuchowej w stanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe węglowodany 1. Mutarotacja Cukry występują głównie w formie pierścieniowej zawartość formy łańcuchowej w stanie
WĘGLOWODANY. 2n C 6 H 12 O 6. n C 12 H 22 O 11. [C 12 H 20 O 10 ] n 1 CH 2 OH C O CHOH O C 5 CH 2 OH 5 CHOH CHOH H O. Chiralność monosacharydów.
![WĘGLOWODANY. 2n C 6 H 12 O 6. n C 12 H 22 O 11. [C 12 H 20 O 10 ] n 1 CH 2 OH C O CHOH O C 5 CH 2 OH 5 CHOH CHOH H O. Chiralność monosacharydów. WĘGLOWODANY. 2n C 6 H 12 O 6. n C 12 H 22 O 11. [C 12 H 20 O 10 ] n 1 CH 2 OH C O CHOH O C 5 CH 2 OH 5 CHOH CHOH H O. Chiralność monosacharydów.](/thumbs/74/69994408.jpg) WĘGLWDANY WĘGLWDANY [ 0 0 ] n n n n n skrobia maltoza glukoza polisacharyd disacharyd monosacharyd ALDZA aldehyd glicerynowy KETZA dihydroksyaceton hydrolizuje do n cząsteczek monosacharydów ALDZY hydrolizuje
WĘGLWDANY WĘGLWDANY [ 0 0 ] n n n n n skrobia maltoza glukoza polisacharyd disacharyd monosacharyd ALDZA aldehyd glicerynowy KETZA dihydroksyaceton hydrolizuje do n cząsteczek monosacharydów ALDZY hydrolizuje
Slajd 1. Slajd 2. Węglowodany. Węglowodany. Wzór sumaryczny C n (H 2 O) n
 Slajd 1 Węglowodany Slajd 2 Wzór sumaryczny C n (H 2 O) n Węglowodany D-glukoza polihydroksy aldehyd D-fruktoza polihydroksy keton Związki, które hydrolizują do polihydroksy aldehydów lub ketonów są również
Slajd 1 Węglowodany Slajd 2 Wzór sumaryczny C n (H 2 O) n Węglowodany D-glukoza polihydroksy aldehyd D-fruktoza polihydroksy keton Związki, które hydrolizują do polihydroksy aldehydów lub ketonów są również
Slajd 1. Slajd 2. Proteiny. Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) Kwas α-aminokarboksylowy aminokwas
 Slajd 1 Proteiny Slajd 2 Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) wiązanie amidowe Kwas α-aminokarboksylowy aminokwas Slajd 3 Aminokwasy z alifatycznym łańcuchem
Slajd 1 Proteiny Slajd 2 Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) wiązanie amidowe Kwas α-aminokarboksylowy aminokwas Slajd 3 Aminokwasy z alifatycznym łańcuchem
Weglowodany. wodziany węgla Ogólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony. O) y
 Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
mie i sz s an a in i a rac r e ac miczn ic a /rac /r e ac mat/ E ime m ry
 Wzór sumaryczny Węglowodany C n H 2n O n Aldehydowe lub ketonowe pochodne alkoholi wielowodorotlenowych Węglowodany - podział CUKRY PROSTE Monosacharydy CUKRY ZŁOŻONE Oligosacharydy (kilka reszt cukrów
Wzór sumaryczny Węglowodany C n H 2n O n Aldehydowe lub ketonowe pochodne alkoholi wielowodorotlenowych Węglowodany - podział CUKRY PROSTE Monosacharydy CUKRY ZŁOŻONE Oligosacharydy (kilka reszt cukrów
Przegląd budowy i funkcji białek
 Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Węglowodany (Cukry) Część 2. Związki wielofunkcyjne
 Węglowodany (Cukry) Część 2 Związki wielofunkcyjne Monosacharydy Glukoza, Fruktoza: - wzory łańcuchowe, wzory Fishera, - właściwości fizyczne i chemiczne (zależności między budową a właściwościami) - funkcje
Węglowodany (Cukry) Część 2 Związki wielofunkcyjne Monosacharydy Glukoza, Fruktoza: - wzory łańcuchowe, wzory Fishera, - właściwości fizyczne i chemiczne (zależności między budową a właściwościami) - funkcje
Cukry. C x H 2y O y lub C x (H 2 O) y
 Cukry Cukry organiczne związki chemiczne składające się z atomów węgla oraz wodoru i tlenu, zazwyczaj w stosunku H:O = 2:1. Zawierają liczne grupy hydroksylowe, karbonylowe a czasami mostki półacetalowe.
Cukry Cukry organiczne związki chemiczne składające się z atomów węgla oraz wodoru i tlenu, zazwyczaj w stosunku H:O = 2:1. Zawierają liczne grupy hydroksylowe, karbonylowe a czasami mostki półacetalowe.
Chemiczne składniki komórek
 Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
I. Część teoretyczna aldozy ketozy
 I. Część teoretyczna Sacharydy (inaczej cukry) są to polihydroksyaldehydy i polihydroksyketony oraz niektóre ich pochodne (aminosacharydy, deoksysacharydy, kwasy uronowe). Nazwa sacharydy wywodzi się od
I. Część teoretyczna Sacharydy (inaczej cukry) są to polihydroksyaldehydy i polihydroksyketony oraz niektóre ich pochodne (aminosacharydy, deoksysacharydy, kwasy uronowe). Nazwa sacharydy wywodzi się od
Weglowodany. wodziany węgla Ogólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony. O) y
 Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Weglowodany Nazwa pochodzi od wzoru sumarycznego: C x ( 2 ) y wodziany węgla gólnie definiuje się je jako: polihydroksy aldehydy i polihydroksy ketony lub jako substancje, które w wyniku hydrolizy dają
Skala słodkości cukrów Laktoza < maltoza < glukoza < sacharoza < fruktoza najsłodsza
 Źródła cukrów (węglowodanów) w produktach spożywczych: Warzywa i owoce (winogrona cukier gronowy glukoza) Produkty zbożowe: pieczywo, kasze, płatki śniadaniowe Funkcja węglowodanów w organizmie: Energetyczna:
Źródła cukrów (węglowodanów) w produktach spożywczych: Warzywa i owoce (winogrona cukier gronowy glukoza) Produkty zbożowe: pieczywo, kasze, płatki śniadaniowe Funkcja węglowodanów w organizmie: Energetyczna:
Monosacharydy Schemat konfiguracyjny
 B I T E N L EMIA G RGANIZNA I A Monosacharydy Schemat konfiguracyjny Aldozy szeregu D ustawia się w schemat wg dwu poniższych reguł: 1. Aldozy zawierające n atomów węgla otrzymuje się z aldoz zawierających
B I T E N L EMIA G RGANIZNA I A Monosacharydy Schemat konfiguracyjny Aldozy szeregu D ustawia się w schemat wg dwu poniższych reguł: 1. Aldozy zawierające n atomów węgla otrzymuje się z aldoz zawierających
ZWIĄZKI NATURALNE SACHARYDY
 ZWIĄZKI NATURALNE SACHARYDY 2 Związki naturalne Etap 0. i 1. ZADANIE 1. Identyfikacja węglowodanów Aldoheksoza szeregu D (związek A) w wyniku utleniania rozcieńczonym kwasem azotowym(v) tworzy kwas aldarowy
ZWIĄZKI NATURALNE SACHARYDY 2 Związki naturalne Etap 0. i 1. ZADANIE 1. Identyfikacja węglowodanów Aldoheksoza szeregu D (związek A) w wyniku utleniania rozcieńczonym kwasem azotowym(v) tworzy kwas aldarowy
Informacje. W sprawach organizacyjnych Slajdy z wykładów
 Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
REAKCJE CHARAKTERYSTYCZNE CUKRÓW
 REAKCJE CHARAKTERYSTYCZNE CUKRÓW Grupa związków organicznych nazywanych węglowodanami, cukrami lub sacharydami obejmuje polihydroksylowe aldehydy i ketony oraz ich pochodne. Nazwa węglowodany pochodzi
REAKCJE CHARAKTERYSTYCZNE CUKRÓW Grupa związków organicznych nazywanych węglowodanami, cukrami lub sacharydami obejmuje polihydroksylowe aldehydy i ketony oraz ich pochodne. Nazwa węglowodany pochodzi
Aminokwasy, peptydy, białka
 Aminokwasy, peptydy, białka Aminokwasy KWAS 1-AMINOCYKLOPROPANOKARBOKSYLOWY α AMINOKWAS KWAS 3-AMINOPROPANOWY β AMINOKWAS KWAS 4-AMINOPROPANOWY γ AMINOKWAS KWAS 2-AMINOETANOSULFONOWY β AMINOKWAS Aminokwasy
Aminokwasy, peptydy, białka Aminokwasy KWAS 1-AMINOCYKLOPROPANOKARBOKSYLOWY α AMINOKWAS KWAS 3-AMINOPROPANOWY β AMINOKWAS KWAS 4-AMINOPROPANOWY γ AMINOKWAS KWAS 2-AMINOETANOSULFONOWY β AMINOKWAS Aminokwasy
Podział związków organicznych
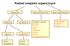 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Protokół: Reakcje charakterystyczne cukrowców
 Protokół: Reakcje charakterystyczne cukrowców 1. Rekcja na obecność cukrów: próba Molischa z -naftolem Jest to najbardziej ogólna reakcja na cukrowce, tak wolne jak i związane. Ujemny jej wynik wyklucza
Protokół: Reakcje charakterystyczne cukrowców 1. Rekcja na obecność cukrów: próba Molischa z -naftolem Jest to najbardziej ogólna reakcja na cukrowce, tak wolne jak i związane. Ujemny jej wynik wyklucza
Cz. XXVIII - c Węglowodany - cukry - sacharydy: disacharydy i polisacharydy
 Cz. XXVIII - c Węglowodany - cukry - sacharydy: disacharydy i polisacharydy I. Budowa i właściwości disacharydów Wiązanie między monosacharydami powstaje z udziałem dwóch grup hydroksylowych pochodzących
Cz. XXVIII - c Węglowodany - cukry - sacharydy: disacharydy i polisacharydy I. Budowa i właściwości disacharydów Wiązanie między monosacharydami powstaje z udziałem dwóch grup hydroksylowych pochodzących
spektroskopia elektronowa (UV-vis)
 spektroskopia elektronowa (UV-vis) rodzaje przejść elektronowych Energia σ* π* 3 n 3 π σ σ σ* daleki nadfiolet (λ max < 200 nm) π π* bliski nadfiolet jednostki energii atomowa jednostka energii = energia
spektroskopia elektronowa (UV-vis) rodzaje przejść elektronowych Energia σ* π* 3 n 3 π σ σ σ* daleki nadfiolet (λ max < 200 nm) π π* bliski nadfiolet jednostki energii atomowa jednostka energii = energia
Reakcje charakterystyczne cukrów
 Reakcje charakterystyczne cukrów Maria Jamrozik Grupa związków organicznych nazywanych węglowodanami, cukrami lub sacharydami obejmuje polihydroksylowe aldehydy i ketony oraz ich pochodne. azwa "węglowodany"
Reakcje charakterystyczne cukrów Maria Jamrozik Grupa związków organicznych nazywanych węglowodanami, cukrami lub sacharydami obejmuje polihydroksylowe aldehydy i ketony oraz ich pochodne. azwa "węglowodany"
Węglowodany (Cukry) Część 3. Związki wielofunkcyjne
 Węglowodany (Cukry) Część 3 Związki wielofunkcyjne Glikozydy Monosacharydy Ryboza, Deoksyryboza: - wzory - funkcje biologiczne, pochodne Disacharydy Sacharoza, Celobioza, Maltoza,Laktoza - wzór - właściwości
Węglowodany (Cukry) Część 3 Związki wielofunkcyjne Glikozydy Monosacharydy Ryboza, Deoksyryboza: - wzory - funkcje biologiczne, pochodne Disacharydy Sacharoza, Celobioza, Maltoza,Laktoza - wzór - właściwości
11. ALDEHYDY, KETONY CH 2. hydroksyloamina. hydrazyna fenylohydrazyna SO 4. semikarbazyd
 11. ALDEYDY, KETY 1. Podać nazwy następujących związków uwzględniając izomerię. C e. f. C g. h. C i. j. k. l. 2. kreślić typ hybrydyzacji atomów węgla, podać rodzaje wiązań chemicznych, kąty między wiązaniami,
11. ALDEYDY, KETY 1. Podać nazwy następujących związków uwzględniając izomerię. C e. f. C g. h. C i. j. k. l. 2. kreślić typ hybrydyzacji atomów węgla, podać rodzaje wiązań chemicznych, kąty między wiązaniami,
Wymagania edukacyjne z chemii w klasie II
 Wymagania edukacyjne z chemii w klasie II kształcenie ogólne w zakresie podstawowym i rozszerzonym Program nauczania: DKOS-4015-88/02 Podręcznik: Chemia organiczna. Kształcenie ogólne w zakresie podstawowym
Wymagania edukacyjne z chemii w klasie II kształcenie ogólne w zakresie podstawowym i rozszerzonym Program nauczania: DKOS-4015-88/02 Podręcznik: Chemia organiczna. Kształcenie ogólne w zakresie podstawowym
Węglowodany metody jakościowe oznaczania cukrów reakcja Molisha, Fehlinga, Selivanowa; ilościowe oznaczanie glukozy metodą Somogyi Nelsona
 Ćwiczenie nr 7 Węglowodany metody jakościowe oznaczania cukrów reakcja Molisha, Fehlinga, Selivanowa; ilościowe oznaczanie glukozy metodą Somogyi Nelsona Celem ćwiczenia jest: zapoznanie z metodami jakościowej
Ćwiczenie nr 7 Węglowodany metody jakościowe oznaczania cukrów reakcja Molisha, Fehlinga, Selivanowa; ilościowe oznaczanie glukozy metodą Somogyi Nelsona Celem ćwiczenia jest: zapoznanie z metodami jakościowej
1.1. AMINOKWASY BIAŁKOWE
 1 ĆWICZENIE 1 BUDOWA I WŁAŚCIWOŚCI AMINOKWASÓW 1.1. AMINOKWASY BIAŁKOWE Aminokwasy są związkami organicznymi zawierającymi co najmniej jedną grupę karboksylową -COOH oraz co najmniej jedną grupę aminową
1 ĆWICZENIE 1 BUDOWA I WŁAŚCIWOŚCI AMINOKWASÓW 1.1. AMINOKWASY BIAŁKOWE Aminokwasy są związkami organicznymi zawierającymi co najmniej jedną grupę karboksylową -COOH oraz co najmniej jedną grupę aminową
Rozdział 9. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 9 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Cukry Zadanie 9.1. Kolejno:
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 9 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Cukry Zadanie 9.1. Kolejno:
Instrukcja do ćwiczeń laboratoryjnych
 Uniwersytet Gdański Wydział Chemii Chemia żywności Katedra Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 2 Węglowodany w żywności: struktura, właściwości, odróżnianie cukrów prostych
Uniwersytet Gdański Wydział Chemii Chemia żywności Katedra Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 2 Węglowodany w żywności: struktura, właściwości, odróżnianie cukrów prostych
Azotowe związki organiczne
 strona 1/1 Azotowe związki organiczne Krystyna Bogdanowicz-Szwed Procesy zachodzące w żywych organizmach są ściśle związane z chemią wielofunkcyjnych związków organicznych zawierających w swoich cząsteczkach
strona 1/1 Azotowe związki organiczne Krystyna Bogdanowicz-Szwed Procesy zachodzące w żywych organizmach są ściśle związane z chemią wielofunkcyjnych związków organicznych zawierających w swoich cząsteczkach
fruktoza α,d(+)glukopiranoza β,d(-)fruktofuranoza
 WĘGLWDANY I. Wprowadzenie teoretyczne ukry, sacharydy, są związkami pochodzenia naturalnego; odgrywają one, podobnie jak białka, olbrzymią rolę w procesach biologicznych. Najbardziej ogólny podział cukrów
WĘGLWDANY I. Wprowadzenie teoretyczne ukry, sacharydy, są związkami pochodzenia naturalnego; odgrywają one, podobnie jak białka, olbrzymią rolę w procesach biologicznych. Najbardziej ogólny podział cukrów
Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, Spis treści
 Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, 2010 Spis treści Część II. Zagadnienia wybrane 25. Halogenki arylów. Substytucja nukleofilowa w pierścieniu
Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, 2010 Spis treści Część II. Zagadnienia wybrane 25. Halogenki arylów. Substytucja nukleofilowa w pierścieniu
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Aminokwasy, peptydy i białka. Związki wielofunkcyjne
 Aminokwasy, peptydy i białka Związki wielofunkcyjne Aminokwasy, peptydy i białka Aminokwasy, peptydy i białka: - wiadomości ogólne Aminokwasy: - ogólna charakterystyka - budowa i nazewnictwo - właściwości
Aminokwasy, peptydy i białka Związki wielofunkcyjne Aminokwasy, peptydy i białka Aminokwasy, peptydy i białka: - wiadomości ogólne Aminokwasy: - ogólna charakterystyka - budowa i nazewnictwo - właściwości
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Oligosacharydy (kilkucukrowce): Dwucukry Trójcukry Czterocukry
 WĘGLWDANY 1. Klasyfikacja węglowodanów Węglowodany, czyli cukry, są to wielohydroksyaldehydy lub wielohydroksyketony oraz produkty ich kondensacji. Skład chemiczny tej grupy połączeń daje się wyrazić ogólnym
WĘGLWDANY 1. Klasyfikacja węglowodanów Węglowodany, czyli cukry, są to wielohydroksyaldehydy lub wielohydroksyketony oraz produkty ich kondensacji. Skład chemiczny tej grupy połączeń daje się wyrazić ogólnym
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Cukry właściwości i funkcje
 Cukry właściwości i funkcje Miejsce cukrów wśród innych składników chemicznych Cukry Z cukrem mamy do czynienia bardzo często - kiedy sięgamy po białe kryształy z cukiernicy. Większość z nas nie uświadamia
Cukry właściwości i funkcje Miejsce cukrów wśród innych składników chemicznych Cukry Z cukrem mamy do czynienia bardzo często - kiedy sięgamy po białe kryształy z cukiernicy. Większość z nas nie uświadamia
Ćwiczenie 6 Aminokwasy
 Ćwiczenie 6 Aminokwasy Aminokwasy są to związki dwufunkcyjne, których cząsteczki zawierają grupy karboksylowe i aminowe: grupa aminowa:nh 2 grupa karboksylowa COOH Nomenklatura aminokwasów: Naturalne aminokwasy
Ćwiczenie 6 Aminokwasy Aminokwasy są to związki dwufunkcyjne, których cząsteczki zawierają grupy karboksylowe i aminowe: grupa aminowa:nh 2 grupa karboksylowa COOH Nomenklatura aminokwasów: Naturalne aminokwasy
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
WYKRYWANIE WIĄZAŃ WIELOKROTNYCH WYKRYWANIE WIĄZAŃ WIELOKROTNYCH
 WYKRYWANIE WIĄZAŃ WIELOKROTNYCH Odbarwienie wody bromowej Woda bromowa roztwór Br 2 w wodzie - Br 2 (aq): brunatna, brązowa lub ciemnoczerwona ciecz. Gdy brom przyłącza się związku nienasyconego barwa
WYKRYWANIE WIĄZAŃ WIELOKROTNYCH Odbarwienie wody bromowej Woda bromowa roztwór Br 2 w wodzie - Br 2 (aq): brunatna, brązowa lub ciemnoczerwona ciecz. Gdy brom przyłącza się związku nienasyconego barwa
AMINOKWASY. I. Wprowadzenie teoretyczne. Aminokwasy są to związki, które w łańcuchu węglowym zawierają zarówno grupę aminową jak i grupę karboksylową.
 AMIKWASY I. Wprowadzenie teoretyczne Aminokwasy są to związki, które w łańcuchu węglowym zawierają zarówno grupę aminową jak i grupę karboksylową. 2 3 WZY GÓLE ATUALY AMIKWASÓW WYSTĘPUJĄY W BIAŁKA Zalicza
AMIKWASY I. Wprowadzenie teoretyczne Aminokwasy są to związki, które w łańcuchu węglowym zawierają zarówno grupę aminową jak i grupę karboksylową. 2 3 WZY GÓLE ATUALY AMIKWASÓW WYSTĘPUJĄY W BIAŁKA Zalicza
1. Napisz schematy reakcji otrzymywania z 1-bromo-2-fenyloetanu i z dowolnych innych reagentów następujących amin: 2-fenyloetyloaminy
 REPETYTORIUM A Z zakresu aminy alifatyczne i aromatyczne, związki heterocykliczne, związki karbopolicykliczne, węglowodany, aminokwasy i peptydy, terpeny, steroidy, lipidy 1. Napisz schematy reakcji otrzymywania
REPETYTORIUM A Z zakresu aminy alifatyczne i aromatyczne, związki heterocykliczne, związki karbopolicykliczne, węglowodany, aminokwasy i peptydy, terpeny, steroidy, lipidy 1. Napisz schematy reakcji otrzymywania
ALDEHYDY, KETONY. 1. Podać nazwy systematyczne i zwyczajowe następujących związków, uwzględnić izomerię:
 ALDEYDY, KETY 1. Podać nazwy systematyczne i zwyczajowe następujących związków, uwzględnić izomerię: C 3 C b. C 3 CC 3 d. e. f. g. h. C i. C *j. k. C C 2 *l. ł. 2. Uzasadnić, dlaczego związki karbonylowe
ALDEYDY, KETY 1. Podać nazwy systematyczne i zwyczajowe następujących związków, uwzględnić izomerię: C 3 C b. C 3 CC 3 d. e. f. g. h. C i. C *j. k. C C 2 *l. ł. 2. Uzasadnić, dlaczego związki karbonylowe
BUDOWA I WŁAŚCIWOŚCI AMINOKWASÓW. 1.1. Aminokwasy białkowe
 BUDOWA I WŁAŚCIWOŚCI AMINOKWASÓW 1.1. Aminokwasy białkowe Aminokwasy są związkami organicznymi, zawierającymi co najmniej jedną grupę karboksylową COOH oraz co najmniej jedną grupę aminową NH 2. W zależności
BUDOWA I WŁAŚCIWOŚCI AMINOKWASÓW 1.1. Aminokwasy białkowe Aminokwasy są związkami organicznymi, zawierającymi co najmniej jedną grupę karboksylową COOH oraz co najmniej jedną grupę aminową NH 2. W zależności
17. DODATKI Tabela 1. Symbole okre laj ce wielokrotno ci i podwielokrotno ci ułamków dziesi tnych Symbol Okre lenie Wielokrotno Tabela 2.
 17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/67/57994710.jpg) Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
Ćwiczenie 4. Identyfikacja wybranych cukrów w oparciu o niektóre reakcje charakterystyczne
 Klasyczna Analiza Jakościowa Organiczna, Ćw. 4 - Identyfikacja wybranych cukrów Ćwiczenie 4 Identyfikacja wybranych cukrów w oparciu o niektóre reakcje charakterystyczne Zagadnienia teoretyczne: 1. Budowa
Klasyczna Analiza Jakościowa Organiczna, Ćw. 4 - Identyfikacja wybranych cukrów Ćwiczenie 4 Identyfikacja wybranych cukrów w oparciu o niektóre reakcje charakterystyczne Zagadnienia teoretyczne: 1. Budowa
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA
 CHEMIA KLASA III 2016-09-01 LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA Treści nauczania Tom III podręcznika Ciekawi świata wyd. Operon I. WĘGLOWODORY 1. Chemia organiczna jako chemia związków
CHEMIA KLASA III 2016-09-01 LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA Treści nauczania Tom III podręcznika Ciekawi świata wyd. Operon I. WĘGLOWODORY 1. Chemia organiczna jako chemia związków
data ĆWICZENIE 5 ANALIZA JAKOŚCIOWA WĘGLOWODANÓW Wstęp merytoryczny
 Imię i nazwisko Uzyskane punkty Nr albumu data /3 podpis asystenta ĆWICZENIE 5 ANALIZA JAKOŚCIOWA WĘGLOWODANÓW Wstęp merytoryczny Węglowodany (syn. cukry, cukrowce sacharydy) należą do grupy związków organicznych
Imię i nazwisko Uzyskane punkty Nr albumu data /3 podpis asystenta ĆWICZENIE 5 ANALIZA JAKOŚCIOWA WĘGLOWODANÓW Wstęp merytoryczny Węglowodany (syn. cukry, cukrowce sacharydy) należą do grupy związków organicznych
ĆWICZENIE 7 BUDOWA I WŁAŚCIWOŚCI CUKROWCÓW
 ĆWIZENIE 7 BUDWA I WŁAŚIWŚI UKRWÓW 7.1. EL ĆWIZENIA Zapoznanie się z budową i właściwościami mono-, di- i polisacharydów oraz identyfikacja sacharydów za pomocą reakcji charakterystycznych. 7.2. KLASYFIKAJA
ĆWIZENIE 7 BUDWA I WŁAŚIWŚI UKRWÓW 7.1. EL ĆWIZENIA Zapoznanie się z budową i właściwościami mono-, di- i polisacharydów oraz identyfikacja sacharydów za pomocą reakcji charakterystycznych. 7.2. KLASYFIKAJA
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Węglowodany (Cukry) Część 1. Związki wielofunkcyjne
 Węglowodany (Cukry) Część 1 Związki wielofunkcyjne Węglowodany - wiadomości ogólne - podział Monosacharydy - wiadomości ogólne - budowa strukturalna - izomeria Węglowodany (Cukry) Węglowodany wiadomości
Węglowodany (Cukry) Część 1 Związki wielofunkcyjne Węglowodany - wiadomości ogólne - podział Monosacharydy - wiadomości ogólne - budowa strukturalna - izomeria Węglowodany (Cukry) Węglowodany wiadomości
Reakcje charakterystyczne aminokwasów
 KATEDRA BIOCHEMII Wydział Biologii i Ochrony Środowiska Reakcje charakterystyczne aminokwasów BIOCHEMIA STRUKTURALNA ĆWICZENIE 1 REAKCJE CHARAKTERYSTYCZNE AMINOKWASÓW A) REAKCJE OGÓLNE ZADANIE 1 WYKRYWANIE
KATEDRA BIOCHEMII Wydział Biologii i Ochrony Środowiska Reakcje charakterystyczne aminokwasów BIOCHEMIA STRUKTURALNA ĆWICZENIE 1 REAKCJE CHARAKTERYSTYCZNE AMINOKWASÓW A) REAKCJE OGÓLNE ZADANIE 1 WYKRYWANIE
Węglowodany. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Węglowodany Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Węglowodany - rozpowszechnienie Zawartość w suchej masie: roślin sięga 80% zwierząt nie przekracza 2% W roślinach są: głównym materiałem
Węglowodany Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Węglowodany - rozpowszechnienie Zawartość w suchej masie: roślin sięga 80% zwierząt nie przekracza 2% W roślinach są: głównym materiałem
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna
 Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
1. Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Umiejętności ponadpodstawowe Ocena bardzo dobra. Temat. Ocena celująca. Ocena dobra. Ocena dopuszczająca. Ocena dostateczna KWASY
 Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII, opracowane na podstawie programu nauczania chemii w szkole podstawowej
Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII, opracowane na podstawie programu nauczania chemii w szkole podstawowej
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/55/35935976.jpg) KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Spis treści. Fotosynteza. 1 Fotosynteza 1.1 WĘGLOWODANY 2 Cykl Krebsa 2.1 Acetylokoenzym A
 Spis treści 1 Fotosynteza 1.1 WĘGLOWODANY 2 Cykl Krebsa 2.1 Acetylokoenzym A Fotosynteza Jest to złożony, wieloetapowy proces redukcji dwutlenku węgla do substancji zawierających atomy węgla na niższych
Spis treści 1 Fotosynteza 1.1 WĘGLOWODANY 2 Cykl Krebsa 2.1 Acetylokoenzym A Fotosynteza Jest to złożony, wieloetapowy proces redukcji dwutlenku węgla do substancji zawierających atomy węgla na niższych
Budowa aminokwasów i białek
 Biofizyka Ćwiczenia 1. E. Banachowicz Zakład Biofizyki Molekularnej IF UAM http://www.amu.edu.pl/~ewas Budowa aminokwasów i białek E.Banachowicz 1 Ogólna budowa aminokwasów α w neutralnym p α N 2 COO N
Biofizyka Ćwiczenia 1. E. Banachowicz Zakład Biofizyki Molekularnej IF UAM http://www.amu.edu.pl/~ewas Budowa aminokwasów i białek E.Banachowicz 1 Ogólna budowa aminokwasów α w neutralnym p α N 2 COO N
Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności
 Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności Kwasy Wymagania edukacyjne z podstawy programowej - klasa VIII Uczeń: definiuje pojęcie kwasy zgodnie z teorią Arrheniusa opisuje
Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności Kwasy Wymagania edukacyjne z podstawy programowej - klasa VIII Uczeń: definiuje pojęcie kwasy zgodnie z teorią Arrheniusa opisuje
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1.
 1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
Cukry. Monocukry to związki dwufunkcyjne definiowane jako polihydroksylowe alkohole zawierające dodatkowo albo aldehydową (przy
 Cukry Z chemicznego punktu widzenia cukry to grupa związków organicznych o ściśle zdefiniowanych właściwościach i znaczeniu biologicznym. Najbardziej znanym przedstawicielem tej grupy jest glukoza, którą
Cukry Z chemicznego punktu widzenia cukry to grupa związków organicznych o ściśle zdefiniowanych właściwościach i znaczeniu biologicznym. Najbardziej znanym przedstawicielem tej grupy jest glukoza, którą
Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII
 Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII Temat 1.Wzory i nazwy kwasów. dopuszczająca - zna zasady bezpiecznego posługiwania
Wymagania edukacyjne niezbędne do otrzymania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii dla klasy VIII Temat 1.Wzory i nazwy kwasów. dopuszczająca - zna zasady bezpiecznego posługiwania
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony.
 WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Disacharydy. Chemia Medyczna dr inż.. Ewa Mironiuk-Puchalska, W CHem PW 1. disacharydy redukujace. disacharydy nieredukujace. atom anomeryczny.
 Disacharydy Disacharydy cukry hydrolizujące (pod wpływem roztworów kwasów mineralnych, maltazy wiązania -glikozydowe, emulsyny wiązania -glikozydowe) glikozydy (powstają z dwóch reszt monosacharydowych
Disacharydy Disacharydy cukry hydrolizujące (pod wpływem roztworów kwasów mineralnych, maltazy wiązania -glikozydowe, emulsyny wiązania -glikozydowe) glikozydy (powstają z dwóch reszt monosacharydowych
CZĘŚĆ PIERWSZA REAKCJE CHARAKTERYSTYCZNE WĘGLOWODANÓW
 ĆWIZENIE 6 ANALIZA JAKŚIWA UKRÓW IDENTYFIKAJA NIEZNANEG UKRU el ćwiczenia: zęść pierwsza: Zapoznanie się z charakterystycznymi barwnymi reakcjami węglowodanów. zęść druga: Identyfikacja cukru ukry analizowane
ĆWIZENIE 6 ANALIZA JAKŚIWA UKRÓW IDENTYFIKAJA NIEZNANEG UKRU el ćwiczenia: zęść pierwsza: Zapoznanie się z charakterystycznymi barwnymi reakcjami węglowodanów. zęść druga: Identyfikacja cukru ukry analizowane
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY
 WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Cukry (sacharydy) znaczenie, podział, budowa, właściwości
 Cukry (sacharydy) znaczenie, podział, budowa, właściwości Cukry - definicje Substancje o słodkim smaku nieprawdziwa! Związki o wzorze ogónym C n (H 2 ) n nieprawdziwa!! Poihydroksyadehydy ub poihydroksyketony
Cukry (sacharydy) znaczenie, podział, budowa, właściwości Cukry - definicje Substancje o słodkim smaku nieprawdziwa! Związki o wzorze ogónym C n (H 2 ) n nieprawdziwa!! Poihydroksyadehydy ub poihydroksyketony
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony
 CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
Reakcje charakterystyczne aminokwasów
 KATEDRA BIOCHEMII Wydział Biologii i Ochrony Środowiska Reakcje charakterystyczne aminokwasów BIOCHEMIA STRUKTURALNA ĆWICZENIE 1 REAKCJE CHARAKTERYSTYCZNE AMINOKWASÓW A) REAKCJE OGÓLNE ZADANIE 1 WYKRYWANIE
KATEDRA BIOCHEMII Wydział Biologii i Ochrony Środowiska Reakcje charakterystyczne aminokwasów BIOCHEMIA STRUKTURALNA ĆWICZENIE 1 REAKCJE CHARAKTERYSTYCZNE AMINOKWASÓW A) REAKCJE OGÓLNE ZADANIE 1 WYKRYWANIE
Własności chemiczne. 1. Kwasowość. Wartości pk a. (aminokwasy zamiast grupy NH 2 muszą mieć grupę NH 3 + ) 2. Zasadowość.
 B I T E N L EMI G GNIZN I Własności chemiczne 1. wasowość. Wartości p a wasowość aminokwasów jest znacznie MNIEJSZ od kwasowości zwykłych WSÓW BSYLWY p a większości aminokwasów mieszczą się w zakresie
B I T E N L EMI G GNIZN I Własności chemiczne 1. wasowość. Wartości p a wasowość aminokwasów jest znacznie MNIEJSZ od kwasowości zwykłych WSÓW BSYLWY p a większości aminokwasów mieszczą się w zakresie
