Farmakofory. metody QSAR
|
|
|
- Krystyna Kowalewska
- 7 lat temu
- Przeglądów:
Transkrypt
1 Farmakofory metody QSAR
2 Strategie projektowania leków Ligand-based drug design nieznana Budowanie modelu miejsc aktywnych liganda (farmakofor) Przeszukiwanie baz danych (screening) Struktura celu molekularnego znana 1D i 3D QSAR (pseudoreceptory i pola molekularne) Dopasowanie ligandów do miejsca aktywnego receptora (dokowanie) Budowa nowych ligandów ab-initio Receptor-based drug design Dynamika kompleksu receptor-ligand
3 Definicja farmakoforu Farmakofor trójwymiarowe ułożenie grup chemicznych wspólnych dla związków aktywnych i niezbędnych dla ich aktywności biologicznej. 3
4 Poszukiwanie farmakoforu Pierwsza hipoteza Wiele hipotez 4
5 Poszukiwanie farmakoforu Więcej związków pozwala zidentyfikować właściwą hipotezę Identyfikacja sterycznych bumps w miejscu aktywnym 5
6 Pharmacophore-based drug design Założenie - związki działają według tego samego mechanizmu, tj. (1) wiążą się z tym samym celem molekularnym i (2) w tym samym miejscu wiążącym. 6
7 Podobieństwo molekularne związki różne chemicznie 2D 7
8 Podobieństwo molekularne związki różne chemicznie 3D 8
9 Nakładanie konformacji bioaktywnych Ważność oddziaływań hydrofobowych i grupy -OH. Brak nałożenia centralnych pierścieni. 9
10 Konformacje bioaktywne 12 kj/mol 3 kcal/mol Ograniczanie liczby konformacji 10
11 Poszukiwanie konformacji bioaktywnej GABA - neurotransmiter Me-GABA związek wciąż labilny agonista receptora GABA (kanał chlorkowy w synapsie) THIP - agonista receptora GABA 11
12 Nakładanie w przestrzeni właściwości = R substrat Inhibitor lek przeciwrakowy Struktura chemiczna inhibitora 12
13 Nakładanie w przestrzeni właściwości Nakładanie według struktur chemicznych Rzeczywiste nakładanie (według struktur krystalicznych) 13
14 Przykład identyfikacji farmakoforu Agoniści receptora dopaminowego Farmakofor: fenyloamina w konformacji rozciągniętej 14
15 Nieprawidłowe użycie informacji strukturalnej Oba związki są aktywne Nieprawidłowa konformacja bioaktywna zw. #2. Wiązanie podwójne jest płaskie 15
16 Pochodne fenylo-imidazolu Inhibitory bakteryjnego cytochromu P-450 Kamfora naturalny substrat 16
17 Nakładanie inhibitorów cytochromu Identyczny kształt Identyczne własności elektrostatyczne 17
18 Nakładanie inhibitorów cytochromu Rzeczywiste nałożenie (struktury krystaliczne z enzymem) Fragment miejsca aktywnego enzymu 18
19 Zasada aktywnych analogów Definiowanie miejsca aktywnego 19
20 Mapowanie receptora Agoniści receptora nikotynowego Ciasne miejsce wiążące i rola entropii 20
21 Dwie generacje farmakoforów I II 21
22 Analog design modyfikacje ligandów Grupy bioizosteryczne podobne własności fizykochemiczne 22
23 Budowanie łącznika do grup farmakoforowych 23
24 Konstrukcja w oparciu o farmakofor Farmakofor Dużo efektów ubocznych z powodu podobieństwa do struktury steroidu Wynik poszukiwań w bazie związków chemicznych 24
25 Równania QSAR 25
26 QSAR Quantitative Structure-Activity Relationship QSPR Property: rozpuszczalność, biodostępność, stabilność metaboliczna, przenikalność przez błony komórkowe, toksyczność, 26
27 Typy deskryptorów ligandów: 1D, 2D i 3D deskryptory 1D 2D związane z topologią (połączeniami między atomami) 3D związane z kształtem cząsteczki 27
28 Elektronowe efekty podstawnikowe Pochodne kwasu benzoesowego Ph-COOH (benzenokarboksylowego) K - stała dysocjacji kwasowej 28
29 Parametr x = log ( K X / K H ) = log K X - log K H Efekt zależny od położenia podstawnika w pierścieniu (dodatkowy efekt rezonansowy w położeniu para) 29
30 Przewidywanie pk a na podstawie równania Hammetta - zależne od rodzaju reakcji chemicznej 30
31 Równanie Hammetta przewidywanie efektu podstawnikowego w reakcjach chemicznych Hydroliza estru Ph-COOEt > 0 dysocjacja kwasowa Ph-COOH (bez odjęcia log K H ) Podstawniki w pozycji orto - duże efekty steryczne Utlenianie tioanizolu Ph-S-Me < 0 dysocjacja kwasowa Ph-COOH 31
32 Współczynnik Hanscha rola hydrofobowości Efekt istotny przy przekraczaniu błon komórkowych przez lek 32
33 logp miara hydrofobowości 33
34 Przykład korelacji z logp Log(1/c) oznacza efekt biologiczny 34
35 Związek efektu biologicznego log(1/c) z potencjałem termodynamicznym [ES] = [E] dla 50 % inhibicji [S] - efektywne stężenie inhibitora IC 50 in vitro, EC 50 - in vivo C efektywne stężenie związku. Aktywności biologiczne powinny być dokładne i pokrywać 2-3 rzędy wielkości 35
36 Definicja deskryptora 36
37 Zależności liniowe i paraboliczne Niedostateczna liczba związków Wyznaczenie optymalnej hydrofobowości 37
38 Parametr steryczny Tafta (ES) Większe podstawniki dają niższe wartości ES (reakcja estryfikacji trudniej zachodzi) 38
39 Kroki analizy QSAR Wybór związków Wybór deskryptorów Budowanie modelu QSAR Walidacja modelu 39
40 Wybór związków i deskryptorów 40
41 Eliminacja obserwacji odstających (outliers) Outlier: inny mechanizm działania lub błędna wartość 41
42 Przykłady dobrych i złych regresji liniowych 42
43 Przykład deskryptorów skorelowanych Masa molekularna (MW) i liczba atomów węgla dla serii alkanów 43
44 Liczba deskryptorów w QSAR Liczba związków większa od liczby deskryptorów 3-5 razy 44
45 Wpływ złożoności równania na predyktywność Niebieski zbiór treningowy Żółty zbiór testowy 45
46 Przykład użycia QSAR r uzyskane współczynniki korelacji Dobre modele: r 2 > 0.5 (r > 0.71) Ocena ważności deskryptorów (w ilu % wyjaśniają efekt biologiczny) 46
47 Wadidacja równania QSAR metoda kros-walidacji Podział na N części i traktowanie jednej części (za każdym razem innej) jako zbioru testowego 47
48 Czynniki wpływające na skuteczność metod QSAR solwatacja liganda i receptora farmakokinetyka leku: ADMET absorption, distribution, metabolism, excretion, toxicity Reguła 5 Lipinskiego (pasywna absorpcja jelitowa ) związek nie będzie dobrym lekiem gdy: MW > 500 [g/mol lub Da] clog P > 5 (calculated logp) HBA (N, O) > 10 HBD (N-H, O-H) > 5 48
49 3D-QSAR 49
50 3D-QSAR Quantitative Structure-Activity Relationship 3D-QSAR pozwala na uzyskanie korelacji pomiędzy polami oddziaływań molekularnych w otoczeniu ligandów a aktywnościami tych związków. Pola oddziaływań sterycznych i elektrostatycznych (korzystne i niekorzystne) 50
51 Różnice pomiędzy QSAR i 3D-QSAR MIF - Molecular Interactions Fields s steric es - electrostatic Deskryptory niezależne od (x,y,z) liczba wiązań rotowalnych, liczba donorów/akceptorów wiązań wodorowych, HOMO/LUMO, Wielkości mierzone w różnych punktach przestrzeni dużo więcej deskryptorów. 51
52 Wyznaczanie oddziaływań związków z sondami molekularnymi Sonda elektrostatyczna (ładunek punktowy H + ) tylko siły elektrostatyczne Sonda hydrofobowa (grupa metylowa atom C_sp 3 ) tylko siły van der Waalsa Sondy wieloatomowe -OH, -NH 2, -NH 3+, -COO, -COOH, H 2 O, siły van der Waalsa + siły elektrostatyczne (trzeba uwzględnić obroty sondy w celu znalezienia najlepszego oddziaływania z ligandem) 52
53 Wykorzystanie siatek (gridów) do umieszczania sond molekularnych Obliczenia przeprowadza się tylko dla sond umieszczonych w węzłach sieci. Ograniczenie tylko do pewnego obszaru w przestrzeni zmniejsza czas obliczeń. Liczba obliczeń = N probes * N grid points * N compounds 53
54 Obliczanie pól elektrostatycznych prawo Coulomba 54
55 Obliczanie pól sterycznych potencjał 6-12 Lennarda-Jonesa 55
56 Elementy pola siłowego
57 Rodzaje pól molekularnych Elektrostatyczne (jednoatomowa sonda H + ) Steryczne (jednoatomowa sonda -CH 3 ) HB donorowe (jednoatomowa sonda amidowy wodór N-H*) HB akceptorowe (jednoatomowa sonda karbonylowy tlen C=O*) Hydrofobowe (sonda H 2 O) Grup funkcyjnych (wieloatomowe sondy dla naładowanych lub obojętnych grup: -NH 2, -NH 3+, -COO, -COOH, ) 57
58 Wykorzystanie pól molekularnych GRID wartości oddziaływań dla pojedynczych ligandów dla różnych sond analiza korelacji pól molekularnych z aktywnościami biologicznymi związków z wykorzystaniem wizualizacji 3D 58
59 CoMFA Comparative Molecular Field Analysis Pierwsza metoda MFA R. D. Cramer 1988 Założenia: (1) związki w konformacjach bioaktywnych (2) nałożone na siebie tak jak w miejscu aktywnym 59
60 Poszukiwanie korelacji z polami molekularnymi IC 50 half maximal inhibitory concentration Można wyznaczyć jako stężenie badanego związku przy 50% wyparcia związku odnośnikowego z celu molekularnego 60
61 Ogólny schemat metody CoMFA 61
62 Założenia metody CoMFA Taki sam mechanizm działania (ten sam cel molekularny) Wiązanie się do tego samego miejsca aktywnego Wiązanie się w ten sam sposób Podobne efekty entropowe dla wszystkich związków (podobna giętkość związków) Podobne efekty desolwacyjne dla wszystkich związków (podobna wielkość związków i podobny stosunek powierzchni lipofilowej do hydrofilowej) 62
63 Zależność wyników od nałożenia związków w ich konformacjach bioaktywnych Rzeczywiste nałożenie (struktury krystaliczne z enzymem CP450-cam) Rzeczywiste nałożenie w miejscu aktywnym może być różne nawet dla bardzo podobnych związków 63
64 Sposoby nakładania związków Nakładanie odpowiadających sobie atomów i/lub pseudoatomów ze wspólnego szkieletu molekularnego Nakładanie grup farmakoforowych 64
65 Sposoby nakładania związków Nakładanie według obliczonych pól molekularnych (nie wymaga znajdowania odpowiadających sobie atomów) Nakładanie według kształtu związków Niebieski potencjał el-stat. dodatni Czerwony potencjał el-stat. ujemny 65
66 Sposoby nakładania związków Nakładanie według kształtu potencjału elektrostatycznego Niebieski potencjał el-stat. dodatni Czerwony potencjał el-stat. ujemny Nakładanie według dokładnych orientacji związków (ze struktur krystalicznych lub dokowania) Jest to sposób idealny 66
67 Równanie QSAR w CoMFA 67
68 Problem nadmiaru deskryptorów w stosunku do liczby związków Dla uzyskania dobrej statystyki potrzeba aby liczba związków była 3-5 razy większa niż liczba deskryptorów 68
69 Metoda (częściowych) najmniejszych kwadratów PLS Partial Least Squares Klasyczna metoda najmniejszych kwadratów (najmniejsze pole sumy kwadratów) Eliminacja deskryptorów skorelowanych - nowe nieskorelowane deskryptory t 1, t 2, 69
70 Redukcja liczby deskryptorów Jeden deskryptor zamiast trzech Uzyskiwanie pierwszego głównego czynnika t 1 : najlepiej opisuje rozmieszczenie punktów w przestrzeni X 70
71 Analiza czynnikowa czynniki t 1, t 2, nie mają znaczenia strukturalnego Kolejny czynnik główny musi być prostopadły do pierwszego (tylko wtedy brak korelacji między nimi) Nowe równanie QSAR: activity = c 1 t 1 + c 2 t 2 + c n t n + k activity = log (1/c) 71
72 Przewidywanie aktywności nowych związków Przewidywanie wykonuje się na podstawie uzyskanego równania regresji i nowych wartości czynników t. Do otrzymania równania regresji oprócz PLS wykorzystuje się także: (1) algorytmy genetyczne i (2) metodę sieci neuronalnych 72
73 Działanie Algorytmów Genetycznych 73
74 Działanie Sieci Neuronalnych 74
75 Powrót do oryginalnych czynników s i, e i - czynniki nieortogonalne t i - czynniki ortogonalne 75
76 Mapy konturowe CoMFA Pole oddziaływań sterycznych Pole oddziaływań elektrostatycznych 76
77 Znaczenie kolorów do opisu map CoMFA Zielony: steryczne - korzystne Żółty: steryczne - niekorzystne Niebieski: dodatni ładunek i HB donor - korzystne ujemny ładunek i HB akceptor - niekorzystne Czerwony: ujemny ładunek i HB akceptor - korzystne dodatni ładunek i HB donor - niekorzystne Brak mapy CoMFA dla tego rejonu odpowiada brakowi zmienności związków w tym rejonie W klasycznym CoMFA są używane tylko dwie sondy: do oddziaływań sterycznych i elektrostatycznych 77
78 Problem stabilności map CoMFA Małe zmiany w nałożeniu związków mogą prowadzić do dużych zmian w mapach 78
79 Związki referencyjne steroidy Cramer steroidów 79
80 Inne metody 3D-QSAR Nie ma najlepszej metody wybór zależy od zestawu związków do analizy 80
81 Omówienie niektórych metod 3D-QSAR 1/2 CoMSIA (comparative molecular similarity index analysis G. Klebe): potencjały zmiękczane przez funkcje Gaussa na atomach i przez to mniej czuła na zmiany w nałożeniu związków i orientacji siatki. Dodatkowe sondy: HB donor i HB akceptor, hydrofobowa. HQSAR (Hologram QSAR T. Heritage): struktury związków zakodowane jako ciągi binarne. Nie wymaga nakładania molekuł może analizować duże zbiory danych. Obecność grup funkcyjnych lub fragmentów molekularnych w danym miejscu tworzy deskryptor. GRIND (Grid INdependent Descriptors G. Gruciani): Używa kombinacji kilku uproszczonych pól molekularnych. Deskryptory oparte na strukturach 3D ale niezależne od orientacji związków w przestrzeni. 81
82 Omówienie niektórych metod 3D-QSAR 2/2 QuaSAR (Quasi-atomistic SAR A. Vedani) pseudoreceptory: powłoka pseudoatomów wokół nałożonych związków (brak siatki). Nowe typy pseudoatomów np. HB flip/flop. Możliwe efekty dopasowania indukcyjnego dopasowanie kształtu powłoki. 4D,5D,6D-QSAR (wielowymiarowe QSAR A. Vedani): uwzględnia wiele konformacji i stanów protonacyjnych tego samego liganda (4D); + hipotetyczne stany dopasowania liganda i receptora (5D); + hipotetyczne stany liganda uwzględniające efekty rozpuszczalnikowe (6D). RD-QSAR (Receptor-Dependent QSAR): uwzględnia strukturę receptora; np. z danymi strukturalnymi receptora estrogenowego, androgenowego i cytochromu P450 do prognozowania toksyczności związków. Wykorzystuje metodę 5D-QSAR: efekty indukcyjne dopasowania ligand-receptor są bardziej realistyczne. 82
83 Pseudoreceptory (QuaSAR) Używane potencjały: Hydrofobowy Jonowy dodatni Jonowy ujemny Donor wiązania H Akceptor wiązania H Hydrofobowy dodatni Hydrofobowy ujemny Powierzchnia molekularna zamiast gridu 83
84 Pseudoreceptory Pseudoreceptor i tworzące go ligandy Oddziaływanie badanej cząsteczki z pseudoreceptorem 84
85 Pseudoreceptory Optymalizacja wewnątrz pseudoreceptora 4 najbardziej aktywne ligandy wszystkie ligandy ligandy po optymalizacji 85
86 Peptydomimetyki 86
87 Leki peptydowe Bardzo dobre działanie w testach in vitro zarówno na izolowanych receptorach i całych komórkach Niedobre własności w testach klinicznych: Szybka proteoliza (rozkład na aminokwasy) Szybki metabolizm (przetwarzanie) Słabe własności transportowe Szybkie wydalanie 87
88 Strukturalne modyfikacje peptydów Peptyd - Modyfikacje łańcuchów bocznych - Mostkowanie - Cyklizacja Związek mniej peptydowy - Modyfikacja węgli C - Modyfikacja wiązań peptydowych Związek niepeptydowy - Nowa główna struktura chemiczna (modelowanie de novo) 88
89 Modyfikacje łańcuchów bocznych Przykłady modyfikacji 89
90 Cyklizacja krótkozasięgowa - mostkowanie Mostkowanie ogranicza liczbę konformacji - konieczność dopasowania do konformacji bioaktywnych 90
91 Cyklizacja łańcucha peptydowego 91
92 Modyfikacje wiązania peptydowego Modyfikacje grupy C=O 92
93 Modyfikacje węgla C Naturalna konf. -turn azapeptydy borapeptydy 93
94 Wydłużanie łańcucha głównego 94
95 Modelowanie de novo Thyrotropin-Releasing Hormone (TRH) nowy szkielet molekularny 95
Komputerowe wspomaganie projektowanie leków
 Komputerowe wspomaganie projektowanie leków wykład VI Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków wykład VI Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków
 Komputerowe wspomaganie projektowanie leków wykład VII Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków wykład VII Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
QSAR i związki z innymi metodami. Karol Kamel Uniwersytet Warszawski
 QSAR i związki z innymi metodami Wstęp QSAR Quantitative Structure-Activity Relationship. Jest to metoda polegająca na znalezieniu (i analizie) zależności pomiędzy strukturą chemiczną (geometria cząsteczki,
QSAR i związki z innymi metodami Wstęp QSAR Quantitative Structure-Activity Relationship. Jest to metoda polegająca na znalezieniu (i analizie) zależności pomiędzy strukturą chemiczną (geometria cząsteczki,
Podstawy projektowania leków wykład 11
 Podstawy projektowania leków wykład 11 Łukasz Berlicki QSAR i 3D QSAR 1964, C. Hansch i T. Fujita: QSAR 1984, P. Andrews: wkład grup funkcyjnych do oddziaływania z celem molekularnym 1985, P. Goodford:
Podstawy projektowania leków wykład 11 Łukasz Berlicki QSAR i 3D QSAR 1964, C. Hansch i T. Fujita: QSAR 1984, P. Andrews: wkład grup funkcyjnych do oddziaływania z celem molekularnym 1985, P. Goodford:
Komputerowe wspomaganie projektowanie leków
 Komputerowe wspomaganie projektowanie leków wykład V Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków wykład V Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków
 Komputerowe wspomaganie projektowanie leków wykład IV Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków wykład IV Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Projektowanie Nowych Chemoterapeutyków
 Jan Mazerski Katedra Technologii Leków i Biochemii Wydział Chemiczny Projektowanie Nowych Chemoterapeutyków XV. QSAR 3D QSAR w przestrzeni Rozwój metod ustalania struktury 3D dla białek i ich kompleksów.
Jan Mazerski Katedra Technologii Leków i Biochemii Wydział Chemiczny Projektowanie Nowych Chemoterapeutyków XV. QSAR 3D QSAR w przestrzeni Rozwój metod ustalania struktury 3D dla białek i ich kompleksów.
cz. VII Metody projektowania leków i modelowanie molekularne
 Oddziaływanie leków z celami molekularnymi cz. VII Metody projektowania leków i modelowanie molekularne Prof. dr hab. Sławomir Filipek Uniwersytet Warszawski, Wydział Chemii 1 Strategie projektowania leków
Oddziaływanie leków z celami molekularnymi cz. VII Metody projektowania leków i modelowanie molekularne Prof. dr hab. Sławomir Filipek Uniwersytet Warszawski, Wydział Chemii 1 Strategie projektowania leków
Lek od pomysłu do wdrożenia
 Lek od pomysłu do wdrożenia Lek od pomysłu do wdrożenia KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU
Lek od pomysłu do wdrożenia Lek od pomysłu do wdrożenia KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU
Komputerowe wspomaganie projektowania leków
 Komputerowe wspomaganie projektowania leków MECHANIKA MOLEKULARNA I KWANTOWA W MM korzysta się z równań wynikających z praw fizyki klasycznej i stosuje się je do jader atomów z pominięciem elektronów,
Komputerowe wspomaganie projektowania leków MECHANIKA MOLEKULARNA I KWANTOWA W MM korzysta się z równań wynikających z praw fizyki klasycznej i stosuje się je do jader atomów z pominięciem elektronów,
Podstawy projektowania leków wykład 10
 Podstawy projektowania leków wykład 10 Łukasz Berlicki Od eksperymentu do teorii 1964, C. Hansch i T. Fujita: QSAR 1984, P. Andrews: wkład grup funkcyjnych do oddziaływania z celem molekularnym 1985, P.
Podstawy projektowania leków wykład 10 Łukasz Berlicki Od eksperymentu do teorii 1964, C. Hansch i T. Fujita: QSAR 1984, P. Andrews: wkład grup funkcyjnych do oddziaływania z celem molekularnym 1985, P.
Komputerowe wspomaganie projektowania leków - QSAR
 Komputerowe wspomaganie projektowania leków - QSAR JAKIE OBIEKTY SĄ INTERESUJĄCE? Długość pojazdu wynosi 2 nm, szerokość 2nm. Pojazd porusza się na kołach złożonych z 60 atomów czystego węgla, uformowanych
Komputerowe wspomaganie projektowania leków - QSAR JAKIE OBIEKTY SĄ INTERESUJĄCE? Długość pojazdu wynosi 2 nm, szerokość 2nm. Pojazd porusza się na kołach złożonych z 60 atomów czystego węgla, uformowanych
Podstawy projektowania leków wykład 12
 Podstawy projektowania leków wykład 12 Łukasz Berlicki Projektowanie wspomagane komputerowo Ligand-based design QSAR i 3D-QSAR Structure-based design projektowanie oparte na strukturze celu molekularnego
Podstawy projektowania leków wykład 12 Łukasz Berlicki Projektowanie wspomagane komputerowo Ligand-based design QSAR i 3D-QSAR Structure-based design projektowanie oparte na strukturze celu molekularnego
Rysunki pochodzą z książki Chemia medyczna, G.L. Patrick, WNT. Odwołanie do wykładu z STL
 Rysunki pochodzą z książki Chemia medyczna, G.L. Patrick, WNT Odwołanie do wykładu z STL Izolacja z surowców naturalnych jak np. rośliny, tkanki zwierzęce Lek naturalny Lek biotechnologiczny Lek syntetyczny
Rysunki pochodzą z książki Chemia medyczna, G.L. Patrick, WNT Odwołanie do wykładu z STL Izolacja z surowców naturalnych jak np. rośliny, tkanki zwierzęce Lek naturalny Lek biotechnologiczny Lek syntetyczny
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Dokowanie molekularne. Karol Kamel Uniwersytet Warszawski
 molekularne Wstęp Dokowanie metoda modelowania molekularnego, pozwalająca na znalezienie położenia (i konformacji) liganda w miejscu wiążącym receptora. Informacja ta pozwala na ocenę energii swobodnej
molekularne Wstęp Dokowanie metoda modelowania molekularnego, pozwalająca na znalezienie położenia (i konformacji) liganda w miejscu wiążącym receptora. Informacja ta pozwala na ocenę energii swobodnej
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Komputerowe wspomaganie projektowanie leków
 Komputerowe wspomaganie projektowanie leków wykład II Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków wykład II Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Modelowanie molekularne w projektowaniu leków
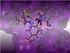 Modelowanie molekularne w projektowaniu leków Wykład I Wstęp (o czym będę a o czym nie będę mówić) Opis układu Solwent (woda z rozpuszczonymi jonami i innymi substancjami) Ligand (potencjalny lek) Makromolekuła
Modelowanie molekularne w projektowaniu leków Wykład I Wstęp (o czym będę a o czym nie będę mówić) Opis układu Solwent (woda z rozpuszczonymi jonami i innymi substancjami) Ligand (potencjalny lek) Makromolekuła
Podstawy projektowania leków wykład 13
 odstawy projektowania leków wykład 13 Łukasz Berlicki rojektowanie wspomagane komputerowo rojektowanie leków oparte na strukturze często wykorzystuje metody komputerowe, aby: rzeanalizować duŝą liczbę
odstawy projektowania leków wykład 13 Łukasz Berlicki rojektowanie wspomagane komputerowo rojektowanie leków oparte na strukturze często wykorzystuje metody komputerowe, aby: rzeanalizować duŝą liczbę
WARSZTATY olimpijskie. Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna Kinetyka
 WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Optymalizacja optymalizacji
 7 maja 2008 Wstęp Optymalizacja lokalna Optymalizacja globalna Algorytmy genetyczne Badane czasteczki Wykorzystane oprogramowanie (Algorytm genetyczny) 2 Sieć neuronowa Pochodne met-enkefaliny Optymalizacja
7 maja 2008 Wstęp Optymalizacja lokalna Optymalizacja globalna Algorytmy genetyczne Badane czasteczki Wykorzystane oprogramowanie (Algorytm genetyczny) 2 Sieć neuronowa Pochodne met-enkefaliny Optymalizacja
Kwas HA i odpowiadająca mu zasada A stanowią sprzężoną parę (podobnie zasada B i kwas BH + ):
 Spis treści 1 Kwasy i zasady 2 Rola rozpuszczalnika 3 Dysocjacja wody 4 Słabe kwasy i zasady 5 Skala ph 6 Oblicznie ph słabego kwasu 7 Obliczanie ph słabej zasady 8 Przykłady obliczeń 81 Zadanie 1 811
Spis treści 1 Kwasy i zasady 2 Rola rozpuszczalnika 3 Dysocjacja wody 4 Słabe kwasy i zasady 5 Skala ph 6 Oblicznie ph słabego kwasu 7 Obliczanie ph słabej zasady 8 Przykłady obliczeń 81 Zadanie 1 811
Podstawy projektowania leków wykład 14
 Podstawy projektowania leków wykład 14 Łukasz Berlicki Korzystne właściwości leków Wysoka aktywność i selektywność Dostępność syntetyczna Brak grup chemicznie reaktywnych MoŜliwość podawania doustnego
Podstawy projektowania leków wykład 14 Łukasz Berlicki Korzystne właściwości leków Wysoka aktywność i selektywność Dostępność syntetyczna Brak grup chemicznie reaktywnych MoŜliwość podawania doustnego
1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych.
 Tematy opisowe 1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych. 2. Dlaczego do kadłubów statków, doków, falochronów i filarów mostów przymocowuje się płyty z
Tematy opisowe 1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych. 2. Dlaczego do kadłubów statków, doków, falochronów i filarów mostów przymocowuje się płyty z
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA. Wykład 2
 PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
Podstawy chemii. dr hab. Wacław Makowski. Wykład 1: Wprowadzenie
 Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
CHEMIA. Wymagania szczegółowe. Wymagania ogólne
 CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
Spis treści. Przedmowa... XI. Rozdział 1. Pomiar: jednostki miar... 1. Rozdział 2. Pomiar: liczby i obliczenia liczbowe... 16
 Spis treści Przedmowa.......................... XI Rozdział 1. Pomiar: jednostki miar................. 1 1.1. Wielkości fizyczne i pozafizyczne.................. 1 1.2. Spójne układy miar. Układ SI i jego
Spis treści Przedmowa.......................... XI Rozdział 1. Pomiar: jednostki miar................. 1 1.1. Wielkości fizyczne i pozafizyczne.................. 1 1.2. Spójne układy miar. Układ SI i jego
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Chemia ogólna nieorganiczna Wykład XII Kinetyka i statyka chemiczna
 Chemia ogólna nieorganiczna Wykład 10 14 XII 2016 Kinetyka i statyka chemiczna Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od
Chemia ogólna nieorganiczna Wykład 10 14 XII 2016 Kinetyka i statyka chemiczna Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od
- parametry geometryczne badanego związku: współrzędne i typy atomów, ich masy, ładunki, prędkości początkowe itp. (w NAMD plik.
 Avogadro Tworzenie i manipulacja modelami związków chemicznych. W symulacjach dynamiki molekularnej kluczowych elementem jest przygotowanie układu do symulacji tzn. stworzyć pliki wejściowe zawierające
Avogadro Tworzenie i manipulacja modelami związków chemicznych. W symulacjach dynamiki molekularnej kluczowych elementem jest przygotowanie układu do symulacji tzn. stworzyć pliki wejściowe zawierające
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 2002 BYŁA DZISIAJ CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY ARKUSZ EGZAMINACYJNY I
 MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Maria Bełtowska-Brzezinska, Tomasz Węsierski
 Ćwiczenie 28 Maria Bełtowska-Brzezinska, Tomasz Węsierski BADANIE ELEKTRONODONOROWYCH I ELEKTRONOAKCEPTOROWYCH WŁAŚCIWOŚCI PODSTAWNIKÓW W OPARCIU O RÓWNANIE HAMMETTA Zagadnienia: Korelacja Hammetta, korelacja
Ćwiczenie 28 Maria Bełtowska-Brzezinska, Tomasz Węsierski BADANIE ELEKTRONODONOROWYCH I ELEKTRONOAKCEPTOROWYCH WŁAŚCIWOŚCI PODSTAWNIKÓW W OPARCIU O RÓWNANIE HAMMETTA Zagadnienia: Korelacja Hammetta, korelacja
2. Właściwości kwasowo-zasadowe związków organicznych
 2. Właściwości owo-zasadowe związków organicznych 1 2.1. Teoria Bronsteda-Lowriego Kwas - indywiduum chemiczne oddające proton Zasada - indywiduum chemiczne przyjmujące proton Proton - kation wodorkowy
2. Właściwości owo-zasadowe związków organicznych 1 2.1. Teoria Bronsteda-Lowriego Kwas - indywiduum chemiczne oddające proton Zasada - indywiduum chemiczne przyjmujące proton Proton - kation wodorkowy
Obliczenia stechiometryczne, bilansowanie równań reakcji redoks
 Obliczenia stechiometryczne, bilansowanie równań reakcji redoks Materiały pomocnicze do zajęć wspomagających z chemii opracował: dr Błażej Gierczyk Wydział Chemii UAM Obliczenia stechiometryczne Podstawą
Obliczenia stechiometryczne, bilansowanie równań reakcji redoks Materiały pomocnicze do zajęć wspomagających z chemii opracował: dr Błażej Gierczyk Wydział Chemii UAM Obliczenia stechiometryczne Podstawą
Oddziaływanie leków z celami molekularnymi i projektowanie leków
 Oddziaływanie leków z celami molekularnymi i projektowanie leków Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania (biomodellab.eu) Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych
Oddziaływanie leków z celami molekularnymi i projektowanie leków Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania (biomodellab.eu) Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych
imię i nazwisko, nazwa szkoły, miejscowość Zadania I etapu Konkursu Chemicznego Trzech Wydziałów PŁ V edycja
 Zadanie 1 (2 pkt.) Zmieszano 80 cm 3 roztworu CH3COOH o stężeniu 5% wag. i gęstości 1,006 g/cm 3 oraz 70 cm 3 roztworu CH3COOK o stężeniu 0,5 mol/dm 3. Obliczyć ph powstałego roztworu. Jak zmieni się ph
Zadanie 1 (2 pkt.) Zmieszano 80 cm 3 roztworu CH3COOH o stężeniu 5% wag. i gęstości 1,006 g/cm 3 oraz 70 cm 3 roztworu CH3COOK o stężeniu 0,5 mol/dm 3. Obliczyć ph powstałego roztworu. Jak zmieni się ph
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM. SCHEMAT OCENIANIA etap wojewódzki
 PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM SCHEMAT OCENIANIA etap wojewódzki 1. Ogólne zasady oceniania Uczeń otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom
PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM SCHEMAT OCENIANIA etap wojewódzki 1. Ogólne zasady oceniania Uczeń otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom
CHARAKTERYSTYKA KARBOKSYLANÓW
 AAKTEYSTYKA KABKSYLANÓW 1. GÓLNA AAKTEYSTYKA KWASÓW KABKSYLWY Spośród związków organicznych, które wykazują znaczną kwasowość najważniejsze są kwasy karboksylowe. Związki te zawierają w cząsteczce grupę
AAKTEYSTYKA KABKSYLANÓW 1. GÓLNA AAKTEYSTYKA KWASÓW KABKSYLWY Spośród związków organicznych, które wykazują znaczną kwasowość najważniejsze są kwasy karboksylowe. Związki te zawierają w cząsteczce grupę
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K
![dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K](/thumbs/55/36391740.jpg) RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
Za poprawną metodę Za poprawne obliczenia wraz z podaniem zmiany ph
 Zadanie 1 ( pkt.) Zmieszano 80 cm roztworu CHCH o stężeniu 5% wag. i gęstości 1,006 g/cm oraz 70 cm roztworu CHCK o stężeniu 0,5 mol/dm. bliczyć ph powstałego roztworu. Jak zmieni się ph roztworu po wprowadzeniu
Zadanie 1 ( pkt.) Zmieszano 80 cm roztworu CHCH o stężeniu 5% wag. i gęstości 1,006 g/cm oraz 70 cm roztworu CHCK o stężeniu 0,5 mol/dm. bliczyć ph powstałego roztworu. Jak zmieni się ph roztworu po wprowadzeniu
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
Atomowa budowa materii
 Atomowa budowa materii Wszystkie obiekty materialne zbudowane są z tych samych elementów cząstek elementarnych Cząstki elementarne oddziałują tylko kilkoma sposobami oddziaływania wymieniając kwanty pól
Atomowa budowa materii Wszystkie obiekty materialne zbudowane są z tych samych elementów cząstek elementarnych Cząstki elementarne oddziałują tylko kilkoma sposobami oddziaływania wymieniając kwanty pól
Egzamin maturalny z chemii - poziom rozszerzony Kryteria oceniania - model odpowiedzi. Kryteria oceniania
 ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne z poleceniem
ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne z poleceniem
Bioinformatyka wykład 9
 Bioinformatyka wykład 9 14.XII.21 białkowa bioinformatyka strukturalna krzysztof_pawlowski@sggw.pl 211-1-17 1 Plan wykładu struktury białek dlaczego? struktury białek geometria i fizyka modyfikacje kowalencyjne
Bioinformatyka wykład 9 14.XII.21 białkowa bioinformatyka strukturalna krzysztof_pawlowski@sggw.pl 211-1-17 1 Plan wykładu struktury białek dlaczego? struktury białek geometria i fizyka modyfikacje kowalencyjne
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Projekt Era inżyniera pewna lokata na przyszłość jest współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego
 TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
ZAGADNIENIA NA POPRAWĘ OCENY NIEDOSTATECZNEJ ZA SEMESTR I 2012/2013 CHEMIA. Klasa I Gimnazjum
 Klasa I Gimnazjum 1. Znajomość podstawowych elementów szkła i sprzętu laboratoryjnego. 2. Umiejętność określania właściwości substancji tj: stan skupienia, barwa, zapach, połysk, smak, palność, twardość,
Klasa I Gimnazjum 1. Znajomość podstawowych elementów szkła i sprzętu laboratoryjnego. 2. Umiejętność określania właściwości substancji tj: stan skupienia, barwa, zapach, połysk, smak, palność, twardość,
Uniwersytet Śląski w Katowicach str. 1 Wydział
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia II stopień Sylabus modułu: : Przedmiot C związany ze specjalnością (0310-CH-S2-003) Nazwa wariantu modułu (opcjonalnie): Chemoinformatyka
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia II stopień Sylabus modułu: : Przedmiot C związany ze specjalnością (0310-CH-S2-003) Nazwa wariantu modułu (opcjonalnie): Chemoinformatyka
Przegląd budowy i funkcji białek
 Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
MAŁOPOLSKI KONKURS CHEMICZNY dla uczniów dotychczasowych gimnazjów i klas dotychczasowych gimnazjów prowadzonych w szkołach innego typu
 MAŁOPOLSKI KONKURS CHEMICZNY dla uczniów dotychczasowych gimnazjów i klas dotychczasowych gimnazjów prowadzonych w szkołach innego typu Etap III (wojewódzki) Materiały dla nauczycieli Rozwiązania zadań
MAŁOPOLSKI KONKURS CHEMICZNY dla uczniów dotychczasowych gimnazjów i klas dotychczasowych gimnazjów prowadzonych w szkołach innego typu Etap III (wojewódzki) Materiały dla nauczycieli Rozwiązania zadań
Chemiczne składniki komórek
 Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Kryteria oceniania z chemii kl VII
 Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD
 Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD Aleksandra Kotynia PRACA DOKTORSKA
Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD Aleksandra Kotynia PRACA DOKTORSKA
Reakcje enzymatyczne. Co to jest enzym? Grupy katalityczne enzymu. Model Michaelisa-Mentena. Hamowanie reakcji enzymatycznych. Reakcje enzymatyczne
 Reakcje enzymatyczne Enzym białko katalizujące reakcje chemiczne w układach biologicznych (przyśpieszają reakcje przynajmniej 0 6 raza) 878, Wilhelm uehne, użył po raz pierwszy określenia enzym (w zaczynie)
Reakcje enzymatyczne Enzym białko katalizujące reakcje chemiczne w układach biologicznych (przyśpieszają reakcje przynajmniej 0 6 raza) 878, Wilhelm uehne, użył po raz pierwszy określenia enzym (w zaczynie)
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
Analiza składowych głównych. Wprowadzenie
 Wprowadzenie jest techniką redukcji wymiaru. Składowe główne zostały po raz pierwszy zaproponowane przez Pearsona(1901), a następnie rozwinięte przez Hotellinga (1933). jest zaliczana do systemów uczących
Wprowadzenie jest techniką redukcji wymiaru. Składowe główne zostały po raz pierwszy zaproponowane przez Pearsona(1901), a następnie rozwinięte przez Hotellinga (1933). jest zaliczana do systemów uczących
1. Przedmiot chemii Orbital, typy orbitali Związki wodoru z innym pierwiastkami
 1. Przedmiot chemii Orbital, typy orbitali Związki wodoru z innym pierwiastkami 2. Stechiometria. Prawa stechiometrii Roztwory buforowe Węglowce - budowa elektronowa. Ogólna charakterystyka 3. Mikro- i
1. Przedmiot chemii Orbital, typy orbitali Związki wodoru z innym pierwiastkami 2. Stechiometria. Prawa stechiometrii Roztwory buforowe Węglowce - budowa elektronowa. Ogólna charakterystyka 3. Mikro- i
Regresja wieloraka Ogólny problem obliczeniowy: dopasowanie linii prostej do zbioru punktów. Najprostszy przypadek - jedna zmienna zależna i jedna
 Regresja wieloraka Regresja wieloraka Ogólny problem obliczeniowy: dopasowanie linii prostej do zbioru punktów. Najprostszy przypadek - jedna zmienna zależna i jedna zmienna niezależna (można zobrazować
Regresja wieloraka Regresja wieloraka Ogólny problem obliczeniowy: dopasowanie linii prostej do zbioru punktów. Najprostszy przypadek - jedna zmienna zależna i jedna zmienna niezależna (można zobrazować
Wydział Chemiczny Wybrzeże Wyspiańskiego 27, Wrocław. Prof. dr hab. Ilona Turowska-Tyrk Wrocław, r.
 Wydział Chemiczny Wybrzeże Wyspiańskiego 27, 50-370 Wrocław Prof. dr hab. Ilona Turowska-Tyrk Wrocław, 18.01.2016 r. Recenzja rozprawy doktorskiej mgr Pauliny Klimentowskiej pt. Krystalochemia wybranych
Wydział Chemiczny Wybrzeże Wyspiańskiego 27, 50-370 Wrocław Prof. dr hab. Ilona Turowska-Tyrk Wrocław, 18.01.2016 r. Recenzja rozprawy doktorskiej mgr Pauliny Klimentowskiej pt. Krystalochemia wybranych
Elektrostatyka ŁADUNEK. Ładunek elektryczny. Dr PPotera wyklady fizyka dosw st podypl. n p. Cząstka α
 Elektrostatyka ŁADUNEK elektron: -e = -1.610-19 C proton: e = 1.610-19 C neutron: 0 C n p p n Cząstka α Ładunek elektryczny Ładunek jest skwantowany: Jednostką ładunku elektrycznego w układzie SI jest
Elektrostatyka ŁADUNEK elektron: -e = -1.610-19 C proton: e = 1.610-19 C neutron: 0 C n p p n Cząstka α Ładunek elektryczny Ładunek jest skwantowany: Jednostką ładunku elektrycznego w układzie SI jest
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Strategie projektowania leków
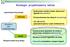 Strategie projektowania leków Ligand-based drug design nieznana Budowanie modelu miejsc aktywnych liganda (farmakofor) Przeszukiwanie baz danych (screening) Struktura celu molekularnego znana 1D i 3D QSAR
Strategie projektowania leków Ligand-based drug design nieznana Budowanie modelu miejsc aktywnych liganda (farmakofor) Przeszukiwanie baz danych (screening) Struktura celu molekularnego znana 1D i 3D QSAR
KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 5 marca 2010 r. zawody III stopnia (wojewódzkie)
 KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 5 marca 2010 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 5 marca 2010 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
Modelowanie interakcji helis transmembranowych
 Modelowanie interakcji helis transmembranowych Witold Dyrka, Jean-Christophe Nebel, Małgorzata Kotulska Instytut Inżynierii Biomedycznej i Pomiarowej, Politechnika Wrocławska Faculty of Computing, Information
Modelowanie interakcji helis transmembranowych Witold Dyrka, Jean-Christophe Nebel, Małgorzata Kotulska Instytut Inżynierii Biomedycznej i Pomiarowej, Politechnika Wrocławska Faculty of Computing, Information
WOJEWÓDZKI KONKURS CHEMICZNY
 Kod ucznia Liczba punktów WOJEWÓDZKI KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM W ROKU SZKOLNYM 2015/2016 9 MARCA 2016 R. 1. Test konkursowy zawiera 10 zadań. Są to zadania otwarte, za które maksymalnie możesz
Kod ucznia Liczba punktów WOJEWÓDZKI KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM W ROKU SZKOLNYM 2015/2016 9 MARCA 2016 R. 1. Test konkursowy zawiera 10 zadań. Są to zadania otwarte, za które maksymalnie możesz
Wiązania kowalencyjne
 Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wymiana ciepła. Ładunek jest skwantowany. q=n. e gdzie n = ±1, ±2, ±3 [1C = 6, e] e=1, C
![Wymiana ciepła. Ładunek jest skwantowany. q=n. e gdzie n = ±1, ±2, ±3 [1C = 6, e] e=1, C Wymiana ciepła. Ładunek jest skwantowany. q=n. e gdzie n = ±1, ±2, ±3 [1C = 6, e] e=1, C](/thumbs/63/50333873.jpg) Wymiana ciepła Ładunek jest skwantowany ładunek elementarny ładunek pojedynczego elektronu (e). Każdy ładunek q (dodatni lub ujemny) jest całkowitą wielokrotnością jego bezwzględnej wartości. q=n. e gdzie
Wymiana ciepła Ładunek jest skwantowany ładunek elementarny ładunek pojedynczego elektronu (e). Każdy ładunek q (dodatni lub ujemny) jest całkowitą wielokrotnością jego bezwzględnej wartości. q=n. e gdzie
Rzędy wiązań chemicznych
 Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Podstawowe prawa opisujące właściwości gazów zostały wyprowadzone dla gazu modelowego, nazywanego gazem doskonałym (idealnym).
 Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Ocenę niedostateczną otrzymuje uczeń, który: Ocenę dopuszczającą otrzymuje uczeń, który: Ocenę dostateczną otrzymuje uczeń, który:
 Kryteria oceniania z chemii dla klasy 3A i 3B Gimnazjum w Borui Kościelnej Rok szkolny: 2015/2016 Semestr: pierwszy Opracowała: mgr Krystyna Milkowska, mgr inż. Malwina Beyga Ocenę niedostateczną otrzymuje
Kryteria oceniania z chemii dla klasy 3A i 3B Gimnazjum w Borui Kościelnej Rok szkolny: 2015/2016 Semestr: pierwszy Opracowała: mgr Krystyna Milkowska, mgr inż. Malwina Beyga Ocenę niedostateczną otrzymuje
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj.
 Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj. Tytuł i numer rozdziału w podręczniku Nr lekcji Temat lekcji Szkło i sprzęt laboratoryjny 1. Pracownia chemiczna.
Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj. Tytuł i numer rozdziału w podręczniku Nr lekcji Temat lekcji Szkło i sprzęt laboratoryjny 1. Pracownia chemiczna.
Reakcje chemiczne. Typ reakcji Schemat Przykłady Reakcja syntezy
 Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab
 SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab CZĄSTECZKA I RÓWNANIE REKCJI CHEMICZNEJ potrafi powiedzieć co to jest: wiązanie chemiczne, wiązanie jonowe, wiązanie
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab CZĄSTECZKA I RÓWNANIE REKCJI CHEMICZNEJ potrafi powiedzieć co to jest: wiązanie chemiczne, wiązanie jonowe, wiązanie
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM ROZSZERZONY
 Próbny egzamin maturalny z chemii 00r. ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach.
Próbny egzamin maturalny z chemii 00r. ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach.
Wykorzystanie bazy Cambridge Structural Database w poszukiwaniu substancji hamujących aktywność enzymatyczną
 ISTRUKCJA DO ĆWICZEŃ LABORATORYJYCH Wykorzystanie bazy Cambridge Structural Database w poszukiwaniu substancji hamujących aktywność enzymatyczną CZĘŚĆ I Zapoznanie się ze strukturą i funkcjami bazy. Demonstracja
ISTRUKCJA DO ĆWICZEŃ LABORATORYJYCH Wykorzystanie bazy Cambridge Structural Database w poszukiwaniu substancji hamujących aktywność enzymatyczną CZĘŚĆ I Zapoznanie się ze strukturą i funkcjami bazy. Demonstracja
- w nawiasach kwadratowych stężenia molowe.
 Cz. VII Dysocjacja jonowa, moc elektrolitów, prawo rozcieńczeń Ostwalda i ph roztworów. 1. Pojęcia i definicja. Dysocjacja elektroniczna (jonowa) to samorzutny rozpad substancji na jony w wodzie lub innych
Cz. VII Dysocjacja jonowa, moc elektrolitów, prawo rozcieńczeń Ostwalda i ph roztworów. 1. Pojęcia i definicja. Dysocjacja elektroniczna (jonowa) to samorzutny rozpad substancji na jony w wodzie lub innych
Wykład 11 Równowaga kwasowo-zasadowa
 Wykład 11 Równowaga kwasowo-zasadowa JS Skala ph Skala ph ilościowa skala kwasowości i zasadowości roztworów wodnych związków chemicznych. Skala ta jest oparta na aktywności jonów hydroniowych [H3O+] w
Wykład 11 Równowaga kwasowo-zasadowa JS Skala ph Skala ph ilościowa skala kwasowości i zasadowości roztworów wodnych związków chemicznych. Skala ta jest oparta na aktywności jonów hydroniowych [H3O+] w
MECHANIZMY FRAGMENTACJI ZWIĄZKÓW ORGANICZNYCH. Copyright 2003 Witold Danikiewicz
 MECANIZMY FAGMENTACJI ZWIĄZKÓW GANICZNYC Copyright 2003 Cechy charakterystyczne zjawiska fragmentacji jonów proces jednocząsteczkowy; szybkość fragmentacji jest mała w porównaniu z szybkością rozpraszania
MECANIZMY FAGMENTACJI ZWIĄZKÓW GANICZNYC Copyright 2003 Cechy charakterystyczne zjawiska fragmentacji jonów proces jednocząsteczkowy; szybkość fragmentacji jest mała w porównaniu z szybkością rozpraszania
Chemia I Semestr I (1 )
 1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
ZASTOSOWANIE TECHNIK CHEMOMETRYCZNYCH W BADANIACH ŚRODOWISKA. dr inż. Aleksander Astel
 ZASTOSOWANIE TECHNIK CHEMOMETRYCZNYCH W BADANIACH ŚRODOWISKA dr inż. Aleksander Astel Gdańsk, 22.12.2004 CHEMOMETRIA dziedzina nauki i techniki zajmująca się wydobywaniem użytecznej informacji z wielowymiarowych
ZASTOSOWANIE TECHNIK CHEMOMETRYCZNYCH W BADANIACH ŚRODOWISKA dr inż. Aleksander Astel Gdańsk, 22.12.2004 CHEMOMETRIA dziedzina nauki i techniki zajmująca się wydobywaniem użytecznej informacji z wielowymiarowych
Podstawy termodynamiki.
 Podstawy termodynamiki. Termodynamika opisuje ogólne prawa przemian energetycznych w układach makroskopowych. Określa kierunki procesów zachodzących w przyrodzie w sposób samorzutny, jak i stanów końcowych,
Podstawy termodynamiki. Termodynamika opisuje ogólne prawa przemian energetycznych w układach makroskopowych. Określa kierunki procesów zachodzących w przyrodzie w sposób samorzutny, jak i stanów końcowych,
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem
 Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Równowaga kwasowo-zasadowa. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowaga kwasowozasadowa Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Krytyka pojęcia ph ph = log [H + ] ph [H+] 1 100 mmol/l D = 90 mmol/l 2 10 mmol/l D = 9 mmol/l 3 1 mmol/l 2 Krytyka pojęcia
Równowaga kwasowozasadowa Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Krytyka pojęcia ph ph = log [H + ] ph [H+] 1 100 mmol/l D = 90 mmol/l 2 10 mmol/l D = 9 mmol/l 3 1 mmol/l 2 Krytyka pojęcia
Sektorowy formalizm porównawczej analizy powierzchni cząsteczkowej (s-comsa) zastosowanie do modelowania zależności struktura-aktywność
 Tomasz Magdziarz Sektorowy formalizm porównawczej analizy powierzchni cząsteczkowej (s-comsa) zastosowanie do modelowania zależności struktura-aktywność Promotor pracy: prof. dr hab. Jarosław Polański
Tomasz Magdziarz Sektorowy formalizm porównawczej analizy powierzchni cząsteczkowej (s-comsa) zastosowanie do modelowania zależności struktura-aktywność Promotor pracy: prof. dr hab. Jarosław Polański
KORELACJE I REGRESJA LINIOWA
 KORELACJE I REGRESJA LINIOWA Korelacje i regresja liniowa Analiza korelacji: Badanie, czy pomiędzy dwoma zmiennymi istnieje zależność Obie analizy się wzajemnie przeplatają Analiza regresji: Opisanie modelem
KORELACJE I REGRESJA LINIOWA Korelacje i regresja liniowa Analiza korelacji: Badanie, czy pomiędzy dwoma zmiennymi istnieje zależność Obie analizy się wzajemnie przeplatają Analiza regresji: Opisanie modelem
Wykład 21 XI 2018 Żywienie
 Wykład 21 XI 2018 Żywienie Witold Bekas SGGW Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od warunków przebiegu reakcji pomaga
Wykład 21 XI 2018 Żywienie Witold Bekas SGGW Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od warunków przebiegu reakcji pomaga
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
