ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(97)/2014
|
|
|
- Maksymilian Jakubowski
- 8 lat temu
- Przeglądów:
Transkrypt
1 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(97)/2014 Władysław Mitianiec 1 MODELOWANIE I SYMULACJA REDUKCJI NO X W SELEKTYWNYM REAKTORZE KATALITYCZNYM l. Wstęp Jednymi z najbardziej szkodliwych składników spalin emitowanych przez silnik wysokoprężny są tlenki azotu. Z tego względu zachodzi potrzeba zmniejszenia lub całkowitej redukcji tych związków poprzez stosowanie redukujących reaktorów katalitycznych. W ostatnich latach do produkcji wprowadzono selektywne redukujące reaktory katalityczne (Selective Catalytic Reduction) zwane krótko SCR. Zjawiska fizyczne i reakcje chemiczne zachodzące w selektywnym reaktorze redukującym (SCR) umożliwiają zmniejszenie ilości emitowanych tlenków azotu przez silnik wysokoprężny. Wtrysk 32,5% wodnego roztworu mocznika (ang. urea) zwanego handlowo jako AdBlue do przewodu przed reaktorem katalitycznym wskutek istnienia jeszcze dużej temperatury gazów spalinowych umożliwia jego odparowanie i uzyskanie mocznika w formie gazowej. Artykuł przedstawia modelowanie i wstępne obliczenia działania redukującego tlenków azotu w selektywnym reaktorze katalitycznym (SCR) z ujęciem termolizy i hydrolizy czynnika redukującego AdBlue. Pokazano wirtualny schemat układu reaktora wraz z modelem obliczeniowym ujmującym reakcje chemiczne hydrolizy i termolizy oraz reakcje redukcji z udziałem katalizatora między amoniakiem i trzema związkami tlenowymi azotu. W pracy przedstawiono wyniki obliczeń stopnia redukcji poszczególnych tlenków azotu z przebiegiem temperatury wewnątrz reaktora i na wylocie z reaktora dla przyjętych wstępnie wartości parametrów wlotowych oraz przyjętej geometrii selektywnego redukującego reaktora katalitycznego. Obliczenia wykonano za pomocą programu GT-Power ver Cel i zakres pracy Nowo produkowane silniki wysokoprężne Heavy Duty (HD) są dostarczane z reaktorem SCR pracującym z układem dostarczania wodnego roztworu mocznika. Z tego względu celem pracy było rozpoznanie zjawisk fizycznych wynikających z warunków przepływu spalin, temperatury oraz składu chemicznego spalin zawierających znaczne ilości NOx, a wpływających na pracę reaktora. Jednym z istotnych celów pracy było przedstawienie zjawisk fizycznych, reakcji chemicznych oraz zmian udziałów masowych i parametrów termodynamicznych w układzie SCR. Zakres pracy obejmował następujące zagadnienia: przedstawienie modelu fizycznego i modelu obliczeniowego, przedstawienie reakcji procesu odparowania, termolizy oraz hydrolizy, a także reakcji powierzchniowych w monolicie reaktora z udziałem zeolitu jako katalizatora. Przedstawienie modelu matematycznego procesów zachodzących w systemie selektywnej redukcji katalitycznej NOx pozwoliło na wykonanie symulacji numerycznych procesów fizycznych i chemicznych w nim zachodzących. Wybrane wyniki badań symulacyjnych zostały przedstawione na wykresach i odpowiednio wyjaśnione. 1 dr hab. inż. Władysław Mitianiec, Prof. PK, Instytut Pojazdów Samochodowych i Silników Spalinowych Politechniki Krakowskiej 89
2 3. Model chemiczny reaktora SCR Reaktor SCR wykorzystuje 32,5% roztwór wodny mocznika (ang. urea) o handlowej nazwie AdBlue, który podlega wstępnemu rozpadowi na amoniak i dwutlenek węgla w celu zmniejszenia udziału molowego, a nawet całkowitej redukcji dwóch tlenków azotu: NO i NO 2 w gazach spalinowych silnika wysokoprężnego. Spaliny po przejściu przez reaktor utleniający DOC oraz filtr cząstek stałych DPF zostają skierowane do reaktora SCR. Wtryskiwany do przewodu wylotowego mocznik przed SCR ulega odparowaniu wskutek jeszcze dużej temperatury spalin, a następnie ulega rozpadowi termicznemu na amoniak i kwas izocyjankowy, a następnie w procesie hydrolizy wydzielony kwas w połączeniu z parą wodną tworzy amoniak i dwutlenek węgla. Mocznik o wzorze chemicznym (NH 2 ) 2 CO w procesie termolizy i hydrolizy wydziela więc dodatkowo niewielkie ilości dwutlenku węgla oraz znaczne ilości amoniaku. Powierzchniowe reakcje chemiczne zachodzące najczęściej w zeolitowym reaktorze SCR między tlenkami azotu, amoniakiem i resztą tlenu w spalinach powodują rozpad tlenków azotu i wydzielenie się azotu oraz pary wodnej. Reakcje redukcji tlenków azotu nie wykorzystują w pełni amoniaku, co wpływa na pozostawanie pewnej ilości amoniaku w spalinach. Ogólny schemat ideowy działania systemu reaktora SCR pokazany jest na Rys. 1 ujmujący przestrzeń wtryskową wodnego roztworu mocznika, moduł obliczeniowy reakcji kinetycznych termolizy i hydrolizy, model selektywnego redukującego reaktora katalitycznego opartego na złożu zeolitowym (Z) jako katalizatorze oraz układ sterowania masowego natężenia przepływu wodnego roztworu mocznika poprzez podanie elektrycznego sygnału otwarcia wtryskiwacza. Rys. 1. Schemat działania układu selektywnego redukującego reaktora katalitycznego Regulacja ilości wtryskiwanego mocznika następuje przez sterownik odbierający sygnał wyjściowy z przewodu za SCR informujący o ilości NOx i NH 3 w gazach wylotowych. Porównanie udziałów objętościowych z zadaną wartością dopuszczalnych ilości tych związków chemicznych przetwarzane jest w sterowniku, który daje sygnał o zwiększeniu lub zmniejszeniu ilości wtryskiwanego roztworu mocznika. Model obliczeniowy uwzględnia te informacje umożliwiając obserwację zmiany ilości tlenków azotu oraz amoniaku na podstawie sygnałów przed i za SCR. 90
3 4. Reakcje chemiczne w SCR Podstawą skutecznego działania reaktora SCR są powierzchniowe reakcje chemiczne między amoniakiem otrzymywanym z mocznika a tlenkami azotu w odpowiedniej temperaturze w ceramicznym lub metalowym złożu pokrytym katalizatorem (najczęściej zeolitem). Ze względów bezpieczeństwa do układu wprowadzony jest wodny roztwór mocznika, który w obecności gorących gazów jest odparowany. Proces odparowania zachodzi zgodnie z równaniem (1). W wyniku tego wytwarza się stały produkt, jakim jest mocznik ora para wodna. [(NH 2 ) 2 CO + H 2 O] liq (NH 2 ) 2 CO sol + H 2 O gas (1) Następnie mocznik podlega procesowi termolizy, gdzie wskutek dostarczonego ciepła od gazów spalinowych rozpada się on na amoniak NH 3 w postaci gazowej oraz kwas izocyjankowy HNCO: 1. (NH 2 ) 2 CO sol NH 3,gas + HNCO gas (2) Kwas izocyjankowy łączy się następnie z parą wodną (reakcja hydrolizy) tworząc gazowy amoniak oraz dwutlenek węgla. 2. HNCO gas + H 2 O gas NH 3,gas + CO 2,gas (3) Reakcja hydrolizy powoduje zwiększenie ilości dwutlenku węgla w gazach wylotowych zależnie od ilości podawanego mocznika do układu SCR. Powyższe reakcje chemiczne zachodzą w strefie przygotowawczej tego reaktora i produktami tych reakcji są amoniak, para wodna oraz dwutlenek węgla. Kolejne reakcje chemiczne dotyczące już redukcji tlenków azotu zachodzą w monolicie SCR przy udziale zeolitu (Z) jako katalizatora i są reakcjami powierzchniowymi [1][2]. Poniżej podano podstawowe powierzchniowe reakcje chemiczne zachodzące w monolicie między amoniakiem, tlenem zawartym w spalinach oraz dwoma tlenkami azotu NO i NO 2 : 3. Z + NH 3 ZNH 3 (4) 4. ZNH 3 Z + NH 3 (5) 5. 4ZNH 3 + 3O 2 2N2 + 6H 2 O + 4Z (6) 6. 4ZNH 3 +4NO + O 2 4N 2 +6H 2 O +4Z (7) 7. NO + 0.5O 2 NO 2 (8) 8. 4ZNH 3 +2NO + 2NO 2 4N 2 +6H 2 O +4Z (9) 9. 8ZNH 3 + 6NO 2 7N H 2 O +8Z (10) Szybkość reakcji kinetycznych zależy od temperatury procesu, energii aktywacji, udziału molowego substratów oraz pewnych stałych ustalonych na drodze doświadczalnej. Szybkości wywiązywania się k-tego związku chemicznego można zapisać w postaci sumy z wszystkich reakcji chemicznych, w których ten związek brał udział: 91
4 gdzie: ki k I q (k = 1,...,K) (11) " ki i 1 ' ki ki i Stopień przyrostu zmiennej q i dla i-tej reakcji określa się jako różnicę szybkości tworzenia danego związku k dla reakcji postępowej i odwrotnej: K ki ' ki (12) q k X k X i fi k ri k k 1 k 1 gdzie: X k - udział molowy związku k w i-tej reakcji, k fi - stała szybkości i-tej reakcji postępowej, k ri - stała szybkości i-tej reakcji odwrotnej Stałe szybkości poszczególnych reakcji postępowych i odwrotnych przedstawia się w formie równań Arrheniusa: k E fa ErA n f MRT n MRT fi AriT e k A T r e ri ri gdzie: A f - stała danej reakcji, E A - energia aktywacji na mol reagentów lub produktów, n - wykładnik temperatury T. 92 K " (13) Tabela 1. Stałe reakcji Arrheniusa w procesie hydrolizy, termolizy i redukcji w SCR [3] Reakcja Nr Stała A ri Wykładnik temperatury n f Energia aktywacji E fa [J/mol] 1 1,0e ,89 2 1,0e ,34 3 0, ,5e ,28 6 0, , Symulacja procesu redukcji NOx w SCR W celu oszacowania szybkości odpowiedzi reakcji układu SCR na zmianę udziału molowego tlenków azotu w spalinach opracowano model symulacyjny procesu redukcji NOx w zeolitowym reaktorze SCR. Model uwzględnia reakcje odparowania, termolizy i hydrolizy oraz powierzchniowe reakcje chemiczne przy udziale zeolitu jako katalizatora na osnowie ceramicznej, którym był kordieryt. Obliczenia przeprowadzono za pomocą programu GT-Suite ver. 7.3 [4]. Schemat modelu obliczeniowego układu SCR jest przedstawiony na Rys. 2 z uwzględnieniem monitorowania NO, NO 2, N 2 O i NH 3 oraz całkowitego udziału masowego NOx w spalinach. Model ten uwzględnia masowe natężenie przepływu czynnika redukującego, jego własności chemiczne i
5 termodynamiczne do wstępnej części układu SCR. W czasie wtrysku wodnego roztworu mocznika analizowany jest stopień odparowania wody zależny od temperatury przepływających gazów spalinowych. Odparowanie wody analizowane jest w całym układzie przepływowym SCR. Drugi moduł obliczeniowy uwzględnia kinetykę reakcji chemicznych procesu termolizy (2) w czasie, którego następuje rozpad mocznika na kwas izocyjankowy i amoniak oraz procesu hydrolizy (3), w wyniku którego powstaje amoniak i dwutlenek węgla z kwasu izocyjankowego i wody. Właściwy proces redukcji tlenków azotu zachodzi w module trzecim, w którym rozpatrywane są powierzchniowe reakcje kinetyczne (3-9) z udziałem zeolitu. Przepływowy model obliczeniowy reaktora SCR traktuje reaktor katalityczny jako zbiór przewodów równoległych o małym przekroju odpowiadającemu średnicy hydraulicznej rzeczywistego kanału i uwzględnia również rzeczywistą liczbę tych kanałów. Model pobiera informacje z wylotu reaktora o bieżącym udziale molowym tlenków azotu i amoniaku i przesyła te informacje do układu sterującego wtryskiem wodnego roztworu mocznika. Rys. 2. Model obliczeniowy redukcji NOx w reaktorze SCR 6. Dane początkowe i brzegowe Do obliczeń przyjęto stałe parametry gazów spalinowych na wlocie podane w Tab. 2, które jednocześnie są warunkami brzegowymi i początkowymi dla przepływu stacjonarnego. Parametry geometryczne monolitu SCR przedstawione są w Tab
6 Tabela 2. Parametry brzegowe i początkowe dla wlotu i wylotu spalin Parametr Jednostka Wartość Masowe natężenie przepływu g/s 15 spalin Temperatura wlotowa K 600 Temperatura początkowa K 400 Udział molowy N 2 na wlocie [-] 0,772 Udział molowy O 2 na wlocie [-] 0,032 Udział molowy NO na wlocie [-] Udział molowy NO 2 na wlocie [-] 0,0015 Udział molowy N 2 O na wlocie [-] 0 Udział molowy H 2 O na wlocie [-] Udział molowy CO 2 na wlocie [-] 0,132 Temperatura ścianek reaktora K 500 Tabela 3. Wymiary monolitu SCR Parametr Jednostka Wymiar Materiał - kordieryt Średnica czynna reaktora mm 90 Długość mm 135 Gęstość komórek 1/cm 2 62 Grubość ścianek mm 0,165 Aktywna gęstość zeolitu mol/m Wyniki obliczeń Obliczenia uwzględniały zarówno warunki przepływu gazów spalinowych jak i reakcje chemiczne podane w paragrafie 4. W stanie początkowym nie uwzględniono udziału NOx w reaktorze SCR, a gazem wypełniającym było powietrze. Badano szybkość reakcji w reaktorze od chwili rozpoczęcia wlotu gazów spalinowych z udziałem NO 2 i NO. Zmiany temperatury gazów, ilości pary wodnej oraz wilgotności spalin w części wtryskowej mocznika przedstawiono na Rys. 3. Temperatura gazów obniża się o prawie 70 K, a udział masowy pary wodnej w spalinach wzrasta od 0 do 0,05 po 10 s od chwili rozpoczęcia wtrysku mocznika. Należy zauważyć szybki wzrost udziału pary wodnej i wilgotności gazów na początku procesu wtrysku mocznika. 94
7 Rys. 3. Zmiana udziału masowego pary wodnej, wilgotności gazu oraz temperatury gazów spalinowych w przewodzie wtryskowym wodnego roztworu mocznika Działanie reaktora SCR jest prawie natychmiastowe, gdyż po około 4 s od chwili początkowej, kiedy gazy spalinowe o temperaturze 600 K wpłynęły do przewodu wtryskowego następuje prawie całkowita redukcja NO (Rys. 4). Dopuszczalna granica 25 ppm (limit) osiągana jest już po 2 s. Podobny charakter zmian zachodzi również w przypadku redukcji NO 2 (Rys. 5). W obliczeniach uwzględniono taki sam udział molowy NO i NO 2 w spalinach na wlocie wynoszący 0,0015. Charakter zmian redukcji tlenków azotu uzależniony jest proporcjonalnie do wzrostu temperatury, gdyż wykładnik temperatury w równaniach Arrheniusa wynosi 0. Najszybciej zachodzi reakcja Nr 7, w której NO przekształca się w NO 2, przy dużej wartości stałej reakcji i dużej wartości energii aktywacji. Ogólna ilość tlenków azotu zmienia się w podobny sposób jak zmiany NO i NO 2, gdyż stosunek molowy tych związków na wlocie wynosił jak 1:1. Porównanie udziału molowego NOx na wlocie i wylocie oraz stopień ich redukcji jest przedstawiony na Rys. 6. Całkowity udział molowy NOx w spalinach został założony na poziomie 3000 ppm. Całkowita redukcja NOx w monolicie SCR w wyniku powierzchniowych reakcji kinetycznych następuje już po 4 s od chwili wlotu gazów spalinowych do reaktora. Niewielki spadek udziału molowego tlenków azotu na wlocie monolitu jest efektem wzrostu masy gazu w wyniku dozowania mocznika przekształconego w reakcjach termolizy i hydrolizy na amoniak i dwutlenek węgla. 95
8 Rys. 4. Zmienność udziału molowego NO przed i za reaktorem SCR w funkcji czasu Rys. 5. Zmienność udziału molowego NO 2 przed i za reaktorem SCR w funkcji czasu W symulacji założono jednakową początkową temperaturę czynnika roboczego w całym układzie równą 400 K. Zmiana temperatury spalin w monolicie oraz ścianek monolitu katalitycznego SCR pokazano na Rys. 7. Stała ilość tlenków azotu o dużym udziale molowym w spalinach na wlocie do reaktora wymaga również dużej ilości mocznika. Powoduje to znaczny przyrost udziału molowego NH 3 przed i za monolitem SCR. Za reaktorem udział molowy NH 3 jest 10-krotnie mniejszy niż przed reaktorem (Rys. 8). Pomimo tego faktu założony limit udziału molowego amoniaku na wylocie 96
9 wynoszący 25 ppm jest wielokrotnie przekroczony. Tylko zmniejszenie udziału molowego tlenków azotu pozwala na ograniczenie ilości emitowanego amoniaku do atmosfery. Rys. 6. Ogólny udział molowy NOx przed i za reaktorem SCR oraz stopień redukcji NOx Rys. 7. Zmienność temperatury spalin w reaktorze i temperatury ścianek reaktora Na Rys. 9 pokazano zmiany udziałów masowych H 2 O, CO 2 i O 2 na wylocie z układu SCR. Efektem działania reaktora SCR jest zwiększenie udziału masowego CO 2 od wartości początkowej 0,196 do wartości 0,197 w wyniku reakcji hydrolizy. Udział masowy pary wodnej w spalinach wzrósł od wartości 0,037 do 0,055, natomiast udział 97
10 masowy tlenu zmniejszył się od wartości początkowej 0,0345 do 0,0337. Masowe natężenie gazów wylotowych zmieniło się poprzez dodanie wodnego roztworu mocznika. Rys. 8. Zmiana udziału molowego amoniaku przed i za reaktorem SCR oraz wartość sterująca dla regulatora wtrysku mocznika Rys. 9. Udziały masowe pary wodnej, tlenu i dwutlenku węgla w spalinach za reaktorem 8. Podsumowanie Zastosowanie reaktora SCR z wtryskiem wodnego roztworu mocznika (AdBlue) umożliwia prawie całkowite usunięcie tlenków azotu ze spalin. W pracy podano metodę sterowania pracą wtryskiwacza AdBlue, przedstawiono reakcje chemiczne zachodzące w 98
11 zeolitowym reaktorze SCR z uwzględnieniem odparowania, procesu hydrolizy i termolizy oraz powierzchniowych reakcji z udziałem zeolitu. Na podstawie badań symulacyjnych stwierdzono następujące zjawiska: 1. Zachodzi niewielki procentowy przyrost dwutlenku węgla w spalinach wynikający z procesu hydrolizy kwasu izocyjankowego. 2. Następuje przyrost masowego udziału pary wodnej o prawie 50% oraz niewielki spadek masowego udziału tlenu (o około 5%) w spalinach. 3. W spalinach stwierdza się obecność amoniaku o udziale molowym około 0, Całkowita redukcja tlenków azotu (NO i NO 2 ) zachodzi w czasie około 5 s od chwili rozpoczęcia wtrysku wodnego roztworu mocznika. 5. Temperatura pracy ścianek reaktora katalitycznego zmienia się o około 1 K, natomiast temperatura spalin w reaktorze zmienia się ustabilizowana jest na jednakowym poziomie około 550 K. 6. Temperatura gazów w przewodzie wtryskowym maleje wskutek odparowania AdBlue o około 65 K, a udział masowy pary wodnej w tym przewodzie wzrasta o około 45%. Przeprowadzenie obliczeń pracy reaktora SCR z wykorzystaniem kinetycznych procesów chemicznych umożliwia dokonanie wstępnej oceny możliwości redukcji tlenków azotu. Natomiast badania doświadczalne na konkretnym silniku z układem SCR powinny służyć do weryfikacji stałych w reakcjach Arrheniusa w czasie rzeczywistym. Literatura: [1] Benjamin S.F i inni: Tuning the standard SCR reaction kinetics to model NO conversion in a diesel engine, SAE paper , Warrendale, 2012 [2] Schaub G. i inni: Kinetic analysis of selective catalytic NOx reduction (SCR) in a catalytic filter, Chemical Engineering and Processes, No 42, p , Elsevier, 2003 [3] Smith M.: Experimental and modeling studies of lean and reach exhaust conditions for selective and catalytic reduction of NOx with NH3, PhD Thesis, University of Michigan, Dearborn, 2010 [4] GT-Suite. Exhaust Aftertreatment. Application Manual, ver. 7.3, Gamma Techn., 2012 Streszczenie Praca przedstawia modelowanie i wstępne obliczenia działania redukującego tlenków azotu w selektywnym reaktorze katalitycznym (SCR) z ujęciem termolizy i hydrolizy czynnika redukującego urea (AdBlue). Pokazano wirtualny schemat układu reaktora wraz z model obliczeniowym ujmującym reakcje chemiczne hydrolizy i termolizy oraz reakcje redukcji z udziałem katalizatora między amoniakiem i związkami tlenowymi azotu. W pracy pokazano wyniki obliczeń stopnia redukcji poszczególnych tlenków azotu oraz zmiany temperatury wewnątrz reaktora i na wylocie z reaktora dla przyjętych wstępnie wartości parametrów wlotowych oraz przyjętej geometrii selektywnego reaktora katalitycznego. Obliczenia wykonano za pomocą programu GT- Power ver.7.3. Słowa kluczowe: SCR, NO x 99
12 MODELLING AND SIMULATION OF NOx REDUCTION IN THE SELECTIVE CATALYTIC REACTOR Abstract The work presents modelling and initial calculations of reduction activity of nitrogen oxides in a reactor with Selective Catalytic Reduction (SCR) with taking into account the hydrolysis and thermolysis reactions of reduction medium such as urea (AdBlue. The virtual scheme of the reactor system is presented with the calculation model containing the chemical reactions of hydrolysis, thermolysis and surface reduction reactions between ammonia and oxygen compounds of nitrogen with a presence of the catalyst. The calculation results of reduction ratio of the particular nitrogen oxides and variations of temperature inside the reactor and in at outflow are presented for the assumed initial parameters of the exhaust gases and assumed geometry of the SCR reactor monolith. The calculations were carried out by means of GT-Suite program ver.7.3. Keywords: SCR, NO x 100
BADANIA SYMULACYJNE I EKSPERYMENTALNE UTLENIAJĄCEGO REAKTORA KATALITYCZNEGO SYSTEMU FILTRA CZĄSTEK STAŁYCH W PROGRAMIE AVL BOOST
 Stanisław Kruczyński 1, Wojciech Kamela 2, Kamil Duniec 2 BADANIA SYMULACYJNE I EKSPERYMENTALNE UTLENIAJĄCEGO REAKTORA KATALITYCZNEGO SYSTEMU FILTRA CZĄSTEK STAŁYCH W PROGRAMIE AVL BOOST Streszczenie.
Stanisław Kruczyński 1, Wojciech Kamela 2, Kamil Duniec 2 BADANIA SYMULACYJNE I EKSPERYMENTALNE UTLENIAJĄCEGO REAKTORA KATALITYCZNEGO SYSTEMU FILTRA CZĄSTEK STAŁYCH W PROGRAMIE AVL BOOST Streszczenie.
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012
 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/12 Stanisław W. Kruczyński 1, Marcin K. Wojs 2, Piotr Orliński 3 OCENA PRZEMIAN TLENKÓW AZOTU W UTLENIAJĄCYCH REAKTORACH KATALITYCZNYCH SYSTEMU FILTRÓW CZĄSTEK
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/12 Stanisław W. Kruczyński 1, Marcin K. Wojs 2, Piotr Orliński 3 OCENA PRZEMIAN TLENKÓW AZOTU W UTLENIAJĄCYCH REAKTORACH KATALITYCZNYCH SYSTEMU FILTRÓW CZĄSTEK
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012
 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012 Wojciech Kamela 1 Stanisław Kruczyński 2 PORÓWNANIE WŁAŚCIWOŚCI KATALITYCZNYCH TLENKOWYCH I PLATYNOWYCH REAKTORÓW SYSTEMU NH 3 -SCR l. Wstęp Największy problem
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012 Wojciech Kamela 1 Stanisław Kruczyński 2 PORÓWNANIE WŁAŚCIWOŚCI KATALITYCZNYCH TLENKOWYCH I PLATYNOWYCH REAKTORÓW SYSTEMU NH 3 -SCR l. Wstęp Największy problem
Materiały pomocnicze do laboratorium z przedmiotu Metody i Narzędzia Symulacji Komputerowej
 Materiały pomocnicze do laboratorium z przedmiotu Metody i Narzędzia Symulacji Komputerowej w Systemach Technicznych Symulacja prosta dyszy pomiarowej Bendemanna Opracował: dr inż. Andrzej J. Zmysłowski
Materiały pomocnicze do laboratorium z przedmiotu Metody i Narzędzia Symulacji Komputerowej w Systemach Technicznych Symulacja prosta dyszy pomiarowej Bendemanna Opracował: dr inż. Andrzej J. Zmysłowski
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012
 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012 Wojciech Kamela 1, Stanisław Kruczyński 2, Piotr Orliński 3, Marcin K. Wojs 4 OCENA WPŁYWU ŁADUNKU PLATYNY NA REDUKCJĘ NO X W REAKTORZE Pt/Al 2 O 3 l. Wstęp
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012 Wojciech Kamela 1, Stanisław Kruczyński 2, Piotr Orliński 3, Marcin K. Wojs 4 OCENA WPŁYWU ŁADUNKU PLATYNY NA REDUKCJĘ NO X W REAKTORZE Pt/Al 2 O 3 l. Wstęp
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA
 SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych
 Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych 1. Równanie kinetyczne, szybkość reakcji, rząd i cząsteczkowość reakcji. Zmiana szybkości reakcji na skutek zmiany
Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych 1. Równanie kinetyczne, szybkość reakcji, rząd i cząsteczkowość reakcji. Zmiana szybkości reakcji na skutek zmiany
Odwracalność przemiany chemicznej
 Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym
 1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych
 Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych I. Reakcje egzoenergetyczne i endoenergetyczne 1. Układ i otoczenie Układ - ogół substancji
Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych I. Reakcje egzoenergetyczne i endoenergetyczne 1. Układ i otoczenie Układ - ogół substancji
PRZEPISY PUBLIKACJA NR 98/P
 PRZEPISY PUBLIKACJA NR 98/P WYTYCZNE DOTYCZĄCE WYMAGAŃ DLA OKRĘTOWYCH SILNIKÓW WYSOKOPRĘŻNYCH WYPOSAŻONYCH W SYSTEM OCZYSZCZANIA GAZÓW SPALINOWYCH Z NO X ZA POMOCĄ SELEKTYWNEJ REDUKCJI KATALITYCZNEJ (SCR)
PRZEPISY PUBLIKACJA NR 98/P WYTYCZNE DOTYCZĄCE WYMAGAŃ DLA OKRĘTOWYCH SILNIKÓW WYSOKOPRĘŻNYCH WYPOSAŻONYCH W SYSTEM OCZYSZCZANIA GAZÓW SPALINOWYCH Z NO X ZA POMOCĄ SELEKTYWNEJ REDUKCJI KATALITYCZNEJ (SCR)
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 2(88)/2012
 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 2(88)/2012 Stanisław W. Kruczyński 1, Janusz Januła 2, Maciej Kintop 3 OBLICZENIA SYMULACYJNE POWSTAWANIA NO X i CO PRZY SPALANIU OLEJU NAPĘDOWEGO I OLEJU RZEPAKOWEGO
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 2(88)/2012 Stanisław W. Kruczyński 1, Janusz Januła 2, Maciej Kintop 3 OBLICZENIA SYMULACYJNE POWSTAWANIA NO X i CO PRZY SPALANIU OLEJU NAPĘDOWEGO I OLEJU RZEPAKOWEGO
Mgr inż. Marta DROSIŃSKA Politechnika Gdańska, Wydział Oceanotechniki i Okrętownictwa
 MECHANIK 7/2014 Mgr inż. Marta DROSIŃSKA Politechnika Gdańska, Wydział Oceanotechniki i Okrętownictwa WYZNACZENIE CHARAKTERYSTYK EKSPLOATACYJNYCH SIŁOWNI TURBINOWEJ Z REAKTOREM WYSOKOTEMPERATUROWYM W ZMIENNYCH
MECHANIK 7/2014 Mgr inż. Marta DROSIŃSKA Politechnika Gdańska, Wydział Oceanotechniki i Okrętownictwa WYZNACZENIE CHARAKTERYSTYK EKSPLOATACYJNYCH SIŁOWNI TURBINOWEJ Z REAKTOREM WYSOKOTEMPERATUROWYM W ZMIENNYCH
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(92)/2013
 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(9)/13 Wojciech Kamela 1, Stanisław W. Kruczyński BADANIA SYMULACYJNE PROCESU MAGAZYNOWANIA NO X W REAKTORZE LNT 1. Wstęp Jednym z najistotniejszych w obecnych czasach
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(9)/13 Wojciech Kamela 1, Stanisław W. Kruczyński BADANIA SYMULACYJNE PROCESU MAGAZYNOWANIA NO X W REAKTORZE LNT 1. Wstęp Jednym z najistotniejszych w obecnych czasach
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
Ocena wpływu dawki amoniaku na poziom konwersji NO X w platynowym reaktorze SCR
 KAMELA Wojciech 1 KRUCZYŃSKI Stanisław 2 Ocena wpływu dawki amoniaku na poziom konwersji NO X w platynowym reaktorze SCR Silniki spalinowe, reaktory katalityczne, redukcja selektywna, tlenki azotu, zanieczyszczenie
KAMELA Wojciech 1 KRUCZYŃSKI Stanisław 2 Ocena wpływu dawki amoniaku na poziom konwersji NO X w platynowym reaktorze SCR Silniki spalinowe, reaktory katalityczne, redukcja selektywna, tlenki azotu, zanieczyszczenie
Koncepcja systemu redukcji tlenków azotu z ognioszczelnego napędu spalinowego
 dr inż. Krzysztof KACZMARCZYK Instytut Techniki Górniczej KOMAG Koncepcja systemu redukcji tlenków azotu z ognioszczelnego napędu spalinowego S t r e s z c z e n i e W artykule omówiono koncepcję systemu
dr inż. Krzysztof KACZMARCZYK Instytut Techniki Górniczej KOMAG Koncepcja systemu redukcji tlenków azotu z ognioszczelnego napędu spalinowego S t r e s z c z e n i e W artykule omówiono koncepcję systemu
4. ODAZOTOWANIE SPALIN
 4. DAZTWANIE SPALIN 4.1. Pochodzenie tlenków azotu w spalinach 4.2. Metody ograniczenia emisji tlenków azotu systematyka metod 4.3. Techniki ograniczania emisji tlenków azotu 4.4. Analiza porównawcza 1
4. DAZTWANIE SPALIN 4.1. Pochodzenie tlenków azotu w spalinach 4.2. Metody ograniczenia emisji tlenków azotu systematyka metod 4.3. Techniki ograniczania emisji tlenków azotu 4.4. Analiza porównawcza 1
Ocena moŝliwości redukcji NO X amoniakiem na reaktorach platynowych
 KAMELA Wojciech 1 KRUCZYŃSKI Stanisław 2 Ocena moŝliwości redukcji NO X amoniakiem na reaktorach platynowych Silniki spalinowe, reaktory katalityczne, redukcja selektywna, tlenki azotu, zanieczyszczenie
KAMELA Wojciech 1 KRUCZYŃSKI Stanisław 2 Ocena moŝliwości redukcji NO X amoniakiem na reaktorach platynowych Silniki spalinowe, reaktory katalityczne, redukcja selektywna, tlenki azotu, zanieczyszczenie
X / \ Y Y Y Z / \ W W ... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Mgr inŝ. Wojciech Kamela Mgr inŝ. Marcin Wojs
 Profesorowie Pracownicy Zakładu adu Silników w Spalinowych prof. dr hab. inŝ. Stanisław W. Kruczyński(kierownik Zakładu) prof. dr hab. inŝ. Zdzisław Chłopek Docenci Doc. dr inŝ. Maciej Tułodziecki Adiunkci
Profesorowie Pracownicy Zakładu adu Silników w Spalinowych prof. dr hab. inŝ. Stanisław W. Kruczyński(kierownik Zakładu) prof. dr hab. inŝ. Zdzisław Chłopek Docenci Doc. dr inŝ. Maciej Tułodziecki Adiunkci
Właściwy silnik do każdego zastosowania. 16936_BlueEfficiencyPower_Polnisch_Schrift_in_Pfade.indd 1 13.02.2013 10:55:33
 Właściwy silnik do każdego zastosowania 16936_BlueEfficiencyPower_Polnisch_Schrift_in_Pfade.indd 1 13.02.2013 10:55:33 16936_BlueEfficiencyPower_Polnisch_Schrift_in_Pfade.indd 2 13.02.2013 10:55:38 16936_BlueEfficiencyPower_Polnisch_Schrift_in_Pfade.indd
Właściwy silnik do każdego zastosowania 16936_BlueEfficiencyPower_Polnisch_Schrift_in_Pfade.indd 1 13.02.2013 10:55:33 16936_BlueEfficiencyPower_Polnisch_Schrift_in_Pfade.indd 2 13.02.2013 10:55:38 16936_BlueEfficiencyPower_Polnisch_Schrift_in_Pfade.indd
Problemy z silnikami spowodowane zaklejonymi wtryskiwaczami Wprowadzenie dodatku do paliwa DEUTZ Clean-Diesel InSyPro.
 0199-99-1210/2 Problemy z silnikami spowodowane zaklejonymi wtryskiwaczami Wprowadzenie dodatku do paliwa DEUTZ Clean-Diesel InSyPro. Na podstawie wytycznych UE oraz wielu innych międzynarodowych przepisów,
0199-99-1210/2 Problemy z silnikami spowodowane zaklejonymi wtryskiwaczami Wprowadzenie dodatku do paliwa DEUTZ Clean-Diesel InSyPro. Na podstawie wytycznych UE oraz wielu innych międzynarodowych przepisów,
Nowoczesne narzędzia obliczeniowe do projektowania i optymalizacji kotłów
 Nowoczesne narzędzia obliczeniowe do projektowania i optymalizacji kotłów Mateusz Szubel, Mariusz Filipowicz Akademia Górniczo-Hutnicza im. Stanisława Staszica w Krakowie AGH University of Science and
Nowoczesne narzędzia obliczeniowe do projektowania i optymalizacji kotłów Mateusz Szubel, Mariusz Filipowicz Akademia Górniczo-Hutnicza im. Stanisława Staszica w Krakowie AGH University of Science and
Wpływ motoryzacji na jakość powietrza
 Instytut Pojazdów Samochodowych i Silników Spalinowych Marek Brzeżański Wpływ motoryzacji na jakość powietrza Spotkanie Grupy Roboczej ds. Ochrony Powietrza i Energetyki Urząd Marszałkowski Województwa
Instytut Pojazdów Samochodowych i Silników Spalinowych Marek Brzeżański Wpływ motoryzacji na jakość powietrza Spotkanie Grupy Roboczej ds. Ochrony Powietrza i Energetyki Urząd Marszałkowski Województwa
c. Oblicz wydajność reakcji rozkładu 200 g nitrogliceryny, jeśli otrzymano w niej 6,55 g tlenu.
 Zadanie 1. Nitrogliceryna (C 3H 5N 3O 9) jest środkiem wybuchowym. Jej rozkład można opisać następującym schematem: 4 C 3 H 5 N 3 O 9 (c) 6 N 2 (g) + 12 CO 2 (g) + 10 H 2 O (g) + 1 O 2 (g) H rozkładu =
Zadanie 1. Nitrogliceryna (C 3H 5N 3O 9) jest środkiem wybuchowym. Jej rozkład można opisać następującym schematem: 4 C 3 H 5 N 3 O 9 (c) 6 N 2 (g) + 12 CO 2 (g) + 10 H 2 O (g) + 1 O 2 (g) H rozkładu =
Wykład z Chemii Ogólnej i Nieorganicznej
 Wykład z Chemii Ogólnej i Nieorganicznej Część 5 ELEMENTY STATYKI CHEMICZNEJ Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika w Toruniu Prof. dr hab. n.chem.
Wykład z Chemii Ogólnej i Nieorganicznej Część 5 ELEMENTY STATYKI CHEMICZNEJ Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika w Toruniu Prof. dr hab. n.chem.
Inżynieria procesów przetwórstwa węgla, zima 15/16
 Inżynieria procesów przetwórstwa węgla, zima 15/16 Ćwiczenia 1 7.10.2015 1. Załóżmy, że balon ma kształt sfery o promieniu 3m. a. Jaka ilość wodoru potrzebna jest do jego wypełnienia, aby na poziomie morza
Inżynieria procesów przetwórstwa węgla, zima 15/16 Ćwiczenia 1 7.10.2015 1. Załóżmy, że balon ma kształt sfery o promieniu 3m. a. Jaka ilość wodoru potrzebna jest do jego wypełnienia, aby na poziomie morza
EKOLOGIA I OCHRONA ŚRODOWISKA W TRANSPORCIE LABORATORIUM Ćwiczenie 5. Temat: Ocena skuteczności działania katalitycznego układu oczyszczania spalin.
 EKOLOGIA I OCHRONA ŚRODOWISKA W TRANSPORCIE LABORATORIUM Ćwiczenie 5 Temat: Ocena skuteczności działania katalitycznego układu oczyszczania spalin. 1. Cel ćwiczenia Celem ćwiczenia jest ocena skuteczności
EKOLOGIA I OCHRONA ŚRODOWISKA W TRANSPORCIE LABORATORIUM Ćwiczenie 5 Temat: Ocena skuteczności działania katalitycznego układu oczyszczania spalin. 1. Cel ćwiczenia Celem ćwiczenia jest ocena skuteczności
OBLICZENIA SILNIKA TURBINOWEGO ODRZUTOWEGO (rzeczywistego) PRACA W WARUNKACH STATYCZNYCH. Opracował. Dr inż. Robert Jakubowski
 OBLICZENIA SILNIKA TURBINOWEGO ODRZUTOWEGO (rzeczywistego) PRACA W WARUNKACH STATYCZNYCH DANE WEJŚCIOWE : Opracował Dr inż. Robert Jakubowski Parametry otoczenia p H, T H Spręż sprężarki, Temperatura gazów
OBLICZENIA SILNIKA TURBINOWEGO ODRZUTOWEGO (rzeczywistego) PRACA W WARUNKACH STATYCZNYCH DANE WEJŚCIOWE : Opracował Dr inż. Robert Jakubowski Parametry otoczenia p H, T H Spręż sprężarki, Temperatura gazów
Sonochemia. Schemat 1. Strefy reakcji. Rodzaje efektów sonochemicznych. Oscylujący pęcherzyk gazu. Woda w stanie nadkrytycznym?
 Schemat 1 Strefy reakcji Rodzaje efektów sonochemicznych Oscylujący pęcherzyk gazu Woda w stanie nadkrytycznym? Roztwór Znaczne gradienty ciśnienia Duże siły hydrodynamiczne Efekty mechanochemiczne Reakcje
Schemat 1 Strefy reakcji Rodzaje efektów sonochemicznych Oscylujący pęcherzyk gazu Woda w stanie nadkrytycznym? Roztwór Znaczne gradienty ciśnienia Duże siły hydrodynamiczne Efekty mechanochemiczne Reakcje
Analiza wymiany ciepła w przekroju rury solarnej Heat Pipe w warunkach ustalonych
 Stanisław Kandefer 1, Piotr Olczak Politechnika Krakowska 2 Analiza wymiany ciepła w przekroju rury solarnej Heat Pipe w warunkach ustalonych Wprowadzenie Wśród paneli słonecznych stosowane są często rurowe
Stanisław Kandefer 1, Piotr Olczak Politechnika Krakowska 2 Analiza wymiany ciepła w przekroju rury solarnej Heat Pipe w warunkach ustalonych Wprowadzenie Wśród paneli słonecznych stosowane są często rurowe
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
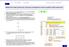 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
a. Dobierz współczynniki w powyższym schemacie tak, aby stał się równaniem reakcji chemicznej.
 Zadanie 1. Nitrogliceryna (C 3 H 5 N 3 O 9 ) jest środkiem wybuchowym. Jej rozkład można opisać następującym schematem: C 3 H 5 N 3 O 9 (c) N 2 (g) + CO 2 (g) + H 2 O (g) + O 2 (g) H rozkładu = - 385 kj/mol
Zadanie 1. Nitrogliceryna (C 3 H 5 N 3 O 9 ) jest środkiem wybuchowym. Jej rozkład można opisać następującym schematem: C 3 H 5 N 3 O 9 (c) N 2 (g) + CO 2 (g) + H 2 O (g) + O 2 (g) H rozkładu = - 385 kj/mol
Procentowa zawartość sodu (w molu tej soli są dwa mole sodu) wynosi:
 Stechiometria Każdą reakcję chemiczną można zapisać równaniem, które jest jakościową i ilościową charakterystyką tej reakcji. Określa ono bowiem, jakie pierwiastki lub związki biorą udział w danej reakcji
Stechiometria Każdą reakcję chemiczną można zapisać równaniem, które jest jakościową i ilościową charakterystyką tej reakcji. Określa ono bowiem, jakie pierwiastki lub związki biorą udział w danej reakcji
CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU.
 CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU. Projekt zrealizowany w ramach Mazowieckiego programu stypendialnego dla uczniów szczególnie uzdolnionych
CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU. Projekt zrealizowany w ramach Mazowieckiego programu stypendialnego dla uczniów szczególnie uzdolnionych
WYDZIAŁ CHEMICZNY POLITECHNIKI WARSZAWSKIEJ KATEDRA TECHNOLOGII CHEMICZNEJ. Laboratorium LABORATORIUM Z TECHNOLOGII CHEMICZNEJ
 WYDZIAŁ CHEMICZNY POLITECHNIKI WARSZAWSKIEJ KATEDRA TECHNOLOGII CHEMICZNEJ Laboratorium LABORATORIUM Z TECHNOLOGII CHEMICZNEJ Instrukcja do ćwiczenia pt. PROCES WYTWARZANIA WODORU Prowadzący: dr inż. Bogdan
WYDZIAŁ CHEMICZNY POLITECHNIKI WARSZAWSKIEJ KATEDRA TECHNOLOGII CHEMICZNEJ Laboratorium LABORATORIUM Z TECHNOLOGII CHEMICZNEJ Instrukcja do ćwiczenia pt. PROCES WYTWARZANIA WODORU Prowadzący: dr inż. Bogdan
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
DETEKCJA FAL UDERZENIOWYCH W UKŁADACH ŁOPATKOWYCH CZĘŚCI NISKOPRĘŻNYCH TURBIN PAROWYCH
 Mgr inż. Anna GRZYMKOWSKA Politechnika Gdańska Wydział Oceanotechniki i Okrętownictwa DOI: 10.17814/mechanik.2015.7.236 DETEKCJA FAL UDERZENIOWYCH W UKŁADACH ŁOPATKOWYCH CZĘŚCI NISKOPRĘŻNYCH TURBIN PAROWYCH
Mgr inż. Anna GRZYMKOWSKA Politechnika Gdańska Wydział Oceanotechniki i Okrętownictwa DOI: 10.17814/mechanik.2015.7.236 DETEKCJA FAL UDERZENIOWYCH W UKŁADACH ŁOPATKOWYCH CZĘŚCI NISKOPRĘŻNYCH TURBIN PAROWYCH
Synteza Nanoproszków Metody Chemiczne II
 Synteza Nanoproszków Metody Chemiczne II Bottom Up Metody chemiczne Wytrącanie, współstrącanie, Mikroemulsja, Metoda hydrotermalna, Metoda solwotermalna, Zol-żel, Synteza fotochemiczna, Synteza sonochemiczna,
Synteza Nanoproszków Metody Chemiczne II Bottom Up Metody chemiczne Wytrącanie, współstrącanie, Mikroemulsja, Metoda hydrotermalna, Metoda solwotermalna, Zol-żel, Synteza fotochemiczna, Synteza sonochemiczna,
ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji
 ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji w tej temperaturze wynosi K p = 0,11. Reaktor został
ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji w tej temperaturze wynosi K p = 0,11. Reaktor został
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Numeryczna symulacja rozpływu płynu w węźle
 231 Prace Instytutu Mechaniki Górotworu PAN Tom 7, nr 3-4, (2005), s. 231-236 Instytut Mechaniki Górotworu PAN Numeryczna symulacja rozpływu płynu w węźle JERZY CYGAN Instytut Mechaniki Górotworu PAN,
231 Prace Instytutu Mechaniki Górotworu PAN Tom 7, nr 3-4, (2005), s. 231-236 Instytut Mechaniki Górotworu PAN Numeryczna symulacja rozpływu płynu w węźle JERZY CYGAN Instytut Mechaniki Górotworu PAN,
PL B1. Instalacja do oczyszczania spalin silników spalinowych i sposób oczyszczania spalin silników spalinowych. WYSOCKA ANNA, Kraków, PL
 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 211235 (13) B1 (21) Numer zgłoszenia: 369701 (51) Int.Cl. B01D 53/94 (2006.01) F01N 3/035 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22)
RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 211235 (13) B1 (21) Numer zgłoszenia: 369701 (51) Int.Cl. B01D 53/94 (2006.01) F01N 3/035 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22)
Ćwiczenie 26 KATALITYCZNE ODWODNIENIE HEPTANOLU
 Ćwiczenie 26 KATALITYCZNE ODWODNIENIE HEPTANOLU Cel ćwiczenia Celem ćwiczenia jest zapoznanie z procesem heterogenicznej katalizy oraz z metodami określania parametrów kinetycznych procesu takich jak:
Ćwiczenie 26 KATALITYCZNE ODWODNIENIE HEPTANOLU Cel ćwiczenia Celem ćwiczenia jest zapoznanie z procesem heterogenicznej katalizy oraz z metodami określania parametrów kinetycznych procesu takich jak:
a) 1 mol b) 0,5 mola c) 1,7 mola d) potrzebna jest znajomość objętości zbiornika, aby można było przeprowadzić obliczenia
 1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
Informacja do zadań 1. 2. Woda morska zawiera średnio 3,5% soli.
 Informacja do zadań 1. 2. Woda morska zawiera średnio 3,5% soli. Zadanie 1. (0.1) Które zdanie jest prawdziwe? A. W 100 g wody morskiej znajduje się 3,5 g soli. B. W 103,5 g wody morskiej znajduje się
Informacja do zadań 1. 2. Woda morska zawiera średnio 3,5% soli. Zadanie 1. (0.1) Które zdanie jest prawdziwe? A. W 100 g wody morskiej znajduje się 3,5 g soli. B. W 103,5 g wody morskiej znajduje się
SELEKTYWNA REDUKCJA KATALITYCZNA TLENKÓW AZOTU W POJAZDACH SPEŁNIAJĄCYCH NORMĘ EMISJI EURO VI
 Rafał SALA, Jakub DZIDA,Jarosław KRASOWSKI SELEKTYWNA REDUKCJA KATALITYCZNA TLENKÓW AZOTU W POJAZDACH SPEŁNIAJĄCYCH NORMĘ EMISJI EURO VI W artykule omówiony został system selektywnej redukcji tlenków azotu
Rafał SALA, Jakub DZIDA,Jarosław KRASOWSKI SELEKTYWNA REDUKCJA KATALITYCZNA TLENKÓW AZOTU W POJAZDACH SPEŁNIAJĄCYCH NORMĘ EMISJI EURO VI W artykule omówiony został system selektywnej redukcji tlenków azotu
Wpływ temperatury na szybkość reakcji chemicznej.
 1 Wpływ temperatury na szybkość reakcji chemicznej. Czas trwania zajęć: 45 minut Pojęcia kluczowe: - szybkość reakcji chemicznej, - temperatura, - zderzenia cząsteczek, - energia cząsteczek. Hipoteza sformułowana
1 Wpływ temperatury na szybkość reakcji chemicznej. Czas trwania zajęć: 45 minut Pojęcia kluczowe: - szybkość reakcji chemicznej, - temperatura, - zderzenia cząsteczek, - energia cząsteczek. Hipoteza sformułowana
Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2018/19)
 Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2018/19) Uwaga! Uzyskane wyniki mogą się nieco różnić od podanych w materiałach, ze względu na uaktualnianie wartości zapisanych
Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2018/19) Uwaga! Uzyskane wyniki mogą się nieco różnić od podanych w materiałach, ze względu na uaktualnianie wartości zapisanych
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
ANALIZA ROZKŁADU CIŚNIEŃ I PRĘDKOŚCI W PRZEWODZIE O ZMIENNYM PRZEKROJU
 Dr inż. Paweł PIETKIEWICZ Dr inż. Wojciech MIĄSKOWSKI Dr inż. Krzysztof NALEPA Piotr LESZCZYŃSKI Uniwersytet Warmińsko-Mazurski w Olsztynie DOI: 10.17814/mechanik.2015.7.283 ANALIZA ROZKŁADU CIŚNIEŃ I
Dr inż. Paweł PIETKIEWICZ Dr inż. Wojciech MIĄSKOWSKI Dr inż. Krzysztof NALEPA Piotr LESZCZYŃSKI Uniwersytet Warmińsko-Mazurski w Olsztynie DOI: 10.17814/mechanik.2015.7.283 ANALIZA ROZKŁADU CIŚNIEŃ I
Fascynujący świat chemii
 Opracowanie pochodzi ze strony www.materiaienergia.pisz.pl Zeskakuj telefonem kod QR i odwiedź nas w Internecie Fascynujący świat chemii Szybkość reakcji chemicznych i katalizatory Wstęp Celem prowadzenia
Opracowanie pochodzi ze strony www.materiaienergia.pisz.pl Zeskakuj telefonem kod QR i odwiedź nas w Internecie Fascynujący świat chemii Szybkość reakcji chemicznych i katalizatory Wstęp Celem prowadzenia
OPTYMALIZACJA STEROWANIA MIKROKLIMATEM W PIECZARKARNI
 Inżynieria Rolnicza 6(131)/2011 OPTYMALIZACJA STEROWANIA MIKROKLIMATEM W PIECZARKARNI Leonard Woroncow, Ewa Wachowicz Katedra Automatyki, Politechnika Koszalińska Streszczenie. W pracy przedstawiono wyniki
Inżynieria Rolnicza 6(131)/2011 OPTYMALIZACJA STEROWANIA MIKROKLIMATEM W PIECZARKARNI Leonard Woroncow, Ewa Wachowicz Katedra Automatyki, Politechnika Koszalińska Streszczenie. W pracy przedstawiono wyniki
Za poprawną metodę Za poprawne obliczenia wraz z podaniem zmiany ph
 Zadanie 1 ( pkt.) Zmieszano 80 cm roztworu CHCH o stężeniu 5% wag. i gęstości 1,006 g/cm oraz 70 cm roztworu CHCK o stężeniu 0,5 mol/dm. bliczyć ph powstałego roztworu. Jak zmieni się ph roztworu po wprowadzeniu
Zadanie 1 ( pkt.) Zmieszano 80 cm roztworu CHCH o stężeniu 5% wag. i gęstości 1,006 g/cm oraz 70 cm roztworu CHCK o stężeniu 0,5 mol/dm. bliczyć ph powstałego roztworu. Jak zmieni się ph roztworu po wprowadzeniu
1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru
 1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru Wzór związku chemicznego podaje jakościowy jego skład z jakich pierwiastków jest zbudowany oraz liczbę atomów poszczególnych pierwiastków
1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru Wzór związku chemicznego podaje jakościowy jego skład z jakich pierwiastków jest zbudowany oraz liczbę atomów poszczególnych pierwiastków
Krzysztof Gosiewski, Anna Pawlaczyk-Kurek
 * Krzysztof Gosiewski, Anna Pawlaczyk-Kurek Instytut Inżynierii Chemicznej PAN ul. Bałtycka 5, 44-100 Gliwice 15 lutego 2018 1 * A. Opracowanie metody modelowania sprzęgającej symulację modelem CFD z wynikami
* Krzysztof Gosiewski, Anna Pawlaczyk-Kurek Instytut Inżynierii Chemicznej PAN ul. Bałtycka 5, 44-100 Gliwice 15 lutego 2018 1 * A. Opracowanie metody modelowania sprzęgającej symulację modelem CFD z wynikami
VII Podkarpacki Konkurs Chemiczny 2014/2015
 II Podkarpacki Konkurs Chemiczny 2014/2015 ETAP I 12.11.2014 r. Godz. 10.00-12.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Który z podanych zestawów zawiera wyłącznie
II Podkarpacki Konkurs Chemiczny 2014/2015 ETAP I 12.11.2014 r. Godz. 10.00-12.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Który z podanych zestawów zawiera wyłącznie
Projekt Inżynier mechanik zawód z przyszłością współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
a) jeżeli przedstawiona reakcja jest reakcją egzotermiczną, to jej prawidłowy przebieg jest przedstawiony na wykresie za pomocą linii...
 1. Spośród podanych reakcji wybierz reakcję egzoenergetyczną: a) Redukcja tlenku miedzi (II) wodorem b) Otrzymywanie tlenu przez rozkład chloranu (V) potasu c) Otrzymywanie wapna palonego w procesie prażenia
1. Spośród podanych reakcji wybierz reakcję egzoenergetyczną: a) Redukcja tlenku miedzi (II) wodorem b) Otrzymywanie tlenu przez rozkład chloranu (V) potasu c) Otrzymywanie wapna palonego w procesie prażenia
Ćwiczenie 12 KATALITYCZNE ODWODORNIENIE HEPTANU
 Ćwiczenie 12 KATALITYCZNE ODWODORNIENIE HEPTANU Cel ćwiczenia Celem ćwiczenia jest zapoznanie z procesem heterogenicznej katalizy oraz z metodami określania parametrów procesu takich jak: stopień przemiany,
Ćwiczenie 12 KATALITYCZNE ODWODORNIENIE HEPTANU Cel ćwiczenia Celem ćwiczenia jest zapoznanie z procesem heterogenicznej katalizy oraz z metodami określania parametrów procesu takich jak: stopień przemiany,
Katalityczne spalanie jako metoda oczyszczania gazów przemysłowych Instrukcja wykonania ćwiczenia nr 18
 Katalityczne spalanie jako metoda oczyszczania gazów przemysłowych Instrukcja wykonania ćwiczenia nr 18 Celem ćwiczenia jest przedstawienie reakcji katalitycznego utleniania węglowodorów jako wysoce wydajnej
Katalityczne spalanie jako metoda oczyszczania gazów przemysłowych Instrukcja wykonania ćwiczenia nr 18 Celem ćwiczenia jest przedstawienie reakcji katalitycznego utleniania węglowodorów jako wysoce wydajnej
Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ
 Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1891374. (96) Data i numer zgłoszenia patentu europejskiego: 14.06.2006 06777335.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1891374 (96) Data i numer zgłoszenia patentu europejskiego: 14.06.06 0677733.8 (13) (1) T3 Int.Cl. F23C / (06.01) F23L 7/00
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1891374 (96) Data i numer zgłoszenia patentu europejskiego: 14.06.06 0677733.8 (13) (1) T3 Int.Cl. F23C / (06.01) F23L 7/00
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Laboratorium Inżynierii Bioreaktorów
 Laboratorium Inżynierii Bioreaktorów Ćwiczenie nr 1 Reaktor chemiczny: Wyznaczanie równania kinetycznego oraz charakterystyka reaktorów o działaniu ciągłym Cele ćwiczenia: 1 Wyznaczenie równania kinetycznego
Laboratorium Inżynierii Bioreaktorów Ćwiczenie nr 1 Reaktor chemiczny: Wyznaczanie równania kinetycznego oraz charakterystyka reaktorów o działaniu ciągłym Cele ćwiczenia: 1 Wyznaczenie równania kinetycznego
Zasada działania maszyny przepływowej.
 Zasada działania maszyny przepływowej. Przyrost ciśnienia statycznego. Rys. 1. Izotermiczny schemat wirnika maszyny przepływowej z kanałem miedzy łopatkowym. Na rys.1. pokazano schemat wirnika maszyny
Zasada działania maszyny przepływowej. Przyrost ciśnienia statycznego. Rys. 1. Izotermiczny schemat wirnika maszyny przepływowej z kanałem miedzy łopatkowym. Na rys.1. pokazano schemat wirnika maszyny
imię i nazwisko, nazwa szkoły, miejscowość Zadania I etapu Konkursu Chemicznego Trzech Wydziałów PŁ V edycja
 Zadanie 1 (2 pkt.) Zmieszano 80 cm 3 roztworu CH3COOH o stężeniu 5% wag. i gęstości 1,006 g/cm 3 oraz 70 cm 3 roztworu CH3COOK o stężeniu 0,5 mol/dm 3. Obliczyć ph powstałego roztworu. Jak zmieni się ph
Zadanie 1 (2 pkt.) Zmieszano 80 cm 3 roztworu CH3COOH o stężeniu 5% wag. i gęstości 1,006 g/cm 3 oraz 70 cm 3 roztworu CH3COOK o stężeniu 0,5 mol/dm 3. Obliczyć ph powstałego roztworu. Jak zmieni się ph
Laboratorium. Hydrostatyczne Układy Napędowe
 Laboratorium Hydrostatyczne Układy Napędowe Instrukcja do ćwiczenia nr Eksperymentalne wyznaczenie charakteru oporów w przewodach hydraulicznych opory liniowe Opracowanie: Z.Kudżma, P. Osiński J. Rutański,
Laboratorium Hydrostatyczne Układy Napędowe Instrukcja do ćwiczenia nr Eksperymentalne wyznaczenie charakteru oporów w przewodach hydraulicznych opory liniowe Opracowanie: Z.Kudżma, P. Osiński J. Rutański,
2. Podczas spalania 2 objętości pewnego gazu z 4 objętościami H 2 otrzymano 1 objętość N 2 i 4 objętości H 2O. Jaki gaz uległ spalaniu?
 1. Oblicz, ilu moli HCl należy użyć, aby poniższe związki przeprowadzić w sole: a) 0,2 mola KOH b) 3 mole NH 3 H 2O c) 0,2 mola Ca(OH) 2 d) 0,5 mola Al(OH) 3 2. Podczas spalania 2 objętości pewnego gazu
1. Oblicz, ilu moli HCl należy użyć, aby poniższe związki przeprowadzić w sole: a) 0,2 mola KOH b) 3 mole NH 3 H 2O c) 0,2 mola Ca(OH) 2 d) 0,5 mola Al(OH) 3 2. Podczas spalania 2 objętości pewnego gazu
Katalityczna redukcja tlenków azotu ze spalin biomasowych kotłów małej mocy
 Marek Kułażyński 1, Łukasz Świątek 2, Katarzyna Pstrowska 3 Politechnika Wrocławska Katalityczna redukcja tlenków azotu ze spalin biomasowych kotłów małej mocy Wstęp Spalanie paliw węglowodorowych takich
Marek Kułażyński 1, Łukasz Świątek 2, Katarzyna Pstrowska 3 Politechnika Wrocławska Katalityczna redukcja tlenków azotu ze spalin biomasowych kotłów małej mocy Wstęp Spalanie paliw węglowodorowych takich
Zadanie 2. (1 pkt) Uzupełnij tabelę, wpisując wzory sumaryczne tlenków w odpowiednie kolumny. CrO CO 2 Fe 2 O 3 BaO SO 3 NO Cu 2 O
 Test maturalny Chemia ogólna i nieorganiczna Zadanie 1. (1 pkt) Uzupełnij zdania. Pierwiastek chemiczny o liczbie atomowej 16 znajduje się w.... grupie i. okresie układu okresowego pierwiastków chemicznych,
Test maturalny Chemia ogólna i nieorganiczna Zadanie 1. (1 pkt) Uzupełnij zdania. Pierwiastek chemiczny o liczbie atomowej 16 znajduje się w.... grupie i. okresie układu okresowego pierwiastków chemicznych,
Laboratorium Niskoemisyjnych Silników Spalinowych. Ćwiczenie 5. Badania symulacyjne reaktora katalitycznego
 Laboratorium Niskoemisyjnych Silników Spalinowych Ćwiczenie 5 Badania symulacyjne reaktora katalitycznego Opracowanie: Marcin K. Wojs Warszawa 2013 1. Wstęp Tematem ćwiczenia jest symulacja reaktora katalitycznego
Laboratorium Niskoemisyjnych Silników Spalinowych Ćwiczenie 5 Badania symulacyjne reaktora katalitycznego Opracowanie: Marcin K. Wojs Warszawa 2013 1. Wstęp Tematem ćwiczenia jest symulacja reaktora katalitycznego
relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
 1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
ANALIZA ROZKŁADU POLA MAGNETYCZNEGO W KADŁUBIE OKRĘTU Z CEWKAMI UKŁADU DEMAGNETYZACYJNEGO
 POZNAN UNIVE RSITY OF TE CHNOLOGY ACADE MIC JOURNALS No 81 Electrical Engineering 2015 Mirosław WOŁOSZYN* Kazimierz JAKUBIUK* Mateusz FLIS* ANALIZA ROZKŁADU POLA MAGNETYCZNEGO W KADŁUBIE OKRĘTU Z CEWKAMI
POZNAN UNIVE RSITY OF TE CHNOLOGY ACADE MIC JOURNALS No 81 Electrical Engineering 2015 Mirosław WOŁOSZYN* Kazimierz JAKUBIUK* Mateusz FLIS* ANALIZA ROZKŁADU POLA MAGNETYCZNEGO W KADŁUBIE OKRĘTU Z CEWKAMI
Podstawowe prawa opisujące właściwości gazów zostały wyprowadzone dla gazu modelowego, nazywanego gazem doskonałym (idealnym).
 Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Pakiet cetanowo-detergentowy do uszlachetniania olejów napędowych przyjaznych środowisku
 ENERGOCET 76 WPROWADZENIE Energocet 76 jest wielofunkcyjnym dodatkiem do paliwa Diesel stosowanym w celu ulepszenia wydajności paliwa i poprawienia dynamiki pojazdów. Dodatek ten spełnia następujące wymagania:
ENERGOCET 76 WPROWADZENIE Energocet 76 jest wielofunkcyjnym dodatkiem do paliwa Diesel stosowanym w celu ulepszenia wydajności paliwa i poprawienia dynamiki pojazdów. Dodatek ten spełnia następujące wymagania:
Wpływ dodatku biowęgla na emisje w procesie kompostowania odpadów organicznych
 BIOWĘGIEL W POLSCE: nauka, technologia, biznes 2016 Serock, 30-31 maja 2016 Wpływ dodatku biowęgla na emisje w procesie kompostowania odpadów organicznych dr hab. inż. Jacek Dach, prof. nadzw.* dr inż.
BIOWĘGIEL W POLSCE: nauka, technologia, biznes 2016 Serock, 30-31 maja 2016 Wpływ dodatku biowęgla na emisje w procesie kompostowania odpadów organicznych dr hab. inż. Jacek Dach, prof. nadzw.* dr inż.
Laboratorium Diagnostyki Pokładowej Pojazdów. Badania symulacyjne reaktora katalitycznego. Opracowanie: Marcin K. Wojs
 Laboratorium Diagnostyki Pokładowej Pojazdów Badania symulacyjne reaktora katalitycznego Opracowanie: Marcin K. Wojs Warszawa 2013 1. Wstęp Tematem ćwiczenia jest symulacja reaktora katalitycznego reprezentowanego
Laboratorium Diagnostyki Pokładowej Pojazdów Badania symulacyjne reaktora katalitycznego Opracowanie: Marcin K. Wojs Warszawa 2013 1. Wstęp Tematem ćwiczenia jest symulacja reaktora katalitycznego reprezentowanego
Opracował: Marcin Bąk
 PROEKOLOGICZNE TECHNIKI SPALANIA PALIW W ASPEKCIE OCHRONY POWIETRZA ATMOSFERYCZNEGO Opracował: Marcin Bąk Spalanie paliw... Przy produkcji energii elektrycznej oraz wtransporcie do atmosfery uwalnia się
PROEKOLOGICZNE TECHNIKI SPALANIA PALIW W ASPEKCIE OCHRONY POWIETRZA ATMOSFERYCZNEGO Opracował: Marcin Bąk Spalanie paliw... Przy produkcji energii elektrycznej oraz wtransporcie do atmosfery uwalnia się
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe
 kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe Zadanie
kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe Zadanie
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012
 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012 Władysław Mitianiec 1 WPŁYW BEZPOŚREDNIEGO WTRYSKU PALIWA NA EMISJĘ SPALIN W DWUSUWOWYM SILNIKU SPALINOWYM ZI 1. Wprowadzenie W małej motoryzacji oraz w gospodarce
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 1(87)/2012 Władysław Mitianiec 1 WPŁYW BEZPOŚREDNIEGO WTRYSKU PALIWA NA EMISJĘ SPALIN W DWUSUWOWYM SILNIKU SPALINOWYM ZI 1. Wprowadzenie W małej motoryzacji oraz w gospodarce
TYPY REAKCJI CHEMICZNYCH
 CHEMIA SPALANIA TYPY REAKCJI CHEMICZNYCH Jednocząsteczkowe (I rzędu): A C+D (np. C 2 H 6 CH 3 + CH 3 ) Dwucząsteczkowe (II- rzędu) (np. H + O 2 OH + O) A + B C + D Trójcząsteczkowe (III rzędu) A + B +
CHEMIA SPALANIA TYPY REAKCJI CHEMICZNYCH Jednocząsteczkowe (I rzędu): A C+D (np. C 2 H 6 CH 3 + CH 3 ) Dwucząsteczkowe (II- rzędu) (np. H + O 2 OH + O) A + B C + D Trójcząsteczkowe (III rzędu) A + B +
Laboratorium Inżynierii Bioreaktorów
 Laboratorium Inżynierii Bioreaktorów Ćwiczenie nr 3 Reaktor chemiczny: Wyznaczanie równania kinetycznego oraz charakterystyka reaktorów o działaniu ciągłym (kaskada reaktorów) Cele ćwiczenia: 1 Wyznaczenie
Laboratorium Inżynierii Bioreaktorów Ćwiczenie nr 3 Reaktor chemiczny: Wyznaczanie równania kinetycznego oraz charakterystyka reaktorów o działaniu ciągłym (kaskada reaktorów) Cele ćwiczenia: 1 Wyznaczenie
DYREKTYWA KOMISJI / /UE. z dnia XXX r.
 KOMISJA EUROPEJSKA Bruksela, dnia XXX [ ](2013) XXX draft DYREKTYWA KOMISJI / /UE z dnia XXX r. zmieniająca załączniki I, II i III do dyrektywy 2003/37/WE Parlamentu Europejskiego i Rady w sprawie homologacji
KOMISJA EUROPEJSKA Bruksela, dnia XXX [ ](2013) XXX draft DYREKTYWA KOMISJI / /UE z dnia XXX r. zmieniająca załączniki I, II i III do dyrektywy 2003/37/WE Parlamentu Europejskiego i Rady w sprawie homologacji
Methods of reducing emission from HDV Euro VI engines
 Article citation info: MERKISZ J. et al. Methods of reducing emission from HDV Euro VI engines. Combustion Engines. 2015, 162(3), 480-486. ISSN 2300-9896. Jerzy MERKISZ Maciej SIEDLECKI Andrzej ZIÓŁKOWSKI
Article citation info: MERKISZ J. et al. Methods of reducing emission from HDV Euro VI engines. Combustion Engines. 2015, 162(3), 480-486. ISSN 2300-9896. Jerzy MERKISZ Maciej SIEDLECKI Andrzej ZIÓŁKOWSKI
dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K
![dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K](/thumbs/55/36391740.jpg) RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
BADANIA KINETYKI REDUKCJI TLENKÓW AZOTU WĘGLOWODORAMI NA KOKSIE AKTYWNYM MODYFIKOWANYM KOBALTEM
 Węgiel aktywny w ochronie środowiska i przemyśle (26) KRZYSZTOF JASTRZĄB, JÓZEF SZARAWARA Politechnika Śląska, Wydział Chemiczny, ul. B. Krzywoustego 6, 44- Gliwice BADANIA KINETYKI REDUKCJI TLENKÓW AZOTU
Węgiel aktywny w ochronie środowiska i przemyśle (26) KRZYSZTOF JASTRZĄB, JÓZEF SZARAWARA Politechnika Śląska, Wydział Chemiczny, ul. B. Krzywoustego 6, 44- Gliwice BADANIA KINETYKI REDUKCJI TLENKÓW AZOTU
PROBLEMY EKSPLOATACJI 201
 3-2006 PROBLEMY EKSPLOATACJI 201 Andrzej DARKOWSKI, Dominika DŁUHA, Małgorzata KSIĘŻOPOLSKA, Politechnika Warszawska BADANIA MAGAZYNOWANIA I REDUKCJI TLENKÓW AZOTU PRZY RÓŻNYCH CZASACH PODAWANIA MIESZANKI
3-2006 PROBLEMY EKSPLOATACJI 201 Andrzej DARKOWSKI, Dominika DŁUHA, Małgorzata KSIĘŻOPOLSKA, Politechnika Warszawska BADANIA MAGAZYNOWANIA I REDUKCJI TLENKÓW AZOTU PRZY RÓŻNYCH CZASACH PODAWANIA MIESZANKI
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje rejonowe
 kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje rejonowe Zadanie
kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje rejonowe Zadanie
Kongres Innowacji Polskich KRAKÓW 10.03.2015
 KRAKÓW 10.03.2015 Zrównoważona energetyka i gospodarka odpadami ZAGOSPODAROWANIE ODPADOWYCH GAZÓW POSTPROCESOWYCH Z PRZEMYSŁU CHEMICZNEGO DO CELÓW PRODUKCJI ENERGII ELEKTRYCZNEJ I CIEPŁA Marek Brzeżański
KRAKÓW 10.03.2015 Zrównoważona energetyka i gospodarka odpadami ZAGOSPODAROWANIE ODPADOWYCH GAZÓW POSTPROCESOWYCH Z PRZEMYSŁU CHEMICZNEGO DO CELÓW PRODUKCJI ENERGII ELEKTRYCZNEJ I CIEPŁA Marek Brzeżański
Przemiany termodynamiczne
 Przemiany termodynamiczne.:: Przemiana adiabatyczna ::. Przemiana adiabatyczna (Proces adiabatyczny) - proces termodynamiczny, podczas którego wyizolowany układ nie nawiązuje wymiany ciepła, lecz całość
Przemiany termodynamiczne.:: Przemiana adiabatyczna ::. Przemiana adiabatyczna (Proces adiabatyczny) - proces termodynamiczny, podczas którego wyizolowany układ nie nawiązuje wymiany ciepła, lecz całość
MODEL ODPOWIEDZI I SCHEMAT OCENIANIA ARKUSZA II
 MDEL DPWIEDZI I SEMAT ENIANIA ARKUSZA II. Zdający otrzymuje punkty tylko za całkowicie prawidłową odpowiedź.. Gdy do jednego polecenia są dwie odpowiedzi (jedna prawidłowa, druga nieprawidłowa), to zdający
MDEL DPWIEDZI I SEMAT ENIANIA ARKUSZA II. Zdający otrzymuje punkty tylko za całkowicie prawidłową odpowiedź.. Gdy do jednego polecenia są dwie odpowiedzi (jedna prawidłowa, druga nieprawidłowa), to zdający
57 Zjazd PTChem i SITPChem Częstochowa, Promotowany miedzią niklowy katalizator do uwodornienia benzenu
 57 Zjazd PTChem i SITPChem Częstochowa, 14-18.09.2014 Promotowany miedzią niklowy katalizator do uwodornienia benzenu Kamila Michalska Kazimierz Stołecki Tadeusz Borowiecki Uwodornienie benzenu do cykloheksanu
57 Zjazd PTChem i SITPChem Częstochowa, 14-18.09.2014 Promotowany miedzią niklowy katalizator do uwodornienia benzenu Kamila Michalska Kazimierz Stołecki Tadeusz Borowiecki Uwodornienie benzenu do cykloheksanu
GAZ DOSKONAŁY. Brak oddziaływań między cząsteczkami z wyjątkiem zderzeń idealnie sprężystych.
 TERMODYNAMIKA GAZ DOSKONAŁY Gaz doskonały to abstrakcyjny, matematyczny model gazu, chociaż wiele gazów (azot, tlen) w warunkach normalnych zachowuje się w przybliżeniu jak gaz doskonały. Model ten zakłada:
TERMODYNAMIKA GAZ DOSKONAŁY Gaz doskonały to abstrakcyjny, matematyczny model gazu, chociaż wiele gazów (azot, tlen) w warunkach normalnych zachowuje się w przybliżeniu jak gaz doskonały. Model ten zakłada:
WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG
 WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG Imię i nazwisko: Klasa i szkoła*: Adres e-mail: Nr telefonu: Czy uczeń jest już uczestnikiem projektu Zdolni z Pomorza - Uniwersytet
WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG Imię i nazwisko: Klasa i szkoła*: Adres e-mail: Nr telefonu: Czy uczeń jest już uczestnikiem projektu Zdolni z Pomorza - Uniwersytet
1. Określ, w którą stronę przesunie się równowaga reakcji syntezy pary wodnej z pierwiastków przy zwiększeniu objętości zbiornika reakcyjnego:
 1. Określ, w którą stronę przesunie się równowaga reakcji syntezy pary wodnej z pierwiastków przy zwiększeniu objętości zbiornika reakcyjnego: 2. Określ w którą stronę przesunie się równowaga reakcji rozkładu
1. Określ, w którą stronę przesunie się równowaga reakcji syntezy pary wodnej z pierwiastków przy zwiększeniu objętości zbiornika reakcyjnego: 2. Określ w którą stronę przesunie się równowaga reakcji rozkładu
b) Podaj liczbę moli chloru cząsteczkowego, która całkowicie przereaguje z jednym molem glinu.
 Informacja do zadań 1 i 2 Chlorek glinu otrzymuje się w reakcji glinu z chlorowodorem lub działając chlorem na glin. Związek ten tworzy kryształy, rozpuszczalne w wodzie zakwaszonej kwasem solnym. Z roztworów
Informacja do zadań 1 i 2 Chlorek glinu otrzymuje się w reakcji glinu z chlorowodorem lub działając chlorem na glin. Związek ten tworzy kryształy, rozpuszczalne w wodzie zakwaszonej kwasem solnym. Z roztworów
KATEDRA INŻYNIERII CHEMICZNEJ I PROCESOWEJ INSTRUKCJE DO ĆWICZEŃ LABORATORYJNYCH LABORATORIUM INŻYNIERII CHEMICZNEJ, PROCESOWEJ I BIOPROCESOWEJ
 KATEDRA INŻYNIERII CHEMICZNEJ I PROCESOWEJ INSTRUKCJE DO ĆWICZEŃ LABORATORYJNYCH LABORATORIUM INŻYNIERII CHEMICZNEJ, PROCESOWEJ I BIOPROCESOWEJ Absorpcja Osoba odiedzialna: Donata Konopacka - Łyskawa dańsk,
KATEDRA INŻYNIERII CHEMICZNEJ I PROCESOWEJ INSTRUKCJE DO ĆWICZEŃ LABORATORYJNYCH LABORATORIUM INŻYNIERII CHEMICZNEJ, PROCESOWEJ I BIOPROCESOWEJ Absorpcja Osoba odiedzialna: Donata Konopacka - Łyskawa dańsk,

 Pracownia Ä2'3$'
Pracownia Ä2'3$'