POUFNE. Wersja ostateczna nr 1 z dnia 5 grudnia 2013 r. Numer ośrodka. Numer pacjenta. Numer wizyty. Badane oko
|
|
|
- Filip Feliks Barański
- 9 lat temu
- Przeglądów:
Transkrypt
1 POUFNE KARTA OBSERWACJI PACJENTA Rejestr pacjentów leczonych preparatem Lucentis (ranibizumab) we wszystkich zarejestrowanych wskazaniach w Polsce (Rejestr PRIME) Wersja ostateczna nr 1 z dnia 5 grudnia 2013 r. Numer ośrodka Numer pacjenta Numer wizyty Badane oko Koordynator badania: Firma prowadząca: Nadzór nad bezpieczeństwem farmakoterapii/ Adam Hapunik Doradca Medyczny Tel adam.hapunik@novartis.com 4 MEDICINE Al. Jerozolimskie , Warszawa Tel rejestrprime@4medicine.pl NOVARTIS POLAND ul. Marynarska , Warszawa Tel dse.poland@novartis.com Osoby otrzymujące niniejsze informacje muszą być świadome, że są one ściśle poufne. Zawartych tu informacji nie wolno ujawniać, kierować do publikacji ani wykorzystywać w żadnym innym celu niż przewidziany w niniejszym dokumencie bez uzyskania uprzedniej pisemnej zgody Sponsora
2 ostateczna 1 Rejestr PRIME (WIZYTA POCZĄTKOWA) Data włączenie do rejestru (podpisania świadomej zgody przez pacjenta): Dzień Miesiąc Rok KRYTERIA WŁĄCZENIA Tak Nie 1. Czy pacjent/pacjentka ma ukończone 18 lat? 2. Czy u pacjenta/pacjentki rozpoznano jedno ze wskazań: a. wysiękowa postać AMD (wamd), b. cukrzycowy obrzęk plamki (DME), c. zakrzep żyły środkowej siatkówki (CRVO), d. zakrzep gałęzi żyły środkowej siatkówki (BRVO), e. CNV w wyniku wysokiej krótkowzroczności (PM)? 3. Czy pacjent/pacjentka otrzymał/a pierwszą iniekcję Lucentis w badanym oku w danym ośrodku? 4. Czy pacjent/pacjentka otrzymał/a pierwszą iniekcję leku Lucentis nie wcześniej niż 90 dni i nie później niż 14 dni przed włączeniem do rejestru? 5. Czy pacjent/pacjentka podpisał/a świadomą zgodę na udział w Rejestrze? Na wszystkie kryteria włączenia musi być udzielona odpowiedź TAK, aby uczestnik mógł kontynuować udział w badaniu. KRYTERIA WYŁĄCZENIA 1. Czy pacjentka jest w ciąży lub planuje zajść w ciążę w ciągu 12 najbliższych miesięcy? Tak Nie 2. Czy pacjentka karmi piersią? 3. Czy pacjent/pacjentka bierze udział lub brał udział w innym badaniu klinicznym w ciągu ostatnich 30 dni (włącznie z badaniem obserwacyjnym)? 4. Czy u pacjenta/pacjentki występują równocześnie dwa lub więcej wskazań (dotyczy obu oczu)? a. wysiękowa postać AMD (wamd), b. cukrzycowy obrzęk plamki (DME), c. zakrzep żyły środkowej siatkówki (CRVO), d. zakrzep gałęzi żyły środkowej siatkówki (BRVO), e. CNV w wyniku wysokiej krótkowzroczności (PM)? Strona 2 z Stan po przeszczepie rogówki (w badanym oku) 6. Stan po witrektomii (w badanym oku) 7. Stwierdzenie zaniku nerwu wzrokowego (w badanym oku) 8. Stan po podaniu preparatu zawierającego glikokortykoid do ciała szklistego (w badanym oku) w ciągu ostatnich 180 dni 9. Czy pacjent/pacjentka otrzymał/a inny preparat anty VEGF w ciągu 30 dni przed pierwszym podaniem leku Lucentis (dotyczy obu oczu)? Na wszystkie kryteria wyłączenia musi być udzielona odpowiedź NIE, aby uczestnik mógł kontynuować udział w badaniu.
3 ostateczna 1 DANE DEMOGRAFICZNE Inicjały pacjenta: Data urodzenia: Dzień Miesiąc Rok Płeć: mężczyzna kobieta Wzrost: cm Masa ciała: kg Wykształcenie: podstawowe średnie wyższe 3 Wykonywany zawód (proszę wpisać): Czynniki ryzyka potencjalnych rozpoznań(można zaznaczyć więcej 1. praca na świeżym powietrzu nasłonecznienie, 2. genetyczne (rodzinne występowanie), 3. palenie tytoniu, 4. jasny kolor tęczówki, 5. jedno z naczyniowych czynników ryzyka (miażdżyca, cukrzyca, nadciśnienie tętnicze) WŁĄCZENIE DO REJESTRU 1. Kiedy postawiono diagnozę? Dzień Miesiąc Rok 2. Kiedy miała miejsce pierwsza iniekcja? Dzień Miesiąc Rok 3. Ile iniekcji podano dotychczas? 4. Data drugiej iniekcji (Proszę wypełnić jeśli wykonano drugą iniekcję) Dzień Miesiąc Rok 5. Data trzeciej iniekcji (Proszę wypełnić jeśli wykonano trzecią iniekcję) Dzień Miesiąc Rok 6. Czy w okresie od pierwszej iniekcji do wpisania pacjenta do rejestru wystąpiło u niego zdarzenie niepożądane związane z podaniem leku Lucentis? (Jeżeli zaznaczono TAK, proszę odpowiedzieć na pytanie a). TAK NIE Strona 3 z 19
4 a. Czy zgłoszono zaistniałe zdarzenie niepożądane? Jeśli zaznaczono NIE proszę przesłać informację na adres mailowy: lub tel.: (+48 22) TAK NIE BADANIE PRZED PIERWSZĄ INIEKCJĄ Proszę wskazać przeprowadzone badania i ich rozpoznanie przed pierwszą iniekcją 1. Ostrość wzroku do dali przed 1 iniekcją (Snellen). (proszę wpisać wartość) 2. Ciśnienie wewnątrzgałkowe w mmhg (proszę wpisać wartość) Brak danych 1 3. AF (angiografia fluoresceinowa) 2 a) klasyczna postać CNV 3 b) ukryta postać CNV 4 c) mieszana postać CNV 5 d) PED (odwarstwienie nabłonka barwnikowego siatkówki) 6 e) PCV (polipoidalna waskulopatia naczyniówkowa) 7 f) RAP (anastomozy naczyniówkowo-siatkówkowe) 8 g) obrzęk plamki ogniskowy 9 h) obrzęk plamki torbielowaty 10 i) obrzęk plamki rozlany 11 j) wylew krwi 12 k) bliznowacenie 13 l) zanik RPE ICG (angiografia indocyjaninowa) 15 a) ukryta postać CNV OCT (optyczna koherentna tomografia) 17 a) PED (odwarstwienie nabłonka barwnikowego siatkówki) 18 b) płyn pod siatkówką sensoryczną 19 c) płyn śródsiatkówkowy 20 d) CNV (neowaskularyzacja naczyniówkowa) 21 e) zanik nabłonka barwnikowego 22 f) błona nasiatkówkowa 23 g) brak powyższych zmian 24 h) wartość grubości centralnej siatkówki w mikrometrach Strona 4 z 19
5 STOSOWANIE ANTYBIOTYKU MIEJSCOWO W LECZONYM OKU W ZWIĄZKU Z 1 INIEKCJĄ 1. Czy w związku z iniekcją stosowano antybiotyk miejscowo w leczonym oku? (jeżeli zaznaczono TAK, proszę odpowiedzieć na pytania 2-5) TAK NIE 2. przed iniekcją 3 a. Proszę podać liczbę dni b. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon 4 2. aminoglikozyd 5 3. makrolid 6 4. inny 7 3. podczas iniekcji 8 a. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon 9 2. aminoglikozyd makrolid inny kolejne dni po iniekcji 13 a. Proszę podać liczbę dni b. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon aminoglikozyd makrolid inny 17 Strona 5 z 19
6 CHOROBY TOWARZYSZĄCE I LECZENIE PRZED 1 INIEKCJĄ Proszę zaznaczyć choroby, które wystąpiły u pacjenta przed pierwszą iniekcją (można zaznaczyć więcej 1. Nadciśnienie tętnicze 1 2. Choroba wieńcowa 2 3. Stan po zawale serca 3 4. Zaburzenia rytmu serca 4 5. hipercholesterolemia 5 6. Stan po udarze mózgu 6 7. Cukrzyca typ I 7 8. Cukrzyca typ II (proszę wskazać sposób leczenia) 8 a. doustne leki przeciwcukrzycowe 9 b. preparaty insulinowe 10 c. terapia skojarzona Powikłania cukrzycy 12 a. nefropatia cukrzycowa 13 b. kardiomiopatia cukrzycowa 14 c. retinopatia prosta bez makulopatii 15 d. stopa cukrzycowa 16 e. polineuropatia Nikotynizm 18 a. od kiedy? (proszę podać liczbę miesięcy) m-cy b. ile papierosów dziennie wypala pacjent? c. jeśli pacjent przestał palić to od kiedy? (proszę podać liczbę miesięcy) m-cy 11. Leki przeciwkrzepliwe 19 a. kwas acetylosalicylowy 20 b. antagoniści witaminy K 21 c. inne 22 Strona 6 z 19
7 CHOROBY OKULISTYCZNE W BADANYM OKU PRZED 1 INIEKCJĄ Proszę wskazać choroby okulistyczne, które występowały u pacjenta w badanym oku przed 1 iniekcją i nadal występują iniekcją (można zaznaczyć więcej 1. Degeneracje obwodowe siatkówki 1 2. Jaskra 2 3. Stan po operacji przeciwjaskrowej 3 4. Zaćma 4 5. Pseudosoczewkowość 5 6. Inne schorzenia oka (proszę wypisać) 6 Strona 7 z 19
8 BADANIE KONTROLNE PRZED 2 INIEKCJĄ Sekcję należy wypełnić, jeżeli przed włączeniem pacjenta do rejestru podano 2 iniekcję Proszę wskazać przeprowadzone badania kontrolne i ich rozpoznania przed 2 iniekcją 1. Ostrość wzroku do dali przed 2 iniekcją (Snellen). (proszę wpisać wartość) 2. Ciśnienie wewnątrzgałkowe w mmhg (proszę wpisać wartość) Brak danych 1 3. AF (angiografia fluoresceinowa) 2 a) klasyczna postać CNV 3 b) ukryta postać CNV 4 c) mieszana postać CNV 5 d) PED (odwarstwienie nabłonka barwnikowego siatkówki) 6 e) PCV (polipoidalna waskulopatia naczyniówkowa) 7 f) RAP (anastomozy naczyniówkowo-siatkówkowe) 8 g) obrzęk plamki ogniskowy 9 h) obrzęk plamki torbielowaty 10 i) obrzęk plamki rozlany 11 j) wylew krwi 12 k) bliznowacenie 13 l) zanik RPE ICG (angiografia indocyjaninowa) 15 a) ukryta postać CNV OCT (optyczna koherentna tomografia) 17 a) PED (odwarstwienie nabłonka barwnikowego siatkówki) 18 b) płyn pod siatkówką sensoryczną 19 c) płyn śródsiatkówkowy 20 d) CNV (neowaskularyzacja naczyniówkowa) 21 e) zanik nabłonka barwnikowego 22 f) błona nasiatkówkowa 23 g) brak powyższych zmian 24 h) wartość grubości centralnej siatkówki w mikrometrach Strona 8 z 19
9 STOSOWANIE ANTYBIOTYKU MIEJSCOWO W LECZONYM OKU W ZWIĄZKU Z 2 INIEKCJĄ Sekcję należy wypełnić, jeżeli przed włączeniem pacjenta do rejestru podano 2 iniekcję 1. Czy w związku z iniekcją stosowano antybiotyk miejscowo w leczonym oku? (jeżeli zaznaczono TAK, proszę odpowiedzieć na pytania 2-5) TAK NIE 2. przed iniekcją 3 a. Proszę podać liczbę dni b. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon 4 2. aminoglikozyd 5 3. makrolid 6 4. inny 7 3. podczas iniekcji 8 a. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon 9 2. aminoglikozyd makrolid inny kolejne dni po iniekcji 13 a. Proszę podać liczbę dni b. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon aminoglikozyd makrolid inny 17 Strona 9 z 19
10 CHOROBY TOWARZYSZĄCE I LECZENIE PRZED 2 INIEKCJĄ Sekcję należy wypełnić, jeżeli przed włączeniem pacjenta do rejestru podano 2 iniekcję Proszę zaznaczyć choroby, które wystąpiły u pacjenta przed 2 iniekcją (można zaznaczyć więcej 1. Nadciśnienie tętnicze 1 2. Choroba wieńcowa 2 3. Stan po zawale serca 3 4. Zaburzenia rytmu serca 4 5. hipercholesterolemia 5 6. Stan po udarze mózgu 6 7. Cukrzyca typ I 7 8. Cukrzyca typ II (proszę wskazać sposób leczenia) 8 a. doustne leki przeciwcukrzycowe 9 b. preparaty insulinowe 10 c. terapia skojarzona Powikłania cukrzycy 12 a. nefropatia cukrzycowa 13 b. kardiomiopatia cukrzycowa 14 c. retinopatia prosta bez makulopatii 15 d. stopa cukrzycowa 16 e. polineuropatia Nikotynizm 18 a. od kiedy? (proszę podać liczbę miesięcy) m-cy b. ile papierosów dziennie wypala pacjent? c. jeśli pacjent przestał palić to od kiedy? (proszę podać liczbę miesięcy) m-cy 11. Leki przeciwkrzepliwe 19 a. kwas acetylosalicylowy 20 b. antagoniści witaminy K 21 c. inne 22 Strona 10 z 19
11 CHOROBY OKULISTYCZNE W BADANYM OKU PRZED 2 INIEKCJĄ Sekcję należy wypełnić, jeżeli przed włączeniem pacjenta do rejestru podano 2 iniekcję Proszę wskazać choroby okulistyczne, które występowały u pacjenta w badanym oku przed 2 iniekcją i nadal występują iniekcją (można zaznaczyć więcej 1. Degeneracje obwodowe siatkówki 1 2. Jaskra 2 3. Stan po operacji przeciwjaskrowej 3 4. Zaćma 4 5. Pseudosoczewkowość 5 6. Inne schorzenia oka (proszę wypisać) 6 Strona 11 z 19
12 BADANIE PRZED 3 INIEKCJĄ Sekcję należy wypełnić, jeżeli przed włączeniem pacjenta do rejestru podano 3 iniekcję Proszę wskazać przeprowadzone badania i ich rozpoznanie przed 3 iniekcją 1. Ostrość wzroku do dali przed 3 iniekcją (Snellen). (proszę wpisać wartość) 2. Ciśnienie wewnątrzgałkowe w mmhg (proszę wpisać wartość) Brak danych 1 3. AF (angiografia fluoresceinowa) 2 a) klasyczna postać CNV 3 b) ukryta postać CNV 4 c) mieszana postać CNV 5 d) PED (odwarstwienie nabłonka barwnikowego siatkówki) 6 e) PCV (polipoidalna waskulopatia naczyniówkowa) 7 f) RAP (anastomozy naczyniówkowo-siatkówkowe) 8 g) obrzęk plamki ogniskowy 9 h) obrzęk plamki torbielowaty 10 i) obrzęk plamki rozlany 11 j) wylew krwi 12 k) bliznowacenie 13 l) zanik RPE ICG (angiografia indocyjaninowa) 15 a) ukryta postać CNV OCT (optyczna koherentna tomografia) 17 a) PED (odwarstwienie nabłonka barwnikowego siatkówki) 18 b) płyn pod siatkówką sensoryczną 19 c) płyn śródsiatkówkowy 20 d) CNV (neowaskularyzacja naczyniówkowa) 21 e) zanik nabłonka barwnikowego 22 f) błona nasiatkówkowa 23 g) brak powyższych zmian 24 h) wartość grubości centralnej siatkówki w mikrometrach Strona 12 z 19
13 STOSOWANIE ANTYBIOTYKU MIEJSCOWO W LECZONYM OKU W ZWIĄZKU Z 3 INIEKCJĄ Sekcję należy wypełnić, jeżeli przed włączeniem pacjenta do rejestru podano 3 iniekcję 1. Czy w związku z iniekcją stosowano antybiotyk miejscowo w leczonym oku? (jeżeli zaznaczono TAK, proszę odpowiedzieć na pytania 2-5) TAK NIE 2. przed iniekcją 3 a. Proszę podać liczbę dni b. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon 4 2. aminoglikozyd 5 3. makrolid 6 4. inny 7 3. podczas iniekcji 8 a. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon 9 2. aminoglikozyd makrolid inny kolejne dni po iniekcji 13 a. Proszę podać liczbę dni b. Proszę wskazać zastosowany antybiotyk (można zaznaczyć więcej 1. chinolon aminoglikozyd makrolid inny 17 Strona 13 z 19
14 CHOROBY TOWARZYSZĄCE I LECZENIE PRZED 3 INIEKCJĄ Sekcję należy wypełnić, jeżeli przed włączeniem pacjenta do rejestru podano 3 iniekcję Proszę zaznaczyć choroby, które wystąpiły u pacjenta przed 3 iniekcją (można zaznaczyć więcej 1. Nadciśnienie tętnicze 1 2. Choroba wieńcowa 2 3. Stan po zawale serca 3 4. Zaburzenia rytmu serca 4 5. hipercholesterolemia 5 6. Stan po udarze mózgu 6 7. Cukrzyca typ I 7 8. Cukrzyca typ II (proszę wskazać sposób leczenia) 8 a. doustne leki przeciwcukrzycowe 9 b. preparaty insulinowe 10 c. terapia skojarzona Powikłania cukrzycy 12 a. nefropatia cukrzycowa 13 b. kardiomiopatia cukrzycowa 14 c. retinopatia prosta bez makulopatii 15 d. stopa cukrzycowa 16 e. polineuropatia Nikotynizm 18 a. od kiedy? (proszę podać liczbę miesięcy) m-cy b. ile papierosów dziennie wypala pacjent? c. jeśli pacjent przestał palić to od kiedy? (proszę podać liczbę miesięcy) m-cy 11. Leki przeciwkrzepliwe 19 a. kwas acetylosalicylowy 20 b. antagoniści witaminy K 21 c. inne 22 Strona 14 z 19
15 CHOROBY OKULISTYCZNE W BADANYM OKU PRZED 3 INIEKCJĄ Sekcję należy wypełnić, jeżeli przed włączeniem pacjenta do rejestru podano 3 iniekcję Proszę wskazać choroby okulistyczne, które występowały u pacjenta w badanym oku przed 3 iniekcją i nadal występują iniekcją (można zaznaczyć więcej 1. Degeneracje obwodowe siatkówki 1 2. Jaskra 2 3. Stan po operacji przeciwjaskrowej 3 4. Zaćma 4 5. Pseudosoczewkowość 5 6. Inne schorzenia oka (proszę wypisać) 6 Strona 15 z 19
16 ROZPOZNANIE Proszę zaznaczyć właściwe rozpoznanie (można zaznaczyć tylko jedną odpowiedź) 1. Neowaskularna (wysiękowa) postać AMD 1 2. Zaburzenie widzenia spowodowane cukrzycowym obrzękiem plamki (DME) 2 3. Zaburzenia widzenia spowodowane obrzękiem plamki wtórnym do niedrożności żyły środkowej siatkówki (CRVO) 4. Zaburzenia widzenia spowodowanych obrzękiem plamki wtórnym do niedrożności gałęzi żyły środkowej siatkówki (BRVO) 5. Zaburzenia widzenia spowodowane CNV w przebiegu patologicznej krótkowzroczności(pm) DOTYCHCZASOWE LECZENIE BADANEGO OKA Proszę wskazać dotychczasowe leczenie badanego oka w okresie 12 miesięcy przed pierwszą iniekcją leku Lucentis 1. PDT 1 Jeśli zaznaczono proszę podać dokładną liczbę zabiegów 2. Inne preparaty anty-vegf 2 Jeśli zaznaczono proszę podać dokładną liczbę iniekcji 3. Fotokoagulacja laserowa (w ciągu 90 dni przed pierwszą iniekcją) 3 4. Podanie preparatu zawierającego glikokortykoid do ciała szklistego (jeśli zaznaczono proszę podać nazwę substancji) 4 Strona 16 z 19
17 BEZPIECZEŃSTWO Proszę wypełnić poniższy formularz w przypadku zaistnienia zdarzenia niepożądanego 1. Ciężkość zdarzenia nieciężkie ciężkie 2. Rozpoznanie 3. Opis 4. Początek zdarzenia niepożądanego 5. Czy zdarzeni trwa nadal? Jeśli zaznaczono NIE proszę podać datę końca zdarzenia niepożądanego Dzień Miesiąc Rok TAK NIE 3 4 a. Koniec zdarzenia niepożądanego Dzień Miesiąc Rok 6. Wynik: 5 a. Całkowity powrót do zdrowia 6 Proszę podać datę Dzień Miesiąc Rok b. Powrót do zdrowia z następstwami 7 c. Stan ulega poprawie 8 d. Stan nadal występuje (bez zmian) 9 e. Stan uległ pogorszeniu Związek z lekiem a. podejrzewany b. niepodejrzewany Strona 17 z 19
18 Formularz zgłoszenia ciężkiego zdarzenia niepożądanego KRAJ: RAPORT: Wstępny Uzupełniający NUMER PACJENTA: Numer Ośrodka: Inicjały pacjenta: Badanie nieinterwencyjne Zgłoszenie Ciężkiego Zdarzenia Niepożądanego (CZN) Strona 18 z 2 I. DANE PACJENTA I OPIS ZDARZENIA NIEPOŻĄDANEGO 1. DATA URODZENIA 2. WIEK dzień miesiąc rok lata / m-ce 3. RASA 4. PŁEĆ 5. WZROST kaukaska żółta mężczyzna czarna latynoska 8. ROZPOZNANIE MEDYCZNE CZN (należy podać diagnozę, jeżeli istnieje taka możliwość) Opis zdarzenia: inna kobieta cm kg 9. KRYTERIA CIĘŻKOŚCI 6. MASA CIAŁA 7. POCZĄTEK PIERWSZYCH OBJAWÓW CZN dzień miesiąc rok NALEŻY ZAZNACZYĆ WSZYSTKIE WŁAŚCIWE POLA Zgon dzień miesiąc rok Zagrożenie życia Hospitalizacja lub jej przedłużenie Trwałe lub znaczące inwalidztwo lub upośledzenie sprawności Inne Kryteria Ciężkości: Upośledzenie płodu/uszkodzenie okołoporodowe Inne istotne medycznie zdarzenia 10. WYNIK CIĘŻKIEGO ZDARZENIA NIEPOŻĄDANEGO Dzień Miesiąc Rok Całkowity powrót do zdrowia Data: Powrót do zdrowia z następstwami Stan ulega poprawie II. Stan nadal występuje (bez zmian) Stan uległ pogorszeniu INFORMACJE NA TEMAT LEKU Zgon Badanie sekcyjne: Nie Tak 11. LEK(I) NOVARTIS: 12. DAWKOWANIE W MOMENCIE WYSTĄPIENIA CIĘŻKIEGO ZDARZENIA NIEPOŻĄDANEGO LUB PRZED JEGO WYSTĄPIENIEM (całkowita dzienna dawka lub sposób dawkowania) 13. DROGA PODANIA 14. OKRES LECZENIA (od/do) dzień miesiąc rok dzień miesiąc rok 15. WSKAZANIA DO STOSOWANIA LEKU(LEKÓW) NOVARTIS 16. INNE LEKI PRZYJMOWANE PRZEZ PACJENTA MAJĄCE ZWIĄZEK Z CIĘŻKIM ZDARZENIEM NIEPOŻĄDANYM (nie dotyczy leków stosowanych w celu leczenia Ciężkiego Zdarzenia Niepożądanego) NAZWA LEKU DAWKA OKRES LECZENIA UZASADNIENIE ZASTOSOWANIA 17. UWAGI: Jeżeli wystąpienie Ciężkiego Zdarzenia Niepożądanego nie było spowodowane stosowaniem produktu Novartis (np. wystąpiło w wyniku przyjmowania innych leków, dotychczasowej historii choroby itp.), tutaj należy podać stosowne informacje. UZUPEŁNIONY FORMULARZ PROSZĘ PRZESŁAĆ FAKSEM DO: NOVARTIS POLAND 22) / Obowiązuje od 27 maja 2013 Pani/Pana dane będą przetwarzane przez Novartis Poland Sp. z o.o. z siedzibą w Warszawie, przy ulicy Marynarskiej 15, w celu prowadzenia rejestru i raportowania działań niepożądanych zgodnie z ustawą z dnia 29 sierpnia 1997 r. o ochronie danych osobowych (t. j. Dz. U. z 2002r. Nr 101, poz. 926 ze zm.). Strona Przysługuje 18 z 19 Pani/Panu prawo do dostępu do treści swoich danych oraz ich poprawiania. Informujemy, iż podanie przedmiotowych danych jest dobrowolne.
19 BADANIE/PROTOKÓŁ: KRAJ: III. NUMER PACJENTA: Numer Ośrodka: Inicjały pacjenta: Badanie nieinterwencyjne Zgłoszenie Ciężkiego Zdarzenia Niepożądanego (CZN) Strona 2 z ISTOTNE DANE Z WYWIADU CHOROBOWEGO PACJENTA (np. współistniejące schorzenia: choroby, alergie, podobne zdarzenia) 19. PODJĘTE DZIAŁANIA (należy zaznaczyć wszystkie odpowiednie pola) Nie podjęto żadnych działań Badany lek został odstawiony na stałe ze względu na zdarzenie niepożądane Dostosowanie dawkowania / okresowe odstawienie leku badanego * Leczenie niefarmakologiczne ** Dodatkowe leczenie farmakologiczne * W polu 8 należy podać nowe dawkowanie. **W polu 8 należy opisać zastosowane leczenie. 20. WYNIKI BADAŃ / TESTÓW LABORATORYJNYCH (należy podać tylko wyniki niezbędne w celu zdiagnozowania lub opisu przebiegu Zdarzenia Niepożądanego) Badanie / Test Data Wynik Wartości prawidłowe 21. OCENA ZWIĄZKU PRZYCZYNOWO-SKUTKOWEGO Podejrzany lek Novartis: Związek z lekiem Novartis Nie podejrzewany Podejrzewany IV. 22. IMIĘ I NAZWISKO, ADRES I NUMER TELEFONU BADACZA DANE OSOBY ZGŁASZAJĄCEJ 23. DATA ZGŁOSZENIA PRZEZ BADACZA / INNĄ OSOBĘ ZGŁASZAJĄCĄ dzień miesiąc rok Podpis: V. INFORMACJA DOTYCZĄCE PODMIOTU ODPOWIEDZIALNEGO (WYPEŁNIA NOVARTIS) Signature: 24. DATA OTRZYMANIA PRZEZ PODMIOT ODPOWIEDZIALNY INFORMACJI O CZN dzień miesiąc rok 25. LOKALNY NUMER ZGŁOSZENIA 26. NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO NALEŻY WPROWADZIĆ ADRES WŁAŚCIWEGO, LOKALNEGO DZIAŁU BEZPIECZEŃSTWA LEKÓW UZUPEŁNIONY FORMULARZ PROSZĘ PRZESŁAĆ FAKSEM DO: NOVARTIS POLAND 22) / Obowiązuje od 27 maja 2013 Pani/Pana dane będą przetwarzane przez Novartis Poland Sp. z o.o. z siedzibą w Warszawie, przy ulicy Marynarskiej 15, w celu prowadzenia rejestru i raportowania działań niepożądanych zgodnie z ustawą z dnia 29 sierpnia 1997 r. o ochronie danych osobowych (t. j. Dz. U. z 2002r. Nr 101, poz. 926 ze zm.). Przysługuje Pani/Panu prawo do dostępu do treści swoich danych oraz ich poprawiania. Informujemy, iż podanie przedmiotowych danych jest dobrowolne. Strona 19 z 19
POUFNE. Wersja ostateczna nr 1 z dnia 5 grudnia 2013 r. Numer ośrodka. Numer pacjenta. Numer wizyty. Badane oko
 POUFNE KARTA OBSERWACJI PACJENTA Rejestr pacjentów leczonych preparatem Lucentis (ranibizumab) we wszystkich zarejestrowanych wskazaniach w Polsce (Rejestr PRIME) Wersja ostateczna nr 1 z dnia 5 grudnia
POUFNE KARTA OBSERWACJI PACJENTA Rejestr pacjentów leczonych preparatem Lucentis (ranibizumab) we wszystkich zarejestrowanych wskazaniach w Polsce (Rejestr PRIME) Wersja ostateczna nr 1 z dnia 5 grudnia
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
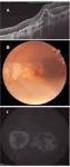 Dziennik Urzędowy Ministra Zdrowia 882 Poz. 79 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Dziennik Urzędowy Ministra Zdrowia 882 Poz. 79 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
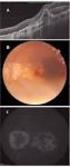 Dziennik Urzędowy Ministra Zdrowia 761 Poz. 48 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY afliberceptem
Dziennik Urzędowy Ministra Zdrowia 761 Poz. 48 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY afliberceptem
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej (wysiękowej) postaci afliberceptem
Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej (wysiękowej) postaci afliberceptem
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
 Dziennik Urzędowy Ministra Zdrowia 904 Poz. 133 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie
Dziennik Urzędowy Ministra Zdrowia 904 Poz. 133 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r.
 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r. ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r. ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Formularz pojedynczego zgłoszenia zdarzenia niepożądanego i sytuacji specjalnej (ICSR Adverse Event and Special Situation Form)
 Instrukcja: Ten formularz może być użyty do zgłaszania zdarzeń niepożądanych i/lub sytuacji specjalnych z okresu po wprowadzeniu do obrotu wliczając, ale nie ograniczając się do raportów spontanicznych
Instrukcja: Ten formularz może być użyty do zgłaszania zdarzeń niepożądanych i/lub sytuacji specjalnych z okresu po wprowadzeniu do obrotu wliczając, ale nie ograniczając się do raportów spontanicznych
data wystąpienia objawów ... Leczenie ambulatoryjne Leczenie szpitalne
 Nr: GMP-1-031/4 Tytuł: Formularz zgłoszenia działania niepożądanego Strona 1 z 5 PIERWSZE DONIESIENIE: DONIESIENIE UZUPEŁNIAJĄCE: - POUFNE - PACJENT: Inicjały Rasa urodzenia/wiek Płeć: K M Masa ciała/wzrost
Nr: GMP-1-031/4 Tytuł: Formularz zgłoszenia działania niepożądanego Strona 1 z 5 PIERWSZE DONIESIENIE: DONIESIENIE UZUPEŁNIAJĄCE: - POUFNE - PACJENT: Inicjały Rasa urodzenia/wiek Płeć: K M Masa ciała/wzrost
Czerwcowe spotkania ze specjalistami. Profilaktyka jaskry. Marek Rzendkowski Pryzmat-Okulistyka, Gliwice
 Czerwcowe spotkania ze specjalistami Profilaktyka jaskry Marek Rzendkowski Pryzmat-Okulistyka, Gliwice Gliwice, czerwiec 2018 Co robić żeby czegoś nie przeoczyć?... - Wada wzroku - okulary - Jaskra ważna
Czerwcowe spotkania ze specjalistami Profilaktyka jaskry Marek Rzendkowski Pryzmat-Okulistyka, Gliwice Gliwice, czerwiec 2018 Co robić żeby czegoś nie przeoczyć?... - Wada wzroku - okulary - Jaskra ważna
Formularz pojedynczego zgłoszenia zdarzenia niepożądanego i sytuacji specjalnej (ICSR Adverse Event and Special Situation Form)
 W przypadku badań nieinterwencyjnych (NIS), kierownicy badań postępują zgodnie z instrukcjami poniżej i usuwają tę stronę przed wysłaniem do badaczy: Zmodyfikuj następujące pole przed wysłaniem tego formularza
W przypadku badań nieinterwencyjnych (NIS), kierownicy badań postępują zgodnie z instrukcjami poniżej i usuwają tę stronę przed wysłaniem do badaczy: Zmodyfikuj następujące pole przed wysłaniem tego formularza
I. INFORMACJE O PACJENCIE II. INFORMACJE O PRODUKCIE LECZNICZYM PODEJRZEWANYM O SPOWODOWANIE DZIAŁANIA
 FORMULARZ ZGŁOSZENIA DZIAŁANIA NIEPOŻĄDANEGO DLA FACHOWEGO PRACOWNIKA SŁUŻBY ZDROWIA RAPORT: WSTĘPNY UZUPEŁNIAJĄCY I. INFORMACJE O PACJENCIE INICJAŁY PACJENTA KRAJ WYSTĄPIENIA DZIAŁANIA NIEPOŻĄDANEGO DATA
FORMULARZ ZGŁOSZENIA DZIAŁANIA NIEPOŻĄDANEGO DLA FACHOWEGO PRACOWNIKA SŁUŻBY ZDROWIA RAPORT: WSTĘPNY UZUPEŁNIAJĄCY I. INFORMACJE O PACJENCIE INICJAŁY PACJENTA KRAJ WYSTĄPIENIA DZIAŁANIA NIEPOŻĄDANEGO DATA
Formularz pojedynczego zgłoszenia zdarzenia niepożądanego i sytuacji specjalnej
 W przypadku badań nieinterwencyjnych (NIS), kierownicy badań postępują zgodnie z instrukcjami poniżej i usuwają tę stronę przed wysłaniem do badaczy: Zmodyfikuj następujące pole przed wysłaniem tego formularza
W przypadku badań nieinterwencyjnych (NIS), kierownicy badań postępują zgodnie z instrukcjami poniżej i usuwają tę stronę przed wysłaniem do badaczy: Zmodyfikuj następujące pole przed wysłaniem tego formularza
Centrum Badań Naukowych, Chirurgia Refrakcyjna "LUMED"
 Terapia anty-vegf i fotokoagulacją laserem żółtym w leczeniu CSCR w grupie młodych mężczyzn Autorzy: dr. Ludmiła Popowska, Lumed Centrum Badań Chirurgii Refrakcyjnej w Opocznie dr. Tomasz Grędysa, Europejskie
Terapia anty-vegf i fotokoagulacją laserem żółtym w leczeniu CSCR w grupie młodych mężczyzn Autorzy: dr. Ludmiła Popowska, Lumed Centrum Badań Chirurgii Refrakcyjnej w Opocznie dr. Tomasz Grędysa, Europejskie
FAX : (22) 488 37 70 PILNE
 KARTA ZAPALENIA OTRZEWNEJ Nr Przypadku Baxter: Data raportu:... Data otrzymania informacji przez Baxter:... (wypełnia Baxter) (wypełnia Baxter) Proszę wypełnić poniższe pola i odesłać faxem do: Baxter
KARTA ZAPALENIA OTRZEWNEJ Nr Przypadku Baxter: Data raportu:... Data otrzymania informacji przez Baxter:... (wypełnia Baxter) (wypełnia Baxter) Proszę wypełnić poniższe pola i odesłać faxem do: Baxter
Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/481361/2018 EMEA/H/C/002392 Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Eylea i w jakim celu się go stosuje Eylea jest lekiem
EMA/481361/2018 EMEA/H/C/002392 Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Eylea i w jakim celu się go stosuje Eylea jest lekiem
Diabetic Retinopathy Clinical Research Network
 Randomizowane badanie porównujące doszklistkowe podanie acetonidu triamcinolonu i fotokoagulacji ogniskowej lub typu grid w przypadku cukrzycowego obrzęku plamki Diabetic Retinopathy Clinical Research
Randomizowane badanie porównujące doszklistkowe podanie acetonidu triamcinolonu i fotokoagulacji ogniskowej lub typu grid w przypadku cukrzycowego obrzęku plamki Diabetic Retinopathy Clinical Research
Choroba cukrzycowa oczu
 Choroba cukrzycowa oczu W języku medycznym cukrzyca w oczach to retinopatia cukrzycowa. Zwykle takie rozpoznanie stawia okulista i kieruje pacjenta na odpowiednie leczenie. Leczeniem cukrzycy w oczach
Choroba cukrzycowa oczu W języku medycznym cukrzyca w oczach to retinopatia cukrzycowa. Zwykle takie rozpoznanie stawia okulista i kieruje pacjenta na odpowiednie leczenie. Leczeniem cukrzycy w oczach
JASKRA SIATKÓWKA. Zaćma ROGÓWKA OKULISTYKA DZIECIĘCA CHIRURGIA REFRAKCYJNA
 JASKRA SIATKÓWKA Zaćma ROGÓWKA OKULISTYKA DZIECIĘCA CHIRURGIA REFRAKCYJNA Copyright American Academy of Ophthalmology, October 2013 www.aao.org 2013 PODSUMOWANIE ZAŁOŻEŃ DLA ZALECANYCH ALGORYTMÓW POSTĘPOWANIA
JASKRA SIATKÓWKA Zaćma ROGÓWKA OKULISTYKA DZIECIĘCA CHIRURGIA REFRAKCYJNA Copyright American Academy of Ophthalmology, October 2013 www.aao.org 2013 PODSUMOWANIE ZAŁOŻEŃ DLA ZALECANYCH ALGORYTMÓW POSTĘPOWANIA
zaburzeniem widzenia spowodowanym obrzękiem plamki wywołanym cukrzycą;
 EMA/677928/2015 EMEA/H/C/002392 Streszczenie EPAR dla ogółu społeczeństwa aflibercept Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/677928/2015 EMEA/H/C/002392 Streszczenie EPAR dla ogółu społeczeństwa aflibercept Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
5. Województwo, w którym mieści się Pani/Pana główne miejsce pracy: G. mazowieckie. H. opolskie. I. podkarpackie. J. podlaskie. K.
 G. G. Page 1 D. D. D. Page 2 METRYCZKA Jeżeli Pani/Pan zatrudniona/y jest u więcej niż jednego pracodawcy proszę o udzielnie odpowiedzi w całej ankiecie zgodnie z głównym miejscem pracy (powyżej 50% czasu
G. G. Page 1 D. D. D. Page 2 METRYCZKA Jeżeli Pani/Pan zatrudniona/y jest u więcej niż jednego pracodawcy proszę o udzielnie odpowiedzi w całej ankiecie zgodnie z głównym miejscem pracy (powyżej 50% czasu
Konsensus okulistyczno-położniczy w sprawie wskazań do rozwiązania porodu drogą cięcia cesarskiego z powodu zmian w narządzie wzroku
 Konsensus okulistyczno-położniczy w sprawie wskazań do rozwiązania porodu drogą cięcia cesarskiego z powodu zmian w narządzie wzroku Wytyczne Polskiego Towarzystwa Okulistycznego 1 Konsensus okulistyczno-położniczy
Konsensus okulistyczno-położniczy w sprawie wskazań do rozwiązania porodu drogą cięcia cesarskiego z powodu zmian w narządzie wzroku Wytyczne Polskiego Towarzystwa Okulistycznego 1 Konsensus okulistyczno-położniczy
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 719 Poz. 27 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem
Dziennik Urzędowy Ministra Zdrowia 719 Poz. 27 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem
Konsensus okulistyczno-położniczy w sprawie wskazań do rozwiązania porodu drogą cięcia cesarskiego z powodu zmian w narządzie wzroku.
 Warszawa, dn. 09.02.2017 r. Konsensus okulistyczno-położniczy w sprawie wskazań do rozwiązania porodu drogą cięcia cesarskiego z powodu zmian w narządzie wzroku. Aktualizacja 9 lutego 2017 Konsensus opracowała
Warszawa, dn. 09.02.2017 r. Konsensus okulistyczno-położniczy w sprawie wskazań do rozwiązania porodu drogą cięcia cesarskiego z powodu zmian w narządzie wzroku. Aktualizacja 9 lutego 2017 Konsensus opracowała
ANEKS WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO I SKUTECZNEGO UŻYWANIA PRODUKTÓW LECZNICZYCH DO SPEŁNIENIA PRZEZ PAŃSTWA CZŁONKOWSKIE
 ANEKS WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO I SKUTECZNEGO UŻYWANIA PRODUKTÓW LECZNICZYCH DO SPEŁNIENIA PRZEZ PAŃSTWA CZŁONKOWSKIE 1/5 WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO
ANEKS WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO I SKUTECZNEGO UŻYWANIA PRODUKTÓW LECZNICZYCH DO SPEŁNIENIA PRZEZ PAŃSTWA CZŁONKOWSKIE 1/5 WARUNKI LUB OGRANICZENIA W ODNIESIENIU DO BEZPIECZNEGO
Organizacja opieki i edukacji diabetologicznej nad pacjentem z cukrzycą w lecznictwie ambulatoryjnym i stacjonarnym. Badanie ogólnopolskie.
 Organizacja opieki i edukacji diabetologicznej nad pacjentem z cukrzycą w lecznictwie ambulatoryjnym i stacjonarnym. Badanie ogólnopolskie. - 1 - Szanowna Pani, Szanowny Panie, Polska Federacja Edukacji
Organizacja opieki i edukacji diabetologicznej nad pacjentem z cukrzycą w lecznictwie ambulatoryjnym i stacjonarnym. Badanie ogólnopolskie. - 1 - Szanowna Pani, Szanowny Panie, Polska Federacja Edukacji
Wytyczne Polskiego Towarzystwa Okulistycznego
 WYTYCZNE LECZENIA OBRZĘKU PLAMKI WTÓRNEGO DO NIEDROŻNOŚCI NACZYŃ ŻYLNYCH SIATKÓWKI Wytyczne Polskiego Towarzystwa Okulistycznego Stan na dzień 10 czerwca 2014 Wytyczne zostały opracowane przez grupę ekspertów
WYTYCZNE LECZENIA OBRZĘKU PLAMKI WTÓRNEGO DO NIEDROŻNOŚCI NACZYŃ ŻYLNYCH SIATKÓWKI Wytyczne Polskiego Towarzystwa Okulistycznego Stan na dzień 10 czerwca 2014 Wytyczne zostały opracowane przez grupę ekspertów
NADCIŚNIENIE ZESPÓŁ METABOLICZNY
 NADCIŚNIENIE ZESPÓŁ METABOLICZNY Poradnik dla pacjenta i jego rodziny Konsultacja: prof. dr hab. med. Zbigniew Gaciong CO TO JEST ZESPÓŁ METABOLICZNY Nadciśnienie tętnicze (inaczej podwyższone ciśnienie
NADCIŚNIENIE ZESPÓŁ METABOLICZNY Poradnik dla pacjenta i jego rodziny Konsultacja: prof. dr hab. med. Zbigniew Gaciong CO TO JEST ZESPÓŁ METABOLICZNY Nadciśnienie tętnicze (inaczej podwyższone ciśnienie
NIEDROŻNOŚĆ ŻYŁY ŚRODKOWEJ SIATKÓWKI (CRVO)
 Przewodnik informacyjny Informacje naukowe na temat CRVO www.scienceofcrvo.org NIEDROŻNOŚĆ ŻYŁY ŚRODKOWEJ SIATKÓWKI (CRVO) W niniejszej broszurze przedstawione zostały informacje na temat CRVO oraz dostępnych
Przewodnik informacyjny Informacje naukowe na temat CRVO www.scienceofcrvo.org NIEDROŻNOŚĆ ŻYŁY ŚRODKOWEJ SIATKÓWKI (CRVO) W niniejszej broszurze przedstawione zostały informacje na temat CRVO oraz dostępnych
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 731 Poz. 66 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Dziennik Urzędowy Ministra Zdrowia 731 Poz. 66 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Badanie w ramach programu pt. Audyt społeczny leczenia w AMD w Polsce realizowanego przez Stowarzyszenie Retina AMD Polska
 Dane demograficzne: Badanie w ramach programu pt. Audyt społeczny leczenia w AMD w Polsce realizowanego przez Stowarzyszenie Retina AMD Polska Opracowanie: dr n. med. Anna Kieszkowska-Grudny 1. Inicjały
Dane demograficzne: Badanie w ramach programu pt. Audyt społeczny leczenia w AMD w Polsce realizowanego przez Stowarzyszenie Retina AMD Polska Opracowanie: dr n. med. Anna Kieszkowska-Grudny 1. Inicjały
Organizacje pozarządowe w diabetologii: realne problemy pacjentów. problem z postrzeganiem cukrzycy typu 2 POLSKIE STOWARZYSZENIE DIABETYKÓW
 POLSKIE STOWARZYSZENIE DIABETYKÓW Organizacje pozarządowe w diabetologii: realne problemy pacjentów problem z postrzeganiem cukrzycy typu 2 Małgorzata Marszałek POSTRZEGANIE CUKRZYCY TYPU 2 Łagodniejszy,
POLSKIE STOWARZYSZENIE DIABETYKÓW Organizacje pozarządowe w diabetologii: realne problemy pacjentów problem z postrzeganiem cukrzycy typu 2 Małgorzata Marszałek POSTRZEGANIE CUKRZYCY TYPU 2 Łagodniejszy,
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem A. Leczenie sildenafilem pacjentów
Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem A. Leczenie sildenafilem pacjentów
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 893 Poz. 133 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Dziennik Urzędowy Ministra Zdrowia 893 Poz. 133 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Retinopatia cukrzycowa
 Retinopatia cukrzycowa Retinopatia cukrzycowa jest w krajach rozwiniętych jedną z głównych przyczyn ślepoty. Rozwija się u znacznej liczby pacjentów długo chorujących na cukrzycę, która może być przyczyną
Retinopatia cukrzycowa Retinopatia cukrzycowa jest w krajach rozwiniętych jedną z głównych przyczyn ślepoty. Rozwija się u znacznej liczby pacjentów długo chorujących na cukrzycę, która może być przyczyną
LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2
 załącznik nr 11 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
załącznik nr 11 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
Aneks III. Zmiany w odpowiednich punktach skróconej charakterystyki produktu leczniczego i ulotce dla pacjenta.
 Aneks III Zmiany w odpowiednich punktach skróconej charakterystyki produktu leczniczego i ulotce dla pacjenta. Uwaga: Niniejsze zmiany w odpowiednich punktach skróconej charakterystyki produktu leczniczego
Aneks III Zmiany w odpowiednich punktach skróconej charakterystyki produktu leczniczego i ulotce dla pacjenta. Uwaga: Niniejsze zmiany w odpowiednich punktach skróconej charakterystyki produktu leczniczego
DEKA SMARTLIPO - LASER LIPOLISI - ADIPOCYTOLIZA LASEROWA IMIĘ I NAZWISKO PACJENTA. Osoba kontaktowa TEL. TEL. KOM.
 DEKA SMARTLIPO - LASER LIPOLISI - ADIPOCYTOLIZA LASEROWA IMIĘ I NAZWISKO PACJENTA Data urodzenia Wiek Waga kg Wzrost cm Leczony obszar.. Wymiary dotyczące obszaru- obwód.. Osoba kontaktowa Zawód ADRES
DEKA SMARTLIPO - LASER LIPOLISI - ADIPOCYTOLIZA LASEROWA IMIĘ I NAZWISKO PACJENTA Data urodzenia Wiek Waga kg Wzrost cm Leczony obszar.. Wymiary dotyczące obszaru- obwód.. Osoba kontaktowa Zawód ADRES
POLSKIE TOWARZYSTWO OKULISTYCZNE
 POLSKIE TOWARZYSTWO OKULISTYCZNE Iwona Grabska-Liberek Badania przesiewowe w kierunku jaskry ważnym elementem profilaktyki Centrum Medyczne Kształcenia Podyplomowego Klinika Okulistyki Działania PTO na
POLSKIE TOWARZYSTWO OKULISTYCZNE Iwona Grabska-Liberek Badania przesiewowe w kierunku jaskry ważnym elementem profilaktyki Centrum Medyczne Kształcenia Podyplomowego Klinika Okulistyki Działania PTO na
Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
 Załącznik nr 10 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny:
Załącznik nr 10 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny:
Różnicowanie. S. Teper, E. Wylęgała
 r8_:layout 1 2011-02-07 00:10 Strona 83 8 Różnicowanie S. Teper, E. Wylęgała Różnicowanie w większości przypadków nie stanowi kłopotu. Pewne wątpliwości mogą się pojawić w zaawansowanym CNV, gdy trudne
r8_:layout 1 2011-02-07 00:10 Strona 83 8 Różnicowanie S. Teper, E. Wylęgała Różnicowanie w większości przypadków nie stanowi kłopotu. Pewne wątpliwości mogą się pojawić w zaawansowanym CNV, gdy trudne
Podziękowania. Przedmowa do wydania polskiego Skróty. Rozdział 1. Powieki 1
 v Podziękowania Przedmowa Przedmowa do wydania polskiego Skróty xii xiii xiv xv Rozdział 1. Powieki 1 Rzęsy.................................................. 2 Przewlekłe zapalenie brzegów powiek.......................
v Podziękowania Przedmowa Przedmowa do wydania polskiego Skróty xii xiii xiv xv Rozdział 1. Powieki 1 Rzęsy.................................................. 2 Przewlekłe zapalenie brzegów powiek.......................
Załącznik nr 1 do zarządzenia Nr 53/2006 Prezesa Narodowego Funduszu Zdrowia. Program profilaktyki chorób układu krążenia
 Program profilaktyki chorób układu krążenia 1 I. UZASADNIENIE CELOWOŚCI WDROŻENIA PROGRAMU PROFILAKTYKI CHORÓB UKŁADU KRĄŻENIA, zwanego dalej Programem. 1. Opis problemu zdrowotnego. Choroby układu krążenia
Program profilaktyki chorób układu krążenia 1 I. UZASADNIENIE CELOWOŚCI WDROŻENIA PROGRAMU PROFILAKTYKI CHORÓB UKŁADU KRĄŻENIA, zwanego dalej Programem. 1. Opis problemu zdrowotnego. Choroby układu krążenia
ZAPROSZENIE NA BADANIA PROFILAKTYCZNE WYKONYWANE W RAMACH PODSTAWOWEJ OPIEKI ZDROWOTNEJ ( )
 ZAPROSZENIE NA BADANIA PROFILAKTYCZNE WYKONYWANE W RAMACH PODSTAWOWEJ OPIEKI ZDROWOTNEJ (2015-08-03) PROFILAKTYKA CHORÓB UKŁADU KRĄŻENIA ADRESACI - Osoby zadeklarowane do lekarza POZ, w wieku 35, 40, 45,
ZAPROSZENIE NA BADANIA PROFILAKTYCZNE WYKONYWANE W RAMACH PODSTAWOWEJ OPIEKI ZDROWOTNEJ (2015-08-03) PROFILAKTYKA CHORÓB UKŁADU KRĄŻENIA ADRESACI - Osoby zadeklarowane do lekarza POZ, w wieku 35, 40, 45,
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 738 Poz. 42 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Dziennik Urzędowy Ministra Zdrowia 738 Poz. 42 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Rejestr codziennej praktyki lekarskiej w zakresie leczenia choroby wieńcowej
 Rejestr codziennej praktyki lekarskiej w zakresie leczenia choroby wieńcowej Badanie Nr: BETAX_L_01459 Autorzy: Dr hab. n. med. Marek Kuch, Klinika Kardiologii, Uniwersytet Medyczny w Warszawie Michał
Rejestr codziennej praktyki lekarskiej w zakresie leczenia choroby wieńcowej Badanie Nr: BETAX_L_01459 Autorzy: Dr hab. n. med. Marek Kuch, Klinika Kardiologii, Uniwersytet Medyczny w Warszawie Michał
Karta badania profilaktycznego w Programie profilaktyki chorób układu krążenia
 Pieczątka świadczeniodawcy nr umowy z NFZ Karta badania profilaktycznego w Programie profilaktyki chorób układu krążenia Uwaga! Kartę należy wypełnić drukowanymi literami, twierdzące odpowiedzi na pytania
Pieczątka świadczeniodawcy nr umowy z NFZ Karta badania profilaktycznego w Programie profilaktyki chorób układu krążenia Uwaga! Kartę należy wypełnić drukowanymi literami, twierdzące odpowiedzi na pytania
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
Monitorowanie niepożądanych działań leków
 Monitorowanie niepożądanych działań leków Anna Wiela-Hojeńska Katedra i Zakład Farmakologii Klinicznej Uniwersytet Medyczny we Wrocławiu Niepożądane działanie leku (ndl) Adverse Drug Reaction (ADR) (definicja
Monitorowanie niepożądanych działań leków Anna Wiela-Hojeńska Katedra i Zakład Farmakologii Klinicznej Uniwersytet Medyczny we Wrocławiu Niepożądane działanie leku (ndl) Adverse Drug Reaction (ADR) (definicja
DME. Science of. UCZ SIĘ, OBSERWUJ, DZIEL SIĘ Przewodnik pacjenta Cukrzycowy obrzęk plamki
 Science of DME www.scienceofdme.org UCZ SIĘ, OBSERWUJ, DZIEL SIĘ Przewodnik pacjenta Cukrzycowy obrzęk plamki Niniejsza broszura jest przeznaczona dla każdej osoby chorującej na cukrzycę typu 1 i typu
Science of DME www.scienceofdme.org UCZ SIĘ, OBSERWUJ, DZIEL SIĘ Przewodnik pacjenta Cukrzycowy obrzęk plamki Niniejsza broszura jest przeznaczona dla każdej osoby chorującej na cukrzycę typu 1 i typu
Aneks III. Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Raport z rejestru REG-DIAB ocena wybranych aspektów leczenia chorych na cukrzycę typu 2 w warunkach codziennej praktyki lekarskiej w Polsce
 Raport z rejestru REG-DIAB ocena wybranych aspektów leczenia chorych na cukrzycę typu 2 w warunkach codziennej praktyki lekarskiej w Polsce Badanie nr: GLIME_L_00670 przeprowadzenie i opracowanie wyników
Raport z rejestru REG-DIAB ocena wybranych aspektów leczenia chorych na cukrzycę typu 2 w warunkach codziennej praktyki lekarskiej w Polsce Badanie nr: GLIME_L_00670 przeprowadzenie i opracowanie wyników
inwalidztwo rodzaj pracy
 Zdrowie jest najważniejsze Wykłady wraz z konsultacjami medycznymi realizowane przez Stowarzyszenia na rzecz rozwoju wsi Bogufałów Źródło Baryczy w ramach wspierania realizacji zadania publicznego przez
Zdrowie jest najważniejsze Wykłady wraz z konsultacjami medycznymi realizowane przez Stowarzyszenia na rzecz rozwoju wsi Bogufałów Źródło Baryczy w ramach wspierania realizacji zadania publicznego przez
Karta badania profilaktycznego w Programie profilaktyki chorób układu krążenia
 Pieczątka świadczeniodawcy nr umowy z NFZ Karta badania profilaktycznego w Programie profilaktyki chorób układu krążenia Uwaga! Kartę należy wypełnić drukowanymi literami, twierdzące odpowiedzi na pytania
Pieczątka świadczeniodawcy nr umowy z NFZ Karta badania profilaktycznego w Programie profilaktyki chorób układu krążenia Uwaga! Kartę należy wypełnić drukowanymi literami, twierdzące odpowiedzi na pytania
EDUKACJA PACJENTA I JEGO RODZINY MAJĄCA NA CELU PODNIESIENIE ŚWIADOMOŚCI NA TEMAT CUKRZYCY, DOSTARCZENIE JAK NAJWIĘKSZEJ WIEDZY NA JEJ TEMAT.
 EDUKACJA PACJENTA I JEGO RODZINY MAJĄCA NA CELU PODNIESIENIE ŚWIADOMOŚCI NA TEMAT CUKRZYCY, DOSTARCZENIE JAK NAJWIĘKSZEJ WIEDZY NA JEJ TEMAT. Prowadząca edukację: piel. Anna Otremba CELE: -Kształtowanie
EDUKACJA PACJENTA I JEGO RODZINY MAJĄCA NA CELU PODNIESIENIE ŚWIADOMOŚCI NA TEMAT CUKRZYCY, DOSTARCZENIE JAK NAJWIĘKSZEJ WIEDZY NA JEJ TEMAT. Prowadząca edukację: piel. Anna Otremba CELE: -Kształtowanie
Aneks III. Uzupełnienia odpowiednich punktów Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta
 Aneks III Uzupełnienia odpowiednich punktów Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta Uwaga: Charakterystyka Produktu Leczniczego i Ulotka dla pacjenta są wynikiem zakończenia procedury
Aneks III Uzupełnienia odpowiednich punktów Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta Uwaga: Charakterystyka Produktu Leczniczego i Ulotka dla pacjenta są wynikiem zakończenia procedury
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Materiały edukacyjne. Diagnostyka i leczenie nadciśnienia tętniczego
 Materiały edukacyjne Diagnostyka i leczenie nadciśnienia tętniczego Klasyfikacja ciśnienia tętniczego (mmhg) (wg. ESH/ESC )
Materiały edukacyjne Diagnostyka i leczenie nadciśnienia tętniczego Klasyfikacja ciśnienia tętniczego (mmhg) (wg. ESH/ESC )
Leczenie neowaskularyzacji naczyniówkowej. w patologicznej krótkowzroczności
 Leczenie neowaskularyzacji naczyniówkowej w patologicznej krótkowzroczności Wytyczne Polskiego Towarzystwa Okulistycznego Stan na dzień 10 czerwca 2014 Wytyczne zostały opracowane przez grupę ekspertów
Leczenie neowaskularyzacji naczyniówkowej w patologicznej krótkowzroczności Wytyczne Polskiego Towarzystwa Okulistycznego Stan na dzień 10 czerwca 2014 Wytyczne zostały opracowane przez grupę ekspertów
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32.a. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE
Załącznik B.32.a. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA
 ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA Poprawki do CHPL oraz ulotki dla pacjenta są ważne od momentu zatwierdzenia Decyzji Komisji. Po zatwierdzeniu Decyzji Komisji,
ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA Poprawki do CHPL oraz ulotki dla pacjenta są ważne od momentu zatwierdzenia Decyzji Komisji. Po zatwierdzeniu Decyzji Komisji,
LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0)
 Załącznik B.22. LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0) WIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii dokonuje Zespół Koordynacyjny ds. Chorób Ultrarzadkich powoływany przez Prezesa Narodowego
Załącznik B.22. LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0) WIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii dokonuje Zespół Koordynacyjny ds. Chorób Ultrarzadkich powoływany przez Prezesa Narodowego
KARTA BADANIA PROFILAKTYCZNEGO
 KARTA BADANIA PROFILAKTYCZNEGO Rodzaj badania profilaktycznego Pozostała działalność profilaktyczna Wstępne (W) Okresowe (O); Kontrolne (K) monitoring stanu zdrowia (M), badanie celowane (C), czynne poradnictwo
KARTA BADANIA PROFILAKTYCZNEGO Rodzaj badania profilaktycznego Pozostała działalność profilaktyczna Wstępne (W) Okresowe (O); Kontrolne (K) monitoring stanu zdrowia (M), badanie celowane (C), czynne poradnictwo
Spis treści. Przedmowa Badanie pacjenta z chorobami sercowo-naczyniowymi... 13
 Spis treści Przedmowa................ 11 1. Badanie pacjenta z chorobami sercowo-naczyniowymi.................. 13 Najważniejsze problemy diagnostyczne....... 13 Ból w klatce piersiowej........... 14 Ostry
Spis treści Przedmowa................ 11 1. Badanie pacjenta z chorobami sercowo-naczyniowymi.................. 13 Najważniejsze problemy diagnostyczne....... 13 Ból w klatce piersiowej........... 14 Ostry
LUCENTIS (RANIBIZUMAB) W LECZENIU CHORÓB PLAMKI
 LUCENTIS (RANIBIZUMAB) W LECZENIU CHORÓB PLAMKI Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/5 02-516 Warszawa Tel. 22 542 41 54 E-mail: biuro@mahta.pl ANALIZA KLINICZNA TOM VI PODSUMOWANIE I WNIOSKI Z ANALIZY
LUCENTIS (RANIBIZUMAB) W LECZENIU CHORÓB PLAMKI Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/5 02-516 Warszawa Tel. 22 542 41 54 E-mail: biuro@mahta.pl ANALIZA KLINICZNA TOM VI PODSUMOWANIE I WNIOSKI Z ANALIZY
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
David Levy. P raktyczna OPIEKA DIABETOLOGICZNA
 David Levy P raktyczna OPIEKA DIABETOLOGICZNA David Levy m d P raktyczna OPIEKA DIABETOLOGICZNA Redakcja naukowa tłumaczenia prof. dr hab. n. med. W ALDEM AR KARNAFEL Z języka angielskiego tłumaczyła dr
David Levy P raktyczna OPIEKA DIABETOLOGICZNA David Levy m d P raktyczna OPIEKA DIABETOLOGICZNA Redakcja naukowa tłumaczenia prof. dr hab. n. med. W ALDEM AR KARNAFEL Z języka angielskiego tłumaczyła dr
ANEKS III UZUPEŁNIENIA DO CHARAKTERYSTYKI PRODUKTU LECZNICZEGO ORAZ ULOTKI PLA PACJENTA
 ANEKS III UZUPEŁNIENIA DO CHARAKTERYSTYKI PRODUKTU LECZNICZEGO ORAZ ULOTKI PLA PACJENTA 42 UZUPEŁNIENIA ZAWARTE W ODPOWIEDNICH PUNKTACH CHARAKTERYSTYKI PRODUKTU LECZNICZEGO DLA PRODUKTÓW ZAWIERAJĄCYCH
ANEKS III UZUPEŁNIENIA DO CHARAKTERYSTYKI PRODUKTU LECZNICZEGO ORAZ ULOTKI PLA PACJENTA 42 UZUPEŁNIENIA ZAWARTE W ODPOWIEDNICH PUNKTACH CHARAKTERYSTYKI PRODUKTU LECZNICZEGO DLA PRODUKTÓW ZAWIERAJĄCYCH
6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej
 6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej 6.2.1. Podsumowanie korzyści wynikających z leczenia Co to jest T2488? T2488
6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej 6.2.1. Podsumowanie korzyści wynikających z leczenia Co to jest T2488? T2488
12 SQ-HDM Grupa farmakoterapeutyczna: Wyciągi alergenowe, kurz domowy; Kod ATC: V01AA03
 SUBSTANCJA CZYNNA (INN) GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC) PODMIOT ODPOWIEDZIALNY NAZWA HANDLOWA PRODUKTU LECZNICZEGO, KTÓREGO DOTYCZY PLAN ZARZĄDZANIA RYZYKIEM 12 SQ-HDM Grupa farmakoterapeutyczna:
SUBSTANCJA CZYNNA (INN) GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC) PODMIOT ODPOWIEDZIALNY NAZWA HANDLOWA PRODUKTU LECZNICZEGO, KTÓREGO DOTYCZY PLAN ZARZĄDZANIA RYZYKIEM 12 SQ-HDM Grupa farmakoterapeutyczna:
PROGRAM RAZEM DLA SERCA Karta Badania Profilaktycznego
 PROGRAM RAZEM DLA SERCA Karta Badania Profilaktycznego ETAP I (wypełni pielęgniarka) Imię i nazwisko:... Adres:... PESEL Wzrost:...cm Wykształcenie:... Masa ciała:...kg Zawód wykonywany:... Obwód talii:...cm
PROGRAM RAZEM DLA SERCA Karta Badania Profilaktycznego ETAP I (wypełni pielęgniarka) Imię i nazwisko:... Adres:... PESEL Wzrost:...cm Wykształcenie:... Masa ciała:...kg Zawód wykonywany:... Obwód talii:...cm
VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości
 VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Szacuje się, że wysokie ciśnienie krwi jest przyczyną
VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Szacuje się, że wysokie ciśnienie krwi jest przyczyną
Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie
 brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
Rejestr codziennej praktyki lekarskiej dotyczący cy leczenia nadciśnienia nienia tętniczego t tniczego. czynnikami ryzyka sercowo- naczyniowego
 Rejestr codziennej praktyki lekarskiej dotyczący cy leczenia nadciśnienia nienia tętniczego t tniczego współwyst występującego z innymi czynnikami ryzyka sercowo- naczyniowego Nr rejestru: HOE 498_9004
Rejestr codziennej praktyki lekarskiej dotyczący cy leczenia nadciśnienia nienia tętniczego t tniczego współwyst występującego z innymi czynnikami ryzyka sercowo- naczyniowego Nr rejestru: HOE 498_9004
LECZENIE CHOROBY GAUCHERA ICD-10 E
 załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Eylea 40 mg/ml roztwór do wstrzykiwań w ampułkostrzykawce 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera
PROGRAM ZAPOBIEGANIA CIĄŻY LISTA KONTROLNA PRZEPISYWANIA LEKU TOCTINO
 PROGRAM ZAPOBIEGANIA CIĄŻY LISTA KONTROLNA PRZEPISYWANIA LEKU TOCTINO Karta pacjenta Imię i nazwisko pacjenta Podmiot odpowiedzialny Stiefel Laboratories (Ireland) Ltd Finisklin Business Park, Sligo Irlandia
PROGRAM ZAPOBIEGANIA CIĄŻY LISTA KONTROLNA PRZEPISYWANIA LEKU TOCTINO Karta pacjenta Imię i nazwisko pacjenta Podmiot odpowiedzialny Stiefel Laboratories (Ireland) Ltd Finisklin Business Park, Sligo Irlandia
Chorujesz na cukrzycę? Zbadaj wzrok. Grozi ci retinopatia cukrzycowa.
 INFORMACJA PRASOWA Chorujesz na cukrzycę? Zbadaj wzrok. Grozi ci retinopatia cukrzycowa. Retinopatia cukrzycowa dotyka wszystkich chorych na cukrzycę typu I oraz ok. 60% pacjentów z cukrzycą typu II. To
INFORMACJA PRASOWA Chorujesz na cukrzycę? Zbadaj wzrok. Grozi ci retinopatia cukrzycowa. Retinopatia cukrzycowa dotyka wszystkich chorych na cukrzycę typu I oraz ok. 60% pacjentów z cukrzycą typu II. To
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
DiabControl RAPORT KOŃCOWY
 DiabControl OCENA WSPÓŁPRACY PACJENTA CHOREGO NA CUKRZYCĘ TYPU 2 Z LEKARZEM PROWADZĄCYM W ZAKRESIE COMPLIANCE, OBSERWACJA ZJAWISKA DYSFAGII (TRUDNOŚCI W POŁYKANIU) RAPORT KOŃCOWY Październik 214 Autor
DiabControl OCENA WSPÓŁPRACY PACJENTA CHOREGO NA CUKRZYCĘ TYPU 2 Z LEKARZEM PROWADZĄCYM W ZAKRESIE COMPLIANCE, OBSERWACJA ZJAWISKA DYSFAGII (TRUDNOŚCI W POŁYKANIU) RAPORT KOŃCOWY Październik 214 Autor
Bezpośredni komunikat do fachowych pracowników ochrony zdrowia
 Bezpośredni komunikat do fachowych pracowników ochrony zdrowia Wersja 2, data zatwierdzenia przez URPL: 07.11.2016 Strona 1/7 Acytretyna (Neotigason): poważne ryzyko działania teratogennego oraz ryzyko
Bezpośredni komunikat do fachowych pracowników ochrony zdrowia Wersja 2, data zatwierdzenia przez URPL: 07.11.2016 Strona 1/7 Acytretyna (Neotigason): poważne ryzyko działania teratogennego oraz ryzyko
PODSTAWY PRAWNE. Rozporządzenie Ministra Zdrowia z dnia 2 sierpnia 2016r. zmieniające rozporządzenie w sprawie recept lekarskich
 LEKI 75+ PODSTAWY PRAWNE Rozporządzenie Ministra Zdrowia z dnia 2 sierpnia 2016r. zmieniające rozporządzenie w sprawie recept lekarskich Resort zdrowia opublikował zmiany w wykazie leków refundowanych,
LEKI 75+ PODSTAWY PRAWNE Rozporządzenie Ministra Zdrowia z dnia 2 sierpnia 2016r. zmieniające rozporządzenie w sprawie recept lekarskich Resort zdrowia opublikował zmiany w wykazie leków refundowanych,
Jedynym obecnie znanym sposobem leczenia jaskry jest obniżanie ciśnienia wewnątrzgałkowego
 Jacek P. Szaflik Katedra i Klinika Okulistyki II Wydziału Lekarskiego Warszawskiego Uniwersytetu Medycznego Kierownik Kliniki: Prof. dr hab. n. med. Jacek P. Szaflik Jaskra jest chorobą nieuleczalną Jednak
Jacek P. Szaflik Katedra i Klinika Okulistyki II Wydziału Lekarskiego Warszawskiego Uniwersytetu Medycznego Kierownik Kliniki: Prof. dr hab. n. med. Jacek P. Szaflik Jaskra jest chorobą nieuleczalną Jednak
Hipercholesterolemia najgorzej kontrolowany czynnik ryzyka w Polsce punkt widzenia lekarza rodzinnego
 XVI Kongres Medycyny Rodzinnej Kielce, 2 5 czerwca 2016 Prof. UJ dr hab. med. Adam Windak Kierownik Zakładu Medycyny Rodzinnej CM UJ Wiceprezes Kolegium Lekarzy Rodzinnych w Polsce Hipercholesterolemia
XVI Kongres Medycyny Rodzinnej Kielce, 2 5 czerwca 2016 Prof. UJ dr hab. med. Adam Windak Kierownik Zakładu Medycyny Rodzinnej CM UJ Wiceprezes Kolegium Lekarzy Rodzinnych w Polsce Hipercholesterolemia
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
PROGRAM RAMOWY Framework programme
 CZWARTEK 6 CZERWCA / Thursday 6 th June Hotel Leonardo Royal, ul. Grzybowska 45, Warszawa Sala Mona i Lisa WALNE ZGROMADZENIE ZARZĄDU GŁÓWNEGO POLSKIEGO TOWARZYSTWA OKULISTYCZNEGO Rada Okulistów Polskich
CZWARTEK 6 CZERWCA / Thursday 6 th June Hotel Leonardo Royal, ul. Grzybowska 45, Warszawa Sala Mona i Lisa WALNE ZGROMADZENIE ZARZĄDU GŁÓWNEGO POLSKIEGO TOWARZYSTWA OKULISTYCZNEGO Rada Okulistów Polskich
Ocena ogólna: Raport całkowity z okresu od 04.05.2007 do 15.11.2007
 W Niepublicznym Zakładzie Opieki Zdrowotnej ABC medic Praktyka Grupowa Lekarzy Rodzinnych w Zielonej Górze w okresie od 04.05.2007-15.11.2007 została przeprowadzona ocena efektów klinicznych u pacjentów
W Niepublicznym Zakładzie Opieki Zdrowotnej ABC medic Praktyka Grupowa Lekarzy Rodzinnych w Zielonej Górze w okresie od 04.05.2007-15.11.2007 została przeprowadzona ocena efektów klinicznych u pacjentów
1. NAZWA PRODUKTU LECZNICZEGO. Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka zawiera 2,3 mg ranibizumabu w 0,23 ml roztworu.
1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka zawiera 2,3 mg ranibizumabu w 0,23 ml roztworu.
Znaczenie wczesnego wykrywania cukrzycy oraz właściwej kontroli jej przebiegu. Krzysztof Strojek Śląskie Centrum Chorób Serca Zabrze
 Znaczenie wczesnego wykrywania cukrzycy oraz właściwej kontroli jej przebiegu Krzysztof Strojek Śląskie Centrum Chorób Serca Zabrze Czynniki ryzyka rozwoju i powikłania cukrzycy Nadwaga i otyłość Retinopatia
Znaczenie wczesnego wykrywania cukrzycy oraz właściwej kontroli jej przebiegu Krzysztof Strojek Śląskie Centrum Chorób Serca Zabrze Czynniki ryzyka rozwoju i powikłania cukrzycy Nadwaga i otyłość Retinopatia
Glaucoma-profi laxis 2015
 bezpłatny zestaw pomiarów: pomiar ciśnienia wewnątrzgałkowego metodą bezkontaktową pachymetria (mierzenie grubości rogówki) autorefraktometria (komputerowy pomiar wad widzenia) Glaucoma-profi laxis 2015
bezpłatny zestaw pomiarów: pomiar ciśnienia wewnątrzgałkowego metodą bezkontaktową pachymetria (mierzenie grubości rogówki) autorefraktometria (komputerowy pomiar wad widzenia) Glaucoma-profi laxis 2015
Śląskie Centrum Chorób Serca. Cukrzyca. Krzysztof Strojek Konsultant Krajowy w dziedzinie diabetologii
 Śląskie Centrum Chorób Serca Cukrzyca Krzysztof Strojek Konsultant Krajowy w dziedzinie diabetologii Warszawa 26.11.2014 Czynniki ryzyka rozwoju i powikłania cukrzycy Nadwaga i otyłość Retinopatia Neuropatia
Śląskie Centrum Chorób Serca Cukrzyca Krzysztof Strojek Konsultant Krajowy w dziedzinie diabetologii Warszawa 26.11.2014 Czynniki ryzyka rozwoju i powikłania cukrzycy Nadwaga i otyłość Retinopatia Neuropatia
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 3/2013 z dnia 7 stycznia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Ozurdex,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 3/2013 z dnia 7 stycznia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Ozurdex,
CHECKLISTA. 13. Zaburzenia gospodarki węglowodanowej przestrzeganie diety cukrzycowej w wywiadzie
 Załącznik nr 1 CHECKLISTA Imię i nazwisko Data wypełnienia ankiety. PESEL: Wykształcenie: podstawowe zawodowe średnie wyższe Proszę zaznaczyć charakter wykonywanej pracy Umysłowa Fizyczna Nie pracuje zawodowo
Załącznik nr 1 CHECKLISTA Imię i nazwisko Data wypełnienia ankiety. PESEL: Wykształcenie: podstawowe zawodowe średnie wyższe Proszę zaznaczyć charakter wykonywanej pracy Umysłowa Fizyczna Nie pracuje zawodowo
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO (TNP) (ICD-10 I 27, I 27.0)
 Załącznik B.31. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO (TNP) (ICD-10 I 27, I 27.0) A. Leczenie TNP u dorosłych 1. Leczenie I rzutu 1.1 Leczenie I rzutu sildenafilem 1.2 Leczenie I rzutu bosentanem 2.
Załącznik B.31. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO (TNP) (ICD-10 I 27, I 27.0) A. Leczenie TNP u dorosłych 1. Leczenie I rzutu 1.1 Leczenie I rzutu sildenafilem 1.2 Leczenie I rzutu bosentanem 2.
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
1. NAZWA PRODUKTU LECZNICZEGO. Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka zawiera 2,3 mg ranibizumabu w 0,23 ml roztworu.
1. NAZWA PRODUKTU LECZNICZEGO Lucentis 10 mg/ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml zawiera 10 mg ranibizumabu*. Każda fiolka zawiera 2,3 mg ranibizumabu w 0,23 ml roztworu.
IX. INNE ŚWIADCZENIA DIAGNOSTYCZNE Nazwa świadczenia gwarantowanego LP. Warunki realizacji świadczeń
 IX. INNE ŚWIADCZENIA DIAGNOSTYCZNE Nazwa świadczenia gwarantowanego LP. Warunki realizacji świadczeń 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. Badanie antygenów zgodności tkankowej wykonywanie w celu typowania spokrewnionych
IX. INNE ŚWIADCZENIA DIAGNOSTYCZNE Nazwa świadczenia gwarantowanego LP. Warunki realizacji świadczeń 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. Badanie antygenów zgodności tkankowej wykonywanie w celu typowania spokrewnionych
