KWASY KARBOKSYLOWE. Krystyna Dzierzbicka
|
|
|
- Zuzanna Markiewicz
- 7 lat temu
- Przeglądów:
Transkrypt
1 KWASY KARBKSYLWE Krystyna Dzierzbicka
2 Kwasy karboksylowe są związkami organicznymi zawierającymi grupę karboksylową -H zbudowaną z grupy karbonylowej () i hydroksylowej (H). R (Ar) H karboksylowy Możemy je podzielić na alifatyczne (grupa alkilowa połączona z grupą karboksylową, np. butanowy, heptanowy) i aromatyczne (grupa arylowa połączona z grupą karboksylową, np. benzoesowy).
3 Przykłady ów H 3 H etanowy octowy H 3 H 3 H H 3 H 2 H propanowy propionowy H 2-metylopropanowy izomasłowy H 3 (H 2 ) 16 H 3 H 2 H 2 butanowy masłowy H oktadekanowy stearynowy H H H 2 H karboksylowych cykloheksanokarboksylowy fenylooctowy H H H benzoesowy 1-naftoesowy 2-naftoesowy
4 Kwasy zawierające grupy funkcyjne y wielokarboksylowe H H H H etanodiowy szczawiowy H H 2 H propanodiowy malonowy H H H 2 H 2 H butanodiowy bursztynowy H H (Z)-butenodiowy maleinowy 1,4-benzenodikarboksylowy tereftalowy H (E)-butenodiowy fumarowy
5 hydroksyy - są substancjami krystalicznymi, niższe hydroksyy są dobrze rozpuszczalne w wodzie, ich zapach jest ostry i drażniący; są silniejszymi ami niż y alkanowe, spowodowane to jest efektem indukcyjnym I grupy hydroksylowej; efekt +M osłabia moc ów hydroksyarenowych.
6 H 3 H H H 2-hydroksypropanowy mlekowy H H H H H 2 H H H 2-hydroksyetanowy glikolowy H 2-hydroksybutanodiowy jabłkowy H H H H H H 2,3-dihydroksybutanodiowy winowy H H H 2 H H 2 H 2-hydroksy-1,2,3- propanotrikarboksylowy cytrynowy
7 trzymywanie a-hydroksyów synteza cyjanohydryn i ich hydroliza H 3 -H 2 - propanal H HN N H 3 H 2 -H- N H cyjanohydryna H 2, H H 3 H 2 -H-H H (R,S)-2-hydroksybutanowy hydroliza a-halogenoów H 3 -H-H l (R,S)-2-chloropropanowy H 2, H H 2, H H 3 -H-H H (R,S)-2-hydroksypropanowy (D,L)-mlekowy
8 redukcja a-oksoów H 3 --H pirogronowy NaBH 4 H 3 -H-H H (R,S)-2-hydroksypropanowy (D,L)-mlekowy reakcja aminoów z em azotowym(iii) H 3 -H-Et NH 2 ester etylowy alaniny HN 2 - H 2 H 3--Et N N diazopropionian etylu H 2, - N 2 H 3 -H-Et H a-hydroksypropionian etylu
9 trzymywanie b-hydroksyów H reakcja Reformackiego benzaldehyd + H 3 BrHEt a-bromopropionian etylu 1. Zn / eter 2. H, H 2 H HR H H 3 3-fenylo-3-hydroksy-2- metylopropanian etylu
10 aldehyd lub keton + BrH 2 R a-bromoester (aktywne a-halogenoestry) Zn eter ZnBr H 2 R produkt addycji zw. cynkoorganicznego ze zw. karbonylowym H, H 2 H 2 R H b-hydroksyester
11 redukcja b-oksoów H 3 H 2 H H 2 / Ni H 3 H H 2 H 3-oksobutanowy H (R,S)-3-hydroksybutanowy (D,L)-b-hydroksymasłowy utlenianie aldoli H 3 H H 2 H P H 3 H H 2 H H H aldol b-hydroksyaldehyd (R,S)-3-hydroksybutanowy (D,L)-b-hydroksymasłowy
12 halogenoy y zawierające atom halogenu w łańcuchu bocznym; ich właściwości zależą od położenia halogenu względem grupy karboksylowej; najbardziej reaktywne w reakcjach S N są a-halogenoy. H H l H 2-chloroetanowy a-chlorooctowy H 3 H Br H 2-bromopropanowy a-bromopropionowy H 3 H I H 2 H 3-jodobutanowy b-jodomasłowy
13 aminoy H 2 N H H 3 H 2-aminopropanowy alanina (Ala; A) H 2 N H H H H H 3 2-amino-3-hydroksybutanowy treonina (Thr; T) H 2 N H (H 2 ) 4 H NH 2 2,6-diaminoheksanowy lizyna (Lys; K)
14 y zawierające pierścień aromatyczny i y nienasycone H H H H H o-hydroksybenzoesowy salicylowy 2-hydroksyfenylooctowy migdałowy H 3 H H H 2 H H propenowy akrylowy H 2 H(H 3 ) 2 2-(p-izobutylofenylo)propanowy ibuprofen H 3 H H 3 H (E)-2-metylobut-2-enowy tyglinowy (składnik naturalnych olejów)
15 oksoy H 3 H 2-oksopropanowy pirogronowy H 2 benzoilooctowy H
16 Budowa grupy karboksylowej hybrydyzacja sp 2 karbonylowego atomu węgla polaryzacja wiązania, struktury mezomeryczne i rozkład ładunków w grupie H -I, -M a H sp 2 H centrum zasadowe (akceptory ów Lewisa) centrum elektrofilowe czynny wodór centrum owe (donor protonu) -I - ujemny efekt indukcyjny -M - ujemny efekt mezomeryczny a H H a H H
17 trzymywanie ów karboksylowych utlenianie alkoholi 1 o, aldehydów lub bocznych łańcuchów w pierścieniu aromatycznym H 3 -H 2 -H 2 -H 2 -H butan-1-ol r 3, H 2 S 4 H 2 H 3 -H 2 -H 2 - butanowy H H 3 -H 2 - propan-1-al H odczynnik Tollensa H3 -H 2 - H propanowy H 2 H 3 H 1. KMn 4, H - 2. H + etylobenzen benzoesowy
18 utlenianie alkenów R-H H R' KMn 4, H 2 R-H + R'-H reakcja haloformowa (metyloketonów, 2-hydroksyalkanów) reakcja halogenu (chlor, brom, jod) z metyloketonem w środowisku zasadowym w wyniku, której otrzymuje się y karboksylowe lub reakcja halogenów z 2-hydroksyalkanami, która daje też y karboksylowe: H 3H - 3 H 3 + 3I 2 I 3 aceton H 3 H - I H 3 H H + HI 3 jodoform + H 3 H octowy
19 hydroliza nitryli w środowisku zasadowym oraz kwaśnym H 2, H + H 3 -N H 3 -H + NH 4 + acetonitryl octowy H 3 H 2 -N H 2, NaH H3 H Na + + NH 3 propionitryl propionian sodu 2 N H 2 -N H 2, H 2 S 4 2 N H 2 -H cyjanek p-nitrobenzylu p-nitrofenylooctowy 1. H 2, NaH, H 3 (H 2 ) 8 -N H 3 (H 2 ) 8 -H dekanonitryl 2. H + dekanowy ( kaprynowy)
20 reakcja związków magnezoorganicznych [R(Ar)MgX] z ditlenkiem węgla ( 2 ) H 3 H 2 MgBr + bromek ditlenek wegla etylomagnezowy A N H 3 H 2 MgBr H 3 + H 3 H 2 H propionowy Br bromek fenylu Mg MgBr + Et 2 ditlenek wegla bromek fenylomagnezowy A N MgBr H 3 + H benzoesowy
21 Właściwości fizyczne ów karboksylowych Kwasy alifatyczne łańcuchowe do 6 atomów węgla w cząsteczce są bezbarwnymi cieczami o ostrym, nieprzyjemnym zapachu. Kwasy do 4 atomów węgla w cząsteczce dobrze rozpuszczają się w wodzie, a do 12 atomów węgla w alkoholu. Aktywność chemiczna ów karboksylowych maleje wraz ze wzrostem długości atomów węgla w cząsteczce. Kwasy karboksylowe są mało lotne, mają one wyższe temperatury wrzenia niż alkohole o porównywalnej masie cząsteczkowej, a wynika to z występowania wiązań wodorowych pomiędzy cząsteczkami ów karboksylowych. Wraz ze wzrostem masy cząsteczkowej u wzrastają ich temperatury wrzenia i topnienia.
22 Właściwości chemiczne ów karboksylowych owość - stała równowagi reakcji dysocjacji jest miarą owości ów karboksylowych: R H + H 2 R - + H 3 + K a = [R - ][H 3 + ] [R H] pk a = - log K a Im mniejsza wartość pka tym mocniejszy.
23 Kwasowość ów alifatycznych maleje w miarę wydłużania łańcucha węglowego; H 3 H H H 3 H H 3 H 2 H H 3 H 2 H 2 H H H H 3 malejąca moc u (zwiększa się hydrofobowość cząsteczki) podstawniki elektronoakceptorowe (np. N 2, N, F, l, Br, F 3 ) przy atomie węgla sąsiadującym z grupą karboksylową zwiększają owość alifatycznych ów karboksylowych; H 2 H H 2 H H 2 N 2 N F H H 2 H H 2 H H H H 2 H 3 H malejąca moc u (malejący efekt -I)
24 oddalenie podstawnika elektronoakceptorowego od grupy karboksylowej zmniejsza efekt -I alifatycznych ów karboksylowych; a b H 3 H 2 H H H 3 HH 2 H H 2 H 2 H 2 H H 3 H 2 H 2 H Br Br Br malejąca moc u wprowadzenie podstawnika elektronoakceptorowego do pierścienia aromatycznego powoduje wzrost owości, a podstawnika elektronodonorowego (np. NH 2, H 3,H 3 ) obniżenie owości aromatycznych ów karboksylowych; H H H H H H N 2 N l H 3 H 3 malejąca moc u
25 reakcje z zasadami (wodorotlenkami, wodorowęglanem potasu lub sodu oraz amoniakiem) otrzymywanie soli ów karboksylowych: R H + NaH R - Na + + H 2 R H + NaH 3 R - Na + + H 2 3 R H + NH 3 R - NH 4 + reakcje z chlorowcopochodnymi siarki (np. chlorkiem tionylu Sl 2 ) i fosforu (np. pentachlorkiem fosforu Pl 5 czy trichlorkiem fosforu Pl 3 ) służą do otrzymywania chlorków ów karboksylowych: R H + Pl 3 R + Pl + Hl l chlorek owy R H + Sl 2 R + S 2 + Hl l chlorek owy
26 estryfikacja Fischera jest to reakcja odwracalna ów karboksylowych z alkoholami w obecności u mineralnego, np. Hl, H 2 S 4 w wyniku, której otrzymuje się estry ów karboksylowych: RH 2 H karboksylowy H + RH 2 - H + + H H H RH 2 + RH 2 H H H + R'-H wolno RH 2 H H + H R' H RH 2 R' + H 2 - H 2 + H 2 RH 2 + H R' - H + RH 2 + H + ester R' Wydajnością reakcji estryfikacji można sterować, bądź przez zastosowanie nadmiaru jednego z reagentów (zwykle tańszego, najczęściej jest nim alkohol) lub przez usuwanie ze środowiska reakcji jednego z produktów (estru lub wody, najczęściej wody za pomocą nasadki azeotropowej).
27 H 3 -H 2 -H 2 - butanowy H 2 S 4 + H 3 -H 2 -H 2 -H H 3 -H 2 -H H 2 H H propan-1-ol 2 H 2 H 3 butanian propylu H 3 -H 2 -H 2 -H 2 - pentanowy H + H 2 H alkohol benzylowy H 2 S 4 H 3 -H 2 -H 2 -H 2 - H 2 pentanian benzylu + H 2
28 HH H 3 H RH 2 H R 2 HH R 3 H Szereg reaktywności ów H 3 H RH 2 H R 2 HH R 3 H Szereg reaktywności alkoholi H + H 3 H H 2 S 4 H 3 + H2 benzoesowy metanol benzoesan metylu
29 Reakcja estryfikacji z wykorzystaniem chlorków owych w środowisku zasadowym R l + chlorek owy pirydyna R' H R alkohol ester R' + Hl l + chlorek benzoilu (H 3 ) 3 H pirydyna tert-butanol + Hl (H 3 ) 3 benzoesan tert-butylu
30 redukcja ów karboksylowych do alkoholi 1 o LiAlH 4 nie można stosować w przypadku ów zawierających inne podstawniki wrażliwe na redukcję, takie jak: -R, -N 2, -N, -, -H. R H karboksylowy 1. LiAlH 4 2. H 2 R H 2 H 1 o alkohol F 3 H p-(trifluorometylo)benzoesowy 1. LiAlH 4, Et 2 2. H 2 F 3 H 2 H alkohol p-(trifluorometylo)benzylowy
31 reakcje odwodnienia ów dikarboksylowych otrzymywanie cyklicznych bezwodników owych. H H ftalowy H H 2 H 2 H bursztynowy + H 2 bezwodnik ftalowy H 2 + H 2 H 2 bezwodnik bursztynowy
32 H 2 H H 2 H 2 H glutarowy H H H H maleinowy H 2 H 2 + H 2 H 2 bezwodnik glutarowy + H 2 bezwodnik maleinowy
33 H 2 H 2 H 2 H 2 H H Ba(H) H 2 adypinowy cyklopentanon H 2 H 2 H 2 H 2 H 2 H H a H 2 pimelinowy cykloheksanon
34 reakcje hydroksyów a-hydroksyy H 3 H H H + H H 2-hydroksypropanowy mlekowy H 3 H H 3 H - 2H 2 laktyd H H 3
35 b-hydroksyy H 3 H H H H 3-hydroksybutanowy H - H 2 H3 H H H krotonowy a b-nienasycony
36 - i -hydroksyy H H - H 2 R -hydroksyy R -lakton H H - H 2 R -hydroksyy R -lakton
37 Przykładowe pytania 1. Wychodząc z u butanowego otrzymać: a. butanol b. butanal c. 1-chlorobutan d. keton fenylowo-propylowy e. oktan-4-on f. 2-bromobutanowy 2. Jakie produkty (wzór + nazwa) otrzymasz w następujących reakcjach:
38 a. H 3 H H H 1. Ag 2, H 2 2. H + b. H 3 H H H EtH, H 2 S 4 c. H 1. LiAlH 4 2. H 2 F 3 d. 1. Mg, Et 2 Br H 3 +
39 3. Zaproponuj metodę rozdzielania mieszaniny zawierającej benzoesowy i naftalen. 4. Uszereguj następujące związki według wzrastającej owości: a. octowy, etan, etanol b. benzen, benzoesowy, alkohol benzylowy c. octowy, etanol, trifluorooctowy, 2,2,2-trifluoroetanol, trifluorometanosulfonowy (F 3 S 2 H) d. cyklopentanon, cyklopenten, cyklopentanokarboksylowy, pentano-2,4-dion 5. Zaproponuj metodę otrzymywania u butanowego z: a. butanol b. butanal c. propanol d. propan-2-ol e. acetaldehyd f. H 3 H 2 H(H) 2
40 6. Mając do dyspozycji toluen zaproponuj syntezę u a-bromofenylooctowego. 7. Przedstaw prosty test chemiczny w celu odróżnienia następujących związków: a. benzoesan metylu i benzoesowy b. benzamid i benzoesan etylu c. benzoesowy i benzamid 8. Niżej podany związek ogrzewano otrzymując izomeryczne produkty. Jaka jest ich struktura. l H H
41 9. Podaj kolejne etapy następującej transformacji: H 3 HH 2 H H H Mając do dyspozycji organiczne i nieorganiczne odczynniki otrzymać: a. 2-metylopropanowy z alkoholu tert-butylowego b. 3,3-dimetylobutanowy z alkoholu tert-butylowego c. 2,4-dimetylobenzoesowy z m-ksylenu d. 4-chloro-3-nitrobenzoesowy z p-chlorotoluenu e. Br z bromku cyklopentylu f. H l H z (E)-lH=HH
42 Dziękuję za uwagę
KWASY KARBOKSYLOWE. Krystyna Dzierzbicka
 KWASY KARBKSYLWE Krystyna Dzierzbicka Kwasy karboksylowe są związkami organicznymi zawierającymi grupę karboksylową - zbudowaną z grupy karbonylowej () i hydroksylowej (). R (Ar) karboksylowy Możemy je
KWASY KARBKSYLWE Krystyna Dzierzbicka Kwasy karboksylowe są związkami organicznymi zawierającymi grupę karboksylową - zbudowaną z grupy karbonylowej () i hydroksylowej (). R (Ar) karboksylowy Możemy je
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
HCOOH kwas metanowy ( mrówkowy ) CH 3. COOH kwas etanowy ( octowy ) CH 2
 Kwasy karboksylowe, Ar Nazewnictwo: Kwasy, które są pochodnymi alkanów o otwartych łańcuchach, są nazywane w sposób systematyczny przez dodanie nazwy kwas i dodanie końcówki owy do alkanu - kwas alkanowy
Kwasy karboksylowe, Ar Nazewnictwo: Kwasy, które są pochodnymi alkanów o otwartych łańcuchach, są nazywane w sposób systematyczny przez dodanie nazwy kwas i dodanie końcówki owy do alkanu - kwas alkanowy
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
Spis treści. Nazewnictwo kwasów karboksylowych.
 Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Kwasy karboksylowe to jednofunkcyjne pochodne węglowodorów o grupie funkcyjnej -COOH zwanej grupą karboksylową.
 Spis treści: Charakterystyka grupy karboksylowej Podział kwasów karboksylowych Nazewnictwo kwasy monokarboksylowe alifatyczne nasycone kwasy monokarboksylowe alifatyczne nienasycone kwasy dikarboksylowe
Spis treści: Charakterystyka grupy karboksylowej Podział kwasów karboksylowych Nazewnictwo kwasy monokarboksylowe alifatyczne nasycone kwasy monokarboksylowe alifatyczne nienasycone kwasy dikarboksylowe
l. at C Wzór sumaryczny pół strukturalny Nazwa systematyczna Nazwa zwyczajowa 1 HCOOH
 KWASY KARBOKSYLOWE Temat: Szereg homologiczny kwasów karboksylowych 1) Występowanie kwasów karboksylowych 2) Podział kwasów karboksylowych 3) Wzory i nazwy kwasów karboksylowych Ad.1 - kwas octowy - kwas
KWASY KARBOKSYLOWE Temat: Szereg homologiczny kwasów karboksylowych 1) Występowanie kwasów karboksylowych 2) Podział kwasów karboksylowych 3) Wzory i nazwy kwasów karboksylowych Ad.1 - kwas octowy - kwas
Zadanie: 3 (1 pkt) W poniższej tabeli podano temperatury wrzenia czterech pierwszych w szeregu homologicznym kwasów monokarboksylowych.
 Zadanie: 1 (2 pkt) Pewien kwas karboksylowy zawiera 40% pierwiastka C. Oblicz masę cząsteczkową tego kwasu. Podaj jego wzór sumaryczny i nazwę Zadanie: 2 (1 pkt) Kwas salicylowy ma właściwości antyseptyczne.
Zadanie: 1 (2 pkt) Pewien kwas karboksylowy zawiera 40% pierwiastka C. Oblicz masę cząsteczkową tego kwasu. Podaj jego wzór sumaryczny i nazwę Zadanie: 2 (1 pkt) Kwas salicylowy ma właściwości antyseptyczne.
Krystyna Dzierzbicka
 Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z atomem węgla: R(Ar)-, R reszta alkilowa;
Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z atomem węgla: R(Ar)-, R reszta alkilowa;
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
PRZYKŁADOWE ZADANIA KWASY
 PRZYKŁADOWE ZADANIA KWASY Zadanie 1014 (3 pkt) Pr.XII/2004 A2 Określ typ podanych niżej reakcji: I. C 17 H 33 COOH + Br 2 C 17 H 33 Br 2 COOH Al 2O 3, temp II. C 2 H 5 OH C 2 H 4 + H 2 O hγ III. CH 4 +
PRZYKŁADOWE ZADANIA KWASY Zadanie 1014 (3 pkt) Pr.XII/2004 A2 Określ typ podanych niżej reakcji: I. C 17 H 33 COOH + Br 2 C 17 H 33 Br 2 COOH Al 2O 3, temp II. C 2 H 5 OH C 2 H 4 + H 2 O hγ III. CH 4 +
Kwasy organiczne. 1. Narysuj wzory półstrukturalne poniższych kwasów:
 Kwasy organiczne 1. arysuj wzory półstrukturalne poniższych kwasów: a. glicerynowy b. cytrynowy c. szczawiooctowy d. bursztynowy e. cynamonowy f. akrylowy g. jabłkowy h. walerianowy i. fosfoenolopirogronowy
Kwasy organiczne 1. arysuj wzory półstrukturalne poniższych kwasów: a. glicerynowy b. cytrynowy c. szczawiooctowy d. bursztynowy e. cynamonowy f. akrylowy g. jabłkowy h. walerianowy i. fosfoenolopirogronowy
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
EGZAMIN WSTĘPNY NA STUDIUM DOKTORANCKIE W CBMIM PAN W ŁODZI. Zestaw pytań z chemii organicznej
 EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
Mg I. I Mg. Nie można ich jednak otrzymać ze związków, które posiadają grupy chlorowcowe w tak zwanym ustawieniu wicynalnym.
 nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
Br Br. Br Br OH 2 OH NH NH 2 2. Zakład Chemii Organicznej: kopiowanie zabronione
 Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Kwasy karboksylowe. 1. Cele lekcji. 2. Metoda i forma pracy. 3. Środki dydaktyczne. 4. Przebieg lekcji. a) Wiadomości.
 Kwasy karboksylowe 1. Cele lekcji a) Wiadomości Uczeń zna budowę kwasów karboksylowych, nazewnictwo kwasów karboksylowych, podział kwasów karboksylowych, sposoby otrzymywania kwasów karboksylowych, właściwości
Kwasy karboksylowe 1. Cele lekcji a) Wiadomości Uczeń zna budowę kwasów karboksylowych, nazewnictwo kwasów karboksylowych, podział kwasów karboksylowych, sposoby otrzymywania kwasów karboksylowych, właściwości
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
Test dla kl. II Związki jednofunkcyjne
 .. imię i nazwisko Test dla kl. II Związki jednofunkcyjne.. klasa. A. Podaj nazwy niżej podanych związków: a) CH 3 -CH 2 -CH 2 -H - b) CH 3 -C-CH 3 - c) CH 3 -CH - d) HCH - e) CH 3 CCH 3-2. Napisz wzory
.. imię i nazwisko Test dla kl. II Związki jednofunkcyjne.. klasa. A. Podaj nazwy niżej podanych związków: a) CH 3 -CH 2 -CH 2 -H - b) CH 3 -C-CH 3 - c) CH 3 -CH - d) HCH - e) CH 3 CCH 3-2. Napisz wzory
Odporność chemiczna - PVC
 dporność chemiczna - PVC dporność chemiczna nieplastyfikowanego PVC niepodlegającego naprężeniu mechanicznemu na płyny przy 20 C i 60 C L.p Chemikalia lub produkty Stężenie Temperatura 20 C 60 C 1. Aceton
dporność chemiczna - PVC dporność chemiczna nieplastyfikowanego PVC niepodlegającego naprężeniu mechanicznemu na płyny przy 20 C i 60 C L.p Chemikalia lub produkty Stężenie Temperatura 20 C 60 C 1. Aceton
Kwasy organiczne G. H. I. J. K. ONa L. Ł. O OH
 ollegium Medicum UJ, Katedra hemii rganicznej, Barbara Drożdż Kwasy organiczne 1. arysuj wzory półstrukturalne poniższych kwasów: a. glicerynowy b. cytrynowy c. szczawiooctowy d. bursztynowy e. cynamonowy
ollegium Medicum UJ, Katedra hemii rganicznej, Barbara Drożdż Kwasy organiczne 1. arysuj wzory półstrukturalne poniższych kwasów: a. glicerynowy b. cytrynowy c. szczawiooctowy d. bursztynowy e. cynamonowy
Kwasy karboksylowe C O OH OH C CH 2 H OH CH 2 C CH 3 C OH C OH C OH. propionowy. mrówkowy. akrylowy. octowy. masłowy metakrylowy.
 Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Zadanie: 2 (4 pkt) Napisz, uzgodnij i opisz równania reakcji, które zaszły w probówkach:
 Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Pochodne kwasów karboksylowych. Krystyna Dzierzbicka
 Pochodne kwasów karboksylowych Krystyna Dzierzbicka halogenki kwasowe X X = l, Br, I bezwodniki kwasowe ' estry ' amidy N 2 sole nitryle N Nazwy grup acylowych 3 3 2 acyl metanoil formyl etanoil acetyl
Pochodne kwasów karboksylowych Krystyna Dzierzbicka halogenki kwasowe X X = l, Br, I bezwodniki kwasowe ' estry ' amidy N 2 sole nitryle N Nazwy grup acylowych 3 3 2 acyl metanoil formyl etanoil acetyl
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
Odporność chemiczna PVC
 Odporność chemiczna PVC Chemikalia lub produkty Stężenie Temperatura 20 o c 60 o c Aceton 100% N Akrylan etylu 100% N N Aldehyd benzoesowy 0.1% N N Aldehyd krotonowy 100% N N Aldehyd octowy 40% N - Aldehyd
Odporność chemiczna PVC Chemikalia lub produkty Stężenie Temperatura 20 o c 60 o c Aceton 100% N Akrylan etylu 100% N N Aldehyd benzoesowy 0.1% N N Aldehyd krotonowy 100% N N Aldehyd octowy 40% N - Aldehyd
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
ALKOHOLE, FENOLE, ALDEHYDY, KETONY
 LKOHOLE, FENOLE, LDEHYDY, KETONY ZDNIE DOMOWE ZDNIE 1. (2 P.): Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. Określ typ każdej reakcji (1. 4.) z powyższego schematu,
LKOHOLE, FENOLE, LDEHYDY, KETONY ZDNIE DOMOWE ZDNIE 1. (2 P.): Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. Określ typ każdej reakcji (1. 4.) z powyższego schematu,
Podział związków organicznych
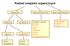 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Alkohole i fenole. Opracowanie: Bartłomiej SIEPSIAK klasa 3d Opiekun: p. Teresa Gębicka
 Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
Reakcje związków karbonylowych. Maria Burgieł R R C O. C O + Nu E C
 eakcje związków karbonylowych Maria Burgieł Związki zawierające grupę = nazywamy związkami karbonylowymi. Do najprostszych związków karbonylowych należą aldehydy, w których grupa = jest połączona z jedną
eakcje związków karbonylowych Maria Burgieł Związki zawierające grupę = nazywamy związkami karbonylowymi. Do najprostszych związków karbonylowych należą aldehydy, w których grupa = jest połączona z jedną
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Materiał powtórzeniowy do sprawdzianu - kwasy karboksylowe, estry, glicerydy - tłuszcze, mydła + przykładowe zadania z rozwiązaniami
 Materiał powtórzeniowy do sprawdzianu - kwasy karboksylowe, estry, glicerydy - tłuszcze, mydła + przykładowe zadania z rozwiązaniami I. Kwasy karboksylowe 1. Budowa i klasyfikacja kwasów karboksylowych
Materiał powtórzeniowy do sprawdzianu - kwasy karboksylowe, estry, glicerydy - tłuszcze, mydła + przykładowe zadania z rozwiązaniami I. Kwasy karboksylowe 1. Budowa i klasyfikacja kwasów karboksylowych
WĘGLOWODORY, ALKOHOLE, FENOLE. I. Wprowadzenie teoretyczne
 WĘGLWDRY, ALKHLE, FENLE I. Wprowadzenie teoretyczne Węglowodory Węglowodory są to połączenia organiczne zbudowane z atomów węgla i wodoru. Ze względu na różne sposoby łączenia się atomów węgla w tych związkach
WĘGLWDRY, ALKHLE, FENLE I. Wprowadzenie teoretyczne Węglowodory Węglowodory są to połączenia organiczne zbudowane z atomów węgla i wodoru. Ze względu na różne sposoby łączenia się atomów węgla w tych związkach
Substytucje Nukleofilowe w Pochodnych Karbonylowych
 J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2
![liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2 liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2](/thumbs/65/54124071.jpg) Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
IV Podkarpacki Konkurs Chemiczny 2011/12. ETAP II r. Godz Zadanie 1 (14 pkt.)
 IV Podkarpacki Konkurs Chemiczny 2011/12 KPKCh ETAP II 22.12.2011 r. Godz. 10.00-12.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (14 pkt.) 1. Wskaż, która z chlorowcopochodnych
IV Podkarpacki Konkurs Chemiczny 2011/12 KPKCh ETAP II 22.12.2011 r. Godz. 10.00-12.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (14 pkt.) 1. Wskaż, która z chlorowcopochodnych
Skala ocen: ndst 0 20, dst , dst , db , db , bdb Informacja:
 Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Przed sprawdzianem z pochodnych węglowodorów karta powtórzeniowa.
 Przed sprawdzianem z pochodnych węglowodorów karta powtórzeniowa. Grupa związków Grupa funkcyjna wzór nazwa Wzór i nazwa przedstawiciela 1. Znajomość pojęć takich jak: fermentacja alkoholowa i octowa,
Przed sprawdzianem z pochodnych węglowodorów karta powtórzeniowa. Grupa związków Grupa funkcyjna wzór nazwa Wzór i nazwa przedstawiciela 1. Znajomość pojęć takich jak: fermentacja alkoholowa i octowa,
Zakład Chemii Organicznej: kopiowanie zabronione 1/5
 Kolokwium z utleniania i redukcji Autorzy: A. Kluczyk, M. Kuczer, D. Myśliwiec Imię i nazwisko Kierunek studiów Nazwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0-20, dst 20,5-24, dst+
Kolokwium z utleniania i redukcji Autorzy: A. Kluczyk, M. Kuczer, D. Myśliwiec Imię i nazwisko Kierunek studiów Nazwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0-20, dst 20,5-24, dst+
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Wytrzymałość chemiczna krat z tworzywa
 Wytrzymałość chemiczna krat z tworzywa 2 A Aceton 25 50 częściowo odporne odporne odporne Aceton 100 każda nieodporne nieodporne nieodporne Aldehyd mrówkowy 44 45 nieodporne częściowo odporne odporne Aldehyd
Wytrzymałość chemiczna krat z tworzywa 2 A Aceton 25 50 częściowo odporne odporne odporne Aceton 100 każda nieodporne nieodporne nieodporne Aldehyd mrówkowy 44 45 nieodporne częściowo odporne odporne Aldehyd
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery.
 CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
Materiały dodatkowe alkohole, fenole, etery
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Egzamin wstępny z Chemii 1 lipca 2011 r.
 Egzamin wstępny z Chemii 1 lipca 2011 r. 1. Wskaż, które z podanych niżej substancji przereagują z wodnym roztworem chlorowodoru. Podaj zbilansowane równania odpowiednich reakcji i określ ich typ. (kwasowo
Egzamin wstępny z Chemii 1 lipca 2011 r. 1. Wskaż, które z podanych niżej substancji przereagują z wodnym roztworem chlorowodoru. Podaj zbilansowane równania odpowiednich reakcji i określ ich typ. (kwasowo
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Budowa tłuszczów // // H 2 C O H HO C R 1 H 2 C O C R 1 // // HC O H + HO C R 2 HC - O C R 2 + 3H 2 O
 Tłuszcze (glicerydy) - Budowa i podział tłuszczów, - Wyższe kwasy tłuszczowe, - Hydroliza (zmydlanie) tłuszczów - Utwardzanie tłuszczów -Próba akroleinowa -Liczba zmydlania, liczba jodowa Budowa tłuszczów
Tłuszcze (glicerydy) - Budowa i podział tłuszczów, - Wyższe kwasy tłuszczowe, - Hydroliza (zmydlanie) tłuszczów - Utwardzanie tłuszczów -Próba akroleinowa -Liczba zmydlania, liczba jodowa Budowa tłuszczów
EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III
 Miejsce na naklejkę z kodem szkoły iejsce na naklejkę z kodem szkoły dysleksja Liczba pkt: Wynik %: Ocena: MCH-R1A1P-062 EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III ARKUSZ II Arkusz
Miejsce na naklejkę z kodem szkoły iejsce na naklejkę z kodem szkoły dysleksja Liczba pkt: Wynik %: Ocena: MCH-R1A1P-062 EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III ARKUSZ II Arkusz
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 VIII Podkarpacki Konkurs Chemiczny 015/016 ETAP III 1.0.016 r. Godz. 1.00-15.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (17 pkt) 1. Cyna ( 50 Sn) jest pierwiastkiem należącym
VIII Podkarpacki Konkurs Chemiczny 015/016 ETAP III 1.0.016 r. Godz. 1.00-15.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (17 pkt) 1. Cyna ( 50 Sn) jest pierwiastkiem należącym
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ
 FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
Program nauczania CHEMIA KLASA 8
 Program nauczania CHEMIA KLASA 8 DZIAŁ VII. Kwasy (12 godzin lekcyjnych) Wzory i nazwy kwasów Kwasy beztlenowe Kwas siarkowy(vi), kwas siarkowy(iv) tlenowe kwasy siarki Przykłady innych kwasów tlenowych
Program nauczania CHEMIA KLASA 8 DZIAŁ VII. Kwasy (12 godzin lekcyjnych) Wzory i nazwy kwasów Kwasy beztlenowe Kwas siarkowy(vi), kwas siarkowy(iv) tlenowe kwasy siarki Przykłady innych kwasów tlenowych
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
A B C D A B C 4. D A B C D
 1. Kartkówka, 21 października 2015; zestaw Imię i azwisko: Zad. 1. (1 p) Wśród podanych związków,, i D, wszystkie atomy węgla występują w tym samym stanie hybrydyzacji w związkach: i i D 3. i 4. i D Zad.
1. Kartkówka, 21 października 2015; zestaw Imię i azwisko: Zad. 1. (1 p) Wśród podanych związków,, i D, wszystkie atomy węgla występują w tym samym stanie hybrydyzacji w związkach: i i D 3. i 4. i D Zad.
Test kompetencji z chemii do liceum. Grupa A.
 Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
REAKCJE W CHEMII ORGANICZNEJ
 Katedra Biochemii ul. Akademicka 12, 20-033 Lublin tel. 081 445 66 08 www.biochwet.up.lublin.pl REAKCJE W CHEMII ORGANICZNEJ I. Reakcje utleniania na przykładzie różnych związków organicznych. 1. Utlenienie
Katedra Biochemii ul. Akademicka 12, 20-033 Lublin tel. 081 445 66 08 www.biochwet.up.lublin.pl REAKCJE W CHEMII ORGANICZNEJ I. Reakcje utleniania na przykładzie różnych związków organicznych. 1. Utlenienie
Pochodne węglowodorów
 Literka.pl Pochodne węglowodorów Data dodania: 2010-01-12 15:53:16 Autor: Janina Tofel-Bykowa Sprawdzian wiadomości i umiejętności z chemii organicznej w kl. III gimnazjum. I Dokończ zdanie: 1. Nazwa grupy
Literka.pl Pochodne węglowodorów Data dodania: 2010-01-12 15:53:16 Autor: Janina Tofel-Bykowa Sprawdzian wiadomości i umiejętności z chemii organicznej w kl. III gimnazjum. I Dokończ zdanie: 1. Nazwa grupy
CH 3 OH C 2 H 5 OH H 3 C CH 2 CH 2 OH H 3 C CH CH 3 OH metanol etanol propan-1-ol propan-2-ol H 2 C CH 2 OH OH H 2 C CH CH 2 OH OH OH
 Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA
 SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
do zadań na konkurs z chemii etapu wojewódzkiego w roku szkolnym 2014/2015
 1 M O D E L O D P O W I E D Z I do zadań na konkurs z chemii etapu wojewódzkiego w roku szkolnym 2014/2015 Zadanie 1. [0-6 pkt.] Zaprojektuj doświadczenie chemiczne, w którym otrzymasz etylen oraz wykażesz
1 M O D E L O D P O W I E D Z I do zadań na konkurs z chemii etapu wojewódzkiego w roku szkolnym 2014/2015 Zadanie 1. [0-6 pkt.] Zaprojektuj doświadczenie chemiczne, w którym otrzymasz etylen oraz wykażesz
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
PRÓBNY EGZAMIN MATURALNY Z CHEMII
 Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO OKRĘGOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE PRÓBNY EGZAMIN MATURALNY Z CHEMII Czas pracy 90 minut Informacje 1.
Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO OKRĘGOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE PRÓBNY EGZAMIN MATURALNY Z CHEMII Czas pracy 90 minut Informacje 1.
PRÓBNY EGZAMIN MATURALNY Z CHEMII
 Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO OKRĘGOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE PRÓBNY EGZAMIN MATURALNY Z CHEMII ARKUSZ II MARZEC 2002 CHEMIA Czas
Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO OKRĘGOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE PRÓBNY EGZAMIN MATURALNY Z CHEMII ARKUSZ II MARZEC 2002 CHEMIA Czas
Wymagania programowe na poszczególne oceny chemia kl. III 2014/2015
 Wymagania programowe na poszczególne oceny chemia kl. III 2014/2015 VI. Sole opisuje budowę soli wskazuje metal i resztę kwasową we wzorze soli zapisuje wzory sumaryczne soli (chlorków, arczków) tworzy
Wymagania programowe na poszczególne oceny chemia kl. III 2014/2015 VI. Sole opisuje budowę soli wskazuje metal i resztę kwasową we wzorze soli zapisuje wzory sumaryczne soli (chlorków, arczków) tworzy
ALDEHYDY, KETONY. I. Wprowadzenie teoretyczne
 ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
Rozdział 7. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 7 Errata do siódmego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 187 Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 7 Errata do siódmego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 187 Zadanie
Estry. 1. Cele lekcji. 2. Metoda i forma pracy. 3. Środki dydaktyczne. a) Wiadomości. b) Umiejętności
 Estry 1. Cele lekcji a) Wiadomości Uczeń: wie, jak zbudowane są cząsteczki estrów, wie, jakie jest zastosowanie estrów, wie, jakie są właściwości fizyczne octanu etylu zna pojęcia: stan równowagi dynamicznej,
Estry 1. Cele lekcji a) Wiadomości Uczeń: wie, jak zbudowane są cząsteczki estrów, wie, jakie jest zastosowanie estrów, wie, jakie są właściwości fizyczne octanu etylu zna pojęcia: stan równowagi dynamicznej,
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
17. DODATKI Tabela 1. Symbole okre laj ce wielokrotno ci i podwielokrotno ci ułamków dziesi tnych Symbol Okre lenie Wielokrotno Tabela 2.
 17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
I. Węgiel i jego związki z wodorem
 NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
MECHANIZMY REAKCJI CHEMICZNYCH. REAKCJE CHARAKTERYSTYCZNE GRUP FUNKCYJNYCH ZWIĄZKÓW ORGANICZNYCH
 Ćwiczenie 2 semestr 2 MECHANIZMY REAKCJI CHEMICZNYCH. REAKCJE CHARAKTERYSTYCZNE GRUP FUNKCYJNYCH ZWIĄZKÓW ORGANICZNYCH Obowiązujące zagadnienia: Związki organiczne klasyfikacja, grupy funkcyjne, reakcje
Ćwiczenie 2 semestr 2 MECHANIZMY REAKCJI CHEMICZNYCH. REAKCJE CHARAKTERYSTYCZNE GRUP FUNKCYJNYCH ZWIĄZKÓW ORGANICZNYCH Obowiązujące zagadnienia: Związki organiczne klasyfikacja, grupy funkcyjne, reakcje
Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
 Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum
 Lucyna Krupa Rok szkolny 2018/2019 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Lucyna Krupa Rok szkolny 2018/2019 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
NIEBEZPIECZNE REAKCJE CHEMICZNE
 NIBPICN RAKCJ CHMICN Niniejsze zestawienie stanowi jedynie wybór i obejmuje jedynie niektóre reakcje niebezpieczne. Wymienione związki mogą ulegać również innym reakcjom niebezpiecznym. Brak na niniejszej
NIBPICN RAKCJ CHMICN Niniejsze zestawienie stanowi jedynie wybór i obejmuje jedynie niektóre reakcje niebezpieczne. Wymienione związki mogą ulegać również innym reakcjom niebezpiecznym. Brak na niniejszej
Substytucja nukleofilowa
 Substytucja nukleofilowa Katarzyna strowska eakcja podstawienia nukleofilowego polega na wymianie grupy X związanej z atomem węgla na odczynnik nukleofilowy. Podstawnikiem X jest przeważnie grupa elektronoakceptorowa,
Substytucja nukleofilowa Katarzyna strowska eakcja podstawienia nukleofilowego polega na wymianie grupy X związanej z atomem węgla na odczynnik nukleofilowy. Podstawnikiem X jest przeważnie grupa elektronoakceptorowa,
WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej
 Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne:
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Krystyna Dzierzbicka
 Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z resztą organiczną: R(Ar)-, R reszta alkilowa;
Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z resztą organiczną: R(Ar)-, R reszta alkilowa;
Krystyna Dzierzbicka
 Krystyna Dzierzbicka Fenole związki organiczne, w których grupa hydroksylowa związana jest bezpośrednio z atomem węgla układu aromatycznego (z węglem o hybrydyzacji sp 2 ). Przykłady i -naftol -naftol
Krystyna Dzierzbicka Fenole związki organiczne, w których grupa hydroksylowa związana jest bezpośrednio z atomem węgla układu aromatycznego (z węglem o hybrydyzacji sp 2 ). Przykłady i -naftol -naftol
