Model matematyczny potencjału membranowego dwuwarstwowego polimerowego opatrunku membranowego
|
|
|
- Mikołaj Gajewski
- 7 lat temu
- Przeglądów:
Transkrypt
1 Model matematyczny potencjału membranowego dwuwarstwowego polimerowego opatrunku membranowego ANDRZEJ ŚLĘZAK Katedra Zdrowia Publicznego, Wydział Zarządzania, Politechnika Częstochowska Streszczenie Stosując formalizm termodynamiczny Kedem-Katchalsky ego, opracowano model matematyczny potencjału membranowego generowanego w komórce elektrochemicznej, zawierającej dwa roztwory elektrolityczne rozdzielone dwuwarstwową membraną polimerową. Ów model przedstawia stęŝeniowe i ciśnieniowe zaleŝności potencjału membranowego. Otrzymane równania modelowe, moŝna uŝyć do analizy potencjałów membranowych generowanych w układzie, zawierającym dwuwarstwowy opatrunek membranowy. Słowa kluczowe: potencjał membranowy, równania Kedem-Katchalsky ego, opatrunek membranowy, zeolity srebra
2 Mathematical model of the membrane potential in double-membranous polymeric dressing Summary Using the Kedem-Katchalsky s thermodynamical formalism, the mathematical model of membrane potential, generated in the electrochemical cell, contained two electrolytic solutions separated by double-layer polymeric membrane. This model presented the concentration and pressure dependencies of the membrane potential. The model equations maybe use to analysis the membrane potentials generated in the system containing the doublelayer membrane dressing. Key words: membrane potential, Kedem-Katchalsky equations, membranous dressing, silver zeolite WSTĘP W procesie leczenia trudno gojących się ran, istotną rolę odgrywa właściwe dobranie i zastosowanie opatrunku, które ma na celu między innymi utrzymanie wilgotnego środowiska, właściwej temperatury i ph w miejscu uszkodzenia [, 2]. Owe warunki są zapewniane przez opatrunki interaktywne, pełniące zarówno rolę ochronną, jak i stymulującą naturalne procesy zachodzące na gojącej się ranie [3]. Opatrunki interaktywne chronią włókna nerwowe przed nadmierną stymulacją bólem i traumą podczas stosowania i zmiany opatrunku. Chronią takŝe delikatne tkanki przed działaniem bodźców mechanicznych i wpływem środowiska zewnętrznego. Zmniejszają teŝ ryzyko infekcji róŝnego typu drobnoustrojami. Ich stosowanie intensyfikuje zarówno aktywność lityczno-fagocytarną jak i proliferacyjną, stymulującą gojenie we wszystkich etapach tego procesu. Ponadto stosowanie opatrunków interaktywnych zapobiega wysychaniu powierzchni rany, tworzenia się strupa i zlepów włóknika, powodujących supresję ziarniny. Opatrunki zawierające srebro stanowią nowoczesną grupę opatrunków interaktywnych, stosowanych w miejscowym zachowawczym leczeniu ran o róŝnej etiologii. Wysoka 2
3 aktywność przeciwdrobnoustrojowa srebra w połączeniu z zaawansowaną technologią samych opatrunków powoduje, Ŝe są one polecane zwłaszcza w przypadku ran powikłanych i zakaŝonych. Jednym z przykładów opatrunku złoŝonego/mieszanego jest dwuwarstwowy polimerowy opatrunek membranowy Textus Bioactiv [4]. Zgodnie z opisem producenta ów opatrunek zbudowany jest z trzech rodzajów niejednorodnych i współpracujących ze sobą termoplastycznych włókien polietylenowych, ułoŝonych w dwie warstwy. Pierwsza warstwa zawiera włókna z hydrofilową powierzchnią i hydrofobowym rdzeniem, oraz całkowicie hydrofilowe włókna absorpcyjne (SAP). Na rycinach, 2 i 3 przedstawiono obrazy powierzchni membrany Textus Bioactiv, otrzymane za pomocą skaningowego mikroskopu elektronowego (Zeiss Supra 35). Obrazy te, przedstawione w poprzednich pracach [5, 6] ujawniają przekroje dwóch typów włókien oraz siateczkę zapobiegającą przywieraniu opatrunku membranowego do leczonej rany. Powierzchnia włókien hydrofilowo-hydrofobowych posiada zainkorporowane zeolity srebra; średnio na kaŝdy centymetr kwadratowy opatrunku przypada około 0,2 mg srebra w postaci jonowej (Ag + ) i/lub zmikronizowanej (Ag). Proces aktywacji opatrunku, polegający na uwalnianiu i wymianie jonów Ag + zawartych w zeolicie na jony Ca 2+, następuje po zwilŝeniu opatrunku płynem Ringera. Migracja jonów Ag + systematycznie uwalnianych z zeolitów odbywa się skokowo, od zeolitów do włókien SAP. W tym procesie jony Ag + przebywają odległość około 50 nm i są wychwytywane przez towarzyszące włóknom polimerowym zawierającym zeolity włókna SAP. Trzeci rodzaj włókien polimerowych znajduje się w drugiej warstwie membrany i jest ułoŝony równolegle do powierzchni skóry, tworząc specjalną siateczkę zapobiegającą przywieraniu opatrunku do leczonej rany. W poprzednich pracach [7-9], przy pomocy równań Kedem-Katchalsky ego, opracowano model transportu osmotyczno-dyfuzyjnego przez podwójną membranę Textus Bioactiv i wyznaczono czasowe i stęŝeniowe charakterystyki współczynników: przepuszczalności hydraulicznej, odbicia i przepuszczalności dyfuzyjnej. Wykazano, Ŝe wartość współczynników odbicia i przepuszczalności dyfuzyjnej nie zaleŝy zarówno od czasu jak i od stęŝenia. Wyniki badań doświadczalnych pokazały, Ŝe polimerowy opatrunek membranowy Textus Bioactiv posiada nieliniowe właściwości transportowe w zakresie objętościowego transportu osmotycznego, które są konsekwencją jego struktury i właściwości fizykochemicznych. Na podstawie wyznaczonych doświadczalnie ciśnieniowych charakterystyk strumienia objętościowego stwierdzono, Ŝe ów strumień jest zaleŝny zarówno od róŝnicy ciśnień hydrostatycznych ( P) jak i róŝnicy stęŝeń roztworów ( C) rozdzielanych przez membranę. Przeprowadzone eksperymenty uzasadniają tezę o właściwościach 3
4 prostowniczych opatrunku membranowego Textus Bioactiv, w odniesienu do objętościowych przepływów osmotycznych. Te właściwości występują powyŝej krytycznej wartości C. W obecnej pracy przedstawiamy model matematyczny potencjału membranowego generowanego polimerowego w komórce elektrochemicznej, zawierającej dwa roztwory elektrolityczne rozdzielone dwuwarstwową membraną polimerową, opracowany w ramach formalizmu termodynamicznego Kedem-Katchalsky ego. Ów model przedstawiający zaleŝności stęŝeniowe i ciśnieniowe potencjału membranowego, moŝna wykorzystać między innymi do analizy potencjałów membranowych generowanych w układzie, w którym dwuwarstwowa membrana polimerowa wykorzystywana jako opatrunek membranowy, rozdziela wodne roztwory soli o róŝnych stęŝeniach. MODEL MATEMATYCZNY POTENCJAŁU MEMBRANOWEGO Opatrunek Textus Bioactiv jest dwuwarstwową membraną polimerową (M), składającą się z dwóch warstw oraz, ułoŝonych w serię. Na rycinie 4 przedstawiono graficznie schemat owej membrany. Warstwa zawiera włókna polimerowe z hydrofobowym rdzeniem oraz hydrofilową powierzchnią, zawierającą zeolity srebra oraz całkowicie hydrofilowe polietylenowe włókna absorpcyjne. Warstwa zawiera włókna polimerowe, tworzące siateczkę zapobiegającą przywieraniu opatrunku do leczonej rany. W prezentowanym modelu kaŝdą z warstw traktujemy jak niezaleŝną membranę (M, M ) o określonych właściwościach transportowych. Owe właściwości opisują współczynniki: przepuszczalności hydraulicznej (L p, L p ), odbicia (σ, σ ), przepuszczalności dyfuzyjnej (ω, ω ) oraz liczby przenoszenia dla anionów (t a ) i kationów (t c ). W chwili początkowej membrana M rozdziela dwa jednorodne roztwory elektrolityczne o stęŝeniach C h i C l (C h >C l ), na które działa ciśnienie hydrostatyczne odpowiednio P h i P l. StęŜenie i ciśnienie roztworu na granicy warstw oraz oznaczymy odpowiednio przez C m i P m. Potencjały membranowe dla warstw i oznaczymy odpowiednio przez i i ψ. ψ Zgodnie z formalizmem termodynamicznym opisanym w pracy [0], równania dla ψ moŝna zapisać w następującej postaci ψ RT C ψ ( t ) ln h = a t c () F C m 4
5 RT C ψ ( t )ln m = a t c (2) F C Dla rozpatrywnego w pracy układu membranowego spełniony jest warunek Uwzględniając równania () i (2) w równaniu (3) otrzymujemy gdzie: t = t a t c, t = t a t c. l ψ = ψ + ψ (3) RT ψ = ( t t )ln Cm + t ln Ch t ln C l F (4) Występująca w równaniu (4) wielkość C m, określająca stęŝenie roztworu na granicy warstwa /warstwa jest nieznana. MoŜna ją jednak obliczyć przy pomocy równań Kedem- Katchalsky ego. Stosując owe równania i procedurę opisaną w pracy [], równania opisujące strumienie solutu przez warstwę ( J s ) i przez warstwę ( J s ), moŝna zapisać w następującej postaci. J = ω ζ RT ( C C ) + J ( σ )( C + C ) (5) s h m 2 v h m J = ω ζ RT ( C C ) + J ( σ )( C + C ) (6) s m l 2 v m l gdzie: Lp Lp Jv = Jv = Jv = {( Ph Pl ) ζ RT[ Cm( σ σ ) + σch σ Cl ]} L + L p p (7) W równaniach (5)-(8), ζ (0 ζ 2) oznacza współczynnik Van Hoff, a RT jest iloczynem stałej gazowej i temperatury termodynamicznej. W stanie ustalonym spełniony jest warunek J = J = J (8) s s s W celu obliczenia C m, weźmy pod uwagę równania (5)-(8). Ich stosunkowo proste przekształcenia upowaŝniają nas do zapisania następującego równania kwadratowego gdzie: 2 2 γ + γ + γ = (9) 2 Cm 2Cm 3 0 γ = ζ σ σ σ σ (0) 2 RT Ls ( )( ) γ = ( σ σ ){ Α + L RTζ [( σ ) C ( σ ) C ]} ζ RT ( ω + ω ) () s l h γ = ζ RT ( ω C + ω C ) + Α[( σ ) C ( σ ) C ] (2) 3 h l 2 h l Α = L [( P P ) ζ RT ( σ C σ C )] (3) s h l h l L = L L ( L + L ) (4) s p p p p 5
6 Równanie (9) moŝna rozwiązać przy pomocy typowego algorytmu rozwiązywania równania kwadratowego. Dla dodatniego wyróŝnika tego równania otrzymujemy rozwiązania w postaci C m =-γ 2 ±(γ 2 2-4γ γ 3 ) 0.5 (2γ ) -. DYSKUSJA Dyskusja współczynników opisanych równaniami (0)-(4), pozwala rozpatrzyć następujące przypadki:. Jeśli jedna z warstw jest nieselektywna (np. warstwa ), co narzuca warunek σ =0, to zamiast wyraŝeń (0)-(4) moŝemy napisać 2 = 2 RT Ls (0a) γ ζ σ γ = σ Α + ζ σ ζ ω + ω (a) 2 2 { LsRT [ Cl ( ) Ch]} RT ( ) γ = ζ RT ( ω C + ω C ) + Α[( σ ) C C ] (2a) 3 h l 2 h l Α = L [( P P ) ζ RTσ C ] (3a) s h l h 2. Jeśli warstwy i są selektywne i ich właściwości transportowe są identyczne, co implikuje warunki L = L = L, σ = σ =σ oraz ω = ω =ω, to równanie (9) upraszcza się do postaci p p p Lp Cm = ( Ch + Cl ) + [( Ph Pl ) RTσ ( Ch Cl )]( σ )( Ch Cl ) (5) 2 8 RTω 3. Jeśli warstwy i mają jednakowe właściwości transportowe i ponadto są nieselektywne, co oznacza, Ŝe (9) upraszcza się do postaci p p p L = L = L, σ = σ =0 oraz ω = ω =ω, wtedy równanie C ( ) m = 2 Ch + Cl (6) Procedurę pomiarową potencjału membranowego narzuca równanie (4). Do wyznaczenia owych potencjałów moŝna wykorzystać typowy układ pomiarowy oraz metodykę pomiarów opisane w poprzedniej pracy [2]. Opisany zestaw pomiarowy składa się z komórki elektrochemicznej dwóch elektrod odwracalnych i elastycznych mostków elektrolitycznych, łączących komórkę z elektrodami. Jeśli roztwory rozdzielane przez membranę zawierają jon Cl -, to do pomiarów potencjałów membranowych moŝna wykorzystać dwie elektrody Ag/AgCl. Opisana w tej w pracy komórka elektrochemiczna składa się z dwóch cylindrycznych naczyń plexiglasowych (h, l) o objętości 200 cm 3, rozdzielonych membraną M o powierzchni 6
7 ,5 cm 2 i wyposaŝonych w mieszadła mechaniczne. Naczynie h naleŝy wypełnić roztworem o stęŝeniu C h, natomiast naczynie l roztworem o stęŝeniu C l (C h >C l ). Do naczynia h jest przyłączona wykalibrowana pipeta (K), słuŝąca do pomiaru przyrostu objętości ( V). Z kolei naczynie l jest połączone za pomocą elastycznego węŝyka z rezerwuarem roztworu o stęŝeniu C l (N). Wysokość ustawienia tego rezerwuaru względem pipety K, moŝe być regulowana w celu zadania róŝnicy ciśnień hydrostatycznych ( P). Naczynia z elektrodami naleŝy wypełnić wodnym roztworem KCl, o stęŝeniu 0 3 mol m -3 nasyconym AgCl. Sposób konstrukcji elektrod Ag/AgCl jest opisany w pracy [3]. Komórkę elektrochemiczną i elektrody naleŝy umieścić w termostatowanej osłonie elektrostatycznej. W celu zapewnienia jednorodności roztworów naleŝy zastosować mieszanie mechaniczne z szybkością przynajmniej 300 obrotów na minutę. LITERATURA [] SZEWCZYK M. T., JAWIEŃ A., CWAJDA J., CIERZNIAKOWSKA K.: Local treatment of venous leg ulcers principles of dresing choice. Klinika ZakaŜeń (2005),, [2] BENBOW M., BURG G., GOMACHO MARTINEZ F.: Guidelines for the outpatient treatment of chronic wound and burns. Blacwell Science, Berlin-Vienne (997), 6, [3] TURNER T. D.: The development of wound management products. Wounds (989), 3, [4] info@biocell.de [5] ŚLĘZAK A.: Termodynamiczna ocena źródła entropii w układzie zawierającym dwuskładnikowy opatrunek membranowy. InŜ. Biomed. (2008) praca złoŝona w Redakcji. [6] ŚLĘZAK A.: Źródło entropii w układzie zawierającym dwuwarstwową membranę polimerową i binarne roztwory elektrolityczne. Ann. Med. Siles. (2008) praca złoŝona w Redakcji. [7] ŚLĘZAK A., GRZEGORCZYN S., ŚLĘZAK I. M., BRYLL A.: Study on the volume and solute flows through double-membranous polymeric dressing with silver ions. J. Membr. Sci. (2006), 285,
8 [8] ŚLĘZAK A., GRZEGORCZYN S., ŚLĘZAK I. M., KUCHARZEWSKI M.: Badanie przepływów objętościowych przez polimerowy opatrunek membranowy z jonami srebra. Polim. Med. (2006), 36, [9] ŚLĘZAK A., KUCHARZEWSKI M., GRZEGORCZYN S., ŚLĘZAK I. M.: Badanie właściwości transportowych polimerowego opatrunku membranowego z jonami srebra. Polim. Med. (2005), 35, 3-. [0] KATCHALSKY A., CURRAN P. F.: Nonequilibrium Thermodynamics in Biophysics. Harvard Univ. Press, Cambridge 965. [] KEDEM O., KATCHALSKY A.: Permeability of composite membranes. Series array of elements. Trans. Faraday Soc. (963), 59, [2] ŚLĘZAK A.: A model equation for gravielectric effectc in electrochemical cells. Biophys. Chem. (990), 38, [3] IVES S. G. J., JANZ G. J.: Reference electrodes. Academic Press, New York 96. Adres do korespondencji Katedra Zdrowia Publicznego, Wydział Zarządzania Politechnika Częstochowska ul Armii Krajowej 36b, Częstochowa tel. (034) , tel./fax (034) aslezak52@gmail.com 8
9 RYC.. Obraz powierzchni dwuwarstwowej membrany Textus Bioactiv od strony włókien polietylenowych, otrzymane przy pomocy skaningowego mikroskopu elektronowego przy zastosowaniu powiększenia 250 razy. Widoczne są przekroje włókien dwuwarstwowych, których rdzeń jest hydrofobowy a hydrofilowe powierzchnie zawierają zeolity srebra oraz całkowicie hydrofilowe polietylenowe włókna absorpcyjne. Badania wykonano dla membrany w stanie suchym [5] FIG.. The scanning electron microscope image of a surface of the double-layer membrane Textus Bioactiv from a side of polyethylene fibers was obtained with magnification 250. We show the cross section of double-layer fibers with hydrophobic core and hydrophilic surfaces containing silver zeolites, and hydrophilic super absorbing polymers. The image of membrane was performed in a dry state [5] 9
10 RYC. 2. Obraz powierzchni dwuwarstwowej membrany Textus Bioactiv od strony włókien polietylenowych, otrzymane przy pomocy skaningowego mikroskopu elektronowego przy zastosowaniu powiększenia 250 razy. Widoczny jest przekrój jednorodnego całkowicie hydrofilowego polietylenowego włókna absorpcyjnego. Badania wykonano dla membrany w stanie suchym [5] FIG. 2. The scanning electron microscope image of a surface of the double-layer membrane Textus Bioactiv from a side of polyethylene fibers was obtained with magnification 250. We show the cross section of hydrophilic super absorbing polymers. The image of membrane was performed in a dry state [5] 0
11 RYC. 3. Obraz powierzchni dwuwarstwowej membrany Textus Bioactiv od strony siateczki zapobiegającej przywieraniu opatrunku membranowego do leczonej rany, otrzymane przy pomocy skaningowego mikroskopu elektronowego przy zastosowaniu powiększenia 94 razy. W oczkach siateczki widoczne są włókna polietylenowe. Badania wykonano dla membrany w stanie suchym [6] FIG. 3. The scanning electron microscope image of a surface of the double-layer membrane Textus Bioactiv. A view from a side of a net that prevents from sticking to a tread wound was obtained with magnification 94. The polymeric fibers are visible in a mesh of the net. The image of membrane was performed in a dry state [6]
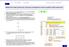
12 RYC 4. Ilustracja dwuwarstwowej (, ) membrany (M): (C h, C m, C l stęŝenia roztworu; P h, P m, P l ciśnienia hydrostatyczne; J v strumień objętościowy; J s strumień substancji rozpuszczonej) [] FIG. 4. Graphic illustration of the double-layer (, ) membrane (M): (C h, C m, C l solution concentrations; P h, P m, P l hydrostatic pressures; J v volume flux; J s solute flux [] 2
Termodynamiczna ocena źródła entropii w układzie zawierającym dwuskładnikowy opatrunek membranowy
 andrzej Ślęzak Polimery w Medycynie 9, T. XXXIX, Nr Termodynamiczna ocena źródła entropii w układzie zawierającym dwuskładnikowy opatrunek membranowy Andrzej Ślęzak Katedra Zdrowia Publicznego Politechnika
andrzej Ślęzak Polimery w Medycynie 9, T. XXXIX, Nr Termodynamiczna ocena źródła entropii w układzie zawierającym dwuskładnikowy opatrunek membranowy Andrzej Ślęzak Katedra Zdrowia Publicznego Politechnika
Determination of thickness of concentration boundary layers for ternary electrolyte solutions and polymeric membrane
 Polimery w Medycynie 00, T. 0, Nr Wyznaczanie grubości stężeniowych warstw granicznych dla wieloskładnikowych roztworów elektrolitów i membrany polimerowej Jolanta Jasik-Ślęzak, Andrzej Ślęzak Katedra
Polimery w Medycynie 00, T. 0, Nr Wyznaczanie grubości stężeniowych warstw granicznych dla wieloskładnikowych roztworów elektrolitów i membrany polimerowej Jolanta Jasik-Ślęzak, Andrzej Ślęzak Katedra
Model matematyczny transportu roztworów substancji dysocjujących przez membranę polimerową z polaryzacją stężeniową
 Model matematyczny transportu roztworów substancji dysocjujących przez membranę polimerową z polaryzacją stężeniową JOLANTA JASIK-ŚLĘZAK, ANDRZEJ ŚLĘZAK Katedra Zdrowia Publicznego, Wydział Zarządzania
Model matematyczny transportu roztworów substancji dysocjujących przez membranę polimerową z polaryzacją stężeniową JOLANTA JASIK-ŚLĘZAK, ANDRZEJ ŚLĘZAK Katedra Zdrowia Publicznego, Wydział Zarządzania
Ciśnieniowe zależności grubości. Mechanical pressure dependencies of the concentration boundary layers for polymeric membrane
 Jolanta Jasik-Ślęzak i inni Polimery w Medycynie 2010, T. 40, Nr 1 Ciśnieniowe zależności grubości stężeniowych warstw granicznych dla membran polimerowych Mechanical pressure dependencies of the concentration
Jolanta Jasik-Ślęzak i inni Polimery w Medycynie 2010, T. 40, Nr 1 Ciśnieniowe zależności grubości stężeniowych warstw granicznych dla membran polimerowych Mechanical pressure dependencies of the concentration
1. za pomocą pomiaru SEM (siła elektromotoryczna róŝnica potencjałów dwóch elektrod) i na podstawie wzoru wyznaczenie stęŝenia,
 Potencjometria Potencjometria instrumentalna metoda analityczna, wykorzystująca zaleŝność pomiędzy potencjałem elektrody wzorcowej, a aktywnością jonów lub cząstek w badanym roztworze (elektrody wskaźnikowej).
Potencjometria Potencjometria instrumentalna metoda analityczna, wykorzystująca zaleŝność pomiędzy potencjałem elektrody wzorcowej, a aktywnością jonów lub cząstek w badanym roztworze (elektrody wskaźnikowej).
Sieciowa postać równań Kedem-Katchalsky ego dla ternarnych roztworów nieelektrolitów. 1. Ocena współczynników Peusnera R ij membrany polimerowej
 praca doświadczalna Polim. Med. 03, 43,, 93 0 ISSN 0370 0747 opyright by Wroclaw Medical University Kornelia M. Batko, Izabella Ślęzak-Prochazka, Andrzej Ślęzak 3 Sieciowa postać równań Kedem-Katchalsky
praca doświadczalna Polim. Med. 03, 43,, 93 0 ISSN 0370 0747 opyright by Wroclaw Medical University Kornelia M. Batko, Izabella Ślęzak-Prochazka, Andrzej Ślęzak 3 Sieciowa postać równań Kedem-Katchalsky
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ
 LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N 7 PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ . Cel ćwiczenia Doświadczalne i teoretyczne wyznaczenie profilu prędkości w rurze prostoosiowej 2. Podstawy teoretyczne:
LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N 7 PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ . Cel ćwiczenia Doświadczalne i teoretyczne wyznaczenie profilu prędkości w rurze prostoosiowej 2. Podstawy teoretyczne:
A4.05 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.05 nstrukcja wykonania ćwiczenia Wyznaczanie współczynników aktywności soli trudno rozpuszczalnej metodą pomiaru rozpuszczalności Zakres zagadnień obowiązujących
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.05 nstrukcja wykonania ćwiczenia Wyznaczanie współczynników aktywności soli trudno rozpuszczalnej metodą pomiaru rozpuszczalności Zakres zagadnień obowiązujących
ZARYS LINIOWEJ TERMODYNAMIKI NIERÓWNOWAGOWEJ UKŁADÓW CIĄGŁYCH I MEMBRANOWYCH
 UNIWERSYTET MIKO AJA KOPERNIKA JÓZEF CEYNOWA ZARYS LINIOWEJ TERMODYNAMIKI NIERÓWNOWAGOWEJ UKŁADÓW CIĄGŁYCH I MEMBRANOWYCH TORUŃ 1997 Recenzenci Bogdan Baranowski, Maciej Leszko ISBN 83-231-0808-0 Printed
UNIWERSYTET MIKO AJA KOPERNIKA JÓZEF CEYNOWA ZARYS LINIOWEJ TERMODYNAMIKI NIERÓWNOWAGOWEJ UKŁADÓW CIĄGŁYCH I MEMBRANOWYCH TORUŃ 1997 Recenzenci Bogdan Baranowski, Maciej Leszko ISBN 83-231-0808-0 Printed
AUTOMATYKA I POMIARY LABORATORIUM - ĆWICZENIE NR 13 WŁAŚCIWOŚCI METROLOGICZNE POTENCJOMETRYCZNYCH CZUJNIKÓW GAZOWYCH
 AUTOMATYKA I POMIARY LABORATORIUM - ĆWICZENIE NR 13 WŁAŚCIWOŚCI METROLOGICZNE POTENCJOMETRYCZNYCH CZUJNIKÓW GAZOWYCH Występowanie dwutlenku węgla w atmosferze i powolny wzrost jego stęŝenia jest główną
AUTOMATYKA I POMIARY LABORATORIUM - ĆWICZENIE NR 13 WŁAŚCIWOŚCI METROLOGICZNE POTENCJOMETRYCZNYCH CZUJNIKÓW GAZOWYCH Występowanie dwutlenku węgla w atmosferze i powolny wzrost jego stęŝenia jest główną
WYZNACZANIE STAŁEJ DYSOCJACJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII ABSORPCYJNEJ
 Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW.
 RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW. Zagadnienia: Zjawisko dysocjacji: stała i stopień dysocjacji Elektrolity słabe i mocne Efekt wspólnego jonu Reakcje strącania osadów Iloczyn rozpuszczalności Odczynnik
RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW. Zagadnienia: Zjawisko dysocjacji: stała i stopień dysocjacji Elektrolity słabe i mocne Efekt wspólnego jonu Reakcje strącania osadów Iloczyn rozpuszczalności Odczynnik
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Wyznaczanie lepkości wodnych roztworów sacharozy. opracowała dr A. Kacperska
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie lepkości wodnych roztworów sacharozy opracowała dr A. Kacperska ćwiczenie nr 20 Zakres zagadnień obowiązujących do ćwiczenia 1. Oddziaływania
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie lepkości wodnych roztworów sacharozy opracowała dr A. Kacperska ćwiczenie nr 20 Zakres zagadnień obowiązujących do ćwiczenia 1. Oddziaływania
Ocena natężenia źródła S-entropii w układzie membranowym spolaryzowanym stężeniowo
 Ann. Acad. Med. Siles. (online 017; 71: 46 54 eissn 1734-05X DOI:10.18794/aams/699 PRAA ORYGINALNA ORIGINAL PAPER Ocena natężenia źródła S-entropii w układzie membranowym spolaryzowanym stężeniowo Evaluation
Ann. Acad. Med. Siles. (online 017; 71: 46 54 eissn 1734-05X DOI:10.18794/aams/699 PRAA ORYGINALNA ORIGINAL PAPER Ocena natężenia źródła S-entropii w układzie membranowym spolaryzowanym stężeniowo Evaluation
WZBOGACANIE BIOGAZU W METAN W KASKADZIE MODUŁÓW MEMBRANOWYCH
 biogaz, wzbogacanie biogazu separacja membranowa Andrzej G. CHMIELEWSKI *, Marian HARASIMOWICZ *, Jacek PALIGE *, Agata URBANIAK **, Otton ROUBINEK *, Katarzyna WAWRYNIUK *, Michał ZALEWSKI * WZBOGACANIE
biogaz, wzbogacanie biogazu separacja membranowa Andrzej G. CHMIELEWSKI *, Marian HARASIMOWICZ *, Jacek PALIGE *, Agata URBANIAK **, Otton ROUBINEK *, Katarzyna WAWRYNIUK *, Michał ZALEWSKI * WZBOGACANIE
Stopień wyekstrahowania w układzie ciecz ciecz
 Wojciech Skrzypiński 1. Wprowadzenie Stopień wyekstrahowania w układzie ciecz ciecz W najprostszym przypadku proces ekstrakcji polega na usuwaniu jednego ze składników ciekłej mieszaniny dwuskładnikowej
Wojciech Skrzypiński 1. Wprowadzenie Stopień wyekstrahowania w układzie ciecz ciecz W najprostszym przypadku proces ekstrakcji polega na usuwaniu jednego ze składników ciekłej mieszaniny dwuskładnikowej
WPŁYW PROCESU TARCIA NA ZMIANĘ MIKROTWARDOŚCI WARSTWY WIERZCHNIEJ MATERIAŁÓW POLIMEROWYCH
 WOJCIECH WIELEBA WPŁYW PROCESU TARCIA NA ZMIANĘ MIKROTWARDOŚCI WARSTWY WIERZCHNIEJ MATERIAŁÓW POLIMEROWYCH THE INFLUENCE OF FRICTION PROCESS FOR CHANGE OF MICROHARDNESS OF SURFACE LAYER IN POLYMERIC MATERIALS
WOJCIECH WIELEBA WPŁYW PROCESU TARCIA NA ZMIANĘ MIKROTWARDOŚCI WARSTWY WIERZCHNIEJ MATERIAŁÓW POLIMEROWYCH THE INFLUENCE OF FRICTION PROCESS FOR CHANGE OF MICROHARDNESS OF SURFACE LAYER IN POLYMERIC MATERIALS
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Lepkościowo średnia masa cząsteczkowa polimeru. opiekun ćwiczenia: dr A.
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Lepkościowo średnia masa cząsteczkowa polimeru ćwiczenie nr 21 opiekun ćwiczenia: dr A. Kacperska Zakres zagadnień obowiązujących do ćwiczenia 1. Związki
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Lepkościowo średnia masa cząsteczkowa polimeru ćwiczenie nr 21 opiekun ćwiczenia: dr A. Kacperska Zakres zagadnień obowiązujących do ćwiczenia 1. Związki
TRANSPORT NIEELEKTROLITÓW PRZEZ BŁONY WYZNACZANIE WSPÓŁCZYNNIKA PRZEPUSZCZALNOŚCI
 Ćwiczenie nr 7 TRANSPORT NIEELEKTROLITÓW PRZEZ BŁONY WYZNACZANIE WSPÓŁCZYNNIKA PRZEPUSZCZALNOŚCI Celem ćwiczenia jest zapoznanie się z podstawami teorii procesów transportu nieelektrolitów przez błony.
Ćwiczenie nr 7 TRANSPORT NIEELEKTROLITÓW PRZEZ BŁONY WYZNACZANIE WSPÓŁCZYNNIKA PRZEPUSZCZALNOŚCI Celem ćwiczenia jest zapoznanie się z podstawami teorii procesów transportu nieelektrolitów przez błony.
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii
 Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali
 Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
Stężeniowe zależności współczynników Peusnera W ij dla ternarnych roztworów nieelektrolitów
 PRACE ORYGINALNE Polim. Med. 04, 44, 3, 79 87 ISSN 0370-0747 Copyright by roclaw Medical University Jolanta Jasik-Ślęzak, A E, Andrzej Ślęzak, A F Stężeniowe zależności współczynników Peusnera ij dla ternarnych
PRACE ORYGINALNE Polim. Med. 04, 44, 3, 79 87 ISSN 0370-0747 Copyright by roclaw Medical University Jolanta Jasik-Ślęzak, A E, Andrzej Ślęzak, A F Stężeniowe zależności współczynników Peusnera ij dla ternarnych
KONDUKTOMETRIA. Konduktometria. Przewodnictwo elektrolityczne. Przewodnictwo elektrolityczne zaleŝy od:
 KONDUKTOMETRIA Konduktometria Metoda elektroanalityczna oparta na pomiarze przewodnictwa elektrolitycznego, którego wartość ulega zmianie wraz ze zmianą stęŝenia jonów zawartych w roztworze. Przewodnictwo
KONDUKTOMETRIA Konduktometria Metoda elektroanalityczna oparta na pomiarze przewodnictwa elektrolitycznego, którego wartość ulega zmianie wraz ze zmianą stęŝenia jonów zawartych w roztworze. Przewodnictwo
POLITECHNIKA WARSZAWSKA WYDZIAŁ ELEKTRYCZNY. PRACOWNIA MATERIAŁOZNAWSTWA ELEKTROTECHNICZNEGO KWNiAE
 POLITECHNIK WRSZWSK WYDZIŁ ELEKTRYCZNY PRCOWNI MTERIŁOZNWSTW ELEKTROTECHNICZNEGO KWNiE ĆWICZENIE 11 WYZNCZNIE ELEKTROCHEMICZNEGO RÓWNOWśNIK MIEDZI ORZ STŁEJ FRDY 1. Elektrolity i przewodnictwo jonowe Ogólnie
POLITECHNIK WRSZWSK WYDZIŁ ELEKTRYCZNY PRCOWNI MTERIŁOZNWSTW ELEKTROTECHNICZNEGO KWNiE ĆWICZENIE 11 WYZNCZNIE ELEKTROCHEMICZNEGO RÓWNOWśNIK MIEDZI ORZ STŁEJ FRDY 1. Elektrolity i przewodnictwo jonowe Ogólnie
FIZYKA Publikacje dotyczące edukacji, oświaty i fizyki
 FIZYKA Publikacje dotyczące edukacji, oświaty i fizyki Zespół Szkół Ponadgimnazjalnych i Placówek Opiekuńczo-Wychowawczych Nr 3 w Piotrków Trybunalskim Brak wody może być najważniejszą kwestią, z którą
FIZYKA Publikacje dotyczące edukacji, oświaty i fizyki Zespół Szkół Ponadgimnazjalnych i Placówek Opiekuńczo-Wychowawczych Nr 3 w Piotrków Trybunalskim Brak wody może być najważniejszą kwestią, z którą
Akademickie Centrum Czystej Energii. Ogniwo paliwowe
 Ogniwo paliwowe 1. Zagadnienia elektroliza, prawo Faraday a, pierwiastki galwaniczne, ogniwo paliwowe 2. Opis Główną częścią ogniwa paliwowego PEM (Proton Exchange Membrane) jest membrana złożona z katody
Ogniwo paliwowe 1. Zagadnienia elektroliza, prawo Faraday a, pierwiastki galwaniczne, ogniwo paliwowe 2. Opis Główną częścią ogniwa paliwowego PEM (Proton Exchange Membrane) jest membrana złożona z katody
Przyspiesza dynamikę procesu leczenia rany Skuteczny i prosty schemat terapeutyczny
 Przyspiesza dynamikę procesu leczenia rany Skuteczny i prosty schemat terapeutyczny Skuteczny i prosty schemat terapeutyczny Innowacyjne leczenie problematycznych ran w środowisku wilgotnym Uniwersalny
Przyspiesza dynamikę procesu leczenia rany Skuteczny i prosty schemat terapeutyczny Skuteczny i prosty schemat terapeutyczny Innowacyjne leczenie problematycznych ran w środowisku wilgotnym Uniwersalny
Katedra Inżynierii Materiałowej
 Katedra Inżynierii Materiałowej Instrukcja do ćwiczenia z Biomateriałów Polaryzacyjne badania korozyjne mgr inż. Magdalena Jażdżewska Gdańsk 2010 Korozyjne charakterystyki stałoprądowe (zależności potencjał
Katedra Inżynierii Materiałowej Instrukcja do ćwiczenia z Biomateriałów Polaryzacyjne badania korozyjne mgr inż. Magdalena Jażdżewska Gdańsk 2010 Korozyjne charakterystyki stałoprądowe (zależności potencjał
Podstawowe pojęcia 1
 Tomasz Lubera Półogniwo Podstawowe pojęcia 1 układ złożony z min. dwóch faz pozostających ze sobą w kontakcie, w którym w wyniku zachodzących procesów utleniania lub redukcji ustala się stan równowagi,
Tomasz Lubera Półogniwo Podstawowe pojęcia 1 układ złożony z min. dwóch faz pozostających ze sobą w kontakcie, w którym w wyniku zachodzących procesów utleniania lub redukcji ustala się stan równowagi,
WSPÓŁCZYNNIK GOTOWOŚCI SYSTEMU LOKOMOTYW SPALINOWYCH SERII SM48
 TECHNIKA TRANSPORTU SZYNOWEGO Andrzej MACIEJCZYK, Zbigniew ZDZIENNICKI WSPÓŁCZYNNIK GOTOWOŚCI SYSTEMU LOKOMOTYW SPALINOWYCH SERII SM48 Streszczenie W artykule wyznaczono współczynniki gotowości systemu
TECHNIKA TRANSPORTU SZYNOWEGO Andrzej MACIEJCZYK, Zbigniew ZDZIENNICKI WSPÓŁCZYNNIK GOTOWOŚCI SYSTEMU LOKOMOTYW SPALINOWYCH SERII SM48 Streszczenie W artykule wyznaczono współczynniki gotowości systemu
Utylizacja i neutralizacja odpadów Międzywydziałowe Studia Ochrony Środowiska
 Utylizacja i neutralizacja odpadów Międzywydziałowe Studia Ochrony Środowiska Instrukcja do Ćwiczenia 14 Zastosowanie metod membranowych w oczyszczaniu ścieków Opracowała dr Elżbieta Megiel Celem ćwiczenia
Utylizacja i neutralizacja odpadów Międzywydziałowe Studia Ochrony Środowiska Instrukcja do Ćwiczenia 14 Zastosowanie metod membranowych w oczyszczaniu ścieków Opracowała dr Elżbieta Megiel Celem ćwiczenia
n liczba moli elektronów E siła elektromotoryczna ogniwa F = en A stała Faradaya C/mol
 Zmiana entalpii swobodnej G podczas reakcji w której zachodzi przepływ elektronów jest pracą nieobjętościową i może być wyrażona jako iloczyn napięcie i ładunku. na przykład procesy oksydo-redukcyjne zachodzące
Zmiana entalpii swobodnej G podczas reakcji w której zachodzi przepływ elektronów jest pracą nieobjętościową i może być wyrażona jako iloczyn napięcie i ładunku. na przykład procesy oksydo-redukcyjne zachodzące
Wyznaczanie stałej szybkości reakcji wymiany jonowej
 Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II
 TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II Czas trwania testu 120 minut Informacje 1. Proszę sprawdzić czy arkusz zawiera 10 stron. Ewentualny brak należy zgłosić nauczycielowi. 2. Proszę rozwiązać
TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II Czas trwania testu 120 minut Informacje 1. Proszę sprawdzić czy arkusz zawiera 10 stron. Ewentualny brak należy zgłosić nauczycielowi. 2. Proszę rozwiązać
PRACOWNIA CHEMII. Wygaszanie fluorescencji (Fiz4)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
LABORATORIUM Z PODSTAW BIOFIZYKI ĆWICZENIE NR 4 1. CEL ĆWICZENIA
 1. CEL ĆWICZENIA Pomiar potencjału dyfuzyjnego roztworów o różnych stężeniach jonów oddzielonych membranami: półprzepuszczalną i jonoselektywną w funkcji ich stężenia. Wykorzystanie równania Nernsta do
1. CEL ĆWICZENIA Pomiar potencjału dyfuzyjnego roztworów o różnych stężeniach jonów oddzielonych membranami: półprzepuszczalną i jonoselektywną w funkcji ich stężenia. Wykorzystanie równania Nernsta do
ZALEŻNOŚĆ CIŚNIENIA KORZENIOWEGO OD PRZEWODNOŚCI HYDRAULICZNEJ RADIALNYCH KORZENIOWYCH SZLAKÓW WODNYCH WEDLE MODELU KORZENIA JAKO MEMBRANY POROWATEJ
 ZAEŻNOŚĆ CIŚNIENIA KORZENIOWEGO OD PRZEWODNOŚCI HYDRAUICZNEJ RADIANYCH KORZENIOWYCH SZAKÓW WODNYCH WEDE MODEU KORZENIA JAKO MEMBRANY POROWATEJ Barbara Cisowska, Grażyna Suchanek, Marian Kargol Cisowska
ZAEŻNOŚĆ CIŚNIENIA KORZENIOWEGO OD PRZEWODNOŚCI HYDRAUICZNEJ RADIANYCH KORZENIOWYCH SZAKÓW WODNYCH WEDE MODEU KORZENIA JAKO MEMBRANY POROWATEJ Barbara Cisowska, Grażyna Suchanek, Marian Kargol Cisowska
Elektrochemia - prawa elektrolizy Faraday a. Zadania
 Elektrochemia - prawa elektrolizy Faraday a Zadania I prawo Faraday a Masa substancji wydzielonej na elektrodach podczas elektrolizy jest proporcjonalna do natężenia prądu i czasu trwania elektrolizy q
Elektrochemia - prawa elektrolizy Faraday a Zadania I prawo Faraday a Masa substancji wydzielonej na elektrodach podczas elektrolizy jest proporcjonalna do natężenia prądu i czasu trwania elektrolizy q
Potencjometryczna metoda oznaczania chlorków w wodach i ściekach z zastosowaniem elektrody jonoselektywnej
 Potencjometryczna metoda oznaczania chlorków w wodach i ściekach z zastosowaniem elektrody jonoselektywnej opracowanie: dr Jadwiga Zawada Cel ćwiczenia: poznanie podstaw teoretycznych i praktycznych metody
Potencjometryczna metoda oznaczania chlorków w wodach i ściekach z zastosowaniem elektrody jonoselektywnej opracowanie: dr Jadwiga Zawada Cel ćwiczenia: poznanie podstaw teoretycznych i praktycznych metody
Sieciowa postać równań Kedem-Katchalsky ego dla ternarnych roztworów nieelektrolitów. 6. Ocena współczynników Peusnera K ij membrany polimerowej
 prace oryginalne Polim. Med. 03, 43, 4, 77 95 ISSN 0370-0747 opyright by Wroclaw Medical University ornelia M. Batko, a e, Izabella Ślęzak-Prochazka, a e, Andrzej Ślęzak3, a f Sieciowa postać równań edem-atchalsky
prace oryginalne Polim. Med. 03, 43, 4, 77 95 ISSN 0370-0747 opyright by Wroclaw Medical University ornelia M. Batko, a e, Izabella Ślęzak-Prochazka, a e, Andrzej Ślęzak3, a f Sieciowa postać równań edem-atchalsky
Ćwiczenie 25. Piotr Skołuda OGNIWA STĘŻENIOWE
 Ćwiczenie 25 Piotr Skołuda OGNIWA STĘŻENIOWE Zagadnienia: Ogniwa stężeniowe z przenoszeniem i bez przenoszenia jonów. Ogniwa chemiczne, ze szczególnym uwzględnieniem ogniw wykorzystywanych w praktyce jako
Ćwiczenie 25 Piotr Skołuda OGNIWA STĘŻENIOWE Zagadnienia: Ogniwa stężeniowe z przenoszeniem i bez przenoszenia jonów. Ogniwa chemiczne, ze szczególnym uwzględnieniem ogniw wykorzystywanych w praktyce jako
ĆWICZENIE 16 Potencjały równowagowe elektrod siła elektromotoryczna ogniw.
 ĆWICZENIE 16 Potencjały równowagowe elektrod siła elektromotoryczna ogniw. Wprowadzenie: Przewodnik elektronowy (np. metal, grafit) zanurzony w elektrolicie (np. wodne roztwory soli, kwasów, zasad; stopiona
ĆWICZENIE 16 Potencjały równowagowe elektrod siła elektromotoryczna ogniw. Wprowadzenie: Przewodnik elektronowy (np. metal, grafit) zanurzony w elektrolicie (np. wodne roztwory soli, kwasów, zasad; stopiona
Wyznaczanie stałej i stopnia dysocjacji kwasu octowego i chlorooctowego
 Wyznaczanie stałej i stopnia dysocjacji kwasu octowego i chlorooctowego (opracowanie: Barbara Krajewska) Celem ćwiczenia jest: 1) wyznaczenie stałych dysocjacji K a dwóch słabych kwasów: octowego CH 3
Wyznaczanie stałej i stopnia dysocjacji kwasu octowego i chlorooctowego (opracowanie: Barbara Krajewska) Celem ćwiczenia jest: 1) wyznaczenie stałych dysocjacji K a dwóch słabych kwasów: octowego CH 3
EGZAMIN MATURALNY CHEMIA POZIOM ROZSZERZONY KRYTERIA OCENIANIA ODPOWIEDZI LUBLIN
 EGZAMIN MATURALNY EMIA PZIM RZSZERZNY KRYTERIA ENIANIA DPWIEDZI LUBLIN gólne zasady oceniania Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach.
EGZAMIN MATURALNY EMIA PZIM RZSZERZNY KRYTERIA ENIANIA DPWIEDZI LUBLIN gólne zasady oceniania Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach.
KOROZJA. Korozja kontaktowa z depolaryzacja tlenową 1
 KOROZJA Słowa kluczowe do ćwiczeń laboratoryjnych z korozji: korozja kontaktowa depolaryzacja tlenowa depolaryzacja wodorowa gęstość prądu korozyjnego natęŝenie prądu korozyjnego prawo Faradaya równowaŝnik
KOROZJA Słowa kluczowe do ćwiczeń laboratoryjnych z korozji: korozja kontaktowa depolaryzacja tlenowa depolaryzacja wodorowa gęstość prądu korozyjnego natęŝenie prądu korozyjnego prawo Faradaya równowaŝnik
Właściwości błony komórkowej
 Właściwości błony komórkowej płynność asymetria selektywna przepuszczalność Transport przez błony Współczynnik przepuszczalności [cm/s] RóŜnice składu jonowego między wnętrzem komórki ssaka a otoczeniem
Właściwości błony komórkowej płynność asymetria selektywna przepuszczalność Transport przez błony Współczynnik przepuszczalności [cm/s] RóŜnice składu jonowego między wnętrzem komórki ssaka a otoczeniem
Modelowanie reakcji chemicznych
 Modelowanie reakcji chemicznych Przykładowe ćwiczenia w Excelu i Modellusie 2007 IT for US Projekt jest finansowany przy wsparciu Komisji Europejskiej, nr grantu 119001-CP-1-2004-1-PL-COMENIUS-C21. Materiały
Modelowanie reakcji chemicznych Przykładowe ćwiczenia w Excelu i Modellusie 2007 IT for US Projekt jest finansowany przy wsparciu Komisji Europejskiej, nr grantu 119001-CP-1-2004-1-PL-COMENIUS-C21. Materiały
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Adsorpcja kwasu octowego na węglu aktywnym. opracowała dr hab. Małgorzata Jóźwiak
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Adsorpcja kwasu octowego na węglu aktywnym opracowała dr hab. Małgorzata Jóźwiak ćwiczenie nr Zakres zagadnień obowiązujących do ćwiczenia 1. Charakterystyka
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Adsorpcja kwasu octowego na węglu aktywnym opracowała dr hab. Małgorzata Jóźwiak ćwiczenie nr Zakres zagadnień obowiązujących do ćwiczenia 1. Charakterystyka
1.1 Przegląd wybranych równań i modeli fizycznych. , u x1 x 2
 Temat 1 Pojęcia podstawowe 1.1 Przegląd wybranych równań i modeli fizycznych Równaniem różniczkowym cząstkowym rzędu drugiego o n zmiennych niezależnych nazywamy równanie postaci gdzie u = u (x 1, x,...,
Temat 1 Pojęcia podstawowe 1.1 Przegląd wybranych równań i modeli fizycznych Równaniem różniczkowym cząstkowym rzędu drugiego o n zmiennych niezależnych nazywamy równanie postaci gdzie u = u (x 1, x,...,
Zastosowania Równania Bernoullego - zadania
 Zadanie 1 Przez zwężkę o średnicy D = 0,2 m, d = 0,05 m przepływa woda o temperaturze t = 50 C. Obliczyć jakie ciśnienie musi panować w przekroju 1-1, aby w przekroju 2-2 nie wystąpiło zjawisko kawitacji,
Zadanie 1 Przez zwężkę o średnicy D = 0,2 m, d = 0,05 m przepływa woda o temperaturze t = 50 C. Obliczyć jakie ciśnienie musi panować w przekroju 1-1, aby w przekroju 2-2 nie wystąpiło zjawisko kawitacji,
KONKURS CHEMICZNY,,ROK PRZED MATURĄ
 KONKURS CHEMICZNY,,ROK PRZED MATURĄ ROK SZKOLNY 2007/2008 ETAP SZKOLNY Numer kodowy Suma punktów: Podpisy Komisji: 1.... 2.... 3.... Informacje dla ucznia: 1. Arkusz zawiera 12 zadań. 2. Pisemnych odpowiedzi
KONKURS CHEMICZNY,,ROK PRZED MATURĄ ROK SZKOLNY 2007/2008 ETAP SZKOLNY Numer kodowy Suma punktów: Podpisy Komisji: 1.... 2.... 3.... Informacje dla ucznia: 1. Arkusz zawiera 12 zadań. 2. Pisemnych odpowiedzi
Właściwości błony komórkowej
 Właściwości błony komórkowej płynność asymetria selektywna przepuszczalność Transport przez błony Cząsteczki < 150Da Błony - selektywnie przepuszczalne RóŜnice składu jonowego między wnętrzem komórki ssaka
Właściwości błony komórkowej płynność asymetria selektywna przepuszczalność Transport przez błony Cząsteczki < 150Da Błony - selektywnie przepuszczalne RóŜnice składu jonowego między wnętrzem komórki ssaka
INSTYTUT INŻYNIERII ŚRODOWISKA ZAKŁAD GEOINŻYNIERII I REKULTYWACJI ĆWICZENIE NR 4 OKREŚLENIE WSPÓŁCZYNNIKA STRAT LOEKALNYCH
 INSTYTUT INŻYNIERII ŚRODOWISKA ZAKŁAD GEOINŻYNIERII I REKULTYWACJI Laboratorium z mechaniki płynów ĆWICZENIE NR 4 OKREŚLENIE WSPÓŁCZYNNIKA STRAT LOEKALNYCH . Cel ćwiczenia Celem ćwiczenia jest doświadczalne
INSTYTUT INŻYNIERII ŚRODOWISKA ZAKŁAD GEOINŻYNIERII I REKULTYWACJI Laboratorium z mechaniki płynów ĆWICZENIE NR 4 OKREŚLENIE WSPÓŁCZYNNIKA STRAT LOEKALNYCH . Cel ćwiczenia Celem ćwiczenia jest doświadczalne
Straty energii podczas przepływu wody przez rurociąg
 1. Wprowadzenie Ć w i c z e n i e 11 Straty energii podczas przepływu wody przez rurociąg Celem ćwiczenia jest praktyczne wyznaczenie współczynników strat liniowych i miejscowych podczas przepływu wody
1. Wprowadzenie Ć w i c z e n i e 11 Straty energii podczas przepływu wody przez rurociąg Celem ćwiczenia jest praktyczne wyznaczenie współczynników strat liniowych i miejscowych podczas przepływu wody
Laboratorium Podstaw Biofizyki Pomiar potencjału dyfuzyjnego i błonowego 4
 CEL ĆWICZENIA Pomiar potencjału dyfuzyjnego roztworów o różnych stężeniach jonów oddzielonych membranami: półprzepuszczalną i jonoselektywną w funkcji ich stężenia. Wykorzystanie równania Nernsta do wyznaczenia
CEL ĆWICZENIA Pomiar potencjału dyfuzyjnego roztworów o różnych stężeniach jonów oddzielonych membranami: półprzepuszczalną i jonoselektywną w funkcji ich stężenia. Wykorzystanie równania Nernsta do wyznaczenia
Ćwiczenie 2. Charakteryzacja niskotemperaturowego czujnika tlenu. (na prawach rękopisu)
 Ćwiczenie 2. Charakteryzacja niskotemperaturowego czujnika tlenu (na prawach rękopisu) W analityce procesowej istotne jest określenie stężeń rozpuszczonych w cieczach gazów. Gazy rozpuszczają się w cieczach
Ćwiczenie 2. Charakteryzacja niskotemperaturowego czujnika tlenu (na prawach rękopisu) W analityce procesowej istotne jest określenie stężeń rozpuszczonych w cieczach gazów. Gazy rozpuszczają się w cieczach
Właściwości błony komórkowej
 Właściwości błony komórkowej płynność asymetria selektywna przepuszczalność Glikokaliks glikokaliks cytoplazma jądro błona komórkowa Mikrografia elektronowa powierzchni limfocytu ludzkiego (wybarwienie
Właściwości błony komórkowej płynność asymetria selektywna przepuszczalność Glikokaliks glikokaliks cytoplazma jądro błona komórkowa Mikrografia elektronowa powierzchni limfocytu ludzkiego (wybarwienie
To jest. Ocena bardzo dobra [ ] energetycznych. s p d f. Ocena dobra [ ] izotopowym. atomowych Z. ,, d oraz f.
![To jest. Ocena bardzo dobra [ ] energetycznych. s p d f. Ocena dobra [ ] izotopowym. atomowych Z. ,, d oraz f. To jest. Ocena bardzo dobra [ ] energetycznych. s p d f. Ocena dobra [ ] izotopowym. atomowych Z. ,, d oraz f.](/thumbs/96/129580154.jpg) 34 Wymagania programowe To jest przyrodniczych,,,,, chemicznego na podstawie zapisu A Z E,,,, podaje masy atomowe pierwiastków chemicznych,, n,,,,, s, p, d oraz f przyrodniczych,,,,, oraz Z,,, d oraz f,,
34 Wymagania programowe To jest przyrodniczych,,,,, chemicznego na podstawie zapisu A Z E,,,, podaje masy atomowe pierwiastków chemicznych,, n,,,,, s, p, d oraz f przyrodniczych,,,,, oraz Z,,, d oraz f,,
WYZNACZENIE WSPÓŁCZYNNIKA OPORU LINIOWEGO PRZEPŁYWU LAMINARNEGO
 LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N 7 WYZNACZENIE WSPÓŁCZYNNIKA OPORU LINIOWEGO PRZEPŁYWU LAMINARNEGO 1. Cel ćwiczenia Doświadczalne wyznaczenie zaleŝności współczynnika oporu linioweo przepływu
LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N 7 WYZNACZENIE WSPÓŁCZYNNIKA OPORU LINIOWEGO PRZEPŁYWU LAMINARNEGO 1. Cel ćwiczenia Doświadczalne wyznaczenie zaleŝności współczynnika oporu linioweo przepływu
KONKURS PRZEDMIOTOWY Z CHEMII
 Pieczęć KONKURS PRZEDMIOTOWY Z CHEMII dla uczniów gimnazjów województwa lubuskiego 26 stycznia 2012 r. zawody II stopnia (rejonowe) Witamy Cię na drugim etapie Konkursu Chemicznego. Przed przystąpieniem
Pieczęć KONKURS PRZEDMIOTOWY Z CHEMII dla uczniów gimnazjów województwa lubuskiego 26 stycznia 2012 r. zawody II stopnia (rejonowe) Witamy Cię na drugim etapie Konkursu Chemicznego. Przed przystąpieniem
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
LABORATORIUM MECHANIKI PŁYNÓW. Ćwiczenie N 2 RÓWNOWAGA WZGLĘDNA W NACZYNIU WIRUJĄCYM WOKÓŁ OSI PIONOWEJ
 LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N RÓWNOWAGA WZGLĘDNA W NACZYNIU WIRUJĄCYM WOKÓŁ OSI PIONOWEJ . Cel ćwiczenia Pomiar współrzędnych powierzchni swobodnej w naczyniu cylindrycznym wirującym wokół
LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N RÓWNOWAGA WZGLĘDNA W NACZYNIU WIRUJĄCYM WOKÓŁ OSI PIONOWEJ . Cel ćwiczenia Pomiar współrzędnych powierzchni swobodnej w naczyniu cylindrycznym wirującym wokół
Seminarium 4 Obliczenia z wykorzystaniem przekształcania wzorów fizykochemicznych
 Seminarium 4 Obliczenia z wykorzystaniem przekształcania wzorów fizykochemicznych Zad. 1 Przekształć w odpowiedni sposób podane poniżej wzory aby wyliczyć: a) a lub m 2 b) m zred h E a 8ma E osc h 4 2
Seminarium 4 Obliczenia z wykorzystaniem przekształcania wzorów fizykochemicznych Zad. 1 Przekształć w odpowiedni sposób podane poniżej wzory aby wyliczyć: a) a lub m 2 b) m zred h E a 8ma E osc h 4 2
Metody Badań Składu Chemicznego
 Metody Badań Składu Chemicznego Wydział Inżynierii Materiałowej i Ceramiki Kierunek: Inżynieria Materiałowa (NIESTACJONARNE) Ćwiczenie 5: Pomiary SEM ogniwa - miareczkowanie potencjometryczne. Pomiary
Metody Badań Składu Chemicznego Wydział Inżynierii Materiałowej i Ceramiki Kierunek: Inżynieria Materiałowa (NIESTACJONARNE) Ćwiczenie 5: Pomiary SEM ogniwa - miareczkowanie potencjometryczne. Pomiary
wykład 6 elektorochemia
 elektorochemia Ogniwa elektrochemiczne Ogniwo elektrochemiczne składa się z dwóch elektrod będących w kontakcie z elektrolitem, który może być roztworem, cieczą lub ciałem stałym. Elektrolit wraz z zanurzona
elektorochemia Ogniwa elektrochemiczne Ogniwo elektrochemiczne składa się z dwóch elektrod będących w kontakcie z elektrolitem, który może być roztworem, cieczą lub ciałem stałym. Elektrolit wraz z zanurzona
POLITECHNIKA SZCZECIŃSKA INSTYTUT INŻYNIERII MATERIAŁOWEJ ZAKŁAD METALOZNAWSTWA I ODLEWNICTWA
 POLITECHNIKA SZCZECIŃSKA INSTYTUT INŻYNIERII MATERIAŁOWEJ ZAKŁAD METALOZNAWSTWA I ODLEWNICTWA PRZEDMIOT: KOROZJA I OCHRONA PRZED KOROZJĄ ĆWICZENIA LABORATORYJNE Temat ćwiczenia: OGNIWA GALWANICZNE Cel
POLITECHNIKA SZCZECIŃSKA INSTYTUT INŻYNIERII MATERIAŁOWEJ ZAKŁAD METALOZNAWSTWA I ODLEWNICTWA PRZEDMIOT: KOROZJA I OCHRONA PRZED KOROZJĄ ĆWICZENIA LABORATORYJNE Temat ćwiczenia: OGNIWA GALWANICZNE Cel
Modelowanie wektora magnetycznego serca na podstawie jonowych prądów komórkowych
 Modelowanie wektora magnetycznego serca na podstawie jonowych prądów komórkowych Wstęp Podstawy modelu komórkowego Proces pobudzenia serca Wektor magnetyczny serca MoŜliwości diagnostyczne Wstęp Przepływający
Modelowanie wektora magnetycznego serca na podstawie jonowych prądów komórkowych Wstęp Podstawy modelu komórkowego Proces pobudzenia serca Wektor magnetyczny serca MoŜliwości diagnostyczne Wstęp Przepływający
K05 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K05 Instrukcja wykonania ćwiczenia Wyznaczanie punktu izoelektrycznego żelatyny metodą wiskozymetryczną Zakres zagadnień obowiązujących do ćwiczenia 1. Układy
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K05 Instrukcja wykonania ćwiczenia Wyznaczanie punktu izoelektrycznego żelatyny metodą wiskozymetryczną Zakres zagadnień obowiązujących do ćwiczenia 1. Układy
Wykład 7. Anna Ptaszek. 13 września Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Fizykochemia biopolimerów - wykład 7.
 Wykład 7 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 13 września 2016 1 / 27 Układ wieloskładnikowy dwufazowy P woda 1 atm lód woda ciek a woda + substancja nielotna para wodna 0 0 100 T 2 / 27
Wykład 7 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 13 września 2016 1 / 27 Układ wieloskładnikowy dwufazowy P woda 1 atm lód woda ciek a woda + substancja nielotna para wodna 0 0 100 T 2 / 27
1.UKŁADY RÓWNAŃ LINIOWYCH
 UKŁADY RÓWNAŃ 1.UKŁADY RÓWNAŃ LINIOWYCH Układ: a1x + b1y = c1 a x + by = c nazywamy układem równań liniowych. Rozwiązaniem układu jest kaŝda para liczb spełniająca kaŝde z równań. Przy rozwiązywaniu układów
UKŁADY RÓWNAŃ 1.UKŁADY RÓWNAŃ LINIOWYCH Układ: a1x + b1y = c1 a x + by = c nazywamy układem równań liniowych. Rozwiązaniem układu jest kaŝda para liczb spełniająca kaŝde z równań. Przy rozwiązywaniu układów
Politechnika Warszawska. Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej
 Politechnika Warszawska Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej Instrukcja do ćwiczenia: SZYBKOŚĆ PRZEMIAN CHEMICZNYCH Opracowała: dr inŝ. Maria Bukowska Płock,
Politechnika Warszawska Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej Instrukcja do ćwiczenia: SZYBKOŚĆ PRZEMIAN CHEMICZNYCH Opracowała: dr inŝ. Maria Bukowska Płock,
WIROWANIE. 1. Wprowadzenie
 WIROWANIE 1. Wprowadzenie Rozdzielanie układów heterogonicznych w polu sił grawitacyjnych może być procesem długotrwałym i mało wydajnym. Sedymentacja może zostać znacznie przyspieszona, kiedy pole sił
WIROWANIE 1. Wprowadzenie Rozdzielanie układów heterogonicznych w polu sił grawitacyjnych może być procesem długotrwałym i mało wydajnym. Sedymentacja może zostać znacznie przyspieszona, kiedy pole sił
BIOTECHNOLOGIA. Materiały do ćwiczeń rachunkowych z chemii fizycznej kinetyka chemiczna, 2014/15
 Zadanie 1. BIOTECHNOLOGIA Materiały do ćwiczeń rachunkowych z chemii fizycznej kinetyka chemiczna, 014/15 W temperaturze 18 o C oporność naczyńka do pomiaru przewodności napełnionego 0,0 M wodnym roztworem
Zadanie 1. BIOTECHNOLOGIA Materiały do ćwiczeń rachunkowych z chemii fizycznej kinetyka chemiczna, 014/15 W temperaturze 18 o C oporność naczyńka do pomiaru przewodności napełnionego 0,0 M wodnym roztworem
Ćwiczenie N 13 ROZKŁAD CIŚNIENIA WZDŁUś ZWĘśKI VENTURIEGO
 LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N ROZKŁAD CIŚNIENIA WZDŁUś ZWĘśKI VENTURIEGO . Cel ćwiczenia Doświadczalne wyznaczenie rozkładu ciśnienia piezometrycznego w zwęŝce Venturiego i porównanie go z
LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N ROZKŁAD CIŚNIENIA WZDŁUś ZWĘśKI VENTURIEGO . Cel ćwiczenia Doświadczalne wyznaczenie rozkładu ciśnienia piezometrycznego w zwęŝce Venturiego i porównanie go z
1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej?
 Tematy opisowe 1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej? 2. Omów pomiar potencjału na granicy faz elektroda/roztwór elektrolitu. Podaj przykład, omów skale potencjału i elektrody
Tematy opisowe 1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej? 2. Omów pomiar potencjału na granicy faz elektroda/roztwór elektrolitu. Podaj przykład, omów skale potencjału i elektrody
K02 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K2 Instrukcja wykonania ćwiczenia Wyznaczanie krytycznego stężenia micelizacji (CMC) z pomiarów napięcia powierzchniowego Zakres zagadnień obowiązujących
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K2 Instrukcja wykonania ćwiczenia Wyznaczanie krytycznego stężenia micelizacji (CMC) z pomiarów napięcia powierzchniowego Zakres zagadnień obowiązujących
Granulowany Węgiel Aktywny z łupin orzechów kokosowych BT bitumiczny AT antracytowy
 Granulowany Węgiel Aktywny z łupin orzechów kokosowych BT bitumiczny AT antracytowy Granulowany Węgiel Aktywny GAC (GAC ang. Granular Activated Carbon) jest wysoce wydajnym medium filtracyjnym. Węgiel
Granulowany Węgiel Aktywny z łupin orzechów kokosowych BT bitumiczny AT antracytowy Granulowany Węgiel Aktywny GAC (GAC ang. Granular Activated Carbon) jest wysoce wydajnym medium filtracyjnym. Węgiel
W zaleŝności od charakteru i ilości cząstek wyróŝniamy: a. opadanie cząstek ziarnistych, b. opadanie cząstek kłaczkowatych.
 BADANIE PROCESU SEDYMENTACJI Wstęp teoretyczny. Sedymentacja, to proces opadania cząstek ciała stałego w cieczy, w wyniku działania siły grawitacji lub sił bezwładności. Zaistnienie róŝnicy gęstości ciała
BADANIE PROCESU SEDYMENTACJI Wstęp teoretyczny. Sedymentacja, to proces opadania cząstek ciała stałego w cieczy, w wyniku działania siły grawitacji lub sił bezwładności. Zaistnienie róŝnicy gęstości ciała
Zadania treningowe na kolokwium
 Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Równania prostych i krzywych; współrzędne punktu
 Równania prostych i krzywych; współrzędne punktu Zad 1: Na paraboli o równaniu y = 1 x znajdź punkt P leŝący najbliŝej prostej o równaniu x + y = 0 Napisz równanie stycznej do tej paraboli, poprowadzonej
Równania prostych i krzywych; współrzędne punktu Zad 1: Na paraboli o równaniu y = 1 x znajdź punkt P leŝący najbliŝej prostej o równaniu x + y = 0 Napisz równanie stycznej do tej paraboli, poprowadzonej
ODWRÓCONA OSMOZA. Separacja laktozy z permeatu mikrofiltracyjnego serwatki
 Wrocław, 01.12.16 ODWRÓCONA OSMOZA Separacja laktozy z permeatu mikrofiltracyjnego serwatki 1. OPIS PROCESU Podstawowym elementem odróżniającym procesy osmozy od ultrafiltracji są znacznie mniejsze rozmiary
Wrocław, 01.12.16 ODWRÓCONA OSMOZA Separacja laktozy z permeatu mikrofiltracyjnego serwatki 1. OPIS PROCESU Podstawowym elementem odróżniającym procesy osmozy od ultrafiltracji są znacznie mniejsze rozmiary
Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ
 Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
WYZNACZANIE WSPÓŁCZYNNIKÓW DYFUZJI I PERMEACJI DLA MEMBRAN TYPU MIXED MATRIX
 WYZNACZANIE WSPÓŁCZYNNIKÓW DYFUZJI I PERMEACJI DLA MEMBRAN TYPU MIXED MATRIX Maciej Szwast 1, Michał Zalewski 1, Daniel Polak 1 1. Wydział Inżynierii Chemicznej i Procesowej, Politechnika Warszawska, ul.
WYZNACZANIE WSPÓŁCZYNNIKÓW DYFUZJI I PERMEACJI DLA MEMBRAN TYPU MIXED MATRIX Maciej Szwast 1, Michał Zalewski 1, Daniel Polak 1 1. Wydział Inżynierii Chemicznej i Procesowej, Politechnika Warszawska, ul.
Roztwory. Homogeniczne jednorodne (jedno-fazowe) mieszaniny dwóch lub więcej składników.
 Roztwory Homogeniczne jednorodne (jedno-fazowe) mieszaniny dwóch lub więcej składników. Własności fizyczne roztworów są związane z równowagę pomiędzy siłami wiążącymi cząsteczki wody i substancji rozpuszczonej.
Roztwory Homogeniczne jednorodne (jedno-fazowe) mieszaniny dwóch lub więcej składników. Własności fizyczne roztworów są związane z równowagę pomiędzy siłami wiążącymi cząsteczki wody i substancji rozpuszczonej.
Ć W I C Z E N I E 5. Kinetyka cementacji metali
 Ć W I C Z E N I E Kinetyka cementacji metali WPROWADZENIE Proces cementacji jest jednym ze sposobów wydzielania metali z roztworów wodnych. Polega on na wytrącaniu jonów metalu bardziej szlachetnego przez
Ć W I C Z E N I E Kinetyka cementacji metali WPROWADZENIE Proces cementacji jest jednym ze sposobów wydzielania metali z roztworów wodnych. Polega on na wytrącaniu jonów metalu bardziej szlachetnego przez
(13) B1 (12) OPIS PATENTOWY (19) PL (11) PL B1 B01D 63/00
 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 175490 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 306490 (22) Data zgłoszenia: 21.12.1994 (51) IntCl6: B01D 61/36 B01D
RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 175490 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 306490 (22) Data zgłoszenia: 21.12.1994 (51) IntCl6: B01D 61/36 B01D
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
Zadanie ChemCad - Batch Reaktor
 Zadanie ChemCad - Batch Reaktor Opracowanie: dr inŝ. E.Wolak Treść zadania: Octan sodu powstaje w wyniku reakcji: NaOH + C2 H5COOCH3 C2H5OH + CH3COONa Wodorotlenek sodu i octan etylu zasilają reaktor okresowy
Zadanie ChemCad - Batch Reaktor Opracowanie: dr inŝ. E.Wolak Treść zadania: Octan sodu powstaje w wyniku reakcji: NaOH + C2 H5COOCH3 C2H5OH + CH3COONa Wodorotlenek sodu i octan etylu zasilają reaktor okresowy
Układy równań liniowych. Ax = b (1)
 Układy równań liniowych Dany jest układ m równań z n niewiadomymi. Liczba równań m nie musi być równa liczbie niewiadomych n, tj. mn. a a... a b n n a a... a b n n... a a... a b m m mn n m
Układy równań liniowych Dany jest układ m równań z n niewiadomymi. Liczba równań m nie musi być równa liczbie niewiadomych n, tj. mn. a a... a b n n a a... a b n n... a a... a b m m mn n m
... kod ucznia Małopolski Konkurs Chemiczny dla Gimnazjalistów
 ... kod ucznia Małopolski Konkurs Chemiczny dla Gimnazjalistów Etap I (szkolny) 21 listopada 2008 roku PoniŜej podano treść pięciu zadań, za rozwiązanie których moŝesz uzyskać 50 punktów. Rozwiązania i
... kod ucznia Małopolski Konkurs Chemiczny dla Gimnazjalistów Etap I (szkolny) 21 listopada 2008 roku PoniŜej podano treść pięciu zadań, za rozwiązanie których moŝesz uzyskać 50 punktów. Rozwiązania i
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Ćw. 5 Absorpcjometria I
 Ćw. 5 Absorpcjometria I Absorpcja promieniowania elektromagnetycznego z obszaru widzialnego i nadfioletowego przez atomy i cząsteczki powoduje zmianę ich stanu elektronowego. Zjawiska te moŝna badać za
Ćw. 5 Absorpcjometria I Absorpcja promieniowania elektromagnetycznego z obszaru widzialnego i nadfioletowego przez atomy i cząsteczki powoduje zmianę ich stanu elektronowego. Zjawiska te moŝna badać za
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 ZALEŻNOŚĆ STAŁEJ SZYBKOŚCI REAKCJI OD TEMPERATURY WSTĘP Szybkość reakcji drugiego rzędu: A + B C (1) zależy od stężenia substratów A oraz B v = k [A][B] (2) Gdy jednym z reagentów jest rozpuszczalnik (np.
ZALEŻNOŚĆ STAŁEJ SZYBKOŚCI REAKCJI OD TEMPERATURY WSTĘP Szybkość reakcji drugiego rzędu: A + B C (1) zależy od stężenia substratów A oraz B v = k [A][B] (2) Gdy jednym z reagentów jest rozpuszczalnik (np.
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów. 07 marca 2019 r. zawody III stopnia (wojewódzkie) Schemat punktowania zadań
 Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 07 marca 2019 r. zawody III stopnia (wojewódzkie) Schemat punktowania zadań Maksymalna liczba punktów 40. 90% 36 pkt. Uwaga! 1. Wszystkie
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 07 marca 2019 r. zawody III stopnia (wojewódzkie) Schemat punktowania zadań Maksymalna liczba punktów 40. 90% 36 pkt. Uwaga! 1. Wszystkie
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW
 WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
Schemat ogniwa:... Równanie reakcji:...
 Zadanie 1. Wykorzystując dane z szeregu elektrochemicznego metali napisz schemat ogniwa, w którym elektroda cynkowa pełni rolę anody. Zapisz równanie reakcji zachodzącej w półogniwie cynkowym. Schemat
Zadanie 1. Wykorzystując dane z szeregu elektrochemicznego metali napisz schemat ogniwa, w którym elektroda cynkowa pełni rolę anody. Zapisz równanie reakcji zachodzącej w półogniwie cynkowym. Schemat
Szkło. T g szkła używanego w oknach katedr wynosi ok. 600 C, a czas relaksacji sięga lat. FIZYKA 3 MICHAŁ MARZANTOWICZ
 Szkło Przechłodzona ciecz, w której ruchy uległy zamrożeniu Tzw. przejście szkliste: czas potrzebny na zmianę konfiguracji cząsteczek (czas relaksacji) jest rzędu minut lub dłuższy T g szkła używanego
Szkło Przechłodzona ciecz, w której ruchy uległy zamrożeniu Tzw. przejście szkliste: czas potrzebny na zmianę konfiguracji cząsteczek (czas relaksacji) jest rzędu minut lub dłuższy T g szkła używanego
LABORATORIUM MECHANIKI PŁYNÓW
 Ćwiczenie numer Pomiar współczynnika oporu liniowego 1. Wprowadzenie Stanowisko służy do analizy zjawiska liniowych strat energii podczas przepływu laminarnego i turbulentnego przez rurociąg mosiężny o
Ćwiczenie numer Pomiar współczynnika oporu liniowego 1. Wprowadzenie Stanowisko służy do analizy zjawiska liniowych strat energii podczas przepływu laminarnego i turbulentnego przez rurociąg mosiężny o
