Materiały wybuchowe. Katarzyna Machnikowska
|
|
|
- Wiktoria Aleksandra Wolska
- 6 lat temu
- Przeglądów:
Transkrypt
1 Materiały wybuchowe Katarzyna Machnikowska
2 Najpopularniejsze materiały wybuchowe Wybuch Trotyl Karbonit Podział materiałów wybuchowych Dynamit Eksplozje chemiczne Piorunian rtęci Proch Bomba Granat ręczny Oktogen
3 TNT, trotyl (trinitrotoluen); HMX, oktogen (środek wybuchowy Jego Wysokości); RDX, heksogen (środek wybuchowy ośrodka badawczego), preparowany z woskami lub syntetycznymi polimerami (plastikowe materiały wybuchowe), stosowany przez terrorystów.
4 Wybuch gwałtowne wydzielenie dużych ilości energii, któremu towarzyszy zwykle nagły wzrost temperatury i ciśnienia oraz emisja promieniowania i fal akustycznych. Wybuchy są spowodowane: *przebiegiem szybkich egzotermicznych reakcji chemicznych *gwałtownymi zjawiskami fizycznymi
5 Trotyl - TNT (NO 2 ) 3 C 6 H 2 CH 3 organiczny związek chemiczny, stosowany jako kruszący materiał wybuchowy. Otrzymuję się go poprzez dwustopniowe nitrowanie toluenu, mieszaniną kwasu siarkowego i azotowego. Jako materiał wybuchowy jest trwały, mało wrażliwy na uderzenie, tarcie i ma wysoką temperaturę wymaganą do zainicjowania wybuchu.
6 Karbonit materiał wybuchowy amonowo saletrzany, stosowany w kopalniach węglowych, w których występuje pył węglowy. Skład karbonitu: -Nitrogliceryna (C 3 H 5 (ONO 2 ) 3 ) -Azotan amonu NH 4 NO 3 -Trotyl (CH 3 -C 6 H 2 -(NO 2 ) 3 ) -Chlorek sodu NaCl -Mączka drzewna
7 Inicjujące np. piorunian rtęci, służą do zapoczątkowania reakcji w materiałach o mniejszej podatności na bodźce lub do wywołania reakcji w jakiś szczególny sposób Kruszące np. trotyl, jest to materiał o największej sile działania Miotające np. proch czarny, materiał stosunkowo powoli wybuchający, służy do napędzania broni palnej bezpieczne - materiały, którym podczas wybuchu nie towarzyszy płomień Masy pirotechniczne służą do wywoływania różnych efektów np. huku, błysku oraz dużej ilości dymu
8 Dynamit materiał wybuchowy wynaleziony przez Alfreda Nobla. Dynamit jest materiałem, który podczas wybuchu wydziela mniej energii niż czysta nitrogliceryna, jednakże jest znacznie odporniejszy na wstrząsy i uderzenia. Jest stosowany głównie do kruszenia tworów geologicznych oraz budynków, ma też zastosowania militarne.
9 Eksplozje chemiczne charakteryzują się sontanicznym rozerwaniem cząsteczek, które rekombinując, dają głównie gazowe produkty (N 2, H 2 O, CO 2 ). Schemat eksplozji
10 Piorunian rtęci zaliczany jest do materiałów wybuchowych inicjujących. Jest związkiem nieorganicznym, trudno rozpuszczalnym w wodzie, ale rozpuszczalny w stężonej wodzie amoniakalnej. Wybucha przez uderzenie, potarcie, iskrę, nakłucie, ogrzanie itd. Produkcja piorunianu rtęci, składa się z dwóch etapów: Powstawanie azotanu rtęci, Synteza piorunianu rtęci.
11 Proch czarny (dymny) jest najstarszym materiałem wybuchowym. Proch czarny używany był jako materiał wybuchowy miotający, a także materiał wybuchowy kruszący. Rodzaje prochu: *proch czarny (proch dymny) *proch chloranowy *proch bezdymny *proch nitrocelulozowy *proch nitroglicerynowy *proch nitroglikolowy *balisty *bezbłyskowy proch bezdymny
12 Bomba broń w postaci ładunku materiału wybuchowego. Służy przede wszystkim do niszczenia obiektów siłą energii wybuchu, rażąc odłamkami lub wywołując pożar. Rodzaje bomb: *atomowo *elektromagnetyczna *głębinowa *kasetowa *lotnicza *paliwo-powietrzna
13 Granat ręczny jest pociskiem wyrzucanym ręcznie, wypełniony materiałem wybuchowym, substancją dymotwórczą lub inną substancją. Wyposażony jest w zapalnik czasowy lub uderzeniowy. Granaty ręczne dzielimy na: *zaczepne *obronne *uniwersalne *ćwiczebne
14 Oktogen jest prawie najsilniejszym ze wszystkich znanych obecnie kruszących materiałów wybuchowych. Jedną z dwóch metod otrzymywanie oktogenu jest metoda polegająca na nitrolizie urotropiny roztworem azotanem amonu w kwasie azotowym, w obecności kwasu octowego, bezwodnika kwasu octowego i trioksanu (trimeru formaldehydu).
15 Wzór sumaryczny C4H8N8O8
16 Grafiki: Google grafika
17 Opiekun: Przemysław Ziemiński Akademickie Liceum Mistrzostwa Sportowego Lublin, ul. Projektowa 4
Technologie Materiałowe II Spajanie materiałów
 KATEDRA INŻYNIERII MATERIAŁOWEJ I SPAJANIA ZAKŁAD INŻYNIERII SPAJANIA Technologie Materiałowe II Spajanie materiałów Wykład 11 Zgrzewanie metali dr inż. Dariusz Fydrych Kierunek studiów: Inżynieria Materiałowa
KATEDRA INŻYNIERII MATERIAŁOWEJ I SPAJANIA ZAKŁAD INŻYNIERII SPAJANIA Technologie Materiałowe II Spajanie materiałów Wykład 11 Zgrzewanie metali dr inż. Dariusz Fydrych Kierunek studiów: Inżynieria Materiałowa
Politechnika Gdańska realizuje projekt dofinansowany z Funduszy Europejskich Zintegrowany Program Rozwoju Politechniki Gdańskiej
 Politechnika Gdańska realizuje projekt dofinansowany z Funduszy Europejskich Zintegrowany Program Rozwoju Politechniki Gdańskiej Celem projektu jest podniesienie jakości kształcenia na studiach II i III
Politechnika Gdańska realizuje projekt dofinansowany z Funduszy Europejskich Zintegrowany Program Rozwoju Politechniki Gdańskiej Celem projektu jest podniesienie jakości kształcenia na studiach II i III
ROZPORZĄDZENIE MINISTRA GOSPODARKI I PRACY 1) z dnia 3 marca 2005 r.
 ROZPORZĄDZENIE MINISTRA GOSPODARKI I PRACY 1) z dnia 3 marca 2005 r. w sprawie sposobu prowadzenia identyfikacji wyrobów piro i amunicji dla potrzeb obrotu materiałami wybuchowymi i ich kontroli 2) Na
ROZPORZĄDZENIE MINISTRA GOSPODARKI I PRACY 1) z dnia 3 marca 2005 r. w sprawie sposobu prowadzenia identyfikacji wyrobów piro i amunicji dla potrzeb obrotu materiałami wybuchowymi i ich kontroli 2) Na
Czyli wybuchowa prezentacja!
 Czyli wybuchowa prezentacja! Co to jest Dynamit? Budowa Dynamitu. Krótka historia wynalazku. Alfred Nobel twórca Dynamitu. Testament Alfreda Nobla. Nagroda Nobla. Zastosowanie Dynamitu. Bibliografia. Dynamit
Czyli wybuchowa prezentacja! Co to jest Dynamit? Budowa Dynamitu. Krótka historia wynalazku. Alfred Nobel twórca Dynamitu. Testament Alfreda Nobla. Nagroda Nobla. Zastosowanie Dynamitu. Bibliografia. Dynamit
= C 6 H 10 O 5 + 6O 2 = 6CO 2 + 5H 2 O (2)
 Chemia materiałów wybuchowych Materiały do wykładów z chemii dla górników Jan Drzymała Wprowadzenie Według mitów greckich ludzkość otrzymała ogień od Prometeusza u zarania dziejów człowieka. Źródła kopalne
Chemia materiałów wybuchowych Materiały do wykładów z chemii dla górników Jan Drzymała Wprowadzenie Według mitów greckich ludzkość otrzymała ogień od Prometeusza u zarania dziejów człowieka. Źródła kopalne
Materiały wybuchowe amonowo-saletrzane HNO 3 + NH 3 NH 4NO 3
 W skład materiałów amonowo-saletrzanych wchodzi głównie azotan amonu (NH 4 NO, saletra amonowa, AA, ang. AN). Azotan amonu jest najtańszym materiałem wybuchowym, ale najtrudniej detonującym. Jego główne
W skład materiałów amonowo-saletrzanych wchodzi głównie azotan amonu (NH 4 NO, saletra amonowa, AA, ang. AN). Azotan amonu jest najtańszym materiałem wybuchowym, ale najtrudniej detonującym. Jego główne
XXI KONKURS CHEMICZNY DLA GIMNAZJALISTÓW ROK SZKOLNY 2013/2014
 IMIĘ I NAZWISKO PUNKTACJA SZKOŁA KLASA NAZWISKO NAUCZYCIELA CHEMII I LICEUM OGÓLNOKSZTAŁCĄCE Inowrocław 24 maja 2014 Im. Jana Kasprowicza INOWROCŁAW XXI KONKURS CHEMICZNY DLA GIMNAZJALISTÓW ROK SZKOLNY
IMIĘ I NAZWISKO PUNKTACJA SZKOŁA KLASA NAZWISKO NAUCZYCIELA CHEMII I LICEUM OGÓLNOKSZTAŁCĄCE Inowrocław 24 maja 2014 Im. Jana Kasprowicza INOWROCŁAW XXI KONKURS CHEMICZNY DLA GIMNAZJALISTÓW ROK SZKOLNY
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe
 kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe Zadanie
kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe Zadanie
Część I ZADANIA PROBLEMOWE (26 punktów)
 Zadanie 1 (0 6 punktów) Część I ZADANIA PROBLEMOWE (26 punktów) W podanym niżej tekście w miejsce kropek wpisz: - kwas solny - kwas mlekowy - kwas octowy - zjełczałe masło - woda sodowa - pokrzywa - zsiadłe
Zadanie 1 (0 6 punktów) Część I ZADANIA PROBLEMOWE (26 punktów) W podanym niżej tekście w miejsce kropek wpisz: - kwas solny - kwas mlekowy - kwas octowy - zjełczałe masło - woda sodowa - pokrzywa - zsiadłe
Produkty firmy HELUKABEL przeznaczone do stref zagrożonych wybuchem
 Produkty firmy HELUKABEL przeznaczone do stref zagrożonych wybuchem HELUKABEL jak powszechnie wiadomo firma rozwiązująca złożone zagadnienia techniczne, dostarczająca kable i przewody oraz osprzęt kablowy
Produkty firmy HELUKABEL przeznaczone do stref zagrożonych wybuchem HELUKABEL jak powszechnie wiadomo firma rozwiązująca złożone zagadnienia techniczne, dostarczająca kable i przewody oraz osprzęt kablowy
... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Aspirynę czyli kwas acetylosalicylowy można otrzymać w reakcji kwasu salicylowego z bezwodnikiem kwasu etanowego (octowego). a. Zapisz równanie reakcji, o której mowa w informacji wstępnej
Zadanie 1. (3 pkt) Aspirynę czyli kwas acetylosalicylowy można otrzymać w reakcji kwasu salicylowego z bezwodnikiem kwasu etanowego (octowego). a. Zapisz równanie reakcji, o której mowa w informacji wstępnej
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak)
 Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Odpowiedź:. Oblicz stężenie procentowe tlenu w wodzie deszczowej, wiedząc, że 1 dm 3 tej wody zawiera 0,055g tlenu. (d wody = 1 g/cm 3 )
 PRZYKŁADOWE ZADANIA Z DZIAŁÓW 9 14 (stężenia molowe, procentowe, przeliczanie stężeń, rozcieńczanie i zatężanie roztworów, zastosowanie stężeń do obliczeń w oparciu o reakcje chemiczne, rozpuszczalność)
PRZYKŁADOWE ZADANIA Z DZIAŁÓW 9 14 (stężenia molowe, procentowe, przeliczanie stężeń, rozcieńczanie i zatężanie roztworów, zastosowanie stężeń do obliczeń w oparciu o reakcje chemiczne, rozpuszczalność)
INSTRUKCJE PISEMNE. Czynności, które powinny być wykonane w razie wypadku lub zagrożenia
 INSTRUKCJE PISEMNE Czynności, które powinny być wykonane w razie wypadku lub zagrożenia W razie zaistnienia podczas przewozu wypadku lub zagrożenia, członkowie załogi pojazdu powinni wykonać następujące
INSTRUKCJE PISEMNE Czynności, które powinny być wykonane w razie wypadku lub zagrożenia W razie zaistnienia podczas przewozu wypadku lub zagrożenia, członkowie załogi pojazdu powinni wykonać następujące
a) proces denaturacji białka następuje w probówce: b) proces zachodzący w probówce nr 1 nazywa się:
 Zadanie 1. (4 pkt) Zaprojektuj doświadczenie chemiczne, za pomocą którego można wykryć siarkę w związkach organicznych. a) opisz przebieg doświadczenia b) zapisz przewidywane spostrzeżenia c) napisz równanie
Zadanie 1. (4 pkt) Zaprojektuj doświadczenie chemiczne, za pomocą którego można wykryć siarkę w związkach organicznych. a) opisz przebieg doświadczenia b) zapisz przewidywane spostrzeżenia c) napisz równanie
Life Cycle Inventory of production processes selected mining explosives. 1), Andrzej Maranda 2)
 Life Cycle Inventory of production processes selected mining explosives 1), Andrzej Maranda ) Keywords I P P L A L I Rys. 1. Tab. 1. 94 6 6 6 1 6 1 6 1 1 1 16 Azotan(V) amonu Olej Odpady (olej) Gotowy
Life Cycle Inventory of production processes selected mining explosives 1), Andrzej Maranda ) Keywords I P P L A L I Rys. 1. Tab. 1. 94 6 6 6 1 6 1 6 1 1 1 16 Azotan(V) amonu Olej Odpady (olej) Gotowy
SPALANIE PALIW GAZOWYCH
 SPALANIE PALIW GAZOWYCH MIESZANKA PALNA Mieszanka palna to mieszanina powietrza z paliwem, w której: po zniknięciu źródła zapłonu proces spalania rozwija się w niej samorzutnie. RODZAJE MIESZANEK PALNYCH
SPALANIE PALIW GAZOWYCH MIESZANKA PALNA Mieszanka palna to mieszanina powietrza z paliwem, w której: po zniknięciu źródła zapłonu proces spalania rozwija się w niej samorzutnie. RODZAJE MIESZANEK PALNYCH
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Instrukcja do zajęć z przedmiotu fakultatywnego: MATERIAŁY WYBUCHOWE. Otrzymywanie i badanie właściwości wysokoenergetycznych związków chemicznych
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY Instrukcja do zajęć z przedmiotu fakultatywnego: MATERIAŁY WYBUCHOWE Otrzymywanie i badanie właściwości wysokoenergetycznych związków chemicznych Gliwice, 2015 Spis
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY Instrukcja do zajęć z przedmiotu fakultatywnego: MATERIAŁY WYBUCHOWE Otrzymywanie i badanie właściwości wysokoenergetycznych związków chemicznych Gliwice, 2015 Spis
XXI Regionalny Konkurs Młody Chemik FINAŁ część I
 Katowice, 16.12.2009 XXI Regionalny Konkurs Młody Chemik FINAŁ część I ZADANIE 1. KRZYśÓWKA ZWIĄZKI WĘGLA I WODORU (9 punktów) RozwiąŜ krzyŝówkę. Litery z wyszczególnionych pól utworzą hasło nazwę węglowodoru:
Katowice, 16.12.2009 XXI Regionalny Konkurs Młody Chemik FINAŁ część I ZADANIE 1. KRZYśÓWKA ZWIĄZKI WĘGLA I WODORU (9 punktów) RozwiąŜ krzyŝówkę. Litery z wyszczególnionych pól utworzą hasło nazwę węglowodoru:
Projektowanie Biznesu Ekologicznego Wykład 2 Adriana Zaleska-Medynska Katedra Technologii Środowiska, p. G202
 Projektowanie Biznesu Ekologicznego Wykład 2 Adriana Zaleska-Medynska Katedra Technologii Środowiska, p. G202 Wykład 2 1. Jak przejść od pomysłu do przemysłu? 2. Projekt procesowy: koncepcja chemiczna
Projektowanie Biznesu Ekologicznego Wykład 2 Adriana Zaleska-Medynska Katedra Technologii Środowiska, p. G202 Wykład 2 1. Jak przejść od pomysłu do przemysłu? 2. Projekt procesowy: koncepcja chemiczna
Małopolski Konkurs Chemiczny dla Gimnazjalistów 23 lutego 2017 r.
 Kod ucznia Małopolski Konkurs Chemiczny dla Gimnazjalistów 23 lutego 2017 r. Etap III (wojewódzki) Wypełnia Komisja Konkursowa Zadanie Max liczba pkt. Liczba punktów KOD oceniającego I II III IV Suma 11
Kod ucznia Małopolski Konkurs Chemiczny dla Gimnazjalistów 23 lutego 2017 r. Etap III (wojewódzki) Wypełnia Komisja Konkursowa Zadanie Max liczba pkt. Liczba punktów KOD oceniającego I II III IV Suma 11
Kod ucznia: Zadanie Maksymalna ilość
 Warszawa 16 maja 2008r. Międzyszkolny konkurs chemiczny KWAS Etap II międzyszkolny Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Maksymalna ilość 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Liczba uzyskana
Warszawa 16 maja 2008r. Międzyszkolny konkurs chemiczny KWAS Etap II międzyszkolny Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Maksymalna ilość 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Liczba uzyskana
Przykładowe zadania z rozdziałów 1 5 (Mol, Stechiometria wzorów i równań chemicznych, Wydajność reakcji i inne)
 Przykładowe zadania z rozdziałów 1 5 (Mol, Stechiometria wzorów i równań chemicznych, Wydajność reakcji i inne) Zadanie 7 (1 pkt) Uporządkuj podane ilości moli związków chemicznych według rosnącej liczby
Przykładowe zadania z rozdziałów 1 5 (Mol, Stechiometria wzorów i równań chemicznych, Wydajność reakcji i inne) Zadanie 7 (1 pkt) Uporządkuj podane ilości moli związków chemicznych według rosnącej liczby
ĆWICZENIA LABORATORYJNE WYKRYWANIE WYBRANYCH ANIONÓW I KATIONÓW.
 ĆWICZENIA LABORATORYJNE WYKRYWANIE WYBRANYCH ANIONÓW I KATIONÓW. Chemia analityczna jest działem chemii zajmującym się ustalaniem składu jakościowego i ilościowego badanych substancji chemicznych. Analiza
ĆWICZENIA LABORATORYJNE WYKRYWANIE WYBRANYCH ANIONÓW I KATIONÓW. Chemia analityczna jest działem chemii zajmującym się ustalaniem składu jakościowego i ilościowego badanych substancji chemicznych. Analiza
HYDROLIZA SOLI. 1. Hydroliza soli mocnej zasady i słabego kwasu. Przykładem jest octan sodu, dla którego reakcja hydrolizy przebiega następująco:
 HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
PL B BUP 23/ WUP 06/14
 PL 217202 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 217202 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 394657 (22) Data zgłoszenia: 22.04.2011 (51) Int.Cl.
PL 217202 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 217202 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 394657 (22) Data zgłoszenia: 22.04.2011 (51) Int.Cl.
Podstawowe wiadomości o zagrożeniach
 1. Proces Palenia Spalanie jest to proces utleniania (łączenia się materiału palnego z tlenem) z wydzielaniem ciepła i światła. W jego wyniku wytwarzane są także produkty spalania: dymy i gazy. Spalanie
1. Proces Palenia Spalanie jest to proces utleniania (łączenia się materiału palnego z tlenem) z wydzielaniem ciepła i światła. W jego wyniku wytwarzane są także produkty spalania: dymy i gazy. Spalanie
NIEBEZPIECZNE REAKCJE CHEMICZNE
 NIBPICN RAKCJ CHMICN Niniejsze zestawienie stanowi jedynie wybór i obejmuje jedynie niektóre reakcje niebezpieczne. Wymienione związki mogą ulegać również innym reakcjom niebezpiecznym. Brak na niniejszej
NIBPICN RAKCJ CHMICN Niniejsze zestawienie stanowi jedynie wybór i obejmuje jedynie niektóre reakcje niebezpieczne. Wymienione związki mogą ulegać również innym reakcjom niebezpiecznym. Brak na niniejszej
Wiadomości pomocne przy ocenie zgodności - ATEX
 Wiadomości pomocne przy ocenie zgodności - ATEX 1. Atmosfera wybuchowa i źródła zapłonu W myśl dyrektywy 2014/34/UE (ATEX), Atmosfera wybuchowa oznacza mieszaninę z powietrzem, w warunkach atmosferycznych,
Wiadomości pomocne przy ocenie zgodności - ATEX 1. Atmosfera wybuchowa i źródła zapłonu W myśl dyrektywy 2014/34/UE (ATEX), Atmosfera wybuchowa oznacza mieszaninę z powietrzem, w warunkach atmosferycznych,
- materiał wybuchowy kruszący - lepiszcze - plstyfikator - stabilizator
 Plastyczne materiały wybuchowe zaliczane do materiałów wybuchowych kruszących potocznie zwane plastykami są to mieszaniny wybuchowe o plastycznej konsystencji, umożliwiającej dowolne formowanie ładunku.
Plastyczne materiały wybuchowe zaliczane do materiałów wybuchowych kruszących potocznie zwane plastykami są to mieszaniny wybuchowe o plastycznej konsystencji, umożliwiającej dowolne formowanie ładunku.
KANCELARIA PREZYDENTA RZECZYPOSPOLITEJ POLSKIEJ. Warszawa, dnia 5 grudnia 2006 r. Szanowni Państwo,
 KANCELARIA PREZYDENTA RZECZYPOSPOLITEJ POLSKIEJ Biuro Administracyjne Warszawa, dnia 5 grudnia 2006 r. Szanowni Państwo, Dotyczy: postępowania prowadzonego w trybie przetargu nieograniczonego na dostawę
KANCELARIA PREZYDENTA RZECZYPOSPOLITEJ POLSKIEJ Biuro Administracyjne Warszawa, dnia 5 grudnia 2006 r. Szanowni Państwo, Dotyczy: postępowania prowadzonego w trybie przetargu nieograniczonego na dostawę
6. ph i ELEKTROLITY. 6. ph i elektrolity
 6. ph i ELEKTROLITY 31 6. ph i elektrolity 6.1. Oblicz ph roztworu zawierającego 0,365 g HCl w 1,0 dm 3 roztworu. Odp 2,00 6.2. Oblicz ph 0,0050 molowego roztworu wodorotlenku baru (α = 1,00). Odp. 12,00
6. ph i ELEKTROLITY 31 6. ph i elektrolity 6.1. Oblicz ph roztworu zawierającego 0,365 g HCl w 1,0 dm 3 roztworu. Odp 2,00 6.2. Oblicz ph 0,0050 molowego roztworu wodorotlenku baru (α = 1,00). Odp. 12,00
Beata Mendak fakultety z chemii II tura PYTANIA Z KLASY PIERWSZEJ
 Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Reakcje chemiczne. Typ reakcji Schemat Przykłady Reakcja syntezy
 Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
ROCKSPLITTER. Nowa niewybuchowa technologia wydobywania kamienia blocznego i odspajania skał
 Nowa niewybuchowa technologia wydobywania kamienia blocznego i odspajania skał Przeznaczenie oraz sposób działania Cebar-DG ma zaszczyt przedstawić urządzenie jako nową niewybuchową technologię wydobywania
Nowa niewybuchowa technologia wydobywania kamienia blocznego i odspajania skał Przeznaczenie oraz sposób działania Cebar-DG ma zaszczyt przedstawić urządzenie jako nową niewybuchową technologię wydobywania
Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych
 Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych I. Reakcje egzoenergetyczne i endoenergetyczne 1. Układ i otoczenie Układ - ogół substancji
Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych I. Reakcje egzoenergetyczne i endoenergetyczne 1. Układ i otoczenie Układ - ogół substancji
SZKOLENIE PODSTAWOWE STRAŻAKÓW RATOWNIKÓW OSP Temat 11: Spalanie wybuchowe. Piotr Wójcik
 SZKOLENIE PODSTAWOWE STRAŻAKÓW RATOWNIKÓW OSP Temat 11: Spalanie wybuchowe Piotr Wójcik 2T Eksplozja Eksplozja - gwałtowny wybuch powodujący powstanie fali uderzeniowej rozchodzącej się z prędkością powyżej
SZKOLENIE PODSTAWOWE STRAŻAKÓW RATOWNIKÓW OSP Temat 11: Spalanie wybuchowe Piotr Wójcik 2T Eksplozja Eksplozja - gwałtowny wybuch powodujący powstanie fali uderzeniowej rozchodzącej się z prędkością powyżej
a) Sole kwasu chlorowodorowego (solnego) to... b) Sole kwasu siarkowego (VI) to... c) Sole kwasu azotowego (V) to... d) Sole kwasu węglowego to...
 Karta pracy nr 73 Budowa i nazwy soli. 1. Porównaj wzory sumaryczne soli. FeCl 2 Al(NO 3 ) 3 K 2 CO 3 Cu 3 (PO 4 ) 2 K 2 SO 4 Ca(NO 3 ) 2 CaCO 3 KNO 3 PbSO 4 AlCl 3 Fe 2 (CO 3 ) 3 Fe 2 (SO 4 ) 3 AlPO 4
Karta pracy nr 73 Budowa i nazwy soli. 1. Porównaj wzory sumaryczne soli. FeCl 2 Al(NO 3 ) 3 K 2 CO 3 Cu 3 (PO 4 ) 2 K 2 SO 4 Ca(NO 3 ) 2 CaCO 3 KNO 3 PbSO 4 AlCl 3 Fe 2 (CO 3 ) 3 Fe 2 (SO 4 ) 3 AlPO 4
Wojewódzki Konkurs Przedmiotowy z Chemii dla uczniów dotychczasowych gimnazjów województwa śląskiego w roku szkolnym 2017/2018
 Wojewódzki Konkurs Przedmiotowy z Chemii dla uczniów dotychczasowych gimnazjów województwa śląskiego w roku szkolnym 2017/2018 PRZYKŁADOWE ROZWIĄZANIA ZADAŃ I SCHEMAT PUNKTOWANIA Maksymalna liczba punktów
Wojewódzki Konkurs Przedmiotowy z Chemii dla uczniów dotychczasowych gimnazjów województwa śląskiego w roku szkolnym 2017/2018 PRZYKŁADOWE ROZWIĄZANIA ZADAŃ I SCHEMAT PUNKTOWANIA Maksymalna liczba punktów
KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 ... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, Witaj w pierwszym etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, Witaj w pierwszym etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
Wykaz niezgodnych substancji chemicznych
 Wykaz niezgodnych substancji chemicznych 1 Wykaz niezgodnych substancji chemicznych Substancje chemiczne zebrane w kolumnie I s niezgodne (niekompatybilne) z substancjami wymienionymi w kolumnie II i powinny
Wykaz niezgodnych substancji chemicznych 1 Wykaz niezgodnych substancji chemicznych Substancje chemiczne zebrane w kolumnie I s niezgodne (niekompatybilne) z substancjami wymienionymi w kolumnie II i powinny
WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG
 WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG Imię i nazwisko: Klasa i szkoła*: Adres e-mail: Nr telefonu: Czy uczeń jest już uczestnikiem projektu? (odp. otoczyć kółkiem) Ocena
WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG Imię i nazwisko: Klasa i szkoła*: Adres e-mail: Nr telefonu: Czy uczeń jest już uczestnikiem projektu? (odp. otoczyć kółkiem) Ocena
2. Procenty i stężenia procentowe
 2. PROCENTY I STĘŻENIA PROCENTOWE 11 2. Procenty i stężenia procentowe 2.1. Oblicz 15 % od liczb: a. 360, b. 2,8 10 5, c. 0.024, d. 1,8 10 6, e. 10 Odp. a. 54, b. 4,2 10 4, c. 3,6 10 3, d. 2,7 10 7, e.
2. PROCENTY I STĘŻENIA PROCENTOWE 11 2. Procenty i stężenia procentowe 2.1. Oblicz 15 % od liczb: a. 360, b. 2,8 10 5, c. 0.024, d. 1,8 10 6, e. 10 Odp. a. 54, b. 4,2 10 4, c. 3,6 10 3, d. 2,7 10 7, e.
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego. I Etap szkolny - 23 listopada 2016
 XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego I Etap szkolny - 23 listopada 2016 Kod ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego I Etap szkolny - 23 listopada 2016 Kod ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych. CHEMIA klasa II.
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa II Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -wymienia zasady bhp
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa II Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -wymienia zasady bhp
VI Podkarpacki Konkurs Chemiczny 2013/2014
 VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
PRZYKŁADOWE ZADANIA WĘGLOWODORY
 PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
AKADEMIA GÓRNICZO-HUTNICZA im. Stanisława Staszica w Krakowie OLIMPIADA O DIAMENTOWY INDEKS AGH 2017/18 CHEMIA - ETAP I
 Związki manganu i manganometria AKADEMIA GÓRNICZO-HUTNICZA 1. Spośród podanych grup wybierz tą, w której wszystkie związki lub jony można oznaczyć metodą manganometryczną: Odp. C 2 O 4 2-, H 2 O 2, Sn
Związki manganu i manganometria AKADEMIA GÓRNICZO-HUTNICZA 1. Spośród podanych grup wybierz tą, w której wszystkie związki lub jony można oznaczyć metodą manganometryczną: Odp. C 2 O 4 2-, H 2 O 2, Sn
KARTA CHARAKTERYSTYKI SUBSTANCJI NIEBEZPIECZNEJ
 KARTA CHARAKTERYSTYKI MATERIAŁU WYBUCHOWEGO SALETROL 9 KARTA CHARAKTERYSTYKI SUBSTANCJI NIEBEZPIECZNEJ 1. Identyfikacja materiału wybuchowego i przedsiębiorstwa 1.1 Identyfikacja preparatu: SALETROL 9
KARTA CHARAKTERYSTYKI MATERIAŁU WYBUCHOWEGO SALETROL 9 KARTA CHARAKTERYSTYKI SUBSTANCJI NIEBEZPIECZNEJ 1. Identyfikacja materiału wybuchowego i przedsiębiorstwa 1.1 Identyfikacja preparatu: SALETROL 9
Kryteria oceniania z chemii kl VII
 Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego
 Tytuł: Reakcja kwasu i wodorotlenku. Powstawanie soli dobrze rozpuszczalnej. Roztwory: HCl, NaOH; fenoloftaleina Probówka, łapa drewniana, palnik, pipeta Do probówki nalewamy ok. 3cm 3 wodorotlenku sodu
Tytuł: Reakcja kwasu i wodorotlenku. Powstawanie soli dobrze rozpuszczalnej. Roztwory: HCl, NaOH; fenoloftaleina Probówka, łapa drewniana, palnik, pipeta Do probówki nalewamy ok. 3cm 3 wodorotlenku sodu
Wszystkie wartości procentowe składników dotyczą wagi NIE objętości! Świece Dymne
 Podstawowe Mieszaniny Pirotechniczne W tym artykule opisze podstawowe mieszaniny pirotechniczne, od których większość zaczynała swoją przygodę z pirotechniką Wszystkie wartości procentowe składników dotyczą
Podstawowe Mieszaniny Pirotechniczne W tym artykule opisze podstawowe mieszaniny pirotechniczne, od których większość zaczynała swoją przygodę z pirotechniką Wszystkie wartości procentowe składników dotyczą
5. STECHIOMETRIA. 5. Stechiometria
 5. STECHIOMETRIA 25 5. Stechiometria 5.1. Ile gramów magnezu wzięło udział w reakcji z tlenem, jeśli otrzymano 6,0 g tlenku magnezu? Odp. 3,60 g 5.2. Do 50 cm 3 roztworu kwasu siarkowego (VI) o stężeniu
5. STECHIOMETRIA 25 5. Stechiometria 5.1. Ile gramów magnezu wzięło udział w reakcji z tlenem, jeśli otrzymano 6,0 g tlenku magnezu? Odp. 3,60 g 5.2. Do 50 cm 3 roztworu kwasu siarkowego (VI) o stężeniu
Zadanie: 2 (4 pkt) Napisz, uzgodnij i opisz równania reakcji, które zaszły w probówkach:
 Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
str. 2 MATERIAŁ NAUCZANIA
 str. 2 MATERIAŁ NAUCZANIA Proces spalania; Spalanie płomieniowe i bezpłomieniowe; Budowa płomienia; Charakterystyka spalania ciał stałych, cieczy i gazów; Metody i sposoby przerywania procesu spalania;
str. 2 MATERIAŁ NAUCZANIA Proces spalania; Spalanie płomieniowe i bezpłomieniowe; Budowa płomienia; Charakterystyka spalania ciał stałych, cieczy i gazów; Metody i sposoby przerywania procesu spalania;
STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia!
 STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia! 001 Obliczyć stężenie molowe jonów Ca 2+ w roztworze zawierającym 2,22g CaCl2 w 100 ml roztworu, przyjmując a = 100%. 002
STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia! 001 Obliczyć stężenie molowe jonów Ca 2+ w roztworze zawierającym 2,22g CaCl2 w 100 ml roztworu, przyjmując a = 100%. 002
mgr inż. Aleksander Demczuk
 ZAGROŻENIE WYBUCHEM mgr inż. Aleksander Demczuk mł. bryg. w stanie spocz. Czy tylko po??? ZAPEWNENIE BEZPIECZEŃSTWA POKÓJ KRYZYS WOJNA REAGOWANIE PRZYGOTOWANIE zdarzenie - miejscowe zagrożenie - katastrofa
ZAGROŻENIE WYBUCHEM mgr inż. Aleksander Demczuk mł. bryg. w stanie spocz. Czy tylko po??? ZAPEWNENIE BEZPIECZEŃSTWA POKÓJ KRYZYS WOJNA REAGOWANIE PRZYGOTOWANIE zdarzenie - miejscowe zagrożenie - katastrofa
1. Podstawowe prawa i pojęcia chemiczne
 1. PODSTAWOWE PRAWA I POJĘCIA CHEMICZNE 5 1. Podstawowe prawa i pojęcia chemiczne 1.1. Wyraź w gramach masę: a. jednego atomu żelaza, b. jednej cząsteczki kwasu siarkowego. Odp. 9,3 10 23 g; 1,6 10 22
1. PODSTAWOWE PRAWA I POJĘCIA CHEMICZNE 5 1. Podstawowe prawa i pojęcia chemiczne 1.1. Wyraź w gramach masę: a. jednego atomu żelaza, b. jednej cząsteczki kwasu siarkowego. Odp. 9,3 10 23 g; 1,6 10 22
Zadanie 2. (1 pkt) Uzupełnij tabelę, wpisując wzory sumaryczne tlenków w odpowiednie kolumny. CrO CO 2 Fe 2 O 3 BaO SO 3 NO Cu 2 O
 Test maturalny Chemia ogólna i nieorganiczna Zadanie 1. (1 pkt) Uzupełnij zdania. Pierwiastek chemiczny o liczbie atomowej 16 znajduje się w.... grupie i. okresie układu okresowego pierwiastków chemicznych,
Test maturalny Chemia ogólna i nieorganiczna Zadanie 1. (1 pkt) Uzupełnij zdania. Pierwiastek chemiczny o liczbie atomowej 16 znajduje się w.... grupie i. okresie układu okresowego pierwiastków chemicznych,
KONKURS CHEMICZNY ROK PRZED MATURĄ
 Wydział Chemii UMCS Polskie Towarzystwo Chemiczne Doradca metodyczny ds. nauczania chemii KONKURS CHEMICZNY ROK PRZED MATURĄ ROK SZKOLNY 2006/2007 ETAP SZKOLNY Numer kodowy Suma punktów Podpisy Komisji:
Wydział Chemii UMCS Polskie Towarzystwo Chemiczne Doradca metodyczny ds. nauczania chemii KONKURS CHEMICZNY ROK PRZED MATURĄ ROK SZKOLNY 2006/2007 ETAP SZKOLNY Numer kodowy Suma punktów Podpisy Komisji:
Wspólny wniosek ROZPORZĄDZENIE RADY
 KOMISJA EUROPEJSKA WYSOKI PRZEDSTAWICIEL UNII EUROPEJSKIEJ DO SPRAW ZAGRANICZNYCH I POLITYKI BEZPIECZEŃSTWA Bruksela, dnia 10.6.2011 KOM(2011) 362 wersja ostateczna 2011/0158 (NLE) Wspólny wniosek ROZPORZĄDZENIE
KOMISJA EUROPEJSKA WYSOKI PRZEDSTAWICIEL UNII EUROPEJSKIEJ DO SPRAW ZAGRANICZNYCH I POLITYKI BEZPIECZEŃSTWA Bruksela, dnia 10.6.2011 KOM(2011) 362 wersja ostateczna 2011/0158 (NLE) Wspólny wniosek ROZPORZĄDZENIE
Badanie reakcji materiałów wysokoenergetycznych na uderzenie strumienia kumulacyjnego
 Bi u l e t y n WAT Vo l. LXII, Nr 1, 2013 Badanie reakcji materiałów wysokoenergetycznych na uderzenie strumienia kumulacyjnego Waldemar A. Trzciński, Jakub Piergies, Artur Steckiewicz 1 Wojskowa Akademia
Bi u l e t y n WAT Vo l. LXII, Nr 1, 2013 Badanie reakcji materiałów wysokoenergetycznych na uderzenie strumienia kumulacyjnego Waldemar A. Trzciński, Jakub Piergies, Artur Steckiewicz 1 Wojskowa Akademia
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
(12) OPIS PATENTOWY (19) PL
 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 178433 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 312817 (2 2 ) Data zgłoszenia: 13.02.1996 ( 5 1) IntCl6: D06M 15/19
RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 178433 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 312817 (2 2 ) Data zgłoszenia: 13.02.1996 ( 5 1) IntCl6: D06M 15/19
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 16 stycznia 2015 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 16 stycznia 2015 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 16 stycznia 2015 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
ROZPORZĄDZENIE MINISTRA GOSPODARKI I PRACY 1) z dnia 29 lipca 2005 r.
 ROZPORZĄDZENIE MINISTRA GOSPODARKI I PRACY 1) z dnia 29 lipca 2005 r. w sprawie wykazu wyrobów pirotechnicznych, na których nabywanie, przechowywanie lub używanie nie jest wymagane uzyskanie pozwolenia
ROZPORZĄDZENIE MINISTRA GOSPODARKI I PRACY 1) z dnia 29 lipca 2005 r. w sprawie wykazu wyrobów pirotechnicznych, na których nabywanie, przechowywanie lub używanie nie jest wymagane uzyskanie pozwolenia
HYDROLIZA SOLI. Przykładem jest octan sodu, dla którego reakcja hydrolizy przebiega następująco:
 HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
wielkość opakowania (nie większa niż 3 litry lub 3 kilogramy) 1 1,4-Dioksan czda POCH l 2 1-Propanol czda POCH BA l
 ZAŁĄCZNIK NR 1 SZCZEGÓŁOWY WYKAZ ODCZYNNIKÓW Lp Nazwa Producent-numer katalogowy (zgodnie z art. 3 1 ust 2 SIWZ) przewidywana ilość* wielkość opakowania (nie większa niż 3 litry lub 3 kilogramy) Cena jednostkowa
ZAŁĄCZNIK NR 1 SZCZEGÓŁOWY WYKAZ ODCZYNNIKÓW Lp Nazwa Producent-numer katalogowy (zgodnie z art. 3 1 ust 2 SIWZ) przewidywana ilość* wielkość opakowania (nie większa niż 3 litry lub 3 kilogramy) Cena jednostkowa
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Sprawozdanie z działalności Centralnego Biura Śledczego KGP za 2010 rok
 Sprawozdanie z działalności Centralnego Biura Śledczego KGP za 2010 rok Warszawa, lipiec 2004 Warszawa 2011 STAN REALIZACJI ZADAŃ CENTRALNEGO BIURA ŚLEDCZEGO KGP W ZAKRESIE ZWALCZANIA PRZESTĘPCZOŚCI ZORGANIZOWANEJ
Sprawozdanie z działalności Centralnego Biura Śledczego KGP za 2010 rok Warszawa, lipiec 2004 Warszawa 2011 STAN REALIZACJI ZADAŃ CENTRALNEGO BIURA ŚLEDCZEGO KGP W ZAKRESIE ZWALCZANIA PRZESTĘPCZOŚCI ZORGANIZOWANEJ
TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II
 TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II Czas trwania testu 120 minut Informacje 1. Proszę sprawdzić czy arkusz zawiera 10 stron. Ewentualny brak należy zgłosić nauczycielowi. 2. Proszę rozwiązać
TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II Czas trwania testu 120 minut Informacje 1. Proszę sprawdzić czy arkusz zawiera 10 stron. Ewentualny brak należy zgłosić nauczycielowi. 2. Proszę rozwiązać
1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru
 1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru Wzór związku chemicznego podaje jakościowy jego skład z jakich pierwiastków jest zbudowany oraz liczbę atomów poszczególnych pierwiastków
1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru Wzór związku chemicznego podaje jakościowy jego skład z jakich pierwiastków jest zbudowany oraz liczbę atomów poszczególnych pierwiastków
XXIV Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych. Etap II rozwiązania zadań
 XXIV Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych Etap II rozwiązania zadań Zadanie 1 Na podstawie informacji o pierwiastku X i jego solach (B-E) możemy stwierdzić, że jest to żelazo. Najbardziej
XXIV Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych Etap II rozwiązania zadań Zadanie 1 Na podstawie informacji o pierwiastku X i jego solach (B-E) możemy stwierdzić, że jest to żelazo. Najbardziej
I KSZTAŁCENIA PRAKTYCZNEGO. Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
Warszawski konkurs chemiczny KWAS. Etap I szkolny. Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17
 Warszawa 17 marca 2009r. Warszawski konkurs chemiczny KWAS Etap I szkolny Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Maksymalna ilość punktów 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Liczba
Warszawa 17 marca 2009r. Warszawski konkurs chemiczny KWAS Etap I szkolny Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Maksymalna ilość punktów 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Liczba
Wiadomości pomocne przy ocenie zgodności - ATEX
 Wiadomości pomocne przy ocenie zgodności - ATEX 1. Przestrzeń zagrożona wybuchem i źródła zapłonu W myśl dyrektywy 94/9/WE (ATEX), przestrzeń zagrożona wybuchem jest to przestrzeń, w której zależnie od
Wiadomości pomocne przy ocenie zgodności - ATEX 1. Przestrzeń zagrożona wybuchem i źródła zapłonu W myśl dyrektywy 94/9/WE (ATEX), przestrzeń zagrożona wybuchem jest to przestrzeń, w której zależnie od
Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
 Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
ZAKRES AKREDYTACJI JEDNOSTKI CERTYFIKUJĄCEJ WYROBY Nr AC 027
 ZAKRES AKREDYTACJI JEDNOSTKI CERTYFIKUJĄCEJ WYROBY Nr AC 027 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-82 Warszawa, ul. Szczotkarska 42 Wydanie nr 8 Data wydania: 26 lutego 2014 r. AC 027 Nazwa i adres
ZAKRES AKREDYTACJI JEDNOSTKI CERTYFIKUJĄCEJ WYROBY Nr AC 027 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-82 Warszawa, ul. Szczotkarska 42 Wydanie nr 8 Data wydania: 26 lutego 2014 r. AC 027 Nazwa i adres
Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów.
 Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów. Wprowadzenie teoretyczne Cel ćwiczeń: Poznanie metod otrzymywania oraz badania właściwości węglowodorów alifatycznych
Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów. Wprowadzenie teoretyczne Cel ćwiczeń: Poznanie metod otrzymywania oraz badania właściwości węglowodorów alifatycznych
Symbole stosowane do oznaczenia niebezpieczeństwa związanego z użyciem związków chemicznych w krajach Unii Europejskiej
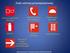 Symbole stosowane do oznaczenia niebezpieczeństwa związanego z użyciem związków chemicznych w krajach Unii Europejskiej Oznaczenie zagrożenia chemicznego czarny piktogram + = oznaczenie zagrożenia Oznaczenia
Symbole stosowane do oznaczenia niebezpieczeństwa związanego z użyciem związków chemicznych w krajach Unii Europejskiej Oznaczenie zagrożenia chemicznego czarny piktogram + = oznaczenie zagrożenia Oznaczenia
OPINIA. FUNDACJA AMICUS UNIVERSITATIS NICOLAI COPERNICI Ul. Gagarina TORUŃ. prof. dr hab. Bogusław Buszewski
 FUNDACJA AMICUS UNIVERSITATIS NICOLAI COPERNICI Ul. Gagarina 11 87-100 TORUŃ OPINIA w zakresie występowania zagrożeń chemicznych, epidemiologicznych, pożarowych oraz występowaniem przedmiotów wybuchowych
FUNDACJA AMICUS UNIVERSITATIS NICOLAI COPERNICI Ul. Gagarina 11 87-100 TORUŃ OPINIA w zakresie występowania zagrożeń chemicznych, epidemiologicznych, pożarowych oraz występowaniem przedmiotów wybuchowych
Scenariusz lekcji w technikum zakres podstawowy 2 godziny
 Scenariusz lekcji w technikum zakres podstawowy 2 godziny Temat : Hydroliza soli. Cele dydaktyczno wychowawcze: Wyjaśnienie przyczyn różnych odczynów soli Uświadomienie różnej roli wody w procesach dysocjacji
Scenariusz lekcji w technikum zakres podstawowy 2 godziny Temat : Hydroliza soli. Cele dydaktyczno wychowawcze: Wyjaśnienie przyczyn różnych odczynów soli Uświadomienie różnej roli wody w procesach dysocjacji
Zajęcia 10 Kwasy i wodorotlenki
 Zajęcia 10 Kwasy i wodorotlenki Według teorii Brönsteda-Lowrego kwasy to substancje, które w reakcjach chemicznych oddają protony, natomiast zasady to substancje, które protony przyłączają. Kwasy, które
Zajęcia 10 Kwasy i wodorotlenki Według teorii Brönsteda-Lowrego kwasy to substancje, które w reakcjach chemicznych oddają protony, natomiast zasady to substancje, które protony przyłączają. Kwasy, które
ZATWIERDZAM. Sprawozdanie z działalności Centralnego Biura Śledczego KGP w 2009 roku
 ZATWIERDZAM Sprawozdanie z działalności Centralnego Biura Śledczego KGP w roku Warszawa, lipiec 2004 Warszawa 2010 1. STAN REALIZACJI ZADAŃ CENTRALNEGO BIURA ŚLEDCZEGO KGP W ZAKRESIE ZWALCZANIA PRZESTĘPCZOŚCI
ZATWIERDZAM Sprawozdanie z działalności Centralnego Biura Śledczego KGP w roku Warszawa, lipiec 2004 Warszawa 2010 1. STAN REALIZACJI ZADAŃ CENTRALNEGO BIURA ŚLEDCZEGO KGP W ZAKRESIE ZWALCZANIA PRZESTĘPCZOŚCI
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie) Kod ucznia Suma punktów Witamy Cię na trzecim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie) Kod ucznia Suma punktów Witamy Cię na trzecim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
XXIII KONKURS CHEMICZNY DLA GIMNAZJALISTÓW ROK SZKOLNY 2015/2016
 IMIĘ I NAZWISKO PUNKTACJA SZKOŁA KLASA NAZWISKO NAUCZYCIELA CHEMII I LICEUM OGÓLNOKSZTAŁCĄCE Inowrocław 21 maja 2016 Im. Jana Kasprowicza INOWROCŁAW XXIII KONKURS CHEMICZNY DLA GIMNAZJALISTÓW ROK SZKOLNY
IMIĘ I NAZWISKO PUNKTACJA SZKOŁA KLASA NAZWISKO NAUCZYCIELA CHEMII I LICEUM OGÓLNOKSZTAŁCĄCE Inowrocław 21 maja 2016 Im. Jana Kasprowicza INOWROCŁAW XXIII KONKURS CHEMICZNY DLA GIMNAZJALISTÓW ROK SZKOLNY
Wojewódzki Konkurs Przedmiotowy z Chemii III etap
 KOD Ucznia Wojewódzki Konkurs Przedmiotowy z Chemii III etap Termin: 05. 04. 2004 r Czas pracy: 90 minut Ilość punktów za rozwiązanie zadań Razem Podpis Część I Cześć II Cześć III Zadania zamknięte i otwarte
KOD Ucznia Wojewódzki Konkurs Przedmiotowy z Chemii III etap Termin: 05. 04. 2004 r Czas pracy: 90 minut Ilość punktów za rozwiązanie zadań Razem Podpis Część I Cześć II Cześć III Zadania zamknięte i otwarte
Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 20 KWAS 2JODOBENZOESOWY NH 2 NaNO 2, HCl Woda, < 5 o C, 15 min N 2 Cl KI Woda, < 5 o C, potem 50 o C, 20 min I Stechiometria reakcji Kwas antranilowy Azotyn sodu Kwas solny stężony 1 ekwiwalent
PREPARAT NR 20 KWAS 2JODOBENZOESOWY NH 2 NaNO 2, HCl Woda, < 5 o C, 15 min N 2 Cl KI Woda, < 5 o C, potem 50 o C, 20 min I Stechiometria reakcji Kwas antranilowy Azotyn sodu Kwas solny stężony 1 ekwiwalent
TYPY REAKCJI CHEMICZNYCH
 1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
Spis treści. Oferta jednostek naukowych i naukowo-badawczych. Referaty naukowe
 Spis treści Oferta jednostek naukowych i naukowo-badawczych Referaty naukowe Streszczenia artykułów Konferencja Naukowo-Techniczna Wspólne działanie Nauki Polskiej dla Obronności Kraju Wojciech SATKOWSKI
Spis treści Oferta jednostek naukowych i naukowo-badawczych Referaty naukowe Streszczenia artykułów Konferencja Naukowo-Techniczna Wspólne działanie Nauki Polskiej dla Obronności Kraju Wojciech SATKOWSKI
ĆWICZENIE I - BIAŁKA. Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi.
 ĆWICZENIE I - BIAŁKA Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi. Odczynniki: - wodny 1% roztwór siarczanu(vi) miedzi(ii), - 10% wodny
ĆWICZENIE I - BIAŁKA Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi. Odczynniki: - wodny 1% roztwór siarczanu(vi) miedzi(ii), - 10% wodny
S Y L A B U S P R Z E D M I O T U
 "Z A T W I E R D Z A M Prof. dr hab. inż. Radosław TRĘBIŃSKI Dziekan Wydziału Mechatroniki i Lotnictwa Warszawa, dnia... NAZWA PRZEDMIOTU: Wersja anglojęzyczna: Kod przedmiotu: S Y L A B U S P R Z E D
"Z A T W I E R D Z A M Prof. dr hab. inż. Radosław TRĘBIŃSKI Dziekan Wydziału Mechatroniki i Lotnictwa Warszawa, dnia... NAZWA PRZEDMIOTU: Wersja anglojęzyczna: Kod przedmiotu: S Y L A B U S P R Z E D
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW. Eliminacje rejonowe II stopień
 POUFNE Pieczątka szkoły 28 stycznia 2016 r. Kod ucznia (wypełnia uczeń) Imię i nazwisko (wypełnia komisja) Czas pracy 90 minut KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 Eliminacje rejonowe
POUFNE Pieczątka szkoły 28 stycznia 2016 r. Kod ucznia (wypełnia uczeń) Imię i nazwisko (wypełnia komisja) Czas pracy 90 minut KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 Eliminacje rejonowe
Spalanie detonacyjne - czy to się opłaca?
 Spalanie detonacyjne - czy to się opłaca? Mgr inż. Dariusz Ejmocki Spalanie Spalanie jest egzotermiczną reakcją chemiczną syntezy, zdolną do samoczynnego przemieszczania się w przestrzeni wypełnionej substratami.
Spalanie detonacyjne - czy to się opłaca? Mgr inż. Dariusz Ejmocki Spalanie Spalanie jest egzotermiczną reakcją chemiczną syntezy, zdolną do samoczynnego przemieszczania się w przestrzeni wypełnionej substratami.
relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
 1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
Zwrot Znaczenie R1 Produkt wybuchowy w stanie suchym. R2 Zagrożenie wybuchem wskutek uderzenia, tarcia, kontaktu z ogniem lub innymi źródłami
 Zwrot Znaczenie R1 Produkt wybuchowy w stanie suchym. R2 Zagrożenie wybuchem wskutek uderzenia, tarcia, kontaktu z ogniem lub innymi źródłami zapłonu. R3 Skrajne zagrożenie wybuchem wskutek uderzenia,
Zwrot Znaczenie R1 Produkt wybuchowy w stanie suchym. R2 Zagrożenie wybuchem wskutek uderzenia, tarcia, kontaktu z ogniem lub innymi źródłami zapłonu. R3 Skrajne zagrożenie wybuchem wskutek uderzenia,
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
Punktacja: po 5 pkt za obliczenie potrzebnej ilości każdego ze składników
 Zad. 1 W 100 g mieszaniny znajduje się 14,8 g HNO 3, 78,2 g etanolu i 7 g wody. Mając do dyspozycji bezwodny etanol, potrzebujemy 78,2/0,785 = 99,62 cm 3 tego związku. Potrzebujemy także 14,8/0,75 = 19,73
Zad. 1 W 100 g mieszaniny znajduje się 14,8 g HNO 3, 78,2 g etanolu i 7 g wody. Mając do dyspozycji bezwodny etanol, potrzebujemy 78,2/0,785 = 99,62 cm 3 tego związku. Potrzebujemy także 14,8/0,75 = 19,73
X Konkurs Chemii Nieorganicznej i Ogólnej rok szkolny 2011/12
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO X Konkurs Chemii Nieorganicznej i Ogólnej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1. (10
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO X Konkurs Chemii Nieorganicznej i Ogólnej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1. (10
