Czy rekomendacje AOTM ywać na koszty farmakoterapii PHARMA INSTITUTE WARSZAWA Hotel Radisson Wojciech Matusewicz
|
|
|
- Karolina Popławska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Czy rekomendacje AOTM mogą wpływa ywać na koszty farmakoterapii PHARMA INSTITUTE WARSZAWA Hotel Radisson Wojciech Matusewicz
2 T A K AOTM nie prowadzi negocjacji cenowych Z Przemysłem, nie wpływa też bezpośrednio na POLITYKĘ LEKOWĄ PAŃSTWA! AOTM (ocena HTA )jest doskonałym narzędziem dla prowadzących politykę lekową może e ułatwiu atwić decyzje politykom. Oceny HTA nie sąs wytycznymi dla klinicystów ( ale dobrze, żeby je studiowali )
3 HTA w POLSCE Zarządzeniem MZ - wrzesień 2005 Nowelizowane Zarządzenia : czerwiec 2006 wrzesień 2007 wrzesień 2008 Obecnie trwają prace w Parlamencie nad Ustawowym zapisem Agencji (w ramach ustawy koszykowej).
4 H T A A -ASSESSMENT ASSESSMENT (ocena analityczna) A -APPRAISAL APPRAISAL (interpretacja wartościuj ciująca) realizowana przez Radę Konsultacyjną w AOTM A ROBI DUŻĄ RÓŻNICĘ!!
5 Agencja Oceny Technologii Medycznych OPINIE RADY KONSULTACYJNEJ AOTM Rada Konsultacyjna AOTM jest organem ponadpolitycznym. Rekomendacje Rady opierają się na dowodach naukowych dołą łączonych przez wnioskodawców, w, zweryfikowanych przez Agencję.
6 Agencja Oceny Technologii Medycznych HTA jest definiowana jako dziedzina międzydyscyplinarna analizująca: - medyczne - ekonomiczne - socjalne - etyczne implikacje rozwoju, rozpowszechniania, użycia u technologii medycznych. INAHTA ( )
7 Agencja Oceny Technologii Medycznych Technologia medyczna (health technology) odnosi się do każdej interwencji, która może e być wykorzystana do promowania zdrowia, zapobiegania, diagnozowania lub leczenia chorób, w rehabilitacji lub opiece długoterminowej. Obejmuje leki (produkty lecznicze), wyroby medyczne, procedury lub systemy organizacyjne stosowane w opiece zdrowotnej.
8 Agencja Oceny Technologii Medycznych Pojęcie to jest stosunkowo nowym określeniem, funkcjonującym cym w polskim systemie ochrony zdrowia. Wprowadzenie go do słownika s pojęć wiąza zało o się z wolą do precyzyjnego wskazania danej interwencji, będącej b przedmiotem analiz. W celu porównania wyników w analiz wykonywanych przez instytucje w różnych r krajach, opracowywane w różnych r językach, j przyjmuje się powyższ szą definicję oraz określenie w języku j angielskim.
9 Agencja Oceny Technologii Medycznych EBM Evidence Based Medecine CER Comparative Effectiveness Research HTA Health Technology Assessment (Appraisal?) są powiązane EBDM Evidence Based Decission Making dowody, dzięki którym powstają decyzje
10 Agencja Oceny Technologii Medycznych Czy to może działać? Dowody na akceptację społeczn eczną Czy to działa? a? <CER> - Porównawcze badania skuteczności ci populacyjnej - EBM - Kliniczne wytyczne - Decyzje dotyczące ce leczenia pacjenta <CED> Czy to jest opłacalne? HTA obiektywne dowody naukowe i dowody na akceptację społeczn eczną danej technologii medycznej
11 Agencja Oceny Technologii Medycznych Rynek lekowy 50 leków wystarcza do leczenia 70% chorych 210 refundowanych leków zażywa chorych Te 210 substancji to 92% rynku Pozostałe e leki to kategoria leku specjalistycznego (w tym leki sieroce) wymagającego ścisłego monitorowania
12 METODY HTA Zasada 1:Hta powinna zawierać w sobie stosowne metody oceny kosztów w i korzyści Zasada 2:HTA powinna brać pod uwagę szeroki zakres dowodów w (np. Świadectwa pacjentów) i wyników naukowych Zasada 3:Przy podejmowaniu ocen HTA powinno się brac pod uwagę pełną perspektywę społeczn eczną i jak najszersze spektrum dowodów Zasada 4:Oceny powinny w sposób b jasny i przejrzysty wskazywać na rozbieżno ności w ocenach Zasada 5 :Oceny HTA powinny brać pod uwagę tematy związane zane z uogólnianiem tematów iich przenośno nością (Tak by były y do wykorzystania w różnych r kontekstach )
13 Tworzenie programów w HTA Zasada 1:Cel i zakres HTA powinien być przejrzysty i odzwierciedlający cy jego użycie u Zasada 2 :HTA musi być obiektywna i transparentna Zasada 3 :HTA powinna powinna zajmować się technologiami mającymi istotne znaczenie Zasada 4 :Powinien istnieć przejrzysty system stwarzający priorytety w pracach HTA ( AOTM _
14 Procesy przeprowadzania ocen HTA Zasada 1:Przeprowadzający oceny powinni włączać aktywnie wszystkie zaangażowane w nie grupy do których sąs kierowane Zasada 2: Przeprowadzają oceny powinni aktywnie poszukiwać wszelkich dowodów w mogących mieć znaczenie dla danej technologii Zasada 3 :Praktyczne wprowadzanie uzyskanych ocen HTA powinno być monitorowane
15 Wykorzystywanie HTA przy podejmowaniu decyzji Zasada 1:Ocena HTA powinna być przeprowadzona w czasie odzwierciedlającym cym rzeczywiste potrzeby Zasada 2 : Wyniki ocen HTA powiiny być niezwłocznie przekazane różnym r decydentom i społecze eczeństwu Zasada 3 :Wszelkie powiązania między wynikami ocen HTA a procesem podejmowania stosownych decyzji (politycznych?) powinny być transparentne i jasno zdefiniowane
16 Rodzaje Rekomendacji 1.Finansowa. Finansować dowody naukowe przekonywujące ce! 2 Finansować tymczasowo pod warunkiem zebrania danych do ostatecznej decyzji dowody naukowe nieprzekonywujące ce,, efektywność kosztowa kontrowersyjna. 3 Finansować przy spełnieniu precyzyjnie zdefiniowanych kryteriach lub w określonych wskazaniach np. zdefiniowanie populacji VECTIBEX.
17 Agencja Oceny Technologii Medycznych ANI CHOROBA RZADKA,, ANI LEK NIE JEST SIEROCY Rak jelita grubego z przerzutami NOWOTWORY HETEROGENNE PANITUMUMAB Vectibex dopuszczony w wyjątkowych okolicznościach ciach TYLKO u chorych wykazujących ekspresję genu KRAS bez mutacji (typ dziki). Rekomendacja 2008 dla Vectibaxu pierwsza tego typu mówiąca o konieczności ci profilowania pacjentów genetycznie.
18 Rekomendacje cd. 4.Finansować pod warunkiem zapewnienia kosztowo efektywnego sposobu finansowania np. risk-sharing sharing scheme price-volume agreements
19 Typy analiz 1 kosztów-efektywno efektywności ( ICER ) 2 kosztów użyteczności ci (QALY, LYG ) 3 kosztów-konsekwencji konsekwencji 4 kosztów-korzy korzyści 5 MINIMALIZACJI KOSZTÓW- TERAPIA INICJUJĄCA CA W PROGRAMACH ZDROWOTNYCH!!! KONTROWERSJE
20 Analiza kosztów efektywności Lata życia skorygowane o jakość QALY (Weinstein i Stason od 1977) Jednostka wyniku w analizie użytecznou yteczności ci kosztów,, która przypisuje każdemu rokowi wartość od 0 do 1. 1 Wartość 1 pełnia zdrowia Wartość 0 zgon
21 Analiza kosztów efektywności cd. W analizie kosztów efektywności tzw. LYQ (Life Years Gained) zaoszczędzone lata życia,, wolne od objawów choroby, odsetek wyleczeń itp. ICER inkrementalny współczynnik Koszt/efektywność tzn. ile kosztuje uzyskanie dodatkowej jednostki wyniku przy zastąpieniu jednej technologii drugą,, lub jakie będąb oszczędno dności. Za kosztowo efektywną technologię uważa a się jeżeli eli LYQ / QALY = 3 x PKB/per capita Dla ciekawość śći i gdzie jestesmy?
22 PKB a sytuacja POLSKI PKB liczone jako parytet siły y nabywczej 1. USA 14,3 bln $ 20. POLSKA 620 mld $ PKB nominalny 1. USA 14,2 bln $ 24. POLSKA 450 mld $ PKB Per capita 1. Luksemburg -84,5 tys.$ 2. 4 największe koncerny farmaceutyczne 50,0 tys.$ Na jednego zatrudnionego 4. USA 45 tys. $ 54. POLSKA 15,9 tys. $
23 Analiza ekonomiczna w wytycznych HTA Analiza farmakoekonomiczna- 1.Dostarcza danych użytecznych u w podejmowaniu decyzji o refundacji danego leku : wyniki tej analizy wskazują, czy nowy lek jest opłacaln acalną alternatywą dla istniejącego sposobu leczenia. 2.Koszty i efekty sąs oceniane na poziomie jednostki. 3.Analiza farmakoekonomiczna jest dokonywana z punktu widzenia społecze eczeństwa
24 cd. 1.Analiza finansowa udziela informacji o konsekwencjach makroekonomicznych. 2.Analizą finansową zainteresowany jest płatnik publiczny 3.Polityków w (patrzących perspektywicznie) powinna interesować analiza makro- np. koszty pośrednie danej patologii i ocenianych procedur.
25 Agencja Oceny Technologii Medycznych OPINIE RADY KONSULTACYJNEJ AOTM W Polsce powinna być wprowadzona metoda dzielenia ryzyka (ang. risk sharing) w odniesieniu do technologii lekowych. Polega ona na warunkowym finansowaniu rekomendowanej technologii przez okres np. dwóch lat, a następnie na ponownej jej ocenie. Jeżeli eli technologia okaże e się nieskuteczna, wnioskodawca (producent technologii lub podmiot odpowiedzialny) powinien ponosić część kosztów w jej warunkowego finansowania.
26 Najbardziej rozpowszechnione formy współpłacenia 1.Współfinansowanie 2.Koasekuracja ( podział albo rozłożenie ryzyka na co najmniej dwa podmioty w kwestiach finansowania ) Zwrot zysków -obowiązkowe potrącenia -Claw-back obniżenie opłaty za zakup leku, bądźb zwrot pieniędzy, ale równier wnież cofnięcie cie ulgi podatkowej -Kontrola wielkości sprzedaży y ( po przekroczeniu limitu sprzedaży y cena leku zostaje obniżona ona, lub firmy partycypują w kosztach refundacji )
27 Kiedy możliwe jest wdrożenie Instytucji współpłacenia Po pierwsze Negatywna ocena AOTM co efektywności kosztowej danej technologii Po drugie - precyzyjne zapisy ustawowe : decyzje płatnika p czy MZ cel umowy Dokładnie wskazane sankcje Precyzyjny opis warunków w umowy
28 negocjacji( bądźb zapisów prawnych)pozwalających cych wprowadzić Risk-sharing sharing 1.Odpowiedź na leki powinna być względnie szybka,łatwo atwo mierzalna i niedwuznaczna 2.Odpowiedź kliniczna na leki musi być połą łączona z wynikami, które zostały y udowodnione w III fazie badań klinicznych.zazwyczaj,dotyczy to leków w,których skuteczność była a mierzona surogatami ( np. leki obniżaj ające poziom cholesterolu) 3.Potrzeba dobrych metod monitorowania leczonych chorych
29 cd. 4.Obserwacje chorych powinny być prowadzone na dobrze zarządzanych oddziałach ach klinicznych? 5.W POZ leki podlegające negocjacjom współpłacenia powinno być kojarzone z poprawą jakości opieki medycznej.musi być pewność,że e leki będąb racjonalnie ordynowane :przy dobrym doborze chorych, w prawidłowych dawkach,w ścisłych wskazaniach a nawet z uwzględnieniem wszelkich danych farmakoekonomiki ( np..chronofarmakologii ) Right drug at the right dose to the right patient at the right time
30 Agencja Oceny Technologii Medycznych INNOWACYJNOŚĆ TECHNOLOGICZNA INNOWACYJNOŚĆ FARMAKOLOGICZNA (nowy mechanizm działania) ania) INNOWACYJNOŚĆ TERAPEUTYCZNA (kliniczna)
31 Kategorie Leków 1 Dodatkowa wartość terapeutyczna(dwt) Major Therapeutic Advance np.lek zmienia śmiertelność, wybitnie wydłuża życie 2 DWT, dotycząca ca jakości życia Ważne elementy jakości Drugorzędowe elementy jakości życia 3 Leki me-too
32 Klasy Zaleceń 1 EBM.CER na przydatność,skuteczność, bezpieczeństwo leku 2 Dane z badań nieprzekonywujące (np.badania non-inferiority inferiority) 3 SąS dowody na nieskuteczność czy wprost Szkodliwość danego leku.
33 Poziom wiarygodności Dane pochodzą z wielu badań klinicznych z Randomizacją lub metaanaliz (np. Biblioteka Cochrana) B-Dane pochodzą z pojedyńczego badania klinicznego z randomizacją lub dużych badań bez randomizacji C-Badania retrospektywne i/lub rejestry
34 Kryteria Innowacyjności ci w HAS (Francja) Są określanie arbitralnie przez Komitet Przejrzystości Stopnie innowacyjność śći: I- III najbardziej innowacyjne, szybki dostęp refundacyjny,znanie ceny,negocjacje cenowe drugoplanowe IV- możliwe finansowanie nawet,jeżeli eli cena nowego leku jest wyższa od komparatora (często leki poprawiające jakość życia ) V brak innowacyjności ci,refundacja tylko jeżeli eli cena nowości niższa niż komparatora.
35 Agencja Oceny Technologii Medycznych GRADACJA INNOWACYJNOŚCI CI wg La Revue Prescrire Przykłady z 2005 roku: BRAVO - RZECZYWISTY POSTĘP - PRZEWAGA nad obecnie dostępnymi (2) ZINC (WILZIN), PEMETREXED (MES) PRAWDOPODOBNIE PRZYDATNE (5) ZAVESCA, LYRICA (ból) NIC NOWEGO (10) PEMETREXED (R.P), STRONTIUM RANELATE, LYRICA (EPI), szczepionka p/cholerze NIEAKCEPTOWANE (8) CELEKOKSYB (ONSENAL), CETUXIMAB BRAK DOWODÓW, W, TRZEBA POCZEKAĆ (1) PORFIMER (PHOTOBARR)
36 NICE Appraisal Committee Podstawowe kryteria Wiarygodność dowodów w klinicznych Wiarygodność wyników w analizy ekonomicznej Górna granica opłacalno acalności ci (ICER) = pounds PKB/per capita Dodatkowo: Cięż ężkość choroby Stopień potrzeby klinicznej na daną technologię w populacji osob z rozpatrywanym wskazaniem Dostępno pność innej technologii w danym wskazaniu Potencjalny wpływ negatywnej decyzji o finansowaniu
37 NICE Appraisal Coomittee Rekomendacje a granica opłacalno acalnościci < PKB/per capita/qaly- Decyzja o akceptowalności ci technologii jako efektywnego dla NHS zużycia zasobów w oparte sąs głównie na wynikach analizy kosztów efektywności ICER PKB/QALY Decyzje o akceptowalności technologii,której wartość zazwyczaj wymaga rozważenia: Stopnia niepewności przy szacowaniu ICER Innowacyjności ci danej technologii Charakterystyki choroby i populacji otrzymujących daną technologię (kto odnieść może e największ kszą korzyść zdrowotną) ICER > PKB/QALY- górna granica opłacalno acalnościci Przyjęcie takiej technologii musi być poparte bardzo silnymi DOWODAMI NAUKOWYMI lub innymi argumentami - POLITYCZNYMI?
38 Ale warto pamięta tać, że IM mniej pieniędzy dzy,, im biedniejszy kraj, tym potrzeba więcej dowodów w naukowych ( Evidence )) na skuteczność nowej technologii niż w krajach bogatych!!
39 Rekomendacje cd. 5. Nie finansować 6. Zwiększy kszyć finansowanie 7. Zmniejszyć finansowanie 8. Nie zmieniać finansowania
40 Agencja Oceny Technologii Medycznych ORPHAN DRUG 1983 r., USA Lek jest zalecany pacjentom cierpiącym cym na rzadko występuj pujące choroby. Rozporządzenie UE 141/2000, 847/2000 Komitet ds. Leków w Sierocych Committee for Orphan Medicinal Products (COMP)
41 Agencja Oceny Technologii Medycznych CHOROBY RZADKIE UE 30 mln chorych USA mln CHORÓB B RZADKICH I ULTRA RZADKICH (a w latach 90. XX wieku tylko ) Japonia 2,5/ UE 5,0/ USA 7,0/ ULTRA RZADKIE 1:50 000/
42 Agencja Oceny Technologii Medycznych Pięć ograniczeń dla pełnej oceny skuteczności ci i bezpieczeństwa leków sierocych ( five( too s ): - too few za mała a liczebność populacji, - too simple za prosty schemat terapeutyczny, - too narrow (dosage range) za wąski w zakres stosowanych dawek, - too median-aged aged za małe e zróżnicowanie wiekowe grupy, - too brief za krótki okres obserwacji
43 Agencja Oceny Technologii Medycznych OPINIE RADY KONSULTACYJNEJ AOTM W związku zku z powołaniem przez Ministerstwo Zdrowia Zespołu u ds. Chorób b Rzadkich i Ultra Rzadkich,, Rada Konsultacyjna nie powinna wydawać rekomendacji dotyczących cych leków sierocych, a jedynie opinie dotyczące ce skuteczności ci i kosztów w efektywności wnioskowanych metod.
44 Dwie ostatnie dekady To olbrzymi postęp p w medycynie: leki generyczne (tanie( tanie) zaspokajają większo kszość potrzeb powszechnych chorób nowe leki w o obszarach zwłaszcza niszowych,, niezaspokajają niestety tych potrzeb. Zawsze paradoksalnie nieprawdopodobny postęp p zwiększa nierówno wności w społecze eczeństwie!
45 Leki Generyczne Trzy drogi rejestracji : Licencja Dowody biorównowa wnoważności well established use (WEU) Leki te generalnie nie podlegają ocenie AOTM. Pozostaje to (opinia refundacyjna ) w gestii ZESPOŁU U ds.. GOSPODARKI LEKIEM organu MZ>
46 Leki generyczne-wątpliwo tpliwości 1 Średnia równowar wnoważność biologiczna nie koniecznie wystarcza do zapewnienia równowar wnoważności biologicznej w przypadku leków w o szerokim i wąskim w zakresie terapeutycznym oraz preparatów retard 2 Nie należy y Wykorzystywać w badaniach równowar wnoważności tzw normalnych normalnych i zdrowych ochotników. 3 Sporne jest wykorzystywanie pojedyńczej dawki 4 Czas rozpadu postaci leku i rozpuszczanie postaci leku różnią się in n vitro i in n vivo 5 Substancje pomocnicze w generykach ( głośno g ostatnio O glikolu propylenowym ) itp. 6 Kopie leków biopochodych budzą najwiecej kontrowersji
47 Leki generyczne-wątpliwo tpliwości 1 Średnia równowar wnoważność biologiczna nie koniecznie wystarcza do zapewnienia równowar wnoważności biologicznej w przypadku leków w o szerokim i wąskim w zakresie terapeutycznym oraz preparatów retard 2 Nie należy y Wykorzystywać w badaniach równowar wnoważności tzw normalnych normalnych i zdrowych ochotników. 3 Sporne jest wykorzystywanie pojedyńczej dawki 4 Czas rozpadu postaci leku i rozpuszczanie postaci leku różnią się in n vitro i in n vivo 5 Substancje pomocnicze w generykach ( głośno g ostatnio O glikolu propylenowym ) itp. 6 Kopie leków biopochodych budzą najwiecej kontrowersji
48 Pokrywanie kosztów w leczenia ze środków w publicznych PYTANIA : 1-czy lista leków w refundowanych 2- może e programy terapeutyczne ściśle monitorowane(koszty,bezpieczeństwo,skuteczność ) Np..leki p-nowotworowe (Erlatynib,Xeloda) leki na Choroby Rzadkie(choroby spichrzeniowe) Leki stosowane w uzależnieniach (Zyban( Zyban) Może e to być przydatne w przyszłości przy negocjacjach cen (Risk( Sharing, pay back )
49 Polityka lekowa To nie bezkrytyczne dawanie pacjentom wielu nowych leków refundowanych, ale dbałość o bezpieczeństwo pacjentów. Pacjent nie rozumie, że jeżeli są ograniczenia do jakiejś terapii to nie jest zła wola decydentów, ale wynika to z przemyślanych decyzji.
50 Ponieważ... Lek jest mało skuteczny (przedłuża życie o 2-3 miesiące, a może jedynie przedłuża agonię?) Lek może być niebezpieczny, chociaż reklamowany jest jako super, np. Avastin (?) Lek może zrujnować budżet płatnika, nie dając oczekiwanych korzyści dla ZDROWIA PUBLICZNEGO (choroby rzadkie i ultra-rzadkie).
51 Jeżeli lek jest bardzo drogi, ale ma zachowany profil bezpieczeństwa i jest bardzo skuteczny (np.nowe leki w PBS) REFUNDOWAĆ! Tylko czy w ramach wykazów leków refundowanych czy w ramach programów terapeutycznych ścisle monitorowanych i kontrolowanej kwalifikacji chorych do terapii?
52 Brak skuteczności leku to też działanie niepożądane Tego można uniknąć! Brak skuteczności ponieważ: lekarz zlecił za małą dawkę lekarz dał drogi orginał i pacjent go nie zrealizował pacjent brał leki o nieodpowiedniej porze dnia pacjent zażywał leki z produktami żywnościowymi, płynami które zmieniały jego aktywność.
53 Pienądze są s Bezpańskie nie należą do nikogo, przepływaj ywają jedynie przez nasze ręce. r Nie sąs niczyją własnościa,, to raczej forma odpowiedzialności i od nas tylko zależy, czy spożytkujemy je właściwie.
Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska
 Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT) Słów kilka o HTA HTA nie jest: nauką o ochronie zdrowia nauką / analizą dot.
Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT) Słów kilka o HTA HTA nie jest: nauką o ochronie zdrowia nauką / analizą dot.
Finansowanie technologii sierocych bariery systemowe w Polsce
 Karolina Skóra Finansowanie technologii sierocych bariery systemowe w Polsce znaczenie dla ekonomiki zdrowia oraz sens oceny technologii sierocych względem progu opłacalności Choroby rzadkie i ultrarzadkie
Karolina Skóra Finansowanie technologii sierocych bariery systemowe w Polsce znaczenie dla ekonomiki zdrowia oraz sens oceny technologii sierocych względem progu opłacalności Choroby rzadkie i ultrarzadkie
Podejście AOTM do oceny wartościującej dla leków sierocych na podstawie dotychczasowych rekomendacji
 Podejście AOTM do oceny wartościującej dla leków sierocych na podstawie dotychczasowych rekomendacji Gabriela Ofierska-Sujkowska Agencja Oceny Technologii Medycznych Warszawa, 12.04.2013 r. Podejmowanie
Podejście AOTM do oceny wartościującej dla leków sierocych na podstawie dotychczasowych rekomendacji Gabriela Ofierska-Sujkowska Agencja Oceny Technologii Medycznych Warszawa, 12.04.2013 r. Podejmowanie
Wpływ nowych terapii na budżet NFZ czy stać nas na refundację?
 Wpływ nowych terapii na budżet NFZ czy stać nas na refundację? Leszek Stabrawa W A R S Z A W A, 1 1 s i e r p n i a 2 0 1 6 Dostęp do innowacyjnych terapii w Polsce o Jednym z celów ustawy refundacyjnej
Wpływ nowych terapii na budżet NFZ czy stać nas na refundację? Leszek Stabrawa W A R S Z A W A, 1 1 s i e r p n i a 2 0 1 6 Dostęp do innowacyjnych terapii w Polsce o Jednym z celów ustawy refundacyjnej
Postulowane zmiany w ustawie refundacyjnej wydzielony budżet na leki oceniane w podejściu egalitarnym uzasadnienie ceny
 Postulowane zmiany w ustawie refundacyjnej wydzielony budżet na leki oceniane w podejściu egalitarnym uzasadnienie ceny Lek. Med. Krzysztof Łanda Dlaczego refundacja leków sierocych wymaga szczególnego
Postulowane zmiany w ustawie refundacyjnej wydzielony budżet na leki oceniane w podejściu egalitarnym uzasadnienie ceny Lek. Med. Krzysztof Łanda Dlaczego refundacja leków sierocych wymaga szczególnego
Granice opłacalności i rozwiązanie takie jak FWR dla IPF i innych chorób ultrarzadkich
 Granice opłacalności i rozwiązanie takie jak FWR dla IPF i innych chorób ultrarzadkich Anna Kordecka K R A K Ó W, 1 8 l i s t o p a d a 2 0 1 5 Refundacja: co chce wiedzieć decydent? 1. Czy jest to technologia
Granice opłacalności i rozwiązanie takie jak FWR dla IPF i innych chorób ultrarzadkich Anna Kordecka K R A K Ó W, 1 8 l i s t o p a d a 2 0 1 5 Refundacja: co chce wiedzieć decydent? 1. Czy jest to technologia
Sens oceny wartościującej względem progu opłacalności w onkologii. Lek. med. Krzysztof Łanda
 Sens oceny wartościującej względem progu opłacalności w onkologii Lek. med. Krzysztof Łanda Refundacja: co chce wiedzieć decydent? 1. Czy jest to technologia o udowodnionej efektywności? 2. Jaka jest siła
Sens oceny wartościującej względem progu opłacalności w onkologii Lek. med. Krzysztof Łanda Refundacja: co chce wiedzieć decydent? 1. Czy jest to technologia o udowodnionej efektywności? 2. Jaka jest siła
Miejsce AOTM w systemie refundacji leków
 Miejsce AOTM w systemie refundacji leków Lek. Iga Lipska Kierownik Wydziału Oceny Technologii Medycznych AOTM Spotkanie - Studenckie Koło Farmakoekonomiki, Warszawa, 24.04.2008 Rada Konsultacyjna, Warszawa
Miejsce AOTM w systemie refundacji leków Lek. Iga Lipska Kierownik Wydziału Oceny Technologii Medycznych AOTM Spotkanie - Studenckie Koło Farmakoekonomiki, Warszawa, 24.04.2008 Rada Konsultacyjna, Warszawa
Kwestie etyczne związane z leczeniem chorób rzadkich w Polsce. Prezes KFO - Mirosław Zieliński
 Kwestie etyczne związane z leczeniem chorób rzadkich w Polsce Prezes KFO - Mirosław Zieliński Imperatyw etyczny: Pomoc innemu w potrzebie jest wpisana w naturę człowieka... Etyka a prawo... w przypadku
Kwestie etyczne związane z leczeniem chorób rzadkich w Polsce Prezes KFO - Mirosław Zieliński Imperatyw etyczny: Pomoc innemu w potrzebie jest wpisana w naturę człowieka... Etyka a prawo... w przypadku
Agencja Oceny Technologii Medycznych polska droga do sukcesu
 Agencja Oceny Technologii Medycznych polska droga do sukcesu Wojciech Matusewicz Agencja Oceny Technologii Medycznych Warszawa, dn. 07.10.2013 Miejsce AOTM w polskim systemie ochrony zdrowia AOTM MZ NFZ
Agencja Oceny Technologii Medycznych polska droga do sukcesu Wojciech Matusewicz Agencja Oceny Technologii Medycznych Warszawa, dn. 07.10.2013 Miejsce AOTM w polskim systemie ochrony zdrowia AOTM MZ NFZ
Szanse i zagrożenia przygotowania RSS na podstawie raportu HTA
 Szanse i zagrożenia przygotowania RSS na podstawie raportu HTA Co może być istotne w procesie tworzenia RSS? Magdalena Władysiuk Ustawa refundacyjna W krajach o średnim dochodzie RSSs są szansą na finansowanie
Szanse i zagrożenia przygotowania RSS na podstawie raportu HTA Co może być istotne w procesie tworzenia RSS? Magdalena Władysiuk Ustawa refundacyjna W krajach o średnim dochodzie RSSs są szansą na finansowanie
Farmakoekonomika podstawy. Paweł Petryszyn Katedra i Zakład Farmakologii Klinicznej UM we Wrocławiu
 Farmakoekonomika podstawy Paweł Petryszyn Katedra i Zakład Farmakologii Klinicznej UM we Wrocławiu Dyrektywa przejrzystości z 1988 r. Obowiązek uzasadniania podjętych decyzji dotyczących cen i refundacji
Farmakoekonomika podstawy Paweł Petryszyn Katedra i Zakład Farmakologii Klinicznej UM we Wrocławiu Dyrektywa przejrzystości z 1988 r. Obowiązek uzasadniania podjętych decyzji dotyczących cen i refundacji
Warszawa, 20 kwietnia - Mirosław Zieliński LEKI SIEROCE. Dostępność Ograniczenia Wyzwania
 Warszawa, 20 kwietnia - Mirosław Zieliński LEKI SIEROCE Dostępność Ograniczenia Wyzwania Rzadka choroba - Rozporządzenie UE 141/2000 art. 3 : za rzadką chorobę uważa się stan chorobowy występujący nie
Warszawa, 20 kwietnia - Mirosław Zieliński LEKI SIEROCE Dostępność Ograniczenia Wyzwania Rzadka choroba - Rozporządzenie UE 141/2000 art. 3 : za rzadką chorobę uważa się stan chorobowy występujący nie
Chemioterapia niestandardowa
 Chemioterapia niestandardowa - Jak podjąć najlepszą decyzję w świetle obowiązujących przepisów? Przebieg procesu decyzyjnego płatnika na podstawie Dolnośląskiego Oddziału Wojewódzkiego NFZ Joanna Krzywkowska
Chemioterapia niestandardowa - Jak podjąć najlepszą decyzję w świetle obowiązujących przepisów? Przebieg procesu decyzyjnego płatnika na podstawie Dolnośląskiego Oddziału Wojewódzkiego NFZ Joanna Krzywkowska
Warszawa, 22 marca Mirosław Zieliński LEKI SIEROCE. Dostępność w Polsce i innych krajach UE
 Warszawa, 22 marca 2016 - Mirosław Zieliński LEKI SIEROCE Dostępność w Polsce i innych krajach UE Warszawa, 22 marca 2016 - Mirosław Zieliński LEKI SIEROCE Dostępność, ograniczenia i wyzwania dla Polski
Warszawa, 22 marca 2016 - Mirosław Zieliński LEKI SIEROCE Dostępność w Polsce i innych krajach UE Warszawa, 22 marca 2016 - Mirosław Zieliński LEKI SIEROCE Dostępność, ograniczenia i wyzwania dla Polski
Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej. Szanowny Panie Marszałku,
 Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej Szanowny Panie Marszałku, w odpowiedzi na interpelację nr 9087 Posłów na Sejm RP: Krystyny Sibińskiej, Marii Janyska,
Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej Szanowny Panie Marszałku, w odpowiedzi na interpelację nr 9087 Posłów na Sejm RP: Krystyny Sibińskiej, Marii Janyska,
Miary innowacyjności w rankingach ograniczenia dostępu do innowacyjnych technologii medycznych w ramach składki podstawowej
 Miary innowacyjności w rankingach ograniczenia dostępu do innowacyjnych technologii medycznych w ramach składki podstawowej Krzysztof Łanda Fundacja Watch Health Care Rozwój gospodarczy a rozwój medycyny
Miary innowacyjności w rankingach ograniczenia dostępu do innowacyjnych technologii medycznych w ramach składki podstawowej Krzysztof Łanda Fundacja Watch Health Care Rozwój gospodarczy a rozwój medycyny
QALY, RSS i inne składowe wpływające na decyzje refundacyjne. Doktor nauk o zdrowiu Radunka Cvejić
 QALY, RSS i inne składowe wpływające na decyzje refundacyjne Doktor nauk o zdrowiu Radunka Cvejić Warszawa, 27.10.2015 Kryteria podejmowania decyzji Art. 12 Minister właściwy do spraw zdrowia, mając na
QALY, RSS i inne składowe wpływające na decyzje refundacyjne Doktor nauk o zdrowiu Radunka Cvejić Warszawa, 27.10.2015 Kryteria podejmowania decyzji Art. 12 Minister właściwy do spraw zdrowia, mając na
Analiza kosztowo-efektywnościowa (Cost-effectiveness analysis)
 Analiza kosztowo-efektywnościowa (Cost-effectiveness analysis) Farmakoekonomika Metody wspomagające optymalne wykorzystanie środków finansowych w ochronie zdrowia przy wprowadzaniu nowych terapii oraz
Analiza kosztowo-efektywnościowa (Cost-effectiveness analysis) Farmakoekonomika Metody wspomagające optymalne wykorzystanie środków finansowych w ochronie zdrowia przy wprowadzaniu nowych terapii oraz
Krótko na temat obowiązujących aktów prawnych, które regulują HTA. Co nowego wprowadziły minimalne wymagania i ustawa refundacyjna?
 KRYTYCZNE ETAPY OPRACOWYWANIA HTA DOSSIER - CZYLI JAK UNIKNĄĆ ODRZUCENIA Z PRZYCZYN METODOLOGICZNYCH? FORMALNE WYMOGI ANALITYCZNE PRZY SKŁADANIU WNIOSKÓW REFUNDACYJNYCH KUCHNIA ANALIZ ; WPŁYW ZMIAN LEGISLACYJNYCH
KRYTYCZNE ETAPY OPRACOWYWANIA HTA DOSSIER - CZYLI JAK UNIKNĄĆ ODRZUCENIA Z PRZYCZYN METODOLOGICZNYCH? FORMALNE WYMOGI ANALITYCZNE PRZY SKŁADANIU WNIOSKÓW REFUNDACYJNYCH KUCHNIA ANALIZ ; WPŁYW ZMIAN LEGISLACYJNYCH
Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się
 (BIA) komu i po co Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się Not everything that can be counted counts, and not everything that counts can be counted A.
(BIA) komu i po co Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się Not everything that can be counted counts, and not everything that counts can be counted A.
Minister van Sociale Zaken en Volksgezondheid
 http://www.maggiedeblock.be/2005/11/18/resolutie-inzake-de-klinischebiologie/ Minister van Sociale Zaken en Volksgezondheid Obecna Minister Zdrowia Maggy de Block wraz z Yolande Avontroodt, i Hilde Dierickx
http://www.maggiedeblock.be/2005/11/18/resolutie-inzake-de-klinischebiologie/ Minister van Sociale Zaken en Volksgezondheid Obecna Minister Zdrowia Maggy de Block wraz z Yolande Avontroodt, i Hilde Dierickx
Wyniki ankiety Polityka lekowa
 Wyniki ankiety Polityka lekowa Innowacyjna, dostępna, transparentna Ankieta przygotowana przez Izbę Gospodarczą FARMACJA POLSKA i Instytut Innowacji i Odpowiedzialnego Rozwoju INNOWO miała na celu zbadanie
Wyniki ankiety Polityka lekowa Innowacyjna, dostępna, transparentna Ankieta przygotowana przez Izbę Gospodarczą FARMACJA POLSKA i Instytut Innowacji i Odpowiedzialnego Rozwoju INNOWO miała na celu zbadanie
Przyszłość refundacji i modeli cenowych gdzie będzie rynek polski za kilka lat? VI POLAND PHARMA COMMERCE FORUM
 Przyszłość refundacji i modeli cenowych gdzie będzie rynek polski za kilka lat? VI POLAND PHARMA COMMERCE FORUM Czerwiec 2015 Total spending on health, % GDP Całkowite wydatki na ochronę zdrowia Polska
Przyszłość refundacji i modeli cenowych gdzie będzie rynek polski za kilka lat? VI POLAND PHARMA COMMERCE FORUM Czerwiec 2015 Total spending on health, % GDP Całkowite wydatki na ochronę zdrowia Polska
Szanowny Panie Marszałku! W odpowiedzi na zapytanie pana Czesława Hoca, posła na Sejm RP, przesłane przy piśmie z dnia 17 września 2014 r.
 Szanowny Panie Marszałku! W odpowiedzi na zapytanie pana Czesława Hoca, posła na Sejm RP, przesłane przy piśmie z dnia 17 września 2014 r., znak: SPS-024-7311/14, w sprawie potrzeby zapewnienia terapii
Szanowny Panie Marszałku! W odpowiedzi na zapytanie pana Czesława Hoca, posła na Sejm RP, przesłane przy piśmie z dnia 17 września 2014 r., znak: SPS-024-7311/14, w sprawie potrzeby zapewnienia terapii
Rola AOTM w procesie kształtowania dostępności do szczepień ochronnych
 Rola AOTM w procesie kształtowania dostępności do szczepień ochronnych experience makes the difference Robert Plisko Świadczenie gwarantowane Świadczenie gwarantowane - świadczenie opieki zdrowotnej finansowane
Rola AOTM w procesie kształtowania dostępności do szczepień ochronnych experience makes the difference Robert Plisko Świadczenie gwarantowane Świadczenie gwarantowane - świadczenie opieki zdrowotnej finansowane
Schemat wystąpienia. Programy lekowe - > Programy terapeutyczne. Program lekowy Zarządzenie 36/2005
 Coverage of highly expensive drugs by a public payer, on the example of Polish NHF theory and practice Schemat wystąpienia Finansowanie szczególnie drogich leków przez publicznego płatnika na przykładzie
Coverage of highly expensive drugs by a public payer, on the example of Polish NHF theory and practice Schemat wystąpienia Finansowanie szczególnie drogich leków przez publicznego płatnika na przykładzie
Finansowanie świadczeń w ramach hematoonkologii miejsca na porozumienia podziału ryzyka. Magdalena Władysiuk, MD, MBA
 Finansowanie świadczeń w ramach hematoonkologii miejsca na porozumienia podziału ryzyka Magdalena Władysiuk, MD, MBA Wydatki NFZ w hematonkologii Wydatki 2010 Onkologia Hematologia JGP 1 411 500 000 zł
Finansowanie świadczeń w ramach hematoonkologii miejsca na porozumienia podziału ryzyka Magdalena Władysiuk, MD, MBA Wydatki NFZ w hematonkologii Wydatki 2010 Onkologia Hematologia JGP 1 411 500 000 zł
Zasadność finansowania mechanicznej trombektomii w leczeniu udaru mózgu. Dr n. med. Przemysław Ryś
 Zasadność finansowania mechanicznej trombektomii w leczeniu udaru mózgu Dr n. med. Przemysław Ryś Czy trombektomia powinna być refundowana? Jakie kryteria brane są pod uwagę? Kto podejmuje decyzję refundacyjną?
Zasadność finansowania mechanicznej trombektomii w leczeniu udaru mózgu Dr n. med. Przemysław Ryś Czy trombektomia powinna być refundowana? Jakie kryteria brane są pod uwagę? Kto podejmuje decyzję refundacyjną?
Wydłużenie życia chorych z rakiem płuca - nowe możliwości
 Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
10 postulatów pacjentów onkologicznych do systemu refundacyjnego. Spotkanie w Ministerstwie Zdrowia
 10 postulatów pacjentów onkologicznych do systemu refundacyjnego Spotkanie w Ministerstwie Zdrowia 22.11.2016 10 postulatów pacjentów onkologicznych do systemu refundacyjnego Postulaty środowiska pacjentów
10 postulatów pacjentów onkologicznych do systemu refundacyjnego Spotkanie w Ministerstwie Zdrowia 22.11.2016 10 postulatów pacjentów onkologicznych do systemu refundacyjnego Postulaty środowiska pacjentów
Podstawowe założenia i zmiany. wprowadzane przez projekt. ustawy refundacyjnej
 Podstawowe założenia i zmiany wprowadzane przez projekt ustawy refundacyjnej 1. Geneza zmian 2. Sposób dojścia do proponowanych rozwiązań 3. Wprowadzone zmiany organizacyjne 4. Podstawowe różnice pomiędzy
Podstawowe założenia i zmiany wprowadzane przez projekt ustawy refundacyjnej 1. Geneza zmian 2. Sposób dojścia do proponowanych rozwiązań 3. Wprowadzone zmiany organizacyjne 4. Podstawowe różnice pomiędzy
Nowa ustawa refundacyjna.
 Nowa ustawa refundacyjna. Co nowego dla pacjenta onkologicznego? Forum Organizacji Pacjentów Onkologicznych - Warszawa, 26 kwietnia 2012 Magdalena Kręczkowska, Fundacja Onkologiczna DUM SPIRO-SPERO USTAWA
Nowa ustawa refundacyjna. Co nowego dla pacjenta onkologicznego? Forum Organizacji Pacjentów Onkologicznych - Warszawa, 26 kwietnia 2012 Magdalena Kręczkowska, Fundacja Onkologiczna DUM SPIRO-SPERO USTAWA
POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED.
 POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED Izabela Pieniążek Klasyczne dossier? Rozporządzenie MZ w sprawie MINIMALNYCH
POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED Izabela Pieniążek Klasyczne dossier? Rozporządzenie MZ w sprawie MINIMALNYCH
Faramkoekonomiczna ocena leków biopodobnych. dr Michał Seweryn
 Faramkoekonomiczna ocena leków biopodobnych dr Michał Seweryn Klasyczny problem ekonomii Potrzeby Dobra Farmakoekonomika (ekonomiczna ocena technologii medycznych) Celem badania farmakoekonomicznego jest
Faramkoekonomiczna ocena leków biopodobnych dr Michał Seweryn Klasyczny problem ekonomii Potrzeby Dobra Farmakoekonomika (ekonomiczna ocena technologii medycznych) Celem badania farmakoekonomicznego jest
Proces refundacyjny w Polsce Rola Agencji Oceny Technologii Medycznych i Taryfikacji
 Proces refundacyjny w Polsce Rola Agencji Oceny Technologii Medycznych i Taryfikacji Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT) Główni gracze w sytemie MINISTERSTWO ZDROWIA NARODOWY FUNDUSZ
Proces refundacyjny w Polsce Rola Agencji Oceny Technologii Medycznych i Taryfikacji Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT) Główni gracze w sytemie MINISTERSTWO ZDROWIA NARODOWY FUNDUSZ
Ustalanie ceny leku w oparciu o jego wartość (value based pricing, VBP)
 Lek. med. Krzysztof Łanda Landa@htaaudit.eu Ustalanie ceny leku w oparciu o jego wartość (value based pricing, VBP) Czynniki wpływające na ceny EKONOMICZNE Rynkowe Konkurencja firm Analiza wpływu na budżet
Lek. med. Krzysztof Łanda Landa@htaaudit.eu Ustalanie ceny leku w oparciu o jego wartość (value based pricing, VBP) Czynniki wpływające na ceny EKONOMICZNE Rynkowe Konkurencja firm Analiza wpływu na budżet
Ocena leków sierocych w Polsce i innych krajach Europy i świata. lek. Magdalena Władysiuk, MBA
 Ocena leków sierocych w Polsce i innych krajach Europy i świata lek. Magdalena Władysiuk, MBA Definicja chorób rzadkich Kraj / organizacja Choroba rzadka rozpowszechnienie na 100 000 Źródło definicji USA
Ocena leków sierocych w Polsce i innych krajach Europy i świata lek. Magdalena Władysiuk, MBA Definicja chorób rzadkich Kraj / organizacja Choroba rzadka rozpowszechnienie na 100 000 Źródło definicji USA
Pozytywne skutki wdrożenia ustawy refundacyjnej - stanowisko rządu
 Warszawa, 23 marca 2017 r. Stanowisko organizacji wspierających pacjentów onkologicznych do sprawozdania z wykonania ustawy z dnia 12 maja 2011 r. o refundacji leków, środków spożywczych specjalnego przeznaczenia
Warszawa, 23 marca 2017 r. Stanowisko organizacji wspierających pacjentów onkologicznych do sprawozdania z wykonania ustawy z dnia 12 maja 2011 r. o refundacji leków, środków spożywczych specjalnego przeznaczenia
Rola HTA w ustalaniu cen leków i refundacji
 Rola HTA w ustalaniu cen leków i refundacji Dr Krzysztof Łanda HTA Audit Treść 1. Wprowadzenie 2. Co jest ważniejsze: decyzje dotyczące ustalania cen czy refundacji? 3. Przykłady umów podziału ryzyka przy
Rola HTA w ustalaniu cen leków i refundacji Dr Krzysztof Łanda HTA Audit Treść 1. Wprowadzenie 2. Co jest ważniejsze: decyzje dotyczące ustalania cen czy refundacji? 3. Przykłady umów podziału ryzyka przy
ABC oceny technologii medycznych. Skąd się biorą ceny leków?
 ABC oceny technologii medycznych. Skąd się biorą ceny leków? Michał Jachimowicz Warszawa, 14 października 2014 roku MAHTA Sp. z o.o. ul. Rejtana 17/5, 02-516 Warszawa, tel.: 22 542 41 54, biuro@mahta.pl
ABC oceny technologii medycznych. Skąd się biorą ceny leków? Michał Jachimowicz Warszawa, 14 października 2014 roku MAHTA Sp. z o.o. ul. Rejtana 17/5, 02-516 Warszawa, tel.: 22 542 41 54, biuro@mahta.pl
Prof. Karina Jahnz-Różyk Wojskowy Instytut Medyczny
 Prof. Karina Jahnz-Różyk Wojskowy Instytut Medyczny Przewlekła choroba układu oddechowego przebiegająca z dusznością Około 2 mln chorych w Polsce, ale tylko 1/3 jest zdiagnozowana (400-500 tys) Brak leczenia
Prof. Karina Jahnz-Różyk Wojskowy Instytut Medyczny Przewlekła choroba układu oddechowego przebiegająca z dusznością Około 2 mln chorych w Polsce, ale tylko 1/3 jest zdiagnozowana (400-500 tys) Brak leczenia
Farmakoekonomika ekonomika farmacji
 Farmakoekonomika ekonomika farmacji Czym jest farmakoekonomika? ekonomia farmacja medycyna farmkoekonomika ekonomia farmakoekonomika ekonomika ochrony zdrowia Analiza farmakoekonomiczna Analiza farmakoekonomiczna
Farmakoekonomika ekonomika farmacji Czym jest farmakoekonomika? ekonomia farmacja medycyna farmkoekonomika ekonomia farmakoekonomika ekonomika ochrony zdrowia Analiza farmakoekonomiczna Analiza farmakoekonomiczna
HTA (Health Technology Assessment)
 Krzysztof Łanda 1 z 5 HTA (Health Technology Assessment) Ocena leków stosowanych w okre lonych wskazaniach podlega tym samym generalnym regu om, co inne technologie terapeutyczne, jednak specyfika interwencji
Krzysztof Łanda 1 z 5 HTA (Health Technology Assessment) Ocena leków stosowanych w okre lonych wskazaniach podlega tym samym generalnym regu om, co inne technologie terapeutyczne, jednak specyfika interwencji
Kim jesteśmy? Od sierpnia 2012 r. Alivia jest organizacją pożytku publicznego. PROGRAM SKARBONKA PROGRAM CZERWONA SKRZYNKA
 Kim jesteśmy? Alivia - Fundacja Onkologiczna Osób Młodych powstała w 2010 r. na bazie doświadczeń Agaty Polińskiej (obecnie wiceprezes fundacji), która w wieku 28 lat zachorowała na raka piersi. Alivia
Kim jesteśmy? Alivia - Fundacja Onkologiczna Osób Młodych powstała w 2010 r. na bazie doświadczeń Agaty Polińskiej (obecnie wiceprezes fundacji), która w wieku 28 lat zachorowała na raka piersi. Alivia
Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych?
 Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych? prof. dr hab. med.. Piotr Fiedor Warszawski Uniwersytet Medyczny
Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych? prof. dr hab. med.. Piotr Fiedor Warszawski Uniwersytet Medyczny
Czy AOTM uczestniczy w procesie kształtowania dostępności do szczepień ochronnych? Magdalena Władysiuk MD, MBA
 Czy AOTM uczestniczy w procesie kształtowania dostępności do szczepień ochronnych? Magdalena Władysiuk MD, MBA Immunoprofilaktyka chorób zakaźnych Uniknięcie negatywnych konsekwencji zdrowotnych związanych
Czy AOTM uczestniczy w procesie kształtowania dostępności do szczepień ochronnych? Magdalena Władysiuk MD, MBA Immunoprofilaktyka chorób zakaźnych Uniknięcie negatywnych konsekwencji zdrowotnych związanych
PODSUMOWANIE seminarium na temat ustawy refundacyjnej
 PODSUMOWANIE seminarium na temat ustawy refundacyjnej Adw. Paulina Kieszkowska Knapik Adw. Katarzyna Czyżewska BUDŻET NA REFUNDACJĘ I TZW. PAY BACK Zmiana zasad kształtowania budżetu wydatków na refundację:
PODSUMOWANIE seminarium na temat ustawy refundacyjnej Adw. Paulina Kieszkowska Knapik Adw. Katarzyna Czyżewska BUDŻET NA REFUNDACJĘ I TZW. PAY BACK Zmiana zasad kształtowania budżetu wydatków na refundację:
Lek. med. Krzysztof Łanda. Niekonstytucyjna nierówność dostępu do chemioterapii niestandardowej na obszarze Polski
 Lek. med. Krzysztof Łanda Niekonstytucyjna nierówność dostępu do chemioterapii niestandardowej na obszarze Polski GENEZA: ch/ns i zapomnianej już (?) f/ns 1. Wentyl bezpieczeństwa systemu (tak jak ID wyjątkowe,
Lek. med. Krzysztof Łanda Niekonstytucyjna nierówność dostępu do chemioterapii niestandardowej na obszarze Polski GENEZA: ch/ns i zapomnianej już (?) f/ns 1. Wentyl bezpieczeństwa systemu (tak jak ID wyjątkowe,
Rynek leków. generycznych. w Polsce i innowacyjnych. Prognozy rozwoju na lata Data publikacji: II kwartał 2012
 Rynek leków generycznych i innowacyjnych w Polsce 2012 Prognozy rozwoju na lata 2012-2014 Data publikacji: II kwartał 2012 Język: polski, angielski Słowo od autora Ustawa refundacyjna, która weszła w życie
Rynek leków generycznych i innowacyjnych w Polsce 2012 Prognozy rozwoju na lata 2012-2014 Data publikacji: II kwartał 2012 Język: polski, angielski Słowo od autora Ustawa refundacyjna, która weszła w życie
Terapie przełomowe: konsekwencje etyczne
 Terapie przełomowe: konsekwencje etyczne Zbigniew Szawarski Narodowy Instytut Zdrowia Publicznego PZH Seminarium WHC, Warszawa 27.I.2016 Nowe jest lepsze! Nowe odkrycia wiemy więcej Nowe terapie ( = terapie
Terapie przełomowe: konsekwencje etyczne Zbigniew Szawarski Narodowy Instytut Zdrowia Publicznego PZH Seminarium WHC, Warszawa 27.I.2016 Nowe jest lepsze! Nowe odkrycia wiemy więcej Nowe terapie ( = terapie
Nowoczesne metody pricingu. Modele umów dotyczących podziału ryzyka
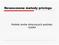 Nowoczesne metody pricingu Modele umów dotyczących podziału ryzyka Lata 1980-2005 Trend wzrostu w 15 krajach OECD nakłady na leki, nakłady na ochronę zdrowia, PKB źródło: OECD Health Data 2007 Raport OECD,
Nowoczesne metody pricingu Modele umów dotyczących podziału ryzyka Lata 1980-2005 Trend wzrostu w 15 krajach OECD nakłady na leki, nakłady na ochronę zdrowia, PKB źródło: OECD Health Data 2007 Raport OECD,
Badania obserwacyjne w ocenie bezpieczeństwa leków This gentle murmur it could be stings of remorse
 Badania obserwacyjne w ocenie bezpieczeństwa leków This gentle murmur it could be stings of remorse Magdalena Władysiuk 1. Pharmacovigilance: Co to jest pharmacovigilance? Podstawowe założenia systemu
Badania obserwacyjne w ocenie bezpieczeństwa leków This gentle murmur it could be stings of remorse Magdalena Władysiuk 1. Pharmacovigilance: Co to jest pharmacovigilance? Podstawowe założenia systemu
 www.korektorzdrowia.pl www.watchhealthcare.eu Dostępność opieki hematologicznej w Polsce na podstawie danych z rankingów i barometru Fundacji Watch Health Care (WHC) Lek. med. Krzysztof Łanda Podstawowe
www.korektorzdrowia.pl www.watchhealthcare.eu Dostępność opieki hematologicznej w Polsce na podstawie danych z rankingów i barometru Fundacji Watch Health Care (WHC) Lek. med. Krzysztof Łanda Podstawowe
Nagradzanie innowacyjno ci versus leki generyczne (odtwórcze)
 Tomasz Laczewski 1 z 5 Nagradzanie innowacyjno ci versus leki generyczne (odtwórcze) Rados aw Rud /Tomasz Laczewski HTA Audit Autorzy rozdzia u: Iwona Skrzekowska Baran, Krzysztof anda, Magdalena W adysiuk,
Tomasz Laczewski 1 z 5 Nagradzanie innowacyjno ci versus leki generyczne (odtwórcze) Rados aw Rud /Tomasz Laczewski HTA Audit Autorzy rozdzia u: Iwona Skrzekowska Baran, Krzysztof anda, Magdalena W adysiuk,
Plany nowelizacji ustawy refundacyjnej - perspektywa pacjentów
 Plany nowelizacji ustawy refundacyjnej - perspektywa pacjentów Ewa Borek, Fundacja MY Pacjenci PROJEKT WSPÓŁFINANSOWANY PRZEZ SZWAJCARIĘ W RAMACH SZWAJCARSKIEGO PROGRAMU WSPÓŁPRACY Z NOWYMI KRAJAMI CZŁONKOWSKIMI
Plany nowelizacji ustawy refundacyjnej - perspektywa pacjentów Ewa Borek, Fundacja MY Pacjenci PROJEKT WSPÓŁFINANSOWANY PRZEZ SZWAJCARIĘ W RAMACH SZWAJCARSKIEGO PROGRAMU WSPÓŁPRACY Z NOWYMI KRAJAMI CZŁONKOWSKIMI
Promocja konsultacji społecznych w ochronie zdrowia
 Promocja konsultacji społecznych w ochronie zdrowia PROJEKT WSPÓŁFINANSOWANY PRZEZ SZWAJCARIĘ W RAMACH SZWAJCARSKIEGO PROGRAMU WSPÓŁPRACY Z NOWYMI KRAJAMI CZŁONKOWSKIMI UNII EUROPEJSKIEJ Maria Libura Instytut
Promocja konsultacji społecznych w ochronie zdrowia PROJEKT WSPÓŁFINANSOWANY PRZEZ SZWAJCARIĘ W RAMACH SZWAJCARSKIEGO PROGRAMU WSPÓŁPRACY Z NOWYMI KRAJAMI CZŁONKOWSKIMI UNII EUROPEJSKIEJ Maria Libura Instytut
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 182/2013 z dnia 9 września 2013 r. w sprawie oceny leku Iressa (gefitynib) we wskazaniu leczenie niedrobnokomórkowego
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 182/2013 z dnia 9 września 2013 r. w sprawie oceny leku Iressa (gefitynib) we wskazaniu leczenie niedrobnokomórkowego
PODSTAWY FARMAKOEKONOMIKI
 PODSTAWY FARMAKOEKONOMIKI FARMAKOEKONOMIKA Pharmakon lek, oikonomia oszczędność Jest to nowoczesna dziedzina wiedzy, obejmująca elementy: farmakologii, medycyny klinicznej, statystyki medycznej oraz ekonomii,
PODSTAWY FARMAKOEKONOMIKI FARMAKOEKONOMIKA Pharmakon lek, oikonomia oszczędność Jest to nowoczesna dziedzina wiedzy, obejmująca elementy: farmakologii, medycyny klinicznej, statystyki medycznej oraz ekonomii,
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 111/2013 z dnia 26 sierpnia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Zoladex,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 111/2013 z dnia 26 sierpnia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Zoladex,
Fundusz ratunkowy jako perspektywa dla leczenia osób z chorobami rzadkimi
 Fundusz ratunkowy jako perspektywa dla leczenia osób z chorobami rzadkimi Wiesław Wiktor Jędrzejczak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawskiego Uniwersytetu Medycznego
Fundusz ratunkowy jako perspektywa dla leczenia osób z chorobami rzadkimi Wiesław Wiktor Jędrzejczak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawskiego Uniwersytetu Medycznego
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 5/2012 z dnia 27 lutego 2012 r. w zakresie zakwalifikowania/niezasadności zakwalifikowania leku Valdoxan (agomelatinum)
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 5/2012 z dnia 27 lutego 2012 r. w zakresie zakwalifikowania/niezasadności zakwalifikowania leku Valdoxan (agomelatinum)
Struktura wydatków na zdrowie Rodzaje ubezpieczeń Rynek ubezpieczeń zdrowotnych w Polsce i Europie Potencjał rozwoju ubezpieczeń zdrowotnych i
 Struktura wydatków na zdrowie Rodzaje ubezpieczeń Rynek ubezpieczeń zdrowotnych w Polsce i Europie Potencjał rozwoju ubezpieczeń zdrowotnych i abonamentów medycznych w Polsce Propozycje Ministerstwa Zdrowia
Struktura wydatków na zdrowie Rodzaje ubezpieczeń Rynek ubezpieczeń zdrowotnych w Polsce i Europie Potencjał rozwoju ubezpieczeń zdrowotnych i abonamentów medycznych w Polsce Propozycje Ministerstwa Zdrowia
Aneks II. Wnioski naukowe
 Aneks II Wnioski naukowe 7 Wnioski naukowe Federalny Instytut Leków i Wyrobów Medycznych (BfArM), Niemcy, i Inspektorat Opieki Zdrowotnej (IGZ) Ministerstwa Zdrowia Holandii przeprowadziły wspólną inspekcję
Aneks II Wnioski naukowe 7 Wnioski naukowe Federalny Instytut Leków i Wyrobów Medycznych (BfArM), Niemcy, i Inspektorat Opieki Zdrowotnej (IGZ) Ministerstwa Zdrowia Holandii przeprowadziły wspólną inspekcję
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 139/2014 z dnia 2 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Giotrif,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 139/2014 z dnia 2 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Giotrif,
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 380/2014 z dnia 29 grudnia 2014 r. w sprawie zasadności objęcia refundacją leku Mimpara (cinacalcetum) w zakresie
Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 380/2014 z dnia 29 grudnia 2014 r. w sprawie zasadności objęcia refundacją leku Mimpara (cinacalcetum) w zakresie
Forum Organizacji Pacjentów Onkologicznych. Problemy dostępu do leczenia
 Forum Organizacji Pacjentów Onkologicznych Problemy dostępu do leczenia Warszawa, 26 kwietnia 2012 1. CIĄGŁOŚĆ LECZENIA ONKOLOGICZNEGO 2. REGULACJA DOSTĘPU DO LECZENIA NA POZIOMIE ROZPORZĄDZEŃ/ZARZĄDZEŃ
Forum Organizacji Pacjentów Onkologicznych Problemy dostępu do leczenia Warszawa, 26 kwietnia 2012 1. CIĄGŁOŚĆ LECZENIA ONKOLOGICZNEGO 2. REGULACJA DOSTĘPU DO LECZENIA NA POZIOMIE ROZPORZĄDZEŃ/ZARZĄDZEŃ
www.korektorzdrowia.pl www.watchhealthcare.eu
 www.korektorzdrowia.pl www.watchhealthcare.eu Rejestracja a refundacja zbiory logiczne tylko częściowo nakładające się Ratio legis a praktyka stanowienia prawa w zakresie refundacji i ustalania cen w Polsce,
www.korektorzdrowia.pl www.watchhealthcare.eu Rejestracja a refundacja zbiory logiczne tylko częściowo nakładające się Ratio legis a praktyka stanowienia prawa w zakresie refundacji i ustalania cen w Polsce,
Etyka finansowania leczenia chorób rzadkich onkologicznych
 Etyka finansowania leczenia chorób rzadkich onkologicznych Piotr Fiedor VI Letnia Akademia Onkologiczna dla Dziennikarzy Opracowano na podstawie źródeł udostępnionych w systemie informacji publicznej 11.08.2016
Etyka finansowania leczenia chorób rzadkich onkologicznych Piotr Fiedor VI Letnia Akademia Onkologiczna dla Dziennikarzy Opracowano na podstawie źródeł udostępnionych w systemie informacji publicznej 11.08.2016
Choroby rzadkie to takie, które występują u mniej niż 5 na 10 tys. osób. W Polsce liczbę chorych szacuje się na 2,5-3 mln.
 . Choroby rzadkie to takie, które występują u mniej niż 5 na 10 tys. osób. Dotychczas (według różnych szacunków) opisano około 8.000 jednostek chorobowych, które zalicza się do chorób rzadkich. Na całym
. Choroby rzadkie to takie, które występują u mniej niż 5 na 10 tys. osób. Dotychczas (według różnych szacunków) opisano około 8.000 jednostek chorobowych, które zalicza się do chorób rzadkich. Na całym
LEGISLACJA A DOSTĘP DO NOWOCZESNYCH TERAPII
 LEGISLACJA A DOSTĘP DO NOWOCZESNYCH TERAPII INFARMA, Katarzyna Połujan Prawo i finanse 2015 Warszawa 08.12.2014 PLANOWANE KIERUNKI DZIAŁAŃ RESORTU ZDROWIA W ZAKRESIE BEZPIECZEŃSTWA ZDROWOTNEGO OBYWATELI
LEGISLACJA A DOSTĘP DO NOWOCZESNYCH TERAPII INFARMA, Katarzyna Połujan Prawo i finanse 2015 Warszawa 08.12.2014 PLANOWANE KIERUNKI DZIAŁAŃ RESORTU ZDROWIA W ZAKRESIE BEZPIECZEŃSTWA ZDROWOTNEGO OBYWATELI
Co ustawa refundacyjna mówi o cenach leków?
 Co ustawa refundacyjna mówi o cenach leków? Natalia Łojko Radca prawny Warszawa, 1. Brak szczególnej regulacji dla leków biologicznych - podlegają tym samym regulacjom refundacyjnym, co inne leki 2 2.
Co ustawa refundacyjna mówi o cenach leków? Natalia Łojko Radca prawny Warszawa, 1. Brak szczególnej regulacji dla leków biologicznych - podlegają tym samym regulacjom refundacyjnym, co inne leki 2 2.
Idea Europejskiej Sieci Badań w Pediatrii
 Idea Europejskiej Sieci Badań w Pediatrii Marek Migdał, Klinika Anestezjologii i Intensywnej Terapii Instytut Pomnik-Centrum Zdrowia Dziecka Warszawa 15.05.2009, Warszawa Konferencja Nowe regulacje Unii
Idea Europejskiej Sieci Badań w Pediatrii Marek Migdał, Klinika Anestezjologii i Intensywnej Terapii Instytut Pomnik-Centrum Zdrowia Dziecka Warszawa 15.05.2009, Warszawa Konferencja Nowe regulacje Unii
Badania Kliniczne w Polsce. Na podstawie raportu wykonanego przez PwC na zlecenie stowarzyszenia INFARMA, GCPpl i POLCRO
 Badania Kliniczne w Polsce Na podstawie raportu wykonanego przez PwC na zlecenie stowarzyszenia INFARMA, GCPpl i POLCRO 1. Wprowadzenie 2. Dlaczego warto wspierać prowadzenie badań klinicznych 3. Analiza
Badania Kliniczne w Polsce Na podstawie raportu wykonanego przez PwC na zlecenie stowarzyszenia INFARMA, GCPpl i POLCRO 1. Wprowadzenie 2. Dlaczego warto wspierać prowadzenie badań klinicznych 3. Analiza
Produkty lecznicze pod szczególnym nadzorem - wybrane kwestie prawne
 Produkty lecznicze pod szczególnym nadzorem - wybrane kwestie prawne Ewa Rutkowska, Partner, Adwokat Agnieszka Zielińska Krywoniuk, Senior Associate, Adwokat "Pharmacovigilance w 2015 r. - nowa praktyka,
Produkty lecznicze pod szczególnym nadzorem - wybrane kwestie prawne Ewa Rutkowska, Partner, Adwokat Agnieszka Zielińska Krywoniuk, Senior Associate, Adwokat "Pharmacovigilance w 2015 r. - nowa praktyka,
Mapowanie ograniczeń dostępu do świadczeń zdrowotnych w Polsce działalność Fundacji Watch Health Care
 www.korektorzdrowia.pl www.watchhealthcare.eu Mapowanie ograniczeń dostępu do świadczeń zdrowotnych w Polsce działalność Fundacji Watch Health Care Za Fundacją Lege Pharmaciae w nawiązaniu do ustawy koszykowej:
www.korektorzdrowia.pl www.watchhealthcare.eu Mapowanie ograniczeń dostępu do świadczeń zdrowotnych w Polsce działalność Fundacji Watch Health Care Za Fundacją Lege Pharmaciae w nawiązaniu do ustawy koszykowej:
a dobór terapii do refundacji 9. Międzynarodowe Sympozjum EBHC HTA for Healthcare Quality Assurance
 Uzyskiwane efekty kliniczne a dobór terapii do refundacji Refundacja nowych terapii HCV jako wyzwanie dla płatników 9. Międzynarodowe Sympozjum EBHC HTA for Healthcare Quality Assurance 15 grudnia 2014
Uzyskiwane efekty kliniczne a dobór terapii do refundacji Refundacja nowych terapii HCV jako wyzwanie dla płatników 9. Międzynarodowe Sympozjum EBHC HTA for Healthcare Quality Assurance 15 grudnia 2014
WZW typu C KOSZTY BEZPOŚREDNIE, POŚREDNIE, SPOŁECZNE, OPŁACALNOŚĆ
 Robert Plisko WZW typu C KOSZTY BEZPOŚREDNIE, POŚREDNIE, SPOŁECZNE, OPŁACALNOŚĆ Konferencja Innowacje w leczeniu HCV ocena dostępności w Polsce 5 stycznia 2015 roku Naturalny przebieg infekcji WZW typu
Robert Plisko WZW typu C KOSZTY BEZPOŚREDNIE, POŚREDNIE, SPOŁECZNE, OPŁACALNOŚĆ Konferencja Innowacje w leczeniu HCV ocena dostępności w Polsce 5 stycznia 2015 roku Naturalny przebieg infekcji WZW typu
Stanisław Maćkowiak Federacja Pacjentów Polskich
 Choroby rzadkie i ultrarzadkie dostępność do leczenia w Polsce na tle Europy Narodowy Plan dla Chorób Rzadkich SEMINARIUM 22 marca 2016 Instytut Biocybernetyki i Inżynierii Biomedycznej PAN, przy ul. Trojdena
Choroby rzadkie i ultrarzadkie dostępność do leczenia w Polsce na tle Europy Narodowy Plan dla Chorób Rzadkich SEMINARIUM 22 marca 2016 Instytut Biocybernetyki i Inżynierii Biomedycznej PAN, przy ul. Trojdena
Mapowanie ograniczeń dostępu do świadczeń zdrowotnych w Polsce działalność Fundacji Watch Health Care
 www.korektorzdrowia.pl www.watchhealthcare.eu Mapowanie ograniczeń dostępu do świadczeń zdrowotnych w Polsce działalność Fundacji Watch Health Care Za Fundacją Lege Pharmaciae w nawiązaniu do ustawy koszykowej:
www.korektorzdrowia.pl www.watchhealthcare.eu Mapowanie ograniczeń dostępu do świadczeń zdrowotnych w Polsce działalność Fundacji Watch Health Care Za Fundacją Lege Pharmaciae w nawiązaniu do ustawy koszykowej:
PLATFORMA DIALOGU DLA ONKOHEMATOLOGII Model kompleksowej i koordynowanej opieki onkohematologicznej Wyniki badania ankietowego
 PLATFORMA DIALOGU DLA ONKOHEMATOLOGII Model kompleksowej i koordynowanej opieki onkohematologicznej Wyniki badania ankietowego Warszawa, 24 kwietnia 2018 r. Cancer Care: Assuring quality to improve survival,
PLATFORMA DIALOGU DLA ONKOHEMATOLOGII Model kompleksowej i koordynowanej opieki onkohematologicznej Wyniki badania ankietowego Warszawa, 24 kwietnia 2018 r. Cancer Care: Assuring quality to improve survival,
Rola AOTM w ocenie wyrobów medycznych. Gabriela Ofierska-Sujkowska Krzysztof Mączka Warszawa, r.
 Rola AOTM w ocenie wyrobów medycznych Gabriela Ofierska-Sujkowska Krzysztof Mączka Warszawa, 24.11.2011 r. Plan prezentacji AOTM - Rola i cel funkcjonowania Proces podejmowania decyzji refundacyjnych w
Rola AOTM w ocenie wyrobów medycznych Gabriela Ofierska-Sujkowska Krzysztof Mączka Warszawa, 24.11.2011 r. Plan prezentacji AOTM - Rola i cel funkcjonowania Proces podejmowania decyzji refundacyjnych w
Art. 24 ust. 7 pkt 2 ustawy o refundacji
 Minimalne wymagania dotyczące analiz uwzględnianych we wnioskach o objęcie refundacją i ustalenie oraz podwyższenie urzędowej ceny zbytu dla produktów, które nie mają odpowiednika refundowanego w danym
Minimalne wymagania dotyczące analiz uwzględnianych we wnioskach o objęcie refundacją i ustalenie oraz podwyższenie urzędowej ceny zbytu dla produktów, które nie mają odpowiednika refundowanego w danym
Plan prezentacji. Choroby rzadkie i ultrarzadkie. Specyfika cen leków sierocych i technologii stosowanych w chorobach rzadkich
 Tomasz Laczewski 1 z 7 i technologii stosowanych w chorobach rzadkich Rados aw Rud /Tomasz Laczewski Autorzy rozdzia u: Jakub Adamski, Joanna Lis, Kamila Wendykowska Plan prezentacji 1. Choroby rzadkie
Tomasz Laczewski 1 z 7 i technologii stosowanych w chorobach rzadkich Rados aw Rud /Tomasz Laczewski Autorzy rozdzia u: Jakub Adamski, Joanna Lis, Kamila Wendykowska Plan prezentacji 1. Choroby rzadkie
End-of-life treatment
 Karolina Skóra End-of-life treatment Technologie stosowane w schyłkowej fazie życia (tzw. end-of-life treatment). End-of-life treatment (EoL) to terapia aktywna, która wydłuża życie, a nie tylko łagodzi
Karolina Skóra End-of-life treatment Technologie stosowane w schyłkowej fazie życia (tzw. end-of-life treatment). End-of-life treatment (EoL) to terapia aktywna, która wydłuża życie, a nie tylko łagodzi
GŁÓWNE POWODY NEGATYWNYCH REKOMENDACJI AOTMIT. Izabela Pieniążek. Krakowskie Sympozjum HTA/MA 2015
 GŁÓWNE POWODY NEGATYWNYCH REKOMENDACJI AOTMIT Izabela Pieniążek Krakowskie Sympozjum HTA/MA 2015 1 ZAKRES ANALIZY REKOMENDACJI REFUNDACYJNYCH Zlecenia Ministra Zdrowia dotyczące przygotowania analizy weryfikacyjnej
GŁÓWNE POWODY NEGATYWNYCH REKOMENDACJI AOTMIT Izabela Pieniążek Krakowskie Sympozjum HTA/MA 2015 1 ZAKRES ANALIZY REKOMENDACJI REFUNDACYJNYCH Zlecenia Ministra Zdrowia dotyczące przygotowania analizy weryfikacyjnej
BADANIA PASS ROLA CRO W PLANOWANIU I ZARZĄDZANIU
 BADANIA PASS ROLA CRO W PLANOWANIU I ZARZĄDZANIU Agnieszka Almgren- Rachtan MD PhD BADANIEM Post- authorisajon safety study Porejestracyjne badanie farmakoepidemiologiczne lub próba kliniczna przeprowadzona
BADANIA PASS ROLA CRO W PLANOWANIU I ZARZĄDZANIU Agnieszka Almgren- Rachtan MD PhD BADANIEM Post- authorisajon safety study Porejestracyjne badanie farmakoepidemiologiczne lub próba kliniczna przeprowadzona
Wnioski i rekomendacje na przykładzie niewydolności serca
 Priorytety zdrowotne w kontekście demograficznego i gospodarczego rozwoju Polski Wnioski i rekomendacje na przykładzie niewydolności serca Streszczenie raportu Długość życia w dobrym zdrowiu obywateli
Priorytety zdrowotne w kontekście demograficznego i gospodarczego rozwoju Polski Wnioski i rekomendacje na przykładzie niewydolności serca Streszczenie raportu Długość życia w dobrym zdrowiu obywateli
MISJA HASCO-LEK. " Produkowanie leków najwyższej jakości, skutecznie zaspokajających potrzeby zdrowotne pacjentów "
 MISJA HASCO-LEK " Produkowanie leków najwyższej jakości, skutecznie zaspokajających potrzeby zdrowotne pacjentów " Rynek farmaceutyczny - dzień dzisiejszy i obserwowane kierunki zmian Michał Byliniak PPF
MISJA HASCO-LEK " Produkowanie leków najwyższej jakości, skutecznie zaspokajających potrzeby zdrowotne pacjentów " Rynek farmaceutyczny - dzień dzisiejszy i obserwowane kierunki zmian Michał Byliniak PPF
,, FARMACJA SZPITALNA, STARE PROBLEMY I NOWE WYZWANIA
 ,, FARMACJA SZPITALNA, STARE PROBLEMY I NOWE WYZWANIA dr n. farm. Beata Kocięcka KATOWICE 2017 Definicja apteki szpitalnej APTEKA SZPITALNA jest placówką ochrony zdrowia publicznego, w której osoby uprawnione
,, FARMACJA SZPITALNA, STARE PROBLEMY I NOWE WYZWANIA dr n. farm. Beata Kocięcka KATOWICE 2017 Definicja apteki szpitalnej APTEKA SZPITALNA jest placówką ochrony zdrowia publicznego, w której osoby uprawnione
Celem Tygodnia Szczepień w Polsce jest podkreślanie roli szczepień powszechnych i indywidualnych poprzez:
 W dniach 22-26 kwietnia obchodzimy, już po raz IX, Europejski Tydzień Szczepień. Jest to inicjatywa Światowej Organizacji Zdrowia (WHO), realizowana i koordynowana na poziomie lokalnym przez poszczególne
W dniach 22-26 kwietnia obchodzimy, już po raz IX, Europejski Tydzień Szczepień. Jest to inicjatywa Światowej Organizacji Zdrowia (WHO), realizowana i koordynowana na poziomie lokalnym przez poszczególne
Omówienie wyników raportu Dostęp pacjentów onkologicznych do terapii lekowych w Polsce na tle aktualnej wiedzy medycznej
 Omówienie wyników raportu Dostęp pacjentów onkologicznych do terapii lekowych w Polsce na tle aktualnej wiedzy medycznej Spotkanie w Ministerstwie Zdrowia 9 czerwca 2017 r. Dlaczego standardy postępowania
Omówienie wyników raportu Dostęp pacjentów onkologicznych do terapii lekowych w Polsce na tle aktualnej wiedzy medycznej Spotkanie w Ministerstwie Zdrowia 9 czerwca 2017 r. Dlaczego standardy postępowania
Ustawa. z dnia.. Art. 1
 PROJEKT Ustawa z dnia.. o zmianie ustawy o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych oraz ustawy o zawodach lekarza i lekarza dentysty Art. 1
PROJEKT Ustawa z dnia.. o zmianie ustawy o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych oraz ustawy o zawodach lekarza i lekarza dentysty Art. 1
MECHANIZMY USTAWY REFUNDACYJNEJ WPROWADZENIE
 MECHANIZMY USTAWY REFUNDACYJNEJ WPROWADZENIE Adw. Paulina Kieszkowska Knapik Adw. Katarzyna Czyżewska BUDŻET NA REFUNDACJĘ I TZW. PAY BACK - Brak limitu wydatków na leki w ramach ogólnego budżetu Narodowego
MECHANIZMY USTAWY REFUNDACYJNEJ WPROWADZENIE Adw. Paulina Kieszkowska Knapik Adw. Katarzyna Czyżewska BUDŻET NA REFUNDACJĘ I TZW. PAY BACK - Brak limitu wydatków na leki w ramach ogólnego budżetu Narodowego
 Rada Przejrzystości działająca przy Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji Stanowisko Rady Przejrzystości nr 95/2016 z dnia 29 sierpnia 2016 roku w sprawie zasadności wydawania zgody
Rada Przejrzystości działająca przy Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji Stanowisko Rady Przejrzystości nr 95/2016 z dnia 29 sierpnia 2016 roku w sprawie zasadności wydawania zgody
Koszyk świadczeń gwarantowanych; pozytywny i negatywny, świadczenia gwarantowane. Karolina Skóra
 Koszyk świadczeń gwarantowanych; pozytywny i negatywny, świadczenia gwarantowane Karolina Skóra Czym jest koszyk świadczeń zdrowotnych Koszyk świadczeń jest zbiorem świadczeń zdrowotnych lub procedur medycznych:
Koszyk świadczeń gwarantowanych; pozytywny i negatywny, świadczenia gwarantowane Karolina Skóra Czym jest koszyk świadczeń zdrowotnych Koszyk świadczeń jest zbiorem świadczeń zdrowotnych lub procedur medycznych:
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 18/2013 z dnia 28 stycznia 2013 r. w sprawie zasadności finansowania leku Myozyme (alglukozydaza alfa) w ramach
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 18/2013 z dnia 28 stycznia 2013 r. w sprawie zasadności finansowania leku Myozyme (alglukozydaza alfa) w ramach
Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r. w sprawie minimalnych wymagań, jakie muszą spełniać analizy
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r. w sprawie minimalnych wymagań, jakie muszą spełniać analizy
Postulaty organizacji wspierających pacjentów onkologicznych wobec polityki lekowej państwa
 Postulaty organizacji wspierających pacjentów onkologicznych wobec polityki lekowej państwa Spotkanie w Ministerstwie Zdrowia 16 października 2017 r. Dlaczego staramy się interesować instytucje naszymi
Postulaty organizacji wspierających pacjentów onkologicznych wobec polityki lekowej państwa Spotkanie w Ministerstwie Zdrowia 16 października 2017 r. Dlaczego staramy się interesować instytucje naszymi
Badania kliniczne nowe otwarcie! Konferencja z okazji Międzynarodowego Dnia Badań Klinicznych 20 maja 2015 r.
 1 2 Badania kliniczne nowe otwarcie! Konferencja z okazji Międzynarodowego Dnia Badań Klinicznych 20 maja 2015 r. Igor Radziewicz-Winnicki Podsekretarz Stanu w Ministerstwie Zdrowia Rozporządzenie Parlamentu
1 2 Badania kliniczne nowe otwarcie! Konferencja z okazji Międzynarodowego Dnia Badań Klinicznych 20 maja 2015 r. Igor Radziewicz-Winnicki Podsekretarz Stanu w Ministerstwie Zdrowia Rozporządzenie Parlamentu
