Podstawowe definicje
|
|
|
- Kazimiera Sosnowska
- 5 lat temu
- Przeglądów:
Transkrypt
1 Wprowadzenie do równowag fazowych () odstawowe definicje Faza dla danej substancji jej postać charakteryzująca się jednorodnym składem chemicznym i stanem fizycznym. W obrę bie fazy niektóre intensywne funkcje stanu (np. gęstość) mają jednakową wartość. rzemiana fazowa przemiana jednej fazy w drugą zachodz w charakterystycznej temperaturze przejścia fazowego (przemia fazowej) przy danym ciśnieniu. Diagram fazowy wykres pokazujący obszary trwałości faz w zależności od ciśnienia i temperatury (dla układów jednoskła nikowych), linie i punkty równowag międzyfazowych.
2 Wprowadzenie do ciecz przechłodz ciecz przegrzan równowag fazowych () Obszary trwałości faz, fazy metastabilne constans
3 Wprowadzenie do równowag fazowych (3) rzykładowy diagram fazowy 0 kt potrójny punkt krytyczny 3 t w kr
4 rężność par () ciecz gaz ciało stałe gaz < para < ciecz faza skondensowana ciało stałe
5 rężność par () 366,4 a Równowaga woda para wodna, a 3, a 4, K 373,5 K K 4 647,3 K
6 Diagram fazowy wody ()
7 miany skali Diagram fazowy wody ()
8 zmiana skali Diagram fazowy CO
9 Diagram fazowy 4 He
10 ermodynamika równowagi fazowej () W stanie równowagi, dg 0, zatem: jeśli: dn dn; dn dn dg G dn; dg G d dg dg + dg ( G G ) dn ponieważ, jako się rzekło: ( dg), zaś dn 0, to G G const const kryterium równowagi fazowej
11 ermodynamika równowagi fazowej () ozważymy teraz zmiany G przy infinitezymalnych zmianach i an równowagi I: G, G,, Stan równowagi II: +d, + G G ynika z tego, że również: dg dg wiemy też, że: dg vd sd G + dg G + dg zatem: dg V d S d oraz: dg V d Sd w konsekwencji: V d S d V d S d
12 Równanie Clausiusa-Clapeyrona () ląc ostatnie r-nie przez d otrzymujemy: V d d S V d d bo: d d S V S V S V S V ( V V ) L gdzie L jest ciepłem przemiany fazowej Jest to ogólna postać równania Clausiusa-Clapeyrona.
13 Równowaga ciecz -para Metody pomiaru prężności par: statyczne (barometryczne) bezpośredni pomiar prężności par nad cieczą w równowadze dynamiczne pomiar temperatury wrzenia przy danym narzuconym ciśnieniu (ebuliometr) transpiracyjne analiza gazu przepływającego przez termostatowaną ciecz i nasyconego parą
14 Równanie Clausiusa Clapeyrona () ównowaga ciecz - para: d d L ( V V ) p p c ałkiem rozsądnym założeniem jest też: V p >>V c a co za tym idzie: Vp Vc Vp R ostatecznie: d ln d L R p lub d L R p d co jest łatwe do scałkowania
15 Równanie Clausiusa Clapeyrona (3) Równowaga ciecz para (c.d.): d L R całkując od do i od do przy założeniu stałości L p w interesującym nas przedziale temperatur (skąd znamy podobne założenie?) zymujemy: ln L p R lub log p L d p Rln0 Lp ałkowaniu nieoznaczonym: ln + const lub log R Są to równania linii parowania na diagramie fazowym a
16 Równanie Clausiusa Clapeyrona (4) yby równowagę ciecz para potraktować jako reakcję chemiczn o symbolicznym zapisie: A(c) M(g) o stosowałoby się do niej równanie van t Hoffa ln K K H R r Zważywszy, że dla tej reakcji K p M / 0 ln H R p
17 Sublimacja Analogicznie: d d L ( V V ) p s s ze bardziej prawdziwe jest też: V p >>V s zatem: V p V Ostatecznie obowiązują analogiczne postaci równania C-C: s R ln Ls R lub log Ls Rln0 Ls a ln + const lub log + R c
18 rzemiany polimorficzne Odmiany alotropowe emperatura przemiany fazowej jest funkcją ciśnienia: d d ( V V ) L rzemiany fazowe w ciałach stałych zachodzą bardzo powoli! C(diament) C(grafit) S(jednoskośna) S(rombowa) (biały) (czerwony)
Podstawowe definicje
 Wprowadzenie do równowag fazowych (1) Podstawowe definicje 1) Faza dla danej substancji jej postać charakteryzująca się jednorodnym składem chemicznym i stanem fizycznym. W obrębie fazy niektóre intensywne
Wprowadzenie do równowag fazowych (1) Podstawowe definicje 1) Faza dla danej substancji jej postać charakteryzująca się jednorodnym składem chemicznym i stanem fizycznym. W obrębie fazy niektóre intensywne
Warunki izochoryczno-izotermiczne
 WYKŁAD 5 Pojęcie potencjału chemicznego. Układy jednoskładnikowe W zależności od warunków termodynamicznych potencjał chemiczny substancji czystej definiujemy następująco: Warunki izobaryczno-izotermiczne
WYKŁAD 5 Pojęcie potencjału chemicznego. Układy jednoskładnikowe W zależności od warunków termodynamicznych potencjał chemiczny substancji czystej definiujemy następująco: Warunki izobaryczno-izotermiczne
Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Wykład 1. Anna Ptaszek. 5 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 1. Anna Ptaszek 1 / 36
 Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Prowadzący. http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5)
 Tomasz Lubera dr Tomasz Lubera mail: luberski@interia.pl Prowadzący http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5) Konsultacje: we wtorki
Tomasz Lubera dr Tomasz Lubera mail: luberski@interia.pl Prowadzący http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5) Konsultacje: we wtorki
chemia wykład 3 Przemiany fazowe
 Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Termodynamiczny opis przejść fazowych pierwszego rodzaju
 Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Wykład 4. Przypomnienie z poprzedniego wykładu
 Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
powierzchnia rozdziału - dwie fazy ciekłe - jedna faza gazowa - dwa składniki
 Przejścia fazowe. powierzchnia rozdziału - skokowa zmiana niektórych parametrów na granicy faz. kropeki wody w atmosferze - dwie fazy ciekłe - jedna faza gazowa - dwa składniki Przykłady przejść fazowych:
Przejścia fazowe. powierzchnia rozdziału - skokowa zmiana niektórych parametrów na granicy faz. kropeki wody w atmosferze - dwie fazy ciekłe - jedna faza gazowa - dwa składniki Przykłady przejść fazowych:
INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH
 INSTYTUT MASZYN I URZĄDZEŃ ENERGETYCZNYCH Politechnika Śląska w Gliwicach INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH WYZNACZANIE WYKRESU RÓWNOWAGI FAZOWEJ (dla stopów dwuskładnikowych) Instrukcja przeznaczona
INSTYTUT MASZYN I URZĄDZEŃ ENERGETYCZNYCH Politechnika Śląska w Gliwicach INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH WYZNACZANIE WYKRESU RÓWNOWAGI FAZOWEJ (dla stopów dwuskładnikowych) Instrukcja przeznaczona
Wykład 3. Diagramy fazowe P-v-T dla substancji czystych w trzech stanach. skupienia. skupienia
 Wykład 3 Substancje proste i czyste Przemiany w systemie dwufazowym woda para wodna Diagram T-v dla przejścia fazowego woda para wodna Diagramy T-v i P-v dla wody Punkt krytyczny Temperatura nasycenia
Wykład 3 Substancje proste i czyste Przemiany w systemie dwufazowym woda para wodna Diagram T-v dla przejścia fazowego woda para wodna Diagramy T-v i P-v dla wody Punkt krytyczny Temperatura nasycenia
RÓWNOWAGI W UKŁADACH WIELOFAZOWYCH
 RÓWNOWAGI W UKŁADACH WIELOFAZOWYCH 321 Pojęcia podstawowe 322 erodynaika równowag fazowych reguła faz Gibbsa 323 Równanie Clausiusa-Clapeyrona 324 Przeiany fazowe I i II rodzaju 31 erodynaika równowag
RÓWNOWAGI W UKŁADACH WIELOFAZOWYCH 321 Pojęcia podstawowe 322 erodynaika równowag fazowych reguła faz Gibbsa 323 Równanie Clausiusa-Clapeyrona 324 Przeiany fazowe I i II rodzaju 31 erodynaika równowag
Zjawiska powierzchniowe
 Zjawiska powierzchniowe Adsorpcja Model Langmuira Model BET 1 Zjawiska powierzchniowe Adsorpcja Proces gromadzenia się substancji z wnętrza fazy na granicy międzyfazowej; Wynika z tego, że w obszarze powierzchniowym
Zjawiska powierzchniowe Adsorpcja Model Langmuira Model BET 1 Zjawiska powierzchniowe Adsorpcja Proces gromadzenia się substancji z wnętrza fazy na granicy międzyfazowej; Wynika z tego, że w obszarze powierzchniowym
prof. dr hab. Małgorzata Jóźwiak
 Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Termodynamika techniczna i chemiczna, 2015/16, zadania do kol. 1, zadanie nr 1 1
 Termodynamika techniczna i chemiczna, 2015/16, zadania do kol. 1, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący 1. Obliczyć zmianę entalpii dla izobarycznej (p = 1 bar) reakcji chemicznej zapoczątkowanej
Termodynamika techniczna i chemiczna, 2015/16, zadania do kol. 1, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący 1. Obliczyć zmianę entalpii dla izobarycznej (p = 1 bar) reakcji chemicznej zapoczątkowanej
CHEMIA FIZYCZNA ZTiM
 CHEMIA FIZYCZNA ZTiM Semestr zimowy 2016/2017 Dr hab. inż. Dorota Warmińska 1. Chemia fizyczna. Termodynamika. Podstawowe pojęcia stosowane w termodynamice. Układ i otoczenie. Przegroda adiabatyczna i
CHEMIA FIZYCZNA ZTiM Semestr zimowy 2016/2017 Dr hab. inż. Dorota Warmińska 1. Chemia fizyczna. Termodynamika. Podstawowe pojęcia stosowane w termodynamice. Układ i otoczenie. Przegroda adiabatyczna i
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 1, zadanie nr 1 1
 Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 1, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 1, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii
 Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Krystalizacja. Zarodkowanie
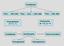 Krystalizacja Ciecz ciało stałe Para ciecz ciało stałe Para ciało stałe Przechłodzenie T = T L - T c Przesycenie p = p g - p z > 0 Krystalizacja Zarodkowanie Rozrost zarodków Homogeniczne Heterogeniczne
Krystalizacja Ciecz ciało stałe Para ciecz ciało stałe Para ciało stałe Przechłodzenie T = T L - T c Przesycenie p = p g - p z > 0 Krystalizacja Zarodkowanie Rozrost zarodków Homogeniczne Heterogeniczne
Ćwiczenia do wykładu Fizyka Statystyczna i Termodynamika
 Ćwiczenia do wykładu Fizyka tatystyczna i ermodynamika Prowadzący dr gata Fronczak Zestaw 5. ermodynamika rzejść fazowych: równanie lausiusa-laeyrona, własności gazu Van der Waalsa 3.1 Rozważ tyowy diagram
Ćwiczenia do wykładu Fizyka tatystyczna i ermodynamika Prowadzący dr gata Fronczak Zestaw 5. ermodynamika rzejść fazowych: równanie lausiusa-laeyrona, własności gazu Van der Waalsa 3.1 Rozważ tyowy diagram
Wykład 3. Fizykochemia biopolimerów- wykład 3. Anna Ptaszek. 30 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego
 Wykład 3 - wykład 3 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 30 października 2013 1/56 Warunek równowagi fazowej Jakich układów dotyczy równowaga fazowa? Równowaga fazowa dotyczy układów: jednoskładnikowych
Wykład 3 - wykład 3 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 30 października 2013 1/56 Warunek równowagi fazowej Jakich układów dotyczy równowaga fazowa? Równowaga fazowa dotyczy układów: jednoskładnikowych
Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak
 Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga ciało
Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga ciało
RÓWNOWAGA CIECZ PARA W UKŁADZIE DWUSKŁADNIKOWYM
 RÓWNOWAGA CIECZ PARA W UKŁADZIE DWUSKŁADNIKOWYM Cel ćwiczenia: wyznaczenie diagramu fazowego ciecz para w warunkach izobarycznych. Układ pomiarowy i opis metody: Pomiary wykonywane są metodą recyrkulacyjną
RÓWNOWAGA CIECZ PARA W UKŁADZIE DWUSKŁADNIKOWYM Cel ćwiczenia: wyznaczenie diagramu fazowego ciecz para w warunkach izobarycznych. Układ pomiarowy i opis metody: Pomiary wykonywane są metodą recyrkulacyjną
Para wodna najczęściej jest produkowana w warunkach stałego ciśnienia.
 PARA WODNA 1. PRZEMIANY FAZOWE SUBSTANCJI JEDNORODNYCH Para wodna najczęściej jest produkowana w warunkach stałego ciśnienia. Przy niezmiennym ciśnieniu zmiana wody o stanie początkowym odpowiadającym
PARA WODNA 1. PRZEMIANY FAZOWE SUBSTANCJI JEDNORODNYCH Para wodna najczęściej jest produkowana w warunkach stałego ciśnienia. Przy niezmiennym ciśnieniu zmiana wody o stanie początkowym odpowiadającym
TERMODYNAMIKA TECHNICZNA I CHEMICZNA
 TERMODYNAMIKA TECHNICZNA I CHEMICZNA WYKŁAD IX RÓWNOWAGA FAZOWA W UKŁADZIE CIAŁO STAŁE-CIECZ (krystalizacja) ADSORPCJA KRYSTALIZACJA, ADSORPCJA 1 RÓWNOWAGA FAZOWA W UKŁADZIE CIAŁO STAŁE-CIECZ (krystalizacja)
TERMODYNAMIKA TECHNICZNA I CHEMICZNA WYKŁAD IX RÓWNOWAGA FAZOWA W UKŁADZIE CIAŁO STAŁE-CIECZ (krystalizacja) ADSORPCJA KRYSTALIZACJA, ADSORPCJA 1 RÓWNOWAGA FAZOWA W UKŁADZIE CIAŁO STAŁE-CIECZ (krystalizacja)
Chemia fizyczna. Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia fizyczna Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny SUBSTANCJE CZYSTE SUBSTANCJE CZYSTE RÓWNOWAGI FAZOWE Fazą danej substancji nazywamy postać materii, która charakteryzuje
Chemia fizyczna Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny SUBSTANCJE CZYSTE SUBSTANCJE CZYSTE RÓWNOWAGI FAZOWE Fazą danej substancji nazywamy postać materii, która charakteryzuje
Ćwiczenie VII: RÓWNOWAGA W UKŁADZIE DWUSKŁADNIKOWYM CIAŁO STAŁE CIECZ
 Ćwiczenie VII: RÓWNOWAGA W UKŁADZIE DWUSKŁADNIKOWYM CIAŁO STAŁE CIECZ opracowanie: Barbara Stypuła Wprowadzenie Celem ćwiczenia jest zapoznanie się z opisem i analizą przemian fizycznych, jakim podlegają
Ćwiczenie VII: RÓWNOWAGA W UKŁADZIE DWUSKŁADNIKOWYM CIAŁO STAŁE CIECZ opracowanie: Barbara Stypuła Wprowadzenie Celem ćwiczenia jest zapoznanie się z opisem i analizą przemian fizycznych, jakim podlegają
ZALEŻNOŚĆ CIŚNIENIA PARY NASYCONEJ WODY OD TEM- PERATURY. WYZNACZANIE MOLOWEGO CIEPŁA PARO- WANIA
 ZALEŻNOŚĆ CIŚNIENIA PARY NASYCONEJ WODY OD TEM- PERATURY. WYZNACZANIE MOLOWEGO CIEPŁA PARO- WANIA I. Cel ćwiczenia: zbadanie zależności ciśnienia pary nasyconej wody od temperatury oraz wyznaczenie molowego
ZALEŻNOŚĆ CIŚNIENIA PARY NASYCONEJ WODY OD TEM- PERATURY. WYZNACZANIE MOLOWEGO CIEPŁA PARO- WANIA I. Cel ćwiczenia: zbadanie zależności ciśnienia pary nasyconej wody od temperatury oraz wyznaczenie molowego
Laboratorium z chemii fizycznej. Zakres zagadnień na kolokwia
 CHEMIA semestr III Laboratorium z chemii fizycznej Zakres zagadnień na kolokwia 1. Wymagania ogólne Podstawą przygotowania do ćwiczeń jest skrypt pt. Chemia fizyczna. Ćwiczenia laboratoryjne, praca zbiorowa
CHEMIA semestr III Laboratorium z chemii fizycznej Zakres zagadnień na kolokwia 1. Wymagania ogólne Podstawą przygotowania do ćwiczeń jest skrypt pt. Chemia fizyczna. Ćwiczenia laboratoryjne, praca zbiorowa
Fizyka, technologia oraz modelowanie wzrostu kryształów
 Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-4 Warszawa, ul Sokołowska 9/37 tel: 88 80 44 e-mail: stach@unipress.waw.pl,
Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-4 Warszawa, ul Sokołowska 9/37 tel: 88 80 44 e-mail: stach@unipress.waw.pl,
Fizyka statystyczna Fenomenologia przejść fazowych. P. F. Góra
 Fizyka statystyczna Fenomenologia przejść fazowych P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Przejście fazowe transformacja układu termodynamicznego z jednej fazy (stanu materii) do innej, dokonywane
Fizyka statystyczna Fenomenologia przejść fazowych P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Przejście fazowe transformacja układu termodynamicznego z jednej fazy (stanu materii) do innej, dokonywane
Ćwiczenia rachunkowe z termodynamiki technicznej i chemicznej Zalecane zadania kolokwium 1. (2014/15)
 Ćwiczenia rachunkowe z termodynamiki technicznej i chemicznej Zalecane zadania kolokwium 1. (2014/15) (Uwaga! Liczba w nawiasie przy odpowiedzi oznacza numer zadania (zestaw.nr), którego rozwiązanie dostępne
Ćwiczenia rachunkowe z termodynamiki technicznej i chemicznej Zalecane zadania kolokwium 1. (2014/15) (Uwaga! Liczba w nawiasie przy odpowiedzi oznacza numer zadania (zestaw.nr), którego rozwiązanie dostępne
Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron
 Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron Zagadka na początek wykładu Diagram fazowy wody w powiększeniu, problem metastabilności aktualny (Nature, 2011) Niższa temperatura topnienia
Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron Zagadka na początek wykładu Diagram fazowy wody w powiększeniu, problem metastabilności aktualny (Nature, 2011) Niższa temperatura topnienia
Badanie zależności temperatury wrzenia wody od ciśnienia
 Ćwiczenie C2 Badanie zależności temperatury wrzenia wody od ciśnienia C2.1. Cel ćwiczenia Celem ćwiczenia jest pomiar zależności temperatury wrzenia wody od ciśnienia (poniżej ciśnienia atmosferycznego),
Ćwiczenie C2 Badanie zależności temperatury wrzenia wody od ciśnienia C2.1. Cel ćwiczenia Celem ćwiczenia jest pomiar zależności temperatury wrzenia wody od ciśnienia (poniżej ciśnienia atmosferycznego),
Wykład 3. Entropia i potencjały termodynamiczne
 Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Wykład 7. Anna Ptaszek. 13 września Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Fizykochemia biopolimerów - wykład 7.
 Wykład 7 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 13 września 2016 1 / 27 Układ wieloskładnikowy dwufazowy P woda 1 atm lód woda ciek a woda + substancja nielotna para wodna 0 0 100 T 2 / 27
Wykład 7 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 13 września 2016 1 / 27 Układ wieloskładnikowy dwufazowy P woda 1 atm lód woda ciek a woda + substancja nielotna para wodna 0 0 100 T 2 / 27
Równanie gazu doskonałego
 Równanie gazu doskonałego Gaz doskonały to abstrakcyjny model gazu, który zakłada, że gaz jest zbiorem sprężyście zderzających się kulek. Wiele gazów w warunkach normalnych zachowuje się jak gaz doskonały.
Równanie gazu doskonałego Gaz doskonały to abstrakcyjny model gazu, który zakłada, że gaz jest zbiorem sprężyście zderzających się kulek. Wiele gazów w warunkach normalnych zachowuje się jak gaz doskonały.
EGZAMIN pisemny z TERMODYNAMIKI TERMODYNAMIKA TECHNICZNA I CHEMICZNA. Lista pytań opisowych (semestr zimowy 2015/16)
 Termodynamika techniczna i chemiczna termodynamika - egzamin 2015/2016 1 EGZAMIN pisemny z TERMODYNAMIKI TERMODYNAMIKA TECHNICZNA I CHEMICZNA Lista pytań opisowych (semestr zimowy 2015/16) Pytania na egzaminie
Termodynamika techniczna i chemiczna termodynamika - egzamin 2015/2016 1 EGZAMIN pisemny z TERMODYNAMIKI TERMODYNAMIKA TECHNICZNA I CHEMICZNA Lista pytań opisowych (semestr zimowy 2015/16) Pytania na egzaminie
W8 40. Para. Równanie Van der Waalsa Temperatura krytyczna ci Przemiany pary. Termodynamika techniczna
 W8 40 Równanie Van der Waalsa Temperatura krytyczna Stopień suchości ci Przemiany pary 1 p T 1 =const T 2 =const 2 Oddziaływanie międzycz dzycząsteczkowe jest odwrotnie proporcjonalne do odległości (liczonej
W8 40 Równanie Van der Waalsa Temperatura krytyczna Stopień suchości ci Przemiany pary 1 p T 1 =const T 2 =const 2 Oddziaływanie międzycz dzycząsteczkowe jest odwrotnie proporcjonalne do odległości (liczonej
Kalorymetria. 1. I zasada termodynamiki, Prawo Hessa, Prawo Kirchhoffa (graficzna interpretacja), ciepło właściwe, termodynamiczne funkcje stanu.
 Kalorymetria 1. I zasada termodynamiki, Prawo Hessa, Prawo Kirchhoffa (graficzna interpretacja), ciepło właściwe, termodynamiczne funkcje stanu. 2. Rodzaje i zasady działania kalorymetrów: a) nieizotermicznego
Kalorymetria 1. I zasada termodynamiki, Prawo Hessa, Prawo Kirchhoffa (graficzna interpretacja), ciepło właściwe, termodynamiczne funkcje stanu. 2. Rodzaje i zasady działania kalorymetrów: a) nieizotermicznego
K raków 26 ma rca 2011 r.
 K raków 26 ma rca 2011 r. Zadania do ćwiczeń z Podstaw Fizyki na dzień 1 kwietnia 2011 r. r. dla Grupy II Zadanie 1. 1 kg/s pary wo dne j o ciśnieniu 150 atm i temperaturze 342 0 C wpada do t urbiny z
K raków 26 ma rca 2011 r. Zadania do ćwiczeń z Podstaw Fizyki na dzień 1 kwietnia 2011 r. r. dla Grupy II Zadanie 1. 1 kg/s pary wo dne j o ciśnieniu 150 atm i temperaturze 342 0 C wpada do t urbiny z
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1. Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski
 Chemia Fizyczna Technologia Chemiczna II rok Wykład 1 Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski Kontakt,informacja i konsultacje Chemia A ; pokój 307 Telefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1 Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski Kontakt,informacja i konsultacje Chemia A ; pokój 307 Telefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl
Równowaga fazowa. Przykładowo: 1. H 2 O (c) w mieszaninie H 2 O (c) + H 2 O (s) 2. mieszanina opiłek żelaza i sproszkowanej siarki
 WYKŁAD 5 RÓWNOWAGA FAZOWA Równowaga fazowa Faza każda fizycznie lub chemicznie odmienna część układu, jednorodna, dającą się mechanicznie (lub odpowiednio dobraną metodą fizyczną) oddzielić od reszty układu.
WYKŁAD 5 RÓWNOWAGA FAZOWA Równowaga fazowa Faza każda fizycznie lub chemicznie odmienna część układu, jednorodna, dającą się mechanicznie (lub odpowiednio dobraną metodą fizyczną) oddzielić od reszty układu.
Zadania treningowe na kolokwium
 Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Wykład 1 i 2. Termodynamika klasyczna, gaz doskonały
 Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Właściwości koligatywne
 Tomasz Lubera Właściwości koligatywne Grupa zjawisk naturalnych niezależnych od rodzaju substancji rozpuszczonej a jedynie od jej ilości. Należą do nich: obniżenie prężności pary, podwyższenie temperatury
Tomasz Lubera Właściwości koligatywne Grupa zjawisk naturalnych niezależnych od rodzaju substancji rozpuszczonej a jedynie od jej ilości. Należą do nich: obniżenie prężności pary, podwyższenie temperatury
Wykład 5. Kalorymetria i przejścia fazowe
 Wykład 5 Kalorymetria Ciepło przemian fazowych Bilans cieplny Proces kwazistatyczny Procesy odwracalne i nieodwracalne Praca Energia wewnętrzna Podstawowe przemiany gazowe W. Dominik Wydział Fizyki UW
Wykład 5 Kalorymetria Ciepło przemian fazowych Bilans cieplny Proces kwazistatyczny Procesy odwracalne i nieodwracalne Praca Energia wewnętrzna Podstawowe przemiany gazowe W. Dominik Wydział Fizyki UW
Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2018/19)
 Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2018/19) Uwaga! Uzyskane wyniki mogą się nieco różnić od podanych w materiałach, ze względu na uaktualnianie wartości zapisanych
Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2018/19) Uwaga! Uzyskane wyniki mogą się nieco różnić od podanych w materiałach, ze względu na uaktualnianie wartości zapisanych
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12
 Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Wykład 1-4. Anna Ptaszek. 6 września Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Fizykochemia biopolimerów - wykład 1-4.
 Wykład 1-4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 6 września 2016 1 / 68 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1-4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 6 września 2016 1 / 68 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów
 Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
TERMODYNAMIKA IM. Semestr letni
 TERMODYNAMIKA IM Semestr letni Ogólny kierunek przebiegu zjawisk i procesów w przyrodzie Układ i otoczenie Układ odosobniony Przegroda adiabatyczna i diatermiczna Układ zamknięty i układ otwarty Zmienne
TERMODYNAMIKA IM Semestr letni Ogólny kierunek przebiegu zjawisk i procesów w przyrodzie Układ i otoczenie Układ odosobniony Przegroda adiabatyczna i diatermiczna Układ zamknięty i układ otwarty Zmienne
Analiza termiczna Krzywe stygnięcia
 Analiza termiczna Krzywe stygnięcia 0 0,2 0,4 0,6 0,8 1,0 T a e j n s x p b t c o f g h k l p d i m y z q u v r w α T B T A T E T k P = const Chem. Fiz. TCH II/10 1 Rozpatrując stygnięcie wzdłuż kolejnych
Analiza termiczna Krzywe stygnięcia 0 0,2 0,4 0,6 0,8 1,0 T a e j n s x p b t c o f g h k l p d i m y z q u v r w α T B T A T E T k P = const Chem. Fiz. TCH II/10 1 Rozpatrując stygnięcie wzdłuż kolejnych
Podstawy termodynamiki
 Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Termodynamika Część 2
 Termodynamika Część 2 Równanie stanu Równanie stanu gazu doskonałego Równania stanu gazów rzeczywistych rozwinięcie wirialne równanie van der Waalsa hipoteza odpowiedniości stanów inne równania stanu Równanie
Termodynamika Część 2 Równanie stanu Równanie stanu gazu doskonałego Równania stanu gazów rzeczywistych rozwinięcie wirialne równanie van der Waalsa hipoteza odpowiedniości stanów inne równania stanu Równanie
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1
 Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
STRUKTURA STOPÓW UKŁADY RÓWNOWAGI FAZOWEJ. Publikacja współfinansowana ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 STRUKTURA STOPÓW UKŁADY RÓWNOWAGI FAZOWEJ Publikacja współfinansowana ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego Wykresy układów równowagi faz stopowych Ilustrują skład fazowy
STRUKTURA STOPÓW UKŁADY RÓWNOWAGI FAZOWEJ Publikacja współfinansowana ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego Wykresy układów równowagi faz stopowych Ilustrują skład fazowy
Temat XXI. Przemiany fazowe
 Temat XXI Przemiany fazowe Definicja: Faza termodynamiczna Faza termodynamiczna jest jednolitą częścią układu fizycznego, oddzieloną od innych jego części powierzchniami, nazywanymi granicami faz. Definicja:
Temat XXI Przemiany fazowe Definicja: Faza termodynamiczna Faza termodynamiczna jest jednolitą częścią układu fizycznego, oddzieloną od innych jego części powierzchniami, nazywanymi granicami faz. Definicja:
I piętro p. 131 A, 138
 CHEMIA NIEORGANICZNA Dr hab. Andrzej Kotarba Zakład Chemii Nieorganicznej Wydział Chemii I piętro p. 131 A, 138 WYKŁAD - 4 RÓWNOWAGA Termochemia i termodynamika funkcje termodynamiczne, prawa termodynamiki,
CHEMIA NIEORGANICZNA Dr hab. Andrzej Kotarba Zakład Chemii Nieorganicznej Wydział Chemii I piętro p. 131 A, 138 WYKŁAD - 4 RÓWNOWAGA Termochemia i termodynamika funkcje termodynamiczne, prawa termodynamiki,
3. Przejścia fazowe pomiędzy trzema stanami skupienia materii:
 Temat: Zmiany stanu skupienia. 1. Energia sieci krystalicznej- wielkość dzięki której można oszacować siły przyciągania w krysztale 2. Energia wiązania sieci krystalicznej- ilość energii potrzebnej do
Temat: Zmiany stanu skupienia. 1. Energia sieci krystalicznej- wielkość dzięki której można oszacować siły przyciągania w krysztale 2. Energia wiązania sieci krystalicznej- ilość energii potrzebnej do
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
Wykład 10 Równowaga chemiczna
 Wykład 10 Równowaga chemiczna REAKCJA CHEMICZNA JEST W RÓWNOWADZE, GDY NIE STWIERDZAMY TENDENCJI DO ZMIAN ILOŚCI (STĘŻEŃ) SUBSTRATÓW ANI PRODUKTÓW RÓWNOWAGA CHEMICZNA JEST RÓWNOWAGĄ DYNAMICZNĄ W rzeczywistości
Wykład 10 Równowaga chemiczna REAKCJA CHEMICZNA JEST W RÓWNOWADZE, GDY NIE STWIERDZAMY TENDENCJI DO ZMIAN ILOŚCI (STĘŻEŃ) SUBSTRATÓW ANI PRODUKTÓW RÓWNOWAGA CHEMICZNA JEST RÓWNOWAGĄ DYNAMICZNĄ W rzeczywistości
Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2016/17)
 Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2016/17) Uwaga! Uzyskane wyniki mogą się nieco różnić od podanych w materiałach, ze względu na uaktualnianie wartości zapisanych
Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2016/17) Uwaga! Uzyskane wyniki mogą się nieco różnić od podanych w materiałach, ze względu na uaktualnianie wartości zapisanych
ĆWICZENIE 22 WYZNACZANIE CIEPŁA PAROWANIA WODY W TEMPERETATURZE WRZENIA
 ĆWICZENIE 22 WYZNACZANIE CIEPŁA PAROWANIA WODY W TEMPERETATURZE WRZENIA Aby parowanie cieczy zachodziło w stałej temperaturze należy dostarczyć jej określoną ilość ciepła w jednostce czasu. Wielkość równą
ĆWICZENIE 22 WYZNACZANIE CIEPŁA PAROWANIA WODY W TEMPERETATURZE WRZENIA Aby parowanie cieczy zachodziło w stałej temperaturze należy dostarczyć jej określoną ilość ciepła w jednostce czasu. Wielkość równą
Termodynamika fazy powierzchniowej Zjawisko sorpcji Adsorpcja fizyczna: izoterma Langmuira oraz BET Zjawiska przylegania
 ermodynamika zjawisk powierzchniowych 3.6.1. ermodynamika fazy powierzchniowej 3.6.2. Zjawisko sorpcji 3.6.3. Adsorpcja fizyczna: izoterma Langmuira oraz BE 3.6.4. Zjawiska przylegania ZJAWISKA PWIERZCHNIWE
ermodynamika zjawisk powierzchniowych 3.6.1. ermodynamika fazy powierzchniowej 3.6.2. Zjawisko sorpcji 3.6.3. Adsorpcja fizyczna: izoterma Langmuira oraz BE 3.6.4. Zjawiska przylegania ZJAWISKA PWIERZCHNIWE
Termodynamika materiałów
 Termodynamika materiałów Plan wykładu 1. Funkcje termodynamiczne, pojemność cieplna. 2. Warunki równowagi termodynamicznej w układach jedno- i wieloskładnikowych, pojęcie potencjału chemicznego. 3. Modele
Termodynamika materiałów Plan wykładu 1. Funkcje termodynamiczne, pojemność cieplna. 2. Warunki równowagi termodynamicznej w układach jedno- i wieloskładnikowych, pojęcie potencjału chemicznego. 3. Modele
TERMODYNAMIKA PROCESOWA I TECHNICZNA
 ERMODYNAMIKA PROCESOWA I ECHNICZNA Wykład II Podstawowe definicje cd. Podstawowe idealizacje termodynamiczne I i II Zasada termodynamiki Proste rzemiany termodynamiczne Prof. Antoni Kozioł, Wydział Chemiczny
ERMODYNAMIKA PROCESOWA I ECHNICZNA Wykład II Podstawowe definicje cd. Podstawowe idealizacje termodynamiczne I i II Zasada termodynamiki Proste rzemiany termodynamiczne Prof. Antoni Kozioł, Wydział Chemiczny
Projekt Inżynier mechanik zawód z przyszłością współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Wykład 6. Klasyfikacja przemian fazowych
 Wykład 6 Klasyfikacja przemian fazowych JS Klasyfikacja Ehrenfesta Ehrenfest klasyfikuje przemiany fazowe w oparciu o potencjał chemiczny. nieciągłość Przemiany fazowe pierwszego rodzaju pochodne potencjału
Wykład 6 Klasyfikacja przemian fazowych JS Klasyfikacja Ehrenfesta Ehrenfest klasyfikuje przemiany fazowe w oparciu o potencjał chemiczny. nieciągłość Przemiany fazowe pierwszego rodzaju pochodne potencjału
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Termodynamika. Energia wewnętrzna ciał
 ermodynamika Energia wewnętrzna ciał Cząsteczki ciał stałych, cieczy i gazów znajdują się w nieustannym ruchu oddziałując ze sobą. Sumę energii kinetycznej oraz potencjalnej oddziałujących cząsteczek nazywamy
ermodynamika Energia wewnętrzna ciał Cząsteczki ciał stałych, cieczy i gazów znajdują się w nieustannym ruchu oddziałując ze sobą. Sumę energii kinetycznej oraz potencjalnej oddziałujących cząsteczek nazywamy
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
TERMODYNAMIKA PROCESOWA
 (pieczęć wydziału) KARTA PRZEDMIOTU 1. Nazwa przedmiotu: TERMODYNAMIKA PROCESOWA 2. Kod przedmiotu: 3. Karta przedmiotu ważna od roku akademickiego:2011/2012 4. Forma kształcenia: studia pierwszego stopnia
(pieczęć wydziału) KARTA PRZEDMIOTU 1. Nazwa przedmiotu: TERMODYNAMIKA PROCESOWA 2. Kod przedmiotu: 3. Karta przedmiotu ważna od roku akademickiego:2011/2012 4. Forma kształcenia: studia pierwszego stopnia
Prężność pary nad roztworem
 Tomasz Lubera Układ: Prężność pary nad roztworem dwuskładnikowy (składniki I i II) dwufazowy (ciecz i gaz) w którym faza ciekła i gazowa to roztwory idealne W stanie równowagi prężności pary składników/układu
Tomasz Lubera Układ: Prężność pary nad roztworem dwuskładnikowy (składniki I i II) dwufazowy (ciecz i gaz) w którym faza ciekła i gazowa to roztwory idealne W stanie równowagi prężności pary składników/układu
II Zasada Termodynamiki c.d.
 Wykład 5 II Zasada Termodynamiki c.d. Pojęcie entropii i temperatury absolutnej II zasada termodynamiki dla procesów nierównowagowych Równania Gibbsa dla procesów quasistatycznych Równania Eulera Relacje
Wykład 5 II Zasada Termodynamiki c.d. Pojęcie entropii i temperatury absolutnej II zasada termodynamiki dla procesów nierównowagowych Równania Gibbsa dla procesów quasistatycznych Równania Eulera Relacje
Rok akademicki: 2017/2018 Kod: WIN s Punkty ECTS: 6. Poziom studiów: Studia I stopnia Forma i tryb studiów: -
 Nazwa modułu: Termodynamika Rok akademicki: 2017/2018 Kod: WIN-1-404-s Punkty ECTS: 6 Wydział: Wiertnictwa, Nafty i Gazu Kierunek: Inżynieria Naftowa i Gazownicza Specjalność: - Poziom studiów: Studia
Nazwa modułu: Termodynamika Rok akademicki: 2017/2018 Kod: WIN-1-404-s Punkty ECTS: 6 Wydział: Wiertnictwa, Nafty i Gazu Kierunek: Inżynieria Naftowa i Gazownicza Specjalność: - Poziom studiów: Studia
Rok akademicki: 2016/2017 Kod: WIN s Punkty ECTS: 6. Poziom studiów: Studia I stopnia Forma i tryb studiów: Stacjonarne
 Nazwa modułu: Termodynamika Rok akademicki: 2016/2017 Kod: WIN-1-404-s Punkty ECTS: 6 Wydział: Wiertnictwa, Nafty i Gazu Kierunek: Inżynieria Naftowa i Gazownicza Specjalność: Poziom studiów: Studia I
Nazwa modułu: Termodynamika Rok akademicki: 2016/2017 Kod: WIN-1-404-s Punkty ECTS: 6 Wydział: Wiertnictwa, Nafty i Gazu Kierunek: Inżynieria Naftowa i Gazownicza Specjalność: Poziom studiów: Studia I
PODSTAWY TERMODYNAMIKI
 ODAWY ERMODYNAMIKI ( punkty (OŚ_3--7 Zad.. W zbiorniku zamkniętym tłokiem znajduje się moli metanu, który można z powodzeniem potraktować jako az doskonały. emperatura początkowa metanu wynosi 5 C a ciśnienie
ODAWY ERMODYNAMIKI ( punkty (OŚ_3--7 Zad.. W zbiorniku zamkniętym tłokiem znajduje się moli metanu, który można z powodzeniem potraktować jako az doskonały. emperatura początkowa metanu wynosi 5 C a ciśnienie
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Zastosowanie destylacji z parą wodną do oznaczania masy cząsteczkowej cieczy niemieszającej się z wodą opracował prof. B. Pałecz ćwiczenie nr 35 Zakres zagadnień
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Zastosowanie destylacji z parą wodną do oznaczania masy cząsteczkowej cieczy niemieszającej się z wodą opracował prof. B. Pałecz ćwiczenie nr 35 Zakres zagadnień
1. PIERWSZA I DRUGA ZASADA TERMODYNAMIKI TERMOCHEMIA
 . PIERWSZA I DRUGA ZASADA ERMODYNAMIKI ERMOCHEMIA Zadania przykładowe.. Jeden mol jednoatomowego gazu doskonałego znajduje się początkowo w warunkach P = 0 Pa i = 300 K. Zmiana ciśnienia do P = 0 Pa nastąpiła:
. PIERWSZA I DRUGA ZASADA ERMODYNAMIKI ERMOCHEMIA Zadania przykładowe.. Jeden mol jednoatomowego gazu doskonałego znajduje się początkowo w warunkach P = 0 Pa i = 300 K. Zmiana ciśnienia do P = 0 Pa nastąpiła:
Badanie równowag ciecz para w układach dwuskładnikowych
 Wprowadzenie Badanie równowag ciecz para w układach dwuskładnikowych Rozważmy równowagę ciecz para w układzie zawierającym dwie ciecze A i B całkowicie mieszające się ze sobą. Zgodnie z regułą faz Gibbsa,
Wprowadzenie Badanie równowag ciecz para w układach dwuskładnikowych Rozważmy równowagę ciecz para w układzie zawierającym dwie ciecze A i B całkowicie mieszające się ze sobą. Zgodnie z regułą faz Gibbsa,
Temperatura jest wspólną własnością dwóch ciał, które pozostają ze sobą w równowadze termicznej.
 1 Ciepło jest sposobem przekazywania energii z jednego ciała do drugiego. Ciepło przepływa pod wpływem różnicy temperatur. Jeżeli ciepło nie przepływa mówimy o stanie równowagi termicznej. Zerowa zasada
1 Ciepło jest sposobem przekazywania energii z jednego ciała do drugiego. Ciepło przepływa pod wpływem różnicy temperatur. Jeżeli ciepło nie przepływa mówimy o stanie równowagi termicznej. Zerowa zasada
Instrukcja dla uczestnika
 III edycja Konkursu Chemicznego Chemik dla uczniów szkół podstawowych i gimnazjalnych rok szkolny 2017/2018 Instrukcja dla uczestnika I etap Konkursu (etap szkolny) 1. Sprawdź, czy arkusz konkursowy, który
III edycja Konkursu Chemicznego Chemik dla uczniów szkół podstawowych i gimnazjalnych rok szkolny 2017/2018 Instrukcja dla uczestnika I etap Konkursu (etap szkolny) 1. Sprawdź, czy arkusz konkursowy, który
Termodynamika Termodynamika
 Termodynamika 1. Wiśniewski S.: Termodynamika techniczna, WNT, Warszawa 1980, 1987, 1993. 2. Jarosiński J., Wiejacki Z., Wiśniewski S.: Termodynamika, skrypt PŁ. Łódź 1993. 3. Zbiór zadań z termodynamiki
Termodynamika 1. Wiśniewski S.: Termodynamika techniczna, WNT, Warszawa 1980, 1987, 1993. 2. Jarosiński J., Wiejacki Z., Wiśniewski S.: Termodynamika, skrypt PŁ. Łódź 1993. 3. Zbiór zadań z termodynamiki
WNIKANIE CIEPŁA PRZY WRZENIU CIECZY
 WNIKANIE CIEPŁA PRZY WRZENIU CIECZY 1. Wprowadzenie Z wrzeniem cieczy jednoskładnikowej A mamy do czynienia wówczas, gdy proces przechodzenia cząstek cieczy w parę zachodzi w takiej temperaturze, w której
WNIKANIE CIEPŁA PRZY WRZENIU CIECZY 1. Wprowadzenie Z wrzeniem cieczy jednoskładnikowej A mamy do czynienia wówczas, gdy proces przechodzenia cząstek cieczy w parę zachodzi w takiej temperaturze, w której
3.1. Równowagi fazowe układach jednoskładnikowych 3.2. Termodynamika równowag fazowych 3.3. Równowagi fazowe układach dwuskładnikowych 3.4.
 Równowagi fazowe w układach jedno- i wieloskładnikowych jedno- lub wielofazowych 3.1. Równowagi fazowe układach jednoskładnikowych 3.2. Termodynamika równowag fazowych 3.3. Równowagi fazowe układach dwuskładnikowych
Równowagi fazowe w układach jedno- i wieloskładnikowych jedno- lub wielofazowych 3.1. Równowagi fazowe układach jednoskładnikowych 3.2. Termodynamika równowag fazowych 3.3. Równowagi fazowe układach dwuskładnikowych
Entropia - obliczanie. Podsumowanie
 Chem. Fiz. CH II/4 Entropia - obliczanie. Podsumowanie 2 ) ( 2 V d C S S S 2 ) ( 2 P d C S S S S k S p S 2 2 ln ln V V R C S V + 2 2 ln ln P P R C S P w izobarze: Funkcja stanu! w izochorze: dla gazu doskonałego:
Chem. Fiz. CH II/4 Entropia - obliczanie. Podsumowanie 2 ) ( 2 V d C S S S 2 ) ( 2 P d C S S S S k S p S 2 2 ln ln V V R C S V + 2 2 ln ln P P R C S P w izobarze: Funkcja stanu! w izochorze: dla gazu doskonałego:
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Wyznaczanie entalpii parowania wody na podstawie pomiaru temperaturowego współczynnika prężności pary
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie entalpii parowania wody na podstawie pomiaru temperaturowego współczynnika prężności pary opiekun ćwiczenia: dr Michał Wasiak ćwiczenie nr 33
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie entalpii parowania wody na podstawie pomiaru temperaturowego współczynnika prężności pary opiekun ćwiczenia: dr Michał Wasiak ćwiczenie nr 33
Badanie zależności temperatury wrzenia cieczy od ciśnienia
 Katedra Silników Spalinowych i Pojazdów ATH ZAKŁAD TERMODYNAMIKI Badanie zależności temperatury wrzenia cieczy od ciśnienia - 1 - Wstęp teoretyczny Gaz rzeczywisty jest jedynym z trzech stanów skupienia
Katedra Silników Spalinowych i Pojazdów ATH ZAKŁAD TERMODYNAMIKI Badanie zależności temperatury wrzenia cieczy od ciśnienia - 1 - Wstęp teoretyczny Gaz rzeczywisty jest jedynym z trzech stanów skupienia
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1. Kontakt,informacja i konsultacje. Co to jest chemia fizyczna?
 Chemia Fizyczna Technologia Chemiczna II ro Wyład 1 Kierowni rzedmiotu: Dr hab. inż. Wojciech Chrzanowsi Kontat,informacja i onsultacje Chemia A ; oój 307 Telefon: 347-2769 E-mail: wojte@chem.g.gda.l tablica
Chemia Fizyczna Technologia Chemiczna II ro Wyład 1 Kierowni rzedmiotu: Dr hab. inż. Wojciech Chrzanowsi Kontat,informacja i onsultacje Chemia A ; oój 307 Telefon: 347-2769 E-mail: wojte@chem.g.gda.l tablica
Fizyka statystyczna. This Book Is Generated By Wb2PDF. using
 http://pl.wikibooks.org/wiki/fizyka_statystyczna This Book Is Generated By Wb2PDF using RenderX XEP, XML to PDF XSL-FO Formatter 18-05-2014 Table of Contents 1. Fizyka statystyczna...4 Spis treści..........................................................................?
http://pl.wikibooks.org/wiki/fizyka_statystyczna This Book Is Generated By Wb2PDF using RenderX XEP, XML to PDF XSL-FO Formatter 18-05-2014 Table of Contents 1. Fizyka statystyczna...4 Spis treści..........................................................................?
Wykresy równowagi układu żelazo-węgiel. Stabilny żelazo grafit Metastabilny żelazo cementyt
 Wykresy równowagi układu żelazo-węgiel Stabilny żelazo grafit Metastabilny żelazo cementyt UKŁAD RÓWNOWAGI FAZOWEJ ŻELAZO-CEMENTYT Schemat wykresu układu równowagi fazowej żelazo-węgiel i żelazo-cementyt
Wykresy równowagi układu żelazo-węgiel Stabilny żelazo grafit Metastabilny żelazo cementyt UKŁAD RÓWNOWAGI FAZOWEJ ŻELAZO-CEMENTYT Schemat wykresu układu równowagi fazowej żelazo-węgiel i żelazo-cementyt
Wykład 2. Anna Ptaszek. 7 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 2. Anna Ptaszek 1 / 1
 Wykład 2 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 7 października 2015 1 / 1 Zjawiska koligatywne Rozpuszczenie w wodzie substancji nielotnej powoduje obniżenie prężności pary nasyconej P woda
Wykład 2 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 7 października 2015 1 / 1 Zjawiska koligatywne Rozpuszczenie w wodzie substancji nielotnej powoduje obniżenie prężności pary nasyconej P woda
CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ
 CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ Ciepło i temperatura Pojemność cieplna i ciepło właściwe Ciepło przemiany Przejścia między stanami Rozszerzalność cieplna Sprężystość ciał Prawo Hooke a Mechaniczne
CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ Ciepło i temperatura Pojemność cieplna i ciepło właściwe Ciepło przemiany Przejścia między stanami Rozszerzalność cieplna Sprężystość ciał Prawo Hooke a Mechaniczne
KARTA PRZEDMIOTU. definiuje podstawowe potencjały termodynamiczne. wyjaśnia pojęcia równowagi i stabilności faz
 1 3 4 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 3 wiedza Symbole efektów kształcenia K_U01 3 umiejętności K_K01 11 kompetencje
1 3 4 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 3 wiedza Symbole efektów kształcenia K_U01 3 umiejętności K_K01 11 kompetencje
Temat 2. Równowaga fazowa i diagramy fazowe
 Temat 2. Równowaga fazowa i diagramy fazowe 2.1. Reguła faz Gibbsa Rozważmy układ złożony z C składników (ang. components) rozdzielonych pomiędzy P homogeniczne fazy (ang. phases). Układ jest w równowadze
Temat 2. Równowaga fazowa i diagramy fazowe 2.1. Reguła faz Gibbsa Rozważmy układ złożony z C składników (ang. components) rozdzielonych pomiędzy P homogeniczne fazy (ang. phases). Układ jest w równowadze
3 Potencjały termodynamiczne i transformacja Legendre a
 3 Potencjały termodynamiczne i transformacja Legendre a literatura: Ingarden, Jamiołkowski i Mrugała, Fizyka Statystyczna i ermodynamika, 9 W.I Arnold, Metody matematyczne mechaniki klasycznej, 14 3.1
3 Potencjały termodynamiczne i transformacja Legendre a literatura: Ingarden, Jamiołkowski i Mrugała, Fizyka Statystyczna i ermodynamika, 9 W.I Arnold, Metody matematyczne mechaniki klasycznej, 14 3.1
Wykład Temperatura termodynamiczna 6.4 Nierówno
 ykład 8 6.3 emperatura termodynamiczna 6.4 Nierówność Clausiusa 6.5 Makroskopowa definicja entropii oraz zasada wzrostu entropii 6.6 Entropia dla czystej substancji 6.8 Cykl Carnota 6.7 Entropia dla gazu
ykład 8 6.3 emperatura termodynamiczna 6.4 Nierówność Clausiusa 6.5 Makroskopowa definicja entropii oraz zasada wzrostu entropii 6.6 Entropia dla czystej substancji 6.8 Cykl Carnota 6.7 Entropia dla gazu
1) Rozmiar atomu to około? Która z odpowiedzi jest nieprawidłowa? a) 0, m b) 10-8 mm c) m d) km e) m f)
 1) Rozmiar atomu to około? Która z odpowiedzi jest nieprawidłowa? a) 0,0000000001 m b) 10-8 mm c) 10-10 m d) 10-12 km e) 10-15 m f) 2) Z jakich cząstek składają się dodatnio naładowane jądra atomów? (e
1) Rozmiar atomu to około? Która z odpowiedzi jest nieprawidłowa? a) 0,0000000001 m b) 10-8 mm c) 10-10 m d) 10-12 km e) 10-15 m f) 2) Z jakich cząstek składają się dodatnio naładowane jądra atomów? (e
Kryteria samorzutności procesów fizyko-chemicznych
 Kryteria samorzutności procesów fizyko-chemicznych 2.5.1. Samorzutność i równowaga 2.5.2. Sens i pojęcie entalpii swobodnej 2.5.3. Sens i pojęcie energii swobodnej 2.5.4. Obliczanie zmian entalpii oraz
Kryteria samorzutności procesów fizyko-chemicznych 2.5.1. Samorzutność i równowaga 2.5.2. Sens i pojęcie entalpii swobodnej 2.5.3. Sens i pojęcie energii swobodnej 2.5.4. Obliczanie zmian entalpii oraz
