Kod znakowania krwi i jej składników w placówkach publicznej słuŝby krwi zgodny ze standardem ISBT 128
|
|
|
- Oskar Szymański
- 9 lat temu
- Przeglądów:
Transkrypt
1 Kod znakowania krwi i jej składników w placówkach publicznej słuŝby krwi zgodny ze standardem ISBT 128 Warszawa, 2009 r. Strona 1 z 134
2 Szanowni Państwo, Konieczność ustanowienia odpowiedniego systemu zapewniającego identyfikację krwi i jej składników określa Dyrektywa 2002/98/EC. System ten musi jednoznacznie identyfikować kaŝdą niepowtarzalną donację i rodzaj składnika krwi. Wysoce poŝądanym jest by taka identyfikacja była moŝliwa nie tylko w kraju wytwórcy, ale teŝ w krajach Wspólnoty Europejskiej. Międzynarodowy Standard ISBT 128 określa sposób identyfikacji, etykietowania krwi i jej składników, a takŝe ludzkich tkanek i narządów. System ten został opracowany przez Międzynarodowe Towarzystwo Przetaczania Krwi (ISBT) w 1994 roku i zatwierdzony przez American Association of Blood Banks (AABB), European Blood Aliance (EBA), Food and Drug Administration (FDA) i European Plasma Fractionators Association (EPFA). Standard ISBT 128 jest zarządzany przez International Council for Commonality in Blood Bank Automation (ICCBBA) w USA. WdroŜenie systemu identyfikacji i etykietowania krwi i jej składników zgodnego ze standardem ISBT 128 wnosi nową, jakość do funkcjonowania słuŝby krwi. Do największych zalet implementacji standardu ISBT 128 naleŝą: - unifikacja nazw składników krwi oraz algorytmów ich produkcji, - dostępność na etykiecie do wszystkich istotnych informacji o składniku krwi i moŝliwość ich automatycznego odczytania i przetwarzania, niezaleŝnie od uŝywanego języka, czy systemu komputerowego, - umoŝliwienie automatycznego przetwarzania danych o składnikach krwi otrzymanych z innych niŝ macierzysta placówek słuŝby krwi, w tym takŝe z zagranicznych stosujących standard ISBT 128, - znaczne ułatwienie w gromadzeniu i przetwarzaniu danych statystycznych w skali całego kraju. Decyzja o wprowadzeniu standardu ISBT 128 w polskiej słuŝbie krwi zapadła w 2006 roku. W tym teŝ roku polska słuŝba krwi została zarejestrowana w ICCBBA. Polska wersja standardu ISBT 128 została opracowana przez Zespół do spraw opracowania zasad i harmonogramu wprowadzenia międzynarodowego kodu znakowania krwi i jej składników w placówkach publicznej słuŝby krwi w składzie: doc. dr hab. Jolanta Korsak zastępca przewodniczącego dr n. med. Mateusz Kuczabski Beata Uszyńska-KałuŜa Strona 2 z 134
3 Paweł Wojtylak Jolanta Fiołek Emilia Przybylska Dorota Śniegórska Radojewski Leszek Marcin Szmecht Dariusz Średziński Andrzej Falger Jacek Południak Pragnę złoŝyć wyrazy uznania wszystkim członkom Zespołu za ogromny wkład pracy włoŝony w to opracowanie i podziękować za miłą i efektywną współpracę. Piotr Radziwon Przewodniczący Zespołu Strona 3 z 134
4 Spis treści 1. Wprowadzenie 4 2. Wzór etykiety Lewy górny kwadrat 2.2. Prawy górny kwadrat 2.3. Lewy dolny kwadrat 2.4. Prawy dolny kwadrat 3. Opis składnika krwi Klasy składników krwi 3.2. Modyfikatory 3.3. Atrybuty 3.4. Typ dawcy i donacji 3.5. Podziały składników krwi 4. Zasady tworzenia słownika składników krwi Słownik składników krwi 21 Strona 4 z 134
5 1. Wprowadzenie Pod koniec lat dziewięćdziesiątych ubiegłego wieku w polskiej słuŝbie krwi wprowadzono jednolity system numeracji składników krwi. System ten identyfikował placówkę słuŝby krwi i kolejną donację pobraną w danej placówce. Numer był niepowtarzalny i jest kontynuowany do dnia dzisiejszego. System ten ujednolicił identyfikację krwi i jej składników w naszym kraju, jednak w bardzo wąskim zakresie. Liczba informacji zawartych na etykiecie oraz skomplikowanie dzisiejszych procedur preparatyki krwi wymuszają wprowadzenie nowego, znacznie szerszego systemu znakowania krwi i jej składników. W dzisiejszym świecie pełnym programów zwalczania skutków katastrof, międzynarodowych misji wojskowych krew pozyskana i rozdzielona na składniki w jednym kraju moŝe być klinicznie wykorzystana w innym. Rzeczą oczywistą stało się, aby najwaŝniejsze informacje takie jak grupa krwi, data waŝności i rodzaj składnika krwi były precyzyjnie zrozumiałe przez personel medyczny dokonujący przetoczeń. Mając na uwadze bezpieczeństwo stosowania krwi i jej składników oraz przejrzystość wykorzystywanych informacji istotne stało się równieŝ, aby dane były łatwe do automatycznego odczytania i przetwarzania przez system komputerowy. Nowy system znakowania krwi i jej składników musi, więc być zgodny ze standardem międzynarodowym. Wprowadzany Standard ISBT 128 oparty jest na kodzie 128. Opisuje on sposób zapisywania i przetwarzania informacji krytycznych takich, jak min.: numer identyfikacyjny donacji, grupa krwi, opis składnika krwi, data waŝności. Określa on równieŝ kształt i strukturę etykiety oraz kod zapisu informacji. Stosowanie standardu ISBT 128 w pełnym zakresie pozwala równieŝ na kodowanie i informacji sposoby wytwarzania składników krwi określone medycznymi zasadami obowiązującymi w placówkach publicznej słuŝby krwi. 2. Wzór etykiety. Standardowo etykieta na składnikach krwi podzielona jest na cztery kwadraty o równych wymiarach 5,08 x 5,08 cm, w których znajdują się kody paskowe. Wymiar całej etykiety wynosi 10,16 x 10,16 cm. Kody paskowe bez względu na miejsce otrzymania składnika krwi i jego rodzaj powinny być umieszczone zawsze w tym samym miejscu. Strona 5 z 134
6 Standard ISBT 128 określa połoŝenie następujących kodów paskowych: * numer identyfikacyjny donacji * grupę krwi * kod składnika krwi * data i godzina waŝności * kod badań dodatkowych. Ponadto na etykiecie znajduje się informacja w postaci tekstu, który powinien być zgodny z wymaganiami słuŝby krwi w naszym kraju. PoniŜsza rycina przedstawia wzór etykiety. Wzór etykiety wg ISBT 128 Kod paskowy numeru donacji Kod paskowy grupy krwi Numer donacji Miejsce wytwarzania Z Regionalne Centrum Krwiodawstwa i Krwiolecznictwa Katowice ul Raciborska ggwo Grupa krwi: ABO Rh * - ujemny * + dodatni Data pobrania Data pobrania: Rh- (ujemny) Data preparatyki Data preparatyki: Kod składnika krwi Nazwa składnika : modyfikator Klasa atrybut Objętość Uwagi αooootds Przemywany KKCz z płynem wzbogacającym Napromieniowany 280 ml Przechowywać w temp. 4 0 C Nie przetaczać w przypadku hemolizy, zmian preparatu lub uszkodzenia pojemnika XXXXXXXX Data waŝności: 30 STY 2009 godz XXXXXXXXXX D cc ee Kk Kp(a+b-)Fy(a-b+) K(a+b)MN SS Le (a+b) Lu(a-b+) Wyniki badań kwalifikacyjnych ujemne Kod paskowy daty waŝności Data waŝności Kod paskowy badań dodatkowych Badania dodatkowe Badania kwalifikacyjne( opcja) 2.1. W lewym górnym kwadracie znajduje się: a) numer donacji zapisany w formie kodu paskowego, pod którym znajduje się zapis alfanumeryczny numeru donacji zgodny ze standardem ISBT 128. Struktura ta składa się z trzynastu znaków ułoŝonych w trzy grupy: pierwsza identyfikuje Strona 6 z 134
7 placówkę pobierającą krew lub składnik krwi, druga rok pobrania i trzecia kolejny numer donacji. Przykład: Z gdzie: * Z 5001 identyfikuje kraj pobrania (dla Polski ustanowiono literę Z) oraz placówkę słuŝby krwi (placówki publicznej słuŝby krwi zarejestrowano w ICCBBA pod numerami od ) * 09 identyfikuje rok pobrania * jest kolejnym numerem donacji przypisanym przez placówkę słuŝby krwi. Dwie cyfry wydrukowane pionowo przy numerze donacji pozwalają na wstępną identyfikację indywidualnego kodu paskowego w systemie numerycznym, w ten sposób stworzono opcję dodania kontroli całego systemu do procedur pobierania, oddzielania i badania składników krwi. Dodatkowy znak jest zamknięty w ramce przy końcu identyfikatora. Jest to znak kontrolny stosowany wówczas, gdy numer wpisywany jest w komputer z klawiatury w celu sprawdzenia, czy klawiatura pracuje prawidłowo. b) nazwa i adres placówki, w której pobrano donację c) data pobrania donacji (np ) d) data preparatyki (np ) 2.2. W prawym górnym kwadracie znajduje się a) grupa krwi zapisana w formie kodu paskowego, pod którą znajduje się zapis alfanumeryczny grupy krwi zgodny ze standardem ISBT 128. Ta struktura danych ma cztery cechy: ggwo gdzie: * gg oznacza grupę krwi ABO/Rh * W określa informacje o fenotypie Rh oraz Kell, które w formie opisowej oraz kodu kreskowego znajdują się w czwartym kwadracie etykiety * O jest zarezerwowane do uŝytku w przyszłości Strona 7 z 134
8 b) grupa krwi układu AB zapis: A, B, 0 lub AB ( w przypadku Rh dodatniego litery wypełnione na czarno, Rh ujemne litery białe z czarną obwódką) c) czynnik Rh: Rh + dodatni czarne litery na białym tle Rh (ujemny) białe litery na czarnym tle 2.3. W lewym dolnym kwadracie znajduje się: a) kod składnika krwi zapisany w formie kodu paskowego, pod którym znajduje się zapis alfanumeryczny numeru donacji zgodny ze standardem ISBT 128. Struktura danych kodu składnika krwi zawiera osiem cech danych: αoooo t ds gdzie: * αoooo jest opisem produktu krwi (ciąg kodów identyfikujących rodzaj składnika krwi i danych dotyczących preparatyki) * t oznacza typ donacji * ds dostarcza informacji o typie produktu krwi i jego podziałach Znak α oznacza grupy produktów znajdujących się w bazie ISBT. Zastąpiony przez litery E, S i T określa: E składniki krwi S komórki krwiotwórcze T - tkanki Pierwszych pięć cech danych (αoooo) zaczerpnięto z bazy danych ISBT 128. Dostarczają one zgodny ze standardem opis składnika krwi; identyfikują klasę składnika krwi (np.: krwinki czerwone, osocze świeŝo mroŝone) oraz atrybuty związane z tym składnikiem (np.: napromieniowanie, produkowany w systemie otwartym). Przykład: E0291 oznacza koncentrat krwinek czerwonych w płynie wzbogacającym ADSOL, otrzymany z jednej jednostki krwi pełnej pobranej na CPD, przechowywany w temp. 4-6 C. b) nazwa składnika krwi, która składa się z 3 części umieszczonych w kolejnych wierszach: modyfikator (średnia czcionka) klasa (duŝa czcionka) Strona 8 z 134
9 atrybut (mała czcionka) istnieje moŝliwość wpisania maksymalnie 6 atrybutów c) objętość składnika krwi d) informacja dla odbiorcy w języku polskim, na temat specyficznego postępowania ze składnikiem krwi i ewentualnie warunków przechowywania W prawym dolnym kwadracie znajduje się : a) data waŝności zapisana w formie kodu paskowego, pod którym znajduje się zapis alfanumeryczny wiek, rok, dzień ewentualnie godzina zgodny z ISBT128 b) rozpisana data waŝności ze skrótem nazwy miesiąca w języku polskim (np.17 GRU 2005) c) kod paskowy badań dodatkowych d) bezpośrednio pod kodem paskowym znajduje się zapis alfanumeryczny kodu wyników badań dodatkowych zgodny ze standardem ISBT 128 dotyczy fenotypu i/lub wyników testów HLA i CMV e) dane wymienne dla polskiej specyfikacji umieszczane w formie tekstu: dla składników zawierających krwinki czerwone: fenotyp rozpisany zgodnie z zasadami immunologii transfuzjologicznej dla składnika rekonstytuowanego zamieszczony jest dodatkowy tekst: zawieszono w osoczu grupy (tu grupa krwi) o numerze donacji osocza (tu nr donacji osocza) dla osocza moŝe być zamieszczony dodatkowy tekst tylko dla biorcy grupy (tu grupa krwi) dla osocza immunizowanego napis: osocze immunizowane Rh lub osocze immunizowane HBs i moŝe być podane miano przeciwciał dla osocza przeznaczonego do frakcjonowania napis osocze do wytwórni dla donacji autologicznej w miejsce kodu paskowego fenotypu znajdują się dane odbiorcy (nazwa szpitala i adres szpitala) a poniŝej informacja: Przeznaczone wyłącznie dla (tu imię i nazwisko biorcy oraz jego data urodzenia) Strona 9 z 134
10 3. Opis składnika krwi Opis składnika krwi. opcjonalnie tekst Wyniki badań kwalifikacyjnych ujemne Opis składnika krwi identyfikuje: * klasę składnika krwi składniki krwi komórkowe i niekomórkowe * modyfikatory określają czynność wykonywaną przy preparatyce. Odnoszą się do podstawowych warunków składnika krwi i odróŝniają go od innych części tej samej klasy składników (np.: przemywany, zamroŝony) * atrybuty dostarczają dodatkowych informacji o składniku krwi związanych z jego przeznaczeniem lub metodą przygotowania. Atrybuty kategoryzowane są, jako warunki niezbędne oraz inne atrybuty. Warunki niezbędne zawierają cechy opisujące pobranie i warunki przechowywania składników krwi. Informują one o rodzaju płynu konserwującego, na który pobierana jest krew lub który stosowany jest w procedurach aferezy, objętości nominalnej pobranej krwi (bez płynu konserwującego) i temperaturze przechowywania składników. Cechy niezbędne są zawsze obecne w opisie składnika krwi. Przykład: CPD>AS-1/450ml/2-6 o C oznacza składnik krwi zawieszony w ADSOL-u otrzymany z jednej jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD przechowywany w temp. 2-6 o C CPDA-1/XX/<=-18 o C oznacza składnik krwi otrzymany NK/XX/20-24 o C z niewyspecyfikowanej objętości krwi pełnej pobranej na CPDA-1 przechowywany w temp. niŝszej lub równej 18 o C oznacza składnik krwi otrzymany z niewyspecyfikowanej objętości krwi pełnej pobranej na nieokreślony kodem płyn konserwujący przechowywany w temp o C Strona 10 z 134
11 3.2. Klasy składników krwi Klasa składnika krwi obejmuje zarówno komórkowe jak i niekomórkowe składniki otrzymywane z krwi pełnej lub metodą aferezy. W przypadku składników krwi aferezowych do opisu dodaje się z aferezy. Wprowadzony Standard ISBT zawiera następujące klasy składników krwi: * krioprecypitat * osocze świeŝo mroŝone * koncentrat granulocytarny * koncentrat leukocytarny * osocze * koncentrat krwinek płytkowych * koŝuszek leukocytarno-płytkowy * osocze bogatopłytkowe * zlewany krioprecypitat * zlewane osocze świeŝo mroŝone * zlewany koncentrat granulocytarny * osocze zlewane * zlewany koncentrat krwinek płytkowych * zlewany koŝuszek leukocytarno-płytkowy * koncentrat krwinek czerwonych * surowica * zlewana surowica * krew pełna Definicje składników krwi znajdują się w publikacji pod redakcją Magdaleny Łętowskiej pt.: Medyczne zasady pobierania krwi, oddzielania jej składników i wydawania, obowiązujące w jednostkach organizacyjnych publicznej słuŝby krwi. Warszawa Modyfikatory. Modyfikatory są opisem dodatkowych czynności wykonywanych przy preparatyce składników krwi. Na ogół zmieniają one warunki niezbędne dla danego składnika np. przemywanie powoduje usuwanie płynu konserwującego ze składnika zmieniając jego środowisko, sposób przechowywania i temperaturę przechowywania. Obowiązujące nazwy i definicje modyfikatorów: Strona 11 z 134
12 deglicerolizowany rozmraŝanie i przemywanie w celu usunięcia glicerolu z krwinek czerwonych mroŝonych deglicerolizowany, aferezowy rozmraŝanie i przemywanie w celu usunięcia glicerolu ze składnika komórkowego otrzymanego metodą aferezy, mroŝonego deglicerolizowany, regenerowany składnik, w którym przed zamroŝeniem krwinki czerwone były regenerowane, następnie został dodany glicerol i krwinki zamroŝono. Po rozmroŝeniu składnik przemyto w celu usunięcia glicerolu. zamroŝony składnik utrzymywany po preparatyce w stanie zmroŝenia zamroŝony, aferezowy składnik otrzymany metodą aferezy i utrzymywany w stanie zamroŝenia po preparatyce zamroŝony, regenerowany - składnik, w którym przed zamroŝeniem komórki krwi były regenerowane, następnie został dodany glicerol i krwinki zamroŝono. płynny składnik krwi przechowywany w stanie płynnym i nieprzeznaczony do zamroŝenia regenerowany stosowanie znanych i dopuszczonych metod powodujących przywrócenie prawidłowych stęŝeń 2,3-DPG i ATP w krwinkach czerwonych. rozmroŝony składnik, który aktualnie znajduje się w stanie płynnym, ale wcześniej był zamroŝony przemywany komórkowy składnik krwi, z którego usunięto białka osocza przemywając 0,9% roztworem soli. aferezowy składniki krwi otrzymane metodami oddzielania, w których pozostałe elementy krwi powracają do dawcy. Połączenie w opisie składnika krwi klasy składnika i modyfikatora tworzy nazwę składnika krwi zmieniając jednocześnie jego kod. Przykład: koncentrat krwinek czerwonych (klasa, kod 002) - koncentrat krwinek czerwonych (nazwa, kod 002) przemywany (modyfikator) + koncentrat krwinek czerwonych (klasa, kod 002) - przemywany koncentrat krwinek czerwonych ( nazwa, kod 003) Strona 12 z 134
13 3.4. Atrybuty Atrybuty dostarczają dodatkowych informacji o składniku krwi związanych z jego przeznaczeniem lub metodą przygotowania. Osobnym rodzajem atrybutów są tzw. warunki niezbędne, które omówiono w pkt.3.1. Obowiązujące warunki niezbędne obecne w opisie kaŝdego składnika krwi: * Antykoagulanty cytrynian sodu formuły A (ACD-A) płyn cytrynianowo-fosforanowo-glukozowy (CPD) płyn cytrynianowo-fosforanowo-glukozowy z adeniną (CPDA-1) cytrynian sodu (NaCytr) cytrynian sodu i hydroksyetylowana skrobia (NaCytr-HES) heparyna * Płyny uzupełniające płyn uzupełniający 1 (AS-1, ADSOL) płyn zawierający chlorek sodu, adeninę, glukozę i mannitol (SAGM) dimetylosulfotlenek (DSMO) roztwór dodawany do koncentratu krwinek płytkowych formuły III (PAS III) glicerol * Inne dotyczące stosowanych płynów konserwujących lub uzupełniających BR - antykoagulant nieobecny, lub ilość nieznacząca, obecny płyn uzupełniający NK - płyn nieokreślony kodem * Objętość nominalna pobranej krwi 450 ml XX - brak informacji o objętości w opisie składnika, ale informacja o nie znajduje się na etykiecie NK - objętość nieokreślona kodem, ale informacja o objętości składnika znajduje się na etykiecie. Strona 13 z 134
14 * Temperatura przechowywania składników krwi o C 2-6 o C zamroŝony - 18 o C - 20 o C - 25 o C - 30 o C < - 65 o C < o C Wszystkie składniki krwi mają ostatecznie określone warunki niezbędne oraz atrybuty dostarczające dodatkowych informacji zaleŝnie od głównych grup atrybutów. Grupy atrybutów stanowią atrybuty zawierające podobną informację dotyczącą składnika krwi. PoniŜej zostały przedstawione grupy główne: * planowane zastosowanie składnika krwi * integralność systemu * napromieniowanie * zawartość leukocytów w składniku * zmiany w składnikach krwi * objętości końcowe składników krwi * preparatyka: informacje dodatkowe * preparatyka: afereza * karencja: informacje dodatkowe * dawka: informacje dodatkowe * metody inaktywacji * wartość hematokrytu * liczba płytek * monitorowanie bakteriologiczne KaŜda grupa atrybutów przy swojej definicji zawiera określenie tzw. stanu podstawowego. Znaczy to, Ŝe jeŝeli w opisie składnika krwi nie ma informacji o atrybucie, a jest informacja o grupie atrybutów to zawsze określa go to, co jest zawarte w określeniu stanu podstawowego. Strona 14 z 134
15 Przykład: grupa atrybutów: integralność systemu stan podstawowy określa zawsze składnik krwi, który został przygotowany w systemie zamkniętym W polskiej specyfikacji przyjęto następujące grupy i naleŝące do nich atrybuty: A. Grupa główna atrybutów: planowane zastosowanie składnika krwi Stan podstawowy: składnik krwi przeznaczony do przetoczenia Atrybuty: * do dalszej preparatyki do uŝytku klinicznego * do dalszej preparatyki nie do uŝytku klinicznego * nie do preparatyki i nie do uŝytku klinicznego B. Grupa główna atrybutów: integralność systemu Stan podstawowy: składnik krwi, który został przygotowany w systemie zamkniętym i integralność tego systemu jest zachowana Atrybuty: * system otwarty C. Grupa główna atrybutów: napromieniowanie Stan podstawowy: składnik krwi, który nie został napromieniowany Atrybuty: * napromieniowany D. Grupa główna atrybutów: zawartość leukocytów Stan podstawowy: składnik krwi, który nie został poddany procedurze usuwania leukocytów Atrybuty: * liczba leukocytów niewyspecyfikowana oznacza, Ŝe procedura redukcji liczby leukocytów była stosowana, ale nie wyspecyfikowano ich liczby * liczba leukocytów < 1 x 10 6 (< 1 log 6) dla składników krwi poddanych filtrowaniu lub produkowanych z krwi pełnej filtrowanej przed oddzieleniem składników Strona 15 z 134
16 * liczba leukocytów < 1,2 x 10 9 (< 1,2 log 9) dla koncentratu krwinek czerwonych pozbawionych koŝuszka leukocytarno-płytkowego E. Grupa główna atrybutów: zmiany w składnikach krwi Stan podstawowy: składnik krwi, który został zmieniony przez dodawanie lub usunięcie roztworów lub niektórych elementów krwi Atrybuty: * dodana albumina do składnika krwi * obniŝone stęŝenie krioprecypitatu * dodane osocze do składnika krwi * zmniejszona objętość osocza * obniŝona liczba płytek krwi * usunięty supernatant * usunięto supernatant / dodano osocze * obniŝona liczba płytek krwi i stęŝenie krioprecypitatu w składniku * zmniejszona objętość supernatantu * usunięty koŝuszek leukocytarno-plytkowy * zmniejszono objętość osocza / dodano osocze F. Grupa główna atrybutów: końcowa objętość stan podstawowy: objętość zgodna, z tym, czego się spodziewamy, zwykle uzyskiwana Atrybuty: * objętość końcowa niekreślona kodem * około 25 ml rzeczywisty zakres objętości składnika krwi ustalony przez placówkę słuŝby krwi * około 50 ml rzeczywisty zakres objętości składnika krwi ustalony przez placówkę słuŝby krwi * objętość końcowa: < 200 ml * objętość końcowa: 200 ml < 400 ml * objętość końcowa: 400 ml < 600 ml * objętość końcowa: 600 ml * objętość końcowa mała: objętość antykoagulantu dostosowana * objętość końcowa mała: objętość antykoagulantu niedostosowana Strona 16 z 134
17 G. Grupa główna atrybutów: preparatyka: informacje dodatkowe stan podstawowy: nie ma dodatkowej informacji o preparatyce składnika krwi Atrybuty: * krwinki płytkowe otrzymane z koŝuszka leukocytarno-płytkowego * osocze mroŝone * 6 godzin * osocze mroŝone * 8 godzin * osocze mroŝone * 24 godzin * osocze mroŝone > 24 godzin * koncentrat granulocytarny otrzymany przy uŝyciu HES H. Grupa: afereza: informacje dodatkowe stan podstawowy: nie ma Ŝadnej dodatkowej informacji na temat procedur aferezy lub liczby pojemników ze składnikiem krwi uzyskanych w czasie procedury. Atrybuty: * afereza manualna * pierwszy pojemnik oznacza pierwszy z dwóch pojemników uzyskiwanych w czasie aferezy manualnej * drugi pojemnik - oznacza drugi z dwóch lub więcej pojemników uzyskiwanych w czasie aferezy manualnej.. * pierwszy pojemnik: nie automatyczny * drugi pojemnik: nie automatyczny I. Grupa główna atrybutów: karencja: informacje dodatkowe stan podstawowy: nie zawiera dodatkowej informacji na temat karencji przed dopuszczeniem składnika krwi do uŝytku klinicznego Atrybuty: * karencja: 112 dni, dawca ponownie zbadany otrzymano wynik negatywny J. Grupa główna atrybutów: dawka: informacje dodatkowe stan podstawowy: nie zawiera dodatkowej informacji odnoszącej się do liczby łączonych składników lub liczby krwinek płytkowych w składniku Strona 17 z 134
18 Atrybuty: * od 2 dawców * od 3 dawców * od 4 dawców * od 5 dawców * od 6 dawców * od 7 dawców * od 8 dawców * od 9 dawców * od 10 dawców * około 120 log9 krwinek płytkowych * około 180 log9 krwinek płytkowych * około 240 log9 krwinek płytkowych * około 300 log9 krwinek płytkowych * około 360 log9 krwinek płytkowych * około 420 log9 krwinek płytkowych * < 3 log11 krwinek płytkowych * 3,0-4,7 log11 krwinek płytkowych * 4,8 5,9 log11 krwinek płytkowych * > 6,0 log11 krwinek płytkowych Opisując koncentrat krwinek płytkowych atrybutem określającym liczbę krwinek płytkowych naleŝy kaŝdy składnik zbadać lub tak wystandaryzować procedury aferezy, aby uzyskać powtarzalność wyników. K. Grupa główna atrybutów: metody inaktywacji stan podstawowy: Ŝadna z metod inaktywacji nie była stosowana Atrybuty: * inaktywacja błękitem metylenowym * inaktywacja psolarenem * inaktywacja z zastosowaniem ryboflawiny L. Grupa główna atrybutów: hematokryt stan podstawowy: hematokryt krwinek czerwonych nie jest określony Strona 18 z 134
19 Atrybuty: * 0,5 0,7 * 0,55 0,75 * > 0,7 Atrybut dotyczący wartości hematokrytu przy opisie składnika krwi moŝna stosować po wykonaniu badań. Ł. Grupa główna atrybutów: badanie bakteriologiczne stan podstawowy: informacja o badaniach bakteriologicznych nie została zamieszczona Atrybuty: * bakteriologicznie monitorowany produkt poddany ciągłemu monitorowaniu bakteriologicznemu * jednorazowe badanie bakteriologiczne przeprowadzony po 24 godzinach lub więcej przechowywania 3.5. Typ dawcy i donacji Krew i jej składniki w placówkach słuŝby krwi pobierane są nie tylko od dawców honorowych. Dawcami mogą być chorzy, którzy oddają krew dla siebie w procedurze autotransfuzji. Mogą być u nich wykonywane zabiegi lecznicze takie jak upusty krwi lub lecznicze erytroferezy. Ponadto dawcy mogą być rodzinni lub stanowić źródło składników o specjalnym charakterze. Po analizie struktury polskich dawców i rodzajów donacji oraz bazy danych ISBT zdefiniowano następujące typy dawców i donacji: Kod 0 niewyspecyfikowane informacja o rodzaju dawcy lub donacji nie została zakodowana. Oznacza dawcę wezwanego w celu wykonania ponownych lub dodatkowych badań Kod V dawca honorowy Kod R dawca honorowy, wielokrotny Kod S dawca honorowy, pierwszorazowy Kod T donacja terapeutyczna - np. krwioupust Kod A donacja autologiczna kod 1 tylko do autologicznego uŝycia, kod X tylko do uŝycia autologicznego, ryzyko zakaŝenia Strona 19 z 134
20 Kod 4 Kod 5 dawca wskazany dawca rodzinny dawca wezwany np. dawca panelowy, specjalny fenotyp Informacja o typie dawcy lub donacji znajduje w kodzie składnika krwi Podziały składników krwi. Jednostka składnika krwi moŝe być podzielona na dwie lub więcej części. Części te posiadają ten sam numer identyfikujący donację. Natomiast informacja o podziałach zawarta jest w kodzie składnika - miejsce ds ( pkt. 2.3 opracowania), jeŝeli podziały nie są wykonywane miejsce to kodowane jest 00. KaŜdy pierwszy podział kodowany jest duŝymi literami alfabetu, np.: A0, B0, C0, D0 itp. Kolejne podziały juŝ wcześniej podzielonych objętości składnika kodowane są małymi literami alfabetu, np.: Aa, Ab, Ac itp. lub Ba, Bb, Bc itp. Przykłady: 1) JeŜeli 300 ml stanowiące jedną jednostkę koncentratu krwinek czerwonych podzielono na trzy porcje po 100 ml to kod składnika: przed podziałem - E koncentrat krwinek czerwonych/cpda-1/450ml/2-6c po podziale E01950A0 koncentrat krwinek czerwonych/cpda-1/450ml/2-6c E01950B0 koncentrat krwinek czerwonych/cpda-1/450ml/2-6c E01950C0 koncentrat krwinek czerwonych/cpda-1/450ml/2-6c 2) JeŜeli z jednej jednostki koncentratu krwinek czerwonych o objętości 300 ml pobrano 50 ml otrzymując dwie porcje (jedna 50 ml, druga 250 ml) to kod składnika: przed podziałem - E koncentrat krwinek czerwonych/cpda-1/450ml/2-6c po podziale E01950A0 koncentrat krwinek czerwonych/cpda-1/450ml/2-6c E01950B0 koncentrat krwinek czerwonych/cpda-1/450ml/2-6c Objętości składnika krwi po podziałach znajdują się w opisie na etykiecie. 3) JeŜeli z porcji krwi o objętości 250 ml otrzymanej z podziału w poprzednim przykładzie pobierzemy 15 ml do transfuzji neonatologicznej to kod składnika: przed podziałem - E koncentrat krwinek czerwonych/cpda-1/450ml/2-6c Strona 20 z 134
21 po pierwszym podziale: E01950A0(250ml) koncentrat krwinek czerwonych/cpda-1/450ml/2-6c E01950B0(50ml) koncentrat krwinek czerwonych/cpda-1/450ml/2-6c po drugim podziale: E01950Aa(235ml) koncentrat krwinek czerwonych/cpda-1/450ml/2-6c E01950Ab(15ml) koncentrat krwinek czerwonych/cpda-1/450ml/2-6c E01950B0(50ml) koncentrat krwinek czerwonych/cpda-1/450ml/2-6c 4. Zasady tworzenia słownika składników krwi. Słownik składników krwi jest zbiorem algorytmów i przypisanych im kodów składników specyficznych dla polskiej słuŝby krwi. Został on zaczerpnięty z głównej bazy danych kodów produktów ISBT 128, ale oparty na przepisach obowiązujących w naszym kraju. Część składników krwi specyficznych dla naszej słuŝby krwi została nowozarejestrowana w ISBT. Zasadą tworzenia prezentowanego słownika było takie określenie składnika krwi, aby było to pojęcie jednoznaczne, dokładnie opisujące dany składnik, a takŝe jednakowo rozumiane przez całą słuŝbę oraz rozpoznawane poza granicami kraju. Zamiarem było, aby składnik był opisany przez klasę składnika, cechy niezbędne ze wszystkimi modyfikatorami i atrybutami oraz odpowiadał kodom zawartym w bazie danych ISBT. PoniŜej zostały przedstawione przykłady tworzenia algorytmów składników krwi: a) Klasa składnika/cechy niezbędne Krew pełna /CPD/450ml/2-6C Oznacza: Jednostkę krwi pełnej o objętości 450 ml ± 10% pobranej na 63 ml CPD przechowywanej w temp. 2 6 o C Koncentrat krwinek czerwonych/cpd AS 1/450 ml/2-6c Oznacza: Krwinki czerwone otrzymane z 1 jednostki krwi pełnej pobranej na 63 ml CPD, zawieszone w płynie wzbogacającym ADSOL przechowywane w temp. 2 6 o C b) Klasa składnika krwi/cechy niezbędne/ atrybuty Koncentrat krwinek czerwonych/cpd/450 ml/2-6c/napromieniowane Oznacza: Krwinki czerwone otrzymane z 1 jednostki krwi pełnej pobranej na 63 ml CPD, przechowywane w temp. 2 6 C, poddane napromieniowaniu Strona 21 z 134
22 Koncentrat krwinek czerwonych/cpd AS 1/450ml/2-6C/napromieniowane/ leuk.<1log6 Oznacza: Krwinki czerwone otrzymane z 1 jednostki krwi pełnej pobranej na 63 ml CPD, zawieszone w płynie wzbogacającym ADSOL, przechowywane w temp. 2 6 C, poddane napromieniowaniu, ubogoleukocytarne c) Klasa składnika/modyfikator/cechy niezbędne/grupa atrybutów Osocze świeŝo mroŝone/rozmroŝone/cpda1/450 ml/-25 o C/karencja Oznacza: RozmroŜone osocze świeŝo mroŝone, otrzymane z 450 ml krwi pełnej, przechowywane w temp. -25 C, poddane karencji d) Klasa składnika krwi/modyfikator/ cechy niezbędne/ atrybuty Koncentrat krwinek czerwonych/przemywane/br/450 ml/2-6c/otwarty Oznacza: Przemywane krwinki czerwone, bez płynu konserwującego, otrzymane z 450 ml krwi pełnej, przechowywane w temp. 2 6 o C, wyprodukowane w systemie otwartym. E Słownik składników krwi. Słownik zawiera zbiór algorytmów składników krwi ich definicje oraz kod w ISBT. Przedstawione poniŝej opracowanie jest tekstem otwartym, bowiem postęp wiedzy oraz potrzeby chorych mogą wymagać tworzenia nowych składników krwi, które naleŝałoby wyszukać w bazie międzynarodowego słownika ISBT lub je w nim zarejestrować. Słownik, zatem będzie uzupełniany o nowe składniki krwi lub ich rodzaje. KREW PEŁNA CPD/450ml/2-6C Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2-6 st.c. E0010 KREW PEŁNA CPD/450ml/2-6C do prep./do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2-6 st.c, przeznaczona do uŝytku klinicznego po dalszej preparatyce, np. po rozdziale jej na składniki krwi. Strona 22 z 134
23 E0011 KREW PEŁNA CPD/450ml/2-6C do prep./nie do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2 6 st.c, do dalszej preparatyki, ale nie do uŝytku klinicznego (np. do produkcji krwinek wzorcowych). E0012 KREW PEŁNA CPD/450ml/2-6C nie do prep./nie do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2 6 st.c, składnik przeznaczony do zniszczenia. E0013 KREW PEŁNA CPD/450ml/2-6C układ otwarty Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2 6 st.c, pobrana w sytuacji, w której integralność systemu została przerwana i istnieje ryzyko kontaminacji mikrobiologicznej. E0014 KREW PEŁNA CPD/450ml/2-6C układ otwarty składnik napromieniowany Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2 6 st.c, pobrana w sytuacji, której integralność systemu została przerwana i istnieje ryzyko kontaminacji mikrobiologicznej, poddana napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych leukocytów - wymagana dawka 25 Gy promieni gamma. E0017 KREW PEŁNA CPD/450ml/2-6C składnik napromieniowany Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2 6 st.c, poddana napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych leukocytów - wymagana dawka 25 Gy promieni gamma. E0020 KREW PEŁNA CPD/450ml/2-6C zmniejszono stęŝenie krio Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2 6 st.c o obniŝonej zawartości składników krzepnięcia krwi np. z powodu zbyt długiego czasu oczekiwania na preparatykę. E0021 KREW PEŁNA CPD/450ml/2-6C zmniejszono liczbę krw. płytk. Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2 6 st.c, o zmniejszonej zawartości krwinek płytkowych. E0022 KREW PEŁNA CPD/450ml/2-6C zmniejsz. l. krw. płyt./krio Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 63 ml CPD przechowywana w temp. 2 6 st.c, o obniŝonej zawartości krwinek płytkowych i czynników krzepnięcia krwi. E0048 KREW PEŁNA CPD/XX/2-6C Nieokreślona objętość krwi pełnej pobranej na 63 ml CPD, przechowywana w temp. 2-6 st.c (informacja o objętości krwi pełnej pobranej nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie). E0049 KREW PEŁNA CPD/XX/2-6C do prep./do klin. Nieokreślona objętość krwi pełnej pobranej na 63 ml CPD, przechowywana w temp. 2-6 st.c (informacja o objętości krwi pełnej pobranej nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie), przeznaczona do uŝytku klinicznego po dalszej preparatyce np. po rozdziale krwi na składniki. Strona 23 z 134
24 E0050 KREW PEŁNA CPD/XX/2-6C do prep./nie do klin. Nieokreślona objętość krwi pełnej pobranej na 63 ml CPD, przechowywana w temp. 2-6 st.c (informacja o objętości krwi pełnej pobranej nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie), przeznaczona do dalszej preparatyki, ale nie do uŝytku klinicznego (np. do produkcji krwinek wzorcowych). E0051 KREW PEŁNA CPD/XX/2-6C nie do prep./nie do klin. Nieokreślona objętość krwi pełnej pobranej na 63 ml CPD, przechowywana w temp. 2-6 st.c (informacja o objętości krwi pełnej pobranej nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie), składnik przeznaczony do zniszczenia. E0052 KREW PEŁNA CPD/XX/2-6C antykoagul. niedostos. do obj. Niska nieokreślona objętość krwi pełnej pobranej na 63 ml CPD, przechowywana w temp. 2-6 st.c (informacja o objętości krwi jest niezakodowana, ale moŝe się znaleźć w tekście na etykiecie), objętość antykoagulantu zbyt duŝa w stosunku do objętości pobranej krwi - nie do uŝytku klinicznego. E0053 KREW PEŁNA CPDA-1/450ml/2-6C Jednostka krwi pełnej o objętości 450 ml +/- 10 % pobrana na 70 ml CPDA-1, przechowywana w temp. 2-6 st.c. E0054 KREW PEŁNA CPDA-1/450ml/2-6C do prep./do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10 % pobrana na 70 ml CPDA-1, przechowywana w temp. 2-6 st.c, przeznaczona do uŝytku klinicznego po dalszej preparatyce, np. po rozdziale na składniki krwi. E0055 KREW PEŁNA CPDA-1/450ml/2-6C do prep./nie do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10 % pobrana na 70 ml CPDA-1, przechowywana w temp. 2-6 st.c, przeznaczona do uŝytku klinicznego po dalszej preparatyce, ale nie do uŝytku klinicznego (np.do produkcji krwinek wzorcowych E0056 KREW PEŁNA CPDA-1/450ml/2-6C nie do prep./nie do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10 % pobrana na 70 ml CPDA-1, przechowywana w temp. 2-6 st.c, składnik przeznaczony do zniszczenia. E0057 KREW PEŁNA CPDA-1/450ml/2-6C układ otwarty Jednostka krwi pełnej o objętości 450 ml +/- 10 % pobrana na 70 ml CPDA-1, przechowywana w temp. 2-6 st.c, pobrana w sytuacji, której integralność systemu została przerwana i istnieje ryzyko kontaminacji mikrobiologicznej. E0058 KREW PEŁNA CPDA-1/450ml/2-6C układ otwarty składnik napromieniowany Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 70 ml CPDA-1 przechowywana w temp. 2-6 st.c, pobrana w sytuacji, w której integralność systemu została przerwana i istnieje ryzyko kontaminacji mikrobiologicznej, poddana napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych leukocytów- wymagana dawka 25 Gy promieni gamma. E0061 KREW PEŁNA CPDA-1/450ml/2-6C składnik napromieniowany Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 70 ml CPDA-1 przechowywana w temp. 2-6 st.c, poddana napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych leukocytów - wymagana dawka 25 Gy promieni gamma. Strona 24 z 134
25 E0064 KREW PEŁNA CPDA-1/450ml/2-6C zmniejszono stęŝenie krio Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 70 ml CPDA-1 przechowywana w temp. 2-6 st.c, o obniŝonej zawartości składników krzepnięcia np. z powodu zbyt długiego czasu oczekiwania na preparatykę. E0065 KREW PEŁNA CPDA-1/450ml/2-6C zmniejszono liczbę krw. płytk. Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 70 ml CPDA-1 przechowywana w temp. 2-6 st.c, o obniŝonej zawartości krwinek płytkowych. E0066 KREW PEŁNA CPDA-1/450ml/2-6C zmniejsz. l. krw. płyt./krio Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 70 ml CPDA-1 przechowywana w temp. 2-6 st.c o obniŝonej zawartości krwinek płytkowych i czynników krzepnięcia krwi. E0067 KREW PEŁNA CPDA-1/450ml/2-6C antykoagul. niedostos. do obj. Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na 70 ml CPDA-1 przechowywana w temp. 2-6 st.c, mała objętość składnika w stosunku do oczekiwanej a antykoagulant nie został dostosowany w celu kompensacji. E0093 KREW PEŁNA CPDA-1/XX/2-6C Nieokreślona objętość krwi pełnej pobranej na CPDA-1 przechowywana w temp. 2-6 st.c (informacja o objętości pobranej krwi nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie krwi. E0094 KREW PEŁNA CPDA-1/XX/2-6C do prep./do klin. Nieokreślona objętość krwi pełnej pobranej na 70 ml CPDA-1 przechowywana w temp. 2-6 st.c (informacja o objętości pobranej krwi nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie krwi.), przeznaczona do uŝytku klinicznego po dalszej preparatyce np. po rozdziale krwi na składniki E0095 KREW PEŁNA CPDA-1/XX/2-6C do prep./nie do klin. Nieokreślona objętość krwi pełnej pobranej na CPDA-1 przechowywana w temp. 2-6 st.c (informacja o objętości pobranej krwi nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie krwi), przeznaczona do dalszej preparatyki nie do uŝytku klinicznego (np..do produkcji krwinek wzorcowych) E0096 KREW PEŁNA CPDA-1/XX/2-6C nie do prep./nie do klin. Nieokreślona objętość krwi pełnej pobranej na CPDA-1 przechowywana w temp. 2-6 st.c(informacja o objętości pobranej krwi nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie krwi), przeznaczona do zniszczenia E0097 KREW PEŁNA CPDA-1/XX/2-6C antykoagul. niedostos. do obj. Nieokreślona objętość krwi pełnej pobranej na CPDA-1 przechowywana w temp. 2-6 st.c(informacja o objętości pobranej krwi nie jest zakodowana, ale moŝe się znaleźć w tekście na etykiecie krwi), objętość antykoagulantu zbyt duŝa w stosunku do objętości pobranej krwi E0135 KREW PEŁNA Heparyna/450ml/2-6C Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na heparynę, przechowywana w temp. 2-6 st.c E0136 KREW PEŁNA Heparyna/450ml/2-6C nie do prep./nie do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10% pobrana na heparynę przechowywana w temp. 2-6 st.c, nie do dalszej preparatyki - nie do uŝytku klinicznego przeznaczona np.do badań naukowych Strona 25 z 134
26 E0139 KREW PEŁNA brak/450ml/2-6c do prep./do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10%, pozbawiona antykoagulantu przechowywana w temp. 2-6 st.c, przeznaczona do dalszej preparatyki i do uŝytku klinicznego E0140 KREW PEŁNA brak/450ml/2-6c do prep./nie do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10%, pozbawiona antykoagulantu, przechowywana w temp. 2-6 st.c, przeznaczona do dalszej preparatyki, ale nie do uŝytku klinicznego E0141 KREW PEŁNA brak/450ml/2-6c nie do prep./nie do klin. Jednostka krwi pełnej o objętości 450 ml +/- 10%, pozbawiona antykoagulantu przechowywana w temp. 2-6 st.c, przeznaczona do zniszczenia E0150 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c E0151 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C do prep./do klin. Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, przeznaczony do uŝytku klinicznego po dalszej preparatyce np.po całkowitym usunięciu osocza lub płynu resuspendującego. E0152 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C do prep./nie do klin. Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, przeznaczony do dalszej preparatyki, ale nie do uŝytku klinicznego np. do produkcji krwinek wzorcowych E0153 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C nie do prep./nie do klin. Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, składnik przeznaczony do zniszczenia E0154 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C układ otwarty Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej E0155 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C układ otwarty składnik napromieniowany Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej, poddany napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych limfocytów, wymagana dawka 25 Gy promieni gamma E0157 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C układ otwarty składnik napromieniowany zawieszono w osoczu Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej, do którego dodano osocze (obniŝenie Ht) oraz poddano napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych limfocytów, wymagana dawka 25 Gy promieni gamma Strona 26 z 134
27 E0159 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C układ otwarty zawieszono w albuminie Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej, do krwinek dodano roztwór albuminy E0160 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C układ otwarty zawieszono w osoczu Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej, do krwinek dodano osocze (obniŝony Ht) E0161 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C składnik napromieniowany Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, poddany napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych limfocytów, wymagana dawka 25 Gy promieni gamma E0163 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C składnik napromieniowany zawieszono w osoczu Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, do którego dodano osocze (obniŝony Ht) oraz poddano napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych limfocytów, wymagana dawka 25 Gy promieni gamma. E0165 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C zawieszono w albuminie Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, krwinki zawieszono w roztworze albuminy E0166 KONCENTRAT KRWINEK CZERWONYCH CPD/450ml/2-6C zawieszono w osoczu Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10% pobranej na 63 ml CPD, przechowywany w temp. 2-6 st.c, do krwinek dodano osocze (obniŝony Ht) E0191 KONCENTRAT KRWINEK CZERWONYCH CPD/XX/2-6C Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości pobranej krwi pełnej pobranej na CPD przechowywany w temp. 2-6 st.c (informacja o objętości krwinek czerwonych moŝe się znaleźć w tekście na etykiecie) E0192 KONCENTRAT KRWINEK CZERWONYCH CPD/XX/2-6C do prep./do klin. Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości krwi pełnej pobranej na CPD, przechowywany w temp. 2-6 st.c, przeznaczony do uŝytku klinicznego po dalszej preparatyce np. po całkowitym usunięciu osocza (informacja o objętości krwinek czerwonych moŝe się znaleźć w tekście na etykiecie) E0193 KONCENTRAT KRWINEK CZERWONYCH CPD/XX/2-6C do prep./nie do klin. Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości krwi pełnej pobranej na CPD, przechowywany w temp. 2-6 st.c, przeznaczony do dalszej preparatyki, ale nie do uŝytku klinicznego (informacja o objętości krwinek czerwonych moŝe się znaleźć w tekście na etykiecie) Strona 27 z 134
28 E0194 KONCENTRAT KRWINEK CZERWONYCH CPD/XX/2-6C nie do prep./nie do klin. Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości krwi pełnej pobranej na CPD, przechowywany w temp. 2-6 st.c, składnik przeznaczony do zniszczenia (informacja o objętości krwinek czerwonych moŝe się znaleźć w tekście na etykiecie) E0195 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C Koncentrat krwinek czerwonych otrzymany z jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c E0196 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C do prep./do klin. Koncentrat krwinek czerwonych otrzymany z jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, przeznaczony do uŝytku klinicznego po dalszej preparatyce, np. po przemyciu E0197 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C do prep./nie do klin. Koncentrat krwinek czerwonych otrzymany z jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywana w temp. 2-6 st.c, przeznaczony do dalszej preparatyki, ale nie do uŝytku klinicznego, (np.do produkcji krwinek wzorcowych) E0198 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C nie do prep./nie do klin. Koncentrat krwinek czerwonych otrzymany z jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, składnik krwi nie moŝe być wykorzystany ani do dalszej preparatyki ani do uŝytku klinicznego (do zniszczenia) E0199 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C układ otwarty Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej E0200 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C układ otwarty składnik napromieniowany Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej, poddany napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych limfocytów wymagana dawka, 25 Gy promieni gamma E0202 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C układ otwarty składnik napromieniowany zawieszono w osoczu Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej, do którego dodano osocze (obniŝony Ht) i poddano napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych limfocytów, wymagana dawka 25 Gy promieni gamma E0204 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C układ otwarty zawieszono w albuminie Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st, powstały w sytuacji, w której integralność systemu została naruszona i istnieje ryzyko kontaminacji mikrobiologicznej, do krwinek dodano roztwór albuminy Strona 28 z 134
29 E0206 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C składnik napromieniowany Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, poddany napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych limfocytów wymagana dawka 25 Gy promieni gamma E0208 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C składnik napromieniowany zawieszono w osoczu Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, do którego dodano osocze (obniŝony Ht) oraz poddano napromieniowaniu wystarczającemu, aby zapobiec proliferacji przetoczonych limfocytów wymagana dawka 25 Gy promieni gamma E0210 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C zawieszono w albuminie Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, krwinki zawieszono w roztworze albuminy E0211 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/450ml/2-6C zawieszono w osoczu Koncentrat krwinek czerwonych otrzymany z 1 jednostki krwi pełnej o objętości 450 ml +/- 10 % pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, do którego dodano osocze E0240 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/XX/2-6C Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości krwi pełnej pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c (informacja o objętości krwinek czerwonych moŝe się znaleźć w tekście na etykiecie) E0241 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/XX/2-6C do prep./do klin. Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości krwi pełnej pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c (informacja o objętości krwinek czerwonych moŝe się znaleźć w tekście na etykiecie), składnik do uŝytku klinicznego po dalszej preparatyce E0242 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/XX/2-6C do prep./nie do klin. Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości krwi pełnej pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c (informacja o objętości krwinek czerwonych moŝe się znaleźć w tekście na etykiecie), składnik przeznaczony do dalszej preparatyki, ale nie do uŝytku klinicznego E0243 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/XX/2-6C nie do prep./nie do klin. Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości krwi pełnej pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c (informacja o objętości krwinek czerwonych moŝe się znaleźć w tekście na etykiecie) składnik przeznaczony do zniszczenia E0244 KONCENTRAT KRWINEK CZERWONYCH CPDA-1/XX/2-6C antykoagul. niedostos. do obj. Koncentrat krwinek czerwonych otrzymany z nieokreślonej objętości krwi pełnej pobranej na 70 ml CPDA-1, przechowywany w temp. 2-6 st.c, mała objętość krwi pełnej, objętość antykoagulantu nieodpowiednia do objętości pobranej krwi E0291 KONCENTRAT KRWINEK CZERWONYCH CPD>AS1/450ml/2-6C Koncentrat krwinek czerwonych otrzymany z 450 ml +/- 10 % pobranej krwi pełnej pobranej na 63 ml CPD i zawieszony w płynie wzbogacającym ADSOL, przechowywany w tem.2-6 st.c Strona 29 z 134
Warszawa, dnia 27 marca 2017 r. Poz. 646 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 7 marca 2017 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 27 marca 2017 r. Poz. 646 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 7 marca 2017 r. w sprawie minimalnych wymagań dotyczących systemu zapewnienia
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 27 marca 2017 r. Poz. 646 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 7 marca 2017 r. w sprawie minimalnych wymagań dotyczących systemu zapewnienia
M I N I S T R A Z D R O W I A 1) z dnia 2016 r. w sprawie określenia wysokości opłat za krew i jej składniki w 2017 r.
 Projekt z dnia 20 maja 2016 r. R O Z P O R Z Ą D Z E N I E M I N I S T R A Z D R O W I A 1) z dnia 2016 r. w sprawie określenia wysokości opłat za krew i jej składniki w 2017 r. Na podstawie art. 19 ust.
Projekt z dnia 20 maja 2016 r. R O Z P O R Z Ą D Z E N I E M I N I S T R A Z D R O W I A 1) z dnia 2016 r. w sprawie określenia wysokości opłat za krew i jej składniki w 2017 r. Na podstawie art. 19 ust.
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2019 r. w sprawie określenia wysokości opłat za krew i jej składniki w 2020 r.
 Proje kt z dnia 23 maja 2019 r. ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2019 r. w sprawie określenia wysokości opłat za krew i jej składniki w 2020 r. Na podstawie art. 19 ust. 2 ustawy z dnia 22 sierpnia
Proje kt z dnia 23 maja 2019 r. ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2019 r. w sprawie określenia wysokości opłat za krew i jej składniki w 2020 r. Na podstawie art. 19 ust. 2 ustawy z dnia 22 sierpnia
Warszawa, dnia 7 czerwca 2017 r. Poz ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 6 czerwca 2017 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 7 czerwca 2017 r. Poz. 1104 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 6 czerwca 2017 r. w sprawie niepowtarzalnego oznakowania, sposobu oznaczania
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 7 czerwca 2017 r. Poz. 1104 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 6 czerwca 2017 r. w sprawie niepowtarzalnego oznakowania, sposobu oznaczania
Gospodarka krwią w szpitalu w wymiarze ekonomicznym
 Gospodarka krwią w szpitalu w wymiarze ekonomicznym Bogusław Grabowski Szpital Kliniczny Przemienienia Pańskiego UM w Poznaniu W procesie leczenia krwią można wyróżnić kilka obszarów 1. Medyczny - wskazania
Gospodarka krwią w szpitalu w wymiarze ekonomicznym Bogusław Grabowski Szpital Kliniczny Przemienienia Pańskiego UM w Poznaniu W procesie leczenia krwią można wyróżnić kilka obszarów 1. Medyczny - wskazania
Krew i jej składniki zasady otrzymywania.
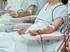 Krew i jej składniki zasady otrzymywania. Krew pełna jest to krew pobrana od zdrowych dawców do sterylnych pojemników z apirogennym płynem konserwującym. Jednostka krwi pełnej to 450 ml krwi pełnej ± 10%
Krew i jej składniki zasady otrzymywania. Krew pełna jest to krew pobrana od zdrowych dawców do sterylnych pojemników z apirogennym płynem konserwującym. Jednostka krwi pełnej to 450 ml krwi pełnej ± 10%
Honorowym krwiodawcą moŝe zostać kaŝda zdrowa osoba w wieku od 18-65 lat.
 WyŜsza Szkoła Kosmetologii i Ochrony Zdrowia w Białymstoku mając na uwadze działania prozdrowotne wśród społeczności akademickiej oraz ich aktywność na rzecz społeczności lokalnej przystąpiła do współpracy
WyŜsza Szkoła Kosmetologii i Ochrony Zdrowia w Białymstoku mając na uwadze działania prozdrowotne wśród społeczności akademickiej oraz ich aktywność na rzecz społeczności lokalnej przystąpiła do współpracy
Iga Niczyporuk II rok licencjat
 Iga Niczyporuk II rok licencjat jeden z płynów ustrojowych w organizmie człowieka, którego objętość wynosi ok. 5 5,5 litrów. Krew spełnia czynności transportowe, dostarcza do tkanek tlen i substancje odżywcze,
Iga Niczyporuk II rok licencjat jeden z płynów ustrojowych w organizmie człowieka, którego objętość wynosi ok. 5 5,5 litrów. Krew spełnia czynności transportowe, dostarcza do tkanek tlen i substancje odżywcze,
PROGRAM SZKOLENIA PIELĘGNIAREK I POŁOŻNYCH DOKONUJĄCYCH PRZETACZANIA KRWI I JEJ SKŁADNIKÓW
 PROGRAM SZKOLENIA PIELĘGNIAREK I POŁOŻNYCH DOKONUJĄCYCH PRZETACZANIA KRWI I JEJ SKŁADNIKÓW opracowany przez Instytut Hematologii i Transfuzjologii w dniu 27 kwietnia 2005r. 1.Szkolenie podstawowe SZKOLENIE
PROGRAM SZKOLENIA PIELĘGNIAREK I POŁOŻNYCH DOKONUJĄCYCH PRZETACZANIA KRWI I JEJ SKŁADNIKÓW opracowany przez Instytut Hematologii i Transfuzjologii w dniu 27 kwietnia 2005r. 1.Szkolenie podstawowe SZKOLENIE
S T A T U T REGIONALNEGO CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA. w Raciborzu. Rozdział I Nazwa, siedziba, obszar działania
 Załącznik do zarządzenia Ministra Zdrowia z dnia13 sierpnia.2004 r. (poz. 91) S T A T U T REGIONALNEGO CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA w Raciborzu Rozdział I Nazwa, siedziba, obszar działania 1.
Załącznik do zarządzenia Ministra Zdrowia z dnia13 sierpnia.2004 r. (poz. 91) S T A T U T REGIONALNEGO CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA w Raciborzu Rozdział I Nazwa, siedziba, obszar działania 1.
Rozporządzenie Ministra Zdrowia w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania krwi i jej składników 1)
 Rozporządzenie Ministra Zdrowia w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania krwi i jej ) z dnia 6 maja 207 r. (Dz.U. z 207 r. poz. 026) Na podstawie art. 2 ust. 7 ustawy z dnia
Rozporządzenie Ministra Zdrowia w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania krwi i jej ) z dnia 6 maja 207 r. (Dz.U. z 207 r. poz. 026) Na podstawie art. 2 ust. 7 ustawy z dnia
Warszawa, dnia 26 maja 2017 r. Poz ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 16 maja 2017 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 26 maja 207 r. Poz. 026 ROZPORZĄDZENIE MINISTRA ZDROWIA ) z dnia 6 maja 207 r. w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 26 maja 207 r. Poz. 026 ROZPORZĄDZENIE MINISTRA ZDROWIA ) z dnia 6 maja 207 r. w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania
ROZPORZĄDZENIE MINISTRA ZDROWIA 1
 Szkolenie pielęgniarek i położnych dokonujących przetaczania krwi i jej składników. Dz.U.07.06 z dnia 07.05.6 Status: Akt obowiązujący Wersja od: 6 maja 07 r. Wejście w życie: 7 czerwca 07 r. ROZPORZĄDZENIE
Szkolenie pielęgniarek i położnych dokonujących przetaczania krwi i jej składników. Dz.U.07.06 z dnia 07.05.6 Status: Akt obowiązujący Wersja od: 6 maja 07 r. Wejście w życie: 7 czerwca 07 r. ROZPORZĄDZENIE
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2016 r. w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania krwi lub jej składników
 Projekt z dnia 5 sierpnia 206 r. ROZPORZĄDZENIE MINISTRA ZDROWIA ) z dnia 206 r. w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania lub jej składników Na podstawie art. 2 ust. 7 ustawy
Projekt z dnia 5 sierpnia 206 r. ROZPORZĄDZENIE MINISTRA ZDROWIA ) z dnia 206 r. w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania lub jej składników Na podstawie art. 2 ust. 7 ustawy
Rozdział Preparatyka krwi i jej składników
 Rozdział Preparatyka krwi i jej składników I. OGÓLNE ZASADY PREPARATYKI KRWI 1. POJEMNIKI DO POBIERANIA I PREPARATYKI KRWI Do pobierania, preparatyki i przechowywania krwi i jej składników należy stosować
Rozdział Preparatyka krwi i jej składników I. OGÓLNE ZASADY PREPARATYKI KRWI 1. POJEMNIKI DO POBIERANIA I PREPARATYKI KRWI Do pobierania, preparatyki i przechowywania krwi i jej składników należy stosować
PDF created with pdffactory Pro trial version www.pdffactory.com
 Procedura nr 195.101 Wersja nr 5 Strona 2/6 1. CEL PROCEDURY Procedura ma za zadanie ujednolicenie sposobu pobierania, przysyłania i przyjmowania próbek krwi wymagających opracowania w Pracowni Serologicznej
Procedura nr 195.101 Wersja nr 5 Strona 2/6 1. CEL PROCEDURY Procedura ma za zadanie ujednolicenie sposobu pobierania, przysyłania i przyjmowania próbek krwi wymagających opracowania w Pracowni Serologicznej
1. Zużycie składników krwi w podmiocie leczniczym w 2016 roku
 ...... pieczątka podmiotu leczniczego.. miejscowość, data 1. Zużycie składników krwi w podmiocie leczniczym w 2016 roku Lp. Oddziały 1 2 3 4 5 6 7 8 9 10 11 12 Liczba łóżek do autotransfuzji w tym: FFP
...... pieczątka podmiotu leczniczego.. miejscowość, data 1. Zużycie składników krwi w podmiocie leczniczym w 2016 roku Lp. Oddziały 1 2 3 4 5 6 7 8 9 10 11 12 Liczba łóżek do autotransfuzji w tym: FFP
ROZPORZĄDZENIE MINISTRA ZDROWIA
 Szkolenie pielęgniarek i położnych dokonujących przetaczania krwi i jej. Dz.U.207.026 z dnia 207.05.26 Status: Akt obowiązujący Wersja od: 26 maja 207 r. Wejście w życie: 27 czerwca 207 r. ROZPORZĄDZENIE
Szkolenie pielęgniarek i położnych dokonujących przetaczania krwi i jej. Dz.U.207.026 z dnia 207.05.26 Status: Akt obowiązujący Wersja od: 26 maja 207 r. Wejście w życie: 27 czerwca 207 r. ROZPORZĄDZENIE
UMOWA NR NA UDZIELANIE ŚWIADCZEŃ ZDROWOTNYCH W ZAKRESIE BADAŃ IMMUNOLOGII TRANSFUZJOLOGICZNE, PREPARATYKI I WYDAWANIA SKŁADNIKÓW KRWI
 Załącznik Nr 2 do SWK UMOWA NR NA UDZIELANIE ŚWIADCZEŃ ZDROWOTNYCH W ZAKRESIE BADAŃ IMMUNOLOGII TRANSFUZJOLOGICZNE, PREPARATYKI I WYDAWANIA SKŁADNIKÓW KRWI zawarta dnia w Zielonej Górze pomiędzy Regionalnym
Załącznik Nr 2 do SWK UMOWA NR NA UDZIELANIE ŚWIADCZEŃ ZDROWOTNYCH W ZAKRESIE BADAŃ IMMUNOLOGII TRANSFUZJOLOGICZNE, PREPARATYKI I WYDAWANIA SKŁADNIKÓW KRWI zawarta dnia w Zielonej Górze pomiędzy Regionalnym
WSKAZANIA DO PRZETOCZENIA KRWI I JEJ SKŁADNIKÓW ORAZ PRODUKTÓW KRWIOPOCHODNYCH
 WSKAZANIA DO PRZETOCZENIA KRWI I JEJ SKŁADNIKÓW ORAZ PRODUKTÓW KRWIOPOCHODNYCH 1 KREW I JEJ SKŁADNIKI Koncentrat Krwinek czerwonych Składniki komórkowe Krew pełna Osocze Koncentrat Krwinek płytkowych Koncentrat
WSKAZANIA DO PRZETOCZENIA KRWI I JEJ SKŁADNIKÓW ORAZ PRODUKTÓW KRWIOPOCHODNYCH 1 KREW I JEJ SKŁADNIKI Koncentrat Krwinek czerwonych Składniki komórkowe Krew pełna Osocze Koncentrat Krwinek płytkowych Koncentrat
Norma ISO 9001/2008 w aspekcie akredytacji Ministerstwa
 SYMPOZJUM CCJ "DOSKONALENIE SYSTEMÓW ZARZĄDZANIA" Norma ISO 9001/2008 w aspekcie akredytacji Ministerstwa mgr Agnieszka Goller Zakład Transfuzjologii Klinicznej Wojskowego Instytutu Medycznego KOŚCIELISKO,
SYMPOZJUM CCJ "DOSKONALENIE SYSTEMÓW ZARZĄDZANIA" Norma ISO 9001/2008 w aspekcie akredytacji Ministerstwa mgr Agnieszka Goller Zakład Transfuzjologii Klinicznej Wojskowego Instytutu Medycznego KOŚCIELISKO,
DIAGNOSTYKA SEROLOGICZNA
 DIAGNOSTYKA SEROLOGICZNA PACJENTÓW W OKRESIE OKOŁOPRZESZCZEPOWYM Katarzyna Popko Zakład Diagnostyki Laboratoryjnej i Immunologii Klinicznej Wieku Rozwojowego WUM ZASADY DOBORU DAWCÓW KOMÓREK KRWIOTWÓRCZYCH
DIAGNOSTYKA SEROLOGICZNA PACJENTÓW W OKRESIE OKOŁOPRZESZCZEPOWYM Katarzyna Popko Zakład Diagnostyki Laboratoryjnej i Immunologii Klinicznej Wieku Rozwojowego WUM ZASADY DOBORU DAWCÓW KOMÓREK KRWIOTWÓRCZYCH
ZARZĄDZENIE MINISTRA ZDROWIA 1) z dnia 13 lutego 2004 r.
 Dz.Urz.MZ.04.2.16 2004.06.29 zm. Dz.Urz.MZ.04.5.57 1 2005.12.30 zm. Dz.Urz.MZ.05.18.98 1 2006.07.01 zm. Dz.Urz.MZ.06.10.52 1 ZARZĄDZENIE MINISTRA ZDROWIA 1) z dnia 13 lutego 2004 r. w sprawie nadania statutu
Dz.Urz.MZ.04.2.16 2004.06.29 zm. Dz.Urz.MZ.04.5.57 1 2005.12.30 zm. Dz.Urz.MZ.05.18.98 1 2006.07.01 zm. Dz.Urz.MZ.06.10.52 1 ZARZĄDZENIE MINISTRA ZDROWIA 1) z dnia 13 lutego 2004 r. w sprawie nadania statutu
Organizacja publicznej służby krwi w Rzeczpospolitej Polskiej i organizacja leczenia krwią i jej składnikami w podmiotach leczniczych
 Organizacja publicznej służby krwi w Rzeczpospolitej Polskiej i organizacja leczenia krwią i jej składnikami w podmiotach leczniczych Podstawa prawna działania jednostek organizacyjnych publicznej służby
Organizacja publicznej służby krwi w Rzeczpospolitej Polskiej i organizacja leczenia krwią i jej składnikami w podmiotach leczniczych Podstawa prawna działania jednostek organizacyjnych publicznej służby
Organizacja publicznej służby krwi w Rzeczpospolitej Polskiej
 Organizacja publicznej służby krwi w Rzeczpospolitej Polskiej Podstawa prawna działania jednostek organizacyjnych publicznej służby krwi w Rzeczpospolitej Polskiej - Ustawa z 22 sierpnia 1997 r. o publicznej
Organizacja publicznej służby krwi w Rzeczpospolitej Polskiej Podstawa prawna działania jednostek organizacyjnych publicznej służby krwi w Rzeczpospolitej Polskiej - Ustawa z 22 sierpnia 1997 r. o publicznej
Organizację leczenia krwią określa Rozporządzenie Ministra Zdrowia z dnia 11 grudnia 2012r. Dz. U. z dnia 04 stycznia 2013 r. Poz.
 Zadania Szpitalnego Banku Krwi Gospodarka krwią w podmiocie leczniczym 1 Organizację leczenia krwią określa Rozporządzenie Ministra Zdrowia z dnia 11 grudnia 2012r. Dz. U. z dnia 04 stycznia 2013 r. Poz.
Zadania Szpitalnego Banku Krwi Gospodarka krwią w podmiocie leczniczym 1 Organizację leczenia krwią określa Rozporządzenie Ministra Zdrowia z dnia 11 grudnia 2012r. Dz. U. z dnia 04 stycznia 2013 r. Poz.
WYTWARZANIE PRODUKTÓW LECZNICZYCH POCHODZĄCYCH Z KRWI LUB OSOCZA LUDZKIEGO
 Załącznik do rozporządzenia Ministra Zdrowia z dnia (poz. ) ANEKS 14 WYTWARZANIE PRODUKTÓW LECZNICZYCH POCHODZĄCYCH Z KRWI LUB OSOCZA LUDZKIEGO 1. Cel 1.1. Wymagania zawarte w Aneksie są stosowane do produktów
Załącznik do rozporządzenia Ministra Zdrowia z dnia (poz. ) ANEKS 14 WYTWARZANIE PRODUKTÓW LECZNICZYCH POCHODZĄCYCH Z KRWI LUB OSOCZA LUDZKIEGO 1. Cel 1.1. Wymagania zawarte w Aneksie są stosowane do produktów
Wojskowe Centrum Krwiodawstwa i Krwiolecznictwa SP ZOZ: Dostawa etykiet donacyjnych z kodem kreskowym OGŁOSZENIE O ZAMÓWIENIU - Dostawy
 1 z 11 2017-10-13, 10:58 Ogłoszenie nr 601870-N-2017 z dnia 2017-10-13 r. Wojskowe Centrum Krwiodawstwa i Krwiolecznictwa SP ZOZ: Dostawa etykiet donacyjnych z kodem kreskowym OGŁOSZENIE O ZAMÓWIENIU -
1 z 11 2017-10-13, 10:58 Ogłoszenie nr 601870-N-2017 z dnia 2017-10-13 r. Wojskowe Centrum Krwiodawstwa i Krwiolecznictwa SP ZOZ: Dostawa etykiet donacyjnych z kodem kreskowym OGŁOSZENIE O ZAMÓWIENIU -
LANGUAGE: NO_DOC_EXT: SOFTWARE VERSION: COUNTRY: PHONE: / NOTIFICATION TECHNICAL: / NOTIFICATION PUBLICATION: /
 LANGUAGE: PL CATEGORY: ORIG FORM: F02 VERSION: R2.0.9.S03 SENDER: ENOTICES CUSTOMER: wckik NO_DOC_EXT: 2019-058818 SOFTWARE VERSION: 9.10.4 ORGANISATION: ENOTICES COUNTRY: EU PHONE: / E-mail: zp@wckik.pl
LANGUAGE: PL CATEGORY: ORIG FORM: F02 VERSION: R2.0.9.S03 SENDER: ENOTICES CUSTOMER: wckik NO_DOC_EXT: 2019-058818 SOFTWARE VERSION: 9.10.4 ORGANISATION: ENOTICES COUNTRY: EU PHONE: / E-mail: zp@wckik.pl
Opis przedmiotu zamówienia (parametry wymagane podane poniżej)
 Załącznik do ogłoszenia o zamówieniu nr 1 Opis przedmiotu zamówienia (parametry wymagane podane poniżej) Dostawa, instalacja i uruchomienie separatorów komórkowych w ilości 2 szt. Lp. Nazwa parametru /
Załącznik do ogłoszenia o zamówieniu nr 1 Opis przedmiotu zamówienia (parametry wymagane podane poniżej) Dostawa, instalacja i uruchomienie separatorów komórkowych w ilości 2 szt. Lp. Nazwa parametru /
Warszawa, dnia 21 sierpnia 2013 r. Poz. 944
 Warszawa, dnia 21 sierpnia 2013 r. Poz. 944 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 10 lipca 2013 r. zmieniające rozporządzenie w sprawie wymagań Dobrej Praktyki Wytwarzania Na podstawie art. 39 ust.
Warszawa, dnia 21 sierpnia 2013 r. Poz. 944 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 10 lipca 2013 r. zmieniające rozporządzenie w sprawie wymagań Dobrej Praktyki Wytwarzania Na podstawie art. 39 ust.
Zobacz, czy moŝesz oddać krew?
 Zobacz, czy moŝesz oddać krew? Bezwzględne przeciwwskazania do oddania krwi cięŝkie choroby układu: krąŝenia, pokarmowego, nerwowego, oddechowego, moczowego, zakaŝenie chorobami zakaźnymi (np. HIV, Ŝółtaczka,
Zobacz, czy moŝesz oddać krew? Bezwzględne przeciwwskazania do oddania krwi cięŝkie choroby układu: krąŝenia, pokarmowego, nerwowego, oddechowego, moczowego, zakaŝenie chorobami zakaźnymi (np. HIV, Ŝółtaczka,
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2013 rok Obowiązuje od: 01 stycznia 2013 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2013 rok Obowiązuje od: 01 stycznia 2013 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
c) biorca oznacza osobę, u której wykonano przetoczenie krwi lub składników krwi;
 L 256/32 Dziennik Urzędowy Unii Europejskiej 1.10.2005 DYREKTYWA KOMISJI 2005/61/WE z dnia 30 września 2005 r. wykonująca dyrektywę 2002/98/WE Parlamentu Europejskiego i Rady w zakresie wymogów dotyczących
L 256/32 Dziennik Urzędowy Unii Europejskiej 1.10.2005 DYREKTYWA KOMISJI 2005/61/WE z dnia 30 września 2005 r. wykonująca dyrektywę 2002/98/WE Parlamentu Europejskiego i Rady w zakresie wymogów dotyczących
PROJEKT USTAWY O ZMIANIE USTAWY O PUBLICZNEJ SŁUŻBIE KRWI ODWRÓCONA TABELA ZGODNOŚCI
 Lp. Przepis projektu ustawy Uzasadnienie wprowadzenia przepisu 1 Art. 1 pkt 1 ustawy o zmianie ustawy o publicznej służbie krwi: art. 1 otrzymuje brzmienie: Art. 1. Ustawa określa: 1) organizację i zadania
Lp. Przepis projektu ustawy Uzasadnienie wprowadzenia przepisu 1 Art. 1 pkt 1 ustawy o zmianie ustawy o publicznej służbie krwi: art. 1 otrzymuje brzmienie: Art. 1. Ustawa określa: 1) organizację i zadania
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Opinia Prezesa Agencji Oceny Technologii Medycznych nr 61/2014 z dnia 22 kwietnia 2014 r. o projekcie programu Krzewienie idei krwiodawstwa na terenie miasta Legionowo
Agencja Oceny Technologii Medycznych Opinia Prezesa Agencji Oceny Technologii Medycznych nr 61/2014 z dnia 22 kwietnia 2014 r. o projekcie programu Krzewienie idei krwiodawstwa na terenie miasta Legionowo
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Opinia Prezesa Agencji Oceny Technologii Medycznych nr 177/2013 z dnia 8 lipca 2013 r. o projekcie programu Krzewienie idei krwiodawstwa na terenie Miasta Legionowo
Agencja Oceny Technologii Medycznych Opinia Prezesa Agencji Oceny Technologii Medycznych nr 177/2013 z dnia 8 lipca 2013 r. o projekcie programu Krzewienie idei krwiodawstwa na terenie Miasta Legionowo
DYREKTYWA KOMISJI 2004/33/WE. z dnia 22 marca 2004 r.
 1 DYREKTYWA KOMISJI 2004/33/WE z dnia 22 marca 2004 r. wykonująca Dyrektywę 2002/98/WE Parlamentu Europejskiego i Rady w zakresie niektórych wymagań technicznych dotyczących krwi i składników krwi (Tekst
1 DYREKTYWA KOMISJI 2004/33/WE z dnia 22 marca 2004 r. wykonująca Dyrektywę 2002/98/WE Parlamentu Europejskiego i Rady w zakresie niektórych wymagań technicznych dotyczących krwi i składników krwi (Tekst
Warszawa: Dostawa etykiet donacyjnych z kodem kreskowym Numer ogłoszenia: 2324-2016; data zamieszczenia: 05.01.2016 OGŁOSZENIE O ZAMÓWIENIU - dostawy
 1 z 5 2016-01-05 10:18 Adres strony internetowej, na której Zamawiający udostępnia Specyfikację Istotnych Warunków Zamówienia: www.wckik.pl Warszawa: Dostawa etykiet donacyjnych z kodem kreskowym Numer
1 z 5 2016-01-05 10:18 Adres strony internetowej, na której Zamawiający udostępnia Specyfikację Istotnych Warunków Zamówienia: www.wckik.pl Warszawa: Dostawa etykiet donacyjnych z kodem kreskowym Numer
1. Zużycie składników krwi w podmiocie leczniczym w 2018 roku
 ...... pieczątka podmiotu leczniczego.. miejscowość, data 1. Zużycie składników krwi w podmiocie leczniczym w 2018 roku 1 2 3 4 5 6 7 8 9 10 11 12 FFP w tym: w tym: KKP (opak.) KKP (opak.) Lp. Oddziały
...... pieczątka podmiotu leczniczego.. miejscowość, data 1. Zużycie składników krwi w podmiocie leczniczym w 2018 roku 1 2 3 4 5 6 7 8 9 10 11 12 FFP w tym: w tym: KKP (opak.) KKP (opak.) Lp. Oddziały
Rozdział 12 Przechowywanie i wydawanie krwi i jej składników oraz produktów krwiopochodnych dział ekspedycji
 Rozdział 12 Przechowywanie i wydawanie krwi i jej składników oraz produktów krwiopochodnych dział ekspedycji Dział ekspedycji wchodzi integralnie w struktury organizacyjne centrum. Jego umiejscowienie
Rozdział 12 Przechowywanie i wydawanie krwi i jej składników oraz produktów krwiopochodnych dział ekspedycji Dział ekspedycji wchodzi integralnie w struktury organizacyjne centrum. Jego umiejscowienie
Systemy liczenia. 333= 3*100+3*10+3*1
 Systemy liczenia. System dziesiętny jest systemem pozycyjnym, co oznacza, Ŝe wartość liczby zaleŝy od pozycji na której się ona znajduje np. w liczbie 333 kaŝda cyfra oznacza inną wartość bowiem: 333=
Systemy liczenia. System dziesiętny jest systemem pozycyjnym, co oznacza, Ŝe wartość liczby zaleŝy od pozycji na której się ona znajduje np. w liczbie 333 kaŝda cyfra oznacza inną wartość bowiem: 333=
PLAN ZARZĄDZANIA WYMAGANIAMI PROJEKT <NAZWA PROJEKTU> WERSJA <NUMER WERSJI DOKUMENTU>
 Załącznik nr 4.4 do Umowy nr 35-ILGW-253-.../20.. z dnia... MINISTERSTWO FINANSÓW DEPARTAMENT INFORMATYKI PLAN ZARZĄDZANIA WYMAGANIAMI PROJEKT WERSJA numer wersji
Załącznik nr 4.4 do Umowy nr 35-ILGW-253-.../20.. z dnia... MINISTERSTWO FINANSÓW DEPARTAMENT INFORMATYKI PLAN ZARZĄDZANIA WYMAGANIAMI PROJEKT WERSJA numer wersji
1. Zużycie składników krwi w podmiocie leczniczym w 2015 roku
 ...... pieczątka podmiotu leczniczego.. miejscowość, data 1. Zużycie składników krwi w podmiocie leczniczym w 2015 roku Lp. Oddziały Liczba łóżek do autotransfuzji w tym: po inaktywacji jednn. FFP w tym:
...... pieczątka podmiotu leczniczego.. miejscowość, data 1. Zużycie składników krwi w podmiocie leczniczym w 2015 roku Lp. Oddziały Liczba łóżek do autotransfuzji w tym: po inaktywacji jednn. FFP w tym:
Organizacja leczenia krwią i jej składnikami w podmiotach leczniczych
 Organizacja leczenia krwią i jej składnikami w podmiotach leczniczych Rozporządzenie Ministra Zdrowia z dnia 16 października 2017 r. w sprawie leczenia krwią i jej składnikami w podmiotach leczniczych
Organizacja leczenia krwią i jej składnikami w podmiotach leczniczych Rozporządzenie Ministra Zdrowia z dnia 16 października 2017 r. w sprawie leczenia krwią i jej składnikami w podmiotach leczniczych
Mazowiecki Szpital Specjalistyczny Sp. z o.o Radom, ul. Aleksandrowicza 5
 tel. centrala: 48 361 30 00 Dział Zamówień Publicznych tel. sekretariat: 48 361 39 00 tel. 48 361 49 69 fax: 48 345 11 18, 345 10 43 fax. 48 361 30 23 e-mail: dzp@wss.com.pl Znak: DZP.341.5.2018r. «Firma»
tel. centrala: 48 361 30 00 Dział Zamówień Publicznych tel. sekretariat: 48 361 39 00 tel. 48 361 49 69 fax: 48 345 11 18, 345 10 43 fax. 48 361 30 23 e-mail: dzp@wss.com.pl Znak: DZP.341.5.2018r. «Firma»
Klub Honorowych Dawców Krwi PCK
 O krwi Czym jest krew? Krew to płynna tkanka w skład której wchodzą: - Krwinki czerwone(erytrocyty) są to komórkowe składniki krwi nie zawierające jądra, zawierające barwnik krwi hemoglobinę, odpowiedzialne
O krwi Czym jest krew? Krew to płynna tkanka w skład której wchodzą: - Krwinki czerwone(erytrocyty) są to komórkowe składniki krwi nie zawierające jądra, zawierające barwnik krwi hemoglobinę, odpowiedzialne
KTO ODDAJE KREW - OKAZUJE SERCE
 Krew i jej składniki: Krew jest tkanką płynną, która krąży w naczyniach krwionośnych. Stanowi 8% całej masy ciała i jest zbudowana z części płynnej, czyli osocza oraz wyspecjalizowanych komórek czyli czerwonych
Krew i jej składniki: Krew jest tkanką płynną, która krąży w naczyniach krwionośnych. Stanowi 8% całej masy ciała i jest zbudowana z części płynnej, czyli osocza oraz wyspecjalizowanych komórek czyli czerwonych
Jeśli potrzebujesz dodatkowych informacji lub szukasz adresu Centrum Krwiodawstwa - znajdziesz je na stronie
 Jeśli potrzebujesz dodatkowych informacji lub szukasz adresu Centrum Krwiodawstwa - znajdziesz je na stronie www.twojakrew.pl Jeśli chcesz zostać Honorowym Krwiodawcą i w ten sposób ratować zdrowie i życie
Jeśli potrzebujesz dodatkowych informacji lub szukasz adresu Centrum Krwiodawstwa - znajdziesz je na stronie www.twojakrew.pl Jeśli chcesz zostać Honorowym Krwiodawcą i w ten sposób ratować zdrowie i życie
Obsługa serwisu kształcenie kwalifikacyjne w zawodzie - nowa formuła egzaminu zawodowego
 Obsługa serwisu kształcenie kwalifikacyjne w zawodzie - nowa formuła egzaminu zawodowego 1. Zgłaszanie szkół/placówek kwalifikacyjnych kursów zawodowych odbywa się za pośrednictwem formularza internetowego
Obsługa serwisu kształcenie kwalifikacyjne w zawodzie - nowa formuła egzaminu zawodowego 1. Zgłaszanie szkół/placówek kwalifikacyjnych kursów zawodowych odbywa się za pośrednictwem formularza internetowego
Informacja dot. kodów kreskowych służących do identyfikacji przesyłek pocztowych w obrocie krajowym(wyciąg z Zarządzenia nr 122/2010 z późn. zm.
 Informacja dot. kodów kreskowych służących przesyłek pocztowych w obrocie krajowym(wyciąg z Zarządzenia nr 122/2010 z późn. zm.) ZAWARTOŚĆ KODU KRESKOWEGO GS1-128 SŁUŻĄCEGO DO IDENTYFIKACJI PRZESYŁEK POCZTOWYCH
Informacja dot. kodów kreskowych służących przesyłek pocztowych w obrocie krajowym(wyciąg z Zarządzenia nr 122/2010 z późn. zm.) ZAWARTOŚĆ KODU KRESKOWEGO GS1-128 SŁUŻĄCEGO DO IDENTYFIKACJI PRZESYŁEK POCZTOWYCH
Etykieta logistyczna GS1
 Współpracując zaspokajamy potrzeby Klientów lepiej, szybciej, taniej i w zrównoważony sposób Etykieta logistyczna GS1 Dobre praktyki Dokument stworzony przez wspólną grupę roboczą członków ECR Polska,
Współpracując zaspokajamy potrzeby Klientów lepiej, szybciej, taniej i w zrównoważony sposób Etykieta logistyczna GS1 Dobre praktyki Dokument stworzony przez wspólną grupę roboczą członków ECR Polska,
DYREKTYWA 2002/98/WE PARLAMENTU EUROPEJSKIEGO I RADY. z dnia 27 stycznia 2003 r.
 DYREKTYWA 2002/98/WE PARLAMENTU EUROPEJSKIEGO I RADY z dnia 27 stycznia 2003 r. ustanawiająca normy jakości i bezpieczeństwa dla pobierania, badania, preparatyki, przechowywania i wydawania krwi ludzkiej
DYREKTYWA 2002/98/WE PARLAMENTU EUROPEJSKIEGO I RADY z dnia 27 stycznia 2003 r. ustanawiająca normy jakości i bezpieczeństwa dla pobierania, badania, preparatyki, przechowywania i wydawania krwi ludzkiej
WYCIECZKA DO LABORATORIUM
 WYCIECZKA DO LABORATORIUM W ramach projektu e-szkoła udaliśmy się do laboratorium w Krotoszynie na ul. Bolewskiego Mieliśmy okazję przeprowadzić wywiad z kierowniczką laboratorium Panią Hanną Czubak Oprowadzała
WYCIECZKA DO LABORATORIUM W ramach projektu e-szkoła udaliśmy się do laboratorium w Krotoszynie na ul. Bolewskiego Mieliśmy okazję przeprowadzić wywiad z kierowniczką laboratorium Panią Hanną Czubak Oprowadzała
1. Wprowadzanie danych w module POZ
 Dokumentacja programu e Zoz Opis uproszczonej metody ewidencjonowania sprawozdawczości ambulatoryjnej w POZ Wersja 1.2.0.1 Zielona Góra 2008-11-09 Aby uprościć procedurę gromadzenia i sprawozdawania danych
Dokumentacja programu e Zoz Opis uproszczonej metody ewidencjonowania sprawozdawczości ambulatoryjnej w POZ Wersja 1.2.0.1 Zielona Góra 2008-11-09 Aby uprościć procedurę gromadzenia i sprawozdawania danych
OŚWIADCZENIE WYKONAWCY
 ... Pieczęć Wykonawcy O F E R T A C E N O W A Załącznik nr 1 do SIWZ Pełna nazwa i adres Wykonawcy (w przypadku oferty składanej wspólnie naleŝy wymienić wszystkie podmioty wchodzące w skład, np. konsorcjum,
... Pieczęć Wykonawcy O F E R T A C E N O W A Załącznik nr 1 do SIWZ Pełna nazwa i adres Wykonawcy (w przypadku oferty składanej wspólnie naleŝy wymienić wszystkie podmioty wchodzące w skład, np. konsorcjum,
KONSMETAL Zamek elektroniczny NT C496-L250 (RAPTOR)
 KONSMETAL Zamek elektroniczny NT C496-L250 (RAPTOR) Instrukcja obsługi Podstawowe cechy zamka: 1 kod główny (Master) moŝliwość zdefiniowania do 8 kodów uŝytkowników długość kodu otwarcia: 6 cyfr długość
KONSMETAL Zamek elektroniczny NT C496-L250 (RAPTOR) Instrukcja obsługi Podstawowe cechy zamka: 1 kod główny (Master) moŝliwość zdefiniowania do 8 kodów uŝytkowników długość kodu otwarcia: 6 cyfr długość
Opis przedmiotu zamówienia
 Załącznik nr 1 do SIWZ PO ZMIANACH Opis przedmiotu zamówienia Przedmiotem zamówienia jest dostawa testów wirusologicznych HBsAg z testami potwierdzenia, testów anty-hcv, testów anty-hiv 1/2, testów do
Załącznik nr 1 do SIWZ PO ZMIANACH Opis przedmiotu zamówienia Przedmiotem zamówienia jest dostawa testów wirusologicznych HBsAg z testami potwierdzenia, testów anty-hcv, testów anty-hiv 1/2, testów do
ZARZĄDZENIE MINISTRA ZDROWIA
 Nadanie statutu Regionalnemu Centrum Krwiodawstwa i Krwiolecznictwa w Lublinie. Dz.Urz.MZ.2012.31 z dnia 2012.05.30 Status: Akt obowiązujący Wersja od: 23 lipca 2016 r. ZARZĄDZENIE MINISTRA ZDROWIA z dnia
Nadanie statutu Regionalnemu Centrum Krwiodawstwa i Krwiolecznictwa w Lublinie. Dz.Urz.MZ.2012.31 z dnia 2012.05.30 Status: Akt obowiązujący Wersja od: 23 lipca 2016 r. ZARZĄDZENIE MINISTRA ZDROWIA z dnia
ETYKIETA LOGISTYCZNA GS1
 ETYKIETA LOGISTYCZNA GS1 Dobre praktyki Dokument stworzony przez wspólną grupę roboczą członków ECR Polska i ekspertów GS1 Polska, by wspomóc i ułatwić jak najszersze wykorzystanie etykiety logistycznej
ETYKIETA LOGISTYCZNA GS1 Dobre praktyki Dokument stworzony przez wspólną grupę roboczą członków ECR Polska i ekspertów GS1 Polska, by wspomóc i ułatwić jak najszersze wykorzystanie etykiety logistycznej
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2016 rok Obowiązuje od: 01 stycznia 2016 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2016 rok Obowiązuje od: 01 stycznia 2016 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
Spis treści. spis treści wygenerowany automatycznie
 Spis treści Rozdział 2.Wymagania edytorskie 2 2.1. Wymagania ogólne 2 2.2. Tytuły rozdziałów i podrozdziałów 2 2.3. Rysunki, tabele i wzory 3 2.3.1. Rysunki 3 2.3.2. Tabele 4 2.3.3. Wzory 4 2.4. Odsyłacze
Spis treści Rozdział 2.Wymagania edytorskie 2 2.1. Wymagania ogólne 2 2.2. Tytuły rozdziałów i podrozdziałów 2 2.3. Rysunki, tabele i wzory 3 2.3.1. Rysunki 3 2.3.2. Tabele 4 2.3.3. Wzory 4 2.4. Odsyłacze
Do wszystkich zainteresowanych,
 INSTYTUT CENTRUM ZDROWIA MATKI POLKI SAMODZIELNA SEKCJA ZAMÓWIEŃ PUBLICZNYCH 93-338 Łódź, ul. Rzgowska 281/289 tel. (0-42) 271-17-52 fax (0-42) 271-17-50 E-mail:malgorzata.drozdowska@iczmp.edu.pl Łódź,
INSTYTUT CENTRUM ZDROWIA MATKI POLKI SAMODZIELNA SEKCJA ZAMÓWIEŃ PUBLICZNYCH 93-338 Łódź, ul. Rzgowska 281/289 tel. (0-42) 271-17-52 fax (0-42) 271-17-50 E-mail:malgorzata.drozdowska@iczmp.edu.pl Łódź,
Dz.U Nr 106 poz z dnia 22 sierpnia 1997 r. o publicznej służbie krwi. Rozdział 1. Przepisy ogólne
 Kancelaria Sejmu s. 1/48 Dz.U. 1997 Nr 106 poz. 681 U S T AWA z dnia 22 sierpnia 1997 r. Opracowano na podstawie: t.j. Dz. U. z 2014 r. poz. 332, z 2016 r. poz. 823. o publicznej służbie krwi Rozdział
Kancelaria Sejmu s. 1/48 Dz.U. 1997 Nr 106 poz. 681 U S T AWA z dnia 22 sierpnia 1997 r. Opracowano na podstawie: t.j. Dz. U. z 2014 r. poz. 332, z 2016 r. poz. 823. o publicznej służbie krwi Rozdział
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2015 rok Obowiązuje od: 01 stycznia 2015 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2015 rok Obowiązuje od: 01 stycznia 2015 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
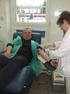 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2015 rok Obowiązuje od: 01 stycznia 2015 roku Aneks obowiązuje od 21 października 2015 roku SPIS
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2015 rok Obowiązuje od: 01 stycznia 2015 roku Aneks obowiązuje od 21 października 2015 roku SPIS
Załącznik nr 1A do SIWZ SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA
 I. PRZEDMIOT ZAMÓWIENIA: SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA Przedmiotem zamówienia jest dzierżawa w pełni zautomatyzowanego analizatora do badań z zakresu immunologii transfuzjologicznej metodą mikrokolumnową,
I. PRZEDMIOT ZAMÓWIENIA: SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA Przedmiotem zamówienia jest dzierżawa w pełni zautomatyzowanego analizatora do badań z zakresu immunologii transfuzjologicznej metodą mikrokolumnową,
NR SPRAWY 30/P/1-2/2013
 S P E C Y F I K A C J A ISTOTNYCH WARUNKÓW ZAMÓWIENIA Regionalne Centrum Krwiodawstwa i Krwiolecznictwa im. prof. dr hab. Tadeusza Dorobisza we Wrocławiu ul. Czerwonego KrzyŜa 5/9 zwane dalej Zamawiającym
S P E C Y F I K A C J A ISTOTNYCH WARUNKÓW ZAMÓWIENIA Regionalne Centrum Krwiodawstwa i Krwiolecznictwa im. prof. dr hab. Tadeusza Dorobisza we Wrocławiu ul. Czerwonego KrzyŜa 5/9 zwane dalej Zamawiającym
BEZPIECZEŃSTWO PRZETACZANIA KRWI I JEJ SKŁADNIKÓW
 BEZPIECZEŃSTWO PRZETACZANIA KRWI I JEJ SKŁADNIKÓW Krew i jej składniki należy stosować tylko w przypadkach koniecznych dla ratowania życia lub poprawy zdrowia. 40-70% powikłań i błędów związanych z transfuzją
BEZPIECZEŃSTWO PRZETACZANIA KRWI I JEJ SKŁADNIKÓW Krew i jej składniki należy stosować tylko w przypadkach koniecznych dla ratowania życia lub poprawy zdrowia. 40-70% powikłań i błędów związanych z transfuzją
Dotyczy zamówienia publicznego ogłoszonego w trybie przetargu nieograniczonego pod nazwą: Dostawa systemów do pozyskiwania osocza bogatopłytkowego
 Piekary Śląskie 28.12.2016 r. Samodzielny Publiczny Wojewódzki Szpital Chirurgii Urazowej im. Dr. Janusza Daaba w Piekarach Śląskich ul. Bytomska 62 41-940 Piekary Śląskie Sekcja d/s zamówień publicznych
Piekary Śląskie 28.12.2016 r. Samodzielny Publiczny Wojewódzki Szpital Chirurgii Urazowej im. Dr. Janusza Daaba w Piekarach Śląskich ul. Bytomska 62 41-940 Piekary Śląskie Sekcja d/s zamówień publicznych
do ustawy z dnia 13 kwietnia 2016 r. o zmianie ustawy o publicznej służbie krwi oraz niektórych innych ustaw (druk nr 149)
 BIURO LEGISLACYJNE/ Materiał porównawczy M A T E R I A Ł P O R Ó W N AW C Z Y do ustawy z dnia 13 kwietnia 2016 r. o zmianie ustawy o publicznej służbie krwi oraz niektórych innych ustaw (druk nr 149)
BIURO LEGISLACYJNE/ Materiał porównawczy M A T E R I A Ł P O R Ó W N AW C Z Y do ustawy z dnia 13 kwietnia 2016 r. o zmianie ustawy o publicznej służbie krwi oraz niektórych innych ustaw (druk nr 149)
INSTRUKCJA INWENTARYZACJI
 INSTRUKCJA INWENTARYZACJI Inwentaryzacją nazywamy czynności zmierzające do sporządzenia szczegółowego spisu z natury stanów magazynowych towaru na określony dzień. Inwentaryzacja polega na ustaleniu za
INSTRUKCJA INWENTARYZACJI Inwentaryzacją nazywamy czynności zmierzające do sporządzenia szczegółowego spisu z natury stanów magazynowych towaru na określony dzień. Inwentaryzacja polega na ustaleniu za
Możliwość sumowania. świadczenie dedykowane do sumowania dla określonej JGP. kat. 1a. kat. 1b
 Katalog świadczeń Możliwość sumowania Nazwa do 1 2 3 4 7 8 9 10 11 2 5.53.01.0000035 Implantacja portu naczyniowego 50 obejmuje koszt wyrobu medycznego (portu) 6 5.53.01.0000938 Plazmafereza lecznicza
Katalog świadczeń Możliwość sumowania Nazwa do 1 2 3 4 7 8 9 10 11 2 5.53.01.0000035 Implantacja portu naczyniowego 50 obejmuje koszt wyrobu medycznego (portu) 6 5.53.01.0000938 Plazmafereza lecznicza
DZIENNIK URZĘDOWY MINISTRA ZDROWIA
 DZIENNIK URZĘDOWY MINISTRA ZDROWIA Warszawa, dnia 30 maja 2012 r. Poz. 31 ZARZĄDZENIE MINISTRA ZDROWIA 1) z dnia 29 maja 2012 r. w sprawie nadania statutu Regionalnemu Centrum Krwiodawstwa i Krwiolecznictwa
DZIENNIK URZĘDOWY MINISTRA ZDROWIA Warszawa, dnia 30 maja 2012 r. Poz. 31 ZARZĄDZENIE MINISTRA ZDROWIA 1) z dnia 29 maja 2012 r. w sprawie nadania statutu Regionalnemu Centrum Krwiodawstwa i Krwiolecznictwa
U S T A W A. z dnia 2008 r. o zmianie ustawy o ewidencji ludności i dowodach osobistych oraz niektórych innych ustaw 1)
 PROJEKT U S T A W A z dnia 2008 r. o zmianie ustawy o ewidencji ludności i dowodach osobistych oraz niektórych innych ustaw 1) Art. 1. W ustawie z dnia 10 kwietnia 1974 r. o ewidencji ludności i dowodach
PROJEKT U S T A W A z dnia 2008 r. o zmianie ustawy o ewidencji ludności i dowodach osobistych oraz niektórych innych ustaw 1) Art. 1. W ustawie z dnia 10 kwietnia 1974 r. o ewidencji ludności i dowodach
REGULAMIN PORZĄDKOWY ( WYPIS )
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA im. dr Konrada Vietha W RADOMIU 26-612 Radom ul. B. Limanowskiego 42 REGULAMIN PORZĄDKOWY ( WYPIS ) DROGA DAWCY W RCKiK RADOM - SCHEMAT Gabinet Lekarski
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA im. dr Konrada Vietha W RADOMIU 26-612 Radom ul. B. Limanowskiego 42 REGULAMIN PORZĄDKOWY ( WYPIS ) DROGA DAWCY W RCKiK RADOM - SCHEMAT Gabinet Lekarski
Podstawowe informacje o obsłudze pliku z uprawnieniami licencja.txt
 Podstawowe informacje o obsłudze pliku z uprawnieniami licencja.txt W artykule znajdują się odpowiedzi na najczęściej zadawane pytania związane z plikiem licencja.txt : 1. Jak zapisać plik licencja.txt
Podstawowe informacje o obsłudze pliku z uprawnieniami licencja.txt W artykule znajdują się odpowiedzi na najczęściej zadawane pytania związane z plikiem licencja.txt : 1. Jak zapisać plik licencja.txt
BEZPIECZEŃSTWO PRZETACZANIA KRWI I JEJ SKŁADNIKÓW
 BEZPIECZEŃSTWO PRZETACZANIA KRWI I JEJ SKŁADNIKÓW Krew i jej składniki należy stosować tylko w przypadkach koniecznych dla ratowania życia lub poprawy zdrowia. 40-70% powikłań i błędów związanych z transfuzją
BEZPIECZEŃSTWO PRZETACZANIA KRWI I JEJ SKŁADNIKÓW Krew i jej składniki należy stosować tylko w przypadkach koniecznych dla ratowania życia lub poprawy zdrowia. 40-70% powikłań i błędów związanych z transfuzją
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2018 rok Obowiązuje od: 01 stycznia 2018 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2018 rok Obowiązuje od: 01 stycznia 2018 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
WZORU PRZEMYSŁOWEGO PL XL-TAPE-INTERNATIONAL SPÓŁKA Z OGRANICZONĄ ODPOWIEDZIALNOŚCIĄ, Kielce, (PL) WUP 12/2016
 PL 23003 RZECZPOSPOLITA POLSKA (12) OPIS OCHRONNY WZORU PRZEMYSŁOWEGO (19) PL (11) 23003 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 24749 (22) Data zgłoszenia: 26.07.2016 (51) Klasyfikacja:
PL 23003 RZECZPOSPOLITA POLSKA (12) OPIS OCHRONNY WZORU PRZEMYSŁOWEGO (19) PL (11) 23003 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 24749 (22) Data zgłoszenia: 26.07.2016 (51) Klasyfikacja:
Komunikat POTWIERDZENIE FAKTURY- KOREKTY. Wersja 1.0
 Komunikat POTWIERDZENIE FAKTURY- KOREKTY Wersja 1.0 EANCOM 97/EDIFACT D.96A przyjęty przez Grupę Roboczą EDI przy Klubie ECR Polska Dokument zawiera tylko te segmenty i elementy danych, które zostały uzgodnione
Komunikat POTWIERDZENIE FAKTURY- KOREKTY Wersja 1.0 EANCOM 97/EDIFACT D.96A przyjęty przez Grupę Roboczą EDI przy Klubie ECR Polska Dokument zawiera tylko te segmenty i elementy danych, które zostały uzgodnione
Opis przedmiotu zamówienia
 Załącznik nr 1 do SIWZ Opis przedmiotu zamówienia PO ZMIANACH Z DN. 30.08.2013 R. 1. Przedmiotem zamówienia jest dostawa systemu informatycznego obejmującego e-usługi w zakresie krwiolecznictwa świadczone
Załącznik nr 1 do SIWZ Opis przedmiotu zamówienia PO ZMIANACH Z DN. 30.08.2013 R. 1. Przedmiotem zamówienia jest dostawa systemu informatycznego obejmującego e-usługi w zakresie krwiolecznictwa świadczone
ROZPORZĄDZENIE MINISTRA ZDROWIA1)2)
 Dz.U.07.138.973 ROZPORZĄDZENIE MINISTRA ZDROWIA 1)2) z dnia 16 lipca 2007 r. w sprawie szczegółowych warunków pobierania, przechowywania i przeszczepiania komórek, tkanek i narządów Na podstawie art. 36
Dz.U.07.138.973 ROZPORZĄDZENIE MINISTRA ZDROWIA 1)2) z dnia 16 lipca 2007 r. w sprawie szczegółowych warunków pobierania, przechowywania i przeszczepiania komórek, tkanek i narządów Na podstawie art. 36
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 29 października 2018 r. Poz. 2060 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 26 października 2018 r. w sprawie szczegółowych warunków pobierania,
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 29 października 2018 r. Poz. 2060 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 26 października 2018 r. w sprawie szczegółowych warunków pobierania,
U S T AWA. z dnia.. o krwiodawstwie i krwiolecznictwie. Rozdział 1. Przepisy ogólne
 Projekt z dnia 13 sierpnia 2014 r. U S T AWA z dnia.. 1), 2) o krwiodawstwie i krwiolecznictwie Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa: 1) zasady: a) oddawania oraz pobierania krwi i jej
Projekt z dnia 13 sierpnia 2014 r. U S T AWA z dnia.. 1), 2) o krwiodawstwie i krwiolecznictwie Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa: 1) zasady: a) oddawania oraz pobierania krwi i jej
Jolanta Antoniewicz-Papis Instytut Hematologii i Transfuzjologii
 Jolanta Antoniewicz-Papis Instytut Hematologii i Transfuzjologii Napotykane ryzyko związane jest z: dawcami biorcami pracownikami jednostek służby krwi i jednostek służby zdrowia Program zarządzania ryzykiem
Jolanta Antoniewicz-Papis Instytut Hematologii i Transfuzjologii Napotykane ryzyko związane jest z: dawcami biorcami pracownikami jednostek służby krwi i jednostek służby zdrowia Program zarządzania ryzykiem
o krew dostarcza tkankom tlen (bierze udział w oddychaniu), w składniki energetyczne, mineralne, witaminy, hormony,
 Co to jest krew Krew płynna tkanka, składająca się z krwinek czerwonych, krwinek białych, płytek krwi i osocza (plazmy). Krew spełnia wiele ważnych funkcji w organizmie człowieka: krwinki czerwone - są
Co to jest krew Krew płynna tkanka, składająca się z krwinek czerwonych, krwinek białych, płytek krwi i osocza (plazmy). Krew spełnia wiele ważnych funkcji w organizmie człowieka: krwinki czerwone - są
pobieramy pierwszą literę komunikatu i wypełniamy nią (wszystkie pozycje tą samą literą) bufor słownikowy.
 komunikat do zakodowania: a a b a b b a b a c c a b a a a a a c a c b c b b c c a a c b a 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 przyjmujemy długość bufora słownikowego
komunikat do zakodowania: a a b a b b a b a c c a b a a a a a c a c b c b b c c a a c b a 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 przyjmujemy długość bufora słownikowego
Instrukcja korzystania z Krajowego Rejestru Agencji Zatrudnienia
 Instrukcja korzystania z Krajowego Rejestru Agencji Zatrudnienia Po uruchomieniu dowolnej przeglądarki internetowej, naleŝy wpisać w jej pasek wyszukiwania (1) adres www.wup.lodz.pl a następnie nacisnąć
Instrukcja korzystania z Krajowego Rejestru Agencji Zatrudnienia Po uruchomieniu dowolnej przeglądarki internetowej, naleŝy wpisać w jej pasek wyszukiwania (1) adres www.wup.lodz.pl a następnie nacisnąć
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG Od 01 maja 2018 roku Obowiązuje od: 01 maja 2018 roku Strona 1 / 6 SPIS TREŚCI I. Badania laboratoryjne
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG Od 01 maja 2018 roku Obowiązuje od: 01 maja 2018 roku Strona 1 / 6 SPIS TREŚCI I. Badania laboratoryjne
Program specjalizacji w TRANSFUZJOLOGII KLINICZNEJ
 CENTRUM MEDYCZNE KSZTAŁCENIA PODYPLOMOWEGO Program specjalizacji w TRANSFUZJOLOGII KLINICZNEJ Warszawa 2000 (c) Copyright by Centrum Medyczne Kształcenia Podyplomowego, Warszawa 2000 Program specjalizacji
CENTRUM MEDYCZNE KSZTAŁCENIA PODYPLOMOWEGO Program specjalizacji w TRANSFUZJOLOGII KLINICZNEJ Warszawa 2000 (c) Copyright by Centrum Medyczne Kształcenia Podyplomowego, Warszawa 2000 Program specjalizacji
FK - Deklaracje CIT-8
 FK - Deklaracje CIT-8 1. Wstęp. Moduł FK umoŝliwia przygotowanie i wydruk formularza deklaracji podatkowej CIT-8. W skład dostępnych formularzy wchodzą deklaracje CIT-8(21) oraz CIT- 8/O(8). Dane do formularza
FK - Deklaracje CIT-8 1. Wstęp. Moduł FK umoŝliwia przygotowanie i wydruk formularza deklaracji podatkowej CIT-8. W skład dostępnych formularzy wchodzą deklaracje CIT-8(21) oraz CIT- 8/O(8). Dane do formularza
NR SPRAWY 06/P/2013 S P E C Y F I K A C J A ISTOTNYCH WARUNKÓW ZAMÓWIENIA
 Regionalne Centrum Krwiodawstwa i Krwiolecznictwa we Wrocławiu ul. Czerwonego KrzyŜa 5/9 S P E C Y F I K A C J A ISTOTNYCH WARUNKÓW ZAMÓWIENIA zwane dalej Zamawiającym zaprasza do udziału w postępowaniu
Regionalne Centrum Krwiodawstwa i Krwiolecznictwa we Wrocławiu ul. Czerwonego KrzyŜa 5/9 S P E C Y F I K A C J A ISTOTNYCH WARUNKÓW ZAMÓWIENIA zwane dalej Zamawiającym zaprasza do udziału w postępowaniu
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 13 lipca 2017 r. Poz. 1371 OBWIESZCZENIE MARSZAŁKA SEJMU RZECZYPOSPOLITEJ POLSKIEJ z dnia 22 czerwca 2017 r. w sprawie ogłoszenia jednolitego tekstu
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 13 lipca 2017 r. Poz. 1371 OBWIESZCZENIE MARSZAŁKA SEJMU RZECZYPOSPOLITEJ POLSKIEJ z dnia 22 czerwca 2017 r. w sprawie ogłoszenia jednolitego tekstu
Projekt r. z dnia. r.
 ROZPORZĄDZENIE Projekt 9.08.2018 r. MINISTRA ZDROWIA 1) z dnia. r. zmieniające rozporządzenie w sprawie leczenia krwią i jej składnikami w podmiotach leczniczych wykonujących działalność leczniczą w rodzaju
ROZPORZĄDZENIE Projekt 9.08.2018 r. MINISTRA ZDROWIA 1) z dnia. r. zmieniające rozporządzenie w sprawie leczenia krwią i jej składnikami w podmiotach leczniczych wykonujących działalność leczniczą w rodzaju
2017/2018 WGGiOS AGH. LibreOffice Base
 1. Baza danych LibreOffice Base Jest to zbiór danych zapisanych zgodnie z określonymi regułami. W węższym znaczeniu obejmuje dane cyfrowe gromadzone zgodnie z zasadami przyjętymi dla danego programu komputerowego,
1. Baza danych LibreOffice Base Jest to zbiór danych zapisanych zgodnie z określonymi regułami. W węższym znaczeniu obejmuje dane cyfrowe gromadzone zgodnie z zasadami przyjętymi dla danego programu komputerowego,
Instrukcja zarządzania kontami i prawami
 Instrukcja zarządzania kontami i prawami uŝytkowników w systemie express V. 6 1 SPIS TREŚCI 1. Logowanie do systemu.... 3 2. Administracja kontami uŝytkowników.... 4 3. Dodawanie grup uŝytkowników....
Instrukcja zarządzania kontami i prawami uŝytkowników w systemie express V. 6 1 SPIS TREŚCI 1. Logowanie do systemu.... 3 2. Administracja kontami uŝytkowników.... 4 3. Dodawanie grup uŝytkowników....
USTAWA. z dnia 22 sierpnia 1997 r. o publicznej słuŝbie krwi. Rozdział 1. Przepisy ogólne
 (Dz. U. z dnia 11 września 1997 r.) USTAWA z dnia 22 sierpnia 1997 r. o publicznej słuŝbie krwi. Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa zasady pobierania, przechowywania i przetwarzania krwi
(Dz. U. z dnia 11 września 1997 r.) USTAWA z dnia 22 sierpnia 1997 r. o publicznej słuŝbie krwi. Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa zasady pobierania, przechowywania i przetwarzania krwi
Technologia informacyjna
 Technologia informacyjna Pracownia nr 9 (studia stacjonarne) - 05.12.2008 - Rok akademicki 2008/2009 2/16 Bazy danych - Plan zajęć Podstawowe pojęcia: baza danych, system zarządzania bazą danych tabela,
Technologia informacyjna Pracownia nr 9 (studia stacjonarne) - 05.12.2008 - Rok akademicki 2008/2009 2/16 Bazy danych - Plan zajęć Podstawowe pojęcia: baza danych, system zarządzania bazą danych tabela,
12. Wprowadzenie Sygnały techniki cyfrowej Systemy liczbowe. Matematyka: Elektronika:
 PRZYPOMNIJ SOBIE! Matematyka: Dodawanie i odejmowanie "pod kreską". Elektronika: Sygnały cyfrowe. Zasadę pracy tranzystorów bipolarnych i unipolarnych. 12. Wprowadzenie 12.1. Sygnały techniki cyfrowej
PRZYPOMNIJ SOBIE! Matematyka: Dodawanie i odejmowanie "pod kreską". Elektronika: Sygnały cyfrowe. Zasadę pracy tranzystorów bipolarnych i unipolarnych. 12. Wprowadzenie 12.1. Sygnały techniki cyfrowej
