Teoretyczne podstawy płynoterapii oparte na fizykochemicznej metodzie Stewarta
|
|
|
- Sylwia Mazurek
- 6 lat temu
- Przeglądów:
Transkrypt
1 PRACE POGLĄDOWE Anestezjologia Intensywna Terapia 201, tom 45, numer 2, ISSN Teoretyczne podstawy płynoterapii oparte na fizykochemicznej metodzie Stewarta Theorethical principles of fluid managment according to physicochemical Stewart approach Piotr Smuszkiewicz, Jakub Szrama Oddział Anestezjologii, Intensywnej Terapii i Leczenia Bólu Szpitala Klinicznego nr 2 w Poznaniu ABSTRACT Interpreting acid base disturbances according to the physicochemical Stewart approach allows the cause of such abnormalities to be discovered. This method is based on three independent variables: SID (strong ion difference), mainly sodium and chloride; weak acids concentration Atot, mainly albumins and phosphate; and carbon dioxide tension pco 2. These three independent variables are responsible for the change of water dissociation and for the change in H+ concentration and, consequently, the change in serum ph value. The SID value of the fluids administered to a patient is responsible for the change of serum SID value and therefore causes a change in the patient s acid base status. During the infusion of a given fluid, the SID value of the serum becomes closer to the SID value of that fluid; on the other hand, the infusion causes a decrease in Atot concentration. In order to avoid acid base disturbances connected with fluid administration, the SID value of fluids being administered should be greater than 0 and lower then the serum SID. It has been suggested that fluids should be given of which the SID value is as close as possible to the actual serum HCO concentration. Knowing the SID value of the fluid administered, and the serum HCO concentration, one can expect a change of serum ph after a fluid infusion. Administering a fluid with a SID greater than the HCO concentration causes a ph increase towards alkalosis. Likewise, administering a a fluid with a SID lower than the HCO concentration causes a ph decrease towards acidosis. It seems that knowledge of the electrolyte concentration and the SID value of an administered fluid is an important factor regarding acid base disturbances. Key words: fluid management, acid base status, Stewart approach Słowa kluczowe: płynoterapia, równowaga kwasowo-zasadowa, metoda Stewarta Anestezjologia Intensywna Terapia 201, tom XLV, nr 2, Wśród lekarzy, w tym także wśród pracujących na oddziałach intensywnej terapii (OIT), istnieje powszechne przekonanie, że wartość ph płynów infuzyjnych wpływa na ogólną równowagę kwasowo-zasadową (RKZ) ustroju. Niektórzy zalecają nawet, aby przetaczać płyny infuzyjne zbilansowane wartością ph, czyli płyny posiadające fizjologiczne lub zbliżone do fizjologicznego ph (ph-balanced fluids). Należy jednak podkreślić, że płyny infuzyjne o różnych wartościach ph wywierają ten sam wpływ na RKZ. Kanadyjski fizjolog, prof. Peter Stewart, opracował metodę fizykochemiczną, która w sposób odmienny od klasycznego podejścia Hendersona-Hasselbalcha (H-H) tłumaczy zmiany zachodzące w ustroju w odniesieniu do równowagi kwasowo-zasadowej. 10
2 Anestezjologia Intensywna Terapia 201; tom 45, nr 2, Omówienie zasad płynoterapii na podstawie metody Stewarta wymaga krótkiego przypomnienia podstawowych założeń tej metody. PODSTAWY METODY STEWARTA Według Stewarta [1], kluczową cząsteczką związaną z zaburzeniami równowagi kwasowo-zasadowej jest woda. Czystą wodę należy traktować jako najprostszy układ kwasowo-zasadowy. Woda jest niewyczerpalnym źródłem jonów wodorowych H + (właściwie jonów hydroniowych, H O + ), które powstają w procesie jej dysocjacji: 2H 2 O = H O + + OH Dla uproszczenia, w dalszej części artykułu, jony H O + będą przedstawiane jako H +. Istotnym elementem jest stała dysocjacji wody K w, która zależy między innymi od siły jonowej roztworu oraz temperatury i wynosi Eq L 1. H + OH = K w = Eq L 1 W warunkach fizjologicznych czysta woda jest w sensie kwasowo-zasadowym obojętna, tzn: H + = OH = 10 7 Eq L 1 Roztwór kwaśny zawiera więcej jonów H +, a zasadowy więcej jonów OH : roztwór kwaśny [H + ] > K w > [OH ], roztwór zasadowy [OH ] > K w > [H + ]. Istotę modelu Stewarta można wyjaśnić na podstawie uproszczonego schematu. Na rycinie 1 przedstawiono schematycznie roztwór chlorku sodowego (NaCl), związku obojętnego w sensie kwasowo-zasadowym, ponieważ liczba jonów H + i OH jest równa i wynosi 10 7 Eq L 1 (ryc. 1A). Gdy dodamy więcej jonów Na + (ryc. 1B) roztwór staje się zasadowy, gdyż zgodnie z prawem elektroobojętności musi pojawić się więcej jonów OH. Dodając kation Na +, zwiększamy pulę ładunków dodatnich, tak więc dla równowagi musi powstać więcej ładunków ujemnych anionów, w tym przypadku OH. Jednak, gdy Na + jest podawany z anionem, na przykład jako NaOH, wówczas w roztworze wodnym jony OH podawane razem z Na + reagują z H +, co zmniejsza stężenie H + i powoduje przewagę ilościową jonów OH. W warunkach klinicznych spotykamy taką sytuację, gdy podajemy choremu roztwór wodorowęglanów NaHCO, chcąc korygować kwasicę metaboliczną. Musimy mieć na uwadze, że alkalizacja osocza po podaniu NaHCO jest wywołana podażą jonów Na +, a nie HCO. Wodorowęglany są jonami towarzyszącymi. Jony HCO reagują z H + w efekcie powstaje Rycina 1. Wpływ dodania 1 meq Na + (B) oraz 1 meq Cl (C) na dysocjację wody H 2 O + CO 2. Powstały CO 2 powinien zostać szybko wydalony, w przeciwnym razie dojdzie do jego kumulacji i dyfuzji do komórek. Podobny efekt alkalizujący można uzyskać, podając octan sodu lub cytrynian sodu. NaHCO to jest de facto NaOH, tyle że nasycony CO 2. Gdy dodać więcej jonów Cl (ryc. 1C) roztwór staje się kwaśny, gdyż zgodnie z prawem elektroobojętności musi pojawić się więcej jonów H +. Podobny stan wywołuje się, podając na przykład HCl, a zachodzące zmiany są analogiczne do tych opisanych na ryc. 1B [2]. Stewart opisał trzy matematycznie niezależne zmienne, które regulują całą RKZ: 1) pco 2 podobnie jak w metodzie H-H, dwutlenek węgla jest odpowiedzialny za zaburzenia o etiologii oddechowej; 2) różnicę silnych jonów (SID, strong ion difference), za którą odpowiadają głównie jony Na i Cl, ale także K, Mg, Ca, mleczany; ) słabe kwasy Atot, głównie albuminy i fosforany, zarówno w formie zdysocjowanej A jak i niezdysocjowanej AH. Przez określenie silne jony określa się te, które są całkowicie zdysocjowane. Zmiany w zakresie osoczowego ph nie są wywoływane przez dodanie czy też usunięcie wolnych jonów H +, lecz powodowane zmianami w zakresie wyżej wymienionych trzech zmiennych niezależnych. Tylko modyfikacja w zakresie jednej lub kilku zmiennych niezależnych powoduje zmianę dysocjacji wody, a więc stężenia H + i w konsekwencji wartości ph [1]. 104
3 Piotr Smuszkiewicz, Jakub Szrama, Płynoterapia według Stewarta pośrednie pochodne cyklu Krebsa siarczany, jabłczany, octany, cytryniany, hipurany pojawiające się w uszkodzeniu nerek. Kwasicę wywołaną ich obecnością określamy jako SIG-acidosis [, 4]. Musimy pamiętać, że w roztworach wodnych, do których należą osocze i płyn pozakomórkowy, zawsze obecne są jony H + i OH, jednak ich stężenie jest tak niskie, że w diagramach są niewidoczne. Zgodnie z opisanymi powyżej zasadami regulacja RKZ odbywa się poprzez wzajemne oddziaływanie trzech zmiennych niezależnych (SID, Atot, pco 2 ) oraz ich wpływ na dysocjację wody. Zgodnie z zasadą elektroobojętności, według której suma kationów i anionów musi być zawsze równa: [Na + ] + [K + ] + [Mg 2 + ] + [Ca 2+ ] + [H + ] = = [Cl ] + [mleczany] + [HCO ] + [białko - ] + [PO 4 2 ] + [OH ] Podstawiając do równania następujące wzory: SID = [Na + ] + [K + ] + [Mg 2 + ] + [Ca 2+ ] [Cl ] [mleczany] Atot = [białko ] + [PO 4 2 ] równanie to po przekształceniu przyjmuje postać: Rycina 2. Zmienne niezależne według podejścia Stewarta SID + H + Atot HCO OH = 0. W osoczu (ryc. 2) silne kationy, głównie Na +, przeważają nad silnymi anionami, głównie Cl. Różnica między nimi nazywa się SID. Będąc przestrzenią obdarzoną ładunkiem elektrycznym, SID wyrażona jest w meq L -1, zaś wyliczona z różnicy stężeń silnych jonów nazywana jest rzeczywistą SID (SIDa, apparent SID). W warunkach fizjologicznych jej wartość wynosi około 40 meq L -1. Skoro SIDa jest dodatnia, musi być zrównoważona ładunkiem ujemnym. Ładunek ujemny, wypełniający tę przestrzeń, tworzą słabe kwasy Atot oraz aniony HCO. Tak wyliczoną SID, czyli pochodzącą z Atot i HCO nazywamy efektywną SID (SIDe, effective SID). W warunkach fizjologicznych SIDa = SIDe, jednak z zastrzeżeniem, że Atot i HCO są jedynymi dodatkowymi anionami oprócz Cl. Gdy SIDa SIDe, a konkretnie, gdy SIDa > SIDe, wskazuje to na obecność tak zwanych anionów niezidentyfikowanych XA. Wówczas wypełniają one przestrzeń kosztem SIDe i stan ten jest określony jako luka silnych jonów (SIG, strong ion gap) [, 4]. XA to aniony pochodzące z kwasów organicznych i nieorganicznych, powstające w przebiegu zaburzeń metabolicznych wtórnych do obserwowanych, chociażby w ciężkiej sepsie, zaburzeń hemodynamicznych i zmniejszenia perfuzji tkankowej na poziomie mikrokrążenia. Są to między innymi powstające we wstrząsie mleczany, w kwasicy ketonowej ciała ketonowe, takie jak acetooctan, betahydroksymaślan czy też Zaburzenia kwasowo-zasadowe według stewarta Z punktu widzenia elektrochemicznego SID wywiera znaczny wpływ na dysocjację wody (ryc. ): 1) zmniejszenie SID, czyli wzrost stężenia Cl (występujący najczęściej) lub spadek stężenia Na + (anion jest wówczas w większym stężeniu) powoduje wzrost dysocjacji wody; zgodnie z prawem elektroobojętności powstaje więcej H + w stosunku do OH i w efekcie rozwija się kwasica metaboliczna; Rycina. Wpływ zmian SID i Atot na RKZ; objaśnienia skrótów w tekście 105
4 Anestezjologia Intensywna Terapia 201; tom 45, nr 2, ) wzrost SID, na przykład w hipernatremii po podaży NaHCO lub hipochloremii u chorego obficie wymiotującego, z zaleganiem i utratą dużej objętości treści żołądkowej czy też leczonego diuretykami pętlowymi, powoduje pojawienie się większej liczby jonów OH i rozwój zasadowicy metabolicznej. Przeciwne efekty wywołują słabe kwasy Atot: 1) podwyższone stężenie Atot powoduje kwasicę; możemy zaobserwować to na przykład w uszkodzeniu nerek, kiedy to w 0% kwasica wywołana jest hiperfosfatemią; 2) odwrotny efekt wywołuje obniżenie stężenia Atot sytuację taką obserwujemy u chorych na OIT. Ponad 90% z nich ma hipoalbuminemię i zasadowicę metaboliczną. Często spotykane u tych chorych dodatnie wartości SBE (nadmiar zasad [SBE standard base excess]) wywołane są między innymi wspomnianym niedoborem albumin [5]. Dlaczego zmiany w zakresie SID osocza wywołują zmiany ph? Warto rozważyć to na przykładzie roztworu NaCl [6] SID w tym przypadku będzie równa różnicy stężeń Na + i Cl. Pozostałe jony w roztworze to H + i OH. Aby podkreślić istotność zagadnienia, na rycinie 4 zignorowano i usunięto Atot i HCO, a stężenia H + i OH zostały wyolbrzymione. W normalnych warunkach stężenia te są tak niskie, że ich nie widać. Według prawa elektroobojętności: Na + + H + = Cl + OH. W warunkach fizjologicznych wartość ph osocza = 7,4 a więc jest ono lekko zasadowe, co oznacza, że stężenie OH jest nieco wyższe niż H +. Po przekształceniu wzoru otrzymujemy go w postaci: H + = OH SID, a to oznacza, że gdy zmniejszy się SID (hiperchloremia, hiponatremia), różnica pomiędzy OH i SID wzrośnie i pojawi się więcej jonów H +, a co za tym idzie kwasica. Odwrotnie, gdy SID ulegnie zwiększeniu (hipochloremia, hipernatremia) powstałe jony OH będą w przewadze, co prowadzi do rozwoju zasadowicy. Wykluczając problematykę oddechową, w której zaburzenia są podobne jak w podejściu H-H (duża i mała pco 2 ) określają, odpowiednio, kwasicę i zasadowicę oddechową, wszystkie metaboliczne zaburzenia równowagi kwasowo- -zasadowej (ZRKZ) można sklasyfikować następująco [7]: 1) kwasice: a) SIG acidosis : kwasica wywołana anionami nieokreślonymi kwasica ketonowa, mleczanowa; w uszkodzeniu nerek, cukrzycy, we wstrząsie, w zatruciach; b) kwasica z niskim SID na przykład hiperchloremiczna; po przetoczeniach płynów; c) kwasica z podwyższonym poziomem Atot; z hiperfosfatemii w uszkodzeniu nerek. 2) zasadowice: a) zasadowica z wysokim SID: rr hipochloremiczna, na przykład utrata treści żołądkowej, leczenie diuretykami pętlowymi, rr hipernatremiczna, na przykład nadmierna podaż Na w żywieniu, infuzja NaHCO ; b) zasadowica z niskimi wartościami Atot, na przykład hipoalbuminemia. Należy zawsze pamiętać, że chory może mieć równocześnie kilka rodzajów metabolicznych ZRKZ, na przykład kwasice: mleczanową i hiperchloremiczną bądź równocześnie kwasicę i zasadowicę, co jest trudne do zdiagnozowania za pomocą tradycyjnej metody H-H. Analizując wynik gazometrii krwi tętniczej, nie stwierdzi się przyczyny obserwowanych zaburzeń; nie wiadomo, co kryje się za wartością SBE, gdy przykładowo jest ona + 6, przy równoczesnym stężeniu mleczanów 7 mmol L -1. Rycina 4. Zależność pomiędzy SID a stężeniem jonów H + Płynoterapia oparta na modelu Stewarta Duże objętości przetoczonych płynów mogą indukować kwasicę metaboliczną. Podanie choremu płynu w postaci wody, roztworu glukozy, mannitolu, 0,9% roztworu chlorku sodu czy też hipotonicznego roztworu chlorku sodu wywołuje kwasicę metaboliczną, ponieważ są to płyny, w których SID = 0, czyli liczba silnych jonów jest równa (roztwór NaCl) lub ich brak (woda, glukoza). Po infuzji tych płynów SID osocza ulega zmniejszeniu. Podając na przykład 0,9% roztwór NaCl, który zawiera równą liczbę jonów Na + i Cl, po 154 meq L 1, uzyskuje się w osoczu relatywnie wyższe stężenie Cl - niż Na +. Ustala się nowa niższa, wartość SID osocza. Zmienia to stopień dysocjacji wody i powoduje rozwój kwasicy metabolicznej. Ale według jakich reguł dokonują się zmiany ph osocza po przetoczeniu płynów? 106
5 Piotr Smuszkiewicz, Jakub Szrama, Płynoterapia według Stewarta Aby odpowiedzieć na to pytanie, należy wspomnieć o wcześniejszych koncepcjach tłumaczących występowanie kwasicy indukowanej przetoczeniami płynów [1]: 1) ph płynów nierzadko uważa się, że ZRKZ po przetoczeniach płynów wywołane są nadmierną aktywnością protonów, czyli jonów H + w podawanym płynie. Jednak jest to niezgodne z regułami opisywanymi w metodzie Stewarta. Jony H + bowiem w wolnym stanie nie mogą być ani dodane, ani usunięte z roztworu wodnego. Jony H + pojawiają się wówczas, gdy warunki ku temu są odpowiednie, czyli gdy nasileniu ulega dysocjacja wody, spowodowana opisanymi wcześniej zmiennymi niezależnymi (pco 2, SID, Atot). Innymi słowy, ph płynów infuzyjnych nie ma większego wpływu na zmiany ph osocza, a tym samym nie ma znaczenia w odniesieniu do wywoływania ZRKZ. 2) rozcieńczenie jonów HCO : często jako przyczynę rozwoju kwasicy po przetoczeniach płynów wskazuje się rozcieńczenie wodorowęglanów. Prawo elektroobojętności nakazuje, że HCO razem z Atot (albuminy, fosforany) wypełnia ujemnie naładowaną przestrzeń utworzoną przez silne jony (ryc. 2). Wyrażenie charakteryzujące elektryczną obojętność dla płynów ustrojowych przedstawia już wcześniej przytaczany wzór: SID + H + Atot HCO OH = 0 Po wyeliminowaniu ilościowo nieistotnych H +, OH możemy wzór uprościć do: SID Atot = HCO. Jakie jest znaczenie powyższego wyrażenia? Jeśli SID się zmniejszy, gdyż wzrośnie stężenie Cl (po przetoczeniu 0,9% NaCl) lub/i wzrośnie Atot (np. wskutek zwiększonego stężenia fosforanów w uszkodzeniu nerek), wówczas różnica między SID i Atot się zmniejszy, co spowoduje spadek stężenia HCO. Przeciwnie, jeśli SID się zwiększy, na przykład w hipernatremii po leczeniu NaHCO lub hipochloremii w przebiegu wymiotów i/lub spadnie stężenie Atot (w hipoalbuminemii), HCO pojawi się w większym stężeniu. Innymi słowy, stężenie HCO zmienia się zależnie od pierwotnych zmian w zakresie zmiennych niezależnych, czyli SID i Atot. Tak więc koncepcja wskazująca na obniżenie stężenia (rozcieńczenie) HCO w osoczu jako przyczynę kwasicy poprzetoczeniowej jest błędna; HCO stanowi zmienną zależną od SID i Atot. Wpływ podaży płynów na równowagę kwasowo-zasadową Każdy płyn infuzyjny ma swój własny skład elektrolitowy i przez to własną wartość SID. Przed przetoczeniem płynu powinno się znać jego wartość SID oraz Atot. W krystaloidach Atot jest równe zero, ale nie dotyczy to niektórych preparatów koloidowych. Podając choremu płyny, wywołuje się zjawisko mieszania się dwóch różnych płynów: płynu przetaczanego oraz osocza (płynu pozakomórkowego) o różnych wartościach SID i Atot. Podając płyn powoduje się z jednej strony kwasicę, gdyż rozcieńczone zostają silne jony i zmniejszony SID osocza, z drugiej strony zasadowicę poprzez rozcieńczenie Atot i obniżenie stężenia albumin. W trakcie przetaczania osoczowy SID ewoluuje w kierunku wartości SID przetaczanego płynu, a końcowy rezultat SID osocza jest wypadkową tego procesu (ryc. 5). Co należałoby zrobić, aby uniknąć wywołanych płynoterapią ZRKZ? Warto rozważyć hipotetyczną sytuację, niemożliwą w rzeczywistości, gdy stosuje się nieograniczoną (nieskończoną) infuzję płynu z wartością SID = 0 (np. 0,9% NaCl) [1, 6]. Przez nieograniczoną infuzję rozumiane jest całkowite zastąpienie płynu pozakomórkowego roztworem 0,9% NaCl. Dla przypomnienia, fizjologiczny SID płynu pozakomórkowego wynosi około 40 meq L -1, a wartość A (zdysocjowana forma Atot) to około 16 meq L -1 przy założeniu, że stężenie albumin waha się w granicach 42 g L -1 [8]. Gdy całkowicie zastąpi się (wyeliminuje) SID osocza, zostaje wywołana olbrzymia kwasica metaboliczna z SBE 40 meq L -1 (można użyć sformułowania: nadmiar/niedobór SID [SIDex, SID excess] 40). Równocześnie, rozcieńczając i eliminując A (albuminy), można wywołać zasadowicę metaboliczną z SBE +16 meq L -1 (SIDex +16). Kombinacja tych dwóch zjawisk pozostawia nadal kwasicę, lecz o mniejszym natężeniu, z SBE (SIDex) 24 meq L -1. Aby przywrócić prawidłowy stan RKZ i uzyskać neutralność elektryczną (SBE = 0), powinno się podnieść Rycina 5. Wpływ przetaczanych płynów na RKZ 107
6 Anestezjologia Intensywna Terapia 201; tom 45, nr 2, Rycina 6. W infuzji nieskończonej, Atot znika i całą przestrzeń wypełniają HCO wartość SBE (SID) o 24 meq L -1. Tak więc, opierając się na prawie elektroobojętności, gdy w trakcie nieograniczonej infuzji wyeliminuje się A, wówczas całą przestrzeń wypełniają HCO (ryc. 6). Chcąc uniknąć ZRKZ po przetoczeniu płynów, wartość ich SID powinna wynosić około 24 meq L -1, a więc powinna być równa fizjologicznemu stężeniu HCO we krwi chorego. Roztwory, które posiadają taką wartość SID, określa się mianem zbilansowanych (balanced solutions). W codziennych warunkach, przetaczając chorym płyny, wywołuje się infuzję ograniczoną, w której A są wciąż obecne, ale w trakcie podawania płynu ich stężenie we krwi zmniejsza się. Aby zapobiec rozwojowi ZRKZ, w trakcie infuzji powinno się osiągnąć równowagę pomiędzy redukcją SID i spadkiem A osocza. W licznych badaniach potwierdzono, że gdy stosuje się płyny z SID = 24 meq L -1, wartości SBE utrzymywane są na prawidłowym poziomie. Podając płyny z SID < 24 meq L -1, a więc z niższym niż stężenie HCO w osoczu, wywołuje się kwasicę metaboliczną, podczas gdy przetaczając płyny z SID > 24, wyższym niż stężenie HCO w osoczu powoduje powstanie zasadowicy metabolicznej. Powyższe zasady wykorzystuje się do tworzenia składu płynów infuzyjnych [911]. Pojawia się jednak kolejny problem: jak należy utworzyć SID płynu tak, aby wynosił 24 meq L -1? Najprościej byłoby zastąpić 24 meq anionów Cl z roztworu 0,9% NaCl innymi anionami. W tabeli 1 przedstawiono roztwory, które są zbilansowane mają wartość SID = 24 meq L -1. Aniony Cl zostały zastąpione odpowiednio anionami OH (roztwór 1) i HCO (roztwór ). Jednak jeśli roztwory te będą znajdowały się w plastikowych butelkach, co należy do codzienności, staną się roztworem nr 2 z powodu permanentnego wyrównywania się stężeń z atmosferycznym CO 2. Warto zwrócić uwagę na wartości ph. Roztwór nr 1 ma bardzo wysokie ph > 12, które jest nie do zaakceptowania, gdy zamierzeniem jest podanie płynu w większej objętości i z dużym przepływem. Natomiast gdy roztwór nr staje się roztworem nr 2, jego ph wzrasta do wartości > 9. Jak wspominano, wartości ph roztworów nie mają wpływu na RKZ, ale mogą być niebezpieczne dla śródbłonka naczyniowego i powodować martwicę tkanek. Przetoczenie każdego z wyżej wymienionych trzech roztworów, pomimo różnych wartości ph, wywoła ten sam efekt w aspekcie równowagi kwasowo-zasadowej, ponieważ wszystkie mają tę samą wartość SID, czyli jednej ze zmiennych niezależnych [5]. Aby wyeliminować szkodliwy wpływ na naczynia krwionośne oraz kwestię równoważenia z atmosferycznym CO 2 i utratę CO 2, jony Cl zastępuje się anionami organicznymi, takimi jak mleczany, jabłczany, glukoniany, cytryniany i in. (ryc. 6). Roztwór 4 (tab. 1) jest przykładem takiego podejścia, gdzie aniony Cl -1 zostały zastąpione mleczanami; SID tego roztworu w warunkach in vitro nadal wynosi 0; wartość SID = 24 (tzw. efektywny SID) pojawi się wówczas, gdy po przetoczeniu płynu mleczan zostanie szybko zmetabolizowany. W warunkach fizjologicznych mleczan jest metabolizowany w ilości 100 mmol h -1, co równoważy się przetoczeniem analizowanego płynu w ilości około 4000 ml h -1. W przypadku, gdy chory ma niewydolność wątroby i mleczan nie ulegnie eliminacji, płyn nadal będzie miał Tabela 1. Roztwory zbilansowane [wg 5] Roztwory nr 1 nr 2 nr nr 4 Na Cl HCO 19,2 24 CO 4,8 OH 24 Mleczan 26 pco 2 0 0, 760 0, ph 12,4 9,5 6,04 6,49 SID
7 Piotr Smuszkiewicz, Jakub Szrama, Płynoterapia według Stewarta wartość SID zbliżoną do zera i jego infuzja będzie prowadziła do rozwoju kwasicy mleczanowej [12]. Na podstawie wyjściowego, sprzed infuzji, stężenia HCO w osoczu chorego oraz wartość SID płynu (krystaloidu, koloidu), można przewidzieć, w jakim kierunku będzie się zmieniać wartość ph krwi w trakcie przetaczania płynów: w kierunku bardziej nasilonej kwasicy, gdy SID przetaczanego płynu będzie mniejsze niż osoczowe stężenie HCO ; w kierunku zasadowym, gdy SID płynu będzie większe niż stężenie HCO w osoczu. Ten sam płyn infuzyjny, z określoną wartością SID, na przykład SID = 24, będzie działać alkalizująco u chorego z kwasicą i niskim stężeniem HCO, rzędu 20 meq L -1 lub zakwaszająco, gdy pierwotnie istnieje zasadowica z wyższą wartością HCO około 0 meq L -1 [1]. W codziennych warunkach klinicznych chorym podaje się różne preparaty krystaloidów i koloidów z różnymi wartościami SID. Zwykle wartość SID nie jest podawana przez producenta. Aby mieć świadomość konsekwencji w zakresie RKZ, powinno się znać stężenia silnych jonów w płynach infuzyjnych, chociażby w odniesieniu do Na, K, Cl oraz anionów organicznych, i wyliczyć wartość SID podawanych płynów. Przed infuzją płynów istotny jest stan RKZ chorego. Jeżeli jest prawidłowy, powinno się stosować płyny z wartościami SID oscylującymi wokół 24 meq L -1, a przynajmniej większymi od 0 i mniejszymi niż SID osocza. Jeśli u pacjenta stwierdza się kwasicę metaboliczną, wówczas zastosowanie płynu z SID wyższym od stężenia HCO osocza wywiera efekt terapeutyczny, zmieniając RKZ w kierunku zasadowym. Odwrotną zależność można zaobserwować w przypadku zasadowicy. W niektórych sytuacjach, na przykład w kwasicy ketonowej (SIG acidosis), podaż płynu z SID = 0 (0,9% NaCl) nasila kwasicę poprzez dodanie komponentu hiperchloremicznego, natomiast podanie płynu z wysokim SID, wyższym od HCO osocza, może prowadzić do zbyt szybkiego wyrównania kwasicy z rozwojem wtórnej zasadowicy z przełamania, szczególnie w czasie leczenia przyczynowego insuliną [10]. Tak jak w przypadku krystaloidów, również wartość SID koloidów jest cechą fundamentalną dla stosowania racjonalnej płynoterapii. Przed infuzją trzeba posiadać wiedzę, które z nich są zbilansowane. Ponadto, płynoterapia przy użyciu koloidów wiąże się z podwyższeniem ciśnienia onkotycznego osocza, co sprzyja redystrybucji wody do przedziału śródnaczyniowego. Konsekwencją jest obniżenie SID osocza i możliwie nieznaczny wpływ zakwaszający. Poza tym, niektóre preparaty koloidów posiadają własną aktywność słabych kwasów (Atot). Dotyczy to głównie albumin oraz roztworów żelatyny, ale nie HES czy dekstranu [8]. Wobec tego, przetaczając większe ilości albumin czy żelatyny, można spodziewać się rozwoju kwasicy spowodowanej wzrostem Atot (ryc. ) [14]. Wobec powyższych twierdzeń niezmiernie istotna wydaje się być wiedza na temat składu elektrolitowego oraz wartości SID płynów infuzyjnych stosowanych w codziennej praktyce. W tabeli 2 przedstawiono parametry najczęściej stosowanych płynów infuzyjnych. WNIOSKI: 1. Istotą modelu Stewarta jest zrozumienie, że tylko zmienne niezależne pco 2, SID i Atot, są ważne w określaniu stężenia H + i wartości ph. 2. Obserwuje się liniową zależność pomiędzy wartością SID płynów infuzyjnych a kierunkiem i wielkością zmian osoczowego SID. Tabela 2. Skład najczęściej stosowanych płynów infuzyjnych Ringer Mleczan Ringera Sterofundin Braun Sterofundin Płyn wieloelektrolitowy Tetraspan 0,9 % NaCl Na 147, K Cl 155, Ca 2,2 1,5 2,5 2,5 2 2,5 Mg ph 57,5 67,5 4,65,4 4,57,5 5,66,4 Mleczan Octan Jabłczan 5 5 Cytrynian SID uj?
8 Anestezjologia Intensywna Terapia 201; tom 45, nr 2, W czasie podaży płynów infuzyjnych redukcji ulega SID osocza, która równoważy spadek stężenia Atot. 4. Aby uniknąć ZRKZ, wartość SID płynu infuzyjnego powinna być > 0 i mniejsza od SID osocza, a najbardziej optymalnie, gdy jest równa wyjściowemu stężeniu anionów HCO osocza. 5. Rezultaty badań podtrzymują hipotezę, że na podstawie znajomości wartości SID płynu infuzyjnego i stężenia HCO można przewidzieć zmiany ph osocza po jego przetoczeniu: SID płynu > HCO osocza ph osocza wzrasta; SID płynu < HCO osocza ph osocza spada. Piśmiennictwo: 1. Kellum JA, Elbers P: Stewart s Textbook of Acid-Base. Copyright 2009 AcidBase.org. 2. Chawla G, Drummond G: Water, strong ions, and weak ions. CEACCP 2008; : Smuszkiewicz P, Jakieła-Sokołowska A: Interpretacja zaburzeń kwasowo- -zasadowych u chorych w oddziale intensywnej terapii. Czy tradycyjne podejście jest wystarczające? Anestezjol Ratown 2011; 5: Rinaldi S, DeGaudio AR: Strong ion difference and strong anion gap: the Stewart approach to acid base disturbances. Curr Anaesth Crit Care 2005; 16: Morgan T: Clinical review: The meaning of acid-base abnormalities in the intensive care unit effects of fluid administration. Crit Care 2005; 9: Story D, Kellum J: Acid-base balance revisited: Stewart and strong ions. Semin Anesth Perioperat Med Pain 2005; 24: Fencl V, Jabor A, Kazda A, Figge J: Diagnosis of metabolic acidbase disturbances in critically ill patients. Am J Respir /Crit Care Med 2000; 162: Figge J, Mydosh T, Fencl V: Serum proteins and acid base equilibria: a follow up. J Lab Clin Med 1992; 120: Morgan TJ, Venkatesh B, Hall J: Crystalloid strong ion difference determines metabolic acid-base change during in vitro haemodilution. Crit Care Med 2002; 0: Morgan T, Venkatesh B, Hall J: Crystalloid strong ion difference determines metabolic Acid-base change during acute normovolaemic haemodilution. Intensive Care Med 2004; 0: Morgan TJ, Venkatesh B, Beindorf A, et al.: Acid-base and bioenergetics during balanced versus unbalanced normovolemic hemodilution. Anaesth Intensive Care 2007; 5: McLean AG, Davenport A, Cox D, Sweny P: Effects of lactate buffered and lactate-free dialysate in CAVHD patients with and without liver dysfunction. Kidney Int 2000; 58: Carlesso E, Maiocchi G, Tallarini F et al.: The rule regulating ph changes during crystalloid infusion. Intensive Care Med 2011; 7: Rehm M, Orth V, Scheingraber S et al.: Acid-base changes caused by 5% albumin versus 6% hydroxyethyl starch solution in patients undergoing acute normovolemic hemodilution: a randomized prospective study. Anesthesiology 2000; 9: Adres do korespondencji: dr n. med. Jakub Szrama Szpital Kliniczny nr 2 ul. Przybyszewskiego 49, 6055 Poznań, tel.: , faks: jakub.szrama@gmail.com Otrzymano: r. Zaakceptowano: r. 110
Anestezjologia Ratownictwo Nauka Praktyka / Anaesthesiology Rescue Medicine Science Practice
 371 Anestezjologia i Ratownictwo 2011; 5: 371-380 ARTYKUŁ POGLĄDOWY/REVIEW PAPER Wpłynęło/Submitted: 03.07.2011 Poprawiono/Corrected: 13.09.2011 Zaakceptowano/Accepted: 15.09.2011 Akademia Medycyny Interpretacja
371 Anestezjologia i Ratownictwo 2011; 5: 371-380 ARTYKUŁ POGLĄDOWY/REVIEW PAPER Wpłynęło/Submitted: 03.07.2011 Poprawiono/Corrected: 13.09.2011 Zaakceptowano/Accepted: 15.09.2011 Akademia Medycyny Interpretacja
 Prof. dr hab. n. med. Anna Wasilewska Zaburzenia gospodarki kwasowozasadowej i ich znaczenie w nefrologii. Do oceny równowagi kwasowo zasadowej potrzebujemy: Gazometria (ph, CO 2 ) Biochemia surowicy krwi
Prof. dr hab. n. med. Anna Wasilewska Zaburzenia gospodarki kwasowozasadowej i ich znaczenie w nefrologii. Do oceny równowagi kwasowo zasadowej potrzebujemy: Gazometria (ph, CO 2 ) Biochemia surowicy krwi
MECHANIZM NEUROHORMONALNY
 MECHANIZM NEUROHORMONALNY bodźce nerwowe docierają do nerek włóknami nerwu trzewnego, wpływają one nie tylko na wielkość GFR i ukrwienie nerek (zmieniając opór naczyń nerkowych), ale również bezpośrednio
MECHANIZM NEUROHORMONALNY bodźce nerwowe docierają do nerek włóknami nerwu trzewnego, wpływają one nie tylko na wielkość GFR i ukrwienie nerek (zmieniając opór naczyń nerkowych), ale również bezpośrednio
Inżynieria Środowiska
 ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
Analiza zaburzeń równowagi kwasowo-zasadowej w cukrzycowej śpiączce ketonowej na podstawie metody Stewarta opis przypadku
 PRACE KAZUISTYCZNE Anestezjologia Intensywna Terapia 2013, tom 45, numer 4, 248 252 ISSN 0209 1712 www.ait.viamedica.pl Analiza zaburzeń równowagi kwasowozasadowej w cukrzycowej śpiączce ketonowej na podstawie
PRACE KAZUISTYCZNE Anestezjologia Intensywna Terapia 2013, tom 45, numer 4, 248 252 ISSN 0209 1712 www.ait.viamedica.pl Analiza zaburzeń równowagi kwasowozasadowej w cukrzycowej śpiączce ketonowej na podstawie
HYDROLIZA SOLI. 1. Hydroliza soli mocnej zasady i słabego kwasu. Przykładem jest octan sodu, dla którego reakcja hydrolizy przebiega następująco:
 HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph
 Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph Dysocjacja elektrolitów W drugiej połowie XIX wieku szwedzki chemik S.A. Arrhenius doświadczalnie udowodnił, że substancje
Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph Dysocjacja elektrolitów W drugiej połowie XIX wieku szwedzki chemik S.A. Arrhenius doświadczalnie udowodnił, że substancje
Mechanizm działania buforów *
 Mechanizm działania buforów * UNIWERSYTET PRZYRODNICZY Z doświadczenia nabytego w laboratorium wiemy, że dodanie kropli stężonego kwasu do 10 ml wody powoduje gwałtowny spadek ph o kilka jednostek. Tymczasem
Mechanizm działania buforów * UNIWERSYTET PRZYRODNICZY Z doświadczenia nabytego w laboratorium wiemy, że dodanie kropli stężonego kwasu do 10 ml wody powoduje gwałtowny spadek ph o kilka jednostek. Tymczasem
Równowaga kwasowo-zasadowa. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowaga kwasowozasadowa Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Krytyka pojęcia ph ph = log [H + ] ph [H+] 1 100 mmol/l D = 90 mmol/l 2 10 mmol/l D = 9 mmol/l 3 1 mmol/l 2 Krytyka pojęcia
Równowaga kwasowozasadowa Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Krytyka pojęcia ph ph = log [H + ] ph [H+] 1 100 mmol/l D = 90 mmol/l 2 10 mmol/l D = 9 mmol/l 3 1 mmol/l 2 Krytyka pojęcia
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak)
 Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Zaburzenia równowagi kwasowo-zasadowej
 17 Zaburzenia równowagi kwasowo-zasadowej Tabela 17.1. Ocena stopnia zaburzeń równowagi kwasowo-zasadowej ph krwi tętniczej Równowaga kwasowo-zasadowa Stężenie jonu wodorowego (nmol/l) < 7,2 Ciężka kwasica
17 Zaburzenia równowagi kwasowo-zasadowej Tabela 17.1. Ocena stopnia zaburzeń równowagi kwasowo-zasadowej ph krwi tętniczej Równowaga kwasowo-zasadowa Stężenie jonu wodorowego (nmol/l) < 7,2 Ciężka kwasica
Chemia - B udownictwo WS TiP
 Chemia - B udownictwo WS TiP dysocjacja elektrolityczna, reakcje w roztworach wodnych, ph wykład nr 2b Teoria dys ocjacji jonowej Elektrolity i nieelektrolity Wpływ polarnej budowy cząsteczki wody na proces
Chemia - B udownictwo WS TiP dysocjacja elektrolityczna, reakcje w roztworach wodnych, ph wykład nr 2b Teoria dys ocjacji jonowej Elektrolity i nieelektrolity Wpływ polarnej budowy cząsteczki wody na proces
Wpływ płynoterapii na krzepnięcie/fibrynolizę
 Wpływ płynoterapii na krzepnięcie/fibrynolizę Piotr Czempik, Katedra i Oddział Anestezjologii i Intensywnej Terapii SUM Uniwersyteckie Centrum Kliniczne w Katowicach Śląska Izba Lekarska, 20.02.2017. 1
Wpływ płynoterapii na krzepnięcie/fibrynolizę Piotr Czempik, Katedra i Oddział Anestezjologii i Intensywnej Terapii SUM Uniwersyteckie Centrum Kliniczne w Katowicach Śląska Izba Lekarska, 20.02.2017. 1
Analiza gazometrii krwi tętniczej
 Analiza gazometrii krwi tętniczej dr hab. n.med. Barbara Adamik Katedra i Klinika Anestezjologii i Intensywnej Terapii Uniwersytet Medyczny we Wrocławiu Analiza gazometrii krwi tętniczej wymiana gazowa
Analiza gazometrii krwi tętniczej dr hab. n.med. Barbara Adamik Katedra i Klinika Anestezjologii i Intensywnej Terapii Uniwersytet Medyczny we Wrocławiu Analiza gazometrii krwi tętniczej wymiana gazowa
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
Równowaga kwasowo-zasadowa. Zakład Chemii Medycznej PUM
 Równowaga kwasowozasadowa Zakład Chemii Medycznej PUM Teorie kwasów i zasad Teoria dysocjacji elektrolitycznej Arheniusa: podczas rozpuszczania w wodzie wodzie kwas: dysocjuje z odszczepieniem kationu
Równowaga kwasowozasadowa Zakład Chemii Medycznej PUM Teorie kwasów i zasad Teoria dysocjacji elektrolitycznej Arheniusa: podczas rozpuszczania w wodzie wodzie kwas: dysocjuje z odszczepieniem kationu
1 Kinetyka reakcji chemicznych
 Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
1 Hydroliza soli. Hydroliza soli 1
 Hydroliza soli 1 1 Hydroliza soli Niektóre sole, rozpuszczone w wodzie, reagują z cząsteczkami rozpuszczalnika. Reakcja ta nosi miano hydrolizy. Reakcję hydrolizy soli o wzorze BA, można schematycznie
Hydroliza soli 1 1 Hydroliza soli Niektóre sole, rozpuszczone w wodzie, reagują z cząsteczkami rozpuszczalnika. Reakcja ta nosi miano hydrolizy. Reakcję hydrolizy soli o wzorze BA, można schematycznie
Kwas HA i odpowiadająca mu zasada A stanowią sprzężoną parę (podobnie zasada B i kwas BH + ):
 Spis treści 1 Kwasy i zasady 2 Rola rozpuszczalnika 3 Dysocjacja wody 4 Słabe kwasy i zasady 5 Skala ph 6 Oblicznie ph słabego kwasu 7 Obliczanie ph słabej zasady 8 Przykłady obliczeń 81 Zadanie 1 811
Spis treści 1 Kwasy i zasady 2 Rola rozpuszczalnika 3 Dysocjacja wody 4 Słabe kwasy i zasady 5 Skala ph 6 Oblicznie ph słabego kwasu 7 Obliczanie ph słabej zasady 8 Przykłady obliczeń 81 Zadanie 1 811
- w nawiasach kwadratowych stężenia molowe.
 Cz. VII Dysocjacja jonowa, moc elektrolitów, prawo rozcieńczeń Ostwalda i ph roztworów. 1. Pojęcia i definicja. Dysocjacja elektroniczna (jonowa) to samorzutny rozpad substancji na jony w wodzie lub innych
Cz. VII Dysocjacja jonowa, moc elektrolitów, prawo rozcieńczeń Ostwalda i ph roztworów. 1. Pojęcia i definicja. Dysocjacja elektroniczna (jonowa) to samorzutny rozpad substancji na jony w wodzie lub innych
LICEALIŚCI LICZĄ PRZYKŁADOWE ZADANIA Z ROZWIĄZANIAMI
 Zadanie 1: Słaby kwas HA o stężeniu 0,1 mol/litr jest zdysocjowany w 1,3 %. Oblicz stałą dysocjacji tego kwasu. Jeżeli jest to słaby kwas, można użyć wzoru uproszczonego: K = α C = (0,013) 0,1 = 1,74 10-5
Zadanie 1: Słaby kwas HA o stężeniu 0,1 mol/litr jest zdysocjowany w 1,3 %. Oblicz stałą dysocjacji tego kwasu. Jeżeli jest to słaby kwas, można użyć wzoru uproszczonego: K = α C = (0,013) 0,1 = 1,74 10-5
HYDROLIZA SOLI. Przykładem jest octan sodu, dla którego reakcja hydrolizy przebiega następująco:
 HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
CHOROBY WEWNĘTRZNE CHOROBY UKŁADU MOCZOWEGO
 CHOROBY WEWNĘTRZNE CHOROBY UKŁADU MOCZOWEGO Dariusz Moczulski Klinika Chorób Wewnętrznych i Nefrodiabetologii Uniwersytecki Szpital Kliniczny im. WAM ul. Żeromskiego 113, Łódź Zaburzenia gospodarki wodno
CHOROBY WEWNĘTRZNE CHOROBY UKŁADU MOCZOWEGO Dariusz Moczulski Klinika Chorób Wewnętrznych i Nefrodiabetologii Uniwersytecki Szpital Kliniczny im. WAM ul. Żeromskiego 113, Łódź Zaburzenia gospodarki wodno
Roztwory elekreolitów
 Imię i nazwisko:... Roztwory elekreolitów Zadanie 1. (2pkt) W teorii Brönsteda sprzężoną parą kwas-zasada nazywa się układ złożony z kwasu oraz zasady, która powstaje z tego kwasu przez odłączenie protonu.
Imię i nazwisko:... Roztwory elekreolitów Zadanie 1. (2pkt) W teorii Brönsteda sprzężoną parą kwas-zasada nazywa się układ złożony z kwasu oraz zasady, która powstaje z tego kwasu przez odłączenie protonu.
6. ph i ELEKTROLITY. 6. ph i elektrolity
 6. ph i ELEKTROLITY 31 6. ph i elektrolity 6.1. Oblicz ph roztworu zawierającego 0,365 g HCl w 1,0 dm 3 roztworu. Odp 2,00 6.2. Oblicz ph 0,0050 molowego roztworu wodorotlenku baru (α = 1,00). Odp. 12,00
6. ph i ELEKTROLITY 31 6. ph i elektrolity 6.1. Oblicz ph roztworu zawierającego 0,365 g HCl w 1,0 dm 3 roztworu. Odp 2,00 6.2. Oblicz ph 0,0050 molowego roztworu wodorotlenku baru (α = 1,00). Odp. 12,00
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW
 WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
Od niego zależy prawidłowy przebieg większości procesów życiowych.
 Prawo zachowania stałości stężenia jonu wodorowego jest jednym z najważniejszych praw dotyczących żywego organizmu. Od niego zależy prawidłowy przebieg większości procesów życiowych. Równanie Hendersona-Hasselbacha
Prawo zachowania stałości stężenia jonu wodorowego jest jednym z najważniejszych praw dotyczących żywego organizmu. Od niego zależy prawidłowy przebieg większości procesów życiowych. Równanie Hendersona-Hasselbacha
Stosowanie Use of Hydroxyethyl roztworów hydroksyetyloskrobi
 Szkolenie Training Stosowanie Use of Hydroxyethyl roztworów hydroksyetyloskrobi Starch Solutions according zgodnie to the z zatwierdzonymi approved European drukami Product informacyjnymi Information w
Szkolenie Training Stosowanie Use of Hydroxyethyl roztworów hydroksyetyloskrobi Starch Solutions according zgodnie to the z zatwierdzonymi approved European drukami Product informacyjnymi Information w
Maksymalne wydzielanie potu w czasie wysiłku fizycznego może osiągać 2-3 litrów na godzinę zastanów się jakie mogą być tego konsekwencje?
 Ćwiczenia IV I. Termoregulacja wysiłkowa. Utrzymanie stałej temperatury ciała jest skomplikowanym procesem. Choć temperatura różnych części ciała może być różna, ważne jest utrzymanie temperatury wewnętrznej
Ćwiczenia IV I. Termoregulacja wysiłkowa. Utrzymanie stałej temperatury ciała jest skomplikowanym procesem. Choć temperatura różnych części ciała może być różna, ważne jest utrzymanie temperatury wewnętrznej
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Metaboliczne skutki płynoterapii
 Metaboliczne skutki płynoterapii Wojciech Dąbrowski Katedra i I Klinika Anestezjologii i Intensywnej Terapii Uniwersytetu Medycznego w Lublinie Członek komitetu naukowego International Fluid Academy Kilka
Metaboliczne skutki płynoterapii Wojciech Dąbrowski Katedra i I Klinika Anestezjologii i Intensywnej Terapii Uniwersytetu Medycznego w Lublinie Członek komitetu naukowego International Fluid Academy Kilka
Równowaga kwasowo-zasadowa i gospodarka wodno-elektrolitowa
 Równowaga kwasowo-zasadowa i gospodarka wodno-elektrolitowa H + HCO 3 - HCO 3 - Konieczne Na + lub K + Nerki Zakwaszenie moczu ph = pk + log [HCO 3- ] 0,03 x pco 2 Alkalizacja moczu ph = -log[h + ] CO
Równowaga kwasowo-zasadowa i gospodarka wodno-elektrolitowa H + HCO 3 - HCO 3 - Konieczne Na + lub K + Nerki Zakwaszenie moczu ph = pk + log [HCO 3- ] 0,03 x pco 2 Alkalizacja moczu ph = -log[h + ] CO
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW
 WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp Mianem rozpuszczalności określamy maksymalną ilość danej substancji (w gramach lub molach), jaką w danej temperaturze można rozpuścić w określonej
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp Mianem rozpuszczalności określamy maksymalną ilość danej substancji (w gramach lub molach), jaką w danej temperaturze można rozpuścić w określonej
Związki nieorganiczne
 strona 1/8 Związki nieorganiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Typy związków nieorganicznych: kwasy, zasady, wodorotlenki, dysocjacja jonowa, odczyn roztworu,
strona 1/8 Związki nieorganiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Typy związków nieorganicznych: kwasy, zasady, wodorotlenki, dysocjacja jonowa, odczyn roztworu,
KWASY I WODOROTLENKI. 1. Poprawne nazwy kwasów H 2 S, H 2 SO 4, HNO 3, to:
 KWASY I WODOROTLENKI 1. Poprawne nazwy kwasów H 2 S, H 2 SO 4, HNO 3, to: 1. kwas siarkowy (IV), kwas siarkowy (VI), kwas azotowy, 2. kwas siarkowy (VI), kwas siarkowy (IV), kwas azotowy (V), 3. kwas siarkowodorowy,
KWASY I WODOROTLENKI 1. Poprawne nazwy kwasów H 2 S, H 2 SO 4, HNO 3, to: 1. kwas siarkowy (IV), kwas siarkowy (VI), kwas azotowy, 2. kwas siarkowy (VI), kwas siarkowy (IV), kwas azotowy (V), 3. kwas siarkowodorowy,
Stanisław Poprzęcki, Adam Zając PRAKTYCZNE ZASTOSOWANIE WODOROWĘGLANU SODU W SPORCIE
 Stanisław Poprzęcki, Adam Zając PRAKTYCZNE ZASTOSOWANIE WODOROWĘGLANU SODU W SPORCIE [H + ] M 10 0 Silnie kwaśne 10-1 10-2 10-3 10-4 10-5 10-6 10-7 10-8 ph Większość żywych komórek ma wąską tolerancję
Stanisław Poprzęcki, Adam Zając PRAKTYCZNE ZASTOSOWANIE WODOROWĘGLANU SODU W SPORCIE [H + ] M 10 0 Silnie kwaśne 10-1 10-2 10-3 10-4 10-5 10-6 10-7 10-8 ph Większość żywych komórek ma wąską tolerancję
Obliczenia chemiczne. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW
 RÓWNOWAGI W ROZTWORACH ELETROLITÓW Opracowanie: dr Jadwiga Zawada, dr inż. rystyna Moskwa, mgr Magdalena Bisztyga 1. Dysocjacja elektrolityczna Substancje, które podczas rozpuszczania w wodzie (lub innych
RÓWNOWAGI W ROZTWORACH ELETROLITÓW Opracowanie: dr Jadwiga Zawada, dr inż. rystyna Moskwa, mgr Magdalena Bisztyga 1. Dysocjacja elektrolityczna Substancje, które podczas rozpuszczania w wodzie (lub innych
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA. Wykład 2
 PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
Badanie płynów stosowanych w płynoterapii okołooperacyjnej analiza obecnie stosowanej praktyki The analysis of current practice in fluid therapy
 262 Anestezjologia i Ratownictwo 2012; 6: 262-267 ARTYKUŁ ORYGINALNY/ORIGINAL PAPER Otrzymano/Submitted: 08.05.2012 Poprawiono/Corrected: 20.09.2012 Zaakceptowano/Accepted: 20.09.2012 Akademia Medycyny
262 Anestezjologia i Ratownictwo 2012; 6: 262-267 ARTYKUŁ ORYGINALNY/ORIGINAL PAPER Otrzymano/Submitted: 08.05.2012 Poprawiono/Corrected: 20.09.2012 Zaakceptowano/Accepted: 20.09.2012 Akademia Medycyny
dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K
![dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K](/thumbs/55/36391740.jpg) RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
Roztwory mocnych elektrolitów ćwiczenia 1
 Roztwory mocnych elektrolitów ćwiczenia 1 1 Stała dysocjacji Słabe kwasy i zasady nie ulegają całkowicie reakcji dysocjacji elektrolitycznej. Oznacza to, że są słabymi elektrolitami. Najczęściej używanym
Roztwory mocnych elektrolitów ćwiczenia 1 1 Stała dysocjacji Słabe kwasy i zasady nie ulegają całkowicie reakcji dysocjacji elektrolitycznej. Oznacza to, że są słabymi elektrolitami. Najczęściej używanym
Płynoterapia małą objętością.
 Waldemar Machała Płynoterapia małą objętością. Kraków, 28 października 2011 r. Klinika Anestezjologii i Intensywnej Terapii Uniwersytecki Szpital Kliniczny Stan pacjenta Przewodnienie, hyperwolemia?. Euwolemia.
Waldemar Machała Płynoterapia małą objętością. Kraków, 28 października 2011 r. Klinika Anestezjologii i Intensywnej Terapii Uniwersytecki Szpital Kliniczny Stan pacjenta Przewodnienie, hyperwolemia?. Euwolemia.
Wodorotlenki. n to liczba grup wodorotlenowych w cząsteczce wodorotlenku (równa wartościowości M)
 Wodorotlenki Definicja - Wodorotlenkami nazywamy związki chemiczne, zbudowane z kationu metalu (zazwyczaj) (M) i anionu wodorotlenowego (OH - ) Ogólny wzór wodorotlenków: M(OH) n M oznacza symbol metalu.
Wodorotlenki Definicja - Wodorotlenkami nazywamy związki chemiczne, zbudowane z kationu metalu (zazwyczaj) (M) i anionu wodorotlenowego (OH - ) Ogólny wzór wodorotlenków: M(OH) n M oznacza symbol metalu.
BUDOWA USTROJU Zaburzenia regulacji wodno-elektrolitowej (C) III Katedra Chirurgii Ogólnej UJ CM
 BUDOWA USTROJU Zaburzenia regulacji wodno-elektrolitowej 2016 (C) III Katedra Chirurgii Ogólnej UJ CM Skład ustroju 100% 90% % wagi ciała 80% Tłuszcz 25% 70% 60% 50% 40% 30% 20% 10% 0% BMC 75% Tłuszcz
BUDOWA USTROJU Zaburzenia regulacji wodno-elektrolitowej 2016 (C) III Katedra Chirurgii Ogólnej UJ CM Skład ustroju 100% 90% % wagi ciała 80% Tłuszcz 25% 70% 60% 50% 40% 30% 20% 10% 0% BMC 75% Tłuszcz
RÓWNOWAGA KWASOWO-ZASADOWA
 RÓWNOWAGA KWASOWO-ZASADOWA Katedra Analityki Medycznej Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie http://www.uwm.edu.pl/wnm/analitykamedyczna/ Patofizjologia równowagi kwasowo-zasadowej
RÓWNOWAGA KWASOWO-ZASADOWA Katedra Analityki Medycznej Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie http://www.uwm.edu.pl/wnm/analitykamedyczna/ Patofizjologia równowagi kwasowo-zasadowej
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO 0,9% Sodium Chloride Braun, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera Chlorek sodu Stężenia elektrolitów:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO 0,9% Sodium Chloride Braun, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera Chlorek sodu Stężenia elektrolitów:
KRYSTALOIDY (jakie?).
 Fluid Therapy Might Be More Difficult Than You Think Robert G. Hahn Anesth Analg 2007 PŁYNOTERAPIA RODZĄCEJ Elżbieta Nowacka I Klinika Anestezjologii i Intensywnej Terapii WUM Kierownik: dr hab.n.med..
Fluid Therapy Might Be More Difficult Than You Think Robert G. Hahn Anesth Analg 2007 PŁYNOTERAPIA RODZĄCEJ Elżbieta Nowacka I Klinika Anestezjologii i Intensywnej Terapii WUM Kierownik: dr hab.n.med..
Współczesne aspekty płynoterapii
 Współczesne aspekty płynoterapii Paweł Sobczyński Katedra i I Klinika Anestezjologii i Intensywnej Terapii Szpital Kliniczny Przemienienia Pańskiego UMP Hahn RG. Anesth Analg 2007; 105: 304-305 Płynoterapia
Współczesne aspekty płynoterapii Paweł Sobczyński Katedra i I Klinika Anestezjologii i Intensywnej Terapii Szpital Kliniczny Przemienienia Pańskiego UMP Hahn RG. Anesth Analg 2007; 105: 304-305 Płynoterapia
Równowagi jonowe - ph roztworu
 Równowagi jonowe - ph roztworu Kwasy, zasady i sole nazywa się elektrolitami, ponieważ przewodzą prąd elektryczny, zarówno w wodnych roztworach, jak i w stanie stopionym (sole). Nie wszystkie wodne roztwory
Równowagi jonowe - ph roztworu Kwasy, zasady i sole nazywa się elektrolitami, ponieważ przewodzą prąd elektryczny, zarówno w wodnych roztworach, jak i w stanie stopionym (sole). Nie wszystkie wodne roztwory
Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak
 Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga ciało
Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga ciało
Zalecenia kliniczne dotyczące postępowania u chorych na cukrzycę 2009. Stanowisko Polskiego Towarzystwa Diabetologicznego
 Zalecenia kliniczne dotyczące postępowania u chorych na cukrzycę 2009 Stanowisko Polskiego Towarzystwa Diabetologicznego Postępowanie w stanach nagłych: I II III IV Hipoglikemia Cukrzycowa kwasica ketonowa
Zalecenia kliniczne dotyczące postępowania u chorych na cukrzycę 2009 Stanowisko Polskiego Towarzystwa Diabetologicznego Postępowanie w stanach nagłych: I II III IV Hipoglikemia Cukrzycowa kwasica ketonowa
CHEMIA BUDOWLANA ĆWICZENIE NR 3
 CHEMIA BUDOWLANA ĆWICZENIE NR 3 HYDROLIZA SOLI I WYZNACZANIE ph ROZTWORÓW WSTĘP TEORETYCZNY Kwasy są to substancje zdolne do oddawania protonów. Zasady są zdolne do wiązania protonów. Definicję kwasów
CHEMIA BUDOWLANA ĆWICZENIE NR 3 HYDROLIZA SOLI I WYZNACZANIE ph ROZTWORÓW WSTĘP TEORETYCZNY Kwasy są to substancje zdolne do oddawania protonów. Zasady są zdolne do wiązania protonów. Definicję kwasów
DIAGNOSTYKA LABORAOTRYJNA ZABURZEŃ GOSPODARKI WODNO-ELEKTROLITOWEJ
 DIAGNOSTYKA LABORAOTRYJNA ZABURZEŃ GOSPODARKI WODNO-ELEKTROLITOWEJ Katedra Analityki Medycznej Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie http://www.uwm.edu.pl/wnm/analitykamedyczna/
DIAGNOSTYKA LABORAOTRYJNA ZABURZEŃ GOSPODARKI WODNO-ELEKTROLITOWEJ Katedra Analityki Medycznej Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie http://www.uwm.edu.pl/wnm/analitykamedyczna/
Płynoterapia w anestezjologii pediatrycznej
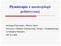 Płynoterapia w anestezjologii pediatrycznej Andrzej Piotrowski, Marcin Gach Kliniczny Oddział Intensywnej Terapii i Anestezjologii II Katedra Pediatrii UM w Łodzi Zmiany rozdziału płynów wg wieku Zapotrzebowanie
Płynoterapia w anestezjologii pediatrycznej Andrzej Piotrowski, Marcin Gach Kliniczny Oddział Intensywnej Terapii i Anestezjologii II Katedra Pediatrii UM w Łodzi Zmiany rozdziału płynów wg wieku Zapotrzebowanie
Reakcje chemiczne. Typ reakcji Schemat Przykłady Reakcja syntezy
 Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyi i Ochrony Środowisa Studia stacjonarne, Ro I, Semestr zimowy 01/14 Dr hab. inż. Tomasz Brylewsi e-mail: brylew@agh.edu.pl tel. 1-617-59 atedra Fizyochemii
Chemia - laboratorium Wydział Geologii, Geofizyi i Ochrony Środowisa Studia stacjonarne, Ro I, Semestr zimowy 01/14 Dr hab. inż. Tomasz Brylewsi e-mail: brylew@agh.edu.pl tel. 1-617-59 atedra Fizyochemii
WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO
 10 WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO CEL ĆWICZENIA Poznanie podstawowych zagadnień teorii dysocjacji elektrolitycznej i problemów związanych z właściwościami kwasów i zasad oraz
10 WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO CEL ĆWICZENIA Poznanie podstawowych zagadnień teorii dysocjacji elektrolitycznej i problemów związanych z właściwościami kwasów i zasad oraz
LABORATORIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE. Ćwiczenie nr 2 Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.
 LABOATOIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE Ćwiczenie nr Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.. Wprowadzenie Proces rozpadu drobin związków chemicznych
LABOATOIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE Ćwiczenie nr Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.. Wprowadzenie Proces rozpadu drobin związków chemicznych
TEST NA EGZAMIN POPRAWKOWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM
 TEST NA EGZAMIN PPRAWKWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM I. Część pisemna: 1. Które z poniższych stwierdzeń jest fałszywe? a.) Kwasy są to związki chemiczne zbudowane z wodoru i reszty kwasowej.
TEST NA EGZAMIN PPRAWKWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM I. Część pisemna: 1. Które z poniższych stwierdzeń jest fałszywe? a.) Kwasy są to związki chemiczne zbudowane z wodoru i reszty kwasowej.
Zastosowanie antykoagulacji cytrynianowej w ciągłej terapii nerkozastępczej u niemowląt z ostrym uszkodzeniem nerek.
 Zastosowanie antykoagulacji cytrynianowej w ciągłej terapii nerkozastępczej u niemowląt z ostrym uszkodzeniem nerek. Klinka Kardiologii i Nefrologii Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu
Zastosowanie antykoagulacji cytrynianowej w ciągłej terapii nerkozastępczej u niemowląt z ostrym uszkodzeniem nerek. Klinka Kardiologii i Nefrologii Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu
RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW.
 RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW. Zagadnienia: Zjawisko dysocjacji: stała i stopień dysocjacji Elektrolity słabe i mocne Efekt wspólnego jonu Reakcje strącania osadów Iloczyn rozpuszczalności Odczynnik
RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW. Zagadnienia: Zjawisko dysocjacji: stała i stopień dysocjacji Elektrolity słabe i mocne Efekt wspólnego jonu Reakcje strącania osadów Iloczyn rozpuszczalności Odczynnik
Wykład 11 Równowaga kwasowo-zasadowa
 Wykład 11 Równowaga kwasowo-zasadowa JS Skala ph Skala ph ilościowa skala kwasowości i zasadowości roztworów wodnych związków chemicznych. Skala ta jest oparta na aktywności jonów hydroniowych [H3O+] w
Wykład 11 Równowaga kwasowo-zasadowa JS Skala ph Skala ph ilościowa skala kwasowości i zasadowości roztworów wodnych związków chemicznych. Skala ta jest oparta na aktywności jonów hydroniowych [H3O+] w
Woda w organizmie człowieka. Właściwości koligatywne roztworów. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Woda w organizmie człowieka. Właściwości koligatywne roztworów. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Do niedawna nasze wiadomości o gospodarce wodnej i elektrolitowej były nie tyle
Woda w organizmie człowieka. Właściwości koligatywne roztworów. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Do niedawna nasze wiadomości o gospodarce wodnej i elektrolitowej były nie tyle
Fresenius Kabi Polska Sp. z o.o. CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO SOLUTIO RINGERI LACTATE FRESENIUS, roztwór do infuzji 2. SKŁAD ILOŚCIOWY I JAKOŚCIOWY 1 ml roztworu zawiera 6,01 mg chlorku sodu (Natrii
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO SOLUTIO RINGERI LACTATE FRESENIUS, roztwór do infuzji 2. SKŁAD ILOŚCIOWY I JAKOŚCIOWY 1 ml roztworu zawiera 6,01 mg chlorku sodu (Natrii
HYDROLIZA SOLI. ROZTWORY BUFOROWE
 Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
WYMAGANIA EDUKACYJNE
 GIMNAZJUM NR 2 W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie II gimnazjum str. 1 Wymagania edukacyjne niezbędne do
GIMNAZJUM NR 2 W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie II gimnazjum str. 1 Wymagania edukacyjne niezbędne do
Zad: 5 Oblicz stężenie niezdysocjowanego kwasu octowego w wodnym roztworze o stężeniu 0,1 mol/dm 3, jeśli ph tego roztworu wynosi 3.
 Zad: 1 Oblicz wartość ph dla 0,001 molowego roztworu HCl Zad: 2 Oblicz stężenie jonów wodorowych jeżeli wartość ph wynosi 5 Zad: 3 Oblicz stężenie jonów wodorotlenkowych w 0,05 molowym roztworze H 2 SO
Zad: 1 Oblicz wartość ph dla 0,001 molowego roztworu HCl Zad: 2 Oblicz stężenie jonów wodorowych jeżeli wartość ph wynosi 5 Zad: 3 Oblicz stężenie jonów wodorotlenkowych w 0,05 molowym roztworze H 2 SO
Scenariusz lekcji w technikum zakres podstawowy 2 godziny
 Scenariusz lekcji w technikum zakres podstawowy 2 godziny Temat : Hydroliza soli. Cele dydaktyczno wychowawcze: Wyjaśnienie przyczyn różnych odczynów soli Uświadomienie różnej roli wody w procesach dysocjacji
Scenariusz lekcji w technikum zakres podstawowy 2 godziny Temat : Hydroliza soli. Cele dydaktyczno wychowawcze: Wyjaśnienie przyczyn różnych odczynów soli Uświadomienie różnej roli wody w procesach dysocjacji
prof. dr hab. Małgorzata Jóźwiak
 Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Hemodynamic optimization fo sepsis- induced tissue hypoperfusion.
 Hemodynamic optimization fo sepsis- induced tissue hypoperfusion. Sergio L, Cavazzoni Z, Delinger RP Critical Care 2006 Opracował: lek. Michał Orczykowski II Zakład Anestezjologii i Intensywnej Terapii
Hemodynamic optimization fo sepsis- induced tissue hypoperfusion. Sergio L, Cavazzoni Z, Delinger RP Critical Care 2006 Opracował: lek. Michał Orczykowski II Zakład Anestezjologii i Intensywnej Terapii
VI Podkarpacki Konkurs Chemiczny 2013/2014
 VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
MAŁOPOLSKI KONKURS CHEMICZNY DLA GIMNAZJALISTÓW
 MAŁOPOLSKI KONKURS CHEMICZNY DLA GIMNAZJALISTÓW Etap I (szkolny) 22 października 2013 roku Materiały dla nauczycieli Rozwiązania zadań wraz z punktacją Uwagi ogólne: - Za prawidłowe rozwiązanie zadań rachunkowych
MAŁOPOLSKI KONKURS CHEMICZNY DLA GIMNAZJALISTÓW Etap I (szkolny) 22 października 2013 roku Materiały dla nauczycieli Rozwiązania zadań wraz z punktacją Uwagi ogólne: - Za prawidłowe rozwiązanie zadań rachunkowych
Płynoterapia okołooperacyjna. Toni Hundle
 Płynoterapia okołooperacyjna Toni Hundle Okołooperacyjna płynoterapia ma na celu: pokrycie zapotrzebowania wodnego, uzupełnienie niedoborów, utrzymanie prawidłowej czynności układu krążenia, zapewnienie
Płynoterapia okołooperacyjna Toni Hundle Okołooperacyjna płynoterapia ma na celu: pokrycie zapotrzebowania wodnego, uzupełnienie niedoborów, utrzymanie prawidłowej czynności układu krążenia, zapewnienie
KONFLIKTY NA ODDZIALE INTENSYWNEJ TERAPII
 KONFLIKTY NA ODDZIALE INTENSYWNEJ TERAPII Maria Wujtewicz Klinika Anestezjologii i Intensywnej Terapii GUMed II Konferencja Naukowa Czasopisma Anestezjologia Intensywna Terapia Sopot 2014 KONFLIKT INTERESÓW
KONFLIKTY NA ODDZIALE INTENSYWNEJ TERAPII Maria Wujtewicz Klinika Anestezjologii i Intensywnej Terapii GUMed II Konferencja Naukowa Czasopisma Anestezjologia Intensywna Terapia Sopot 2014 KONFLIKT INTERESÓW
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Przestrzenie wodne organizmu
 ROZDZIAŁ 3 Przestrzenie wodne organizmu Agnieszka Kosowska Agnieszka Kłych Dorota Polańska Jolanta Czerniak Woda jest głównym składnikiem organizmu. Stanowi 60% masy ciała dorosłego człowieka, a jej zawartość
ROZDZIAŁ 3 Przestrzenie wodne organizmu Agnieszka Kosowska Agnieszka Kłych Dorota Polańska Jolanta Czerniak Woda jest głównym składnikiem organizmu. Stanowi 60% masy ciała dorosłego człowieka, a jej zawartość
W rozdziale tym omówione będą reakcje związków nieorganicznych w których pierwiastki nie zmieniają stopni utlenienia. Do reakcji tego typu należą:
 221 Reakcje w roztworach Wiele reakcji chemicznych przebiega w roztworach. Jeżeli są to wodne roztwory elektrolitów wtedy faktycznie reagują między sobą jony. Wśród wielu reakcji chemicznych zachodzących
221 Reakcje w roztworach Wiele reakcji chemicznych przebiega w roztworach. Jeżeli są to wodne roztwory elektrolitów wtedy faktycznie reagują między sobą jony. Wśród wielu reakcji chemicznych zachodzących
Odwracalność przemiany chemicznej
 Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
Eksperyment laboratoryjny, burza mózgów, pogadanka, praca z całym zespołem, praca w grupach, praca indywidualna.
 Hydroliza soli 1. Cele lekcji a) Wiadomości Uczeń zna: istotę reakcji hydrolizy, pojęcia: hydroliza kationowa i hydroliza anionowa. Uczeń wie: które sole ulegają hydrolizie, które sole nie ulegają hydrolizie.
Hydroliza soli 1. Cele lekcji a) Wiadomości Uczeń zna: istotę reakcji hydrolizy, pojęcia: hydroliza kationowa i hydroliza anionowa. Uczeń wie: które sole ulegają hydrolizie, które sole nie ulegają hydrolizie.
Równowaga kwasowo-zasadowa. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Równowaga kwasowozasadowa Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Teorie kwasów i zasad Teoria dysocjacji elektrolitycznej Arheniusa: podczas rozpuszczania w wodzie wodzie kwas: dysocjuje
Równowaga kwasowozasadowa Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Teorie kwasów i zasad Teoria dysocjacji elektrolitycznej Arheniusa: podczas rozpuszczania w wodzie wodzie kwas: dysocjuje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO 0,9% Sodium Chloride Braun, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera Sodu chlorek Stężenia elektrolitów:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO 0,9% Sodium Chloride Braun, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera Sodu chlorek Stężenia elektrolitów:
OCENA CZYSTOŚCI WODY NA PODSTAWIE POMIARÓW PRZEWODNICTWA. OZNACZANIE STĘŻENIA WODOROTLENKU SODU METODĄ MIARECZKOWANIA KONDUKTOMETRYCZNEGO
 OCENA CZYSTOŚCI WODY NA PODSTAWIE POMIAÓW PZEWODNICTWA. OZNACZANIE STĘŻENIA WODOOTLENKU SODU METODĄ MIAECZKOWANIA KONDUKTOMETYCZNEGO Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu
OCENA CZYSTOŚCI WODY NA PODSTAWIE POMIAÓW PZEWODNICTWA. OZNACZANIE STĘŻENIA WODOOTLENKU SODU METODĄ MIAECZKOWANIA KONDUKTOMETYCZNEGO Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu
SPRAWOZDANIE 2. Data:... Kierunek studiów i nr grupy...
 SPRAWOZDANIE 2 Imię i nazwisko:... Data:.... Kierunek studiów i nr grupy..... Doświadczenie 1.1. Wskaźniki ph stosowane w laboratorium chemicznym. Zanotować obserwowane barwy roztworów w obecności badanych
SPRAWOZDANIE 2 Imię i nazwisko:... Data:.... Kierunek studiów i nr grupy..... Doświadczenie 1.1. Wskaźniki ph stosowane w laboratorium chemicznym. Zanotować obserwowane barwy roztworów w obecności badanych
Skale i wskaźniki jakości leczenia w OIT
 Skale i wskaźniki jakości leczenia w OIT Katarzyna Rutkowska Szpital Kliniczny Nr 1 w Zabrzu Wyniki leczenia (clinical outcome) śmiertelność (survival) sprawność funkcjonowania (functional outcome) jakość
Skale i wskaźniki jakości leczenia w OIT Katarzyna Rutkowska Szpital Kliniczny Nr 1 w Zabrzu Wyniki leczenia (clinical outcome) śmiertelność (survival) sprawność funkcjonowania (functional outcome) jakość
Równowaga kwasowo-zasadowa
 Równowaga kwasowo-zasadowa Elektrolity - substancje, które rozpuszczając się w wodzie lub innych rozpuszczalnikach rozpadają się na jony dodatnie i ujemne, czyli ulegają dysocjacji elektrolitycznej Stopień
Równowaga kwasowo-zasadowa Elektrolity - substancje, które rozpuszczając się w wodzie lub innych rozpuszczalnikach rozpadają się na jony dodatnie i ujemne, czyli ulegają dysocjacji elektrolitycznej Stopień
Losy pacjentów po wypisie z OIT Piotr Knapik
 Losy pacjentów po wypisie z OIT Piotr Knapik Oddział Kliniczny Kardioanestezji i Intensywnej Terapii Śląskie Centrum Chorób Serca w Zabrzu Jaki sens ma to co robimy? Warto wiedzieć co się dzieje z naszymi
Losy pacjentów po wypisie z OIT Piotr Knapik Oddział Kliniczny Kardioanestezji i Intensywnej Terapii Śląskie Centrum Chorób Serca w Zabrzu Jaki sens ma to co robimy? Warto wiedzieć co się dzieje z naszymi
Ocena metaboliczna chorego w OIT Kurs Doskonalący Jak żywić w OIT Gdańsk 21 września 2011
 Ocena metaboliczna chorego w OIT Kurs Doskonalący Jak żywić w OIT Gdańsk 21 września 2011 Katarzyna Karwowska I Klinika Anestezjologii i Intensywnej Terapii UM im. Karola Marcinkowskiego w Poznaniu Po
Ocena metaboliczna chorego w OIT Kurs Doskonalący Jak żywić w OIT Gdańsk 21 września 2011 Katarzyna Karwowska I Klinika Anestezjologii i Intensywnej Terapii UM im. Karola Marcinkowskiego w Poznaniu Po
Równowaga kwasowo-zasadowa
 Równowaga kwasowo-zasadowa Dorosły człowiek wytwarza ok. 18 moli tj 448 l CO 2 na dobę. Ponad 90% CO 2 wydalanego przez płuca powstaje w 3 reakcjach katalizowanych przez dekarboksylazy w mitochondriach.
Równowaga kwasowo-zasadowa Dorosły człowiek wytwarza ok. 18 moli tj 448 l CO 2 na dobę. Ponad 90% CO 2 wydalanego przez płuca powstaje w 3 reakcjach katalizowanych przez dekarboksylazy w mitochondriach.
Kuratorium Oświaty w Lublinie
 Kuratorium Oświaty w Lublinie ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 KOD UCZNIA ETAP OKRĘGOWY Instrukcja dla ucznia 1. Zestaw konkursowy zawiera 12 zadań. 2. Przed
Kuratorium Oświaty w Lublinie ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 KOD UCZNIA ETAP OKRĘGOWY Instrukcja dla ucznia 1. Zestaw konkursowy zawiera 12 zadań. 2. Przed
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali
 Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NATRIUM CHLORATUM 0,9 % FRESENIUS, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 9,0 mg sodu chlorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NATRIUM CHLORATUM 0,9 % FRESENIUS, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 9,0 mg sodu chlorku
 Dostępy dożylne- pielęgnacja wkłucia Płynoterapia. KRYTERIA WYBORU DOSTĘPU ŻYLNEGO Odporność żyły na działanie podawanych do niej płynów i leków(osmolarność i ph) Przewidywany czas wlewu Stan układu żylnego
Dostępy dożylne- pielęgnacja wkłucia Płynoterapia. KRYTERIA WYBORU DOSTĘPU ŻYLNEGO Odporność żyły na działanie podawanych do niej płynów i leków(osmolarność i ph) Przewidywany czas wlewu Stan układu żylnego
Równowaga kwasowo-zasadowa
 Równowaga kwasowo-zasadowa Dorosły człowiek wytwarza ok. 18 moli tj 448 l CO 2 na dobę. Ponad 90% CO 2 wydalanego przez płuca powstaje w 3 reakcjach katalizowanych przez dekarboksylazy w mitochondriach.
Równowaga kwasowo-zasadowa Dorosły człowiek wytwarza ok. 18 moli tj 448 l CO 2 na dobę. Ponad 90% CO 2 wydalanego przez płuca powstaje w 3 reakcjach katalizowanych przez dekarboksylazy w mitochondriach.
Homeostaza DR ROBERT MERONKA ZAKŁAD EKOLOGII INSTYTUT ZOOLOGII WYDZIAŁ BIOLOGII UNIWERSYTET WARSZAWSKI
 Homeostaza DR ROBERT MERONKA ZAKŁAD EKOLOGII INSTYTUT ZOOLOGII WYDZIAŁ BIOLOGII UNIWERSYTET WARSZAWSKI Różnorodność środowisk Stałość warunków w organizmie Podstawy procesów fizjologicznych Procesy zachodzące
Homeostaza DR ROBERT MERONKA ZAKŁAD EKOLOGII INSTYTUT ZOOLOGII WYDZIAŁ BIOLOGII UNIWERSYTET WARSZAWSKI Różnorodność środowisk Stałość warunków w organizmie Podstawy procesów fizjologicznych Procesy zachodzące
TYPY REAKCJI CHEMICZNYCH
 1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
Zrównoważony rozwój przemysłowych procesów pralniczych. Moduł 1 Zastosowanie wody. Rozdział 3b. Zmiękczanie wody
 Projekt Leonardo da Vinci Zrównoważony rozwój przemysłowych procesów pralniczych Moduł 1 Zastosowanie wody Rozdział 3b Zmiękczanie wody Moduł 1 Zastosowanie wody Rozdział 3 Zmiękczanie wody 1 Treść Twardość
Projekt Leonardo da Vinci Zrównoważony rozwój przemysłowych procesów pralniczych Moduł 1 Zastosowanie wody Rozdział 3b Zmiękczanie wody Moduł 1 Zastosowanie wody Rozdział 3 Zmiękczanie wody 1 Treść Twardość
