Prawa rozpadu promieniotwórczego
|
|
|
- Kajetan Leszczyński
- 8 lat temu
- Przeglądów:
Transkrypt
1 Prawa rozpadu promieniotwórczego Prawa rozpadu promieniotwórczego podlegają rozkładowi statystycznemu. ie moŝna przewidzieć kiedy dany atom ulegnie rozpadowi. W jądrze zachodzą ciągłe zmiany rozkładu energii i w kaŝdej chwili moŝe zdarzyć się konfiguracja implikująca zaistnienie rozpadu promieniotwórczego. JeŜeli odpowiednio duŝa liczba rozpadów promieniotwórczych jest obserwowana moŝna zaobserwować prawo rozpadu. Aktywność (A) radionuklidu jest jego szybkością rozpadu promieniotwórczego - d wyraŝana równaniem: dt d A = = λ dt gdzie: λ jest współczynnikiem proporcjonalności zwanym stałą rozpadu, d oznacza liczbę atomów, które uległy rozpadowi w czasie dt, znak minus oznacza zmniejszenie się liczby atomów wskutek rozpadu promieniotwórczego.
2 Liczba atomów pierwiastka promieniotwórczego, rozpadających się w jednostce czasu, jest w kaŝdej chwili proporcjonalna do ogólnej liczby atomów tego pierwiastka. Rozdzielając zmienne i całkując (w granicach o, ) otrzymujemy: o d = λtdt ln o = λt lub w postaci wykładniczej = o e λt gdzie: liczba atomów po czasie t, o początkowa liczba atomów, λ - stała rozpadu, t czas.
3 Okres, po którym liczba atomów pierwiastka zmniejszyła się o połowę nosi nazwę czasu połowicznego rozpadu. = o e λt = o = o o e λt 1/ 1 ln( ) = λt 1/ t ln λ 1 / = = 0,693 λ
4 t1/ t1/ t1/ / / 4 / t 1/ = 5730y 5730
5 Jednostką radioaktywności jest w systemie SI bequerel (Bq) 1Bq= 1 rozpad/s Starszą jednostką jednak wciąŝ stosowaną jest curie (Ci) 1Ci = aktywność (ilość rozpadów/s) 1 g 6 Ra Czas połowicznego rozpadu 6 Ra t 1/ = 1600 lat = 5,05x10 10 s 3 ln 6,03x10 x0,693 1 Ci = x = = 3,7x10 10 M t 6x5,05x10 Av 10 at A =λ Ra 1/ Bq Aktywność właściwa A w = A m (Bq/g)
6 Równowaga promieniotwórcza nuklid 1 nuklid onuklid 3 np.: 90 Sr 90 Y 90 Zr nuklid 1 jest nuklidem macierzystym (mother) nuklid jest pochodnym (daughter) nuklid 3 (granddaughter) d Szybkość produkcji (narastania) nuklidu ( ) czyli rozpadu 1 jest proporcjonalna do dt ilosci atomow 1 i jest równa róŝnicy szybkości rozpadu nuklidu 1 i rozpadu nuklidu d dt =λ 1 1 -λ
7 Rozwiązując równanie róŝniczkowe dochodzimy do równania = λ λ 1 λ 1 1 [1 e MoŜna wyróŝnić następujące przypadki: ( λ λ1) t ] t 1/ (1)>> t 1/ () czyli λ 1 <<λ wzór upraszcza się do = λ λ 1 λ t 1( 1 e ) po około 10 x t 1/ t λ1 = λ 1/ () e λ 0 i t (1) 1 = t 1/
8 1 λ1 = λ = t 1/ t 1/ () (1) Jest waŝny i częsty przypadek w pomiarach radiochemicznych np. pomiar 137 Cs lat Cs 137m,55min Ba aby zmierzyć aktywność 137 Cs po wydzieleniu jego z próbki naleŝy odczekać ok. 5 min aŝ powstanie równowagowa ilość atomów 137m Ba. Wzór teŝ pozwala na obliczenie czasu połowicznego rozpadu długoŝyjących izotopów np. 137 Ba lat Ra Rn 3dni Znając aktywność i t 1/ Rn moŝemy obliczyć ilość atomów Rn. Znając masę preparatu 6 Ra moŝemy obliczyć jego ilość jego atomów, a ze wzoru czas Ŝycia.
9 t 1/ (1)<< t 1/ () czyli λ 1 >>λ Izotop pochodny ma znacznie dłuŝszy czas Ŝycia niŝ macierzysty uklid macierzysty zanika i narasta nuklid pochodny. ie ustala się równowaga promieniotwórcza. p. 99m 6godz. 99,1x10 lat 99 Tc Tc 5 Ru t 1/ (1) t 1/ () czyli λ 1 λ Przy bardzo zbliŝonych czasach rozpadu równowaga silnie zaleŝy, który izotop rozpada się wolniej
10 Sukcesywna przemiana promieniotwórcza n... Równanie d n dt =λ n-1 n-1 -λ n n RozwiaŜanie tego równania jest złoŝone, ale bardzo szybkie numerycznie. Z rozwiązania tego równania dochodzimy do fundamentalnej zaleŝnośći Ŝe w jakimkolwiek szeregu promieniotwórczym niezaleŝnie od czasu Ŝycia poszczególnych nuklidów w stanie równowagi promieniotwórczej aktywności nuklidów są takie same: A(1)=A()=A(3)... Ilość atomów (moli) pierwiastków promieniotrczych w szeregu promieniotworczym w stanie rownowagi: 1 n T = T 1/ 1/ (1) ( n)
11 Datowanie 1. Radionuklidy kosmogeniczne 14 C 14 C 14 + e + n e Promieniowanie kosmiczne powoduje synteze 14 C w atmosferze. W CO 14 C / 1 C = i tyle samo w zywych organizmach Kiedy organizm umiera nie wymiany C z atmosfera, i stosunek 14 C 14 C/ 1 C maleje z czasem: t 1/ 14 C = 5730 yr. Pozwala na datowanie w zakresie od 1,000 5,000 lat.
12 Zakłada się, Ŝe stęŝenie 14 C w atmosferze jest w zasadzie stałe przez ostatnie lat i wahało się w zaleŝności od aktywności słońca. Ostatnio trzeba wziąć pod uwagę takŝe 14 C powstały z przemysłu jądrowego oraz zwiększoną produkcję CO zakłócającego równowagę chemiczną. Stosunek 14 C/ 1 C mierzy się akcelatorową spektroskopią masową. Tryt T 1/ =1,43 lat 3 1 H Okres datowania 0,5-80 lat Tryt tworzy się w atmosferze w wyniku oddziaływania z promieniami kosmicznymi. JednakŜe jego zastosowanie jest ograniczone ze względu wybuchy termojądrowe przeprowadzone w atmosferze oraz eksploatację elektrowni jądrowych. Równowaga została silnie zachwiana.
13 Przykład 1 W butelce starego wina na którego etykiecie była data produkcji 1937 r. zmierzono stęŝenie T O (T tryt) i porównano go ze stęŝeniem T O w wodzie powierzchniowej. StęŜenie T w winie było 4 razy mniejsze niŝ w wodzie. Czy data produkcji na butelce była prawdziwa? StęŜenie trytu w winie stanowiło 5% stęŝenia w wodzie Po 1,4 lat stęŝenie T wynosi 50% Po 4,8 lat - - wynosi 5% Czyli wino miało około 5 lat. Przykład Znaleziono drewniane szczątki prehistorycznej budowli. Pobrano próbkę, zwęglono ją zmierzono ilość 14 C. Stwierdzono, Ŝe stosunek 14 C/ 1 C w próbce był razy niŝszy niŝ w CO w atmosferze. Z jakiego wieku pochodziła budowla?
14 U / 8Pb U / 8Pb 90Th / 8Pb 3 08 Datowania geologiczne T 1/ =4,5x10 9 lat T 1/ =7x10 8 lat T 1/ =1,4x10 10 lat Okres datowania>3x10 7 lat Okres datowania >5x10 6 lat Okres datowania >3x10 8 lat W datowaniu skał wykorzystuje się stosunek powstałych z rozpadu izotopów ołowiu Pb 8Pb 8Pb do powstałego nie z rozpadu 8 Pb 40 K/ Ar 87 Rb/ Sr T 1/ =4,8x10 10 lat T 1/ =1,3x10 9 lat Okres datowania >5x10 8 lat Okres datowania >3x10 7 lat
15 MoŜna obliczyć wiek skorupy ziemskiej na podstawie składu izotopowego minerału uranitu 61,14% U, 18,1% Pb). PoniewaŜ masa atomowa ołowiu w uranicie wynosiła 06,06 jest więc równa masie atomowej 06 Pb. MoŜna więc przyjąć, Ŝe cały ołów pochodził z rozpadu uranu. Stała rozpadu 38 U 1,6x10-10 lat. 61,14 Liczba moli uranu w 100 g = = 38 18,1 Liczba moli ołowiu w 100 g = = 06 0,5689 0, Liczba atomów 38 U w czasie pomiaru = 0,5689x A Początkowa liczba atomów 38 U równa jest liczbie atomów 38 U w czasie pomiaru + ilość atomów powstałego z rozpadu 06 Pb, o =(0,5689+0,087864)x A Z wzoru na rozpad = 0 e λt t = 1 ln λ o =,303 1,6 x10 10 log 0, A A = 1,8 x10 9 lat
16 Efekt chemiczny reakcji jądrowych Energia wiązań atomów w cząsteczce jest rzędu kj mol -1 (0,4-4 ev) a energia rozpadów jądrowych jest rzędu MeV i część energii rozpadu jest przekazywana atomom jako energia odrzutu czy wzbudzenia. Reakcje jądrowe mogą powodować rozerwanie wiązań. Dla emisji cząstki β- i antyneutrina elektronowego Ze stałości zachowania momentu pędu mamy: m ν V ν +m β V β =m a V a E β m β =E a m a
17 Gdy cząstka ma prędkość zbliŝoną do prędkości światła otrzymujemy po uwzględnieniu poprawki relatywistycznej: o m E 1 = E + m 1 E m c 1 Emisja kwantu γ: E 1 = E γ mc
18 Emisja cząstki α lub β i kwantu γ Energie odrzutu przy emisji p, n i α oraz e - i e + mogą być na tyle duŝe, Ŝe wiązania ulegają rozerwaniu. Gdy emitowany jest kwant γ energia jest za mała aby rozerwać wiązania chemiczne.
19 Efekty wzbudzenia Reakcja jądrowa moŝe wzbudzić powłoki elektronowe atomu poprzez: - energię odrzutu - zmianę liczby atomowej wskutek rozpadu - wychwyt elektronu lub przemianę wewnętrzną jądra Gdy energia odrzutu jest duŝa, część elektronów nie podąŝa za jądrem i następuje jonizacja. Atomy odrzutu po zerwaniu wiązań z cząsteczką poruszają się z duŝą prędkością w ośrodku zawierającym atomy i cząsteczki. Atomy odrzutu przenikają powłoki elektronowe ulegają spowolnieniu wskutek jonizacji i wzbudzenia atomów środowiska. Mogą zachodzić reakcje nieosiągalne w innych warunkach.
20 W przemianie α powstaje jądro Z`=Z-, mamy dwa nadmiarowe elektrony, które mogą, być emitowane. Rn Po - +α W skutek zmniejszania się ładunku jądra następuje ekspansja elektronów połoŝonych blisko jądra. W przemianie α efekty związane ze wzbudzeniem są znacznie mniejsze niŝ efekty odrzutu jądra. W skutek zmniejszania się ładunku jądra następuje ekspansja elektronów połoŝonych blisko jądra. W przemianie α efekty związane ze wzbudzeniem są znacznie mniejsze niŝ efekty odrzutu jądra. W przemianie β rozpad cząsteczki w wyniku odrzutu jest moŝliwy jedynie w przypadku bardzo lekkich atomów i wysokiej energii cząstek β. W innych przypadkach energia odrzutu wynosi ułamki ev co nie wystarcza do rozerwania wiązań.
21 W przemianie β- lub wychwycie elektronu Z`=Z+1. Mamy niedomiar jednego elektronu na wewnętrznym orbitalu. Elektrony spadają na ten orbital z bardziej zewnętrznych powłok, następuje emisja promieniowania X i emitowane są elektrony Augera. Zmiana Z w wyniku rozpadu β powoduje, Ŝe atom znajduje się w niezwykłym otoczeniu np. β 14 CH 3 CH 3 ( 14 H 3 CH 3 ) 14 H 3 + CH H 3+ + CH 3 W ten sposób otrzymano tlenowe połączenia Xe 19 JO 4 β 19 XeO 4
22 Efekt Szilarda-Chalmersa Reakcje atomów gorących pozwalają otrzymać beznośnikowe izotopy. Po naświetleniu neutronami izotop w wyniku reakcji odrzutu lub wzbudzenia atomu znajduje się w innej formie niŝ nuklid macierzysty i moŝe być wydzielony metodami chemicznymi. p.: 17 JO 3 (n, γ) 18 J
23 Wpływ wiązania chemicznego na rozpad jąder Wpływ otoczenia elektronowego najłatwiej zauwaŝyć w przypadku wychwytu elektronowego lekkich atomów. Dla 7 Be. 7 e Be Gęstość elektronów 1s w jądrze zmienia się w zaleŝności od otoczenia. Zmiana t 1/ /t 1/ x10 3 dla róŝnych związków 7 Be w porównaniu z 7 Be metalicznym 7 Be + - 1s. Li związek BeS Be(H O) 4 + Be(metal) t 1/ /t 1/ x ,3 +,3 0 BeO -1,4 BeF -1,0 BeBr -16,
24 Bardzo duŝy efekt obserwowano dla konwersji wewnętrznej 35m U (t 1/ =6,1 min). Poziom wzbudzenia jądra 35m U jest jedynie o 68 ev wyŝszy niŝ pozom podstawowy. Mogą więc ulegać konwersji jedynie elektrony o małej energii wiązania - z orbitali 6s, 7s, 6p, 5f i 6d. Energia tych elektronów będących walencyjnymi silnie zaleŝy od otoczenia chemicznego Związek 35m UC 35m UO t 1/ (min.) 6, 4,7
25 Efekt Mössbauera Spektroskopia Mossbauera opiera się na zjawisku rezonansowej absorpcji kwantu gamma przez jądra atomowe. p. 57 Fe ma stan wzbudzony wyŝszy o 14,4 kev od podstawowego i emituje kwanty γ o tej energii. Kwanty γ o tej samej energii są pochłaniane przez inne atomy Fe w stanie podstawowym. Aby mógł zajść rezonans atom 57m Fe źródła nie moŝe ulegać odrzutowi gdyŝ zmniejszyła by się energia γ.
26
27 W krystalicznym ciele stałym atom Fe jest związany i nie ulega odrzutowi. Otoczenie elektronowe jądra moŝe wpływać na poziom rezonansowy. JeŜeli otoczenie chemiczne atomu źródła i adsorbera jest róŝne nie moŝe zajść rezonans. PoniewaŜ wpływ otoczenia elektronowego na poziomy rezonansowe jądra jest bardzo mały, do zajścia rezonansu wystarczy powoli przesuwaćźródło względem adsorbera aby dodać energię kinetyczną fotonu ( E γ ). Szybkość przesuwu źródła jest tzw przesunięciem izomerowym - δ. Wielkość d zaleŝy od otocznia elektronowego stopnia utlenienia, ligandowów etc. uklidy mogące byćźródłami w spektroskopii Mossbauera muszą mieć czasy Ŝycia stanu wzbudzonego rzędu nanosekund. Energia fotonu nie moŝe przekraczać 100eV. ajpopularniejszym Ŝródłem jest 57 Co rozpadający się do 57m Fe (t 1/ =98ns). Adsorberem jest naturalne Ŝelazo o zawartości,17% 57 Fe.
28 Spektroskopia Mossbauera związków p na roŝnych stopniach utlenienia. Związek Stopień utlenienia p δ mm s -1 Li 5 po K 3 po F po (OH) pf pf
29 Izotopy Mossbauerowskie Latwe do badania trudniejsze b. trudne
Podstawowe własności jąder atomowych
 Podstawowe własności jąder atomowych 1. Ilość protonów i neutronów Z, N 2. Masa jądra M j = M p + M n - B 2 2 Q ( M c ) ( M c ) 3. Energia rozpadu p 0 k 0 Rozpad zachodzi jeżeli Q > 0, ta nadwyżka energii
Podstawowe własności jąder atomowych 1. Ilość protonów i neutronów Z, N 2. Masa jądra M j = M p + M n - B 2 2 Q ( M c ) ( M c ) 3. Energia rozpadu p 0 k 0 Rozpad zachodzi jeżeli Q > 0, ta nadwyżka energii
Zadanie 3. (2 pkt) Uzupełnij zapis, podając liczbę masową i atomową produktu przemiany oraz jego symbol chemiczny. Th... + α
 Zadanie: 1 (2 pkt) Określ liczbę atomową pierwiastka powstającego w wyniku rozpadów promieniotwórczych izotopu radu 223 88Ra, w czasie których emitowane są 4 cząstki α i 2 cząstki β. Podaj symbol tego
Zadanie: 1 (2 pkt) Określ liczbę atomową pierwiastka powstającego w wyniku rozpadów promieniotwórczych izotopu radu 223 88Ra, w czasie których emitowane są 4 cząstki α i 2 cząstki β. Podaj symbol tego
Promieniotwórczość naturalna. Jądro atomu i jego budowa.
 Promieniotwórczość naturalna. Jądro atomu i jego budowa. Doświadczenie Rutherforda (1909). Polegało na bombardowaniu złotej folii strumieniem cząstek alfa (jąder helu) i obserwacji odchyleń ich toru ruchu.
Promieniotwórczość naturalna. Jądro atomu i jego budowa. Doświadczenie Rutherforda (1909). Polegało na bombardowaniu złotej folii strumieniem cząstek alfa (jąder helu) i obserwacji odchyleń ich toru ruchu.
Odkrycie jądra atomowego - doświadczenie Rutherforda 1909 r.
 Odkrycie jądra atomowego - doświadczenie Rutherforda 1909 r. 1 Budowa jądra atomowego Liczba atomowa =Z+N Liczba masowa Liczba neutronów Izotopy Jądra o jednakowej liczbie protonów, różniące się liczbą
Odkrycie jądra atomowego - doświadczenie Rutherforda 1909 r. 1 Budowa jądra atomowego Liczba atomowa =Z+N Liczba masowa Liczba neutronów Izotopy Jądra o jednakowej liczbie protonów, różniące się liczbą
Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość Monika Gałkiewicz Zad. 1 () Przedstaw pełną konfigurację elektronową atomu pierwiastka
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość Monika Gałkiewicz Zad. 1 () Przedstaw pełną konfigurację elektronową atomu pierwiastka
Promieniowanie jonizujące
 Promieniowanie jonizujące Wykład II Promieniotwórczość Fizyka MU, semestr 2 Uniwersytet Rzeszowski, 8 marca 2017 Wykład II Promieniotwórczość Promieniowanie jonizujące 1 / 22 Jądra pomieniotwórcze Nuklidy
Promieniowanie jonizujące Wykład II Promieniotwórczość Fizyka MU, semestr 2 Uniwersytet Rzeszowski, 8 marca 2017 Wykład II Promieniotwórczość Promieniowanie jonizujące 1 / 22 Jądra pomieniotwórcze Nuklidy
Promieniowanie jonizujące
 Promieniowanie jonizujące Wykład II Krzysztof Golec-Biernat Promieniotwórczość Uniwersytet Rzeszowski, 18 października 2017 Wykład II Krzysztof Golec-Biernat Promieniowanie jonizujące 1 / 23 Jądra pomieniotwórcze
Promieniowanie jonizujące Wykład II Krzysztof Golec-Biernat Promieniotwórczość Uniwersytet Rzeszowski, 18 października 2017 Wykład II Krzysztof Golec-Biernat Promieniowanie jonizujące 1 / 23 Jądra pomieniotwórcze
pobrano z serwisu Fizyka Dla Każdego - - zadania z fizyki, wzory fizyczne, fizyka matura
 14. Fizyka jądrowa zadania z arkusza I 14.10 14.1 14.2 14.11 14.3 14.12 14.4 14.5 14.6 14.13 14.7 14.8 14.14 14.9 14. Fizyka jądrowa - 1 - 14.15 14.23 14.16 14.17 14.24 14.18 14.25 14.19 14.26 14.27 14.20
14. Fizyka jądrowa zadania z arkusza I 14.10 14.1 14.2 14.11 14.3 14.12 14.4 14.5 14.6 14.13 14.7 14.8 14.14 14.9 14. Fizyka jądrowa - 1 - 14.15 14.23 14.16 14.17 14.24 14.18 14.25 14.19 14.26 14.27 14.20
Fizyka współczesna. Jądro atomowe podstawy Odkrycie jądra atomowego: 1911, Rutherford Rozpraszanie cząstek alfa na cienkich warstwach metalu
 Odkrycie jądra atomowego: 9, Rutherford Rozpraszanie cząstek alfa na cienkich warstwach metalu Tor ruchu rozproszonych cząstek (fakt, że część cząstek rozprasza się pod bardzo dużym kątem) wskazuje na
Odkrycie jądra atomowego: 9, Rutherford Rozpraszanie cząstek alfa na cienkich warstwach metalu Tor ruchu rozproszonych cząstek (fakt, że część cząstek rozprasza się pod bardzo dużym kątem) wskazuje na
Budowa atomu. Izotopy
 Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
1. JĄDROWA BUDOWA ATOMU. A1 - POZIOM PODSTAWOWY.
 . JĄDROWA BUDOWA ATOMU. A - POIOM PODSTAWOWY. Na początek - przeczytaj uważnie tekst i wykonaj zawarte pod nim polecenia.. Dwie reakcje jądrowe zachodzące w górnych warstwach atmosfery: N + n C + p N +
. JĄDROWA BUDOWA ATOMU. A - POIOM PODSTAWOWY. Na początek - przeczytaj uważnie tekst i wykonaj zawarte pod nim polecenia.. Dwie reakcje jądrowe zachodzące w górnych warstwach atmosfery: N + n C + p N +
Rozpady promieniotwórcze
 Rozpady promieniotwórcze Przez rozpady promieniotwórcze rozumie się spontaniczne procesy, w których niestabilne jądra atomowe przekształcają się w inne jądra atomowe i emitują specyficzne promieniowanie
Rozpady promieniotwórcze Przez rozpady promieniotwórcze rozumie się spontaniczne procesy, w których niestabilne jądra atomowe przekształcają się w inne jądra atomowe i emitują specyficzne promieniowanie
A - liczba nukleonów w jądrze (protonów i neutronów razem) Z liczba protonów A-Z liczba neutronów
 Włodzimierz Wolczyński 40 FIZYKA JĄDROWA A - liczba nukleonów w jądrze (protonów i neutronów razem) Z liczba protonów A-Z liczba neutronów O nazwie pierwiastka decyduje liczba porządkowa Z, a więc ilość
Włodzimierz Wolczyński 40 FIZYKA JĄDROWA A - liczba nukleonów w jądrze (protonów i neutronów razem) Z liczba protonów A-Z liczba neutronów O nazwie pierwiastka decyduje liczba porządkowa Z, a więc ilość
OCHRONA RADIOLOGICZNA PACJENTA. Promieniotwórczość
 OCHRONA RADIOLOGICZNA PACJENTA Promieniotwórczość PROMIENIOTWÓRCZOŚĆ (radioaktywność) zjawisko samorzutnego rozpadu jąder atomowych niektórych izotopów, któremu towarzyszy wysyłanie promieniowania α, β,
OCHRONA RADIOLOGICZNA PACJENTA Promieniotwórczość PROMIENIOTWÓRCZOŚĆ (radioaktywność) zjawisko samorzutnego rozpadu jąder atomowych niektórych izotopów, któremu towarzyszy wysyłanie promieniowania α, β,
Spis treści. Trwałość jądra atomowego. Okres połowicznego rozpadu
 Spis treści 1 Trwałość jądra atomowego 2 Okres połowicznego rozpadu 3 Typy przemian jądrowych 4 Reguła przesunięć Fajansa-Soddy ego 5 Szeregi promieniotwórcze 6 Typy reakcji jądrowych 7 Przykłady prostych
Spis treści 1 Trwałość jądra atomowego 2 Okres połowicznego rozpadu 3 Typy przemian jądrowych 4 Reguła przesunięć Fajansa-Soddy ego 5 Szeregi promieniotwórcze 6 Typy reakcji jądrowych 7 Przykłady prostych
Reakcje rozpadu jądra atomowego
 Reakcje rozpadu jądra atomowego O P R A C O W A N I E : P A W E Ł Z A B O R O W S K I K O N S U L T A C J A M E R Y T O R Y C Z N A : M A Ł G O R Z A T A L E C H Trwałość izotopów Czynnikiem decydującym
Reakcje rozpadu jądra atomowego O P R A C O W A N I E : P A W E Ł Z A B O R O W S K I K O N S U L T A C J A M E R Y T O R Y C Z N A : M A Ł G O R Z A T A L E C H Trwałość izotopów Czynnikiem decydującym
I ,11-1, 1, C, , 1, C
 Materiał powtórzeniowy - budowa atomu - cząstki elementarne, izotopy, promieniotwórczość naturalna, okres półtrwania, średnia masa atomowa z przykładowymi zadaniami I. Cząstki elementarne atomu 1. Elektrony
Materiał powtórzeniowy - budowa atomu - cząstki elementarne, izotopy, promieniotwórczość naturalna, okres półtrwania, średnia masa atomowa z przykładowymi zadaniami I. Cząstki elementarne atomu 1. Elektrony
Elementy Fizyki Jądrowej. Wykład 3 Promieniotwórczość naturalna
 Elementy Fizyki Jądrowej Wykład 3 Promieniotwórczość naturalna laboratorium Curie troje noblistów 1903 PC, MSC 1911 MSC 1935 FJ, IJC Przemiany jądrowe He X X 4 2 4 2 A Z A Z e _ 1 e X X A Z A Z e 1 e
Elementy Fizyki Jądrowej Wykład 3 Promieniotwórczość naturalna laboratorium Curie troje noblistów 1903 PC, MSC 1911 MSC 1935 FJ, IJC Przemiany jądrowe He X X 4 2 4 2 A Z A Z e _ 1 e X X A Z A Z e 1 e
W2. Struktura jądra atomowego
 W2. Struktura jądra atomowego Doświadczenie Rutherforda - badanie odchylania wiązki cząstek alfa w cienkiej folii metalicznej Hans Geiger, Ernest Marsden, Ernest Rutherford ( 1911r.) detektor pierwiastek
W2. Struktura jądra atomowego Doświadczenie Rutherforda - badanie odchylania wiązki cząstek alfa w cienkiej folii metalicznej Hans Geiger, Ernest Marsden, Ernest Rutherford ( 1911r.) detektor pierwiastek
Opracowała: mgr Agata Wiśniewska PRZYKŁADOWE SPRAWDZIANY WIADOMOŚCI l UMIEJĘTNOŚCI Współczesny model budowy atomu (wersja A)
 PRZYKŁADOW SPRAWDZIANY WIADOMOŚCI l UMIJĘTNOŚCI Współczesny model budowy atomu (wersja A) 1. nuklid A. Zbiór atomów o tej samej wartości liczby atomowej. B. Nazwa elektrycznie obojętnej cząstki składowej
PRZYKŁADOW SPRAWDZIANY WIADOMOŚCI l UMIJĘTNOŚCI Współczesny model budowy atomu (wersja A) 1. nuklid A. Zbiór atomów o tej samej wartości liczby atomowej. B. Nazwa elektrycznie obojętnej cząstki składowej
Autorzy: Zbigniew Kąkol, Piotr Morawski
 Rodzaje rozpadów jądrowych Autorzy: Zbigniew Kąkol, Piotr Morawski Rozpady jądrowe zachodzą zawsze (prędzej czy później) jeśli jądro o pewnej liczbie nukleonów znajdzie się w stanie energetycznym, nie
Rodzaje rozpadów jądrowych Autorzy: Zbigniew Kąkol, Piotr Morawski Rozpady jądrowe zachodzą zawsze (prędzej czy później) jeśli jądro o pewnej liczbie nukleonów znajdzie się w stanie energetycznym, nie
Foton, kwant światła. w klasycznym opisie świata, światło jest falą sinusoidalną o częstości n równej: c gdzie: c prędkość światła, długość fali św.
 Foton, kwant światła Wielkość fizyczna jest skwantowana jeśli istnieje w pewnych minimalnych (elementarnych) porcjach lub ich całkowitych wielokrotnościach w klasycznym opisie świata, światło jest falą
Foton, kwant światła Wielkość fizyczna jest skwantowana jeśli istnieje w pewnych minimalnych (elementarnych) porcjach lub ich całkowitych wielokrotnościach w klasycznym opisie świata, światło jest falą
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 OZNACZANIE OKRESU PÓŁROZPADU DLA NUKLIDU 40 K WSTĘP Naturalny potas stanowi mieszaninę trzech nuklidów: 39 K (93.08%), 40 K (0.012%) oraz 41 K (6.91%). Nuklid 40 K jest izotopem promieniotwórczym, którego
OZNACZANIE OKRESU PÓŁROZPADU DLA NUKLIDU 40 K WSTĘP Naturalny potas stanowi mieszaninę trzech nuklidów: 39 K (93.08%), 40 K (0.012%) oraz 41 K (6.91%). Nuklid 40 K jest izotopem promieniotwórczym, którego
Elementy Fizyki Jądrowej. Wykład 8 Rozszczepienie jąder i fizyka neutronów
 Elementy Fizyki Jądrowej Wykład 8 Rozszczepienie jąder i fizyka neutronów Rozszczepienie lata 30 XX w. poszukiwanie nowych nuklidów n + 238 92U 239 92U + reakcja przez jądro złożone 239 92 U 239 93Np +
Elementy Fizyki Jądrowej Wykład 8 Rozszczepienie jąder i fizyka neutronów Rozszczepienie lata 30 XX w. poszukiwanie nowych nuklidów n + 238 92U 239 92U + reakcja przez jądro złożone 239 92 U 239 93Np +
Promieniowanie jonizujące
 Promieniowanie jonizujące Wykład III Krzysztof Golec-Biernat Reakcje jądrowe Uniwersytet Rzeszowski, 8 listopada 2017 Wykład III Krzysztof Golec-Biernat Promieniowanie jonizujące 1 / 12 Energia wiązania
Promieniowanie jonizujące Wykład III Krzysztof Golec-Biernat Reakcje jądrowe Uniwersytet Rzeszowski, 8 listopada 2017 Wykład III Krzysztof Golec-Biernat Promieniowanie jonizujące 1 / 12 Energia wiązania
Promieniowanie jonizujące i metody radioizotopowe. dr Marcin Lipowczan
 Promieniowanie jonizujące i metody radioizotopowe dr Marcin Lipowczan Budowa atomu 897 Thomson, 0 0 m, kula dodatnio naładowana ładunki ujemne 9 Rutherford, rozpraszanie cząstek alfa na folię metalową,
Promieniowanie jonizujące i metody radioizotopowe dr Marcin Lipowczan Budowa atomu 897 Thomson, 0 0 m, kula dodatnio naładowana ładunki ujemne 9 Rutherford, rozpraszanie cząstek alfa na folię metalową,
Poziom nieco zaawansowany Wykład 2
 W2Z Poziom nieco zaawansowany Wykład 2 Witold Bekas SGGW Promieniotwórczość Henri Becquerel - 1896, Paryż, Sorbona badania nad solami uranu, odkrycie promieniotwórczości Maria Skłodowska-Curie, Piotr Curie
W2Z Poziom nieco zaawansowany Wykład 2 Witold Bekas SGGW Promieniotwórczość Henri Becquerel - 1896, Paryż, Sorbona badania nad solami uranu, odkrycie promieniotwórczości Maria Skłodowska-Curie, Piotr Curie
WYZNACZANIE PROMIENIOWANIA RADONU Instrukcja dla uczniów szkół ponadpodstawowych
 WYZNACZANIE PROMIENIOWANIA RADONU Instrukcja dla uczniów szkół ponadpodstawowych WSTĘP I. ROZPAD PROMIENIOTWÓRCZY I RODZAJE PROMIENIOWANIA JĄDROWEGO Rozpadem promieniotwórczym (przemianą promieniotwórczą)
WYZNACZANIE PROMIENIOWANIA RADONU Instrukcja dla uczniów szkół ponadpodstawowych WSTĘP I. ROZPAD PROMIENIOTWÓRCZY I RODZAJE PROMIENIOWANIA JĄDROWEGO Rozpadem promieniotwórczym (przemianą promieniotwórczą)
Anna Grych Test z budowy atomu i wiązań chemicznych
 Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Oddziaływanie promieniowania jonizującego z materią
 Oddziaływanie promieniowania jonizującego z materią Plan Promieniowanie ( particle radiation ) Źródła (szybkich) elektronów Ciężkie cząstki naładowane Promieniowanie elektromagnetyczne (fotony) Neutrony
Oddziaływanie promieniowania jonizującego z materią Plan Promieniowanie ( particle radiation ) Źródła (szybkich) elektronów Ciężkie cząstki naładowane Promieniowanie elektromagnetyczne (fotony) Neutrony
r. akad. 2012/2013 Wykład IX-X Podstawy Procesów i Konstrukcji Inżynierskich Fizyka jądrowa Zakład Biofizyki 1
 r. akad. 2012/2013 Wykład IX-X Podstawy Procesów i Konstrukcji Inżynierskich Fizyka jądrowa Zakład Biofizyki 1 Budowa jądra atomowego każde jądro atomowe składa się z dwóch rodzajów nukleonów: protonów
r. akad. 2012/2013 Wykład IX-X Podstawy Procesów i Konstrukcji Inżynierskich Fizyka jądrowa Zakład Biofizyki 1 Budowa jądra atomowego każde jądro atomowe składa się z dwóch rodzajów nukleonów: protonów
CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna. Model atomu Bohra
 CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna Model atomu Bohra SPIS TREŚCI: 1. Modele budowy atomu Thomsona, Rutherforda i Bohra 2. Budowa atomu 3. Liczba atomowa a liczba
CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna Model atomu Bohra SPIS TREŚCI: 1. Modele budowy atomu Thomsona, Rutherforda i Bohra 2. Budowa atomu 3. Liczba atomowa a liczba
Oddziaływanie cząstek z materią
 Oddziaływanie cząstek z materią Trzy główne typy mechanizmów reprezentowane przez Ciężkie cząstki naładowane (cięższe od elektronów) Elektrony Kwanty gamma Ciężkie cząstki naładowane (miony, p, cząstki
Oddziaływanie cząstek z materią Trzy główne typy mechanizmów reprezentowane przez Ciężkie cząstki naładowane (cięższe od elektronów) Elektrony Kwanty gamma Ciężkie cząstki naładowane (miony, p, cząstki
SYMULACJA GAMMA KAMERY MATERIAŁ DLA STUDENTÓW. Szacowanie pochłoniętej energii promieniowania jonizującego
 SYMULACJA GAMMA KAMERY MATERIAŁ DLA STUDENTÓW Szacowanie pochłoniętej energii promieniowania jonizującego W celu analizy narażenia na promieniowanie osoby, której podano radiofarmaceutyk, posłużymy się
SYMULACJA GAMMA KAMERY MATERIAŁ DLA STUDENTÓW Szacowanie pochłoniętej energii promieniowania jonizującego W celu analizy narażenia na promieniowanie osoby, której podano radiofarmaceutyk, posłużymy się
doświadczenie Rutheforda Jądro atomowe składa się z nuklonów: neutronów (obojętnych elektrycznie) i protonów (posiadających ładunek dodatni +e)
 1 doświadczenie Rutheforda Jądro atomowe składa się z nuklonów: neutronów (obojętnych elektrycznie) i protonów (posiadających ładunek dodatni +e) Ilość protonów w jądrze określa liczba atomowa Z Ilość
1 doświadczenie Rutheforda Jądro atomowe składa się z nuklonów: neutronów (obojętnych elektrycznie) i protonów (posiadających ładunek dodatni +e) Ilość protonów w jądrze określa liczba atomowa Z Ilość
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Fizyka promieniowania jonizującego. Zygmunt Szefliński
 Fizyka promieniowania jonizującego Zygmunt Szefliński 1 Wykład 3 Ogólne własności jąder atomowych (masy ładunki, izotopy, izobary, izotony izomery). 2 Liczba atomowa i masowa Liczba nukleonów (protonów
Fizyka promieniowania jonizującego Zygmunt Szefliński 1 Wykład 3 Ogólne własności jąder atomowych (masy ładunki, izotopy, izobary, izotony izomery). 2 Liczba atomowa i masowa Liczba nukleonów (protonów
NEUTRONOWA ANALIZA AKTYWACYJNA ANALITYKA W KONTROLI JAKOŚCI PODSTAWOWE INFORMACJE O REAKCJACH JĄDROWYCH - NEUTRONOWA ANALIZA AKTYWACYJNA
 ANALITYKA W KONTROLI JAKOŚCI WYKŁAD 3 NEUTRONOWA ANALIZA AKTYWACYJNA - PODSTAWOWE INFORMACJE O REAKCJACH JĄDROWYCH - NEUTRONOWA ANALIZA AKTYWACYJNA REAKCJE JĄDROWE Rozpad promieniotwórczy: A B + y + ΔE
ANALITYKA W KONTROLI JAKOŚCI WYKŁAD 3 NEUTRONOWA ANALIZA AKTYWACYJNA - PODSTAWOWE INFORMACJE O REAKCJACH JĄDROWYCH - NEUTRONOWA ANALIZA AKTYWACYJNA REAKCJE JĄDROWE Rozpad promieniotwórczy: A B + y + ΔE
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
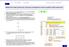 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
Fizyka 3. Konsultacje: p. 329, Mechatronika
 Fizyka 3 Konsultacje: p. 329, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 2 sprawdziany (10 pkt każdy) lub egzamin (2 części po 10 punktów) 10.1 12 3.0 12.1 14 3.5 14.1 16 4.0 16.1 18 4.5 18.1 20 5.0
Fizyka 3 Konsultacje: p. 329, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 2 sprawdziany (10 pkt każdy) lub egzamin (2 części po 10 punktów) 10.1 12 3.0 12.1 14 3.5 14.1 16 4.0 16.1 18 4.5 18.1 20 5.0
III Podkarpacki Konkurs Chemiczny 2010/2011. ETAP I r. Godz Zadanie 1
 III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
Zadanie 2. (1 pkt) Jądro izotopu U zawiera A. 235 neutronów. B. 327 nukleonów. C. 143 neutrony. D. 92 nukleony
 Zadanie 1. (1 pkt) W jednym z naturalnych szeregów promieniotwórczych występują m.in. trzy izotopy polonu, których okresy półtrwania podano w nawiasach: Po-218 (T 1/2 = 3,1minuty), Po-214 (T 1/2 = 0,0016
Zadanie 1. (1 pkt) W jednym z naturalnych szeregów promieniotwórczych występują m.in. trzy izotopy polonu, których okresy półtrwania podano w nawiasach: Po-218 (T 1/2 = 3,1minuty), Po-214 (T 1/2 = 0,0016
Rozpady promieniotwórcze
 Rozpady promieniotwórcze Przez rozpady promieniotwórcze rozumie się spontaniczne procesy, w których niestabilne jądra atomowe przekształcają się w inne jądra atomowe i emitują specyficzne promieniowanie
Rozpady promieniotwórcze Przez rozpady promieniotwórcze rozumie się spontaniczne procesy, w których niestabilne jądra atomowe przekształcają się w inne jądra atomowe i emitują specyficzne promieniowanie
Szkolny konkurs chemiczny Grupa B. Czas pracy 80 minut
 Szkolny konkurs chemiczny Grupa B Czas pracy 80 minut Piła 1 czerwca 2017 1 Zadanie 1. (0 3) Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie: elektrony rozmieszczone
Szkolny konkurs chemiczny Grupa B Czas pracy 80 minut Piła 1 czerwca 2017 1 Zadanie 1. (0 3) Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie: elektrony rozmieszczone
E 2 E = 2. Zjawisko Mössbauera. Spoczywające jądro doznaje przejścia e-m z emisją fotonu γ. Zastosujmy zasadę zachowania energii i pędu:
 Zjawisko Mössbauera Spoczywające jądro doznaje przejścia e-m z emisją fotonu γ. Zastosujmy zasadę zachowania energii i pędu: E = E + E + T = p + p i f γ R 0 γ R E = E E γ T = E T Energia fotonu: jest więc
Zjawisko Mössbauera Spoczywające jądro doznaje przejścia e-m z emisją fotonu γ. Zastosujmy zasadę zachowania energii i pędu: E = E + E + T = p + p i f γ R 0 γ R E = E E γ T = E T Energia fotonu: jest więc
Fizyka jądrowa. Podstawowe pojęcia. Izotopy. budowa jądra atomowego przemiany promieniotwórcze reakcje jądrowe. jądra atomowe (nuklidy) dzielimy na:
 Fizyka jądrowa budowa jądra atomowego przemiany promieniotwórcze reakcje jądrowe Podstawowe pojęcia jądra atomowe (nuklidy) dzielimy na: trwałe (stabilne) nietrwałe (promieniotwórcze) jądro składa się
Fizyka jądrowa budowa jądra atomowego przemiany promieniotwórcze reakcje jądrowe Podstawowe pojęcia jądra atomowe (nuklidy) dzielimy na: trwałe (stabilne) nietrwałe (promieniotwórcze) jądro składa się
Wykłady z Geochemii Ogólnej
 Wykłady z Geochemii Ogólnej III rok WGGiOŚ AGH 2010/11 dr hab. inż. Maciej Manecki A-0 p.24 www.geol.agh.edu.pl/~mmanecki ELEMENTY KOSMOCHEMII Nasza wiedza o składzie materii Wszechświata pochodzi z dwóch
Wykłady z Geochemii Ogólnej III rok WGGiOŚ AGH 2010/11 dr hab. inż. Maciej Manecki A-0 p.24 www.geol.agh.edu.pl/~mmanecki ELEMENTY KOSMOCHEMII Nasza wiedza o składzie materii Wszechświata pochodzi z dwóch
autor: Włodzimierz Wolczyński rozwiązywał (a)... ARKUSIK 40 FIZYKA JĄDROWA
 autor: Włodzimierz Wolczyński rozwiązywał (a)... ARKUSIK 40 FIZYKA JĄDROWA Rozwiązanie zadań należy zapisać w wyznaczonych miejscach pod treścią zadania TEST JEDNOKROTNEGO WYBORU UWAGA: Tekst poniżej,
autor: Włodzimierz Wolczyński rozwiązywał (a)... ARKUSIK 40 FIZYKA JĄDROWA Rozwiązanie zadań należy zapisać w wyznaczonych miejscach pod treścią zadania TEST JEDNOKROTNEGO WYBORU UWAGA: Tekst poniżej,
Prawo rozpadu promieniotwórczego. Metoda datowania izotopowego.
 Prawo rozpadu promieniotwórczego. Metoda datowania izotopowego. Prawo rozpadu promieniotwórczego. Rodzaje promieniowania PROMIENIOWANIE ŁADUNEK ELEKTRYCZNY MASA CECHY CHARAKTERYSTYCZNE alfa +2e 4u beta
Prawo rozpadu promieniotwórczego. Metoda datowania izotopowego. Prawo rozpadu promieniotwórczego. Rodzaje promieniowania PROMIENIOWANIE ŁADUNEK ELEKTRYCZNY MASA CECHY CHARAKTERYSTYCZNE alfa +2e 4u beta
Wyznaczanie czasu połowicznego zaniku izotopu promieniotwórczego
 Ćwiczenie 8 Wyznaczanie czasu połowicznego zaniku izotopu promieniotwórczego 8.. Zasada ćwiczenia Celem ćwiczenia jest wyznaczenie czasu połowicznego zaniku izotopu promieniotwórczego Ba-37m (izotop wtórny)
Ćwiczenie 8 Wyznaczanie czasu połowicznego zaniku izotopu promieniotwórczego 8.. Zasada ćwiczenia Celem ćwiczenia jest wyznaczenie czasu połowicznego zaniku izotopu promieniotwórczego Ba-37m (izotop wtórny)
Rozpad alfa. albo od stanów wzbudzonych (np. po rozpadzie beta) są to tzw. długozasięgowe cząstki alfa
 Rozpad alfa Samorzutny rozpad jądra (Z,A) na cząstkę α i jądro (Z-2,A-4) tj. rozpad 2-ciałowy, stąd Widmo cząstek α jest dyskretne bo przejścia zachodzą między określonymi stanami jądra początkowego i
Rozpad alfa Samorzutny rozpad jądra (Z,A) na cząstkę α i jądro (Z-2,A-4) tj. rozpad 2-ciałowy, stąd Widmo cząstek α jest dyskretne bo przejścia zachodzą między określonymi stanami jądra początkowego i
Energetyka Jądrowa. Wykład 3 14 marca Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów
 Energetyka Jądrowa Wykład 3 14 marca 2017 Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów szef@fuw.edu.pl http://www.fuw.edu.pl/~szef/ Henri Becquerel 1896 Promieniotwórczość 14.III.2017 EJ
Energetyka Jądrowa Wykład 3 14 marca 2017 Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów szef@fuw.edu.pl http://www.fuw.edu.pl/~szef/ Henri Becquerel 1896 Promieniotwórczość 14.III.2017 EJ
Promieniowanie jonizujące
 Promieniowanie jonizujące Wykład IV Krzysztof Golec-Biernat Promieniotwórczość naturalna Uniwersytet Rzeszowski, 22 listopada 2017 Wykład IV Krzysztof Golec-Biernat Promieniowanie jonizujące 1 / 21 Reakcja
Promieniowanie jonizujące Wykład IV Krzysztof Golec-Biernat Promieniotwórczość naturalna Uniwersytet Rzeszowski, 22 listopada 2017 Wykład IV Krzysztof Golec-Biernat Promieniowanie jonizujące 1 / 21 Reakcja
Rozpad gamma. Przez konwersję wewnętrzną (emisję wirtualnego kwantu gamma, który przekazuje swą energię elektronom z powłoki atomowej)
 Rozpad gamma Deekscytacja jądra atomowego (przejście ze stanu wzbudzonego o energii do niższego stanu o energii ) może zachodzić dzięki oddziaływaniu elektromagnetycznemu przez tzw. rozpad gamma Przejście
Rozpad gamma Deekscytacja jądra atomowego (przejście ze stanu wzbudzonego o energii do niższego stanu o energii ) może zachodzić dzięki oddziaływaniu elektromagnetycznemu przez tzw. rozpad gamma Przejście
Słowniczek pojęć fizyki jądrowej
 Słowniczek pojęć fizyki jądrowej atom - najmniejsza ilość pierwiastka jaka może istnieć. Atomy składają się z małego, gęstego jądra, zbudowanego z protonów i neutronów (nazywanych inaczej nukleonami),
Słowniczek pojęć fizyki jądrowej atom - najmniejsza ilość pierwiastka jaka może istnieć. Atomy składają się z małego, gęstego jądra, zbudowanego z protonów i neutronów (nazywanych inaczej nukleonami),
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
Badanie absorpcji promieniowania γ
 Badanie absorpcji promieniowania γ 29.1. Zasada ćwiczenia W ćwiczeniu badana jest zależność natężenia wiązki osłabienie wiązki promieniowania γ po przejściu przez warstwę materiału absorbującego w funkcji
Badanie absorpcji promieniowania γ 29.1. Zasada ćwiczenia W ćwiczeniu badana jest zależność natężenia wiązki osłabienie wiązki promieniowania γ po przejściu przez warstwę materiału absorbującego w funkcji
Wyznaczanie bezwzględnej aktywności źródła 60 Co. Tomasz Winiarski
 Wyznaczanie bezwzględnej aktywności źródła 60 Co metoda koincydencyjna. Tomasz Winiarski 24 kwietnia 2001 WSTEP TEORETYCZNY Rozpad promieniotwórczy i czas połowicznego zaniku. Rozpad promieniotwórczy polega
Wyznaczanie bezwzględnej aktywności źródła 60 Co metoda koincydencyjna. Tomasz Winiarski 24 kwietnia 2001 WSTEP TEORETYCZNY Rozpad promieniotwórczy i czas połowicznego zaniku. Rozpad promieniotwórczy polega
Budowa atomu Poziom: podstawowy Zadanie 1. (1 pkt.)
 Budowa atomu Poziom: podstawowy Zadanie 1. (1 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Atomy pewnego pierwiastka w stanie podstawowym mają następującą konfigurację elektronów walencyjnych: 2s 2 2p 3 (
Budowa atomu Poziom: podstawowy Zadanie 1. (1 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Atomy pewnego pierwiastka w stanie podstawowym mają następującą konfigurację elektronów walencyjnych: 2s 2 2p 3 (
Wykłady z Chemii Ogólnej i Biochemii. Dr Sławomir Lis
 Wykłady z Chemii Ogólnej i Biochemii Dr Sławomir Lis Chemia, jako nauka zajmuje się otrzymywaniem i wszechstronnym badaniem własności, struktury oraz reakcji chemicznych pierwiastków i ich połączeń. Chemia
Wykłady z Chemii Ogólnej i Biochemii Dr Sławomir Lis Chemia, jako nauka zajmuje się otrzymywaniem i wszechstronnym badaniem własności, struktury oraz reakcji chemicznych pierwiastków i ich połączeń. Chemia
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Jądro atomowe Wielkości charakteryzujące jądro atomowe
 Fizyka jądrowa Jądro atomowe Wielkości charakteryzujące jądro atomowe A - liczba masowa Z - liczba porządkowa pierwiastka w układzie okresowym N - liczba neutronów Oznaczenie jądra atomowego : A X lub
Fizyka jądrowa Jądro atomowe Wielkości charakteryzujące jądro atomowe A - liczba masowa Z - liczba porządkowa pierwiastka w układzie okresowym N - liczba neutronów Oznaczenie jądra atomowego : A X lub
PRACOWNIA CHEMII. Wygaszanie fluorescencji (Fiz4)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
Fizyka 2. Janusz Andrzejewski
 Fizyka 2 wykład 15 Janusz Andrzejewski Janusz Andrzejewski 2 Egzamin z fizyki I termin 31 stycznia2014 piątek II termin 13 luty2014 czwartek Oba egzaminy odbywać się będą: sala 301 budynek D1 Janusz Andrzejewski
Fizyka 2 wykład 15 Janusz Andrzejewski Janusz Andrzejewski 2 Egzamin z fizyki I termin 31 stycznia2014 piątek II termin 13 luty2014 czwartek Oba egzaminy odbywać się będą: sala 301 budynek D1 Janusz Andrzejewski
Ćwiczenie 3. POMIAR ZASIĘGU CZĄSTEK α W POWIETRZU Rozpad α
 39 40 Ćwiczenie 3 POMIAR ZASIĘGU CZĄSTEK α W POWIETRZU W ćwiczeniu dokonuje się pomiaru zasięgu w powietrzu cząstek α emitowanych przez źródło promieniotwórcze. Pomiary wykonuje się za pomocą komory jonizacyjnej
39 40 Ćwiczenie 3 POMIAR ZASIĘGU CZĄSTEK α W POWIETRZU W ćwiczeniu dokonuje się pomiaru zasięgu w powietrzu cząstek α emitowanych przez źródło promieniotwórcze. Pomiary wykonuje się za pomocą komory jonizacyjnej
Reakcje jądrowe dr inż. Romuald Kędzierski
 Reakcje jądrowe dr inż. Romuald Kędzierski Wybuch bomby Ivy Mike (fot. National Nuclear Security Administration/Nevada Site Office, domena publiczna) Przemiany jądrowe 1. Spontaniczne (niewymuszone) związane
Reakcje jądrowe dr inż. Romuald Kędzierski Wybuch bomby Ivy Mike (fot. National Nuclear Security Administration/Nevada Site Office, domena publiczna) Przemiany jądrowe 1. Spontaniczne (niewymuszone) związane
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Energetyka konwencjonalna odnawialna i jądrowa
 Energetyka konwencjonalna odnawialna i jądrowa Wykład 8-27.XI.2018 Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów szef@fuw.edu.pl http://www.fuw.edu.pl/~szef/ Wykład 8 Energia atomowa i jądrowa
Energetyka konwencjonalna odnawialna i jądrowa Wykład 8-27.XI.2018 Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów szef@fuw.edu.pl http://www.fuw.edu.pl/~szef/ Wykład 8 Energia atomowa i jądrowa
Jądro atomowe A 1/ cm r j. promienie jąder r j. = r o. promienie atomowe r at cm. masa jądra m j.
 Jądro atomowe promienie jąder r j 10-13 - 10-12 cm r j = r o A 1/3 promienie atomowe r at 10-8 cm masa jądra m j 10-24 - 10-22 g gęstość materii jądrowej 10 14 g cm -3 1 cm 3 materii jądrowej waŝyłby 130
Jądro atomowe promienie jąder r j 10-13 - 10-12 cm r j = r o A 1/3 promienie atomowe r at 10-8 cm masa jądra m j 10-24 - 10-22 g gęstość materii jądrowej 10 14 g cm -3 1 cm 3 materii jądrowej waŝyłby 130
Transport elektronów w biomolekułach
 Transport elektronów w biomolekułach Równanie Arrheniusa, energia aktywacji Większość reakcji chemicznych zachodzi ze stałą szybkości (k) zaleŝną od temperatury (T) i energii aktywacji ( G*) tej reakcji,
Transport elektronów w biomolekułach Równanie Arrheniusa, energia aktywacji Większość reakcji chemicznych zachodzi ze stałą szybkości (k) zaleŝną od temperatury (T) i energii aktywacji ( G*) tej reakcji,
Promieniowanie w środowisku człowieka
 Promieniowanie w środowisku człowieka Jeżeli przyjrzymy się szczegółom mapy nuklidów zauważymy istniejące w przyrodzie w stosunkowo dużych ilościach nuklidy nietrwałe. Ich czasy zaniku są duże, większe
Promieniowanie w środowisku człowieka Jeżeli przyjrzymy się szczegółom mapy nuklidów zauważymy istniejące w przyrodzie w stosunkowo dużych ilościach nuklidy nietrwałe. Ich czasy zaniku są duże, większe
Nukleony. Nukleony cząstki jądra atomowego suma protonów i neutronów.
 JĄDRO ATOMOWE Nukleony Nukleony cząstki jądra atomowego suma protonów i neutronów. A Z X np. dla izotopów wodoru: -jądro najpospolitszego izotopu H (Z=, A=) składa się z jednego protonu: H -jądro deuteru
JĄDRO ATOMOWE Nukleony Nukleony cząstki jądra atomowego suma protonów i neutronów. A Z X np. dla izotopów wodoru: -jądro najpospolitszego izotopu H (Z=, A=) składa się z jednego protonu: H -jądro deuteru
PODSTAWY DATOWANIA RADIOWĘGLOWEGO
 Dni Otwarte Wydziału Chemii 2008 PODSTAWY DATOWANIA RADIOWĘGLOWEGO Andrzej Komosa Zakład Radiochemii i Chemii Koloidów UMCS 1 Nagroda Nobla z chemii w roku 1960 Willard Frank Libby 1908-1980 Książka: Radiocarbon
Dni Otwarte Wydziału Chemii 2008 PODSTAWY DATOWANIA RADIOWĘGLOWEGO Andrzej Komosa Zakład Radiochemii i Chemii Koloidów UMCS 1 Nagroda Nobla z chemii w roku 1960 Willard Frank Libby 1908-1980 Książka: Radiocarbon
UKŁAD OKRESOWY PIERWIASTKÓW
 UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
Wykład 41 Liczby magiczne. Model powłokowy jąder
 Wykład 4 Liczby magiczne Model powłokowy jąder Na podstawie modelu kroplowego można prawidłowo ocenić masy, energii wiązania jąder, wyznaczyć energetyczne warunki rozpadu jąder, zbudować jakościową teorie
Wykład 4 Liczby magiczne Model powłokowy jąder Na podstawie modelu kroplowego można prawidłowo ocenić masy, energii wiązania jąder, wyznaczyć energetyczne warunki rozpadu jąder, zbudować jakościową teorie
ĆWICZENIE NR 17. EFEKT SZILARDA-CHALMERSA. WYDZIELENIE IZOMERU 80 Br
 ĆWICZEIE R 17 EFEKT SZILARDA-CHALMERSA. WYDZIELEIE IZOMERU 80 Br PODSTAWY FIZYKO - CHEMICZE ZJAWISKA Badania przemian chemicznych, towarzyszących procesom jądrowym stanowią ważny rozdział chemii jądrowej
ĆWICZEIE R 17 EFEKT SZILARDA-CHALMERSA. WYDZIELEIE IZOMERU 80 Br PODSTAWY FIZYKO - CHEMICZE ZJAWISKA Badania przemian chemicznych, towarzyszących procesom jądrowym stanowią ważny rozdział chemii jądrowej
Elementy fizyki jądrowej
 Elementy fizyki jądrowej Cząstka elementarna Fermiony (cząstki materii) -leptony: elektron, neutrino elektronowe, mion, neutrino mionowe, taon, neutrino taonowe -kwarki: kwark dolny, kwark górny, kwark
Elementy fizyki jądrowej Cząstka elementarna Fermiony (cząstki materii) -leptony: elektron, neutrino elektronowe, mion, neutrino mionowe, taon, neutrino taonowe -kwarki: kwark dolny, kwark górny, kwark
III. EFEKT COMPTONA (1923)
 III. EFEKT COMPTONA (1923) Zjawisko zmiany długości fali promieniowania roentgenowskiego rozpraszanego na swobodnych elektronach. Zjawisko to stoi u podstaw mechaniki kwantowej. III.1. EFEKT COMPTONA Rys.III.1.
III. EFEKT COMPTONA (1923) Zjawisko zmiany długości fali promieniowania roentgenowskiego rozpraszanego na swobodnych elektronach. Zjawisko to stoi u podstaw mechaniki kwantowej. III.1. EFEKT COMPTONA Rys.III.1.
Promieniotwórczość NATURALNA
 Promieniotwórczość NATURALNA Badając świecenie różnych substancji, zauważyłem, że wszystkie związki uranu wysyłają promieniowanie przenikające przez czarny papier i inne osłony oraz powodują naświetlenie
Promieniotwórczość NATURALNA Badając świecenie różnych substancji, zauważyłem, że wszystkie związki uranu wysyłają promieniowanie przenikające przez czarny papier i inne osłony oraz powodują naświetlenie
TYPY REAKCJI CHEMICZNYCH
 CHEMIA SPALANIA TYPY REAKCJI CHEMICZNYCH Jednocząsteczkowe (I rzędu): A C+D (np. C 2 H 6 CH 3 + CH 3 ) Dwucząsteczkowe (II- rzędu) (np. H + O 2 OH + O) A + B C + D Trójcząsteczkowe (III rzędu) A + B +
CHEMIA SPALANIA TYPY REAKCJI CHEMICZNYCH Jednocząsteczkowe (I rzędu): A C+D (np. C 2 H 6 CH 3 + CH 3 ) Dwucząsteczkowe (II- rzędu) (np. H + O 2 OH + O) A + B C + D Trójcząsteczkowe (III rzędu) A + B +
Piotr Kosztołowicz. Powtórka przed maturą. Chemia. Zadania. Zakres rozszerzony
 Piotr Kosztołowicz Zakres rozszerzony Chemia Powtórka przed maturą Zadania 95 Spis treści Wstęp Rozdział 1. Budowa atomów Rozdział 2. Przemiany jądrowe Rozdział 3. Struktura elektronowa atomu Rozdział
Piotr Kosztołowicz Zakres rozszerzony Chemia Powtórka przed maturą Zadania 95 Spis treści Wstęp Rozdział 1. Budowa atomów Rozdział 2. Przemiany jądrowe Rozdział 3. Struktura elektronowa atomu Rozdział
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
FIZYKA IV etap edukacyjny zakres podstawowy
 FIZYKA IV etap edukacyjny zakres podstawowy Cele kształcenia wymagania ogólne I. Wykorzystanie wielkości fizycznych do opisu poznanych zjawisk lub rozwiązania prostych zadań obliczeniowych. II. Przeprowadzanie
FIZYKA IV etap edukacyjny zakres podstawowy Cele kształcenia wymagania ogólne I. Wykorzystanie wielkości fizycznych do opisu poznanych zjawisk lub rozwiązania prostych zadań obliczeniowych. II. Przeprowadzanie
KONKURS PRZEDMIOTOWY Z CHEMII
 Pieczęć KONKURS PRZEDMIOTOWY Z CHEMII dla uczniów gimnazjów województwa lubuskiego 26 stycznia 2012 r. zawody II stopnia (rejonowe) Witamy Cię na drugim etapie Konkursu Chemicznego. Przed przystąpieniem
Pieczęć KONKURS PRZEDMIOTOWY Z CHEMII dla uczniów gimnazjów województwa lubuskiego 26 stycznia 2012 r. zawody II stopnia (rejonowe) Witamy Cię na drugim etapie Konkursu Chemicznego. Przed przystąpieniem
ODKRYCIE PROMIENIOTWÓRCZOŚCI PROMIENIOWANIE JĄDROWE I JEGO WŁAŚCIWOŚCI
 ODKRYCIE PROMIENIOTWÓRCZOŚCI PROMIENIOWANIE JĄDROWE I JEGO WŁAŚCIWOŚCI Wilhelm Roentgen 1896 Stan wiedzy na rok 1911 1. Elektron masa i ładunek znikomy ułamek masy atomu 2. Niektóre atomy samorzutnie emitują
ODKRYCIE PROMIENIOTWÓRCZOŚCI PROMIENIOWANIE JĄDROWE I JEGO WŁAŚCIWOŚCI Wilhelm Roentgen 1896 Stan wiedzy na rok 1911 1. Elektron masa i ładunek znikomy ułamek masy atomu 2. Niektóre atomy samorzutnie emitują
Promieniowanie jonizujące
 Promieniowanie jonizujące Wykład IV Oddziaływanie promieniowania jonizującego z materią Fizyka MU, semestr 2 Uniwersytet Rzeszowski, 26 kwietnia 2017 Wykład IV Oddziaływanie promieniowania jonizującego
Promieniowanie jonizujące Wykład IV Oddziaływanie promieniowania jonizującego z materią Fizyka MU, semestr 2 Uniwersytet Rzeszowski, 26 kwietnia 2017 Wykład IV Oddziaływanie promieniowania jonizującego
2008/2009. Seweryn Kowalski IVp IF pok.424
 2008/2009 seweryn.kowalski@us.edu.pl Seweryn Kowalski IVp IF pok.424 Plan wykładu Wstęp, podstawowe jednostki fizyki jądrowej, Własności jądra atomowego, Metody wyznaczania własności jądra atomowego, Wyznaczanie
2008/2009 seweryn.kowalski@us.edu.pl Seweryn Kowalski IVp IF pok.424 Plan wykładu Wstęp, podstawowe jednostki fizyki jądrowej, Własności jądra atomowego, Metody wyznaczania własności jądra atomowego, Wyznaczanie
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Badanie schematu rozpadu jodu 128 I
 J8 Badanie schematu rozpadu jodu 128 I Celem doświadczenie jest wyznaczenie schematu rozpadu jodu 128 I Wiadomości ogólne 1. Oddziaływanie kwantów γ z materią [1,3] a) efekt fotoelektryczny b) efekt Comptona
J8 Badanie schematu rozpadu jodu 128 I Celem doświadczenie jest wyznaczenie schematu rozpadu jodu 128 I Wiadomości ogólne 1. Oddziaływanie kwantów γ z materią [1,3] a) efekt fotoelektryczny b) efekt Comptona
Dwie lub więcej cząstek poza zamkniętą powłoką
 Dwie lub więcej cząstek poza zamkniętą powłoką Rozważmy dwa (takie same) nukleony (lub dwie dziury) na orbitalu j poza zamkniętymi powłokami. Te dwie cząstki mogą sprzęgać się do momentu pędu J = j + j,
Dwie lub więcej cząstek poza zamkniętą powłoką Rozważmy dwa (takie same) nukleony (lub dwie dziury) na orbitalu j poza zamkniętymi powłokami. Te dwie cząstki mogą sprzęgać się do momentu pędu J = j + j,
Budowa atomu. Wiązania chemiczne
 strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
KI + Pb(NO 3 ) 2 PbI 2 + KNO 3. fermentacja alkoholowa
 Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
Promieniowanie jonizujące
 Promieniowanie jonizujące Wykład V Krzysztof Golec-Biernat Oddziaływanie promieniowania jonizującego z materią Uniwersytet Rzeszowski, 6 grudnia 2017 Wykład V Krzysztof Golec-Biernat Promieniowanie jonizujące
Promieniowanie jonizujące Wykład V Krzysztof Golec-Biernat Oddziaływanie promieniowania jonizującego z materią Uniwersytet Rzeszowski, 6 grudnia 2017 Wykład V Krzysztof Golec-Biernat Promieniowanie jonizujące
3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u]
![3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u] 3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u]](/thumbs/58/41892324.jpg) 1. Masa cząsteczkowa tlenku dwuwartościowego metalu wynosi 56 [u]. Masa atomowa tlenu wynosi 16 [u]. Ustal jaki to metal i podaj jego nazwę. Napisz wzór sumaryczny tego tlenku. 2. Ile razy masa atomowa
1. Masa cząsteczkowa tlenku dwuwartościowego metalu wynosi 56 [u]. Masa atomowa tlenu wynosi 16 [u]. Ustal jaki to metal i podaj jego nazwę. Napisz wzór sumaryczny tego tlenku. 2. Ile razy masa atomowa
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY OZNACZANIE AKTYWNOŚCI, OKRESU PÓŁTRWANIA I MAKSYMALNEJ ENERGII PROMIENIOWANIA
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW OZNACZANIE AKTYWNOŚCI, OKRESU PÓŁTRWANIA I MAKSYMALNEJ ENERGII PROMIENIOWANIA Opiekun ćwiczenia: Jerzy Żak Miejsce ćwiczenia:
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW OZNACZANIE AKTYWNOŚCI, OKRESU PÓŁTRWANIA I MAKSYMALNEJ ENERGII PROMIENIOWANIA Opiekun ćwiczenia: Jerzy Żak Miejsce ćwiczenia:
VI Podkarpacki Konkurs Chemiczny 2013/2014
 VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
Badanie schematu rozpadu jodu 128 J
 J8A Badanie schematu rozpadu jodu 128 J Celem doświadczenie jest wyznaczenie schematu rozpadu jodu 128 J Wiadomości ogólne 1. Oddziaływanie kwantów γ z materią (1,3) a/ efekt fotoelektryczny b/ efekt Comptona
J8A Badanie schematu rozpadu jodu 128 J Celem doświadczenie jest wyznaczenie schematu rozpadu jodu 128 J Wiadomości ogólne 1. Oddziaływanie kwantów γ z materią (1,3) a/ efekt fotoelektryczny b/ efekt Comptona
O egzotycznych nuklidach i ich promieniotwórczości
 O egzotycznych nuklidach i ich promieniotwórczości Marek Pfützner Instytut Fizyki Doświadczalnej Uniwersytet Warszawski Tydzień Kultury w VIII LO im. Władysława IV, 13 XII 2005 Instytut Radowy w Paryżu
O egzotycznych nuklidach i ich promieniotwórczości Marek Pfützner Instytut Fizyki Doświadczalnej Uniwersytet Warszawski Tydzień Kultury w VIII LO im. Władysława IV, 13 XII 2005 Instytut Radowy w Paryżu
VII Podkarpacki Konkurs Chemiczny 2014/2015
 II Podkarpacki Konkurs Chemiczny 2014/2015 ETAP I 12.11.2014 r. Godz. 10.00-12.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Który z podanych zestawów zawiera wyłącznie
II Podkarpacki Konkurs Chemiczny 2014/2015 ETAP I 12.11.2014 r. Godz. 10.00-12.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Który z podanych zestawów zawiera wyłącznie
BUDOWA ATOMU. Pierwiastki chemiczne
 BUDOWA ATOMU Pierwiastki chemiczne p.n.e. Sb Sn n Pb Hg S Ag C Au Fe Cu ()* do XVII w. As (5 r.) P (669 r.) () XVIII w. N Cl Cr Co Y Mn Mo () Ni Pt Te O U H W XIX w. (m.in.) Na Ca Al Si F Cs Ba B Bi I
BUDOWA ATOMU Pierwiastki chemiczne p.n.e. Sb Sn n Pb Hg S Ag C Au Fe Cu ()* do XVII w. As (5 r.) P (669 r.) () XVIII w. N Cl Cr Co Y Mn Mo () Ni Pt Te O U H W XIX w. (m.in.) Na Ca Al Si F Cs Ba B Bi I
