ELEKTROFOREZA ŻELOWA KOLAGENU
|
|
|
- Ignacy Bednarek
- 5 lat temu
- Przeglądów:
Transkrypt
1 ELEKTROFOREZA ŻELOWA KOLAGENU I. PRZYGOTOWANIE ŻELU POLIAKRYLAMIDOWEGO DO ELEKTROFOREZY BIAŁEK W WARUNKACH DENATURUJĄCYCH (SDS-PAGE) Żele poliakrylamidowe do elektroforezy wytwarza się poprzez wolnorodnikową polimeryzację monomerów akryl amidowych, których długie łańcuchy są łączone kowalencyjnie w wyniku działania czynnika sieciującego N,N'-metyleno-bis-akrylamidu. Gęstość żelu zależy od całkowitego stężenia obu składników, natomiast stopień usieciowania zależy od stężenia bis-akrylamidu. Reakcja polimeryzacji jest inicjowana przez wolne rodniki dostarczone przez nadsiarczan amonu i katalizowana przez N,N,N,N -czterometyloetylenodwuaminę (TEMED). Reakcja trwa około min, lecz czas ten może różnić się w zależności od stężeń nadsiarczanu amonu i TEMEDu. Polimeryzacja zachodzi bez dostępu tlenu, który jest inhibitorem tej reakcji. Możliwa jest także fotopolimeryzacja, czynnikiem inicjującym reakcję polimeryzacji jest wówczas UV. Akrylamid O O H 2 C CH 2 NH NH N,N'-Metylenodiakrylamid = Bisakrylamid N,N,N,N -czterometylo-etylenodwuamina = TEMED Rys. 1 Chemiczne struktury związków stosowanych do przygotowania żeli poliakrylamidowych. 1
2 SO 4 : + n H 2 C O NH 2 H 2 N O CH 2. CH 2. O NH 2 O NH 2 n Rys.2 Polimeryzacja bez udziału bisakrylamidu. Rys. 3 Polimeryzacja z udziałem bisakrylamidu. 2
3 Wielkość por w żelu poliakrylamidowym zależy od procentowej zawartości akrylamidów. Zwiększenie procentowości żelu prowadzi do zmniejszenia wielkości porów. Jeśli chcemy rozdzielić fragmenty charakteryzujące się szerokim zakresem wielkości, można zastosować żel gradientowy. W takim żelu wielkość porów jest większa u góry (przy studzienkach), zmniejszając się gradientowo w kierunku do dołu żelu. Elektroforezę białek w żelu poliakrylamidowym zazwyczaj prowadzi się w wersji dwuwarstwowej (górna, stosunkowo wąska warstwa żel zagęszczający i dolana, szersza warstwa żel rozwijający). Obie warstwy różnią się stężeniem akrylamidu, siłą jonową buforu i jego ph. Uwaga: Akrylamidy niespolimeryzowane są neurotoksyczne, efekt toksyczny ma charakter kumulatywny, tzn. objawy patologiczne mogą wystąpić po wielu latach niewielkiej, ale systematycznej ekspozycji, należy więc unikać kontaktu ze skórą i błonami śluzowymi!!! CZĘŚĆ I. PRZYGOTOWANIE ŻELU POLIAKRYLAMIDOWYM DO ELEKTROFOREZY BIAŁEK W WARUNKACH DENATURUJĄCYCH (SDS-PAGE) Materiały Płytka szklana wewnętrzna o wymiarach Płytka szklana z przekładkami (spacer ami) Ramka do płytek Uszczelka sylikonowa so statywu Statyw Grzebień teflonowy Zlewki do przygotowania żeli Odczynniki chemiczne: Roztwór akrylamid : N, N-metyleno-bisakrylamid (37,5 : 1 ) Woda 2x dejonizowana 3
4 10% roztwór SDS (dodecylo siarczan sodu) 10% roztwór APS (nadsiarczan amonu) 1.5 M bufor Tris-HCl (ph 8.8) 0,5 M bufor Tris-HCl (ph 6.8) TEMED - N, N, N, N - tetrametyloetylenodiamina Przygotowanie żelu poliakrylamidowego SDS-PAGE - Wykonanie 1. Starannie umyć szybki detergentem (płyn do mycia naczyń, roztwór SDS), osuszyć czystym ręcznikiem papierowym i przetrzeć wewnętrzne powierzchnie szybek etanolem lub denaturatem. 2. Ustaw płytkę z krawędziami zgodnie z oznaczeniem up i włóż złożone ze sobą płytki do ramki do wylewania żelu, tak, aby krótsza płytka znalazła się od strony zacisków ramki. Uwaga: Płytki muszą być ułożone równolegle do siebie. 3. Zabezpieczone w ramce do wylewania żelu płytki umieść w statywie z dopasowaną uszczelką. 4. Sporządzić roztwór żelu rozdzielającego (wg Tabeli 1). Polimeryzacja zaczyna się, gdy w mieszaninie znajdują się nadsiarczan amonu i TEMED, dlatego należy je dodawać na końcu. Tabela 1. Składniki żelu rozdzielającego, całkowita objętość 10 ml. % żelu H2O [ml] Akrylamid/ Bis [ml] 1,5 M Tris-HCl ph 8,8 [ml] 10% SDS [ml] TEMED [µl] 10% APS [µl] 5% 5,7 1,7 2,5 0, % 4,7 2,7 2,5 0, % 4,1 3,2 2,5 0, % 3,4 4,0 2,5 0, Przy pomocy pipety wlać żel rozdzielający (4-5 ml). Wyrównać powierzchnie żelu przez kołysanie. 6. Warstwę żelu rozdzielającego zalać wodą (zabezpieczy przed wysuszeniem powierzchni żelu i przyspieszy polimeryzację. 4
5 7. Sporządzić roztwór żelu zagęszczającego (wg Tabeli 2). Tabela 1. Składniki żelu zagęszczającego, całkowita objętość 5 ml. % żelu H2O [ml] Akrylamid/ Bis [ml] 0,5 M Tris-HCl ph 6,8 [ml] 10% SDS [ml] TEMED [µl] 10% APS [µl] 5% 2,85 0,85 1,25 0, % 2,35 1,85 1,25 0, % 2,05 1,6 1,25 0, Po zakończeniu polimeryzacji żelu rozdzielającego (około 30 min) wylać wodę i odsączyć jej resztki przy pomocy ligniny lub ręcznika papierowego. 9. Przy pomocy pipety wlać żel zagęszczający (ok. 1.5 ml), umieścić grzebień teflonowy w żelu tak aby leązł równolegle z brzegiem krótszej płytki szklanej. Pozostaw na około minut, aby żel spolimeryzował. 10. Po zakończeniu polimeryzacji żelu zagęszczającego wyjąć grzebień, zdjąć żel (tzn. żel z szybami pomiędzy którymi się znajduje) z ramki do wylewania i żel wraz z płytkami umieścić w ramce wewnętrznej. Zamknąć płytki z żelem w ramce, używając przystosowanych do tego zacisków. 11. Przepłukać studzienki wodą i odsączyć resztki wody ligniną lub ręcznikiem papierowym. II. ELEKTROFOREZA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM W WARUNKACH DENATURUJĄCYCH. DETEKCJA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM ELEKTROFOREZA POLIAKRYLAMIDOWA BIAŁEK W WARUNKACH NATYWNYCH (ELEKTROFOREZA NATYWNA) Elektroforeza pozwala na rozdzielanie białek ze względu na ich gęstość ładunku, w tym przypadku ruchliwość elektroforetyczna składników próbki zależy zarówno od ładunku molekuł, jak i ich masy. Bufory użyte podczas elektroforezy natywnej pozwalają na utrzymanie białek w stanie niedenaturowanym. Enzymy po elektroforezie zachowują swoją aktywność. Elektroforeza natywna jest używana głównie do określenia czystości białek np. oznaczenia czystości preparatyki enzymów. W elektroforezie natywnej białek używa się nieciągłego 5
6 systemu buforowego. Stosowane są dwa żele zagęszczający o niższym stężeniu akrylamidów i niższym ph, oraz rozdzielający o mniejszych porach (wyższe stężenie akrylamidów) i wyższe ph. Rozwiązanie to, stosowane także w żelach denaturujących, umożliwia uzyskanie zagęszczenia preparatu na styku żeli i migracji białek w żelu rozdzielającym w postaci ostrych prążków. ELEKTROFOREZA POLIAKRYLAMIDOWA BIAŁEK W WARUNKACH DENATURUJĄCYCH (SDS-PAGE) Elektroforeza w żelu poliakrylamidowym jest użyteczną i powszechnie stosowaną metodą rozdzielania i charakterystyki białek. Jest to stosunkowo prosta i szybka technika. Na jednym żelu można przeprowadzić jednocześnie analizę wielu próbek, a rozdzielone białka można skutecznie wykrywać w żelu np. metodami barwienia, immunoprecypitacji czy autoradiografii. Można więc stosować tę technikę na przykład przy analizie białek we frakcjach zbieranych w trakcie rozdzielania na kolumnie chromatograficznej. W SDS-PAGE stwarza się warunki, w których wszystkie składniki próbki mają ten sam ładunek; ich ruchliwość jest więc jedynie funkcją mas cząsteczkowych (SDS-PAGE). Użycie anionowego detergentu soli sodowej kwasu dodecylosiarkowego (SDS ang. Sodium Dodecyl Sulfate) pozwala na rozdzielenie elektroforetytczne białek zgodnie z ich masą cząsteczkową. Przed i w trakcie elektroforezy białka ulegają dysocjacji i denaturacji w obecności SDS, który łączy się z białkami specyficznie w stosunku masowym 4,1:1. Zapewnia to przejęcie przez białko ujemnego ładunku elektrycznego netto o stałej gęstości bez względu na jego długość. Dla całkowitego rozwinięcia polipeptydu i zapewnienia mu pierwszorzędowej struktury, niezbędne jest dodatkowo zniszczenie mostków dwusiarczkowych (β-merkaptoetanol lub ditiotretiol). Opłaszczenie białka przez SDS oraz redukcja mostków dwusiarczkowych pozwalają na separację białek w żelu poliakrylamidowym ze względu na ich wielkość, a zatem pośrednio masę cząsteczkową. Szybkość migracji w SDS-PAGE nie jest determinowana przez ładunek elektryczny białka zależny od ph i konformacji białka. Dzięki możliwości rozdzielenia białek na podstawie ich wielkości możemy oznaczyć masę cząsteczkową nieznanego białka, porównując jego położenie w żelu w stosunku do innych białek (tzw. białek wzorcowych) po zakończonej migracji i wybarwieniu. 6
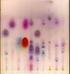
7 BARWIENIE I DOKUMENTACJA Ukończenie rozdzielania elektroforetycznego nie kończy procedury. Większość białek i kwasów nukleinowych nie jest widoczna w świetle białym. Niezbędne jest ich wybarwienie (wizualizacja) w żelach lub na membranach, tak aby uzyskać informację o dystansie ich migracji i ich ilości w prążku. Stosowanych jest wiele metod wizualizacji żeli i membran. Białka najczęściej wybarwia się stosując naturalne barwniki, takie jak błękit kumassi (ang. Coomassie Brilant Blue) czy czerń amidową. Barwnik dodawany jest zwykle do roztworu utrwalającego położenie białka w żelu (denaturacja i unieruchomienie molekuł), po czym nadmiar barwnika jest wymywany. Pozostaje tylko barwnik związany z białkami. Czułość takiej detekcji białek jest stosunkowo dobra. Można w ten sposób znaleźć 1 μg białka w prążku. Znacznie bardziej czułą metodą jest barwienie srebrem. Metoda ta pozwala oznaczyć 10 ng białka w prążku. Przy pomocy srebra można również wybarwić kwasy nukleinowe oraz oligonukleotydy, a czułość detekcji zbliżona jest również do 10 ng DNA na prążek. Rys. 4. Przykładowe rozdzielenie białek w żelu poliakrylamidowym przedstawiono na rysunku. Żel barwiono Coomassie Brilliant Blue R-250. Najprostszą formą dokumentacji rozdzielonych w procesie elektroforezy w żelach poliakrylamidowych składników jest ich wysuszenie pomiędzy warstwą bibuły i celofanu lub pomiędzy dwoma warstwami celofanu. Wysuszony w ten sposób żel można przechowywać dowolnie długo bez widocznego uszczerbku w jakości tego dokumentu. Żele poliakrylamidowe przygotowane na folii można suszyć bez okrywania celofanem. Trudności pojawiają się wtedy, gdy trzeba wysuszyć żel o zawartości akrylamidu powyżej 15%. Odwodnienie żelu powoduje silne jego obkurczenie i w rezultacie pękanie. Można temu przeciwdziałać wypierając z żelu 7
8 wodę przez dodanie glicerolu. Żele takie pozostają jednak nieco lepkie i muszą być okryte folią. Żele agarozowe nie poddają się jednak tej formie dokumentowania. Najprostszym sposobem utrwalenia informacji zawartej w żelu agarozowym jest sporządzenie jego fotografii lub skanu. Technikę tę można zastosować również do żeli poliakrylamidowych. Od kilku lat do dokumentacji rozdziałów elektroforetycznych stosuje się z powodzeniem kamery cyfrowe, a uzyskany obraz przechowywany jest w formie elektronicznej w pamięci komputera lub na innych nośnikach pamięci. Kamery cyfrowe pozwalają na uzyskanie i przetworzenie obrazu żeli i membran wizualizowanych barwieniem, z zastosowaniem znaczników fluorescencyjnych. KOLAGEN Kolagen jest szeroko rozpowszechnionym białkiem, stanowiącym główny składnik większości tkanek łącznych u ssaków, pełniącym funkcje strukturalne. Będąc najważniejszym składnikiem zewnątrzkomórkowej macierzy jest dla skóry białkiem kluczowym, odpowiadającym za jej elastyczność i wytrzymałość. Do białek kolagenu zalicza się 28 typów, zbudowanych z co najmniej 46 różnych łańcuchów polipeptydowych. Wspólną cechą strukturalną kolagenów jest obecność potrójnej spirali, której zawartość w poszczególnych typach waha się od 96% do 10%. Ze względu na swoje właściwości biologiczne jest powszechnie stosowany w przemyśle kosmetycznym, farmaceutycznym oraz medycynie estetycznej. CZĘŚĆ II Materiały Aparat do elektroforezy (moduł elektrody + ramka zewnętrzna + mini tank + pokrywa) Zasilacz prądu stałego Pipety automatyczne Probówki typu Eppendorff 0,5 ml Łopatka do usuwania żelu z płytki Naczynia do wybarwiania żeli 8
9 Odczynniki chemiczne Marker białek firmy Life Technologies Ekstrakty białek kolagenu Bufor redukujący z SDS do barwienia i denaturacji próbek (62,5 mm Tris-HCl ph 6,8; 25% glicerol; 2% SDS; 0,05% błękit bromofenylowy; 2-merkaptoetanol 5%) Bufor glicynowy do elektroforezy SDS-PAGE ( Tris-base; glicyna; SDS) Bufor Tris/HCl 0,5M ph = 10 Roztwór barwiący (100 ml) 50 ml metanolu 10 ml lodowatego kwasu octowego 0.25 g Coomassie blue R ml wody Roztwór odbarwiający (1000 ml) 300 ml metanolu 100 ml lodowatego kwasu octowego 600 ml wody Czułość: do 0.1 μg Zaletą metody jest prostota wykonania i niezawodność. Wadą jest niewielka relatywnie czułość. Wymagane środki ostrożności W trakcie wykonywania ćwiczenia student powinien nosić odzież ochronną. Roztworów nie należy wdychać i pipetować ustami. Identyfikacja zagrożeń (Klasyfikacja zgodnie z dyrektywami UE 67/548/EWG lub 1999/45/WE): Akryloamid - T Produkt toksyczny R25, R48/23/24/25, R45, R46, R62; Xn Produkt szkodliwy R20/21; Xi Produkt drażniący R36/38, R43 Nadsiarczan amonu - O Produkt utleniający R 8; Xn Produkt szkodliwy R22; Xi Produkt drażniący R36/37/38, R42/43 TEMED - F Produkt wysoce łatwopalny R11; C Produkt żrący R34; Xn Produkt szkodliwy R20/22 9
10 2-merkaptoetanol - T, N Produkt toksyczny, Produkt niebezpieczny dla środowiska R23/24/25, R38, R41, R43, R48/22, R50/53 Metanol F, T Produkt wysoce latwopalny, Produkt toksyczny R11, R23/24/25, R39/23/24/25 Kwas octowy Latwopalna ciecz i pary, R10, C, R35 Pierwsza pomoc: - w razie kontaktu ze skórą: spłukać dużą ilością wody. - w razie kontaktu z oczami: przepłukać dużą ilością wody, przy szeroko otwartej powiece. - jeżeli osoba poszkodowana oddycha, przenieść na świeże powietrze. Jeżeli osoba poszkodowana nie oddycha, zastosować sztuczne oddychanie. Zasięgnąć porady medycznej. - w przypadku wystąpienia podrażnień skontaktować się z lekarzem. - w razie spożycia: przepłukać usta wodą. Dokładne instrukcje postępowania są zawarte w dołączonych kartach charakterystyk substancji. Wykonanie Rozdzielanie elektroforetyczne białek w żelu poliakrylamidowym: 1. W celu wykonania rozdzielenia elektroforetycznego należy umocować żel (znajdujący się pomiędzy szybkami) w ramce wewnętrznej z zaciskami, tak żeby okienko do wprowadzania próbek znajdowało się od wewnętrznej strony górnej części aparatu. Krawędź szybki z przekładkami powinna znajdować się na równi z krawędzią górnej części aparatu. Niestaranne przymocowanie szybek z żelem do aparatu może powodować przelewanie buforu elektroforetycznego z górnej części aparatu do dolnej oraz może być przyczyną nierównego rozdzielenia elektroforetycznego. 2. Po przeciwnej stronie aparatu należy w analogiczny sposób zamontować drugi żel lub samą szybkę, stanowiącą w drugim przypadku zaporę dla buforu znajdującego się w górnej komorze. Górną część aparatu z przymocowanymi żelami należy umieścić w dolnej komorze (mini tank). 3. Następnie należy nalać bufor elektroforetyczny do obydwu komór, w taki sposób, aby bufor ten dochodził do górnej i dolnej krawędzi żelu, wypełnił studzienki, umożliwiając w ten sposób przepływ prądu (obwód zamknięty). 4. Ekstrakty kolagenu z próbek tkanek dla każdego ze stężeń kwasu octowego należy zmieszać z odpowiednią ilością buforu redukujacego (95 µl buforu denaturującego + 5 µl MeSH) do nanoszenia białek oraz buforem stabilizującym ph próbki Tris/HCl 1 0
11 (przygotowanie próbki: ekstrakt ze skóry kurczaka 15 µl, bufor denaturujący 10 µl, bufor Tris/HCl 10 µl). Bufor redukujacy powoduje denaturację białek, nadaje białkom wypadkowy ładunek ujemny, obciąża próbkę, dzięki czemu łatwo można ją nanieść do studzienek żelu oraz zawiera barwnik umożliwiający kontrolę postępu elektroforezy. 5. Podłączyć elektrody do zasilacza. 6. Włączyć zasilacz i ustawić napięcie o wartości 150 V w czasie 60 minut. 7. Po zakończonej elektroforezie białek, odłączyć aparat do elektroforezy od prądu i wyciągnąć ramkę wewnętrzną z żelami. 8. Wyciągnąć żele z ramki wewnętrznej. 9. Delikatnie odrzucić mniejszą szybkę. 10. Za pomocą łopatki zsunąć żel z płytki szklanej i umieścić żel w roztworze barwiącym. 11. Żel w roztworze barwiącym inkubować przy delikatnym kołysaniu przez min lub dłużej w celu zwiększenia czułości detekcji. 12. Zlać roztwór barwiący (można wykorzystać do kolejnych barwień), odmyć resztki roztworu barwiącego wodą destylowaną, zalać roztworem odbarwiającym. 13. Inkubować 2-16 h przy delikatnym kołysaniu. Wymiana roztworu odbarwiającego przyspiesza i poprawia jakość detekcji. 14. Umieścić żel w wodzie. Żele mogą być przechowywane przez czas praktycznie nieokreślony w wodzie bez utraty intensywności prążków, ale przy dłuższym przechowywaniu w wodzie pęcznieją. Aby zapobiec pęcznieniu można dolać 20 glicerolu. Przechowywanie w buforze odbarwiającym prowadzi do osłabienia intensywności prążków. 15. W celu trwałej archiwizacji żel przełożyć do przezroczystej folii i zeskanować. Przyspieszenie odbarwiania: - częsta zmiana buforu - inkubacja w temperaturze do 45 C - dodanie kawałka gąbki pochłaniającego kumarynę. Sprawozdanie W sprawozdaniu z wykonanych ćwiczeń należy umieścić krótki wstęp teoretyczny, zawierający informacje o podstawowej technice elektroforezy, jak również, informacje o innych 1 1
12 modyfikacjach tej metody oraz o metodach barwienia białek w żelach poliakrylamidowych. Podać cel ćwiczenia i opisać poszczególne jego etapy. Przeprowadzić analizę żelu (umieścić zdjęcie żelu wraz z opisem). Zmierzyć drogę migracji poszczególnych białek wzorcowych. Odczytać wartości mas cząsteczkowych nieznanych białek. Przeprowadzić dyskusję wyników i podać wnioski. Literatura 1. "Techniki elektromigracyjne - teoria i praktyka" [Red.] Buszewski B., Dziubakiewicz E., Szumski M., Wydawnictwo Malamut, Warszawa 2012, ISBN Berg J.M, Tymoczko J.L, Stryer L. (2005) Biochemia. (według V wyd. amerykańskiego) Wydawnictwo Naukowe PWN, Warszawa. 3. Jóźwiak Z., Bartosz G. Biofizyka. Wybrane zagadnienia wraz z ćwiczeniami. PWN (2007) 4. (Przepisy i porady) 5. D. Żelaszczyk, A. Waszkiewicz, H. Marona, Kolagen - struktura oraz zastosowanie w kosmetologii I medycynie estetycznej, Estetol Med Kosmetol 2012; 2(1):
ĆWICZENIE II. PRZYGOTOWANIE ŻELU POLIAKRYLAMIDOWEGO DO ELEKTROFOREZY BIAŁEK W WARUNKACH DENATURUJĄCYCH (SDS-PAGE)
 ĆWICZENIE II. ELEKTROFOREZA W ŻELU POLIAKRYLAMIDOWYM (ANG. POLYACRYLAMIDE GEL ELECTROPHORESIS - PAGE) PRZYGOTOWANIE ŻELU POLIAKRYLAMIDOWEGO DO ELEKTROFOREZY BIAŁEK W WARUNKACH DENATURUJĄCYCH (SDS-PAGE)
ĆWICZENIE II. ELEKTROFOREZA W ŻELU POLIAKRYLAMIDOWYM (ANG. POLYACRYLAMIDE GEL ELECTROPHORESIS - PAGE) PRZYGOTOWANIE ŻELU POLIAKRYLAMIDOWEGO DO ELEKTROFOREZY BIAŁEK W WARUNKACH DENATURUJĄCYCH (SDS-PAGE)
ĆWICZENIE III. ELEKTROFOREZA W ŻELU POLIAKRYLAMIDOWYM (ANG. POLYACRYLAMIDE GEL ELECTROPHORESIS - PAGE)
 ĆWICZENIE III. ELEKTROFOREZA W ŻELU POLIAKRYLAMIDOWYM (ANG. POLYACRYLAMIDE GEL ELECTROPHORESIS - PAGE) ELEKTROFOREZA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM W WARUNKACH DENATURUJĄCYCH (SDS-PAGE) DETEKCJA BIAŁEK
ĆWICZENIE III. ELEKTROFOREZA W ŻELU POLIAKRYLAMIDOWYM (ANG. POLYACRYLAMIDE GEL ELECTROPHORESIS - PAGE) ELEKTROFOREZA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM W WARUNKACH DENATURUJĄCYCH (SDS-PAGE) DETEKCJA BIAŁEK
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Farmacja 2016
 Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Farmacja 2016 Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa farmacjamolekularna@wum.edu.pl
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Farmacja 2016 Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa farmacjamolekularna@wum.edu.pl
ELEKTROFOREZA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM W WARUNKACH DENATURUJĄCYCH
 ELEKTROFOREZA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM W WARUNKACH DENATURUJĄCYCH WPROWADZENIE Elektroforeza od ponad 60 lat pozostaje najczęściej stosowaną metodą izolacji makrocząstek w układach biologicznych
ELEKTROFOREZA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM W WARUNKACH DENATURUJĄCYCH WPROWADZENIE Elektroforeza od ponad 60 lat pozostaje najczęściej stosowaną metodą izolacji makrocząstek w układach biologicznych
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA
 Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa Ćwiczenie 3 Izolacja i rozdział
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa Ćwiczenie 3 Izolacja i rozdział
ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO
 ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO CZĘŚĆ TEORETYCZNA Metody badań i cechy w oparciu o które przeprowadzana jest klasyfikacja i identyfikacja mikroorganizmówh Struktura
ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO CZĘŚĆ TEORETYCZNA Metody badań i cechy w oparciu o które przeprowadzana jest klasyfikacja i identyfikacja mikroorganizmówh Struktura
Metody badania ekspresji genów
 Metody badania ekspresji genów dr Katarzyna Knapczyk-Stwora Warunki wstępne: Proszę zapoznać się z tematem Metody badania ekspresji genów zamieszczonym w skrypcie pod reakcją A. Lityńskiej i M. Lewandowskiego
Metody badania ekspresji genów dr Katarzyna Knapczyk-Stwora Warunki wstępne: Proszę zapoznać się z tematem Metody badania ekspresji genów zamieszczonym w skrypcie pod reakcją A. Lityńskiej i M. Lewandowskiego
ELEKTROFORETYCZNY ROZDZIAŁ
 POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 2 ELEKTROFORETYCZNY ROZDZIAŁ BIAŁEK I. WSTĘP TEORETYCZNY Elektroforeza jest ruchem fazy rozproszonej względem fazy rozpraszanej,
POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 2 ELEKTROFORETYCZNY ROZDZIAŁ BIAŁEK I. WSTĘP TEORETYCZNY Elektroforeza jest ruchem fazy rozproszonej względem fazy rozpraszanej,
Multipol Standard. Aparat do jednoczesnego wylewania do 6 żeli poliakrylamidowych. Instrukcja Obsługi. Numer katalogowy:
 Multipol Standard Aparat do jednoczesnego wylewania do 6 żeli poliakrylamidowych Instrukcja Obsługi Numer katalogowy: 101-150 Aby uzys k ać pomoc techniczną : T 22 668 71 47 Spis treści 1. Informacje ogólne
Multipol Standard Aparat do jednoczesnego wylewania do 6 żeli poliakrylamidowych Instrukcja Obsługi Numer katalogowy: 101-150 Aby uzys k ać pomoc techniczną : T 22 668 71 47 Spis treści 1. Informacje ogólne
NA ŻELU POLIAKRYLAMIDOWYM
 Z48 ELEKTROFOREZA BIAŁEK NA ŻELU POLIAKRYLAMIDOWYM Terminem elektroforeza określa się zjawisko migracji cząstek lub cząsteczek w polu elektrycznym w zależności od posiadanego ładunku. Elektroforeza jako
Z48 ELEKTROFOREZA BIAŁEK NA ŻELU POLIAKRYLAMIDOWYM Terminem elektroforeza określa się zjawisko migracji cząstek lub cząsteczek w polu elektrycznym w zależności od posiadanego ładunku. Elektroforeza jako
ĆWICZENIE I. ELEKTROFOREZA ŻELOWA BARWNIKÓW SPOŻYWCZYCH. µ = ν / E ELEKTROFOREZA
 ĆWICZENIE I. ELEKTROFOREZA ŻELOWA BARWNIKÓW SPOŻYWCZYCH ELEKTROFOREZA Elektroforeza jest ruchem fazy rozproszonej względem fazy rozpraszanej, zachodzącym pod wpływem przyłożonej zewnętrznie różnicy potencjałów
ĆWICZENIE I. ELEKTROFOREZA ŻELOWA BARWNIKÓW SPOŻYWCZYCH ELEKTROFOREZA Elektroforeza jest ruchem fazy rozproszonej względem fazy rozpraszanej, zachodzącym pod wpływem przyłożonej zewnętrznie różnicy potencjałów
ELEKTROFOREZA ŻELOWA BARWNIKÓW SPOŻYWCZYCH
 ELEKTROFOREZA ŻELOWA BARWNIKÓW SPOŻYWCZYCH Instrukcja wykonana w Katedrze Chemii Środowiska ELEKTROFOREZA Elektroforeza jest ruchem fazy rozproszonej względem fazy rozpraszanej, zachodzącym pod wpływem
ELEKTROFOREZA ŻELOWA BARWNIKÓW SPOŻYWCZYCH Instrukcja wykonana w Katedrze Chemii Środowiska ELEKTROFOREZA Elektroforeza jest ruchem fazy rozproszonej względem fazy rozpraszanej, zachodzącym pod wpływem
MINIPOL 2. Zestaw do minielektroforezy płytowej w jednym lub dwóch żelach poliakrylamidowych. Instrukcja Obsługi. Numer katalogowy:
 MINIPOL 2 Zestaw do minielektroforezy płytowej w jednym lub dwóch żelach poliakrylamidowych Instrukcja Obsługi Numer katalogowy: 103-100 Aby uzys k ać pomoc techniczną : T 22 668 71 47 Spis treści 1. Informacje
MINIPOL 2 Zestaw do minielektroforezy płytowej w jednym lub dwóch żelach poliakrylamidowych Instrukcja Obsługi Numer katalogowy: 103-100 Aby uzys k ać pomoc techniczną : T 22 668 71 47 Spis treści 1. Informacje
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA
 Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa IZOLACJA DNA Z HODOWLI KOMÓRKOWEJ.
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa IZOLACJA DNA Z HODOWLI KOMÓRKOWEJ.
ELEKTROFOREZA. Wykonanie ćwiczenia 8. ELEKTROFOREZA BARWNIKÓW W ŻELU AGAROZOWYM
 Wykonanie ćwiczenia 8. ELEKTROFOREZA BARWNIKÓW W ŻELU AGAROZOWYM Zadania: 1. Wykonać elektroforezę poziomą wybranych barwników w żelu agarozowym przy trzech różnych wartościach ph roztworów buforowych.
Wykonanie ćwiczenia 8. ELEKTROFOREZA BARWNIKÓW W ŻELU AGAROZOWYM Zadania: 1. Wykonać elektroforezę poziomą wybranych barwników w żelu agarozowym przy trzech różnych wartościach ph roztworów buforowych.
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA
 Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa tel. 22 572 0735, 606448502
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa tel. 22 572 0735, 606448502
Western Blot. Praktyczny poradnik.
 Western Blot. Praktyczny poradnik. Western Blot jest techniką powszechnie stosowaną w biologii molekularnej w różnych laboratoriach na całym świecie. W przeciwieństwie do hybrydyzacji Southern i Northern,
Western Blot. Praktyczny poradnik. Western Blot jest techniką powszechnie stosowaną w biologii molekularnej w różnych laboratoriach na całym świecie. W przeciwieństwie do hybrydyzacji Southern i Northern,
BADANIE WŁASCIWOSCI FIZYKOCHEMICZNYCH KWASÓW NUKLEINOWYCH
 BADANIE WŁASCIWOSCI FIZYKOCHEMICZNYCH KWASÓW NUKLEINOWYCH ROZPUSZCZALNOŚĆ KWASÓW NUKLEINOWYCH Kwasy nukleinowe mają charakter polianionowy, wynikający z bogactwa reszt fosforanowych w ich strukturze, dzięki
BADANIE WŁASCIWOSCI FIZYKOCHEMICZNYCH KWASÓW NUKLEINOWYCH ROZPUSZCZALNOŚĆ KWASÓW NUKLEINOWYCH Kwasy nukleinowe mają charakter polianionowy, wynikający z bogactwa reszt fosforanowych w ich strukturze, dzięki
Plan ćwiczeń wykonywanych w ramach Pracowni Biologii Molekularnej, część II Ekspresja i oczyszczanie białek.
 Pracownia Biologii Molekularnej Część II Plan ćwiczeń wykonywanych w ramach Pracowni Biologii Molekularnej, część II Ekspresja i oczyszczanie białek. Spis treści 1 I spotkanie: Ekspresja białka w komórkach
Pracownia Biologii Molekularnej Część II Plan ćwiczeń wykonywanych w ramach Pracowni Biologii Molekularnej, część II Ekspresja i oczyszczanie białek. Spis treści 1 I spotkanie: Ekspresja białka w komórkach
Próba kontrolna (PK) 1000 l 1000 l
 Ćwiczenie 10. A. Oznaczanie stężenia bilirubiny całkowitej w surowicy krwi. Wymagane zagadnienia teoretyczne 1. Biosynteza hemu - metabolity pośrednie syntezy hemu. 2. Katabolizm hemu - powstawanie barwników
Ćwiczenie 10. A. Oznaczanie stężenia bilirubiny całkowitej w surowicy krwi. Wymagane zagadnienia teoretyczne 1. Biosynteza hemu - metabolity pośrednie syntezy hemu. 2. Katabolizm hemu - powstawanie barwników
HYDROLIZA SOLI. ROZTWORY BUFOROWE
 Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
1. Wprowadzenie teoretyczne Co to jest elektroforeza Parametry elektryczne Podstawowe informacje na temat białek...
 ELEKTROFOREZA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM Spis treści 1. Wprowadzenie teoretyczne... 2 1.1. Co to jest elektroforeza... 2 1.2. Parametry elektryczne... 2 1.3. Podstawowe informacje na temat białek...
ELEKTROFOREZA BIAŁEK W ŻELU POLIAKRYLAMIDOWYM Spis treści 1. Wprowadzenie teoretyczne... 2 1.1. Co to jest elektroforeza... 2 1.2. Parametry elektryczne... 2 1.3. Podstawowe informacje na temat białek...
TaqNova-RED. Polimeraza DNA RP20R, RP100R
 TaqNova-RED Polimeraza DNA RP20R, RP100R RP20R, RP100R TaqNova-RED Polimeraza DNA Rekombinowana termostabilna polimeraza DNA Taq zawierająca czerwony barwnik, izolowana z Thermus aquaticus, o przybliżonej
TaqNova-RED Polimeraza DNA RP20R, RP100R RP20R, RP100R TaqNova-RED Polimeraza DNA Rekombinowana termostabilna polimeraza DNA Taq zawierająca czerwony barwnik, izolowana z Thermus aquaticus, o przybliżonej
Gel-Out. 50 izolacji, 250 izolacji. Nr kat , Zestaw do izolacji DNA z żelu agarozowego. wersja 0617
 Gel-Out Zestaw do izolacji DNA z żelu agarozowego. wersja 0617 50 izolacji, 250 izolacji Nr kat. 023-50, 023-250 Pojemność kolumny do izolacji DNA - do 20 µg DNA, minimalna pojemność - 2 µg DNA (przy zawartości
Gel-Out Zestaw do izolacji DNA z żelu agarozowego. wersja 0617 50 izolacji, 250 izolacji Nr kat. 023-50, 023-250 Pojemność kolumny do izolacji DNA - do 20 µg DNA, minimalna pojemność - 2 µg DNA (przy zawartości
Spis treści. Definicja
 Spis treści 1 Definicja 2 Podstawy fizyczne 3 Czynniki wpływające na przebieg elektroforezy 4 Etapy planowania i wykonania elektroforezy 5 Wybór nośnika elektroforetycznego 5.1 Główne rodzaje nośników
Spis treści 1 Definicja 2 Podstawy fizyczne 3 Czynniki wpływające na przebieg elektroforezy 4 Etapy planowania i wykonania elektroforezy 5 Wybór nośnika elektroforetycznego 5.1 Główne rodzaje nośników
Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 1 O H 2 SO 4 COOH + HO t. wrz., 1 godz. O OCTAN IZOAMYLU Stechiometria reakcji Kwas octowy lodowaty Alkohol izoamylowy Kwas siarkowy 1.5 ekwiwalenta 1 ekwiwalentów 0,01 ekwiwalenta Dane do
PREPARAT NR 1 O H 2 SO 4 COOH + HO t. wrz., 1 godz. O OCTAN IZOAMYLU Stechiometria reakcji Kwas octowy lodowaty Alkohol izoamylowy Kwas siarkowy 1.5 ekwiwalenta 1 ekwiwalentów 0,01 ekwiwalenta Dane do
K05 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K05 Instrukcja wykonania ćwiczenia Wyznaczanie punktu izoelektrycznego żelatyny metodą wiskozymetryczną Zakres zagadnień obowiązujących do ćwiczenia 1. Układy
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K05 Instrukcja wykonania ćwiczenia Wyznaczanie punktu izoelektrycznego żelatyny metodą wiskozymetryczną Zakres zagadnień obowiązujących do ćwiczenia 1. Układy
ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1)
 ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1) z dnia 6 listopada 2002 r. w sprawie metodyk referencyjnych badania stopnia biodegradacji substancji powierzchniowoczynnych zawartych w produktach, których stosowanie
ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1) z dnia 6 listopada 2002 r. w sprawie metodyk referencyjnych badania stopnia biodegradacji substancji powierzchniowoczynnych zawartych w produktach, których stosowanie
ĆWICZENIE 1 i 2 Modyfikacja geu wołowej beta-laktoglobuliny przy użyciu metody Overlap Extension PCR (wydłużania nakładających się odcinków)
 ĆWICZENIE 1 i 2 Modyfikacja geu wołowej beta-laktoglobuliny przy użyciu metody Overlap Extension PCR (wydłużania nakładających się odcinków) Celem ćwiczenia jest wprowadzenie mutacji punktowej do genu
ĆWICZENIE 1 i 2 Modyfikacja geu wołowej beta-laktoglobuliny przy użyciu metody Overlap Extension PCR (wydłużania nakładających się odcinków) Celem ćwiczenia jest wprowadzenie mutacji punktowej do genu
Elektroforeza kwasów nukleinowych
 Elektroforeza kwasów nukleinowych Elektroforeza jest podstawową techniką wizualizacji kwasów nukleinowych pozwala bezpośrednio identyfikować cząsteczki DNA ze stosunkowo wysoką czułością (po odpowiednim
Elektroforeza kwasów nukleinowych Elektroforeza jest podstawową techniką wizualizacji kwasów nukleinowych pozwala bezpośrednio identyfikować cząsteczki DNA ze stosunkowo wysoką czułością (po odpowiednim
Elektroforeza kwasów nukleinowych
 Elektroforeza kwasów nukleinowych Elektroforeza jest podstawową techniką wizualizacji kwasów nukleinowych pozwala bezpośrednio identyfikować cząsteczki DNA i jest stosunkowo czuła (po odpowiednim wybarwieniu
Elektroforeza kwasów nukleinowych Elektroforeza jest podstawową techniką wizualizacji kwasów nukleinowych pozwala bezpośrednio identyfikować cząsteczki DNA i jest stosunkowo czuła (po odpowiednim wybarwieniu
Elektroforeza kwasów nukleinowych
 Elektroforeza kwasów nukleinowych Elektroforeza jest podstawową techniką wizualizacji kwasów nukleinowych pozwala bezpośrednio identyfikować cząsteczki DNA ze stosunkowo wysoką czułością (po odpowiednim
Elektroforeza kwasów nukleinowych Elektroforeza jest podstawową techniką wizualizacji kwasów nukleinowych pozwala bezpośrednio identyfikować cząsteczki DNA ze stosunkowo wysoką czułością (po odpowiednim
CEL ĆWICZENIA: Zapoznanie się z przykładową procedurą odsalania oczyszczanych preparatów enzymatycznych w procesie klasycznej filtracji żelowej.
 LABORATORIUM 3 Filtracja żelowa preparatu oksydazy polifenolowej (PPO) oczyszczanego w procesie wysalania siarczanem amonu z wykorzystaniem złoża Sephadex G-50 CEL ĆWICZENIA: Zapoznanie się z przykładową
LABORATORIUM 3 Filtracja żelowa preparatu oksydazy polifenolowej (PPO) oczyszczanego w procesie wysalania siarczanem amonu z wykorzystaniem złoża Sephadex G-50 CEL ĆWICZENIA: Zapoznanie się z przykładową
1 ekwiwalent 6 ekwiwalentów 0,62 ekwiwalentu
 PREPARAT NR 31 Stechiometria reakcji Metanol Kwas siarkowy(vi) stężony OH MeOH, H OCH 3 2 SO 4 t. wrz., 3 godz. 1 ekwiwalent 6 ekwiwalentów 0,62 ekwiwalentu 2-METOKSYNAFTALEN Dane do obliczeń Związek molowa
PREPARAT NR 31 Stechiometria reakcji Metanol Kwas siarkowy(vi) stężony OH MeOH, H OCH 3 2 SO 4 t. wrz., 3 godz. 1 ekwiwalent 6 ekwiwalentów 0,62 ekwiwalentu 2-METOKSYNAFTALEN Dane do obliczeń Związek molowa
CHROMATOGRAFIA BARWNIKÓW ROŚLINNYCH
 POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 1 CHROMATOGRAFIA BARWNIKÓW ROŚLINNYCH I. Wiadomości teoretyczne W wielu dziedzinach nauki i techniki spotykamy się z problemem
POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 1 CHROMATOGRAFIA BARWNIKÓW ROŚLINNYCH I. Wiadomości teoretyczne W wielu dziedzinach nauki i techniki spotykamy się z problemem
AmpliTest Babesia spp. (PCR)
 AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
- oznaczenia naukowo-badawcze. - jedna z podstawowych technik. - oznaczenia laboratoryjnodiagnostyczne. Elektroforeza. badawczych.
 Elektroforeza - jedna z podstawowych technik badawczych - oznaczenia naukowo-badawcze - oznaczenia laboratoryjnodiagnostyczne Annals of the New York Academy of Sciences 928:54-64 (2001) 2001 New York
Elektroforeza - jedna z podstawowych technik badawczych - oznaczenia naukowo-badawcze - oznaczenia laboratoryjnodiagnostyczne Annals of the New York Academy of Sciences 928:54-64 (2001) 2001 New York
Sporządzanie roztworów buforowych i badanie ich właściwości
 Sporządzanie roztworów buforowych i badanie ich właściwości (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zbadanie właściwości roztworów buforowych. Przygotujemy dwa roztwory buforowe: octanowy
Sporządzanie roztworów buforowych i badanie ich właściwości (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zbadanie właściwości roztworów buforowych. Przygotujemy dwa roztwory buforowe: octanowy
1 ekwiwalent 4 ekwiwalenty 5 ekwiwalentów
 PREPARAT NR 9 NH 2 NH 2 HCOOH 100 o C, 1 godz. N N H BENZIMIDAZOL Stechiometria reakcji Kwas mrówkowy Amoniak (25% m/m w wodzie) 1 ekwiwalent 4 ekwiwalenty 5 ekwiwalentów Dane do obliczeń Związek molowa
PREPARAT NR 9 NH 2 NH 2 HCOOH 100 o C, 1 godz. N N H BENZIMIDAZOL Stechiometria reakcji Kwas mrówkowy Amoniak (25% m/m w wodzie) 1 ekwiwalent 4 ekwiwalenty 5 ekwiwalentów Dane do obliczeń Związek molowa
1 ekwiwalent 2 ekwiwalenty 2 krople
 PREPARAT NR 5 COOH OH H 2 SO 4 COOH O ASPIRYNA 50-60 o C, 30 min. O Stechiometria reakcji Kwas salicylowy bezwodny Bezwodnik kwasu octowego Kwas siarkowy stęż. 1 ekwiwalent 2 ekwiwalenty 2 krople Dane
PREPARAT NR 5 COOH OH H 2 SO 4 COOH O ASPIRYNA 50-60 o C, 30 min. O Stechiometria reakcji Kwas salicylowy bezwodny Bezwodnik kwasu octowego Kwas siarkowy stęż. 1 ekwiwalent 2 ekwiwalenty 2 krople Dane
Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 2 2,4,6-TRIBROMOANILINA NH 2 NH 2 Br Br Br 2 AcOH, 0 o C, 1 godz. Br Stechiometria reakcji Anilina 1 ekwiwalent 3.11 ekwiwalenta Dane do obliczeń Związek molowa (g/mol) Gęstość (g/ml) Anilina
PREPARAT NR 2 2,4,6-TRIBROMOANILINA NH 2 NH 2 Br Br Br 2 AcOH, 0 o C, 1 godz. Br Stechiometria reakcji Anilina 1 ekwiwalent 3.11 ekwiwalenta Dane do obliczeń Związek molowa (g/mol) Gęstość (g/ml) Anilina
STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI
 Ćwiczenie 8 Semestr 2 STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI Obowiązujące zagadnienia: Stężenie jonów wodorowych: ph, poh, iloczyn jonowy wody, obliczenia rachunkowe, wskaźniki
Ćwiczenie 8 Semestr 2 STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI Obowiązujące zagadnienia: Stężenie jonów wodorowych: ph, poh, iloczyn jonowy wody, obliczenia rachunkowe, wskaźniki
TWARDOŚĆ WODY. Ca(HCO 3 ) HCl = CaCl 2 + 2H 2 O + 2CO 2. Mg(HCO 3 ) 2 + 2HCl = MgCl 2 + 2H 2 O + 2CO 2
 TWARDOŚĆ WODY Ćwiczenie 1. Oznaczanie twardości przemijającej wody wodociągowej Oznaczenie twardości przemijającej wody polega na miareczkowaniu określonej ilości badanej wody roztworem kwasu solnego o
TWARDOŚĆ WODY Ćwiczenie 1. Oznaczanie twardości przemijającej wody wodociągowej Oznaczenie twardości przemijającej wody polega na miareczkowaniu określonej ilości badanej wody roztworem kwasu solnego o
Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 31 Stechiometria reakcji Metanol Kwas siarkowy(vi) stężony OH MeOH, H OCH 3 2 SO 4 t. wrz., 3 godz. 1 ekwiwalent 6 ekwiwalentów 0,62 ekwiwalentu 2-METOKSYNAFTALEN Dane do obliczeń Związek molowa
PREPARAT NR 31 Stechiometria reakcji Metanol Kwas siarkowy(vi) stężony OH MeOH, H OCH 3 2 SO 4 t. wrz., 3 godz. 1 ekwiwalent 6 ekwiwalentów 0,62 ekwiwalentu 2-METOKSYNAFTALEN Dane do obliczeń Związek molowa
ĆWICZENIE 1. Aminokwasy
 ĆWICZENIE 1 Aminokwasy Przygotować 5 (lub więcej) 1% roztworów poszczególnych aminokwasów i białka jaja kurzego i dla każdego z nich wykonać wszystkie reakcje charakterystyczne. Reakcja ksantoproteinowa
ĆWICZENIE 1 Aminokwasy Przygotować 5 (lub więcej) 1% roztworów poszczególnych aminokwasów i białka jaja kurzego i dla każdego z nich wykonać wszystkie reakcje charakterystyczne. Reakcja ksantoproteinowa
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 CZĘŚĆ PRAKTYCZNA
 Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2018 Nazwa kwalifikacji: Przygotowywanie sprzętu, odczynników chemicznych i próbek do badań analitycznych
Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2018 Nazwa kwalifikacji: Przygotowywanie sprzętu, odczynników chemicznych i próbek do badań analitycznych
OCENA CZYSTOŚCI WODY NA PODSTAWIE POMIARÓW PRZEWODNICTWA. OZNACZANIE STĘŻENIA WODOROTLENKU SODU METODĄ MIARECZKOWANIA KONDUKTOMETRYCZNEGO
 OCENA CZYSTOŚCI WODY NA PODSTAWIE POMIAÓW PZEWODNICTWA. OZNACZANIE STĘŻENIA WODOOTLENKU SODU METODĄ MIAECZKOWANIA KONDUKTOMETYCZNEGO Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu
OCENA CZYSTOŚCI WODY NA PODSTAWIE POMIAÓW PZEWODNICTWA. OZNACZANIE STĘŻENIA WODOOTLENKU SODU METODĄ MIAECZKOWANIA KONDUKTOMETYCZNEGO Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu
bi ~ Zestaw dydal<tyczny umożliwiający przeprowadzenie izolacji genomowego DNA z bakterii EasyLation Genomie DNA INSTRUI<CJA DLA STUDENTÓW
 Zestaw dydaktyczny EasyLation Genomie DNA Nr kat. DY80 Wersja zestawu: 1.2014 Zestaw dydal
Zestaw dydaktyczny EasyLation Genomie DNA Nr kat. DY80 Wersja zestawu: 1.2014 Zestaw dydal
Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616
 Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616 10 izolacji Nr kat. 995-10 Pojemność kolumny do oczyszczania DNA wynosi 500 µg 1 Skład zestawu Składnik Ilość Temp. Przechowywania Kolumny
Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616 10 izolacji Nr kat. 995-10 Pojemność kolumny do oczyszczania DNA wynosi 500 µg 1 Skład zestawu Składnik Ilość Temp. Przechowywania Kolumny
Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 24 BENZOESAN 2-NAFTYLU OH PhCOCl, NaOH H 2 O, t. pok., 2 godz. O O Stechiometria reakcji Chlorek benzoilu NaOH 1 ekwiwalent 1 ekwiwalent 1,05 ekwiwalenta Dane do obliczeń Związek molowa (g/mol)
PREPARAT NR 24 BENZOESAN 2-NAFTYLU OH PhCOCl, NaOH H 2 O, t. pok., 2 godz. O O Stechiometria reakcji Chlorek benzoilu NaOH 1 ekwiwalent 1 ekwiwalent 1,05 ekwiwalenta Dane do obliczeń Związek molowa (g/mol)
Deproteinizacja jako niezbędny etap przygotowania próbek biologicznych
 Deproteinizacja jako niezbędny etap przygotowania próbek biologicznych Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu Łódzkiego. 1. Wstęp Określenie próbka biologiczna jest
Deproteinizacja jako niezbędny etap przygotowania próbek biologicznych Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu Łódzkiego. 1. Wstęp Określenie próbka biologiczna jest
Zestaw do oczyszczania DNA po reakcjach enzymatycznych
 Cat. No. EM07.1 Wersja: 1.2017 NOWA WERSJA Zestaw do oczyszczania DNA po reakcjach enzymatycznych EXTRACTME jest zarejestrowanym znakiem towarowym BLIRT S.A. www.blirt.eu Nr kat. EM07.1 I. PRZEZNACZENIE
Cat. No. EM07.1 Wersja: 1.2017 NOWA WERSJA Zestaw do oczyszczania DNA po reakcjach enzymatycznych EXTRACTME jest zarejestrowanym znakiem towarowym BLIRT S.A. www.blirt.eu Nr kat. EM07.1 I. PRZEZNACZENIE
Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 24 BENZOESAN 2-NAFTYLU OH PhCOCl, NaOH H 2 O, t. pok., 2 godz. O O Stechiometria reakcji Chlorek benzoilu NaOH 1 ekwiwalent 1 ekwiwalent 1,05 ekwiwalenta Dane do obliczeń Związek molowa (g/mol)
PREPARAT NR 24 BENZOESAN 2-NAFTYLU OH PhCOCl, NaOH H 2 O, t. pok., 2 godz. O O Stechiometria reakcji Chlorek benzoilu NaOH 1 ekwiwalent 1 ekwiwalent 1,05 ekwiwalenta Dane do obliczeń Związek molowa (g/mol)
Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 6 NaO 3 S Oranż 2-naftolu NH 2 + OH 5 o C N N OH SO 3 H Stechiometria reakcji 2-Naftol Kwas sulfanilowy Azotan III sodu 1 ekwiwalent 1 ekwiwalent 1 ekwiwalent Dane do obliczeń Związek molowa
PREPARAT NR 6 NaO 3 S Oranż 2-naftolu NH 2 + OH 5 o C N N OH SO 3 H Stechiometria reakcji 2-Naftol Kwas sulfanilowy Azotan III sodu 1 ekwiwalent 1 ekwiwalent 1 ekwiwalent Dane do obliczeń Związek molowa
Laboratorium 5. Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna
 Laboratorium 5 Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna Prowadzący: dr inż. Karolina Labus 1. CZĘŚĆ TEORETYCZNA Szybkość reakcji enzymatycznej zależy przede wszystkim od stężenia substratu
Laboratorium 5 Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna Prowadzący: dr inż. Karolina Labus 1. CZĘŚĆ TEORETYCZNA Szybkość reakcji enzymatycznej zależy przede wszystkim od stężenia substratu
ANALIZA I OCZYSZCZANIE BIAŁEK
 Ćwiczenie 3 ANALIZA I CZYSZCZANIE BIAŁEK Część doświadczalna obejmuje: rozdział białek zawartych w surowicy krwi metodą elektroforezy w żelu agarozowym rozdział hemoglobiny od chromianu potasu metodą sączenia
Ćwiczenie 3 ANALIZA I CZYSZCZANIE BIAŁEK Część doświadczalna obejmuje: rozdział białek zawartych w surowicy krwi metodą elektroforezy w żelu agarozowym rozdział hemoglobiny od chromianu potasu metodą sączenia
Kolor i stan skupienia: czerwone ciało stałe. Analiza NMR: Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 22 HO OH ZnCl 2 (bezw.) HO O O FLUORESCEINA 180210 o C, 40 min COOH Stechiometria reakcji ZnCl 2 bezw. 1 ekwiwalent 2.5 ekwiwalenta 0.5 ekwiwalenta Dane do obliczeń Związek molowa (g/mol) Gęstość
PREPARAT NR 22 HO OH ZnCl 2 (bezw.) HO O O FLUORESCEINA 180210 o C, 40 min COOH Stechiometria reakcji ZnCl 2 bezw. 1 ekwiwalent 2.5 ekwiwalenta 0.5 ekwiwalenta Dane do obliczeń Związek molowa (g/mol) Gęstość
KARTA CHARAKTERYSTYKI PREPARATU. 1.2. Istotne zidentyfikowanie zastosowania substancji lub mieszaniny oraz zastosowanie odradzane:
 z dnia 18 grudnia 2006 r. w sprawie rejestracji, oceny, udzielenia zezwoleń i stosowanych ograniczeń w zakresie chemikaliów (REACH) i Data sporządzenia karty: 09.02.2004r. Data aktualizacji: 20.01.2012r.
z dnia 18 grudnia 2006 r. w sprawie rejestracji, oceny, udzielenia zezwoleń i stosowanych ograniczeń w zakresie chemikaliów (REACH) i Data sporządzenia karty: 09.02.2004r. Data aktualizacji: 20.01.2012r.
1 ekwiwalent 2.5 ekwiwalenta 0.5 ekwiwalenta
 PREPARAT NR 10 HO OH ZnCl 2 (bezw.) HO O O FLUORESCEINA 180-210 o C, 40 min COOH Stechiometria reakcji ZnCl 2 bezw. 1 ekwiwalent 2.5 ekwiwalenta 0.5 ekwiwalenta Dane do obliczeń Związek molowa (g/mol)
PREPARAT NR 10 HO OH ZnCl 2 (bezw.) HO O O FLUORESCEINA 180-210 o C, 40 min COOH Stechiometria reakcji ZnCl 2 bezw. 1 ekwiwalent 2.5 ekwiwalenta 0.5 ekwiwalenta Dane do obliczeń Związek molowa (g/mol)
ELEKTROFOREZA JAKO METODA ANALIZY BIAŁEK
 Ćwiczenie 2 ELEKTROFOREZA JAKO METODA ANALIZY BIAŁEK 2.1.CEL ĆWICZENIA Zapoznanie się z techniką elektroforezy białek, w szczególności elektroforezy w żelu poliakrylamidowym w warunkach denaturujących
Ćwiczenie 2 ELEKTROFOREZA JAKO METODA ANALIZY BIAŁEK 2.1.CEL ĆWICZENIA Zapoznanie się z techniką elektroforezy białek, w szczególności elektroforezy w żelu poliakrylamidowym w warunkach denaturujących
Karta danych bezpieczeństwa produktu
 Punkt 1. Identyfikacja produktu i producenta 1.1 Numer modelu VS0061F v2 1.2 Opis Płyn do wykrywania wycieków w układach spalania (250 ml) 1.3 Producent Sealey Group Kempson Way, Bury St. Edmunds, Suffolk
Punkt 1. Identyfikacja produktu i producenta 1.1 Numer modelu VS0061F v2 1.2 Opis Płyn do wykrywania wycieków w układach spalania (250 ml) 1.3 Producent Sealey Group Kempson Way, Bury St. Edmunds, Suffolk
SubDNA. Zestaw do elektroforezy horyzontalnej w żelu agarozowym z chłodzeniem* Instrukcja Obsługi
 * SubDNA Zestaw do elektroforezy horyzontalnej w żelu agarozowym z chłodzeniem* Instrukcja Obsługi Numer katalogowy: 130-100 Numer katalogowy: 131-100* Aby uzys k ać pomoc techniczną (+48) 22 668 71 47
* SubDNA Zestaw do elektroforezy horyzontalnej w żelu agarozowym z chłodzeniem* Instrukcja Obsługi Numer katalogowy: 130-100 Numer katalogowy: 131-100* Aby uzys k ać pomoc techniczną (+48) 22 668 71 47
1 ekwiwalent 1 ekwiwalent
 PREPARAT NR 1 1,1 -BINAFTYLO-2,2 -DIOL FeCl 3 *6H 2 O H 2 O, t. wrz. Stechiometria reakcji Chlorek żelaza(iii) sześciowodny 1 ekwiwalent 1 ekwiwalent Dane do obliczeń Związek molowa (g/mol) Gęstość (g/ml)
PREPARAT NR 1 1,1 -BINAFTYLO-2,2 -DIOL FeCl 3 *6H 2 O H 2 O, t. wrz. Stechiometria reakcji Chlorek żelaza(iii) sześciowodny 1 ekwiwalent 1 ekwiwalent Dane do obliczeń Związek molowa (g/mol) Gęstość (g/ml)
Kuratorium Oświaty w Lublinie ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJUM ROK SZKOLNY 2016/2017 ETAP TRZECI
 Kuratorium Oświaty w Lublinie.. Imię i nazwisko ucznia Pełna nazwa szkoły Liczba punktów ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJUM ROK SZKOLNY 2016/2017 ETAP TRZECI Instrukcja dla ucznia
Kuratorium Oświaty w Lublinie.. Imię i nazwisko ucznia Pełna nazwa szkoły Liczba punktów ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJUM ROK SZKOLNY 2016/2017 ETAP TRZECI Instrukcja dla ucznia
CHROMATOGRAFIA ADSORPCYJNA I PODZIAŁOWA. 1. Rozdział barwników roślinnych metodą chromatografii adsorpcyjnej (techniką kolumnową)
 Ćwiczenie nr 7 CHROMATOGRAFIA ADSORPCYJNA I PODZIAŁOWA 1. Rozdział barwników roślinnych metodą chromatografii adsorpcyjnej (techniką kolumnową) Zasada: Barwniki roślinne charakteryzują się różnym powinowactwem
Ćwiczenie nr 7 CHROMATOGRAFIA ADSORPCYJNA I PODZIAŁOWA 1. Rozdział barwników roślinnych metodą chromatografii adsorpcyjnej (techniką kolumnową) Zasada: Barwniki roślinne charakteryzują się różnym powinowactwem
Wpływ ilości modyfikatora na współczynnik retencji w technice wysokosprawnej chromatografii cieczowej
 Wpływ ilości modyfikatora na współczynnik retencji w technice wysokosprawnej chromatografii cieczowej WPROWADZENIE Wysokosprawna chromatografia cieczowa (HPLC) jest uniwersalną techniką analityczną, stosowaną
Wpływ ilości modyfikatora na współczynnik retencji w technice wysokosprawnej chromatografii cieczowej WPROWADZENIE Wysokosprawna chromatografia cieczowa (HPLC) jest uniwersalną techniką analityczną, stosowaną
Genomic Mini AX Milk Spin
 Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Zakład Chemii Organicznej, Wydział Chemii UMCS Strona 1
 PREPARAT NR 20 KWAS 2JODOBENZOESOWY NH 2 NaNO 2, HCl Woda, < 5 o C, 15 min N 2 Cl KI Woda, < 5 o C, potem 50 o C, 20 min I Stechiometria reakcji Kwas antranilowy Azotyn sodu Kwas solny stężony 1 ekwiwalent
PREPARAT NR 20 KWAS 2JODOBENZOESOWY NH 2 NaNO 2, HCl Woda, < 5 o C, 15 min N 2 Cl KI Woda, < 5 o C, potem 50 o C, 20 min I Stechiometria reakcji Kwas antranilowy Azotyn sodu Kwas solny stężony 1 ekwiwalent
1 ekwiwalent 1 ekwiwalent
 PREPARAT NR 32 4-[BENZYLIDENOAMINO]FENOL HO NH 2 PhCHO Etanol, t. wrz., 1,5 godz. N HO Stechiometria reakcji p-aminofenol Aldehyd benzoesowy 1 ekwiwalent 1 ekwiwalent Dane do obliczeń Związek molowa (g/mol)
PREPARAT NR 32 4-[BENZYLIDENOAMINO]FENOL HO NH 2 PhCHO Etanol, t. wrz., 1,5 godz. N HO Stechiometria reakcji p-aminofenol Aldehyd benzoesowy 1 ekwiwalent 1 ekwiwalent Dane do obliczeń Związek molowa (g/mol)
ANALIZA PORÓWNAWCZA IZOFORM PEROKSYDAZY W KOLE- OPTYLACH OWSA METOD
 ANALIZA PORÓWNAWCZA IZOFORM PEROKSYDAZY W KOLE- OPTYLACH OWSA METODĄ ELEKTROFOREZY W śelu POLIAKRYLOAMIDOWYM. WYBARWIANIE ROZDZIELONYCH BIAŁEK COOMASSIE BRILLANT BLUE-G250 WSTĘP Powstawanie nadtlenku wodoru
ANALIZA PORÓWNAWCZA IZOFORM PEROKSYDAZY W KOLE- OPTYLACH OWSA METODĄ ELEKTROFOREZY W śelu POLIAKRYLOAMIDOWYM. WYBARWIANIE ROZDZIELONYCH BIAŁEK COOMASSIE BRILLANT BLUE-G250 WSTĘP Powstawanie nadtlenku wodoru
Zestaw dydaktyczny. genotypowanie szczepów 5taphy/ococcus aureus metodą PCR-RFLP
 2014-07-17 Zestaw dydaktyczny EasyGenotyping PCR-RFLP - S. aureus genotypowanie szczepów 5taphy/ococcus aureus metodą PCR-RFLP Celem ćwiczenia jest przeprowadzenie typowania genetycznego dostarczonych
2014-07-17 Zestaw dydaktyczny EasyGenotyping PCR-RFLP - S. aureus genotypowanie szczepów 5taphy/ococcus aureus metodą PCR-RFLP Celem ćwiczenia jest przeprowadzenie typowania genetycznego dostarczonych
Współczesne metody chromatograficzne: Chromatografia cienkowarstwowa
 Ćwiczenie 2: Chromatografia dwuwymiarowa (TLC 2D) 1. Celem ćwiczenia jest zaobserwowanie rozdziału mieszaniny aminokwasów w dwóch układach rozwijających. Aminokwasy: Asp, Cys, His, Leu, Ala, Val (1% roztwory
Ćwiczenie 2: Chromatografia dwuwymiarowa (TLC 2D) 1. Celem ćwiczenia jest zaobserwowanie rozdziału mieszaniny aminokwasów w dwóch układach rozwijających. Aminokwasy: Asp, Cys, His, Leu, Ala, Val (1% roztwory
ĆWICZENIA Z BIOLOGII MOLEKULARNEJ
 UNIWERSYTET MARII CURIE-SKŁODOWSKIEJ WYDZIAŁ BIOLOGII I BIOTECHNOLOGII ZAKŁAD BIOLOGII MOLEKULARNEJ ĆWICZENIA Z BIOLOGII MOLEKULARNEJ (załącznik do ćwiczeń) dla studentów II roku biologii oraz III roku
UNIWERSYTET MARII CURIE-SKŁODOWSKIEJ WYDZIAŁ BIOLOGII I BIOTECHNOLOGII ZAKŁAD BIOLOGII MOLEKULARNEJ ĆWICZENIA Z BIOLOGII MOLEKULARNEJ (załącznik do ćwiczeń) dla studentów II roku biologii oraz III roku
Zestaw do wykrywania Chlamydia trachomatis w moczu lub w kulturach komórkowych
 Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
ĆWICZENIE 5 Barwniki roślinne. Ekstrakcja barwników asymilacyjnych. Rozpuszczalność chlorofilu
 ĆWICZENIE 5 Barwniki roślinne Ekstrakcja barwników asymilacyjnych 400 mg - zhomogenizowany w ciekłym azocie proszek z natki pietruszki 6 ml - etanol 96% 2x probówki plastikowe typu Falcon na 15 ml 5x probówki
ĆWICZENIE 5 Barwniki roślinne Ekstrakcja barwników asymilacyjnych 400 mg - zhomogenizowany w ciekłym azocie proszek z natki pietruszki 6 ml - etanol 96% 2x probówki plastikowe typu Falcon na 15 ml 5x probówki
Genomic Mini AX Plant Spin
 Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
PARAMETRY TECHNICZNE PRZEDMIOTU ZAMÓWIENIA
 Załącznik nr 1A.do SIWZ PARAMETRY TECHNICZNE PRZEDMIOTU ZAMÓWIENIA Zadanie nr 1. AUTOKLAW Objętość Ciśnienie robocze Płaszcz grzejny Manometr Inne Katedra Chemii - 200 ml 100 bar a) z regulatorem temperatury
Załącznik nr 1A.do SIWZ PARAMETRY TECHNICZNE PRZEDMIOTU ZAMÓWIENIA Zadanie nr 1. AUTOKLAW Objętość Ciśnienie robocze Płaszcz grzejny Manometr Inne Katedra Chemii - 200 ml 100 bar a) z regulatorem temperatury
Genomic Midi AX. 20 izolacji
 Genomic Midi AX Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura z precypitacją DNA. wersja 0517 20 izolacji Nr kat. 895-20 Pojemność kolumny do oczyszczania
Genomic Midi AX Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura z precypitacją DNA. wersja 0517 20 izolacji Nr kat. 895-20 Pojemność kolumny do oczyszczania
GeneMATRIX Agarose-Out DNA Purification Kit
 Wersja zestawu 7.1 Kwiecień 2019 GeneMATRIX Agarose-Out DNA Purification Kit Uniwersalny zestaw do izolacji DNA z żeli agarozowych kat. nr. E3540 EURx Ltd. 80-297 Gdansk Poland ul. Przyrodnikow 3, NIP
Wersja zestawu 7.1 Kwiecień 2019 GeneMATRIX Agarose-Out DNA Purification Kit Uniwersalny zestaw do izolacji DNA z żeli agarozowych kat. nr. E3540 EURx Ltd. 80-297 Gdansk Poland ul. Przyrodnikow 3, NIP
KARTA CHARAKTERYSTYKI
 62 200 Gniezno, ul. Pałucka 2733 tel./fax. (061) 667 53 33 do 34 Data aktualizacji: 2009.01.12 Data wydruku: 2009.01.12 KARTA CHARAKTERYSTYKI (podstawa: Rozporządzenie MZ. Dz. U. Nr 140. poz. 1171 z dnia
62 200 Gniezno, ul. Pałucka 2733 tel./fax. (061) 667 53 33 do 34 Data aktualizacji: 2009.01.12 Data wydruku: 2009.01.12 KARTA CHARAKTERYSTYKI (podstawa: Rozporządzenie MZ. Dz. U. Nr 140. poz. 1171 z dnia
Elementy enzymologii i biochemii białek. Skrypt dla studentów biologii i biotechnologii
 Elementy enzymologii i biochemii białek Skrypt dla studentów biologii i biotechnologii NR 166 Danuta Wojcieszyńska, Urszula Guzik Elementy enzymologii i biochemii białek Skrypt dla studentów biologii i
Elementy enzymologii i biochemii białek Skrypt dla studentów biologii i biotechnologii NR 166 Danuta Wojcieszyńska, Urszula Guzik Elementy enzymologii i biochemii białek Skrypt dla studentów biologii i
LABORATORIUM Z KATALIZY HOMOGENICZNEJ I HETEROGENICZNEJ WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej
 Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej Wprowadzenie: Większość lądowych organizmów kręgowych część jonów amonowych NH + 4, produktu rozpadu białek, wykorzystuje w biosyntezie
Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej Wprowadzenie: Większość lądowych organizmów kręgowych część jonów amonowych NH + 4, produktu rozpadu białek, wykorzystuje w biosyntezie
Genomic Mini AX Bacteria+ Spin
 Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
Plasmid Mini. 50 izolacji, 250 izolacji. Zestaw do izolacji plazmidów wysokokopijnych wersja Nr kat ,
 Plasmid Mini Zestaw do izolacji plazmidów wysokokopijnych wersja 1016 50 izolacji, 250 izolacji Nr kat. 020-50, 020-250 Pojemność kolumny do oczyszczania DNA wynosi 20 µg. 1 Skład zestawu Składnik 50 izolacji
Plasmid Mini Zestaw do izolacji plazmidów wysokokopijnych wersja 1016 50 izolacji, 250 izolacji Nr kat. 020-50, 020-250 Pojemność kolumny do oczyszczania DNA wynosi 20 µg. 1 Skład zestawu Składnik 50 izolacji
PEHAMETRIA I ROZTWORY BUFOROWE
 4. PEHAMETRIA I ROZTWORY BUFOROWE 1. Sporządzanie i oznaczanie buforu octanowego Pehametria jest analizą instrumentalną, słuŝącą do potencjometrycznego bezpośredniego pomiaru wskaźnika stęŝenia jonów H
4. PEHAMETRIA I ROZTWORY BUFOROWE 1. Sporządzanie i oznaczanie buforu octanowego Pehametria jest analizą instrumentalną, słuŝącą do potencjometrycznego bezpośredniego pomiaru wskaźnika stęŝenia jonów H
PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika
 PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika Spis treści 1. Zawartość 2 1.1 Składniki zestawu 2 2. Opis produktu 2 2.1 Założenia metody 2 2.2 Instrukcja 2 2.3 Specyfikacja
PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika Spis treści 1. Zawartość 2 1.1 Składniki zestawu 2 2. Opis produktu 2 2.1 Założenia metody 2 2.2 Instrukcja 2 2.3 Specyfikacja
INFORMACJE O ZAGROŻENIACH SUBSTANCJAMI CHEMICZNYMI ĆWICZENIE 20
 INFORMACJE O ZAGROŻENIACH SUBSTANCJAMI CHEMICZNYMI ĆWICZENIE 20 Wykaz substancji: 1. KMnO 4 2. 10% roztwór H 2 O 2 3. acetyloaceton 4. etanol 5. CH 3 COONa 6. Fe(NO 3 ) 3 9H 2 O 7. Co(NO 3 ) 2 6H 2 O 8.
INFORMACJE O ZAGROŻENIACH SUBSTANCJAMI CHEMICZNYMI ĆWICZENIE 20 Wykaz substancji: 1. KMnO 4 2. 10% roztwór H 2 O 2 3. acetyloaceton 4. etanol 5. CH 3 COONa 6. Fe(NO 3 ) 3 9H 2 O 7. Co(NO 3 ) 2 6H 2 O 8.
Inżynieria Środowiska
 ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
Elektroforeza kapilarna oznaczanie benzoesanu sodu w próbkach wodnych + +
 Elektroforeza kapilarna oznaczanie benzoesanu sodu w próbkach wodnych Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu Łódzkiego. 1. Wstęp Zjawisko elektroforezy polega na poruszaniu
Elektroforeza kapilarna oznaczanie benzoesanu sodu w próbkach wodnych Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu Łódzkiego. 1. Wstęp Zjawisko elektroforezy polega na poruszaniu
Ilościowa analiza mieszaniny alkoholi techniką GC/FID
 Ilościowa analiza mieszaniny alkoholi techniką GC/FID WPROWADZENIE Pojęcie chromatografii obejmuje grupę metod separacji substancji, w których występują diw siły: siła powodująca ruch cząsteczek w określonym
Ilościowa analiza mieszaniny alkoholi techniką GC/FID WPROWADZENIE Pojęcie chromatografii obejmuje grupę metod separacji substancji, w których występują diw siły: siła powodująca ruch cząsteczek w określonym
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak)
 Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 CZĘŚĆ PRAKTYCZNA
 Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2018 Nazwa kwalifikacji: Przygotowywanie sprzętu, odczynników chemicznych i próbek do badań analitycznych
Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2018 Nazwa kwalifikacji: Przygotowywanie sprzętu, odczynników chemicznych i próbek do badań analitycznych
KINETYKA HYDROLIZY SACHAROZY (REAKCJA ENZYMATYCZNA I CHEMICZNA)
 Ćwiczenie nr 2 KINETYKA HYDROLIZY SACHAROZY (REAKCJA ENZYMATYCZNA I CHEMICZNA) ĆWICZENIE PRAKTYCZNE I. Kinetyka hydrolizy sacharozy reakcja chemiczna Zasada: Sacharoza w środowisku kwaśnym ulega hydrolizie
Ćwiczenie nr 2 KINETYKA HYDROLIZY SACHAROZY (REAKCJA ENZYMATYCZNA I CHEMICZNA) ĆWICZENIE PRAKTYCZNE I. Kinetyka hydrolizy sacharozy reakcja chemiczna Zasada: Sacharoza w środowisku kwaśnym ulega hydrolizie
PARAMETRY TECHNICZNE I ILOŚCIOWE PRZEDMIOTU NINIEJSZEGO POSTĘPOWANIA
 Znak sprawy: 13/G/2016 Załącznik nr 2 PARAMETRY TECHNICZNE I ILOŚCIOWE PRZEDMIOTU NINIEJSZEGO POSTĘPOWANIA 1. [APARAT DO AUTOMATYCZNEJ IZOLACJI KWASÓW NUKLEINOWYCH] MagCore HF16Plus szt.1 / NIE 1 Automatyczna
Znak sprawy: 13/G/2016 Załącznik nr 2 PARAMETRY TECHNICZNE I ILOŚCIOWE PRZEDMIOTU NINIEJSZEGO POSTĘPOWANIA 1. [APARAT DO AUTOMATYCZNEJ IZOLACJI KWASÓW NUKLEINOWYCH] MagCore HF16Plus szt.1 / NIE 1 Automatyczna
A4.05 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.05 nstrukcja wykonania ćwiczenia Wyznaczanie współczynników aktywności soli trudno rozpuszczalnej metodą pomiaru rozpuszczalności Zakres zagadnień obowiązujących
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.05 nstrukcja wykonania ćwiczenia Wyznaczanie współczynników aktywności soli trudno rozpuszczalnej metodą pomiaru rozpuszczalności Zakres zagadnień obowiązujących
Genomic Mini AX Body Fluids zestaw do izolacji DNA z płynów ustrojowych wersja 1115
 Genomic Mini AX Body Fluids zestaw do izolacji DNA z płynów ustrojowych wersja 1115 20 izolacji Nr kat. 052-20M tel: +48 58 7351194, fax: +48 58 6228578 info@aabiot.com www.aabiot.com 1 Skład zestawu Składnik
Genomic Mini AX Body Fluids zestaw do izolacji DNA z płynów ustrojowych wersja 1115 20 izolacji Nr kat. 052-20M tel: +48 58 7351194, fax: +48 58 6228578 info@aabiot.com www.aabiot.com 1 Skład zestawu Składnik
Zakłady Chemiczne EmiChem P.P.
 KARTA CHARAKTERYSTYKI PREPARATU CHEMICZNEGO Karta charakterystyki zgodna z wymogami przepisów Rozporządzenia (WE) NR 1907/2006 Europejskiego z dnia 18 grudnia 2006. r. (REACH) Parlamentu 1. IDENTYFIKACJA
KARTA CHARAKTERYSTYKI PREPARATU CHEMICZNEGO Karta charakterystyki zgodna z wymogami przepisów Rozporządzenia (WE) NR 1907/2006 Europejskiego z dnia 18 grudnia 2006. r. (REACH) Parlamentu 1. IDENTYFIKACJA
Zestaw do oczyszczania DNA po reakcjach enzymatycznych. Nr kat. EM03 Wersja zestawu:
 Zestaw do oczyszczania DNA po reakcjach enzymatycznych Nr kat. EM03 Wersja zestawu: 1.2012 I. PRZEZNACZENIE ZESTAWU Zestaw EXTRACTME DNA CLEAN-UP przeznaczony jest do szybkiego i wydajnego oczyszczania
Zestaw do oczyszczania DNA po reakcjach enzymatycznych Nr kat. EM03 Wersja zestawu: 1.2012 I. PRZEZNACZENIE ZESTAWU Zestaw EXTRACTME DNA CLEAN-UP przeznaczony jest do szybkiego i wydajnego oczyszczania
Mechanizm działania buforów *
 Mechanizm działania buforów * UNIWERSYTET PRZYRODNICZY Z doświadczenia nabytego w laboratorium wiemy, że dodanie kropli stężonego kwasu do 10 ml wody powoduje gwałtowny spadek ph o kilka jednostek. Tymczasem
Mechanizm działania buforów * UNIWERSYTET PRZYRODNICZY Z doświadczenia nabytego w laboratorium wiemy, że dodanie kropli stężonego kwasu do 10 ml wody powoduje gwałtowny spadek ph o kilka jednostek. Tymczasem
