GROMADA VI-7 SIARCZANY I SIARCZYNY
|
|
|
- Mikołaj Wiśniewski
- 9 lat temu
- Przeglądów:
Transkrypt
1 GROMADA VI-7 SIARCZANY I SIARCZYNY Podstawowym elementem struktury jest anion [SO 4 ] 2-. Powstają w niskich temperaturach w środowisku utleniającym; są produktami utworów hipergenicznych, zwłaszcza ewaporacji wód morskich i jeziornych. Wiele siarczanów metali cięŝkich powstaje w strefie utlenienia kruszców. KLASA 2. SIARCZANY BEZWODNE Siarczany pojedyncze krystalizują w układzie rombowym, w klasie bipiramidy rombowej mmm. Anhydryt CaSO 4 - pokrój tabliczkowy, słupowy, - skupienia ziarniste, zbite, pręcikowe lub włókniste; często skupienia w halicie (trzewiowiec), - tw. 3.5; łupliwość doskonała (010) i (100), - bezbarwny, biały, szary, niebieski, czerwonawy, czasem niemal czarny; połysk szklisty lub perłowy rozpuszcza się w HCl i H 2 SO 4, pod wpływem wody przechodzi w gips, - niektóre okazy wykazują czerwoną luminescencję, - jest rozpowszechnionym składnikiem skał solnych i innych skał osadowych, takŝe powstaje w utworach hydrotermalnych niskich temperatur, - współwystępuje z gipsem, halitem, polihalitem i inymi siarczanami z K-Mg złóŝ soli. - występowanie w Polsce: skały anhydrytowe i anhydrytowo-gipsowe w niecce północnosudeckiej, skały cechsztyńskie NiŜu Polskiego (Kłodawa, Inowrocław), osady mioceńskie przedkarpacia (Wieliczka, Bochnia, Barycz). Celestyn SrSO 4 - kryształy tabliczkowe i słupkowe, szczotki krystaliczne, - skupienia ziarniste, włókniste, zbite, - tw ; łupliwość doskonała (001), - bezbarwny, biały, często niebieskawy, czasem Ŝółty, czerwony; połysk szklisty, perłowy, - niektóre okazy wykazują luminescencję, - jest minerałem utworów osadowych, rzadziej spotykany w hydrotermalnych, - parageneza: siarka, kalcyt, aragonit, - występuje w pogipsowych osadach węglanowych, w marglach kredowych i K-Mg złoŝach soli (Tarnobrzeg, Czarkowice, Swoszowice, Kazimierz n/wisłą). Baryt BaSO 4 - pokrój kryształów i skupień ziarnistych tabliczkowy, - tw ; łupliwość doskonała (001), - minerał cięŝki cwł. 4,48 g/cm 3, - bezbarwny, biały lub zabarwiony na szaro, Ŝółto, niebiesko, czerwono, brązowo; połysk szklisty lub perłowy, - czasem wykazuje luminescencję, - pochodzenie hydrotermalne (raczej niskie temperatury), rzadziej w utworach osadowych czy wietrzeniowych, - paragenza: minerały kruszcowe, zwłaszcza galena, kalcyt, fluoryt, kwarc, - występowanie w Polsce: Boguszów k/wałbrzycha, Stanisławów k/jawora, Góry Świętokrzyskie.
2 Anglezyt PbSO 4 - kryształy słupowe, tabliczkowe, bipiramidalne; pseudomorfozy po galenie, - skupienia ziarniste, naskorupienia na galenie, - tw. 3.0; łupliwość niewyraźna, - biały, szary; silny połysk- diamentowy, jedwabisty, - jest minerałem utworów hydrotermalnych, powstaje w strefie utlenienia kruszców Pb, - współwystępuje z galeną, cerusytem, tlenowodorotlenkami Fe. Glauberyt CaNa 2 [SO 4 ] 2 - układ jednoskośny, - tabliczki lub słupki; skupienia ziarniste, - tw. 2-3; przełam muszlowy, - bezbarwny, szary; połysk szklisty lub woskowy, - jest składnikiem ewaporatów morskich, - współwystępuje z halitem, sylwinem, karnalitem i innymi solami K-Mg złóŝ soli (Kłodawa). Langbeinit K 2 Mg 2 [SO 4 ] 3 i Glaseryt K 3 Na[SO 4 ] 2 często występują w skupieniach drobnoziarnistych, średnia twardość 3-4, bezbarwne, białawe, Ŝółtawe, czerwone, o szklistym połysku. Często tworzą wykwity w ewaporatach morskich i jeziornych. Występują w K-Mg złoŝach soli. KLASA 3. SIARCZANY BEZWODNE ZAWIERAJĄCE INNY ANION Oprócz anionu (SO 4 ) 2- zawierają takŝe anion (OH) - lub Cl -, O 2-, F - [CO 3 ] 2_. Najczęściej występują w strefie utlenienia, takŝe w obszarach działalności ekshalacji wulkanicznej, a takŝe roztworów hydrotermalnych, najczęściej niskich temperatur. Wiele z nich powstaje jako ewaporaty jeziorne. Ałunit Kal 3 [(OH) 6 (SO 4 ) 2 ] - kryształy romboedryczne kostki, tabliczki, - skupienia ziarniste, zbite lub włókniste, - tw ; łupliwość dobra (001), - biały, często szaro, Ŝółtawo, czerwonawo lub brunatnie zabarwiony; połysk szklisty lub perłowy, ziemisty, - jest produktem działalności powulkanicznej; powstaje wskutek oddziaływania wód siarczanowych na skały magmowe ałunityzacja skaleni potasowych. Znany jest takŝe z utworów hydrotermalnych i osadowych takŝe ewaporatów morskich. Jarosyty to nazwa na roztwory stałe między następującymi ogniwami: Jarosyt KFe 3 [(OH) 6 (SO 4 ) 2 ] natrojarosyt NaFe 3 [(OH) 6 (SO 4 ) 2 ] - hydroniojarosyt (H 3 O)[(OH) 6 (SO 4 ) 2 ] - kryształy romboedryczne, tabliczkowe - sk. ziarniste, włókniste, łuskowe, naskorupienia, naloty, - tw ; niewyraźna łupliwość, - barwa Ŝółta, brązowa, ochrowoŝółta lub brunatnoczarna; połysk szklisty lub ziemisty, - w dotyku tłusty; nie rozpuszcza się w wodzie (jak podobny do niego copiapit), rozpuszcza się w HCl, - jest produktem przeobraŝeń pirytu lub markasytu, - występuje w łupkach menilitowych, gnejsach, w wyrobiskach kopalń kruszców i węgla, - współwystępuje z ałunitem i uwodnionymi siarczanami Ŝelaza. 2
3 Brochantyt Cu 4 [(OH) 6 SO 4 ] - kryształy słupowe, - częściej skupienia igiełkowe, włókniste lub ziarniste, - tw ; przełam muszlowy, - barwa szmaragdowa, zielona (jasno-lub ciemnozielona); połysk szklisty lub perłowy, - powstaje w strefie utlenienia kruszców Cu, zwłaszcza w klimacie suchym, - parageneza: azuryt, malachit, kupryt, tenoryt, atacamit, chryzokola. KLASA 4. SIARCZANY UWODNIONE Są to minerały strefy utlenienia oraz produkty ewaporatów. Ilość drobin wody od 0,5 H 2 O do 18 H 2 O. Proste siarczany uwodnione: Gips CaSO 4 2H 2 O - klasa słupa jednoskośnego 2/m, - pokrój kryształów najczęściej tabliczkowy, słupowy (znanych jest około 70 postaci), najczęściej ściany (010), (110), (111); często zbliźniaczony (100), (010) jaskółcze ogony, - skupienia bezbarwne, przezroczyste i grubotabliczkowe selenit, skupienia włókniste szpak gipsowy, tworzy takŝe skupienia rozetkowe, drobnowłókniste, z wrostkami ziaren piasku róŝe pustyni oraz skupienia drobnoziarniste, zbite- alabaster, - tw ; łupliwość doskonała(010), - bezbarwny; domieszki zabarwiają go na biało, szaro, Ŝółtawo, brązowo lub niebieskawo, - rozpuszcza się w gorącym HCl, - jest minerałem wtórnym, krystalizuje z wody morskiej (T niŝsza niŝ dla krystalizacji anhydrytu), powstaje równieŝ jako produkt hydratacji anhydrytu; jest składnikiem skał anhydrytowo-gipsowych i pospolitym składnikiem skał solnych, - jest produktem wietrzenia siarczków; znany jest takŝe z utworów hydrotermalnych, - parageneza: siarka, halit, aragonit, anhydryt, celestyn, Kizeryt MgSO 4 H 2 O - najczęściej występuje w skupieniach ziarnistych, takŝe zbitych, - tw. 3.5, - biały, Ŝółtawy, brunatny, czerwony; połysk szklisty lub perłowy, - łatwo rozpuszcza się w wodzie, absorbuje wilgoć i przechodzi w epsomit, - jest składnikiem ewaporatów morskich, - występuje w K-Mg złoŝach soli. Rozenit FeSO 4 4H 2 O - najczęściej tworzy wykwity na wietrzejących siarczkach Fe; tworzy takŝe skupienia zbite i ziemiste, - bezbarwny, białawy; połysk szklisty (dla skupień ziemistych matowy). Chalkantyt CuSO 4 5H 2 O - układ trójskośny, - kryształy o pokroju grubotabliczkowym, krótkosłupowym, - często tworzy naloty, naskorupienia, nacieki, - tw. 2.5, - barwa niebieska; połysk szklisty, - łatwo rozpuszcza siew wodzie, - powstaje w strefie utlenienia kruszców miedzi. 3
4 Melanteryt FeSO 4 7H 2 O - kryształy krótkosłupowe, tabliczkowe, - często skupienia naciekowe, naskorupienia, skupienia proszkowe, - tw. 2.0, - barwa zielona, Ŝółtozielona; połysk szklisty, - na powietrzu traci wodę i rozsypuje się na proszek, - występuje w strefie utlenienia kruszców Ŝelaza i wśród skał zawierających piryt lub markasyt, - parageneza: piryt, markasyt, epsomit, halotrichit, copiapit. Epsomit MgSO 4 7H 2 O - najczęściej wykształcony w postaci skupień włóknistych, naskorupień, stalaktytów, - nacieków, skupień ziemistych lub proszkowych, - tw , - bezbarwny, czasem zabarwiony na Ŝółtawo, zielonawo, czerwonawo; połysk jedwabisty, - na powietrzu traci wodę i matowieje; smak gorzki, rozpuszcza się w wodzie, - rozpowszechniony w strefie przeobraŝeń minerałów i skał, z których uruchomiona została siarka; pospolity na hałdach i w wyrobiskach górniczych, znany z K-M złóŝ soli, - paragenza: melanteryt, halotrichit, kizeryt. Mirabilit Na 2 SO 4 10H 2 O - znany pod nazwą sól glauberska, - krótkie słupki lub igiełki; często skupienia zbite, naskorupienia, - tw , - bezbarwny lub biały; połysk szklisty, - na powietrzu ulega odwodnieniu i rozsypuje się na proszek; łatwo rozpuszcza się w kwasach, - smak kwaśnosłodki, - występuje wśród osadów słonych jezior i w złoŝach soli oceanicznej, - parageneza: gips, halit, thenardyt (Na 2 SO 4 ). Pikromeryt K 2 Mg[SO 4 ] 2 6Η 2 Ο, Syngenit K 2 Ca[SO 4 ] 2 H 2 O posiadają wiele wspólnych cech: - kryształy słupowe lub wydłuŝone tabliczki, skupienia ziarniste, - tw. 2.5, - bezbarwne lub zabarwione na odcienie róŝowawe; połysk szklisty, - występują w K-Mg złoŝach soli, - parageneza: polihalit, kainit, langbeinit. ZłoŜone siarczany uwodnione: Polihalit K 2 MgCa 2 [SO 4 ] 4 2H 2 O - kryształy tabliczkowe dość rzadko, - częściej skupienia włókniste, sferolity, skupienia ziarniste lub zbite, - tw. 3.5, - bezbarwny, róŝowy, czarny, Ŝółtawy, szarawy; połysk szklisty lub Ŝywiczny, - rozpuszcza się w wodzie, - minerał solnych ewaporatów morskich, - tworzy skały polihalitowe, - parageneza: halit, sylwin, gips, anhydryt. Halotrichit FeAl 2 [SO 4 ] 4 22H 2 O - kryształy igiełkowe lub włókniste, - skupienia zbite lub spilśnione (azbesty), 4
5 - tw. 1.5, - bezbarwny, białawy, Ŝółtawy, zielonawy; połysk szklisty lub jedwabisty, - łatwo rozpuszcza się w wodzie, pod wpływem powietrza łatwo się kruszy, - powstaje w strefie wietrzenia skał ilastych zawierających piryt lub markasyt; znany ze złóŝ węgla, - często współwystępuje z copiapitem. KLASA 5. SIARCZANY UWODNIONE ZAWIERAJĄCE INNY ANION Kainit KMg[Cl SO 4 ] 3H 2 O - kryształy tabliczkowe, - skupienia ziarniste, - tw ; łupliwość dokładna, - bezbarwny, szarawy, Ŝółty, czerwonawy, fioletowy; połysk szklisty, - smak gorzkosłony, łatwo rozpuszcza się w wodzie, - jest składnikiem ewaporatów solnych, - parageneza: sylwin, halit, karnalit i inne siarczany K-Mg. Copiapit (Fe 2+, Mg)Fe 3+ 4[OH (SO 4 ) 3 ] 2 20H 2 O - rzadko wykształca kryształy, - częściej tworzy luźne skupienia lub naskorupienia, skupienia zbite, - tw , - barwa Ŝółta do pomarańczowej lub zielonawej; połysk perłowy, - rozpuszcza się w wodzie, - współwystępuje z melanterytem, halotrichitem, pirytem i markasytem jako produkt przeobraŝenia tych siarczków. GROMADA VI-8 CHROMIANY I DWUCHROMIANY W tej grupie minerałów chrom występuje w anionie [CrO 4 ] 2- jako kation Cr 6+. Utlenienie chromu do jego najwyŝszego stopnia ma miejsce w środowisku o silnym potencjale utleniającym. W strefie utlenienia kruszców Pb, Pb-Ag, Pb-Cu lub Pb-Zb krystalizują chromiany metali cięŝkich. W przyrodzie występują głównie chromiany ołowiu. Krokoit PbCrO 4 - układ jednoskośny; klasa 2/m, - często wykształca kryształy o pokroju słupowym, - skupienia pręcikowe, ziarniste, powłoki na kruszcach, - tw , - minerał bardzo cięŝki cwł. 6,0 g/cm 3, - charakterystyczna pomarańczowoczerwona barwa i rysa; silny diamentowy połysk, - powstaje w strefie utlenienia galeny, - współwystępuje z cerusytem, piromorfitem, kwarcem. GROMADA VI-9 MOLIBDENIANY Molibdeniany powstają w warunkach bardzo wysokiego potencjału utleniającego z molibdenitu MoS 2 tworzy się wpierw tlenek molibdenu. W tej grupie minerałów występuje anion [MoO 4 ] 2-, w którym pierwiastek molibden jest utleniony do Mo 6+. W przyrodzie znane są molibdeniany Pb, Ca i Fe 3+. Najpowszechniej występuje wulfenit. Wulfenit PbMoO 4 - układ tetragonalny, 5
6 - kryształy tabliczkowe, bliźniaki, - skupienia siatkowe, ziarniste lub zbite, - tw. 3.0; łupliwość niewyraźna, przełam muszlowy, - minerał bardzo cięŝki - cwł. 6,8-7,0 g/cm 3, - barwa Ŝółta, miodowa, lekko czerwonawa; rysa biała; połysk diamentowy, tłusty, - występuje w strefie utlenienia galeny, - parageneza: galena, kalcyt, dolomit. GROMADA VI-10 WOLFRAMIANY Podobnie jak chromiany i molibdeniany to takŝe nieliczna grupa minerałów. W ich strukturze występuje anion [WO 4 ] 2-, a wolfram ma takŝe wartościowość (6+). Wolframiany powstają w utworach pneumatolitowych, hydrotermalich oraz w strefie metamorfizmu kontaktowego. Najpowszechniej występującymi w przyrodzie minerałami tej grupy są scheelit i wolframity. Ferberyt FeWO 4 - układ jednoskośny, - kryształy tabliczkowe, słupowe, - skupienia ziarniste i zbite, - tw. 5.5; łupliwość doskonała, - barwa czarna, szaroczarna; rysa ciemnobrązowa do czarnej; połysk półmetaliczny, matowy, - minerał bardzo cięŝki cwł. 6,8-7,5 g/cm 3, - utwory pneumatolitowe, hydrotermalne; jest częstym składnikiem pegmatytów, - parageneza: scheelit, topaz, turmaliny, kasyteryt, beryl, molibdenit, miki litowe. - Hübneryt MnWO 4 - układ jednoskośny, - kryształy płytkowe, - skupienia płytkowe, półkuliste, - tw. 5,0; łupliwość doskonała, - barwa brunatnoczerwona lub brunatnoczarna; rysa brązowa, zielonkawoszara; połysk półmetaliczny, matowy, - minerał bardzo cięŝki cwł. 6,4-7,1 g/cm 3, - utwory pneumatolitowe, hydrotermalne; jest częstym składnikiem pegmatytów, - parageneza: scheelit, topaz, turmaliny, kasyteryt, beryl, molibdenit, miki litowe, Wolframit (Fe,Mn)WO 4 - jest środkowym członem szeregu izomorficznego ferberyt hübneryt - układ jednoskośny - kryształy tabliczkowe, słupowe, - skupienia zbite i ziarniste, - tw ; doskonała łupliwość, - barwa czarna, ciemnobrązowa; rysa czarna, czarnobrązowa; połysk półmetaliczny, matowy, - minerał bardzo cięŝki cwł. 7,1-7,5 g/cm 3, - utwory pneumatolitowe, hydrotermalne; jest częstym składnikiem pegmatytów, - parageneza: scheelit, topaz, turmaliny, kasyteryt, beryl, molibdenit, miki litowe. 6
7 Scheelit CaWO 4 - układ tetragonalny, - kryształy bipiramidalne, piramidalne, tabliczkowe, - skupienia ziarniste, zbite, naskorupienia, - tw ; łupliwość niewyraźna, - barwa biała, Ŝółta, brązowa, czasem zielonkawa, czerwonawa; połysk diamentowy, tłusty, - silna luminescencja, - występuje w pegmatytach, utworach metamorfizmu kontaktowego i hydrotermalnych, - parageneza: wolframit, molibdenit, fluoryt, kwarc. GROMADA VI-11 FOSFORANY W grupie tej anion fosforanowy [PO 4 ] 3-, gdzie P 5+. Fosforany to jedna z najliczniejszych grup minerałów. Większość fosforanów to minerały utworów pegmatytowych, hydrotermalnych i osadowych. W wielu fosforanach występują dodatkowe aniony (OH) -, Cl -,(CO 3 ) 2_, (SO 4 ) 2-, (SiO 4 ) 4_, (AsO 4 ) 3_. KLASA 2. FOSFORANY BEZWODNE Minerały te związane są z krystalizacją pegmatytów litowych i berylowych oraz z ich strefami utlenienia. Monacyt CePO 4 - układ jednoskośny, - kryształy tabliczkowe, słupowe, - tw ; łupliwość wyraźna, - barwa brązowa, Ŝółta, czerwona, pomarańczowa,; rysa szarobiała; połysk diamentowy, - jest dość cięŝki cwł. 5g/cm 3, - zawiera domieszki lantanowców oraz Th wtedy jest minerałem radioaktywnym, - występuje w pegmatytach, granitach i gnejsach, - parageneza: ilmenit, rutyl, cyrkon, ksenotym, - jest odporny na działanie czynników klimatycznych, przechodzi do osadów mechanicznych piaski monacytowe. Ksenotym YPO 4 - układ teragonalny, - kryształy słupowe, bipiramidalne, tabliczkowe, - skupienia gruboziarniste i promieniste, - tw ; łupliwość doskonała, - barwa Ŝółtobrązowa, zielonkawa, szara, czerwona, rysa Ŝółtawobrązowa; połysk tłusty, szklisty, - jest dość cięŝkim minerałem cwł bliski 5g/cm 3, - zawiera liczne domieszki lantanowców, a takŝe Zr oraz uranu i thoru, co sprawia, Ŝe ma własności radioaktywne, - występuje w utworach pegmatytowych i osadowych - jest odporny na działanie czynników klimatycznych, przechodzi do osadów mechanicznych, - parageneza: monacyt, apatyt, fergusonit, cyrkon, gadolinit, uraninit. KLASA 3. FOSFORANY BEZWODNE ZAWIERAJĄCE INNY ANION Fluoroapatyt Ca 5 [F (PO 4 ) 3 ] - układ heksagonalny, - często wykształca kryształy o pokroju słupowym lub grubotabliczkowym, - tworzy takŝe skupienia ziarniste, zbite, skorupowe, ziemiste i oolitowe, - tw. 5.0; łupliwość niewyraźna, 7
8 - barwa: w zasadzie bezbarwny, lecz złoŝone przyczyny nadają mu zabarwienie białe, Ŝółtawozielone, zielone, niebieskawe, fioletowe, czerwone; połysk szklisty lub tłusty, - często zawiera domieszki lantanowców (nadaje się im lokalne nazwy), - bardzo często wykazuje luminescencję, - występuje w utworach pegmatytowych, pneumatolitowych, hydrotermalnych i osadowych, - tworzą skały magmowe neapit, apaneit -płw. Kola, - odporne na działanie czynników klimatycznych przechodzą do utworów osadowych, - parageneza: fluoryt, kasyteryt, topaz, - jest waŝnym składnikiem fosforytów. Apatyty to grupa fosforanów obejmująca fluoroapatyt a takŝe apatyt hydroksylowy Ca 5 [OH (PO 4 ) 3 ], apatyt chlorowy Ca 5 [Cl (PO 4 ) 3 ] i apatyt węglanowy Ca 5 [F (PO 4,CO 3,OH) 3 ]. Apatyty węglanowe i hydroksylowe budują organizmy zwierząt, nagromadzając się w osadach ilastych, mułkowych i piaszczystych. Bardzo drobnoziarnista mieszanina apatytu węglanowego, hydroksylowego i fluorowego tworzy kolofan, który jest głównym składnikiem apatytów. - tw.3,0-4,0, - barwa szara, brunatna, Ŝółtawa; połysk matowy. Pseudomalmachit Cu 5 [(OH) 2 PO 4 ] 2 - kryształy słupkowe rzadko, - częściej skupienia naciekowe, groniaste, stalaktyty, naskorupienia, - tw , - barwa ciemnoszmaragdowa, ciemnozielona; rysa zielona; połysk szklisty, tłusty, - powstaje w strefie utlenienia kruszców miedzi, - współwystępuje z azurytem, malachitem, innymi wtórnymi minerałami miedzi (cornvallit, olivenit, austinit), a takŝe kalcytem, chalcedonem. Piromorfit Pb 5 [Cl (PO 4 ) 3 ] - układ heksagonalny, - kryształy słupowe, czasem tabliczkowe, - skupienia ziarniste, sferolitowe, groniaste, - tw. 3,5-4,0; brak łupliwości; przełam muszlowy, - barwa zielona, Ŝółta, brązowa, Ŝółtawoczerwona; silny diamentowy połysk, - występuje w strefie utlenienia kruszców ołowiu, - często tworzy pseudomorfozy po galenie i cerusycie, - tworzy ciągły szereg izomorficzny z arsenianem ołowiu mimetezytem. KLASA 4. FOSFORANY UWODNIONE Minerały tej klasy powstają w warunkach hydrotermalnych oraz w strefie utlenienia. Waryscyt Al[PO 4 ] 2H 2 O - kryształy pseudoregularne, ośmiościenne rzadko, - częściej tworzy skupienia ziarniste, naskorupienia, skupienia nerkowate, groniaste, sferolitowe, - tw. 3.5; łupliwość wyraźna, - biały, zielony, niebieskawozielony; rysa biała; połysk szklisty, - tworzy się w warunkach hipergenicznych lub hydrotermalnych niskich temperatur, - współwystępuje z wavellitem, crandalitem, limonitem, - znany z Gór Świętokrzyskich. 8
9 Wiwianit Fe 2+ 3[PO 4 ] 8H 2 O - kryształy słupowe, tabliczkowe, - skupienia włókniste, promieniste, ziemiste, - tw. 2; łupliwość doskonała, - barwa biała szybko przechodząca w indygo lub niebieskoczarną; połysk szklisty lub perłowy, - powstaje z przeobraŝenia kruszców Ŝelaza, - znany z torfów, rud darniowych, - parageneza: syderyt, limonit. KLASA 5. FOSFORANY UWODNIONE ZAWIERAJĄCE INNY ANION Turkus CuAl 6 [(OH) 2 PO 4 ] 4 4H 2 O i Chalkosyderyt CuFe 6 [(OH) 2 PO 4 ] 4 4H 2 O Tworzą ciągły szereg izomorficzny. - kryształy bardzo rzadkie, słupowe, - najczęściej występuje w postaci skupień drobnokrystalicznych, zbitych, naskorupień i nacieków, - tw , - barwa od niebieskiej do zielonej; rysa biała lub zielonawa; połysk tłusty, - powstają w strefie wietrzenia, - parageneza: goethyt, chalcedon, kaolinit. Wavellit Al 3 [(OH) 3 (PO 4 ) 2 ] 5H 2 O - kryształy słupowe lub igiełkowe, - skupienia promieniste, włókniste, - tw ; łupliwość dokładna, - biały, Ŝółty, zielonkawy, niebieskawy, brązowy; rysa biała; połysk szklisty, perłowy lub jedwabisty, - krystalizuje z roztworów hydrotermalnych niskich temperatur; powstaje takŝe w strefie hipergenicznej, - parageneza: hematyt. GROMADA VI-12 ARSENINY I ARSENIANY W strukturze arseninów występuje anion [AsO 3 ] - i te minerały są rzadsze od arsenianów, w których występuje anion tetraedryczny [AsO 4 ] 3-. Występują w strefach kontaktowo-metasomatowych, ekshalacji wulkanicznych i w strefie utlenienia kruszców. KLASA3. ARSENIANY BEZWODNE ZAWIERAJĄCE INNY ANION Olivenit Cu[OH AsO 4 ] - kryształy słupowe, igiełkowe i tabliczkowe, - skupienia nerkowate, włókniste, ziemiste, - tw. 3.0, - barwa oliwkowozielone, brunatne, szarawe; połysk szklisty lub diamentowy, - powstaje w strefie utlenienia kruszców Cu. Mimetezyt Pb 5 [Cl (AsO 4 ) 3 ] - kryształy słupowe, tabliczkowe, - skupienia ziarniste, ziemiste i włókniste, - tw , 9
10 - barwa biała, Ŝółta, pomarańczowa, brązowa, zielona, szara; połysk diamentowy i tłusty, - parageneza: galena, piromorfit. KLASA 4 ARSENIANY UWODNIONE Erytryn Co 3 [AsO 4 ] 2 8H 2 O - kryształy słupowe, igiełkowe, - tworzy skupienia włóknisto-promieniste, wykwity kwiat kobaltowy, skupienia ziemiste i proszkowe, - tw , - barwa róŝowoczerwona, fiołkowa; połysk diamentowy, perłowy, - powstaje w strefie utlenienia kruszców Co. Annabergit Ni 3 [AsO 4 ] 2 8H 2 O - kryształy włoskowe, - wykwity kwiat niklowy - oraz naskorupienia, skupienia ziemiste i proszkowe, - tw , - barwa i rysa zielona; połysk szklisty, - powstaje w strefie utlenienia kruszców Ni. GROMADA VI-14 WANADANY Wanadynit Pb 5 [Cl (VO 4 ) 3 ] - kryształy słupowe z bipiramidą, - skupienia włókniste, ziarniste, - tw. 3.0; brak łupliwości, przełam muszlowy, - barwa Ŝółta, czerwona, brunatna; połysk diamentowy, - występuje w strefie utlenienia kruszców Pb, - parageneza: piromorfit, mimetezyt, wulfenit, cerusyt. 10
11 NajwaŜniejsze cechy omawianych minerałów: Nazwa Wzór Sposób występowania Anhydryt CaSO 4 sk.ziarniste, tabliczki, słupki Twardość Łupliwość Barwa/zabarwienie Parageneza Szczególna cecha 3,5 doskonała bezbarwny/nieb.czerw. gips, halit, - polihalit i innie siarczany K-Mg - Celestyn SrSO 4 słupki 3,0-3,5 doskonała bezbarwny/niebieski siarka, kalcyt, aragonit Baryt BaSO 4 kryształy i skupienia płytkowe Gips CaSO 2 2H 2O tabliczki i sk. tabliczkowe Melanteryt FeSO 4 7H 2O sk. ziarniste, proszkowe 3,0-3,5 doskonała bezbarwny/ŝółty/róŝowy galena, kalcyt, fluoryt, kwarc 1,5-2,0 doskonała bezbarwny/ŝółty siarka, aragonit, anhydryt, celestyn 2,0 - Ŝółty/zielony piryt, markasyt, epsomit, cocpiapit, halotruchit Polihalit K 2MgCa 2[SO 4] 4 2H 2O sk. ziarniste 3,5 - czerwonawy halit, sylwin, inne siarczany K-Mg Wolframity (Fe,Mn)WO 4 sk.ziarniste 5,0-5,5 doskonała brązowoczarny molibdenit scheelit, topaz, turmaliny, beryl, miki litowe Scheelit CaWO 4 sk.ziarniste 4,5-5,0 niewyraźna bezb. /czerwony, Ŝółty wolframit, molibdenit, fluoryt, kwarc Fluoroapatyt Fluoroapatyt Ca 5[F (PO 4) 3] kr. słupkowe 5,0 niewyraźna bezb./ŝółty, zielony niebieski, czerwony fluoryt, kasyteryt. topaz Pseudomalachit Cu 5[(OH) 2 PO 4] 2 sk. ziarniste 4,5-5,0 - szmaragdowy olivenit, cornwallit, malachit inne wtórne min Cu; kalcyt Turkus i CuAl 6[(OH) 2 PO 4] 4 4H 2O sk. ziarniste 3,5-4,0 - niebieska do zielonej geothyt, chalcedon chalkosyderyt CuFe 6[(OH) 2 PO 4] 4 4H 2O minerał cięŝki - na powietrzu rozsypuje się na proszek - czarnobrązowa rysa wł. luminesc. wł. luminesc
12 Zapamiętaj paragenezy: I.Minerały występujące w strefie utlenienia kruszców Fe: Tlenki i tlenowodorotlenkiŝelaza, syderyt, rozenit, melanteryt, jarosyty, halotrichit i copiapit II.Minerały wystepujące w strefie utlenienia kruszców Zn-Pb: Smitsonit, hydrocynkit, (hemimorfit), cerusyt, fosgenit, anglezyt, wanadynit, wulfenit, krokoit, piromorfit i mimetezyt. III.Minerały- ewaporaty wód morskich i jeziornych: Halit, sylwin, karnalit, bischofit, boraks rodzimy, kolemanit, anhydryt, langbeinit, glaseryt, glauberyt, kizeryt, epsomit, pikromeryt, polohalit, syngenit i kainit. IV. W strefie utlenienia kruszców Co erytryn Ni annabergit, Cu atacamit, azuryt, malachit, pseudomalachit, turkus, chalkosyderyt i chalkantyt, olivenit, austinit. GROMADA VI-15 MINERAŁY URANYLU. W warunkach podwyŝszonego potencjału utleniającego uran przechodzi od walencyjności U 4+, jaką posiada np. w uraninicie UO 2, do walencyjności U 6+. Tworzy się wtedy jon uranylowy [OU 2 ] 2+. Ten złoŝony kation krystalizuje w wodorotlenkach, węglanach, siarczanach, fosforanach, arsenianach, wanadanach, moliobdenianach i innych oraz w krzemianach. Kation [UO 2 ] 2+ występuje z grupą hydroksylową i anionem [CO 3 ] 2-, [SO 4 ] 2-. Becquerelit 6[UO 2 ][OH] 2 Ca(OH) 2 4H 2 O - kryształy heksagonalne, - tw. 2,0-3,0, - minerał cięŝki cwł. około 6g/cm 3, - barwa Ŝółta w róŝnych odcieniach, rysa Ŝółta; połysk tłusty, - jest minerałem promieniotwórczym, - występuje w strefie utlenienia uraninitu. Curit 3PbO 8UO 3 4H 2 O - kryształy igiełkowe, słupkowe, skupienia igiełkowe, zbite, ziemiste, - tw , - barwa i rysa pomiarańczowoczerwona; połysk szklisty, - strefa utlenienia uraninitu. Gummit - to mieszanina wodorotlenków uranylu, - skupienia zbite i naskorupienia, - tw , - barwa Ŝółta, pomarańczowa, czerwona, brunatna; połysk woskowy, tłusty, matowy i tłusty. Autunit Ca[UO 2 ][PO 4 ] 2 10(12-18)H 2 O Torbenit Cu[UO 2 ][PO 4 ] 2 10(12-18)H 2 O - tworzą kryształy tabliczkowe, 12
13 - skupienia łuskowe, - tw , - barwa intensywnie Ŝółta autunit i intensywnie zielona torbenit; połysk szklisty, - silnie promieniotwórcze, - występują w strefie utlenienia utworów hydrotermalnych i pegmatytów. Uranofan (H 3 O) 2 Ca[UO 2 ][SiO 4 ] 2 3H 2 O - słupki lub igiełki, - skupienia promieniste, włókniste i zbite, - tw , - barwa cytrynowa lub słomkowoŝółta; połysk szklisty, - występuje w strefie hipergenicznej. Opracowała: dr hab. Maria Czaja 13
GROMADA VI SOLE KWASÓW TLENOWYCH
 GROMADA VI SOLE KWASÓW TLENOWYCH Gromada ta obejmuje azotany, jodany i chlorany, węglany, telluryny i tellurany, borany, siarczany, chromiany i dwuchromiany, molibdeniany, wolframiany, fosforany, arseniny
GROMADA VI SOLE KWASÓW TLENOWYCH Gromada ta obejmuje azotany, jodany i chlorany, węglany, telluryny i tellurany, borany, siarczany, chromiany i dwuchromiany, molibdeniany, wolframiany, fosforany, arseniny
GLAUKONIT K 2 (Fe 3+, Al, Fe 2+, Mg) 4 (Si 7 AlO 20 )(OH) 4 (jednoskośny)
 GLAUKONIT K 2 (Fe 3+, Al, Fe 2+, Mg) 4 (Si 7 AlO 20 )(OH) 4 (jednoskośny) CECHA Forma/wykształcenie Łupliwość Relief glaukonit pseudoheksagonalne kryształy, rzadkie i źle wykształcone zwykle drobne łuseczki,
GLAUKONIT K 2 (Fe 3+, Al, Fe 2+, Mg) 4 (Si 7 AlO 20 )(OH) 4 (jednoskośny) CECHA Forma/wykształcenie Łupliwość Relief glaukonit pseudoheksagonalne kryształy, rzadkie i źle wykształcone zwykle drobne łuseczki,
MINERAŁY są podstawowymi składnikami, z których zbudowane są skały.
 2a. Minerały MINERAŁY są podstawowymi składnikami, z których zbudowane są skały. Pod tym określeniem ukrywają się powstałe w naturalnych procesach przebiegających w środowisku przyrodniczym Ziemi (na powierzchni
2a. Minerały MINERAŁY są podstawowymi składnikami, z których zbudowane są skały. Pod tym określeniem ukrywają się powstałe w naturalnych procesach przebiegających w środowisku przyrodniczym Ziemi (na powierzchni
Materiałoznawstwo optyczne KRYSZTAŁY
 Materiałoznawstwo optyczne KRYSZTAŁY Kryształy kryształ: ciało o prawidłowej budowie wewnętrznej, fizycznie i chemicznie jednorodne, anizotropowe, mające wszystkie wektorowe własności fizyczne jednakowe
Materiałoznawstwo optyczne KRYSZTAŁY Kryształy kryształ: ciało o prawidłowej budowie wewnętrznej, fizycznie i chemicznie jednorodne, anizotropowe, mające wszystkie wektorowe własności fizyczne jednakowe
Skały budujące Ziemię
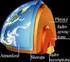 Skały budujące Ziemię Minerały Minerał pierwiastek lub związek chemiczny powstały w przyrodzie w sposób naturalny, jednorodny pod względem chemicznym i fizycznym. Minerały w większości mają budowę krystaliczną.
Skały budujące Ziemię Minerały Minerał pierwiastek lub związek chemiczny powstały w przyrodzie w sposób naturalny, jednorodny pod względem chemicznym i fizycznym. Minerały w większości mają budowę krystaliczną.
GROMADA V TLENKI I WODOROTLENKI
 GROMADA V TLENKI I WODOROTLENKI Zalicza się tu tlenki, wodorotlenki i tlenowodorotlenki, oprócz minerałów grupy SiO 2, które zostały włączone do krzemianów przestrzennych. W kryształach tych dominuje jonowy
GROMADA V TLENKI I WODOROTLENKI Zalicza się tu tlenki, wodorotlenki i tlenowodorotlenki, oprócz minerałów grupy SiO 2, które zostały włączone do krzemianów przestrzennych. W kryształach tych dominuje jonowy
asfaltowych warstw ścieralnych Dr inż. Bartłomiej Grzesik
 Przeobrażenia P b ż i mineralne i l w kruszywach k h naturalnych w kwaśnym środowisku asfaltowych warstw ścieralnych Dr inż. Bartłomiej Grzesik Geneza podjętej problematyki Darłowo Zieluń Żuromin Siemiątkowo
Przeobrażenia P b ż i mineralne i l w kruszywach k h naturalnych w kwaśnym środowisku asfaltowych warstw ścieralnych Dr inż. Bartłomiej Grzesik Geneza podjętej problematyki Darłowo Zieluń Żuromin Siemiątkowo
Test z geologii. 4) Jaka panuje stała temperatura w naszym klimacie na głębokości 26 m? a) 5 0 C b) 15 0 C c) 8 0 C d) 12 0 C
 Test z geologii 1) Promień równikowy Ziemi wynosi: a) 637,8 km b) 6378,4 km c) 36561,31 km d) 3656,1 km 2) Największą gęstość posiada: a) Atmosfera b) Litosfera c) Mezosfera d) Barysfera 3) Na Śląsku stopień
Test z geologii 1) Promień równikowy Ziemi wynosi: a) 637,8 km b) 6378,4 km c) 36561,31 km d) 3656,1 km 2) Największą gęstość posiada: a) Atmosfera b) Litosfera c) Mezosfera d) Barysfera 3) Na Śląsku stopień
WYKŁAD HISTORIA GEOLOGII starożytność XVI-XVII wiek XVIII-XIX wiek (początki) kamienie milowe WSTĘP DO NAUK O ZIEMI
 WYKŁAD 2017 Historia geologii, minerały, skały HISTORIA GEOLOGII starożytność XVI-XVII wiek XVIII-XIX wiek (początki) kamienie milowe PLANETA ZIEMIA BUDOWA WNĘTRZA ZIEMI MINERAŁY, SKAŁY POWIERZCHNIA ZIEMI
WYKŁAD 2017 Historia geologii, minerały, skały HISTORIA GEOLOGII starożytność XVI-XVII wiek XVIII-XIX wiek (początki) kamienie milowe PLANETA ZIEMIA BUDOWA WNĘTRZA ZIEMI MINERAŁY, SKAŁY POWIERZCHNIA ZIEMI
Technologie Materiałów Budowlanych Wykład 1. Surowce kamienne
 Technologie Materiałów Budowlanych Wykład 1 Surowce kamienne Skały Skały magmowe Skały osadowe Skały metamorficzne Skały magmowe Skały magmowe (wulkaniczne) występują jako głębinowe (np. granit, sjenit)
Technologie Materiałów Budowlanych Wykład 1 Surowce kamienne Skały Skały magmowe Skały osadowe Skały metamorficzne Skały magmowe Skały magmowe (wulkaniczne) występują jako głębinowe (np. granit, sjenit)
Nikielin NiAs heksagonalny
 GROMADA III SIARCZKI I POKREWNE KRUSZCE Minerały należące do tej gromady najczęściej są nieprzezroczyste, charakteryzują się połyskiem metalicznym lub półmetalicznym oraz dużą gęstością. W przypadku makroskopowo
GROMADA III SIARCZKI I POKREWNE KRUSZCE Minerały należące do tej gromady najczęściej są nieprzezroczyste, charakteryzują się połyskiem metalicznym lub półmetalicznym oraz dużą gęstością. W przypadku makroskopowo
KORDIERYT Al 3 (Mg,Fe 2+ ) 2 Si 5 AlO 18 (rombowy-pseudoheksagonalny)
 KORDIERYT Al 3 (Mg,Fe 2+ ) 2 Si 5 AlO 18 (rombowy-pseudoheksagonalny) CECHA Wykształcenie Forma Łupliwość Relief Barwa/pleochroizm Bliźniaki kordieryt ziarna, krótkie słupki o przekroju pseudoheksagonalnym
KORDIERYT Al 3 (Mg,Fe 2+ ) 2 Si 5 AlO 18 (rombowy-pseudoheksagonalny) CECHA Wykształcenie Forma Łupliwość Relief Barwa/pleochroizm Bliźniaki kordieryt ziarna, krótkie słupki o przekroju pseudoheksagonalnym
SUROWCE MINERALNE. Wykład 5
 SUROWCE MINERALNE Wykład 5 PROCESY POMAGMOWE Etap pegmatytowy (800-600 0 C) w resztkach pomagmowych składniki krzemianowe przewaŝają jeszcze nad składnikami łatwolotnymi. Obfitość tych ostatnich nadaje
SUROWCE MINERALNE Wykład 5 PROCESY POMAGMOWE Etap pegmatytowy (800-600 0 C) w resztkach pomagmowych składniki krzemianowe przewaŝają jeszcze nad składnikami łatwolotnymi. Obfitość tych ostatnich nadaje
WYKŁAD HISTORIA GEOLOGII starożytność XVI-XVII wiek XVIII-XIX wiek (początki) kamienie milowe WSTĘP DO NAUK O ZIEMI
 WYKŁAD 2017 Historia geologii, minerały, skały HISTORIA GEOLOGII starożytność XVI-XVII wiek XVIII-XIX wiek (początki) kamienie milowe PLANETA ZIEMIA BUDOWA WNĘTRZA ZIEMI MINERAŁY, SKAŁY POWIERZCHNIA ZIEMI
WYKŁAD 2017 Historia geologii, minerały, skały HISTORIA GEOLOGII starożytność XVI-XVII wiek XVIII-XIX wiek (początki) kamienie milowe PLANETA ZIEMIA BUDOWA WNĘTRZA ZIEMI MINERAŁY, SKAŁY POWIERZCHNIA ZIEMI
GEOLOGIA: Petrologia i petrografia Mineralogia i geochemia Geologia dynamiczna Gleboznawstwo Tektonika Stratygrafia Paleontologia Kartowanie
 GEOLOGIA: Petrologia i petrografia Mineralogia i geochemia Geologia dynamiczna Gleboznawstwo Tektonika Stratygrafia Paleontologia Kartowanie geologiczne Geologia inżynierska, geofizyka, hydrogeologia,
GEOLOGIA: Petrologia i petrografia Mineralogia i geochemia Geologia dynamiczna Gleboznawstwo Tektonika Stratygrafia Paleontologia Kartowanie geologiczne Geologia inżynierska, geofizyka, hydrogeologia,
 http://muzeum.if.pw.edu.pl/ W jaki sposób Maria Skłodowska-Curie wydzieliła polon i rad z blendy uranowej? Warsztaty metodyczne dla nauczycieli chemii szkół gimnazjalnych i ponadgimnazjalnych 29 stycznia
http://muzeum.if.pw.edu.pl/ W jaki sposób Maria Skłodowska-Curie wydzieliła polon i rad z blendy uranowej? Warsztaty metodyczne dla nauczycieli chemii szkół gimnazjalnych i ponadgimnazjalnych 29 stycznia
BADAMY WŁAŚCIWOŚCI SKAŁ, SKAMIENIAŁOŚCI I MINERAŁÓW
 BADAMY WŁAŚCIWOŚCI SKAŁ, SKAMIENIAŁOŚCI I MINERAŁÓW Zdzisław Nowak ZCDN Szczecin 15.02.2017 r. O czym mówimy? O ogromnej różnorodności wytworów nieożywionych natury. Łącznie jest to kilkanaście tysięcy
BADAMY WŁAŚCIWOŚCI SKAŁ, SKAMIENIAŁOŚCI I MINERAŁÓW Zdzisław Nowak ZCDN Szczecin 15.02.2017 r. O czym mówimy? O ogromnej różnorodności wytworów nieożywionych natury. Łącznie jest to kilkanaście tysięcy
a) Sole kwasu chlorowodorowego (solnego) to... b) Sole kwasu siarkowego (VI) to... c) Sole kwasu azotowego (V) to... d) Sole kwasu węglowego to...
 Karta pracy nr 73 Budowa i nazwy soli. 1. Porównaj wzory sumaryczne soli. FeCl 2 Al(NO 3 ) 3 K 2 CO 3 Cu 3 (PO 4 ) 2 K 2 SO 4 Ca(NO 3 ) 2 CaCO 3 KNO 3 PbSO 4 AlCl 3 Fe 2 (CO 3 ) 3 Fe 2 (SO 4 ) 3 AlPO 4
Karta pracy nr 73 Budowa i nazwy soli. 1. Porównaj wzory sumaryczne soli. FeCl 2 Al(NO 3 ) 3 K 2 CO 3 Cu 3 (PO 4 ) 2 K 2 SO 4 Ca(NO 3 ) 2 CaCO 3 KNO 3 PbSO 4 AlCl 3 Fe 2 (CO 3 ) 3 Fe 2 (SO 4 ) 3 AlPO 4
Rozdział 28 - Inne galeny
 Rozdział 28 - Inne galeny Okaz 1 - MCh/P/11403 - Galena druzowa - 2-6-2: Próbka z II horyzontu rudnego, Trzebionka, rejon szybiku 18. Galena druzowa narastająca na dnie dużej kawerny w dolomitach kruszconośnych.
Rozdział 28 - Inne galeny Okaz 1 - MCh/P/11403 - Galena druzowa - 2-6-2: Próbka z II horyzontu rudnego, Trzebionka, rejon szybiku 18. Galena druzowa narastająca na dnie dużej kawerny w dolomitach kruszconośnych.
Geomateriały. minerały, skaly i inne.. Co to jest minerał?
 Geomateriały minerały, skaly i inne.. Co to jest minerał? Minerał Nieorganiczny, powstały w naturze, stały materiał o zdefiniowanym, konkretnym składzie chemicznym* i strukturze krystalicznej. *Uwaga:
Geomateriały minerały, skaly i inne.. Co to jest minerał? Minerał Nieorganiczny, powstały w naturze, stały materiał o zdefiniowanym, konkretnym składzie chemicznym* i strukturze krystalicznej. *Uwaga:
ANDALUZYT Al 2 SiO 5 (rombowy)
 ANDALUZYT Al 2 SiO 5 (rombowy) CECHA Wykształcenie andaluzyt ziarna, krótkie słupki, częste agregaty ziarniste lub pręcikowe Forma kryształy auto- i hipautomorficzne rzadkie, zwykle ksenomorficzny Łupliwość
ANDALUZYT Al 2 SiO 5 (rombowy) CECHA Wykształcenie andaluzyt ziarna, krótkie słupki, częste agregaty ziarniste lub pręcikowe Forma kryształy auto- i hipautomorficzne rzadkie, zwykle ksenomorficzny Łupliwość
ĆWICZENIE 1 OZNACZANIE MINERAŁÓW GLEBOTWÓRCZYCH METODĄ ORGANOLEPTYCZNĄ
 ĆWICZENIE 1 OZNACZANIE MINERAŁÓW GLEBOTWÓRCZYCH METODĄ ORGANOLEPTYCZNĄ Minerały - pierwiastki lub związki chemiczne o stałym składzie chemicznym i tych samych właściwościach fizycznych. Występują w przyrodzie
ĆWICZENIE 1 OZNACZANIE MINERAŁÓW GLEBOTWÓRCZYCH METODĄ ORGANOLEPTYCZNĄ Minerały - pierwiastki lub związki chemiczne o stałym składzie chemicznym i tych samych właściwościach fizycznych. Występują w przyrodzie
Ć W I C Z E N I E. Analiza jakościowa
 Ć W I C Z E N I E 5a Analiza jakościowa Podział kationów na grupy analityczne Podstawą podziału kationów na grupy analityczne jest wielkość iloczynu rozpuszczalności poszczególnych soli metali. Jak wiadomo
Ć W I C Z E N I E 5a Analiza jakościowa Podział kationów na grupy analityczne Podstawą podziału kationów na grupy analityczne jest wielkość iloczynu rozpuszczalności poszczególnych soli metali. Jak wiadomo
Piotr Chojnacki. Geochemia Ołowiu
 Piotr Chojnacki Wrocław dn. 6 czerwca 2005 roku Geochemia Ołowiu Piotr Chojnacki Astronomowie uważają, że dzieje Wszechświata zaczęły się od punktu w nieskończenie wielkiej temperaturze, gęstości i ciśnieniu.
Piotr Chojnacki Wrocław dn. 6 czerwca 2005 roku Geochemia Ołowiu Piotr Chojnacki Astronomowie uważają, że dzieje Wszechświata zaczęły się od punktu w nieskończenie wielkiej temperaturze, gęstości i ciśnieniu.
SUROWCE I RECYKLING. Wykład 8
 SUROWCE I RECYKLING Wykład 8 WYBRANE NIEMETALICZNE SUROWCE MINERALNE surowce krzemionkowe, tj. zasobne w SiO 2, surowce ilaste, surowce glinowe, glinokrzemianowe i zawierające alkalia, surowce wapniowe,
SUROWCE I RECYKLING Wykład 8 WYBRANE NIEMETALICZNE SUROWCE MINERALNE surowce krzemionkowe, tj. zasobne w SiO 2, surowce ilaste, surowce glinowe, glinokrzemianowe i zawierające alkalia, surowce wapniowe,
WYKŁAD WSTĘP DO NAUK O ZIEMI. Wokół geologii
 Wokół geologii 10.01.2019 - Wojewoda, J., 2019. Czas i Przestrzeń geologiczna. W ramach wystawy izraelskiej artystki Elli Littwitz - "I wody stały się piołunem". Muzeum Współczesne we Wrocławiu, 18:00.
Wokół geologii 10.01.2019 - Wojewoda, J., 2019. Czas i Przestrzeń geologiczna. W ramach wystawy izraelskiej artystki Elli Littwitz - "I wody stały się piołunem". Muzeum Współczesne we Wrocławiu, 18:00.
w_08 Chemia mineralnych materiałów budowlanych c.d. Chemia metali budowlanych
 w_08 Chemia mineralnych materiałów budowlanych c.d. Chemia metali budowlanych Spoiwa krzemianowe Kompozyty krzemianowe (silikatowe) kity, zaprawy, farby szkło wodne Na 2 SiO 3 + 2H 2 O H 2 SiO 3 +
w_08 Chemia mineralnych materiałów budowlanych c.d. Chemia metali budowlanych Spoiwa krzemianowe Kompozyty krzemianowe (silikatowe) kity, zaprawy, farby szkło wodne Na 2 SiO 3 + 2H 2 O H 2 SiO 3 +
Identyfikacja wybranych kationów i anionów
 Identyfikacja wybranych kationów i anionów ZACHOWAĆ SZCZEGÓLNĄ OSTRORZNOŚĆ NIE ZATYKAĆ PROBÓWKI PALCEM Zadanie 1 Celem zadania jest wykrycie jonów Ca 2+ a. Próba z jonami C 2 O 4 ZACHOWAĆ SZCZEGÓLNĄ OSTRORZNOŚĆ
Identyfikacja wybranych kationów i anionów ZACHOWAĆ SZCZEGÓLNĄ OSTRORZNOŚĆ NIE ZATYKAĆ PROBÓWKI PALCEM Zadanie 1 Celem zadania jest wykrycie jonów Ca 2+ a. Próba z jonami C 2 O 4 ZACHOWAĆ SZCZEGÓLNĄ OSTRORZNOŚĆ
WIETRZENIE. Rozpuszczanie polega na łączeniu się minerałów z wodą i doprowadzeniu ich do roztworu. Tego typu wietrzeniu ulegają głównie sole.
 WIETRZENIE Wietrzenie to proces prowadzący do rozpadu lub rozkładu skały RODZAJE WIETRZENIA WIETRZENIE FIZYCZNE = MECHANICZNE v INSOLACJA v ZAMRÓZ (MROZOWE) v SKAŁ ILASTYCH v SOLNE WIETRZENIE CHEMICZNE
WIETRZENIE Wietrzenie to proces prowadzący do rozpadu lub rozkładu skały RODZAJE WIETRZENIA WIETRZENIE FIZYCZNE = MECHANICZNE v INSOLACJA v ZAMRÓZ (MROZOWE) v SKAŁ ILASTYCH v SOLNE WIETRZENIE CHEMICZNE
Minerały. Autorstwo: Jackowiak Maciej Kamiński Kamil Wróblewska Natalia
 Minerały Autorstwo: Jackowiak Maciej Kamiński Kamil Wróblewska Natalia Klasyfikacja minerałów ze względu na skałę macierzystą Minerały skał magmowych Minerały skał osadowych Minerały skał metamorficznych
Minerały Autorstwo: Jackowiak Maciej Kamiński Kamil Wróblewska Natalia Klasyfikacja minerałów ze względu na skałę macierzystą Minerały skał magmowych Minerały skał osadowych Minerały skał metamorficznych
Scenariusz lekcji chemii w klasie drugiej gimnazjum
 mgr Sylwia Pięta nauczyciel chemii i matematyki Zespół Szkół z Oddziałami Sportowymi nr 1 61-638 Poznań, Os. Pod Lipami 106 Cele lekcji Temat lekcji: Poznajemy sole Formy pracy: Metody pracy: Scenariusz
mgr Sylwia Pięta nauczyciel chemii i matematyki Zespół Szkół z Oddziałami Sportowymi nr 1 61-638 Poznań, Os. Pod Lipami 106 Cele lekcji Temat lekcji: Poznajemy sole Formy pracy: Metody pracy: Scenariusz
Wapń i jego związki. -występowanie i otrzymywanie -właściwości fizyczne i chemiczne - ważniejsze związki wapnia
 Wapń i jego związki -występowanie i otrzymywanie -właściwości fizyczne i chemiczne - ważniejsze związki wapnia Wapń występowanie Występowanie: występuje wyłącznie w postaci związanej CaCO 3 w minerałachkalcyt,
Wapń i jego związki -występowanie i otrzymywanie -właściwości fizyczne i chemiczne - ważniejsze związki wapnia Wapń występowanie Występowanie: występuje wyłącznie w postaci związanej CaCO 3 w minerałachkalcyt,
SUROWCE I RECYKLING. Wykład 2
 SUROWCE I RECYKLING Wykład 2 Układ krystalograficzny grupuje kryształy o pewnych wspólnych cechach symetrii geometrycznej Postacie krystalograficzne Kryształy ograniczone ścianami jednoznacznymi stanowią
SUROWCE I RECYKLING Wykład 2 Układ krystalograficzny grupuje kryształy o pewnych wspólnych cechach symetrii geometrycznej Postacie krystalograficzne Kryształy ograniczone ścianami jednoznacznymi stanowią
W probówkach oznaczonych numerami 1-8 znajdują się wodne roztwory (o stężeniu 0,1
 XLVIII OLIMPIADA CHEMICZA Etap II KOMITET GŁÓWY OLIMPIADY CHEMICZEJ Zadanie laboratoryjne W probówkach oznaczonych numerami 1-8 znajdują się wodne roztwory (o stężeniu 0,1 mol/dm 3 ) pojedynczych substancji
XLVIII OLIMPIADA CHEMICZA Etap II KOMITET GŁÓWY OLIMPIADY CHEMICZEJ Zadanie laboratoryjne W probówkach oznaczonych numerami 1-8 znajdują się wodne roztwory (o stężeniu 0,1 mol/dm 3 ) pojedynczych substancji
WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH
 WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH PODZIAŁ ZWIĄZKÓW NIEORGANICZNYCH Tlenki (kwasowe, zasadowe, amfoteryczne, obojętne) Związki niemetali Kwasy (tlenowe, beztlenowe) Wodorotlenki
WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH PODZIAŁ ZWIĄZKÓW NIEORGANICZNYCH Tlenki (kwasowe, zasadowe, amfoteryczne, obojętne) Związki niemetali Kwasy (tlenowe, beztlenowe) Wodorotlenki
Przeróbka kopalin fluorowych
 Przeróbka kopalin fluorowych Fluor (łac. fluorum F) pierwiastek reprezentatywny rozpoczynający główną rodzinę fluorowce (F, Cl, Br. J). Fluor jest pierwiastkiem dość pospolitym. Jego zawartość w skorupie
Przeróbka kopalin fluorowych Fluor (łac. fluorum F) pierwiastek reprezentatywny rozpoczynający główną rodzinę fluorowce (F, Cl, Br. J). Fluor jest pierwiastkiem dość pospolitym. Jego zawartość w skorupie
Niemetaliczne materiały konstrukcyjne pochodzenia mineralnego
 CHEMIA A SPOŁECZEŃSTWO Niemetaliczne materiały konstrukcyjne pochodzenia mineralnego Marek Kwiatkowski Zakład Dydaktyki Chemii Wydział Chemii UG ul. Sobieskiego 18, 80-952 Gdańsk tel. (058) 3450 462 e-mail:
CHEMIA A SPOŁECZEŃSTWO Niemetaliczne materiały konstrukcyjne pochodzenia mineralnego Marek Kwiatkowski Zakład Dydaktyki Chemii Wydział Chemii UG ul. Sobieskiego 18, 80-952 Gdańsk tel. (058) 3450 462 e-mail:
Tlen. Występowanie i odmiany alotropowe Otrzymywanie tlenu Właściwości fizyczne i chemiczne Związki tlenu tlenki, nadtlenki i ponadtlenki
 Tlen Występowanie i odmiany alotropowe Otrzymywanie tlenu Właściwości fizyczne i chemiczne Związki tlenu tlenki, nadtlenki i ponadtlenki Ogólna charakterystyka tlenowców Tlenowce: obejmują pierwiastki
Tlen Występowanie i odmiany alotropowe Otrzymywanie tlenu Właściwości fizyczne i chemiczne Związki tlenu tlenki, nadtlenki i ponadtlenki Ogólna charakterystyka tlenowców Tlenowce: obejmują pierwiastki
XXXV OLIMPIADA GEOGRAFICZNA Zawody II stopnia pisemne podejście 1
 -1/1- XXXV OLIMPIADA GEOGRAFICZNA Zawody II stopnia pisemne podejście 1 W zadaniach 1-3 należy wykorzystać mapę (s. 4) i przekrój geologiczny (s. 5). Zadanie 1. Uwaga: w miejscach pozostawionych po poleceniach
-1/1- XXXV OLIMPIADA GEOGRAFICZNA Zawody II stopnia pisemne podejście 1 W zadaniach 1-3 należy wykorzystać mapę (s. 4) i przekrój geologiczny (s. 5). Zadanie 1. Uwaga: w miejscach pozostawionych po poleceniach
SKAŁY NATURALNE SKUPISKA MINERAŁÓW JEDNORODNYCH LUB RÓŻNORODNYCH KALSYFIKACJA SKAŁ ZE WZGLĘDU NA ICH GENEZĘ
 SKAŁY NATURALNE SKUPISKA MINERAŁÓW JEDNORODNYCH LUB RÓŻNORODNYCH KALSYFIKACJA SKAŁ ZE WZGLĘDU NA ICH GENEZĘ MAGMOWE POWSTAJĄCE Z KRYSTALIZACJI MAGMY, LAWY I SUBSTANCJI IM TOWARZYSZĄCYCH OSADOWE POWSTAJĄCE
SKAŁY NATURALNE SKUPISKA MINERAŁÓW JEDNORODNYCH LUB RÓŻNORODNYCH KALSYFIKACJA SKAŁ ZE WZGLĘDU NA ICH GENEZĘ MAGMOWE POWSTAJĄCE Z KRYSTALIZACJI MAGMY, LAWY I SUBSTANCJI IM TOWARZYSZĄCYCH OSADOWE POWSTAJĄCE
GEOCHEMIA WYBRANYCH PIERWIASTKÓW
 GEOCHEMIA WYBRANYCH PIERWIASTKÓW Na, K i inne metale alkaliczne silnie elektrododatnie metale o dużych promieniach jonowych tworzące jony +1 i wiązania w przewadze jonowe sód i potas są składnikami minerałów
GEOCHEMIA WYBRANYCH PIERWIASTKÓW Na, K i inne metale alkaliczne silnie elektrododatnie metale o dużych promieniach jonowych tworzące jony +1 i wiązania w przewadze jonowe sód i potas są składnikami minerałów
Zadanie 3 Zapisz wzory sumaryczne głównych składników przedstawionych skał i minerałów. kalcyt kreda kwarc gips agat
 CZĘŚĆ 1 Zadanie 1 Wyjaśnij pojęcia. wapno palone, hydraty, zaprawa gipsowa, zaprawa wapienna, wietrzenie skał, wapno gaszone, próchnica, degradacja gleby, właściwości sorpcyjne gleby, wapno palone, degradacja
CZĘŚĆ 1 Zadanie 1 Wyjaśnij pojęcia. wapno palone, hydraty, zaprawa gipsowa, zaprawa wapienna, wietrzenie skał, wapno gaszone, próchnica, degradacja gleby, właściwości sorpcyjne gleby, wapno palone, degradacja
PIERWIASTKI RODZIME, STOPY I ZWIĄZKI MIĘDZYMETALICZNE
 GROMADA I PIERWIASTKI RODZIME, STOPY I ZWIĄZKI MIĘDZYMETALICZNE Procentowy udział pierwiastków rodzimych w skorupie ziemskiej nie przekracza 0,1 %wag. Najczęstsze z nich, wyłączając składniki atmosfery,
GROMADA I PIERWIASTKI RODZIME, STOPY I ZWIĄZKI MIĘDZYMETALICZNE Procentowy udział pierwiastków rodzimych w skorupie ziemskiej nie przekracza 0,1 %wag. Najczęstsze z nich, wyłączając składniki atmosfery,
Zasoby naturalne Ziemi. Podział i rola surowców mineralnych. Dział: Przemysł Poziom rozszerzony NPP NE
 Zasoby naturalne Ziemi. Podział i rola surowców mineralnych Dział: Przemysł Poziom rozszerzony NPP NE Zasoby naturalne Ziemi Biotyczne Abiotyczne Energia Surowce mineralne Ich eksploatacja zmienia się
Zasoby naturalne Ziemi. Podział i rola surowców mineralnych Dział: Przemysł Poziom rozszerzony NPP NE Zasoby naturalne Ziemi Biotyczne Abiotyczne Energia Surowce mineralne Ich eksploatacja zmienia się
Identyfikacja jonów metali w roztworach wodnych
 Identyfikacja jonów metali w roztworach wodnych Podział kationów na grupy analityczne Podstawą podziału kationów na grupy analityczne jest wielkość iloczynu rozpuszczalności poszczególnych soli metali.
Identyfikacja jonów metali w roztworach wodnych Podział kationów na grupy analityczne Podstawą podziału kationów na grupy analityczne jest wielkość iloczynu rozpuszczalności poszczególnych soli metali.
Rozdział 4 - Blendy warstwowane
 Rozdział 4 - Blendy warstwowane Okaz 1 - MCh/P/11302 - Blenda warstwowana z galeną - 1-1-3: Próbka z II horyzontu rudnego, Trzebionka, rejon szybiku nr 29, część południowa. Blenda warstwowana ze skupieniami
Rozdział 4 - Blendy warstwowane Okaz 1 - MCh/P/11302 - Blenda warstwowana z galeną - 1-1-3: Próbka z II horyzontu rudnego, Trzebionka, rejon szybiku nr 29, część południowa. Blenda warstwowana ze skupieniami
Sole. 2. Zaznacz reszty kwasowe w poniższych solach oraz wartościowości reszt kwasowych: CaBr 2 Na 2 SO 4
 Sole 1. Podkreśl poprawne uzupełnienia zdań: Sole to związki, które dysocjują w wodzie na kationy/aniony metali oraz kationy/ aniony reszt kwasowych. W temperaturze pokojowej mają stały/ ciekły stan skupienia
Sole 1. Podkreśl poprawne uzupełnienia zdań: Sole to związki, które dysocjują w wodzie na kationy/aniony metali oraz kationy/ aniony reszt kwasowych. W temperaturze pokojowej mają stały/ ciekły stan skupienia
Rozdział 6 - Ruda ziemista, blendy ziemiste oraz skorupowe
 Rozdział 6 - Ruda ziemista, blendy ziemiste oraz skorupowe Okaz 1 - MCh/P/11322 - Ruda ziemista - 1-4-14: Próbka z III horyzontu rudnego, Trzebionka, część centralna ciała rudnego. Kontakt blendy ziemistej
Rozdział 6 - Ruda ziemista, blendy ziemiste oraz skorupowe Okaz 1 - MCh/P/11322 - Ruda ziemista - 1-4-14: Próbka z III horyzontu rudnego, Trzebionka, część centralna ciała rudnego. Kontakt blendy ziemistej
Spis treści. Właściwości fizyczne. Wodorki berylowców. Berylowce
 Berylowce Spis treści 1 Właściwości fizyczne 2 Wodorki berylowców 3 Tlenki berylowców 4 Nadtlenki 5 Wodorotlenki 6 Iloczyn rozpuszczalności 7 Chlorki, fluorki, węglany 8 Siarczany 9 Twardość wody 10 Analiza
Berylowce Spis treści 1 Właściwości fizyczne 2 Wodorki berylowców 3 Tlenki berylowców 4 Nadtlenki 5 Wodorotlenki 6 Iloczyn rozpuszczalności 7 Chlorki, fluorki, węglany 8 Siarczany 9 Twardość wody 10 Analiza
Wydział Chemii UJ Podstawy chemii -wykład 13/1 dr hab. W. Makowski
 !"#$% &%'( )'%!"#$ ( *('+( ',"("%-%'(.& *('+( ',"("%-%'( /014516 7689:6;9:9?@;60 A4B11 1 65671< =6C9D1904= :4?E FE G414:H I
!"#$% &%'( )'%!"#$ ( *('+( ',"("%-%'(.& *('+( ',"("%-%'( /014516 7689:6;9:9?@;60 A4B11 1 65671< =6C9D1904= :4?E FE G414:H I
Temat 2: Nazewnictwo związków chemicznych. Otrzymywanie i właściwości tlenków
 Zasada ogólna: We wzorze sumarycznym pierwiastki zapisujemy od metalu do niemetalu, natomiast odczytujemy nazwę zaczynając od niemetalu: MgO, CaS, NaF Nazwy związków chemicznych najczęściej tworzymy, korzystając
Zasada ogólna: We wzorze sumarycznym pierwiastki zapisujemy od metalu do niemetalu, natomiast odczytujemy nazwę zaczynając od niemetalu: MgO, CaS, NaF Nazwy związków chemicznych najczęściej tworzymy, korzystając
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego. I Etap szkolny - 23 listopada 2016
 XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego I Etap szkolny - 23 listopada 2016 Kod ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego I Etap szkolny - 23 listopada 2016 Kod ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
Plan: 1) krutki opis w ramach wstępu 2) Występowanie 3) Otrzymywanie 4) Właściwości 5) Związki 6) Izotopy 7) Zastosowanie 8) Znaczenie biologiczne
 Mied ź Plan: 1) krutki opis w ramach wstępu 2) Występowanie 3) Otrzymywanie 4) Właściwości 5) Związki 6) Izotopy 7) Zastosowanie 8) Znaczenie biologiczne 1) krutki opis w ramach wstępu Miedź (Cu, łac.
Mied ź Plan: 1) krutki opis w ramach wstępu 2) Występowanie 3) Otrzymywanie 4) Właściwości 5) Związki 6) Izotopy 7) Zastosowanie 8) Znaczenie biologiczne 1) krutki opis w ramach wstępu Miedź (Cu, łac.
Fragmenty Działu 7 z Tomu 1 REAKCJE UTLENIANIA I REDUKCJI
 Fragmenty Działu 7 z Tomu 1 REAKCJE UTLENIANIA I REDUKCJI Zadanie 726 (1 pkt.) V/2006/A1 Konfigurację elektronową atomu glinu w stanie podstawowym można przedstawić następująco: 1s 2 2s 2 2p 6 3s 2 3p
Fragmenty Działu 7 z Tomu 1 REAKCJE UTLENIANIA I REDUKCJI Zadanie 726 (1 pkt.) V/2006/A1 Konfigurację elektronową atomu glinu w stanie podstawowym można przedstawić następująco: 1s 2 2s 2 2p 6 3s 2 3p
2.4. ZADANIA STECHIOMETRIA. 1. Ile moli stanowi:
 2.4. ZADANIA 1. Ile moli stanowi: STECHIOMETRIA a/ 52 g CaCO 3 b/ 2,5 tony Fe(OH) 3 2. Ile g stanowi: a/ 4,5 mmol ZnSO 4 b/ 10 kmol wody 3. Obl. % skład Fe 2 (SO 4 ) 3 6H 2 O 4. Obl. % zawartość tlenu
2.4. ZADANIA 1. Ile moli stanowi: STECHIOMETRIA a/ 52 g CaCO 3 b/ 2,5 tony Fe(OH) 3 2. Ile g stanowi: a/ 4,5 mmol ZnSO 4 b/ 10 kmol wody 3. Obl. % skład Fe 2 (SO 4 ) 3 6H 2 O 4. Obl. % zawartość tlenu
ĆWICZENIA LABORATORYJNE WYKRYWANIE WYBRANYCH ANIONÓW I KATIONÓW.
 ĆWICZENIA LABORATORYJNE WYKRYWANIE WYBRANYCH ANIONÓW I KATIONÓW. Chemia analityczna jest działem chemii zajmującym się ustalaniem składu jakościowego i ilościowego badanych substancji chemicznych. Analiza
ĆWICZENIA LABORATORYJNE WYKRYWANIE WYBRANYCH ANIONÓW I KATIONÓW. Chemia analityczna jest działem chemii zajmującym się ustalaniem składu jakościowego i ilościowego badanych substancji chemicznych. Analiza
PODSTAWY CHEMII ANALITYCZNEJ. Wykład 11 Wstęp do Analizy Jakościowej
 PODSTAWY CHEMII ANALITYCZNEJ Wykład 11 Wstęp do Analizy Jakościowej 1 PRÓBA i PRÓBKA PRÓBKA PRÓBA Obserwacja Co widzę? Przedmiot analizy ciało stałe, ciecz, gaz, roztwór, sól, minerał, nawóz Czynność:
PODSTAWY CHEMII ANALITYCZNEJ Wykład 11 Wstęp do Analizy Jakościowej 1 PRÓBA i PRÓBKA PRÓBKA PRÓBA Obserwacja Co widzę? Przedmiot analizy ciało stałe, ciecz, gaz, roztwór, sól, minerał, nawóz Czynność:
Rozdział 23 - Okazy z barytem
 Rozdział 23 - Okazy z barytem Okaz 1 - MCh/P/11445 - Nacieki barytowo-markasytowe 4-1-2: Próbka z Trzebionki, rejon szybiku nr 36, strefa tektoniczna. Skupienia markasytu przypominające nacieki (ziegenbart),
Rozdział 23 - Okazy z barytem Okaz 1 - MCh/P/11445 - Nacieki barytowo-markasytowe 4-1-2: Próbka z Trzebionki, rejon szybiku nr 36, strefa tektoniczna. Skupienia markasytu przypominające nacieki (ziegenbart),
Nazwy pierwiastków: A +Fe 2(SO 4) 3. Wzory związków: A B D. Równania reakcji:
 Zadanie 1. [0-3 pkt] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Suma protonów i elektronów anionu X 2- jest równa 34. II. Stosunek masowy
Zadanie 1. [0-3 pkt] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Suma protonów i elektronów anionu X 2- jest równa 34. II. Stosunek masowy
Kationy grupa analityczna I
 Kompendium - Grupy analityczne kationów Kationy grupa analityczna I Odczynnik Ag + Hg 2 2+ Pb 2+ roztwór bezbarwny roztwór bezbarwny roztwór bezbarwny HCl rozc. biały osad [1] biały osad [2] biały osad
Kompendium - Grupy analityczne kationów Kationy grupa analityczna I Odczynnik Ag + Hg 2 2+ Pb 2+ roztwór bezbarwny roztwór bezbarwny roztwór bezbarwny HCl rozc. biały osad [1] biały osad [2] biały osad
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW. Eliminacje rejonowe II stopień
 POUFNE Pieczątka szkoły 28 stycznia 2016 r. Kod ucznia (wypełnia uczeń) Imię i nazwisko (wypełnia komisja) Czas pracy 90 minut KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 Eliminacje rejonowe
POUFNE Pieczątka szkoły 28 stycznia 2016 r. Kod ucznia (wypełnia uczeń) Imię i nazwisko (wypełnia komisja) Czas pracy 90 minut KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 Eliminacje rejonowe
SUROWCE I RECYKLING. Wykład 4
 SUROWCE I RECYKLING Wykład 4 Minerały główne skał magmowych Kwarc SiO 2 Skalenie ortoklaz K[AlSi 3 O 8 ] albit Na[AlSi 3 O 8 ] anortyt - Ca[Al 2 Si 2 O 8 ] Miki muskowit KAl 2 [(OH,F) 2 AlSi 3 O 10 ] biotyt
SUROWCE I RECYKLING Wykład 4 Minerały główne skał magmowych Kwarc SiO 2 Skalenie ortoklaz K[AlSi 3 O 8 ] albit Na[AlSi 3 O 8 ] anortyt - Ca[Al 2 Si 2 O 8 ] Miki muskowit KAl 2 [(OH,F) 2 AlSi 3 O 10 ] biotyt
Ważniejsze składniki mineralne - Minerały ilaste, tlenki żelaza oraz węglany
 Opracował dr inż. Cezary Kaźmierowski (UAM) i mgr M. Hahnel (KGiR WMiI UP w Poznaniu) 1 Ważniejsze składniki mineralne - Minerały ilaste, tlenki żelaza oraz węglany W skorupie ziemskiej występuje ponad
Opracował dr inż. Cezary Kaźmierowski (UAM) i mgr M. Hahnel (KGiR WMiI UP w Poznaniu) 1 Ważniejsze składniki mineralne - Minerały ilaste, tlenki żelaza oraz węglany W skorupie ziemskiej występuje ponad
LITERATURA: ZAKRES MATERIAŁU OBOWIĄZUJĄCEGO NA ĆWICZENIE:
 ĆWICZENIE nr 8 Identyfikacja soli na podstawie właściwości fizykochemicznych. Analiza przeliczeń dotyczących stężeń roztworów, ph mocnych i słabych elektrolitów oraz roztworów buforowych LITERATURA: 1.
ĆWICZENIE nr 8 Identyfikacja soli na podstawie właściwości fizykochemicznych. Analiza przeliczeń dotyczących stężeń roztworów, ph mocnych i słabych elektrolitów oraz roztworów buforowych LITERATURA: 1.
ĆWICZENIE 11 CHEMICZNE BARWIENIE METALI I STOPÓW
 ĆWICZENIE 11 CHEMICZNE BARWIENIE METALI I STOPÓW WPROWADZENIE Jednym ze sposobów obróbki powierzchni metali i ich stopów jest barwienie. Proces ten prowadzi się w celach dekoracyjnych, nadania patyny lub
ĆWICZENIE 11 CHEMICZNE BARWIENIE METALI I STOPÓW WPROWADZENIE Jednym ze sposobów obróbki powierzchni metali i ich stopów jest barwienie. Proces ten prowadzi się w celach dekoracyjnych, nadania patyny lub
Wodorotlenki. n to liczba grup wodorotlenowych w cząsteczce wodorotlenku (równa wartościowości M)
 Wodorotlenki Definicja - Wodorotlenkami nazywamy związki chemiczne, zbudowane z kationu metalu (zazwyczaj) (M) i anionu wodorotlenowego (OH - ) Ogólny wzór wodorotlenków: M(OH) n M oznacza symbol metalu.
Wodorotlenki Definicja - Wodorotlenkami nazywamy związki chemiczne, zbudowane z kationu metalu (zazwyczaj) (M) i anionu wodorotlenowego (OH - ) Ogólny wzór wodorotlenków: M(OH) n M oznacza symbol metalu.
PROCESY BIOGEOCHEMICZNE NA LĄDACH
 PROCESY BIOGEOCHEMICZNE NA LĄDACH Ekosystemy lądowe Ekosystemy wodne Ekosystemy lądowe Ekosystemy wilgotne Ekosystemy wodne Ekosystemy lądowe Ekosystemy wilgotne Ekosystemy wodne skała macierzysta Wietrzenie
PROCESY BIOGEOCHEMICZNE NA LĄDACH Ekosystemy lądowe Ekosystemy wodne Ekosystemy lądowe Ekosystemy wilgotne Ekosystemy wodne Ekosystemy lądowe Ekosystemy wilgotne Ekosystemy wodne skała macierzysta Wietrzenie
Przeróbka kopalin molibdenowych
 Przeróbka kopalin molibdenowych Molibden (łac. molybdaenum Mo) pierwiastek przejściowy należący do dodatkowej rodziny 6a chromowce. Posiada 7 izotopów trwałych: 92 Mo, 94 Mo, 95 Mo, 96 Mo, 97 Mo, 98 Mo,
Przeróbka kopalin molibdenowych Molibden (łac. molybdaenum Mo) pierwiastek przejściowy należący do dodatkowej rodziny 6a chromowce. Posiada 7 izotopów trwałych: 92 Mo, 94 Mo, 95 Mo, 96 Mo, 97 Mo, 98 Mo,
Powstawanie żelazianu(vi) sodu przebiega zgodnie z równaniem: Ponieważ termiczny rozkład kwasu borowego(iii) zachodzi zgodnie z równaniem:
 Zad. 1 Ponieważ reakcja jest egzoenergetyczna (ujemne ciepło reakcji) to wzrost temperatury spowoduje przesunięcie równowagi w lewo, zatem mieszanina przyjmie intensywniejszą barwę. Układ będzie przeciwdziałał
Zad. 1 Ponieważ reakcja jest egzoenergetyczna (ujemne ciepło reakcji) to wzrost temperatury spowoduje przesunięcie równowagi w lewo, zatem mieszanina przyjmie intensywniejszą barwę. Układ będzie przeciwdziałał
CHEMIA BUDOWLANA ĆWICZENIE NR 1
 CHEMIA BUDOWLANA ĆWICZENIE NR 1 PODSTAWY CHEMICZNEJ ANALIZY JAKOŚCIOWEJ ANALIZA IDENTYFIKACYJNA WYBRANYCH KATIONÓW WSTĘP TEORETYCZNY Znajomość składu chemicznego materiałów daje informacje o tym jaki to
CHEMIA BUDOWLANA ĆWICZENIE NR 1 PODSTAWY CHEMICZNEJ ANALIZY JAKOŚCIOWEJ ANALIZA IDENTYFIKACYJNA WYBRANYCH KATIONÓW WSTĘP TEORETYCZNY Znajomość składu chemicznego materiałów daje informacje o tym jaki to
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje rejonowe
 kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje rejonowe Zadanie
kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje rejonowe Zadanie
PODSTAWY STECHIOMETRII
 PODSTAWY STECHIOMETRII 1. Obliczyć bezwzględne masy atomów, których względne masy atomowe wynoszą: a) 7, b) 35. 2. Obliczyć masę próbki wody zawierającej 3,01 10 24 cząsteczek. 3. Która z wymienionych
PODSTAWY STECHIOMETRII 1. Obliczyć bezwzględne masy atomów, których względne masy atomowe wynoszą: a) 7, b) 35. 2. Obliczyć masę próbki wody zawierającej 3,01 10 24 cząsteczek. 3. Która z wymienionych
II. CHEMIA NIEORGANICZNA
 pitagoras.d2.pl II. CHEMIA NIEORGANICZNA TLENKI: Tlenki to związki tlenu z innymi pierwiastkami. Tlen w tlenkach ma zawsze II. pierwiastka X I II III IV V VI VII wzór tlenku X 2 O XO X 2 O 3 XO 2 X 2 O
pitagoras.d2.pl II. CHEMIA NIEORGANICZNA TLENKI: Tlenki to związki tlenu z innymi pierwiastkami. Tlen w tlenkach ma zawsze II. pierwiastka X I II III IV V VI VII wzór tlenku X 2 O XO X 2 O 3 XO 2 X 2 O
II Etap rejonowy 28 styczeń 2019 r. Imię i nazwisko ucznia: Czas trwania: 60 minut
 XVI Wojewódzki Konkurs z Chemii dla uczniów klas trzecich gimnazjów oraz klas trzecich oddziałów gimnazjalnych prowadzonych w szkołach innego typu województwa świętokrzyskiego w roku szkolnym 2018/2019
XVI Wojewódzki Konkurs z Chemii dla uczniów klas trzecich gimnazjów oraz klas trzecich oddziałów gimnazjalnych prowadzonych w szkołach innego typu województwa świętokrzyskiego w roku szkolnym 2018/2019
Fluorowce - chlor. -Ogólna charakterystyka fluorowców -Występowanie i właściwości chloru -Ważniejsze związki chloru
 Fluorowce - chlor -Ogólna charakterystyka fluorowców -Występowanie i właściwości chloru -Ważniejsze związki chloru Fluorowce Ogólna charakterystyka: fluor, chlor, brom i jod są niemetalami, astat jest
Fluorowce - chlor -Ogólna charakterystyka fluorowców -Występowanie i właściwości chloru -Ważniejsze związki chloru Fluorowce Ogólna charakterystyka: fluor, chlor, brom i jod są niemetalami, astat jest
Litowce i berylowce- lekcja powtórzeniowa, doświadczalna.
 Doświadczenie 1 Tytuł: Badanie właściwości sodu Odczynnik: Sód metaliczny Szkiełko zegarkowe Metal lekki o srebrzystej barwie Ma metaliczny połysk Jest bardzo miękki, można kroić go nożem Inne właściwości
Doświadczenie 1 Tytuł: Badanie właściwości sodu Odczynnik: Sód metaliczny Szkiełko zegarkowe Metal lekki o srebrzystej barwie Ma metaliczny połysk Jest bardzo miękki, można kroić go nożem Inne właściwości
Chmura pyłu nad wulkanem Eyjafjoll, Fot. Jon Gustafsson AP
 METALE CIĘśKIE Chmura pyłu nad wulkanem Eyjafjoll, 16.04.2010 Fot. Jon Gustafsson AP Chmura pyłu nad wulkanem Eyjafjoll, Fot. Jon Gustafsson AP Metal Fe Znaczenie ferredoksyna, hem Co witamina B 12 Ni
METALE CIĘśKIE Chmura pyłu nad wulkanem Eyjafjoll, 16.04.2010 Fot. Jon Gustafsson AP Chmura pyłu nad wulkanem Eyjafjoll, Fot. Jon Gustafsson AP Metal Fe Znaczenie ferredoksyna, hem Co witamina B 12 Ni
Piotr Chojnacki 1. Cel: Celem ćwiczenia jest wykrycie jonu Cl -- za pomocą reakcji charakterystycznych.
 SPRAWOZDANIE: REAKCJE CHARAKTERYSTYCZNE WYBRANYCH ANIONÓW. Imię Nazwisko Klasa Data Uwagi prowadzącego 1.Wykrywanie obecności jonu chlorkowego Cl - : Cel: Celem ćwiczenia jest wykrycie jonu Cl -- za pomocą
SPRAWOZDANIE: REAKCJE CHARAKTERYSTYCZNE WYBRANYCH ANIONÓW. Imię Nazwisko Klasa Data Uwagi prowadzącego 1.Wykrywanie obecności jonu chlorkowego Cl - : Cel: Celem ćwiczenia jest wykrycie jonu Cl -- za pomocą
pierwiastek lub związek chemiczny, jaki występuje w przyrodzie w naturalnej postaci.
 MINERAŁY I SKAŁY MINERAŁY Minerał - pierwiastek lub związek chemiczny, jaki występuje w przyrodzie w naturalnej postaci. Jest najmniejszym (w sensie geologicznym) elementem skorupy ziemskiej, wytworzonym
MINERAŁY I SKAŁY MINERAŁY Minerał - pierwiastek lub związek chemiczny, jaki występuje w przyrodzie w naturalnej postaci. Jest najmniejszym (w sensie geologicznym) elementem skorupy ziemskiej, wytworzonym
METALE PRZEJ CIOWE /blok d/
 METALE PRZEJ CIOWE /blok d/ Chrom 24Cr Mangan 25 Mn [Ar] 3d 5 4s 1 [Ar] 3d 5 4s 2 metal chromit FeCr 2 O 4 srebrzystoniebieski silny połysk kruchy wysoka temperatura topnienia (1910 o C) braunsztyn - MnO
METALE PRZEJ CIOWE /blok d/ Chrom 24Cr Mangan 25 Mn [Ar] 3d 5 4s 1 [Ar] 3d 5 4s 2 metal chromit FeCr 2 O 4 srebrzystoniebieski silny połysk kruchy wysoka temperatura topnienia (1910 o C) braunsztyn - MnO
WYKRYWANIE OŁOWIU W WINIE
 WYKRYWANIE OŁOWIU W WINIE WYKONANIE DOŚWIADCZENIA Do 5 kieliszków zawierających białe wino zanurzono papierki nasączone roztworem siarczku sodu. OBSERWACJE Po zanurzeniu w winie znajdującym się w 2 kieliszkach
WYKRYWANIE OŁOWIU W WINIE WYKONANIE DOŚWIADCZENIA Do 5 kieliszków zawierających białe wino zanurzono papierki nasączone roztworem siarczku sodu. OBSERWACJE Po zanurzeniu w winie znajdującym się w 2 kieliszkach
TEST NA EGZAMIN POPRAWKOWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM
 TEST NA EGZAMIN PPRAWKWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM I. Część pisemna: 1. Które z poniższych stwierdzeń jest fałszywe? a.) Kwasy są to związki chemiczne zbudowane z wodoru i reszty kwasowej.
TEST NA EGZAMIN PPRAWKWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM I. Część pisemna: 1. Które z poniższych stwierdzeń jest fałszywe? a.) Kwasy są to związki chemiczne zbudowane z wodoru i reszty kwasowej.
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Inżynieria Środowiska. Metody analizy jakościowej
 Metody analizy jakościowej Metody analizy jakościowej oparte na reakcjach chemicznych badanych jonów czy cząsteczek nazywa się metodami chemicznymi. Oprócz metod chemicznych w analizie jakościowej wykorzystywane
Metody analizy jakościowej Metody analizy jakościowej oparte na reakcjach chemicznych badanych jonów czy cząsteczek nazywa się metodami chemicznymi. Oprócz metod chemicznych w analizie jakościowej wykorzystywane
Ćwiczenie 50: Określanie tożsamości jonów (Farmakopea VII-IX ( )).
 Ćwiczenie 50: Określanie tożsamości jonów (Farmakopea VII-IX (2008-2013)). Badanie tożsamości wg Farmakopei Polskiej należy wykonywać w probówkach. Odczynniki bezwzględnie należy dodawać w podawanej kolejności.
Ćwiczenie 50: Określanie tożsamości jonów (Farmakopea VII-IX (2008-2013)). Badanie tożsamości wg Farmakopei Polskiej należy wykonywać w probówkach. Odczynniki bezwzględnie należy dodawać w podawanej kolejności.
Wodorotlenki O O O O. I n. I. Wiadomości ogólne o wodorotlenkach.
 Wodorotlenki I. Wiadomości ogólne o wodorotlenkach. Wodorotlenki są to związki chemiczne zbudowane z atomu metalu i grupy wodorotlenowej. Wzór ogólny wodorotlenków: wartościowość metalu M n ( ) grupa wodorotlenowa
Wodorotlenki I. Wiadomości ogólne o wodorotlenkach. Wodorotlenki są to związki chemiczne zbudowane z atomu metalu i grupy wodorotlenowej. Wzór ogólny wodorotlenków: wartościowość metalu M n ( ) grupa wodorotlenowa
REAKCJE CHARAKTERYSTYCZNE KATIONÓW I ANIONÓW
 REAKCJE CHARAKTERYSTYCZNE KATIONÓW I ANIONÓW WSTĘP TEORETYCZNY Celem ćwiczeń jest zapoznanie się z wybranymi reakcjami charakterystycznymi kationów i anionów w roztworach wodnych. W analizie chemicznej
REAKCJE CHARAKTERYSTYCZNE KATIONÓW I ANIONÓW WSTĘP TEORETYCZNY Celem ćwiczeń jest zapoznanie się z wybranymi reakcjami charakterystycznymi kationów i anionów w roztworach wodnych. W analizie chemicznej
Lp. Odczynnik Równanie reakcji Efekt działania Rozpuszczalność osadu. osad,
 Pierwsza grupa analityczna CHARAKTERYSTYKA GRUPY Kationy I grupy wytrącają chlorki trudno rozpuszczalne w wodzie i w rozcieńczonych kwasach. Rozpuszczalność chlorków jest różna. Maleje w szeregu: Pb 2,
Pierwsza grupa analityczna CHARAKTERYSTYKA GRUPY Kationy I grupy wytrącają chlorki trudno rozpuszczalne w wodzie i w rozcieńczonych kwasach. Rozpuszczalność chlorków jest różna. Maleje w szeregu: Pb 2,
Opisy ćwiczeń laboratoryjnych z chemii. Semestr I (zimowy) Rok akademicki 2012/13
 WYDZIAŁ KSZTAŁTOWANIA ŚRODOWISKA I ROLNICTWA KIERUNEK: ROLNICTWO I ROK STUDIA NIESTACJONARNE PIERWSZEGO STOPNIA Opisy ćwiczeń laboratoryjnych z chemii Semestr I (zimowy) Rok akademicki 2012/13 Opracowała:
WYDZIAŁ KSZTAŁTOWANIA ŚRODOWISKA I ROLNICTWA KIERUNEK: ROLNICTWO I ROK STUDIA NIESTACJONARNE PIERWSZEGO STOPNIA Opisy ćwiczeń laboratoryjnych z chemii Semestr I (zimowy) Rok akademicki 2012/13 Opracowała:
Wykaz ważniejszych symboli agadnienia ogólne Wstęp Zarys historii chemii analitycznej
 Spis rzeczy Z Wykaz ważniejszych symboli............................. 13 1. agadnienia ogólne................................. 15 1.1. Wstęp..................................... 15 1.. Zarys historii chemii
Spis rzeczy Z Wykaz ważniejszych symboli............................. 13 1. agadnienia ogólne................................. 15 1.1. Wstęp..................................... 15 1.. Zarys historii chemii
BUDOWA ATOMU 1. Wymień 3 korzyści płynące z zastosowania pierwiastków promieniotwórczych. 2. Dokończ reakcję i nazwij powstałe pierwiastki:
 BUDOWA ATOMU 1. Wymień 3 korzyści płynące z zastosowania pierwiastków promieniotwórczych. 2. Dokończ reakcję i nazwij powstałe pierwiastki: 235 4 92 U + 2 He 198. 79 Au + ß - 3. Spośród atomów wybierz
BUDOWA ATOMU 1. Wymień 3 korzyści płynące z zastosowania pierwiastków promieniotwórczych. 2. Dokończ reakcję i nazwij powstałe pierwiastki: 235 4 92 U + 2 He 198. 79 Au + ß - 3. Spośród atomów wybierz
Przykłady ważniejszych minerałów występujących w skorupie ziemskiej
 Powtórzenie materiału do sprawdzianu skały i minerały I. Minerały i skały 1. Minerały - pierwiastki w stanie wolnym lub związki chemiczne, które występują przyrodzie i powstały w wyniku naturalnych procesów
Powtórzenie materiału do sprawdzianu skały i minerały I. Minerały i skały 1. Minerały - pierwiastki w stanie wolnym lub związki chemiczne, które występują przyrodzie i powstały w wyniku naturalnych procesów
Część I. TEST WYBORU 18 punktów
 Część I TEST WYBORU 18 punktów Test zawiera zadania, w których podano propozycje czterech odpowiedzi: A), B), C), D). Tylko jedna odpowiedź jest prawidłowa. Prawidłową odpowiedź zaznacz znakiem X. W razie
Część I TEST WYBORU 18 punktów Test zawiera zadania, w których podano propozycje czterech odpowiedzi: A), B), C), D). Tylko jedna odpowiedź jest prawidłowa. Prawidłową odpowiedź zaznacz znakiem X. W razie
Załącznik nr 1 do SIWZ Instytut Chemii i Techniki Jądrowej Warszawa, ul Dorodna 16 Tel. (22) ; Fax (22)
 Załącznik nr 1 do SIWZ Instytut Chemii i Techniki Jądrowej 03 195 Warszawa, ul Dorodna 16 Tel. (22) 504 12 20; 504 12 14 Fax (22) 811 19 17 Wykonanie projektu procesowego instalacji pozyskiwania uranu
Załącznik nr 1 do SIWZ Instytut Chemii i Techniki Jądrowej 03 195 Warszawa, ul Dorodna 16 Tel. (22) 504 12 20; 504 12 14 Fax (22) 811 19 17 Wykonanie projektu procesowego instalacji pozyskiwania uranu
minerwa.pl http://www.minerwa.pl Cennik z dnia 2016-06-29. Wszystkie podane ceny są cenami brutto.
 minerwa.pl http://www.minerwa.pl Cennik z dnia 2016-06-29. Wszystkie podane ceny są cenami brutto. Archiwum Turmalin - bryłka nieregularna gładka(~25-16 mm) Archiwum / Bola i krawaty Bolo - jaspis Bolo
minerwa.pl http://www.minerwa.pl Cennik z dnia 2016-06-29. Wszystkie podane ceny są cenami brutto. Archiwum Turmalin - bryłka nieregularna gładka(~25-16 mm) Archiwum / Bola i krawaty Bolo - jaspis Bolo
Magnez. Wagowy udział pierwiastków w masie Ziemi. Wagowy udział pierwiastków w masie skorupy ziemskiej
 WAPŃ Magnez 100% 80% inne
WAPŃ Magnez 100% 80% inne
Zadanie 1. a & b. Najczęstsze błędy: rysowanie izomeru 1 fenyloetylo. Najczęstsze błędy: stosowanie notacji D i L
 Zadanie 1 a & b. Najczęstsze błędy: rysowanie izomeru 1 fenyloetylo c. Najczęstsze błędy: stosowanie notacji D i L d. Akceptowano dowolną poprawną drogę syntezy, na przykład: Najczęstsze błędy: prowadzenie
Zadanie 1 a & b. Najczęstsze błędy: rysowanie izomeru 1 fenyloetylo c. Najczęstsze błędy: stosowanie notacji D i L d. Akceptowano dowolną poprawną drogę syntezy, na przykład: Najczęstsze błędy: prowadzenie
II. CHEMIA NIEORGANICZNA
 pitagoras.d2.pl II. CHEMIA NIEORGANICZNA TLENKI: Tlenki to związki tlenu z innymi pierwiastkami. Tlen w tlenkach ma zawsze wartościowość II. wartościowość pierwiastka X I II III IV V VI VII wzór tlenku
pitagoras.d2.pl II. CHEMIA NIEORGANICZNA TLENKI: Tlenki to związki tlenu z innymi pierwiastkami. Tlen w tlenkach ma zawsze wartościowość II. wartościowość pierwiastka X I II III IV V VI VII wzór tlenku
PODSTAWOWE POJĘCIA I PRAWA CHEMICZNE
 PODSTAWOWE POJĘCIA I PRAWA CHEMICZNE Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Jaka jest średnia masa atomowa miedzi stanowiącej mieszaninę izotopów,
PODSTAWOWE POJĘCIA I PRAWA CHEMICZNE Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Jaka jest średnia masa atomowa miedzi stanowiącej mieszaninę izotopów,
