Rodzina białek Rho i ich rola w cytoszkielecie komórki The Rho protein family and its role in the cellular cytoskeleton
|
|
|
- Eleonora Maciejewska
- 6 lat temu
- Przeglądów:
Transkrypt
1 Postepy Hig Med Dosw. (online), 2008; 62: e-issn Review Received: Accepted: Published: Rodzina białek Rho i ich rola w cytoszkielecie komórki The Rho protein family and its role in the cellular cytoskeleton Jakub Marcin Nowak, Alina Grzanka, Agnieszka Żuryń, Aleksandra Stępień Katedra i Zakład Histologii i Embriologii, UMK w Toruniu Collegium Medicum im. L. Rydygiera w Bydgoszczy Streszczenie Białka z rodziny Rho (RhoA, Rac1, Cdc42) działają na zasadzie molekularnych przełączników, regulują wiele procesów komórkowych. Zaangażowane są m.in. w migrację komórek, kontrolę cyklu komórkowego, procesy apoptozy i regulację transkrypcji genów. Białka Rho są aktywne przede wszystkim w cytoszkielecie komórki, biorąc udział w reorganizacji mikrofilamentów aktynowych oraz mikrotubul. W ciągu ostatnich lat dokonał się znaczący postęp w zrozumieniu biochemicznej i genetycznej natury wielu procesów, w które są zaangażowane białka Rho. Pozostaje jednak wiele niewiadomych oraz wymagających potwierdzenia hipotez. Jednocześnie pojawiają się coraz nowsze i bardziej precyzyjne wyniki badań, pozwalające na zrozumienie procesów kontrolowanych przez białka Rho. Sugerowane jest między innymi zastosowanie ich w terapii pewnych schorzeń. Celem niniejszej pracy jest próba scharakteryzowania znaczenia rodziny białek Rho w cytoszkielecie komórki. Słowa kluczowe: białka Rho cytoszkielet aktyna Summary Proteins of the Rho protein family (RhoA, Rac1, Cdc42) work as molecular switches in the regulation of many cellular processes. They are involved in cell migration, cell-cycle control, apoptosis, and the regulation of gene transcription. Rho proteins show their activity mainly in the cell s cytoskeleton by taking part in the reorganization of microfilaments and microtubules. In recent years, significant progress has been made in understanding the biochemical and genetic nature of many processes controlled by Rho proteins. Although there are still seveal unknowns and hypothesizes which require confirmation, newer and more precise experimental results allow us to better understand these processes. It has also been suggested to use Rho family proteins in the therapy of some diseases. The purpose of this study was to characterize the significance of Rho processes in the cellular cytoskeleton. Key words: Rho proteins cytoskeleton actin Full-text PDF: Word count: 3535 Tables: 1 Figures: 3 References:
2 Nowak J.M. i wsp. Rodzina białek Rho i ich rola w cytoszkielecie komórki Adres autora: dr Agnieszka Żuryń, Katedra i Zakład Histologii i Embriologii, Collegium Medicum UMK, ul. Karłowicza 24, Bydgoszcz; azuryn@cm.umk.pl Wykaz skrótów: ABP białka wiążące się z aktyną (actin binding proteins); ARP2/3 białko spokrewnione z aktyną 2/3 (actin related protein 2/3); ATP adenozyno 5 trifosforan (adenosine 5 -triphosphate); ATPaza adenozyno 5 trifosfataza (adenosine 5 -triphosphatase); DFF czynnik fragmentacji DNA (DNA fragmentation factor); DH domena DH odpowiedzialna za wymianę nukletydów w białkach GEF (1-Db1 homology); DRF por. mdia (diaphanous-related formins); EGF czynnik wzrostu naskórka (epidermal growth factor); ERM spokrewnione białka: ezryna, radaksyna i moezyna umocowujące mikrofilamenty do błony plazmatycznej, np. w mikrokosmkach (ezrin, radexin, moesin); FAK kinaza FAK (focal adhesion kinase); GAP białko indukujące aktywność GTP-azy małych białek G (GTPase accelerating protein); GDI GDI wiążą nieaktywne białko Rho i hamują wymianę GDP na GTP (guanine nucleotide dissociation inhibitors); GDP guanozyno-5 difosforan (guanosine-5 diphosphate); GEF białko zaangażowane w wymianę GDP na GTP, aktywujące małe białka G (guanine nucleotid exchange factor); GTP guanozyno-5 trifosforan (guanosine- 5 triphosphate); GTP-aza guanozyno-5 trifosfataza (guanosine-5 triphosphatase); LIM białko LIM (LIM protein); LIMK kinaza LIM (LIM kinase); LPA kwas lizofosfatydowy (lysophosphatidic acid); MAP białka towarzyszące mikrotubulom (microtubule associated proteins); mdia białko efektorowe małych białek G rodziny Rho (mammalian homologue of Drosophila diaphanous) (DIA=DRF); Miro białko rodziny Rho występujące w mitochondrium (mitochondrial Rho); MLC lekkie łańcuchy miozyny (myosine light chains); MLCK kinaza lekkich łańcuchów miozyny (myosine light chains kinase); MLCP fosfataza lekkich łańcuchów miozyny (myosine light chains phosphatase); MAPK kinaza aktywowana przez mitogen (mitogen activated protein kinase); PCD programowana śmierć komórki apoptoza (programmed cell death); PDGF czynnik wzrostu pochodzący z płytek krwi (platelet-derived growth factor); PH domena białek GEF (pleckstrin homology); PIP 2 fosfatydyloinozytylo-4,5-bisfosforan (phosophatidylinositol-4,5-bisphosphate); Rac małe białko G z rodziny Rho; Ras małe białko G kodowane przez protoonkogen ras będący homologiem wirusowego onkogenu zidentyfikowanego w wirusie mięsaka myszy (rat sarcoma); Rb protoonkogenne fosfobiałko jądrowe (105 kda), uczestniczące w regulacji cyklu komórkowego (Rb protein, retinoblastoma protein); Rho białko należące do rodziny małych białek G (Ras homologous); ROCK kinaza zależna od Rho (Rho kinase); SCAR/WAVE białka należące do rodziny białek WASP (WASP family verprolin homologous protein); SRF czynniki transkrypcyjne aktywowane przez mitogeny surowicy (serum response factor); WASP białka kodowane przez gen wasp (Wiskott-Aldrich syndrom protein). RODZINA BIAŁEK RHO Białka Rho (Ras homologous) należą do nadrodziny małych białek G (białka Ras), które są monomerami o masie cząsteczkowej kda. Rho wiążą nukleotyd guaninowy (GTP lub GDP) [10,29]. Gen Rho odkryli w 1985 r. badacze pracujący nad glonem morskim Aplasi. Na podstawie sekwencji genu Rho wyizolowanego z Aplasi wyodrębniono trzy blisko spokrewnione geny ssacze, nazwane RhoA, RhoB oraz RhoC. Białko Rac natomiast, również należące do grupy białek Rho, zostało po raz pierwszy zidentyfikowane jako substrat transferazy C3 [29]. Był to zaledwie początek wielu odkryć związanych z tą rodziną białek. Dotąd zidentyfikowano ponad 100 różnych białek, należących do nadrodziny Ras, do których zaliczane są białka Rho. Rodzinę białek Rho podzielono na sześć podrodzin (ryc.1) uwzględniając zarówno podobieństwo w budowie, jak i pełnioną funkcję [4]. Przynależność do rodziny białek Rho jest uwarunkowana obecnością domen GTP-azowych typowych dla tej rodziny białek. Cechą charakterystyczną tych struktur jest obecność tzw. domeny Rho, która jest umiejscowiona pomiędzy piątym łańcuchem b a czwartą helisą a. Dzięki takiej budowie możliwe jest odróżnienie białek rodziny Rho od innych małych białek G. Większość Rho jest stosunkowo małymi białkami ( reszt aminokwasowych) i składa się głównie z domeny GTPazowej oraz krótkich elementów terminalnych na C-końcu i N-końcu [37]. Zidentyfikowano ponadto kilka nietypowych białek należących do tej rodziny zawierających dodatkowe domeny, które mogą mieć długość ponad 700 aminokwasów. Domeny GTP-azowe białek rodziny Rho wykazują homologię sekwencji aminokwasowej w 40 95%. Każde białko należące do tej rodziny ma sekwencję, dzięki której jest w stanie związać GTP lub GDP [37]. Białka te występują w dwóch postaciach: pierwsza związana z GTP aktywna i druga nieaktywna wiążąca GDP, działają na zasadzie molekularnych przełączników (ryc. 2). W postaci związanej z GTP są w stanie oddziaływać z efektorami lub cząsteczkami docelowymi zapoczątkowując łańcuch kolejnych reakcji [19,24,29,37]. Przejście w stan aktywny wymaga udziału dodatkowych białek re- 111
3 Postepy Hig Med Dosw (online), 2008; tom 62: Ryc. 1. Białka rodziny Rho z podziałem na sześć głównych grup: Rho-A spokrewnione, Rac-spokrewnione, Cdc42-spokrewnione, białka Rnd, białka RhoBTB oraz białka Miro gulatorowych. Białka regulujące aktywność GTP-az, do których zalicza się: GDI, GEF, GAP, odgrywają główną rolę w przekazywaniu sygnałów wewnątrzkomórkowych, pośredniczą w aktywowaniu czynników biorących udział w rearanżacji cytoszkieletu aktynowego oraz aktywują oksydazę NADPH u fagocytów [24,29]. Białka GEF zawierają dwie charakterystyczne domeny: DH (1-Db1 homology), odpowiedzialną za wymianę nukleotydów oraz domenę PH (pleckstrin homology), dzięki której białka te mogą się wiązać z fosfolipidami, np. błony cytoplazmatycznej [12,17]. Za swoistość szlaków sygnałowych związanych z białkami Rho są odpowiedzialne właśnie białka regulatorowe GEF, które oprócz tego, że są odpowiedzialne za aktywację białek rodziny małych GTP-az, wyznaczają również konkretną drogę przekazywania informacji przez białka Rho [17,20]. Koniec karboksylowy większości białek należących do podrodziny małych białek G ulega potranslacyjnej modyfikacji. Różnice w sekwencji C-końca oraz przemiany potranslacyjne wpływają na umiejscowienie białka wewnątrz komórki, determinując wiązanie z błoną, co istotnie wpływa na funkcję, jaką pełnią [37]. Białka homologiczne do Rho czy Rac zidentyfikowano u wszystkich organizmów eukariotycznych. Nie stwierdzono natomiast ich występowania u Procaryota [29]. Białka te, mimo że nie pełnią funkcji strukturalnych, często są umiejscowione w kilku różnych obszarach komórki. Mogą być również równomiernie rozprowadzone w cytoplazmie, a także wiązać się z błoną cytoplazmatyczną. Za przemieszczanie się, wiązanie i dysocjację białek Rho odpowiada swoista sekwencja końca karboksylowego tego białka, która podlega potranslacyjnej modyfikacji z udziałem lipidów. RhoGDI, jeden z czynników regulujących aktywność białka Rho, wiąże się z C-końcem białka, rozpoznając lipid znajdujący się na końcu karboksylowym, co w konsekwencji powoduje jego oddysocjowanie od błony cytoplazmatycznej i jednoczesne zahamowanie wymiany GDP-GTP. Ostatecznie białko Rho przyjmuje postać nieaktywną, wiążącą GDP i umiejscawia się w cytoplazmie [39]. Badania biochemiczne przeprowadzone przez Ryc. 2. Regulacja cyklu GTP-az Rho. Przejście z postaci nieaktywnej Rho- GDP w postać aktywną Rho-GTP wymaga białek regulatorowych GDI, GAP i GEF. GDI wiążą nieaktywne białko Rho i hamują wymianę GDP na GTP. GAP białko indukujące aktywność GTP-azy małych białek G GEF białko zaangażowane w wymianę GDP na GTP, aktywujące małe białka G (wg [8] zmodyfikowano) Fleminga i wsp. [13] dowiodły, że odpowiedzialnymi za te procesy mogą być czynniki pozakomórkowe, takie jak kwas LPA, który stymuluje transport i wiązanie białek do błony cytoplazmatycznej. Lokalizacja podrodziny małych białek G jest bardzo istotna, ponieważ umiejscowienie zwykle wiąże się z określoną funkcją białka. Rodzina białek Rho bierze udział w wielu różnorodnych procesach komórkowych, takich jak: organizacja cytoszkieletu, adhezja komórek, ich ruchliwość, egzocytoza czy transkrypcja. Bardzo istotne okazało się zbadanie dokładnej lokalizacji białek Rho w komórce podczas jej zmian morfologicznych oraz podczas odpowiedzi komórkowej na czynniki zewnętrzne. Yonemura i wsp. [39] wykazali obecność białek RhoA zarówno w błonie cytoplazmatycznej, jak i w samej cytoplazmie, a obserwowano komórki epitelialne oraz fibroblastyczne. Białka Rho gromadziły się w cytoplazmie, głównie w okolicach formujących się włókien naprężeniowych, ogniskach adhezyjnych oraz w bruździe podziałowej, a także w mikrowypustkach komórkowych. Udowodniono również, że Rho potrafią przemieszczać się i gromadzić w odpowiedzi na charakterystyczne czynniki stymulujące (lowostatyna LPA) [39]. Na poziomie tkankowym zaobserwowano dużą liczbę tych molekularnych przełączników w komórkach mezotelialnych oraz nabłonka wielowarstwowego języka, w rzęskach komórek epitelialnych tchawicy, w nabłonku pęcherza moczowego, a także w wielu innych tkankach [13]. 112
4 Nowak J.M. i wsp. Rodzina białek Rho i ich rola w cytoszkielecie komórki FUNKCJA BIOLOGICZNA Białka Rho są zaangażowane w regulację różnych funkcji komórkowych. Zaobserwowano, że odgrywają one ogromną rolę w wielu procesach komórkowych, takich jak: migracja komórek, regulacja transkrypcji czy transport pęcherzykowy. Dlaczego biorą one udział w tak wielu różnych procesach? Otóż białka te mają zdolność współdziałania z wieloma efektorami [11,20,29]. Odkryto, że te małe GTP-azy odgrywają również ważną rolę w procesie regulacji programowanej śmierci komórki (PCD) [4]. Rho zostało również scharakteryzowane jako regulator organizacji cytoszkieletu aktynowego. Badania dowiodły, że Rho stymuluje oraz reguluje formowanie włókien naprężeniowych zbudowanych z aktyny, jest mediatorem uczestniczącym w reorganizacji struktur aktynowych, m.in. w komórkach nerwowych. Pełni ponadto rolę w regulacji ruchliwości komórek np. neutrofili. Działanie Rho polega m.in. na regulacji fosforylacji lekkiego łańcucha miozyny [31]. Białko Rac1 promuje reorganizację aktyny w struktury zwane lamellipodiami, które są formowane na brzegu wiodącym komórki w pierwszym etapie jej ruchu [11,30]. Inne białko należące do tej rodziny RhoA, wpływa na formowanie ognisk adhezji, co promuje przyczepianie się komórek do podłoża. Białko RhoE natomiast powoduje destabilizację tych struktur, a w konsekwencji zaokrąglenie komórki [30]. Zmiany dynamiki cytoszkieletu regulowane przez GTP-azy Rho wiążą się z transportem wewnątrzkomórkowym, powstawaniem połączeń międzykomórkowych, cytokinezą oraz wpływają na polarność komórki. Dynamiczne rearanżacje cytoszkieletu powodowane aktywnością białek Rho wpływają na kształt komórki, kontakt między komórkami oraz między komórkami i macierzą zewnątrzkomórkową. Odzwierciedleniem tego jest wpływ na inwazyjność oraz zdolność komórek nowotworowych do metastazy [5,30]. Kolejną ważną funkcją, jaką pełnią GTP-azy Rho jest regulacja aktywności wielu czynników transkrypcyjnych. Białka Rac1, RhoA oraz Cdc42 aktywują SRF (serum response factor), który przez współdziałanie z innymi czynnikami moduluje aktywność SRE (serum response element) [16]. Białka Rho aktywują także wiele innych czynników transkrypcyjnych. Ich różnorodność, podlegająca regulacji przez małe białka G sugeruje, że białka Rho pełnią funkcję mediatorów transformacji [30]. Wykazano, że podrodzina małych białek G jest w stanie regulować postęp cyklu komórkowego oraz stymulować proliferację komórek. Aktywne postaci białek Rac1, RhoA oraz Cdc42 wpływają na postęp fazy G1 cyklu komórkowego poprzez modulowanie zarówno pozytywnych jak i negatywnych regulatorów supresora nowotworu Rb, którego zadaniem jest regulowanie postępu fazy G1. RhoA pełni funkcję antagonisty ekspresji dwóch negatywnych regulatorów progresji fazy G1: cyklinozależnych inhibitorów kinazy p21 CIP1 oraz p27 KIP1. Inhibicja p21 CIP1 jest jednym z mechanizmów, dzięki którym GTP-azy Rho mogą uaktywnić białka Ras, będące jednostkami stymulującymi wzrost komórki [24,30]. WPŁYW BIAŁEK RHO NA ORGANIZACJĘ CYTOSZKIELETU Jak dotąd najlepiej poznanymi białkami rodziny Rho są Cdc42, Rac1 oraz RhoA. Hall i wsp. [15] w swoich badaniach wykazali, że aktywacja poszczególnych białek tej rodziny prowadzi do formowania struktur zbudowanych z aktyny. Aktywacja Cdc42 stanowi sygnał do formowania filopodiów, Rac1 reguluje powstawanie lamellipodiów, RhoA natomiast wpływa na formowanie włókien naprężeniowych oraz ognisk kontaktowych [18,33,35]. Białko Cdc42 bierze udział w odbieraniu sygnałów z przestrzeni międzykomórkowej, stymulując wydłużanie filopodiów oraz wpływa na ustalenie polarności komórki podczas ukierunkowanej migracji. Wydłużanie lamellipodiów przez polimeryzację aktyny przy krawędzi wiodącej komórki jest kontrolowane przez GTP-azę Rho Rac1 [6,11]. Kolejne białko rodziny małych białek G, RhoA, stymuluje polimeryzację aktyny przez aktywację białek Dia (zwanych również DRFs - diaphanous-releted formins), które stymulują dodawanie monomerów aktyny do końca (+) plus filamentu. DRF współdziałają razem z kinazami ROCK, co prowadzi ostatecznie do powstania włókien naprężeniowych [15,38]. Współdziałanie ROCK z DRF odgrywa główną rolę w regulacji polarności komórki oraz organizacji mikrotubul. Ich stabilność jest regulowana przez kinazę ROCK, odpowiedzialną za fosforylację białek Tau oraz MAP2. Działanie DRF, polegające na stabilizowaniu oraz koordynowaniu orientacji mikrotubul, wywołane jest przez miejscową aktywację białek Rho z udziałem szlaku integryna/fak [38]. Małe białka G, głównie białka Ras oraz Rho wzajemnie na siebie oddziałują. Ras mają zdolność aktywacji Rac (dlatego Ras indukuje powstawanie lamellipodiów), Cdc42 wpływają na Rac, które z kolei inicjują działanie Rho. Oddziaływania między białkami rodzin Rho i Rac wskazują, że są one głównymi molekułami, które odbierają sygnały z receptorów powierzchniowych i wpływają na organizację cytoszkieletu aktynowego [18]. Machesky i Hall w badaniach nad rolą polimeryzacji aktyny i adhezji dowiedli, że Rac indukuje szybkie tworzenie filamentów aktynowych w miejsce pofałdowań błony komórkowej, podczas gdy Rho powoduje montaż włókien naprężeniowych przez formowanie skupień włókien F-aktyny. Aktywacja zarówno Rac jak i Rho prowadzi do formowania kompleksów adhezyjnych, w których powstawaniu pośredniczą integryny. Łączenie się cząsteczek integryny nie jest wymagane w indukowanym przez Rho tworzeniu skupień aktomiozynowych wiązek filamentów oraz przy wiązaniu z pęczkami aktyny. Jest natomiast konieczne podczas tworzenia włókien naprężeniowych. Białka Rac i Rho wywołują zmiany cytoszkieletu w dwóch kierunkach. Lamellipodia powstają niezależnie od tworzenia kompleksów integryn na skutek miejscowej polimeryzacji aktyny z udziałem białek Rac w części peryferyjnej komórki. Natomiast włókna naprężeniowe powstałe w następstwie działania białek Rho są tworzone poprzez zależne od kompleksów integryn formowanie pęczków filamentów aktynowych [22]. Rodzina białek Rho jest głównym regulatorem organizacji cytoszkieletu. Dzieje się to w wyniku działania GTP-az Rho na białka efektorowe, takie jak: kinazy Rho-zależne (ROCK1, ROCK2) i białka mdia (mdia1,2). Aktywacja mdia z udziałem Rho inicjuje polimeryzację aktyny dzięki białku wiążącemu aktynę profilinie. Białko mdia reguluje natomiast formowanie i organizację mikrotubul. Kinazy ROCK1,2 aktywują kinazy LIM1 i LIM2, które powodują 113
5 Postepy Hig Med Dosw (online), 2008; tom 62: Tabela 1. Wpływ białek rodziny Rho na organizację cytoszkieletu (wg [3] zmodyfikowano) GTP-azy Występowanie Działanie na cytoszkielet aktynowy Rac1 powszechnie lamellipodia, pofałdowanie błon, ogniska kontaktowe Rac2 komórki krwiotwórcze aktywowanie oksydazy NADHP, ogniska kontaktowe Rac3 serce, łożysko, mózg, trzustka formowanie ognisk kontaktowych, lamellipodia RhoG powszechnie pofałdowanie błony, lamellipodia Cdc42 powszechnie filopodia, dezorganizacja włókien naprężeniowych TC10 mięśnie szkieletowe, serce, wątroba dezorganizacja włókien naprężeniowych, tworzenie ognisk kontaktowych Rnd1 (Rho6) mózg, wątroba dezorganizacja włókien naprężeniowych, zniesienie adhezji Rnd2 (Rho7) jądra, mózg, wątroba dezorganizacja włókien naprężeniowych, zniesienie adhezji RhoE (Rnd3) powszechnie dezorganizacja włókien naprężeniowych (komórki MDCK), pofałdowanie błony (makrofagi) RhoA powszechnie tworzenie ognisk kontaktowych i włókien naprężeniowych RhoB powszechnie włókna naprężeniowe RhoC powszechnie włókna naprężeniowe RhoH (TTF) komórki krwiotwórcze brak wpływu na cytoszkielet aktynowy RhoD (HP1) powszechnie (niski poziom w mózgu i komórkach krwiotwórczych) pofałdowanie błony, dezorganizacja włókien naprężeniowych, filopodia Rif powszechnie filopodia Miro-1 powszechnie brak wpływu na cytoszkielet aktynowy (występuje jedynie w mitochodrium) Miro-2 powszechnie brak wpływu na cytoszkielet aktynowy (występuje jedynie w mitochodrium) RhoBTB-1 powszechnie umiarkowany wpływ na organizację włókien naprężeniowych RhoBTB-2 mózg umiarkowany wpływ na organizację włókien naprężeniowych fosforylację kofiliny białka odpowiedzialnego m.in. za depolimeryzację F-aktyny, prowadząc do jej inaktywacji. Zwiększa to intensywność polimeryzacji filamentów aktynowych oraz wpływa na stabilizację włókien naprężeniowych. Kinazy ROCK1,2 fosforylują lekki łańcuch miozyny (MLC-P), co zwiększa kurczliwość miozyny i hamuje fasfatazę MLC (MLC-PPaza). Aktywacja kinaz ROCK1,2 przez GTP-azy Rho prowadzi zarówno do formowania aktynowych włókien naprężeniowych, jak i do zwiększenia kurczliwości struktur włóknistych (aktomiozynowych), co obserwuje się m.in. w takich procesach jak: formowanie kompleksów integryn, tworzenie ognisk kontaktowych, a także w adhezji komórek (ryc. 3) [6]. SZLAKI SYGNALIZACYJNE Z UDZIAŁEM BIAŁEK RHO Białka rodziny Rho funkcjonujące na zasadzie molekularnych przełączników kontrolują poprzez kaskady sygnalizacyjne organizację i dynamikę cytoszkieletu aktynowego. Droga sygnałowa z udziałem białek Rho jest inicjowana przez różne receptory znajdujące się na błonie komórkowej. Są to m.in.: receptor kinazy tyrozynowej, receptory cytokin czy też receptory wiążące białka G. Stymulacja tych receptorów zachodzi m.in. przez ligandy (kwas lizofasfatydowy, bombezyna, bradykinina czy trombina) oraz z udziałem cząsteczek adhezyjnych, takich jak integryny, kadhedryny i białka nadrodziny immunoglobulin [12,20]. Białka Rho odbierają również sygnały z receptorów aktywowanych przez naskórkowy i płytkopochodny czynnik wzrostu (EGF, PDGF), czy też przez insulinę [20]. Receptory aktywują białko regulatorowe GEF odpowiedzialne za przejście nieaktywnego białka Rho związanego z GDP w aktywne, połączone z GTP [3]. Dotąd poznano wiele białek, które wiążą się z aktywną postacią białek Rho i pełnią funkcję białek efektorowych. Na szczególne zainteresowanie zasługuje kinaza ROCK (Rho kinase), zwana również p160rho [2,12]. ROCK jest kinazą serynowo/treoninową, zidentyfikowano ją prawie 10 lat temu jako białko wiążące się z Rho-GTP. Występuje w postaci dwóch izoform ROCK1 i ROCK2. Kinazy te wykazują swoistość tkankową. Izoformy ROCK1 występują głównie w takich narządach jak serce, płuca, mięśnie szkieletowe, natomiast ROCK2 jest obecna przede wszystkim w mózgu. Kinazy ROCK pełnią istotne funkcje w procesach migracji komórki, proliferacji oraz są odpowiedzialne za przeżycie komórki [25]. Wpływają na kształt komórek wpływając na kurczliwość struktur aktynowych i miozynowych [11]. Nieprawidłowa aktywacja drogi sygnałowej Rho/ROCK prowadzi do wielu zaburzeń ośrodkowego układu nerwo- 114
6 Nowak J.M. i wsp. Rodzina białek Rho i ich rola w cytoszkielecie komórki wiążące aktynę, tzw. białka ABP (m.in. profilina, kofilina, a-aktynina, winkulina, spektryna), a co się z tym wiąże na formowanie włókien naprężeniowych i ognisk kontaktowych [12]. Profilina jest niezbędna do formowania połączeń pomiędzy włóknami naprężeniowymi oraz ogniskami kontaktowymi [20]. Kolejnym fizjologicznie aktywnym efektorem białek Rho jest białko p140mdia. Stymuluje ono polimeryzację aktyny na dwa sposoby, bezpośrednio lub pośrednio przez oddziaływanie z mikrotubulami czy przez interakcje z profiliną, wiążącą monomery aktynowe i promującą polimeryzację. Białko p140mdia jest istotnym czynnikiem regulującym ilość i strukturę włókien naprężeniowych [20]. BIAŁKA RHO A POLIMERYZACJA AKTYNY Ryc. 3. Regulacja cytoszkieletu przez białka Rho (wg [6] zmodyfikowano) wego [25]. Kinaza ta została odkryta i scharakteryzowana jako białko pośredniczące w indukowanym przez Rho formowaniu włókien naprężeniowych i ognisk kontaktowych [20]. Kinazy ROCK prowadzą do fosforylacji wielu białek. Jednym z głównych substratów kinazy ROCK jest lekki łańcuch miozyny MLC (myosin light chain). Fosforylacja MLC prowadzi do formowania struktur aktomiozynowych. ROCK pośrednio reguluje ilość ufosforylowanych MLC poprzez inaktywowanie fosfatazy MLC, czyli MLCP [12]. Kolejnym substratem kinaz ROCKs są Ser/Thr kinazy LIM (LIMK1 i LIMK2). Ufosforylowana kinaza LIM prowadzi do zahamowania działania kofiliny (przez fosforylację), a co się z tym wiąże do stabilizacji struktur zbudowanych z filamentów aktynowych [7,26]. ROCK fosforyluje również białka z rodziny ERM (ezrin, radexin, moesin) oraz inne białka zaangażowane w regulację cytoszkieletu. Substratami są również białka filamentów pośrednich, takie jak: wimentyna, kwaśne fibrylarne białka glejowe, neurofilamenty, które podczas fosforylacji przez ROCK ulegają depolimeryzacji [2,12]. Także białka towarzyszące mikrotubulom tzw. MAP2 (microtubule associated protein) oraz białka tau, należą do substratów kinaz ROCK. Fosforylacja białek tau zmniejsza ich aktywność, co promuje formowanie mikrotubul in vitro [25]. Aktywność kinazy ROCK wzrasta w niewielkim stopniu po związaniu Rho-GTP. Leung i wsp. [12] udowodnili, że nadekspresja białka kinazy aktywowanej przez Rho powoduje formowanie się włókien naprężeniowych i ognisk kontaktowych w komórce [12]. Drugim ważnym działaniem białek Rho jest wpływ na syntezę fosfatydyloinozytolu-4,5-bisfosforanu, PI(4,5)P 2. Kinaza fosforylująca fosfatydyloinozytolo-4-fosforan jest aktywowana bezpośrednio przez wiązanie się z aktywną postacią białka Rho [32]. Stymulacja syntezy PI(4,5)P 2 może wpływać na reorganizację aktyny poprzez białka W komórkach eukariotycznych G-aktyna pozostaje w dynamicznej równowadze ze spolimeryzowaną F-aktyną. Wzrost filamentów F-aktyny zachodzi na końcach plus (barbed ends), natomiast demontaż na końcach minus (pointed ends). Polimeryzacja na końcu plus podlega kontroli przez białka czapeczkujące (np. gelsolina), które przyłączają się z dużym powinowactwem i zapobiegają elongacji filamentów aktynowych. Polimeryzacja aktyny wywoływana jest przez wiele mechanizmów, jednym z nich jest nukleacja de novo wywołana przez kompleks białek ARP2/3 (actin related protein 2/3). W wyniku tego procesu dochodzi do formowania sieci rozgałęzień F-aktyny w kształcie litery Y. Mechanizm ten jest istotny podczas fagocytozy, migracji komórki oraz w jej polaryzacji [12,22]. Kompleks ARP2/3 aktywowany jest przez cząsteczki ATP, a kontrola tego procesu zachodzi z udziałem wielu białek [1,35,36]. Należą do nich białka rodziny WASP (Wiskott-Aldrich syndrom protein), nerwowe (N-) WASP oraz trzy izoformy białek SCAR/WAVE (WASP family verprolin homologous protein) [1,2,35]. Białka rodziny WASP mają na karboksylowym końcu domenę WCA, do której przyłącza się kompleks ARP2/3. Natomiast w regionie N-terminalnym białek WASP znajduje się domena GBD odpowiadająca za wiązanie GTP-azy Cdc42, jednego z najlepiej scharakteryzowanych białek rodziny Rho. Domena WCA inicjuje nukleację aktyny z udziałem kompleksu ARP2/3. Białka WASP podlegają autoinhibicji przez łączenie regionu centralnego domeny WCA z domeną B/GBD, która znajduje się w pobliżu regionu odpowiedzialnego za przyłączanie Cdc42/Rac. Autoinhibicja może zostać zahamowana, gdy z domeną GBD zwiąże się postać Cdc42 z przyłączonym GTP. W ten sposób białko rodziny Rho ma możliwość bezpośrednio aktywować nukleację aktyny [1,35]. CYTOSZKIELET A APOPTOZA WPŁYW BIAŁEK RHO Podczas apoptozy komórka podlega charakterystycznym zmianom morfologicznym, m.in. kurczy się, chromosomy ulegają kondensacji, tworzą się pęcherzyki apoptotyczne [28]. Wiele badań zostało poświęconych organizacji aktyny podczas zmian błony cytoplazmatycznej w procesie programowanej śmierci komórki [6,9,14,27]. Dowiedziono, że F-aktyna jest konieczna podczas uwypuklania błony komórkowej w celu formowania pęcherzyków (blebbing) oraz tworzenia ciałek apoptotycznych [14,23]. Ilość F-aktyny koreluje z wielkością pęcherzyków. Jest ona obecna w podstawie formujących się pęcherzyków podczas apop- 115
7 Postepy Hig Med Dosw (online), 2008; tom 62: tozy i ulega trawieniu przez kaspazy. Jednak nie tylko aktyna odgrywa istotną rolę podczas zmian strukturalnych prowadzących do wytworzenia pęcherzyków apoptotycznych. Na podstawie modelu doświadczalnego stworzonego przez Millsa i wsp. [23] udowodniono, że tworzenie uwypukleń błony komórkowej połączone z wytworzeniem pęcherzyków jest regulowane przede wszystkim przez fosforylację lekkiego łańcuchach miozyny MLC. Fosforylacja MLC pozwala konwencjonalnej miozynie (miozyna II) przyłączyć aktynę, co prowadzi do wytworzenia siły warunkującej ruchliwość, kurczenie się komórek. W fosforylacji MLC pośredniczy swoista miozynowo fosfataza MLCK (kinaza lekkich łańcuchów miozyny) oraz ROCK (kinaza Rho zależna). ROCK odgrywa podwójną rolę, po pierwsze bezpośrednio w fosforylacji i aktywacji MLC, po drugie pośrednio przez inhibicję fosfatazy MLC (ryc. 3) [23]. Skojarzenie funkcji miozyny II z mechanizmem powodującym powstanie uwypukleń błony komórkowej prowadzącym do wytworzenia pęcherzyków pozwoliło stworzyć model, wyjaśniający zmiany morfologiczne komórki we wczesnej fazie wykonawczej apoptozy. Skurcze pierścienia aktynowego usytuowanego w części peryferycznej komórki, tuż pod błoną komórkową, powodują wytworzenie siły dośrodkowej, która implikuje koncentrację cytoplazmy w obrębie centrum komórki. Jeżeli białka strukturalne (fodryna, ABP białka wiążące aktynę), łączące błonę komórkową z warstwą korową aktyny ulegną inaktywacji, wówczas siła dośrodkowa wepchnie pierścień aktynowy do wewnątrz komórki i spowoduje wypchnięcie cytoplazmy w miejscach osłabionego wiązania aktyny z błoną cytoplazmatyczną. Ostatecznie objawia się to wytworzeniem pęcherzyków i potwierdza, że siła skurczowa potrzebna do wytworzenia pęcherzyków jest generowana przez struktury aktomiozynowe [9,23]. Destabilizacja mikrotubul odgrywa istotną rolę w regulacji tworzenia ciałek apoptotycznych. Mikrotubule ulegają dezorganizacji podczas końcowych etapów apoptozy, co prowadzi do kurczenia się komórek apoptotycznych. Jest to związane ze zwiększeniem fosforylacji MLC [23,24]. Hangmann i wsp. [14] potwierdzili, że tworzenie pęcherzyków na skutek uwypuklenia błony cytoplazmatycznej jest regulowane przez trzy podstawowe elementy cytoszkieletu: mikrofilamenty, filamenty pośrednie oraz mikrotubule. Przedstawili oni model, w którym krótkotrwałe formowanie pęcherzyków poprzez aktywację miozyny było indukowane kwasem lizofosfatydowym (LPA). Jako pierwsi bezpośrednio wykazali, że akumulacja aktyny wzdłuż przestrzeni cytoplazmatycznej błony pęcherzyka wiąże się z fazą apoptozy, w której następuje kurczenie się pęcherzyka [14]. Białka rodziny Rho pełnią wiele istotnych funkcji w procesach apoptotycznych. Udowodniono, że biorą udział w reorganizacji cytoszkieletu podczas apoptozy, wpływając tym samym na zmiany w morfologii komórek apoptotycznych [9,23,27]. Rho, należące do małych białek G regulując fosforylację lekkich łańcuchów miozyny (MLC) odgrywają istotną rolę podczas tworzenia pęcherzyków na początku fazy wykonawczej programowanej śmierci komórki. W fosforylację MLC zaangażowane są ROCK i MLCK. Rho pośredniczy w fosforylacji MLC przez aktywację ROCK. Kinaza zależna od Rho fosforyluje serynę w pozycji 19, tak jak MLCK. ROCK fosforyluje ponadto i inaktywuje podjednostkę fosfatazy MLC, powodując zwiększenie fosforylacji MLC [6]. W badaniach przeprowadzonych przez Millsa i wsp. [23] wykazano, że białka Rho, które zwiększają fosforylację MLC, pełnią istotne funkcje podczas formowania pęcherzyków apoptotycznych. Inaktywacja białek Rho w komórkach ulegających apoptozie prowadzi do zahamowania procesów, które prowadzą do wytworzenia ciałek apoptotycznych [23]. Najlepiej dotąd scharakteryzowanym przedstawicielem rodziny małych białek G, zaangażowanym w procesy regulacji zmian morfologicznych komórek ulegających apoptozie jest RhoA. Odpowiada ono m.in. za formowanie aktynowych włókien naprężeniowych oraz za generowanie siły skurczowej przez kompleks aktyny i miozyny II. Zaproponowano, że to właśnie RhoA jest odpowiedzialne za kurczenie się komórek i formowanie pęcherzyków podczas apoptozy [9]. Dzieje się to przede wszystkim w wyniku aktywacji przez RhoA określonych białek efektorowych, głównie ROCK1 i ROCK2. Badania prowadzone przez Colemana i wsp. [9] wykazały również, że białko efektorowe GTP-az Rho, jakim jest ROCK1 wpływa na procesy mające związek ze zmianami morfologii komórki podczas apoptozy, dzięki aktywacji ROCK1 przez kaspazy. Prowadzi to do fosforylacji lekkich łańcuchów miozyny, aktywacji miozyny ATP-azowej i sprzężenia filamentów aktomiozynowych z błoną cytoplazmatyczną. Aktywność ROCK1 jest konieczna i jednocześnie wystarczająca zarówno do formowania pęcherzyków na skutek uwypukleń błony, jak również do relokalizacji fragmentów DNA do pęcherzyków i ciałek apoptotycznych [9]. Kinazy Rho regulują nie tylko fragmentację, ale również fagocytozę komórek apoptotycznych, co udowodnili Orlando i wsp. [27]. Wykazali oni, że przekazywanie sygnałów z udziałem ROCK1 wpływa na regulację fragmentacji umierającej komórki i upakowanie produktów jej rozkładu w ciałka apoptotyczne. Zaproponowali model doświadczalny, w którym ROCK1 jest rozcinana i aktywowana przez kaspazy podczas programowanej śmierci komórki, oraz że aktywna ROCK1 zwiększa siłę skurczową struktur aktomiozynowych. Prowadzi to z kolei do fragmentacji i wytworzenia ciałek apoptotycznych. Po raz pierwszy zauważyli i potwierdzili w swoich badaniach, że aktywacja ROCK1 odrywa istotną rolę podczas przygotowania komórek do procesu fagocytozy poprzez kontrolę ich fragmentacji [27]. Aktywacja kinazy Rho-zależnej przyczynia się do generowania siły skurczowej struktur aktomiozynowych poprzez fosforylację wielu białek efektorowych. Zależna od Rho aktywacja LIMK1 i LIMK2 prowadzi do fosforylacji i inaktywacji kofiliny. ROCK fosforyluje bezpośrednio MLC, kalponinę oraz białko CPI-17, co również prowadzi do zwiększenia siły skurczowej struktur aktomiozynowych. Reasumując, aktywacja ROCK objawia się tym, że komórka może się kurczyć i tworzyć charakterystyczne struktury obserwowane podczas apoptozy [8]. Kinaza Rho-zależna może być aktywowana dwiema drogami, albo dzięki kaspazom, albo dzięki małym białkom G. 116
8 Nowak J.M. i wsp. Rodzina białek Rho i ich rola w cytoszkielecie komórki Obydwa te szlaki prowadzą do generowania skurczów aktomiozynowych, koniecznych podczas zmian morfologicznych w procesie programowanej śmierci komórki. PODSUMOWANIE Białka należące do rodziny Rho wpływają na wiele procesów komórkowych. Wielu badaczy zajmuje się analizowaniem tej cały czas powiększającej grupy białek, a w ciągu ostatnich lat dokonał się znaczący postęp w zrozumieniu zarówno biochemicznej, jak i genetycznej natury procesów, w które są zaangażowane białka Rho. Rodzina GTPaz Rho wpływa na organizację cytoszkieletu komórki i adhezję komórek. Białka te są zaangażowane również w takie procesy komórkowe, jak: migracja, transport pęcherzykowy, regulacja transkrypcji, egzocytoza, cykl komórkowy i apoptoza. Wpływ białek Rho na organizację cytoszkieletu przejawia się w ustalaniu polarności komórki, wydłużaniu filopodiów (Cdc42), wydłużaniu lamellipodiów poprzez polimeryzację aktyny (Rac1) oraz tworzeniu włókien naprężeniowych (RhoA). Ponadto, białka te dzięki oddziaływaniu na ROCK stabilizują i koordynują orientację mikrotubul. Wykazano również, że zwiększają one kurczliwość struktur włóknistych, co zaobserwowano podczas formowania kompleksów integryn, tworzeniu ognisk kontaktowych i adhezji komórek. Cytoszkielet aktynowy stanowi dynamiczny układ, który podlega ciągłym przeobrażeniom. Białka rodziny Rho pełnią nadrzędną funkcję w kontrolowaniu zjawisk komórkowych powiązanych z reorganizacją cytoszkieletu. Stanowią one główny regulator tych procesów a poprzez interakcje z białkami docelowymi, zapewniają skoordynowaną regulację innych czynności komórkowych, takich jak transkrypcja genów oraz adhezja, a także ruch komórkowy oraz apoptoza. Dokładne poznanie funkcji regulacyjnych białek Rho podczas istotnych procesów komórkowych, w które białka te są zaangażowane prawdopodobnie pozwoli w przyszłości na ich potencjalne wykorzystanie w terapii wielu schorzeń. PIŚMIENNICTWO [1] Aktories K., Barbieri J.T.: Bacterial cytotoxins: targeting eukaryotic switches. Nat. Rev. Microbiol., 2005; 5: [2] Aspenstrőm P.: Effectors for the Rho GTPases. Curr. Opin. Cell. Biol., 1999; 11: [3] Aspenstrőm P., Fransson A., Saras J.: Rho GTPases have diverse effects on the organization of the actin filament system. Biochem. J., 2004; 377: [4] Aznar S., Lacal J.C.: Rho signals to cell growth and apoptosis. Cancer. Lett., 2001; 165: 1 10 [5] Begum R., Nur-E-Kamal M.S., Zaman M.A.: The role of Rho GTPases in the regulation of rearrangement of actin cytoskeleton and cell movement. Exp. Mol. Med., 2004; 36: [6] Besson A., Assoian R.K., Roberts J.M.: Regulation of the cytoskeleton: an oncogenic function for CDK inhibitors. Nat. Rev. Cancer, 2004; 4: [7] Bishop A., Hall A.: Rho GTPases and their effector proteins. Biochem. J., 2000; 348: [8] Coleman M.L., Olson M.F.: Rho GTPase signalling pathways in the morphological changes associated with apoptosis. Cell Death Differ., 2002; 9: [9] Coleman M.L., Sahai E.A., Yeo M., Bosch M., Dewar A., Olson M.F.: Membrane blebbing during apoptosis results form caspase-mediated activation of ROCK I. Nat. Cell. Biol., 2001; 3: [10] Corbett K.D., Alber T.: The many faces of Ras: Recognition of small GTP-binding proteins. Trends Biochem. Sci., 2001; 26: [11] Etienne-Manneville S., Hall A.: Rho GTPases in cell biology. Nature, 2002; 420: [12] Fabczak H.: Rodzina białek Rho a cytoszkielet. Kosmos, 2001; 252: [13] Fleming I.N., Elliott C.M., Exton J.H.: Differential translocation of rho family GTPases by lysophosphatidic acid, endothelin-1, and platelet-derived growth factor. J. Biol. Chem., 1996; 271: [14] Hagmann J., Burger M.M., Dagan D.: Regulation of plasma mebrane blebbing by the cytoskeleton. J. Cell. Biochem., 1999; 73: [15] Hall A., Nobes C.D.: Rho GTPases: molecular switches that control the organization and dynamics of the actin cytoskeleton. Philos. Trans. R. Soc. Lond. B. Biol. Sci., 2000; 355: [16] Hill C.S., Wynne J., Treisman R.: The Rho family GTPases RhoA, Rac1 and Cdc42Hs regulated transcriptional activation by SRF. Cell, 1995; 81: [17] Hornstein I., Alcover A., Katzav S.: Vav proteins, masters of the world cytoskeleton organization. Cell Signal., 2004; 16: 1 11 [18] Karnoub A.E., Der C.J.: Rho family GTPases and cellular transformation. Eurekah Bioscience 2003; bv.fcgi?rid=eurekah.chapter ( ) [19] Kjoller L., Hall A.: Signalling to Rho GTPases. Exp. Cell. Res., 1999; 253: [20] Kłopocka W., Barańska J.: Rola rodziny białek Rho w kontroli migracji komórek pełzających. Post. Biochem., 2005; 54: [21] Luo L.: Rho GTPases in neuronal morphogenesis Nat. Rev. Neurosci., 2000; 1: [22] Machesky L.M, Hall A.: Role of actin polymerization and adhesion to extracellular matrix in Rac- and Rho-induced cytoskeletal reorganization. J. Cell Biol., 1997; 138: [23] Mills J.C., Stone N.L., Erhardt J., Pittman R.N.: Apoptotic membrane blebbing is regulated by myosin light chain phosphorylation. J. Cell Biol., 1998; 140: [24] Moon S.Y., Zheng Y.: Rho GTPase-activating proteins in cell regulation. Trends. Cell Biol., 2003; 13: [25] Mueller B.K., Mack H., Teusch N.: Rho kinase, a promising drug target for neurological disorders. Nat. Rev. Drug. Discov., 2005; 4: [26] Olson M.F, Paterson H.F., Marshall C.J.: Signals from Ras and Rho GTPases interact to regulate expression of p21waf1/cip1. Nature, 1998; 394: [27] Orlando K.A., Stone N.L., Pittman R.N.: Rho kinase regulates fragmentation and phagocytosis of apoptotic cells. Exp. Cell Res., 2006; 312: 5 15 [28] Ostrowski M., Grzanka A., Izdebska M.: Rola aktyny w chorobie Alzheimera. Post. Hig. Med. Dośw., 2005; 59: [29] Ridley A.: Rho family proteins: coordinating cell response. Trends Cell Biol., 2001; 11: [30] Ridley A.: Rho proteins: linking signaling with membrane trafficking. Traffic 2001; 2: [31] Ridley A.J.: The GTP-binding protein Rho. Int. J. Biochem. Cell Biol., 1997; 29: [32] Small J.V., Rottner K., Kaverina I.: Functional design in the actin cytoskeleton. Curr. Opin. Cell Biol., 1999; 11: [33] Small J.V., Stradal T., Vignal E., Rottner K.: The lamellipodium: where motility begins. Trends Cell Biol., 2002; 12: [34] Song Y., Hoang B.Q., Chang D.D.: ROCK-II-induced membrane blebbing and chromatin condensation require actin cytoskeleton. Exp. Cell. Res., 2002; 278: [35] Tapon N., Hall. A.: Rho, Rac, and Cdc42 GTPases regulate the organization of the cytoskeleton. Curr. Opin. Cell. Biol., 1997; 9: [36] Weed S.A., Parsons J.T.: Cortactin: coupling membrane dynamics to cortical actin assembly. Oncogene, 2001; 20: [37] Wennerberg K., Der C.J.: Rho-family GTPases: it s not only Rac and Rho (and I like it). J. Cell Sci., 2004; 117: [38] Wheeler A.P., Ridley A.J.: Why three Rho proteins? RhoA, RhoB, RhoC, and cell motility. Exp. Cell Res., 2004; 301: [39] Yonemura S., Hirao-Minakuchi K., Nishimura Y.: Rho localization in cell and tissues. Exp. Cell Res., 2004; 295:
CYTOSZKIELET CYTOSZKIELET
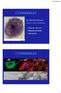 CYTOSZKIELET Sieć włókienek białkowych; struktura wysoce dynamiczna Filamenty aktynowe Filamenty pośrednie Mikrotubule Fibroblast CYTOSZKIELET 1 CYTOSZKIELET 7nm 10nm 25nm Filamenty pośrednie ich średnica
CYTOSZKIELET Sieć włókienek białkowych; struktura wysoce dynamiczna Filamenty aktynowe Filamenty pośrednie Mikrotubule Fibroblast CYTOSZKIELET 1 CYTOSZKIELET 7nm 10nm 25nm Filamenty pośrednie ich średnica
CYTOSZKIELET CYTOSZKIELET Cytoplazma podstawowa (macierz cytoplazmatyczna) Komórka eukariotyczna. cytoplazma + jądro komórkowe.
 Komórka eukariotyczna cytoplazma + jądro komórkowe (układ wykonawczy) cytoplazma podstawowa (cytozol) Cytoplazma złożony koloid wodny cząsteczek i makrocząsteczek (centrum informacyjne) organelle i kompleksy
Komórka eukariotyczna cytoplazma + jądro komórkowe (układ wykonawczy) cytoplazma podstawowa (cytozol) Cytoplazma złożony koloid wodny cząsteczek i makrocząsteczek (centrum informacyjne) organelle i kompleksy
Filamenty aktynowe ORGANIZACJA CYTOPLAZMY. komórki CHO (Chinese hamster ovary cells ) Hoechst jądra, BOPIPY TR-X phallacidin filamenty aktynowe
 Filamenty aktynowe ORGANIZACJA CYTOPLAZMY komórki CHO (Chinese hamster ovary cells ) Hoechst jądra, BOPIPY TR-X phallacidin filamenty aktynowe Cytoszkielet aktynowy G-aktyna 370 aminokwasów 42 43 kda izoformy:
Filamenty aktynowe ORGANIZACJA CYTOPLAZMY komórki CHO (Chinese hamster ovary cells ) Hoechst jądra, BOPIPY TR-X phallacidin filamenty aktynowe Cytoszkielet aktynowy G-aktyna 370 aminokwasów 42 43 kda izoformy:
ROLA WAPNIA W FIZJOLOGII KOMÓRKI
 ROLA WAPNIA W FIZJOLOGII KOMÓRKI Michał M. Dyzma PLAN REFERATU Historia badań nad wapniem Domeny białek wiążące wapń Homeostaza wapniowa w komórce Komórkowe rezerwuary wapnia Białka buforujące Pompy wapniowe
ROLA WAPNIA W FIZJOLOGII KOMÓRKI Michał M. Dyzma PLAN REFERATU Historia badań nad wapniem Domeny białek wiążące wapń Homeostaza wapniowa w komórce Komórkowe rezerwuary wapnia Białka buforujące Pompy wapniowe
Komórka eukariotyczna organizacja
 Komórka eukariotyczna organizacja Centrum informacyjne jądro Układ wykonawczy cytoplazma cytoplazma podstawowa (cytozol) organelle cytoplazma + jądro komórkowe = protoplazma Komórka eukariotyczna organizacja
Komórka eukariotyczna organizacja Centrum informacyjne jądro Układ wykonawczy cytoplazma cytoplazma podstawowa (cytozol) organelle cytoplazma + jądro komórkowe = protoplazma Komórka eukariotyczna organizacja
Komórka eukariotyczna organizacja
 Komórka eukariotyczna organizacja Centrum informacyjne jądro Układ wykonawczy cytoplazma cytoplazma organelle podstawowa (cytozol) cytoplazma + jądro komórkowe = protoplazma Komórka eukariotyczna organizacja
Komórka eukariotyczna organizacja Centrum informacyjne jądro Układ wykonawczy cytoplazma cytoplazma organelle podstawowa (cytozol) cytoplazma + jądro komórkowe = protoplazma Komórka eukariotyczna organizacja
Nukleotydy w układach biologicznych
 Nukleotydy w układach biologicznych Schemat 1. Dinukleotyd nikotynoamidoadeninowy Schemat 2. Dinukleotyd NADP + Dinukleotydy NAD +, NADP + i FAD uczestniczą w procesach biochemicznych, w trakcie których
Nukleotydy w układach biologicznych Schemat 1. Dinukleotyd nikotynoamidoadeninowy Schemat 2. Dinukleotyd NADP + Dinukleotydy NAD +, NADP + i FAD uczestniczą w procesach biochemicznych, w trakcie których
THE UNFOLDED PROTEIN RESPONSE
 THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
CYTOSZKIELET. Mikrotubule. podjednostki strukturalne. 450 aminokwasów. 13 (11-16) 55kDa i 53kDa strukturalna polarność
 CYTOSZKIELET Mikrotubule podjednostki strukturalne 13 (11-16) 55kDa i 53kDa strukturalna polarność 450 aminokwasów Mikrotubule wydłuŝanie / /skracanie Mikrotubule elongacja + - in vitro in vivo - dodawanie
CYTOSZKIELET Mikrotubule podjednostki strukturalne 13 (11-16) 55kDa i 53kDa strukturalna polarność 450 aminokwasów Mikrotubule wydłuŝanie / /skracanie Mikrotubule elongacja + - in vitro in vivo - dodawanie
Komórka eukariotyczna
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Rozmnażanie i wzrost komórek sąściśle kontrolowane. Genetyczne podłoże nowotworzenia
 Rozmnażanie i wzrost komórek sąściśle kontrolowane Genetyczne podłoże nowotworzenia Rozmnażanie i wzrost komórek sąściśle kontrolowane Rozmnażanie i wzrost komórek sąściśle kontrolowane Połączenia komórek
Rozmnażanie i wzrost komórek sąściśle kontrolowane Genetyczne podłoże nowotworzenia Rozmnażanie i wzrost komórek sąściśle kontrolowane Rozmnażanie i wzrost komórek sąściśle kontrolowane Połączenia komórek
Składniki cytoszkieletu. Szkielet komórki
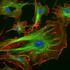 Składniki cytoszkieletu. Szkielet komórki aktynowe pośrednie aktynowe pośrednie 1 Elementy cytoszkieletu aktynowe pośrednie aktynowe filamenty aktynowe inaczej mikrofilamenty filamenty utworzone z aktyny
Składniki cytoszkieletu. Szkielet komórki aktynowe pośrednie aktynowe pośrednie 1 Elementy cytoszkieletu aktynowe pośrednie aktynowe filamenty aktynowe inaczej mikrofilamenty filamenty utworzone z aktyny
Transport makrocząsteczek
 Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Rola białek z rodziny Rho w kontroli migracji komórek pełzających
 Rola białek z rodziny Rho w kontroli migracji komórek pełzających Wanda Kłopocka * Jolanta Barańska Pracownia Przekaźników Sygnałów, Instytut Biologii Doświadczalnej im. M. Nenckiego, Warszawa * Pracownia
Rola białek z rodziny Rho w kontroli migracji komórek pełzających Wanda Kłopocka * Jolanta Barańska Pracownia Przekaźników Sygnałów, Instytut Biologii Doświadczalnej im. M. Nenckiego, Warszawa * Pracownia
MECHANIZMY WZROSTU i ROZWOJU ROŚLIN
 MECHANIZMY WZROSTU i ROZWOJU ROŚLIN Jaka jest rola kinaz MA (generalnie)? Do czego służy roślinom (lub generalnie) fosfolipaza D? Czy u roślin występują hormony peptydowe? Wymień znane Ci rodzaje receptorów
MECHANIZMY WZROSTU i ROZWOJU ROŚLIN Jaka jest rola kinaz MA (generalnie)? Do czego służy roślinom (lub generalnie) fosfolipaza D? Czy u roślin występują hormony peptydowe? Wymień znane Ci rodzaje receptorów
Fizjologia człowieka
 Fizjologia człowieka Wykład 2, część A CZYNNIKI WZROSTU CYTOKINY 2 1 Przykłady czynników wzrostu pobudzających proliferację: PDGF - cz.wzrostu z płytek krwi działa na proliferację i migrację fibroblastów,
Fizjologia człowieka Wykład 2, część A CZYNNIKI WZROSTU CYTOKINY 2 1 Przykłady czynników wzrostu pobudzających proliferację: PDGF - cz.wzrostu z płytek krwi działa na proliferację i migrację fibroblastów,
Organizacja tkanek - narządy
 Organizacja tkanek - narządy Architektura skóry tkanki kręgowców zbiór wielu typów komórek danej tkanki i spoza tej tkanki (wnikają podczas rozwoju lub stale, w trakcie Ŝycia ) neurony komórki glejowe,
Organizacja tkanek - narządy Architektura skóry tkanki kręgowców zbiór wielu typów komórek danej tkanki i spoza tej tkanki (wnikają podczas rozwoju lub stale, w trakcie Ŝycia ) neurony komórki glejowe,
Kosm os. PROBLEMY NAUKBIOLOGICZNYĆH Polskie Towarzystwo Przyrodników im. Kopernika. Tom 50, 2001 Numer 3 (252) Strony
 Kosm os Tom 50, 2001 Numer 3 (252) Strony 283-293 PROBLEMY NAUKBIOLOGICZNYĆH Polskie Towarzystwo Przyrodników im. Kopernika H a n n a Fa b c z a k Zakład. Biologii Komórki Instytut Biologii Doświadczalnej
Kosm os Tom 50, 2001 Numer 3 (252) Strony 283-293 PROBLEMY NAUKBIOLOGICZNYĆH Polskie Towarzystwo Przyrodników im. Kopernika H a n n a Fa b c z a k Zakład. Biologii Komórki Instytut Biologii Doświadczalnej
Wykład 5. Remodeling chromatyny
 Wykład 5 Remodeling chromatyny 1 Plan wykładu: 1. Przebudowa chromatyny 2. Struktura, funkcje oraz mechanizm działania kompleksów remodelujących chromatynę 3. Charakterystyka kompleksów typu SWI/SNF 4.
Wykład 5 Remodeling chromatyny 1 Plan wykładu: 1. Przebudowa chromatyny 2. Struktura, funkcje oraz mechanizm działania kompleksów remodelujących chromatynę 3. Charakterystyka kompleksów typu SWI/SNF 4.
Receptory nukleotydowe a dynamika cytoszkieletu aktynowego
 Receptory nukleotydowe a dynamika cytoszkieletu aktynowego STRESZCZENIE Receptory nukleotydowe poprzez aktywację podjednostek α heterotrimerycznych białek G q, G o, G 12 kontrolują procesy zależne od dynamiki
Receptory nukleotydowe a dynamika cytoszkieletu aktynowego STRESZCZENIE Receptory nukleotydowe poprzez aktywację podjednostek α heterotrimerycznych białek G q, G o, G 12 kontrolują procesy zależne od dynamiki
Udział białek Rho w regulacji postępu fazy G1 cyklu komórkowego* Involvement of Rho proteins in G1 phase cell cycle progression
 Postepy Hig Med Dosw (online), 2013; 67: 15-25 e-issn 1732-2693 www.phmd.pl Review Received: 2012.07.13 Accepted: 2012.11.19 Published: 2013.01.11 Udział białek Rho w regulacji postępu fazy G1 cyklu komórkowego*
Postepy Hig Med Dosw (online), 2013; 67: 15-25 e-issn 1732-2693 www.phmd.pl Review Received: 2012.07.13 Accepted: 2012.11.19 Published: 2013.01.11 Udział białek Rho w regulacji postępu fazy G1 cyklu komórkowego*
października 2013: Elementarz biologii molekularnej. Wykład nr 2 BIOINFORMATYKA rok II
 10 października 2013: Elementarz biologii molekularnej www.bioalgorithms.info Wykład nr 2 BIOINFORMATYKA rok II Komórka: strukturalna i funkcjonalne jednostka organizmu żywego Jądro komórkowe: chroniona
10 października 2013: Elementarz biologii molekularnej www.bioalgorithms.info Wykład nr 2 BIOINFORMATYKA rok II Komórka: strukturalna i funkcjonalne jednostka organizmu żywego Jądro komórkowe: chroniona
Cykl komórkowy. Rozmnażanie komórek G 1, S, G 2. (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza)
 Rozmnażanie komórek (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza) G 1, S, G 2 podział komórki (faza M) Obejmuje: podwojenie zawartości komórki (skopiowanie
Rozmnażanie komórek (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza) G 1, S, G 2 podział komórki (faza M) Obejmuje: podwojenie zawartości komórki (skopiowanie
błona zewnętrzna błona wewnętrzna (tworzy grzebienie lamelarne lub tubularne) przestrzeń międzybłonowa macierz Błona wewnętrzna: Macierz:
 Mitochondria KOMÓRKA Cz. III błona zewnętrzna błona wewnętrzna (tworzy grzebienie lamelarne lub tubularne) przestrzeń międzybłonowa macierz Błona wewnętrzna: Błona zewnętrzna: białka/lipidy 1:1 poryny
Mitochondria KOMÓRKA Cz. III błona zewnętrzna błona wewnętrzna (tworzy grzebienie lamelarne lub tubularne) przestrzeń międzybłonowa macierz Błona wewnętrzna: Błona zewnętrzna: białka/lipidy 1:1 poryny
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 5 Droga od genu do
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 5 Droga od genu do
Molekularne przełączniki
 Molekularne przełączniki - nie wszystkie procesy przebiegają w komórce równocześnie część działa cyklicznie, kontrolując zachowanie komórki i jej reakcje w zależności od różnorodnych sygnałów - takie białka,
Molekularne przełączniki - nie wszystkie procesy przebiegają w komórce równocześnie część działa cyklicznie, kontrolując zachowanie komórki i jej reakcje w zależności od różnorodnych sygnałów - takie białka,
Podział tkanki mięśniowej w zależności od budowy i lokalizacji w organizmie
 Tkanka mięśniowa Podział tkanki mięśniowej w zależności od budowy i lokalizacji w organizmie Tkanka mięśniowa poprzecznie prążkowana poprzecznie prążkowana serca gładka Tkanka mięśniowa Podstawową własnością
Tkanka mięśniowa Podział tkanki mięśniowej w zależności od budowy i lokalizacji w organizmie Tkanka mięśniowa poprzecznie prążkowana poprzecznie prążkowana serca gładka Tkanka mięśniowa Podstawową własnością
Wykład 14 Biosynteza białek
 BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
starszych na półkuli zachodniej. Typową cechą choroby jest heterogenny przebieg
 STRESZCZENIE Przewlekła białaczka limfocytowa (PBL) jest najczęstszą białaczką ludzi starszych na półkuli zachodniej. Typową cechą choroby jest heterogenny przebieg kliniczny, zróżnicowane rokowanie. Etiologia
STRESZCZENIE Przewlekła białaczka limfocytowa (PBL) jest najczęstszą białaczką ludzi starszych na półkuli zachodniej. Typową cechą choroby jest heterogenny przebieg kliniczny, zróżnicowane rokowanie. Etiologia
Interfaza to niemal 90% cyklu komórkowego. Dzieli się na 3 fazy: G1, S i G2.
 W wyniku podziału komórki powstaje komórka potomna, która ma o połowę mniej DNA od komórki macierzystej i jest o połowę mniejsza. Aby komórka potomna była zdolna do kolejnego podziału musi osiągnąć rozmiary
W wyniku podziału komórki powstaje komórka potomna, która ma o połowę mniej DNA od komórki macierzystej i jest o połowę mniejsza. Aby komórka potomna była zdolna do kolejnego podziału musi osiągnąć rozmiary
Terapia celowana. Część I. Mechanizmy przesyłania sygnałów przy udziale receptorów o aktywności kinazy tyrozynowej
 Współczesna Onkologia (2007) vol. 11; 7 (331 336) Prawidłowe funkcjonowanie komórki jest uzależnione od ścisłej kontroli przekazywania informacji. W proces przenoszenia sygnałów zaangażowane są substancje
Współczesna Onkologia (2007) vol. 11; 7 (331 336) Prawidłowe funkcjonowanie komórki jest uzależnione od ścisłej kontroli przekazywania informacji. W proces przenoszenia sygnałów zaangażowane są substancje
Transport przez błony
 Transport przez błony Transport bierny Nie wymaga nakładu energii Transport aktywny Wymaga nakładu energii Dyfuzja prosta Dyfuzja ułatwiona Przenośniki Kanały jonowe Transport przez pory w błonie jądrowej
Transport przez błony Transport bierny Nie wymaga nakładu energii Transport aktywny Wymaga nakładu energii Dyfuzja prosta Dyfuzja ułatwiona Przenośniki Kanały jonowe Transport przez pory w błonie jądrowej
Profil metaboliczny róŝnych organów ciała
 Profil metaboliczny róŝnych organów ciała Uwaga: tkanka tłuszczowa (adipose tissue) NIE wykorzystuje glicerolu do biosyntezy triacylogliceroli Endo-, para-, i autokrynna droga przekazu informacji biologicznej.
Profil metaboliczny róŝnych organów ciała Uwaga: tkanka tłuszczowa (adipose tissue) NIE wykorzystuje glicerolu do biosyntezy triacylogliceroli Endo-, para-, i autokrynna droga przekazu informacji biologicznej.
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu w porównaniu z analizą trankryptomu:
Mechanochemiczny przełącznik między wzrostem i różnicowaniem komórek
 Mechanochemiczny przełącznik między wzrostem i różnicowaniem komórek Model tworzenia mikrokapilar na podłożu fibrynogenowym eksponencjalny wzrost tempa proliferacji i syntezy DNA wraz ze wzrostem stężenia
Mechanochemiczny przełącznik między wzrostem i różnicowaniem komórek Model tworzenia mikrokapilar na podłożu fibrynogenowym eksponencjalny wzrost tempa proliferacji i syntezy DNA wraz ze wzrostem stężenia
Dr. habil. Anna Salek International Bio-Consulting 1 Germany
 1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
Streszczenie. Summary. Anna Klimaszewska 1 *, Anna Stenzel 1 *, Jakub Marcin Nowak 1, Alina Grzanka 1,2
 Postepy Hig Med Dosw (online), 2011; 65: 704-713 e-issn 1732-2693 www.phmd.pl Review Received: 2011.06.14 Accepted: 2011.10.21 Published: 2011.11.17 Białka Rho kluczowe regulatory cytoszkieletu w przebiegu
Postepy Hig Med Dosw (online), 2011; 65: 704-713 e-issn 1732-2693 www.phmd.pl Review Received: 2011.06.14 Accepted: 2011.10.21 Published: 2011.11.17 Białka Rho kluczowe regulatory cytoszkieletu w przebiegu
UDZIAŁ KOMPLEKSU BIAŁEK Arp2/3 W NUKLEACJI AKTYNY W KOMÓRCE. MECHANIZM RUCHU BAKTERII LISTERIA MONOCYTOGENES
 Kosm os Tom 50, 2001 Numer 3 (252) Strony 213-221 PROBLEMY NAUK BIOLOGICZNYCH Polskie Towarzystwo Przyrodników im. Kopernika K a t a r z y n a Kw ia t k o w s k a Zakład Biologii Komórki Instytut Biologii
Kosm os Tom 50, 2001 Numer 3 (252) Strony 213-221 PROBLEMY NAUK BIOLOGICZNYCH Polskie Towarzystwo Przyrodników im. Kopernika K a t a r z y n a Kw ia t k o w s k a Zakład Biologii Komórki Instytut Biologii
AUTOREFERAT ROZPRAWY DOKTORSKIEJ. The role of Sdf-1 in the migration and differentiation of stem cells during skeletal muscle regeneration
 mgr Kamil Kowalski Zakład Cytologii Wydział Biologii UW AUTOREFERAT ROZPRAWY DOKTORSKIEJ The role of Sdf-1 in the migration and differentiation of stem cells during skeletal muscle regeneration Wpływ chemokiny
mgr Kamil Kowalski Zakład Cytologii Wydział Biologii UW AUTOREFERAT ROZPRAWY DOKTORSKIEJ The role of Sdf-1 in the migration and differentiation of stem cells during skeletal muscle regeneration Wpływ chemokiny
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Transport makrocząsteczek (białek)
 Transport makrocząsteczek (białek) Transport makrocząsteczek sortowanie białek - sekwencje sygnałowe lata 70-te XX w. - Günter Blobel - hipoteza sygnałowa; 1999r - nagroda Nobla Sekwencja sygnałowa: A
Transport makrocząsteczek (białek) Transport makrocząsteczek sortowanie białek - sekwencje sygnałowe lata 70-te XX w. - Günter Blobel - hipoteza sygnałowa; 1999r - nagroda Nobla Sekwencja sygnałowa: A
INICJACJA ELONGACJA TERMINACJA
 INICJACJA ELONGACJA TERMINACJA 2007 by National Academy of Sciences Kornberg R D PNAS 2007;104:12955-12961 Struktura chromatyny pozwala na różny sposób odczytania informacji zawartej w DNA. Możliwe staje
INICJACJA ELONGACJA TERMINACJA 2007 by National Academy of Sciences Kornberg R D PNAS 2007;104:12955-12961 Struktura chromatyny pozwala na różny sposób odczytania informacji zawartej w DNA. Możliwe staje
Cytoplazma. podstawowa (cytozol) Cytoplazma podstawowa (macierz cytoplazmatyczna)
 Cytoplazma złoŝony koloid wodny cząsteczek i makrocząsteczek Cytoplazma cytoplazma podstawowa (cytozol) organelle Cytoplazma podstawowa (macierz cytoplazmatyczna) ok. 55% objętości komórki złoŝony koloid
Cytoplazma złoŝony koloid wodny cząsteczek i makrocząsteczek Cytoplazma cytoplazma podstawowa (cytozol) organelle Cytoplazma podstawowa (macierz cytoplazmatyczna) ok. 55% objętości komórki złoŝony koloid
TRANSKRYPCJA - I etap ekspresji genów
 Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Zawartość. Wstęp 1. Historia wirusologii. 2. Klasyfikacja wirusów
 Zawartość 139585 Wstęp 1. Historia wirusologii 2. Klasyfikacja wirusów 3. Struktura cząstek wirusowych 3.1. Metody określania struktury cząstek wirusowych 3.2. Budowa cząstek wirusowych o strukturze helikalnej
Zawartość 139585 Wstęp 1. Historia wirusologii 2. Klasyfikacja wirusów 3. Struktura cząstek wirusowych 3.1. Metody określania struktury cząstek wirusowych 3.2. Budowa cząstek wirusowych o strukturze helikalnej
Hormony Gruczoły dokrewne
 Hormony Gruczoły dokrewne Dr n. biol. Urszula Wasik Zakład Biologii Medycznej HORMON Przekazuje informacje między poszczególnymi organami regulują wzrost, rozwój organizmu efekt biologiczny - niewielkie
Hormony Gruczoły dokrewne Dr n. biol. Urszula Wasik Zakład Biologii Medycznej HORMON Przekazuje informacje między poszczególnymi organami regulują wzrost, rozwój organizmu efekt biologiczny - niewielkie
Dr hab. Janusz Matuszyk. Ocena rozprawy doktorskiej. Pani mgr Hanny Baurskiej
 Dr hab. Janusz Matuszyk INSTYTUT IMMUNOLOGII I TERAPII DOŚWIADCZALNEJ im. Ludwika Hirszfelda P OLSKIEJ A K A D E M I I N AUK Centrum Doskonałości: IMMUNE ul. Rudolfa Weigla 12, 53-114 Wrocław tel. (+48-71)
Dr hab. Janusz Matuszyk INSTYTUT IMMUNOLOGII I TERAPII DOŚWIADCZALNEJ im. Ludwika Hirszfelda P OLSKIEJ A K A D E M I I N AUK Centrum Doskonałości: IMMUNE ul. Rudolfa Weigla 12, 53-114 Wrocław tel. (+48-71)
Spis treści. 1. Jak powstają odmienne fenotypy komórek Budowa cząsteczkowa i funkcjonalne składniki błony komórkowej 29 SPIS TREŚCI / 7
 SPIS TREŚCI / 7 Spis treści 1. Jak powstają odmienne fenotypy komórek 13 Ewolucja dyscyplin naukowych 13 Fenotypy komórek ssaków 14 Organizacja komórek w tkankach 15 Zmienność fenotypów komórkowych w czterech
SPIS TREŚCI / 7 Spis treści 1. Jak powstają odmienne fenotypy komórek 13 Ewolucja dyscyplin naukowych 13 Fenotypy komórek ssaków 14 Organizacja komórek w tkankach 15 Zmienność fenotypów komórkowych w czterech
cytoplazma + jądro komórkowe = protoplazma Jądro komórkowe
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
TATA box. Enhancery. CGCG ekson intron ekson intron ekson CZĘŚĆ KODUJĄCA GENU TERMINATOR. Elementy regulatorowe
 Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych
 Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych Zalety w porównaniu z analizą trankryptomu: analiza transkryptomu komórki identyfikacja mrna nie musi jeszcze oznaczać
Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych Zalety w porównaniu z analizą trankryptomu: analiza transkryptomu komórki identyfikacja mrna nie musi jeszcze oznaczać
PODSTAWY IMMUNOLOGII Komórki i cząsteczki biorące udział w odporności nabytej (cz.i): wprowadzenie (komórki, receptory, rozwój odporności nabytej)
 PODSTAWY IMMUNOLOGII Komórki i cząsteczki biorące udział w odporności nabytej (cz.i): wprowadzenie (komórki, receptory, rozwój odporności nabytej) Nadzieja Drela ndrela@biol.uw.edu.pl Konspekt do wykładu
PODSTAWY IMMUNOLOGII Komórki i cząsteczki biorące udział w odporności nabytej (cz.i): wprowadzenie (komórki, receptory, rozwój odporności nabytej) Nadzieja Drela ndrela@biol.uw.edu.pl Konspekt do wykładu
z Hsp90 w sposób bezpośredni. Ponadto pokazano, iż pomimo podobieństwa sekwencji CacyBP/SIP i Sgt1, białka te nie współzawodniczą ze sobą o wiązanie
 Mgr Agnieszka Góral Dziedzina: nauki biologiczne Dyscyplina: biologia Otwarcie: 28.06.2013 r. Temat: Białko CacyBP/SIP: oddziaływanie z białkiem szoku cieplnego Hsp90 oraz rola w odpowiedzi komórek na
Mgr Agnieszka Góral Dziedzina: nauki biologiczne Dyscyplina: biologia Otwarcie: 28.06.2013 r. Temat: Białko CacyBP/SIP: oddziaływanie z białkiem szoku cieplnego Hsp90 oraz rola w odpowiedzi komórek na
Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej
 Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej PRAKTIKUM Z BIOLOGII KOMÓRKI () ćwiczenie prowadzone we współpracy z Pracownią Biofizyki Komórki Badanie dynamiki białek
Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej PRAKTIKUM Z BIOLOGII KOMÓRKI () ćwiczenie prowadzone we współpracy z Pracownią Biofizyki Komórki Badanie dynamiki białek
The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna
 Streszczenie rozprawy doktorskiej pt. The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna mgr Tomasz Turowski, promotor prof. dr hab.
Streszczenie rozprawy doktorskiej pt. The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna mgr Tomasz Turowski, promotor prof. dr hab.
Recenzja rozprawy doktorskiej mgr inż. Artura Zajkowicza
 dr hab. Beata Schlichtholz Gdańsk, 20 października 2015 r. Katedra i Zakład Biochemii Gdański Uniwersytet Medyczny ul. Dębinki 1 80-211 Gdańsk Recenzja rozprawy doktorskiej mgr inż. Artura Zajkowicza pt.
dr hab. Beata Schlichtholz Gdańsk, 20 października 2015 r. Katedra i Zakład Biochemii Gdański Uniwersytet Medyczny ul. Dębinki 1 80-211 Gdańsk Recenzja rozprawy doktorskiej mgr inż. Artura Zajkowicza pt.
Zagadnienia seminaryjne w semestrze letnim I Błony biologiczne
 Zagadnienia seminaryjne w semestrze letnim 2019 I Błony biologiczne 1. Budowa i składniki błon biologicznych - fosfolipidy - steroidy - białka - glikoproteiny i glikolipidy 2. Funkcje błony komórkowej
Zagadnienia seminaryjne w semestrze letnim 2019 I Błony biologiczne 1. Budowa i składniki błon biologicznych - fosfolipidy - steroidy - białka - glikoproteiny i glikolipidy 2. Funkcje błony komórkowej
Nowoczesne systemy ekspresji genów
 Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Wykład 13. Regulacja cyklu komórkowego w odpowiedzi na uszkodzenia DNA. Mechanizmy powstawania nowotworów
 Wykład 13 Regulacja cyklu komórkowego w odpowiedzi na uszkodzenia DNA Mechanizmy powstawania nowotworów Uszkodzenie DNA Wykrycie uszkodzenia Naprawa DNA Zatrzymanie cyklu kom. Apoptoza Źródła uszkodzeń
Wykład 13 Regulacja cyklu komórkowego w odpowiedzi na uszkodzenia DNA Mechanizmy powstawania nowotworów Uszkodzenie DNA Wykrycie uszkodzenia Naprawa DNA Zatrzymanie cyklu kom. Apoptoza Źródła uszkodzeń
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem informacji odebranej przez komórkę. Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Receptor cząsteczka chemiczna ( peptyd
Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem informacji odebranej przez komórkę. Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Receptor cząsteczka chemiczna ( peptyd
WITAMY NA KURSIE HISTOLOGII
 KOMÓRKA WITAMY NA KURSIE HISTOLOGII www.histologia.cm-uj.krakow.pl Wielkość komórek ZróŜnicowanie komórek Jednostki: 1 µm = 10-3 mm, 1 nm = 10-3 µm kształt najmniejsze komórki (komórki przytarczyc, niektóre
KOMÓRKA WITAMY NA KURSIE HISTOLOGII www.histologia.cm-uj.krakow.pl Wielkość komórek ZróŜnicowanie komórek Jednostki: 1 µm = 10-3 mm, 1 nm = 10-3 µm kształt najmniejsze komórki (komórki przytarczyc, niektóre
Sieć interakcji międzykomórkowych w obrębie tkanki łącznej
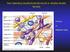 Sieć interakcji międzykomórkowych w obrębie tkanki łącznej Adhezja vs. stabilność niszy 1 Funkcja Niszy czyli mikrośrodowiska komórek w transformacji nowotworowej Mediatory wymiany informacji między komórką
Sieć interakcji międzykomórkowych w obrębie tkanki łącznej Adhezja vs. stabilność niszy 1 Funkcja Niszy czyli mikrośrodowiska komórek w transformacji nowotworowej Mediatory wymiany informacji między komórką
1. Lista publikacji wchodzących w skład rozprawy
 1. Lista publikacji wchodzących w skład rozprawy a) Toma A, Widłak W, Vydra N (2012) Rola czynnika transkrypcyjnego HSF1 w procesie nowotworzenia. Postępy Biologii Komórki 39(2):269 288 b) Vydra N, Toma
1. Lista publikacji wchodzących w skład rozprawy a) Toma A, Widłak W, Vydra N (2012) Rola czynnika transkrypcyjnego HSF1 w procesie nowotworzenia. Postępy Biologii Komórki 39(2):269 288 b) Vydra N, Toma
Ocena rozprawy doktorskiej Pana mgr Kamila Jastrzębskiego pt. "Role of the Rho GTPases in trafficking and signaling of platelet-derived growth factor"
 Dr hab. Jarosław Czyż Zakład Biologii Komórki Wydział Biochemii, Biofizyki i Biotechnologii Uniwersytet Jagielloński ul. Gronostajowa 7 30-387 Kraków e-mail: jarek.czyz@uj.edu.pl Kraków, 2 grudnia 2015
Dr hab. Jarosław Czyż Zakład Biologii Komórki Wydział Biochemii, Biofizyki i Biotechnologii Uniwersytet Jagielloński ul. Gronostajowa 7 30-387 Kraków e-mail: jarek.czyz@uj.edu.pl Kraków, 2 grudnia 2015
Ruch ameboidalny komórek nowotworowych Ameboid movement of cancer cells
 Postepy Hig Med Dosw (online), 2018; 72: 21-34 e-issn 1732-2693 www.phmd.pl Review Received: 05.02.2016 Accepted: 10.08.2017 Published: 25.01.2018 Ruch ameboidalny komórek nowotworowych Ameboid movement
Postepy Hig Med Dosw (online), 2018; 72: 21-34 e-issn 1732-2693 www.phmd.pl Review Received: 05.02.2016 Accepted: 10.08.2017 Published: 25.01.2018 Ruch ameboidalny komórek nowotworowych Ameboid movement
Ruch zwiększa recykling komórkowy Natura i wychowanie
 Wiadomości naukowe o chorobie Huntingtona. Prostym językiem. Napisane przez naukowców. Dla globalnej społeczności HD. Ruch zwiększa recykling komórkowy Ćwiczenia potęgują recykling komórkowy u myszy. Czy
Wiadomości naukowe o chorobie Huntingtona. Prostym językiem. Napisane przez naukowców. Dla globalnej społeczności HD. Ruch zwiększa recykling komórkowy Ćwiczenia potęgują recykling komórkowy u myszy. Czy
Mięśnie. dr Magdalena Markowska
 Mięśnie dr Magdalena Markowska Zjawisko ruchu 1) Jako możliwość przemieszczania przestrzennego mięśnie poprzecznie prążkowane 2) Pompa serce 3) Jako podstawa do utrzymywania czynności życiowych mięśnie
Mięśnie dr Magdalena Markowska Zjawisko ruchu 1) Jako możliwość przemieszczania przestrzennego mięśnie poprzecznie prążkowane 2) Pompa serce 3) Jako podstawa do utrzymywania czynności życiowych mięśnie
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Ocena ekspresji genu ABCG2 i białka oporności raka piersi (BCRP) jako potencjalnych czynników prognostycznych w raku jelita grubego
 Aleksandra Sałagacka Ocena ekspresji genu ABCG2 i białka oporności raka piersi (BCRP) jako potencjalnych czynników prognostycznych w raku jelita grubego Pracownia Biologii Molekularnej i Farmakogenomiki
Aleksandra Sałagacka Ocena ekspresji genu ABCG2 i białka oporności raka piersi (BCRP) jako potencjalnych czynników prognostycznych w raku jelita grubego Pracownia Biologii Molekularnej i Farmakogenomiki
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
The Mos/mitogen-activated protein kinase (MAPK) pathway regulates the size and degradation of the first polar body in maturing mouse oocytes
 The Mos/mitogen-activated protein kinase (MAPK) pathway regulates the size and degradation of the first polar body in maturing mouse oocytes TAESAENG CHOI*, KENJI FUKASAWA*, RENPING ZHOUt, LINO TESSAROLLO*,
The Mos/mitogen-activated protein kinase (MAPK) pathway regulates the size and degradation of the first polar body in maturing mouse oocytes TAESAENG CHOI*, KENJI FUKASAWA*, RENPING ZHOUt, LINO TESSAROLLO*,
Transport pęcherzykowy
 Transport pęcherzykowy sortowanie przenoszonego materiału zachowanie asymetrii zachowanie odrębności organelli precyzyjne oznakowanie Transport pęcherzykowy etapy transportu Transport pęcherzykowy przemieszczanie
Transport pęcherzykowy sortowanie przenoszonego materiału zachowanie asymetrii zachowanie odrębności organelli precyzyjne oznakowanie Transport pęcherzykowy etapy transportu Transport pęcherzykowy przemieszczanie
CHOROBY NOWOTWOROWE. Twór składający się z patologicznych komórek
 CHOROBY NOWOTWOROWE Twór składający się z patologicznych komórek Powstały w wyniku wielostopniowej przemiany zwanej onkogenezą lub karcinogenezą Morfologicznie ma strukturę zbliżoną do tkanki prawidłowej,
CHOROBY NOWOTWOROWE Twór składający się z patologicznych komórek Powstały w wyniku wielostopniowej przemiany zwanej onkogenezą lub karcinogenezą Morfologicznie ma strukturę zbliżoną do tkanki prawidłowej,
CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A. imię i nazwisko :. klasa :.. ilość punktów :.
 CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A imię i nazwisko :. klasa :.. ilość punktów :. Zadanie 1 Przeanalizuj schemat i wykonaj polecenia. a. Wymień cztery struktury występujące zarówno w komórce roślinnej,
CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A imię i nazwisko :. klasa :.. ilość punktów :. Zadanie 1 Przeanalizuj schemat i wykonaj polecenia. a. Wymień cztery struktury występujące zarówno w komórce roślinnej,
Część V: Przekazywanie sygnałów. DO WYKŁADÓW Z PODSTAW BIOFIZYKI IIIr. Biotechnologii prof. dr hab. inż. Jan Mazerski
 MATERIAŁY PMCNICZE D WYKŁADÓW Z PDSTAW BIFIZYKI IIIr. Biotechnologii prof. dr hab. inż. Jan Mazerski PRZEKAZYWANIE SYGNAŁÓW Cechą charakterystyczną układów żywych jest zdolność do zachowywania wewnętrznej
MATERIAŁY PMCNICZE D WYKŁADÓW Z PDSTAW BIFIZYKI IIIr. Biotechnologii prof. dr hab. inż. Jan Mazerski PRZEKAZYWANIE SYGNAŁÓW Cechą charakterystyczną układów żywych jest zdolność do zachowywania wewnętrznej
Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych. źródło: (3)
 Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych źródło: (3) Interakcje białko-białko Ze względu na zadanie: strukturalne lub funkcjonalne. Ze względu na właściwości fizyczne: stałe lub
Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych źródło: (3) Interakcje białko-białko Ze względu na zadanie: strukturalne lub funkcjonalne. Ze względu na właściwości fizyczne: stałe lub
Składniki diety a stabilność struktury DNA
 Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Numer 4 (253) Strony PROBLEMY NAUK BIOLOGICZNYCH Polskie Towarzystwo Przyrodników im. Kopernika
 Tom 50, 2001 Kosm os Numer 4 (253) Strony 359-374 PROBLEMY NAUK BIOLOGICZNYCH Polskie Towarzystwo Przyrodników im. Kopernika Re n a t a Dą b r o w s k a i R o b e r t m a k u c h Zakład. Biochemii Mięśni
Tom 50, 2001 Kosm os Numer 4 (253) Strony 359-374 PROBLEMY NAUK BIOLOGICZNYCH Polskie Towarzystwo Przyrodników im. Kopernika Re n a t a Dą b r o w s k a i R o b e r t m a k u c h Zakład. Biochemii Mięśni
Onkogeneza i zjawisko przejścia nabłonkowomezenchymalnego. Gabriel Wcisło Klinika Onkologii Wojskowego Instytutu Medycznego, CSK MON, Warszawa
 Onkogeneza i zjawisko przejścia nabłonkowomezenchymalnego raka jajnika Gabriel Wcisło Klinika Onkologii Wojskowego Instytutu Medycznego, CSK MON, Warszawa Sześć diabelskich mocy a komórka rakowa (Gibbs
Onkogeneza i zjawisko przejścia nabłonkowomezenchymalnego raka jajnika Gabriel Wcisło Klinika Onkologii Wojskowego Instytutu Medycznego, CSK MON, Warszawa Sześć diabelskich mocy a komórka rakowa (Gibbs
Udział jonów wapnia w regulacji oddziaływań aktyny z miozyną
 Udział jonów wapnia w regulacji oddziaływań aktyny z miozyną STRESZCZENIE Skurcz komórek mięśniowych oraz różnorodne formy ruchliwości komórek niemięśniowych są uzależnione od cyklicznych oddziaływań pomiędzy
Udział jonów wapnia w regulacji oddziaływań aktyny z miozyną STRESZCZENIE Skurcz komórek mięśniowych oraz różnorodne formy ruchliwości komórek niemięśniowych są uzależnione od cyklicznych oddziaływań pomiędzy
Maria Szumiło, Iwonna Rahden-Staroń. Katedra i Zakład Biochemii Akademii Medycznej w Warszawie
 Postepy Hig Med Dosw. (online), 2006; 60: 421-430 e-issn 1732-2693 Received: 2006.05.04 Accepted: 2006.07.12 Published: 2006.08.09 Słowa kluczowe: Key words: Fosfolipaza D w komórkach ssaków budowa, właściwości,
Postepy Hig Med Dosw. (online), 2006; 60: 421-430 e-issn 1732-2693 Received: 2006.05.04 Accepted: 2006.07.12 Published: 2006.08.09 Słowa kluczowe: Key words: Fosfolipaza D w komórkach ssaków budowa, właściwości,
Cytoplazma. Cytoplazma. cytoplazma + jądro komórkowe = protoplazma. cytoplazma organelle podstawowa (cytozol) Kompleksy białkowe (+RNA)
 Cytoplazma cytoplazma + jądro komórkowe = protoplazma Cytoplazma cytoplazma organelle podstawowa (cytozol) złoŝony koloid wodny cząsteczek i makrocząsteczek Kompleksy białkowe (+RNA) Cytoplazma podstawowa
Cytoplazma cytoplazma + jądro komórkowe = protoplazma Cytoplazma cytoplazma organelle podstawowa (cytozol) złoŝony koloid wodny cząsteczek i makrocząsteczek Kompleksy białkowe (+RNA) Cytoplazma podstawowa
UKŁAD DOKREWNY cz. 2. Wysepki trzustkowe (Langerhansa): grupy komórek dokrewnych produkujących hormony białkowe
 Wysepki trzustkowe (Langerhansa): grupy komórek dokrewnych produkujących hormony białkowe UKŁAD DOKREWNY cz. 2 Elementy składowe: komórki dokrewne kapilary okienkowe włókna nerwowe Typy komórek dokrewnych
Wysepki trzustkowe (Langerhansa): grupy komórek dokrewnych produkujących hormony białkowe UKŁAD DOKREWNY cz. 2 Elementy składowe: komórki dokrewne kapilary okienkowe włókna nerwowe Typy komórek dokrewnych
Gdański Uniwersytet Medyczny Wydział Lekarski. Udział mikrorna w procesie starzenia się ludzkich limfocytów T. Joanna Frąckowiak
 Gdański Uniwersytet Medyczny Wydział Lekarski Udział mikrorna w procesie starzenia się ludzkich limfocytów T Joanna Frąckowiak Rozprawa doktorska Praca wykonana w Katedrze i Zakładzie Fizjopatologii Gdańskiego
Gdański Uniwersytet Medyczny Wydział Lekarski Udział mikrorna w procesie starzenia się ludzkich limfocytów T Joanna Frąckowiak Rozprawa doktorska Praca wykonana w Katedrze i Zakładzie Fizjopatologii Gdańskiego
SESJA 6 BŁONY KOMÓRKOWE: SYGNALIZACJA I BIOENERGETYKA WARSZTATY
 SESJA 6 BŁONY KOMÓRKOWE: SYGNALIZACJA I BIOENERGETYKA WARSZTATY 146 SESJA 6 WARSZTATY R06-01 ROLA BIAŁEK MRP W DETOKSYKACJI KSENOBIOTYKÓW Błażej Rychlik Katedra Biofizyki Molekularnej, Uniwersytet Łódzki,
SESJA 6 BŁONY KOMÓRKOWE: SYGNALIZACJA I BIOENERGETYKA WARSZTATY 146 SESJA 6 WARSZTATY R06-01 ROLA BIAŁEK MRP W DETOKSYKACJI KSENOBIOTYKÓW Błażej Rychlik Katedra Biofizyki Molekularnej, Uniwersytet Łódzki,
(MIKROSKOP ELEKTRONOWY, ORGANELLE KOMÓRKOWE).
 ĆWICZENIE 2. Temat: ULTRASTRUKTURA KOMÓRKI (1). (MIKROSKOP ELEKTRONOWY, ORGANELLE KOMÓRKOWE). 1. Podstawy technik mikroskopowo-elektronowych (Schemat N/2/1) 2. Budowa i działanie mikroskopu elektronowego
ĆWICZENIE 2. Temat: ULTRASTRUKTURA KOMÓRKI (1). (MIKROSKOP ELEKTRONOWY, ORGANELLE KOMÓRKOWE). 1. Podstawy technik mikroskopowo-elektronowych (Schemat N/2/1) 2. Budowa i działanie mikroskopu elektronowego
OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011
 OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011 DLACZEGO DOROSŁY CZŁOWIEK (O STAŁEJ MASIE BIAŁKOWEJ CIAŁA) MUSI SPOŻYWAĆ BIAŁKO? NIEUSTAJĄCA WYMIANA BIAŁEK
OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011 DLACZEGO DOROSŁY CZŁOWIEK (O STAŁEJ MASIE BIAŁKOWEJ CIAŁA) MUSI SPOŻYWAĆ BIAŁKO? NIEUSTAJĄCA WYMIANA BIAŁEK
Interakcje między abiotycznymi i biotycznymi czynnikami stresowymi: od teorii do praktyki Elżbieta Kuźniak Joanna Chojak
 Katedra Fizjologii i Biochemii Roślin Uniwersytetu Łódzkiego Interakcje między abiotycznymi i biotycznymi czynnikami stresowymi: od teorii do praktyki Elżbieta Kuźniak Joanna Chojak Plan wykładu Przykłady
Katedra Fizjologii i Biochemii Roślin Uniwersytetu Łódzkiego Interakcje między abiotycznymi i biotycznymi czynnikami stresowymi: od teorii do praktyki Elżbieta Kuźniak Joanna Chojak Plan wykładu Przykłady
Przemiana materii i energii - Biologia.net.pl
 Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Transport pęcherzykowy i plazmodesmy
 Transport pęcherzykowy i plazmodesmy 1 Rola plazmodesmów (desmosomy, złącza szczelinowe) Zambryski & Crawford 2000 PD kanały ciągłości cytoplazmatyczno-jądrowej w ścianie komórkowej zapewniające komunikację
Transport pęcherzykowy i plazmodesmy 1 Rola plazmodesmów (desmosomy, złącza szczelinowe) Zambryski & Crawford 2000 PD kanały ciągłości cytoplazmatyczno-jądrowej w ścianie komórkowej zapewniające komunikację
Translacja i proteom komórki
 Translacja i proteom komórki 1. Kod genetyczny 2. Budowa rybosomów 3. Inicjacja translacji 4. Elongacja translacji 5. Terminacja translacji 6. Potranslacyjne zmiany polipeptydów 7. Translacja a retikulum
Translacja i proteom komórki 1. Kod genetyczny 2. Budowa rybosomów 3. Inicjacja translacji 4. Elongacja translacji 5. Terminacja translacji 6. Potranslacyjne zmiany polipeptydów 7. Translacja a retikulum
FOCUS Plus - Silniejsza ryba radzi sobie lepiej w trudnych warunkach
 FOCUS Plus - Silniejsza ryba radzi sobie lepiej w trudnych warunkach FOCUS Plus to dodatek dostępny dla standardowych pasz tuczowych BioMaru, dostosowany specjalnie do potrzeb ryb narażonych na trudne
FOCUS Plus - Silniejsza ryba radzi sobie lepiej w trudnych warunkach FOCUS Plus to dodatek dostępny dla standardowych pasz tuczowych BioMaru, dostosowany specjalnie do potrzeb ryb narażonych na trudne
Wprowadzenie do biologii molekularnej.
 Wprowadzenie do biologii molekularnej. Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego. Biologia molekularna zajmuje się badaniem biologicznych
Wprowadzenie do biologii molekularnej. Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego. Biologia molekularna zajmuje się badaniem biologicznych
Nowe terapie choroby Huntingtona. Grzegorz Witkowski Katowice 2014
 Nowe terapie choroby Huntingtona Grzegorz Witkowski Katowice 2014 Terapie modyfikujące przebieg choroby Zahamowanie produkcji nieprawidłowej huntingtyny Leki oparte o palce cynkowe Małe interferujące RNA
Nowe terapie choroby Huntingtona Grzegorz Witkowski Katowice 2014 Terapie modyfikujące przebieg choroby Zahamowanie produkcji nieprawidłowej huntingtyny Leki oparte o palce cynkowe Małe interferujące RNA
SESJA 10 ODPOWIEDŹ ORGANIZMÓW NA CZYNNIKI BIOTYCZNE I ABIOTYCZNE WYKŁADY
 SESJA 10 ODPOWIEDŹ ORGANIZMÓW NA CZYNNIKI BIOTYCZNE I ABIOTYCZNE WYKŁADY 238 SESJA 10 WYKŁADY W10-01 REAKTYWNE FORMY TLENU JAKO ELEMENT REAKCJI KOMÓREK NA STRES Grzegorz Bartosz Katedra Biofizyki Molekularnej
SESJA 10 ODPOWIEDŹ ORGANIZMÓW NA CZYNNIKI BIOTYCZNE I ABIOTYCZNE WYKŁADY 238 SESJA 10 WYKŁADY W10-01 REAKTYWNE FORMY TLENU JAKO ELEMENT REAKCJI KOMÓREK NA STRES Grzegorz Bartosz Katedra Biofizyki Molekularnej
Geny, a funkcjonowanie organizmu
 Geny, a funkcjonowanie organizmu Wprowadzenie do genów letalnych Geny kodują Białka Kwasy rybonukleinowe 1 Geny Występują zwykle w 2 kopiach Kopia pochodząca od matki Kopia pochodząca od ojca Ekspresji
Geny, a funkcjonowanie organizmu Wprowadzenie do genów letalnych Geny kodują Białka Kwasy rybonukleinowe 1 Geny Występują zwykle w 2 kopiach Kopia pochodząca od matki Kopia pochodząca od ojca Ekspresji
IMMUNOHISTOCHEMICZNA OCENA MERKERÓW PROLIFERACJI KOMÓRKOWEJ W RAKU JELITA GRUBEGO
 IMMUNOHISTOCHEMICZNA OCENA MERKERÓW PROLIFERACJI KOMÓRKOWEJ W RAKU JELITA GRUBEGO EWA STĘPIEŃ ZAKŁAD PATOMORFOLOGII OGÓLNEJ AKADEMII MEDYCZNEJ W BIAŁYMSTOKU KIEROWNIK I OPIEKUN PRACY: Dr KATARZYNA GUZIŃSKA-USTYMOWICZ
IMMUNOHISTOCHEMICZNA OCENA MERKERÓW PROLIFERACJI KOMÓRKOWEJ W RAKU JELITA GRUBEGO EWA STĘPIEŃ ZAKŁAD PATOMORFOLOGII OGÓLNEJ AKADEMII MEDYCZNEJ W BIAŁYMSTOKU KIEROWNIK I OPIEKUN PRACY: Dr KATARZYNA GUZIŃSKA-USTYMOWICZ
MIGRACJA REGULACJA ZJAWISKA PRZEZ WYBRANE SZLAKI SYGNAŁOWE
 Tom 67 2018 Numer 1 (318) Strony 207 218 Wanda Kłopocka 1, Jarosław Korczyński 2 1 Wydział Biologii i Nauk o Środowisku Uniwersytet Kardynała Stefana Wyszyńskiego Wóycickiego 1/3, 01-938 Warszawa 2 Centrum
Tom 67 2018 Numer 1 (318) Strony 207 218 Wanda Kłopocka 1, Jarosław Korczyński 2 1 Wydział Biologii i Nauk o Środowisku Uniwersytet Kardynała Stefana Wyszyńskiego Wóycickiego 1/3, 01-938 Warszawa 2 Centrum
Ruch i mięśnie. dr Magdalena Markowska
 Ruch i mięśnie dr Magdalena Markowska Zjawisko ruchu Przykład współpracy wielu układów Szkielet Szkielet wewnętrzny: szkielet znajdujący się wewnątrz ciała, otoczony innymi tkankami. U kręgowców składa
Ruch i mięśnie dr Magdalena Markowska Zjawisko ruchu Przykład współpracy wielu układów Szkielet Szkielet wewnętrzny: szkielet znajdujący się wewnątrz ciała, otoczony innymi tkankami. U kręgowców składa
