O 2 HCO 3. Wit K. Karboksylacja grup ε-aminowych lizyny w białku zwiększa jego podatność na proteolizę.
|
|
|
- Małgorzata Zalewska
- 8 lat temu
- Przeglądów:
Transkrypt
1 16. EMIZE MDYFIKAJE RESZT AMIKWASWY Iwona śak Posttranslacyjnym modyfikacjom łańcuchów bocznych aminokwasów ulega 15, spośród 20 aminokwasów białkowych, z wyjątkiem alaniny, waliny, leucyny, izoleucyny i metioniny. hemiczne modyfikacje reszt aminokwasowych w białkach polegają na reakcjach: fosforylacji, γ-karboksylacji, acetylacji, metylacji, hydroksylacji, acylacji: mirystylacji i palmitylacji, prenylacji: farnezylacji i geranylogeranylacji, tworzenia glikozylofosfatydyloinozytolowych (GIP)-pochodnych, racemizacji, ADP-rybozylacji, adenylacji, ubikwitynacji, sieciowania białek z udziałem poliamin, tworzenia allizyny i poprzecznych wiązań między łańcuchami polipeptydowymi, glikozylacji oraz glikacji nieenzymatycznej. FSFRYLAJA Reakcje fosforylacji polegają na przeniesieniu końcowej grupy fosforanowej (czyli γ) z ATP na atom tlenu grupy hydroksylowej specyficznej reszty aminokwasowej, mianowicie: Ser, Thr lub Tyr. 2 ATP ADP kinaza serynowa 2 fosfataza P i 2 reszta serynypolipeptydu - P - reszta fosfoserynypolipeptydu reszta serynypolipeptydu Zmodyfikowane białko na skutek fosforylacji uzyskuje dwa dodatkowe ujemne ładunki. Fosforylacja reszty seryny w polipeptydzie zmniejsza podatność białka na proteolizę. Fosforylacja histonu 1 towarzyszy kondensacji chromosomów podczas mitozy. 275
2 Dołączona do białka grupa fosforanowa moŝe tworzyć trzy wiązania wodorowe, które dzięki tetraedrycznemu układowi przestrzennemu są silnie ukierunkowane. Zmiany te mogą powodować znoszenie dotychczasowych oddziaływań elektrostatycznych w białku i przyczyniać się do tworzenia nowych oddziaływań. Powstające w ten sposób zmiany strukturalne mogą zasadniczo zmieniać aktywność biologiczną białka, w tym aktywność katalityczną, wiązanie substratu, jeśli fosforylowanym białkiem jest enzym. Fosforylacja jest skutecznym sposobem aktywacji wielu białek, ale są i takie białka, które w wyniku fosforylacji ulegają inaktywacji (np. fosforylaza glikogenowa jest aktywowana, a syntaza glikogenowa inaktywowana). Wiele enzymów, kanałów i innych białek wewnątrzkomórkowych jest regulowana dzięki fosforylacji. Proces ten zachodzi wewnątrz komórki, gdzie jest duŝe stęŝenie ATP. Białka zewnątrzkomórkowe nie są regulowane przez odwracalną fosforylację. Reakcje fosforylacji, zachodzące w organizmie są katalizowane enzymatycznie przez kinazy (fosfotransferazy), wśród których wyróŝnia się dwie klasy: kinazy białkowe fosforylujące Ser lub Thr (klasa I) i kinazy białkowe fosforylujące Tyr (klasa II). Defosforylację, czyli hydrolizę wiązania z regeneracją grupy wodorotlenowej aminokwasu w białku i uwolnieniem ortofosforanu (P i ), katalizują fosfatazy, które znoszą skutki działania kinaz. Białka mogą podlegać cyklicznej przemianie między formą ufosforylowaną i nieufosforylowaną, z szybkością zaleŝną od aktywności kinaz i fosfataz w komórce. Fosforylacja i defosforylacja mogą przebiegać w czasie krótszym niŝ jedna sekunda lub trwać kilka godzin. Skutkiem fosforylacji jest często silne wzmocnienie początkowego sygnału np. hormonalnego. Jedna cząsteczka zaktywowanej kinazy moŝe w krótkich odstępach czasu ufosforylować setki białek docelowych, które jeśli są enzymami, przekształcą duŝą ilość substratu. KARBKSYLAJA Karboksylacja reszt glutaminianu do γ-karboksyglutaminianu w białkach uczestniczących w krzepnięciu krwi dostarcza miejsc wiąŝących jony a +2, przekształcając je ze słabych chelatorów wapnia w silne. Reakcja katalizowana jest przez system enzymatyczny zaleŝny od witaminy K. Jednym z białek uczestniczących w krzepnięciu krwi jest protrombina, która w rejonie swego -końca polipeptydu posiada 10 reszt glutaminianu, ulegających procesowi karboksylacji. Wytworzone γ-karboksyglutaminiany w protrombinie wiąŝą jony wapnia, dzięki czemu protrombina wiąŝe się z fosfolipidami błonowymi płytek krwi. Związanie protrombiny z powierzchnią płytek krwi uprzystępnia ją innym czynnikom krzepnięcia (mianowicie: czynnikowi X i V), które przekształcają pro- 276
3 trombinę w trombinę. Aktywna trombina moŝe przekształcać fibrynogen w fibrynę. Pod wpływem antykoagulantów (np. dikumarolu) lub gdy w organizmie brak jest witaminy K, protrombina nie zawiera γ-karboksyglutaminianów, dlatego nie wiąŝe jonów a i proces krzepnięcia krwi zostaje zahamowany reszta glutamylowapolipeptydu 3 - Wit K reszta γ karboksyglutamylowapolipeptydu Karboksylacja grup ε-aminowych lizyny w białku zwiększa jego podatność na proteolizę. AETYLAJA Acetylacja jest modyfikacją chemiczną szczególnie rozpowszechnioną wśród białek jąder komórkowych. Proces ten katalizują acylotransferazy przenoszące resztę acetylową z acetylo-oa na grupę ε-aminową łańcucha bocznego lizyny. W wyniku tej odwracalnej reakcji acetylacji powstaje ε -acetylolizyna. Acetylacja obniŝa ładunek dodatni lizyny. Acetylacja reszt lizyny w -końcowych domenach histonów rdzeniowych oktameru nukleosomowego towarzyszy aktywnej transkrypcji chromatyny. 2 3 S oa acetylotransferaza oas octan deacetylaza 2 2 reszta lizyny-polipeptydu 3 reszta ε -acetylolizynypolipeptydu Usunięcie reszty octanu z białka odbywa się przy udziale deacetylazy. 277
4 W nieodwracalnej acetylacji białek modyfikowana jest grupa α-aminowa - -końcowego aminokwasu polipeptydu, sprawia to, Ŝe tak zmodyfikowane białko ma zmniejszoną podatność na proteolizę. METYLAJA Reakcję metylacji katalizują metylotransferazy, które przenoszą grupę metylową z aktywnego donora (S-adenozylometioniny lub betainy) na akceptor metylu. Akceptorami grupy metylowej mogą być atomy azotu grupy aminowej w aminokwasach zasadowych i glutaminie oraz atom tlenu w asparaginie. S-adenozylometionina S-adenozylohomocys teina reszta glutaminianupolipeptydu reszta γ metyloglutamylowapolipeptydu YDRKSYLAJA Reakcji hydroksylacji ulegają dwa aminokwasy, mianowicie lizyna i prolina, które w wyniku tej reakcji są przekształcane do 5-hydroksylizyny oraz 4-hydroksyproliny, a nieco rzadziej do 3-hydroksyproliny. Proces hydroksylacji jest katalizowany przez dioksygenazy, inaczej zwane hydroksylazami lub oksygenazami hydroksylującymi. 2 - ADP ADP askorbinian 5-dioksygenaza lizyny 2-oksoglutaranu reszta lizynypolipeptydu 2-oksoglutaran reszta 5-hydroksylizyny polipeptydu bursztynian Dioksygenazy wbudowują jeden atom zaktywowanego tlenu cząsteczkowego w substrat (lizynę lub prolinę) z wytworzeniem w nim grupy. Podczas 278
5 przebiegu reakcji potrzebny jest czynnik redukujący (ADP+ + ), który powoduje redukcję drugiego atomu tlenu do wody reszta prolinypolipeptydu oksoglutaran ADP ADP askorbinian 4-dioksygenaza proliny 2-oksoglutaranu 2 2 reszta 4-hydroksyprolinypolipeptydu bursztynian ydroksylacja proliny i lizyny przebiega w obecności 2-oksoglutaranu, który przekształcany jest w oksydacyjnej dekarboksylacji do bursztynianu. Proces hydroksylacji do hydroksylizyny i hydroksyproliny wymaga obecności witaminy (askorbinianu) jako czynnika redukującego. Askorbinian utrzymuje w niezmiennym stanie jon Ŝelazawy, znajdujący się w centrum aktywnym oksygenaz hydroksylujących. AYLAJA Acylacja jest chemiczną modyfikacją białek, w wyniku której rozpuszczalne białko cytoplazmatyczne uzyskuje hydrofobową kotwicę (acyl), która umoŝliwia zaczepienie białka w błonie. Przykładami acylacji mogą być reakcje mirystylacji i palmitylacji. Mirystylacja polega na przeniesieniu reszty kwasu mirystynowego ( 14 ) (lub innej grupy acylowej) na -końcową resztę glicyny polipeptydu. W wyniku tej reakcji powstaje na -końcu polipeptydu -mirystoiloglicyna, w której obecne jest wiązanie peptydowe wytworzone z grupy kwasu mirystynowego i grupy 2 - aminokwasu. Aktywnym donorem reszty acylowej jest mirystoilo- -oa. Reakcję katalizuje enzym transferaza -mirystoilu. Mirystylacja umoŝliwia zmodyfikowanemu białku interakcję z receptorem błonowym lub z dwuwarstwą lipidową. 279
6 2 polipeptyd -mirystoiloglicyna--końca polipeptydu Palmitylacja polega na przeniesieniu reszty kwasu palmitynowego z palmitoilo-oa na grupę hydrosulfidową reszt cysteiny. W wyniku reakcji powstają pochodne S-palmitoilowe białka. Do białka rodopsyny przyłączone są dwie grupy S-palmitoilowe, które słuŝą do zakotwiczenia rodopsyny w błonie. S 2 S-palmitoilocysteina-polipeptydu PREYLAJA Prenylacja polega na przyłączaniu do białek pochodnych izoprenowych, takich jak jednostka farnezylowa ( 15 ) lub geranylogeranylowa ( 20 ). Farnezylacja jest reakcją przyłączania wiązaniem tioeterowym grup farnezylowych do reszt cysteiny, znajdujących się przy -końcu polipeptydu. S-farnezylocysteina-polipeptydu S ys X X Y - -koniec polipeptydu Reszty cysteinowe, ulegające farnezylacji, znajdują się w specyficznej sekwencji aminokwasowej XXY ( cysteina; X reszty alifatyczne; Y reszta z grupą karboksylową). Po przyłączeniu farnezylu do cysteiny, reszty XXY są proteolitycznie usuwane, a nowa końcowa grupa karboksylowa ulega metylacji. Farnezylacji ulega wiele białek, szczególnie te, które uczestniczą w przekazywaniu sygnałów lub w docelowym kierowaniu białek. Przykładowo, białko ras, dopóki nie ulegnie farnezylacji nie jest zdolne przekazać sygnałów wzrostowych, gdyŝ nie zostało włączone do błony komórkowej. Zamiast farnezylacji zachodzi geranylogeranylacja wówczas, gdy w rejonie -końca polipeptydu występuje jedna ze specyficznych sekwencji aminokwasowych:, Y lub YY ( cysteina; Y to reszta aminokwasowa z grupą karboksylową). Jednostka geranylogeranylu 280
7 przyłączana jest do jednej lub obu reszt cystein. Modyfikacja ta zachodzi w małych białkach wiąŝących GTP z rodziny rab, które biorą udział w kierowaniu białek do błon siateczki śródplazmatycznej. Przyłączenie tej wysoce hydrofobowej kotwicy jest niezbędne do związania białka z błoną. GLIKZYLFSFATYDYLIZYTLWE-PDE iektóre białka występujące na powierzchni komórki są zakotwiczone w błonie poprzez jednostki glikozylofosfatydyloinozytolowe (GPI), znajdujące się na -końcu polipeptydu. koniec polipeptydu Asp 2 2 P - Galα1 reszta fosfoetanoloaminy 6Manα1 2Galα1 Galα1 2Manα1 6 Galα1 2 jednostka oligosacharydowa 6 Man1 3 4Glcα1 jednostka fosfatydyloinozytolu 6 Inozytol 1 jednostka fosfatydyloinozytolu miejsce zakotwiczenia w błonie W błonie zwykle zakotwiczone są tylko długie łańcuchy acylowe kwasów tłuszczowych z jednostki fosfatydyloinozytolu GPI. becność glikozylofosfatydyloinozytolowej kotwicy sprawia, Ŝe połączenie białka z błoną jest elastyczne. Takie połączenie ułatwia białkom błonowym oddziaływanie z cząsteczkami znajdującymi się poza komórką, tym bardziej, Ŝe całe białko jest umiejscowione poza komór- 2 - P 2 ( 2 ) 12 ( 2 )
8 ką, z wyjątkiem acyli glikolipidowej kotwicy. Wiele enzymów hydrolitycznych i adhezyn łączy się z powierzchnią komórki poprzez jednostkę GPI. RAEMIZAJA Reakcja racemizacji L-asparaginianu w D-asparaginian jest chemiczną modyfikacją białek, związaną z wiekiem. Białkiem podatnym na tę modyfikację jest np. α-krystalina prawidłowej soczewki. Reakcja racemizacji nasilona jest w zaćmie. ADP-RYBZYLAJA Proces ADP-rybozylacji moŝe regulować funkcję wielu białek, w tym enzymatycznych, przypuszczalnie zaangaŝowany jest teŝ w tak waŝne zjawiska biologiczne, jak pamięć i uczenie. Mono-ADP-rybozylacja polega na przeniesieniu pojedynczej reszty adenozynodifosforybozy (ADP-rybozy) na białko akceptorowe w reakcji katalizowanej przez mono-adp-rybozylotransferazę. Donorem grup ADP-rybozy jest dinukleotyd nikotynamidoadeninowy (AD + ). W procesie tym mogą być modyfikowane białka pozajądrowe komórki, mianowicie czynnik elongacyjny EF2 procesu translacji lub białko G przez niektóre toksyny. Szkodliwe działanie toksyny błonicy z orynebacterium diphtheriae (gen tej toksyny pochodzi z lizogennego faga Ŝyjącego w tych bakteriach), wynika z faktu, Ŝe fragment A jej polipeptydu wykazuje aktywność katalityczną ADP-rybozylotransferazy i modyfikuje czynnik elongacyjny EF-2 translacji. ADP-rybozylowany czynnik EF-2 nie jest zdolny do przeprowadzania translokacji rosnącego polipeptydu, blokując proces translacji. becny w cytoplazmie nawet pojedynczy fragment A tej toksyny moŝe zabić komórkę. Toksyna cholery wykazuje równieŝ aktywność ADP-rybozylotransferazy i katalizuje ADP-rybozylację reszty argininy w podjednostce-α białek G sα. Modyfikacja ta w wysokim stopniu hamuje zdolność białka G sα do hydrolizowania GTP do GDP, tym samym utrzymuje przedłuŝoną jego aktywność stymulowania cyklazy adenylanowej i w ten sposób doprowadza do znacznego wzrostu stęŝenia camp. Proces poli-adp-rybozylacji modyfikuje białka jądrowe, takie jak histony 1, endonukleazy. Reakcję poli-adp-rybozylacji katalizuje ADP-rybozylotransferaza polimeryzująca, inaczej zwana syntazą poli(adpr), która sprawia, Ŝe w modyfikowanym białku znajdują się polimery adenozynodifosforybozy, czyli poli(adpr). Polimeryzacja grup ADP-rybozy następuje poprzez wytwarzanie wiązań glikozydowych pomiędzy atomem 1 rybozy jednego monomeru ADP-rybozy (który powstał z AD po usunięciu amidu kwasu nikotynowego), a atomem -2 rybozy 282
9 innego monomeru ADP-rybozy. Wytwarzanie wiązań glikozydowych między poszczególnymi monomerami doprowadza do wytworzenia oligomeru lub polimeru, czyli poli(adpr). 2 2 BIAŁK AKEPTRWE + 2 P - AD + P nikotynamid BIAŁK AKEPTRWE 2 P - P - 2 2' ADP-rybozylowane białko miejsce przyłączenia kolejnej cząsteczki ADPR przy tworzeniu poli (ADPR) Łańcuch poli-adp-rybozy zwykle połączony jest z atomem tlenu grupy γ- -karboksylowej kwasu glutaminowego lub β -fosfoseryny modyfikowanego białka. Modyfikacja ta jest odwracalna, poniewaŝ moŝe nastąpić hydrolityczne rozerwanie kolejnych wiązań glikozydowych między resztami rybozy-rybozy kolejnych monomerów i usunięcie tych cząsteczek. ADEYLAJA Adenylacja polega na kowalencyjnym przyłączeniu adenozynomonofosforanu (AMP) wiązaniem fosfodiestrowym do grupy hydroksylowej łańcucha bocznego aminokwasu w białku. Reakcja katalizowana jest przez transferazę adenylilową. Przykładem białka ulegającego adenylacji moŝe być syntetaza glutaminianowa. W tym białku enzymatycznym akceptorem AMP jest grupa hydroksylowa 283
10 specyficznej reszty tyrozynowej, znajdująca się w kaŝdej podjednostce enzymu. Adenylilowany enzym jest bardziej wraŝliwy na inhibicję stymulowaną zgodnie z zasadą sprzęŝenia zwrotnego niŝ forma enzymu niezmodyfikowanego. 2 ATP PP i 2 transferaza adenylilowa reszta tyrozynylowapolipeptydu P ryboza adenina - reszta AMP--tyrozynylowa polipeptydu Przyłączona wiązaniem fosfodiestrowym reszta AMP, w reakcji odwrotnej, moŝe być usunięta z białka w wyniku fosforolizy, katalizowanej przez ten sam enzym, który przeprowadził adenylację syntetazy glutaminianowej. UBIKWITYAJA Ubikwitynacja jest posttranslacyjną modyfikacją białka, która polega na połączeniu wiązaniem izopeptydowym ubikwityny poprzez jej -końcową resztę glicyny z grupą ε-aminową lizyny białka podlegającego tej modyfikacji. W wyniku reakcji powstaje zmodyfikowane białko zawierające monoubikwitynę. Wiązanie izopeptydowe występuje, gdy uczestniczy w nim inna grupa aminowa niŝ α-aminowa, przykładowo ε-aminowa aminokwasu. Ubikwityna jest polipeptydem (75 reszt aminokwasowych), często określanym jako niskocząsteczkowe białko (masa cząsteczkowa rzędu 8500 D), które jest wysoce termostabilne, czyli ma niezwykłą wytrzymałość na wysoką temperaturę, szeroki zakres zmian p i polarności środowiska. Monoubikwitynacja oznacza, Ŝe białko zostało zmodyfikowane pojedynczymi resztami ubikwityny. Multiubikwitynacja oznacza, Ŝe do białka dołączone są liczne reszty ubikwityny, które tworzą łańcuchy poliubikwitynowe proste lub rozgałęzione. Proces ubikwitynacji katalizują trzy enzymy (E1, E2, E3), energia (ATP) wymagana jest tylko na początkowym etapie aktywacji ubikwityny. Po monoubikwitynacji z reguły ma miejsce wiązanie się cząsteczek ubikwityny między sobą poprzez ich -końcową grupę karboksylową glicyny a miejscem akceptorowym innej cząsteczki ubikwityny, którym jest grupa ε-aminowa reszt 284
11 lizyny, znajdujących się w pozycji 48 lub 63 polipeptydu ubikwityny. Prowadzi to do powstania prostych lub rozgałęzionych łańcuchów poliubikwitynowych w modyfikowanym białku. Ryc. 1. Proces ubikwitynacji białek. 285
12 Proces ubikwitynacji jest uniwersalnym systemem u eukariota oznakowywania białek, przeznaczonych do zniszczenia. znakowanie białka ubikwityną, szczególnie w formie łańcuchów poliubikwitynowych, ukierunkowuje białko na drogę proteolizy. Ubikwitynowane białka szybko ulegają degradacji przez proteazy pozalizosomalne w strukturach zwanych proteasomami, dzięki czemu białka są eliminowane z puli białek podobnych, ale niezmodyfikowanych. W ten sposób degradowane są w cytoplazmie białka nieprawidłowo zsyntetyzowane, źle rozmieszczone w strukturach subkomórkowych lub starzejące się. SIEIWAIE BIAŁEK PLIAMIAMI ieodwracalna, posttranslacyjna modyfikacja białek, polegająca na wbudowaniu poliamin i specyficznym związaniu (sieciowaniu) łańcuchów polipeptydowych modyfikuje właściwości i funkcje białek. Białka sieciowane poliaminami występują w sieci fibrynowej krzepnącej krwi, w przestrzeni międzykomórkowej oraz w rogowaciejącej warstwie skóry i jej wytworach. Wewnątrz komórki sieciowanie poliaminami białek moŝe stabilizować cytoszkielet. Reakcje sieciowania katalizują transglutaminazy, które tworzą wiązanie γ-glutamyloaminowe między I-rzędową grupą aminową poliaminy, a resztą γ-glutamylową białek. 1 białko ( 2 ) 2 2 γ 1 białko ( 2 ) 2 γ 1 białko ( 2 ) 2 γ + ( 2 ) n 2 ( 2 ) n γ 2 ( 2 ) n 2 poliamina 2 + białko ( 2 ) 2 γ 2 2 ( 2 ) n białko wiązanie, -bis (γ glutamylo)- poliaminowe Połączenie białek wiązaniami,-bis(γ-glutamylo)poliaminowymi sprawia, Ŝe białka (tak zmodyfikowane) stają się stabilnymi polimerami, niewraŝliwymi na proteolizę, czyli degradację enzymatyczną, chemiczną i fizyczną. Białka tak zmodyfikowane mogą zwiększać odporność struktur subkomórkowych i tkanek. Przykładem mogą być keratocyty w stanie chorobowym zwanym łuszczycą, które mają 286
13 wysoki poziom poliamin i liczba wiązań,-bis(γ-glutamylo)spermidynowych wzrasta kilkakrotnie. Podobne zjawisko ma miejsce podczas apoptozy. TWRZEIE WIĄZAŃ PPRZEZY Tworzenie wiązań poprzecznych (krzyŝowych) między łańcuchami polipeptydowymi ma szczególne znaczenie podczas dojrzewania dwóch głównych białek tkanki łącznej, mianowicie kolagenu i elastyny. Podczas tworzenia wiązań poprzecznych modyfikacja chemiczna dotyczy głównie aminokwasu białkowego lizyny, choć inne teŝ mogą uczestniczyć. Ryc. 2. Przebieg powstawania wiązań krzyŝowych lizynonorleucynowych. 287
14 Proces inicjuje reakcja oksydacyjnej dezaminacji reszt lizyny w polipeptydach tropokolagenu lub elastyny, której produktem jest aldehydowa pochodna lizyny, semialdehyd 2-aminoadypinianu, zwany allizyną. Reakcję katalizuje oksydaza lizynowa, (miedzioproteina). W dalszych, złoŝonych etapach tworzenia wiązań poprzecznych, mogą być zaangaŝowane dwie, trzy lub cztery reszty aminokwasowe, przy czym ostateczny typ wiązania poprzecznego zaleŝy od tego, czy na wstępie oddziałują ze sobą reszty lizyny i allizyny (ryc. 2), czy dwie allizyny (ryc. 3). ( 2 ) ( 2 ) 2 res zty lizynydwóch polipeptydów oksydacyjna dezaminacja ( 2 ) ( 2 ) 2 res zty allizynydwóch polipeptydów kondensacja aldolowa ( 2 ) 2 2 ( 2 ) 2 aldolowe wiązanie poprzeczne 2 ( 2 ) 2 2 ( 2 ) 2 wiązanie poprzeczne histydynowo-aldolowe Ryc. 3. Przebieg powstawania aldolowych wiązań krzyŝowych. 288
15 Produktem reakcji między resztą lizyny jednego polipeptydu a allizyną drugiego polipeptydu jest najpierw połączenie typu zasady Schiffa w postaci dehydrolizynonorleucyny, które ulega redukcji do stabilnej pochodnej lizynonorleucyny, stanowiącej wiązanie poprzeczne w kolagenie i elastynie (ryc. 2). W wyniku kondensacji aldolowej dwóch allizyn pochodzących z róŝnych łańcuchów tropokolagenu powstaje między nimi aldolowe wiązanie poprzeczne, czyli z wolną grupą aldehydową. Aldolowe wiązanie poprzeczne między dwoma polipeptydami moŝe być wykorzystane do przyłączenia trzeciego łańcucha tropokolagenu poprzez jego pierścień imidazolowy reszty histydyny. statecznie uformowane wiązanie tego typu nazywa się poprzecznym wiązaniem histydynowoaldolowym (ryc. 3). Innego typu wiązanie krzyŝowe powstaje w elastynie, które łączy cztery łańcuchy polipeptydowe poprzez poliaminokwas desmozynę lub jej izomeryczną postać izodesmozynę. ba poliaminokwasy zawierają jednakowy pierścień pirydynowy, lecz róŝnią się połoŝeniem reszt lizynowych, w desmozynie znajdują się w pozycjach 3, 4, 5, a w izodesmozynie 2, 3, 5. ( 2 ) 2 ( 2 ) 3 ( 2 ) 2 + ( 2 ) 4 desmozyna W procesie tworzenia tego typu wiązania krzyŝowego uczestniczą trzy cząsteczki allizyn pochodzące z róŝnych polipeptydów oraz jedna cząsteczka lizyny z czwartego polipeptydu elastyny. Produktem kondensacji tych czterech reszt jest heterocykliczny pierścień pirymidynowy desmozyny lub izodesmozyny. GLIKZYLAJA Glikozylacja białek polega na przyłączaniu wiązaniem glikozydowym cukrowców do określonych reszt aminokwasowych polipeptydu. Wynikiem tych reakcji jest dobudowanie składnika węglowodanowego do białka i przekształcenie go w glikoproteinę. Wszystkie białka sekrecyjne ulegają glikozylacji, zatem są glikoproteinami, przynajmniej na etapie transportu z retikulum endoplazmatycznego, poprzez aparat Golgiego do błony plazmatycznej. Reakcje glikozylacji polipeptydów odpowiedzialne są za nadanie polipeptydom specyficznego cukrowego pięt- 289
16 na, które pełni rolę drogowskazu, kierującego białko do właściwego mu miejsca przeznaczenia na terenie komórki lub poza komórkę. Proces glikozylacji jest wieloetapowy i zachodzi kotranslacyjnie oraz posttranslacyjnie. Glikozylacja katalizowana jest enzymatycznie przez specyficzne glikozylotransferazy. Enzymy te są grupowane w rodziny na podstawie rodzaju przenoszonego cukru, np. galaktozylotransferazy, mannozylotransferazy, sjalilotransferazy i in. KaŜdy typ wiązania glikozydowego występujący w oligosacharydach glikoprotein tworzy odrębna glikozylotransferaza. Glikozylotransferazy przenoszą cukrowce z określonego aktywnego donora na swoistą grupę akceptora. Bezpośrednimi donorami określonych reszt monocukrowych w tkankach ssaków mogą być zarówno nukleozydodifosfomonocukry, jak i dolichylofosfomonocukry. Donorem prekursorowego oligosacharydu jest dolichylodifosfooligosacharyd Glc 3 Man 9 GlcAc 2 -P-P-Dol. Bezpośrednimi akceptorami w procesie glikozylacji mogą być: grupa aminowa przy β-karboksylowej grupie asparaginy tripeptydowej sekwencji Asn-X-Ser/Thr-polipeptydu, gdzie X nie moŝe być resztą proliny; grupy hydroksylowe aminokwasów seryny lub treoniny oraz hydroksylizyny polipeptydu; grupy hydroksylowe określonych reszt cukrowych łańcucha oligosacharydowego glikopeptydów, glikoprotein lub prekursorów dolicholowych. Glikozylacja, czyli dobudowywanie składnika cukrowego do polipeptydu, ma odmienny przebieg podczas tworzenia -glikanów i -glikanów. Tworzenie wszystkich -glikanów glikoprotein następuje drogą glikozylacji sekwencyjnej, tj. kolejno następującego po sobie przyłączania reszt monocukrowych do białka. WydłuŜanie -oligosacharydu charakteryzuje się tym, Ŝe produkt działania jednej glikozylotransferazy staje się akceptorem-substratem dla następnej glikozylotransferazy. Właściwy typ i liczba dodanych monosacharydów zaleŝą od substratu białkowego oraz typów glikozylotransferaz, które są produkowane w danej komórce (czyli od profilu glikozylacyjnego komórki). Tworzenie wszystkich -glikanów glikoprotein następuje drogą -glikozylacji z udziałem difosfodolichylowego przenośnika prekursorowego oligosacharydu (ryc. 4). Podczas inicjowania -glikozylacji ma miejsce kotranslacyjne przeniesienie en block, czyli w całości prekursorowego oligosacharydu (Glc 3 Man 9 GlcAc 2 -) na grupę aminową reszty asparaginy polipeptydu. Biosynteza -glikanów glikoprotein moŝe obejmować cztery oddzielne złoŝone etapy: syntezę difosfodolichylowego prekursorowego oligosacharydu; inicjację -glikozylacji polipeptydu; obróbkę (ang. processing) inaczej modyfikację prekursorowego oligosacharydu związanego z białkiem; 290
17 291
18 292
19 elongację łańcuchów zewnętrznych jednostek złoŝonych drogą glikozylacji sekwencyjnej. Synteza difosfodolichylowego prekursorowego oligosacharydu zachodzi w cyklu fosfodolicholowym (D-P), w którym synteza prekursorowego oligosacharydu odbywa się na fosfodolicholowej kotwicy błonowej (lipidowy nośnik) drogą glikozylacji sekwencyjnej. Lipidowe kotwice fosfodolicholowe osadzone są w błonie szorstkiej siateczki śródplazmatycznej (RER) i mają zdolność do zmiany orientacji (ruch flip ). Synteza prekursorowego oligosacharydu rozpoczyna się od cytozolowej strony błony RER przeniesieniem reszty GlcAc-P na fosfodolichol (ryc. 4). ligosacharyd wydłuŝany jest w wyniku kolejno następującego po sobie przyłączania dalszych 6 reszt monocukrowych (GlcAc i 5Man) przenoszonych z nukleotydowych aktywnych donorów. Po stronie cytozolowej powstaje tylko intermediat heptasacharydowy [-GlcAcGlcAc(Man) 5 ]. Dzięki odwróceniu orientacji difosfodolichylowego intermediatu heptasacharydowego następne monosacharydy (4Man i 3Glc) są dobudowywane od strony światła RER (ryc. 4). W przestrzeni luminalnej RER dawcami reszt Man i Glc mogą być tylko aktywne fosfodolichylowe pochodne tych monocukrów, dzięki mającej miejsce zmianie ich orientacji w błonie, poniewaŝ powstają po cytoplazmatycznej stronie błony RER. Błony RER nie są przepuszczalne dla nukleotydowych pochodnych cukrowych. Wytworzony prekursorowy oligosacharyd Glc 3 Man 9 GlcAc 2 - związany jest z dolicholem przez wiązanie pirofosforanowe o wysokiej energii. Energia ta wykorzystywana jest do przeniesienia oligosacharydu na białko w reakcji katalizowanej przez oligosacharydylotransferazę polipeptydylową: Dol-P zaleŝną, enzym związany z błoną wewnętrzną RER. Ma to miejsce podczas etapu inicjacji -glikozylacji, zachodzącej kotranslacyjnie (ryc. 4). W czasie gdy -glikozylowane białko jest jeszcze w przestrzeni luminalnej RER, moŝe zacząć się następny etap syntezy, mianowicie obróbka, czyli enzymatyczna modyfikacja prekursorowego oligosacharydu związanego z białkiem. Usuwane są trzy reszty glukozy (przez specyficzne glukozydazy) i jedna reszta mannozy (przez specyficzną mannozydazę), wówczas dopiero glikozylowane białko mo- Ŝe przemieścić się do aparatu Golgiego, gdzie jego oligosacharydy mogą być dalej modyfikowane. W aparacie Golgiego następuje przebudowa -oligosacharydów z wielomannozowych na hybrydowe po czym w złoŝone. Polega to na dalszym przycinaniu oligosacharydu (czyli usunięciu maksymalnie pięciu reszt mannozy) oraz na dobudowaniu innych monocukrów, m.in. GlcAc, Gal (ryc. 4) i ich elongacji, juŝ na zasadzie glikozylacji sekwencyjnej. 293
20 Glikozylacja terminalna odpowiedzialna jest za dobudowanie końcowych monocukrów, czyli znajdujących się na nieredukującym końcu dojrzałego -glikanu. W kwaśnych jednostkach reszty kwasu sjalowego zwykle są tymi monocukrami. GLIKAJA IEEZYMATYZA ieenzymatyczna glikacja jest bezpośrednią reakcją chemiczną między redukującym cukrem, najczęściej glukozą, a pierwszorzędową wolną grupą aminową białka, w której nie powstaje glikozyd. Reakcje tego typu mogą mieć miejsce w organizmie Ŝywym. Początkowy produkt jest labilną zasadą Schiffa (aldoiminą), która ulega powolnemu przegrupowaniu Amadori do stabilnej ketoaminowej pochodnej białka. Produkty przegrupowania Amadori mogą przybierać konformację cykliczną piranozy lub furanozy (ryc. 5). statecznym produktem nieenzymatycznej glikacji białka jest -(1-amino- -1-deoksyfrukto)-białko, które nie jest glikozydem, dlatego reakcji tej nie moŝna nazywać reakcją glikozylacji. W organizmie Ŝywym nieenzymatyczne przyłączenie cukrowca naleŝy rozpatrywać jako strukturalną i funkcjonalną modyfikację białek, mającą znaczenie w mechanizmie starzenia, która ma szczególnie wyraźny wpływ na białka o długim okresie półtrwania w organizmie. Reakcja ma miejsce w ciągu naturalnego procesu starzenia się białek i uwydatniana jest w stanach patologicznych. Tej chemicznej modyfikacji sprzyja podwyŝszony poziom monocukrów redukujących, tak jak to ma miejsce w cukrzycy. Efektywność glikacji nieenzymatycznej jest wprost proporcjonalna do czasu trwania reakcji i do stopnia hiperglikemii. Wiele róŝnych białek moŝe zawierać cukier włączony w procesie glikacji nieenzymatycznej. Wśród nich znajduje się hemoglobina, albumina i inne białka surowicy, krystalina, białka błon plazmatycznych, podstawnych, osłonek mielinowych ośrodkowego i obwodowego układu nerwowego, białka macierzy łącznotkankowej, np. kolagen. Analityczne oznaczanie glikowanych białek (szczególnie albuminy i hemoglobiny) jest wykorzystywane w diagnostyce hiperglikemii do monitorowania postępów leczenia cukrzycy, gdyŝ moŝe dostarczać informacji na temat wyrównania metabolizmu cukrów. Ze względu na krótszy okres półtrwania albuminy (17 dni) w porównaniu z hemoglobiną (120 dni), pomiar glikowanej albuminy moŝe dostarczyć informacji w znacznie krótszym czasie niŝ pomiar glikowanej hemoglobiny, która jest raczej długotrwałym wskaźnikiem wyrównania metabolizmu w cukrzycy. 294
21 + 2 białko 2 glukoza 2 białko 2 białko 2 zasada Schiffa przegrupowanie Amadori ketoamina białko białko podstawiona-1-amino-1- deoksyfruktopiranoza -podstawiona-1-amino-1- deoksyfruktofuranoza Ryc. 5. Proces nieenzymatycznej glikacji. Glikowane białka błon plazmatycznych i podstawnych oraz glikowany kolagen ścian naczyń mogą zaburzać molekularną lub elektryczną integralność kapilarnej bariery filtracyjnej, co moŝe prowadzić do zwiększonej przepuszczalności mikronaczyniowej, np. w nerkach. Glikacja krystaliny soczewki oka powoduje zmiany konformacyjne, ułatwiające tworzenie wiązań krzyŝowych w tym białku i przyczynia się do powstawania wielkocząsteczkowych agregatów krystaliny, które charakteryzują się zwiększonym pochłanianiem światła. PowyŜszy mechanizm sprzyja wytworzeniu katarakty u osób chorych na cukrzycę. Glikacja apolipoproteiny B-100 na tyle modyfikuje to białko, Ŝe lipoproteiny LDL nie są rozpoznawane przez receptor wysokiego powinowactwa i stęŝenie 295
22 LDL wzrasta w krąŝeniu. Wzrost stęŝenia LDL sprzyja rozwojowi zmian miaŝdŝycowych. Glikacja nieenzymatyczna uwaŝana jest równieŝ za pierwszy etap wielu reakcji, którym ulegają białka poza organizmem (in vitro), w obecności redukujących cukrów, np. podczas dłuŝszego przechowywania mleka i jego przetworów lub w czasie pieczenia chleba. W 1992 roku Polskie Słownictwo Biochemiczne zaleciło stosowanie terminu glikacja na określenie wszystkich reakcji polegających na przyłączaniu cukru do białka, niezaleŝnie od tego, czy tworzone jest wiązanie glikozydowe, czy nie. Produktem glikacji ma być zarówno glikozyd, którym jest glikoproteina, jak i produkt reakcji nieenzymatycznej, nie będący glikozydem, tak jak np. glikohemoglobina. Tymczasem termin glikacja stosowany jest praktycznie do określania reakcji nieenzmatycznego przyłączania cukrów do białek, w celu odróŝnienia tego procesu od glikozylacji enzymatycznej. Reakcje enzymatycznego przyłączania cukrów do białek wiązaniami glikozydowymi nadal określa się powszechnym terminem glikozylacja. 296
Chemiczne składniki komórek
 Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Nukleotydy w układach biologicznych
 Nukleotydy w układach biologicznych Schemat 1. Dinukleotyd nikotynoamidoadeninowy Schemat 2. Dinukleotyd NADP + Dinukleotydy NAD +, NADP + i FAD uczestniczą w procesach biochemicznych, w trakcie których
Nukleotydy w układach biologicznych Schemat 1. Dinukleotyd nikotynoamidoadeninowy Schemat 2. Dinukleotyd NADP + Dinukleotydy NAD +, NADP + i FAD uczestniczą w procesach biochemicznych, w trakcie których
Czy białka zbudowane są tylko z 20 rodzajów aminokwasów?
 Czy białka zbudowane są tylko z 20 rodzajów aminokwasów? mgr Adrian Jasiński Seminarium Zakładu Biofizyki i Fizyki Medycznej Plan prezentacji Wstęp Niestandardowe aminokwasy Wariacje standardowego kodu
Czy białka zbudowane są tylko z 20 rodzajów aminokwasów? mgr Adrian Jasiński Seminarium Zakładu Biofizyki i Fizyki Medycznej Plan prezentacji Wstęp Niestandardowe aminokwasy Wariacje standardowego kodu
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Przegląd budowy i funkcji białek
 Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl
 Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl Wszelkie treści i zasoby edukacyjne publikowane na łamach Portalu www.szkolnictwo.pl mogą byd wykorzystywane przez jego Użytkowników
Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl Wszelkie treści i zasoby edukacyjne publikowane na łamach Portalu www.szkolnictwo.pl mogą byd wykorzystywane przez jego Użytkowników
Substancje o Znaczeniu Biologicznym
 Substancje o Znaczeniu Biologicznym Tłuszcze Jadalne są to tłuszcze, które może spożywać człowiek. Stanowią ważny, wysokoenergetyczny składnik diety. Z chemicznego punktu widzenia głównym składnikiem tłuszczów
Substancje o Znaczeniu Biologicznym Tłuszcze Jadalne są to tłuszcze, które może spożywać człowiek. Stanowią ważny, wysokoenergetyczny składnik diety. Z chemicznego punktu widzenia głównym składnikiem tłuszczów
Czy białka zbudowane są z 20 rodzajów aminokwasów? jak radzi sobie z tym problemem modelowanie molekularne.
 Czy białka zbudowane są z 20 rodzajów aminokwasów? jak radzi sobie z tym problemem modelowanie molekularne. mgr Adrian Jasiński Zespół Teoretycznej Biofizyki Molekularnej Plan prezentacji Wstęp Niestandardowe
Czy białka zbudowane są z 20 rodzajów aminokwasów? jak radzi sobie z tym problemem modelowanie molekularne. mgr Adrian Jasiński Zespół Teoretycznej Biofizyki Molekularnej Plan prezentacji Wstęp Niestandardowe
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER)
 Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
WYKŁAD 4: MOLEKULARNE MECHANIZMY BIOSYNTEZY BIAŁEK. Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej.
 Pierwsza litera Trzecia litera 2018-10-26 WYKŁAD 4: MOLEKULARNE MECHANIZMY BIOSYNTEZY BIAŁEK Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Druga litera 1 Enancjomery para nienakładalnych
Pierwsza litera Trzecia litera 2018-10-26 WYKŁAD 4: MOLEKULARNE MECHANIZMY BIOSYNTEZY BIAŁEK Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Druga litera 1 Enancjomery para nienakładalnych
Metabolizm białek. Ogólny schemat metabolizmu bialek
 Metabolizm białek Ogólny schemat metabolizmu bialek Trawienie białek i absorpcja aminokwasów w przewodzie pokarmowym w żołądku (niskie ph ~2, rola HCl)- hydratacja, homogenizacja, denaturacja białek i
Metabolizm białek Ogólny schemat metabolizmu bialek Trawienie białek i absorpcja aminokwasów w przewodzie pokarmowym w żołądku (niskie ph ~2, rola HCl)- hydratacja, homogenizacja, denaturacja białek i
Informacje. W sprawach organizacyjnych Slajdy z wykładów
 Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Profil metaboliczny róŝnych organów ciała
 Profil metaboliczny róŝnych organów ciała Uwaga: tkanka tłuszczowa (adipose tissue) NIE wykorzystuje glicerolu do biosyntezy triacylogliceroli Endo-, para-, i autokrynna droga przekazu informacji biologicznej.
Profil metaboliczny róŝnych organów ciała Uwaga: tkanka tłuszczowa (adipose tissue) NIE wykorzystuje glicerolu do biosyntezy triacylogliceroli Endo-, para-, i autokrynna droga przekazu informacji biologicznej.
Komórka eukariotyczna
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Przemiana materii i energii - Biologia.net.pl
 Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Spis treści. 1. Wiadomości wstępne Skład chemiczny i funkcje komórki Przedmowa do wydania czternastego... 13
 Przedmowa do wydania czternastego... 13 Częściej stosowane skróty... 15 1. Wiadomości wstępne... 19 1.1. Rys historyczny i pojęcia podstawowe... 19 1.2. Znaczenie biochemii w naukach rolniczych... 22 2.
Przedmowa do wydania czternastego... 13 Częściej stosowane skróty... 15 1. Wiadomości wstępne... 19 1.1. Rys historyczny i pojęcia podstawowe... 19 1.2. Znaczenie biochemii w naukach rolniczych... 22 2.
Aminokwasy. COO - l. H 3 N C H l R
 Aminokwasy COO - l + H 3 N C H l R Aminokwasy hydrofobowe z alifatycznymi grupami R glicyna alanina walina leucyna izoleucyna prolina metionina cysteina Aminokwasy hydrofobowe z aromatycznymi grupami R
Aminokwasy COO - l + H 3 N C H l R Aminokwasy hydrofobowe z alifatycznymi grupami R glicyna alanina walina leucyna izoleucyna prolina metionina cysteina Aminokwasy hydrofobowe z aromatycznymi grupami R
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER
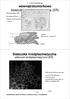 Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Bliskie spotkania z biologią METABOLIZM. dr hab. Joanna Moraczewska, prof. UKW. Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki
 Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Nośnikiem informacji genetycznej są bardzo długie cząsteczki DNA, w których jest ona zakodowana w liniowej sekwencji nukleotydów A, T, G i C
 MATERIAŁ GENETYCZNY KOMÓRKI BIOSYNTEZA BIAŁEK MATERIAŁ GENETYCZNY KOMÓRKI Informacja genetyczna - instrukcje kierujące wszystkimi funkcjami komórki lub organizmu zapisane jako określone, swoiste sekwencje
MATERIAŁ GENETYCZNY KOMÓRKI BIOSYNTEZA BIAŁEK MATERIAŁ GENETYCZNY KOMÓRKI Informacja genetyczna - instrukcje kierujące wszystkimi funkcjami komórki lub organizmu zapisane jako określone, swoiste sekwencje
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
MECHANIZMY WZROSTU i ROZWOJU ROŚLIN
 MECHANIZMY WZROSTU i ROZWOJU ROŚLIN Jaka jest rola kinaz MA (generalnie)? Do czego służy roślinom (lub generalnie) fosfolipaza D? Czy u roślin występują hormony peptydowe? Wymień znane Ci rodzaje receptorów
MECHANIZMY WZROSTU i ROZWOJU ROŚLIN Jaka jest rola kinaz MA (generalnie)? Do czego służy roślinom (lub generalnie) fosfolipaza D? Czy u roślin występują hormony peptydowe? Wymień znane Ci rodzaje receptorów
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER)
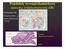 Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Aminotransferazy. Dehydrogenaza glutaminianowa. Szczawiooctan. Argininobursztynian. Inne aminokwasy. asparaginian. fumaran. Arginina.
 Inne aminokwasy Szczawiooctan Aminotransferazy asparaginian Cytrulina Argininobursztynian Cykl mocznikowy Arginina fumaran Ornityna Aminotransferazy -ketoglutaran karbamoilofosforan Mocznik kwas glutaminowy
Inne aminokwasy Szczawiooctan Aminotransferazy asparaginian Cytrulina Argininobursztynian Cykl mocznikowy Arginina fumaran Ornityna Aminotransferazy -ketoglutaran karbamoilofosforan Mocznik kwas glutaminowy
protos (gr.) pierwszy protein/proteins (ang.)
 Białka 1 protos (gr.) pierwszy protein/proteins (ang.) cząsteczki życia materiał budulcowy materii ożywionej oraz wirusów wielkocząsteczkowe biopolimery o masie od kilku tysięcy do kilku milionów jednostek
Białka 1 protos (gr.) pierwszy protein/proteins (ang.) cząsteczki życia materiał budulcowy materii ożywionej oraz wirusów wielkocząsteczkowe biopolimery o masie od kilku tysięcy do kilku milionów jednostek
SEMINARIUM 8:
 SEMINARIUM 8: 24.11. 2016 Mikroelementy i pierwiastki śladowe, definicje, udział w metabolizmie ustroju reakcje biochemiczne zależne od aktywacji/inhibicji przy udziale mikroelementów i pierwiastków śladowych,
SEMINARIUM 8: 24.11. 2016 Mikroelementy i pierwiastki śladowe, definicje, udział w metabolizmie ustroju reakcje biochemiczne zależne od aktywacji/inhibicji przy udziale mikroelementów i pierwiastków śladowych,
Mechanizmy działania i regulacji enzymów
 Mechanizmy działania i regulacji enzymów Enzymy: są katalizatorami, które zmieniają szybkość reakcji, same nie ulegając zmianie są wysoce specyficzne ich aktywność może być regulowana m.in. przez modyfikacje
Mechanizmy działania i regulacji enzymów Enzymy: są katalizatorami, które zmieniają szybkość reakcji, same nie ulegając zmianie są wysoce specyficzne ich aktywność może być regulowana m.in. przez modyfikacje
Transport przez błony
 Transport przez błony Transport bierny Nie wymaga nakładu energii Transport aktywny Wymaga nakładu energii Dyfuzja prosta Dyfuzja ułatwiona Przenośniki Kanały jonowe Transport przez pory w błonie jądrowej
Transport przez błony Transport bierny Nie wymaga nakładu energii Transport aktywny Wymaga nakładu energii Dyfuzja prosta Dyfuzja ułatwiona Przenośniki Kanały jonowe Transport przez pory w błonie jądrowej
Przedziały komórkowe siateczka endoplazmatyczna (ER)
 Pochodzenie ER Przedziały komórkowe siateczka endoplazmatyczna (ER) inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum endoplazmatyczne
Pochodzenie ER Przedziały komórkowe siateczka endoplazmatyczna (ER) inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum endoplazmatyczne
Przedziały komórkowe siateczka endoplazmatyczna (ER)
 Przedziały komórkowe siateczka endoplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum endoplazmatyczne
Przedziały komórkowe siateczka endoplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum endoplazmatyczne
Bioinformatyka wykład 9
 Bioinformatyka wykład 9 14.XII.21 białkowa bioinformatyka strukturalna krzysztof_pawlowski@sggw.pl 211-1-17 1 Plan wykładu struktury białek dlaczego? struktury białek geometria i fizyka modyfikacje kowalencyjne
Bioinformatyka wykład 9 14.XII.21 białkowa bioinformatyka strukturalna krzysztof_pawlowski@sggw.pl 211-1-17 1 Plan wykładu struktury białek dlaczego? struktury białek geometria i fizyka modyfikacje kowalencyjne
Wykład 14 Biosynteza białek
 BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
Budowa i funkcje białek
 Budowa i funkcje białek Białka Wszystkie organizmy zawierają białko Każdy organizm wytwarza własne białka Podstawowe składniki białek - aminokwasy Roślinne mogą wytwarzać aminokwasy ze związków nieorganicznych
Budowa i funkcje białek Białka Wszystkie organizmy zawierają białko Każdy organizm wytwarza własne białka Podstawowe składniki białek - aminokwasy Roślinne mogą wytwarzać aminokwasy ze związków nieorganicznych
Wykład 2. Kinetyka reakcji enzymatycznych.
 Wykład 2 Kinetyka reakcji enzymatycznych. Kofaktory enzymów wd_2 2 Ryboflawina witamina B 2 Ryboflawina wit. B 2 FAD dinukleotyd flawinoadeninowy wd_2 3 Niacyna witamina PP (B 3 ) NAD + dinukleotyd nikotynamidoadeninowy
Wykład 2 Kinetyka reakcji enzymatycznych. Kofaktory enzymów wd_2 2 Ryboflawina witamina B 2 Ryboflawina wit. B 2 FAD dinukleotyd flawinoadeninowy wd_2 3 Niacyna witamina PP (B 3 ) NAD + dinukleotyd nikotynamidoadeninowy
Aminokwasy, peptydy i białka. Związki wielofunkcyjne
 Aminokwasy, peptydy i białka Związki wielofunkcyjne Aminokwasy, peptydy i białka Aminokwasy, peptydy i białka: - wiadomości ogólne Aminokwasy: - ogólna charakterystyka - budowa i nazewnictwo - właściwości
Aminokwasy, peptydy i białka Związki wielofunkcyjne Aminokwasy, peptydy i białka Aminokwasy, peptydy i białka: - wiadomości ogólne Aminokwasy: - ogólna charakterystyka - budowa i nazewnictwo - właściwości
OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011
 OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011 DLACZEGO DOROSŁY CZŁOWIEK (O STAŁEJ MASIE BIAŁKOWEJ CIAŁA) MUSI SPOŻYWAĆ BIAŁKO? NIEUSTAJĄCA WYMIANA BIAŁEK
OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011 DLACZEGO DOROSŁY CZŁOWIEK (O STAŁEJ MASIE BIAŁKOWEJ CIAŁA) MUSI SPOŻYWAĆ BIAŁKO? NIEUSTAJĄCA WYMIANA BIAŁEK
Dr. habil. Anna Salek International Bio-Consulting 1 Germany
 1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
Slajd 1. Slajd 2. Proteiny. Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) Kwas α-aminokarboksylowy aminokwas
 Slajd 1 Proteiny Slajd 2 Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) wiązanie amidowe Kwas α-aminokarboksylowy aminokwas Slajd 3 Aminokwasy z alifatycznym łańcuchem
Slajd 1 Proteiny Slajd 2 Peptydy i białka są polimerami aminokwasów połączonych wiązaniem amidowym (peptydowym) wiązanie amidowe Kwas α-aminokarboksylowy aminokwas Slajd 3 Aminokwasy z alifatycznym łańcuchem
Białka Aminokwasy Przemiany
 Białka Aminokwasy Przemiany Profil białkowy osocza Oznaczanie osoczowego stężenia białka i profili białkowych ma duże znaczenie diagnostyczne. Pierwszym sygnałem jest zwykle zmiana stosunku Albuminy:Globuliny.
Białka Aminokwasy Przemiany Profil białkowy osocza Oznaczanie osoczowego stężenia białka i profili białkowych ma duże znaczenie diagnostyczne. Pierwszym sygnałem jest zwykle zmiana stosunku Albuminy:Globuliny.
Tłuszcze jako główny zapasowy substrat energetyczny
 Tłuszcze jako główny zapasowy substrat energetyczny Utlenienie 1 g tłuszczy pozwala na wyprodukowanie 37 kj (9 kcal) energii, podczas gdy utlenienie 1 g węglowodanów lub białek dostarcza tylko 17 kj (4
Tłuszcze jako główny zapasowy substrat energetyczny Utlenienie 1 g tłuszczy pozwala na wyprodukowanie 37 kj (9 kcal) energii, podczas gdy utlenienie 1 g węglowodanów lub białek dostarcza tylko 17 kj (4
Translacja i proteom komórki
 Translacja i proteom komórki 1. Kod genetyczny 2. Budowa rybosomów 3. Inicjacja translacji 4. Elongacja translacji 5. Terminacja translacji 6. Potranslacyjne zmiany polipeptydów 7. Translacja a retikulum
Translacja i proteom komórki 1. Kod genetyczny 2. Budowa rybosomów 3. Inicjacja translacji 4. Elongacja translacji 5. Terminacja translacji 6. Potranslacyjne zmiany polipeptydów 7. Translacja a retikulum
Reakcje zachodzące w komórkach
 Reakcje zachodzące w komórkach W każdej sekundzie we wszystkich organizmach żywych zachodzi niezliczona ilość reakcji metabolicznych. Metabolizm (gr. metabole - przemiana) to przemiany materii i energii
Reakcje zachodzące w komórkach W każdej sekundzie we wszystkich organizmach żywych zachodzi niezliczona ilość reakcji metabolicznych. Metabolizm (gr. metabole - przemiana) to przemiany materii i energii
Źródła energii dla mięśni. mgr. Joanna Misiorowska
 Źródła energii dla mięśni mgr. Joanna Misiorowska Skąd ta energia? Skurcz włókna mięśniowego wymaga nakładu energii w postaci ATP W zależności od czasu pracy mięśni, ATP może być uzyskiwany z różnych źródeł
Źródła energii dla mięśni mgr. Joanna Misiorowska Skąd ta energia? Skurcz włókna mięśniowego wymaga nakładu energii w postaci ATP W zależności od czasu pracy mięśni, ATP może być uzyskiwany z różnych źródeł
Transport makrocząsteczek
 Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Bliskie spotkania z biologią. METABOLIZM część II. dr hab. Joanna Moraczewska, prof. UKW
 Bliskie spotkania z biologią METABOLIZM część II dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki METABOLIZM KATABOLIZM - rozkład związków chemicznych
Bliskie spotkania z biologią METABOLIZM część II dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki METABOLIZM KATABOLIZM - rozkład związków chemicznych
Potranslacyjne modyfikacje białek i ich losy wkomórce
 Rozdział 28 Potranslacyjne modyfikacje białek i ich losy wkomórce 28.1. Wewnątrzkomórkowy transport białek oraz ich wydzielanie Losy cząsteczki białka p owsta jącego w pro cesie translacji są do p ewnego
Rozdział 28 Potranslacyjne modyfikacje białek i ich losy wkomórce 28.1. Wewnątrzkomórkowy transport białek oraz ich wydzielanie Losy cząsteczki białka p owsta jącego w pro cesie translacji są do p ewnego
Miarą zwiększenia lub utraty zasobu białek organizmu jest BILANS AZOTOWY:
 Aminokwasy Miarą zwiększenia lub utraty zasobu białek organizmu jest BILANS AZOTOWY: STAN RÓWNOWAGI AZOTOWEJ ilość azotu białkowego pobranego z pokarmem = ilość azotu wydalonego DODATNI występuje u rosnących
Aminokwasy Miarą zwiększenia lub utraty zasobu białek organizmu jest BILANS AZOTOWY: STAN RÓWNOWAGI AZOTOWEJ ilość azotu białkowego pobranego z pokarmem = ilość azotu wydalonego DODATNI występuje u rosnących
Zagadnienia do egzaminu z biochemii (studia niestacjonarne)
 Zagadnienia do egzaminu z biochemii (studia niestacjonarne) Aminokwasy, białka, cukry i ich metabolizm 1. Aminokwasy, wzór ogólny i charakterystyczne grupy. 2. Wiązanie peptydowe. 3. Białka, ich struktura.
Zagadnienia do egzaminu z biochemii (studia niestacjonarne) Aminokwasy, białka, cukry i ich metabolizm 1. Aminokwasy, wzór ogólny i charakterystyczne grupy. 2. Wiązanie peptydowe. 3. Białka, ich struktura.
cytoplazma + jądro komórkowe = protoplazma Jądro komórkowe
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
U grzybów i zwierząt synteza kwasów tłuszczowych zachodzi w multienzymatycznym kompleksie syntazy kwasów tłuszczowych (FAS)
 U grzybów i zwierząt synteza kwasów tłuszczowych zachodzi w multienzymatycznym kompleksie syntazy kwasów tłuszczowych (FAS) U drożdży FAS (2.4x10 6 D) składa się z dwóch typów podjednostek (α - 213 kd,
U grzybów i zwierząt synteza kwasów tłuszczowych zachodzi w multienzymatycznym kompleksie syntazy kwasów tłuszczowych (FAS) U drożdży FAS (2.4x10 6 D) składa się z dwóch typów podjednostek (α - 213 kd,
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
Fizjologia nauka o czynności żywego organizmu
 nauka o czynności żywego organizmu Stanowi zbiór praw, jakim podlega cały organizm oraz poszczególne jego układy, narządy, tkanki i komórki prawa rządzące żywym organizmem są wykrywane doświadczalnie określają
nauka o czynności żywego organizmu Stanowi zbiór praw, jakim podlega cały organizm oraz poszczególne jego układy, narządy, tkanki i komórki prawa rządzące żywym organizmem są wykrywane doświadczalnie określają
Właściwości błony komórkowej
 płynność asymetria Właściwości błony komórkowej selektywna przepuszczalność Płynność i stan fazowy - ruchy rotacyjne: obrotowe wokół długiej osi cząsteczki - ruchy fleksyjne zginanie łańcucha alifatycznego
płynność asymetria Właściwości błony komórkowej selektywna przepuszczalność Płynność i stan fazowy - ruchy rotacyjne: obrotowe wokół długiej osi cząsteczki - ruchy fleksyjne zginanie łańcucha alifatycznego
Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko. Syllabus przedmiotowy 2016/ /2019
 Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko Syllabus przedmiotowy 2016/2017-2018/2019 Wydział Fizjoterapii Kierunek studiów Fizjoterapia Specjalność ----------- Forma studiów Stacjonarne / Niestacjonarne
Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko Syllabus przedmiotowy 2016/2017-2018/2019 Wydział Fizjoterapii Kierunek studiów Fizjoterapia Specjalność ----------- Forma studiów Stacjonarne / Niestacjonarne
Ćwiczenie 4. Reakcja aminokwasów z ninhydryną. Opisz typy reakcji przebiegających w tym procesie i zaznacz ich miejsca przebiegu.
 azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
BIOENERGETYKA cz. I METABOLIZM WĘGLOWODANÓW I LIPIDÓW. dr hab. prof. AWF Agnieszka Zembroń-Łacny
 BIOENERGETYKA cz. I METABOLIZM WĘGLOWODANÓW I LIPIDÓW dr hab. prof. AWF Agnieszka Zembroń-Łacny METABOLIZM/ENERGIA WĘGLOWODANY i LIPIDY WYKŁAD 6 Trawienie i wchłanianie WĘGLOWODANY TŁUSZCZE BIAŁKA Katabolizm
BIOENERGETYKA cz. I METABOLIZM WĘGLOWODANÓW I LIPIDÓW dr hab. prof. AWF Agnieszka Zembroń-Łacny METABOLIZM/ENERGIA WĘGLOWODANY i LIPIDY WYKŁAD 6 Trawienie i wchłanianie WĘGLOWODANY TŁUSZCZE BIAŁKA Katabolizm
Program zajęć z biochemii dla studentów kierunku weterynaria I roku studiów na Wydziale Lekarskim UJ CM w roku akademickim 2013/2014
 Program zajęć z biochemii dla studentów kierunku weterynaria I roku studiów na Wydziale Lekarskim UJ CM w roku akademickim 2013/2014 S E M E S T R II Tydzień 1 24.02-28.02 2 03.03-07.03 3 10.03-14.03 Wykłady
Program zajęć z biochemii dla studentów kierunku weterynaria I roku studiów na Wydziale Lekarskim UJ CM w roku akademickim 2013/2014 S E M E S T R II Tydzień 1 24.02-28.02 2 03.03-07.03 3 10.03-14.03 Wykłady
AMINOKWASY. I. Wprowadzenie teoretyczne. Aminokwasy są to związki, które w łańcuchu węglowym zawierają zarówno grupę aminową jak i grupę karboksylową.
 AMIKWASY I. Wprowadzenie teoretyczne Aminokwasy są to związki, które w łańcuchu węglowym zawierają zarówno grupę aminową jak i grupę karboksylową. 2 3 WZY GÓLE ATUALY AMIKWASÓW WYSTĘPUJĄY W BIAŁKA Zalicza
AMIKWASY I. Wprowadzenie teoretyczne Aminokwasy są to związki, które w łańcuchu węglowym zawierają zarówno grupę aminową jak i grupę karboksylową. 2 3 WZY GÓLE ATUALY AMIKWASÓW WYSTĘPUJĄY W BIAŁKA Zalicza
11. Związki heterocykliczne w codziennym życiu
 11. Związki heterocykliczne w codziennym życiu a podstawie: J. A. Joule, K. Mills eterocyclic chemistry at a glace, 2nd ed., Wiley 2013. S. Rolski Chemia środków leczniczych, wyd. III, PZWL 1968. Związki
11. Związki heterocykliczne w codziennym życiu a podstawie: J. A. Joule, K. Mills eterocyclic chemistry at a glace, 2nd ed., Wiley 2013. S. Rolski Chemia środków leczniczych, wyd. III, PZWL 1968. Związki
Transport makrocząsteczek (białek)
 Transport makrocząsteczek (białek) Transport makrocząsteczek sortowanie białek - sekwencje sygnałowe lata 70-te XX w. - Günter Blobel - hipoteza sygnałowa; 1999r - nagroda Nobla Sekwencja sygnałowa: A
Transport makrocząsteczek (białek) Transport makrocząsteczek sortowanie białek - sekwencje sygnałowe lata 70-te XX w. - Günter Blobel - hipoteza sygnałowa; 1999r - nagroda Nobla Sekwencja sygnałowa: A
(MIKROSKOP ELEKTRONOWY, ORGANELLE KOMÓRKOWE).
 ĆWICZENIE 2. Temat: ULTRASTRUKTURA KOMÓRKI (1). (MIKROSKOP ELEKTRONOWY, ORGANELLE KOMÓRKOWE). 1. Podstawy technik mikroskopowo-elektronowych (Schemat N/2/1) 2. Budowa i działanie mikroskopu elektronowego
ĆWICZENIE 2. Temat: ULTRASTRUKTURA KOMÓRKI (1). (MIKROSKOP ELEKTRONOWY, ORGANELLE KOMÓRKOWE). 1. Podstawy technik mikroskopowo-elektronowych (Schemat N/2/1) 2. Budowa i działanie mikroskopu elektronowego
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem informacji odebranej przez komórkę. Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Receptor cząsteczka chemiczna ( peptyd
Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem informacji odebranej przez komórkę. Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Receptor cząsteczka chemiczna ( peptyd
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Integracja metabolizmu
 Integracja metabolizmu 1 Kluczowe związki w metabolizmie Glukozo- 6 -fosforan Pirogronian AcetyloCoA 2 Glukoza po wejściu do komórki ulega fosforylacji Metaboliczne przemiany glukozo- 6-fosforanu G-6-P
Integracja metabolizmu 1 Kluczowe związki w metabolizmie Glukozo- 6 -fosforan Pirogronian AcetyloCoA 2 Glukoza po wejściu do komórki ulega fosforylacji Metaboliczne przemiany glukozo- 6-fosforanu G-6-P
Biomolekuły (3) Bogdan Walkowiak. Zakład Biofizyki Instytut Inżynierii Materiałowej Politechnika Łódzka. piątek, 7 listopada 2014 Biofizyka
 Wykład 3 Biomolekuły (3) Bogdan Walkowiak Zakład Biofizyki Instytut Inżynierii Materiałowej Politechnika Łódzka 1 Monomery i Polimery (1) Biomolekuły dzielimy na 4 klasy: białka kwasy nukleinowe wielocukry
Wykład 3 Biomolekuły (3) Bogdan Walkowiak Zakład Biofizyki Instytut Inżynierii Materiałowej Politechnika Łódzka 1 Monomery i Polimery (1) Biomolekuły dzielimy na 4 klasy: białka kwasy nukleinowe wielocukry
CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A. imię i nazwisko :. klasa :.. ilość punktów :.
 CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A imię i nazwisko :. klasa :.. ilość punktów :. Zadanie 1 Przeanalizuj schemat i wykonaj polecenia. a. Wymień cztery struktury występujące zarówno w komórce roślinnej,
CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A imię i nazwisko :. klasa :.. ilość punktów :. Zadanie 1 Przeanalizuj schemat i wykonaj polecenia. a. Wymień cztery struktury występujące zarówno w komórce roślinnej,
Mechanizmy regulacji białek
 Mechanizmy regulacji białek Funkcja białka jest kontrolowana na wielu poziomach: -lokalizacja produktu genu i/lub jego partnerów -kowalencyjne i niekowalencyjne wiązanie efektorów -ilość i czas życia aktywnego
Mechanizmy regulacji białek Funkcja białka jest kontrolowana na wielu poziomach: -lokalizacja produktu genu i/lub jego partnerów -kowalencyjne i niekowalencyjne wiązanie efektorów -ilość i czas życia aktywnego
Antyoksydanty pokarmowe a korzyści zdrowotne. dr hab. Agata Wawrzyniak, prof. SGGW Katedra Żywienia Człowieka SGGW
 Antyoksydanty pokarmowe a korzyści zdrowotne dr hab. Agata Wawrzyniak, prof. SGGW Katedra Żywienia Człowieka SGGW Warszawa, dn. 14.12.2016 wolne rodniki uszkodzone cząsteczki chemiczne w postaci wysoce
Antyoksydanty pokarmowe a korzyści zdrowotne dr hab. Agata Wawrzyniak, prof. SGGW Katedra Żywienia Człowieka SGGW Warszawa, dn. 14.12.2016 wolne rodniki uszkodzone cząsteczki chemiczne w postaci wysoce
(przekaźniki II-go rzędu)
 (przekaźniki II-go rzędu) Gabriel Nowak, Małgorzata Dybała Receptory i mechanizmy przekazywania sygnału (J.Z. Nowak, J.B. Zawilska, red.) Wyd. Nauk. PWN, Warszawa, 2004 Zakład Cytobiologii i Histochemii,
(przekaźniki II-go rzędu) Gabriel Nowak, Małgorzata Dybała Receptory i mechanizmy przekazywania sygnału (J.Z. Nowak, J.B. Zawilska, red.) Wyd. Nauk. PWN, Warszawa, 2004 Zakład Cytobiologii i Histochemii,
Geometria wiązania hemu w oksymioglobinie
 Białka wiążące tlen Geometria wiązania hemu w oksymioglobinie Hem Hb A tetrametr zbudowany z dwóch identycznych łańcuchów α (141 reszt aminokwasowych, N koniec stanowi walina, a C koniec arginina) i dwóch
Białka wiążące tlen Geometria wiązania hemu w oksymioglobinie Hem Hb A tetrametr zbudowany z dwóch identycznych łańcuchów α (141 reszt aminokwasowych, N koniec stanowi walina, a C koniec arginina) i dwóch
THE UNFOLDED PROTEIN RESPONSE
 THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU KSZTAŁT BIAŁEK.
 SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU KSZTAŁT BIAŁEK. SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU KSZTAŁT BIAŁEK. SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
Enzymy katalizatory biologiczne
 Enzymy katalizatory biologiczne Kataliza zjawisko polegające na obniżeniu energii aktywacji reakcji i zwiększeniu szybkości reakcji chemicznej i/lub skierowaniu reakcji na jedną z termodynamicznie możliwych
Enzymy katalizatory biologiczne Kataliza zjawisko polegające na obniżeniu energii aktywacji reakcji i zwiększeniu szybkości reakcji chemicznej i/lub skierowaniu reakcji na jedną z termodynamicznie możliwych
Właściwości fizykochemiczne białek
 Białka Definicja Wielkocząsteczkowe związki zbudowane wyłącznie lub w dużej mierze z aminokwasów, a które stanowią największą część występujących w żywej komórce związków organicznych. Białka Podziały
Białka Definicja Wielkocząsteczkowe związki zbudowane wyłącznie lub w dużej mierze z aminokwasów, a które stanowią największą część występujących w żywej komórce związków organicznych. Białka Podziały
B) podział (aldolowy) na 2 triozy. 2) izomeryzacja do fruktozo-6-p (aldoza w ketozę, dla umoŝliwienia kolejnych przemian)
 Glikoliza (Przegląd kluczowych struktur i reakcji) A) przygotowanie heksozy do podziału na dwie triozy: 1)fosforylacja glukozy (czyli przekształcenie w formę metabolicznie aktywną) 2) izomeryzacja do fruktozo-6-p
Glikoliza (Przegląd kluczowych struktur i reakcji) A) przygotowanie heksozy do podziału na dwie triozy: 1)fosforylacja glukozy (czyli przekształcenie w formę metabolicznie aktywną) 2) izomeryzacja do fruktozo-6-p
Budowa aminokwasów i białek
 Biofizyka Ćwiczenia 1. E. Banachowicz Zakład Biofizyki Molekularnej IF UAM http://www.amu.edu.pl/~ewas Budowa aminokwasów i białek E.Banachowicz 1 Ogólna budowa aminokwasów α w neutralnym p α N 2 COO N
Biofizyka Ćwiczenia 1. E. Banachowicz Zakład Biofizyki Molekularnej IF UAM http://www.amu.edu.pl/~ewas Budowa aminokwasów i białek E.Banachowicz 1 Ogólna budowa aminokwasów α w neutralnym p α N 2 COO N
TRANSKRYPCJA - I etap ekspresji genów
 Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Biochemia zwierząt - A. Malinowska
 Spis treści Biochemia zwierząt - A. Malinowska 1. Wstęp 1.1. Wpływ środowiska zewnętrznego na organizm zwierzęcy 1.2. Podstawowe składniki organizmu zwierzęcego 1.3. Woda 1.4. Składniki mineralne 1.4.1.
Spis treści Biochemia zwierząt - A. Malinowska 1. Wstęp 1.1. Wpływ środowiska zewnętrznego na organizm zwierzęcy 1.2. Podstawowe składniki organizmu zwierzęcego 1.3. Woda 1.4. Składniki mineralne 1.4.1.
Właściwości błony komórkowej
 Właściwości błony komórkowej płynność asymetria selektywna przepuszczalność Transport przez błony Cząsteczki < 150Da Błony - selektywnie przepuszczalne RóŜnice składu jonowego między wnętrzem komórki ssaka
Właściwości błony komórkowej płynność asymetria selektywna przepuszczalność Transport przez błony Cząsteczki < 150Da Błony - selektywnie przepuszczalne RóŜnice składu jonowego między wnętrzem komórki ssaka
46 i 47. Wstęp do chemii -aminokwasów
 46 i 47. Wstęp do chemii -aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 21.1. Budowa ogólna -aminokwasów i klasyfikacja peptydów H 2 H H 2 R H R R 1 H
46 i 47. Wstęp do chemii -aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 21.1. Budowa ogólna -aminokwasów i klasyfikacja peptydów H 2 H H 2 R H R R 1 H
Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD
 Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD Aleksandra Kotynia PRACA DOKTORSKA
Wydział Farmaceutyczny z Oddziałem Analityki Medycznej Badanie oddziaływania polihistydynowych cyklopeptydów z jonami Cu 2+ i Zn 2+ w aspekcie projektowania mimetyków SOD Aleksandra Kotynia PRACA DOKTORSKA
Chemiczne składniki komórek
 Chemiczne składniki komórek Komórki wykorzystują prawa fizyki i chemii, aby przeżyć Zbudowane z takich samych pierwiastków i związków jak materia nieożywiona Chemia komórki dominują: H 2 O związki organiczne
Chemiczne składniki komórek Komórki wykorzystują prawa fizyki i chemii, aby przeżyć Zbudowane z takich samych pierwiastków i związków jak materia nieożywiona Chemia komórki dominują: H 2 O związki organiczne
Scenariusz lekcji przyrody/biologii (2 jednostki lekcyjne)
 Joanna Wieczorek Scenariusz lekcji przyrody/biologii (2 jednostki lekcyjne) Strona 1 Temat: Budowa i funkcje kwasów nukleinowych Cel ogólny lekcji: Poznanie budowy i funkcji: DNA i RNA Cele szczegółowe:
Joanna Wieczorek Scenariusz lekcji przyrody/biologii (2 jednostki lekcyjne) Strona 1 Temat: Budowa i funkcje kwasów nukleinowych Cel ogólny lekcji: Poznanie budowy i funkcji: DNA i RNA Cele szczegółowe:
WSPÓŁCZESNE TECHNIKI ZAMRAŻANIA
 WSPÓŁCZESNE TECHNIKI ZAMRAŻANIA Temat: Denaturacja białek oraz przemiany tłuszczów i węglowodorów, jako typowe przemiany chemiczne i biochemiczne zachodzące w żywności mrożonej. Łukasz Tryc SUChiKL Sem.
WSPÓŁCZESNE TECHNIKI ZAMRAŻANIA Temat: Denaturacja białek oraz przemiany tłuszczów i węglowodorów, jako typowe przemiany chemiczne i biochemiczne zachodzące w żywności mrożonej. Łukasz Tryc SUChiKL Sem.
Chemia organiczna. Aminokwasy. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Aminokwasy Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 Aminokwasy aminokwasy zawierają przynajmniej jedną grupę aminową i jedną karboksylową wzajemne ułożenie grupy
Chemia organiczna Aminokwasy Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 Aminokwasy aminokwasy zawierają przynajmniej jedną grupę aminową i jedną karboksylową wzajemne ułożenie grupy
wielkość, kształt, typy
 Mitochondria 0,5-1µm wielkość, kształt, typy 1-7µm (10µm) Filmowanie poklatkowe (w mikroskopie fluorescencyjnym) sieci mitochondrialnej w komórkach droŝdŝy (krok czasowy 3 min) Mitochondria liczebność,
Mitochondria 0,5-1µm wielkość, kształt, typy 1-7µm (10µm) Filmowanie poklatkowe (w mikroskopie fluorescencyjnym) sieci mitochondrialnej w komórkach droŝdŝy (krok czasowy 3 min) Mitochondria liczebność,
Model : - SCITEC 100% Whey Protein Professional 920g
 Białka > Model : - Producent : Scitec 100% Whey Protein Professional - jest najwyższej jakości, wolnym od laktozy, czystym koncentratem i izolat białek serwatkowych (WPC + WPI) o bardzo dobrej rozpuszczalności
Białka > Model : - Producent : Scitec 100% Whey Protein Professional - jest najwyższej jakości, wolnym od laktozy, czystym koncentratem i izolat białek serwatkowych (WPC + WPI) o bardzo dobrej rozpuszczalności
Geny i działania na nich
 Metody bioinformatyki Geny i działania na nich prof. dr hab. Jan Mulawka Trzy królestwa w biologii Prokaryota organizmy, których komórki nie zawierają jądra, np. bakterie Eukaryota - organizmy, których
Metody bioinformatyki Geny i działania na nich prof. dr hab. Jan Mulawka Trzy królestwa w biologii Prokaryota organizmy, których komórki nie zawierają jądra, np. bakterie Eukaryota - organizmy, których
TATA box. Enhancery. CGCG ekson intron ekson intron ekson CZĘŚĆ KODUJĄCA GENU TERMINATOR. Elementy regulatorowe
 Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
WŁASNOŚCI SPEKTRALNE NUKLEOTYDÓW PIRYDYNOWYCH (NAD +, NADP + ) OZNACZANIE AKTYWNOŚCI TRANSAMINAZY ALANINOWEJ
 WŁASNOŚCI SPEKTRALNE NUKLEOTYDÓW PIRYDYNOWYCH (NAD +, NADP + ) OZNACZANIE AKTYWNOŚCI TRANSAMINAZY ALANINOWEJ WSTĘP Nukleotydy pirydynowe (NAD +, NADP + ) pełnią funkcję koenzymów dehydrogenaz przenosząc
WŁASNOŚCI SPEKTRALNE NUKLEOTYDÓW PIRYDYNOWYCH (NAD +, NADP + ) OZNACZANIE AKTYWNOŚCI TRANSAMINAZY ALANINOWEJ WSTĘP Nukleotydy pirydynowe (NAD +, NADP + ) pełnią funkcję koenzymów dehydrogenaz przenosząc
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
(węglowodanów i tłuszczów) Podstawowym produktem (nośnikiem energii) - ATP
 śycie - wymaga nakładu energii źródłem - promienie świetlne - wykorzystywane do fotosyntezy - magazynowanie energii w wiązaniach chemicznych Wszystkie organizmy (a zwierzęce wyłącznie) pozyskują energię
śycie - wymaga nakładu energii źródłem - promienie świetlne - wykorzystywane do fotosyntezy - magazynowanie energii w wiązaniach chemicznych Wszystkie organizmy (a zwierzęce wyłącznie) pozyskują energię
Rzęski, wici - budowa Mikrotubule. rozmieszczenie organelli. Stabilne mikrotubule szkielet rzęsek i wici
 Mikrotubule dynamiczna niestabilność - stabilizacja rozmieszczenie organelli ER Golgi organizują wnętrze komórki - polaryzacja komórki Mt Mt organizacja ER, aparatu Golgiego przemieszczanie mitochondriów
Mikrotubule dynamiczna niestabilność - stabilizacja rozmieszczenie organelli ER Golgi organizują wnętrze komórki - polaryzacja komórki Mt Mt organizacja ER, aparatu Golgiego przemieszczanie mitochondriów
21. Wstęp do chemii a-aminokwasów
 21. Wstęp do chemii a-aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2016/2017 1 21.1. Budowa ogólna a-aminokwasów i klasyfikacja peptydów H 2 N H kwas 2-aminooctowy
21. Wstęp do chemii a-aminokwasów Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2016/2017 1 21.1. Budowa ogólna a-aminokwasów i klasyfikacja peptydów H 2 N H kwas 2-aminooctowy
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Fizjologia człowieka
 Fizjologia człowieka Wykład 2, część A CZYNNIKI WZROSTU CYTOKINY 2 1 Przykłady czynników wzrostu pobudzających proliferację: PDGF - cz.wzrostu z płytek krwi działa na proliferację i migrację fibroblastów,
Fizjologia człowieka Wykład 2, część A CZYNNIKI WZROSTU CYTOKINY 2 1 Przykłady czynników wzrostu pobudzających proliferację: PDGF - cz.wzrostu z płytek krwi działa na proliferację i migrację fibroblastów,
Geny, a funkcjonowanie organizmu
 Geny, a funkcjonowanie organizmu Wprowadzenie do genów letalnych Geny kodują Białka Kwasy rybonukleinowe 1 Geny Występują zwykle w 2 kopiach Kopia pochodząca od matki Kopia pochodząca od ojca Ekspresji
Geny, a funkcjonowanie organizmu Wprowadzenie do genów letalnych Geny kodują Białka Kwasy rybonukleinowe 1 Geny Występują zwykle w 2 kopiach Kopia pochodząca od matki Kopia pochodząca od ojca Ekspresji
Joanna Bereta, Aleksander Ko j Zarys biochemii. Seria Wydawnicza Wydziału Bio chemii, Biofizyki i Biotechnologii Uniwersytetu Jagiellońskiego
 Joanna Bereta, Aleksander Ko j Zarys biochemii Seria Wydawnicza Wydziału Bio chemii, Biofizyki i Biotechnologii Uniwersytetu Jagiellońskiego Copyright by Wydział Bio chemii, Biofizyki i Biotechnologii
Joanna Bereta, Aleksander Ko j Zarys biochemii Seria Wydawnicza Wydziału Bio chemii, Biofizyki i Biotechnologii Uniwersytetu Jagiellońskiego Copyright by Wydział Bio chemii, Biofizyki i Biotechnologii
