Regulacja procesu glikozylacji białek przez kaskadę camp
|
|
|
- Gabriela Szewczyk
- 8 lat temu
- Przeglądów:
Transkrypt
1 Regulacja procesu glikozylacji białek przez kaskadę camp STRESZCZENIE Glikozylacja jest jedną z najczęściej występujących modyfikacji potranslacyjnych. Spośród znanych jej form najpowszechniejsze są N- i O-glikozylacja. Inna z potranslacyjnych modyfikacji białek, fosforylacja jest powszechnym sposobem regulacji aktywności białek enzymatycznych. Regulacji tej podlegają także enzymy prowadzące reakcje na wczesnych etapach procesów N- i O-glikozylacji. Jednym z nich jest syntaza mannozylofosfodolicholu prowadząca reakcję dołączania pierwszej reszty mannozy do fosfodolicholu i tym samym rozpoczynająca syntezę struktury oligosacharydowej w procesie N-glikozylacji. Indukowana przez kaskadę camp, a realizowaną przez kinazę białek A fosforylacja syntazy mannozylofosfodolicholu, powoduje wzmacnianie jej aktywności. Innym enzymem wczesnych etapów N-glikozylacji, regulowanym przez camp jest cis-prenyltransferaza, katalizująca syntezę fosfodolicholu, a regulacja opiera się o zmiany ekspresji genu tego białka. Wpływ camp na przebieg O-glikozylacji opisany został w odniesieniu syntezy struktur O-GlcNAc. Fosforylacja reguluje aktywność syntetyzującej glukozaminę amidotransferazy glutamina fruktozo-6-fosforan i prowadzi do ograniczenia syntezy O-GlcNAc. Obserwacje te sugerują istotną rolę czynników oddziałujących poprzez GPCR na syntezę N- i O-glikanów. WPROWADZENIE Cukry to jedna z największych grup związków organicznych, występujących w każdym żywym organizmie. Pełnią one kluczową rolę w przebiegu większości procesów życiowych, będąc głównym materiałem budulcowym i energetycznym. Ich struktura, synteza oraz biologiczna funkcja w stanach fizjologicznych oraz w przebiegu procesów patologicznych są przedmiotem badań glikobiologii. Całość składnika cukrowcowego, zarówno odrębnych cząsteczek węglowodanów, jak i tych budujących bardziej złożone struktury, określa się mianem glikomu. W sposób systematyczny jego różnymi aspektami (m. in. genetycznym, fizjologicznym, patologicznym) zajmuje się glikomika, stanowiąca jedną z gałęzi glikobiologii. Jedną z głównych klas glikomu stanowią węglowodany kompleksowe, czyli glikokoniugaty, które w swej strukturze zawierają co najmniej jeden łańcuch oligosacharydowy. Wszystkie glikokoniugaty są produktami procesu glikozylacji, czyli enzymatycznego tworzenia wiązań kowalencyjnych między łańcuchami oligosacharydowymi a łańcuchami białek (w przypadku glikoprotein i proteoglikanów) lub lipidów (w glikolipidach). Magdalena Surman Marcelina Janik * Zakład Biochemii Glikokoniugatów, Instytut Zoologii, Uniwersytet Jagielloński, Kraków * Zakład Biochemii Glikokoniugatów, Instytut Zoologii, Uniwersytet Jagielloński, ul. Gronostajowa 9, Kraków; tel.: (12) , faks: (12) ; marcelina. janik@uj.edu.pl Artykuł otrzymano 28 lutego 2014 r. Artykuł zaakceptowano 9 czerwca 2014 r. Słowa kluczowe: glikozylacja, kaskada camp, syntaza mannozylofosfodolicholu, białka G, cyklaza adenylanowa Wykaz skrótów: AC cyklaza adenylanowa; camp cykliczny adenozynomonofosforan; CMP cytozynomonofosforan; Dol- -P fosforan dolicholu; DPMS syntaza mannozylofosfodolicholu; Gal galaktoza, GDP guanozynodifosforan; GEF czynnik wymiany nukleotydów guaninowych; GlcNAc N-acetyloglukozoamina; GPCR receptory sprzężone z białkiem G; GTP guanozynotrifosforan; LLO jednostka oligosacharydowa związana z nośnikiem lipidowym; Man mannoza; PKA kinaza białkowa A; RER szorstkie retikulum endoplazmatyczne; UDP urydynodifosforan Biosynteza struktur oligosacharydowych, czy to bezpośrednio na łańcuchu polipeptydowym, czy na lipidowym nośniku, odbywa się przy udziale glikozylotransferaz, dodających wybrane reszty cukrowe do rozbudowywanej struktury oraz glikozydaz, które usuwają określone monosacharydy ze struktury cukrowca. Są to reakcje charakterystyczne dla filogenetycznie szerokiego spektrum organizmów żywych, począwszy od Archea i Eubacteria, po Eukaryota [1]. W przypadku białek glikozylacja jest najczęstszą potranslacyjną modyfikacją, w wyniku której różnorodne oligosacharydy zostają przyłączone nawet do 50% powstających łańcuchów polipeptydowych [2]. Niewątpliwie stanowi ona jeden z głównych czynników decydujących o chemicznej i funkcjonalnej różnorodności białek, i wpływa na ich biologiczną aktywność. Jak stwierdzono, wzory glikozylacji są charakterystyczne dla konkretnych łańcuchów białkowych syntetyzowanych w określonych typach komórek bądź w konkretnych tkankach. Obserwacje te sugerują, że w przypadku glikoprotein to nie komponenta białkowa, ale właśnie część cukrowa stanowi podstawę złożoności ich struktur, a przez to modyfikuje ich funkcje [3]. Zróżnicowanie glikoprotein wynikać może z modyfikacji, do jakich dochodzi w trakcie syntezy, a które odnoszą się do różnych aspektów ich struktury, począwszy od typu i miejsca utworzenia wiązania glikozydowego, poprzez strukturę łańcucha oligosacharydowego (rodzaje reszt cukrowych) i jego długość, skończywszy na obecności lub braku rozgałęzień. Zdolność monomerów budujących oligosacharydy do łączenia się ze sobą na wiele sposobów gwarantuje chemiczną różnorodność. Jej źródłem jest przede Postępy Biochemii 60 (3)
2 wszystkim duża liczba naturalnie występujących monosacharydów i ich izomerów, anomeryczność wiązania glikozydowego, tworzenie rozgałęzień, ale także możliwe modyfikacje reszt cukrowych poprzez przyłączanie grup siarczanowych, acetylowych lub fosforanowych [4]. Do syntezy łańcuchów oligosacharydowych w komórkach eukariotycznych dochodzi w świetle szorstkiej siateczki endoplazmatycznej (RER), a poszczególne reszty cukrowe są usuwane bądź dodawane podczas transportu glikoproteiny z RER, poprzez aparat Golgiego, na powierzchnię komórki. Obecność reszt cukrowych w strukturze białka zmienia jego właściwości fizyczne, w tym rozmiar, kształt, stopień sfałdowania, rozpuszczalność i ładunek elektryczny. Pod względem biologicznym, białka poddane glikozylacji mogą różnić się poziomem sekrecji, aktywnością czy immunogennością. Przykładem wpływu glikozylacji na stabilność cząsteczki są hormony ssaków, będące glikoproteinami, które najczęściej występują w formie dimerycznej, łańcuchy oligosacharydowe umożliwiają tu połączenie między dwiema cząsteczkami białka i zapewniają odporność na proteolizę. Ponadto glikozylacja jest istotna dla mechanizmu wzajemnego rozpoznawania się komórek (np. podczas tworzenia przerzutów nowotworowych) czy procesu zapłodnienia (częściowo zależnego od wiązania się łańcuchów oligosacharydowych znajdujących się na powierzchni oocytu i plemnika) [5]. Spośród ok. 200 naturalnie występujących monosacharydów, zaledwie 8 powszechnie występuje w łańcuchach oligosacharydowych glikoprotein [1]. Co istotne w większości reakcji biosyntezy glikoprotein nie biorą udziału wolne, czy ufosforylowane formy cukrów lecz wykorzystywane są odpowiadające im nukleotydocukry. Większość z nich powstaje w cytoplazmie z nukleotydów, takich jak urydynodifosforan (UDP), guanozynodifosforan (GDP) bądź cytozynomonofosforan (CMP). Wyjątkiem są pochodne kwasów sjalowych, które związane z CMP wytwarzane są w jądrze [6]. Zaktywowane cukry zostają włączone w struktury łańcuchów oligosacharydowych pod warunkiem dostępności swoistych glikozylotransferaz. Większość z tych enzymów wymaga do pełnej aktywności obecności dwuwartościowego kationu (głównie jonu Mn 2+ ) i jest wysoce specyficzna względem akceptora, oligosacharydu, cukru nukleotydowego oraz rodzaju połączenia cukru z akceptorem [7], i co istotne, większość z nich (poza kilkoma wyjątkami) należy do glikoprotein [8]. Kolejność dodawania reszt cukrowych do tworzonego łańcucha oligosacharydowego, a tym samym jego struktura, zależy również od rozmieszczenia glikozylotransferaz w poszczególnych przedziałach komórkowych. Wybrana reszta cukrowa jest włączana w strukturę oligosacharydu tylko wtedy, gdy znajdzie się on w przedziale, w którym występuje właściwa glikozylotransferaza. Pierwsze reszty cukrowe lub prekursorowe łańcuchy oligosacharydowe są przyłączane do łańcuchów polipeptydowych w obrębie RER. Proces ten może zachodzić zarówno w trakcie translacji jak i po jej zakończeniu, a utworzona w jego wyniku cząsteczka podlega dalszym modyfikacjom w aparacie Golgiego [8]. Rozmieszczenie glikozylotransferaz w jego poszczególnych przedziałach jest charakterystyczne, enzymy biorące udział w początkowych etapach syntezy struktur oligosacharydowych przeważają ilościowo w części cis i cysternach pośrednich, natomiast enzymy właściwe dla etapów późniejszych są zgromadzone w części trans [9]. Wytworzenie wiązania pomiędzy pierwszą resztą cukrową a aminokwasem jest kluczowe dla biosyntezy łańcuchów oligosacharydowych w procesie glikozylacji, uruchamia ono złożoną serię potranslacyjnych reakcji enzymatycznych. Dotychczas zidentyfikowano 13 różnych monosacharydów (uwzględniając izomery) i 8 reszt aminokwasowych zdolnych do utworzenia 41 różnych wiązań między resztą cukrową a resztą aminokwasową w glikoproteinach. Na podstawie ich szczegółowej struktury wyróżnia się 5 typów glikozylacji: O-glikozylację, N-glikozylację, C-glikozylację, glipiację i fosfoglikozylację [1]. Najpowszechniej występujące N- i O-glikoproteiny charakteryzują połączenia oligosacharydów z resztami aminokwasowymi w łańcuchu polipeptydowym poprzez Asn w przypadku N-oligosacharydów i Ser/Thr w przypadku O-oligosacharydów. MECHANIZM SYNTEZY JEDNOSTEK OLIGOSACHARYDOWYCH ZWIĄZANYCH Z NOŚNIKIEM LIPIDOWYM W PRZEBIEGU N-GLIKOZYLACJI Dotychczas opublikowane wyniki badań nad regulacją procesu glikozylacji białek przez kaskadę cyklicznego adenozynomonofosforanu (camp), dotyczyły w przeważającej mierze procesu N-glikozylacji. Powstałe w jego wyniku glikoproteiny posiadają oligosacharydy połączone wiązaniem N- -glikozydowym z Asn w łańcuchu polipeptydowym o wspólnym rdzeniu składającym się z pięciu reszt cukrowych: Manα(1,3)-Man-α(1,6)-Man-β(1,4)-GlcNAc-β(1,4)-GlcNAc-β1. Typowa struktura rdzenia powstaje w efekcie wspólnego dla wszystkich N-glikanów pierwszego etapu ich biosyntezy, który nie wymaga obecności łańcuchów białkowych lecz odbywa się z wykorzystaniem związanego z błoną ER lipidowego nośnika, fosforanu dolicholu (Dol-P). Dol-P stanowi podstawę do syntezy prekursorowej jednostki oligosacharydowej związanej z nośnikiem lipidowym (LLO, ang. lipid linked oligosaccharide) (Ryc. 1), który następnie jest przenoszony na atom azotu grupy amidowej Asn w strukturze docelowego białka [10]. Dolichol to jeden z najdłuższych, naturalnie występujących alkoholi, zawierający około jednostek izoprenowych (C 5 ). W pierwszych reakcjach procesu N-glikozylacji ulega on fosforylacji do Dol-P, kinaza dolicholowa katalizuje reakcję przeniesienia reszty fosforanowej z adenozynotrifosforanu (ATP) na dolichol. Ufosforylowana forma tworzy wiązanie z łańcuchem oligosacharydowym poprzez końcową grupę fosforanową [11,12]. Reszty cukrowe są przyłączane do Dol-P kolejno od cytosolowej, a następnie od luminarnej strony RER. W wyniku kolejnych reakcji powstaje jednostka oligosacharydowa LLO, składająca się z dwóch reszt GlcNAc, dziewięciu reszt Man i trzech reszt Glc (GlcNAc 2 -Man 9 -Glc 3 ). Związany z difosfodolicholem łańcuch oligosacharydowy jest następnie przenoszony w całości na nowo zsyntetyzowane białko związane z błoną RER [13]. Tam przy udziale transferazy oligosacharydowo-białkowej, związanej z błoną wewnętrzną RER, wytwarzane jest wiązanie N-glikozydowe z udziałem atomu azotu grupy amidowej Asn łańcucha 306
3 Rycina 1. Schemat syntezy LLO. Na lipidowym nośniku, jakim jest fosforan dolicholu, rozbudowywany jest łańcuch oligosacharydowy. Proces ten rozpoczyna się od przyłączenia do fosforanu dolicholu dwóch reszt N-acetyloglukozoaminy, do których następnie dołączanych jest kolejnych 5 reszt mannozy z donora, jakim jest guanozynodifosforan mannozy (GDP-Man). Tak rozbudowany oligosacharyd przenoszony jest do światła siateczki endoplazmatycznej. W tym miejscu istotna jest aktywność syntazy mannozylofosfodolicholu (DPMS), dzięki której syntetyzowane są donory w postaci Dol-P-Man, niezbędne do dalszej rozbudowy oligosacharydu. polipeptydowego. Transferaza ta może przenosić dowolne cząsteczki o strukturze Dol-P-P-(GlcNAc) 2 -R, jednak wykazuje preferencyjne powinowactwo w stosunku do związku o strukturze Dol-P-P-GlcNAc 2 -Man 9 -Glc 3. Drugim produktem reakcji katalizowanej przez transferazę oligosacharydowo-białkową jest Dol-P-P. Jest on następnie przekształcany do Dol-P przy udziale fosfatazy i może posłużyć do syntezy kolejnego łańcucha oligosacharydo-p-p-dolicholu [14,15]. Proces N-glikozylacji nie kończy się na przeniesieniu reszt cukrowych z Dol-P-P-GlcNAc 2 -Man 9 -Glc 3 i związaniu ich z polipeptydem, co często określa się mianem glikozylacji rdzeniowej. W wyniku późniejszych przekształceń łańcucha oligosacharydowego powstają makrocząsteczki posiadające wspólny pentasacharydowy rdzeń GlcNAc 2- -Man 3, jednak odmienne pod względem struktury dalszej części łańcucha. Na podstawie różnic w budowie wydzielono trzy zasadnicze klasy N-wiązanych oligosacharydów: kompleksowe, hybrydowe i wysokomannozowe. Struktury kompleksowe oligosacharydów u człowieka zakończone są zwykle resztą kwasu sjalowego (kwas N-acetyloneuraminowy, NeuAc) podczas gdy u innych kręgowców w tej pozycji wbudowywany jest kwas N-glikoliloneuraminowy (Neu5Gc). Dla tego typu oligosacharydów charakterystyczne są także wydłużone łańcuchy poli-n-acetylolaktozaminylowe, rozbudowane resztami GlcNAc i Gal, tworzące powtarzający się fragment N-acetylolaktozaminylowy. Alternatywne zakończenie łańcucha mogą stanowić reszty Gal lub Fuc. Większość zawiera od 2 do 4 zewnętrznych rozgałęzień nazywanych antenami. Oligosacharydy bogate w mannozę oprócz rdzenia pentasacharydowego zawierają od 2 do 6 dodatkowych reszt mannozy, natomiast struktury o charakterze hybrydowym posiadają cechy właściwe dla obu klas [3,16]. KASKADA CYKLICZNEGO AMP W trakcie biosyntezy łańcuchów polipeptydowych glikoprotein ich skład aminokwasowy jest ściśle zdeterminowany sekwencją fragmentu mrna kodującego dane białko. W odróżnieniu od tego procesu synteza łańcuchów oligosacharydowych zachodzi na drodze serii specyficznych reakcji enzymatycznych, dzięki temu jej przebieg może być regulowany przez wiele czynników, a efektem tego jest obserwowana ogromna różnorodność powstających struktur oligosacharydowych [17]. Jednym z czynników regulujących aktywność białek enzymatycznych w komórkach jest camp inicjujący wewnątrzkomórkowy szlak przekazu sygnału określany jako kaskada camp. Był on pierwszym zidentyfikowanym przekaźnikiem drugiego rzędu [18], a jego biologiczna rola pozostaje w kręgu zainteresowań naukowców od lat 50-tych XX wieku. Kluczowym było udowodnienie, iż wewnątrzkomórkowa synteza camp, jako przekaźnika drugiego rzędu, zachodzi w odpowiedzi na sygnały przekazywane pomiędzy komórkami przez przekaźniki pierwszego rzędu (np. neuroprzekaźniki czy hormony) [19]. Ich Postępy Biochemii 60 (2)
4 cząsteczki nie wnikają do komórek, lecz wiążą się ze specyficznymi receptorami obecnymi w błonie komórkowej, których aktywacja prowadzi do cyklizacji ATP. Wewnątrzcząsteczkowe przejście prowadzące do utworzenia wiązania fosfodiestrowego w cząsteczce ATP z jednoczesnym uwolnieniem pirofosforanu katalizuje cyklaza adenylanowa (AC), integralne białko błonowe o masie 120 kda i wielu segmentach transbłonowych [20-23]. Stężenie powstającego camp podlega regulacji dzięki silnie egzoergicznej reakcji hydrolizy tej cząsteczki do 5 -AMP katalizowanej przez specyficzną fosfodiesterazę camp. W efekcie dochodzi do zahamowania przekazu sygnału wewnątrzkomórkowego [20,24,25]. Kaskada camp jest modelowym przykładem systemu sygnalizacji inicjowanego przez receptory sprzężone z białkami G (GPCRs, ang. G-protein-coupled receptors). Synteza camp następuje zazwyczaj na skutek aktywacji receptorów, które w odpowiedzi na bodziec docierający do komórki, stymulują lub hamują AC za pośrednictwem heterotrimerycznych białek G (Ryc. 2). Jest to najliczniejsza i najbardziej zróżnicowana pod względem funkcjonalnym grupa receptorów dla hydrofilowych związków o charakterze przekaźników chemicznych. Zalicza się do niej białka receptorowe swoiście wiążące neuroprzekaźniki, neuromodulatory i hormony (receptory adrenergiczne, receptory dopaminowe, receptory serotoninowe, receptory histaminowe, błonowe receptory melatoninowe), a także rodopsynę, receptor dla światła [26-28]. Wszystkie GPCRs zlokalizowane są w błonie komórkowej, a czas od związania agonisty do uzyskania odpowiedzi układu efektorowego (kanału jonowego czy enzymu) w ich przypadku jest rzędu sekund [28]. Wszystkie GPCRs mają ten sam schemat budowy i mechanizm działania, łańcuch białka receptorowego siedmiokrotnie przechodzi przez błonę komórkową, w wyniku czego powstaje siedem α-helikalnych transbłonowych odcinków zbudowanych z reszt hydrofobowych aminokwasów, które połączone są pętlami wewnątrz- i zewnątrzkomórkowymi; N-koniec zlokalizowany jest na zewnątrz komórki, a C-koniec łańcucha polipeptydowego znajduje się w cytozolu i zawiera sekwencje mogące ulegać fosforylacji. Miejsce wiązania się liganda z receptorem znajduje się w obrębie hydrofobowej kieszeni utworzonej w błonie komórkowej przez transbłonowe α-helisy, natomiast białka G łączą się z receptorem w pobliżu błony komórkowej za pośrednictwem cytoplazmatycznej, najbliższej C-końcowi pętli [28]. Funkcjonalna wszechstronność systemów sygnalizacji komórkowej wykorzystujących białko G w roli mediatora, opiera się na jego modułowej strukturze (zbudowane jest z trzech podjednostek: α, β i γ) i istnieniu wielu jego podtypów [29]. Prowadzone w ostatnich dekadach badania wykazały, że powstające w wyniku dysocjacji zaktywowanego białka G podjednostki Gα i Gβγ są w stanie niezależnie wpływać na działanie kilku układów efektorowych, a efekt tego oddziaływania jest synergistyczny bądź przeciwstawny [30]. GPCR po związaniu liganda odgrywa rolę czynnika wymiany nukleotydów guaninowych (GEF, ang. guanine nucleotide exchange factor). Po przejściu guanozynodifosforanu (GDP) w guanozynotrifosforan (GTP), heterotrimeryczny kompleks białka G dysocjuje na podjednostki Gβγ i Gα. Kompleks Gα s GTP aktywuje AC, podczas gdy kompleks Rycina 2. Aktywacja kaskady camp przez receptor sprzężony z białkiem G (GPCR). GPCR związane z białkiem G, w skład którego wchodzi podjednostka G s α, po związaniu liganda aktywują cyklazę adenylanową (AC). W efekcie tej aktywacji dochodzi do przekształcenia ATP do formy cyklicznego AMP, które następnie łącząc się z regulatorowymi (R) podjednostkami kinazy białkowej A (PKA), powoduje ich zmiany konformacyjne, co wywołuje oddysocjowanie podjednostek katalitycznych (C), umożliwiając im prowadzenie reakcji fosforylacji na wybranych substratach białkowych. Gα i GTP jest jej inhibitorem. Ponadto podjednostka Gα posiada aktywność GTPazy, która doprowadza do hydrolizy GTP do GDP, co hamuje jej oddziaływanie na AC [23]. Mechanizm cyklizacji związanego przez AC ATP do camp wymaga ponadto obecności dwóch jonów Mg 2+, które wiążą się z AC oraz z powstałym kompleksem AC i ATP [31]. Cykliczny AMP, jako element wielu szlaków sygnalizacji wewnątrzkomórkowej, bierze udział w regulacji różnych procesów fizjologicznych. Do jego efektorów zalicza się białka Epac 1 i 2 (EPAC, ang. exchange protein directly activated by camp), które są białkowymi GEF aktywowanymi przez camp, a oddziałującymi przede wszystkim z GTPazami Rap 1 i 2 [32]. Efektorami camp są również kanały jonowe bramkowane cyklicznymi nukleotydami, które są szczególnie istotne dla funkcjonowania narządów zmysłów (zapachu i smaku). Większość efektów wywoływanych w komórkach eukariotycznych przez camp zachodzi jednak w wyniku aktywacji pojedynczej kinazy białkowej, określanej jako kinaza białkowa A (PKA). Utworzony przy udziale AC camp oddysocjowuje od błony do cytosolu, a gdy jego stężenie osiągnie wartość rzędu 10 nm, aktywuje PKA [33]. PKA zbudowana jest z dwóch rodzajów podjednostek, dimerycznej podjednostki regulatorowej oraz dwóch podjednostek katalitycznych. Podjednostki katalityczne pozostają związane z podjednostką regulacyjną, tworząc nieaktywną formę holoenzymu. W odpowiedzi na aktywację AC przez GPCR i wytworzenie drugorzędowego przekaźnika w po
5 staci camp, cztery jego cząsteczki wiążą się z podjednostką regulatorową PKA. Dochodzi wówczas do zmian konformacyjnych w obrębie podjednostki regulatorowej PKA, co prowadzi do zmniejszenia jej powinowactwa do podjednostek katalitycznych (do ), które oddysocjowując z kompleksu uzyskują zdolność do fosforylacji białkowego substratu [34]. Fosforylacja oznacza przeniesienie przez kinazy białkowe końcowej grupy fosforanowej z ATP na resztę hydroksylową specyficznego aminokwasu (seryny lub treoniny, w przypadku PKA, bądź tyrozyny). Niezmodyfikowana forma białka może być regenerowana dzięki aktywności fosfataz białkowych. Katalizują one reakcje hydrolizy grup fosforanowych połączonych z białkami, w wyniku których dochodzi do odwrócenia skutków działania kinaz poprzez odtworzenie grupy hydroksylowej łańcucha bocznego i powstanie ortofosforanu. W przypadku białek enzymatycznych fosforylacja przez PKA prowadzi do zmiany ich aktywności [2]. REGULACJA PROCESU GLIKOZYLACJI BIAŁEK PRZEZ KASKADĘ camp Większość dotychczas prowadzonych badań nad regulacyjnym wpływem kaskady camp na przebieg proces glikozylacji dotyczyła jednej z pierwszych reakcji zachodzących w trakcie syntezy N-oligosacharydów, syntezy Dol-P-Man, będącego donorem części reszt mannozy podczas syntezy LLO. Reakcję syntezy Dol-P-Man z GDP-Man i Dol-P, która zachodzi po cytosolowej stronie RER, katalizuje syntaza mannozylofosfodolicholu (DPMS) i to właśnie aktywność tego enzymu podlega regulacji przez kaskadę camp [35-39]. Dol-P-Man ulega następnie translokacji do światła RER, gdzie stanowi jedyny donor mannozy w procesie glikozylacji, w związku z brakiem transporterów dla GDP-Man. W efekcie DMPS jest silnie zaangażowana w syntezę LLO, który następnie przenoszony jest na łańcuch polipeptydowy w procesie N-glikozylacji [40]. Badania struktury DMPS ssaków pokazały, że składa się ona z trzech białek: DPM1, DPM2, DPM3. DMP1 odpowiada bezpośrednio za katalizowanie reakcji syntezy Dol- -P-Man (Ryc. 3). Rolę dwóch pozostałych białek ustalono na podstawie obserwacji linii komórek z zahamowaną ich syntezą (linie komórek z jajnika chomika chińskiego: Lec15 z deficytem DPM2 i CHO2.38 z deficytem DPM3). Wszystkie trzy białka wpływają na aktywność katalityczną DPMS. DPM1 wiąże się bezpośrednio z DPM3, a poprzez DPM3 Rycina 3. Struktura syntazy mannozylofosfodolicholu (DPMS). DPMS zbudowana jest z 3 podjednostek: DPM1, DPM2, DPM3. Pierwsza z nich posiada aktywność katalityczną, podczas gdy dwie pozostałe odpowiednio: kotwiczą ją w błonie siateczki endoplazmatycznej (ER) DPM3 oraz ułatwiają wiązanie z Dol-P w przebiegu reakcji enzymatycznej DPM2. także pośrednio z DPM2. DPM2, tworząc specyficzne warunki przestrzenne, ułatwia wiązanie Dol-P, co podnosi wydajność DPMS, natomiast DPM3 stabilizuje kompleks DPMS w błonie RER. Jak zaobserwowano brak DPM3 powodował związanie DPM1 z białkiem CHIP, a tak wyznakowany kompleks przeznaczony był do degradacji w proteasomie [40]. Odpowiedzialne za aktywność katalityczną DPMS białko DPM1 jest kodowane przez gen strukturalny (determinujący pierwotną sekwencję aminokwasową tworzonego białka) Dpm1, po raz pierwszy wyizolowany i opisany u Saccharomyces cerevisiae [41]. Na przestrzeni lat odnaleziono analogiczne sekwencje w genomie przedstawicieli Protozoa, grzybów, a także w genomie mysim i ludzkim. Na podstawie różnic w strukturze, białka DMP1 dzieli się na dwie klasy, z których pierwszą charakteryzuje hydrofobowy region na C-końcu łańcucha (u S. cerevisiae, U. maydis, T. brucei, Leishmania mexicana), a druga jest go pozbawiona i dzięki temu pozostaje rozpuszczalna (u S. pombe, C. briggsiae, Trichoderma reesei i ludzi) [42]. Należące do pierwszej z klas, białko DMP1 jest zdolne do samodzielnego katalizowania syntezy Dol-P-Man, podczas gdy DMP1 pozbawione hydrofobowego regionu wymaga obecności dodatkowych elementów (DMP2 i DMP3) umożliwiających zakotwiczenie jej w błonie ER tak by mogła efektywniej oddziaływać z obecnym tam substratem reakcji, Dol-P. Obecnie za mechanizm katalityczny charakterystyczny dla DPMS uznaje się inwersję konfiguracji anomerycznej. DPM1, jako komponent katalityczny, wykorzystuje GDP-Man jako donor i Dol-P jako akceptor reszty Man w syntezie Dol-P-Man [40]. Symulacje in silico oraz analizy wykorzystujące zjawisko rezonansowego przeniesienia energii (FRET, ang. Förster Resonance Energy Transfer) pozwoliły stworzyć model struktury 3D DPMS, uwzględniający stopień i sposób sfałdowania białek oraz ukazujący lokalizację miejsca aktywnego i wyjaśniający mechanizm zachodzącej w nim katalizy [42]. Jak pokazano aktywność DPMS, a co za tym idzie dostępność LLO, jest regulowana poprzez zależny od PKA cykl fosforylacji/defosforylacji. Jest to zjawisko uniwersalne, gdyż zostało zaobserwowane u różnych organizmów (od grzybów po ssaki) [35-39,43]. W efekcie ufosforylowania enzymu ilość powstającego produktu była wyższa o 40 80% w przypadku komórek izolowanych ze ślinianek szczura [38], do nawet % u E. histolityca [43]. Ponieważ wyższa aktywność katalityczna enzymów może wynikać zarówno ze zwiększenia ilości białka syntezowanego de novo jak i aktywacji endogennego enzymu poprzez jego kowalencyjną modyfikację, konieczne było jednoznaczne wykazanie molekularnego mechanizmu odpowiadającego za aktywację DPMS. Badania aktywności DPMS prowadzono z wykorzystaniem izoproterenolu, agonisty receptorów β-adrenergicznych, będących typowymi GPCR. W hodowanych w obecności izoproterenolu komórkach ślinianek przyusznych szczurów [38] oraz komórkach śródbłonka naczyń włosowatych krowy [39] wykazano, że regulacja N- -glikozylacji zachodziła za pośrednictwem kaskady camp, której czynnikiem efektorowym była PKA prowadząca fosforylację docelowego enzymu. W efekcie obserwowano Postępy Biochemii 60 (3)
6 zarówno wzrost szybkości syntezy Dol-P-Man [38], jak i wynikający z niego wzrost ilości tworzonego produktu, biorącego później udział w syntezie LLO [39]. Ponadto w przypadku komórek śródbłonka zaobserwowano wzrost ilości włączanych w trakcie syntezy LLO reszt mannozy (wydłużanie Man 5 GlcNAc 2 -P-P-Dol do Man 9 GlcNAc 2 -P-P-Dol). Analogiczne obserwacje przeprowadzono w tych komórkach po ich inkubacji w obecności innych związków zwiększających wewnątrzkomórkowe stężenie camp takich jak: forskolina, toksyna cholery czy prostaglandyna E1 [39]. Otrzymane wyniki sugerują, że w efekcie wzrostu stężenia camp i aktywacji kaskady przekazu sygnału prowadzącej do aktywacji PKA następował wzrost syntezy LLO. Analiza puli N-glikanów w komórkach po stymulacji izoproterenolem potwierdziła ogólny wzrost ilości tych struktur. Pokazano także na przykładzie czynnika VIIIC, który jest glikoproteiną zaangażowaną w proces angiogenezy i stale obecną w komórkach śródbłonka naczyń włosowatych, iż stymulacja syntezy camp przez izoproterenol spowodowała wzrost ilości struktur oligosacharydowych włączonych w strukturę tego konkretnego białka [39]. W celu wyjaśnienia mechanizmu prowadzącego do wzmożonej produkcji N- -glikanów w komórkach, w których stymulowana była synteza camp wykluczono tezę iż wzrost aktywności DPMS jest wynikiem zwiększonej ekspresji genów dla jego podjednostek. Po dodaniu aktynomycyny (antybiotyku z grupy cytostatyków, blokującego syntezę DNA, RNA i białek) zwiększona na skutek działania izoproterenolu aktywność enzymu pozostawała nie zmieniona [44]. Hipotezę iż cząsteczki zdolne do zwiększania wewnątrzkomórkowego stężenia camp mogą regulować proces N- -glikozylacji białek na drodze fosforylacji/defosforylacji z udziałem PKA potwierdziły również wyniki inkubacji frakcji mikrosomalnych lub komórek w obecności czynników sprzyjających fosforylacji tj.: ATP oraz podjednostek katalitycznych PKA. W tym układzie in vitro na skutek fosforylacji białek obserwowano zwiększoną aktywność enzymatyczną DPMS we frakcjach mikrosomalnych izolowanych z komórek patogennego grzyba Candida albicans [35] oraz z komórek ślinianek przyusznych szczurów [38], a także wzrost aktywności rekombinowanego białka enzymatycznego z Saccharomyces cerevisiae [37]. Wykorzystując DMPS wyizolowany z komórek Saccharomyces cerevisiae określono również konsensusową sekwencję, która może ulegać fosforylacji, Tyr-Arg-Arg-Val-Ile-Ser. W obrębie cząsteczki DPMS pierwotnym miejscem fosforylacji przez PKA w odpowiedzi na sygnalizację indukowaną camp jest reszta Ser141, występująca w rejonie o strukturze podobnej do białka DPM1 [37]. Potwierdzeniem zaangażowania PKA w regulację procesu N-glikozylacji były wyniki badań na linii komórek wyizolowanych z jajników samic chomika chińskiego (linia CHO). Do komórek tych wprowadzono trzy różne mutacje hamujące ekspresję genu kodującego PKA, a grupę kontrolną stanowiły komórki o fenotypie dzikim (z prawidłową ekspresją genu kodującego PKA). W przypadku komórek z mutacjami warunkującymi deficyt PKA zaobserwowano obniżony stopień N-glikozylacji białek, po inkubacji komórek w obecności 8Br-cAMP indeks glikozylacji (stosunek włączonej 3 H-mannozy do 14 C-leucyny w strukturę glikoprotein) w przypadku komórek o fenotypie dzikim wyniósł 120%, przy zaledwie 7 23% dla komórek z mutacjami. Ponadto fosforylacja enzymu pochodzącego z komórek z mutacjami prowadzona w warunkach in vitro przez egzogenną PKA skutkowała przywróceniem aktywności katalitycznej w stopniu zbliżonym do tego obserwowanego w komórkach o fenotypie dzikim [36]. Obserwacje związane z wpływem camp na N-glikozylację prowadzono także na komórkach raka kosmówki (ang. choriocarcinoma) JEG-3 [45,46]. Komórki hodowane w obecności 8-bromo-cAMP wykazywały podwyższony poziom syntezy glikoprotein, ale efekt ten obserwowany był tylko przy wydłużonych czasach inkubacji. Sugerowało to, że mechanizmem odpowiedzialnym za ten efekt jest raczej wzmożona produkcja białek enzymatycznych zaangażowanych w przebieg procesów N-glikozylacji, a konkretnie w syntezę LLO, a nie ich fosforylacja [45]. Jak pokazano enzymem, którego aktywność była w tym wypadku regulowana przez wewnątrzkomórkowe stężenia camp jest cis- -prenyltransferaza. Katalizuje ona syntezę Dol-P poprzez przyłączenie reszt izopentynylowych do difosforanufarnezylu. W komórkach JEG-3 stymulowanych 8-bromo- -camp, wzrastała aktywność tego enzymu, co powodowało zwiększoną syntezę Dol-P, kluczowego substratu pierwszego etapu N-glikozylacji. Jak pokazano wzrost aktywności cis-prenyltransferazy, nie wynikał z fosforylacji białka enzymatycznego, lecz był efektem wzmożonej jego syntezy, wywołanej przez camp [46]. Regulacyjny wpływ camp został opisany także w stosunku do przebiegu O-glikozylacji, a konkretnie do procesu, w wyniku którego białka zostają zmodyfikowane poprzez dołączenie wiązaniem O-glikozydowym N-acetyloglukozoaminy (O-GlcNAc) do reszt Ser lub Thr w łańcuchu polipeptydowym [47-49]. Modyfikacji takiej podlegają głównie białka jądrowe oraz czynniki transkrypcyjne, w tym czynnik Sp1 [47] odpowiadający za aktywację genów transkrybowanych w każdej komórce [50]. Obserwacje wpływu kaskady camp na liczbę struktur O-GlcNAc związanych z białkami prowadzono w hodowlach mysich neuronów móżdżku [48] oraz w linii fibroblastów nerki szczura [47,49]. Jak stwierdzono aktywacja kaskady camp powodowała ogólne obniżenie liczby struktur O-GlcNAc związanych z białkami cytoszkieletu w przypadku neuronów móżdżku myszy [48] oraz prowadziła do częściowej lub całkowitej deglikozylacji białka Sp1 szczurzych fibroblastów [47]. W przypadku fibroblastów nasilenie efektu deglikozylacji obserwowano w hodowlach dodatkowo głodzonych (hodowanych przy braku glukozy). Elementem bezpośrednio regulowanym przez kaskadę była amidotransferaza glutamina:fruktozo-6-fosforan (ang. human glutamine:fructose-6-phosphate amidotransferase, hgfat) ludzka, enzym prowadzący reakcję syntezy glukozoaminy. Dodatkowo prowadzona przez PKA fosforylacja wyizolowanej aktywnej formy enzymu powodowała zahamowanie jego aktywności. Postulowany charakter oddziaływania kaskady camp na hgfat powoduje, że w sytuacji braku dostępnej glukozy głównym szlakiem regulującym jej przemiany jest tor heksozaminowy. W przypadku ograniczonej dostępności glukozy hormony działające poprzez kaskadę camp umożliwiają wykorzystanie istniejącej glukozy jako źródła energii, ograniczając wykorzystanie jej do syntezy glikoprotein [49]
7 PODSUMOWANIE Glikoproteiny pełnią kluczową rolę w przebiegu wielu procesów biologicznych, takich jak adhezja komórkowa, kierowanie białek do odpowiednich przedziałów komórkowych lub ich sekrecja, aktywacja receptorów, przekaz sygnałów czy endocytoza [5]. Co za tym idzie ich znaczenie dla utrzymania stanu fizjologicznego komórek oraz rola w stanach patologicznych jest niepodważalna. Wykazany w różnych układach badawczych, stymulujący wpływ wzrostu wewnątrzkomórkowego stężenia camp na syntezę LLO, realizowany poprzez aktywację syntazy mannozylofosfodolicholu na drodze jej fosforylacji zależnej od PKA oraz wywołanych sygnalizacją indukowaną przez camp zmian w syntezie cis-prenyltransferazy czy też wpływ fosforylacji przez PKA na prowadzoną przez hgfat syntezę glukozoaminy, sugeruje znaczący wpływ czynników humoralnych, będących ligandami receptorów sprzężonych z białkami G, na przebieg procesu N-glikozylacji, a także O-glikozylacji. Te obserwacje stanowią istotny krok ku zrozumieniu roli czynników wpływających na biosyntezę łańcuchów cukrowych na samym jej początku, a fizjologiczne i medyczne implikacje tego mechanizmu regulacji i jego rola w rozwoju chorób związanych z zaburzeniami glikozylacji powinny stać się przedmiotem przyszłych badań. Ponieważ dotychczasowe eksperymenty przeprowadzane były w większości metodami in vitro, na białkach enzymatycznych izolowanych z pojedynczych komórek, nie można jednoznacznie stwierdzić czy aktywacja kaskady camp (np. przez podanie agonistów receptorów β-adrenergicznych) w podobnym bądź równym stopniu podnosiłaby lub hamowała aktywność enzymu w warunkach in vivo. Niezbędne są zatem dodatkowe badania z wykorzystaniem żywych organizmów, które jednoznacznie potwierdziłyby założenie, że cykl fosforylacji/defosforylacji w znaczący sposób reguluje aktywność DPMS i cis-prenyltransferazy (i w efekcie syntezę LLO w procesie N-glikozylacji) [35-46] czy hgfat [47-48] w warunkach przyżyciowych. Co istotne, wyniki opisanych badań sugerują, że kaskada camp może być uniwersalnym mechanizmem regulującym proces glikozylacji białek także w innych tkankach organizmów zwierzęcych niż te, z których pochodziły wykorzystane do badań komórki, np. DPMS znajduje się bowiem w komórkach narządów nawet tak odmiennych, jak jajowód kury i mózg krowy [39]. Warto zaznaczyć, że przedmiotem badań były tylko wybrane enzymy z początkowych etapów procesów N- i O-glikozylacji, dlatego potencjalnie interesującym kierunkiem badawczym wydaje się być analiza możliwości regulacji tych procesów na innych etapach (wpływ kaskady camp na inne glikozylotransferazy). Interesujące byłoby także zbadanie regulacyjnego wpływu kaskady camp na przebieg pozostałych, znanych procesów glikozylacji. PIŚMIENNICTWO 1. Spiro RG (2002) Protein glycosylation: Nature, distribution, enzymatic formation, disease implications of glycopeptide bonds. Glycobiology 12: Ryšlava H, Doubnerova V, Kavan D, Vanĕk O (2013) Effect of posttranslational modifications on enzyme function and assembly. J Proteomics 91: Przybyło M (1998) Budowa i synteza łańcuchów cukrowych glikoprotein. Kosmos 47: Mariño K, Bones J, Kattla JJ, Rudd PM (2010) A systematic approach to protein glycosylation analysis: a path through the maze. Nat Chem Biol 6: Ohtsubo K, Marth JD (2006) Glycosylation in cellular mechanisms of health and disease. Cell 126: Jimenez del Val I, Kyriakopoulos S, Polizzi KM, Kontoravdi C (2013) An optimized method for extraction and quantification of nucleotides and nucleotide sugars from mammalian cells. Anal Biochem 443: Breton C, Fournel-Gigleux S, Palcic MM (2012) Recent structures, evolution and mechanisms of glycosyltransferases. Curr Opin Struct Biol 22: Czlapinski JL, Bertozzi CR (2006) Synthetic glycobiology: exploits in the Golgi compartment. Curr Opin Chem Biol 10: Opat AS, van Vilet C, Gleeson PA (2001) Trafficking and localization of resident Golgi glycosylation enzymes. Biochimie 83: Banerjee DK (2012) N-glycans in cell survival and death: Cross-talk between glycosyltransferases. Biochim Biophys Acta 1820: Haeuptle MA, Hülsmeier AJ, Hennet T (2009) HPLC and mass spectrometry analysis of dolichol-phosphates at the cell culture scale. Anal Biochem 396: Hartley MD, Imperiali B (2012) At the membrane frontier: A prospectus on the remarkable evolutionary conservation of polyprenols and polyprenyl-phosphates. Arch Biochem Biophys 517: Burda P, Aebi M (1999) The dolichol pathway of N-linked glycosylation. Biochim Biophys Acta 1426: Schwarz F, Aebi M (2011) Mechanism and principles of N-linked protein glycosylation. Curr Opin Struci Biol 21: Aebi M (2013) N-linked protein glycosylation in the ER. Biochim Biophys Acta 1833: Trombetta ES (2003) The contribution of N-glycans and their processing in the endoplasmic reticulum to glycoprotein biosyntheis. Glycobiology 13: 77R-91R 17. Przybyło M (1999) Czynniki wpływające na proces biosyntezy N-glikanów w glikoproteinach. Kosmos 48: Sutherland EW, Rall TW (1958) Fractionation and characterization of cyclic ribonucleotide formed by tissue particles. J Biol Chem 232: Sutherland EW, Robinson GA, Butcher RW (1968) Some Aspects of the Biological Role of Adenosine 3,5 -monophosphate (Cyclic AMP). Circulation 37: Antoni FA (2012) New paradigms in camp signalling. Mol Cell Endocrinol 353: Cooper DM (2003) Regulation and organization of adenylyl cyclases and camp. Biochem J 375: Linder JU, Schultz JE (2008) Versatility of signal transduction encoded in dimeric adenylyl cyclases. Curr Opin Struct Biol 18: Antoni FA (2000) Molecular diversity od cyclic AMP signalling. Front Endocriniol 21: Bender AT, Beavo JA (2006) Cyclic nucleotide phosphodiesterases: molecular regulation to clinical use. Pharmacol Rev 58: Essayan DM (2001) Cyclic nucleotide phosphodiesterases. J Allergy Clin Immunol 108: Heng BC, Aubel D, Fussenegger M (2013) An overview of the diverse roles of G-protein coupled receptors (GPCRs) in the pathophysiology of various human diseases. Biotechnol Adv 31: Ward RJ, Milligan G (2014) Structural and biophysical characterisation of G protein-coupled receptor ligand binding using resonance energy transfer and fluorescent labelling techniques. Biochim Biophys Acta 1838: Vázquez-Prado J, Casas-González P, García-Sáinz JA (2003) G protein coupled receptor cross-talk: pivotal roles of protein phosphorylation and protein-protein interactions. Cell Signal 15: Cotton M, Claing A (2009) G protein-coupled receptors stimulation and the control of cell migration. Cell Signal 21: Postępy Biochemii 60 (3)
8 30. Wettschureck N, Offermans S (2005) Mammalian G proteins and their cell type specific functions. Physiol Rev 85: Hurley JH (1999) Structure, mechanism, and regulation of mammalian adenylyl cyclases. J Biol Chem 274: Bos JL (2006) Epac proteins: multi-purpose camp targets. Trends Biochem Sci 31: Sassone-Corsi P (2012) The Cyclic AMP Pathway. Cold Spring Harb Perspect Biol 4: Taylor SS, Kim C, Cheng CY, Brown SHJ, Wu J, Kannan N (2008) Signaling through camp and camp-dependent protein kinase: Diverse strategies for drug design. Biochim Biophys Acta 1784: Arroyo-Flores BL, Calvo-Méndez C, Flores-Carreón A, López-Romero E (2005) Biosynthesis of glycoproteins in the pathogenic fungus Candida albicans: Activation of dolichol phosphate mannose synthase by camp-mediated protein phosphorylation. FEMS Immunol Med Microbiol 45: Banerjee DK, Aponte E, Dasilva JJ (2004) Low expression of lipid-linked oligosaccharide due to a functionally altered Dol-P-Man synthase reduces protein Glycosylation in camp-dependent protein kinase deficient Chinase hamster ovary cells. Glycoconj J 21: Banerjee DK, Carrasquillo EA, Hughey P, Schutzbach JS, Martínez JA, Baksi K (2005) In Vitro Phosphorylation by camp-dependent Protein Kinase Up-regulates recombinant Saccharomyces cerevisiae Mannosylphosphodolichol Synthase. J Biol Chem 280: Banerjee DK, Kousvelari EE, Baum BJ (1987) camp-mediated protein phosphorylation of microsomal membranes increases mannosylphospodolichol synthase activity. Proc Natl Acad Sci USA 84: Martínez JA, Tavárez JJ, Oliveira CM, Banerjee DK (2006) Potentation of angiogenic switch in capillary endothelial cells by camp: A crosstalk between up-regulated LLO biosynthesis and the HSP-70 expression. Glycoconj J 23: Maeda Y, Kinoshita T (2008) Dolicholphosphate mannose synthase: Structure, function and regulation. Biochim Biophys Acta 1780: Orlean P, Albright CH, Robbins PW (1988) Cloning and sequencing of the least gene for dolichol phosphate mannose synthase, an essentials protein. J Biol Chem 263: Lamani E, Mewbourne RB, Fletcher DS, Maltsev SD, Danilov LL, Veselovsky VV, Lozanova AV, Grigorieva NY, Pinsker OA, Xing J, Forsee WT, Cheung HC, Schutzbach JS, Shibaev VN, Jedrzejas MJ (2006) Structural studies and mechanism of Saccharomyces cerevisiae dolichol-phosphate-mannose synthase: insights into the initial step of synthesis of dolichylphosphate-linked oligosaccharide chains in membranes of endoplasmic retikulum. Glycobiology 16: Villagómez-Castro JC, Calvo-Méndez C, Flores-Carreón A, López-Romero E (2000) Partial purification and characterization of dolichol phosphate mannose synthase from Entameba histolytica. Glycobiology 10: Baksi K, Tavárez-Pagán JJ, Martínez JA, Benerjee DK (2008) Unique structural motif supports mannosylphosphodolichol synthase: an important angiogenesis regulator. Curr Drug Targets 9: Konrad M, Merz WE (1994) Regulation of N-glycosylation. Long-term effect of cyclic AMP mediates enhances synthesis of the dolichol pyrophosphate core oligosaccharide. J Biol Chem 269: Konrad M, Merz WE (1996) Long-term effect of cyclic AMP on N-glycosylation is caused by an increase in the activity of the cis-prenyltransferase. Biochem J 316: Chang Q, Su K, Baker JR, Yang X, Patterson AJ, Kudlow JE (2004) Phosphorylation of human glutamine-fructose-6-phosphate amidotransferase by camp-dependent protein kinase at serine 205 blocks the enzyme activity. J Biol Chem 275: Griffith LS, Schmitz B (1999) O-linked N-acetyloglucosamine levels in cerebellar neurons respond reciprocally to perturbations of phoshorylation. Eur J Biochem 262: Han I, Kudlow JE (1997) Reduced O-glycosylation of Sp-1 is associated with increased proteasome susceptibility. Mol Cell Biol 17: Czyż M (2001) Sp1 transcription factor. Postepy Biochem 47: 10-8 camp cascade in regulation of protein glycosylation Magdalena Surman, Marcelina Janik * Department of Glycoconjgate Biochemistry, Institute of Zoology, Jagiellonian University, 9 Gronostajowa St., Kraków, Poland * marcelina.janik@uj.edu.pl Key words: glycosylation, camp cascade, dolichol phosphate mannose synthase, G proteins, adenylyl cyclase ABSTRACT O- and N-glycosylation are the most common and complex of the post-translational modifications. Both are enzymatic processes and it was suggested that both could be regulated by camp cascade at the early stages. N-glycosylation starts with the formation of lipid-linked oligosaccharides and this process is catalysed by crucial glycosyltransferase dolichol phosphate mannose synthase. The results of several studies strongly suggest that the camp acting through a camp-dependent protein kinase A-mediated protein phosphorylation/dephosphorylation cycle may modulate activation of this enzyme. It was shown that camp can also up regulate another enzyme involved in phosphodolichole synthesis cis-prenyltransferase. The mechanism acting here is the alteration of the rate of its gene expression. camp cascade is also involved in regulation of O-glycosylation since phosphorylation of human glutamine:fructose-6-phosphate amidotransferase results in depletion of O-GlcNAc structure formation. These observation suggested an important role of GPCRs and their ligand in regulation of N- and O-glycan synthesis
Nukleotydy w układach biologicznych
 Nukleotydy w układach biologicznych Schemat 1. Dinukleotyd nikotynoamidoadeninowy Schemat 2. Dinukleotyd NADP + Dinukleotydy NAD +, NADP + i FAD uczestniczą w procesach biochemicznych, w trakcie których
Nukleotydy w układach biologicznych Schemat 1. Dinukleotyd nikotynoamidoadeninowy Schemat 2. Dinukleotyd NADP + Dinukleotydy NAD +, NADP + i FAD uczestniczą w procesach biochemicznych, w trakcie których
MECHANIZMY WZROSTU i ROZWOJU ROŚLIN
 MECHANIZMY WZROSTU i ROZWOJU ROŚLIN Jaka jest rola kinaz MA (generalnie)? Do czego służy roślinom (lub generalnie) fosfolipaza D? Czy u roślin występują hormony peptydowe? Wymień znane Ci rodzaje receptorów
MECHANIZMY WZROSTU i ROZWOJU ROŚLIN Jaka jest rola kinaz MA (generalnie)? Do czego służy roślinom (lub generalnie) fosfolipaza D? Czy u roślin występują hormony peptydowe? Wymień znane Ci rodzaje receptorów
Wykład 14 Biosynteza białek
 BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
Chemiczne składniki komórek
 Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Dr. habil. Anna Salek International Bio-Consulting 1 Germany
 1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER)
 Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
ROLA WAPNIA W FIZJOLOGII KOMÓRKI
 ROLA WAPNIA W FIZJOLOGII KOMÓRKI Michał M. Dyzma PLAN REFERATU Historia badań nad wapniem Domeny białek wiążące wapń Homeostaza wapniowa w komórce Komórkowe rezerwuary wapnia Białka buforujące Pompy wapniowe
ROLA WAPNIA W FIZJOLOGII KOMÓRKI Michał M. Dyzma PLAN REFERATU Historia badań nad wapniem Domeny białek wiążące wapń Homeostaza wapniowa w komórce Komórkowe rezerwuary wapnia Białka buforujące Pompy wapniowe
TRANSKRYPCJA - I etap ekspresji genów
 Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
TATA box. Enhancery. CGCG ekson intron ekson intron ekson CZĘŚĆ KODUJĄCA GENU TERMINATOR. Elementy regulatorowe
 Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
Nowoczesne systemy ekspresji genów
 Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER
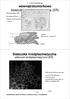 Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Profil metaboliczny róŝnych organów ciała
 Profil metaboliczny róŝnych organów ciała Uwaga: tkanka tłuszczowa (adipose tissue) NIE wykorzystuje glicerolu do biosyntezy triacylogliceroli Endo-, para-, i autokrynna droga przekazu informacji biologicznej.
Profil metaboliczny róŝnych organów ciała Uwaga: tkanka tłuszczowa (adipose tissue) NIE wykorzystuje glicerolu do biosyntezy triacylogliceroli Endo-, para-, i autokrynna droga przekazu informacji biologicznej.
Transport przez błony
 Transport przez błony Transport bierny Nie wymaga nakładu energii Transport aktywny Wymaga nakładu energii Dyfuzja prosta Dyfuzja ułatwiona Przenośniki Kanały jonowe Transport przez pory w błonie jądrowej
Transport przez błony Transport bierny Nie wymaga nakładu energii Transport aktywny Wymaga nakładu energii Dyfuzja prosta Dyfuzja ułatwiona Przenośniki Kanały jonowe Transport przez pory w błonie jądrowej
października 2013: Elementarz biologii molekularnej. Wykład nr 2 BIOINFORMATYKA rok II
 10 października 2013: Elementarz biologii molekularnej www.bioalgorithms.info Wykład nr 2 BIOINFORMATYKA rok II Komórka: strukturalna i funkcjonalne jednostka organizmu żywego Jądro komórkowe: chroniona
10 października 2013: Elementarz biologii molekularnej www.bioalgorithms.info Wykład nr 2 BIOINFORMATYKA rok II Komórka: strukturalna i funkcjonalne jednostka organizmu żywego Jądro komórkowe: chroniona
Przemiana materii i energii - Biologia.net.pl
 Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Przedziały komórkowe siateczka endoplazmatyczna (ER)
 Przedziały komórkowe siateczka endoplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum endoplazmatyczne
Przedziały komórkowe siateczka endoplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum endoplazmatyczne
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 5 Droga od genu do
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 5 Droga od genu do
Bliskie spotkania z biologią METABOLIZM. dr hab. Joanna Moraczewska, prof. UKW. Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki
 Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER)
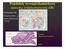 Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
Przedziały wewnątrzkomórkowe siateczka śródplazmatyczna (ER) Pochodzenie ER inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum
THE UNFOLDED PROTEIN RESPONSE
 THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
Translacja i proteom komórki
 Translacja i proteom komórki 1. Kod genetyczny 2. Budowa rybosomów 3. Inicjacja translacji 4. Elongacja translacji 5. Terminacja translacji 6. Potranslacyjne zmiany polipeptydów 7. Translacja a retikulum
Translacja i proteom komórki 1. Kod genetyczny 2. Budowa rybosomów 3. Inicjacja translacji 4. Elongacja translacji 5. Terminacja translacji 6. Potranslacyjne zmiany polipeptydów 7. Translacja a retikulum
The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna
 Streszczenie rozprawy doktorskiej pt. The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna mgr Tomasz Turowski, promotor prof. dr hab.
Streszczenie rozprawy doktorskiej pt. The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna mgr Tomasz Turowski, promotor prof. dr hab.
Joanna Bereta, Aleksander Ko j Zarys biochemii. Seria Wydawnicza Wydziału Bio chemii, Biofizyki i Biotechnologii Uniwersytetu Jagiellońskiego
 Joanna Bereta, Aleksander Ko j Zarys biochemii Seria Wydawnicza Wydziału Bio chemii, Biofizyki i Biotechnologii Uniwersytetu Jagiellońskiego Copyright by Wydział Bio chemii, Biofizyki i Biotechnologii
Joanna Bereta, Aleksander Ko j Zarys biochemii Seria Wydawnicza Wydziału Bio chemii, Biofizyki i Biotechnologii Uniwersytetu Jagiellońskiego Copyright by Wydział Bio chemii, Biofizyki i Biotechnologii
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
Przegląd budowy i funkcji białek
 Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Przegląd budowy i funkcji białek Co piszą o białkach? Wyraz wprowadzony przez Jönsa J. Berzeliusa w 1883 r. w celu podkreślenia znaczenia tej grupy związków. Termin pochodzi od greckiego słowa proteios,
Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl
 Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl Wszelkie treści i zasoby edukacyjne publikowane na łamach Portalu www.szkolnictwo.pl mogą byd wykorzystywane przez jego Użytkowników
Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl Wszelkie treści i zasoby edukacyjne publikowane na łamach Portalu www.szkolnictwo.pl mogą byd wykorzystywane przez jego Użytkowników
Przedziały komórkowe siateczka endoplazmatyczna (ER)
 Pochodzenie ER Przedziały komórkowe siateczka endoplazmatyczna (ER) inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum endoplazmatyczne
Pochodzenie ER Przedziały komórkowe siateczka endoplazmatyczna (ER) inwaginacja błony - (kanały trnslokacyjne) i rozrost cysterny spłaszczone woreczki tubule Siateczka śródplazmatyczna retikulum endoplazmatyczne
CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A. imię i nazwisko :. klasa :.. ilość punktów :.
 CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A imię i nazwisko :. klasa :.. ilość punktów :. Zadanie 1 Przeanalizuj schemat i wykonaj polecenia. a. Wymień cztery struktury występujące zarówno w komórce roślinnej,
CORAZ BLIŻEJ ISTOTY ŻYCIA WERSJA A imię i nazwisko :. klasa :.. ilość punktów :. Zadanie 1 Przeanalizuj schemat i wykonaj polecenia. a. Wymień cztery struktury występujące zarówno w komórce roślinnej,
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Informacje. W sprawach organizacyjnych Slajdy z wykładów
 Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Biochemia Informacje W sprawach organizacyjnych malgorzata.dutkiewicz@wum.edu.pl Slajdy z wykładów www.takao.pl W sprawach merytorycznych Takao Ishikawa (takao@biol.uw.edu.pl) Kiedy? Co? Kto? 24 lutego
Spis treści. 1. Wiadomości wstępne Skład chemiczny i funkcje komórki Przedmowa do wydania czternastego... 13
 Przedmowa do wydania czternastego... 13 Częściej stosowane skróty... 15 1. Wiadomości wstępne... 19 1.1. Rys historyczny i pojęcia podstawowe... 19 1.2. Znaczenie biochemii w naukach rolniczych... 22 2.
Przedmowa do wydania czternastego... 13 Częściej stosowane skróty... 15 1. Wiadomości wstępne... 19 1.1. Rys historyczny i pojęcia podstawowe... 19 1.2. Znaczenie biochemii w naukach rolniczych... 22 2.
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem informacji odebranej przez komórkę. Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Receptor cząsteczka chemiczna ( peptyd
Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem informacji odebranej przez komórkę. Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Receptor cząsteczka chemiczna ( peptyd
Nośnikiem informacji genetycznej są bardzo długie cząsteczki DNA, w których jest ona zakodowana w liniowej sekwencji nukleotydów A, T, G i C
 MATERIAŁ GENETYCZNY KOMÓRKI BIOSYNTEZA BIAŁEK MATERIAŁ GENETYCZNY KOMÓRKI Informacja genetyczna - instrukcje kierujące wszystkimi funkcjami komórki lub organizmu zapisane jako określone, swoiste sekwencje
MATERIAŁ GENETYCZNY KOMÓRKI BIOSYNTEZA BIAŁEK MATERIAŁ GENETYCZNY KOMÓRKI Informacja genetyczna - instrukcje kierujące wszystkimi funkcjami komórki lub organizmu zapisane jako określone, swoiste sekwencje
Część V: Przekazywanie sygnałów. DO WYKŁADÓW Z PODSTAW BIOFIZYKI IIIr. Biotechnologii prof. dr hab. inż. Jan Mazerski
 MATERIAŁY PMCNICZE D WYKŁADÓW Z PDSTAW BIFIZYKI IIIr. Biotechnologii prof. dr hab. inż. Jan Mazerski PRZEKAZYWANIE SYGNAŁÓW Cechą charakterystyczną układów żywych jest zdolność do zachowywania wewnętrznej
MATERIAŁY PMCNICZE D WYKŁADÓW Z PDSTAW BIFIZYKI IIIr. Biotechnologii prof. dr hab. inż. Jan Mazerski PRZEKAZYWANIE SYGNAŁÓW Cechą charakterystyczną układów żywych jest zdolność do zachowywania wewnętrznej
Bioinformatyka wykład 9
 Bioinformatyka wykład 9 14.XII.21 białkowa bioinformatyka strukturalna krzysztof_pawlowski@sggw.pl 211-1-17 1 Plan wykładu struktury białek dlaczego? struktury białek geometria i fizyka modyfikacje kowalencyjne
Bioinformatyka wykład 9 14.XII.21 białkowa bioinformatyka strukturalna krzysztof_pawlowski@sggw.pl 211-1-17 1 Plan wykładu struktury białek dlaczego? struktury białek geometria i fizyka modyfikacje kowalencyjne
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa
 Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Sygnalizacja międzykomórkowa i wewnątrzkomórkowa Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Informator (przekaźnik) pierwotny czynnik fizyczny lub chemiczny będący nośnikiem
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Organizacja tkanek - narządy
 Organizacja tkanek - narządy Architektura skóry tkanki kręgowców zbiór wielu typów komórek danej tkanki i spoza tej tkanki (wnikają podczas rozwoju lub stale, w trakcie Ŝycia ) neurony komórki glejowe,
Organizacja tkanek - narządy Architektura skóry tkanki kręgowców zbiór wielu typów komórek danej tkanki i spoza tej tkanki (wnikają podczas rozwoju lub stale, w trakcie Ŝycia ) neurony komórki glejowe,
WYKŁAD: Klasyczny przepływ informacji ( Dogmat) Klasyczny przepływ informacji. Ekspresja genów realizacja informacji zawartej w genach
 WYKŁAD: Ekspresja genów realizacja informacji zawartej w genach Prof. hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Klasyczny przepływ informacji ( Dogmat) Białka Retrowirusy Białka Klasyczny
WYKŁAD: Ekspresja genów realizacja informacji zawartej w genach Prof. hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Klasyczny przepływ informacji ( Dogmat) Białka Retrowirusy Białka Klasyczny
SEMINARIUM 8:
 SEMINARIUM 8: 24.11. 2016 Mikroelementy i pierwiastki śladowe, definicje, udział w metabolizmie ustroju reakcje biochemiczne zależne od aktywacji/inhibicji przy udziale mikroelementów i pierwiastków śladowych,
SEMINARIUM 8: 24.11. 2016 Mikroelementy i pierwiastki śladowe, definicje, udział w metabolizmie ustroju reakcje biochemiczne zależne od aktywacji/inhibicji przy udziale mikroelementów i pierwiastków śladowych,
Zawartość. Wstęp 1. Historia wirusologii. 2. Klasyfikacja wirusów
 Zawartość 139585 Wstęp 1. Historia wirusologii 2. Klasyfikacja wirusów 3. Struktura cząstek wirusowych 3.1. Metody określania struktury cząstek wirusowych 3.2. Budowa cząstek wirusowych o strukturze helikalnej
Zawartość 139585 Wstęp 1. Historia wirusologii 2. Klasyfikacja wirusów 3. Struktura cząstek wirusowych 3.1. Metody określania struktury cząstek wirusowych 3.2. Budowa cząstek wirusowych o strukturze helikalnej
Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko. Syllabus przedmiotowy 2016/ /2019
 Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko Syllabus przedmiotowy 2016/2017-2018/2019 Wydział Fizjoterapii Kierunek studiów Fizjoterapia Specjalność ----------- Forma studiów Stacjonarne / Niestacjonarne
Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko Syllabus przedmiotowy 2016/2017-2018/2019 Wydział Fizjoterapii Kierunek studiów Fizjoterapia Specjalność ----------- Forma studiów Stacjonarne / Niestacjonarne
Regulacja Ekspresji Genów
 Regulacja Ekspresji Genów Wprowadzenie o Ekspresja genu jest to złożony proces jego transkrypcji do mrna, o Obróbki tego mrna, a następnie o Translacji do białka. 4/17/2019 2 4/17/2019 3 E 1 GEN 3 Promotor
Regulacja Ekspresji Genów Wprowadzenie o Ekspresja genu jest to złożony proces jego transkrypcji do mrna, o Obróbki tego mrna, a następnie o Translacji do białka. 4/17/2019 2 4/17/2019 3 E 1 GEN 3 Promotor
ROZPORZĄDZENIE KOMISJI (UE) / z dnia r.
 KOMISJA EUROPEJSKA Bruksela, dnia 29.5.2018 C(2018) 3193 final ROZPORZĄDZENIE KOMISJI (UE) / z dnia 29.5.2018 r. zmieniające rozporządzenie (WE) nr 847/2000 w odniesieniu do definicji pojęcia podobnego
KOMISJA EUROPEJSKA Bruksela, dnia 29.5.2018 C(2018) 3193 final ROZPORZĄDZENIE KOMISJI (UE) / z dnia 29.5.2018 r. zmieniające rozporządzenie (WE) nr 847/2000 w odniesieniu do definicji pojęcia podobnego
Transport makrocząsteczek
 Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii
 Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii 1. Technologia rekombinowanego DNA jest podstawą uzyskiwania genetycznie zmodyfikowanych organizmów 2. Medycyna i ochrona zdrowia
Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii 1. Technologia rekombinowanego DNA jest podstawą uzyskiwania genetycznie zmodyfikowanych organizmów 2. Medycyna i ochrona zdrowia
Badanie oddziaływań związków biologicznie aktywnych z modelowymi membranami lipidowymi
 UNIWERSYTET JAGIELLOŃSKI W KRAKOWIE WYDZIAŁ CHEMII STRESZCZENIE ROZPRAWY DOKTORSKIEJ Badanie oddziaływań związków biologicznie aktywnych z modelowymi membranami lipidowymi Marcelina Gorczyca Promotorzy:
UNIWERSYTET JAGIELLOŃSKI W KRAKOWIE WYDZIAŁ CHEMII STRESZCZENIE ROZPRAWY DOKTORSKIEJ Badanie oddziaływań związków biologicznie aktywnych z modelowymi membranami lipidowymi Marcelina Gorczyca Promotorzy:
Substancje o Znaczeniu Biologicznym
 Substancje o Znaczeniu Biologicznym Tłuszcze Jadalne są to tłuszcze, które może spożywać człowiek. Stanowią ważny, wysokoenergetyczny składnik diety. Z chemicznego punktu widzenia głównym składnikiem tłuszczów
Substancje o Znaczeniu Biologicznym Tłuszcze Jadalne są to tłuszcze, które może spożywać człowiek. Stanowią ważny, wysokoenergetyczny składnik diety. Z chemicznego punktu widzenia głównym składnikiem tłuszczów
DNA musi współdziałać z białkami!
 DNA musi współdziałać z białkami! Specyficzność oddziaływań między DNA a białkami wiążącymi DNA zależy od: zmian konformacyjnych wzdłuż cząsteczki DNA zróżnicowania struktury DNA wynikającego z sekwencji
DNA musi współdziałać z białkami! Specyficzność oddziaływań między DNA a białkami wiążącymi DNA zależy od: zmian konformacyjnych wzdłuż cząsteczki DNA zróżnicowania struktury DNA wynikającego z sekwencji
Komórka eukariotyczna
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Tematy- Biologia zakres rozszerzony, klasa 2TA,2TŻ-1, 2TŻ-2
 Tematy- Biologia zakres rozszerzony, klasa 2TA,2TŻ-1, 2TŻ-2 Nr lekcji Temat Zakres treści 1 Zapoznanie z PSO, wymaganiami edukacyjnymi i podstawą programową PSO, wymagania edukacyjne i podstawa programowa
Tematy- Biologia zakres rozszerzony, klasa 2TA,2TŻ-1, 2TŻ-2 Nr lekcji Temat Zakres treści 1 Zapoznanie z PSO, wymaganiami edukacyjnymi i podstawą programową PSO, wymagania edukacyjne i podstawa programowa
WYNALAZKI BIOTECHNOLOGICZNE W POLSCE. Ewa Waszkowska ekspert UPRP
 WYNALAZKI BIOTECHNOLOGICZNE W POLSCE Ewa Waszkowska ekspert UPRP Źródła informacji w biotechnologii projekt SLING Warszawa, 9-10.12.2010 PLAN WYSTĄPIENIA Umocowania prawne Wynalazki biotechnologiczne Statystyka
WYNALAZKI BIOTECHNOLOGICZNE W POLSCE Ewa Waszkowska ekspert UPRP Źródła informacji w biotechnologii projekt SLING Warszawa, 9-10.12.2010 PLAN WYSTĄPIENIA Umocowania prawne Wynalazki biotechnologiczne Statystyka
Priony. co dobrego mówią nam drożdże? Takao Ishikawa Zakład Biologii Molekularnej Uniwersytet Warszawski
 Priony co dobrego mówią nam drożdże? Takao Ishikawa Zakład Biologii Molekularnej Uniwersytet Warszawski Choroba Kreutzfeldta-Jakoba Pierwsze opisy pochodzą z lat 30. XX wieku Zakaźna choroba, często rodzinna
Priony co dobrego mówią nam drożdże? Takao Ishikawa Zakład Biologii Molekularnej Uniwersytet Warszawski Choroba Kreutzfeldta-Jakoba Pierwsze opisy pochodzą z lat 30. XX wieku Zakaźna choroba, często rodzinna
Bliskie spotkania z biologią. METABOLIZM część II. dr hab. Joanna Moraczewska, prof. UKW
 Bliskie spotkania z biologią METABOLIZM część II dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki METABOLIZM KATABOLIZM - rozkład związków chemicznych
Bliskie spotkania z biologią METABOLIZM część II dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki METABOLIZM KATABOLIZM - rozkład związków chemicznych
Ocena ekspresji genów proangiogennych w komórkach nowotworowych OVP-10 oraz transfektantach OVP-10/SHH i OVP-10/VEGF
 Agnieszka Gładysz Ocena ekspresji genów proangiogennych w komórkach nowotworowych OVP-10 oraz transfektantach OVP-10/SHH i OVP-10/VEGF Katedra i Zakład Biochemii i Chemii Klinicznej Akademia Medyczna Prof.
Agnieszka Gładysz Ocena ekspresji genów proangiogennych w komórkach nowotworowych OVP-10 oraz transfektantach OVP-10/SHH i OVP-10/VEGF Katedra i Zakład Biochemii i Chemii Klinicznej Akademia Medyczna Prof.
Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych. źródło: (3)
 Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych źródło: (3) Interakcje białko-białko Ze względu na zadanie: strukturalne lub funkcjonalne. Ze względu na właściwości fizyczne: stałe lub
Kamila Muraszkowska Znaczenie wąskich gardeł w sieciach białkowych źródło: (3) Interakcje białko-białko Ze względu na zadanie: strukturalne lub funkcjonalne. Ze względu na właściwości fizyczne: stałe lub
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 4 Jak działają geny?
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 4 Jak działają geny?
INICJACJA ELONGACJA TERMINACJA
 INICJACJA ELONGACJA TERMINACJA 2007 by National Academy of Sciences Kornberg R D PNAS 2007;104:12955-12961 Struktura chromatyny pozwala na różny sposób odczytania informacji zawartej w DNA. Możliwe staje
INICJACJA ELONGACJA TERMINACJA 2007 by National Academy of Sciences Kornberg R D PNAS 2007;104:12955-12961 Struktura chromatyny pozwala na różny sposób odczytania informacji zawartej w DNA. Możliwe staje
Geny i działania na nich
 Metody bioinformatyki Geny i działania na nich prof. dr hab. Jan Mulawka Trzy królestwa w biologii Prokaryota organizmy, których komórki nie zawierają jądra, np. bakterie Eukaryota - organizmy, których
Metody bioinformatyki Geny i działania na nich prof. dr hab. Jan Mulawka Trzy królestwa w biologii Prokaryota organizmy, których komórki nie zawierają jądra, np. bakterie Eukaryota - organizmy, których
Źródła energii dla mięśni. mgr. Joanna Misiorowska
 Źródła energii dla mięśni mgr. Joanna Misiorowska Skąd ta energia? Skurcz włókna mięśniowego wymaga nakładu energii w postaci ATP W zależności od czasu pracy mięśni, ATP może być uzyskiwany z różnych źródeł
Źródła energii dla mięśni mgr. Joanna Misiorowska Skąd ta energia? Skurcz włókna mięśniowego wymaga nakładu energii w postaci ATP W zależności od czasu pracy mięśni, ATP może być uzyskiwany z różnych źródeł
Właściwości błony komórkowej
 płynność asymetria Właściwości błony komórkowej selektywna przepuszczalność Płynność i stan fazowy - ruchy rotacyjne: obrotowe wokół długiej osi cząsteczki - ruchy fleksyjne zginanie łańcucha alifatycznego
płynność asymetria Właściwości błony komórkowej selektywna przepuszczalność Płynność i stan fazowy - ruchy rotacyjne: obrotowe wokół długiej osi cząsteczki - ruchy fleksyjne zginanie łańcucha alifatycznego
OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011
 OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011 DLACZEGO DOROSŁY CZŁOWIEK (O STAŁEJ MASIE BIAŁKOWEJ CIAŁA) MUSI SPOŻYWAĆ BIAŁKO? NIEUSTAJĄCA WYMIANA BIAŁEK
OPTYMALNY POZIOM SPOŻYCIA BIAŁKA ZALECANY CZŁOWIEKOWI JANUSZ KELLER STUDIUM PODYPLOMOWE 2011 DLACZEGO DOROSŁY CZŁOWIEK (O STAŁEJ MASIE BIAŁKOWEJ CIAŁA) MUSI SPOŻYWAĆ BIAŁKO? NIEUSTAJĄCA WYMIANA BIAŁEK
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA
 SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
(przekaźniki II-go rzędu)
 (przekaźniki II-go rzędu) Gabriel Nowak, Małgorzata Dybała Receptory i mechanizmy przekazywania sygnału (J.Z. Nowak, J.B. Zawilska, red.) Wyd. Nauk. PWN, Warszawa, 2004 Zakład Cytobiologii i Histochemii,
(przekaźniki II-go rzędu) Gabriel Nowak, Małgorzata Dybała Receptory i mechanizmy przekazywania sygnału (J.Z. Nowak, J.B. Zawilska, red.) Wyd. Nauk. PWN, Warszawa, 2004 Zakład Cytobiologii i Histochemii,
Temat: Komórka jako podstawowa jednostka strukturalna i funkcjonalna organizmu utrwalenie wiadomości.
 SCENARIUSZ LEKCJI BIOLOGII DLA KLASY I GIMNAZJUM Temat: Komórka jako podstawowa jednostka strukturalna i funkcjonalna organizmu utrwalenie wiadomości. Cele: Utrwalenie pojęć związanych z budową komórki;
SCENARIUSZ LEKCJI BIOLOGII DLA KLASY I GIMNAZJUM Temat: Komórka jako podstawowa jednostka strukturalna i funkcjonalna organizmu utrwalenie wiadomości. Cele: Utrwalenie pojęć związanych z budową komórki;
Grzegorz Satała, Tomasz Lenda, Beata Duszyńska, Andrzej J. Bojarski. Instytut Farmakologii Polskiej Akademii Nauk, ul.
 Grzegorz Satała, Tomasz Lenda, Beata Duszyńska, Andrzej J. Bojarski Instytut Farmakologii Polskiej Akademii Nauk, ul. Smętna 12, Kraków Plan prezentacji: Cel naukowy Podstawy teoretyczne Przyjęta metodyka
Grzegorz Satała, Tomasz Lenda, Beata Duszyńska, Andrzej J. Bojarski Instytut Farmakologii Polskiej Akademii Nauk, ul. Smętna 12, Kraków Plan prezentacji: Cel naukowy Podstawy teoretyczne Przyjęta metodyka
Reakcje enzymatyczne. Co to jest enzym? Grupy katalityczne enzymu. Model Michaelisa-Mentena. Hamowanie reakcji enzymatycznych. Reakcje enzymatyczne
 Reakcje enzymatyczne Enzym białko katalizujące reakcje chemiczne w układach biologicznych (przyśpieszają reakcje przynajmniej 0 6 raza) 878, Wilhelm uehne, użył po raz pierwszy określenia enzym (w zaczynie)
Reakcje enzymatyczne Enzym białko katalizujące reakcje chemiczne w układach biologicznych (przyśpieszają reakcje przynajmniej 0 6 raza) 878, Wilhelm uehne, użył po raz pierwszy określenia enzym (w zaczynie)
Hormony Gruczoły dokrewne
 Hormony Gruczoły dokrewne Dr n. biol. Urszula Wasik Zakład Biologii Medycznej HORMON Przekazuje informacje między poszczególnymi organami regulują wzrost, rozwój organizmu efekt biologiczny - niewielkie
Hormony Gruczoły dokrewne Dr n. biol. Urszula Wasik Zakład Biologii Medycznej HORMON Przekazuje informacje między poszczególnymi organami regulują wzrost, rozwój organizmu efekt biologiczny - niewielkie
Komputerowe wspomaganie projektowanie leków
 Komputerowe wspomaganie projektowanie leków wykład II Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków wykład II Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Bezpośrednia embriogeneza somatyczna
 Bezpośrednia embriogeneza somatyczna Zarodki somatyczne formują się bezpośrednio tylko z tych komórek roślinnych, które są kompetentne już w momencie izolowania z rośliny macierzystej, czyli z proembriogenicznie
Bezpośrednia embriogeneza somatyczna Zarodki somatyczne formują się bezpośrednio tylko z tych komórek roślinnych, które są kompetentne już w momencie izolowania z rośliny macierzystej, czyli z proembriogenicznie
biologiczne mechanizmy zachowania seminarium + laboratorium M.Eng. Michal Adam Michalowski
 biologiczne mechanizmy zachowania seminarium + laboratorium M.Eng. Michal Adam Michalowski michal.michalowski@uwr.edu.pl michaladamichalowski@gmail.com michal.michalowski@uwr.edu.pl https://mmichalowskiuwr.wordpress.com/
biologiczne mechanizmy zachowania seminarium + laboratorium M.Eng. Michal Adam Michalowski michal.michalowski@uwr.edu.pl michaladamichalowski@gmail.com michal.michalowski@uwr.edu.pl https://mmichalowskiuwr.wordpress.com/
Transport pęcherzykowy
 Transport pęcherzykowy sortowanie przenoszonego materiału zachowanie asymetrii zachowanie odrębności organelli precyzyjne oznakowanie Transport pęcherzykowy etapy transportu Transport pęcherzykowy przemieszczanie
Transport pęcherzykowy sortowanie przenoszonego materiału zachowanie asymetrii zachowanie odrębności organelli precyzyjne oznakowanie Transport pęcherzykowy etapy transportu Transport pęcherzykowy przemieszczanie
Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej
 Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej PRAKTIKUM Z BIOLOGII KOMÓRKI () ćwiczenie prowadzone we współpracy z Pracownią Biofizyki Komórki Badanie dynamiki białek
Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej PRAKTIKUM Z BIOLOGII KOMÓRKI () ćwiczenie prowadzone we współpracy z Pracownią Biofizyki Komórki Badanie dynamiki białek
prof. dr hab. Maciej Ugorski Efekty kształcenia 2 Posiada podstawowe wiadomości z zakresu enzymologii BC_1A_W04
 BIOCHEMIA (BC) Kod przedmiotu Nazwa przedmiotu Kierunek Poziom studiów Profil Rodzaj przedmiotu Semestr studiów 2 ECTS 5 Formy zajęć Osoba odpowiedzialna za przedmiot Język Wymagania wstępne Skrócony opis
BIOCHEMIA (BC) Kod przedmiotu Nazwa przedmiotu Kierunek Poziom studiów Profil Rodzaj przedmiotu Semestr studiów 2 ECTS 5 Formy zajęć Osoba odpowiedzialna za przedmiot Język Wymagania wstępne Skrócony opis
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu w porównaniu z analizą trankryptomu:
Wykład 1. Od atomów do komórek
 Wykład 1. Od atomów do komórek Skład chemiczny komórek roślinnych Składniki mineralne (nieorganiczne) - popiół Substancje organiczne (sucha masa) - węglowodany - lipidy - kwasy nukleinowe - białka Woda
Wykład 1. Od atomów do komórek Skład chemiczny komórek roślinnych Składniki mineralne (nieorganiczne) - popiół Substancje organiczne (sucha masa) - węglowodany - lipidy - kwasy nukleinowe - białka Woda
Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych
 Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych Zalety w porównaniu z analizą trankryptomu: analiza transkryptomu komórki identyfikacja mrna nie musi jeszcze oznaczać
Proteomika: umożliwia badanie zestawu wszystkich lub prawie wszystkich białek komórkowych Zalety w porównaniu z analizą trankryptomu: analiza transkryptomu komórki identyfikacja mrna nie musi jeszcze oznaczać
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU KSZTAŁT BIAŁEK.
 SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU KSZTAŁT BIAŁEK. SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU KSZTAŁT BIAŁEK. SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
Bliskie spotkania z biologią METABOLIZM. dr hab. Joanna Moraczewska, prof. UKW. Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki
 Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Drożdżowe systemy ekspresyjne
 Drożdże Drożdżowe systemy ekspresyjne Zalety: możliwość uzyskania dużej biomasy modyfikacje postranslacyjne eksprymowanych białek transport eksprymowanych białek do pożywki Duża biomasa W przypadku hodowli
Drożdże Drożdżowe systemy ekspresyjne Zalety: możliwość uzyskania dużej biomasy modyfikacje postranslacyjne eksprymowanych białek transport eksprymowanych białek do pożywki Duża biomasa W przypadku hodowli
Mechanizmy działania i regulacji enzymów
 Mechanizmy działania i regulacji enzymów Enzymy: są katalizatorami, które zmieniają szybkość reakcji, same nie ulegając zmianie są wysoce specyficzne ich aktywność może być regulowana m.in. przez modyfikacje
Mechanizmy działania i regulacji enzymów Enzymy: są katalizatorami, które zmieniają szybkość reakcji, same nie ulegając zmianie są wysoce specyficzne ich aktywność może być regulowana m.in. przez modyfikacje
UKŁAD DOKREWNY cz. 2. Wysepki trzustkowe (Langerhansa): grupy komórek dokrewnych produkujących hormony białkowe
 Wysepki trzustkowe (Langerhansa): grupy komórek dokrewnych produkujących hormony białkowe UKŁAD DOKREWNY cz. 2 Elementy składowe: komórki dokrewne kapilary okienkowe włókna nerwowe Typy komórek dokrewnych
Wysepki trzustkowe (Langerhansa): grupy komórek dokrewnych produkujących hormony białkowe UKŁAD DOKREWNY cz. 2 Elementy składowe: komórki dokrewne kapilary okienkowe włókna nerwowe Typy komórek dokrewnych
Fizjologia nauka o czynności żywego organizmu
 nauka o czynności żywego organizmu Stanowi zbiór praw, jakim podlega cały organizm oraz poszczególne jego układy, narządy, tkanki i komórki prawa rządzące żywym organizmem są wykrywane doświadczalnie określają
nauka o czynności żywego organizmu Stanowi zbiór praw, jakim podlega cały organizm oraz poszczególne jego układy, narządy, tkanki i komórki prawa rządzące żywym organizmem są wykrywane doświadczalnie określają
Komputerowe wspomaganie projektowanie leków
 Komputerowe wspomaganie projektowanie leków wykład VI Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
Komputerowe wspomaganie projektowanie leków wykład VI Prof. dr hab. Sławomir Filipek Grupa BIOmodelowania Uniwersytet Warszawski, Wydział Chemii oraz Centrum Nauk Biologiczno-Chemicznych Cent-III www.biomodellab.eu
cytoplazma + jądro komórkowe = protoplazma Jądro komórkowe
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
WYKŁAD 4: MOLEKULARNE MECHANIZMY BIOSYNTEZY BIAŁEK. Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej.
 Pierwsza litera Trzecia litera 2018-10-26 WYKŁAD 4: MOLEKULARNE MECHANIZMY BIOSYNTEZY BIAŁEK Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Druga litera 1 Enancjomery para nienakładalnych
Pierwsza litera Trzecia litera 2018-10-26 WYKŁAD 4: MOLEKULARNE MECHANIZMY BIOSYNTEZY BIAŁEK Prof. dr hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Druga litera 1 Enancjomery para nienakładalnych
Cukry właściwości i funkcje
 Cukry właściwości i funkcje Miejsce cukrów wśród innych składników chemicznych Cukry Z cukrem mamy do czynienia bardzo często - kiedy sięgamy po białe kryształy z cukiernicy. Większość z nas nie uświadamia
Cukry właściwości i funkcje Miejsce cukrów wśród innych składników chemicznych Cukry Z cukrem mamy do czynienia bardzo często - kiedy sięgamy po białe kryształy z cukiernicy. Większość z nas nie uświadamia
Nowe terapie choroby Huntingtona. Grzegorz Witkowski Katowice 2014
 Nowe terapie choroby Huntingtona Grzegorz Witkowski Katowice 2014 Terapie modyfikujące przebieg choroby Zahamowanie produkcji nieprawidłowej huntingtyny Leki oparte o palce cynkowe Małe interferujące RNA
Nowe terapie choroby Huntingtona Grzegorz Witkowski Katowice 2014 Terapie modyfikujące przebieg choroby Zahamowanie produkcji nieprawidłowej huntingtyny Leki oparte o palce cynkowe Małe interferujące RNA
Enzymy katalizatory biologiczne
 Enzymy katalizatory biologiczne Kataliza zjawisko polegające na obniżeniu energii aktywacji reakcji i zwiększeniu szybkości reakcji chemicznej i/lub skierowaniu reakcji na jedną z termodynamicznie możliwych
Enzymy katalizatory biologiczne Kataliza zjawisko polegające na obniżeniu energii aktywacji reakcji i zwiększeniu szybkości reakcji chemicznej i/lub skierowaniu reakcji na jedną z termodynamicznie możliwych
protos (gr.) pierwszy protein/proteins (ang.)
 Białka 1 protos (gr.) pierwszy protein/proteins (ang.) cząsteczki życia materiał budulcowy materii ożywionej oraz wirusów wielkocząsteczkowe biopolimery o masie od kilku tysięcy do kilku milionów jednostek
Białka 1 protos (gr.) pierwszy protein/proteins (ang.) cząsteczki życia materiał budulcowy materii ożywionej oraz wirusów wielkocząsteczkowe biopolimery o masie od kilku tysięcy do kilku milionów jednostek
BIOENERGETYKA cz. I METABOLIZM WĘGLOWODANÓW I LIPIDÓW. dr hab. prof. AWF Agnieszka Zembroń-Łacny
 BIOENERGETYKA cz. I METABOLIZM WĘGLOWODANÓW I LIPIDÓW dr hab. prof. AWF Agnieszka Zembroń-Łacny METABOLIZM/ENERGIA WĘGLOWODANY i LIPIDY WYKŁAD 6 Trawienie i wchłanianie WĘGLOWODANY TŁUSZCZE BIAŁKA Katabolizm
BIOENERGETYKA cz. I METABOLIZM WĘGLOWODANÓW I LIPIDÓW dr hab. prof. AWF Agnieszka Zembroń-Łacny METABOLIZM/ENERGIA WĘGLOWODANY i LIPIDY WYKŁAD 6 Trawienie i wchłanianie WĘGLOWODANY TŁUSZCZE BIAŁKA Katabolizm
Czy żywność GMO jest bezpieczna?
 Instytut Żywności i Żywienia dr n. med. Lucjan Szponar Czy żywność GMO jest bezpieczna? Warszawa, 21 marca 2005 r. Od ponad połowy ubiegłego wieku, jedną z rozpoznanych tajemnic życia biologicznego wszystkich
Instytut Żywności i Żywienia dr n. med. Lucjan Szponar Czy żywność GMO jest bezpieczna? Warszawa, 21 marca 2005 r. Od ponad połowy ubiegłego wieku, jedną z rozpoznanych tajemnic życia biologicznego wszystkich
Oddychanie komórkowe. Pozyskiwanie i przetwarzanie energii w komórkach roślinnych. Oddychanie zachodzi w mitochondriach Wykład 7.
 Wykład 7. Pozyskiwanie i przetwarzanie energii w komórkach roślinnych Literatura dodatkowa: Oddychanie to wielostopniowy proces utleniania substratów związany z wytwarzaniem w komórce metabolicznie użytecznej
Wykład 7. Pozyskiwanie i przetwarzanie energii w komórkach roślinnych Literatura dodatkowa: Oddychanie to wielostopniowy proces utleniania substratów związany z wytwarzaniem w komórce metabolicznie użytecznej
Scenariusz lekcji przyrody/biologii (2 jednostki lekcyjne)
 Joanna Wieczorek Scenariusz lekcji przyrody/biologii (2 jednostki lekcyjne) Strona 1 Temat: Budowa i funkcje kwasów nukleinowych Cel ogólny lekcji: Poznanie budowy i funkcji: DNA i RNA Cele szczegółowe:
Joanna Wieczorek Scenariusz lekcji przyrody/biologii (2 jednostki lekcyjne) Strona 1 Temat: Budowa i funkcje kwasów nukleinowych Cel ogólny lekcji: Poznanie budowy i funkcji: DNA i RNA Cele szczegółowe:
TRANSLACJA II etap ekspresji genów
 TRANSLACJA II etap ekspresji genów Tłumaczenie informacji genetycznej zawartej w mrna (po transkrypcji z DNA) na aminokwasy budujące konkretne białko. trna Operon (wg. Jacob i Monod) Zgrupowane w jednym
TRANSLACJA II etap ekspresji genów Tłumaczenie informacji genetycznej zawartej w mrna (po transkrypcji z DNA) na aminokwasy budujące konkretne białko. trna Operon (wg. Jacob i Monod) Zgrupowane w jednym
Komórka - budowa i funkcje
 Komórka - budowa i funkcje Komórka - definicja Komórka to najmniejsza strukturalna i funkcjonalna jednostka organizmów żywych zdolna do przeprowadzania wszystkich podstawowych procesów życiowych (takich
Komórka - budowa i funkcje Komórka - definicja Komórka to najmniejsza strukturalna i funkcjonalna jednostka organizmów żywych zdolna do przeprowadzania wszystkich podstawowych procesów życiowych (takich
WYBRANE SKŁADNIKI POKARMOWE A GENY
 WYBRANE SKŁADNIKI POKARMOWE A GENY d r i n ż. Magdalena Górnicka Zakład Oceny Żywienia Katedra Żywienia Człowieka WitaminyA, E i C oraz karotenoidy Selen Flawonoidy AKRYLOAMID Powstaje podczas przetwarzania
WYBRANE SKŁADNIKI POKARMOWE A GENY d r i n ż. Magdalena Górnicka Zakład Oceny Żywienia Katedra Żywienia Człowieka WitaminyA, E i C oraz karotenoidy Selen Flawonoidy AKRYLOAMID Powstaje podczas przetwarzania
Składniki diety a stabilność struktury DNA
 Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Plan działania opracowała Anna Gajos
 Plan działania 15.09-15.10 opracowała Anna Gajos Jakie zagadnienia trzeba opanować z następujących działów: 1. Budowa chemiczna organizmów. 2. Budowa i funkcjonowanie komórki 3. Cykl komórkowy 4. Metabolizm
Plan działania 15.09-15.10 opracowała Anna Gajos Jakie zagadnienia trzeba opanować z następujących działów: 1. Budowa chemiczna organizmów. 2. Budowa i funkcjonowanie komórki 3. Cykl komórkowy 4. Metabolizm
