Jak determinowana jest płeć?
|
|
|
- Zdzisław Góra
- 8 lat temu
- Przeglądów:
Transkrypt
1 Dr Marta Polańska Dr hab. Piotr Bębas Jak determinowana jest płeć? Zwierzęta są organizmami rozdzielnopłciowymi lub obojnakami. W pierwszym przypadku poszczególne osobniki danego gatunku najczęściej są albo samicami, produkujacymi komórki jajowe na terenie jajników, albo samcami wytwarzającymi plemniki w jądrach. Omawiane różnice fenotypu między płcią żeńską i męską określamy jako dymorfizm płciowy. Obojnaki posiadają oba typy gonad i dzięki temu produkują zarówno plemniki jak i jaja. U niektórych gatunków dymorfizm płciowy może mieć inny charakter i jak w przypadku C. elegans obok samców występują obojnaki. Płeć osobnika u gatnków wykazujących dymorfizm płciowy ustala się w procesie zwanym determinacją płci. Jego przebieg może zostać określony w czasie zapłodnienia i być konsekwencją odziedziczenia przez zygotę określonej kombinacji genów. W takim przypadku mówimy o genotypowej determinacji płci. W sytuacji gdy płeć osobnika ustala się po zapłodnieniu i jest konsekwencją wpływu czynników z otoczenia (temperatury, obecności osobników określonej płci, czy zagęszczenia populacji) mamy do czynienia ze środowiskową determinacją płci. Genotypowa determinacja płci może odbywać się na kilka różnych sposobów. U ssaków, związana jest z obecnościa chromosomu Y, który do zygoty zostaje wprowadzony przez plemnika. Samce ssaków wytwarzają bowiem dwa rodzaje gamet, które obok haploidalnego zestawu autosomów (identycznego u obu płci, zaznaczanego skrótowo A) zawierają jeden z chromosomów płci: Y lub X. Ze względu na możliwość wytwarzania dwóch rodzajów plemników, a więc XA i YA, płeć męską u ssaków określa sie mianem heterogametycznej. Z kolei samice produkują tylko jeden rodzaj jaj, które zawierają zestaw chromosomów XA, stąd płeć żeńska ssaków zwana jest homogametyczną. Powstająca w wyniku zapłodnienia zygota może posiąść jedną z dwóch kombinacji chromosomów: XXAA, co determinuje żeńską płeć rozwijającego się z niej organizmu lub XYAA, co z kolei określa męski typ zarodka. Obserwacje anomalii związanych z nietypową liczbą i różnymi kombinacjami w występowaniu chromosomów płci u ssaków wykazały, że obecność chromosomu Y zawsze determinuje rozwój organizmu męskiego, a jego brak jest wystarczający do rozwoju samicy. U ptaków determinacja płci ma bardzo podobny charakter z tym, że heterogametyczną jest w tym przypadku płeć żeńska (zestaw chromosomów płci samca oznacza się ZZ, a samicy ZW). Inne mechanizmy genotypowej determinacji płci spotykamy u owadów. Przykładowo u. muchy domowej, nie stwierdza się typowych różnic morfologicznych między autosomami, a chromosomami płci. U tych zwierząt płeć osobnika określana jest jakością alleli jednego z genów. Samice są mianowicie homozygotami (m/m), a samce heterozygotami (M/m). Jednak u najważniejszego z punktu widzenia badań molekularnych gatunku owada D. melanogaster, determinacja płci ma zupełnie inny charakter. Występowanie chromosomu Y jest niezbędne u samca do przebiegu spermatogenezy, jednak jego obecność nie jest czynnikiem determinującym płeć. To czy osobnik rozwinie się w samca czy samicę zależy od stosunku liczbowego zespołu autosomów (A) do chromosomów X w komórkach ciała (należy zaznaczyć, że w haploidalnym zespole oznaczanym A znajdują się 3 autosomy). Jeżeli wartość parametru X:A jest równa 0,5 (XY:AA) to mamy do czynienia z samcem, natomiast gdy osiąga wartość 1,0 (XX:AA) osobnik jest samicą. Ze względu na fakt, iż osobniki triploidalne D. melanogaster są płodne, możliwe są także inne kombinacje zespołu chromosomów u ich potomstwa. Prawdopodobny jest więc układ, gdzie X:A ma wartość niższą od 0,5, pomiędzy 0,5 a 1,0 i powyżej 1,0. Owady, u których stosunek X:A ma wartość równą 0,67 zwane są interseksualnymi. Są to zwierzęta mozaikowe tzn. ich ciała budują tkanki charakterystyczne dla samców i samic. Zjawisko to jest niepodważalnym dowodem na
2 autonomię przebiegu determinacji płci na poziomie pojedynczych komórek, charakterystyczną dla D. melanogaster, jak i wielu innych gatunków owadów. Kolejny mechanizm determinacji płci spotykamy u błonkówek np. pszczół i os. Polega on na rozwoju samic z zapłodnionych jaj, natomiast samców z niezapłodnionych, co określamy jako arrhenotokię. W efekcie komórki linii somatycznej, jak i płciowej męskiego osobnika takich owadów mają haploidalny zestaw chromosomów, co z kolei diametralnie zmienia przebieg u nich spermatogenezy. Jeszcze inny model oparty o wpływ liczby chromosomów na determinację płci spotykamy w przypadku C. elegans. Jest on niemal identyczny z obserwowanym u D. melanogaster, niemniej wykazuje sobie tylko właściwe cechy. Rozwój osobnika męskiego bądź hermafrodyty zależy od stosunku liczby chromosomów X do zespołów autosomów. U samców wartość X:A jest równa, bądź mniejsza od 0,5. Z kolei u osobników hermafrodytycznych stosunek ten zawiera się między 0,75 i 1,5. Inaczej niż w przypadku D. melanogaster osobniki u których X:A jest równy 0,67 są samcami, a nie postaciami interseksualnymi. Sytuacja ta jest spowodowana omawianym wcześniej zjawiskiem efektu grupy. Inaczej więc niż w przypadku D. melanogaster u C. elegans nie obserwujemy daleko posunietej autonomii w determinacji płci poszczególnych komórek. U nicienia brak jest także chromosomu Y, a haploidalny zespół chromosomów w plemnikach ma postać XA lub OA (gdzie O oznacza brak chromosomu płci). W procesie determinacji, a następnie rozwoju płci podstawową rolę pełni początkowy sygnał, który wpływa na aktywność genów regulatorowych, co z kolei określa przebieg różnicowania płciowego. Badania prowadzone na modelowych organizmach, pozwoliły ustalić, że geny zaangażowane w ten proces tworzą rodzaj hierarchicznego systemu w którym wyróżnia się trzy równolegle aktywowane szlaki odpowiedzi znane jako: mechanizm kompensacyjny, różnicowanie płci somatycznej i różnicowanie płci komórek rozrodczych. Mechanizm kompensacyjny odpowiada za regulację poziomu transkrypcji genów położonych na chromosomach X. Wiadomo, że na chromosomie X zlokalizowanych jest szereg genów, które nie mają związku z determinacją płci, a ich produkty pełnia istotną rolę w metabolizmie. Należy się spodziewać, że liczba kopii tych genów będzie inna u samicy (lub osobnika hermafrodytycznego) niż u samca, co jest spowodowane różną liczbą posiadanych chromosomów X. Problem tych dysproporcji może wydawać się szczególnie poważny gdy uświadomimy sobie, że w DNA chromosomu X u D. melanogaster zapisana jest 1/5 informacji jaka znajduje się w całym genomie tego owada. Analizy efektów jakie wywołują utraty lub duplikacje fragmentów chromosomów u osobników diploidalnych wykazały, że haploidalość lub triploidia obejmująca zaledwie kilka procent spośród wszystkich genów organizmu, powoduje jego poważne uszkodzenia lub jest letalna. Rodzi się więc pytanie jak organizmy radzą sobie z nierównocenną dystrybucją informacji genetycznej u osobników obu płci? Okazuje się, że różne grupy zwierząt znalazły odmienne sposoby, które pozwalają im na zmniejszenie tych dysproporcji. Zostały one wspólnie nazwane mechanizmem kompensacyjnym. Saaki osiągneły ten cel poprzez inaktywację jednego z chromosomów X (oznacznego jako Xi) w niemal wszytkich komórkach u samic. W jądrze interfazowym chromosom taki widoczny jest on jako skupisko heterochromatyny, zwane ciałkiem Barra lub chromatyną płciową. Mimo silnej kondensacji DNA chromosomu Xi ulega replikacji podczas mitozy, niemniej stan jego inaktywacji przenosi się na komóeki potomne. U osobników
3 aneuploidalnych wszystkie z chromosomów X, poza jednym są inaktywowane, natomiast u XO żaden. Proces ten odbywa się na bardzo wczesnym etapie rozwoju (stadium blastocysty) i wydaje się przypadkowo dotyczyć chromosomu pochodzącego od ojca lub matki. Udowodniły to badania przeprowadzone na myszach będących heterozygotami względem alleli genu kodującego ubarwienie sierści, który jest zlokalizowany na chromosomie X. Osobniki takie są łaciate, co świdczy o aktywności genów pochodzenia tylko ojcowskiego lub tylko matczynego w różnych obszarach skóry. Nieliczne odstępstwa od tej reguły pochodzą z obserwacji komórek wchodzących w skład endodermy u gryzoni i komórek somatycznych u torbaczy, w których inaktywacji ulega głównie chromosom X pochodzenia ojcowskiego. Inaktywacja chromosomu X związana jest z obecnością tnaskryptu oznaczanego Xist, który wykazuje cechy charakterystyczne dla mrna, ale nie ulega translacji. Kodujący go gen zlokalizowany jest na chromosomie X, w jego środkowej części zwanej centrum inaktywacyjnym chromosomu X, albo w skrócie Xic (ang. X-inactivation center). W początkowym okresie rozwoju transkrycja Xist zachodzi na terenia obu chromosomów X jednak wkrótce ulega ona wyciszeniu na Xa (aktywny chromosom X) utrzymując się na wysokim poziomie w przypadku Xi. Powstające w jej wyniku cząsteczki RNA nie opuszczają jądra komórkowego tylko rozchodzą się wzdłuż całego inaktywowanego chromosomu i pokrywają go. Przemieszczaniu się transkryptów od centrum inaktywacyjnego towarzyszy wyciszanie aktywności prawie wszystkich genów Xi z wyjątkiem tych, które w liczbie dwóch kopii konieczne są do prawidłowego funkcjonowania samicy. Regulacja ekspresji Xist zarówno na Xi jak i Xa związana jest z obecnością antysensownego transkryptu Tsix, który jest kodowany w obszarze Xic obejmującym także całą sekwencję genu Xist. Wysoki poziom ekspresji Tsix na tym chromosomie, który ma zostać aktywny, powoduje represję Xist, a odwrotnie w przypadku chromosomu, który ma ulec inaktywacji, wyciszenie transkrypcji Tsix powoduje gromadzenie się transkryptu Xist, co prowadzi do sukcesywnego wyłączania ekspresji genów na Xi. Procesowi temu towarzyszy postępująca metylacja DNA, która aktywuje ekspresję Xist. Istnieje conajmniej kilka hipotez tłumaczących sposób w jaki Xist i Tsix oddziałują na siebie prowadząc do wykształcenia fenotypu komórek, w których aktywny jest tylko jeden chromosom X. Najbardziej trafną wydaje się być ta, która zakłada możliwość tworzenia kompleksów Xist/Tsix dzięki wystepowaniu obszarów komplementarnych miedzy oboma cząsteczkami. Jak się wydaje, może to powodować degradację powstającego dwuniciowego RNA lub prowadzi do zakrycia obszarów Xist, które są szczególnie istotne w inaktywacji chromosomu. Podobnie molekularny mechanizm działania transkryptu Xist nie jest znany, istnieją jednak przypuszczenia, że jego wpływ na tworzenie heterochromatyny może odbywać się poprzez aktywację metylacji histonów oraz zwiększenie aktywności deacetylaz w Xi. Mechanizm kompensacyjny u D. melanogaster zwany jako samcza hipertranskrypcja (ang. male hypertranscription) inaczej niż u ssaków związany jest z dwukrotnym zwiększeniem aktywności transkrypcyjnej genów zlokalizowanych na chromosomie X. Jest to możliwe dzięki dużej liczbie wzmacniaczy działających w pozycji cis na położone blisko geny oraz wiąże się z wpływem czynników transkrypcyjnych działających w układzie trans. Spośród nich majważniejsze są kodowane przez grupę kilku autosomalnych genów określanych jako male-specific lethal. Mutacje powodujące utratę funkcji tych genów, zawsze kończą się śmiercią osobników XY. Dzieje się tak w konsekwencji niewystarczającej aktywności transkrypcyjnej na terenie chromosomu X. Białka MSL (MSL1, MSL2, MSL3, MOF i MLE) w bardzo dużej ilości łączą się bezpośrednio z sekwencjami wspomnianych wzmacniaczy, działających w pozycji cis, aktywując ekspresję położonych tam genów. Jedno z nich, oznaczane jako MLE (ang. maleless), wykazuje właściwości helikazy, która ma zdolność rozkręcania spiral DNA i RNA. Dzięki niemu struktura męskiego chromosomu X jest
4 zdecydowanie luźniejsza od tej jaką stwiedza się w przypadku żeńskiego X. Dodatkowo u samców obserwuje się bardzo bogatą acetylację histonów H4 w pozycji 16 (położenie lizyny), na obszarze calego chromosomu X, za sprawą acetylotransferazy MOF, co jak wiadomo zmniejsza siłę oddziaływań między histonami oraz stabilność struktury nukleosomu. Każda ze wspomnianych zmian struktury chromatyny zwiększa dostępność obszarów regulatorowych dla czynników transkrypcyjnych, tym samym może zwiększać poziom ekspresji genów. Zrozumienie mechanizmu hipertranskrypcji obserwowanej u samców wymaga także prześledzenia aktywności genów w obrębie chromosomów X u samic. Wiadomo bowiem, że w proces ten zaangażowany jest produkt genu regulatorowego zwanego Sxl (ang. Sex-lethal), który jest usytuowany bardzo wysoko w hierarchii systemu odpowiadającego za determinację płci u D. melanogaster. Jego rola w mechanizmie kompensacyjnym nie jest w pełni jasna. Wydaje się, że obecność białka SXL u samic zmienia przebieg składania transkryptu msl2 produktu jednego z genów male-specific lethal. Powstające w efekcie mrna nie ulega translacji, a przy braku białka MSL-2 niemożliwa jest aktywacja transkrypcji genów na poziomie obserwowanym u samców. Istnieją również dowody, że sexlethal nie działa na premrna lecz dojrzały transkrypt mls2, przyłączając się do jego 5 UTR oraz 3 UTR i w ten sposób powoduje represję jego translacji. Niezależnie od sposobu w jaki u samic realizowana jest funkcja genu Sxl wiadomo, że ma ona postać regulacji negatywnej. Z kolei u samców gdzie nie stwierdza się obecności SXL, białko MSL-2 jest produkowane bez przeszkód i wraz z pokrewnymi czynnikami aktywuje ekspresję genów chromosomu X. W mechanizmie kompensacyjnym D. melanogaster kluczowa rolę odgrywaja także swoiste transkrypty, podobnie jak ma to miejsce w przypadku Xist u ssaków. U muchy na chromosomie X położone są dwa bardzo charakterystyczne geny rox1 i rox2. Kodują one duże cząsteczki RNA, które podlegają składaniu, a na ich terenie nie stwierdza się otwartych ramek odczytu, tak więc nie ulegaja one translacji. Transkrypty rox1 i rox2 nie opuszczaja jądra, tylko wiążą się z białkami MSL, co ochrania je przed degradacją. Oddziaływanie to ma także charakter pozytywnej regulacji w przypadku stabilizowania kompleksów MSL, które nie powstają i nie mogą pełnić swej funkcji przy braku przynajmniej jednego rodzaju RNA rox. Powszechnie akceptowany model mechanizmu kompensacyjnego zakłada, że białka grupy MSL associują na chromosomie X w obszarze genów rox, wychwytując powstające tam transkrypty. Następnie przemieszczają się do innych obszarów chrmosomu, a podczas tej wedrówki dojrzewają, co ponownie wiąże się z wychwytywaniem transkryptów rox. Wreszcie osiagają swe przeznaczenie, w miejscach regulatorowych genów, gdzie powodują przemodelowanie chromatyny wpływające na zwiększenie jej aktywności transkrypcyjnej. Mechanizm kompensacyjny przybiera jeszcze inny charakter u C. elegans. Zmniejszeniu do połowy ulega poziom ekspresji genów zlokalizowanych na chromosomach X u osobników hermafrodytycznych tego gatunku. W proces zaangażowana są dwie grupy genów. Pierwsza z nich sdc (ang. sex determination and dose compensation) obejmuje geny (sdc-1, sdc-2 i sdc-3) kodujące białka odpowiedzialne za koordynację przebiegu różnicowania płci oraz regulację mechanizmu kompensacyjnego, druga grupa dcd (ang. dosage compensation dumpies) jest jedynie zaangażowana w mechanizm kompensacyjny (dpy-21, dpy-26, dpy-27, dpy-28 i dpy- 30). Mutacje w każdym z tych genów powodują podwyższenie poziomu transkrypcji w obrębie chromosomów X u hermafrodytów, a z wyjątkiem dpy-21 i sdc-1, także bardzo wysoką śmiertelność mutantów. Wspomnianych efektów (z wyjątkiem mutacji w dpy-30) nigdy nie stwierdza się u samców (XO), które mimo mutacji we wspomnianych genach zawsze charakteryzuje dziki fenotyp. W omawiany proces zaangażowane są jeszcze produkty dwóch innych genów, mix-1 (ang. mitosis and X-associated) oraz xol-1 (ang. XO lethal). Białko MIX-1 ma istotne znaczenie w procesie segregacji chromosomów podczas podziałów komórkowych, natomiast XOL-1 odgrywa nadrzędną rolę w determinacji i różnicowaniu się
5 męskiej płci. Działanie mechanizmu kompensacyjnego polega na tworzeniu wielobiałkowych kompleksów, które wchodzą w fizyczny związek z chromosomami X. Spośród nich kluczową rolę odgrywa białko SDC-2, które jak się sądzi odpowiada za rozpoznawanie chromosomu, do którego mają przyłaczyć się elekemty kompleksu oraz odpowiada za samą ich asocjację. SDC-2 także jako jedyne może wiązać się z chromosomem bez obecności innych czynników. Po jego przyłaczeniu i stworzeniu pary z SDC-3 do powstałego kompleksu dołączają jego pozostałe elementy: DPY-26, DPY-27, DPY-28, MIX-1 oraz SDC-1. Należy zaznaczyć, że bez SDC-2, określanego także osiowym czynnikiem inicjującym, żadne z białek DPY nie łączą się ze sobą, nie są w stanie tworzyć kompleksu, ani wejść w jakiekolwiek interakcje z chromatyną. Pomiędzy poszczególnymi białkami istnieją ścisłe zależności, które wyrażają się koniecznością występowania jednych, aby inne z nich mogły spełnić swe funkcje. Przykładowo, do tego, aby z chromosomem mogło związać się MIX-1, w realizacji procesu kompensacyjnego, niezbędna jest obecność DPY-27. Z kolei asocjacja DPY-27 z chromosomem wymaga białka DPY-30, które samo nie wchodzi w skład omawianego kompleksu, natomiast wydaje się wpływać także na zwiększenie metylacji histonu H3 w nukleosomach, co wpływa na wyciszenie ekspresji genów. Szczególną pozycję w charakteryzowanych relacjach odgrywa produkt genu xol-1, który w odpowiedzi na sygnał jakim jest stosunek X:A, reguluje poziom ekspresji genów znajdujących się na chromosomie X. Białko XOL-1 odpowiada za inicjację rozwoju samców poprzez represję aktywności wszystkich trzech genów sdc oraz genów z grupy dcd. Z kolei bardzo niska ekspresja xol-1 u osobników hermafrodytycznych, umożliwia realizację programu kompensacji. Różnicowanie płci somatycznej u ssaków Rozwój ssaków zaczyna się od stadium, które nie jest zróżnicowane płciowo i można go podzielić na dwa etapy. Pierwszy dotyczy czasu, gdy z zawiązków gonad zaczną rozwijać się jądra bądź jajniki i określany jest jako pierwotne różnicowanie płci, albo inaczej różnicowanie się pierwszorzędowych cech płciowych. Drugim etapem natomiast jest różnicowanie się drugorzędowytch cech płciowych, które zależy od aktywności hormonalnej powstających gonad. Rozwój normalnego zarodka męskiego u ssaków zależy od sygnału pochodzącego z chromosomu Y. Wstępne badania wykazały, że wspomnianym elementem sygnałowym u myszy jest czynnik Tdy (ang. testis determining gene on the Y), a u człowieka TDF (ang. testis determining factor) często stosuje się dla nich wspólne oznaczenie TDF/Tdy. Zlokalizowano je na chromosomach Y, jednak dla uściślenia używanych w literaturze sformułowań, Tdy i TDF nie są genami, ani ich produktami, lecz określeniami stosowanym dla opisu źródła sygnału, który determinuje rozwój męskiej gonady. Jak udowodniły badania prowadzone na osobnikach mozaikowych myszy tzw. chimerach, które składają się z dwóch typów komórek zawierających w zespole chromosomów XX, jak i XY, Tdy nie ma wpływu na przebieg gametogenezy, a więc nie określa tego czy osobnik będzie produkował plemniki czy jaja. Stwierdzono bowiem, że u chimer mogą rozwijać się żeńskie komórki płciowe, w których kariotypie stwierdzamy XY. Wynik ten jednoznacznie wskazuje brak związku Tdy z różnicowaniem się męskich komórek płciowych. Z kolei stwierdzenie, iż spermatogonia mogą powstawać u osobników pozbawionych chromosomu Y podkreśliły brak jakiejkolwiek roli Tdy, także w determinacji męskiego kierunku rozwoju komórek płciowych. W związku z tym uznano, że jedynym potencjalnym obiektem oddziaływania omawianego czynnika muszą być komórki somatyczne. Jak się okazało są nimi płodowe komórki podporowe jąder (w przyszłości komórki Sertoliego), a do ich różnicowania niezbędny jest chromosom Y niosący ze sobą Tdy. W czasie rozwoju wpływają one na inne komórki z najbliższego otoczenia, poprzez opisany wcześniej mechanizm zwany efektem grupy i kierują je na szlak różnicowania
6 konieczny do wykształcenia jądra. W ten sposób, niezależnie od posiadanego zespołu chromosomów, powstają dodatkowe dwie linie komórkowe dająca początek komórkom śródmiąższowym, produkującym męskie hormony steroidowe oraz komórkom tkanek łącznych, które formują zrąb jądra. Ostateczne ustalenie lokalizacji TDF/Tdy na chromosomie Y oraz określenie czy jest on pojedynczym genem czy może ich grupą, a także jaki jest mechanizm jego działania stało się możliwe dzięki badaniom osobników wykazujących anomalie chromosomowe. Prawdopodobne jest bowiem, że podczas rekombinacji, która ma miejsce w czasie mejozy, u samców może dojsć do przeniesienia fragmentu chromosomu Y, zawierającego TDF/Tdy, na chromosom X. W efekcie gdy plemnik, który odziedziczy w wyniku segregacji chromosomów taki X i zapłodni komórkę jajową, to rozwijający się osobnik, mimo żeńskiego zespołu chromosomów płci będzie rozwijał się w osobnika męskiego. Z kolei osobnik męski powstający z zygoty, do której plemnik wprowadził chromosom Y bez TDF/Tdy, będzie miał fenotyp żeński. Zjawisko takie spotykamy znacznie częściej u ludzi niż u myszy, co z kolei tłumaczy położenie locus omawianego czynnika na chromosomach Y u obu gatunków. Na chromosomach płci znajduje się obszar pseudoautosomalny (ang. pseudoautosomal region PAR) w obrębie którego X i Y są homologiczne, a co za tym idzie podczas mejozy ulega on procesowi crossing-over. U ludzi strefa obejmująca TDF znajduje się tuż przy obszarze PAR, co w sporadycznych przypadkach nieprawidłowego przebiegu rekombinajcji, może spowodować przeniesienie omawianego czynnika na chromosom X. Przedstawiony przebieg zdarzeń początkowo uznawany za hipotetyczny, został jednak szybko poparty dowodami pochodzącymi z analiz miejsc podlegających crossing-over u ludzi z anomaliami chromosomowymi. Wykazano, że TDF zlokalizowany jest na krótkim ramieniu chromosomu Y i znajduje się na odcinku DNA o długości ok. 35 kb. W przypadku myszy, zjawiska przeniesienia fragmentów chrmosomu Y z Tdy na X praktycznie nie spotykamy, gdyż u tego gatunku Tdy oraz PAR zajmują się w bardzo dużej odległości od siebie. Niemniej znane są przypadki osobników myszy z aberacjami chromosomowymi, których efekt jest analogiczny z opisanym u człowieka, jednak zmiany te mają przynajmniej częściowo inne podłoże. Opisano bowiem osobnika męskiego posiadającego normalny zestaw chromosomów płci, a więc XY, który przekazywał swemu potomstwu czynnik określany jako Sxr, powodujący zamianę płci (ang. Sex-reversed). Jak się okazało, u samca takiego nastąpiła duplikacja fragmentu obejmującego Tdy i w ten sposób powstał Sxr, który usytuował się tuż przy obszarze PAR. Produktami spermatogenezy u takiego samca były między innymi plemniki posiadające chromosom X z Sxr (czyli funkcjonalnym Tdy). Translokacja tego czynnika na X odbywała się w sposób analogiczny z opisanym wcześniej dla TDF u człowieka. Osobnik powstały po zapłodnieniu jaja plemnikiem z chromosomem X, niosącym Srx, był pod względem fenotypu samcem, jednak o kariotypie XX. Na początku lat 90 zeszłego wieku wykazano, że na opisanym wczesniej fragmencie chromosomu Y o długości 35 kb, niosącym czynnik TDF, znajduje się tylko jeden gen. Wkrótce potwierdzono jego duże podobieństwo do sekwencji lokalizowanej na obszarze mysiego Tdy. Od tego momentu locus TDF/Tdy opisywał położenie genu nazwanego u człwieka SRY, a u myszy Sry (ang. sex-determining region of Y). Sry determinuje płeć męską komórek somatycznych jąder oraz odpowiada za przebieg różnicowania się pierwszorzędowych cech płciowych u ssaków Ostatecznym dowodem na udział Sry w determinacji płci somatycznej było doświadczenie jakie wykonano z wykorzystaniem myszy transgenicznych. Do zapłodnionych jaj wprowadzono fragment genomowego DNA o długości 14 kb, który zawierał tylko funkcjonalny gen Sry. Następnie analizowano rozwój tych zarodków, biorąc pod uwagę
7 osobniki o kariotypie XX. Okazało się, że u części z nich rozwinęły się jądra z typowo wykształconymi kanalikami nasiennymi oraz wszystkimi charakterystycznymi komórkami Sertoliego, Leydiga i budującymi zrąb gonady. Wynik opisanego eksperymentu stał się argumentem jednoznacznie potwierdzającym tezę o nardzędnej roli Sry, a co za tym idzie chromosomu Y, w determinacji i rozwoju płci męskiej u ssaków. Powstaje jednak pytanie, w jaki sposób Sry pełni swą funkcję wpływając na powstawanie pierwszorzędowych cech płciowych? Jak przekonamy się za chwilę, odpowiedź na to pytanie nie jest prosta, gdyż charakterystyka współzależności między ekspresją Sry i innych genów w wielu przypadkach jest wynikiem dedukcji prowadzonych w oparciu o faragmentaryczne dane eksperymentalne. Analiza molekularna białka Sry wykazała, że jest ono czynnikiem regulującym transkrypcję, zawierającym w swej strukturze domenę HMG, która określa jego przynależność do grupy HMG (ang. high mobility group), obejmującą szereg białek niehistonowych wiążących DNA. Sry rozpoznaje i przyłącza się do obszarów o ściśle określonych sekwencjach (A/TAACAAT/A) i co bardzo istotne, poprzez domenę HMG wpływa na zagięcie nici chromatynowej powodując, że zbliżają się do siebie znacznie oddalone elementy regulatorowe działające w pozycji cis. Aktywność transkrypcyjna Sry jest ograniczona zaledwie do dwóch dni w okresie wczesnego rozwoju zarodkowego myszy. Już na tej podstawie łatwo wywnioskować, że białko Sry jest czynnikem sygnałowym, indukującym cykl zdarzeń, których realizacja w postaci wykształcenia męskiej gonady, wymaga znacznie dłuższego czasu. Faktycznie Sry lokalizuje się na szczycie hierarchicznego systemu, w którym ekspresja kolejnych genów zależy od obecności białek regulatorowych. Te z kolei są produktami genów aktywnych na wyższych pietrach wspomnianego systemu. Pierwszym elementem szlaku, na którym działa Sry jest Dax1 (ang. dosage sensitive sex-reversal-adrenal hypoplasia congenita-critical region of the X chromosome, gene 1), gen zlokalizowany na chromosomie X. U myszy, niezależnie od płci, moment rozpoczęcia jego ekspresji zbiega się w czasie z aktywnością Sry u samców, która ma miejsce począwszy od 11 doby po zapłodnieniu. Wtedy też ujawnia się rola białka Sry, które działa jako represor transkrypcji Dax1, szybko wyłączając jego ekspresję. Oczywiście u samic, ze względu na brak Sry, aktywność Dax1 nie jest hamowana i utrzymuje się na wysokim poziomie, co prowadzi do włączenia szlaku rowojowego jajników. Wkrótce po zainicjowaniu aktywności transkrypcyjnej Sry, u samców myszy obserwuje się wzrost aktywności kilku genów autosomalnych, na początku Sox9 (ang. Sry-related HMG box, 9), a w dalszej kolejności Wt1 (ang. Wilm s-tumor-associated gene 1), Sf1 (ang. steroidogenic factor 1) i Amh (ang. anti- Müllerian hormone). Należy jednak pamiętać, że zarówno Wt1, Sf1, jak i Sox9 są eksprymowane na niskim poziomie jeszcze w niezróżnicowanych komórkach gonad, zarówno u samców jak i samic. W oparciu o analizy budowy promotorów każdego z tych genów oraz ich aktywność transkrypcyjną w tkankach hodowanych in vitro, storzono model, który obrazuje schemat zdarzeń, które jak się sądzi, mają miejsce w czasie determinacji płci komórek somatycznych gonad u ssaków. Wczesna ekspresja Sf1 i Wt1 prawdopodobnie wpływa na aktywację Sry, co w konsekwencji prowadzi do zwiększenia poziomu transkrypcji samego Sf1, jak i Sox9 w płodowych komórkach podporowych, aż do poziomu wymaganego dla rozwoju jąder. Rola Sf1 w omawianym systemie jest dość złożona. Koduje on sierocy receptor jądrowy, który pełni kluczową rolę w regulacji szlaku rozwojowego gonad i nadnerczy oraz reguluje biosyntezę steroidów u samców. Istnieją dowody świadczace o bezpośredniej, pozytywnej regulacji ekspresji Sry przez Sf1. Informacje te pochodzą z badań prowadzonych na komórkach owadzich z wprowadzonym konstruktem, w którym promotor Sry podłączono do genu reporterowego. Następnie komórki te kotransfekowano wektorem z genem Sf1 i jak się okazało, powstające w tym układzie białko Sf1, aktywowało transkrypcję genu reporterowego. Niestey zależności tej nie potwierdzono w warunkach in vivo, a więc na
8 terenie komórek różnicujacych się jąder. Troche inne światło na rolę Sf1 w determinacji płci rzucają analizy prowadzone na myszach z mutacją w tym genie. U osobników homozygotycznych posiadających niefunkcjonalne allele Sf1, najwcześniejsze etapy rozwoju niezróżnicowanych zawiązków gonad (tzw. grzebieni płciowych) przebiegają bez jakichkolwiek zakłóceń. Dopiero od momentu gdy incjowany jest proces tworzenia jąder bądź jajników, ulegają one całkowitej degeneracji. Obserwacja ta sprawiła, że Sf1 uznany został za jeden z elementów niezbędnych do wytworzenia środowiska, w którym wyrazi się rola Sry. Podobne znaczenie wydaje się mieć WT1, czynnik transkrypcyjny, z zaopatrzoną w palce cynkowe domeną wiążącą DNA, który obok swej funkcji na terenie grzebieni płciowych odgrywa też kluczową role w czasie rozwoju nerek. Sf1 i Wt1 nie są więc bezpośrednio zaagażowane w determiację płci, ale ich udział jest konieczny w kształtowaniu biochemicznego podłoża, warunkujacego określenie przeznaczenia komórek somatycznych. Dość silnym argumentem przemawiającym za słusznością tej koncepcji jest opisanie zdolności WT1 do wiązania RNA. Bezpośrednim efektem tej interakcji może być stabilizacja transkryptu oraz pozytywna regulacja odczytu zawartej w nim informacji. Zgodnie z tą koncepcją WT1 może wpływać na efektywność Sry we wczesnych etapach determinacji płci. Do grupy charakteryzowanych genów dołącza jeszcze jeden Sox9, którego ekspresja uznawana jest za kolejny krok w różnicowaniu płci, po wcześniejszym zainicjowaniu procesu przez Sry. Niewielkie ilości mrna Sox9 obecne są w komórkach jeszcze przed momentem rozpoczęcia ekspresji Sry. Niemniej ze względu na bardzo znaczny wzrost transkrypcji Sox9 w zarodkowych komórkach podporowych, co ma miejsce wkrótce po aktywacji Sry, wydaje się, że procesy te są ze sobą powiązane. W układzie tym, Sox9 uznawany jest za element podległy Sry, który reguluje jego ekspresję w sposób bezpośredni, bądź pośredni, niemniej wyjaśnienie tej kwestii wymaga dalszych badań. Omawiane zjawisko jest złożone, szczególnie gdy powtórnie uzmysłowimy sobie, iż Sry jest aktywny transkrypcyjnie bardzo krótko w czasie ontogenezy, natomiast ekspresja Sox9 utrzymuje się znacznie dłużej podczas rozwoju jąder. W związku z tym Sry może być czynnkiem sprawczym wysokiej aktywności transkrypcyjnej Sox9, ale napewno nie jest wymagany do jej utrzymania w późniejszych okresach morfogenezy. Rola Sox9 w determinacji płci stała się ewidentna przy analizach osobników z wyraźną nadekspresją tego genu, która jest efektem duplikacji jego locus lub mutacji w rejonie regulatorowym, zwiększającej poziom transkrypcji. Osobniki takie, przy kariotypie XX, są pod względem fenotypu samcami. Wynika z tego jednoznaczna konkluzja, że wysoki poziom SOX9 jest wystarczającym sygnałem do osiągnięcia przez zarodkowe komórki stanu zdeterminowania wymaganego przy tworzeniu jąder, nawet w sytuacji braku Sry. Analogiczna sytuacja występuje u mutanta myszy zwanego Odsex, który otrzymano w czasie manipulacji mających na celu stworzenie zwierząt transgenicznych. U osobników żeńskich takich myszy (XX Ods/+) swierdzono insercję w obszarze regulatorowym Sox9, która spowodowała derepresję tego genu, który u samic normalnie nie jest aktywny. Ostatecznym efektem omawianego eksperymentu było uzyskanie zwierząt o fenotypie męskim z kariotypem XX. Zależność przebiegu determinacji płci od aktywności Sox9 jest szczególnie ewidentna, gdy spojrzymy na jego pozycję w historii rozwoju tego procesu u zwierząt kręgowych. W odróżnieniu od Sry, który jest reprezentowany w genomie tylko ssaków, Sox9 pozostaje głównym elementem sprawczym rozwoju jąder u ptaków, gadów, a nawet ryb. Wyłania się z tego obraz, w którym właśnie Sox9 kieruje bardzo stabilnym pod względem zmian ewolucyjnych szlakiem rozwojowym, natomiast Sry zajął pierwszą pozycję w systemie hierarchicznym determinacji płci stosunkowo niedawno. W związku z powyższym nie dziwi także fakt, że budowa aminokwasowa białka SOX9 jest wysoce konserwatywna ewolucyjnie u wszystkich kręgowców. W jego strukturze wyróżniono między innymi 3 ważne domeny określanące funkcję i przynależnośc do grupy czynników regulujacych transkrypcję. Są nimi domena HMG odpowiedzialna za wiązanie DNA i
9 zaginanie nici chromatynowej, która jest podstawowym kryterium klasyfikowania Sox9 do tej samej co Sry rodziny genów zwanej Sox (ang. Sry-related HMG box genes). Z kolei dwie domeny aktywujące transkrypcję jednoznacznie określają jego funkcję jako typowego czynnika transkrypcyjnego. W tym momencie samoistnie nasuwa się pytanie o elementy w systemie determinacji płci, które podlegają wpływom Sox9. Najlepiej udokumentowaną w literaturze zależnością tego typu jest pozytywna regulacja ekspresji Amh przez SOX9. Jej efektem jest wzrost poziomu glikoproteiny AMH (zwanej także MIS ang. Müllerianinhibiting substance) w zarodkowych komórkach podporowych, która wydzielana do nabliższego otoczenia determinuje kierunek rozwoju przewodów rozrodczych u powstającego osobnika. Innymi słowy AMH działa jako hormon, który wywołuje regresję przewodów Müllera (rozwijających się u samic w jajowody, macice i górny odcinek pochwy) jednocześnie stwarzając odpowiednie środowisko do działania androgenów uwalnianych przez różnicujące się komórki Leydiga. Te z kolei kierują rozwojem kanałów Wolffa, co w ostatecznym rozrachunku prowadzi do utworzenia męskich przewodów rozrodczych. W omawianym procesie SOX9 łączy się z promotorem Amh i przy współudziale Sf1, WT1, białka szoku cieplnego HSP70 oraz dodatkowego czynnika zwanego GATA4, bezpośrednio reguluje jego ekspresję. Białka SOX9 i Sf1 pełnią w tym systemie kluczową rolę, gdyż od pierwszego z nich zależy sama inicjacja transkrypcji, natomiast drugie pozwala utrzymać ją na wysokim poziomie. Pozostałe elementy pełnią rolę wspomagającą w tym procesie. GATA4 poprzez swą domenę z palcami cynkowymi wzmacnia efekt jaki wywiera białko Sf1na promotor Amh. Z kolei HSP70 wiąże się zarówno z SOX9, jak i WT1 i tym samym inicjuje tworzenie wielobiałkowego kompleksu. Wspóldziałanie każdego z tych elementów wygląda następująco: białko SOX9 dzięki domenie HMG powoduje zagięcie DNA zbliżając zasocjowany Sf1 do wzmacniającego jego aktywność GATA4, jednocześnie pozostaje w zwiazku z WT1, a za pośrednictwem HSP70 wpływa na tworzenie wielobiałkowej struktury regulującej transkrypcję genu Amh. Wróćmy jeszcze na chwilę do przedstawienia zależności, które leżą u podstaw determinacji i różnicowania się płci somatycznej u samic. Oczywiście jak to już wspomniano powyżej, głównym czynnikiem sprawczym w tym procesie jest brak Sry oraz działanie Dax1, genu którego ekspresja wywiera hamujący wpływ na rozwój męskich cech zarodka. Kodowane przez niego białko DAX1, należy do nadrodziny receptorów jądrowych, z wysoce konserwatywną domeną wiążącą ligand, ale nietypowo zbudowanym N-terminalnym końcem, gdzie brak charakterystycznej struktury palców cynkowych odpowiadających za wiązanie DNA. Informacja ta, wraz z brakiem jakichkolwiek dowodów na bezposrednie łączenie się DAX1 z sekwencjami regulatorowymi genów, skłaniają do wniosku, że omawiany czynnik wpływa na ich ekspresję poprzez interakcje z innymi białkami. Pomimo braku w chwili obecnej jednoznacznych dowodów, które tłumaczyły by jak działa DAX1 w zarodkowych komórkach gonad samic, wydaje się, iż najprawdopodobniej jego funkcja polega na znoszeniu efektu generowanego przez SF1 oraz represji transkrypcji Sf1 i Sox9, które jak wiadomo ulegają ekspresji na terenie grzebieni płciowych, które nie osiągnęły jeszcze stanu zdeterminowania do rozwoju w jądra lub jajniki. Niemniej w sferze domysłów pozostaje mechanizm tych wpływów, które mogą mieć charakter interakcji białko-białko (np. tworzenie heterodimeru DAX1:SF1) lub aktywacji nieznanych korepresorów oraz co mało prawdopodone, jak już wspomniano, interakcji DAX1 z DNA. Bardzo możliwe, że każdy z opisanych wariantów oddziaływań ma miejsce i zależy od aktualniego stanu fizjologicznego oraz etapu rozwoju komórek. W systemie różnicowani płci u samic ssaków ogromne znaczenie ma ekspresja jeszcze jednego genu Wnt4, kodującego działającą miejscowo glikoproteinę. Jej funkcja przejawia się promowaniem rozwoju przewodów Müllera oraz supresją różnicowania komórek Leydiga. Jak wykazały badania prowadzone na osobnikach z duplikacjami Wnt4 i Dax1, ich efektem jest nadekspresja tych genów, prowdząca do rozwoju
10 fenotypu żenskiego u osobników o kariotypie XY. Wynik ten świdczy o zaangażowaniu obu genów w proces determinacji płci somatycznej u samic. Przy realizacji omawianego programu rozwojowego, ewidentny jest wpływ białka WNT4, które pozytywnie reguluje ekspresję Dax1 w czym wspomaga go SF1, powodując tym samym zmniejszenie poziomu transkrypcji własnego genu. Charakteryzowane powyżej zależności między ekspresją genów zaangażowanych w determinację, a następnie różnicowanie płci somatycznej u ssaków, coraz częściej skłaniają do wniosku, że w procesie tym mamy raczej do czynienia z wielopoziomową siecią zależności, a nie klasycznym układem hierarchicznym. Jak to wynika z treści niniejszego rozdziału, pełne wyjaśnienie omawianych zagadnień wymaga przeprowadzenia wielu szczegółowych badań, które co należy szczególnie podkreslić, mogą zrewolucjonizować nasz podląd na przebieg rozwoju płci somatycznej u ssaków. Potranskrypcyjna regulacja ekspresji genów jest głównym elementem szlaku różnicowania się płci somatycznej u D. melanogaster Pierwszym sygnałem określającym przebieg determinacji płci somatycznej u D. melanogaster jest stosunek liczbowy X:A. Od niego w dalszej kolejności zależy ekspresja opisanego w jednym z poprzednich podrozdziałów genu Slx (ang. Sex-lethal), który jest aktywny tylko u samic. Decyzja o jego ekspresji podejmowana jest na bardzo wczesnym etapie rozwoju tzn. jeszcze przed tworzeniem się blastodermy i zależy od trzech klas czynników: numeratorów, denominatora i elementów matczynych. Numeratorami określamy grupę genów, które lokują się na chromosomie X. Zaliczamy do nich sisa, sisb, sisc (ang. sisterless) oraz run (ang. runt). Kryterium służącym do klasyfikacji genu do grupy numeratorów jest efekt, jaki powoduje jego duplikacja u zarodka o kariotypie XY oraz delecja u osobników XX. Rezultatem pierwszej aberacji jest śmiertelność samców wynikająca z ekspresji normalnie nieaktywnego u tej płci genu Sxl. Drugi z przypadków wyraża się przez letalny fenotyp samic, wynikający z braku ekspresji Sxl. Mianem denominatora określamy autosomalny gen dpn (ang. deadpan), kodujący czynnik, pełniący funkcję negatywnego regulatora ekspresji Sxl. Produkty sis jak i dpn są czynnikami transkrypcyjnymi z nadrodziny HLH (ang. helix-loop-helix), które mogą tworzyć homodimery, jak i łaczyć sie z innymi białkami tworząc heterodimery. Ostatnią grupę spośród omawianych elementów stanowią czynniki matczyne. Grupujemy je w dwie klasy, pierwszą, która obejmuje produkty genu da (ang. daughterless) i her (ang. hermaphrodite) pozytywnie regulujące transkrypcję Sxl oraz drugą, tworzoną przez czynniki hamujące ten proces produkty emc (ang. extramacrochaetae) i gro (ang. groucho). Podczas determinacji płci główną rolę odgrywają numeratory, natomiast geny matczyne oraz denominator są elementami wspomagającymi, ułatwiającymi interpretację sygnału, który stanowi stosunek X:A. Jest to oczywiste, gdy uświadomimy sobie, że ilość produktów powstających w wyniku ekspresji sis jest dwukrotnie wyższa u samic niż samców, co oczywiście jest podyktowane różną liczbą chromosomów X u osobników każdej z płci. Jedynym problemem w realizacji omawianego procesu mógłby być mechanizm kompensacyjny u samców, niemniej jak się sądzi jest on uruchamiany później w czasie rozwoju, a więc po tym gdy komórki oszacują wartość X:A. Białka SIS, kodowane przez geny numeratory łączą się z produktem denominatora DPN, czego konsekwencją jest wytworzenie heterodimerów, działających jako negatywne regulatory transkrypcji Sxl. W sytuacji dużej ilości SIS, co ma miejsce u samic, tylko część z nich ulega heterodimeryzacji z DPN, natomiast pozostałe mogą wiązać się z produktami matczynego genu da i tym samym aktywować ekspresję Sxl. Rola dwóch pozostałych białek tego systemu, a więc GRO i EMC, jest nadal niejasna. GRO wydaje się pełnić funkcję
11 korepresora wiążącego się z DPN, natomiast EMC prawdopodobnie inaktywuje DA i SISB tworząc z nimi nieaktywne heterodimery. Przebieg poszczególnych etapów determinacji płci u D. melanogaster jest niezwykły, gdyż opiera się głównie na regulacji potranskrypcyjnej. Jeszcze przed powstaniem blastodermy, w żeńskim zarodku obserwujemy wzrost transkrypcji Sxl po aktywacji jednego z dwóch promotorów tego genu, oznaczanego jako Sxl Pe, co z kolei zależy od opisanego powyżej sygnału generowanego stosunkiem X:A. Wkrótce jednak ekspresja ta jest wyciszana na korzyść aktywacji drugiego z promotorów Sxl, oznaczanego Sxl Pm. Transkrypcja ta, zwana późną, ma miejsce u obu płci. Białko SXL, które u samic powstało we wczesnym etapie, a więc podczas aktywności Sxl Pe, reguluje proces składania mrna powstającego w czasie późnej ekspresji Sxl. Ma to na celu usunięcie trzeciego egzonu, a co za tym idzie utworzenia otwartej ramki oddczytu. Podobnej regulacji nie obserwujemy jednak u samców, co jest oczywiste z powodu braku wczesnej ekspresji Sxl rozpoczynającej sięz promotora Sxl Pe. W efekcie powstający późny transkrypt nie jest składany i zawiera trzeci egzon, w którego sekwencji znajduje się kodon stop, co z kolei prowadzi do przedwczesnej terminacji translacji i powstania niefunkcjonalnego białka. SXL może wiązać RNA dzięki dwum konserwatywnym ewolucyjnie domenom, oznaczanym RPM (ang. RNA recognition motif). Białko to łączy się nie tylko z transkryptem własnego genu. Wiadomo bowiem, że w podobny sposób reguluje ekspresję omówionego wcześniej msl-2, zaangażowanego w mechanizm kompensacyjny, jak również genu tra (ang. transformer), który jest kolejnym po Sxl elementem w hierarchicznym systemie determinacji płci somatycznej. Powstanie dojrzałego transkryptu tra z otwartą ramką odczytu, także wymaga funkcjonalnego SXL, co może zostać zrealizowane tylko u samic. Do wyrażenia swej funkcji, białko TRA wymaga partnera, którym jest produkt konstytutywnie eksprymowanego genu tra-2 (ang. transformer-2). TRA i TRA-2 powodują, że spliceosom łączy się w strefie poprzedzającej 4 egzon na terenie transkryptu dsx (ang. doublesex) produktu kolejnego genu. W ostatecznym rozrachunku mrna dsx, jak i tworzone na jego bazie białko u samic mają inną sekwencję, niż analogiczne produkty dsx, które u samców powstają przy braku TRA. Różnice te dotyczą przede wszystkim końca C-terminalnego białek, co określa charakter realizowanych przez nie funkcji. DSXM (występujące u samców) i DSXF (wystepujące u samic) są bowiem regulatorami transkrypcji wiążącymi się z DNA, które wpływaja na ekspresję genów wykonawczych, aktywnych podczas różnicowania płciowego. DSXM aktywuje geny wymagane do rozwoju męskich cech zarodka, jednoczesnie działając jako represor w stosunku do genów promujących powstanie cech żeńskich, natomiast DSXF odwrotnie, zapobiega męskiemu charakterowi różnicowania realizując program wymagany dla rozwoju samic. Do wyrażenia swej funkcji, DSXF wymaga matczynego czynnika her, o którym wspomniano już wcześniej, niemniej mechanizm tej interakcji nie został dotychczas w pełni opisany. Nleży także wspomnieć o trzech dodatkowych genach: snf (ang. sans fille lub splicing necessary factor), fl(2)d (ang. female-lethal(2)d) i vir (ang. virilizer). Pierwszy z nich koduje białko SNF, współdziałające z SXL w maskowaniu miejsc składania 3 egzonu transkryptu Sxl, co powoduje, iż jest on traktowany jak intron i wycinany. Rola pozostałych genów jest niejasna, sądzi się, że one również uczestniczą w regulacji obróbki potranslacyjnej Sxl. Należy także wspomnieć o conajmniej dwóch odstępstwach od reguły zakładającej determinację cech somatycznych zarodka przez dsx. Wiadomo bowiem, że rozwój unerwienia mięśni odwłokowych u samców, podobnie jak i płeć ośrodkowego układu nerwowego (CNS) oraz związana z nim indukcja charakterystycznych dla danej płci zachowań seksualnych, są kontrolowane przez tra. W omawianych procesach białko TRA reguluje ekspresję genów fru (ang. fruitless) i dsf (ang. dissatisfaction), kodujących czynniki transkrypcyjne, bezpośrednio regulujące aktywność genów wykonawczych, w rozwijającym się CNS.
12 W determinacji płci somatycznej C. elegans szczególną rolę odgrywa efekt grupy U C. elegans w determinację płci somatycznej zaangażowanych jest jeszcze więcej genów niż u D. melanogaster, niemniej opiszemy tu funkcję tylko kilku z nich. Podstawowym elementem, który odpowiada za etap wykonawczy procesu, jest czynnik transkrypcyjny TRA- 1, z palcami cynkowymi w domenie wiążącej DNA. Stan aktywności genu, który go koduje, tra-1 (ang. transformer-1), zależy z kolei od ekspresji szeregu czynników odbierających informację o stosunku X:A. Spośród nich najlepiej scharakteryzowanymi są geny her-1 (ang. hermaphroditization) i tra-2. Kodowane przez niego białko TRA-2 jest receptorem błonowym, który w dużej liczbie kopii występuje na terenie komórek o kariotypie XX, a niewielkiej o XO. Z kolei białko HER-1, którego produkcja jest domeną przyszłych męskich komórek, może łaczyć się z receptorem TRA-2, co prowadzi do jego inaktywaji. W sytuacji gdy komórka niezdeterminowana znajdzie się w otoczeniu, gdzie występuje duże stężenie HER-1, jej receptory TRA-2 zostają zablokowane. To wyznacza jej przeznaczenie do stania się komórką męską, co wiąże się bezpośrednio z mobilizacją trzech białek: FEM-1, FEM-2 i FEM-3 kodowanych przez geny fem (ang. feminization), które działaja jako represowy funkcji wykonawczej TRA-1. Z kolei komórka charakteryzująca się wysoką aktywnością HER-1, w sytuacji gdy znajdzie się w otoczeniu komórek posiadających dużą liczbę receptorów TRA-2 ulegnie feminizacji. Jest to oczywiste, gdy wyobrazimy sobie, że nie jest ona w stanie wytworzyć dostatecznej ilości białka HER-1, które blokując receptory TRA-2 doprowadziłoby do maskulinizacji komórek z otoczenia, jak i niej samej. Występujące w dużej liczbie receptory TRA-2 za pomocą swej domeny cytoplazmatycznej, znajdującej się na końcu C-terminalnym białka, wiążą pulę FEM-3, tym samym znosząc hamujący wpływ białek FEM na aktywność TRA-1. Podczas determinacji płci komórek o kariotypie XX, duże znacznie ma także kalpaina TRA-3, która odcina fragment receptora TRA-2 (oznaczany jako TRA-2c), a ten z kolei przemieszcza się do jądra komórkowego, gdzie wzmacnia feminizujący efekt białka TRA-1. Jak wynika z powyższej charakterystyki, w mechanizmie determinacji płci u C. elegans szczególną role odgrywają sygnały molekularne przekazywane między sąsiadujacymi ze sobą komórkami. Mamy tu bowiem do czynienia z klasycznych efektem grupy, który zdefiniowaliśmy na początku rozdziału. Osiąganie stanu przeznaczenia i determinacja płci komórek rozrodczych To czy komórki linii płciowej rozpoczną spermatogenezę, czy oogenezę, zależy od ich genotypu, jak również w bardzo znacznym stopniu od środowiska, które stwarza rozwijająca się gonada. Zasada ta dotyczy wszystkich charakteryzowanych w tym rozdziale gatunków zwierząt. U myszy, pierwotne komórki płciowe (PGC) powstają w epiblaście, a czynnikiem, biorącym udział w ustalaniu ich przeznaczenia jest białko BMP-4 (ang. bone morfogenetic protein 4), wydzielane z pozazarodkowej ektodermy. Około 7 dnia rozwoju, na podstawie wysokiej aktywności alkalicznej fosfatazy, PGC są identyfikowane w pozazarodkowej mezodermie. Stąd migrują do omoczni, a dalej przez endodermę i wzdłuż jelita na teren formujących się grzebieni płciowych. Podczas wędrówki, jak i po osiagnięciu miejsca docelowego, dzielą się mitotycznie. Wtedy też, w PGC o kariotypie XX, dochodzi od reaktywacji wyciszonego chromosomu X oraz wyłączenia ekspresji genu Xist. Dalszy etap, to przygotowanie do mejozy, czego wyrazem jest np. wzrost ekspresji genu Scp3, którego aktywność warunkuje tworzenie kompleksów synaptonemalnych podczas mejozy. Właśnie na tym etapie zachodzi determinacja płci komórek rozrodczych. Jeżeli PGC znajdą się w
13 otoczeniu zarodkowych komórek podporowych jąder, nie rozpoczynają podziału redukcyjnego, pozostając w fazie G1 cyklu komórkowego. Natomiast gdy otoczeniem PGC są tkanki różnicujących się jajników, to wchodzą one w profazę mejotyczną, charakterystyczną dla oogenezy i po osiągnięciu stadium diplotenu, przechodzą w stan spoczynku podziałowego. Zjawisko to nie zależy od zespołu chromosomów płci, jakie niosą ze sobą komórki, co wykazano doświadczalnie w badaniach chimer oraz przeszczepiając komórki linii płciowej samców do rozwijających się jajników, bądź komórki płciowe samic do jąder. Stwierdzono, że PGC stają się oocytami w środowisku jajników, a spermatocytami w jądrach. Z kolei, jeśli PGC zostaną przeniesione w otoczenie komórek somatycznych, np. nadnerczy, to niezależnie od ich genotypu stają się oocytami, gdyż nie otrzymują swoistego sygnału o zatrzymaniu podziałów. Obserwacje te pozwalają na wyciągnięcie dwóch wniosków, po pierwsze, komórki somatyczne gonad determinują sposób różnicowania się PGC, po drugie, decyzja o rozpoczęciu podziałów należy do samych komórek płciowych. W determinacji płci PGC u D. melanogaster mamy do czynienia z kompilacją wpływu otoczenia oraz sygnałów o charakterze autonomicznym, pochodzącym tylko z komórek rozrodczych. PGC u tego gatunku są pierwszymi komórkami jakie powstają podczas rozwoju. Tworzone są w tylnej części bruzdkującego zarodka, a ich cytoplazma, zawiera między innymi tzw. ziarna biegunowe, zbudowane z RNA i białek. Składniki te są głównie produktami genów aktywnych w trofocytach, skąd są transportowane do oocytu podczas jego dojrzewania (stąd nazywane są czynnikami matczynymi). Jednym z nich jest transkrypt genu osc (ang. oscar). Przy udziale białka Staufen (także produkt genu matczynego), transkrypty osc są transportowane do tylnego bieguna jaja, gdzie podlegają translacji. Powstające biłako Oscar, wiąże się ze Staufen oraz Vasa (produkt ekspresji kolejnego genu matczynego - vas). Efektem tych interakcji jest zakotwiczenie cząsteczek mrna osc na elemetach cytoszkieletu plazmy biegunowej (płciowej), a do powstałego kompleksu nukloproteinowego dołączają pozostałe elementy ziaren biegunowych. W rezultacie powstające na tym obszarze komórki dziedziczą charakterystyczne tylko dla nich komponenty, co ostatecznie determinuje ich przeznaczenie jako PGC. Warto zaznaczyć, że liczba powstających PGC zależy od ilości transkryptu oscar, który jest dostarczany do plazmy biegunowej. Wykazano, że przeszczepienie tych komórek z zarodka męskiego do żeńskiego nie zmienia radykalnie charakteru ich różnicowania i rozpoczynają one spermatogenezę. Podobnie zachowują się PGC o kariotypie XX, które zostaną przeniesione do organizmu samca. Na tej podstawie łatwo wywnioskować, że podjęcie decyzji o rozpoczęciu oogenezy wymaga sygnału pochodzącego ze środowiska, natomiast inicjacja spermatogenezy w męskich komórkach, ma charakter autonomiczny. Łatwo też zauważyć, że wpływ sygnałów z męskiego zarodka jest bodźcem o większej sile sprawczej przy określaniu przeznaczenia, niż genotyp jaki niosą ze sobą komórki PGC o kariotypie XX. Mimo intensywnych badań, podłoże molekularne omawianych zjawisk jest wyjątkowo słabo poznane. Istnieje kilka dowodów na udział w omawianym procesie genu Sxl, jednak tutaj nie pełni on roli nadrzędnego czynnika, jak to ma miejsce przy determinacji płci somatycznej, a jego udział jest znacznie silniej zaznaczony podczas rozwoju komórek płciowych u samic niż samców. Aktywność Sxl u osobników XX jest utrzymywana na drodze autoregulacji, tak jak to ma miejsce w komórkach somatycznych, dzięki funkcji snf, fl(2)d i vir, a także dwóch genów aktywnych specyficznie w PGC ovo i out (ang. ovarian tumor). Mechanizm ten jest bardzo słabo poznany. Sxl wydaje się regulować podziały mitotyczne komórek płciowych w germarium (szczytowa część jajnika), zamianę mitozy na mejozę w czasie gametogenezy oraz przebieg crossig-over. Hermafrodytyzm u C. elegans jest zjawiskiem wtórnym, a osobniki obupłciowe wyewoluowały z samic. Dlatego omawiając determinację płci PGC u tego gatunku, trzeba przede wszystkim zwrócić uwagę na mechanizm, który prowadzi do ustalenia męskiego charakteru komórek w ciele osobnika o żeńskich cechach, którego organizm, jak wiadomo
Sposoby determinacji płci
 W CZASIE WYKŁADU TELEFONY KOMÓRKOWE POWINNY BYĆ WYŁĄCZONE LUB WYCISZONE Sposoby determinacji płci TSD thermal sex determination GSD genetic sex determination 26 o C Środowiskowa: ekspresja genu
W CZASIE WYKŁADU TELEFONY KOMÓRKOWE POWINNY BYĆ WYŁĄCZONE LUB WYCISZONE Sposoby determinacji płci TSD thermal sex determination GSD genetic sex determination 26 o C Środowiskowa: ekspresja genu
Sposoby determinacji płci
 Sposoby determinacji płci TSD thermal sex determination GSD genetic sex determination 26 o C Środowiskowa: ekspresja genu DMRT zależna jest od warunków środowiska ~30 o C ~33 o C ~35 o C n=16
Sposoby determinacji płci TSD thermal sex determination GSD genetic sex determination 26 o C Środowiskowa: ekspresja genu DMRT zależna jest od warunków środowiska ~30 o C ~33 o C ~35 o C n=16
Sposoby determinacji płci
 GAMETOGENEZA spermatogonium oogonium spermatocyty I-ego rzędu spermatocyty II-ego rzędu oocyty II-ego rzędu oocyty I-ego rzędu pierwsze ciałko kierunkowe spermatydy ootydy drugie ciałko kierunkowe plemniki
GAMETOGENEZA spermatogonium oogonium spermatocyty I-ego rzędu spermatocyty II-ego rzędu oocyty II-ego rzędu oocyty I-ego rzędu pierwsze ciałko kierunkowe spermatydy ootydy drugie ciałko kierunkowe plemniki
Dr. habil. Anna Salek International Bio-Consulting 1 Germany
 1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
Konspekt do zajęć z przedmiotu Genetyka dla kierunku Położnictwo dr Anna Skorczyk-Werner Katedra i Zakład Genetyki Medycznej
 Seminarium 1 część 1 Konspekt do zajęć z przedmiotu Genetyka dla kierunku Położnictwo dr Anna Skorczyk-Werner Katedra i Zakład Genetyki Medycznej Genom człowieka Genomem nazywamy całkowitą ilość DNA jaka
Seminarium 1 część 1 Konspekt do zajęć z przedmiotu Genetyka dla kierunku Położnictwo dr Anna Skorczyk-Werner Katedra i Zakład Genetyki Medycznej Genom człowieka Genomem nazywamy całkowitą ilość DNA jaka
Temat 6: Genetyczne uwarunkowania płci. Cechy sprzężone z płcią.
 Temat 6: Genetyczne uwarunkowania płci. Cechy sprzężone z płcią. 1. Kariotyp człowieka. 2. Determinacja płci u człowieka. 3. Warunkowanie płci u innych organizmów. 4. Cechy związane z płcią. 5. Cechy sprzężone
Temat 6: Genetyczne uwarunkowania płci. Cechy sprzężone z płcią. 1. Kariotyp człowieka. 2. Determinacja płci u człowieka. 3. Warunkowanie płci u innych organizmów. 4. Cechy związane z płcią. 5. Cechy sprzężone
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
Modyfikacje epigenetyczne w czasie wzrostu oocytów związane z rozszerzeniem rozwoju partenogenetycznego u myszy. Małgorzata Karney
 Modyfikacje epigenetyczne w czasie wzrostu oocytów związane z rozszerzeniem rozwoju partenogenetycznego u myszy. Małgorzata Karney Epigenetyka Epigenetyka zwykle definiowana jest jako nauka o dziedzicznych
Modyfikacje epigenetyczne w czasie wzrostu oocytów związane z rozszerzeniem rozwoju partenogenetycznego u myszy. Małgorzata Karney Epigenetyka Epigenetyka zwykle definiowana jest jako nauka o dziedzicznych
Imię i nazwisko...kl...
 Gimnazjum nr 4 im. Ojca Świętego Jana Pawła II we Wrocławiu SPRAWDZIAN GENETYKA GR. A Imię i nazwisko...kl.... 1. Nauka o regułach i mechanizmach dziedziczenia to: (0-1pkt) a) cytologia b) biochemia c)
Gimnazjum nr 4 im. Ojca Świętego Jana Pawła II we Wrocławiu SPRAWDZIAN GENETYKA GR. A Imię i nazwisko...kl.... 1. Nauka o regułach i mechanizmach dziedziczenia to: (0-1pkt) a) cytologia b) biochemia c)
Interfaza to niemal 90% cyklu komórkowego. Dzieli się na 3 fazy: G1, S i G2.
 W wyniku podziału komórki powstaje komórka potomna, która ma o połowę mniej DNA od komórki macierzystej i jest o połowę mniejsza. Aby komórka potomna była zdolna do kolejnego podziału musi osiągnąć rozmiary
W wyniku podziału komórki powstaje komórka potomna, która ma o połowę mniej DNA od komórki macierzystej i jest o połowę mniejsza. Aby komórka potomna była zdolna do kolejnego podziału musi osiągnąć rozmiary
The Maternal Nucleolus Is Essential for Early Embryonic Development in Mammals
 The Maternal Nucleolus Is Essential for Early Embryonic Development in Mammals autorstwa Sugako Ogushi Science vol 319, luty 2008 Prezentacja Kamil Kowalski Jąderko pochodzenia matczynego jest konieczne
The Maternal Nucleolus Is Essential for Early Embryonic Development in Mammals autorstwa Sugako Ogushi Science vol 319, luty 2008 Prezentacja Kamil Kowalski Jąderko pochodzenia matczynego jest konieczne
Pamiętając o komplementarności zasad azotowych, dopisz sekwencję nukleotydów brakującej nici DNA. A C C G T G C C A A T C G A...
 1. Zadanie (0 2 p. ) Porównaj mitozę i mejozę, wpisując do tabeli podane określenia oraz cyfry. ta sama co w komórce macierzystej, o połowę mniejsza niż w komórce macierzystej, gamety, komórki budujące
1. Zadanie (0 2 p. ) Porównaj mitozę i mejozę, wpisując do tabeli podane określenia oraz cyfry. ta sama co w komórce macierzystej, o połowę mniejsza niż w komórce macierzystej, gamety, komórki budujące
Gonocyty komórki prapłciowe
 GAMETOGENEZA Gametogeneza Gametogeneza (z grec. gamete żona, gametes mąż) Proces powstawania oraz rozwoju specjalnej populacji komórek, które nazywa się gametami lub komórkami rozrodczymi. Mejoza i różnicowanie
GAMETOGENEZA Gametogeneza Gametogeneza (z grec. gamete żona, gametes mąż) Proces powstawania oraz rozwoju specjalnej populacji komórek, które nazywa się gametami lub komórkami rozrodczymi. Mejoza i różnicowanie
Materiały dydaktyczne do kursów wyrównawczych z przedmiotu biologia
 Człowiek najlepsza inwestycja Materiały dydaktyczne do kursów wyrównawczych z przedmiotu biologia Autor: dr inż. Anna Kostka Projekt współfinansowany ze środków Unii Europejskiej w ramach Europejskiego
Człowiek najlepsza inwestycja Materiały dydaktyczne do kursów wyrównawczych z przedmiotu biologia Autor: dr inż. Anna Kostka Projekt współfinansowany ze środków Unii Europejskiej w ramach Europejskiego
Epigenetic modifications during oocyte growth correlates with extended parthenogenetic developement in the mouse
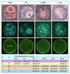 Epigenetic modifications during oocyte growth correlates with extended parthenogenetic developement in the mouse Tomohiro Kono, Yayoi Obata, Tomomi Yoshimzu, Tatsuo Nakahara & John Carroll Rozwój partenogenetyczny
Epigenetic modifications during oocyte growth correlates with extended parthenogenetic developement in the mouse Tomohiro Kono, Yayoi Obata, Tomomi Yoshimzu, Tatsuo Nakahara & John Carroll Rozwój partenogenetyczny
Disruption of c-mos causes parthenogenetic development of unfertilized mouse eggs
 Disruption of c-mos causes parthenogenetic development of unfertilized mouse eggs W. H. Colledge, M. B. L. Carlton, G. B. Udy & M. J. Evans przygotowała Katarzyna Czajkowska 1 Dysrupcja (rozbicie) genu
Disruption of c-mos causes parthenogenetic development of unfertilized mouse eggs W. H. Colledge, M. B. L. Carlton, G. B. Udy & M. J. Evans przygotowała Katarzyna Czajkowska 1 Dysrupcja (rozbicie) genu
Komórka stuktura i funkcje. Bogusław Nedoszytko. WSZPIZU Wydział w Gdyni
 Komórka stuktura i funkcje Bogusław Nedoszytko WSZPIZU Wydział w Gdyni Jądro komórkowe Struktura i funkcje Podziały komórkowe Jądro komórkowe 46 chromosomów 2,6 metra DNA 3 miliardy par nukleotydów (A,T,G,C)
Komórka stuktura i funkcje Bogusław Nedoszytko WSZPIZU Wydział w Gdyni Jądro komórkowe Struktura i funkcje Podziały komórkowe Jądro komórkowe 46 chromosomów 2,6 metra DNA 3 miliardy par nukleotydów (A,T,G,C)
Konkurs szkolny Mistrz genetyki etap II
 onkurs szkolny istrz genetyki etap II 1.W D pewnego pierwotniaka tymina stanowi 28 % wszystkich zasad azotowych. blicz i zapisz, jaka jest zawartość procentowa każdej z pozostałych zasad w D tego pierwotniaka.
onkurs szkolny istrz genetyki etap II 1.W D pewnego pierwotniaka tymina stanowi 28 % wszystkich zasad azotowych. blicz i zapisz, jaka jest zawartość procentowa każdej z pozostałych zasad w D tego pierwotniaka.
TATA box. Enhancery. CGCG ekson intron ekson intron ekson CZĘŚĆ KODUJĄCA GENU TERMINATOR. Elementy regulatorowe
 Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
Promotory genu Promotor bliski leży w odległości do 40 pz od miejsca startu transkrypcji, zawiera kasetę TATA. Kaseta TATA to silnie konserwowana sekwencja TATAAAA, występująca w większości promotorów
października 2013: Elementarz biologii molekularnej. Wykład nr 2 BIOINFORMATYKA rok II
 10 października 2013: Elementarz biologii molekularnej www.bioalgorithms.info Wykład nr 2 BIOINFORMATYKA rok II Komórka: strukturalna i funkcjonalne jednostka organizmu żywego Jądro komórkowe: chroniona
10 października 2013: Elementarz biologii molekularnej www.bioalgorithms.info Wykład nr 2 BIOINFORMATYKA rok II Komórka: strukturalna i funkcjonalne jednostka organizmu żywego Jądro komórkowe: chroniona
Fragment cząsteczki DNA stanowiący matrycę dla syntezy cząsteczki lub podjednostki białka nazywamy GENEM
 KONTROLA EKSPRESJI GENU PRZEKAZYWANIE INFORMACJI GENETYCZNEJ Informacja genetyczna - instrukcje kierujące wszystkimi funkcjami komórki lub organizmu zapisane jako określone, swoiste sekwencje nukleotydów
KONTROLA EKSPRESJI GENU PRZEKAZYWANIE INFORMACJI GENETYCZNEJ Informacja genetyczna - instrukcje kierujące wszystkimi funkcjami komórki lub organizmu zapisane jako określone, swoiste sekwencje nukleotydów
Disruption of c-mos causes parthenogenetic develepment of unfertilized mouse eggs. W.H Colledge, M.B.L. Carlton, G.B. Udy & M.J.
 Disruption of c-mos causes parthenogenetic develepment of unfertilized mouse eggs. W.H Colledge, M.B.L. Carlton, G.B. Udy & M.J.Evans Partenogeneza-dzieworództwo, to sposób rozmnażania polegający na rozwoju
Disruption of c-mos causes parthenogenetic develepment of unfertilized mouse eggs. W.H Colledge, M.B.L. Carlton, G.B. Udy & M.J.Evans Partenogeneza-dzieworództwo, to sposób rozmnażania polegający na rozwoju
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 5 Droga od genu do
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Wykład 5 Droga od genu do
Sposoby determinacji płci
 Gametogeneza, determinacja płci Sposoby determinacji płci TSD thermal sex determination GSD genetic sex determination SPOSOBY DETERMINACJI PŁCI 26 o C Środowiskowa: ekspresja genu DMRT zależna
Gametogeneza, determinacja płci Sposoby determinacji płci TSD thermal sex determination GSD genetic sex determination SPOSOBY DETERMINACJI PŁCI 26 o C Środowiskowa: ekspresja genu DMRT zależna
Wykład 14 Biosynteza białek
 BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ gamety matczyne Genetyka
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ gamety matczyne Genetyka
Biologia molekularna z genetyką
 Biologia molekularna z genetyką P. Golik i M. Koper Konwersatorium 2: Analiza genetyczna eukariontów Drosophilla melanogaster Makrokierunek: Bioinformatyka i Biologia Systemów; 2016 Opracowano na podstawie
Biologia molekularna z genetyką P. Golik i M. Koper Konwersatorium 2: Analiza genetyczna eukariontów Drosophilla melanogaster Makrokierunek: Bioinformatyka i Biologia Systemów; 2016 Opracowano na podstawie
Bezpośrednia embriogeneza somatyczna
 Bezpośrednia embriogeneza somatyczna Zarodki somatyczne formują się bezpośrednio tylko z tych komórek roślinnych, które są kompetentne już w momencie izolowania z rośliny macierzystej, czyli z proembriogenicznie
Bezpośrednia embriogeneza somatyczna Zarodki somatyczne formują się bezpośrednio tylko z tych komórek roślinnych, które są kompetentne już w momencie izolowania z rośliny macierzystej, czyli z proembriogenicznie
mikrosatelitarne, minisatelitarne i polimorfizm liczby kopii
 Zawartość 139371 1. Wstęp zarys historii genetyki, czyli od genetyki klasycznej do genomiki 2. Chromosomy i podziały jądra komórkowego 2.1. Budowa chromosomu 2.2. Barwienie prążkowe chromosomów 2.3. Mitoza
Zawartość 139371 1. Wstęp zarys historii genetyki, czyli od genetyki klasycznej do genomiki 2. Chromosomy i podziały jądra komórkowego 2.1. Budowa chromosomu 2.2. Barwienie prążkowe chromosomów 2.3. Mitoza
TRANSKRYPCJA - I etap ekspresji genów
 Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Eksparesja genów TRANSKRYPCJA - I etap ekspresji genów Przepisywanie informacji genetycznej z makrocząsteczki DNA na mniejsze i bardziej funkcjonalne cząsteczki pre-mrna Polimeraza RNA ETAP I Inicjacja
Komórka eukariotyczna
 Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Komórka eukariotyczna http://pl.wikipedia.org/w/index.php?title=plik:hela_cells_stained_with_hoechst_33258.jpg cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii,
Zmienność. środa, 23 listopada 11
 Zmienność http://ggoralski.com Zmienność Zmienność - rodzaje Zmienność obserwuje się zarówno między poszczególnymi osobnikami jak i między populacjami. Różnice te mogą mieć jednak różne podłoże. Mogą one
Zmienność http://ggoralski.com Zmienność Zmienność - rodzaje Zmienność obserwuje się zarówno między poszczególnymi osobnikami jak i między populacjami. Różnice te mogą mieć jednak różne podłoże. Mogą one
6. Z pięciowęglowego cukru prostego, zasady azotowej i reszty kwasu fosforowego, jest zbudowany A. nukleotyd. B. aminokwas. C. enzym. D. wielocukier.
 ID Testu: F5679R8 Imię i nazwisko ucznia Klasa Data 1. Na indywidualne cechy danego osobnika ma (maja) wpływ A. wyłacznie czynniki środowiskowe. B. czynniki środowiskowe i materiał genetyczny. C. wyłacznie
ID Testu: F5679R8 Imię i nazwisko ucznia Klasa Data 1. Na indywidualne cechy danego osobnika ma (maja) wpływ A. wyłacznie czynniki środowiskowe. B. czynniki środowiskowe i materiał genetyczny. C. wyłacznie
INICJACJA ELONGACJA TERMINACJA
 INICJACJA ELONGACJA TERMINACJA 2007 by National Academy of Sciences Kornberg R D PNAS 2007;104:12955-12961 Struktura chromatyny pozwala na różny sposób odczytania informacji zawartej w DNA. Możliwe staje
INICJACJA ELONGACJA TERMINACJA 2007 by National Academy of Sciences Kornberg R D PNAS 2007;104:12955-12961 Struktura chromatyny pozwala na różny sposób odczytania informacji zawartej w DNA. Możliwe staje
WYKŁAD: Klasyczny przepływ informacji ( Dogmat) Klasyczny przepływ informacji. Ekspresja genów realizacja informacji zawartej w genach
 WYKŁAD: Ekspresja genów realizacja informacji zawartej w genach Prof. hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Klasyczny przepływ informacji ( Dogmat) Białka Retrowirusy Białka Klasyczny
WYKŁAD: Ekspresja genów realizacja informacji zawartej w genach Prof. hab. n. med. Małgorzata Milkiewicz Zakład Biologii Medycznej Klasyczny przepływ informacji ( Dogmat) Białka Retrowirusy Białka Klasyczny
GENETYCZNE PODSTAWY ZMIENNOŚCI ORGANIZMÓW ZASADY DZIEDZICZENIA CECH PODSTAWY GENETYKI POPULACYJNEJ
 GENETYCZNE PODSTAWY ZMIENNOŚCI ORGANIZMÓW ZASADY DZIEDZICZENIA CECH PODSTAWY GENETYKI POPULACYJNEJ ZMIENNOŚĆ - występowanie dziedzicznych i niedziedzicznych różnic między osobnikami należącymi do tej samej
GENETYCZNE PODSTAWY ZMIENNOŚCI ORGANIZMÓW ZASADY DZIEDZICZENIA CECH PODSTAWY GENETYKI POPULACYJNEJ ZMIENNOŚĆ - występowanie dziedzicznych i niedziedzicznych różnic między osobnikami należącymi do tej samej
Wykład 5. Remodeling chromatyny
 Wykład 5 Remodeling chromatyny 1 Plan wykładu: 1. Przebudowa chromatyny 2. Struktura, funkcje oraz mechanizm działania kompleksów remodelujących chromatynę 3. Charakterystyka kompleksów typu SWI/SNF 4.
Wykład 5 Remodeling chromatyny 1 Plan wykładu: 1. Przebudowa chromatyny 2. Struktura, funkcje oraz mechanizm działania kompleksów remodelujących chromatynę 3. Charakterystyka kompleksów typu SWI/SNF 4.
TERMINY BIOLOGICZNE. ZADANIE 5 (3 pkt) Na podstawie ryc. 2 wykonaj polecenia: B. Ustal, w którym etapie cyklu tej komórki kaŝdy
 KARTA PRACY Porównanie mitozy i mejozy ZADANIE 1 (1 pkt) Zaznacz odpowiedź opisującą efekt podziału mitotycznego komórki zawierającej 16 chromosomów. a). 2 komórki zawierające po 8 chromosomów; b). 2 komórki
KARTA PRACY Porównanie mitozy i mejozy ZADANIE 1 (1 pkt) Zaznacz odpowiedź opisującą efekt podziału mitotycznego komórki zawierającej 16 chromosomów. a). 2 komórki zawierające po 8 chromosomów; b). 2 komórki
GIMNAZJUM SPRAWDZIANY SUKCES W NAUCE
 GIMNAZJUM SPRAWDZIANY BIOLOGIA klasa III SUKCES W NAUCE II GENETYKA CZŁOWIEKA Zadanie 1. Cechy organizmu są warunkowane przez allele dominujące i recesywne. Uzupełnij tabelę, wykorzystując poniższe określenia,
GIMNAZJUM SPRAWDZIANY BIOLOGIA klasa III SUKCES W NAUCE II GENETYKA CZŁOWIEKA Zadanie 1. Cechy organizmu są warunkowane przez allele dominujące i recesywne. Uzupełnij tabelę, wykorzystując poniższe określenia,
I. Genetyka. Dział programu Lp. Temat konieczny podstawowy rozszerzający
 I. Genetyka 1. Czym jest genetyka? wymienia cechy gatunkowe i indywidualne podanych organizmów wyjaśnia, że jego podobieństwo do rodziców jest wynikiem dziedziczenia cech definiuje pojęcia genetyka oraz
I. Genetyka 1. Czym jest genetyka? wymienia cechy gatunkowe i indywidualne podanych organizmów wyjaśnia, że jego podobieństwo do rodziców jest wynikiem dziedziczenia cech definiuje pojęcia genetyka oraz
Informacje dotyczące pracy kontrolnej
 Informacje dotyczące pracy kontrolnej Słuchacze, którzy z przyczyn usprawiedliwionych nie przystąpili do pracy kontrolnej lub otrzymali z niej ocenę negatywną zobowiązani są do dnia 06 grudnia 2015 r.
Informacje dotyczące pracy kontrolnej Słuchacze, którzy z przyczyn usprawiedliwionych nie przystąpili do pracy kontrolnej lub otrzymali z niej ocenę negatywną zobowiązani są do dnia 06 grudnia 2015 r.
TRANSLACJA II etap ekspresji genów
 TRANSLACJA II etap ekspresji genów Tłumaczenie informacji genetycznej zawartej w mrna (po transkrypcji z DNA) na aminokwasy budujące konkretne białko. trna Operon (wg. Jacob i Monod) Zgrupowane w jednym
TRANSLACJA II etap ekspresji genów Tłumaczenie informacji genetycznej zawartej w mrna (po transkrypcji z DNA) na aminokwasy budujące konkretne białko. trna Operon (wg. Jacob i Monod) Zgrupowane w jednym
PODSTAWY GENETYKI. Prowadzący wykład: prof. dr hab. Jarosław Burczyk
 PODSTAWY GENETYKI Prawa Mendla (jako punkt wyjścia) Epistaza (interakcje między genami) Sprzężenia genetyczne i mapowanie genów Sprzężenie z płcią Analiza rodowodów Prowadzący wykład: prof. dr hab. Jarosław
PODSTAWY GENETYKI Prawa Mendla (jako punkt wyjścia) Epistaza (interakcje między genami) Sprzężenia genetyczne i mapowanie genów Sprzężenie z płcią Analiza rodowodów Prowadzący wykład: prof. dr hab. Jarosław
Plan wykładów z genetyki ogólnej
 Plan wykładów z genetyki ogólnej 01 Metody genetyki klasycznej 02 Metody analizy DNA 03 Metody analizy genomu 04 Genomy prokariontów 05 Genomy eukariontów 06 Zmienność genomów w populacjach 07 Genomy a
Plan wykładów z genetyki ogólnej 01 Metody genetyki klasycznej 02 Metody analizy DNA 03 Metody analizy genomu 04 Genomy prokariontów 05 Genomy eukariontów 06 Zmienność genomów w populacjach 07 Genomy a
Nowoczesne systemy ekspresji genów
 Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Prezentuje: Magdalena Jasińska
 Prezentuje: Magdalena Jasińska W którym momencie w rozwoju embrionalnym myszy rozpoczyna się endogenna transkrypcja? Hipoteza I: Endogenna transkrypcja rozpoczyna się w embrionach będących w stadium 2-komórkowym
Prezentuje: Magdalena Jasińska W którym momencie w rozwoju embrionalnym myszy rozpoczyna się endogenna transkrypcja? Hipoteza I: Endogenna transkrypcja rozpoczyna się w embrionach będących w stadium 2-komórkowym
CYKL KOMÓRKOWY I PODZIAŁY KOMÓRKOWE
 CYKL KOMÓRKOWY I PODZIAŁY KOMÓRKOWE 1. Cykl komórkowy. Każda komórka powstaje z już istniejącej komórki. Nowe komórki powstają więc z podziału innych, tzw. komórek macierzystych. Po powstaniu komórki rosną,
CYKL KOMÓRKOWY I PODZIAŁY KOMÓRKOWE 1. Cykl komórkowy. Każda komórka powstaje z już istniejącej komórki. Nowe komórki powstają więc z podziału innych, tzw. komórek macierzystych. Po powstaniu komórki rosną,
Praca kontrolna z biologii LO dla dorosłych semestr V
 Praca kontrolna z biologii LO dla dorosłych semestr V Poniższa praca składa się z 15 zadań. Przy każdym poleceniu podano liczbę punktów możliwą do uzyskania za prawidłową odpowiedź. Za rozwiązanie zadań
Praca kontrolna z biologii LO dla dorosłych semestr V Poniższa praca składa się z 15 zadań. Przy każdym poleceniu podano liczbę punktów możliwą do uzyskania za prawidłową odpowiedź. Za rozwiązanie zadań
Zgodnie z tzw. modelem interpunkcji trna, cząsteczki mt-trna wyznaczają miejsca
 Tytuł pracy: Autor: Promotor rozprawy: Recenzenci: Funkcje białek ELAC2 i SUV3 u ssaków i ryb Danio rerio. Praca doktorska wykonana w Instytucie Genetyki i Biotechnologii, Wydział Biologii UW Lien Brzeźniak
Tytuł pracy: Autor: Promotor rozprawy: Recenzenci: Funkcje białek ELAC2 i SUV3 u ssaków i ryb Danio rerio. Praca doktorska wykonana w Instytucie Genetyki i Biotechnologii, Wydział Biologii UW Lien Brzeźniak
Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii
 Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii 1. Technologia rekombinowanego DNA jest podstawą uzyskiwania genetycznie zmodyfikowanych organizmów 2. Medycyna i ochrona zdrowia
Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii 1. Technologia rekombinowanego DNA jest podstawą uzyskiwania genetycznie zmodyfikowanych organizmów 2. Medycyna i ochrona zdrowia
Kono et al. Nature, 2004
 Kono et al. Nature, 2004 Aleksandra Respondek Listopad 2011 Partenogeneza odmiana rozmnażania, polegająca na rozwoju osobników potomnych z komórki jajowej bez udziału plemnika Naturalnie: wrotki nicienie
Kono et al. Nature, 2004 Aleksandra Respondek Listopad 2011 Partenogeneza odmiana rozmnażania, polegająca na rozwoju osobników potomnych z komórki jajowej bez udziału plemnika Naturalnie: wrotki nicienie
Geny i działania na nich
 Metody bioinformatyki Geny i działania na nich prof. dr hab. Jan Mulawka Trzy królestwa w biologii Prokaryota organizmy, których komórki nie zawierają jądra, np. bakterie Eukaryota - organizmy, których
Metody bioinformatyki Geny i działania na nich prof. dr hab. Jan Mulawka Trzy królestwa w biologii Prokaryota organizmy, których komórki nie zawierają jądra, np. bakterie Eukaryota - organizmy, których
Algorytm genetyczny (genetic algorithm)-
 Optymalizacja W praktyce inżynierskiej często zachodzi potrzeba znalezienia parametrów, dla których system/urządzenie będzie działać w sposób optymalny. Klasyczne podejście do optymalizacji: sformułowanie
Optymalizacja W praktyce inżynierskiej często zachodzi potrzeba znalezienia parametrów, dla których system/urządzenie będzie działać w sposób optymalny. Klasyczne podejście do optymalizacji: sformułowanie
Napisz, który z przedstawionych schematycznie rodzajów replikacji (A, B czy C) ilustruje replikację semikonserwatywną. Wyjaśnij, na czym polega ten
 Napisz, który z przedstawionych schematycznie rodzajów replikacji (A, B czy C) ilustruje replikację semikonserwatywną. Wyjaśnij, na czym polega ten proces. Na schemacie przedstawiono etapy przekazywania
Napisz, który z przedstawionych schematycznie rodzajów replikacji (A, B czy C) ilustruje replikację semikonserwatywną. Wyjaśnij, na czym polega ten proces. Na schemacie przedstawiono etapy przekazywania
Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej
 Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej PRAKTIKUM Z BIOLOGII KOMÓRKI () ćwiczenie prowadzone we współpracy z Pracownią Biofizyki Komórki Badanie dynamiki białek
Badanie dynamiki białek jądrowych w żywych komórkach metodą mikroskopii konfokalnej PRAKTIKUM Z BIOLOGII KOMÓRKI () ćwiczenie prowadzone we współpracy z Pracownią Biofizyki Komórki Badanie dynamiki białek
Tematyka zajęć z biologii
 Tematyka zajęć z biologii klasy: I Lp. Temat zajęć Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania, wymaganiami edukacyjnymi i podstawą programową Podstawowe zagadnienia materiału nauczania
Tematyka zajęć z biologii klasy: I Lp. Temat zajęć Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania, wymaganiami edukacyjnymi i podstawą programową Podstawowe zagadnienia materiału nauczania
CHOROBY NOWOTWOROWE. Twór składający się z patologicznych komórek
 CHOROBY NOWOTWOROWE Twór składający się z patologicznych komórek Powstały w wyniku wielostopniowej przemiany zwanej onkogenezą lub karcinogenezą Morfologicznie ma strukturę zbliżoną do tkanki prawidłowej,
CHOROBY NOWOTWOROWE Twór składający się z patologicznych komórek Powstały w wyniku wielostopniowej przemiany zwanej onkogenezą lub karcinogenezą Morfologicznie ma strukturę zbliżoną do tkanki prawidłowej,
Biologiczne podstawy ewolucji. Informacja genetyczna. Co to jest ewolucja.
 Biologiczne podstawy ewolucji. Informacja genetyczna. Co to jest ewolucja. Historia } Selekcja w hodowli zwierząt, co najmniej 10 000 lat temu } Sztuczne zapłodnienie (np. drzewa daktylowe) 1000 lat temu
Biologiczne podstawy ewolucji. Informacja genetyczna. Co to jest ewolucja. Historia } Selekcja w hodowli zwierząt, co najmniej 10 000 lat temu } Sztuczne zapłodnienie (np. drzewa daktylowe) 1000 lat temu
THE UNFOLDED PROTEIN RESPONSE
 THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
THE UNFOLDED PROTEIN RESPONSE Anna Czarnecka Źródło: Intercellular signaling from the endoplasmatic reticulum to the nucleus: the unfolded protein response in yeast and mammals Ch. Patil & P. Walter The
Badanie funkcji genu
 Badanie funkcji genu Funkcję genu można zbadać różnymi sposobami Przypadkowa analizy funkcji genu MUTACJA FENOTYP GEN Strategia ukierunkowanej analizy funkcji genu GEN 1. wprowadzenie mutacji w genie 2.
Badanie funkcji genu Funkcję genu można zbadać różnymi sposobami Przypadkowa analizy funkcji genu MUTACJA FENOTYP GEN Strategia ukierunkowanej analizy funkcji genu GEN 1. wprowadzenie mutacji w genie 2.
Podstawowe techniki barwienia chromosomów
 Prążek C Chromatyna nie kondensuje równomiernie! Euchromatyna-najmniej kondensująca (fragmenty helisy DNA bogate w guaninę i cytozynę) Heterochromatyna fakultatywna Jasne prążki G Ciemne prążki G Heterochromatyna
Prążek C Chromatyna nie kondensuje równomiernie! Euchromatyna-najmniej kondensująca (fragmenty helisy DNA bogate w guaninę i cytozynę) Heterochromatyna fakultatywna Jasne prążki G Ciemne prążki G Heterochromatyna
Podziały komórkowe cz. I
 Podziały komórkowe cz. I Tam gdzie powstaje komórka, musi istnieć komórka poprzednia, tak samo jak zwierzęta mogą powstawać tylko ze zwierząt, a rośliny z roślin. Ta doktryna niesie głębokie przesłanie
Podziały komórkowe cz. I Tam gdzie powstaje komórka, musi istnieć komórka poprzednia, tak samo jak zwierzęta mogą powstawać tylko ze zwierząt, a rośliny z roślin. Ta doktryna niesie głębokie przesłanie
MOLEKULARNE MECHANIZMY DETERMINACJI PŁCI
 MOLEKULARNE MECHANIZMY DETERMINACJI PŁCI Anna C. Majewska EFEKT KOŃCOWY Po zakończeniu seminarium powinieneś umieć: omówić chromosomowe mechanizmy determinacji płci, omówić środowiskowy mechanizm determinacji
MOLEKULARNE MECHANIZMY DETERMINACJI PŁCI Anna C. Majewska EFEKT KOŃCOWY Po zakończeniu seminarium powinieneś umieć: omówić chromosomowe mechanizmy determinacji płci, omówić środowiskowy mechanizm determinacji
Geny, a funkcjonowanie organizmu
 Geny, a funkcjonowanie organizmu Wprowadzenie do genów letalnych Geny kodują Białka Kwasy rybonukleinowe 1 Geny Występują zwykle w 2 kopiach Kopia pochodząca od matki Kopia pochodząca od ojca Ekspresji
Geny, a funkcjonowanie organizmu Wprowadzenie do genów letalnych Geny kodują Białka Kwasy rybonukleinowe 1 Geny Występują zwykle w 2 kopiach Kopia pochodząca od matki Kopia pochodząca od ojca Ekspresji
Cykl komórkowy. Rozmnażanie komórek G 1, S, G 2. (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza)
 Rozmnażanie komórek (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza) G 1, S, G 2 podział komórki (faza M) Obejmuje: podwojenie zawartości komórki (skopiowanie
Rozmnażanie komórek (powstanie 2 identycznych genetycznie komórek potomnych): podwojenie zawartości (interfaza) G 1, S, G 2 podział komórki (faza M) Obejmuje: podwojenie zawartości komórki (skopiowanie
The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna
 Streszczenie rozprawy doktorskiej pt. The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna mgr Tomasz Turowski, promotor prof. dr hab.
Streszczenie rozprawy doktorskiej pt. The Role of Maf1 Protein in trna Processing and Stabilization / Rola białka Maf1 w dojrzewaniu i kontroli stabilności trna mgr Tomasz Turowski, promotor prof. dr hab.
Składniki diety a stabilność struktury DNA
 Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Składniki diety a stabilność struktury DNA 1 DNA jedyna makrocząsteczka, której synteza jest ściśle kontrolowana, a powstałe błędy są naprawiane DNA jedyna makrocząsteczka naprawiana in vivo Replikacja
Czy grozi nam seksmisja? Renata Gontarz
 Czy grozi nam seksmisja? Renata Gontarz Dominujący Y TDF (ang. testisdetermining factor) = SRY (ang. Sexdetermining region Y) Za Aitken, J.R. & Krausz, C. Reprod. 122, 497-506 (2001) Determinacja płci
Czy grozi nam seksmisja? Renata Gontarz Dominujący Y TDF (ang. testisdetermining factor) = SRY (ang. Sexdetermining region Y) Za Aitken, J.R. & Krausz, C. Reprod. 122, 497-506 (2001) Determinacja płci
BIOLOGIA KOMÓRKI - KARIOKINEZY
 BIOLOGIA KOMÓRKI - KARIOKINEZY M A Ł G O R Z A T A Ś L I W I Ń S K A 60 µm 1. KOMÓRKI SĄ ZBYT MAŁE, BY OBSERWOWAĆ JE BEZ POWIĘKSZENIA Wymiary komórek podaje się w mikrometrach (µm): 1 µm = 10-6 m; 1000
BIOLOGIA KOMÓRKI - KARIOKINEZY M A Ł G O R Z A T A Ś L I W I Ń S K A 60 µm 1. KOMÓRKI SĄ ZBYT MAŁE, BY OBSERWOWAĆ JE BEZ POWIĘKSZENIA Wymiary komórek podaje się w mikrometrach (µm): 1 µm = 10-6 m; 1000
WPROWADZENIE DO GENETYKI MOLEKULARNEJ
 WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
Podział komórkowy u bakterii
 Mitoza Podział komórkowy u bakterii Najprostszy i najszybszy podział komórkowy występuje u bakterii, które nie mają jądra komórkowego, lecz jedynie pojedynczy chromosom tzw. chromosom bakteryjny. Podczas
Mitoza Podział komórkowy u bakterii Najprostszy i najszybszy podział komórkowy występuje u bakterii, które nie mają jądra komórkowego, lecz jedynie pojedynczy chromosom tzw. chromosom bakteryjny. Podczas
ZARZĄDZANIE POPULACJAMI ZWIERZĄT
 ZARZĄDZANIE POPULACJAMI ZWIERZĄT Ćwiczenia 1 mgr Magda Kaczmarek-Okrój magda_kaczmarek_okroj@sggw.pl 1 ZAGADNIENIA struktura genetyczna populacji obliczanie frekwencji genotypów obliczanie frekwencji alleli
ZARZĄDZANIE POPULACJAMI ZWIERZĄT Ćwiczenia 1 mgr Magda Kaczmarek-Okrój magda_kaczmarek_okroj@sggw.pl 1 ZAGADNIENIA struktura genetyczna populacji obliczanie frekwencji genotypów obliczanie frekwencji alleli
GENETYKA. Genetyka. Dziedziczność przekazywanie cech rodziców potomstwu Zmienność występowanie różnic pomiędzy różnymi osobnikami tego samego gatunku
 GENETYKA Genetyka Nauka o dziedziczności i zmienności organizmów, wyjaśniająca prawa rządzące podobieństwami i różnicami pomiędzy osobnikami spokrewnionymi przez wspólnego przodka Dziedziczność przekazywanie
GENETYKA Genetyka Nauka o dziedziczności i zmienności organizmów, wyjaśniająca prawa rządzące podobieństwami i różnicami pomiędzy osobnikami spokrewnionymi przez wspólnego przodka Dziedziczność przekazywanie
Jak działają geny. Podstawy biologii molekularnej genu
 Jak działają geny Podstawy biologii molekularnej genu Uniwersalność życia Podstawowe mechanizmy są takie same u wszystkich znanych organizmów budowa DNA i RNA kod genetyczny repertuar aminokwasów budujących
Jak działają geny Podstawy biologii molekularnej genu Uniwersalność życia Podstawowe mechanizmy są takie same u wszystkich znanych organizmów budowa DNA i RNA kod genetyczny repertuar aminokwasów budujących
BUDOWA I FUNKCJA GENOMU LUDZKIEGO
 BUDOWA I FUNKCJA GENOMU LUDZKIEGO Magdalena Mayer Katedra i Zakład Genetyki Medycznej UM w Poznaniu 1. Projekt poznania genomu człowieka: Cele programu: - skonstruowanie szczegółowych map fizycznych i
BUDOWA I FUNKCJA GENOMU LUDZKIEGO Magdalena Mayer Katedra i Zakład Genetyki Medycznej UM w Poznaniu 1. Projekt poznania genomu człowieka: Cele programu: - skonstruowanie szczegółowych map fizycznych i
Podstawy genetyki. Genetyka klasyczna, narzędzia badawcze genetyki
 Podstawy genetyki Genetyka klasyczna, narzędzia badawcze genetyki Podręczniki } Podstawy biologii molekularnej L.A. Allison } Genomy TA Brown, wyd. 3 } Genetyka molekularna P Węgleński (red.), wyd. 2 2
Podstawy genetyki Genetyka klasyczna, narzędzia badawcze genetyki Podręczniki } Podstawy biologii molekularnej L.A. Allison } Genomy TA Brown, wyd. 3 } Genetyka molekularna P Węgleński (red.), wyd. 2 2
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Zadania maturalne z biologii - 2
 Koło Biologiczne Liceum Ogólnokształcące nr II w Gliwicach 2015-2016 Zadania maturalne z biologii - 2 Zadania: Zad. 1(M. Borowiecki, J. Błaszczak 3BL) Na podstawie podanych schematów określ sposób w jaki
Koło Biologiczne Liceum Ogólnokształcące nr II w Gliwicach 2015-2016 Zadania maturalne z biologii - 2 Zadania: Zad. 1(M. Borowiecki, J. Błaszczak 3BL) Na podstawie podanych schematów określ sposób w jaki
Dlaczego kariotypy mężczyzn i kobiet różnią się pod względem zestawów chromosomów płci skoro Ewa została utworzona z żebra Adama?
 Dlaczego kariotypy mężczyzn i kobiet różnią się pod względem zestawów chromosomów płci skoro Ewa została utworzona z żebra Adama? Spotkałem się z ciekawym zarzutem: Weźmy np. stworzenie człowieka. Nauka
Dlaczego kariotypy mężczyzn i kobiet różnią się pod względem zestawów chromosomów płci skoro Ewa została utworzona z żebra Adama? Spotkałem się z ciekawym zarzutem: Weźmy np. stworzenie człowieka. Nauka
Transport makrocząsteczek
 Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
Komórka eukariotyczna cytoplazma + jądro komórkowe = protoplazma W cytoplazmie odbywa się: cała przemiana materii, dzięki której organizm uzyskuje energię biosynteza białka i innych związków Transport
NaCoBeZu klasa 8 Dział Temat nacobezu programu I. Genetyka 1. Czym jest genetyka? 2. Nośnik informacji genetycznej DNA 3. Podziały komórkowe
 NaCoBeZu klasa 8 Dział programu Temat nacobezu I. Genetyka 1. Czym jest genetyka? wymieniam zakres badao genetyki rozróżniam cechy dziedziczne i niedziedziczne wskazuję cechy indywidualne i gatunkowe omawiam
NaCoBeZu klasa 8 Dział programu Temat nacobezu I. Genetyka 1. Czym jest genetyka? wymieniam zakres badao genetyki rozróżniam cechy dziedziczne i niedziedziczne wskazuję cechy indywidualne i gatunkowe omawiam
PRZEDMIOTOWY SYSTEM OCENIANIA BIOLOGIA POZIOM ROZSZERZONY Opracowany w oparciu o program DKOS /02 KLASA III
 PRZEDMIOTOWY SYSTEM OCENIANIA BIOLOGIA POZIOM ROZSZERZONY Opracowany w oparciu o program DKOS 4015 5/02 ZAKRES WYMAGAŃ NA POSZCZEGÓLNE STOPNIE KLASA III DZIAŁ PROGRAMOWY I. Informacja genetyczna II. Przekazywanie
PRZEDMIOTOWY SYSTEM OCENIANIA BIOLOGIA POZIOM ROZSZERZONY Opracowany w oparciu o program DKOS 4015 5/02 ZAKRES WYMAGAŃ NA POSZCZEGÓLNE STOPNIE KLASA III DZIAŁ PROGRAMOWY I. Informacja genetyczna II. Przekazywanie
Badanie funkcji genu
 Badanie funkcji genu Funkcję genu można zbadać różnymi sposobami Przypadkowa analizy funkcji genu MUTACJA FENOTYP GEN Strategia ukierunkowanej analizy funkcji genu GEN 1. wprowadzenie mutacji w genie 2.
Badanie funkcji genu Funkcję genu można zbadać różnymi sposobami Przypadkowa analizy funkcji genu MUTACJA FENOTYP GEN Strategia ukierunkowanej analizy funkcji genu GEN 1. wprowadzenie mutacji w genie 2.
Analizy DNA in silico - czyli czego można szukać i co można znaleźć w sekwencjach nukleotydowych???
 Analizy DNA in silico - czyli czego można szukać i co można znaleźć w sekwencjach nukleotydowych??? Alfabet kwasów nukleinowych jest stosunkowo ubogi!!! Dla sekwencji DNA (RNA) stosuje się zasadniczo*
Analizy DNA in silico - czyli czego można szukać i co można znaleźć w sekwencjach nukleotydowych??? Alfabet kwasów nukleinowych jest stosunkowo ubogi!!! Dla sekwencji DNA (RNA) stosuje się zasadniczo*
Podstawy genetyki. ESPZiWP 2010
 Podstawy genetyki ESPZiWP 2010 Genetyka - nauka o dziedziczności i zmienności organizmów, wyjaśniająca prawa rządzące podobieństwami i różnicami pomiędzy osobnikami spokrewnionymi przez wspólnego przodka
Podstawy genetyki ESPZiWP 2010 Genetyka - nauka o dziedziczności i zmienności organizmów, wyjaśniająca prawa rządzące podobieństwami i różnicami pomiędzy osobnikami spokrewnionymi przez wspólnego przodka
Rozkład materiału z biologii do klasy III.
 Rozkład materiału z biologii do klasy III. L.p. Temat lekcji Treści programowe Uwagi 1. Nauka o funkcjonowaniu przyrody. 2. Genetyka nauka o dziedziczności i zmienności. -poziomy różnorodności biologicznej:
Rozkład materiału z biologii do klasy III. L.p. Temat lekcji Treści programowe Uwagi 1. Nauka o funkcjonowaniu przyrody. 2. Genetyka nauka o dziedziczności i zmienności. -poziomy różnorodności biologicznej:
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA
 SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU Transkrypcja RNA SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III. Karty pracy. 1. Karta
WPROWADZENIE DO GENETYKI MOLEKULARNEJ
 WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
białka wiążące specyficzne sekwencje DNA czynniki transkrypcyjne
 białka wiążące specyficzne sekwencje DNA czynniki transkrypcyjne http://www.umass.edu/molvis/bme3d/materials/jtat_080510/exploringdna/ch_flex/chapter.htm czynniki transkrypcyjne (aktywatory/represory)
białka wiążące specyficzne sekwencje DNA czynniki transkrypcyjne http://www.umass.edu/molvis/bme3d/materials/jtat_080510/exploringdna/ch_flex/chapter.htm czynniki transkrypcyjne (aktywatory/represory)
Wymagania edukacyjne Biologia na czasie zakres podstawowy
 Wymagania edukacyjne Biologia na czasie zakres podstawowy Dział programu Temat Poziom wymagań konieczny (K) podstawowy (P) rozszerzający (R) dopełniający (D) I. Od genu do cechy Budowa i funkcje kwasów
Wymagania edukacyjne Biologia na czasie zakres podstawowy Dział programu Temat Poziom wymagań konieczny (K) podstawowy (P) rozszerzający (R) dopełniający (D) I. Od genu do cechy Budowa i funkcje kwasów
Oocyty myszy stopniowo rozwijają zdolność do aktywacji podczas bloku w metafazie II. Jacek Z. Kubiak
 Oocyty myszy stopniowo rozwijają zdolność do aktywacji podczas bloku w metafazie II Jacek Z. Kubiak Wprowadzenie W normalnych warunkach oocyty myszy są zapładniane podczas bloku metafazy II Wniknięcie
Oocyty myszy stopniowo rozwijają zdolność do aktywacji podczas bloku w metafazie II Jacek Z. Kubiak Wprowadzenie W normalnych warunkach oocyty myszy są zapładniane podczas bloku metafazy II Wniknięcie
ZARZĄDZANIE POPULACJAMI ZWIERZĄT 1. RÓWNOWAGA GENETYCZNA POPULACJI. Prowadzący: dr Wioleta Drobik Katedra Genetyki i Ogólnej Hodowli Zwierząt
 ZARZĄDZANIE POPULACJAMI ZWIERZĄT 1. RÓWNOWAGA GENETYCZNA POPULACJI Fot. W. Wołkow Prowadzący: dr Wioleta Drobik Katedra Genetyki i Ogólnej Hodowli Zwierząt POPULACJA Zbiór organizmów żywych, które łączy
ZARZĄDZANIE POPULACJAMI ZWIERZĄT 1. RÓWNOWAGA GENETYCZNA POPULACJI Fot. W. Wołkow Prowadzący: dr Wioleta Drobik Katedra Genetyki i Ogólnej Hodowli Zwierząt POPULACJA Zbiór organizmów żywych, które łączy
Spis treści CYKL KOMÓRKOWY
 Spis treści 1 CYKL KOMÓRKOWY 1.1 Faza M 1.2 Faza G1 (część interfazy) 1.3 Faza S (część interfazy) 1.4 Faza G2 (część interfazy) 1.5 Faza G0 2 MITOZA (podział pośredni) 2.1 Profaza 2.2 Metafaza 2.3 Anafaza
Spis treści 1 CYKL KOMÓRKOWY 1.1 Faza M 1.2 Faza G1 (część interfazy) 1.3 Faza S (część interfazy) 1.4 Faza G2 (część interfazy) 1.5 Faza G0 2 MITOZA (podział pośredni) 2.1 Profaza 2.2 Metafaza 2.3 Anafaza
TEST Z CYTOLOGII GRUPA II
 TEST Z CYTOLOGII GRUPA II Zad. 1 (4p.) Rysunek przedstawia schemat budowy pewnej struktury komórkowej. a/ podaj jej nazwę i określ funkcję w komórce, b/ nazwij elementy oznaczone cyframi 2 i 5 oraz określ
TEST Z CYTOLOGII GRUPA II Zad. 1 (4p.) Rysunek przedstawia schemat budowy pewnej struktury komórkowej. a/ podaj jej nazwę i określ funkcję w komórce, b/ nazwij elementy oznaczone cyframi 2 i 5 oraz określ
Ćwiczenie 16/17. Szacowanie częstości mutacji punktowych. Mutacje chromosomowe strukturalne. Mutacje chromosomowe liczbowe.
 Ćwiczenie 16/17 Szacowanie częstości mutacji punktowych. Mutacje chromosomowe strukturalne. Mutacje chromosomowe liczbowe. Prof. dr hab. Roman Zieliński 1. Szacowanie częstości mutacji punktowych 1.1.
Ćwiczenie 16/17 Szacowanie częstości mutacji punktowych. Mutacje chromosomowe strukturalne. Mutacje chromosomowe liczbowe. Prof. dr hab. Roman Zieliński 1. Szacowanie częstości mutacji punktowych 1.1.
MEDYCYNA ROZRODU Z SEKSUOLOGIĄ RÓŻNICOWANIE PŁCIOWE
 MEDYCYNA ROZRODU Z SEKSUOLOGIĄ RÓŻNICOWANIE PŁCIOWE Różnicowaniem płciowym nazywamy procesy zachodzące w okresie płodowym, które na podstawie płci genetycznej doprowadzają do powstania różnic w budowie
MEDYCYNA ROZRODU Z SEKSUOLOGIĄ RÓŻNICOWANIE PŁCIOWE Różnicowaniem płciowym nazywamy procesy zachodzące w okresie płodowym, które na podstawie płci genetycznej doprowadzają do powstania różnic w budowie
6. Uzupełnij zdanie, wstawiajac w odpowiednie miejsce wyrażenie ujawni się lub nie ujawni się :
 ID Testu: 9S6C1A4 Imię i nazwisko ucznia Klasa Data 1. Allelami nazywamy A. takie same formy jednego genu. B. różne formy różnych genów. C. takie same formy różnych genów. D. różne formy jednego genu.
ID Testu: 9S6C1A4 Imię i nazwisko ucznia Klasa Data 1. Allelami nazywamy A. takie same formy jednego genu. B. różne formy różnych genów. C. takie same formy różnych genów. D. różne formy jednego genu.
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu w porównaniu z analizą trankryptomu:
Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją).
 Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją). Czym jest życie? metabolizm + informacja (replikacja) 2 Cząsteczki organiczne mog y powstać w atmosferze pierwotnej
Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją). Czym jest życie? metabolizm + informacja (replikacja) 2 Cząsteczki organiczne mog y powstać w atmosferze pierwotnej
