Zestaw do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn
|
|
|
- Karol Stachowiak
- 5 lat temu
- Przeglądów:
Transkrypt
1 Zestaw do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn Przestroga: Na mocy prawa federalnego sprzedaż tego wyrobu może być prowadzona wyłącznie przez lekarza lub na jego zlecenie. Przed użyciem produktu użytkownicy powinni dokładnie zapoznać się z niniejszą ulotką dołączoną do opakowania. Podczas przeprowadzania testu należy postępować ściśle według zaleceń. Niezastosowanie się do zaleceń może skutkować uzyskaniem błędnych wyników testu. OGRANICZENIA Test ten nie został zatwierdzony do stosowania u pacjentów, którym nie wszczepiono kompletnej endoprotezy stawu. Test ten jest dostępny wyłącznie na receptę. NAZWA I PRZEZNACZENIE Zestaw testu bocznego przepływu Synovasure do oznaczania alfa-defensyn jest jakościowym, odczytywanym wizualnie testem immunochromatograficznym do wykrywania białek odpowiedzi gospodarza ludzkiego, alfa-defensyn 1-3, w mazi stawowej u osób dorosłych po operacji wszczepienia kompletnej endoprotezy stawu, którzy są oceniani pod kątem zabiegu rewizyjnego. Wyniki zestawu testu bocznego przepływu Synovasure do oznaczania alfa-defensyn powinny być wykorzystywane w połączeniu z innymi wynikami klinicznymi i diagnostycznymi w celu ułatwienia rozpoznania (PJI). Zestaw testu bocznego przepływu Synovasure do oznaczania alfa-defensyn nie jest przeznaczony do oznaczenia etiologii ani nasilenia stawu. Zestaw kontrolny Synovasure do oznaczania alfa-defensyn jest stosowany w zestawie testu bocznego przepływu Synovasure do oznaczania alfa-defensyn jako badane próbki kontroli jakości w celu monitorowania wydajności i niezawodności zestawu testu bocznego przepływu Synovasure do oznaczania alfa-defensyn. WYMAGANIA WŁAŚCIWE DLA KRAJU W Stanach Zjednoczonych ten test jest przeznaczony do stosowania wyłącznie na receptę, a w Kanadzie i Australii do użytku laboratoryjnego. We wszystkich krajach poza Stanami Zjednoczonymi, Kanadą i Australią test jest przeznaczony wyłącznie do użytku profesjonalnego. ZASADA TESTU Zestaw testu bocznego przepływu Synovasure do oznaczania alfa-defensyn to oznaczenie immunologiczne do wykrywania obecności alfa-defensyn w mazi stawowej u pacjentów z możliwym zakażeniem okołoprotezowym. Alfa-defensyny to peptydy o aktywności przeciwbakteryjnej, uwalniane przez aktywowane neutrofile w odpowiedzi na zakażenie. W skład testu wchodzi wyrób jednorazowy, fiolka z odmierzoną wstępnie ilością buforu rozcieńczającego, jednorazowa probówka Microsafe oraz pojemnik na próbkę. Każdy wyrób zawiera pasek odczynnikowy ze wszystkimi koniecznymi do wykonania testu składnikami. Rozcieńczenie wykonuje się przez zebranie próbki z aspirowanej mazi stawowej przy użyciu jednorazowej probówki Microsafe i dodanie próbki do wstępnie odmierzonego buforu rozcieńczającego. Następnie do zestawu testowego dodaje się trzy (3) pełne, wolno spadające krople rozcieńczonej próbki w celu rozpoczęcia testu. Materiał komórkowy jest usuwany na pierwszej wkładce. Roztwór następnie migruje do wkładki buforującej i miesza się z koniugatem złota, który został oznakowany przeciwciałami anty-alfa defensyn. Mieszanina badana następnie migruje przez linię testu i linię kontrolną. Linia wyniku testu ( T ) zostanie utworzona, jeśli poziom alfa-defensyn w próbce będzie większy niż stężenie odcięcia. Utworzenie linii kontrolnej ( C ) stanowi potwierdzenie, że roztwór prawidłowo przepłynął przez zestaw testowy. Wyniki można odczytać po 10 do 20 minutach. OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI Test jest przeznaczony do diagnostyki in vitro. Wyniki testu powinny być wykorzystywane w połączeniu z innymi wynikami klinicznymi i diagnostycznymi w celu ułatwienia rozpoznania. Niezastosowanie się do podanej instrukcji może prowadzić do uzyskania błędnych wyników. Wszystkie składniki zestawu testowego można wykorzystać tylko jeden raz, po czym należy je odpowiednio zutylizować. NIE wolno używać ponownie żadnego ze składników testu. Produkt ten nie jest sterylny i NIE należy go umieszczać w sterylnym polu. Strona 1 z 10
2 Zestaw ten został opracowany do stosowania wyłącznie ze świeżo pobraną mazią stawową. Zastosowanie niniejszego zestawu testowego z próbką innego rodzaju może prowadzić do uzyskania błędnych wyników testu. Zastosowanie mazi stawowej rozcieńczonej w roztworze soli fizjologicznej, krwi, środku kontrastowym lub dowolnymi substancjami wstrzykiwanej do stawu może prowadzić do wyników fałszywie ujemnych. Obecność czerwonych krwinek (RBC) w ilości powyżej 1 miliona/µl w próbce mazi stawowej może prowadzić do wyników fałszywie ujemnych. Oznacza to rozcieńczenie próbki mazi stawowej z ilością krwi większą niż 20%. Test ten należy stosować wyłącznie u pacjentów z całkowitą protezą stawu. Wykonanie tego testu zostało zatwierdzone tylko dla warunków ocenionych przez kryteria MSIS (ang. Musculoskeletal Infection Society). Spadek wrażliwości (zwiększone prawdopodobieństwo uzyskania wyników fałszywie ujemnych) obserwowano przy obecności przetoki docierającej do protezy. Ponieważ obecność przetoki stanowi definitywny dowód, NIE zalecamy stosowania tego testu w takich warunkach. Wyniki fałszywie dodatnie zgłaszano przy występowaniu metalozy. Ujemny wynik testu NIE wyklucza możliwości. Maź stawowa uzyskana po kilkukrotnych aspiracjach w krótkim okresie czasu może prowadzić do wyników fałszywie ujemnych ze względu na brak nagromadzonych alfa-defensyn. Test ten NIE jest przeznaczony do stosowania w celu ustalenia ram czasowych reimplantacji w przypadku procedur dwuetapowych. DOSTARCZANE ODCZYNNIKI I MATERIAŁY NR KAT Zestaw testu bocznego przepływu Synovasure do oznaczania alfa-defensyn Ilość Instrukcja 1 użytkowania NR KAT. P50023 Zestaw testowy 5 Zamknięta torebka zawierająca powleczoną membranę z linią testową antyalfa-defensyn i linią kontrolną przeciwciała anty-mysiego, powlekaną cząstkami złota wkładkę anty-alfa-defensyn, wkładkę buforującą oraz wkładkę do usuwania materiału komórkowego; całość umieszczono w ochronnej obudowie z tworzywa sztucznego zamkniętej w torebce z osuszaczem. NR KAT. P50024 Zestaw do przygotowania próbki 5 Zamknięta torebka: - 1 NR KAT. P50025 Butelka do rozcieńczania próbek (wstępnie napełniony bufor fosforanowy, kroplomierz) - 2 Jednorazowe probówki Microsafe - 1 Pojemnik na próbki Dostępne także w ilości 1 sztuki (NR KAT ); 10 sztuk (NR KAT ); 30 sztuk (NR KAT ) UWAGA: NIE należy zastępować ze testowych ani ich składników innymi zestawami bądź składnikami o różnych numerach serii. PRZECHOWYWANIE, POSTĘPOWANIE I STABILNOŚĆ ODCZYNNIKÓW Test należy wykonać w temperaturze pokojowej (12 25 C). NIE należy przeprowadzać testu w temperaturze wykraczającej poza ten zakres. Zalecana temperatura przechowywania zestawu testowego to 2 30 C, obowiązuje ona do daty ważności wydrukowanej na etykiecie opakowania. Przed użyciem testu zawsze należy sprawdzić datę ważności i NIE używać odczynników po upływie daty ważności wydrukowanej na etykiecie opakowania. Nie przechowywać żadnych materiałów w pobliżu otworów wentylacyjnych lub chłodzących lub w bezpośrednim świetle słonecznym. NIE otwierać opakowania torebki, dopóki próbka nie będzie gotowa do przetestowania. Po otwarciu opakowania torebki, wyrób należy zużyć jak najszybciej. Wydajność zestawu testu bocznego przepływu Synovasure do oznaczania alfa-defensyn została ustalona przy użyciu próbek mazi stawowej zebranych zgodnie ze standardowymi procedurami poprzez aspirację mazi stawowej do strzykawki z polipropylenu i przetransportowanie go w probówce z politereftalanu etylenu (PET) bez dodatków (np.: przezroczysta probówka z czerwonym korkiem). Jeśli wymagana jest wysyłka próbki, zaleca się wysłanie jej z dostawą tego samego dnia lub ekspresową pocztą kurierską. Próbki mazi stawowej zachowują stabilność do siedmiu (7) dni w temperaturze 4 32 C. Niewłaściwe pobieranie, transport lub przechowywanie próbek może negatywnie wpłynąć na wydajność testu. Strona 2 z 10
3 ŚRODKI BEZPIECZEŃSTWA Wyroby użyte przy produkcji zestawu testu bocznego przepływu Synovasure do oznaczania alfa-defensyn są uważane za potencjalnie stanowiące zagrożenie biologiczne i powinny być utylizowane zgodnie z lokalnymi, stanowymi i federalnymi wymogami dotyczącymi utylizacji odpadów. Z wszystkimi próbkami i odpadami należy obchodzić się tak, jak z materiałami zdolnymi do przenoszenia czynników zakaźnych. Należy przestrzegać wytycznych bezpieczeństwa, takich jak te opisane w CDC/NIH Biosafety in Microbiological and Biomedical Laboratories [1] the CLSI Document M29-A4 Protection of Laboratory Workers from Occupationally Acquired Infections [2], lub innych właściwych wytycznych. Podczas kontaktu z próbkami pochodzącymi od pacjenta i ich testowania należy nosić odpowiednie środki ochrony indywidualnej (PPE), w tym (jednak nie wyłącznie) jednorazowe rękawice bezpudrowe i fartuchy laboratoryjne. Chronić skórę, oczy i błony śluzowe. Podczas pracy z odczynnikami lub próbkami należy często zmieniać rękawiczki. Pracując z próbkami biologicznymi należy postępować zgodnie z procedurami bezpieczeństwa obowiązującymi w danej instytucji. Kroplomierz zawarty w tym zestawie zawiera bufor rozcieńczający. Bufor rozcieńczający zawiera środek konserwujący, który może powodować reakcję alergiczną skóry. Unikać wdychania mgły lub oparów. Może powodować podrażnienie skóry, oczu i dróg oddechowych. Pełna karta charakterystyki jest dostępna na stronie MATERIAŁY WYMAGANE, ALE NIEDOSTARCZANE Minutnik MATERIAŁY DODATKOWE Zestaw kontrolny Synovasure do oznaczania alfa-defensyn NR KAT Zewnętrzne kontrole dodatnie i ujemne dostępne do zestawu testu bocznego przepływu Synovasure do oznaczania alfa-defensyn PROCEDURA ZESTAWU TESTU BOCZNEGO PRZEPŁYWU SYNOVASURE DO OZNACZANIA ALFA-DEFENSYN Przed wykonaniem testu zweryfikować poniższą listę kontrolną 1. Otworzyć pudełko z zestawem i sprawdzić jego zawartość. Sprawdzić datę przydatności przed użyciem. NIE należy używać ze testowych po upływie daty ważności podanej na opakowaniu. Jeśli którykolwiek ze składników został uszkodzony, wybrać nowy składnik do badania. 2. Test musi być przeprowadzony na płaskiej, stabilnej powierzchni w obszarze o wystarczającym oświetleniu. 3. Test wykonać w temperaturze pokojowej, między 12 C 25 C. 4. Upewnić się, że dostępny jest stoper i ustawiono go na 10 minut. 5. Zestaw kontrolny Synovasure do oznaczania alfa-defensyn ( ) powinien być stosowany zgodnie z wymogami lokalnymi. Krok Instrukcja Deklaracja 1 Wyjąć jedną (1) białą torebkę i jedną (1) srebrną torebkę z pudełka Synovasure. Jeśli zestaw nie był przechowywany w temperaturze pokojowej, zaczekać, aż torebki osiągną temperaturę pokojową. Biała torebka Zestaw testowy o 1 x zestaw Synovasure Srebrna torebka Zestaw do przygotowania próbki o 1 x pojemnik na próbkę o 2 x probówki Microsafe o 1 x butelka do rozcieńczania 2 Otworzyć opakowanie srebrnej torebki zestawu do przygotowania próbki. Aspirowana maź stawowa musi znajdować się w naczyniu, które umożliwi pobranie próbki probówką Microsafe lub pipetą wyporową. Pojemnik na próbki jest dostarczony w zestawie do przygotowania próbki. A. Zestaw testowy B. Zestaw do przygotowania próbki Strona 3 z 10
4 3 Rozcieńczenie: Usunąć i odłożyć fioletowy korek z kroplomierza. Skorzystać z próbówki Microsafe, aby uzyskać maź stawową do rozcieńczenia. Trzymając probówkę Microsafe poziomo, dotknąć końcówką probówki Microsafe próbki mazi stawowej. Przepływ kapilarny automatycznie podciągnie próbkę do czarnej linii poziomu wypełnienia i ją zatrzyma. NIE należy ściskać probówki podczas pobierania próbki. NIE ściskać UWAGA 1: Do pobrania próbki można użyć pipety wyporowej ustawionej na 15 µl, o ile dostępna. UWAGA 2: NIE należy zakrywać wylotu przy czarnej linii poziomu wypełnienia. Przed przejściem do kolejnych czynności należy odczekać, aż maź dotrze do linii poziomu wypełnienia. Jeśli nie można uzyskać mazi stawowej z pojemnika z mazią, należy przenieść niewielką ilość płynu do dostarczonego pojemnika na próbkę. Zebranie próbki mazi stawowej o wysokiej lepkości może potrwać dłużej. Jeśli przy użyciu pierwszej probówki, nie można pobrać mazi stawowej, probówkę wyrzucić i użyć drugiej dostarczonej probówki. 4 Po zebraniu mazi stawowej należy ją umieścić w napełnionym kroplomierzu. Przepłukać probówkę Microsafe w napełnionym kroplomierzu, ściskając i zwalniając zbiorniczek na końcu probówki Microsafe pięć (5) razy, aby usunąć lepką maź stawową. Nałożyć ponownie korek na kroplomierz i wymieszać zawartość przez delikatne odwracanie. Czarna linia poziomu wypełnienia UWAGA: W tym momencie właściwe jest ściśnięcie zbiorniczka, aby upewnić się, że zawartość zostanie w całości przeniesiona. 5 Otworzyć opakowanie białej torebki zestawu testowego. NIE używać zestawu, jeśli torebka jest naruszona. Umieścić zestaw testowy na płaskiej powierzchni. Usunąć przezroczysty korek z kroplomierza. Trzymając kroplomierz w pozycji pionowej (90 ) odmierzyć trzy (3) pełne, wolno spadające krople rozcieńczonej próbki mazi stawowej do studzienki na próbki zestawu testowego. Zestaw testowy musi leżeć płasko w trakcie całej procedury. 6 Monitorować zestaw, aby upewnić się, że próbka przepływa przez okno odczytu (tło powinno zmienić kolor na czerwono-różowy, a ostatecznie przezroczysty). W przypadku braku przepływu próbki przez okno odczytu, najprawdopodobniej dodano niewystarczającą ilość próbki do zestawu. Powtórzyć test z użyciem nowego zestawu testowego. Można wykorzystać poprzednią butelkę do rozcieńczania. Powtórny test należy wykonać w ciągu czterech (4) godzin. 7 Odczekać dziesięć (10) minut bez zakłóceń na zakończenie przebiegu testu. Wyniki można odczytać po 10 do 20 minutach od odmierzenia próbki do studzienki na próbki. Zinterpretować wyniki testu zgodnie z opisem podanym w punkcie Interpretacja wyników testu. NIE odczytywać wyników po 20 minutach. Na rozjaśnionym tle okienka testowego pojawia się czerwono-różowa linia kontrolna. Linia kontrolna [C] to najwyżej położona linia w kanale testu. PROCEDURA ZESTAWU KONTROLNEGO SYNOVASURE DO OZNACZANIA ALFA-DEFENSYN Kontrole zewnętrzne należy przeprowadzać zgodnie z wytycznymi lub wymogami regulacji lokalnych, stanowych i/lub federalnych lub regulacji instytucji akredytujących. Zaleca się, aby kontrole były przeprowadzane przez nowego użytkownika w celu oceny kompetencji, w przypadku otrzymania nowej serii zestawu lub nowej przesyłki z zestawami i gdy warunki przechowywania materiału ulegają zmianom wykraczając poza określone limity. 1. Przygotować kontrole zgodnie z instrukcją użytkowania dostarczoną wraz z zestawem kontrolnym Synovasure do oznaczania alfa-defensyn. Strona 4 z 10
5 2. Przeanalizować kontrole jak próbki kliniczne zgodnie z powyższą instrukcją dostarczoną wraz z zestawem do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn. WEWNĘTRZNA KONTROLA JAKOŚCI: Proceduralna linia kontrolna ( C ) jest wbudowana w każdy zestaw testowy, wskazując, że płyn prawidłowo przepływa przez zestaw testowy. INTERPRETACJA WYNIKÓW Uwaga: Alfa-defensyny są reprezentowane przez linię T na zestawie testowym. Intensywność zabarwienia linii kontrolnych i linii testowych (wyników testu) zestawu testowego może być różna. Każda kompletna czerwono-różowa linia, bez względu na intensywność lub rozmiar, to linia. NIE należy interpretować testu po dwudziestu (20) minutach. Ujemny: Wynik UJEMNY w odniesieniu do alfa-defensyn to obecność TYLKO czerwono-różowej linii kontrolnej w zestawie testowym (C) i brak linii wyniku testu (T) po dziesięciu (10) minutach. Obecność linii kontrolnej wskazuje, że test jest ważny. Dodatni (nie ujemny): Wynik DODATNI w odniesieniu do alfa-defensyn to obecność czerwono-różowej linii kontrolnej w zestawie testowym (C) ORAZ czerwono-różowej linii wyniku testu (T). Obecność linii kontrolnej wskazuje, że test jest ważny. Test nieważny: Przed odczytaniem linii wyniku testu należy sprawdzić, czy została utworzona linia kontrolna zestawu testowego, oznaczona jako C. Jeżeli linia kontrolna zestawu nie pojawi się, linia wyniku testu nie utworzy się całkowicie lub tło nie stanie się przezroczyste, test jest nieważny, a jego wyników nie można wykorzystać. Test należy powtórzyć, używając nowego zestawu testowego. Można wykorzystać poprzednią butelkę do rozcieńczania. Powtórny test należy wykonać w ciągu czterech (4) godzin. Przykłady wyników Test ważny Test nieważny Ujemny Dodatni Dodatni Dodatni Brak linii kontrolnej Linia testowa nie w pełni utworzona Tło nie staje się przezroczyste CHARAKTERYSTYKA WYDAJNOŚCI METODY BOCZNEGO PRZEPŁYWU SYNOVASURE DO OZNACZANIA ALFA-DEFENSYNY Charakterystyka wydajności metody bocznego przepływu Badanie kliniczne było prospektywnym badaniem testu bocznego przepływu Synovasure do oznaczania alfa-defensyn, do którego próbki pobrano w trzech (3) amerykańskich ośrodkach medycznych, w których przeprowadza się dużą liczbę operacji rewizyjnych. Do badania rekrutowano pacjentów po operacji wszczepienia kompletnej endoprotezy stawu kolanowego i/lub biodrowego, u których rozważano przeprowadzenie zabiegu rewizyjnego. Próbki pobierano od co najmniej 300 pacjentów ogółem, dopóki nie pobrano ich od co najmniej 50 pacjentów z dodatnim wynikiem (z zakażeniem) w kierunku według kryteriów MSIS. Przetwarzanie próbek, standardowe testy i testy zestawu w fazie badań odbywały się w co najmniej dwóch (2) ośrodkach, w których pobierano próbki. Pobieranie próbek i standardowe testy przeprowadzane były w dodatkowych ośrodkach, jednak przesyłały one próbki do centralnego laboratorium, gdzie prowadzano testy zestawu w fazie badań. Próbki te były wysyłane z miejsca pobrania do miejsca badania za pośrednictwem firmy kurierskiej z dostawą tego samego dnia lub ekspresową pocztą kurierską. Strona 5 z 10
6 Po dotarciu do laboratorium próbki zostały najpierw podzielone na porcje do wykorzystania w zleconym przez lekarza diagnostycznym badaniu laboratoryjnym, a pozostałą część próbki wykorzystano do badania w badaniu klinicznym za pomocą testu bocznego przepływu Synovasure do oznaczania alf-defensyn. Próbki testowano przy użyciu testu bocznego przepływu Synovasure do oznaczania alfa-defensyn, postępując zgodnie z procedurami testowania i kontroli jakości określonymi w ulotce dołączonej do opakowania. Strona 6 z 10
7 Rozpoznanie zdefiniowane według kryteriów MSIS ustalił niezależny zespół orzekający trzech (3) lekarzy z doświadczeniem w zakresie zakażeń, którzy mają dostęp do wszystkich danych pacjenta niezbędnych do postawienia diagnozy klinicznej (np. wystarczające kryteria MSIS i historia pacjenta). Zespół orzekający nie znał wyników testu bocznego przepływu Synovasure do oznaczania alfa-defensyn. Wyniki testu bocznego przepływu Synovasure do oznaczania alfa-defensyn porównano osobno z diagnozą kliniczną każdego pacjenta postawioną na podstawie kryteriów MSIS. Poniżej (Tabela 1) przedstawiono wydajność kliniczną testu obliczoną w odniesieniu do kryteriów MSIS dla wszystkich prospektywnych próbek. Obejmuje to próbki o > 20% rozcieńczeniu krwią. Tabela 1: Szacunkowa wydajność kliniczna testu bocznego przepływu Synovasure do oznaczania alfa-defensyn Dodatni Ujemny Kliniczne rozpoznanie Dodatni w 51 6 kierunku Ujemny w kierunku Czułość 89,5% (51/57) (78,5% - 96,0%) Swoistość 94,8% (235/248) (91,2% - 97,2%) 79,7% (51/64) (67,8% - 88,7%) predykcyjna 97,5% (235/241) (94,7% - 99,1%) predykcyjna Poniżej przedstawiono wydajność kliniczną testu bocznego przepływu Synovasure do oznaczania alfa-defensyn obliczoną w odniesieniu do kryteriów MSIS z wyłączeniem próbek rozcieńczonych > 20% krwi (RBC > ) (Tabela 2). Tabela 2: Szacunkowa wydajność kliniczna testu bocznego przepływu Synovasure do oznaczania alfa-defensyn z wyłączeniem próbek rozcieńczonych > 20% krwi (RBC > ) Dodatni Ujemny Kliniczne rozpoznanie Dodatni w 50 3 kierunku Ujemny w kierunku Czułość 94,3% (50/53) (84,3% - 98,8%) Swoistość 94,5% (222/235) (90,7% - 97,0%) 79,4% (50/63) (67,3% - 88,5%) predykcyjna Strona 7 z 10
8 98,7% (222/225) (96,2% - 99,7%) predykcyjna Uwaga: Obecność krwinek czerwonych w mazi stawowej w ilości powyżej 1 miliona/µl, oznacza rozcieńczenie próbki mazi stawowej ilością krwi większą niż 20%, może prowadzić do wyników fałszywie ujemnych. Wydajność kliniczną oszacowaną na podstawie danych prospektywnych uzupełniono o retrospektywne próbki dodatnie zbierane kolejno w CD Laboratories. Od dnia 16 maja 2017 r. do 31 sierpnia 2017 r. zebrano 65 próbek oznaczonych jako dodatnie zgodnie ze zmodyfikowanymi kryteriami MSIS ( 3000 krwinek białych, 80% neutrofili i dodatni posiew) i przetestowano je za pomocą testu bocznego przepływu Synovasure do oznaczania alfa-defensyn. Poniżej przedstawiono procentową zgodność wyników dodatnich (PPA) testu bocznego przepływu Synovasure do oznaczania alf-defensyn ze zmodyfikowanymi kryteriami MSIS, oszacowaną na podstawie tych dodatnich próbek retrospektywnych (Tabela 3). Tabela 3: Szacunkowa wydajność kliniczna dla wszystkich retrospektywnych próbek dodatnich Dodatni Ujemny Łączny wynik Dodatni w kierunku Procentowa zgodność wyników dodatnich (PPA) 98.5% (64/65) (91.7% %) Na podstawie prospektywnej populacji próbek, w których RBC < 1 milion komórek/µl, przeprowadzono analizy współzmiennych w celu określenia potencjalnego wpływu bieżącego stosowania antybiotyku (Tabela 4), historii chorób zapalnych (Tabela 5) oraz posiewu gram dodatniego i ujemnego (Tabela 6) na wydajność kliniczną testu bocznego przepływu Synovasure do oznaczania alfa-defensyn. Poniżej przedstawiono wyniki tych analiz. Dodatkowe oceniane współzmienne obejmowały wiek, rasę, płeć, historię zakażeń, stosowanie leków przeciwzapalnych i badany staw. Nie zaobserwowano istotnych różnic w wydajności testu. Tabela 4. Analiza współzmiennych w celu oszacowania wydajności klinicznej u uczestników obecnie stosujących i niestosujących antybiotyki Uczestnicy stosujący obecnie antybiotyki Czułość 96,2% (25/26) (80,4% - 99,9%) Swoistość 92,3% (12/13) (64,0% - 99,8%) predykcyjna 96,2% (25/26) (80,4% - 99,9%) predykcyjna 92,3% (12/13) (64,0% - 99,8%) Uczestnicy niestosujący obecnie antybiotyków Czułość 88,9% (8/9) (51,8% - 99,7%) Swoistość 92,3% (60/65) (83,0% - 97,5%) predykcyjna 61,5% (8/13) (31,6-86,1%) predykcyjna 98,4% (60/61) (91,2% - 100,0%) Tabela 5: Analiza współzmiennych w celu oszacowania wydajności klinicznej u uczestników z chorobą zapalną i bez choroby zapalnej w wywiadzie Uczestnicy z chorobą zapalną w wywiadzie Czułość 92,3% (12/13) (64,0% - 99,8%) Swoistość 96,3% (52/54) (87,3% - 99,5%) Strona 8 z 10
9 predykcyjna 85,7% (12/14) (57,2% - 98,2%) predykcyjna 98,1% (52/53) (89,9% - 100,0%) Uczestnicy bez choroby zapalnej w wywiadzie Czułość 95,0% (38/40) (83,1% - 99,4%) Swoistość 93,9% (170/181) (89,4-96,9%) predykcyjna 77,6% (38/49) (63,4% - 88,2%) predykcyjna 98,8% (170/172) (95,9% - 99,9%) Tabela 6: Analiza współzmiennych w celu oszacowania wydajności klinicznej u uczestników z posiewem gram dodatnim i gram ujemnym Posiew gram dodatni Czułość 90,6% (29/32) (75,0% - 98,0%) Swoistość 91,3% (21/23) (72,0% - 98,9%) predykcyjna 93,5% (29/31) (78,6% - 99,2%) predykcyjna 87,5% (21/24) (67,6% - 97,3%) Posiew gram ujemny Czułość 85,7 (6/7) (42,1% - 99,6%) Swoistość Niemożliwy do oszacowania predykcyjna 100,0% (6/6) (54,1% - 100,0%) predykcyjna 0,0% (0/1) (0,0% - 97,5%) Precyzja Badanie precyzji przeprowadzono w trzech (3) zewnętrznych laboratoriach w ciągu co najmniej pięć (5) dni z trzema (3) operatorami na ośrodek, 3 serie dziennie, 18 zaślepionych próbek na serię składającą się z dwóch do czterech (2-4) zaślepionych powtórzeń każdej próbki. Wszystkie próbki były testowane jako singlet. Każda seria zawierała w singlecie kontrole ujemne i dodatnie. Wyniki przedstawiono poniżej. Tabela 7: Procent wyników dodatnich i wyników ujemnych dla wszystkich członków panelu precyzji Próbka % dodatnich 95% CI % ujemnych 95% CI Ujemny 1,0% = 4 / 403 (0,3%, 2,5%) 99,0% = 399 / 403 (97,5%, 99,7%) Wysoki 9,9% = 40 / 404 (7,2%, 13,2%) 90,1% = 364 / 404 (86,8%, 92,8%) ujemny Odcięcie 49,9% = 202 / 405 (44,9%, 54,9%) 50,1% = 203 / 405 (45,1%, 55,1%) Niski dodatni 79,7% = 321 / 403 (75,4%, 83,5%) 20,3% = 82 / 403 (16,5%, 24,6%) Dodatni 96,0% = 388 / 404 (93,6%, 97,7%) 4,0% = 16 / 404 (2,3%, 6,4%) Wysoki dodatni 98,5% = 396 / 402 (96,8%, 99,5%) 1,5% = 6 / 402 (0,5%, 3,2%) Strona 9 z 10
10 Substancje zakłócające Badano endogenne czynniki zakłócające pochodzące z naturalnie występujących substancji znajdujących się w próbkach pacjentów. Badano również egzogenne czynniki zakłócające, pochodzące z materiałów znalezionych w próbce pacjenta z powodu obecności implantu stawu. Wyniki przedstawiono poniżej. Tabela 8: Wyniki testu czynników zakłócających Substancja Stężenie, przy którym zestaw testowy nie wykazuje zakłóceń Czynnik reumatoidalny 300 j,m, Bilirubina (niesprzężona) 20 mg/dl Bilirubina (sprzężona) 29 mg/dl Trójglicerydy (TG) 418 mg/dl Hemoglobina z pełnej krwi 12,1 g/dl Hemoglobina po lizie 8,7 g/dl Kwas hialuronowy (HA) 8 mg/ml Jony metalu kobalt 150 mg/l Jony metalu chrom 150 mg/l Jony metalu tytan 150 mg/l Cement kostny 10 mg/ml UHMWPE 10 mg/ml Synovasure to licencjonowany znak towarowy firmy Zimmer Biomet Holdings Inc., następcy firmy Zimmer Holdings Inc. Piśmiennictwo 1. Biosafety in Microbiological and Biomedical Laboratories (BMBL) Institute, C.L.S., Protection of Laboratory Workers From Occupationally Acquired Infections; Approved Guideline - Third Edition M29-A CLSI. Protection of Laboratory Workers from Occupationally Acquired Infections; Approved Guideline Fourth Edition. CLSI document M29-A4 (ISBN ). CLSI, 940 West Valley Road, Suite 1400, Wayne, Pennsylvania USA, Deirmengian C, Kardos K, Kilmartin P, Cameron A, Schiller K, Parvizi J. Diagnosing Periprosthetic Joint Infection: Has the Era of the Biomarker Arrived? Clin Orthop Relat Res Nov; 472(11): Parvizi, J., Zmistowski, B., Della Valle, C., Bauer, T. W., Malizos, K. N., Alavi, A., Bedair, H., et al. (2013). Diagnosis of Periprosthetic Joint Infection. The Journal of Arthroplasty p CLSI. Interference Testing in Clinical Chemistry; Approved Guideline Second Edition. CLSI document EP7-A2 (ISBN ). CLSI, 940 West Valley Road, Suite 1400, Wayne, Pennsylvania USA, Objaśnienie symboli Aby uzyskać dodatkową pomoc techniczną, odwiedź witrynę Wyrób medyczny przeznaczony do diagnostyki in vitro Należy zapoznać się z instrukcją użytkowania Autoryzowany przedstawiciel w Unii Europejskiej 36 F 2 C Nie używać ponownie 86 F 30 C Ograniczenie temperatury Wytwórca Wyrób niesterylny Zawiera ilość wystarczającą do <n> testów Data przydatności do użycia CD Diagnostics, Inc. 650 Naamans Road, Suite 100 Claymont, DE USA Zimmer GmbH Sulzerallee Winterthur Switzerland Strona 10 z 10
Zestaw do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn
 Zestaw do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn Test przeznaczony do diagnostyki in vitro Dystrybutor Aby uzyskać dodatkowe informacje o produkcie, odwiedź witrynę www.cddiagnostics.com
Zestaw do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn Test przeznaczony do diagnostyki in vitro Dystrybutor Aby uzyskać dodatkowe informacje o produkcie, odwiedź witrynę www.cddiagnostics.com
Zestaw do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn
 Zestaw do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn Aby uzyskać dodatkowe informacje o produkcie, odwiedź witrynę www.cddiagnostics.com Przed użyciem produktu użytkownicy powinni
Zestaw do testu bocznego przepływu Synovasure do oznaczania alfa-defensyn Aby uzyskać dodatkowe informacje o produkcie, odwiedź witrynę www.cddiagnostics.com Przed użyciem produktu użytkownicy powinni
Zestaw do testu bocznego przepływu Synovasure PJI
 Zestaw do testu bocznego przepływu Synovasure PJI Test na obecność alfa-defensyn do identyfikacji zakażeń okołoprotezowych stawów Dystrybutor Aby uzyskać dodatkowe informacje o produkcie, odwiedź witrynę
Zestaw do testu bocznego przepływu Synovasure PJI Test na obecność alfa-defensyn do identyfikacji zakażeń okołoprotezowych stawów Dystrybutor Aby uzyskać dodatkowe informacje o produkcie, odwiedź witrynę
ROTA-ADENO Virus Combo Test Device
 Kod produktu: 8.04.73.0.0020 ROTA-ADENO Virus Combo Test Device Tylko do diagnostyki in vitro Przechowywać w 2-30 C ZASTOSOWANIE Wykrywanie antygenów Rotawirusów i Adenowirusów w próbkach kału. WSTĘP Rotawirusy
Kod produktu: 8.04.73.0.0020 ROTA-ADENO Virus Combo Test Device Tylko do diagnostyki in vitro Przechowywać w 2-30 C ZASTOSOWANIE Wykrywanie antygenów Rotawirusów i Adenowirusów w próbkach kału. WSTĘP Rotawirusy
Ulotka dołączona do opakowania: informacja dla użytkownika. Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych
 Ulotka dołączona do opakowania: informacja dla użytkownika Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
INSTRUKCJA STOSOWANIA
 Strona 1 z 6 INSTRUKCJA STOSOWANIA Zawiesiny pasożytów w formalinie PRZEZNACZENIE Zawiesiny pasożytów oferowane przez Microbiologics przeznaczone są do programów zapewnienia jakości tam, gdzie do przeprowadzenia
Strona 1 z 6 INSTRUKCJA STOSOWANIA Zawiesiny pasożytów w formalinie PRZEZNACZENIE Zawiesiny pasożytów oferowane przez Microbiologics przeznaczone są do programów zapewnienia jakości tam, gdzie do przeprowadzenia
(Akty o charakterze nieustawodawczym) DECYZJE
 19.7.2019 PL L 193/1 II (Akty o charakterze nieustawodawczym) DECYZJE DECYZJA WYKONAWCZA KOMISJI (UE) 2019/1244 z dnia 1 lipca 2019 r. zmieniająca decyzję 2002/364/WE w odniesieniu do wymogów dotyczących
19.7.2019 PL L 193/1 II (Akty o charakterze nieustawodawczym) DECYZJE DECYZJA WYKONAWCZA KOMISJI (UE) 2019/1244 z dnia 1 lipca 2019 r. zmieniająca decyzję 2002/364/WE w odniesieniu do wymogów dotyczących
AmpliTest Salmonella spp. (Real Time PCR)
 AmpliTest Salmonella spp. (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzaju Salmonella techniką Real Time PCR Nr kat.: BAC01-50 Wielkość zestawu: 50 oznaczeń Objętość
AmpliTest Salmonella spp. (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzaju Salmonella techniką Real Time PCR Nr kat.: BAC01-50 Wielkość zestawu: 50 oznaczeń Objętość
AmpliTest GMO screening-nos (Real Time PCR)
 AmpliTest GMO screening-nos (Real Time PCR) Zestaw do wykrywania sekwencji DNA terminatora NOS techniką Real Time PCR Nr kat.: GMO03-50 GMO03-100 Wielkość zestawu: 50 reakcji 100 reakcji Objętość pojedynczej
AmpliTest GMO screening-nos (Real Time PCR) Zestaw do wykrywania sekwencji DNA terminatora NOS techniką Real Time PCR Nr kat.: GMO03-50 GMO03-100 Wielkość zestawu: 50 reakcji 100 reakcji Objętość pojedynczej
AmpliTest Babesia spp. (PCR)
 AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
AE/ZP-27-74/16 Załącznik Nr 6
 AE/ZP-27-74/16 Załącznik Nr 6 Wymagania dla UWAGA! Oferta nie spełniająca poniższych wymagań będzie odrzucona L.p. Wymagane parametry Wymagania wobec przedmiotu zmówienia oferowanego w Pakiecie Nr 1 Wszystkie
AE/ZP-27-74/16 Załącznik Nr 6 Wymagania dla UWAGA! Oferta nie spełniająca poniższych wymagań będzie odrzucona L.p. Wymagane parametry Wymagania wobec przedmiotu zmówienia oferowanego w Pakiecie Nr 1 Wszystkie
Jeszcze raz o infekcjach okołoprotezowych. Co nowego?
 Dariusz Grzelecki Jeszcze raz o infekcjach okołoprotezowych. Co nowego? Knee Master 24.11.2018 Klinika Ortopedii i Reumoortopedii CMKP Diagnostyka Za 85%; Przeciw 13%; wstrzymało się 2% Poziom wiarygodności:
Dariusz Grzelecki Jeszcze raz o infekcjach okołoprotezowych. Co nowego? Knee Master 24.11.2018 Klinika Ortopedii i Reumoortopedii CMKP Diagnostyka Za 85%; Przeciw 13%; wstrzymało się 2% Poziom wiarygodności:
AmpliTest Chlamydia/Chlamydophila (Real Time PCR)
 AmpliTest Chlamydia/Chlamydophila (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzajów Chlamydia i Chlamydophila techniką Real Time PCR Nr kat.: BAC18-50 BAC18-100 Wielkość
AmpliTest Chlamydia/Chlamydophila (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzajów Chlamydia i Chlamydophila techniką Real Time PCR Nr kat.: BAC18-50 BAC18-100 Wielkość
10) istotne kliniczne dane pacjenta, w szczególności: rozpoznanie, występujące czynniki ryzyka zakażenia, w tym wcześniejsza antybiotykoterapia,
 Załącznik nr 2 Standardy jakości w zakresie mikrobiologicznych badań laboratoryjnych, w tym badań technikami biologii molekularnej, oceny ich jakości i wartości diagnostycznej oraz laboratoryjnej interpretacji
Załącznik nr 2 Standardy jakości w zakresie mikrobiologicznych badań laboratoryjnych, w tym badań technikami biologii molekularnej, oceny ich jakości i wartości diagnostycznej oraz laboratoryjnej interpretacji
AE/ZP-27-03/16 Załącznik Nr 6
 AE/ZP--0/ Załącznik Nr Wymagania dla przedmiotu zamówienia oferowanego w Pakietach Nr - Lp Parametry wymagane Wymagania dla przedmiotu zamówienia oferowanego w Pakiecie Nr poz..... Surowica antyglobulinowa
AE/ZP--0/ Załącznik Nr Wymagania dla przedmiotu zamówienia oferowanego w Pakietach Nr - Lp Parametry wymagane Wymagania dla przedmiotu zamówienia oferowanego w Pakiecie Nr poz..... Surowica antyglobulinowa
Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu
 Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu PROGRAM WHO ELIMINACJI ODRY/RÓŻYCZKI Program eliminacji odry i różyczki został uchwalony przez Światowe Zgromadzenie Zdrowia 28 maja 2003 roku. Realizacja
Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu PROGRAM WHO ELIMINACJI ODRY/RÓŻYCZKI Program eliminacji odry i różyczki został uchwalony przez Światowe Zgromadzenie Zdrowia 28 maja 2003 roku. Realizacja
Opis przedmiotu zamówienia wraz z wymaganiami technicznymi i zestawieniem parametrów
 Załącznik nr 1 do SIWZ Nazwa i adres Wykonawcy Opis przedmiotu zamówienia wraz z wymaganiami technicznymi i zestawieniem parametrów Przedmiot zamówienia; automatyczny system do diagnostyki molekularnej:
Załącznik nr 1 do SIWZ Nazwa i adres Wykonawcy Opis przedmiotu zamówienia wraz z wymaganiami technicznymi i zestawieniem parametrów Przedmiot zamówienia; automatyczny system do diagnostyki molekularnej:
Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu.
 WSTĘP Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu. Test jest przeznaczony wyłącznie do stosowania ZASADA OZNACZENIA Ten test immunoenzymatyczny
WSTĘP Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu. Test jest przeznaczony wyłącznie do stosowania ZASADA OZNACZENIA Ten test immunoenzymatyczny
INSTRUKCJA UŻYTKOWANIA
 INSTRUKCJA UŻYTKOWANIA n Parasite Suspensions w formalinie PRZEZNACZENIE Preparaty Parasite Suspensions firmy Microbiologics są wykorzystywane w programach zapewniania jakości jako materiały porównawcze
INSTRUKCJA UŻYTKOWANIA n Parasite Suspensions w formalinie PRZEZNACZENIE Preparaty Parasite Suspensions firmy Microbiologics są wykorzystywane w programach zapewniania jakości jako materiały porównawcze
Dyrektywa 98/79/WE. Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.
 Dyrektywa 98/79/WE Załącznik nr 23 Załącznik nr 23 Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.pl Według Dziennika Urzędowego UE (2013/C
Dyrektywa 98/79/WE Załącznik nr 23 Załącznik nr 23 Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.pl Według Dziennika Urzędowego UE (2013/C
Poniższe wytyczne dotyczą wszystkich rodzajów materiału klinicznego.
 Strona 1 z 5 Wytyczne dotyczące zlecania, pobierania, oznakowania, przechowywania, transportowania i rejestrowania próbek materiału klinicznego do badań w Pracowni PCR Niżej przedstawione wytyczne dotyczące
Strona 1 z 5 Wytyczne dotyczące zlecania, pobierania, oznakowania, przechowywania, transportowania i rejestrowania próbek materiału klinicznego do badań w Pracowni PCR Niżej przedstawione wytyczne dotyczące
SNAP* BVD. Bovine Virus Diarrhea Antigen Test Kit. Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD)
 SNAP* BVD Bovine Virus Diarrhea Antigen Test Kit Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD) 06-20814-01 Bovine Virus Diarrhea Antigen Test Kit
SNAP* BVD Bovine Virus Diarrhea Antigen Test Kit Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD) 06-20814-01 Bovine Virus Diarrhea Antigen Test Kit
Alergia na jony metali jako przyczyna niepowodzeń aloplastyki stawu kolanowego
 Alergia na jony metali jako przyczyna niepowodzeń aloplastyki stawu kolanowego Jakub Kamiński, Damian Kusz, Piotr Wojciechowski Alergiczne przyczyny niepowodzeń Alergiczne przyczyny niepowodzenia całkowitej
Alergia na jony metali jako przyczyna niepowodzeń aloplastyki stawu kolanowego Jakub Kamiński, Damian Kusz, Piotr Wojciechowski Alergiczne przyczyny niepowodzeń Alergiczne przyczyny niepowodzenia całkowitej
PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika
 PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika Spis treści 1. Zawartość 2 1.1 Składniki zestawu 2 2. Opis produktu 2 2.1 Założenia metody 2 2.2 Instrukcja 2 2.3 Specyfikacja
PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika Spis treści 1. Zawartość 2 1.1 Składniki zestawu 2 2. Opis produktu 2 2.1 Założenia metody 2 2.2 Instrukcja 2 2.3 Specyfikacja
Ulotka dołączona do opakowania: informacja dla użytkownika. Mucofluid, 50 mg/ml, aerozol do nosa, roztwór. Mesnum
 Ulotka dołączona do opakowania: informacja dla użytkownika Mucofluid, 50 mg/ml, aerozol do nosa, roztwór Mesnum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
Ulotka dołączona do opakowania: informacja dla użytkownika Mucofluid, 50 mg/ml, aerozol do nosa, roztwór Mesnum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
1.2. Zlecenie może być wystawione w formie elektronicznej z zachowaniem wymagań, o których mowa w poz. 1.1.
 Załączniki do rozporządzenia Ministra Zdrowia z dnia 2005 r. (poz. ) Załącznik Nr 1 Podstawowe standardy jakości w czynnościach laboratoryjnej diagnostyki medycznej, ocenie ich jakości i wartości diagnostycznej
Załączniki do rozporządzenia Ministra Zdrowia z dnia 2005 r. (poz. ) Załącznik Nr 1 Podstawowe standardy jakości w czynnościach laboratoryjnej diagnostyki medycznej, ocenie ich jakości i wartości diagnostycznej
Elcometer 134A. Zestaw do wykrywania chlorków soli w ścierniwie. Instrukcja obsługi
 Elcometer 134A Zestaw do wykrywania chlorków soli w ścierniwie Instrukcja obsługi Zawartość 1.0. Ważne uwagi 2.0. Zakres dostawy 3.0. Obsługa 4.0. Specyfikacja rurki miareczkującej 4.1. Właściwości 4.2.
Elcometer 134A Zestaw do wykrywania chlorków soli w ścierniwie Instrukcja obsługi Zawartość 1.0. Ważne uwagi 2.0. Zakres dostawy 3.0. Obsługa 4.0. Specyfikacja rurki miareczkującej 4.1. Właściwości 4.2.
Grupa SuperTaniaApteka.pl Utworzono : 30 wrzesień 2016
 TESTY CIĄŻOWE I DIAGNOSTYCZNE > Model : 9048435 Producent : HYDREX PRZED.TECH.HANDL. Testy paskowe Insight BIAŁKO Test są przeznaczone do wykonania ogólnego badania moczu w warunkach domowych. Testy BIAŁKO
TESTY CIĄŻOWE I DIAGNOSTYCZNE > Model : 9048435 Producent : HYDREX PRZED.TECH.HANDL. Testy paskowe Insight BIAŁKO Test są przeznaczone do wykonania ogólnego badania moczu w warunkach domowych. Testy BIAŁKO
PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL
 PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO Szanowny Farmaceuto, Należy
PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO Szanowny Farmaceuto, Należy
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
(Publikacja tytułów i odniesień do norm zharmonizowanych na mocy prawodawstwa harmonizacyjnego Unii) (Tekst mający znaczenie dla EOG) (2015/C 226/03)
 10.7.2015 PL Dziennik Urzędowy Unii Europejskiej C 226/43 Komunikat Komisji w ramach wdrażania dyrektywy Parlamentu Europejskiego i Rady nr 98/79/WE z dnia 27 października 1998 r. w sprawie wyrobów medycznych
10.7.2015 PL Dziennik Urzędowy Unii Europejskiej C 226/43 Komunikat Komisji w ramach wdrażania dyrektywy Parlamentu Europejskiego i Rady nr 98/79/WE z dnia 27 października 1998 r. w sprawie wyrobów medycznych
Komunikat Komisji w ramach wdrażania dyrektywy 98/79/WE Parlamentu Europejskiego i Rady w sprawie wyrobów medycznych używanych do diagnozy in vitro
 C 173/136 PL Dziennik Urzędowy Unii Europejskiej 13.5.2016 Komunikat Komisji w ramach wdrażania dyrektywy 98/79/WE Parlamentu Europejskiego i Rady w sprawie wyrobów medycznych używanych do diagnozy in
C 173/136 PL Dziennik Urzędowy Unii Europejskiej 13.5.2016 Komunikat Komisji w ramach wdrażania dyrektywy 98/79/WE Parlamentu Europejskiego i Rady w sprawie wyrobów medycznych używanych do diagnozy in
Pozostałe zapisy SIWZ nie ulegają zmianie.
 Znak sprawy: ZP/72/83/2017/PN/72 Dotyczy: Modyfikacji SIWZ Zabrze, 13.12.2017r. Dyrektor dr n. med. Dariusz Budziński ul. 3-go Maja 13-15 41-800 Zabrze SEKRETARIAT fax: (32) 370 45 22 sekretariat@szpital.zabrze.pl
Znak sprawy: ZP/72/83/2017/PN/72 Dotyczy: Modyfikacji SIWZ Zabrze, 13.12.2017r. Dyrektor dr n. med. Dariusz Budziński ul. 3-go Maja 13-15 41-800 Zabrze SEKRETARIAT fax: (32) 370 45 22 sekretariat@szpital.zabrze.pl
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH
 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH BUTELKA 500 ML 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI ŁUG LECZNICZY roztwór, produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Skład 1 l roztworu
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH BUTELKA 500 ML 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI ŁUG LECZNICZY roztwór, produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Skład 1 l roztworu
Zał Nr 1- Pak Nr 7- Analizator parametrów krytycznych 1 sztuka. Parametry oferowane. Parametry wymagane. Opis / Parametry wymagane
 Zał Nr 1- Pak Nr 7- Analizator parametrów krytycznych 1 sztuka Lp Opis / Parametry wymagane Parametry wymagane Parametry oferowane /podać zakresy lub opisać 1 Producent 2 Model 3 Rok produkcji min 2018
Zał Nr 1- Pak Nr 7- Analizator parametrów krytycznych 1 sztuka Lp Opis / Parametry wymagane Parametry wymagane Parametry oferowane /podać zakresy lub opisać 1 Producent 2 Model 3 Rok produkcji min 2018
PCR bez izolacji testujemy Direct PCR Kits od ThermoFisher Scientific
 PCR bez izolacji testujemy Direct PCR Kits od ThermoFisher Scientific Specjalnie dla Was przetestowaliśmy w naszym laboratorium odczynniki firmy Thermo Scientific umożliwiające przeprowadzanie reakcji
PCR bez izolacji testujemy Direct PCR Kits od ThermoFisher Scientific Specjalnie dla Was przetestowaliśmy w naszym laboratorium odczynniki firmy Thermo Scientific umożliwiające przeprowadzanie reakcji
HEMATOLOGIA. Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice.
 HEMATOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi. Zdezynfekować
HEMATOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi. Zdezynfekować
Genomic Mini AX Bacteria+ Spin
 Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
Komunikat Komisji w ramach wdrażania dyrektywy 98/79/WE. (Publikacja tytułów i odniesień do norm zharmonizowanych na mocy dyrektywy) (2010/C 183/04)
 7.7.2010 Dziennik Urzędowy Unii Europejskiej C 183/45 Komunikat Komisji w ramach wdrażania dyrektywy 98/79/WE (Tekst mający znaczenie dla EOG) (Publikacja tytułów i odniesień do norm zharmonizowanych na
7.7.2010 Dziennik Urzędowy Unii Europejskiej C 183/45 Komunikat Komisji w ramach wdrażania dyrektywy 98/79/WE (Tekst mający znaczenie dla EOG) (Publikacja tytułów i odniesień do norm zharmonizowanych na
(Tekst mający znaczenie dla EOG) (Publikacja tytułów i odniesień do norm zharmonizowanych na mocy dyrektywy) (2012/C 262/03)
 30.8.2012 Dziennik Urzędowy Unii Europejskiej C 262/29 Komunikat Komisji w ramach wdrażania dyrektywy Parlamentu Europejskiego i Rady 98/79/WE z dnia 27 października 1998 r. w sprawie wyrobów medycznych
30.8.2012 Dziennik Urzędowy Unii Europejskiej C 262/29 Komunikat Komisji w ramach wdrażania dyrektywy Parlamentu Europejskiego i Rady 98/79/WE z dnia 27 października 1998 r. w sprawie wyrobów medycznych
Kiedy nie stosować Homeoplasmine Jeśli pacjent ma uczulenie na substancje czynne lub którykolwiek
 Ulotka dołączona do opakowania: informacja dla pacjenta Homeoplasmine, maść Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta. Lek
Ulotka dołączona do opakowania: informacja dla pacjenta Homeoplasmine, maść Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta. Lek
Genomic Mini AX Plant Spin
 Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
wielkość opakowania ilość opakowań rocznie
 Pakiet I. Odczynniki i akcesoria do analizatora hematologicznego Cell -Dyn 3700 Lp Asortyment nr kat. firmy ABBOTT nr kat. wielkość opakowania ilość opakowań 1. Isotonic Diluent a 20 L 99231 13 2. Detergent
Pakiet I. Odczynniki i akcesoria do analizatora hematologicznego Cell -Dyn 3700 Lp Asortyment nr kat. firmy ABBOTT nr kat. wielkość opakowania ilość opakowań 1. Isotonic Diluent a 20 L 99231 13 2. Detergent
ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01
![ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01 ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01](/thumbs/25/4516998.jpg) ACCESS Immunoassay System HIV combo QC4 & QC5 B22822 Do monitorowania wydajności testu Access HIV combo. - [PL] - 2015/01 Spis treści Access HIV combo QC4 & QC5 1 Przeznaczenie... 3 2 Podsumowanie i objaśnienie
ACCESS Immunoassay System HIV combo QC4 & QC5 B22822 Do monitorowania wydajności testu Access HIV combo. - [PL] - 2015/01 Spis treści Access HIV combo QC4 & QC5 1 Przeznaczenie... 3 2 Podsumowanie i objaśnienie
Genomic Micro AX Blood Gravity 96-well
 Genomic Micro AX Blood Gravity 96-well Zestaw do izolacji DNA z krwi w formacie płytek na 96 studzienek dedykowany do pracy z pipetą wielokanałową lub automatem typu liquid handler. 960 izolacji Nr kat.
Genomic Micro AX Blood Gravity 96-well Zestaw do izolacji DNA z krwi w formacie płytek na 96 studzienek dedykowany do pracy z pipetą wielokanałową lub automatem typu liquid handler. 960 izolacji Nr kat.
Program dla praktyki lekarskiej
 Program dla praktyki lekarskiej ErLab Instrukcja konfiguracji i obsługi Spis Treści 1. Wstęp... 2 2. Konfiguracja... 3 2.1. Serwer... 3 2.2. Laboratorium... 3 2.3. Punkt pobrań... 4 3. Wysyłanie skierowania...
Program dla praktyki lekarskiej ErLab Instrukcja konfiguracji i obsługi Spis Treści 1. Wstęp... 2 2. Konfiguracja... 3 2.1. Serwer... 3 2.2. Laboratorium... 3 2.3. Punkt pobrań... 4 3. Wysyłanie skierowania...
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. Aqua pro injectione Baxter 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Aqua pro injectione Baxter 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ Każdy worek zawiera wodę do wstrzykiwań 100% m/v 3. POSTAĆ
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Aqua pro injectione Baxter 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ Każdy worek zawiera wodę do wstrzykiwań 100% m/v 3. POSTAĆ
Informacje dla użytkownika. 2.1 Instrukcja używania
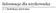 Informacje dla użytkownika 2.1 Instrukcja używania Przed użyciem produktu należy dokładnie zapoznać się z niniejszą instrukcją używania. Zachowaj tę instrukcję używania, w razie potrzeby ponownego przeczytania.
Informacje dla użytkownika 2.1 Instrukcja używania Przed użyciem produktu należy dokładnie zapoznać się z niniejszą instrukcją używania. Zachowaj tę instrukcję używania, w razie potrzeby ponownego przeczytania.
Ulotka dołączona do opakowania: informacja dla pacjenta. DISTREPTAZA Streptokinaza + Streptodornaza j.m j.m. Czopki doodbytnicze
 Ulotka dołączona do opakowania: informacja dla pacjenta DISTREPTAZA Streptokinaza + Streptodornaza 15 000 j.m. + 1250 j.m. Czopki doodbytnicze Należy zapoznać się z treścią ulotki przed zastosowaniem leku,
Ulotka dołączona do opakowania: informacja dla pacjenta DISTREPTAZA Streptokinaza + Streptodornaza 15 000 j.m. + 1250 j.m. Czopki doodbytnicze Należy zapoznać się z treścią ulotki przed zastosowaniem leku,
Genomic Mini AX Milk Spin
 Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej
 VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej Pałeczki Gram-ujemne niefermentujące Ćwiczenie 1. Wykonanie i ocena preparatu
VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej Pałeczki Gram-ujemne niefermentujące Ćwiczenie 1. Wykonanie i ocena preparatu
Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej
 Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej Wprowadzenie: Większość lądowych organizmów kręgowych część jonów amonowych NH + 4, produktu rozpadu białek, wykorzystuje w biosyntezie
Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej Wprowadzenie: Większość lądowych organizmów kręgowych część jonów amonowych NH + 4, produktu rozpadu białek, wykorzystuje w biosyntezie
KARTA CHARAKTERYSTYKI. Sekcja 1 Identyfikacja produktu chemicznego. Sekcja 2 Skład/informacja o składnikach
 KARTA CHARAKTERYSTYKI Sekcja 1 Identyfikacja produktu chemicznego Nazwa handlowa: MODYFIKOWANY STABILIZATOR LS-2 Sekcja 2 Skład/informacja o składnikach NAZWA SKŁADNIKA NUMER CAS ZAWARTOŚĆ (%) DWUTLENEK
KARTA CHARAKTERYSTYKI Sekcja 1 Identyfikacja produktu chemicznego Nazwa handlowa: MODYFIKOWANY STABILIZATOR LS-2 Sekcja 2 Skład/informacja o składnikach NAZWA SKŁADNIKA NUMER CAS ZAWARTOŚĆ (%) DWUTLENEK
Allergen FlowThrough ALERGENY. Do oceny skuteczności procesu mycia (Zaakceptowane/odrzucone)
 Allergen FlowThrough Do oceny skuteczności procesu mycia (Zaakceptowane/odrzucone) ALERGENY Badanie jakościowe Wymaz: min. Ekstrakcja: min. Test: 0 min. Czas łączny: 2 min. Testy jakościowe do wykrywania
Allergen FlowThrough Do oceny skuteczności procesu mycia (Zaakceptowane/odrzucone) ALERGENY Badanie jakościowe Wymaz: min. Ekstrakcja: min. Test: 0 min. Czas łączny: 2 min. Testy jakościowe do wykrywania
Pakiet I. Barwniki hematologiczne i inne odczynniki gotowe. cena jednostkowa netto zł. Lp. Asortyment nr kat. oferenta.
 Pakiet I. Barwniki hematologiczne i inne odczynniki gotowe Lp. Asortyment nr kat. oferenta ilość opakowań 1. Płyn rozcieńczający krwinki białe (Tűrka) 2 1 op. a 150 ml 2. Barwnik Giemsy (roztwór ) do barwienia
Pakiet I. Barwniki hematologiczne i inne odczynniki gotowe Lp. Asortyment nr kat. oferenta ilość opakowań 1. Płyn rozcieńczający krwinki białe (Tűrka) 2 1 op. a 150 ml 2. Barwnik Giemsy (roztwór ) do barwienia
3. Jak stosować Camilia 4. Możliwe działania niepożądane 5. Jak przechowywać Camilia 6. Zawartość opakowania i inne informacje
 Ulotka dołączona do opakowania: informacja dla pacjenta Camilia, roztwór doustny Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Ulotka dołączona do opakowania: informacja dla pacjenta Camilia, roztwór doustny Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
(Tekst mający znaczenie dla EOG) (Publikacja tytułów i odniesień do norm zharmonizowanych na mocy dyrektywy) (2013/C 22/03) 9.8.
 C 22/30 Dziennik Urzędowy Unii Europejskiej 24.1.2013 Komunikat Komisji w ramach wdrażania dyrektywy 98/79/WE Parlamentu Europejskiego i Rady z dnia 27 października 1998 r. w sprawie wyrobów medycznych
C 22/30 Dziennik Urzędowy Unii Europejskiej 24.1.2013 Komunikat Komisji w ramach wdrażania dyrektywy 98/79/WE Parlamentu Europejskiego i Rady z dnia 27 października 1998 r. w sprawie wyrobów medycznych
Laboratorium z bionanostruktur. Prowadzący: mgr inż. Jan Procek Konsultacje: WT D- 1 8A
 Laboratorium z bionanostruktur Prowadzący: mgr inż. Jan Procek Konsultacje: WT 9.00-10.00 D- 1 8A Regulamin Studenci są dopuszczeni do wykonywania ćwiczenia jeżeli posiadają: Buty na płaskim obcasie, Fartuchy,
Laboratorium z bionanostruktur Prowadzący: mgr inż. Jan Procek Konsultacje: WT 9.00-10.00 D- 1 8A Regulamin Studenci są dopuszczeni do wykonywania ćwiczenia jeżeli posiadają: Buty na płaskim obcasie, Fartuchy,
Zawiadomienie o zmianie treści specyfikacji istotnych warunków zamówienia
 nr sprawy: WIW.AD.I.271.16.2011 Siedlce, dn. 21 kwietnia 2011 r. Wykonawcy wszyscy Zawiadomienie o zmianie treści specyfikacji istotnych warunków zamówienia Zgodnie z art. 38 ust. 4 ustawy z dnia 29 stycznia
nr sprawy: WIW.AD.I.271.16.2011 Siedlce, dn. 21 kwietnia 2011 r. Wykonawcy wszyscy Zawiadomienie o zmianie treści specyfikacji istotnych warunków zamówienia Zgodnie z art. 38 ust. 4 ustawy z dnia 29 stycznia
ULOTKA DLA PACJENTA 1
 ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla użytkownika Supremin MAX, 1,5 mg/ml, syrop Butamirati citras Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla użytkownika Supremin MAX, 1,5 mg/ml, syrop Butamirati citras Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
ZP/220/106/17 Parametry wymagane dla zadania nr 1 załącznik nr 4 do formularza oferty PO MODYFIKACJI
 Zadanie nr 1 odczynniki do badań serologicznych UWAGA: wszystkie metodyki badań opracowane przez producentów powinny być zgodne z obowiązującymi przepisami. Lp. Nazwa PARAMETRY WYMAGANE TAK / NIE Reagujący
Zadanie nr 1 odczynniki do badań serologicznych UWAGA: wszystkie metodyki badań opracowane przez producentów powinny być zgodne z obowiązującymi przepisami. Lp. Nazwa PARAMETRY WYMAGANE TAK / NIE Reagujący
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH
 WOREK 10 KG 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY proszek do sporządzania roztworu na skórę produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Co zawiera Ciechociński szlam leczniczy
WOREK 10 KG 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY proszek do sporządzania roztworu na skórę produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Co zawiera Ciechociński szlam leczniczy
VES TEC VACU TEC VACU CODE. Producent: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) - Włochy
 PL 1/5 VES TEC VACU TEC VACU CODE Producent: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) - Włochy Paragraf Zmiany wprowadzone w aktualnej wersji 1 6 8 PL 2/5 1. ZASTOSOWANIE
PL 1/5 VES TEC VACU TEC VACU CODE Producent: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) - Włochy Paragraf Zmiany wprowadzone w aktualnej wersji 1 6 8 PL 2/5 1. ZASTOSOWANIE
Specyfikacja techniczno-cenowa. Wymagania dla aparatury przeznaczonej do badań mikrometodą kolumnową
 Specyfikacja techniczno-cenowa Zał. nr 1 do SIWZ Dostawa odczynników diagnostycznych i materiałów zużywalnych do mikrometody wraz z dzierżawą aparatury do badań immunohematologicznych z zakresu serologii
Specyfikacja techniczno-cenowa Zał. nr 1 do SIWZ Dostawa odczynników diagnostycznych i materiałów zużywalnych do mikrometody wraz z dzierżawą aparatury do badań immunohematologicznych z zakresu serologii
Dotyczy: przetargu nieograniczonego na dostawa odczynników, krwinek wzorcowych do serologii grup krwi- metody probówkowe/szkiełkowe
 Numer sprawy: DTZ.382.10.2018 Golub-Dobrzyń, dn. 23.03.2018r. Dotyczy: przetargu nieograniczonego na dostawa odczynników, krwinek wzorcowych do serologii grup krwi- metody probówkowe/szkiełkowe W związku
Numer sprawy: DTZ.382.10.2018 Golub-Dobrzyń, dn. 23.03.2018r. Dotyczy: przetargu nieograniczonego na dostawa odczynników, krwinek wzorcowych do serologii grup krwi- metody probówkowe/szkiełkowe W związku
Dräger DCD 5000 Pobieranie płynu z jamy ustnej
 Dräger DCD 5000 Pobieranie płynu z jamy ustnej Proste, szybkie i bezpieczne wykrywanie środków odurzających i narkotyków: Dräger DCD 5000 nie tylko pozwala w łatwy sposób pobrać próbkę śliny (płyn z jamy
Dräger DCD 5000 Pobieranie płynu z jamy ustnej Proste, szybkie i bezpieczne wykrywanie środków odurzających i narkotyków: Dräger DCD 5000 nie tylko pozwala w łatwy sposób pobrać próbkę śliny (płyn z jamy
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
PILNE: KOREKTA SPRZĘTU MEDYCZNEGO
 W imieniu firmy Comesa Polska Sp. z o.o.; wyłącznego dystrybutora produktów firmy Zimmer, informujemy o prowadzeniu działań korygujących dotyczących niżej opisanego sprzętu medycznego. PILNE: KOREKTA SPRZĘTU
W imieniu firmy Comesa Polska Sp. z o.o.; wyłącznego dystrybutora produktów firmy Zimmer, informujemy o prowadzeniu działań korygujących dotyczących niżej opisanego sprzętu medycznego. PILNE: KOREKTA SPRZĘTU
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA HANDLOWA LEKU GOTOWEGO SALICYLOL 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH (W PRZELICZENIU NA 100g)
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA HANDLOWA LEKU GOTOWEGO SALICYLOL 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH (W PRZELICZENIU NA 100g)
Genomic Maxi AX Direct
 Genomic Maxi AX Direct Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura bez etapu precypitacji. wersja 0517 10 izolacji Nr kat. 995-10D Pojemność kolumny
Genomic Maxi AX Direct Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura bez etapu precypitacji. wersja 0517 10 izolacji Nr kat. 995-10D Pojemność kolumny
ODPOWIEDZI NA PYTANIA
 Kraków, 11 września 2015r. wg rozdzielnika NR POSTĘPOWANIA: DZP.272-18/15 Przetarg nieograniczony pn. " Dostawa odczynników" ODPOWIEDZI NA PYTANIA działając na podstawie art. 38 ustawy z dn. 29 stycznia
Kraków, 11 września 2015r. wg rozdzielnika NR POSTĘPOWANIA: DZP.272-18/15 Przetarg nieograniczony pn. " Dostawa odczynników" ODPOWIEDZI NA PYTANIA działając na podstawie art. 38 ustawy z dn. 29 stycznia
AmpliTest Panel odkleszczowy (Real Time PCR)
 AmpliTest Panel odkleszczowy (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii Borrelia burgdorferi, Anaplasma, Ehrlichia oraz pierwotniaków rodzaju Babesia (B. canis, B. gibsoni,
AmpliTest Panel odkleszczowy (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii Borrelia burgdorferi, Anaplasma, Ehrlichia oraz pierwotniaków rodzaju Babesia (B. canis, B. gibsoni,
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2019 ZASADY OCENIANIA
 Układ graficzny CKE 2019 EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2019 ZASADY OCENIANIA Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Nazwa kwalifikacji: Sporządzanie
Układ graficzny CKE 2019 EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2019 ZASADY OCENIANIA Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Nazwa kwalifikacji: Sporządzanie
Ulotka dołączona do opakowania: informacja dla użytkownika. Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji
 Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Tytuł: Kontrola glukometrów
 Data obowiązywania: Wydanie: 1 Strona 1 z 6 Karta zmian 1. CEL: Nr Punktu Podpunktu rozdziału Zmiany Akapitu lub fragmentu tekstu ze strony nr Opis Data Podpis autora ZATWIERDZIŁ Dyrektor Szpitala Dr n.
Data obowiązywania: Wydanie: 1 Strona 1 z 6 Karta zmian 1. CEL: Nr Punktu Podpunktu rozdziału Zmiany Akapitu lub fragmentu tekstu ze strony nr Opis Data Podpis autora ZATWIERDZIŁ Dyrektor Szpitala Dr n.
Pełna nazwa i typ sprzętu:... Nazwa producenta:... Kraj producenta:... Rok produkcji:... 1 Analizator w pełni automatyczny. TAK
 Załącznik nr 1 do SIWZ FORMULARZ OFERTY TECHNICZNEJ NA DOSTAWĘ ZESTAWÓW ODCZYNNIKÓW I MATERIAŁÓW DO BADAŃ MORFOLOGII KRWI WRAZ Z DZIERŻAWĄ AUTOMATYCZNEGO ANALIZATORA HEMATOLOGICZNEGO NA POTRZEBY WOJSKOWEJ
Załącznik nr 1 do SIWZ FORMULARZ OFERTY TECHNICZNEJ NA DOSTAWĘ ZESTAWÓW ODCZYNNIKÓW I MATERIAŁÓW DO BADAŃ MORFOLOGII KRWI WRAZ Z DZIERŻAWĄ AUTOMATYCZNEGO ANALIZATORA HEMATOLOGICZNEGO NA POTRZEBY WOJSKOWEJ
KOAGULOLOGIA. Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice.
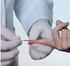 KOAGULOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi.
KOAGULOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi.
Ważna informacja dotycząca bezpieczeństwa stosowania
 ADVIA Centaur ADVIA Centaur XP ADVIA Centaur CP Ważna informacja dotycząca bezpieczeństwa stosowania 10819674, Zmiana A Wrzesień 2014 r. Informacja dotycząca Kalibratora E przeznaczonego do użytku z Systemami
ADVIA Centaur ADVIA Centaur XP ADVIA Centaur CP Ważna informacja dotycząca bezpieczeństwa stosowania 10819674, Zmiana A Wrzesień 2014 r. Informacja dotycząca Kalibratora E przeznaczonego do użytku z Systemami
ULOTKA DLA PACJENTA 1
 ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla pacjenta Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml Foeniculi semen oleum + Natrii hydrogenocarbonas Należy uważnie
ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla pacjenta Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml Foeniculi semen oleum + Natrii hydrogenocarbonas Należy uważnie
dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę odczynników do koagulologii wraz z dzierżawa analizatorów.
 Toruń, dn. 25.10.2013r. L.dz. SSM.DZP.200.170.2013 dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę odczynników do koagulologii wraz z dzierżawa analizatorów.
Toruń, dn. 25.10.2013r. L.dz. SSM.DZP.200.170.2013 dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę odczynników do koagulologii wraz z dzierżawa analizatorów.
AOSEPT PLUS CE INSTRUKCJA UŻYTKOWANIA
 AOSEPT PLUS CE INSTRUKCJA UŻYTKOWANIA NINIEJSZA INSTRUKCJA ZAWIERA ISTOTNE INFORMACJE DOTYCZĄCE SPOSOBU UŻYCIA I BEZPIECZEŃSTWA STOSOWANIA PRODUKTU. PROSIMY O UWAŻNE ZAPOZNANIE SIĘ Z JEJ TREŚCIĄ. INSTRUKCJĘ
AOSEPT PLUS CE INSTRUKCJA UŻYTKOWANIA NINIEJSZA INSTRUKCJA ZAWIERA ISTOTNE INFORMACJE DOTYCZĄCE SPOSOBU UŻYCIA I BEZPIECZEŃSTWA STOSOWANIA PRODUKTU. PROSIMY O UWAŻNE ZAPOZNANIE SIĘ Z JEJ TREŚCIĄ. INSTRUKCJĘ
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum)
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona ważne informacje
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona ważne informacje
INSTRUKCJA UŻYTKOWANIA
 INSTRUKCJA UŻYTKOWANIA Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny Epower zawiera liofilizowane, standaryzowane ilościowo preparaty mikroorganizmów, które
INSTRUKCJA UŻYTKOWANIA Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny Epower zawiera liofilizowane, standaryzowane ilościowo preparaty mikroorganizmów, które
QMS Quality in Microbiology Scheme Wydanie 14 Data wydania: czerwiec 2018
 Przyjęcie i przechowywanie Po otrzymaniu materiału do badań należy zapisać datę otrzymania, a następnie przechowywać w lodówce w temperaturze 2-8 º C do momentu przeprowadzenia badania. Materiał do badań
Przyjęcie i przechowywanie Po otrzymaniu materiału do badań należy zapisać datę otrzymania, a następnie przechowywać w lodówce w temperaturze 2-8 º C do momentu przeprowadzenia badania. Materiał do badań
Ulotka dołączona do opakowania: informacja dla pacjenta Linomag, 1 g/g płyn na skórę (Lini oleum virginale)
 Ulotka dołączona do opakowania: informacja dla pacjenta Linomag, 1 g/g płyn na skórę (Lini oleum virginale) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Linomag, 1 g/g płyn na skórę (Lini oleum virginale) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
 Wojewódzka Stacja Pogotowia Ratunkowego i Transportu Sanitarnego MEDITRANS SPZOZ w Warszawie ul. Poznańska 22 Lp ZADANIE 2. Igły doszpikowe Opis przedmiotu zamówienia Nazwa producenta i numer katalogowy
Wojewódzka Stacja Pogotowia Ratunkowego i Transportu Sanitarnego MEDITRANS SPZOZ w Warszawie ul. Poznańska 22 Lp ZADANIE 2. Igły doszpikowe Opis przedmiotu zamówienia Nazwa producenta i numer katalogowy
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 ZASADY OCENIANIA
 EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 ZASADY OCENIANIA Układ graficzny CKE 2018 Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Nazwa kwalifikacji: Asystowanie
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 ZASADY OCENIANIA Układ graficzny CKE 2018 Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Nazwa kwalifikacji: Asystowanie
Aneks II. Wnioski naukowe
 Aneks II Wnioski naukowe 8 Wnioski naukowe Solu-Medrol 40 mg, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań (zwany dalej Solu-Medrol ) zawiera metyloprednisolon i (jako substancję pomocniczą)
Aneks II Wnioski naukowe 8 Wnioski naukowe Solu-Medrol 40 mg, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań (zwany dalej Solu-Medrol ) zawiera metyloprednisolon i (jako substancję pomocniczą)
Cena jedn. netto 70 8%
 Pakiet nr 1 Lp. Nazwa, postać farmaceutyczna, dawka 1. Filgrastim, roztwór do wstrzykiwań lub infuzji 48 mln j/0,5 ml, przejrzysty, bezbarwny lub lekko żółtawy roztwór, ampułko-strzykawka z osłoną zabezpieczającą
Pakiet nr 1 Lp. Nazwa, postać farmaceutyczna, dawka 1. Filgrastim, roztwór do wstrzykiwań lub infuzji 48 mln j/0,5 ml, przejrzysty, bezbarwny lub lekko żółtawy roztwór, ampułko-strzykawka z osłoną zabezpieczającą
Zakład Patologii i Diagnostyki Laboratoryjnej
 1. Zasady transportu materiału do badań patomorfologicznych z jednostki zewnętrznej. 1.1. może być przeprowadzany jedynie przez przeszkolone, wyznaczone do tego celu osoby lub samego pacjenta w przypadku
1. Zasady transportu materiału do badań patomorfologicznych z jednostki zewnętrznej. 1.1. może być przeprowadzany jedynie przez przeszkolone, wyznaczone do tego celu osoby lub samego pacjenta w przypadku
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH
 Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE
 NARODOWY INSTYTUT ZDROWIA PUBLICZNEGO - PAŃSTWOWY ZAKŁAD HIGIENY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE ZAKŁAD WIRUSOLOGII NIZP-PZH UL. CHOCIMSKA 24 00-791 WARSZAWA
NARODOWY INSTYTUT ZDROWIA PUBLICZNEGO - PAŃSTWOWY ZAKŁAD HIGIENY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE ZAKŁAD WIRUSOLOGII NIZP-PZH UL. CHOCIMSKA 24 00-791 WARSZAWA
Czyszczenie i dezynfekcja Głowica pomiarowa tonometru, szkła kontaktowe oraz zestaw dezynfekcyjny Desinset
 ČESKY БЪЛГАРСКИ MAGYAR POLSKI HRVATSKI ΕΛΛΗΝΙΚΗ DANSK NORSK INSTRUKCJA UŻYTKOWANIA Czyszczenie i dezynfekcja Głowica pomiarowa tonometru, szkła kontaktowe oraz zestaw dezynfekcyjny Desinset 2. Edycja /
ČESKY БЪЛГАРСКИ MAGYAR POLSKI HRVATSKI ΕΛΛΗΝΙΚΗ DANSK NORSK INSTRUKCJA UŻYTKOWANIA Czyszczenie i dezynfekcja Głowica pomiarowa tonometru, szkła kontaktowe oraz zestaw dezynfekcyjny Desinset 2. Edycja /
AmpliTest TBEV (Real Time PCR)
 AmpliTest TBEV (Real Time PCR) Zestaw do wykrywania sekwencji RNA specyficznych dla TBEV (Tick-borne encephalitis virus) techniką Real Time PCR Nr kat.: RV03-50 Wielkość zestawu: 50 oznaczeń Objętość pojedynczej
AmpliTest TBEV (Real Time PCR) Zestaw do wykrywania sekwencji RNA specyficznych dla TBEV (Tick-borne encephalitis virus) techniką Real Time PCR Nr kat.: RV03-50 Wielkość zestawu: 50 oznaczeń Objętość pojedynczej
Tłumaczenie oryginalnej instrukcji obsługi, instalacji i serwisowania PURO MINI. Separator Olej/woda 02/14
 Tłumaczenie oryginalnej instrukcji obsługi, instalacji i serwisowania PURO MINI Separator Olej/woda OGÓLNE INFORMACJE O OBSŁUDZE 02/14 Separator PURO MINI został zaprojektowany do oddzielania oleju z kondensatu
Tłumaczenie oryginalnej instrukcji obsługi, instalacji i serwisowania PURO MINI Separator Olej/woda OGÓLNE INFORMACJE O OBSŁUDZE 02/14 Separator PURO MINI został zaprojektowany do oddzielania oleju z kondensatu
Ulotka dołączona do opakowania: informacja dla pacjenta Oscillococcinum, granulki w pojemniku jednodawkowym
 Ulotka dołączona do opakowania: informacja dla pacjenta Oscillococcinum, granulki w pojemniku jednodawkowym Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Oscillococcinum, granulki w pojemniku jednodawkowym Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 ZASADY OCENIANIA
 Układ graficzny CKE 2018 EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 ZASADY OCENIANIA Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Nazwa kwalifikacji: Sporządzanie
Układ graficzny CKE 2018 EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 ZASADY OCENIANIA Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Nazwa kwalifikacji: Sporządzanie
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH
 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH BUTELKA Z POLIETYLENU Z DOZOWNIKIEM I NAKRĘTKĄ 1. NAZWA PRODUKTU LECZNICZEGO (9,8 mg + 9,8 mg + 245 mg)/g (Benzocainum + Mentholum + Zinci oxidum),
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH BUTELKA Z POLIETYLENU Z DOZOWNIKIEM I NAKRĘTKĄ 1. NAZWA PRODUKTU LECZNICZEGO (9,8 mg + 9,8 mg + 245 mg)/g (Benzocainum + Mentholum + Zinci oxidum),
URZĄDZENIE TESTOWE DO UŻYTKU DOMOWEGO
 TEST JAKOŚ CI SPERMY Okienko analizy Okienko wyników Wgłębienie na próbkę Suwak URZĄDZENIE TESTOWE DO UŻYTKU DOMOWEGO ! Przed wykonaniem testu należy: Kiedy można przetestować jakość spermy? Przeczytać
TEST JAKOŚ CI SPERMY Okienko analizy Okienko wyników Wgłębienie na próbkę Suwak URZĄDZENIE TESTOWE DO UŻYTKU DOMOWEGO ! Przed wykonaniem testu należy: Kiedy można przetestować jakość spermy? Przeczytać
ARKUSZ EGZAMINACYJNY ETAP PRAKTYCZNY EGZAMINU POTWIERDZAJĄCEGO KWALIFIKACJE ZAWODOWE CZERWIEC 2010
 Zawód: technik analityk Symbol cyfrowy zawodu: 311[02] Numer zadania: Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu 311[02]-0-102 Czas trwania egzaminu: 240 minut ARKUSZ EGZAMINACYJNY
Zawód: technik analityk Symbol cyfrowy zawodu: 311[02] Numer zadania: Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu 311[02]-0-102 Czas trwania egzaminu: 240 minut ARKUSZ EGZAMINACYJNY
