Leki biologiczne oryginalne i biopodobne - co powinien wiedzieć dyrektor szpitala, aby zapewnić bezpieczeństwo pacjenta?
|
|
|
- Kacper Wierzbicki
- 9 lat temu
- Przeglądów:
Transkrypt
1 Leki biologiczne oryginalne i biopodobne - co powinien wiedzieć dyrektor szpitala, aby zapewnić bezpieczeństwo pacjenta? Prof. n. med. Michał Nowicki Klinika Nefrologii, Hipertensjologii i Transplantologii Nerek
2 Prezentacja ta zawiera odpowiedzi na następujące pytania: 1. Czym są leki biologiczne? 2. Jaki jest profil bezpieczeństwa leków biologicznych i na jakie kliniczne aspekty ich bezpieczeństwa należy zwracać uwagę? 3. Jakich korzyści i zagrożeń możemy spodziewamy się po wprowadzeniu leków biopodobnych (na podstawie dotychczasowych doświadczeń klinicznych)?
3 Czym są dla klinicysty leki biologiczne (biofarmaceutyki)? Definicje leków biologicznych ulegają zmianom wraz z postępem naszej wiedzy: Pierwsza definicja pochodzi z roku 1902 gdy FDA określiła lek biologiczny jako używane w celach leczniczych wirusy, surowice i ich pochodne, toksyny i antytoksyny, szczepionki, krew i składniki krwi (są to tradycyjne leki biologiczne). We współczesnym szerokim rozumieniu (wg FDA) leki biologiczne to substancje, które są pozyskiwane od żywych organizmów ludzi, zwierząt, roślin i mikroorganizmów i znajdują zastosowanie w zapobieganiu i leczeniu chorób u ludzi
4 Czym są leki biologiczne we współczesnym (wąskim) rozumieniu? Leki biologiczne (biofarmaceutyki) są wytwarzane metodami biotechnologicznymi (z użyciem żywych komórek roślinnych, zwierzęcych, bakterii, wirusów lub drożdży). Leki biologiczne zawierają przeważnie białka uzyskane dzięki rekombinacji genetycznej Leki biologiczne konfrontowane są z tradycyjnymi lekami wytwarzanymi drogą syntezy chemicznej lub pozyskiwanymi ze źródeł naturalnych
5 Nowe leki biologiczne są już stosowane w większości specjalności medycznych Historia nowoczesnych leków biologicznych: 1982 insulina ludzka 1985 hormon wzrostu 1986 interferon alfa 1987 tkankowy aktywator plazminogenu 1989 epoetyna alfa >150 leków biologicznych Współczesne leki biologiczne Cytokiny Hormony Czynniki krzepnięcia Przeciwciała monoklonalne Szczepionki Produkty do terapii tkankowych i komórkowych pdf
6
7 Leki biologiczne w fazie badań (rok 2011) przyszłe zastosowania kliniczne Podział wg kategorii terapeutycznych pdf
8 Nowe leki na rynku amerykańskim w roku 2010 dane FDA ⱱ (14 nowych preparatów z czego 6 zupełnie nowych leków biologicznych i 1 kolejny preparat w danym wskazaniu)
9 Leki biologiczne znaczenie we współczesnej medycynie Biofarmaceutyki najczęściej : zastępują, uzupełniają, usuwają Leki biologiczne dają szansę na terapię skrojoną dla potrzeb danego chorego naturalne białka wytwarzane w organizmie i dzięki temu umożliwiają leczenie wielu chorób, w których do tej pory tradycyjne leki chemiczne były nieskuteczne: Przykład: Choroby sieroce np. wrodzone niedobory enzymów
10 Leki biotechnologiczne i chemiczne kluczowe różnice istotne dla klinicysty Produkty biotechnologiczne są trudne do wytwarzania i do naśladowania ponieważ pochodzą od żywych organizmów. Małe różnice w procesie wytwarzania mogą powodować trudne do przewidzenia skutki a otrzymany w ich efekcie produkt może się znacząco różnić się od pierwotnego
11 Leki biodobne Produkty biopodobne naśladują oryginalne produkty biotechnologiczne... mogą być wprowadzane po wygaśnięciu ochrony patentowej produktów oryginalnych (ale nie z naruszeniem tej ochrony!)... są wytwarzane przez innego producenta korzystającego z innej linii komórkowej, nowego procesu technologicznego i nowych metod analitycznych
12 Terminologia określenie generyki dla leków biopodobnych jest nieprawidłowe EU = Biosimilars US = Follow-on Biologics (FOBs) Polska = biopodobne produkty lecznicze.. ale nigdy nie są to generyki czy biogeneryki
13 Leki biopodobne są dostępne w Europie od 2006 roku Rok rejestracji przez EMA: - Omnitrope (biopodobny do innowacyjnego preparatu ludzkiego hormonu wzrostu Genotropin) - Valtropin (lek referencyjny Humatrope) - Alpheon (biopodobny do Roferonu-A) - odmowa rejestracji - Binocrit - Sandoz GmbH - Epoetin alfa Hexal - Hexal Biotech Forschungs GmbH - Abseamed - Medice Arzneimittel Pütter GmbH & Co, - Silapo Stada Arzneimittel AG - Retacrit Hospira Enterprises B.V. - Biograstim (CT Arnzneimittel GmbH) - biopodobny do filgrastimu - G-CSF - Tevagrastim (Teva Generics GmbH) - Filigrastim Ratiopharm (Ratiopharm GmbH) i Ratiograstin (Ratiopharm GmbH) - Zarzio (Sandoz GmbH), Filgrastim HEXAL (Hexal AG) Lek referencyjny epoetyna alfa Nazwa międzynarodowa (INN) epoetyna alfa Nazwa międzynarodowa (INN) epoetyna zeta
14 Na świecie dostępnych jest też wiele kopii bioleków np. epoetyny alfa Niektóre skopiowane epoetyny zostały już niezależnie ocenione Stwierdzono istotne różnice w zakresie: jakości produktu jego aktywności biologicznej jakości oznakowania
15 Zagrożeniem dla rozwoju rynku bezpiecznych leków biologicznych może być dzisiaj niedostateczna kontrola nad wytwarzaniem leków naśladowczych przez producentów w wielu krajach świata
16 Leki biologiczne są podawane pozajelitowo i są bardzo wrażliwe na czynniki fizyczne (np. złe warunki przechowywania)
17 Ważną klinicznie cechę biofarmaceutyków stanowi ich immunogenność Genetycznie zmodyfikowane białka mają zdolność do pobudzania odpowiedzi immunologicznej organizmu System immunologiczny może początkowo jedynie odpowiedzieć na różnice pomiędzy natywnym białkiem a lekiem a potem poszerzyć odpowiedź na natywne białko odpowiedź krzyżowa (zmiana jego działania lub inaktywacja) Działania niepożądane związane z powstawaniem przeciwciał są rzadkie ale groźne (np. aplazja czystoczerwonokrwinkowa (PRCA) Działania niepożądane występują najczęściej późno Należy monitorować powstawanie przeciwciał zarówno na etapie opracowywania nowego leku jak i wiele lat po jego wprowadzeniu ( farmakoczujność )
18 Następstwa kliniczne immunogenności Zmniejszenie siły działania Insulina Streptokinaza Stafylokinaza Kalcytonina łososiowa Czynnik VIII Interferon alfa 2 Interferon beta IL-2 GnRH IgG1 HCG GM-CSF/IL-3 Zwiększenie siły działania Hormon wzrostu Neutralizacja natywnego białka MGDF epoetyny Odczyny immunologiczne Alergia Anafilaksja Choroba surowicza Inne następstwa???? Schellekens H: Presentation ERA-EDTA Congress 20005
19 Wykrycie immunogenności po wprowadzeniu leku do stosowania - przykład epoetyny alfa Ludzką rekombinowaną erytropoetynę alfa wprowadzono do lecznictwa w roku 1989 W 1998 w wielu krajach (poza USA) z roztworu stabilizującego epoetynę alfa (Erypo, Eprex ) usunięto ludzką albuminę zastępując ją polisorbatem-80 i glicyną Po tej zmianie w latach zaobserwowano w Europie zwiększoną częstość przypadków PRCA (aplazji czystoczerwonokrwinkowej) będącej następstwem wytworzenia przeciwciał neutralizujących erytropoetynę reagujących krzyżowo ze wszystkimi dostępnymi komercyjnie epoetynami Ryzyko rozwoju PRCA przy leczeniu czynnikami erytropoetycznymi wynosi 0,02 0,03 na pacjento-lat (Macdougall IC et al. Kidney Int 2012; 81: )
20 liczba przypadków/ pacj.-lat Wzrost liczby przypadków działania niepożądanego leku (PRCA) wystąpił po ponad 10 latach po wprowadzeniu leku do stosowania Epogen Eprex/Erypo NeoRecormon Częstość wykrywania PRCA w zależności od rodzaju epoetyny wg Casadevall and Rossert Best Pract Res Clin Haematol 2005; 18: 381
21 Czynniki ryzyka rozwoju PRCA u chorych leczonych lekami biologicznymi Macdougall et al. Kidney Int 2012; 81:
22 2008 publikacja pierwszego przypadku aplazji czerwonokrwinkowej po zastosowaniu naśladowczej epoetyny alfa wytwarzanej w Indiach przez Wepox (Wockhardt Ltd, Mumbai)
23 Przypadku PRCA obserwowane w badaniu klinicznym, w którym podawano podskórnie biopodobną epoetynę alfa (HX- 575, Abseamed ) doprowadziły do wstrzymania programu badań klinicznych tego preparatu
24 Aplazja czystoczerwonokrwinkowa sytuacja po wprowadzeniu leków biopodobnych
25 Aplazja czystoczerwonokrwinkowa po podawaniu biopodobnych czynników erytropoetycznych dane z Tajlandii Epoetyna alfa została tam wprowadzona w 1990 roku, a beta w 1998 Pierwszy czynnik biopodobny do leczenia niedokrwistości nerkopochdnej wprowadzono w 1997 Do końca 2009 zarejestrowano 14 leków biopodobnych (pochodzą z Argentyny, Chin, Korei Południowej i Indii W roku 2008 obserwowano 30 przypadków oporności na podawanie czynnika erytropoetycznego, wszyscy chorzy byli leczeni lekami innowacyjnymi przed zmianą leczenia na preparat biopodobny, u 23 z nich wykryto przeciwciała neutralizujące, wszyscy otrzymywali lek podskórnie W 2008 roku w Tajlandii chorych otrzymywało czynniki erytropoetyczne z powodu niedokrwistości nerkopochodnej 78% chorych otrzymywało biopodobne czynniki erytropoetyczne (Thai ESA Registry) Wyliczono, że 1 na 2608 chorych (0,04%) leczonych biopodobnym czynnikiem erytropoetyzznym rozwija PRCA Praditpornsilpa et al. Kidney Int 2011; 80: 86-92
26 Czy leki biologiczne są aż tak bezpieczne? JAMA. 2008;300:
27 Czy leki biologiczne są aż tak bezpieczne? Ostrzeżenia w czarnych ramkach Listy do lekarzy ( Drogi Lekarzu ) Bezpośrednia informacja dla lekarza Ryzyko wystąpienia niespodziewanych działań niepożądanych wynosi średnio 30% w czasie 10 lat od wprowadzenia leku biologicznego JAMA. 2008;300:1887
28 JAMA. 2008;300(16): Czy leki biologiczne są aż tak bezpieczne? Czas jaki upływa od wprowadzenia leku biologicznego do wydania ostrzeżenia jest długi!
29 Ogólne założenia zaleceń EMA dotyczących rejestracji produktów biopodobnych Konieczność zaangażowania się lekarzy w program śledzenia działań niepożądanych (raportowanie!) Producent produktu biopodobnego musi jednoznacznie identyfikować produkt referencyjny oraz przeprowadzić badania przedkliniczne i kliniczne a nie tylko badania biorównoważności Należy wprowadzić program śledzenia działań niepożądanych ( farmakoczujność, ang. pharmacovigilance)
30 Ryzyko automatycznej zamiany leków biologicznych na biopodobne Zamiana automatyczna to zamiana zachodząca bez udziału lekarza jeśli: Lekarz przepisuje lek wg nazwy międzynarodowej (INN) Lekarz przepisuje konkretny lek ale nie oznacza nie zamieniać NZ wtedy farmaceuta może wydać generyk wg swojej preferencji jeśli ma on tą samą nazwę międzynarodową Ponieważ lek biopodobny nie jest generykiem (lekiem identycznym) oczywiste jest, że nie może być zamieniany jednak w prawie farmaceutycznym większości krajów UE brak jest wyróżnienia leków biopodobnych (wyjątkiem jest Francja od 2007 roku).
31 Możliwość automatycznej substytucji wynika z braku jednoznacznych zasad dotyczących nazewnictwa leków biologicznych i biopodobnych System nazw międzynarodowych (ang. INN International Nonproprietary Names) został stworzony w 1950 roku aby każdemu (chemicznemu) produktowi farmaceutycznemu nadać nazwę, która: Jednoznacznie go identyfikuje i odróżnia Nie może być przedmiotem ochrony prawnej (w przeciwieństwie do nazwy handlowej) Ułatwia rozpoznanie do jakiej grupy leków należy dany produkt (system przedrostków, końcówek i rdzeni nazw) Zasady nazewnictwa leków biologicznych i biopodobnych nie zostały określone przez WHO (45. Consultation on INN, INN Working Doc ) Nie ma jednoznacznych przepisów zmuszających producenta leku biopodobnego do wystąpienia o nadanie mu innej nazwy międzynarodowej niż lek oryginalny (co uniemożliwiałoby automatyczną zamianę w aptece bez udziału lekarza)
32 Sytuacja prawna innowacyjnych i biopodobnych w Polsce Brak wyróżnienia (definicji) klasy leków biologicznych w Prawie Farmaceutycznym W dużej noweli Prawa Farmaceutycznego (weszła w życie w maju 2007) dokonano implementacji Dyrektywy 2001/83/WE dotyczącej dopuszczania do obrotu leków biopodobnych (art. 15., ust 5.) Brak jest odrębnych regulacji prawnych dotyczących automatycznej substytucji leków biologicznych Ustawa o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych zezwala na substytucję na poziomie apteki leków o tej samej nazwie międzynarodowej (INN)
33 Podsumowanie: Bezpieczeństwo stosowania leków biologicznych i biologicznych preparatów naśladowczych Naczelna zasada: Chorzy potrzebują bezpiecznych i skutecznych leków Biotechnologia umożliwiła wytworzenie wielu leków, które dokonały przełomu we współczesnej medycynie Leki biologiczne są bezpieczne w stosowaniu Duży koszt leków biologicznych stwarza ryzyko ich nielegalnej, niekontrolowanej produkcji i nieprzewidywalnych działań niepożądanych Wprowadzanie biologicznych leków naśladowczych (leków biopodobnych) będące naturalną konsekwencją wygasania ochrony patentowej oryginalnych preparatów powinno następować według jednoznacznych i przejrzystych kryteriów (czego przykładem są regulacje w Unii Europejskiej)
34 Wymagania względem innowacyjnych leków biotechnologicznych i leków biopodobnych (2) Wymagania stawiane nowym produktom biotechnologicznym w tym lekom biopodobnym powinny być przejrzyste, oparte na wynikach badań naukowych, przewidywalne i zależne od rodzaju produktu Lekarz zlecający dany lek powinien być zapoznany z problematyką preparatów biopodobnych i mieć możliwość aktywnego udziału w decyzjach dotyczących ich ewentualnej substytucji (zachodzącej na różnym poziomie urzędów, płatnika, szpitala, apteki) Zasady przepisywania leków biopodobnych powinny umożliwiać wieloletnie śledzenie bezpieczeństwa ich stosowania (pharmacovigilance)
Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych?
 Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych? prof. dr hab. med.. Piotr Fiedor Warszawski Uniwersytet Medyczny
Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych? prof. dr hab. med.. Piotr Fiedor Warszawski Uniwersytet Medyczny
Leki chemiczne a leki biologiczne
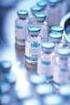 Leki chemiczne a leki biologiczne LEKI CHEMICZNE A LEKI BIOLOGICZNE Produkt syntezy chemicznej Produkt roślinny Produkt immunologiczny BIOLOGICZNE Produkt homeopatyczny Produkt z krwi/osocza - BIOLOGICZNE
Leki chemiczne a leki biologiczne LEKI CHEMICZNE A LEKI BIOLOGICZNE Produkt syntezy chemicznej Produkt roślinny Produkt immunologiczny BIOLOGICZNE Produkt homeopatyczny Produkt z krwi/osocza - BIOLOGICZNE
LEKI CHEMICZNE A LEKI BIOLOGICZNE
 LEKI CHEMICZNE A LEKI BIOLOGICZNE PRODUKT LECZNICZY - DEFINICJA Art. 2 pkt.32 Ustawy - Prawo farmaceutyczne Substancja lub mieszanina substancji, przedstawiana jako posiadająca właściwości: zapobiegania
LEKI CHEMICZNE A LEKI BIOLOGICZNE PRODUKT LECZNICZY - DEFINICJA Art. 2 pkt.32 Ustawy - Prawo farmaceutyczne Substancja lub mieszanina substancji, przedstawiana jako posiadająca właściwości: zapobiegania
Katarzyna Łuszkiewicz Maria Kurzyk
 Katarzyna Łuszkiewicz Maria Kurzyk leki biologiczne, których substancję czynną stanowią substancje biologiczne otrzymane z żywych komórek leki podobne do już zarejestrowanego biologicznego produktu leczniczego
Katarzyna Łuszkiewicz Maria Kurzyk leki biologiczne, których substancję czynną stanowią substancje biologiczne otrzymane z żywych komórek leki podobne do już zarejestrowanego biologicznego produktu leczniczego
SPOTKANIE NAUKOWE - 8 kwietnia 2015 r.
 SPOTKANIE NAUKOWE - 8 kwietnia 2015 r. PROGRAM 16:00-16:45 Walenty Zajdel - Leki oryginalne i generyczne, leki biologiczne i biopodobne 16:45-17:30 Przemysław Krajewski - Medical and Hospital Relationship
SPOTKANIE NAUKOWE - 8 kwietnia 2015 r. PROGRAM 16:00-16:45 Walenty Zajdel - Leki oryginalne i generyczne, leki biologiczne i biopodobne 16:45-17:30 Przemysław Krajewski - Medical and Hospital Relationship
Czym są biologiczne leki referencyjne i biopodobne. Dr nauk farm Leszek Borkowski Szpital Wolski Warszawa , godz. 10,00
 Czym są biologiczne leki referencyjne i biopodobne Dr nauk farm Leszek Borkowski Szpital Wolski Warszawa 27.02.2018, godz. 10,00 Nie biorównoważne a biopodobne W przypadku produktów biologicznych oraz
Czym są biologiczne leki referencyjne i biopodobne Dr nauk farm Leszek Borkowski Szpital Wolski Warszawa 27.02.2018, godz. 10,00 Nie biorównoważne a biopodobne W przypadku produktów biologicznych oraz
Leki biopodobne - szanse i ograniczenia
 Leki biopodobne - szanse i ograniczenia Aleksandra Mazur Komentarz do opracowania Dr hab.n. med. Sławomir Jeka 1 Opracowała: Aleksandra Mazur http://laboratoria.net/pl/artykul/12299.html Leki biopodobne
Leki biopodobne - szanse i ograniczenia Aleksandra Mazur Komentarz do opracowania Dr hab.n. med. Sławomir Jeka 1 Opracowała: Aleksandra Mazur http://laboratoria.net/pl/artykul/12299.html Leki biopodobne
Leki biologiczne a regulacje prawne. Kwestie zamiennictwa. Adw. Monika Duszyńska 5 grudnia 2017
 Leki biologiczne a regulacje prawne. Kwestie zamiennictwa Adw. Monika Duszyńska 5 grudnia 2017 Prawo polskie Obowiązujące regulacje odnoszące się do leków biologicznych: szczególne wymogi dotyczące rejestracji
Leki biologiczne a regulacje prawne. Kwestie zamiennictwa Adw. Monika Duszyńska 5 grudnia 2017 Prawo polskie Obowiązujące regulacje odnoszące się do leków biologicznych: szczególne wymogi dotyczące rejestracji
Leki biopodobne - definicja. Leki biopodobne. Leki biopodobne. Wytyczne EMA w sprawie rejestracji leków biopodobnych. Radosław Rudź 1 z 10
 w polityce Radosław Rudź 1 z 10 Leki biopodobne - definicja Lek biopodobny (biofarmaceutyk na ladowczy) to lek zbli ony lecz nie identyczny w odniesieniu do leku biologicznego, który zosta dopuszczony
w polityce Radosław Rudź 1 z 10 Leki biopodobne - definicja Lek biopodobny (biofarmaceutyk na ladowczy) to lek zbli ony lecz nie identyczny w odniesieniu do leku biologicznego, który zosta dopuszczony
Produkty lecznicze pod szczególnym nadzorem - wybrane kwestie prawne
 Produkty lecznicze pod szczególnym nadzorem - wybrane kwestie prawne Ewa Rutkowska, Partner, Adwokat Agnieszka Zielińska Krywoniuk, Senior Associate, Adwokat "Pharmacovigilance w 2015 r. - nowa praktyka,
Produkty lecznicze pod szczególnym nadzorem - wybrane kwestie prawne Ewa Rutkowska, Partner, Adwokat Agnieszka Zielińska Krywoniuk, Senior Associate, Adwokat "Pharmacovigilance w 2015 r. - nowa praktyka,
Biologiczne leki biopodobne w pytaniach
 Biologiczne leki biopodobne w pytaniach Dlaczego pacjent powinien wiedzieć więcej? W związku z rozwojem współczesnej medycyny, my pacjenci jesteśmy informowani o jej osiągnięciach, które bezpośrednio mają
Biologiczne leki biopodobne w pytaniach Dlaczego pacjent powinien wiedzieć więcej? W związku z rozwojem współczesnej medycyny, my pacjenci jesteśmy informowani o jej osiągnięciach, które bezpośrednio mają
Leki biologiczne i czujność farmakologiczna - punkt widzenia klinicysty. Katarzyna Pogoda
 Leki biologiczne i czujność farmakologiczna - punkt widzenia klinicysty Katarzyna Pogoda Leki biologiczne Immunogenność Leki biologiczne mają potencjał immunogenny mogą być rozpoznane jako obce przez
Leki biologiczne i czujność farmakologiczna - punkt widzenia klinicysty Katarzyna Pogoda Leki biologiczne Immunogenność Leki biologiczne mają potencjał immunogenny mogą być rozpoznane jako obce przez
Faramkoekonomiczna ocena leków biopodobnych. dr Michał Seweryn
 Faramkoekonomiczna ocena leków biopodobnych dr Michał Seweryn Klasyczny problem ekonomii Potrzeby Dobra Farmakoekonomika (ekonomiczna ocena technologii medycznych) Celem badania farmakoekonomicznego jest
Faramkoekonomiczna ocena leków biopodobnych dr Michał Seweryn Klasyczny problem ekonomii Potrzeby Dobra Farmakoekonomika (ekonomiczna ocena technologii medycznych) Celem badania farmakoekonomicznego jest
Terminologia. Leki biopodobne. Leki chemiczne vs leki. Leki biotechnologiczne. Wytyczne EMA dotyczące oceny immunogenności leków biologicznych
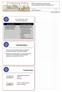 Anna Kordecka 1 z 7 Leki chemiczne vs leki biotechnologiczne Leki chemiczne Uzyskiwane drog syntezy chemicznej lub chemicznej modyfikacji substancji pochodzenia naturalnego Leki biotechnologiczne Wytwarzane
Anna Kordecka 1 z 7 Leki chemiczne vs leki biotechnologiczne Leki chemiczne Uzyskiwane drog syntezy chemicznej lub chemicznej modyfikacji substancji pochodzenia naturalnego Leki biotechnologiczne Wytwarzane
Mikroorganizmy Zmodyfikowane Genetycznie
 Mikroorganizmy Zmodyfikowane Genetycznie DEFINICJA Mikroorganizm (drobnoustrój) to organizm niewidoczny gołym okiem. Pojęcie to nie jest zbyt precyzyjne lecz z pewnością mikroorganizmami są: bakterie,
Mikroorganizmy Zmodyfikowane Genetycznie DEFINICJA Mikroorganizm (drobnoustrój) to organizm niewidoczny gołym okiem. Pojęcie to nie jest zbyt precyzyjne lecz z pewnością mikroorganizmami są: bakterie,
Rejestracja leków innowacyjnych - porównanie CP vs DCP Grzegorz Cessak
 Rejestracja leków innowacyjnych - porównanie CP vs DCP Grzegorz Cessak Prezes Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych 1 Procedura centralna Procedurę centralną
Rejestracja leków innowacyjnych - porównanie CP vs DCP Grzegorz Cessak Prezes Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych 1 Procedura centralna Procedurę centralną
Aneks IV. Wnioski naukowe i podstawy do zmiany warunków pozwoleń na dopuszczenie do obrotu
 Aneks IV Wnioski naukowe i podstawy do zmiany warunków pozwoleń na dopuszczenie do obrotu 137 Wnioski naukowe CHMP rozważył poniższe zalecenie PRAC z dnia 5 grudnia 2013 r. odnoszące się do procedury zgodnej
Aneks IV Wnioski naukowe i podstawy do zmiany warunków pozwoleń na dopuszczenie do obrotu 137 Wnioski naukowe CHMP rozważył poniższe zalecenie PRAC z dnia 5 grudnia 2013 r. odnoszące się do procedury zgodnej
Leczenie biologiczne
 Leczenie biologiczne ważne informacje Informator dla pacjenta Konsultacja merytoryczna: dr Michał Szymczyk, mec. Paulina Kieszkowska-Knapik Broszura wydana przez Instytut Praw Pacjenta i Edukacji Zdrowotnej
Leczenie biologiczne ważne informacje Informator dla pacjenta Konsultacja merytoryczna: dr Michał Szymczyk, mec. Paulina Kieszkowska-Knapik Broszura wydana przez Instytut Praw Pacjenta i Edukacji Zdrowotnej
BIOFARMACEUTYKI A LEKI BIOPODOBNE DOSTĘPNOŚĆ I KOSZTY LECZENIA W POLSCE
 Nowiny Lekarskie 2013, 82, 5, 355 362 PIOTR RATAJCZAK, ELŻBIETA NOWAKOWSKA, DOROTA KOLIGAT, KRZYSZTOF KUS, ANNA PACZKOWSKA, TOMASZ ZAPRUTKO BIOFARMACEUTYKI A LEKI BIOPODOBNE DOSTĘPNOŚĆ I KOSZTY LECZENIA
Nowiny Lekarskie 2013, 82, 5, 355 362 PIOTR RATAJCZAK, ELŻBIETA NOWAKOWSKA, DOROTA KOLIGAT, KRZYSZTOF KUS, ANNA PACZKOWSKA, TOMASZ ZAPRUTKO BIOFARMACEUTYKI A LEKI BIOPODOBNE DOSTĘPNOŚĆ I KOSZTY LECZENIA
Aneks III. Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Magdalena Szymaniak EMA, Biologics Working Party
 Magdalena Szymaniak EMA, Biologics Working Party Punkty prezentacji Biologiczne produkty lecznicze, w tym referencyjne i biopodobne Sposoby rejestracji leków biologicznych Wymagania rejestracyjne dla leków
Magdalena Szymaniak EMA, Biologics Working Party Punkty prezentacji Biologiczne produkty lecznicze, w tym referencyjne i biopodobne Sposoby rejestracji leków biologicznych Wymagania rejestracyjne dla leków
LECZENIE NIEDOKRWISTOŚCI W PRZEBIEGU PRZEWLEKŁEJ NIEWYDOLNOŚCI
 Nazwa programu: Terapeutyczne Programy Zdrowotne 2008 załącznik nr 18 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. LECZENIE NIEDOKRWISTOŚCI W PRZEBIEGU PRZEWLEKŁEJ NIEWYDOLNOŚCI
Nazwa programu: Terapeutyczne Programy Zdrowotne 2008 załącznik nr 18 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. LECZENIE NIEDOKRWISTOŚCI W PRZEBIEGU PRZEWLEKŁEJ NIEWYDOLNOŚCI
Najbardziej obiecujące terapie lekami biopodobnymi - Rak piersi
 Warszawa, 27.02.2018 MEDYCYNA XXI wieku III EDYCJA Leki biopodobne 2018 Najbardziej obiecujące terapie lekami biopodobnymi - Rak piersi Dr n. med. Agnieszka Jagiełło-Gruszfeld 1 Breast Cancer (C50.0-C50.9):
Warszawa, 27.02.2018 MEDYCYNA XXI wieku III EDYCJA Leki biopodobne 2018 Najbardziej obiecujące terapie lekami biopodobnymi - Rak piersi Dr n. med. Agnieszka Jagiełło-Gruszfeld 1 Breast Cancer (C50.0-C50.9):
Etyka finansowania leczenia chorób rzadkich onkologicznych
 Etyka finansowania leczenia chorób rzadkich onkologicznych Piotr Fiedor VI Letnia Akademia Onkologiczna dla Dziennikarzy Opracowano na podstawie źródeł udostępnionych w systemie informacji publicznej 11.08.2016
Etyka finansowania leczenia chorób rzadkich onkologicznych Piotr Fiedor VI Letnia Akademia Onkologiczna dla Dziennikarzy Opracowano na podstawie źródeł udostępnionych w systemie informacji publicznej 11.08.2016
Leki biologiczne i biopodobne. Iwona Korzeniewska-Rybicka Katedra i Zakład Farmakologii Doświadczalnej i Klinicznej WUM
 Leki biologiczne i biopodobne Iwona Korzeniewska-Rybicka Katedra i Zakład Farmakologii Doświadczalnej i Klinicznej WUM LEKI BIOLOGICZNE......to leki wytwarzane w procesach biologicznych, wykorzystujących
Leki biologiczne i biopodobne Iwona Korzeniewska-Rybicka Katedra i Zakład Farmakologii Doświadczalnej i Klinicznej WUM LEKI BIOLOGICZNE......to leki wytwarzane w procesach biologicznych, wykorzystujących
Biotechnologia farmaceutyczna
 Biotechnologia farmaceutyczna Charakterystyka specjalności Tematyka prac dyplomowych Obszary badawcze Potencjał zawodowy Charakterystyka specjalności Tematyka prac dyplomowych Obszary badawcze Potencjał
Biotechnologia farmaceutyczna Charakterystyka specjalności Tematyka prac dyplomowych Obszary badawcze Potencjał zawodowy Charakterystyka specjalności Tematyka prac dyplomowych Obszary badawcze Potencjał
sulfadiazyny i 66,7 mg/g trimetoprimu
 ANEKS I NAZWA, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTU LECZNICZEGO, GATUNKI ZWIERZĄT, DROGA PODANIA I PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU 1/7 Wnioskodawca lub podmiot odpowiedzialny
ANEKS I NAZWA, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTU LECZNICZEGO, GATUNKI ZWIERZĄT, DROGA PODANIA I PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU 1/7 Wnioskodawca lub podmiot odpowiedzialny
LEKI BIORÓWNOWAŻNE. Jaka jest ich przyszłość. w Polsce i na świecie POLSKI ZWIĄZEK PRACODAWCÓW PRZEMYSŁU FARMACEUTYCZNEGO
 LEKI BIORÓWNOWAŻNE Jaka jest ich przyszłość w Polsce i na świecie POLSKI ZWIĄZEK PRACODAWCÓW PRZEMYSŁU FARMACEUTYCZNEGO Czym jest lek biorównoważny? Lek biorównoważny to odpowiednik zarejestrowanego jako
LEKI BIORÓWNOWAŻNE Jaka jest ich przyszłość w Polsce i na świecie POLSKI ZWIĄZEK PRACODAWCÓW PRZEMYSŁU FARMACEUTYCZNEGO Czym jest lek biorównoważny? Lek biorównoważny to odpowiednik zarejestrowanego jako
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta
 Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta:informacja dla użytkownika Medivitan iv ampułko-strzykawka 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta:informacja dla użytkownika Medivitan iv ampułko-strzykawka 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny
SPIS TREŒCI. Przedmowa przewodnicz¹cego Rady Naukowej Czasopisma Aptekarskiego... 13. Rozdzia³ 1
 SPIS TREŒCI Przedmowa przewodnicz¹cego Rady Naukowej Czasopisma Aptekarskiego........................... 13 Rozdzia³ 1 NADCIŒNIENIE TÊTNICZE JAKO PROBLEM ZDROWOTNY prof. dr hab. n. farm. S³awomir Lipski,
SPIS TREŒCI Przedmowa przewodnicz¹cego Rady Naukowej Czasopisma Aptekarskiego........................... 13 Rozdzia³ 1 NADCIŒNIENIE TÊTNICZE JAKO PROBLEM ZDROWOTNY prof. dr hab. n. farm. S³awomir Lipski,
Badania obserwacyjne w ocenie bezpieczeństwa leków This gentle murmur it could be stings of remorse
 Badania obserwacyjne w ocenie bezpieczeństwa leków This gentle murmur it could be stings of remorse Magdalena Władysiuk 1. Pharmacovigilance: Co to jest pharmacovigilance? Podstawowe założenia systemu
Badania obserwacyjne w ocenie bezpieczeństwa leków This gentle murmur it could be stings of remorse Magdalena Władysiuk 1. Pharmacovigilance: Co to jest pharmacovigilance? Podstawowe założenia systemu
KOMPLEKSOWE PODEJŚCIE DO TERAPII
 KOMPLEKSOWE PODEJŚCIE DO TERAPII Ból PRZYWRACANIE ZDROWIA W SZCZEGÓLNY SPOSÓB 2 Krążenie Zapalenie Naprawa tkanek Większość z nas uważa zdrowie za pewnik. Zdarzają się jednak sytuacje, kiedy organizm traci
KOMPLEKSOWE PODEJŚCIE DO TERAPII Ból PRZYWRACANIE ZDROWIA W SZCZEGÓLNY SPOSÓB 2 Krążenie Zapalenie Naprawa tkanek Większość z nas uważa zdrowie za pewnik. Zdarzają się jednak sytuacje, kiedy organizm traci
BADANIA PASS ROLA CRO W PLANOWANIU I ZARZĄDZANIU
 BADANIA PASS ROLA CRO W PLANOWANIU I ZARZĄDZANIU Agnieszka Almgren- Rachtan MD PhD BADANIEM Post- authorisajon safety study Porejestracyjne badanie farmakoepidemiologiczne lub próba kliniczna przeprowadzona
BADANIA PASS ROLA CRO W PLANOWANIU I ZARZĄDZANIU Agnieszka Almgren- Rachtan MD PhD BADANIEM Post- authorisajon safety study Porejestracyjne badanie farmakoepidemiologiczne lub próba kliniczna przeprowadzona
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Leczenie biologiczne co prawnie wpływa na jego dostępność dla chorych w Polsce. Paulina Kieszkowska-Knapik, Partner, Adwokat Warszawa 29 maja 2015r.
 Leczenie biologiczne co prawnie wpływa na jego dostępność dla chorych w Polsce Paulina Kieszkowska-Knapik, Partner, Adwokat Warszawa 29 maja 2015r. Słownik pojęć - lek biologiczny Legislator europejski
Leczenie biologiczne co prawnie wpływa na jego dostępność dla chorych w Polsce Paulina Kieszkowska-Knapik, Partner, Adwokat Warszawa 29 maja 2015r. Słownik pojęć - lek biologiczny Legislator europejski
Biotechnologia jest dyscypliną nauk technicznych, która wykorzystuje procesy biologiczne na skalę przemysłową. Inaczej są to wszelkie działania na
 Biotechnologia jest dyscypliną nauk technicznych, która wykorzystuje procesy biologiczne na skalę przemysłową. Inaczej są to wszelkie działania na żywych organizmach prowadzące do uzyskania konkretnych
Biotechnologia jest dyscypliną nauk technicznych, która wykorzystuje procesy biologiczne na skalę przemysłową. Inaczej są to wszelkie działania na żywych organizmach prowadzące do uzyskania konkretnych
Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
Leczenie preparatami biopodobnymi regulacje prawne, szanse, ograniczenia
 Leczenie preparatami biopodobnymi regulacje prawne, szanse, ograniczenia Warszawa, 23 lutego 2018 r. adwokat Przemysław Wierzbicki wspólnik zarządzający Agenda Czyli co weźmiemy pod lupę? 1.Status leków
Leczenie preparatami biopodobnymi regulacje prawne, szanse, ograniczenia Warszawa, 23 lutego 2018 r. adwokat Przemysław Wierzbicki wspólnik zarządzający Agenda Czyli co weźmiemy pod lupę? 1.Status leków
CO WARTO WIEDZIEĆ LEKI BIOPODOBNE. Polskie Towarzystwo Onkologii Klinicznej oraz Fundacja Tam i z Powrotem
 Polskie Towarzystwo Onkologii Klinicznej oraz Fundacja Tam i z Powrotem CO WARTO WIEDZIEĆ LEKI BIOPODOBNE Patronat merytoryczny: Polskie Towarzystwo Onkologii Klinicznej WWW.PROGRAMEDUKACJIONKOLOGICZNEJ.PL
Polskie Towarzystwo Onkologii Klinicznej oraz Fundacja Tam i z Powrotem CO WARTO WIEDZIEĆ LEKI BIOPODOBNE Patronat merytoryczny: Polskie Towarzystwo Onkologii Klinicznej WWW.PROGRAMEDUKACJIONKOLOGICZNEJ.PL
Zdobycze biotechnologii w medycynie i ochronie środowiska
 Zdobycze biotechnologii w medycynie i ochronie środowiska InŜynieria genetyczna - badania biomedyczne Jednym z najbardziej obiecujących zastosowań nowych technologii opartych na przenoszeniu genów z jednego
Zdobycze biotechnologii w medycynie i ochronie środowiska InŜynieria genetyczna - badania biomedyczne Jednym z najbardziej obiecujących zastosowań nowych technologii opartych na przenoszeniu genów z jednego
Konieczność monitorowania działań niepożądanych leków elementem bezpiecznej farmakoterapii
 Konieczność monitorowania działań niepożądanych leków elementem bezpiecznej farmakoterapii dr hab. Anna Machoy-Mokrzyńska, prof. PUM Katedra Farmakologii Regionalny Ośrodek Monitorujący Działania Niepożądane
Konieczność monitorowania działań niepożądanych leków elementem bezpiecznej farmakoterapii dr hab. Anna Machoy-Mokrzyńska, prof. PUM Katedra Farmakologii Regionalny Ośrodek Monitorujący Działania Niepożądane
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 12 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4,
Załącznik nr 12 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4,
Mabion otrzymał wszystkie zgody na Litwie. Ruszają badania kliniczne MabionuCD20 w 2 krajach
 Informacja prasowa Warszawa, 23 stycznia 2013 Mabion otrzymał wszystkie zgody na Litwie Ruszają badania kliniczne MabionuCD20 w 2 krajach Mabion SA polska firma biotechnologiczna, rozwijająca i wprowadzająca
Informacja prasowa Warszawa, 23 stycznia 2013 Mabion otrzymał wszystkie zgody na Litwie Ruszają badania kliniczne MabionuCD20 w 2 krajach Mabion SA polska firma biotechnologiczna, rozwijająca i wprowadzająca
ASMAG FORTE 34 mg jonów magnezu, tabletki Magnesii hydroaspartas
 Ulotka dołączona do opakowania: informacja dla użytkownika ASMAG FORTE 34 mg jonów magnezu, tabletki Magnesii hydroaspartas Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika ASMAG FORTE 34 mg jonów magnezu, tabletki Magnesii hydroaspartas Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Farmakologia nauka o interakcjach pomiędzy substancjami chemicznymi a żywymi organizmami.
 Farmakologia nauka o interakcjach pomiędzy substancjami chemicznymi a żywymi organizmami. Każda substancja chemiczna oddziałująca na organizmy żywe może być zdefiniowana jako środek farmakologiczny (ang.
Farmakologia nauka o interakcjach pomiędzy substancjami chemicznymi a żywymi organizmami. Każda substancja chemiczna oddziałująca na organizmy żywe może być zdefiniowana jako środek farmakologiczny (ang.
Jak definiujemy leki generyczne?
 Jak definiujemy leki generyczne? Definicja leku generycznego wg Światowej Organizacji Zdrowia (WHO) Lek generyczny jest pełno wartościowym produktem farmaceutycznym stanowiącym odpowiednik (zamiennik)
Jak definiujemy leki generyczne? Definicja leku generycznego wg Światowej Organizacji Zdrowia (WHO) Lek generyczny jest pełno wartościowym produktem farmaceutycznym stanowiącym odpowiednik (zamiennik)
Specjalność (studia II stopnia) Oczyszczanie i analiza produktów biotechnologicznych
 Specjalność (studia II stopnia) Oczyszczanie i analiza produktów biotechnologicznych Studia magisterskie przedmioty specjalizacyjne Bioinformatyka w analizie genomu Diagnostyka molekularna Elementy biosyntezy
Specjalność (studia II stopnia) Oczyszczanie i analiza produktów biotechnologicznych Studia magisterskie przedmioty specjalizacyjne Bioinformatyka w analizie genomu Diagnostyka molekularna Elementy biosyntezy
Kolory biotechnologii
 Autor artykułu: Mariusz Kosakowski (http://www.e-biotechnologia.pl/artykuly/podzial_biotechnologia) Biotechnologia to świadczenie dóbr i usług z wykorzystaniem metod biologicznych. Tak brzmi oficjalna
Autor artykułu: Mariusz Kosakowski (http://www.e-biotechnologia.pl/artykuly/podzial_biotechnologia) Biotechnologia to świadczenie dóbr i usług z wykorzystaniem metod biologicznych. Tak brzmi oficjalna
Aneks II. Wnioski naukowe
 Aneks II Wnioski naukowe 8 Wnioski naukowe Solu-Medrol 40 mg, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań (zwany dalej Solu-Medrol ) zawiera metyloprednisolon i (jako substancję pomocniczą)
Aneks II Wnioski naukowe 8 Wnioski naukowe Solu-Medrol 40 mg, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań (zwany dalej Solu-Medrol ) zawiera metyloprednisolon i (jako substancję pomocniczą)
Leki biologiczne biopodobne w UE
 NAUKA LEKI ZDROWIE Komisja Europejska Leki biologiczne biopodobne w UE Przewodnik dla personelu medycznego Opracowany wspólnie przez Europejską Agencję Leków i Komisję Europejską Tłumaczenie i wydanie:
NAUKA LEKI ZDROWIE Komisja Europejska Leki biologiczne biopodobne w UE Przewodnik dla personelu medycznego Opracowany wspólnie przez Europejską Agencję Leków i Komisję Europejską Tłumaczenie i wydanie:
biopodobnych produktach leczniczych Co musisz wiedzieć o
 Komisja Europejska Co musisz wiedzieć o biopodobnych produktach leczniczych Proces pobudzania odpowiedzialności społecznej sektora farmaceutycznego Dostęp do leków w Europie Informacja na temat uzgodnionego
Komisja Europejska Co musisz wiedzieć o biopodobnych produktach leczniczych Proces pobudzania odpowiedzialności społecznej sektora farmaceutycznego Dostęp do leków w Europie Informacja na temat uzgodnionego
Dr nauk farm Leszek Borkowski Szpital Wolski Warszawa 2017 r
 Jak korzystać pacjencie ze swoich praw w leczeniu i na co zwracać uwagę przy podawaniu leku. Odpowiednie postępowanie całego personelu opieki zdrowotnej może w znacznym stopniu poprawić jakość życia zapewniając
Jak korzystać pacjencie ze swoich praw w leczeniu i na co zwracać uwagę przy podawaniu leku. Odpowiednie postępowanie całego personelu opieki zdrowotnej może w znacznym stopniu poprawić jakość życia zapewniając
Keytruda (pembrolizumab)
 EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
Rynek farmaceutyczny
 Rynek farmaceutyczny Czy Pharma jest tak ważna jak wydaje się jej pracownikom? Czas naszego życia się wydłuża Przez ostatnie 65 lat w Europie obserwowana jest istotna poprawa średniej długości życia Średnia
Rynek farmaceutyczny Czy Pharma jest tak ważna jak wydaje się jej pracownikom? Czas naszego życia się wydłuża Przez ostatnie 65 lat w Europie obserwowana jest istotna poprawa średniej długości życia Średnia
Leki biopodobne w UE. Poradnik dla pracowników służby zdrowia. Przygotowany wspólnie przez Europejską Agencję Leków i Komisję Europejską
 Leki biopodobne w UE Poradnik dla pracowników służby zdrowia Przygotowany wspólnie przez Europejską Agencję Leków i Komisję Europejską Spis treści Przedmowa 2 Streszczenie 3 Leki biologiczne: informacje
Leki biopodobne w UE Poradnik dla pracowników służby zdrowia Przygotowany wspólnie przez Europejską Agencję Leków i Komisję Europejską Spis treści Przedmowa 2 Streszczenie 3 Leki biologiczne: informacje
Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się
 (BIA) komu i po co Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się Not everything that can be counted counts, and not everything that counts can be counted A.
(BIA) komu i po co Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się Not everything that can be counted counts, and not everything that counts can be counted A.
Europejskie stanowisko dotyczące farmacji szpitalnej Bruksela, maj 2014 r.
 Europejskie stanowisko dotyczące farmacji szpitalnej Bruksela, maj 2014 r. Poniżej publikujemy dla Państwa stanowisko wypracowane przez Europejskie Stowarzyszenie Farmaceutów Szpitalnych wspólnie z organizacjami
Europejskie stanowisko dotyczące farmacji szpitalnej Bruksela, maj 2014 r. Poniżej publikujemy dla Państwa stanowisko wypracowane przez Europejskie Stowarzyszenie Farmaceutów Szpitalnych wspólnie z organizacjami
Wsparcie merytoryczne i logistyczne niekomercyjnych badań klinicznych
 Wsparcie merytoryczne i logistyczne niekomercyjnych badań klinicznych Badanie kliniczne definicje badaniem klinicznym jest każde badanie prowadzone z udziałem ludzi w celu odkrycia lub potwierdzenia klinicznych,
Wsparcie merytoryczne i logistyczne niekomercyjnych badań klinicznych Badanie kliniczne definicje badaniem klinicznym jest każde badanie prowadzone z udziałem ludzi w celu odkrycia lub potwierdzenia klinicznych,
Opis struktury zagadnień rozważanych w obszarach badawczych projektu Quality of Life w czasie spotkania #1 Perspektywa Dynamiki Systemów
 Opis struktury zagadnień rozważanych w obszarach badawczych projektu Quality of Life w czasie spotkania #1 Perspektywa Dynamiki Systemów Elementy określone przez liderów sekcji w obszarze Biotechnologia
Opis struktury zagadnień rozważanych w obszarach badawczych projektu Quality of Life w czasie spotkania #1 Perspektywa Dynamiki Systemów Elementy określone przez liderów sekcji w obszarze Biotechnologia
Dopuszczanie do obrotu produktów leczniczych
 Dopuszczanie do obrotu produktów leczniczych Podstawy prawne Zgodnie z obowiązującym prawem, poza ściśle określonymi wyjątkami, w obrocie mogą znajdować się wyłącznie produkty lecznicze (leki), które uzyskały
Dopuszczanie do obrotu produktów leczniczych Podstawy prawne Zgodnie z obowiązującym prawem, poza ściśle określonymi wyjątkami, w obrocie mogą znajdować się wyłącznie produkty lecznicze (leki), które uzyskały
Ulotka dla pacjenta: Informacja dla użytkownika Neuro-Medivitan tabletki powlekane
 Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Neuro-Medivitan tabletki powlekane Substancje czynne: tiaminy chlorku chlorowodorek / pirydoksyny
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Neuro-Medivitan tabletki powlekane Substancje czynne: tiaminy chlorku chlorowodorek / pirydoksyny
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks III Zmiany Charakterystyki Produktu Leczniczego i ulotki dołączonej do opakowania
 Aneks III Zmiany Charakterystyki Produktu Leczniczego i ulotki dołączonej do opakowania Uwaga: Poniższe zmiany należy dodać do ważnej Charakterystyki Produktu Leczniczego, oznakowania i ulotki dla pacjenta,
Aneks III Zmiany Charakterystyki Produktu Leczniczego i ulotki dołączonej do opakowania Uwaga: Poniższe zmiany należy dodać do ważnej Charakterystyki Produktu Leczniczego, oznakowania i ulotki dla pacjenta,
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
Minister van Sociale Zaken en Volksgezondheid
 http://www.maggiedeblock.be/2005/11/18/resolutie-inzake-de-klinischebiologie/ Minister van Sociale Zaken en Volksgezondheid Obecna Minister Zdrowia Maggy de Block wraz z Yolande Avontroodt, i Hilde Dierickx
http://www.maggiedeblock.be/2005/11/18/resolutie-inzake-de-klinischebiologie/ Minister van Sociale Zaken en Volksgezondheid Obecna Minister Zdrowia Maggy de Block wraz z Yolande Avontroodt, i Hilde Dierickx
Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa.
 Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa. Niniejszy dokument stanowi streszczenie Europejskiego Publicznego Sprawozdania Oceniajc ego (EPAR). Wyja nia, jak Komitet ds. Produktów Leczniczych
Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa. Niniejszy dokument stanowi streszczenie Europejskiego Publicznego Sprawozdania Oceniajc ego (EPAR). Wyja nia, jak Komitet ds. Produktów Leczniczych
Rola przeciwciał neutralizujących w terapiach SM (ciągle dyskutowana) Konrad Rejdak
 Rola przeciwciał neutralizujących w terapiach SM (ciągle dyskutowana) Konrad Rejdak Katedra i Klinika Neurologii Uniwersytet Medyczny w Lublinie Immunogeniczność preparatów biologicznych Rossman, 2004
Rola przeciwciał neutralizujących w terapiach SM (ciągle dyskutowana) Konrad Rejdak Katedra i Klinika Neurologii Uniwersytet Medyczny w Lublinie Immunogeniczność preparatów biologicznych Rossman, 2004
Międzynarodowa nazwa. niezastrzeżona (INN) Ferri hydroxidum dextranum
 Aneks I 1 Państwo członkowskie Podmiot odpowiedzialny posiadający pozwolenie Kontakt z lokalnym Międzynarodowa nazwa Nazwa własna Moc Postać farmaceutyczna Droga podania (w EOG) na dopuszczenie do obrotu
Aneks I 1 Państwo członkowskie Podmiot odpowiedzialny posiadający pozwolenie Kontakt z lokalnym Międzynarodowa nazwa Nazwa własna Moc Postać farmaceutyczna Droga podania (w EOG) na dopuszczenie do obrotu
Moc Gatunki zwierząt. Postać farmaceutyczna. Samice psów. Enurace 50 Tabletki 50 mg
 ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTU LECZNICZEGO, GATUNKI ZWIERZĄT, DROGA PODANIA I PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH
ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTU LECZNICZEGO, GATUNKI ZWIERZĄT, DROGA PODANIA I PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta
 Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Medivitan iv ampułki 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny chlorowodorek
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Medivitan iv ampułki 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny chlorowodorek
Katedra i Zakład Technologii Postaci Leku Wydziału Farmaceutycznego z O. Analityki Medycznej
 Katedra i Zakład Technologii Postaci Leku Wydziału Farmaceutycznego z O. Analityki Medycznej Szanowni Państwo, Jestem studentką V roku farmacji Uniwersytetu Medycznego im. Piastów Śląskich we Wrocławiu.
Katedra i Zakład Technologii Postaci Leku Wydziału Farmaceutycznego z O. Analityki Medycznej Szanowni Państwo, Jestem studentką V roku farmacji Uniwersytetu Medycznego im. Piastów Śląskich we Wrocławiu.
PROPOZYCJE ZMIAN W PROGRAMIE II LINII. Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK
 PROPOZYCJE ZMIAN W PROGRAMIE II LINII Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK PROGRAM II LINII P R O B L E M Y Z G Ł A S Z A N E W 2 0 1 7 r o k u Brak możliwości
PROPOZYCJE ZMIAN W PROGRAMIE II LINII Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK PROGRAM II LINII P R O B L E M Y Z G Ł A S Z A N E W 2 0 1 7 r o k u Brak możliwości
Aspekty prawne Farmacji Szpitalnej. mgr Ewa Steckiewicz- Bartnicka wojewódzki konsultant w dziedzinie Farmacji Szpitalnej
 Aspekty prawne Farmacji Szpitalnej mgr Ewa Steckiewicz- Bartnicka wojewódzki konsultant w dziedzinie Farmacji Szpitalnej Podstawy prawne Ustawa z dnia 6 września 2001r. - Prawo farmaceutyczne ( Dz.U.2016.2142
Aspekty prawne Farmacji Szpitalnej mgr Ewa Steckiewicz- Bartnicka wojewódzki konsultant w dziedzinie Farmacji Szpitalnej Podstawy prawne Ustawa z dnia 6 września 2001r. - Prawo farmaceutyczne ( Dz.U.2016.2142
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
IO3 - The Total Business Plants materiały szkoleniowe
 Numer projektu: 2016-1-EL01-KA202-023491 IO3 - The Total Business Plants materiały szkoleniowe Moduł nr.3 Zapewnienie jakości produktu końcowego (rośliny lecznicze) 2 Zapewnienie jakości produktu końcowego
Numer projektu: 2016-1-EL01-KA202-023491 IO3 - The Total Business Plants materiały szkoleniowe Moduł nr.3 Zapewnienie jakości produktu końcowego (rośliny lecznicze) 2 Zapewnienie jakości produktu końcowego
czerniak (nowotwór skóry), który rozprzestrzenił się lub którego nie można usunąć chirurgicznie;
 EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Celem Tygodnia Szczepień w Polsce jest podkreślanie roli szczepień powszechnych i indywidualnych poprzez:
 W dniach 22-26 kwietnia obchodzimy, już po raz IX, Europejski Tydzień Szczepień. Jest to inicjatywa Światowej Organizacji Zdrowia (WHO), realizowana i koordynowana na poziomie lokalnym przez poszczególne
W dniach 22-26 kwietnia obchodzimy, już po raz IX, Europejski Tydzień Szczepień. Jest to inicjatywa Światowej Organizacji Zdrowia (WHO), realizowana i koordynowana na poziomie lokalnym przez poszczególne
PRZEWODNIK DYDAKTYCZNY I PROGRAM NAUCZANIA PRZEDMIOTU FAKULTATYWNEGO NA KIERUNKU LEKARSKIM ROK AKADEMICKI 2016/2017
 PRZEWODNIK DYDAKTYCZNY I PROGRAM NAUCZANIA PRZEDMIOTU FAKULTATYWNEGO NA KIERUNKU LEKARSKIM ROK AKADEMICKI 2016/2017 1. NAZWA PRZEDMIOTU : Krwiolecznictwo-aspekty praktyczne 2. NAZWA JEDNOSTKI (jednostek
PRZEWODNIK DYDAKTYCZNY I PROGRAM NAUCZANIA PRZEDMIOTU FAKULTATYWNEGO NA KIERUNKU LEKARSKIM ROK AKADEMICKI 2016/2017 1. NAZWA PRZEDMIOTU : Krwiolecznictwo-aspekty praktyczne 2. NAZWA JEDNOSTKI (jednostek
Leki biologiczne to wizytówka współczesnej medycyny. Czy można bez przeszkód stosować ich tańsze zamienniki, dość niefortunnie nazwane biopodobnymi?
 Leki biologiczne to wizytówka współczesnej medycyny. Czy można bez przeszkód stosować ich tańsze zamienniki, dość niefortunnie nazwane biopodobnymi? Wydawało się, że długi spór na temat różnic między lekami
Leki biologiczne to wizytówka współczesnej medycyny. Czy można bez przeszkód stosować ich tańsze zamienniki, dość niefortunnie nazwane biopodobnymi? Wydawało się, że długi spór na temat różnic między lekami
Produkty złożone (combo) stosowane w nadciśnieniu tętniczym a system refundacji leków ocena potencjału oszczędności
 Produkty złożone (combo) stosowane w nadciśnieniu tętniczym a system refundacji leków ocena potencjału oszczędności MIEJ SERCE I PATRZAJ W SERCE... I TĘTNICE HEALTH PROJECT MANAGEMENT 23 maja 2016 r. Nieprzestrzeganie
Produkty złożone (combo) stosowane w nadciśnieniu tętniczym a system refundacji leków ocena potencjału oszczędności MIEJ SERCE I PATRZAJ W SERCE... I TĘTNICE HEALTH PROJECT MANAGEMENT 23 maja 2016 r. Nieprzestrzeganie
ZAKAŻENIA SZPITALNE. Michał Pytkowski Zdrowie Publiczne III rok
 ZAKAŻENIA SZPITALNE Michał Pytkowski Zdrowie Publiczne III rok REGULACJE PRAWNE WHO Ustawa z dnia 5 grudnia 2008 r. o zapobieganiu oraz zwalczaniu zakażeń i chorób zakaźnych u ludzi Rozporządzenie Ministra
ZAKAŻENIA SZPITALNE Michał Pytkowski Zdrowie Publiczne III rok REGULACJE PRAWNE WHO Ustawa z dnia 5 grudnia 2008 r. o zapobieganiu oraz zwalczaniu zakażeń i chorób zakaźnych u ludzi Rozporządzenie Ministra
Lipophoral Tablets 150mg. Mediator 150 mg Tabletka Podanie doustne. Benfluorex Qualimed. Mediator 150mg Tabletka Podanie doustne
 ANEKS I WYKAZ NAZW WŁASNYCH, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTÓW LECZNICZYCH, DROGA PODANIA, PODMIOTY ODPOWIEDZIALNE POSIADAJĄCE POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH (EOG) 1
ANEKS I WYKAZ NAZW WŁASNYCH, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTÓW LECZNICZYCH, DROGA PODANIA, PODMIOTY ODPOWIEDZIALNE POSIADAJĄCE POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH (EOG) 1
WYNALAZKI BIOTECHNOLOGICZNE W POLSCE. Ewa Waszkowska ekspert UPRP
 WYNALAZKI BIOTECHNOLOGICZNE W POLSCE Ewa Waszkowska ekspert UPRP Źródła informacji w biotechnologii projekt SLING Warszawa, 9-10.12.2010 PLAN WYSTĄPIENIA Umocowania prawne Wynalazki biotechnologiczne Statystyka
WYNALAZKI BIOTECHNOLOGICZNE W POLSCE Ewa Waszkowska ekspert UPRP Źródła informacji w biotechnologii projekt SLING Warszawa, 9-10.12.2010 PLAN WYSTĄPIENIA Umocowania prawne Wynalazki biotechnologiczne Statystyka
Nowy model oceny etycznej badań klinicznych w Polsce
 Nowy model oceny etycznej badań klinicznych w Polsce Dr hab. n. med. M. Czarkowski Warszawski Uniwersytet Medyczny Ośrodek Bioetyki NRL Badanie nieinterwencyjne Polskie przepisy: art. 37al PF Badania nieinterwencyjne
Nowy model oceny etycznej badań klinicznych w Polsce Dr hab. n. med. M. Czarkowski Warszawski Uniwersytet Medyczny Ośrodek Bioetyki NRL Badanie nieinterwencyjne Polskie przepisy: art. 37al PF Badania nieinterwencyjne
Prawa pacjenta przy stosowaniu leków biologicznych. Paulina Kieszkowska-Knapik, Partner, Adwokat Warszawa, 11 lutego 2017 r.
 Prawa pacjenta przy stosowaniu leków biologicznych Paulina Kieszkowska-Knapik, Partner, Adwokat Warszawa, 11 lutego 2017 r. Punkt wyjścia - prawa pacjenta? Ustawa z dnia 6 listopada 2008 r. o prawach pacjenta
Prawa pacjenta przy stosowaniu leków biologicznych Paulina Kieszkowska-Knapik, Partner, Adwokat Warszawa, 11 lutego 2017 r. Punkt wyjścia - prawa pacjenta? Ustawa z dnia 6 listopada 2008 r. o prawach pacjenta
Centralne zakupy produktów leczniczych na przykładzie leków przeciw AIDS
 Centralne zakupy produktów leczniczych na przykładzie leków przeciw AIDS Adwokat Katarzyna Bondaryk Członek Zarządu Fundacji WHC 10 lutego 2012 r., Warszawa Zakup centralny = większy dostęp do leczenia
Centralne zakupy produktów leczniczych na przykładzie leków przeciw AIDS Adwokat Katarzyna Bondaryk Członek Zarządu Fundacji WHC 10 lutego 2012 r., Warszawa Zakup centralny = większy dostęp do leczenia
Szanse i zagrożenia na poprawę leczenia chorób zapalnych stawów w Polsce rok 2014 Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób
 Szanse i zagrożenia na poprawę leczenia chorób zapalnych stawów w Polsce rok 2014 Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób Wewnętrznych, Uniwersytet Medyczny im. Piastów Śląskich
Szanse i zagrożenia na poprawę leczenia chorób zapalnych stawów w Polsce rok 2014 Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób Wewnętrznych, Uniwersytet Medyczny im. Piastów Śląskich
HEMLIBRA w Narodowym Programie Leczenia Hemofilii i Pokrewnych Skaz Krwotocznych na lata
 HEMLIBRA w Narodowym Programie Leczenia Hemofilii i Pokrewnych Skaz Krwotocznych na lata 2019-2023 Krystyna Zawilska Uniwersytet Medyczny im. Karola Marcinkowskiego; Centrum Diagnostyczno-Lecznicze INTERLAB
HEMLIBRA w Narodowym Programie Leczenia Hemofilii i Pokrewnych Skaz Krwotocznych na lata 2019-2023 Krystyna Zawilska Uniwersytet Medyczny im. Karola Marcinkowskiego; Centrum Diagnostyczno-Lecznicze INTERLAB
Aneks III. Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Terapeutyczne Programy Zdrowotne 2008 Leczenie stwardnienia rozsianego
 załącznik nr 16 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia I.
załącznik nr 16 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia I.
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
Spis treści. 1. Przyczyny nadciśnienia tętniczego Bogdan Wyrzykowski... 13
 Spis treści 1. Przyczyny nadciśnienia tętniczego Bogdan Wyrzykowski........ 13 Genetyczne uwarunkowania pierwotnego nadciśnienia tętniczego..... 14 Nadciśnienie monogeniczne..................................
Spis treści 1. Przyczyny nadciśnienia tętniczego Bogdan Wyrzykowski........ 13 Genetyczne uwarunkowania pierwotnego nadciśnienia tętniczego..... 14 Nadciśnienie monogeniczne..................................
INNOWACJE W LECZENIU RAKA NERKI- OCENA DOSTĘPNOŚCI W POLSCE. Prof. Cezary Szczylik Lek. Przemysław Langiewicz CSK WIM
 INNOWACJE W LECZENIU RAKA NERKI- OCENA DOSTĘPNOŚCI W POLSCE Prof. Cezary Szczylik Lek. Przemysław Langiewicz CSK WIM I/II linia leczenia rozsianego raka nerki Pazopanib - Produkt Votrient jest wskazany
INNOWACJE W LECZENIU RAKA NERKI- OCENA DOSTĘPNOŚCI W POLSCE Prof. Cezary Szczylik Lek. Przemysław Langiewicz CSK WIM I/II linia leczenia rozsianego raka nerki Pazopanib - Produkt Votrient jest wskazany
BIOTECHNOLOGIA STUDIA I STOPNIA
 BIOTECHNOLOGIA STUDIA I STOPNIA OPIS ZAKŁADANYCH EFEKTÓW KSZTAŁCENIA 1) Tabela odniesień kierunkowych efektów kształcenia (EKK) do obszarowych efektów kształcenia (EKO) SYMBOL EKK KIERUNKOWE EFEKTY KSZTAŁCENIA
BIOTECHNOLOGIA STUDIA I STOPNIA OPIS ZAKŁADANYCH EFEKTÓW KSZTAŁCENIA 1) Tabela odniesień kierunkowych efektów kształcenia (EKK) do obszarowych efektów kształcenia (EKO) SYMBOL EKK KIERUNKOWE EFEKTY KSZTAŁCENIA
POSTANOWIENIE. z dnia 19 maja 2014 r. Przewodniczący:
 Sygn. akt: KIO 901/14 POSTANOWIENIE z dnia 19 maja 2014 r. Krajowa Izba Odwoławcza - w składzie: Przewodniczący: Protokolant: Agnieszka Trojanowska Rafał Komoń po rozpoznaniu na posiedzeniu niejawnym z
Sygn. akt: KIO 901/14 POSTANOWIENIE z dnia 19 maja 2014 r. Krajowa Izba Odwoławcza - w składzie: Przewodniczący: Protokolant: Agnieszka Trojanowska Rafał Komoń po rozpoznaniu na posiedzeniu niejawnym z
biopodobne przez żywe komórki. Pojęcie to obejmuje szerokie spektrum substancji,
 Polski Związek Pracodawców Przemysłu Farmaceutycznego październik 201450 Leki biologiczne biopodobne Leki biologiczne otworzyły nowe perspektywy przed medycyną. Wprowadzenie możliwości rejestracji poprzez
Polski Związek Pracodawców Przemysłu Farmaceutycznego październik 201450 Leki biologiczne biopodobne Leki biologiczne otworzyły nowe perspektywy przed medycyną. Wprowadzenie możliwości rejestracji poprzez
Ogólnopolska Konferencja Naukowa Farmaceuta na oddziale szpitalnym korzyści i wyzwania. Wrocław, 22 kwietnia 2017.
 Ogólnopolska Konferencja Naukowa Farmaceuta na oddziale szpitalnym korzyści i wyzwania Wrocław, 22 kwietnia 2017 Oferta Sponsorska Szanowni Państwo! Organizowana przez nas konferencja stawia czoła zwiększającym
Ogólnopolska Konferencja Naukowa Farmaceuta na oddziale szpitalnym korzyści i wyzwania Wrocław, 22 kwietnia 2017 Oferta Sponsorska Szanowni Państwo! Organizowana przez nas konferencja stawia czoła zwiększającym
FORUM FARMACJI PRZEMYSŁOWEJ doświadczenia i plany w obszarze rejestracji. Łódź, października 2019 r.
 FORUM FARMACJI PRZEMYSŁOWEJ 2019- doświadczenia i plany w obszarze rejestracji Łódź, 16-18 października 2019 r. 16.10.2018 r. (środa) 15.00 15.15 Powitanie gości: przedstawiciel PTFarm 15.15 15.45 Wykład
FORUM FARMACJI PRZEMYSŁOWEJ 2019- doświadczenia i plany w obszarze rejestracji Łódź, 16-18 października 2019 r. 16.10.2018 r. (środa) 15.00 15.15 Powitanie gości: przedstawiciel PTFarm 15.15 15.45 Wykład
Podmiot odpowiedzialny Nazwa Moc Postać farmaceutyczna. Leflunomide Actavis 10 mg, filmomhulde tabletten
 Aneks I Wykaz nazw, postaci farmaceutycznych, mocy produktów leczniczych, droga podania, podmiot odpowiedzialny posiadający pozwolenie na dopuszczenie do obrotu w państwach członkowskich 1 Państwo Członkowskie
Aneks I Wykaz nazw, postaci farmaceutycznych, mocy produktów leczniczych, droga podania, podmiot odpowiedzialny posiadający pozwolenie na dopuszczenie do obrotu w państwach członkowskich 1 Państwo Członkowskie
