Praktyczne konsekwencje wprowadzenia badań DNA HBV u dawców krwi
|
|
|
- Bronisława Lewicka
- 8 lat temu
- Przeglądów:
Transkrypt
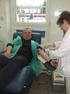
1 PRACA POGLĄDOWA Review Article Acta Haematologica Polonica 2009, 40, Nr 1, str PIOTR GRABARCZYK, GRZEGORZ LISZEWSKI, MARIA MIKULSKA, ANETA KOPACZ, MAGDALENA ŁĘTOWSKA, EWA BROJER, GRUPA BADAWCZA ds. WIRUSÓW REGIONALNYCH CENTRÓW KRWIODAW- STWA I KRWIOLECZNICTWA Praktyczne konsekwencje wprowadzenia badań DNA HBV u dawców krwi Practical consequences of HBV DNA screening implementation in blood donors Z Zakładu Immunologii Hematologicznej i Transfuzjologicznej Kierownik: Prof. dr hab. Ewa Brojer Z Zakładu Diagnostyki Hematologicznej i Transfuzjologicznej, Instytut Hematologii i Transfuzjologii Kierownik: Doc. dr hab. Magdalena Łętowska STRESZCZENIE W pracy omówiono metodyką i wyniki badań przeglądowych DNA HBV, które w roku 2005 wprowadzono jako obowiązkowe u polskich dawców krwi obok dotychczas wykonywanych badań anty-hcv, anty-hiv, HBsAg i RNA HCV. Podsumowano teŝ wyniki analiz serologicznych (anty-hbc,anty-hbs, anty-hbe) i molekularnych (poziomu wiremii i analizy sekwencji genu kodujacego białko HBs u dawców z DNA HBV, a bez HBsAg. SŁOWA KLUCZOWE: Dawcy krwi DNA HBV HBsAg Ukryte zakaŝenia HBV SUMMARY In present paper we review methodology and results of obligatory HBV DNA screening launched in 2005 in Polish blood donors. We present the results of serological (anti-hbc, anti- HBs, HBsAg and anti-hbe) and molecular (viraemia level and sequence analysis of the gene encoding HBs antigen) study of HBV DNA positive donors without HBsAg. KEY WORDS: Blood donors DNA HBV HBsAg Occult HBV WSTĘP Stan obecny wirusologicznych badań przeglądowych dawców krwi technikami biologii molekularnej na świecie Od 2000 roku dawcy krwi w krajach rozwiniętych, w tym w Polsce, badani są w kierunku markerów wirusowych nie tylko technikami serologicznymi (anty-hcv, anty-hiv i HBsAg), lecz takŝe technikami opartymi na namnaŝaniu kwasów nukleinowych wirusów techniką PCR (polymerase chain reaction reakcja łańcuchowa
2 46 P. GRABARCZYK i wsp. polimerazy) lub TMA (transcription mediated amplification namnaŝanie przez transkrypcję). Badania molekularne pozwalają na identyfikację dawców z aktywnym zaka- Ŝeniem w okresie okienka serologicznego i mają wyŝszą czułość niŝ badania serologiczne. Stosuje się róŝne algorytmy badań. Najczęściej bada się techniką PCR tzw. pule osocza zlane próbki od wielu (6 96) dawców. Alternatywną metodą TMA badane są na ogół pojedyncze próbki. Obligatoryjnie bada się dawców w kierunku RNA HCV; w niektórych krajach równolegle wykonuje się badania RNA HIV, a w nielicznych DNA HBV [1, 2, 3, 4]. Badania DNA HBV wykonywane są rutynowo od kilku lat tylko w nielicznych krajach np. w Niemczech i w Japonii [5, 6]. W obu tych krajach wykonuje się badania w pulach osocza złoŝonych z próbek 96 dawców. W roku 2005 w Polsce rozpoczęto badania DNA HBV. Przedmiotem obecnej pracy jest przedstawienie przyczyn i celów, dla których te badania wprowadzono oraz prezentacja ich wstępnych wyników. PRZYCZYNY WPROWADZENIA BADAŃ DNA HBV Ocenia się, Ŝe na świecie Ŝyje około 300 mln osób zakaŝonych HBV. Polska nale- Ŝy do krajów o wysokim stopniu zapadalności na wirusowe zapalenie wątroby typu B (wzw typu B) [7]. Do roku 2005 badania przeglądowe dawców krwi w naszym kraju były oparte, podobnie jak w innych krajach Europy na badaniu HBsAg metodą immunoenzymatyczną. Częstość wykrywania antygenu HBs u dawców pierwszorazowych w ostatnich latach wynosiła około od 0,04% do 1,4% w zaleŝności od regionu (8). Wśród dawców regularnie oddających krew była około 10 krotnie niŝsza. Zgodnie z analizami prowadzonymi w innych krajach [9] ryzyko przeniesienia zakaŝenia HBV przez krew badaną jedynie metodami serologicznymi wynosi około 1: (Tabela 1). Tabela 1. Ryzyko przeniesienia zakaŝenia przez przetoczenie w zaleŝności od metod badań przeglądowych dawców (wg Stramer, 2004)* [4] Table 1. Estimated risk of transfusion transmitted infection for different blood donors screening methods (according S.Stramer, 2004) [4] Wirus Badania serologiczne Badania molekularne w mini pulach w poj. donacjach HIV 0,75 (1: ) 0,52 (1: ) 0,33 (1: ) HCV 4,3 (1: ) 0,61 (1: ) 0,43 (1: ) HBV 5,5 (1: ) 4,8 (1: ) 2,4 (1: ) *dane dotyczą Stanów Zjednoczonych, gdzie częstość markerów zakaŝenia wirusem HBV i HCV jest niŝsza niŝ w Polsce. RYZYKO ZAKAśENIA HBV PRZEZ KREW BADANĄ SEROLOGICZNIE I METODY JEGO OGRANICZANIA Największe ryzyko przeniesienia zakaŝenia HBV przez krew badaną testami serologicznymi wiąŝe się z przetoczeniem krwi pobranej u dawcy we wczesnym okresie zakaŝenia, przed pojawieniem się HBsAg [10, 11]. W przeciwieństwie do zakaŝenia
3 Praktyczne konsekwencje wprowadzenia badań DNA HBV 47 HCV poziom wiremii HBV w okresie okienka serologicznego jest niski i wynosi od kilku kopii do kilku tysięcy kopii DNA w ml osocza. Wirus namnaŝa się powoli liczba wirionów podwaja się co 2 6 dni [5, 12]. W następnym okresie, w ostrej fazie zakaŝenia, gdy we krwi wykrywany jest antygen HBs DNA-emia wynosi od kopii/ ml. Antygen HBs wykrywa się w surowicy jako pierwszy serologiczny marker zakaŝenia po około 30 do 60 dniach po ekspozycji. Moment wykrycia zakaŝenia zaleŝy od czułości stosowanych testów. Testy serologiczne oparte na technikach enzymatycznych, które w Polsce były uzywane do roku 2006 mają czułość 0,13 0,62 ng HBsAg/ml, co odpowiada około IU DNA HBV/ml (1 IU= około 4 kopii). Testy nowej generacji oparte na chemiluminometrii mają czułość 0,07 0,12 ng/ml ( IU DNA HBV/ml) [11]. Czułość analityczna testów opartych na technikach biologii molekularnej jest wyŝsza i dla testu TMA (Chiron Corp) wynosi około 6 16 IU DNA HBV/ml [13, 14], a dla testu Ampliscreen HBV (Roche Diag) około 5 IU/ml [15]. UŜycie tych metod do badań przeglądowych pozwala na skrócenie okienka serologicznego przy badaniach pulowanego osocza o 9 11 dni, a pojedynczych donacji o dni. Drugą przyczyną przeniesienia zakaŝenia HBV przez krew dawcy badanego w kierunku HBsAg moŝe być tzw. ukryte zakaŝenie HBV manifestujące się obecnością DNA HBV przy niewykrywaniu antygenu HBs [10]. Taki stan moŝe mieć charakter przewlekły u tzw. zdrowych nosicieli HBV lub moŝe wystąpić w końcowych etapach zakaŝenia, które ulega ograniczeniu (tzw. drugie okienko serologiczne przed wytworzeniem anty-hbs, lub w okresie późniejszym, gdy poziom anty-hbs spada). W tych dwóch grupach osób poziom DNA HBV w osoczu jest na ogół bardzo niski waha się od kilku do kilkudziesięciu kopii w mililitrze. Nie wykrycie HBsAg w trakcie toczącej się infekcji ma często związek z zakaŝeniem mutantem HBV. Mutanty mogą mieć zmienioną strukturę antygenu powierzchniowego tak, Ŝe nie istnieją w nim epitopy rozpoznawane przez testy serologiczne uŝywane do wykrywania HBsAg. Poziom wiremii u osób zakaŝonych takim mutantem moŝe być, choć nie musi, stosunkowo wysoki. Nie wykrywanie antygenu wynika bowiem z jego własności antygenowych, a nie ze zbyt małej czułości testu serologicznego. W genomie zmutowanych szczepów obecne są inne niŝ w szczepie dzikim podstawienia amninokwasów w regionie a, szczególnie w pętli 4 w pozycji 145. Mutacje mogą zachodzić teŝ w promotorze białek rdzenia lub w regionie pre-core. Niektóre mutanty wirusa cechują się zmniejszoną zdolnością replikacji wirusa [16, 17]. U osób z ukrytym zakaŝeniem HBV wykrywa się na ogół przeciwciała anty-hbc. Obecne u nich mogą teŝ być inne serologiczne markery zakaŝenia (anty-hbe, czy niskie stęŝenie anty-hbs). Nie jest znana częstość wykrywania ukrytego zakaŝenia HBV szczególnie wśród osób bez objawów klinicznych. W regionach o endemicznym występowaniu zakaŝenia HBV, ukryte zakaŝenie wykrywano u 1 24% osób z anty- HBc [10, 18]. W badania przeprowadzonych w Regionalnym Centrum Krwiodawstwa i Krwiolecznictwa w Krakowie anty-hbc wykryto u 60/1012 dawców krwi (6%). U Ŝadnego z nich nie wykryto DNA HBV przy pomocy testu TMA o czułości 5 IU/ml (J. Kuśmierczyk informacja ustna).
4 48 P. GRABARCZYK i wsp. WaŜnym zagadnieniem z punktu widzenia bezpieczeństwa biorców krwi jest zakaźność preparatów krwi od osób z ukrytym zakaŝeniem HBV. ZaleŜy ona od dawki wirusa oraz od stanu immunologicznego biorcy, a w przypadku HBV takŝe od stęŝenia przeciwciał anty-hbs, które mają własności neutralizujące. Wysokie stęŝenie tych przeciwciał chroni przed przeniesieniem zakaŝenia, a przy niskim poziomie anty-hbs (<0.1IU/ml) około 10% donacji moŝe przenieść zakaŝenie [19]. UwaŜa się, Ŝe krew dawców z przeciwciałami anty-hbc, u których nie wykrywa się HBV DNA nie moŝe być źródłem zakaŝenia. Krew opisanego ostatnio dawcy, u którego wykryto DNA HBV dopiero przy pomocy ultra czułej metody (stęŝenie 3,8 IU/ml) nie przeniosła zakaŝenia. W archiwalnych próbkach osocza tego dawcy wykryto DNA HBV w stęŝeniu od 8 do 260 IU/ml. W badaniach typu look back nie wykazano przeniesienia zakaŝenia przez preparaty krwi przygotowane z tych donacji [20]. BADANIA DNA HBV W POLSCE Metodyka badań przeglądowych i weryfikacyjnych Badania przeglądowe DNA HBV wykonywane są w Pracowniach Biologii Molekularnej w 12 Centrach Krwiodawstwa i Krwiolecznictwa. Stosuje się dwie metody badań. W Centrach w Białymstoku, Bydgoszczy, Gdańsku, Kaliszu, Olsztynie, Poznaniu, Raciborzu wykonuje się badania metodą PCR (Cobas Ampliscreen HBV Roche) ze zlanych w pulę próbek od 24 dawców. Od początku 2007 stopniowo wprowadzano badania oparte na technice Real time PCR testem typu multiplex (HCV,HBV,HIV) Cobas 201 w pulach po 6 donacji. W Centrach w Kielcach, Krakowie, Lublinie, Łodzi, Rzeszowie, Warszawie i Szczecinie wykonuje się badania pojedynczych próbek metodą TMA (Ultrio HBV/HCV/HIU; Chiron Corp). Test Ultrio jest, podobnie jak test Cobas 201 testem typu multiplex. Dodatni wynik badania świadczy o obecności RNA HCV, RNA HIV lub DNA HBV. Dla ustalenia, który z wirusów jest obecny w próbce trzeba wykonać dalsze badania trzema testami wykrywającymi kaŝdy z badanych wirusów (tzw. testy dyskryminacji). Zgodnie z przyjętym obecnie algorytmem krew od wszystkich dawców bez markerów serologicznych z dodatnimi wynikami testów molekularnych, a takŝe dawców, których wyniki badań wzbudzają wątpliwości (np. dodatnie w teście typu multiplex, a ujemne we wszystkich trzech testach dyskryminacji) jest niszczona. Osocze tych dawców oraz dostępne próbki archiwalne i nowo pobrane są przesyłane do IHiT w celu dalszych badań. Wykonuje się w nich badania DNA HBV; jeśli ilość osocza jest wystarczająca to izolację DNA wykonuje się metodą automatyczną (Nuclisens Extractor- Biomerieux) z duŝej objętości (2 ml). Ocenia się teŝ poziom wiremii (Amplicor Monitor HBV Roche Diag lub techniką real time PCR Arthus) oraz wykonuje badania serologicznych markerów zakaŝenia HBV: HBsAg testami o wyŝszej czułości, niŝ te uŝyte do badań przeglądowych oraz badania anty-hbc, anty-hbs, anty-hbe i HBeAg.
5 Praktyczne konsekwencje wprowadzenia badań DNA HBV 49 Wyniki badań przeglądowych oraz charakterystyka serologiczna i molekularna donacji HBV DNA dodatnich HBsAg ujemnych Do końca 2005 roku badania DNA HBV wykonano w próbkach osocza dawców bez markerów serologicznych. DNA HBV wykryto w 8/ próbek badanych w pulach oraz w 9/ badanych pojedynczo testem TMA. Dodatkowo DNA HBV wykryto w 11 próbkach, w których wyniki testu Ultrio były dodatnie, a wyniki testu dyskryminującego ujemne. Częstość wykrywania DNA HBV wynosiła 0,003% (1:36000). Poziom wiremii w momencie wykrycia DNA HBV przy ujemnym wyniku testu przeglądowego HBsAg wynosił od <10 IU/ml do 4, IU/ml. Wiremia u 21/28 dawców była około 10 IU/ml, u 4/ do 1000 IU, a u , IU/ml. U dwóch dawców z poziomem wiremii 3, i 1, IU/ml wykryto HBsAg testem o wyŝszej czułości. Tabela 2. Analiza markerów serologicznych w próbkach dawców bez HBsAg z wykrytym DNA HBV Table 2. Serological markers analysis in blood donors samples HBsAg negative, HBV DNA positive Przeciwciała anty- HBc Liczba dawców IgM Total HBs HBe HBe Ag Dwudziestu trzech dawców było badanych w kierunku anty-hbs, anty-hb-c i anty-hbe (Tabela 2). U 4 nie wykryto Ŝadnych markerów serologicznych HBV. Badania kolejnych próbek u 3 z nich potwierdziły, Ŝe dawca w momencie wykrycia DNA HBV był w okienku serologicznym w następnej próbce wykryto HBsAg. U jednego z nich po 11 tygodniach nie wykryto HBsAg ani DNA HBV. Wykryto natomiast anty- HBc, anty-hbe i anty HBs. Aktywność ALT była w granicach normy. Dawca nie zgłaszał Ŝadnych dolegliwości i nie miał świadomości, Ŝe przebył zakaŝenia HBV (Rycina 1 AR). U 17 dawców badania wykazały obecność anty-hbc: u 8 był to jedyny marker serologiczny, u 6 towarzyszyły mu przeciwciała anty-hbe, u 2 dawców przeciwciała anty-hbs, a u 1 przeciwciała anty-hbs i anty-hbe. U jednego dawcy wykryto tylko przeciwciała anty-hbs, a u jednego anty-hbs i anty-hbe. Przykładowe wyniki badań kolejnych próbek u analizowanych dawców przedstawiono na Rycinie 1.
6 50 P. GRABARCZYK i wsp. AR kopie HBV DNA\ml ALAT 15 HBcAb-/- ALAT 20 HBcAb-/- HBsAb- HBeAb- HBsAg tygodnie ALAT 20 HBcAb+/+ HBsAb+ HBeAb+ PA ALAT 11 HBcAb -/ + HBeAg + HBsAg + kopie HBV DNA/ml ALAT 18 HBc Ab -/- HBs Ab - ALAT 22 HBcAb -/ tygodnie
7 Praktyczne konsekwencje wprowadzenia badań DNA HBV 51 PW HBV DNA kopie/ml ALAT 25 HBcAb+/- HBsAb- HBeAb+(66) HBsAg- ALAT 28 HBcAb+/- HBsAb- HBeAb+(67) ALAT 38 HBcAb+/- HBsAb- HBeAb+(65) ALAT 34 HBcAb+/- HBsAb- HBeAb+(61) tygodnie KB HBcAb+/+ HBeAb +(82) poziom wiremii (kopie/ml) tygodnie HBcAb+/+ HBcAb+/- HbeAg - HBeAb +(87) HBeAb +
8 52 P. GRABARCZYK i wsp. HM anty HBs IU/L ALAT 20 DNA HBV - nb HBcAb +/- ALAT 15 DNA HBV - nb HBcAb +/- ALAT 20 DNA HBV - HBcAb +/ tygodnie ALAT 20 DNA HBV - HBcAb +/- ALAT 23 DNA HBV - HBcAb+/ - ALAT 23 DNA HBV + HBcAb +/- Ryc. 1. Badania kolejnych próbek osocza dawców, u których w badaniach przeglądowych wykryto HBV DNA, a nie wykryto HBsAg. AR PA zakaŝenie HBV w okienku serologicznym bez Ŝadnych markerów serologicznych; PW przewlekłe ukryte zakaŝenie; KB faza eliminacji zakaŝenia, HM zakaŝenie ukryte, (oznaczenia ab przeciwciała, ag antygen, nb nie badane, HBcAb+/ : wynik badania anty HBc total/igm) Fig. 1. Testing of follow-up and look-back plasma samples from blood donors with HBV DNA screening assay positive results and HBsAg negative: AR PA HBV infection in window period without any serological marker, PW chronic occult infection, KB infection limitation, HM chronic occult infection (abreviations: ab - antibodies, ag antigen, nb not tested, HBcAb+/ : testing results of anti HBc total/igm) PODSUMOWANIE Wykrycie DNA HBV u dawcy krwi powoduje odsunięcie od oddawania krwi, czego konsekwencją jest z pewnością zwiększenie bezpieczeństwa przetoczeń (Tabela 1). Inną konsekwencją prowadzonych badań jest przekazywanie dawcom informacji o wykryciu DNA HBV bez wykrytego HBsAg. Dawca jest kierowany do lekarza pierwszego kontaktu, który powinien zająć się jego dalszymi losami. Niestety nie jest obecnie wiadomo jaki schemat postępowania naleŝy przyjąć. Nie ma na ten temat opinii równieŝ w innych krajach. KaŜdy przypadek wymaga indywidualnej obserwacji i decyzji. Z przeprowadzonych przez nas badań wynika, Ŝe poziom wiremii u dawców w momencie identyfikacji zakaŝenia HBV jest niski. Dla wypowiedzenia się jaki etap zaka- Ŝenia zidentyfikowano, jaka jest prognoza i jaki sposób postępowania naleŝy przyjąć konieczne jest wykonanie panelu badań serologicznych i molekularnych w próbce
9 Praktyczne konsekwencje wprowadzenia badań DNA HBV 53 wyjściowej, w kolejnych próbkach dawcy oraz ewentualnie w dostępnych próbkach wcześniejszych. W naszych badaniach wykazaliśmy, Ŝe identyfikujemy dawców na róŝnych etapach zakaŝenia. Spośród dawców bez markerów serologicznych u wszystkich prócz jednego w kolejnej próbce wykryto HBsAg, co potwierdziło, Ŝe zidentyfikowano u nich zakaŝenie w okienku serologicznym. Dalsze obserwacje u jednego z dawców z okienka wykazały bardzo szybkie samowyleczenie z eliminacją HBsAg i DNA HBV. Dawcy z DNA HBV i z obecnymi przeciwciałami anty-hbc i/lub anty-hbs i/ lub anty-hbe stanowili natomiast bardzo zróŝnicowaną grupę. Byli wśród nich dawcy we wczesnym okresie zakaŝenia z przeciwciałami anty-hbc klasy IgM i dawcy w okresie zdrowienia, gdy zanika HBsAg, a jeszcze nie pojawia się anty-hbs. U niektórych dawców obserwowano przewlekłe ukryte zakaŝenie z wahającym się poziomem wiremii. U jednego z badanych wykryto mutację w pozycji 145 genu S. Wydaje się, Ŝe ocena ilości DNA HBV oraz analiza mutacji genomu wirusa stanowią konieczne badania konsultacyjne w tej grupie dawców. Bardzo waŝne byłoby poddanie tej grupy dawców specjalistycznym badaniom hepatologicznym by ocenić istotność kliniczną ukrytego zakaŝenia. Z pewnością badania dawców z wykrytym DNA HBV pozwalają na nowe obserwacje naturalnego przebiegu zakaŝenia HBV i mogą wnieść nowe dane na temat biologii tego znanego od wielu lat wirusa. Obserwacje dawców z okienka pozwolą na analizę częstości i przebiegu samoistnej eliminacji zakaŝenia u osób, które nie mają Ŝadnych objawów klinicznych i w inny sposób niŝ badania w krwiodawstwie nie byłyby zidentyfikowane. Dodatkowe badania takich osób (np. badania HLA, badania immunologicznej odpowiedzi komórkowej) mogą zidentyfikować nieznane dotąd mechanizmy skutecznej walki organizmu z zakaŝeniem HBV oraz istotne czynniki rokownicze. Badania u dawców z ukrytym zakaŝeniem pozwolą poszerzyć wiedzę o naturze tego zjawiska. Podziękowania Badania przeglądowe DNA HBV dawców krwi wykonane były w Pracowniach Biologii Molekularnej Regionalnych Centrów Krwiodawstwa i Krwiolecznictwa w Białymstoku, Bydgoszczy, Gdańsku, Kaliszu, Kielcach, Krakowie, Łodzi, Poznaniu, Raciborzu, Rzeszowie, Szczecinie i Warszawie. Wszystkie te Centra, a takŝe Centra w Słupsku, Olsztynie, Zielonej Górze, Katowicach, i Radomiu prowadziły badania lekarskie, badania ALT i badania serologiczne oraz dostarczały do IHiT próbki osocza dawców. Dziękujemy wszystkim Pracownikom RCKiK za ich wysiłek. Badania częściowo finansowane z projektu badawczego nr N /3601 finansowanego przez MNiSW. PIŚMIENNICTWO 1. Coste J, Reesink HW, Engelfriet P i wsp. International Forum. Implementation of donors screening for infectious agents transmitted by blood by nucleic acid technology: update to Vox Sang 2005; 88:
10 54 P. GRABARCZYK i wsp. 2. Brojer E. Implementation of donor sreening for infectious agents transmitted by blood by nucleic acid technology in Poland.Vox Sang, 2005; 89: Brojer E, Łetowska M, Gronowska A. Nucleic Acid Testing for virus screening in Polish blood donors. Transf Med 2004; 14: Stramer SL, Glynn SA, Kleinman SH, i wsp. National Heart, Lung and Blood Institute Nucleic Acid Test Study Group: Detection of HIV-1 and HCV infections among antibody-negative blood donors by nucleic acid-amplification testing. N Engl J Med. 2004; 351: Roth K, Weber W i wsp. NAT for HBV and anti-hbc testing increase blood safety. Transfusion 2002; 42 (7): Murokawa, H, Yoshikawa, A, Ohnuma H i wsp. Epidemiology of blood donors in Japan, positive for hepatitis B virus and hepatitis C virus by nucleic acid amplification testing. Vox Sang 2005; 88: Magdzik W. Wirusowe zapalenie wątroby typu B w Polsce do 2002 roku. PZH. Warszawa Seyfried H, Grabarczyk P, Mikulska M. i wsp. Analiza częstości wykrywania antygenu HBs u polskich dawców krwi w latach (w przygotowaniu do druku). 9. Stramer S.L. US NAT yield: where are we after 2 years? Transfusion Clinique et Biol 2003; 10: Alain JP. Occult hepatitis B infection: implications in transfusion.vox Sang 2004; 86: Biswas R, Tabor E, Hsia CC, i wsp. Comparative sensitivity of HBV NATs and HBsAg assays for detection of acute HBV infection. Transfusion 2003; 43: Yoshikawa A, Gotanda Y, Itabashi M i wsp. HBV NAT positive blood donors in the early and late stages of HBV infection: analyses of the window period and kinetics of DNA HBV. Vox Sang 2005; 88: Brojer E, Łętowska M, Medyńska J. i wsp. Validation of Procleix Ultrio assay in Poland. Vox Sang 2004, 87 (suppl 3): Chudy M, Amberg I, Hanker-Dusel C. i wsp. Procleix Ultrio Assay performance trial. Vox Sang 2004; 87 (suppl 3), Koppelman M, Sjerps M, Reesink H i wsp. Evaluation of Cobas AmpliPrep-AmpliScreen assay for DNA HBV screening. Vox Sang 2004; 87 (suppl 3): Iwamoto M, Jernigan DB, Kao J. i wsp. A molecular analysisis of pres/susrface and pre-core.core promoter genes of hepatitis B virus in chronic hepatitis C patients with occult HBV infection. J Med Virol 2002; 68: Yamamoto K, Horkita M, Tsuda F. i wsp. Naturally occurring escape mutants of hepatitis B virus with various mutations in the S gene in carriers seropositive for antibody to hepatitis B surface antigen. J Virol 1994; 68: Kleinman SH, Kuhmns MC, Todd DS i wsp. Frequency of DNA HBV detection in US blood donors testing positive for anti-hbc: implications for transfusion transmission and donor screening. Transfusion 2003; 43: Mosley JW, Stevens CE, Aach RD i wsp. Donor screening for antibody to hepatitids B core antigen and hepatitis B virus infection in transfusion recipients. Transfusion 1995; 35: Dreier J, Kroger M, Diekmann J. i wsp. Low-level viraemia of hepatitis B virus in an anti-hbc- and anti-hbs-positive blood donor. Transfus Med 2004; 14: Praca wpłynęła do Redakcji r. i została zakwalifikowana do druku r. Adres do korespondencji: Prof. dr hab. med. Ewa Brojer Instytut Hematologii i Transfuzzjologii ul. Chocimska Warszawa ebrojer@ihit.waw.pl
PRACA ORYGINALNA. Elżbieta Ćwikowska, Izabela Michalczak, Karolina Stasik-Pierechod, Danuta Pruszkowska, Barbara Wyrwińska, Małgorzata Szafran
 PRACA ORYGINALNA Journal of Transfusion Medicine 2010, tom 3, nr 2, 55 61 Copyright 2010 Via Medica ISSN 1689 6017 Badania technikami biologii molekularnej wirusów zapalenia wątroby typu B i typu C oraz
PRACA ORYGINALNA Journal of Transfusion Medicine 2010, tom 3, nr 2, 55 61 Copyright 2010 Via Medica ISSN 1689 6017 Badania technikami biologii molekularnej wirusów zapalenia wątroby typu B i typu C oraz
BADANIA WIRUSÓW PRZENOSZONYCH PRZEZ KREW U DAWCÓW KRWI W POLSCE
 PRZEGL EPIDEMIOL 2015; 69: 591-595 Problemy zakażeń Piotr Grabarczyk, Aneta Kopacz, Ewa Sulkowska, Dorota Kubicka-Russel, Maria Mikulska, Ewa Brojer, Magdalena Łętowska BADANIA WIRUSÓW PRZENOSZONYCH PRZEZ
PRZEGL EPIDEMIOL 2015; 69: 591-595 Problemy zakażeń Piotr Grabarczyk, Aneta Kopacz, Ewa Sulkowska, Dorota Kubicka-Russel, Maria Mikulska, Ewa Brojer, Magdalena Łętowska BADANIA WIRUSÓW PRZENOSZONYCH PRZEZ
Epidemiologia zakaŝeń wirusowych wykrywanych w RCKiK w Bydgoszczy w latach
 PRACA ORYGINALNA Original Article Acta Haematologica Polonica 2011, 42, Nr 3, str. 549 557 MAŁGORZATA MAJKOWSKA Epidemiologia zakaŝeń wirusowych wykrywanych w RCKiK w Bydgoszczy w latach 2000-2009 Epidemiology
PRACA ORYGINALNA Original Article Acta Haematologica Polonica 2011, 42, Nr 3, str. 549 557 MAŁGORZATA MAJKOWSKA Epidemiologia zakaŝeń wirusowych wykrywanych w RCKiK w Bydgoszczy w latach 2000-2009 Epidemiology
Algorytmy postępowania w diagnostyce zakażeń wirusów przenoszonych przez krew
 Algorytmy postępowania w diagnostyce zakażeń wirusów przenoszonych przez krew Ewa Sulkowska, Piotr Grabarczyk Zakład Wirusologii IHiT XIX Zjazd PTDL Wrzesień 2017, Kraków Dawca krwi, kandydat na dawcę
Algorytmy postępowania w diagnostyce zakażeń wirusów przenoszonych przez krew Ewa Sulkowska, Piotr Grabarczyk Zakład Wirusologii IHiT XIX Zjazd PTDL Wrzesień 2017, Kraków Dawca krwi, kandydat na dawcę
Wirus zapalenia wątroby typu B
 Wirus zapalenia wątroby typu B Kliniczne następstwa zakażenia odsetek procentowy wyzdrowienie przewlekłe zakażenie Noworodki: 10% 90% Dzieci 1 5 lat: 70% 30% Dzieci starsze oraz 90% 5% - 10% Dorośli Choroby
Wirus zapalenia wątroby typu B Kliniczne następstwa zakażenia odsetek procentowy wyzdrowienie przewlekłe zakażenie Noworodki: 10% 90% Dzieci 1 5 lat: 70% 30% Dzieci starsze oraz 90% 5% - 10% Dorośli Choroby
Zwiększenie bezpieczeństwa przetoczeń w Polsce przez wprowadzenie statusu kandydata na dawcę
 ARTYKUŁ POGLĄDOWY Journal of Transfusion Medicine 2016, tom 9, nr 1, 1 5 Copyright 2016 Roche Diagnostics Polska Sp. z o.o. ISSN 1689 6017 Zwiększenie bezpieczeństwa przetoczeń w Polsce przez wprowadzenie
ARTYKUŁ POGLĄDOWY Journal of Transfusion Medicine 2016, tom 9, nr 1, 1 5 Copyright 2016 Roche Diagnostics Polska Sp. z o.o. ISSN 1689 6017 Zwiększenie bezpieczeństwa przetoczeń w Polsce przez wprowadzenie
Serological markers of hepatitis B virus
 MED. DOŚW. MIKROBIOL., 2018, 70: 77-82 Serologiczne markery wirusowego zapalenia wątroby typu B Serological markers of hepatitis B virus Joanna Wróblewska, Wiesława Chudobińska Kula, Marcin Ziuziakowski,
MED. DOŚW. MIKROBIOL., 2018, 70: 77-82 Serologiczne markery wirusowego zapalenia wątroby typu B Serological markers of hepatitis B virus Joanna Wróblewska, Wiesława Chudobińska Kula, Marcin Ziuziakowski,
GENOTYPY HCV U POLSKICH DAWCÓW KRWI W OKRESIE 1995-2007 1
 PRZEGL EPIDEMIOL 2008; 62: 163-169 Ewa Brojer, Piotr Grabarczyk, Aneta Kopacz, Anna Potępa, Joanna Medyńska, Justyna Smolarczyk-Wodzyńska, Magdalena Łętowska GENOTYPY HCV U POLSKICH DAWCÓW KRWI W OKRESIE
PRZEGL EPIDEMIOL 2008; 62: 163-169 Ewa Brojer, Piotr Grabarczyk, Aneta Kopacz, Anna Potępa, Joanna Medyńska, Justyna Smolarczyk-Wodzyńska, Magdalena Łętowska GENOTYPY HCV U POLSKICH DAWCÓW KRWI W OKRESIE
/LF]EDZ\NU\W\FKEDGDQ\FK
![/LF]EDZ\NU\W\FKEDGDQ\FK /LF]EDZ\NU\W\FKEDGDQ\FK](/thumbs/21/1202494.jpg) PRZEGL Nr 2 EPIDEMIOL Badania 2005; 59:511 517 serologicznych i molekularnych markerów HCV 511 Ewa Brojer BADANIA SEROLOGICZNYCH I MOLEKULARNYCH MARKERÓW HCV U DAWCÓW KRWI W POLSCE Instytut Hematologii
PRZEGL Nr 2 EPIDEMIOL Badania 2005; 59:511 517 serologicznych i molekularnych markerów HCV 511 Ewa Brojer BADANIA SEROLOGICZNYCH I MOLEKULARNYCH MARKERÓW HCV U DAWCÓW KRWI W POLSCE Instytut Hematologii
Epidemiologia zakażenia HIV na przykładzie dawców RCKiK we Wrocławiu
 ARTYKUŁ poglądowy Journal of Transfusion Medicine 2015, tom 8, nr 4, 162 167 Copyright 2015 Roche Diagnostics Polska Sp. z o.o. ISSN 1689 6017 Epidemiologia zakażenia HIV na przykładzie dawców RCKiK we
ARTYKUŁ poglądowy Journal of Transfusion Medicine 2015, tom 8, nr 4, 162 167 Copyright 2015 Roche Diagnostics Polska Sp. z o.o. ISSN 1689 6017 Epidemiologia zakażenia HIV na przykładzie dawców RCKiK we
Ocena aktywności AlAT jako testu pomagającego wykluczać dawców krwi zakażonych wirusem zapalenia wątroby
 PRACA ORYGINALNA Journal of Transfusion Medicine 2008, tom 1, nr 1, 28 35 Copyright 2008 Via Medica ISSN 1689 6017 Ocena aktywności AlAT jako testu pomagającego wykluczać dawców krwi zakażonych wirusem
PRACA ORYGINALNA Journal of Transfusion Medicine 2008, tom 1, nr 1, 28 35 Copyright 2008 Via Medica ISSN 1689 6017 Ocena aktywności AlAT jako testu pomagającego wykluczać dawców krwi zakażonych wirusem
"Samowystarczalność Polski w zakresie zaopatrzenia w bezpieczną krew, jej składniki i produkty krwiopochodne na lata 2005-2008".
 Ministerstwo Zdrowia PROGRAM POLITYKI ZDROWOTNEJ PAŃSTWA Nazwa programu: "Samowystarczalność Polski w zakresie zaopatrzenia w bezpieczną krew, jej składniki i produkty krwiopochodne na lata 2005-2008".
Ministerstwo Zdrowia PROGRAM POLITYKI ZDROWOTNEJ PAŃSTWA Nazwa programu: "Samowystarczalność Polski w zakresie zaopatrzenia w bezpieczną krew, jej składniki i produkty krwiopochodne na lata 2005-2008".
NA ZAKAŻENIE HBV i HCV
 NA ZAKAŻENIE HBV i HCV Wojewódzka Stacja Sanitarno-Epidemiologiczna w Gdańsku 18.04.2016r. Aneta Bardoń-Błaszkowska HBV - Hepatitis B Virus Simplified diagram of the structure of hepatitis B virus, Autor
NA ZAKAŻENIE HBV i HCV Wojewódzka Stacja Sanitarno-Epidemiologiczna w Gdańsku 18.04.2016r. Aneta Bardoń-Błaszkowska HBV - Hepatitis B Virus Simplified diagram of the structure of hepatitis B virus, Autor
Journal of Transfusion Medicine 2009, tom 2, nr 3, Copyright 2009 Via Medica ISSN PRACA ORYGINALNA
 PRACA ORYGINALNA Journal of Transfusion Medicine 2009, tom 2, nr 3, 137 149 Copyright 2009 Via Medica ISSN 1689 6017 Roczne doświadczenie w badaniu metodami biologii molekularnej ludzkiego wirusa niedoboru
PRACA ORYGINALNA Journal of Transfusion Medicine 2009, tom 2, nr 3, 137 149 Copyright 2009 Via Medica ISSN 1689 6017 Roczne doświadczenie w badaniu metodami biologii molekularnej ludzkiego wirusa niedoboru
Magdalena Durlik Klinika Medycyny Transplantacyjnej i Nefrologii Instytut Transplantologii Warszawski Uniwersytet Medyczny
 Magdalena Durlik Klinika Medycyny Transplantacyjnej i Nefrologii Instytut Transplantologii Warszawski Uniwersytet Medyczny Ryzyko przeniesienia choroby od dawcy do biorcy przeszczepu Zakażenia bakteryjne,
Magdalena Durlik Klinika Medycyny Transplantacyjnej i Nefrologii Instytut Transplantologii Warszawski Uniwersytet Medyczny Ryzyko przeniesienia choroby od dawcy do biorcy przeszczepu Zakażenia bakteryjne,
Mikrobiologia - Wirusologia
 5650 Wirus cytomegalii - przeciwciała Mikrobiologia - Wirusologia 3 próbki płynnego ludzkiego osocza (>0,7 ml). Przeciwciała przeciwko CMV całkowite, klasy: IgG, IgM, IgG awidność i komentarz 5635 Wirus
5650 Wirus cytomegalii - przeciwciała Mikrobiologia - Wirusologia 3 próbki płynnego ludzkiego osocza (>0,7 ml). Przeciwciała przeciwko CMV całkowite, klasy: IgG, IgM, IgG awidność i komentarz 5635 Wirus
(Akty o charakterze nieustawodawczym) DECYZJE
 19.7.2019 PL L 193/1 II (Akty o charakterze nieustawodawczym) DECYZJE DECYZJA WYKONAWCZA KOMISJI (UE) 2019/1244 z dnia 1 lipca 2019 r. zmieniająca decyzję 2002/364/WE w odniesieniu do wymogów dotyczących
19.7.2019 PL L 193/1 II (Akty o charakterze nieustawodawczym) DECYZJE DECYZJA WYKONAWCZA KOMISJI (UE) 2019/1244 z dnia 1 lipca 2019 r. zmieniająca decyzję 2002/364/WE w odniesieniu do wymogów dotyczących
Mikrobiologia - Wirusologia
 5650 Wirus cytomegalii - przeciwciała Mikrobiologia - Wirusologia 3 próbki płynnego ludzkiego osocza (>0,7 ml). Przeciwciała przeciwko CMV całkowite, klasy: IgG, IgM, IgG awidność i komentarz 5635 Wirus
5650 Wirus cytomegalii - przeciwciała Mikrobiologia - Wirusologia 3 próbki płynnego ludzkiego osocza (>0,7 ml). Przeciwciała przeciwko CMV całkowite, klasy: IgG, IgM, IgG awidność i komentarz 5635 Wirus
Mikrobiologia - Wirusologia
 Mikrobiologia - Wirusologia 5650 Wirus cytomegalii - przeciwciała (EQA 3 -sprawdzian zintegrowany) 3 próbki płynnego ludzkiego osocza (0,5 ml). Przeciwciała przeciwko CMV całkowite, klasy: IgG, IgM, IgG
Mikrobiologia - Wirusologia 5650 Wirus cytomegalii - przeciwciała (EQA 3 -sprawdzian zintegrowany) 3 próbki płynnego ludzkiego osocza (0,5 ml). Przeciwciała przeciwko CMV całkowite, klasy: IgG, IgM, IgG
Efekty leczenia lamiwudyną przewlekłych wirusowych zapaleń wątroby typu B na podstawie materiału własnego.
 Efekty leczenia lamiwudyną przewlekłych wirusowych zapaleń wątroby typu B na podstawie materiału własnego. Hanna Berak Wojewódzki Szpital Zakaźny w Warszawie Wskazania do leczenia lamiwudyną nieskuteczna
Efekty leczenia lamiwudyną przewlekłych wirusowych zapaleń wątroby typu B na podstawie materiału własnego. Hanna Berak Wojewódzki Szpital Zakaźny w Warszawie Wskazania do leczenia lamiwudyną nieskuteczna
Badania w krwiodawstwie jako źródło wiedzy o czynnikach zakaźnych przenoszonych przez krew
 PRZEGLĄD PIŚMIENNICTWA Journal of Transfusion Medicine 2016, tom 9, nr 1, 32 37 Copyright 2016 Via Medica ISSN 1689 6017 Badania w krwiodawstwie jako źródło wiedzy o czynnikach zakaźnych przenoszonych
PRZEGLĄD PIŚMIENNICTWA Journal of Transfusion Medicine 2016, tom 9, nr 1, 32 37 Copyright 2016 Via Medica ISSN 1689 6017 Badania w krwiodawstwie jako źródło wiedzy o czynnikach zakaźnych przenoszonych
Białko jako marker molekularny
 Białko jako marker molekularny Markery białkowe: - obecność lub brak (lub zmiana ilości) określonego białka wskazuje na istnienie określonej zmiany fizjologicznej lub chorobowej (np. pojawienie się we
Białko jako marker molekularny Markery białkowe: - obecność lub brak (lub zmiana ilości) określonego białka wskazuje na istnienie określonej zmiany fizjologicznej lub chorobowej (np. pojawienie się we
MEDYCZNE ZASADY POBIERANIA KRWI, ODDZIELANIA JEJ SKŁADNIKÓW I WYDAWANIA, OBOWIĄZUJĄCE W JEDNOSTKACH ORGANIZACYJNYCH PUBLICZNEJ SŁUŻBY KRWI
 MEDYCZNE ZASADY POBIERANIA KRWI, ODDZIELANIA JEJ SKŁADNIKÓW I WYDAWANIA, OBOWIĄZUJĄCE W JEDNOSTKACH ORGANIZACYJNYCH PUBLICZNEJ SŁUŻBY KRWI Diagnostyka czynników zakaźnych przenoszonych przez krew 1.1 Zasady
MEDYCZNE ZASADY POBIERANIA KRWI, ODDZIELANIA JEJ SKŁADNIKÓW I WYDAWANIA, OBOWIĄZUJĄCE W JEDNOSTKACH ORGANIZACYJNYCH PUBLICZNEJ SŁUŻBY KRWI Diagnostyka czynników zakaźnych przenoszonych przez krew 1.1 Zasady
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2015 rok Obowiązuje od: 01 stycznia 2015 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2015 rok Obowiązuje od: 01 stycznia 2015 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
ARTYKUŁ ORYGINALNY. Journal of Transfusion Medicine 2018, tom 11, nr 3, Copyright 2018 Via Medica ISSN
 ARTYKUŁ ORYGINALNY Journal of Transfusion Medicine 2018, tom 11, nr 3, 91 99 Copyright 2018 Via Medica ISSN 1689 6017 Charakterystyka testu cobas DPX przeznaczonego do badania dawców krwi na obecność DNA
ARTYKUŁ ORYGINALNY Journal of Transfusion Medicine 2018, tom 11, nr 3, 91 99 Copyright 2018 Via Medica ISSN 1689 6017 Charakterystyka testu cobas DPX przeznaczonego do badania dawców krwi na obecność DNA
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2013 rok Obowiązuje od: 01 stycznia 2013 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2013 rok Obowiązuje od: 01 stycznia 2013 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
Ukryte zakaŝenie wirusem HBV w hematologii i transfuzjologii
 PRACA POGLĄDOWA Review Article Acta Haematologica Polonica 2009, 40, Nr 2, str. 435 449 EWA BROJER Ukryte zakaŝenie wirusem HBV w hematologii i transfuzjologii Occult B infection in haematology and blood
PRACA POGLĄDOWA Review Article Acta Haematologica Polonica 2009, 40, Nr 2, str. 435 449 EWA BROJER Ukryte zakaŝenie wirusem HBV w hematologii i transfuzjologii Occult B infection in haematology and blood
Epidemiologia zakażeń wirusami zapalenia wątroby typu B i C wśród zmarłych dawców narządów w Polsce
 Pszenny Probl Hig A Epidemiol i wsp. Epidemiologia 2012, 93(3): zakażeń 579-585 wirusami zapalenia wątroby typu B i C wśród zmarłych dawców narządów 579 Epidemiologia zakażeń wirusami zapalenia wątroby
Pszenny Probl Hig A Epidemiol i wsp. Epidemiologia 2012, 93(3): zakażeń 579-585 wirusami zapalenia wątroby typu B i C wśród zmarłych dawców narządów 579 Epidemiologia zakażeń wirusami zapalenia wątroby
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2018 rok Obowiązuje od: 01 stycznia 2018 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2018 rok Obowiązuje od: 01 stycznia 2018 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
metody diagnostyczne
 Zakażenie wirusem zapalenia wątroby typu E sytuacja epidemiologiczna oraz metody diagnostyczne Piotr Grabarczyk Zakład Wirusologii XIX Zjazd Polskiego Towarzystwa Diagnostyki Laboratoryjnej Kraków, 3-6
Zakażenie wirusem zapalenia wątroby typu E sytuacja epidemiologiczna oraz metody diagnostyczne Piotr Grabarczyk Zakład Wirusologii XIX Zjazd Polskiego Towarzystwa Diagnostyki Laboratoryjnej Kraków, 3-6
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2015 rok Obowiązuje od: 01 stycznia 2015 roku Aneks obowiązuje od 21 października 2015 roku SPIS
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2015 rok Obowiązuje od: 01 stycznia 2015 roku Aneks obowiązuje od 21 października 2015 roku SPIS
(Akty przyjęte na mocy Traktatów WE/Euratom, których publikacja nie jest obowiązkowa) DECYZJE KOMISJA
 PL 4.12.2009 Dziennik Urzędowy Unii Europejskiej L 318/25 II (Akty przyjęte na mocy Traktatów WE/Euratom, których publikacja nie jest obowiązkowa) DECYZJE KOMISJA DECYZJA KOMISJI z dnia 27 listopada 2009
PL 4.12.2009 Dziennik Urzędowy Unii Europejskiej L 318/25 II (Akty przyjęte na mocy Traktatów WE/Euratom, których publikacja nie jest obowiązkowa) DECYZJE KOMISJA DECYZJA KOMISJI z dnia 27 listopada 2009
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2016 rok Obowiązuje od: 01 stycznia 2016 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG na 2016 rok Obowiązuje od: 01 stycznia 2016 roku SPIS TREŚCI I. Badania laboratoryjne II. III. Krew
CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG Od 01 maja 2018 roku Obowiązuje od: 01 maja 2018 roku Strona 1 / 6 SPIS TREŚCI I. Badania laboratoryjne
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA W LUBLINIE CENNIK KRWI I JEJ SKŁADNIKÓW ORAZ USŁUG Od 01 maja 2018 roku Obowiązuje od: 01 maja 2018 roku Strona 1 / 6 SPIS TREŚCI I. Badania laboratoryjne
Jolanta Antoniewicz-Papis Instytut Hematologii i Transfuzjologii
 Jolanta Antoniewicz-Papis Instytut Hematologii i Transfuzjologii Napotykane ryzyko związane jest z: dawcami biorcami pracownikami jednostek służby krwi i jednostek służby zdrowia Program zarządzania ryzykiem
Jolanta Antoniewicz-Papis Instytut Hematologii i Transfuzjologii Napotykane ryzyko związane jest z: dawcami biorcami pracownikami jednostek służby krwi i jednostek służby zdrowia Program zarządzania ryzykiem
Zastosowania analizatora cobas p 312 do automatyzacji fazy przedanalitycznej badań wirusologicznych w Centrum Krwiodawstwa i Krwiolecznictwa
 ARTYKUŁ POGLĄDOWY Journal of Transfusion Medicine 2016, tom 9, nr 1, 24 31 Copyright 2016 Roche Diagnostics Polska Sp. z o.o. ISSN 1689 6017 Zastosowania analizatora cobas p 312 do automatyzacji fazy przedanalitycznej
ARTYKUŁ POGLĄDOWY Journal of Transfusion Medicine 2016, tom 9, nr 1, 24 31 Copyright 2016 Roche Diagnostics Polska Sp. z o.o. ISSN 1689 6017 Zastosowania analizatora cobas p 312 do automatyzacji fazy przedanalitycznej
Geneza powstania Programu
 Postępy w biegłości wykonywania badań przedtransfuzyjnych, ocenie i formułowaniu wyników w czasie prowadzenia Krajowego Programu Oceny Jakości dla Laboratoriów Immunologii Transfuzjologicznej Bogumiła
Postępy w biegłości wykonywania badań przedtransfuzyjnych, ocenie i formułowaniu wyników w czasie prowadzenia Krajowego Programu Oceny Jakości dla Laboratoriów Immunologii Transfuzjologicznej Bogumiła
Ewa Brojer, Magdalena Łętowska. Czynniki zakaźne przenoszone przez krew
 SPRAWOZDANIE Journal of Transfusion Medicine 2010, tom 3, nr 1, 27 33 Copyright 2010 Via Medica ISSN 1689 6017 Sprawozdanie z XIX Regionalnego Zjazdu Międzynarodowego Towarzystwa Przetaczania Krwi (ISBT)
SPRAWOZDANIE Journal of Transfusion Medicine 2010, tom 3, nr 1, 27 33 Copyright 2010 Via Medica ISSN 1689 6017 Sprawozdanie z XIX Regionalnego Zjazdu Międzynarodowego Towarzystwa Przetaczania Krwi (ISBT)
Opis przedmiotu zamówienia
 Załącznik nr 1 do SIWZ PO ZMIANACH Opis przedmiotu zamówienia Przedmiotem zamówienia jest dostawa testów wirusologicznych HBsAg z testami potwierdzenia, testów anty-hcv, testów anty-hiv 1/2, testów do
Załącznik nr 1 do SIWZ PO ZMIANACH Opis przedmiotu zamówienia Przedmiotem zamówienia jest dostawa testów wirusologicznych HBsAg z testami potwierdzenia, testów anty-hcv, testów anty-hiv 1/2, testów do
KOMISJA DECYZJE. L 39/34 Dziennik Urzędowy Unii Europejskiej
 L 39/34 Dziennik Urzędowy Unii Europejskiej 10.2.2009 II (Akty przyjęte na mocy Traktatów WE/Euratom, których publikacja nie jest obowiązkowa) DECYZJE KOMISJA DECYZJA KOMISJI z dnia 3 lutego 2009 r. zmieniająca
L 39/34 Dziennik Urzędowy Unii Europejskiej 10.2.2009 II (Akty przyjęte na mocy Traktatów WE/Euratom, których publikacja nie jest obowiązkowa) DECYZJE KOMISJA DECYZJA KOMISJI z dnia 3 lutego 2009 r. zmieniająca
ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67)
 Załącznik B.15. ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii pierwotnej i wtórnej
Załącznik B.15. ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii pierwotnej i wtórnej
WYROK z dnia 11 lutego 2013 r.
 Sygn. akt: KIO 185/13 Krajowa Izba Odwoławcza - w składzie: WYROK z dnia 11 lutego 2013 r. Przewodniczący: Małgorzata Rakowska Protokolant: Radosław Cwyl po rozpoznaniu na rozprawie w dniu 7 lutego 2013
Sygn. akt: KIO 185/13 Krajowa Izba Odwoławcza - w składzie: WYROK z dnia 11 lutego 2013 r. Przewodniczący: Małgorzata Rakowska Protokolant: Radosław Cwyl po rozpoznaniu na rozprawie w dniu 7 lutego 2013
STAŻ KIERUNKOWY: CELE I ZADANIA PLACÓWEK PUBLICZNEJ SŁUŻBY KRWI. L.p. Nazwa jednostki Adres Województwo Liczba miejsc Uwagi. ul.ks.
 Lista ministra właściwego do spraw zdrowia podmiotów uprawnionych do prowadzenia staży kierunkowych w ramach specjalizacji diagnostów laboratoryjnych w dziedzinie: LABORATORYJNA TRANSFUZJOLOGIA MEDYCZNA
Lista ministra właściwego do spraw zdrowia podmiotów uprawnionych do prowadzenia staży kierunkowych w ramach specjalizacji diagnostów laboratoryjnych w dziedzinie: LABORATORYJNA TRANSFUZJOLOGIA MEDYCZNA
Systemy diagnostyczne stosowane do wykrywania zakaŝeń wirusem HIV w latach 1987 do 2009 w Regionalnym Centrum Krwiodawstwa i Krwiolecznictwa
 PRACA ORYGINALNA Original Article Acta Haematologica Polonica 2011, 42, Nr 3, str. 531 539 L. BASTA 1, B. MAZUR 2, E. RUDOWSKA 1, S. DYLĄG 1, B. DRYBAŃSKA 1 Systemy diagnostyczne stosowane wykrywania zakaŝeń
PRACA ORYGINALNA Original Article Acta Haematologica Polonica 2011, 42, Nr 3, str. 531 539 L. BASTA 1, B. MAZUR 2, E. RUDOWSKA 1, S. DYLĄG 1, B. DRYBAŃSKA 1 Systemy diagnostyczne stosowane wykrywania zakaŝeń
Kwestionariusz wiedzy dla pracowników programów i placówek narkotykowych
 Inicjatywa EMCDDA na rzecz redukcji szkód Zwiększanie testowania na obecność wirusa zapalenia wątroby (WZW) typu C oraz skierowań do leczenia wśród iniekcyjnych użytkowników narkotyków w programach i placówkach
Inicjatywa EMCDDA na rzecz redukcji szkód Zwiększanie testowania na obecność wirusa zapalenia wątroby (WZW) typu C oraz skierowań do leczenia wśród iniekcyjnych użytkowników narkotyków w programach i placówkach
Małgorzata Pawłowska, Waldemar Halota
 PRZEGL EPIDEMIOL 2007; 61: 427-431 Małgorzata Pawłowska, Waldemar Halota SZYBKA ODPOWIEDŹ WIRUSOLOGICZNA W PRZEBIEGU LECZENIA PEGYLOWANYM INTERFERONEM ALFA-2A PRZEWLEKŁEGO ZAPALENIA WĄTROBY TYPU B U DZIECI
PRZEGL EPIDEMIOL 2007; 61: 427-431 Małgorzata Pawłowska, Waldemar Halota SZYBKA ODPOWIEDŹ WIRUSOLOGICZNA W PRZEBIEGU LECZENIA PEGYLOWANYM INTERFERONEM ALFA-2A PRZEWLEKŁEGO ZAPALENIA WĄTROBY TYPU B U DZIECI
Diagnostyka czynników zakaźnych przenoszonych przez krew*
 ARTYKUŁ REDAKCYJNY Journal of Transfusion Medicine 2008, tom 1, nr 1, 1 19 Copyright 2008 Via Medica ISSN 1689 6017 Diagnostyka czynników zakaźnych przenoszonych przez krew* Diagnostics of blood transmitted
ARTYKUŁ REDAKCYJNY Journal of Transfusion Medicine 2008, tom 1, nr 1, 1 19 Copyright 2008 Via Medica ISSN 1689 6017 Diagnostyka czynników zakaźnych przenoszonych przez krew* Diagnostics of blood transmitted
METODA REAL - TIME PCR W DIAGNOSTYCE ZAKAŻEŃ WIRUSEM EPSTEINA-BARR
 MED. DOŚW. MIKROBIOL., 2009, 61: 253-258 Agnieszka Trzcińska, Joanna Siennicka METODA REAL - TIME PCR W DIAGNOSTYCE ZAKAŻEŃ WIRUSEM EPSTEINA-BARR Zakład Wirusologii NIZP-PZH w Warszawie Kierownik: doc.
MED. DOŚW. MIKROBIOL., 2009, 61: 253-258 Agnieszka Trzcińska, Joanna Siennicka METODA REAL - TIME PCR W DIAGNOSTYCE ZAKAŻEŃ WIRUSEM EPSTEINA-BARR Zakład Wirusologii NIZP-PZH w Warszawie Kierownik: doc.
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r.
 Dziennik Ustaw Nr 269 15693 Poz. 1598 1598 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na
Dziennik Ustaw Nr 269 15693 Poz. 1598 1598 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na
STAŻ KIERUNKOWY: CELE I ZADANIA PLACÓWEK PUBLICZNEJ SŁUŻBY KRWI. L.p. Nazwa jednostki Adres Województwo Liczba miejsc Uwagi. ul.ks.
 Lista ministra właściwego do spraw zdrowia podmiotów uprawnionych do prowadzenia staży kierunkowych w ramach specjalizacji diagnostów laboratoryjnych w dziedzinie: LABORATORYJNA TRANSFUZJOLOGIA MEDYCZNA
Lista ministra właściwego do spraw zdrowia podmiotów uprawnionych do prowadzenia staży kierunkowych w ramach specjalizacji diagnostów laboratoryjnych w dziedzinie: LABORATORYJNA TRANSFUZJOLOGIA MEDYCZNA
PROGRAM SZKOLENIA PIELĘGNIAREK I POŁOŻNYCH DOKONUJĄCYCH PRZETACZANIA KRWI I JEJ SKŁADNIKÓW
 PROGRAM SZKOLENIA PIELĘGNIAREK I POŁOŻNYCH DOKONUJĄCYCH PRZETACZANIA KRWI I JEJ SKŁADNIKÓW opracowany przez Instytut Hematologii i Transfuzjologii w dniu 27 kwietnia 2005r. 1.Szkolenie podstawowe SZKOLENIE
PROGRAM SZKOLENIA PIELĘGNIAREK I POŁOŻNYCH DOKONUJĄCYCH PRZETACZANIA KRWI I JEJ SKŁADNIKÓW opracowany przez Instytut Hematologii i Transfuzjologii w dniu 27 kwietnia 2005r. 1.Szkolenie podstawowe SZKOLENIE
Diagnostyka zakażeń EBV
 Diagnostyka zakażeń EBV Jakie wyróżniamy główne konsekwencje kliniczne zakażenia EBV: 1) Mononukleoza zakaźna 2) Chłoniak Burkitta 3) Potransplantacyjny zespół limfoproliferacyjny Jakie są charakterystyczne
Diagnostyka zakażeń EBV Jakie wyróżniamy główne konsekwencje kliniczne zakażenia EBV: 1) Mononukleoza zakaźna 2) Chłoniak Burkitta 3) Potransplantacyjny zespół limfoproliferacyjny Jakie są charakterystyczne
Epidemiologia raka szyjki
 Epidemiologia raka szyjki W 2004 roku na raka szyjki macicy (kanału łączącego trzon macicy z pochwą) zachorowało blisko 3 500 Polek, a prawie 2 000 zmarło z jego powodu. Wśród wszystkich zachorowań kobiet
Epidemiologia raka szyjki W 2004 roku na raka szyjki macicy (kanału łączącego trzon macicy z pochwą) zachorowało blisko 3 500 Polek, a prawie 2 000 zmarło z jego powodu. Wśród wszystkich zachorowań kobiet
Zakład Zamówień Publicznych przy Ministrze Zdrowia informujemy, iż do siedziby zamawiającego wpłynęły zapytania wykonawców następującej treści :
 Warszawa, dnia 05.09.2012r. Znak: ZZP/ZP/91/692/12 W Y K O N A W C Y Dotyczy: udzielenia zamówienia publicznego w sprawie dostawy testów do badania markerów wirusów przenoszonych drogą krwi tj. testy wirusologiczne
Warszawa, dnia 05.09.2012r. Znak: ZZP/ZP/91/692/12 W Y K O N A W C Y Dotyczy: udzielenia zamówienia publicznego w sprawie dostawy testów do badania markerów wirusów przenoszonych drogą krwi tj. testy wirusologiczne
Nazwa programu: LECZENIE PRZEWLEKŁEGO WZW TYPU B W OPORNOŚCI NA LAMIWUDYNĘ ICD - 10 B 18.1 - przewlekłe zapalenie wątroby typu B
 załącznik nr 25 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE PRZEWLEKŁEGO WZW TYPU B W OPORNOŚCI NA LAMIWUDYNĘ ICD - 10 B 18.1 - przewlekłe zapalenie wątroby
załącznik nr 25 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE PRZEWLEKŁEGO WZW TYPU B W OPORNOŚCI NA LAMIWUDYNĘ ICD - 10 B 18.1 - przewlekłe zapalenie wątroby
Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010
 Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010 1. Leczeniem powinni być objęci chorzy z ostrym, przewlekłym zapaleniem wątroby oraz wyrównaną
Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010 1. Leczeniem powinni być objęci chorzy z ostrym, przewlekłym zapaleniem wątroby oraz wyrównaną
Diagnostyka laboratoryjna zakażeń wirusem zapalenia wątroby typu C Rekomendacje Polskiej Grupy Roboczej 2012/2013
 diagnostyka laboratoryjna Journal of Laboratory Diagnostics 2013 Volume 49 Number 1 65-70 Rekomendacje Recommendations Diagnostyka laboratoryjna zakażeń wirusem zapalenia wątroby typu C Rekomendacje Polskiej
diagnostyka laboratoryjna Journal of Laboratory Diagnostics 2013 Volume 49 Number 1 65-70 Rekomendacje Recommendations Diagnostyka laboratoryjna zakażeń wirusem zapalenia wątroby typu C Rekomendacje Polskiej
SZCZEGÓŁOWY OPIS PRZEDMIOTU OFERTY
 Numer postępowania: NA-ZP-250/07/09/16 Załącznik nr 1 do SIWZ (Pieczęć Wykonawcy) SZCZEGÓŁOWY OPIS PRZEDMIOTU OFERTY A.1 Dostawa jakościowych testów markerów wirusowych przenoszonych drogą krwi tj. testów
Numer postępowania: NA-ZP-250/07/09/16 Załącznik nr 1 do SIWZ (Pieczęć Wykonawcy) SZCZEGÓŁOWY OPIS PRZEDMIOTU OFERTY A.1 Dostawa jakościowych testów markerów wirusowych przenoszonych drogą krwi tj. testów
Pilotażowy Program Profilaktyki Zakażeń HCV. Zakażenia i zachorowania etiologii HCV - epidemiologia i profilaktyka
 Pilotażowy Program Profilaktyki Zakażeń HCV Zakażenia i zachorowania etiologii HCV - epidemiologia i profilaktyka Rozpowszechnienie zakażeń HCV Światowa Organizacja Zdrowia szacuje, że zakażeni HCV stanowią
Pilotażowy Program Profilaktyki Zakażeń HCV Zakażenia i zachorowania etiologii HCV - epidemiologia i profilaktyka Rozpowszechnienie zakażeń HCV Światowa Organizacja Zdrowia szacuje, że zakażeni HCV stanowią
DIAGNOSTYKA Wirusowego Zapalenia Wątroby
 11-08 / 010PL99028A / Ten dokument nie jest prawnie obowiazujacy. biomerieux zastrzega prawa do modyfikacji bez powiadomienia / BIOMERIEUX i jego niebieskie logo, VIDIA, Vironostika, VIDAS sa zarejestrowanymi
11-08 / 010PL99028A / Ten dokument nie jest prawnie obowiazujacy. biomerieux zastrzega prawa do modyfikacji bez powiadomienia / BIOMERIEUX i jego niebieskie logo, VIDIA, Vironostika, VIDAS sa zarejestrowanymi
Częstość zakażeń wirusem HIV w populacji krwiodawców w Polsce w latach 1988 2007
 PRACA ORYGINALNA Journal of Transfusion Medicine 2008, tom 1, nr 1, 20 27 Copyright 2008 Via Medica ISSN 1689 6017 Częstość zakażeń wirusem HIV w populacji krwiodawców w Polsce w latach 1988 2007 Prevalence
PRACA ORYGINALNA Journal of Transfusion Medicine 2008, tom 1, nr 1, 20 27 Copyright 2008 Via Medica ISSN 1689 6017 Częstość zakażeń wirusem HIV w populacji krwiodawców w Polsce w latach 1988 2007 Prevalence
Bezpieczeństwo leczenia krwią i jej składnikami
 PRACA POGLĄDOWA Review Article Acta Haematologica Polonica 2008, 39, Nr 4, str. 677 686 DIONIZA MARCINIAK-BIELAK Bezpieczeństwo leczenia krwią i jej składnikami Safety of blood transfusion Regionalne Centrum
PRACA POGLĄDOWA Review Article Acta Haematologica Polonica 2008, 39, Nr 4, str. 677 686 DIONIZA MARCINIAK-BIELAK Bezpieczeństwo leczenia krwią i jej składnikami Safety of blood transfusion Regionalne Centrum
WYROK z dnia 12 kwietnia 2011 r. Przewodniczący:
 Sygn. akt KIO 646/11 WYROK z dnia 12 kwietnia 2011 r. Krajowa Izba Odwoławcza - w składzie: Przewodniczący: Aneta Mlącka Protokolant: Agata Dziuban po rozpoznaniu na rozprawie w dniu 8 kwietnia 2011 r.
Sygn. akt KIO 646/11 WYROK z dnia 12 kwietnia 2011 r. Krajowa Izba Odwoławcza - w składzie: Przewodniczący: Aneta Mlącka Protokolant: Agata Dziuban po rozpoznaniu na rozprawie w dniu 8 kwietnia 2011 r.
Analiza molekularnych i serologicznych markerów zakażenia HIV u polskich krwiodawców
 ARTYKUŁ ORYGINALNY Journal of Transfusion Medicine 2013, tom 6, nr 1, 1 7 Copyright 2013 Via Medica ISSN 1689 6017 Analiza molekularnych i serologicznych markerów zakażenia HIV u polskich krwiodawców Molecular
ARTYKUŁ ORYGINALNY Journal of Transfusion Medicine 2013, tom 6, nr 1, 1 7 Copyright 2013 Via Medica ISSN 1689 6017 Analiza molekularnych i serologicznych markerów zakażenia HIV u polskich krwiodawców Molecular
Rozszerzona ankieta epidemiologiczna (10.1) Informacja o ankiecie:
 Ankieta 10.4. Ankieta służąca do analizy potencjalnych źródeł zakażenia u dawców niedawno zakażonych HCV, HBV i HIV (dawcy wielokrotni oraz zakażeni w tzw. okienku serologicznym ) opracowana przez Zakład
Ankieta 10.4. Ankieta służąca do analizy potencjalnych źródeł zakażenia u dawców niedawno zakażonych HCV, HBV i HIV (dawcy wielokrotni oraz zakażeni w tzw. okienku serologicznym ) opracowana przez Zakład
REGULAMIN ORGANIZACYJNY. Regionalnego Centrum Krwiodawstwa i Krwiolecznictwa w Lublinie
 REGULAMIN ORGANIZACYJNY Regionalnego Centrum Krwiodawstwa i Krwiolecznictwa w Lublinie ustalony przez Dyrektora Regionalnego Centrum na podstawie: art. 23 i 24 ustawy z dnia 15 kwietnia 2011 r. o działalności
REGULAMIN ORGANIZACYJNY Regionalnego Centrum Krwiodawstwa i Krwiolecznictwa w Lublinie ustalony przez Dyrektora Regionalnego Centrum na podstawie: art. 23 i 24 ustawy z dnia 15 kwietnia 2011 r. o działalności
Diagnostyka laboratoryjna zakażenia parvowirusem B19 u kobiet w ciąży Zalecenia polskiej grupy ekspertów, 2014
 diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab 2015; 51(2): 157-168 Rekomendacje Recommendations Diagnostyka laboratoryjna zakażenia parvowirusem B19 u kobiet w ciąży Zalecenia polskiej
diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab 2015; 51(2): 157-168 Rekomendacje Recommendations Diagnostyka laboratoryjna zakażenia parvowirusem B19 u kobiet w ciąży Zalecenia polskiej
Wirusowe zapalenie wątroby typu C w Polsce, w województwie kujawsko-pomorskim, w krwiodawstwie w latach 2005 2010
 PRACA ORYGINALNA Original Article Acta Haematologica Polonica 2011, 42, Nr 3, str. 541 547 KAMILLA KLEDZIK Wirusowe zapalenie wątroby typu C w Polsce, w województwie kujawsko-pomorskim, w krwiodawstwie
PRACA ORYGINALNA Original Article Acta Haematologica Polonica 2011, 42, Nr 3, str. 541 547 KAMILLA KLEDZIK Wirusowe zapalenie wątroby typu C w Polsce, w województwie kujawsko-pomorskim, w krwiodawstwie
UMOWA ZPU 44/KO/2018
 UMOWA ZPU 44/KO/2018 z dnia...2018 r. zawarta zgodnie z przepisami ustawy o działalności leczniczej pomiędzy: Regionalnym Centrum Krwiodawstwa i Krwiolecznictwa w Opolu z siedzibą przy ul. Kośnego 55,
UMOWA ZPU 44/KO/2018 z dnia...2018 r. zawarta zgodnie z przepisami ustawy o działalności leczniczej pomiędzy: Regionalnym Centrum Krwiodawstwa i Krwiolecznictwa w Opolu z siedzibą przy ul. Kośnego 55,
Załącznik do rozporządzenia Ministra Zdrowia z dnia 18 lutego 2011 r. 21. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU B (ICD-10 B 18.
 ŚWIADCZENIOBIORCY 1. Kryteria Kwalifikacji 1.1. Do programu są kwalifikowani świadczeniobiorcy w wieku powyżej 3 lat, chorzy na przewlekłe wirusowe zapalenie wątroby typu B, charakteryzujący się obecnością
ŚWIADCZENIOBIORCY 1. Kryteria Kwalifikacji 1.1. Do programu są kwalifikowani świadczeniobiorcy w wieku powyżej 3 lat, chorzy na przewlekłe wirusowe zapalenie wątroby typu B, charakteryzujący się obecnością
starszych na półkuli zachodniej. Typową cechą choroby jest heterogenny przebieg
 STRESZCZENIE Przewlekła białaczka limfocytowa (PBL) jest najczęstszą białaczką ludzi starszych na półkuli zachodniej. Typową cechą choroby jest heterogenny przebieg kliniczny, zróżnicowane rokowanie. Etiologia
STRESZCZENIE Przewlekła białaczka limfocytowa (PBL) jest najczęstszą białaczką ludzi starszych na półkuli zachodniej. Typową cechą choroby jest heterogenny przebieg kliniczny, zróżnicowane rokowanie. Etiologia
Ukryte zakażenie wirusem zapalenia wątroby typu B u krwiodawców w Tajlandii
 TŁUMACZENIE Journal of Transfusion Medicine 2011, tom 4, nr 3, 143 154 Copyright 2011 Via Medica ISSN 1689 6017 Ukryte zakażenie wirusem zapalenia wątroby typu B u krwiodawców w Tajlandii Occult hepatitis
TŁUMACZENIE Journal of Transfusion Medicine 2011, tom 4, nr 3, 143 154 Copyright 2011 Via Medica ISSN 1689 6017 Ukryte zakażenie wirusem zapalenia wątroby typu B u krwiodawców w Tajlandii Occult hepatitis
UNIWERSYTET MEDYCZNY IM. KAROLA MARCINKOWSKIEGO W POZNANIU. Andrzej Kaczmarek Centrum Dializ Fresenius Nephrocare Stacja Dializ Nr 1 w Pleszewie
 UNIWERSYTET MEDYCZNY IM. KAROLA MARCINKOWSKIEGO W POZNANIU Andrzej Kaczmarek Centrum Dializ Fresenius Nephrocare Stacja Dializ Nr 1 w Pleszewie Przeciwciała przeciw antygenowi rdzeniowemu wirusa zapalenia
UNIWERSYTET MEDYCZNY IM. KAROLA MARCINKOWSKIEGO W POZNANIU Andrzej Kaczmarek Centrum Dializ Fresenius Nephrocare Stacja Dializ Nr 1 w Pleszewie Przeciwciała przeciw antygenowi rdzeniowemu wirusa zapalenia
Program specjalizacji w TRANSFUZJOLOGII KLINICZNEJ
 CENTRUM MEDYCZNE KSZTAŁCENIA PODYPLOMOWEGO Program specjalizacji w TRANSFUZJOLOGII KLINICZNEJ Warszawa 2000 (c) Copyright by Centrum Medyczne Kształcenia Podyplomowego, Warszawa 2000 Program specjalizacji
CENTRUM MEDYCZNE KSZTAŁCENIA PODYPLOMOWEGO Program specjalizacji w TRANSFUZJOLOGII KLINICZNEJ Warszawa 2000 (c) Copyright by Centrum Medyczne Kształcenia Podyplomowego, Warszawa 2000 Program specjalizacji
STAŻ KIERUNKOWY: CELE I ZADANIA PLACÓWEK PUBLICZNEJ SŁUŻBY KRWI. L.p. Nazwa jednostki Adres Województwo Liczba miejsc Uwagi
 Lista ministra właściwego do spraw zdrowia podmiotów uprawnionych do prowadzenia staży kierunkowych w ramach specjalizacji diagnostów laboratoryjnych w dziedzinie: LABORATORYJNA TRANSFUZJOLOGIA MEDYCZNA
Lista ministra właściwego do spraw zdrowia podmiotów uprawnionych do prowadzenia staży kierunkowych w ramach specjalizacji diagnostów laboratoryjnych w dziedzinie: LABORATORYJNA TRANSFUZJOLOGIA MEDYCZNA
Diagnostyka wirusologiczna w praktyce klinicznej
 Diagnostyka wirusologiczna w praktyce klinicznej Ponad 60% zakażeń w praktyce klinicznej jest wywołana przez wirusy. Rodzaj i jakość materiału diagnostycznego (transport!) oraz interpretacja wyników badań
Diagnostyka wirusologiczna w praktyce klinicznej Ponad 60% zakażeń w praktyce klinicznej jest wywołana przez wirusy. Rodzaj i jakość materiału diagnostycznego (transport!) oraz interpretacja wyników badań
Bankowanie próbek krwi dawców i biorców a podnoszenie bezpieczeństwa przetoczeń krwi
 PRACA POGLĄDOWA Journal of Transfusion Medicine 2011, tom 4, nr 3, 136 142 Copyright 2011 Via Medica ISSN 1689 6017 Bankowanie próbek krwi dawców i biorców a podnoszenie bezpieczeństwa przetoczeń krwi
PRACA POGLĄDOWA Journal of Transfusion Medicine 2011, tom 4, nr 3, 136 142 Copyright 2011 Via Medica ISSN 1689 6017 Bankowanie próbek krwi dawców i biorców a podnoszenie bezpieczeństwa przetoczeń krwi
Pracownia Zgodności Tkankowej / Immunogenetyczna LIiTK UCML UCK
 Pracownia Zgodności Tkankowej / Immunogenetyczna LIiTK UCML UCK Kontakt: Kierownik: dr n. med. Grażyna Moszkowska Tel.: (058) 349-21-89 Fax: (058) 349-21-91 mail: gramos@gumed.edu.pl Laboratorium Immunologii
Pracownia Zgodności Tkankowej / Immunogenetyczna LIiTK UCML UCK Kontakt: Kierownik: dr n. med. Grażyna Moszkowska Tel.: (058) 349-21-89 Fax: (058) 349-21-91 mail: gramos@gumed.edu.pl Laboratorium Immunologii
Oferowana ilość pełnych opakowań. Nr katalogowy. wielkość opakowania
 Załącznik Nr 2.. Nowy PAKIET I ODCZYNNIKI, MATERIAŁY ZUŻYWALNE ORAZ KONTROLE DO PRACOWNI SEROLOGII TRANSFUZJOLOGICZNEJ DO OZNACZEŃ IMMUNOTRANSFUZJOLOGICZNYCH Z WYKORZYSTANIEM MIKROMETODY ŻELOWEJ OPARTEJ
Załącznik Nr 2.. Nowy PAKIET I ODCZYNNIKI, MATERIAŁY ZUŻYWALNE ORAZ KONTROLE DO PRACOWNI SEROLOGII TRANSFUZJOLOGICZNEJ DO OZNACZEŃ IMMUNOTRANSFUZJOLOGICZNYCH Z WYKORZYSTANIEM MIKROMETODY ŻELOWEJ OPARTEJ
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 2 października 201 r. Poz. 118 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 23 października 201 r. w sprawie wymagań zdrowotnych dla kandydata na dawcę
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 2 października 201 r. Poz. 118 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 23 października 201 r. w sprawie wymagań zdrowotnych dla kandydata na dawcę
Diagnostyka laboratoryjna zakażeń wirusem zapalenia wątroby typu C
 Diagnostyka laboratoryjna zakażeń wirusem zapalenia wątroby typu C Wydanie II Rekomendacje Grupy Roboczej: Krajowa Izba Diagnostów Laboratoryjnych 2, Narodowy Instytut Zdrowia Publicznego Państwowy Zakład
Diagnostyka laboratoryjna zakażeń wirusem zapalenia wątroby typu C Wydanie II Rekomendacje Grupy Roboczej: Krajowa Izba Diagnostów Laboratoryjnych 2, Narodowy Instytut Zdrowia Publicznego Państwowy Zakład
ul. Stanisława Dubois 5A Warszawa tel.: fax:
 1 e-krew co to jest? e-krew to realizowany przez Centrum Systemów Informacyjnych Ochrony Zdrowia projekt budowy systemu informatycznego, odpowiadający na potrzeby: dawców i kandydatów na dawców krwi, podmiotów
1 e-krew co to jest? e-krew to realizowany przez Centrum Systemów Informacyjnych Ochrony Zdrowia projekt budowy systemu informatycznego, odpowiadający na potrzeby: dawców i kandydatów na dawców krwi, podmiotów
Promotor: prof. dr hab. Katarzyna Bogunia-Kubik Promotor pomocniczy: dr inż. Agnieszka Chrobak
 INSTYTUT IMMUNOLOGII I TERAPII DOŚWIADCZALNEJ IM. LUDWIKA HIRSZFELDA WE WROCŁAWIU POLSKA AKADEMIA NAUK mgr Milena Iwaszko Rola polimorfizmu receptorów z rodziny CD94/NKG2 oraz cząsteczki HLA-E w patogenezie
INSTYTUT IMMUNOLOGII I TERAPII DOŚWIADCZALNEJ IM. LUDWIKA HIRSZFELDA WE WROCŁAWIU POLSKA AKADEMIA NAUK mgr Milena Iwaszko Rola polimorfizmu receptorów z rodziny CD94/NKG2 oraz cząsteczki HLA-E w patogenezie
ZAŁĄCZNIKI ZAŁĄCZNIK Nr 1 KRYTERIA KWALIFIKOWANIA DAWCÓW DO ODDAWANIA KRWI PEŁNEJ I JEJ SKŁADNIKÓW
 ROZPORZĄDZENIE MINISTRA ZDROWIA z dnia 18 kwietnia 2005 r. w sprawie warunków pobierania krwi od kandydatów na dawców krwi i dawców krwi (Dz. U. z dnia 9 maja 2005 r.) Na podstawie art. 16 ustawy z dnia
ROZPORZĄDZENIE MINISTRA ZDROWIA z dnia 18 kwietnia 2005 r. w sprawie warunków pobierania krwi od kandydatów na dawców krwi i dawców krwi (Dz. U. z dnia 9 maja 2005 r.) Na podstawie art. 16 ustawy z dnia
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 kwietnia 2005 r. w sprawie warunków pobierania krwi od kandydatów na dawców krwi i dawców krwi
 Dz.U.05.79.691 2007.11.15 zm. Dz.U.07.212.1568 1 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 kwietnia 2005 r. w sprawie warunków pobierania krwi od kandydatów na dawców krwi i dawców krwi (Dz. U. z dnia
Dz.U.05.79.691 2007.11.15 zm. Dz.U.07.212.1568 1 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 kwietnia 2005 r. w sprawie warunków pobierania krwi od kandydatów na dawców krwi i dawców krwi (Dz. U. z dnia
REGULAMIN PORZĄDKOWY ( WYPIS )
 REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA im. dr Konrada Vietha W RADOMIU 26-612 Radom ul. B. Limanowskiego 42 REGULAMIN PORZĄDKOWY ( WYPIS ) DROGA DAWCY W RCKiK RADOM - SCHEMAT Gabinet Lekarski
REGIONALNE CENTRUM KRWIODAWSTWA I KRWIOLECZNICTWA im. dr Konrada Vietha W RADOMIU 26-612 Radom ul. B. Limanowskiego 42 REGULAMIN PORZĄDKOWY ( WYPIS ) DROGA DAWCY W RCKiK RADOM - SCHEMAT Gabinet Lekarski
Terapeutyczne Programy Zdrowotne 2008 Zapobieganie krwawieniom u dzieci z hemofilią A i B.
 załącznik nr 5 do zarządzenia 45/2008/DGL z dnia 7 lipca 2008 r. załącznik nr 33 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z
załącznik nr 5 do zarządzenia 45/2008/DGL z dnia 7 lipca 2008 r. załącznik nr 33 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z
Epigenes jedyne źródło wiedzy o polskich pacjentach zakażonych HBV
 Epigenes jedyne źródło wiedzy o polskich pacjentach zakażonych HBV Jerzy Jaroszewicz, Małgorzata Pawłowska, Anna Piekarska, Krzysztof Tomasiewicz, Krzysztof Simon, Włodzimierz Mazur, Dorota Zarębska- Michaluk,
Epigenes jedyne źródło wiedzy o polskich pacjentach zakażonych HBV Jerzy Jaroszewicz, Małgorzata Pawłowska, Anna Piekarska, Krzysztof Tomasiewicz, Krzysztof Simon, Włodzimierz Mazur, Dorota Zarębska- Michaluk,
Pracownia Diagnostyki Molekularnej. kierownik dr n. med. Janusz Stańczak. tel. (22) tel. (22)
 kierownik dr n. med. Janusz Stańczak tel. (22) 33 55 261 tel. (22) 33 55 278 e-mail jstanczak@zakazny.pl 1 / 6 1. Struktura Pracownia Diagnostyki Molekularnej (PDM) zawiera trzy działy: Mikrobiologii Klinicznej,
kierownik dr n. med. Janusz Stańczak tel. (22) 33 55 261 tel. (22) 33 55 278 e-mail jstanczak@zakazny.pl 1 / 6 1. Struktura Pracownia Diagnostyki Molekularnej (PDM) zawiera trzy działy: Mikrobiologii Klinicznej,
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na podstawie art. 31d ustawy z dnia 27 sierpnia 2004 r. o
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na podstawie art. 31d ustawy z dnia 27 sierpnia 2004 r. o
WYROK. z dnia 2 grudnia 2013 r. Protokolant: Rafał Komoń
 WYROK z dnia 2 grudnia 2013 r. Krajowa Izba Odwoławcza w składzie: Przewodniczący: Piotr Kozłowski Protokolant: Rafał Komoń po rozpoznaniu na rozprawie w dniu 2 grudnia 2013 r. w Warszawie odwołania wniesionego
WYROK z dnia 2 grudnia 2013 r. Krajowa Izba Odwoławcza w składzie: Przewodniczący: Piotr Kozłowski Protokolant: Rafał Komoń po rozpoznaniu na rozprawie w dniu 2 grudnia 2013 r. w Warszawie odwołania wniesionego
Wykaz pojęć i skrótów
 Wykaz pojęć i skrótów CKiK RCKiK KKCz KKP KPK FFP NAT HBV HCV VNRD Centra Krwiodawstwa i Krwiolecznictwa: Regionalne Centra Krwiodawstwa, Wojskowe Centrum Krwiodawstwa i Krwiolecznictwa oraz Centrum Krwiodawstwa
Wykaz pojęć i skrótów CKiK RCKiK KKCz KKP KPK FFP NAT HBV HCV VNRD Centra Krwiodawstwa i Krwiolecznictwa: Regionalne Centra Krwiodawstwa, Wojskowe Centrum Krwiodawstwa i Krwiolecznictwa oraz Centrum Krwiodawstwa
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 kwietnia 2005 r. w sprawie warunków pobierania krwi od kandydatów na dawców krwi i dawców krwi
 Dz.U.05.79.691 2007-11-15 zm. Dz.U.2007.212.1568 1 2010-02-02 zm. Dz.U.2010.7.50 1 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 kwietnia 2005 r. w sprawie warunków pobierania krwi od kandydatów na dawców
Dz.U.05.79.691 2007-11-15 zm. Dz.U.2007.212.1568 1 2010-02-02 zm. Dz.U.2010.7.50 1 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 kwietnia 2005 r. w sprawie warunków pobierania krwi od kandydatów na dawców
SZCZEGÓŁOWE WARUNKI KONKURSU OFERT NA UDZIELENIE ZAMÓWIENIA NA UDZIELANIE ŚWIADCZEŃ ZDROWOTNYCH zwane dalej SWK
 SZCZEGÓŁOWE WARUNKI KONKURSU OFERT NA UDZIELENIE ZAMÓWIENIA NA UDZIELANIE ŚWIADCZEŃ ZDROWOTNYCH zwane dalej SWK Spis treści I. INFORMACJE OGÓLNE... 2 II. SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA... 2 III.
SZCZEGÓŁOWE WARUNKI KONKURSU OFERT NA UDZIELENIE ZAMÓWIENIA NA UDZIELANIE ŚWIADCZEŃ ZDROWOTNYCH zwane dalej SWK Spis treści I. INFORMACJE OGÓLNE... 2 II. SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA... 2 III.
Rekomendacje PGE HBV 2017 a obowiązujący program lekowy
 Rekomendacje PGE HBV 2017 a obowiązujący program lekowy Robert Flisiak Klinika Chorób Zakaźnych i Hepatologii Uniwersytetu Medycznego w Białymstoku Forum Wirusologiczne, Łódź 20-21 kwietnia 2018 Wartość
Rekomendacje PGE HBV 2017 a obowiązujący program lekowy Robert Flisiak Klinika Chorób Zakaźnych i Hepatologii Uniwersytetu Medycznego w Białymstoku Forum Wirusologiczne, Łódź 20-21 kwietnia 2018 Wartość
Personalizacja leczenia w hematoonkologii dziecięcej
 MedTrends 2016 Europejskie Forum Nowoczesnej Ochrony Zdrowia Zabrze, 18-19 marca 2016 r. Personalizacja leczenia w hematoonkologii dziecięcej Prof. dr hab. n. med. Tomasz Szczepański Katedra i Klinika
MedTrends 2016 Europejskie Forum Nowoczesnej Ochrony Zdrowia Zabrze, 18-19 marca 2016 r. Personalizacja leczenia w hematoonkologii dziecięcej Prof. dr hab. n. med. Tomasz Szczepański Katedra i Klinika
Rozporządzenie Ministra Zdrowia w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania krwi i jej składników 1)
 Rozporządzenie Ministra Zdrowia w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania krwi i jej ) z dnia 6 maja 207 r. (Dz.U. z 207 r. poz. 026) Na podstawie art. 2 ust. 7 ustawy z dnia
Rozporządzenie Ministra Zdrowia w sprawie szkolenia pielęgniarek i położnych dokonujących przetaczania krwi i jej ) z dnia 6 maja 207 r. (Dz.U. z 207 r. poz. 026) Na podstawie art. 2 ust. 7 ustawy z dnia
Kryteria kwalifikowania dawców do oddawania krwi pełnej i jej składników
 Załączniki do rozporządzenia Ministra Zdrowia z dnia 18 kwietnia 2005 r. Załącznik nr 1 Kryteria kwalifikowania dawców do oddawania krwi pełnej i jej składników 1. Kryteria dopuszczenia dawców do oddawania
Załączniki do rozporządzenia Ministra Zdrowia z dnia 18 kwietnia 2005 r. Załącznik nr 1 Kryteria kwalifikowania dawców do oddawania krwi pełnej i jej składników 1. Kryteria dopuszczenia dawców do oddawania
z dnia 6 maja 2011 r. Przewodniczący:
 Sygn. akt KIO 847/11 WYROK z dnia 6 maja 2011 r. Krajowa Izba Odwoławcza - w składzie: Przewodniczący: Renata Tubisz Protokolant: Łukasz Listkiewicz po rozpoznaniu na rozprawie w dniu 6 maja 2011r. odwołania
Sygn. akt KIO 847/11 WYROK z dnia 6 maja 2011 r. Krajowa Izba Odwoławcza - w składzie: Przewodniczący: Renata Tubisz Protokolant: Łukasz Listkiewicz po rozpoznaniu na rozprawie w dniu 6 maja 2011r. odwołania
WIRUSOWE ZAPALENIA WĄTROBY Marta Wróblewska Katedra i Zakład Mikrobiologii Lekarskiej, Warszawski Uniwersytet Medyczny
 WIRUSOWE ZAPALENIA WĄTROBY Marta Wróblewska Katedra i Zakład Mikrobiologii Lekarskiej, Warszawski Uniwersytet Medyczny WIRUSY ZAPALENIA WĄTROBY Pierwotnie hepatotropowe: HAV, HBV, HCV, HDV, HEV, HGV Inne
WIRUSOWE ZAPALENIA WĄTROBY Marta Wróblewska Katedra i Zakład Mikrobiologii Lekarskiej, Warszawski Uniwersytet Medyczny WIRUSY ZAPALENIA WĄTROBY Pierwotnie hepatotropowe: HAV, HBV, HCV, HDV, HEV, HGV Inne
