ANALIZA WPŁYWU NA BUDŻET INTERFERON BETA-1A I.M. (AVONEX ) W TERAPII RZUTOWO-REMISYJNEJ POSTACI STWARDNIENIA ROZSIANEGO
|
|
|
- Nadzieja Świderska
- 9 lat temu
- Przeglądów:
Transkrypt
1 ANALIZA WPŁYWU NA BUDŻET INTERFERON BETA-1A I.M. (AVONEX ) W TERAPII RZUTOWO-REMISYJNEJ POSTACI STWARDNIENIA ROZSIANEGO Wersja 1.0 Kraków kwiecień 2014
2 HTA Consulting spółka z ograniczoną odpowiedzialnością spółka komandytowa ul. Starowiślna 17/ Kraków Tel.: +48 (0) ; Faks: +48 (0) Projekt zakończono 27 stycznia 2014 roku Uzupełnienie projektu: 7 kwietnia 2014 Zgodnie z procedurami firmy HTA Consulting analizę poddano wewnętrznej kontroli jakości w następujących obszarach: Kontrola obliczeń: Kontrola merytoryczna: Powielanie tego dokumentu w całości, w częściach jak również wykorzystywanie całości tekstu lub jego fragmentów wymaga zgody właściciela praw majątkowych oraz podania źródła. Analiza została sfinansowana i przeprowadzona na zlecenie: Biogen Idec Poland Sp. z o.o. ul. Prusa Warszawa Zamawiającego reprezentował: Cezary Głogowski Head of Public Affairs HTA Consulting 2014 ( Strona 2
3 SPIS TREŚCI INDEKS SKRÓTÓW... 5 STRESZCZENIE WPROWADZENIE Cel Problem zdrowotny Stan aktualny Technologia oceniana Interwencje alternatywne Kwalifikacja do grupy limitowej METODYKA I DANE ŹRÓDŁOWE Sposób przeprowadzenia analizy Forma analizy Perspektywa analizy Horyzont czasowy analizy Populacja zgodna ze wskazaniem rejestracyjnym Populacja docelowa Zużycie leków Koszty Analiza wrażliwości WYNIKI Scenariusz istniejący Populacja i zużycie leków Scenariusz nowy Populacja i zużycie leków Wydatki inkrementalne HTA Consulting 2014 ( Strona 3
4 4. ANALIZA WRAŻLIWOŚCI ANALIZA WPŁYWU NA SYSTEM OCHRONY ZDROWIA Wpływ na organizację udzielania świadczeń zdrowotnych Aspekty etyczne i społeczne PODSUMOWANIE I WNIOSKI OGRANICZENIA DYSKUSJA BIBLIOGRAFIA SPIS TABEL ZGODNOŚĆ Z MINIMALNYMI WYMAGANIAMI ANEKS Epidemiologia stwardnienia rozsianego Chorobowość Zapadalność Umieralność Ograniczenia w dostępie do świadczeń kolejki HTA Consulting 2014 ( Strona 4
5 INDEKS SKRÓTÓW AOTM ChPL DDD DOT EDSS IFNB i.m. MRI NICE NFZ RRSM Agencja Oceny Technologii Medycznych w Polsce Charakterystyka Produktu Leczniczego Zdefiniowana dawka dobowa (Defined Daily Dose) Dzień leczenia (Day od treatment) Rozszerzona Skala Niepełnosprawności Ruchowej Kurtzkego (Expanded disability status scale) Interferon beta Wstrzyknięcie domięśniowe Rezonans magnetyczny (Magnetic resonance imaging) Brytyjska agencja oceny technologii medycznych (National Institute for Clinical Excellence) Narodowy Fundusz Zdrowia Rzutowo-remisyjna postać stwardnienia rozisanego (Relapsing-Remittinf Multiple Sclerosis) s.c. SM WHO Wstrzyknięcie podskórne Stwardnienie rozsiane (Sclerosis multiplex) Światowa Organizacja Zdrowia (World Health Organization) HTA Consulting 2014 ( Strona 5
6 STRESZCZENIE Cel Celem analizy wpływu na budżet jest prognoza wydatków płatnika publicznego (Narodowego Funduszu Zdrowia) związanych z finansowaniem leków immunomodulujących, w szczególności interferonu beta-1a i.m. (preparatu Avonex ), w programie leczenia stwardnienia rozsianego w przypadku całkowitego zniesienia administracyjnego ograniczenia czasu trwania leczenia w tym programie. Obecnie czas leczenia jest ograniczony maksymalnie do 60 miesięcy (5 lat), także w przypadku pacjentów odpowiadających na leczenie. Metodyka Analiza wpływu na budżet została przeprowadzona z perspektywy podmiotu zobowiązanego do finansowania świadczeń ze środków publicznych (NFZ) w 3-letnim horyzoncie czasowym ( ). Analizę opracowano przy założeniu, że zniesienie ograniczeń administracyjnych dla leków w programie leczenia stwardnienia rozsianego obowiązywać będzie począwszy od 1 stycznia 2014 roku i będzie to jedyna zmiana względem aktualnie obowiązującego programu Leczenie stwardnienia rozsianego, w szczególności zachowane zostaną kryteria włączenia/wyłączenia z programu. Rozważono dwa scenariusze analizy: istniejący, w którym interferony beta i octan glatirameru dostępne są w programie leczenia stwardnienia rozsianego na obecnych zasadach, oraz nowy, w którym czas leczenia w programie lekowym nie jest administracyjnie ograniczany (pacjenci korzystają z terapii tak długo, jak długo odnoszą korzyści z leczenia). Wyznaczono ponadto wydatki inkrementalne określające wpływ na budżet rozważanej zmiany programu lekowego. W oparciu o dane Narodowego Funduszu Zdrowia określono liczebność populacji leczonej interferonem beta i octanem glatirameru w ramach programu lekowego. W celu wyznaczenia liczby pacjentów leczonych w programie lekowym w kolejnych latach wykorzystano dane o dynamice realizacji programu lekowego/terapeutycznego programu zdrowotnego w ubiegłych latach. W latach programem objęto ok osób każdego roku, Prognozę sprzedaży i wydatków związanych z realizacją programu leczenia stwardnienia rozsianego w najbliższych latach oparto na danych ze sprawozdań NFZ i komunikatów NFZ. HTA Consulting 2014 ( Strona 6
7 Wyniki analizy obejmują całkowite koszty związane z realizacją programu lekowego, tj. koszty leków ponoszone w ramach budżetu na refundację, a także koszty diagnostyki i monitorowania leczenia. Wyniki Liczba refundowanych rocznych terapii Liczba rocznych terapii SM (pacjento-lata) w scenariuszu istniejącym określona została na poziomie. W przypadku zniesienia ograniczenia czasu leczenia w rozważanym programie lekowym dla pacjentów ze stwardnieniem rozsianym liczbę pacjento-lat oszacowano na W scenariuszu istniejącym liczba pełnych rocznych terapii realizowanych z zastosowaniem interferonu beta-1a i.m. oszacowana została na terapii w kolejnych latach prognozy, a w scenariuszu nowym na w kolejnych latach prognozy. Wpływ na budżet Wydatki płatnika publicznego na terapie immunomodulujące w ramach programu leczenia stwardnienia rozsianego w scenariuszu istniejącym, przy utrzymaniu obowiązujących ograniczeń maksymalnego czasu leczenia, oszacowano na w 2014 roku, w 2015 roku i w 2016 roku, tych kosztów stanowią wydatki na refundację leków. W tych kwotach odpowiednio w 2014 roku, w 2015 roku i w 2016 roku stanowią wydatki na interferon beta-1a i.m. Wydatki płatnika publicznego na terapie immunomodulujące w ramach programów leczenia stwardnienia rozsianego w scenariuszu nowym, przy zniesieniu ograniczenia maksymalnego czasu leczenia w programie, oszacowano na w 2014 roku, w 2015 roku w 2016 roku, tych kosztów stanowią wydatki na refundację leków. W tych kwotach odpowiednio w 2014 roku, 2015 roku i w 2016 roku stanowią wydatki na interferon beta-1a i.m.. Zniesienie ograniczenia długości leczenia w ramach programu Leczenie stwardnienia rozsianego spowoduje wzrost całkowitych kosztów związanych z realizacją tego programu o w 2014 roku, w 2015 roku i w 2016 roku. Wzrost kosztów w ramach budżetu na refundację wyniesie w 2014 roku, w 2015 roku i w 2016 roku. HTA Consulting 2014 ( Strona 7
8 Wzrost kosztów refundacji interferonu beta-1a i.m. wyniesie w 2014 roku, w 2015 roku i w 2016 roku. Wnioski Wyniki analizy wskazują, że zniesienie ograniczenia czasu trwania terapii w rozważanym programie lekowym Rezygnacja ze sztucznie ustanowionego limitu czasu leczenia pozwoli jednak na kontunuowanie terapii u pacjentów, którzy odnoszą z niej korzyści. Efektywne leczenie pozwoli zwiększyć sprawność ruchową pacjentów ze stwardnieniem rozsianym i powstrzymać lub spowolnić postęp choroby i umożliwi chorym czynne życie i pracę zawodową. Przez zmniejszenie postępu niepełnosprawności pacjenci będą mogli realizować szerszy zakres funkcji społecznych. Umożliwienie aktywności zawodowej osobom ze stwardnieniem rozsianym lub ich bliskim, którzy w przypadku postępu niepełnosprawności musieliby ograniczyć swoją aktywność na rzecz opieki nad chorymi, zmniejszy ponadto koszty społeczne choroby. Ze względów etycznych i społecznych należy rozważyć zniesienie sztucznie ustanowionych ograniczeń w czasie trwania terapii. HTA Consulting 2014 ( Strona 8
9 1. WPROWADZENIE 1.1. Cel Celem analizy wpływu na budżet jest prognoza wydatków płatnika publicznego (Narodowego Funduszu Zdrowia) związanych z finansowaniem leków immunomodulujących, w szczególności interferonu beta-1a i.m. (preparatu Avonex ), w programie leczenia stwardnienia rozsianego w przypadku całkowitego zniesienia administracyjnego ograniczenia czasu trwania leczenia w tym programie. Obecnie czas leczenia jest ograniczony maksymalnie do 60 miesięcy (5 lat), także w przypadku pacjentów odpowiadających na leczenie Problem zdrowotny Stwardnienie rozsiane (sclerosis multiplex, SM) jest przewlekłym schorzeniem ośrodkowego układu nerwowego o nieznanej etiologii, charakteryzującym się postępującym i/lub nawrotowym przebiegiem związanym z występowaniem rozsianych ognisk demielinizacji (tzw. demielinizacja pierwotna) w ośrodkowym układzie nerwowym (OUN). [1] Demielinizacja jest patologicznym procesem polegającym na uszkodzeniu i rozpadzie osłonek mielinowych włókien nerwowych, powodującym powstawanie w OUN zmian ogniskowych nazywanych plakami. Może mieć charakter pierwotny lub wtórny. Demielinizacja pierwotna, o nieustalonym jednoznacznie patomechanizmie, nie powoduje zmian w samej komórce nerwowej, natomiast upośledza funkcję przewodzenia impulsów nerwowych, co w rezultacie powoduje powstanie objawów ubytkowych. Z kolei demielinizacja wtórna, wynikająca z działania na tkankę nerwową czynników toksycznych, niedokrwienia lub zapalenia, prowadzi zarówno do uszkodzenia osłonki mielinowej, jak i całego neuronu, oraz powstania odczynu zapalnego w tkance otaczającej. [1] Stwardnienie rozsiane jest najczęstszą przyczyną nieurazowej niepełnosprawności w grupie młodych dorosłych. Szacuje się, że na świecie choruje około 9 mln osób, z czego tylko u 3 mln choroba jest rozpoznana. Zachorowalność na stwardnienie rozsiane stale wzrasta. [1] Analogicznie do większości chorób autoimmunologicznych, SM częściej dotyczy kobiet. Ocenia się, iż stanowią one około 75 80% chorych, a częstość zachorowania w stosunku do mężczyzn wzrasta wraz z wiekiem. Najwyższa zachorowalność dotyczy osób w 3 5 dekadzie życia, choć mogą się zdarzać zachorowania wśród dzieci i młodzieży, jak również u osób w wieku podeszłym. Około 3 18% wszystkich przypadków stwardnienia rozsianego rozpoznawanych jest poniżej 18 roku życia, w tym przedziale wiekowym stwierdza się również wzrost zachorowalności dziewczynek w stosunku do chłopców wraz z wiekiem (tj. zbliżaniem się do wieku pokwitania). [1] HTA Consulting 2014 ( Strona 9
10 Według danych epidemiologicznych chorobowość SM charakteryzuje również nierównomierny rozkład w zależności od rasy oraz lokalizacji geograficznej dominuje rasa biała i strefy klimatu chłodnego do umiarkowanego. Największą częstość (30 60 na mieszkańców) występowania notuje się w krajach środkowej i północnej Europy, północnej części USA oraz południowej części Kanady. Z kolei w krajach tropikalnych czy Japonii chorobowość wynosi 1/ mieszkańców. Stwierdza się ponadto ogniska epidemiczne zachorowań na SM, tj. obszary, na których współczynnik chorobowości wynosi kilkukrotnie więcej niż na terenach przyległych, osiągając poziom 258/ (m.in.: w Finlandii, Danii, we Włoszech, Chorwacji, Francji, Kanadzie, USA oraz na Orkadach i Szetlandach). Pod względem chorobowości na SM Polska znajduje się w grupie krajów wysokiego ryzyka. Szczegółowa analiza danych epidemiologicznych dla Polski przeprowadzona została w rozdziale Stan aktualny Terapia stwardnienia rozsianego z wykorzystaniem leków modyfikujących przebieg choroby jest w Polsce finansowana w ramach dwóch programów lekowych (PL): Leczenie stwardnienia rozsianego oraz Leczenie stwardnienia rozsianego po niepowodzeniu terapii lekami pierwszego rzutu lub szybko rozwijającej się ciężkiej postaci stwardnienia rozsianego [2]. W ramach PL Leczenie stwardnienia rozsianego po niepowodzeniu terapii lekami pierwszego rzutu lub szybko rozwijającej się ciężkiej postaci stwardnienia rozsianego finansowane są: fingolimod oraz natalizumab. [2] PL Leczenie stwardnienia rozsianego obejmuje finansowanie interferonu beta-1a, interferonu beta- 1b oraz octanu glatirameru. [2] Kryteria kwalifikacji do terapii interferonami beta w ramach PL obejmują [2]: wiek od 12. roku życia; rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach diagnostycznych McDonalda (Polman 2005 [3]); włącznie z badaniami rezonansem magnetycznym, przed i po kontraście; uzyskanie co najmniej 15 punktów według punktowego systemu kwalifikacji określonego w programie (Tabela 1); pisemna deklaracja współpracy przy realizacji programu ze strony pielęgniarki podstawowej opieki zdrowotnej obejmującej opieką świadczeniobiorcę. Kryteria kwalifikacji do terapii octanem glatirameru są takie same jak dla terapii interferonami beta. Oceny skuteczności leczenia dokonuje się co 12 miesięcy. Brak skuteczności określa się jako wystąpienie jednej z sytuacji: 2 lub więcej rzutów umiarkowanych lub 1 ciężki rzut po 6 miesiącach terapii, HTA Consulting 2014 ( Strona 10
11 progresja choroby mimo leczenia (wzrost EDSS o 2 punkty, gdy EDSS <4 lub wzrost o 1 punkt gdy EDSS 4), zmiany w badaniu rezonansu magnetycznego (więcej niż jedna nowa zmiana Gd(+), więcej niż dwie nowe zmiany w sekwencji T2), przejście RRSM do SPSM, więcej niż 6 punktów w skali EDSS. [2] Schemat dawkowania leków w ramach programu lekowego jest zgodny z zapisami charakterystyk produktów leczniczych (ChPL). Leczenie w ramach opisywanego programu trwa do 24 miesięcy z możliwością przedłużenia maksymalnie do 60 miesięcy. Po każdym roku leczenia dokonuje się oceny skuteczności terapii, a w razie stwierdzenia jej braku następuje zmiana leczenia. Warunkiem przedłużenia terapii powyżej 2 lat jest brak rzutów lub rzuty łagodne, lub 1 rzut umiarkowany lub brak progresji choroby w okresie ostatniego roku leczenia, brak wyraźnych cech aktywności i progresji choroby w badaniu kontrastowym wykonanym rezonansem magnetycznym z gadoliną. [2] Tabela 1. Punktowy system kwalifikacji do leczenia interferonem beta Kryterium Wartość punktowa 0 3 lata 6 Czas trwania choroby 3 6 lat lat 2 Powyżej 10 lat 1 Postać choroby Rzutowa bez objawów ubytkowych Liczba rzutów w ostatnim roku Brak Stan neurologiczny w okresie międzyrzutowym (przy rozpoczynaniu leczenia) w skali EDSS 2, ,5 5 2 Powyżej 5 1 Program Leczenie stwardnienia rozsianego obowiązuje w obecnym kształcie od 2013 roku, kiedy to rozszerzono zakres refundacyjny dla octanu glatirameru o wszystkich pacjentów leczonych I linią terapii (wcześniej refundowany był tylko w przypadku przeciwwskazań do interferonu beta). Długość terapii w ramach obowiązującego programu ograniczona jest do maksymalnie 5 lat. Okres ten został wydłużony z 3 do 5 lat w 2012 roku. W niniejszej analizie rozważa się zniesienie administracyjnego ograniczenia czasu długości terapii w ramach programu Leczenie stwardnienia rozsianego (dot. interferonów beta i octanu glatirameru). HTA Consulting 2014 ( Strona 11
12 W 2011 roku programem leczenia stwardnienia rozsianego w Polsce objętych było niecałe 5 tys. osób (świadczenia w programie rozliczono u pacjentów, a wydanie substancji czynnych u osób) [4]. Wartość substancji czynnych wydanych w ramach tego programu w roku 2011 wyniosła 127 mln zł i odpowiadała pełnym rocznym terapiom (pacjento-lata). Liczba osób, objętych leczeniem w ramach programu była wyższa niż liczba pacjento-lat ze względu na fakt, że u części pacjentów terapia realizowana była tylko przez część roku kalendarzowego (liczba pacjentów wyższa o ok niż liczba pacjento-lat). Program obowiązujący w 2011 różnił się od obecnego w zakresie maksymalnego czasy terapii (3 lata) oraz częściowo kryteriami kwalifikacji dot. wieku pacjenta (większe szanse uzyskania zgody na terapię mieli pacjenci młodsi). W roku 2012 zarówno liczba pacjento-lat terapii, jak i wartość świadczeń związanych z refundacją leków immunomodulujących, była znacznie wyższa niż w roku Wynikało to zarówno ze zmiany zakresu refundacji (wydłużenie dopuszczalnego czasu leczenia bez konieczności ponownej kwalifikacji, zniesienie ograniczeń wiekowych), jak i z dynamiki włączania pacjentów do programu Wpływ na wartość udzielonych świadczeń miała również zmiana sposobu rozliczania preparatów immunomodulujących (wprowadzenie programu lekowego w miejsce terapeutycznego programu zdrowotnego). W 2013 roku nastąpiła kolejna zmiana w programie lekowym polegająca na umożliwieniu zastosowania octanu glatirameru w I linii terapii (nie tylko u pacjentów z przeciwwskazaniami do interferonu beta). W roku tym nastąpiło też realne wydłużenie czasu leczenia pacjentów w programie (ze względu na dynamikę wprowadzania zmian w programie lekowym/terapeutycznym dopiero w tym roku leczenie mogło być po raz pierwszy przeprowadzone pacjentów powyżej 48. miesiąca terapii). Raportowane przez NFZ w roku 2011 i 2012 roku oraz prognozowane na rok 2013 zużycie terapii immunomodulujących i wartość refundacji przedstawione zostało w poniższej tabeli (Tabela 2). Tabela 2. Wartość i zużycie świadczeń terapie immunomodulujące finansowane przez NFZ stan aktualny b Wartość świadczeń [mln zł] 127,0 142,8 Roczne terapie a) na podstawie wartości i ilości rozliczonych świadczeń; b) prognoza HTA Consulting 2014 ( Strona 12
13 1.4. Technologia oceniana Interferon beta-1a (L03AB07) [1] Postać farmaceutyczna Proszek do przygotowania roztworu do wstrzyknięć domięśniowych (30 µg substancji czynnej co jest równe 6 milionów j.m.) lub gotowy roztwór do wstrzyknięć domięśniowych 30 µg / 0,5 ml (6 milionów j.m. / 0,5 ml). [1] Dawkowanie i schemat leczenia Rzutowo-remisyjna postać stwardnienia rozsianego (RRSM) u pacjentów powyżej 12. i poniżej 65. roku życia: 30 µg interferonu raz w tygodniu, w iniekcjach domięśniowych; zwiększenie dawki nie daje dodatkowych korzyści klinicznych. U osób powyżej 65 roku życia w oparciu o aktualne wyniki badań klinicznych nie stwierdzono podstaw do modyfikacji wielkości dawki i schematu leczenia. Ze względu na brak badań dla dzieci poniżej 12 roku życia, nie należy stosować leku w tej populacji. Miejsce wstrzyknięcia domięśniowego należy zmieniać co tydzień. Aktualnie brak jest danych o optymalnym czasie stosowania leczenia w związku z tym zaleca się podjęcie decyzji o kontynuacji/zaprzestaniu leczenia w oparciu o badanie kliniczne po dwóch latach stosowania leczenia. Przez 1 dobę przed i po podaniu interferonu, w celu zmniejszenia objawów grypopodobnych, zaleca się stosowanie leków przeciwgorączkowych i przeciwbólowych. [1] Wskazania do stosowania Rzutowo-remisyjna postać SM tj. dwa lub więcej rzutów choroby w okresie ostatnich trzech lat bez oznak postępu choroby między nawrotami. Wystąpienie pojedynczego ogniska demielinizacji z czynnym procesem zapalnym, którego ciężkość kwalifikuje pacjenta do leczenia podawanymi dożylnie kortykosteroidami; jednocześnie zostały wykluczone alternatywne rozpoznania i istnieje duże ryzyko rozwoju klinicznie jawnego stwardnienia rozsianego. [1] Działania niepożądane Do najczęściej obserwowanych działań niepożądanych zalicza się: objawy grypopodobne, bezpośrednio po podaniu, przejściowe objawy sugerujące nasilenie choroby podstawowej, przejściowe wzmożenie napięcia mięśniowego i/lub ciężkie osłabienie mięśniowe uniemożliwiające HTA Consulting 2014 ( Strona 13
14 wykonywanie ruchów dowolnych, objawy ze strony przewodu pokarmowego (nudności, wymioty, biegunka, utrata apetytu). [1] 1.5. Interwencje alternatywne W warunkach polskich alternatywą dla zastosowania interferonu beta-1a i.m. są wszystkie pozostałe preparaty stosowane obecnie w ramach programu lekowego dla stwardnienia rozsianego: interferon beta-1a s.c. (preparat Rebif), interferon beta-1b s.c. (preparaty Betaferon i Extavia), octan glatirameru (preparat Copaxone) Kwalifikacja do grupy limitowej Interferon beta-1a i.m. (preparat Avonex) jest obecnie finansowany ze środków publicznych w ramach programu lekowego Leczenie stwardnienia rozsianego. Refundowany jest jedno opakowanie tego leku (EAN ) o zawartości 4 ampułko-strzykawek zawierających po 30 mcg substancji czynnej. Lek ten jest finansowany w ramach odrębnej grupy limitowej , Interferonum beta 1a a 30 mcg. W grupie ten znajduje się wyłącznie jeden produkt, a limit finansowania wyznaczony jest przez cenę hurtową tego leku. W ramach niniejszej analizy rozważa się wyłącznie zmianę zakresu refundacji interferonu beta-1a i.m., tj. zniesienie administracyjnego ograniczenia długości terapii w programie lekowym. W ramach analizy rozważa się utrzymanie obecnych zasad finansowania leku. Wnioskowana zmiana w programie lekowym nie ma wpływu na kwalifikację leku do grupy limitowej. HTA Consulting 2014 ( Strona 14
15 2. METODYKA I DANE ŹRÓDŁOWE 2.1. Sposób przeprowadzenia analizy Analizę wpływu na budżet przeprowadzono w następujący sposób: 1. Zdefiniowano populację docelową zgodnie z projektem programu lekowego. Oszacowano liczebność populacji docelowej i przeprowadzono prognozę na kolejne lata horyzontu czasowego analizy. 2. Obliczono przewidywane wydatki płatnika w latach w przypadku utrzymania scenariusza istniejącego, czyli w przypadku utrzymania administracyjnego ograniczenia długości terapii. 3. Obliczono przewidywane wydatki płatnika w latach w scenariuszu nowym, czyli w przypadku zniesienia administracyjnego ograniczenia długości terapii. 4. Wyznaczono wydatki inkrementalne, czyli różnicę w wydatkach pomiędzy scenariuszem nowym a scenariuszem istniejącym. Jeżeli wydatki inkrementalne przyjmują wartości ujemne, oznaczają oszczędności dla płatnika, w przeciwnym razie oznaczają dodatkowe koszty. 5. Przeprowadzono analizę wrażliwości dla zmiennych, które w największym stopniu wpływają na wyniki analizy wpływu na budżet oraz takich, których oszacowanie charakteryzuje się największą niepewnością Forma analizy Analiza wpływu na budżet składa się z dwóch części niniejszego dokumentu oraz arkusza kalkulacyjnego wykonanego w programie MS Excel 2007, umożliwiającego obliczenie prognozowanych wydatków płatnika w zależności od przyjętych założeń. Arkusz kalkulacyjny umożliwia również przeprowadzenie jednokierunkowych i wielokierunkowych analiz wrażliwości Perspektywa analizy Analizę przeprowadzono z perspektywy podmiotu zobowiązanego do finansowania świadczeń ze środków publicznych Narodowego Funduszu Zdrowia (NFZ). Leki uwzględnione w analizie (interferony beta, octan glatirameru) finansowane są w ramach programu lekowego i, zgodnie z zasadami refundacji, pacjenci nie partycypują w kosztach terapii. HTA Consulting 2014 ( Strona 15
16 2.4. Horyzont czasowy analizy Analizę przeprowadzono w 3-letnim horyzoncie czasowym, przy założeniu, że administracyjne ograniczenie długości terapii zostanie zniesione z dniem 1 stycznia 2014 roku. Horyzont ten obejmuje zgodny z ustawą refundacyjną [5] okres obowiązywania drugiej decyzji refundacyjnej, tj. 2 lata. Analizę opracowano przy założeniu, że zasady i poziom finansowania interferonów beta i octanu glatirameru pozostaną niezmienione w okresie, którego dotyczy prognoza. Zgodnie z wytycznymi Agencji Oceny Technologii Medycznych (AOTM), horyzont czasowy analizy wpływu na budżet powinien obejmować okres do momentu ustalenia się stanu równowagi lub co najmniej w ciągu 2 lat od wprowadzenia nowej technologii [6]. Rozważana w analizie strategia refundacyjna stanowi rozszerzenie strategii realizowanej obecnie i nie wiąże się z finansowaniem dodatkowych technologii. Ze względu na wieloletnią realizację programu dla pacjentów ze stwardnieniem rozsianym można oceniać, że stan równowagi w analizowanym sektorze jest już ustalony. Zniesienie ograniczenia czasu trwania terapii nie powinno wpłynąć na zmianę tej równowagi, pacjenci bowiem najprawdopodobniej będą kontynuować aktualnie prowadzone leczenie. Dynamika zużycia leków wiązać się będzie zatem wyłącznie z przedłużeniem czasu pozostawania pacjentów w programie. Okres 3 lat wydaje się być wystarczający dla oceny skali wzrostu wydatków płatnika publicznego wynikającego ze zmian w programie. Należy mieć jednak na uwadze, że stan ustabilizowania się liczby pacjentów w programie osiągnięty może być dopiero w znacznie dłuższym horyzoncie czasowym (kilkanaście lat), tj. w okresie, w którym liczba nowych pacjentów kwalifikowanych do programu i pochodna zapadalności zrównoważy się z liczbą pacjentów przerywających leczenie w kolejnych latach terapii. Argumentem dla ograniczenia prognozy do 3-letniego horyzontu, jest szczególna i niezależna od błędu prognoz niepewność wyników określanych w dłuższym horyzoncie. Ograniczona wiarygodność obliczeń dla odległego horyzontu czasowego jest nieusuwalnym elementem każdej prognozy wydatków przeznaczonych na refundację, jednak w przypadku analizowanego problemu zdrowotnego zwiększać ją mogą dodatkowe i specyficzne da rozważanego zagadnienia czynniki. Znaczna dynamika kształtu programów leczenia stwardnienia rozsianego w ubiegłych latach (stopniowe wydłużanie dostępu do terapii i rozszerzanie kryteriów kwalifikacji) jest głównym czynnikiem, który wpływa na zużycie terapii immunomodulujących w Polsce. W przypadku kontynuacji w najbliższych latach realizowanej dotychczas linii zmian, prognozy dla horyzontu dłuższego niż 3 lata nie byłyby wiarygodne Populacja zgodna ze wskazaniem rejestracyjnym Populacja w której zgodnie ze wskazaniem rejestracyjnym może być zastosowany interferon beta-1a obejmuje dorosłych chorych z rzutowo-remisyjną postacią stwardnienia rozsianego. HTA Consulting 2014 ( Strona 16
17 Zgodnie z oszacowaniami ekspertów, liczba osób jakie mogłyby stosować leczenie immunomodulujące wynosi w Polsce tysięcy chorych [7]. Liczba ta jest blisko czterokrotnie wyższa niż liczba pacjentów leczonych w ramach programu w ciągu roku kalendarzowego: osób w 2009 roku, osób w 2010, osób w 2011 oraz osób w 2012 roku [4, 8, 9] Tabela 3. Tabela 3. Liczba pacjentów biorących udział w programie lekowym dla stwardnienia rozsianego w latach Liczba pacjentów biorących udział w programie lekowym W tym: interferon beta-1a (30 µg) bd bd W przypadku rozważanej interwencji, tj. zmiany w istniejącym programie lekowym polegającej na wydłużeniu czasu leczenia pacjentów zakwalifikowanych do leczenia w programie, oszacowania populacji docelowej, rozumianej jako pacjenci, którzy mogliby stosować leczenie immunomodulujące, ma relatywnie niewielkie znaczenie. W ciągu najbliższych lat żaden pacjent, który nie został uprzednio zakwalifikowany do programu lekowego w obowiązującym obecnie kształcie nie będzie również mógł korzystać z przedłużonej terapii lekami immunomodulującymi. Ponadto również w sytuacji, gdyby odsetek pacjentów ze stwardnieniem rozsianym, u których rozpoczynane będzie leczenie w programie lekowym wzrósł w kolejnych latach (np. przez ograniczenie czasu oczekiwania na kwalifikację lub zmianę kryteriów kwalifikacji do programu) dodatkowi pacjenci objęci terapią będą mogli korzystać z leczenia przedłużonego, którego dotyczy analiza, dopiero w latach następnych (powyżej przyjętego horyzontu analizy). W żadnej sytuacji kwestia rozpowszechnienia leczenia immunomodulującego wśród pacjentów z SM nie ma więc wpływu na koszty różniące porównywanych scenariuszy (istniejącego z ograniczeniem czasu leczenia do 5 lat i nowego, bez ograniczenia dla długości terapii) Populacja docelowa Populację docelową dla rozważanej strategii refundacyjnej stanowią pacjenci spełniający kryteria kwalifikacji do programu lekowego Leczenie stwardnienia rozsianego, zgodnie z obowiązującym kształtem tego programu [2]. HTA Consulting 2014 ( Strona 17
18 Liczbę pacjento-lat w scenariuszu istniejącym (I linia terapii w programie lekowym), przy utrzymaniu ograniczenia maksymalnego czasu terapii do 5 lat, oszacowano na podstawie historycznych danych NFZ na (Tabela 4). W roku 2011 liczba pacjentów objętych (w dowolnym zakresie) leczeniem immunomodulującym była o ok. wyższa niż liczba pełnych rocznych kursów terapii, natomiast w roku 2012 liczba ta była o większa niż liczba pełnych terapii (por. rozdział 1.3). Pacjento-lata interpretować można natomiast jako średnią liczbę pacjentów leczonych aktywnie w programie w dowolnym momencie roku kalendarzowego. Liczbę rocznych terapii w scenariuszu nowym (I linia terapii w programie lekowym), przy zniesieniu ograniczenia maksymalnego czasu leczenia w programie, oszacowano na (Tabela 4). Wzrost liczby terapii względem scenariusza istniejącego wynosi Tabela 4. Populacja docelowa liczba rocznych kursów terapii w I linii leczenia stwardnienia rozsianego w programie lekowym Scenariusz istniejący Scenariusz nowy W analizie przyjęto, że w populacji docelowej zarówno w scenariuszu istniejącym jak i nowym pacjentów leczonych interferonami beta stosować będzie interferon beta-1a i.m. (na podstawie rozpowszechnienia leku w roku 2013) Tabela 5. Przyjęty stały odsetek jest poparty analizą trendu, która wykazała brak tendencji wzrostowej lub spadkowej w okresie od kwietnia 2011 do sierpnia Tabela 5. Populacja docelowa liczba rocznych kursów terapii interferonem beta-1a i.m. w programie lekowym Scenariusz istniejący Scenariusz nowy HTA Consulting 2014 ( Strona 18
19 Szczegóły dotyczące obliczeń liczby rocznych terapii przedstawiono w kolejnym rozdziale (rozdział 2.7) Zużycie leków Dane historyczne Zużycie substancji w programach dedykowanych terapii stwardnienia rozsianego oszacowano na podstawie komunikatów Departamentu Gospodarki Lekami NFZ za okres od stycznia 2011 do sierpnia 2013 [10] oraz sprawozdań NFZ za lata [11 14]. W latach dane nie były raportowane tak szczegółowo jak od 2011 roku, dostępne informacje dot. kosztów refundacji substancji stosowanych w programach obejmują m.in. całkowitą roczną kwotę refundacji interferonu beta-1a (za lata 2008, 2009 i 2010) oraz całkowitą roczną kwotę refundacji interferonu beta-1b (za lata 2008 i 2009). Wartość refundacji raportowaną przez NFZ i skojarzoną z nią liczbę świadczeń (jednostek wydanej substancji czynnej) przedstawiono w tabelach poniżej (Tabela 6, Tabela 7). Tabela 6. Koszty refundacji substancji czynnych stosowanych w programach leczenia SM w latach Substancja Interferon beta 1a Dawka a 22 µg Dawka a 44 µg Dawka a 30 µg Refundacja w tys. zł Interferon beta 1b Octan glatirameru HTA Consulting 2014 ( Strona 19
20 Tabela 7. Zużycie substancji czynnych stosowanych w programach leczenia SM w roku 2011 Substancja Zużycie w jednostkach naturalnych w 2011 Interferon beta 1a Interferon beta 1b Octan glatirameru Dawka a 22 µg Dawka a 44 µg Dawka a 30 µg 25 mg mg 894 mg mg mg W celu oszacowania zużycia leków w latach wykorzystane zostały informacje publikowane przez NFZ w comiesięcznych komunikach Departamentu Gospodarki Lekami. Na podstawie zawartości opakowań leków immunomodulujących refundowanych zgodnie z obwieszczeniem Ministra Zdrowia z 23 grudnia 2013 roku [2] oraz dawkowania i sposobu podawania tych leków opisanych w charakterystykach produktów leczniczych [15 19] obliczono liczbę dni terapii przypadających na jedno opakowanie danego leku (DOT day of treatment, Tabela 8). Tabela 8. Oszacowanie liczby dni terapii (DOT) przypadającej na jedno opakowanie Lek Zawartość opakowania Dawkowanie DOT / opakowanie Octan glatirameru (Copaxone) 28 amp.-strz. (4 blist. a 7 amp.-strz. a 1 ml) 1x / doba 28 Interferon beta 1a i.m. (Avonex) 4 amp.-strz. (+ 4 igły) 1x / tydzień 28 Interferon beta 1a s.c. (Rebif) 12 amp.-strz. a 0,5 ml 3x / tydzień 28 Interferon beta 1b s.c. (Betaferon) 15 zest. 1x / 2dni 30 Interferon beta 1b s.c. (Extavia) 15 fiol. (+15 a.-strz. rozp. a 1,2 ml) 1x / 2dni 30 W oparciu o informacje o dawkowaniu oraz o dane o zużyciu świadczeń refundowanych w poszczególnych okresach (styczeń 2011 sierpień 2013) oszacowana została liczba pełnych kursów terapii (pacjento-lat) realizowanych w poszczególnych latach. latach przedstawiono w kolejnej tabeli (Tabela 9). Oszacowane w ten sposób zużycie terapii immunomodulujących w HTA Consulting 2014 ( Strona 20
21 W analizie uwzględniono także octan glatirameru, jako że jest on refundowany w ramach tego samego programu lekowego co interferony beta. W 2013 zmieniono zakres refundacji tego leku umożliwiając stosowanie go w I linii terapii. Tabela 9. Zużycie interferonu beta w programie leczenia stwardnienia rozsianego w latach Interferon beta liczba pełnych rocznych kursów terapii Lek a a) Dane rzeczywiste za okres od stycznia do sierpnia i prognoza na okres od września do grudnia Prognoza Standardy leczenia stwardnienia rozsianego w ramach terapii refundowanej przez płatnika publicznego zmieniały się wielokrotnie w okresie, dla którego dostępne są dane o zużyciu poszczególnych preparatów. Najważniejsze zmiany obejmowały przedłużenie możliwego czasu leczenia w programie bez konieczności kolejnej kwalifikacji z 2 do 3 lat w roku 2009 i z 3 do 5 lat w roku 2012 [20], a także wycofanie z programu octanu glatirameru (w roku 2008) i ponowne włączenie go do refundacji z ograniczeniem jego stosowania jako terapii drugiej linii lub u osób z przeciwwskazaniami do interferonu beta (w roku 2009) [21, 22]. W przypadku refundacji interferonów kluczowe znaczenie mają przede wszystkim zmiany dotyczące wydłużenia czasu leczenia w programie lekowym. Reguły ponownej kwalifikacji pacjentów do leczenia w ramach programu są dosyć ogólne [23 25], ponadto powtórna kwalifikacja pacjentów była ograniczana kryteriami włączenia, w których pacjenci z dłuższym czasem choroby i bardziej zaawansowanym wiekiem (kryterium zlikwidowane w roku 2012 [20]) mieli mniej punktów, niż pacjenci, którzy po raz pierwszy starają się o kwalifikację do terapii. Czynniki te sprawiają, że liczba pacjentów obejmowanych leczeniem jest ściśle zależna od czasu trwania podstawowej terapii, jaki określony został przez płatnika publicznego. HTA Consulting 2014 ( Strona 21
22 Tabela 10. Zużycie leków w scenariuszu istniejącym przy utrzymaniu maksymalnego czasu terapii (5 lat) Scenariusz istniejący liczba rocznych terapii interferonem beta Scenariusz istniejący liczba rocznych terapii octanem glatirameru Scenariusz istniejący liczba rocznych terapii W prognozie zużycia interferonów w przypadku wydłużenia czasu leczenia w programie wykorzystano dane HTA Consulting 2014 ( Strona 22
23 Oszacowanie liczby rocznych terapii w przypadku zniesienia ograniczenia czasu terapii przedstawiono w poniższej tabeli (Tabela 11). Tabela 11. Zużycie leków w scenariuszu nowym przy zniesieniu ograniczenia maksymalnego czasu terapii Scenariusz istniejący liczba rocznych terapii interferonem beta Scenariusz istniejący liczba rocznych terapii octanem glatirameru Scenariusz nowy liczba rocznych terapii Koszty W analizie uwzględniono wyłącznie bezpośrednie koszty medyczne. Ograniczono się do kosztów związanych z prowadzeniem i realizacją rozważanego programu lekowego: kosztów leków, kosztów diagnostyki i podania leków. HTA Consulting 2014 ( Strona 23
24 Koszty leków Cenę interferonu beta-1a i.m. (Avonex) uzyskano od Zamawiającego (Tabela 12). Jedno opakowanie produktu Avonex (EAN: ) zawiera 4 ampułko-strzykawki z 1 ml roztworu do wstrzyknięcia domięśniowego. W każdym ml znajduje się 30 µg substancji czynnej (interferonu beta- 1a). Jedno opakowanie (4 dawki) wystarcza na czterotygodniową terapię. Proponowana cena zbytu netto za opakowanie wynosi cena hurtowa brutto przy uwzględnieniu marży hurtowej w wysokości 5% wyniesie Tabela 12. Cena interferonu beta-1a i.m. Nazwa handlowa Substancja czynna Dawka Opakowanie Avonex Interferon beta 30 µg 4 amp.-strz. (+ 4 igły) ł ł a) VAT = 8% Ceny jednostkowe pozostałych aktualnie refundowanych substancji ustalone na podstawie rozporządzenia obwieszczenia Ministra Zdrowia z 23 grudnia 2013 roku [2], obowiązujące w styczniulutym 2014, przedstawiono w kolejnej tabeli (Tabela 13). Przyjęte w analizie ceny są zgodne z cenami wprowadzonymi w obwieszczeniu Ministra Zdrowia obowiązującym od 1 marca 2014 r. [26] Tabela 13. Ceny aktualnie refundowanych preparatów zawierających interferon beta lub octan glatirameru (styczeń 2014) Nazwa handlowa Substancja czynna Dawka Opakowanie Urzędowa cena zbytu Cena hurtowa brutto a Rebif Interferonum beta 1a s.c. 44 µg 12 amp.-strz. a 0,5 ml 4 086,72 zł 4 291,06 zł Betaferon Interferonum beta 1b s.c. 250 µg 15 zest ,48 zł 3 210,35 zł Extavia Interferonum beta 1b s.c. 250 µg Copaxone Glatirameri acetas 20 mg a) VAT = 8%; marża hurtowa = 5% 15 fiol. (+15 a.-strz. rozp. a 1,2 ml) 28 amp.-strz. (4 blist. a 7 amp.-strz. a 1 ml) 2 862,00 zł 3 005,10 zł 3 780,00 zł 3 969,00 zł HTA Consulting 2014 ( Strona 24
25 Diagnostyka i koszty podania leku Zgodnie z Zarządzeniem Prezesa NFZ z 10 maja 2012 z późniejszymi zmianami [27] diagnostyka pacjentów leczonych w ramach programu leczenia stwardnienia rozsianego rozliczana jest na podstawie rocznej opłaty ryczałtowej (Tabela 14). Tabela 14. Diagnostyka w programie leczenia stwardnienia rozsianego Świadczenia Wycena punktowa Cena punktu rozliczeniowego Roczny ryczałt za diagnostykę Diagnostyka w programie leczenia stwardnienia rozsianego zł W analizie przyjęto, że ryczałt ten jest rozliczany proporcjonalnie do czasu leczenia pacjenta w programie. W obliczeniach uwzględniono ponadto koszty związane z podawaniem leku (Tabela 15). Przyjęto, że wszystkie aktualnie dostępne preparaty wydawane lub podawane są pacjentom w ramach porady ambulatoryjnej i że w ramach jednej porady pacjent otrzymuje jedno opakowanie leku. Tabela 15. Koszt podania leków w programie leczenia stwardnienia rozsianego Kod Nazwa Wycena punktowa Cena punktu rozliczeniowego Koszt jednorazowy Przyjęcie pacjenta w trybie ambulatoryjnym związane z wykonaniem programu zł HTA Consulting 2014 ( Strona 25
26 2.10. Analiza wrażliwości W analizie wrażliwości przedstawiono w jakim zakresie mogą się zmieniać inkrementalne wydatki płatnika, jeśli zmianie podlegać będą następujące parametry (przy pozostałych parametrach ustalonych na poziomie wartości z podstawowej analizy): Prognoza wzrostu zużycia leków immunomodulujących w scenariuszu istniejącym +/- 10%; Prognoza wzrostu zużycia leków immunomodulujących w scenariuszu nowym +/- 10%. HTA Consulting 2014 ( Strona 26
27 3. WYNIKI W rozdziale przedstawione zostały wyniki analizy wpływu na budżet płatnika w scenariuszu istniejącym i nowym, wyznaczone przy podstawowych założeniach analizy. Wszystkie szczegółowe wyniki dostępne są w skoroszycie obliczeniowym Scenariusz istniejący Populacja i zużycie leków Zużycie preparatów immunomodulujących w terapii stwardnienia rozsianego realizowanej w ramach programu lekowego Leczenie stwardnienia rozsianego, przy zachowaniu administracyjnego ograniczenia długości leczenia do maksymalnie 5 lat, oszacowano na rocznych terapii w 2014 roku do ok rocznych terapii w 2016 roku. W tych wartościach rocznych terapii to leczenie z zastosowaniem interferonu beta-1a i.m. (Tabela 16). W scenariuszu istniejącym liczba pełnych rocznych terapii realizowanych z zastosowaniem interferonu beta-1a i.m. oszacowana została na od terapii w kolejnych latach prognozy a w scenariuszu nowym na w kolejnych latach prognozy. Tabela 16. Prognozowana liczba terapii I linii leczenia SM scenariusz istniejący Interferon beta-1a Interferon beta 1b Octan glatirameru Razem Lek W tym: interferon beta-1a i.m. HTA Consulting 2014 ( Strona 27
28 ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł HTA Consulting 2014 ( Strona 28
29 3.2. Scenariusz nowy Populacja i zużycie leków Zużycie preparatów immunomodulujących w terapii stwardnienia rozsianego realizowanej w ramach programu lekowego Leczenie stwardnienia rozsianego, przy zniesieniu ograniczenia długości leczenia, oszacowano na od rocznych terapii w 2014 roku do rocznych terapii w 2016 roku. W tych wartościach rocznych terapii to leczenie z zastosowaniem interferonu beta- 1a i.m. (Tabela 19). Tabela 19. Prognozowana liczba terapii I linii leczenia SM scenariusz nowy Interferon beta 1a Interferon beta 1b Octan glatirameru Razem Lek W tym: interferon beta-1a i.m. HTA Consulting 2014 ( Strona 29
30 ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł HTA Consulting 2014 ( Strona 30
31 3.3. Wydatki inkrementalne W analizie przewiduje się znaczący wzrost wydatków płatnika na leczenie immunomodulujące w ramach programu lekowego leczenia stwardnienia rozsianego w przypadku zniesienia ograniczenia czasu leczenia w tym programie. ł ł ł ł ł ł ł ł ł ł ł ł ł HTA Consulting 2014 ( Strona 31
32 ł ł ł ł ł ł ł ł ł ł ł ł ł HTA Consulting 2014 ( Strona 32
33 4. ANALIZA WRAŻLIWOŚCI Dane uwzględnione w analizie wpływu na budżet mogą podlegać zmianom w zależności od różnych czynników i okoliczności, których nie sposób na obecnym etapie przewidzieć. Dynamicznie zmienia się system refundacji substancji stosowanych w programach terapeutycznych/lekowych a poziom wydatków NFZ regulowany jest zarówno dostępnymi publicznie aktami prawnymi, jak i niepublikowanymi umowami podziału ryzyka pomiędzy NFZ i producentami leków. Skala wydatków ze środków publicznych zależy również od dostępności świadczeń gwarantowanych zarówno w scenariuszu zachowania aktualnego zakresu refundacji, jak i w scenariuszu z brakiem systemowych ograniczeń czasu trwania leczenia w programie lekowym. Podjęta w opracowaniu próba oceny zakresu niepewności uzyskiwanych wyników służy uzupełnieniu głównych rezultatów analizy o zakres zmienności wynikający z możliwych realizacji poszczególnych parametrów. W analizie wrażliwości przedstawiono, w jakim zakresie mogą się zmieniać inkrementalne wydatki płatnika, jeśli zmianie podlegać będą następujące parametry (przy pozostałych parametrach ustalonych na poziomie wartości z podstawowej analizy): Prognoza wzrostu zużycia leków immunomodulujących w scenariuszu istniejącym +/- 10% wariant A analizy wrażliwości Prognoza wzrostu zużycia leków immunomodulujących w scenariuszu nowym +/- 10% - wariant B analizy wrażliwości Zestawienie parametrów podlegających zmianom w jednokierunkowej analizie wrażliwości przedstawione zostało w tabeli poniżej (Tabela 24). Wyniki inkrementalne dla poszczególnych wariantów obliczeń (wydatki inkrementalne na substancje czynne, diagnostykę i podanie leku oraz pozostałe koszty terapii) przedstawiono w kolejnej tabeli (Tabela 25). Tabela 24. Opis wariantów analizy wrażliwości Parametr Wariant Opis wariantu analizy wrażliwości Wzrost zużycia leków immunomodulujących w scenariuszu istniejącym Rok Wariant A0 Wariant A1 Wariant A2 Rok Wzrost zużycia leków immunomodulujących w scenariuszu nowym Wariant B0 Wariant B1 Wariant B2 HTA Consulting 2014 ( Strona 33
34 Tabela 25. Wyniki jednokierunkowej analizy wrażliwości Perspektywa Wszystkie leki w PL Interferon beta-1a i.m. Wariant ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł ł Szczegółowe wyniki analiz wrażliwości dostępne są w arkuszu kalkulacyjnym BIA po ustawieniu odpowiednich opcji analizy. Największy wpływ na wyniki ma dynamika wzrostu zużycia w scenariuszu nowym. Zwiększenie lub zmniejszenie stopy wzrostu zużycia leków immunomodulujących o 10% implikuje, że wydatki inkrementalne w kolejnych latach są odpowiednio wyższe/niższe niż wydatki określone w scenariuszu podstawowym o HTA Consulting 2014 ( Strona 34
35 5. ANALIZA WPŁYWU NA SYSTEM OCHRONY ZDROWIA 5.1. Wpływ na organizację udzielania świadczeń zdrowotnych Zniesienie ograniczenia czasu trwania terapii w programie Leczenia stwardnienia rozsianego polegać będzie na modyfikacji istniejącego programu lekowego. Wydłużenie czasu leczenia w programie, przy zapewnieniu środków finansowych na odpowiednim poziomie, zwiększy liczbę pacjentów biorących udział w programie. Przyczyni się to do zwiększenia zapotrzebowania na pozostałe świadczenia realizowane w ramach programu m.in. badania kontrolne związane z oceną skuteczności leczenia. W ujęciu wartościowym wzrost ten został oszacowany w ramach niniejszej analizy. Na podstawie danych o efektywności leku można oczekiwać, że przedłużenie terapii u pacjentów odpowiadających na leczenia ponad 60 miesięcy zmniejszy częstość rzutów i pozwoli na redukcję progresji choroby i niepełnosprawności u pacjentów, którzy otrzymają tę terapię. Czynniki te powinny mieć korzystny wpływ na liczbę świadczeń realizowanych w związku z terapią stwardnienia rozsianego w kolejnych latach Aspekty etyczne i społeczne W tabeli poniżej przestawiona została ocena poszczególnych aspektów z zakresu etycznych i społecznych konsekwencji zniesienia ograniczenia czasu terapii w programie w analizowanym wskazaniu. Tabela 26. Podsumowanie wyników analizy aspektów etycznych i społecznych decyzji polegającej zniesieniu ograniczenia czasu trwania terapii w programie lekowym leczenia stwardnienia rozsianego Aspekt Ocena Ocena wpływu pozytywnej decyzji refundacyjnej w świetle wyników analizy kosztów efektywności Czy koszty efektywności różnią się w poszczególnych podgrupach? Grupy pacjentów, które mogą być faworyzowane na skutek założeń przyjętych w analizie ekonomicznej Nie zidentyfikowano podgrup w analizie efektywności klinicznej. Nie zidentyfikowano. Ocena wpływu pozytywnej decyzji refundacyjnej w świetle aspektów społecznych Zapewnienie równości dostępu pacjentów o zbliżonych potrzebach do badanej technologii Zaspakajanie niezaspokojonych dotychczas potrzeb grup społecznie upośledzonych Dostęp do programu lekowego może być zagrożony wyłącznie w przypadku niedostatecznego zakontraktowania świadczeń w programie. Już w chwili obecnej na realizację świadczeń w ramach programu oczekuje liczba chorych odpowiadająca 20% populacji leczonej. Usunięcia ograniczenia czasu leczenia w programie będzie stanowić ważny krok w celu zaspokojenia potrzeb pacjentów, dla których terapia z zastosowaniem HTA Consulting 2014 ( Strona 35
36 Aspekt Odpowiedź na potrzeby osób o największych potrzebach zdrowotnych, dla których nie ma obecnie dostępnej żadnej metody leczenia Zgodność z aktualnie obowiązującymi regulacjami prawnymi Wpływ na prawa pacjenta lub prawa człowieka Ocena interferonu beta i octanu glatirameru przynosi korzyści. Przedłużenie czasu aktywnego leczenia pozwoli im na realizację w szerszym zakresie funkcji społecznych i wpłynie korzystnie na koszty z perspektywy społecznej. Funkcjonujące sztuczne ograniczenie dostępu do leczenia ma na celu wyłącznie ograniczenie wydatków płatnika publicznego i nie jest w żadnym zakresie podparte wiedzą medyczną. Finansowanie technologii jest zgodne z obowiązującym prawem, wymagać będzie modyfikacji istniejącego programu lekowego. Korzystny wpływ na prawa pacjenta. Zgodnie z Ustawą o prawach pacjenta i Rzeczniku Prawa Pacjenta pacjent ma prawo do świadczeń zdrowotnych odpowiadających wymaganiom aktualnej wiedzy medycznej. Ograniczenie czasu leczenia do 5 lat jest administracyjnym przepisem nie mającym żadnego odzwierciedlenia w wytycznych leczenia i zaleceniach w tym zakresie. Należy wręcz ocenić, że ograniczanie czasu terapii w ten sposób łamie podstawowe prawa pacjenta. Ocena wpływu pozytywnej decyzji refundacyjnej w świetle aspektów etycznych Wpływ na poziom satysfakcji pacjentów z otrzymywanej opieki medycznej Ryzyko niezaakceptowania terapii przez poszczególnych chorych Możliwość stygmatyzacji chorych Możliwość wywoływania lęku Możliwość powodowania dylematów moralnych Możliwość stwarzania problemów dotyczących płci lub rodzinnych. Konieczność szczególnego informowania lub uzyskiwania zgody pacjenta na podanie leku Potrzeba zapewnienia pacjentowi niekrępujących warunków lub poufności przy podaniu leku Potrzeba czynnego udziału pacjenta w podejmowaniu decyzji o wyborze terapii Potrzeba uwzględniania indywidualnych preferencji pacjenta przy wyborze terapii Wprowadzenie tej metody terapeutycznej z dużym prawdopodobieństwem zwiększy satysfakcję pacjentów z otrzymywanej opieki medycznej. Celem programu lekowego jest poprawa sprawności ruchowej, powstrzymanie postępu choroby i zapobieganie wystąpieniu lub pogłębianiu się inwalidztwa uniemożliwiającego czynne życie i pracę zawodową. Zbliżona do obecnie stosowanych metod terapii. Zbliżona do obecnie stosowanych metod terapii. Zbliżona do obecnie stosowanych metod terapii. Zbliżona do obecnie stosowanych metod terapii. Zbliżona do obecnie stosowanych metod terapii. Zbliżona do obecnie stosowanych metod. Identyczna jak dla obecnie stosowanych metod. Identyczna jak dla obecnie stosowanych metod. Identyczna jak dla obecnie stosowanych metod. HTA Consulting 2014 ( Strona 36
37 6. PODSUMOWANIE I WNIOSKI Liczba refundowanych rocznych terapii Liczba rocznych terapii SM (pacjento-lata) w scenariuszu istniejącym określona została na poziomie od w roku 2014 do w roku W przypadku zniesienia ograniczenia czasu leczenia w rozważanym programie lekowym dla pacjentów ze stwardnieniem rozsianym liczbę pacjento-lat oszacowano na od w roku 2014 do w roku W scenariuszu istniejącym liczba pełnych rocznych terapii realizowanych z zastosowaniem interferonu beta-1a i.m. oszacowana została na od do terapii w kolejnych latach prognozy, a w scenariuszu nowym na w kolejnych latach prognozy. HTA Consulting 2014 ( Strona 37
FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ
 FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ Prof. dr hab. med. Halina Bartosik - Psujek Katedra i Klinika Neurologii Uniwersytet Medyczny w Lublinie LEKI I RZUTU PREPARATY INTERFERONU
FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ Prof. dr hab. med. Halina Bartosik - Psujek Katedra i Klinika Neurologii Uniwersytet Medyczny w Lublinie LEKI I RZUTU PREPARATY INTERFERONU
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r.
 Dziennik Ustaw Nr 269 15687 Poz. 1597 1597 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na
Dziennik Ustaw Nr 269 15687 Poz. 1597 1597 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
Terapeutyczne Programy Zdrowotne 2009 Leczenie stwardnienia rozsianego
 Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia Załącznik nr 9 do Zarządzenia Nr 16/2009 Prezesa NFZ z dnia 10 marca 2009 roku I. Cel
Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia Załącznik nr 9 do Zarządzenia Nr 16/2009 Prezesa NFZ z dnia 10 marca 2009 roku I. Cel
Terapeutyczne Programy Zdrowotne 2012 Leczenie stwardnienia rozsianego
 Załącznik nr 15 do zarządzenia nr 59/2011/DGL Prezesa NFZ Załącznik nr 6 do zarządzenia nr 10/2012/DGL Prezesa NFZ z dnia 15 lutego 2012 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35
Załącznik nr 15 do zarządzenia nr 59/2011/DGL Prezesa NFZ Załącznik nr 6 do zarządzenia nr 10/2012/DGL Prezesa NFZ z dnia 15 lutego 2012 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35
Leczenie stwardnienia rozsianego w Polsce. Jak poprawić sytuację polskich pacjentów? Izabela Obarska Warszawa,
 Leczenie stwardnienia rozsianego w Polsce. Jak poprawić sytuację polskich pacjentów? Izabela Obarska Warszawa, 18.04.2019 Epidemiologia Polska znajduje się w pierwszej dziesiątce krajów o największym wskaźniku
Leczenie stwardnienia rozsianego w Polsce. Jak poprawić sytuację polskich pacjentów? Izabela Obarska Warszawa, 18.04.2019 Epidemiologia Polska znajduje się w pierwszej dziesiątce krajów o największym wskaźniku
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Terapeutyczne Programy Zdrowotne 2008 Leczenie stwardnienia rozsianego
 załącznik nr 16 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia I.
załącznik nr 16 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia I.
DEFERAZYROKS W LECZENIU PRZEWLEKŁEGO OBCIĄŻENIA ŻELAZEM W WYNIKU TRANSFUZJI KRWI U DOROSŁYCH
 DEFERAZYROKS W LECZENIU PRZEWLEKŁEGO OBCIĄŻENIA ŻELAZEM W WYNIKU TRANSFUZJI KRWI U DOROSŁYCH ANALIZA WPŁYWU NA SYSTEM OCHRONY ZDROWIA Wersja 1.1 Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/33 02-516 Warszawa
DEFERAZYROKS W LECZENIU PRZEWLEKŁEGO OBCIĄŻENIA ŻELAZEM W WYNIKU TRANSFUZJI KRWI U DOROSŁYCH ANALIZA WPŁYWU NA SYSTEM OCHRONY ZDROWIA Wersja 1.1 Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/33 02-516 Warszawa
PROPOZYCJE ZMIAN W PROGRAMIE II LINII. Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK
 PROPOZYCJE ZMIAN W PROGRAMIE II LINII Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK PROGRAM II LINII P R O B L E M Y Z G Ł A S Z A N E W 2 0 1 7 r o k u Brak możliwości
PROPOZYCJE ZMIAN W PROGRAMIE II LINII Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK PROGRAM II LINII P R O B L E M Y Z G Ł A S Z A N E W 2 0 1 7 r o k u Brak możliwości
Lenalidomid (Revlimid ) w skojarzeniu z deksametazonem w leczeniu chorych ze szpiczakiem mnogim po niepowodzeniu wcześniejszego leczenia
 Lenalidomid (Revlimid ) w skojarzeniu z deksametazonem w leczeniu chorych ze szpiczakiem mnogim po niepowodzeniu wcześniejszego leczenia Analiza wpływu na system ochrony zdrowia maj 2013 Autorzy raportu:
Lenalidomid (Revlimid ) w skojarzeniu z deksametazonem w leczeniu chorych ze szpiczakiem mnogim po niepowodzeniu wcześniejszego leczenia Analiza wpływu na system ochrony zdrowia maj 2013 Autorzy raportu:
STWARDNIENIE ROZSIANE - ZARZĄDZANIE CHOROBĄ
 STWARDNIENIE ROZSIANE - ZARZĄDZANIE CHOROBĄ PROPOZYCJE ROZWIĄZAŃ PROBLEMÓW Warszawa, 26 kwietnia 2016 r. Projekt badawczy STWARDNIENIE ROZSIANE - ZARZĄDZANIE CHOROBĄ Projekt jest kontynuacją prac badawczych
STWARDNIENIE ROZSIANE - ZARZĄDZANIE CHOROBĄ PROPOZYCJE ROZWIĄZAŃ PROBLEMÓW Warszawa, 26 kwietnia 2016 r. Projekt badawczy STWARDNIENIE ROZSIANE - ZARZĄDZANIE CHOROBĄ Projekt jest kontynuacją prac badawczych
ANALIZA RACJONALIZACYJNA
 ANALIZA RACJONALIZACYJNA SOFOSBUWIR W TERAPII PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C (WZW C) Wersja 1.0 DOKUMENT POUFNY Kraków marzec 2015 HTA Consulting spółka z ograniczoną odpowiedzialnością
ANALIZA RACJONALIZACYJNA SOFOSBUWIR W TERAPII PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C (WZW C) Wersja 1.0 DOKUMENT POUFNY Kraków marzec 2015 HTA Consulting spółka z ograniczoną odpowiedzialnością
XTANDI (ENZALUTAMID) W LECZENIU DOROSŁYCH CHORYCH NA RAKA GRUCZOŁU KROKOWEGO OPORNEGO NA KASTRACJĘ PO NIEPOWODZENIU TERAPII DOCETAKSELEM
 XTANDI (ENZALUTAMID) W LECZENIU DOROSŁYCH CHORYCH NA RAKA GRUCZOŁU KROKOWEGO OPORNEGO NA KASTRACJĘ PO NIEPOWODZENIU TERAPII DOCETAKSELEM Wykonawca: MAHTA Sp z oo ul Rejtana 17/5 02-516 Warszawa Tel 22
XTANDI (ENZALUTAMID) W LECZENIU DOROSŁYCH CHORYCH NA RAKA GRUCZOŁU KROKOWEGO OPORNEGO NA KASTRACJĘ PO NIEPOWODZENIU TERAPII DOCETAKSELEM Wykonawca: MAHTA Sp z oo ul Rejtana 17/5 02-516 Warszawa Tel 22
Analiza racjonalizacyjna Wersja 1.0. Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/5 02-516 Warszawa Tel. 22 542 41 54 E-mail: biuro@mahta.
 Adcetris (brentuksymab vedotin) w leczeniu dorosłych oraz dzieci od 12 r.ż. chorych na nawrotowego lub opornego na leczenie chłoniaka Hodgkina CD30+ oraz układowego chłoniaka anaplastycznego z dużych komórek
Adcetris (brentuksymab vedotin) w leczeniu dorosłych oraz dzieci od 12 r.ż. chorych na nawrotowego lub opornego na leczenie chłoniaka Hodgkina CD30+ oraz układowego chłoniaka anaplastycznego z dużych komórek
ANALIZA RACJONALIZACYJNA
 ANALIZA RACJONALIZACYJNA PALIWIZUMAB (SYNAGIS ) W ZAPOBIEGANIU CIĘŻKIEJ CHOROBIE DOLNYCH DRÓG ODDECHOWYCH WYWOŁANEJ WIRUSEM RS U DZIECI Z ISTOTNĄ HEMODYNAMICZNIE WRODZONĄ WADĄ SERCA Wersja 1.00 Kraków
ANALIZA RACJONALIZACYJNA PALIWIZUMAB (SYNAGIS ) W ZAPOBIEGANIU CIĘŻKIEJ CHOROBIE DOLNYCH DRÓG ODDECHOWYCH WYWOŁANEJ WIRUSEM RS U DZIECI Z ISTOTNĄ HEMODYNAMICZNIE WRODZONĄ WADĄ SERCA Wersja 1.00 Kraków
Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza wpływu na budżet
 Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza wpływu na budżet Dominik Golicki, Katarzyna Jaśkowiak, Iwona Dworakowska, Maciej Niewada Warszawa 2014
Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza wpływu na budżet Dominik Golicki, Katarzyna Jaśkowiak, Iwona Dworakowska, Maciej Niewada Warszawa 2014
Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r. w sprawie minimalnych wymagań, jakie muszą spełniać analizy
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r. w sprawie minimalnych wymagań, jakie muszą spełniać analizy
Xeplion (palmitynian paliperydonu) w leczeniu schizofrenii
 1 Wykonawca: Raport został wykonany na zlecenie i sfinansowany przez firmę Janssen-Cilag Polska Sp. z o.o. Autorzy nie zgłosili konfliktu interesów. Wersja 2.0 ostatnia aktualizacja dnia 4 sierpnia 2015
1 Wykonawca: Raport został wykonany na zlecenie i sfinansowany przez firmę Janssen-Cilag Polska Sp. z o.o. Autorzy nie zgłosili konfliktu interesów. Wersja 2.0 ostatnia aktualizacja dnia 4 sierpnia 2015
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Konsultacyjna Stanowisko Rady Konsultacyjnej nr 86/2011 z dnia 26 września 2011 r. w sprawie zasadności zakwalifikowania świadczenia opieki zdrowotnej Leczenie
Agencja Oceny Technologii Medycznych Rada Konsultacyjna Stanowisko Rady Konsultacyjnej nr 86/2011 z dnia 26 września 2011 r. w sprawie zasadności zakwalifikowania świadczenia opieki zdrowotnej Leczenie
Informacja na temat problemów osób chorych na stwardnienie rozsiane
 Warszawa, dnia 14 maja 2012 r. Informacja na temat problemów osób chorych na stwardnienie rozsiane Stwardnienie rozsiane (SM) jest jedną z najczęstszych chorób układu nerwowego (mózgu i rdzenia kręgowego).
Warszawa, dnia 14 maja 2012 r. Informacja na temat problemów osób chorych na stwardnienie rozsiane Stwardnienie rozsiane (SM) jest jedną z najczęstszych chorób układu nerwowego (mózgu i rdzenia kręgowego).
Co ustawa refundacyjna mówi o cenach leków?
 Co ustawa refundacyjna mówi o cenach leków? Natalia Łojko Radca prawny Warszawa, 1. Brak szczególnej regulacji dla leków biologicznych - podlegają tym samym regulacjom refundacyjnym, co inne leki 2 2.
Co ustawa refundacyjna mówi o cenach leków? Natalia Łojko Radca prawny Warszawa, 1. Brak szczególnej regulacji dla leków biologicznych - podlegają tym samym regulacjom refundacyjnym, co inne leki 2 2.
Warszawa, dnia 18.12.2012
 Warszawa, dnia 18.12.2012 Opinia dotycząca zasad rozliczania świadczeń z zakresu lecznictwa szpitalnego chemioterapia, w oparciu o obowiązujące prawo oraz regulacje wynikające z zarządzeń Prezesa Narodowego
Warszawa, dnia 18.12.2012 Opinia dotycząca zasad rozliczania świadczeń z zakresu lecznictwa szpitalnego chemioterapia, w oparciu o obowiązujące prawo oraz regulacje wynikające z zarządzeń Prezesa Narodowego
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 90/2012 z dnia 15 października 2012 r. w sprawie zasadności finansowania leku Primacor (chlorowodorek lerkanidypiny)
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 90/2012 z dnia 15 października 2012 r. w sprawie zasadności finansowania leku Primacor (chlorowodorek lerkanidypiny)
Szanse i zagrożenia przygotowania RSS na podstawie raportu HTA
 Szanse i zagrożenia przygotowania RSS na podstawie raportu HTA Co może być istotne w procesie tworzenia RSS? Magdalena Władysiuk Ustawa refundacyjna W krajach o średnim dochodzie RSSs są szansą na finansowanie
Szanse i zagrożenia przygotowania RSS na podstawie raportu HTA Co może być istotne w procesie tworzenia RSS? Magdalena Władysiuk Ustawa refundacyjna W krajach o średnim dochodzie RSSs są szansą na finansowanie
DZIENNIK URZĘDOWY MINISTRA ZDROWIA
 DZIENNIK URZĘDOWY MINISTRA ZDROWIA Warszawa, dnia 29 października 2012 r. Poz. 77 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy
DZIENNIK URZĘDOWY MINISTRA ZDROWIA Warszawa, dnia 29 października 2012 r. Poz. 77 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy
Analiza wpływu na system ochrony zdrowia finansowania produktu leczniczego Ruconest (konestat alfa) w ramach programu lekowego w Polsce w leczeniu
 Analiza wpływu na system ochrony zdrowia finansowania produktu leczniczego Ruconest (konestat alfa) w ramach programu lekowego w Polsce w leczeniu ostrych, zagrażających życiu, napadów obrzęku naczynioruchowego
Analiza wpływu na system ochrony zdrowia finansowania produktu leczniczego Ruconest (konestat alfa) w ramach programu lekowego w Polsce w leczeniu ostrych, zagrażających życiu, napadów obrzęku naczynioruchowego
Katarzyna Adamczyk Ewa Borek Analiza wykonana na zlecenie BMS Polska
 Katarzyna Adamczyk Ewa Borek Analiza wykonana na zlecenie BMS Polska Analizy racjonalizacyjne. gdy wykonana analiza wpływu na budżet płatnika (BIA) dała w wyniku wzrost kosztów ponoszonych na finansowanie
Katarzyna Adamczyk Ewa Borek Analiza wykonana na zlecenie BMS Polska Analizy racjonalizacyjne. gdy wykonana analiza wpływu na budżet płatnika (BIA) dała w wyniku wzrost kosztów ponoszonych na finansowanie
Tikagrelor (Brilique ) w prewencji wtórnej ostrych zespołów wieńcowych Analiza racjonalizacyjna
 Tikagrelor (Brilique ) w prewencji wtórnej ostrych zespołów wieńcowych Analiza racjonalizacyjna Tomasz Macioch, Małgorzata Polkowska, Maciej Niewada Warszawa Listopad 2013 Autorzy raportu: lek. Tomasz
Tikagrelor (Brilique ) w prewencji wtórnej ostrych zespołów wieńcowych Analiza racjonalizacyjna Tomasz Macioch, Małgorzata Polkowska, Maciej Niewada Warszawa Listopad 2013 Autorzy raportu: lek. Tomasz
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE 1. Dawkowanie oraz sposób modyfikacji dawkowania w programie:
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska
 Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT) Słów kilka o HTA HTA nie jest: nauką o ochronie zdrowia nauką / analizą dot.
Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT) Słów kilka o HTA HTA nie jest: nauką o ochronie zdrowia nauką / analizą dot.
Neurologia Organizacja i wycena świadczeń. Danuta Ryglewicz Instytut Psychiatrii i Neurologii Warszawa
 Neurologia Organizacja i wycena świadczeń Danuta Ryglewicz Instytut Psychiatrii i Neurologii Warszawa Choroby neurologiczne wg. WHO Bardzo wysokie wskażniki rozpowszechnienia aktualnie na świecie u miliarda
Neurologia Organizacja i wycena świadczeń Danuta Ryglewicz Instytut Psychiatrii i Neurologii Warszawa Choroby neurologiczne wg. WHO Bardzo wysokie wskażniki rozpowszechnienia aktualnie na świecie u miliarda
Wpływ nowych terapii na budżet NFZ czy stać nas na refundację?
 Wpływ nowych terapii na budżet NFZ czy stać nas na refundację? Leszek Stabrawa W A R S Z A W A, 1 1 s i e r p n i a 2 0 1 6 Dostęp do innowacyjnych terapii w Polsce o Jednym z celów ustawy refundacyjnej
Wpływ nowych terapii na budżet NFZ czy stać nas na refundację? Leszek Stabrawa W A R S Z A W A, 1 1 s i e r p n i a 2 0 1 6 Dostęp do innowacyjnych terapii w Polsce o Jednym z celów ustawy refundacyjnej
Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się
 (BIA) komu i po co Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się Not everything that can be counted counts, and not everything that counts can be counted A.
(BIA) komu i po co Nie wszystko co się liczy może być policzone, nie wszystko co może być policzone liczy się Not everything that can be counted counts, and not everything that counts can be counted A.
ANNALES UNIVERSITATIS MARIAE CURIE-SKŁODOWSKA LUBLIN - POLONIA VOL.LX, SUPPL. XVI, 7 SECTIO D 2005
 ANNALES UNIVERSITATIS MARIAE CURIE-SKŁODOWSKA LUBLIN - POLONIA VOL.LX, SUPPL. XVI, 7 SECTIO D 5 1 Państwowa Wyższa Szkoła Zawodowa w Białej Podlaskiej Instytut Pielęgniarstwa Higher State Vocational School
ANNALES UNIVERSITATIS MARIAE CURIE-SKŁODOWSKA LUBLIN - POLONIA VOL.LX, SUPPL. XVI, 7 SECTIO D 5 1 Państwowa Wyższa Szkoła Zawodowa w Białej Podlaskiej Instytut Pielęgniarstwa Higher State Vocational School
PLAN FINANSOWY ORAZ ŚRODKI NA KONTRAKTY W 2014 ROKU. 1. Plan finansowy na 2014 rok
 2 518 2 704 3 003 3 481 4 139 4 507 4 668 4 736 4 977 5 302 5 302 PLAN FINANSOWY ORAZ ŚRODKI NA KONTRAKTY W 2014 ROKU Wartość planów finansowych MOW NFZ koszty świadczeń zdrowotnych 2011-2014 r. w mln
2 518 2 704 3 003 3 481 4 139 4 507 4 668 4 736 4 977 5 302 5 302 PLAN FINANSOWY ORAZ ŚRODKI NA KONTRAKTY W 2014 ROKU Wartość planów finansowych MOW NFZ koszty świadczeń zdrowotnych 2011-2014 r. w mln
LISTA OSÓB ZAANGAŻOWANYCH W OPRACOWANIE ANALIZY EKONOMICZNEJ
 Ocena zasadności ekonomicznej z perspektywy płatnika publicznego, z perspektywy wspólnej i z perspektywy społecznej stosowania produktu Plegridy (peginterferon beta- 1a) w I linii leczenia dorosłych pacjentów
Ocena zasadności ekonomicznej z perspektywy płatnika publicznego, z perspektywy wspólnej i z perspektywy społecznej stosowania produktu Plegridy (peginterferon beta- 1a) w I linii leczenia dorosłych pacjentów
Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej. Szanowny Panie Marszałku,
 Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej Szanowny Panie Marszałku, w odpowiedzi na interpelację nr 9087 Posłów na Sejm RP: Krystyny Sibińskiej, Marii Janyska,
Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej Szanowny Panie Marszałku, w odpowiedzi na interpelację nr 9087 Posłów na Sejm RP: Krystyny Sibińskiej, Marii Janyska,
Rekomendacja nr 19/2016 Prezesa AOTM z dnia 6 kwietnia 2016r.
 Agencja Oceny Technologii Medycznych i Taryfikacji www.aotmit.gov.pl Rekomendacja nr 19/2016 z dnia 6 kwietnia 2016r. Prezesa Agencji Oceny Technologii Medycznych i Taryfikacji w sprawie zakwalifikowania
Agencja Oceny Technologii Medycznych i Taryfikacji www.aotmit.gov.pl Rekomendacja nr 19/2016 z dnia 6 kwietnia 2016r. Prezesa Agencji Oceny Technologii Medycznych i Taryfikacji w sprawie zakwalifikowania
ANALIZA RACJONALIZACYJNA NALMEFEN (SELINCRO ) STOSOWANY W CELU REDUKCJI SPOŻYCIA ALKOHOLU U DOROSŁYCH UZALEŻNIONYCH PACJENTÓW
 ANALIZA RACJONALIZACYJNA NALMEFEN (SELINCRO ) STOSOWANY W CELU REDUKCJI SPOŻYCIA ALKOHOLU U DOROSŁYCH UZALEŻNIONYCH PACJENTÓW Wersja 1.0 HTA Consulting spółka z ograniczoną odpowiedzialnością spółka komandytowa
ANALIZA RACJONALIZACYJNA NALMEFEN (SELINCRO ) STOSOWANY W CELU REDUKCJI SPOŻYCIA ALKOHOLU U DOROSŁYCH UZALEŻNIONYCH PACJENTÓW Wersja 1.0 HTA Consulting spółka z ograniczoną odpowiedzialnością spółka komandytowa
Azilect fakty Czym jest Azilect? Jak działa Azilect? Kto może skorzystać na leczeniu Azilectem?
 Azilect fakty Czym jest Azilect? Azilect (rasagilina 1mg) jest pierwszym, prawdziwie innowacyjnym lekiem stosowanym w chorobie Parkinsona (PD Parkinson s Disease) wprowadzonym w ostatnich latach. Jest
Azilect fakty Czym jest Azilect? Azilect (rasagilina 1mg) jest pierwszym, prawdziwie innowacyjnym lekiem stosowanym w chorobie Parkinsona (PD Parkinson s Disease) wprowadzonym w ostatnich latach. Jest
Art. 24 ust. 7 pkt 2 ustawy o refundacji
 Minimalne wymagania dotyczące analiz uwzględnianych we wnioskach o objęcie refundacją i ustalenie oraz podwyższenie urzędowej ceny zbytu dla produktów, które nie mają odpowiednika refundowanego w danym
Minimalne wymagania dotyczące analiz uwzględnianych we wnioskach o objęcie refundacją i ustalenie oraz podwyższenie urzędowej ceny zbytu dla produktów, które nie mają odpowiednika refundowanego w danym
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
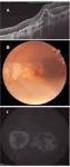 Dziennik Urzędowy Ministra Zdrowia 882 Poz. 79 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Dziennik Urzędowy Ministra Zdrowia 882 Poz. 79 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
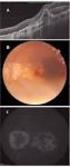 Dziennik Urzędowy Ministra Zdrowia 761 Poz. 48 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY afliberceptem
Dziennik Urzędowy Ministra Zdrowia 761 Poz. 48 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY afliberceptem
Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon
 VI.2 VI.2.1 Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon Omówienie rozpowszechnienia choroby Deksametazonu sodu fosforan w postaci roztworu do wstrzykiwań stosowany jest
VI.2 VI.2.1 Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon Omówienie rozpowszechnienia choroby Deksametazonu sodu fosforan w postaci roztworu do wstrzykiwań stosowany jest
12 SQ-HDM Grupa farmakoterapeutyczna: Wyciągi alergenowe, kurz domowy; Kod ATC: V01AA03
 SUBSTANCJA CZYNNA (INN) GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC) PODMIOT ODPOWIEDZIALNY NAZWA HANDLOWA PRODUKTU LECZNICZEGO, KTÓREGO DOTYCZY PLAN ZARZĄDZANIA RYZYKIEM 12 SQ-HDM Grupa farmakoterapeutyczna:
SUBSTANCJA CZYNNA (INN) GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC) PODMIOT ODPOWIEDZIALNY NAZWA HANDLOWA PRODUKTU LECZNICZEGO, KTÓREGO DOTYCZY PLAN ZARZĄDZANIA RYZYKIEM 12 SQ-HDM Grupa farmakoterapeutyczna:
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1.Kryteria kwalifikacji ŚWIADCZENIOBIORCY 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1.Kryteria kwalifikacji ŚWIADCZENIOBIORCY 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 380/2014 z dnia 29 grudnia 2014 r. w sprawie zasadności objęcia refundacją leku Mimpara (cinacalcetum) w zakresie
Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 380/2014 z dnia 29 grudnia 2014 r. w sprawie zasadności objęcia refundacją leku Mimpara (cinacalcetum) w zakresie
Faramkoekonomiczna ocena leków biopodobnych. dr Michał Seweryn
 Faramkoekonomiczna ocena leków biopodobnych dr Michał Seweryn Klasyczny problem ekonomii Potrzeby Dobra Farmakoekonomika (ekonomiczna ocena technologii medycznych) Celem badania farmakoekonomicznego jest
Faramkoekonomiczna ocena leków biopodobnych dr Michał Seweryn Klasyczny problem ekonomii Potrzeby Dobra Farmakoekonomika (ekonomiczna ocena technologii medycznych) Celem badania farmakoekonomicznego jest
LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Dziennik Urzędowy Ministra Zdrowia 732 Poz. 71 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Dziennik Urzędowy Ministra Zdrowia 732 Poz. 71 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
Szanse i zagrożenia na poprawę leczenia chorób zapalnych stawów w Polsce rok 2014 Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób
 Szanse i zagrożenia na poprawę leczenia chorób zapalnych stawów w Polsce rok 2014 Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób Wewnętrznych, Uniwersytet Medyczny im. Piastów Śląskich
Szanse i zagrożenia na poprawę leczenia chorób zapalnych stawów w Polsce rok 2014 Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób Wewnętrznych, Uniwersytet Medyczny im. Piastów Śląskich
Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008.
 załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Załącznik B.36. LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW ŚWIADCZENIOBIORCY W PROGRAMIE
Załącznik B.36. LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW ŚWIADCZENIOBIORCY W PROGRAMIE
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Opinia Prezesa Agencji Oceny Technologii Medycznych nr 177/2012 z dnia 10 sierpnia 2012 o projekcie programu Rehabilitacja pacjentów ze schorzeniami narządu ruchu mieszkańców
Agencja Oceny Technologii Medycznych Opinia Prezesa Agencji Oceny Technologii Medycznych nr 177/2012 z dnia 10 sierpnia 2012 o projekcie programu Rehabilitacja pacjentów ze schorzeniami narządu ruchu mieszkańców
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
Pan. Pozwalam sobie przedstawić Panu Ministrowi obawy w zakresie dostępu. obywateli, po dniu 1 lipca 2012 r., do leków stosowanych w ramach programów
 RZECZPOSPOLITA POLSKA Rzecznik Praw Obywatelskich Irena LIPOWICZ RPO-700858-V/12/AA 00-090 Warszawa Tel. centr. 22 551 77 00 Al. Solidarności 77 Fax 22 827 64 53 Pan BARTOSZ ARŁUKOWICZ Minister Zdrowia
RZECZPOSPOLITA POLSKA Rzecznik Praw Obywatelskich Irena LIPOWICZ RPO-700858-V/12/AA 00-090 Warszawa Tel. centr. 22 551 77 00 Al. Solidarności 77 Fax 22 827 64 53 Pan BARTOSZ ARŁUKOWICZ Minister Zdrowia
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej (wysiękowej) postaci afliberceptem
Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej (wysiękowej) postaci afliberceptem
POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED.
 POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED Izabela Pieniążek Klasyczne dossier? Rozporządzenie MZ w sprawie MINIMALNYCH
POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED Izabela Pieniążek Klasyczne dossier? Rozporządzenie MZ w sprawie MINIMALNYCH
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 7 czerwca 2017 r. Komisja Europejska (KE) otrzymała informację o przypadku zabójczej niewydolności wątroby u pacjenta po zastosowaniu leczenia daklizumabem
Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 7 czerwca 2017 r. Komisja Europejska (KE) otrzymała informację o przypadku zabójczej niewydolności wątroby u pacjenta po zastosowaniu leczenia daklizumabem
Warszawa, dnia 29 października 2012 r. Poz. 77
 Warszawa, dnia 29 października 2012 r. Poz. 77 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu
Warszawa, dnia 29 października 2012 r. Poz. 77 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu
Sekcja I: Instytucja zamawiająca/podmiot zamawiający
 Unia Europejska Publikacja Suplementu do Dziennika Urzędowego Unii Europejskiej 2, rue Mercier, 2985 Luxembourg, Luksemburg Faks: +352 29 29 42 670 E-mail: ojs@publications.europa.eu Informacje i formularze
Unia Europejska Publikacja Suplementu do Dziennika Urzędowego Unii Europejskiej 2, rue Mercier, 2985 Luxembourg, Luksemburg Faks: +352 29 29 42 670 E-mail: ojs@publications.europa.eu Informacje i formularze
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Danuta Ryglewicz Instytut Psychiatrii i Neurologii
 Danuta Ryglewicz Instytut Psychiatrii i Neurologii SM - postępująca, przewlekła choroba oun SM zróżnicowany obraz kliniczny SM zróżnicowany przebieg kliniczny choroby SM choroba młodych dorosłych Kolejne
Danuta Ryglewicz Instytut Psychiatrii i Neurologii SM - postępująca, przewlekła choroba oun SM zróżnicowany obraz kliniczny SM zróżnicowany przebieg kliniczny choroby SM choroba młodych dorosłych Kolejne
LECZENIE CHOROBY GAUCHERA ICD-10 E
 załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
Zarządzenie Nr 27/2012/DGL. Prezesa. Narodowego Funduszu Zdrowia z dnia 10 maja 2012 r.
 Zarządzenie Nr 27/2012/DGL Prezesa Narodowego Funduszu Zdrowia z dnia 10 maja 2012 r. w sprawie określenia warunków zawierania i realizacji umów w rodzaju leczenie szpitalne w zakresie programy zdrowotne
Zarządzenie Nr 27/2012/DGL Prezesa Narodowego Funduszu Zdrowia z dnia 10 maja 2012 r. w sprawie określenia warunków zawierania i realizacji umów w rodzaju leczenie szpitalne w zakresie programy zdrowotne
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 111/2013 z dnia 26 sierpnia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Zoladex,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 111/2013 z dnia 26 sierpnia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Zoladex,
Podstawowe założenia i zmiany. wprowadzane przez projekt. ustawy refundacyjnej
 Podstawowe założenia i zmiany wprowadzane przez projekt ustawy refundacyjnej 1. Geneza zmian 2. Sposób dojścia do proponowanych rozwiązań 3. Wprowadzone zmiany organizacyjne 4. Podstawowe różnice pomiędzy
Podstawowe założenia i zmiany wprowadzane przez projekt ustawy refundacyjnej 1. Geneza zmian 2. Sposób dojścia do proponowanych rozwiązań 3. Wprowadzone zmiany organizacyjne 4. Podstawowe różnice pomiędzy
Wyniki ankiety Polityka lekowa
 Wyniki ankiety Polityka lekowa Innowacyjna, dostępna, transparentna Ankieta przygotowana przez Izbę Gospodarczą FARMACJA POLSKA i Instytut Innowacji i Odpowiedzialnego Rozwoju INNOWO miała na celu zbadanie
Wyniki ankiety Polityka lekowa Innowacyjna, dostępna, transparentna Ankieta przygotowana przez Izbę Gospodarczą FARMACJA POLSKA i Instytut Innowacji i Odpowiedzialnego Rozwoju INNOWO miała na celu zbadanie
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 5/2012 z dnia 27 lutego 2012 r. w zakresie zakwalifikowania/niezasadności zakwalifikowania leku Valdoxan (agomelatinum)
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 5/2012 z dnia 27 lutego 2012 r. w zakresie zakwalifikowania/niezasadności zakwalifikowania leku Valdoxan (agomelatinum)
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
 Dziennik Urzędowy Ministra Zdrowia 904 Poz. 133 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie
Dziennik Urzędowy Ministra Zdrowia 904 Poz. 133 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie
Rola współpracy między lekarzem a pacjentem jaskrowym Anna Kamińska
 Rola współpracy między lekarzem a pacjentem jaskrowym Anna Kamińska Katedra i Klinika Okulistyki, II WL, Warszawski Uniwersytet Medyczny Kierownik Kliniki: Profesor Jacek P. Szaflik Epidemiologia jaskry
Rola współpracy między lekarzem a pacjentem jaskrowym Anna Kamińska Katedra i Klinika Okulistyki, II WL, Warszawski Uniwersytet Medyczny Kierownik Kliniki: Profesor Jacek P. Szaflik Epidemiologia jaskry
MISJA HASCO-LEK. " Produkowanie leków najwyższej jakości, skutecznie zaspokajających potrzeby zdrowotne pacjentów "
 MISJA HASCO-LEK " Produkowanie leków najwyższej jakości, skutecznie zaspokajających potrzeby zdrowotne pacjentów " Rynek farmaceutyczny - dzień dzisiejszy i obserwowane kierunki zmian Michał Byliniak PPF
MISJA HASCO-LEK " Produkowanie leków najwyższej jakości, skutecznie zaspokajających potrzeby zdrowotne pacjentów " Rynek farmaceutyczny - dzień dzisiejszy i obserwowane kierunki zmian Michał Byliniak PPF
Systemowe aspekty leczenia WZW typu C
 Systemowe aspekty leczenia WZW typu C Dr n. med. Jakub Gierczyński, MBA Narodowy Instytut Zdrowia Publicznego-PZH Instytut Zarządzania w Ochronie Zdrowia, Uczelnia Łazarskiego Warszawa, 06.06.2017 r. Systemowe
Systemowe aspekty leczenia WZW typu C Dr n. med. Jakub Gierczyński, MBA Narodowy Instytut Zdrowia Publicznego-PZH Instytut Zarządzania w Ochronie Zdrowia, Uczelnia Łazarskiego Warszawa, 06.06.2017 r. Systemowe
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe Od czasu dopuszczenia produktu Esmya do obrotu zgłoszono cztery przypadki poważnego uszkodzenia wątroby prowadzącego do transplantacji wątroby. Ponadto zgłoszono
Aneks IV Wnioski naukowe 1 Wnioski naukowe Od czasu dopuszczenia produktu Esmya do obrotu zgłoszono cztery przypadki poważnego uszkodzenia wątroby prowadzącego do transplantacji wątroby. Ponadto zgłoszono
Rozdział 1 Postanowienia ogólne
 Zarządzenie Nr 27/2012/DGL Prezesa Narodowego Funduszu Zdrowia z dnia 10 maja 2012 r. w sprawie określenia warunków zawierania i realizacji umów w rodzaju leczenie szpitalne w zakresie programy zdrowotne
Zarządzenie Nr 27/2012/DGL Prezesa Narodowego Funduszu Zdrowia z dnia 10 maja 2012 r. w sprawie określenia warunków zawierania i realizacji umów w rodzaju leczenie szpitalne w zakresie programy zdrowotne
OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu
 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu aktów normatywnych i niektórych innych aktów
OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu aktów normatywnych i niektórych innych aktów
KOSZTY LECZENIA SM, JAKO DETERMINANTA ZMIAN ORGANIZACJI OPIEKI. Dr n. ekon. Małgorzata Gałązka-Sobotka
 KOSZTY LECZENIA SM, JAKO DETERMINANTA ZMIAN ORGANIZACJI OPIEKI Dr n. ekon. Małgorzata Gałązka-Sobotka Koszty hospitalizacji z tytułu SM to średnio ok. 45 mln zł rocznie. Koszty bezpośrednie generowane
KOSZTY LECZENIA SM, JAKO DETERMINANTA ZMIAN ORGANIZACJI OPIEKI Dr n. ekon. Małgorzata Gałązka-Sobotka Koszty hospitalizacji z tytułu SM to średnio ok. 45 mln zł rocznie. Koszty bezpośrednie generowane
Waldemar Halota HCV. RAPORT W BUDOWIE Instytut Ochrony Zdrowia
 Waldemar Halota HCV RAPORT W BUDOWIE Instytut Ochrony Zdrowia Instytut Ochrony Zdrowia Członkowie Rady Konsultacyjnej Waldemar Halota, Robert Flisiak, Małgorzata Pawłowska, Krzysztof Tomasiewicz, Mirosław
Waldemar Halota HCV RAPORT W BUDOWIE Instytut Ochrony Zdrowia Instytut Ochrony Zdrowia Członkowie Rady Konsultacyjnej Waldemar Halota, Robert Flisiak, Małgorzata Pawłowska, Krzysztof Tomasiewicz, Mirosław
Krajobraz Stwardnienia Rozsianego w Europie
 Krajobraz Stwardnienia Rozsianego w Europie Polska na tle krajów europejskich Analiza przygotowana na zlecenie firmy Biogen Tomasz Kluszczyński Principal, Consulting Copyright 2018 IQVIA. All rights reserved.
Krajobraz Stwardnienia Rozsianego w Europie Polska na tle krajów europejskich Analiza przygotowana na zlecenie firmy Biogen Tomasz Kluszczyński Principal, Consulting Copyright 2018 IQVIA. All rights reserved.
o rządowym projekcie ustawy o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych (druk nr 3491).
 SEJM RZECZYPOSPOLITEJ POLSKIEJ Druk nr 3924-A VI kadencja D O D A T K O W E S P R A W O Z D A N I E KOMISJI ZDROWIA o rządowym projekcie ustawy o refundacji leków, środków spożywczych specjalnego przeznaczenia
SEJM RZECZYPOSPOLITEJ POLSKIEJ Druk nr 3924-A VI kadencja D O D A T K O W E S P R A W O Z D A N I E KOMISJI ZDROWIA o rządowym projekcie ustawy o refundacji leków, środków spożywczych specjalnego przeznaczenia
Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza ekonomiczna
 Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza ekonomiczna Iwona Dworakowska, Dominik Golicki, Maciej Niewada Warszawa 214 Autorzy raportu: Iwona Dworakowska,
Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza ekonomiczna Iwona Dworakowska, Dominik Golicki, Maciej Niewada Warszawa 214 Autorzy raportu: Iwona Dworakowska,
ANEKS WNIOSKI NAUKOWE I PODSTAWY DO ODMOWY PRZEDSTAWIONE PRZEZ EMEA
 ANEKS WNIOSKI NAUKOWE I PODSTAWY DO ODMOWY PRZEDSTAWIONE PRZEZ EMEA PONOWNE ZBADANIE OPINII CHMP Z 19 LIPCA 2007 R. NA TEMAT PREPARATU NATALIZUMAB ELAN PHARMA Podczas posiedzenia w lipcu 2007 r. CHMP przyjął
ANEKS WNIOSKI NAUKOWE I PODSTAWY DO ODMOWY PRZEDSTAWIONE PRZEZ EMEA PONOWNE ZBADANIE OPINII CHMP Z 19 LIPCA 2007 R. NA TEMAT PREPARATU NATALIZUMAB ELAN PHARMA Podczas posiedzenia w lipcu 2007 r. CHMP przyjął
Aneks III. Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
NARODOWY FUNDUSZ ZDROWIA
 NARODOWY FUNDUSZ ZDROWIA Departament Gospodarki Lekami Centrali NFZ Sporządzono na podstawie szczegółowych danych statystycznych sprawozdanych przez apteki do systemu informatycznego NFZ 1 Zasady refundacji
NARODOWY FUNDUSZ ZDROWIA Departament Gospodarki Lekami Centrali NFZ Sporządzono na podstawie szczegółowych danych statystycznych sprawozdanych przez apteki do systemu informatycznego NFZ 1 Zasady refundacji
ECONOMEDICA SM. Wybrane wyniki. Maj 2019 TYTUŁ RAPORTU
 ECONOMEDICA SM Wybrane wyniki Maj 2019 TYTUŁ RAPORTU 1 Spis treści 1. CEL PROJEKTU... 3 2. CZAS REALIZACJI BADANIA... 3 3. ELEMENTY PROJEKTU... 3 4. WIELKOŚĆ I SPOSÓB DOBORU PRÓBY... 4 5. WAŻENIE I EKSTRAPOLACJA
ECONOMEDICA SM Wybrane wyniki Maj 2019 TYTUŁ RAPORTU 1 Spis treści 1. CEL PROJEKTU... 3 2. CZAS REALIZACJI BADANIA... 3 3. ELEMENTY PROJEKTU... 3 4. WIELKOŚĆ I SPOSÓB DOBORU PRÓBY... 4 5. WAŻENIE I EKSTRAPOLACJA
DZPZ / 333 / 22UEPN / 2013 Olsztyn, dnia 3 stycznia 2014 r.
 Wojewódzki Szpital Specjalistyczny ul. Żołnierska 18 10 561 Olsztyn Dotyczy: postępowania o udzielenie zamówienia publicznego prowadzonego w trybie przetargu nieograniczonego na wybór Wykonawcy zadania:
Wojewódzki Szpital Specjalistyczny ul. Żołnierska 18 10 561 Olsztyn Dotyczy: postępowania o udzielenie zamówienia publicznego prowadzonego w trybie przetargu nieograniczonego na wybór Wykonawcy zadania:
Warszawa, dnia 11 stycznia 2013 r. Poz. 44 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 20 grudnia 2012 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 stycznia 2013 r. Poz. 44 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 20 grudnia 2012 r. w sprawie wzorów wniosków w zakresie refundacji leku, środka
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 stycznia 2013 r. Poz. 44 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 20 grudnia 2012 r. w sprawie wzorów wniosków w zakresie refundacji leku, środka
Wydatki Narodowego Funduszu Zdrowia na refundację po wejściu w życie Ustawy o refundacji
 Wydatki Narodowego Funduszu Zdrowia na refundację po wejściu w życie Ustawy o refundacji Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/5 02-516 Warszawa Tel. 22 542 41 54 E-mail: biuro@mahta.pl Analiza danych
Wydatki Narodowego Funduszu Zdrowia na refundację po wejściu w życie Ustawy o refundacji Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/5 02-516 Warszawa Tel. 22 542 41 54 E-mail: biuro@mahta.pl Analiza danych
Xofigo (dichlorek radu-223) w leczeniu chorych z opornym na kastrację rakiem gruczołu krokowego, z objawowymi przerzutami do kości, bez stwierdzonych
 1 Wykonawca: ''''''''''''''' '''''' ''''''''''''''' '''''''''''''' ''''''''' ''''''''''''' ''''' '''''''''''''''''''''' '''''''' ''''''''''''''' ''''''''''''''' ''''''''''''''' ''''''''''''' ''''' '''''
1 Wykonawca: ''''''''''''''' '''''' ''''''''''''''' '''''''''''''' ''''''''' ''''''''''''' ''''' '''''''''''''''''''''' '''''''' ''''''''''''''' ''''''''''''''' ''''''''''''''' ''''''''''''' ''''' '''''
Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza problemu decyzyjnego
 Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza problemu decyzyjnego Alicja Wójcik, Dominik Golicki, Maciej Niewada Warszawa 2014 Autorzy raportu: mgr
Fumaran dimetylu (Tecfidera ) w leczeniu postaci rzutowo-remisyjnej stwardnienia rozsianego Analiza problemu decyzyjnego Alicja Wójcik, Dominik Golicki, Maciej Niewada Warszawa 2014 Autorzy raportu: mgr
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r.
 PROJEKT 29.12.2004 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia...2004 r. zmieniające rozporządzenie w sprawie ustalenia cen urzędowych hurtowych i detalicznych na produkty lecznicze i wyroby medyczne Na
PROJEKT 29.12.2004 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia...2004 r. zmieniające rozporządzenie w sprawie ustalenia cen urzędowych hurtowych i detalicznych na produkty lecznicze i wyroby medyczne Na
ABC oceny technologii medycznych. Skąd się biorą ceny leków?
 ABC oceny technologii medycznych. Skąd się biorą ceny leków? Michał Jachimowicz Warszawa, 14 października 2014 roku MAHTA Sp. z o.o. ul. Rejtana 17/5, 02-516 Warszawa, tel.: 22 542 41 54, biuro@mahta.pl
ABC oceny technologii medycznych. Skąd się biorą ceny leków? Michał Jachimowicz Warszawa, 14 października 2014 roku MAHTA Sp. z o.o. ul. Rejtana 17/5, 02-516 Warszawa, tel.: 22 542 41 54, biuro@mahta.pl
