LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
|
|
|
- Laura Antczak
- 7 lat temu
- Przeglądów:
Transkrypt
1 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach diagnostycznych McDonalda (2010), łącznie z badaniami rezonansem magnetycznym, przed i po podaniu kontrastu; 2) w przypadku rozpoznania postaci rzutowej stwardnienia rozsianego, wystąpienie minimum 1 rzutu klinicznego albo co najmniej 1 nowe ognisko GD+ w okresie 12 miesięcy przed kwalifikacją; 3) uzyskanie co najmniej 10 punktów według punktowego systemu kwalifikacji określonego w ust. 3; 4) pisemna deklaracja współpracy przy realizacji programu ze strony pielęgniarki. Kryteria kwalifikacji muszą być spełnione łącznie Leczenie octanem glatirameru: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach diagnostycznych McDonalda (2010), łącznie z badaniami rezonansem magnetycznym, przed i po podaniu kontrastu; 2) w przypadku rozpoznania postaci rzutowej stwardnienia rozsianego, wystąpienie minimum 1 rzutu klinicznego albo co najmniej 1 nowe ognisko GD+ w okresie 12 miesięcy ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE 1. Dawkowanie oraz sposób modyfikacji dawkowania w programie: 1) dawkowanie oraz sposób modyfikacji dawkowania w leczeniu interferonem beta, peginterferonem beta- 1a, octanem glatirameru, fumaranem dimetylu, teryflunomidem lub alemtuzumabem należy prowadzić zgodnie z zapisami stosownych Charakterystyk Produktów Leczniczych,z zastrzeżeniem pkt 2 poniżej 2) dawkowanie octanu glatirameru,dla dawki 20 mg u dzieci i młodzieży: zalecane dawkowanie wynosi 20 mg octanu glatirameru we wstrzyknięciu podskórnym, raz na dobę. BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1. Badania przy kwalifikacji: 1) badania biochemiczne w tym oceniające: a) funkcje nerek, b) funkcje wątroby, c) funkcje tarczycy; 2) badanie ogólne moczu; 3) morfologia krwi z rozmazem; 4) rezonans magnetyczny przed i po podaniu kontrastu; rezonans magnetyczny wykonuje się w okresie kwalifikacji do programu. Jeżeli leczenie nie zostanie rozpoczęte w okresie 60 dni od jego wykonania to badanie powtarza się tuż przed zastosowaniem pierwszej dawki leku; 5) w przypadkach wątpliwych diagnostycznie wskazane badanie białka oligoklonalnego IgG w płynie mózgowordzeniowym. 6) test ciążowy u pacjentek w wieku rozrodczym; 7) ocena stanu neurologicznego z określeniem EDSS; 8) badania w kierunku HIV, oznaczenie jakościowe w kierunku wiremii HBV, HCV (dotyczy terapii alemtuzumabem); 9) konsultacja specjalisty ds. chorób zakaźnych lub specjalisty chorób płuc (dotyczy terapii alemtuzumabem);
2 przed kwalifikacją; 3) uzyskanie co najmniej 10 punktów według punktowego systemu kwalifikacji określonego w ust. 3; 4) pisemna deklaracja współpracy przy realizacji programu ze strony pielęgniarki; 5) kobiety ciężarne włączane są do leczenia po przekazaniu im pisemnej informacji dotyczącej aktualnego stanu wiedzy na temat bezpieczeństwa i skuteczności stosowania octanu glatirameru u kobiet w ciąży oraz po uzyskaniu pisemnej, świadomej zgody na stosowanie leku; Kryteria kwalifikacji muszą być spełnione łącznie Leczenie fumaranem dimetylu: 1) wiek od 12 roku życia z zastrzeżeniem, że a) pacjentów w wieku poniżej 18 roku życia kwalifikuje się do leczenia wyłącznie w ośrodkach zapewniających leczenie pod opieką zespołów lekarskich składających się z neurologów i neurologów dziecięcych posiadających doświadczenie w leczeniu SM; b) pacjentów w wieku poniżej 18 roku życia kwalifikuje się do leczenia pod warunkiem przekazania opiekunom chorych/chorym kwalifikowanym do terapii pisemnej informacji na temat aktualnego stanu wiedzy na temat bezpieczeństwa i skuteczności stosowania leku w tej grupie wiekowej oraz po uzyskaniu pisemnej, świadomej zgody na jego zastosowanie; 2) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach diagnostycznych McDonalda(2010), łącznie z badaniami rezonansem magnetycznym, przed i po podaniu kontrastu; 2. Monitorowanie leczenia: 2.0. Ocena stanu neurologicznego, co 3 miesiące Monitorowanie leczenia interferonem beta lub octanem glatirameru: Badania laboratoryjne, o których mowa w ust. 1 wykonywane są: a) u dorosłych: przez pierwsze 6 miesięcy leczenia - co 3 miesiące, następnie co 6 miesięcy, z wyjątkiem morfologii i parametrów wątrobowych, które wykonywane są co 3 miesiące, b) u dzieci i młodzieży: przez pierwsze 3 miesiące co miesiąc, następnie co 3 miesiące; 1) rezonans magnetyczny przed i po podaniu kontrastu po każdych 12 miesiącach leczenia; 2) badania oceniające skuteczność leczenia i umożliwiające kontynuacje leczenia w programie wykonuje się każdorazowo po 12 miesiącach leczenia Monitorowanie leczenia fumaranem dimetylu: 1) badania biochemiczne oceniające: a) funkcje nerek i wątroby - po 3 i 6 miesiącach leczenia, następnie co 6 do 12 miesięcy oraz według wskazań klinicznych, b) morfologię krwi z rozmazem- co 3 miesiące leczenia U pacjentów, u których liczba limfocytów będzie
3 3) w przypadku rozpoznania postaci rzutowej stwardnienia rozsianego, wystąpienie minimum 1 rzutu klinicznego albo co najmniej 1 nowe ognisko GD+ w okresie 12 miesięcy przed kwalifikacją; 4) uzyskanie co najmniej 10 punktów według punktowego systemu kwalifikacji określonego w ust. 3; 5) pisemna deklaracja współpracy przy realizacji programu ze strony pielęgniarki. Kryteria kwalifikacji muszą być spełnione łącznie Leczenie peginterferonem beta-1a: 1) wiek od 12 roku życia z zastrzeżeniem, że a) pacjentów w wieku poniżej 18 roku życia kwalifikuje się do leczenia wyłącznie w ośrodkach zapewniających leczenie pod opieką zespołów lekarskich składających się z neurologów i neurologów dziecięcych posiadających doświadczenie w leczeniu SM; b) pacjentów w wieku poniżej 18 roku życia kwalifikuje się do leczenia pod warunkiem przekazania opiekunom chorych/chorym kwalifikowanym do terapii pisemnej informacji na temat aktualnego stanu wiedzy na temat bezpieczeństwa i skuteczności stosowania leku w tej grupie wiekowej oraz po uzyskaniu pisemnej, świadomej zgody na jego zastosowanie; 2) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach diagnostycznych McDonalda (2010), łącznie z badaniami rezonansem magnetycznym, przed i po podaniu kontrastu; 3) w przypadku rozpoznania postaci rzutowej stwardnienia rozsianego, wystąpienie minimum 1 rzutu klinicznego albo utrzymywała się na poziomie poniżej 500/ µl przez ponad 6 miesięcy, należy ponownie rozważyć bilans korzyści i ryzyka w tym wziąć pod uwagę przerwanie leczenia. 2) rezonans magnetyczny przed i po podaniu kontrastu po każdych 12 miesiącach leczenia; 3) badania oceniające skuteczność leczenia i umożliwiające kontynuacje leczenia w programie wykonuje się każdorazowo po 12 miesiącach leczenia 2.3. Monitorowanie leczenia peginterferonem beta-1a: 1) badania laboratoryjne, o których mowa w ust. 1 wykonywane są: - przez pierwsze 6 miesięcy leczenia - co 3 miesiące, - następnie co 6 miesięcy, z wyjątkiem morfologii i parametrów wątrobowych, które wykonywane są co 3 miesiące 2) rezonans magnetyczny przed i po podaniu kontrastu po każdych 12 miesiącach leczenia; 3) badania oceniające skuteczność leczenia i umożliwiające kontynuacje leczenia w programie wykonuje się każdorazowo po 12 miesiącach leczenia 2.4. Monitorowanie leczenia teryflunomidem: 1) badania laboratoryjne, o których mowa w ust. 1 wykonywane są: a) przez pierwsze 6 miesięcy leczenia, kontrola co 3 miesiące, b) następnie co 6 miesięcy, z wyjątkiem morfologii, ciśnienia tętniczego krwi i parametrów wątrobowych, które wykonuje się co 3 miesiące; 2) rezonans magnetyczny przed i po podaniu kontrastu - po każdych 12 miesiącach leczenia;
4 co najmniej 1 nowe ognisko GD+ w okresie 12 miesięcy przed kwalifikacją; 4) uzyskanie co najmniej 10 punktów według punktowego systemu kwalifikacji określonego w ust. 3; 5) pisemna deklaracja współpracy przy realizacji programu ze strony pielęgniarki. Kryteria kwalifikacji muszą być spełnione łącznie 1.5. Leczenie teryflunomidem: 1) wiek od 12 roku życia, z zastrzeżeniem, że a) pacjentów w wieku poniżej 18 roku życia kwalifikuje się do leczenia wyłącznie w ośrodkach zapewniających leczenie pod opieką zespołów lekarskich składających się z neurologów i neurologów dziecięcych posiadających doświadczenie w leczeniu SM; b) pacjentów w wieku poniżej 18 roku życia kwalifikuje się do leczenia pod warunkiem przekazania opiekunom chorych/chorym kwalifikowanym do terapii pisemnej informacji na temat aktualnego stanu wiedzy na temat bezpieczeństwa i skuteczności stosowania leku w tej grupie wiekowej oraz po uzyskaniu pisemnej, świadomej zgody na jego zastosowanie; 2) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach diagnostycznych McDonalda (2010); łącznie z badaniami rezonansem magnetycznym, przed i po podaniu kontrastu; 3) w przypadku rozpoznania postaci rzutowej stwardnienia rozsianego, wystąpienie minimum 1 rzutu klinicznego albo co najmniej 1 nowe ognisko GD+ w okresie 12 miesięcy przed kwalifikacją; 3) badania oceniające skuteczność leczenia i umożliwiające kontynuacje leczenia w programie wykonuje się każdorazowo po 12 miesiącach leczenia Monitorowanie leczenia alemtuzumabem: 1) co miesiąc: a) morfologia krwi z rozmazem, b) oznaczenie stężenia kreatyniny w surowicy, c) badanie ogólne moczu, 2) co 3 miesiące oznaczenie hormonu tyreotropowego (TSH); 3) przed drugim podaniem leku: a) u kobiet w wieku rozrodczym test ciążowy b) badania w kierunku HIV, oznaczenie jakościowe w kierunku wiremii HBV, HCV, c) ocena stanu neurologicznego z określeniem EDSS. 4) Zalecane wykonania RM minimum co 12 miesięcy 3. Monitorowanie programu: 1) gromadzenie w dokumentacji medycznej pacjenta danych dotyczących monitorowania leczenia i każdorazowe ich przedstawianie na żądanie kontrolerów Narodowego Funduszu Zdrowia; 2) uzupełnienie danych zawartych w rejestrze (SMPT) dostępnym za pomocą aplikacji internetowej udostępnionej przez OW NFZ, z częstotliwością zgodną z opisem programu oraz na zakończenie leczenia; 3) przekazywanie informacji sprawozdawczorozliczeniowych do NFZ: informacje przekazuje się do NFZ w formie papierowej lub w formie elektronicznej, zgodnie z wymaganiami opublikowanymi przez Narodowy Fundusz Zdrowia.
5 4) uzyskanie co najmniej 10 punktów według punktowego systemu kwalifikacji określonego w ust. 3; 5) w przypadku kobiet w wieku rozrodczym stosowanie antykoncepcji; 6) pisemna deklaracja współpracy przy realizacji programu ze strony pielęgniarki. Kryteria kwalifikacji muszą być spełnione łącznie Leczenie alemtuzumabem: 1) wiek od 18 roku życia; 2) brak wcześniejszego leczenia alemtuzumabem; 3) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach diagnostycznych McDonalda (2010) łącznie z badaniami rezonansem magnetycznym, przed i po podaniu kontrastu; 4) Szybko rozwijająca się, ciężka postać choroby rozpoznawana kiedy w okresie 12 miesięcy przed kwalifikacją zostaną spełnione oba poniższe parametry: a) liczba i ciężkość rzutów: - co najmniej dwa rzuty wymagające leczenia sterydami powodujące niesprawność (w czasie rzutu wzrost EDSS o minimum 2 pkt), b) zmiany w badaniu rezonansu magnetycznego - więcej niż jedna nowa zmiana GD(+) lub - więcej niż dwie nowe zmiany w sekwencji T2 (w sumie nie mniej niż 9 zmian). 5) W przypadku kobiet w wieku rozrodczym stosowanie antykoncepcji; 7) Pisemna deklaracja współpracy przy realizacji programu ze strony pielęgniarki.
6 Kryteria kwalifikacji muszą być spełnione łącznie Dopuszcza się zamiany leków pierwszej linii (interferon beta, peginterferon beta-1a, octan glatirameru, fumaran dimetylu, teryflunomid) w przypadku wystąpienia objawów niepożądanych lub częściowej nieskuteczności terapii definiowanej jako wystąpienie jednego z kryteriów wymienionych w punkcie Do programu włączane są, bez konieczności ponownej kwalifikacji, pacjentki wyłączone z programu w związku z ciążą, które w momencie wyłączenia spełniały pozostałe kryteria przedłużenia leczenia Ponadto do programu lekowego, w celu zapewnienia kontynuacji terapii są kwalifikowani również pacjenci uprzednio leczeni interferonem beta, peginterferonem beta-1a, octanem glatirameru, fumaranem dimetylu lub teryflunomidem w ramach innego sposobu finansowania terapii, o ile na dzień rozpoczęcia terapii spełnili stosowne kryteria kwalifikacji wskazane w punktach oraz jednocześnie nie spełniali kryteriów uniemożliwiających włączenie do programu wskazanych w punktach Kryteria uniemożliwiające włączenie do programu: 2.1. Przeciwwskazaniem do stosowania interferonów beta jest wystąpienie przynajmniej jednego z poniższych przeciwwskazań: 1) nadwrażliwość na interferon beta; 2) pierwotnie lub wtórnie postępująca postać choroby; 3) zdekompensowana niewydolność wątroby (enzymy
7 wątrobowe 2 razy lub więcej powyżej normy); 4) zaburzenia czynności tarczycy (bez eutyreozy); 5) depresja nie poddająca się leczeniu; 6) próby samobójcze; 7) padaczka z wyłączeniem napadów, które u dzieci i młodzieży wystąpiły w czasie rzutu stwardnienia rozsianego; 8) leukopenia poniżej 3000/µl; 9) istotna klinicznie niedokrwistość; 10) ciąża; 11) inne przeciwwskazania wymienione w Charakterystyce Produktu Leczniczego Przeciwwskazaniem do stosowania octanu glatirameru jest wystąpienie przynajmniej jednego z poniższych przeciwskazań: 1) nadwrażliwość na octan glatirameru lub mannitol; 2) pierwotnie lub wtórnie postępująca postać choroby; 3) inne przeciwwskazania wymienione w Charakterystyce Produktu Leczniczego Przeciwwskazaniem do stosowania fumaranu dimetylu jest wystąpienie przynajmniej jednego z poniższych przeciwskazań: 1) nadwrażliwość na fumaran dimetylu lub substancje pomocnicze; 2) pierwotnie lub wtórnie postępująca postać choroby; 3) ciąża; 4) inne przeciwwskazania wymienione w Charakterystyce Produktu Leczniczego Przeciwwskazaniem do stosowania peginterferonu beta -1a jest wystąpienie przynajmniej jednego z poniższych
8 przeciwskazań: 1) nadwrażliwość na naturalny lub rekombinowany interferon beta, lub peginterferon; 2) rozpoczęcie leczenia u kobiet w ciąży; 3) aktualnie ciężkie zaburzenia depresyjne i (lub) myśli samobójcze; 4) przeciwwskazania wymienione w Charakterystyce Produktu Leczniczego; 5) pierwotnie lub wtórnie postępująca postać choroby Przeciwwskazaniem do stosowania teryflunomidu jest wystąpienie przynajmniej jednego z poniższych przeciwwskazań: 1) nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą; 2) ciężkie zaburzenia czynności wątroby (klasa C według skali Childa-Pugha); 3) ciąża, karmienie piersią lub niestosowanie skutecznych metod antykoncepcji u kobiet w wieku rozrodczym; 4) ciężkie niedobory odporności; 5) znaczne zaburzenia czynności szpiku kostnego albo znacząca niedokrwistość, leukopenia, neutropenia lub małopłytkowość: a) hematokryt < 24 % lub b) całkowita liczba białych krwinek < /µl lub c) całkowita liczba neutrofilii /µl lub d) liczba płytek krwi < /µl; 6) ciężkie, czynne zakażenia; 7) ciężkie zaburzenia czynności nerek u pacjentów
9 dializowanych; 8) ciężka hipoproteinemia Przeciwwskazaniem do stosowania alemtuzumabu jest wystąpienie przynajmniej jednego z poniższych przeciwskazań: 1) nadwrażliwość na alemtuzumab lub substancje pomocnicze; 2) zakażenie ludzkim wirusem niedoboru odporności (HIV); 3) ciąża; 4) wiremia HBV, HCV; 5) czynna gruźlica; 5) czynne zakażenia do momentu ich wyleczenia; 6) nowotwór złośliwy. 3. Punktowy system oceny i kwalifikacji do leczenia stwardnienia rozsianego interferonem beta, peginterferonem beta-1a, octanem glatirameru, fumaranem dimetylu, teryflunomidem i alemtuzumabem: 1) czas trwania choroby: a) od 0 do 3 lat - 6 pkt., b) od 3 do 6 lat - 4 pkt., c) powyżej 6 lat - 2 pkt.; 2) liczba rzutów choroby w ostatnim roku: a) 3 i więcej - 5 pkt., b) od 1 do 2-4 pkt., c) brak rzutów w trakcie leczenia immunomodulacyjnego (w ostatnim roku) - 3 pkt., d) brak rzutów - 1 pkt; 3) stan neurologiczny w okresie międzyrzutowym (przy rozpoczynaniu leczenia): a) EDSS od 0 do 2-6 pkt., b) EDSS od 2,5 do 4-5 pkt.,
10 c) EDSS od 4,5 do 5-2 pkt. 4. Kryteria wyłączenia: 4.1. Leczenie interferonem beta: 1) nadwrażliwość na interferon beta - ostre reakcje nadwrażliwości (wstrząs anafilaktyczny, skurcz oskrzeli, pokrzywka); 2) przejście w postać wtórnie postępującą- pogorszenie w skali EDSS o 1 pkt w ciągu 12 miesięcy nie związane z aktywnością rzutową; 3) stan kliniczny chorego oceniany w trakcie badania kontrolnego w skali EDSS powyżej 5,0 (w trakcie remisji); 4) ciąża; 5) zdekompensowana niewydolność wątroby (enzymy wątrobowe 5 razy lub więcej powyżej normy potwierdzone badaniem kontrolnym i utrzymujące się pomimo modyfikacji leczenia); 6) zaburzenia czynności tarczycy (bez eutyreozy); 7) istotne klinicznie zmiany skórne; 8) zmiana parametrów krwi w następującym zakresie: a) stężenie hemoglobiny poniżej 9 g/dl, b) leukopenia poniżej 3000/µl, c) limfopenia poniżej 500/µl, d) trombocytopenia poniżej 75000/µl - potwierdzone badaniem kontrolnym i utrzymujące się pomimo modyfikacji leczenia; 9) depresja niepoddająca się leczeniu; 10) padaczka, z wyłączeniem napadów występujących u dzieci i młodzieży jako objaw rzutu stwardnienia rozsianego; 11) pojawienie się innych przeciwwskazań wymienionych w Charakterystyce Produktu Leczniczego.
11 4.2. Leczenie octanem glatirameru: 1) nadwrażliwość na octan glatirameru lub mannitol; 2) przejście w postać wtórnie postępującą - pogorszenie w skali EDSS o 1 pkt w ciągu 12 miesięcy nie związane z aktywnością rzutową; 3) stan kliniczny chorego oceniany w trakcie badania kontrolnego w skali EDSS powyżej 5,0 (w trakcie remisji); 4) istotne klinicznie zmiany skórne; 5) pojawienie się innych przeciwwskazań wymienionych w Charakterystyce Produktu Leczniczego Leczenie fumaranem dimetylu: 1) nadwrażliwość na fumaran dimetylu lub substancje pomocnicze; 2) przejście w postać wtórnie postępującą- pogorszenie w skali EDSS o 1 pkt w ciągu 12 miesięcy nie związane z aktywnością rzutową; 3) stan kliniczny chorego oceniany w trakcie badania kontrolnego w skali EDSS powyżej 5,0 (w trakcie remisji); 4) ciąża. 5) pojawienie się innych przeciwwskazań wymienionych w Charakterystyce Produktu Leczniczego Leczenie peginterferonem beta-1a: 1) nadwrażliwość na naturalny lub rekombinowany interferon beta lub peginterferon albo na którąkolwiek substancję pomocniczą; 2) przejście w postać wtórnie postępującą- pogorszenie w skali EDSS o 1 pkt w ciągu 12 miesięcy nie związane z aktywnością rzutową; 3) stan kliniczny chorego oceniany w trakcie badania kontrolnego w skali EDSS powyżej 5,0 (w trakcie remisji); 5) ciąża
12 6) aktualnie ciężkie zaburzenia depresyjne i (lub) myśli samobójcze 7) pojawienie się innych przeciwwskazań wymienionych w Charakterystyce Produktu Leczniczego 4.5. Leczenie teryflunomidem: 1) nadwrażliwość na teryflunomid lub leflunomid; 2) przejście w postać wtórnie postępującą - pogorszenie w skali EDSS o 1 pkt w ciągu 12 miesięcy nie związane z aktywnością rzutową; 3) stan kliniczny chorego oceniany w trakcie badania kontrolnego w skali EDSS powyżej 5,0 (w trakcie remisji); 4) podejrzenie uszkodzenia wątroby - należy rozważyć przerwanie leczenia teryflunomidem, jeżeli potwierdzono zwiększenie aktywności enzymów wątrobowych przekraczające trzykrotnie górną granicę normy (GGN); 5) ciężkie zaburzenia czynności wątroby (klasa C według skali Childa-Pugha); 6) ciąża, karmienie piersią lub niestosowanie skutecznych metod antykoncepcji u kobiet w wieku rozrodczym; 7) ciężkie niedobory odporności; 8) znaczne zaburzenia czynności szpiku kostnego albo znacząca niedokrwistość, leukopenia, neutropenia lub małopłytkowość: a) hematokryt < 24 % lub b) całkowita liczba białych krwinek < /µl lub c) całkowita liczba neutrofilii /µl lub d) liczba płytek krwi < /µl; 9) ciężkie, czynne zakażenia; 10) ciężkie zaburzenia czynności nerek u pacjentów dializowanych; 11) ciężka hipoproteinemia.
13 4.6. Leczenie alemtuzumabem: 1) nadwrażliwość na alemtuzumab lub substancje pomocnicze; 2) nieprzestrzeganie zasad leczenia; 3) brak stabilizacji lub postęp choroby pomimo leczenia (dwa rzuty wymagające sterydoterapii lub pogorszenie o 2 punkty w EDSS w ciągu roku); 4) czynna choroba tarczycy, chyba, że potencjalne korzyści z zastosowanego leczenia usprawiedliwiają ryzyko wystąpienia autoimmunologicznej choroby tarczycy; 5) nietolerancja alemtuzumabu (ciężkie reakcje związane z infuzją, reakcje anafilaktyczne); 6) ciąża, chyba, że potencjalne korzyści dla matki z zastosowanego leczenia przewyższają potencjalne zagrożenie dla płodu; 7) zakażenie w trakcie terapii ludzkim wirusem niedoboru odporności (HIV); 8) wiremia HBV, HCV; 9) klinicznie istotna choroba autoimmunizacyjna inna niż SM; 10) czynne zakażenia do momentu ich wyleczenia; 11) nowotwór złośliwy. 5. Określenie czasu leczenia w programie: 5.1. Określenie czasu leczenia w programie interferonem beta, peginterferonem beta-1a, octanem glatirameru, fumaranem dimetylu, teryflunomidem. Po 12 miesiącach trwania leczenia dokonuje się oceny skuteczności leczenia. Za brak skuteczności wymagający zmiany leczenia przyjmuje się wystąpienie obu poniższych sytuacji: 1) liczba i ciężkość rzutów: a) 2 lub więcej rzutów umiarkowanych (wzrost EDSS o 1 do 2 pkt. w zakresie jednego lub dwóch układów
14 funkcjonalnych lub o 1 pkt w czterech lub większej liczbie układów funkcjonalnych) lub b) 1 ciężki rzut po pierwszych 6 miesiącach (wzrost w EDSS większy niż w definicji rzutu umiarkowanego tj. powyżej 2 pkt.) oraz 2) zmiany w badaniu rezonansu magnetycznego, gdy stwierdza się jedno z poniższych: a) więcej niż jedna nowa zmiana Gd (+), b) więcej niż dwie nowe zmiany w sekwencji T Określenie czasu leczenia w programie alemtuzumabem. Maksymalny czas leczenia alemtuzumabem w ramach programu obejmuje podanie 2 kursów leczenia oraz 48- miesięczny okres obserwacji od podania drugiej dawki leku Kryteria kontynuacji leczenia w programie interferonem beta, peginterferonem beta-1a, octanem glatirameru, fumaranem dimetylu, teryflunomidem: 1) terapia interferonem beta, peginterferonem beta-1a, octanem glatirameru, fumaranem dimetylu lub teryflunomidem może być przedłużona o każde kolejne 12 miesięcy u pacjentów niespełniających kryteriów wyłączenia zgodnie z pkt. 4 i kryteriów nieskuteczności pkt. 5.1; 2) leczenie powinno być stosowane tak długo jak osiągana jest skuteczność kliniczna oraz nie wystąpią kryteria wyłączenia; 3) po ukończeniu 18 r.ż. nie ma konieczności ponownej kwalifikacji pacjenta do programu po przeniesieniu leczenia do ośrodka dla dorosłych.
15
ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE 1. Dawkowanie oraz sposób modyfikacji dawkowania w programie:
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r.
 Dziennik Ustaw Nr 269 15687 Poz. 1597 1597 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na
Dziennik Ustaw Nr 269 15687 Poz. 1597 1597 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Terapeutyczne Programy Zdrowotne 2012 Leczenie stwardnienia rozsianego
 Załącznik nr 15 do zarządzenia nr 59/2011/DGL Prezesa NFZ Załącznik nr 6 do zarządzenia nr 10/2012/DGL Prezesa NFZ z dnia 15 lutego 2012 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35
Załącznik nr 15 do zarządzenia nr 59/2011/DGL Prezesa NFZ Załącznik nr 6 do zarządzenia nr 10/2012/DGL Prezesa NFZ z dnia 15 lutego 2012 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35
Terapeutyczne Programy Zdrowotne 2009 Leczenie stwardnienia rozsianego
 Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia Załącznik nr 9 do Zarządzenia Nr 16/2009 Prezesa NFZ z dnia 10 marca 2009 roku I. Cel
Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia Załącznik nr 9 do Zarządzenia Nr 16/2009 Prezesa NFZ z dnia 10 marca 2009 roku I. Cel
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Terapeutyczne Programy Zdrowotne 2008 Leczenie stwardnienia rozsianego
 załącznik nr 16 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia I.
załącznik nr 16 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE STWARDNIENIA ROZSIANEGO ICD-10 G.35 - stwardnienie rozsiane Dziedzina medycyny: neurologia I.
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1.Kryteria kwalifikacji ŚWIADCZENIOBIORCY 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1.Kryteria kwalifikacji ŚWIADCZENIOBIORCY 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Dziennik Urzędowy Ministra Zdrowia 862 Poz. 71 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji:
Dziennik Urzędowy Ministra Zdrowia 862 Poz. 71 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji:
Warszawa, dnia 29 października 2012 r. Poz. 77
 Warszawa, dnia 29 października 2012 r. Poz. 77 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu
Warszawa, dnia 29 października 2012 r. Poz. 77 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu
OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu
 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu aktów normatywnych i niektórych innych aktów
OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu aktów normatywnych i niektórych innych aktów
DZIENNIK URZĘDOWY MINISTRA ZDROWIA
 DZIENNIK URZĘDOWY MINISTRA ZDROWIA Warszawa, dnia 29 października 2012 r. Poz. 77 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy
DZIENNIK URZĘDOWY MINISTRA ZDROWIA Warszawa, dnia 29 października 2012 r. Poz. 77 OBWIESZCZENIE MINISTRA ZDROWIA 1) z dnia 29 października 2012 r. o sprostowaniu błędu Na podstawie art. 17 ust. 4 ustawy
Informacja na temat problemów osób chorych na stwardnienie rozsiane
 Warszawa, dnia 14 maja 2012 r. Informacja na temat problemów osób chorych na stwardnienie rozsiane Stwardnienie rozsiane (SM) jest jedną z najczęstszych chorób układu nerwowego (mózgu i rdzenia kręgowego).
Warszawa, dnia 14 maja 2012 r. Informacja na temat problemów osób chorych na stwardnienie rozsiane Stwardnienie rozsiane (SM) jest jedną z najczęstszych chorób układu nerwowego (mózgu i rdzenia kręgowego).
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32.a. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE
Załącznik B.32.a. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE
PROPOZYCJE ZMIAN W PROGRAMIE II LINII. Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK
 PROPOZYCJE ZMIAN W PROGRAMIE II LINII Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK PROGRAM II LINII P R O B L E M Y Z G Ł A S Z A N E W 2 0 1 7 r o k u Brak możliwości
PROPOZYCJE ZMIAN W PROGRAMIE II LINII Czy potrzebne są nowe kryteria włączenia do programu II linii? HALINA BARTOSIK-PSUJEK PROGRAM II LINII P R O B L E M Y Z G Ł A S Z A N E W 2 0 1 7 r o k u Brak możliwości
LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0)
 Załącznik B.65. LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia dazatynibem ostrej białaczki limfoblastycznej z obecnością chromosomu
Załącznik B.65. LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia dazatynibem ostrej białaczki limfoblastycznej z obecnością chromosomu
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
LECZENIE PACJENTÓW Z WRZODZIEJĄCYM ZAPALENIEM JELITA GRUBEGO (WZJG) (ICD-10 K51)
 Załącznik B.55. LECZENIE PACJENTÓW Z WRZODZIEJĄCYM ZAPALENIEM JELITA GRUBEGO (WZJG) (ICD-10 K51) ZAKRES ŚWIADCZENIA GWARANTOWANEGO 1. Kryteria włączenia ŚWIADCZENIOBIORCY Do leczenia infliksymabem mogą
Załącznik B.55. LECZENIE PACJENTÓW Z WRZODZIEJĄCYM ZAPALENIEM JELITA GRUBEGO (WZJG) (ICD-10 K51) ZAKRES ŚWIADCZENIA GWARANTOWANEGO 1. Kryteria włączenia ŚWIADCZENIOBIORCY Do leczenia infliksymabem mogą
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Dziennik Urzędowy Ministra Zdrowia 618 Poz. 51 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dziennik Urzędowy Ministra Zdrowia 618 Poz. 51 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Dziennik Urzędowy Ministra Zdrowia 615 Poz. 27 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Dziennik Urzędowy Ministra Zdrowia 615 Poz. 27 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Załącznik B.36. LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW ŚWIADCZENIOBIORCY W PROGRAMIE
Załącznik B.36. LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW ŚWIADCZENIOBIORCY W PROGRAMIE
Leczenie stwardnienia rozsianego w Polsce. Jak poprawić sytuację polskich pacjentów? Izabela Obarska Warszawa,
 Leczenie stwardnienia rozsianego w Polsce. Jak poprawić sytuację polskich pacjentów? Izabela Obarska Warszawa, 18.04.2019 Epidemiologia Polska znajduje się w pierwszej dziesiątce krajów o największym wskaźniku
Leczenie stwardnienia rozsianego w Polsce. Jak poprawić sytuację polskich pacjentów? Izabela Obarska Warszawa, 18.04.2019 Epidemiologia Polska znajduje się w pierwszej dziesiątce krajów o największym wskaźniku
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Substancja czynna finansowana w ramach programu: chlorowodorek fingolimodu Postać farmaceutyczna, dawka: kapsułka twarda 0.5 mg.
 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Dziennik Urzędowy Ministra Zdrowia 732 Poz. 71 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Dziennik Urzędowy Ministra Zdrowia 732 Poz. 71 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0)
 Załącznik B.22. LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0) WIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii dokonuje Zespół Koordynacyjny ds. Chorób Ultrarzadkich powoływany przez Prezesa Narodowego
Załącznik B.22. LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0) WIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii dokonuje Zespół Koordynacyjny ds. Chorób Ultrarzadkich powoływany przez Prezesa Narodowego
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 765 Poz. 42 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 765 Poz. 42 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 731 Poz. 66 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Dziennik Urzędowy Ministra Zdrowia 731 Poz. 66 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 719 Poz. 27 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem
Dziennik Urzędowy Ministra Zdrowia 719 Poz. 27 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem
Substancja czynna finansowana w ramach programu: chlorowodorek fingolimodu Postać farmaceutyczna, dawka: kapsułka twarda 0.5 mg.
 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4)
 Załącznik B.53..docx LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Załącznik B.53..docx LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 893 Poz. 133 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Dziennik Urzędowy Ministra Zdrowia 893 Poz. 133 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 738 Poz. 42 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Dziennik Urzędowy Ministra Zdrowia 738 Poz. 42 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Dziennik Urzędowy Ministra Zdrowia 809 Poz. 133
 Dziennik Urzędowy Ministra Zdrowia 809 Poz. 133 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA
Dziennik Urzędowy Ministra Zdrowia 809 Poz. 133 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA
Dziennik Urzędowy Ministra Zdrowia 665 Poz. 42
 Dziennik Urzędowy Ministra Zdrowia 665 Poz. 42 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA
Dziennik Urzędowy Ministra Zdrowia 665 Poz. 42 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA
LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20)
 Dziennik Urzędowy Ministra Zdrowia 511 Poz. 42 Załącznik B.4. LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie zaawansowanego
Dziennik Urzędowy Ministra Zdrowia 511 Poz. 42 Załącznik B.4. LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie zaawansowanego
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem A. Leczenie sildenafilem pacjentów
Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem A. Leczenie sildenafilem pacjentów
LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48)
 Dziennik Urzędowy Ministra Zdrowia 492 Poz. 66 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Dziennik Urzędowy Ministra Zdrowia 492 Poz. 66 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
LECZENIE RAKA NERKI (ICD-10 C 64)
 Załącznik B.10. LECZENIE RAKA NERKI (ICD-10 C 64) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1 2 3 1. Leczenie
Załącznik B.10. LECZENIE RAKA NERKI (ICD-10 C 64) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1 2 3 1. Leczenie
ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67)
 Załącznik B.15. ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii pierwotnej i wtórnej
Załącznik B.15. ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii pierwotnej i wtórnej
LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4)
 Załącznik B.53. LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Załącznik B.53. LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
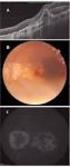 Dziennik Urzędowy Ministra Zdrowia 761 Poz. 48 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY afliberceptem
Dziennik Urzędowy Ministra Zdrowia 761 Poz. 48 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY afliberceptem
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
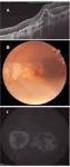 Dziennik Urzędowy Ministra Zdrowia 882 Poz. 79 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Dziennik Urzędowy Ministra Zdrowia 882 Poz. 79 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Substancja czynna finansowana w ramach programu: chlorowodorek fingolimodu Postać farmaceutyczna, dawka: kapsułka twarda 0.5 mg.
 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
Substancja czynna finansowana w ramach programu: chlorowodorek fingolimodu Postać farmaceutyczna, dawka: kapsułka twarda 0.5 mg.
 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0)
 Załącznik B.47. LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) Kwalifikacja do programu ŚWIADCZENIOBIORCY A. Kryteria kwalifikacji do leczenia ustekinumabem albo adalimumabem w ramach
Załącznik B.47. LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) Kwalifikacja do programu ŚWIADCZENIOBIORCY A. Kryteria kwalifikacji do leczenia ustekinumabem albo adalimumabem w ramach
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA W TROBY TYPU B (ICD-10 B 18.1)
 Załącznik B.1. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA W TROBY TYPU B (ICD-10 B 18.1) ZAKRES WIADCZENIA GWARANTOWANEGO WIADCZENIOBIORCY 1. Kryteria kwalifikacji 1.1. Do programu są kwalifikowani świadczeniobiorcy
Załącznik B.1. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA W TROBY TYPU B (ICD-10 B 18.1) ZAKRES WIADCZENIA GWARANTOWANEGO WIADCZENIOBIORCY 1. Kryteria kwalifikacji 1.1. Do programu są kwalifikowani świadczeniobiorcy
LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45)
 Załącznik B.44. LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie ciężkiej
Załącznik B.44. LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie ciężkiej
LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48)
 Dziennik Urzędowy Ministra Zdrowia 546 Poz. 71 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Dziennik Urzędowy Ministra Zdrowia 546 Poz. 71 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE 1. Fingolimod
 Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
Załącznik B.46. LECZENIE STWARDNIENIA ROZSIANEGO PO NIEPOWODZENIU TERAPII LEKAMI PIERWSZEGO RZUTU LUB SZYBKO ROZWIJAJĄCEJ SIĘ CIĘŻKIEJ POSTACI STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.
LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD 10: L40.0)
 Załącznik B.47. LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD 10: L40.0) ŚWIADCZENIOBIORCY Kwalifikacja do programu A. Kryteria kwalifikacji do leczenia ustekinumabem w ramach programu 1.Do programu
Załącznik B.47. LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD 10: L40.0) ŚWIADCZENIOBIORCY Kwalifikacja do programu A. Kryteria kwalifikacji do leczenia ustekinumabem w ramach programu 1.Do programu
LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0)
 Załącznik B.47. LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) A. Kryteria kwalifikacjiś WIADCZENIOBIORCY 1. Pacjent jest kwalifikowany do programu przez Zespół Koordynacyjny
Załącznik B.47. LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) A. Kryteria kwalifikacjiś WIADCZENIOBIORCY 1. Pacjent jest kwalifikowany do programu przez Zespół Koordynacyjny
FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ
 FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ Prof. dr hab. med. Halina Bartosik - Psujek Katedra i Klinika Neurologii Uniwersytet Medyczny w Lublinie LEKI I RZUTU PREPARATY INTERFERONU
FARMAKOTERAPIA STWARDNIENIA ROZSIANEGO TERAŹNIEJSZOŚĆ I PRZYSZŁOŚĆ Prof. dr hab. med. Halina Bartosik - Psujek Katedra i Klinika Neurologii Uniwersytet Medyczny w Lublinie LEKI I RZUTU PREPARATY INTERFERONU
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.
 Dziennik Urzędowy Ministra Zdrowia 701 Poz. 9 Załącznik B.64. LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.9)
Dziennik Urzędowy Ministra Zdrowia 701 Poz. 9 Załącznik B.64. LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.9)
LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45)
 Załącznik B.44. LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie ciężkiej
Załącznik B.44. LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie ciężkiej
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej (wysiękowej) postaci afliberceptem
Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej (wysiękowej) postaci afliberceptem
LECZENIE CHOROBY LE NIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LE NIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES WIADCZENIA GWARANTOWANEGO WIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
Załącznik B.32. LECZENIE CHOROBY LE NIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES WIADCZENIA GWARANTOWANEGO WIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
LECZENIE CHORYCH NA OPORNEGO LUB NAWROTOWEGO SZPICZAKA PLAZMOCYTOWEGO (ICD10 C90.0)
 Załącznik B.54. LECZENIE CHORYCH NA OPORNEGO LUB NAWROTOWEGO SZPICZAKA PLAZMOCYTOWEGO (ICD10 C90.0) ŚWIADCZENIOBIORCY 1. Leczenie lenalidomidem chorych na opornego lub nawrotowego szpiczaka plazmocytowego.
Załącznik B.54. LECZENIE CHORYCH NA OPORNEGO LUB NAWROTOWEGO SZPICZAKA PLAZMOCYTOWEGO (ICD10 C90.0) ŚWIADCZENIOBIORCY 1. Leczenie lenalidomidem chorych na opornego lub nawrotowego szpiczaka plazmocytowego.
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka szpikowa
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka szpikowa
LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.
 Załącznik B.64. LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.9) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY
Załącznik B.64. LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.9) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3)
 Dziennik Urzędowy Ministra Zdrowia 904 Poz. 133 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie
Dziennik Urzędowy Ministra Zdrowia 904 Poz. 133 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3) ŚWIADCZENIOBIORCY 1. Leczenie
LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45)
 Załącznik B.44. LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie ciężkiej
Załącznik B.44. LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie ciężkiej
LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45)
 Załącznik B.44. LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie ciężkiej
Załącznik B.44. LECZENIE CIĘŻKIEJ ASTMY ALERGICZNEJ IGE ZALEŻNEJ (ICD-10 J 45.0) ORAZ CIĘŻKIEJ ASTMY EOZYNOFILOWEJ (ICD-10 J 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie ciężkiej
LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.
 Dziennik Urzędowy Ministra Zdrowia 879 Poz. 133 Załącznik B.64. LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.9)
Dziennik Urzędowy Ministra Zdrowia 879 Poz. 133 Załącznik B.64. LECZENIE HORMONEM WZROSTU NISKOROSŁYCH DZIECI URODZONYCH JAKO ZBYT MAŁE W PORÓWNANIU DO CZASU TRWANIA CIĄŻY (SGA lub IUGR) (ICD-10 R 62.9)
LECZENIE RAKA NERKI (ICD-10 C 64)
 Dziennik Urzędowy Ministra Zdrowia 538 Poz. 86 Załącznik B.10. LECZENIE RAKA NERKI (ICD-10 C 64) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE
Dziennik Urzędowy Ministra Zdrowia 538 Poz. 86 Załącznik B.10. LECZENIE RAKA NERKI (ICD-10 C 64) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE
21. Leczenie przewlekłego wirusowego zapalenia wątroby typu B (ICD-10 B 18.1)
 Załącznik do rozporządzenia Ministra Zdrowia z dnia 28 października 2011 r. 21. Leczenie przewlekłego wirusowego zapalenia wątroby typu B (ICD-10 B 18.1) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji 1.1.
Załącznik do rozporządzenia Ministra Zdrowia z dnia 28 października 2011 r. 21. Leczenie przewlekłego wirusowego zapalenia wątroby typu B (ICD-10 B 18.1) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji 1.1.
Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
 Załącznik nr 10 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny:
Załącznik nr 10 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny:
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Dziennik Urzędowy Ministra Zdrowia 624 Poz. 71 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dziennik Urzędowy Ministra Zdrowia 624 Poz. 71 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 12 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4,
Załącznik nr 12 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4,
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r.
 Dziennik Ustaw Nr 269 15678 Poz. 1593 1593 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na podstawie
Dziennik Ustaw Nr 269 15678 Poz. 1593 1593 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na podstawie
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C (ICD-10 B 18.2)
 Załącznik B.2. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C (ICD-10 B 18.2) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji 1.1. Do programu kwalifikowani są świadczeniobiorcy
Załącznik B.2. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C (ICD-10 B 18.2) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji 1.1. Do programu kwalifikowani są świadczeniobiorcy
LECZENIE CHOROBY LE NIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LE NIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES WIADCZENIA GWARANTOWANEGO WIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
Załącznik B.32. LECZENIE CHOROBY LE NIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES WIADCZENIA GWARANTOWANEGO WIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0)
 Załącznik B.47. LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) A. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1. Podczas pierwszej kwalifikacji do programu oraz gdy jest to
Załącznik B.47. LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) A. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1. Podczas pierwszej kwalifikacji do programu oraz gdy jest to
LECZENIE RAKA NERKI (ICD-10 C 64)
 Załącznik B.10. LECZENIE RAKA NERKI (ICD-10 C 64) ZAKRES WIADCZENIA GWARANTOWANEGO WIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1 2 3 1. Leczenie
Załącznik B.10. LECZENIE RAKA NERKI (ICD-10 C 64) ZAKRES WIADCZENIA GWARANTOWANEGO WIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1 2 3 1. Leczenie
Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010
 Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010 1. Leczeniem powinni być objęci chorzy z ostrym, przewlekłym zapaleniem wątroby oraz wyrównaną
Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010 1. Leczeniem powinni być objęci chorzy z ostrym, przewlekłym zapaleniem wątroby oraz wyrównaną
LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka
Załącznik B.14. LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C (ICD-10 B 18.2)
 Dziennik Urzędowy Ministra Zdrowia 540 Poz. 71 Załącznik B.2. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C (ICD-10 B 18.2) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji
Dziennik Urzędowy Ministra Zdrowia 540 Poz. 71 Załącznik B.2. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C (ICD-10 B 18.2) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji
Załącznik do rozporządzenia Ministra Zdrowia z dnia 18 lutego 2011 r. 21. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU B (ICD-10 B 18.
 ŚWIADCZENIOBIORCY 1. Kryteria Kwalifikacji 1.1. Do programu są kwalifikowani świadczeniobiorcy w wieku powyżej 3 lat, chorzy na przewlekłe wirusowe zapalenie wątroby typu B, charakteryzujący się obecnością
ŚWIADCZENIOBIORCY 1. Kryteria Kwalifikacji 1.1. Do programu są kwalifikowani świadczeniobiorcy w wieku powyżej 3 lat, chorzy na przewlekłe wirusowe zapalenie wątroby typu B, charakteryzujący się obecnością
LECZENIE NIEDOKRWISTOŚCI W PRZEBIEGU PRZEWLEKŁEJ NIEWYDOLNOŚCI
 Nazwa programu: Terapeutyczne Programy Zdrowotne 2008 załącznik nr 18 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. LECZENIE NIEDOKRWISTOŚCI W PRZEBIEGU PRZEWLEKŁEJ NIEWYDOLNOŚCI
Nazwa programu: Terapeutyczne Programy Zdrowotne 2008 załącznik nr 18 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. LECZENIE NIEDOKRWISTOŚCI W PRZEBIEGU PRZEWLEKŁEJ NIEWYDOLNOŚCI
LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2
 załącznik nr 11 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
załącznik nr 11 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r.
 Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r. ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
Załącznik B.70. LECZENIE NEOWASKULARNEJ (WYSIĘKOWEJ) POSTACI ZWYRODNIENIA PLAMKI ZWIĄZANEGO Z WIEKIEM (AMD) (ICD-10 H35.3). Ważne: od dnia 01 stycznia 2017 r. ŚWIADCZENIOBIORCY 1. Leczenie neowaskularnej
LECZENIE CHOROBY GAUCHERA ICD-10 E
 załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
Nazwa programu: LECZENIE RAKA WĄTROBOKOMÓRKOWEGO
 Załącznik nr 48 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE RAKA WĄTROBOKOMÓRKOWEGO ICD-10 C 22.0 Rak komórek wątroby Dziedzina medycyny: Onkologia
Załącznik nr 48 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE RAKA WĄTROBOKOMÓRKOWEGO ICD-10 C 22.0 Rak komórek wątroby Dziedzina medycyny: Onkologia
