Agencja Oceny Technologii Medycznych
|
|
|
- Władysława Brzozowska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Agencja Oceny Technologii Medycznych Rekomendacja nr 229/2014 z dnia 13 października 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację produktu leczniczego Nalcrom (acidum cromoglicicum), kapsułki a 100 mg, we wskazaniu: alergia pokarmowa, wieloważna oraz atopowe zapalenie skóry o ciężkim przebiegu Prezes Agencji nie rekomenduje wydawania zgód na refundację produktu leczniczego Nalcrom (acidum cromoglicicum), kapsułki a 100 mg, we wskazaniu: alergia pokarmowa, wieloważna oraz atopowe zapalenie skóry o ciężkim przebiegu. Uzasadnienie rekomendacji Prezes Agencji, przychylając się do stanowiska Rady Przejrzystości uważa, że brak jest wysokiej jakości badań klinicznych dotyczących stosowania kromoglikanu sodu w ocenianych wskazaniach, natomiast wyniki badań niższej jakości są niejednoznaczne. W przypadku atopowego zapalenia skóry, rekomendacje kliniczne nie odnoszą się lub nie zalecają kromoglikanu sodu w tym wskazaniu. Także eksperci kliniczni nie popierają finansowania ocenianego leku w atopowym zapaleniu skóry, wskazując na brak przesłanek potwierdzających jego skuteczność. W przypadku alergii pokarmowej, jeden z ekspertów widzi miejsce ocenianej technologii w praktyce klinicznej w ramach uzupełnienia leczenia dietetycznego ciężkich alergii wielopokarmowych z objawami ze strony przewodu pokarmowego. Jednakże stanowisko to nie znalazło poparcia w wytycznych klinicznych, gdyż tylko jedna z ośmiu rekomendacji wskazuje na możliwy niewielki efekt kromoglikanu sodu w alergii pokarmowej (w alergicznym eozynofilowym zapaleniu przełyku / żołądka i jelit). Nie odnaleziono również rekomendacji refundacyjnych odnoszących się do finansowania kromoglikanu sodu (Nalcrom) w ocenianych wskazaniach. Przedmiot wniosku Produkt leczniczy Nalcrom nie jest dopuszczony do obrotu w Polsce i nie znajduje się na listach refundacyjnych, może być jednak sprowadzany z zagranicy, jeżeli jego zastosowanie jest niezbędne dla ratowania życia lub zdrowia pacjenta, na warunkach i w trybie określonym w art. 4 ustawy z dnia 6 września 2001 r. Prawo farmaceutyczne, tj. na podstawie zapotrzebowania wystawianego przez szpital albo lekarza prowadzącego leczenie poza szpitalem, potwierdzone przez konsultanta z danej dziedziny medycyny. Minister Zdrowia może wydać zgodę na refundację sprowadzanego leku Agencja Oceny Technologii Medycznych ul. I. Krasickiego 26, Warszawa tel fax sekretariat@aotm.gov.pl
2 na podstawie art. 39 ustawy o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych (dalej: ustawy o refundacji). Problem zdrowotny Alergia pokarmowa wieloważna jest to nadwrażliwość o podłożu immunologicznym, objawiająca się niepożądanymi reakcjami organizmu po przyjęciu pokarmów należących do różnych grup produktów spożywczych. Z epidemiologicznego punktu widzenia problem alergii pokarmowych nie jest obecnie dokładnie poznany. Istnieją jedynie przybliżone dane, co wynika z faktu, że brak jest do chwili obecnej uniwersalnego testu laboratoryjnego rozstrzygającego jednoznacznie o istnieniu choroby. Częstość tej dolegliwości różnie kształtuje się w zależności od wieku i płci badanych osób. Światowa Organizacja Zdrowia (WHO) uznała alergię pokarmową za problem zdrowotny dotykający 1 3% dorosłych oraz 4 6% dzieci. Dwukrotnie częściej objawy nadwrażliwości na pokarmy stwierdzane są u kobiet. Brak jest dokładnych danych epidemiologicznych na temat alergii wieloważnej. Przyczyną pojawienia się objawów klinicznych może być każdy alergen pokarmowy. Zjawisko polialergii jest zazwyczaj konsekwencją osobniczego podłoża atopowego i dotyczy starszych dzieci ze współistniejącą alergią pokarmową i wziewną oraz wielonarządową manifestacją tego uczulenia. Wyróżniamy alergię wieloważną typu natychmiastowego i opóźnionego. Szczególnym przejawem alergii wieloważnej jest alergia krzyżowa. Występuje u osób uczulonych na pyłki roślin, po spożyciu niektórych warzyw lub owoców, objawiająca się najczęściej pod postacią zespołu jamy ustnej (ang. oral allergy syndrome, OAS), ale może dotyczyć całego ustroju zespół pyłkowo-pokarmowy (ang. pollen-food allergy syndorme, PFS). Leczeniem z wyboru w każdym przypadku udowodnionej alergii bądź nietolerancji pokarmowej jest dieta eliminacyjna, czyli czasowe lub stałe usunięcie z żywienia chorej osoby szkodliwego lub źle tolerowanego pokarmu lub składnika pokarmowego z jednoczasowym wprowadzeniem w to miejsce składników zastępczych o równoważnych wartościach odżywczych. Czas i rodzaj stosowanej diety eliminacyjnej ustala się indywidualnie dla każdego przypadku klinicznego (najczęściej 12 miesięcy). Leczenie farmakologiczne jest jedynie elementem wspomagającym prawidłowo prowadzonego leczenia dietetycznego. Atopowe zapalenie skóry (AZS) to choroba zapalna skóry o przebiegu przewlekłym lub nawrotowym, któremu towarzyszy nasilony świąd oraz charakterystyczne zmiany skórne. Dane epidemiologiczne szacują, że 10-15% populacji krajów zachodnich cierpi na AZS. Choroba objawia się głównie w okresie dzieciństwa. W Polsce choruje 4,7% dzieci między 3 a 8 r.ż., natomiast chorzy dorośli stanowią 1,4%. Brak jest danych określających liczbę osób chorujących na AZS o ciężkim przebiegu. AZS jest chorobą o podłożu genetycznym zależnym od osobniczych skłonności do atopii i wieloczynnikowej etiologii. Dodatkowo na rozwój choroby wpływają czynniki środowiskowe. Do chwili obecnej nie ustalono jednorodnych zasad postepowania. Dobór terapii zależy od wieku pacjenta oraz stopnia nasilenia zmian chorobowych. Terapia AZS ze względu na przewlekły charakter i wieloczynnikową patogenezę jest bardzo trudna. Polega głównie na leczeniu objawowym, przeciwzapalnym i wzmacniającym uszkodzoną naturalną warstwę skóry. Leczenie farmakologiczne obejmuje leczenie miejscowe zmienionej chorobowo skóry oraz leczenie ogólne. Leczenie miejscowe u chorych z AZS ma na celu uzyskanie remisji ostrego stanu zapalnego skóry, a następnie uzyskanie stabilizacji choroby. W leczeniu miejscowym stosowane są emolienty, glikokortykosteroidy oraz niesteroidowe leki immunosupresyjne takie jak tackrolimus, pimecrolimus. W leczeniu ogólnym używane są leki przeciwhistaminowe II generacji. W ostrych stanach AZS podawane są przez krótki okres czasu doustnie glikokortykosteroidy; cyklosporyna A i MMF (mykofenolat mofetilu) jako leki immunosupresyjne. Obok farmakoterapii można także zastosować fototerapię. 2
3 Opis wnioskowanego świadczenia Rekomendacja nr 229/2014 Prezesa AOTM z dnia 13 października 2014 r. Produkt leczniczy Nalcrom zawiera substancję czynną kromoglikan sodu (SCG) i zgodnie z klasyfikacją ATC jest zaliczany do grupy: Leki przeciwalergjczne, z wyjątkiem kortykosteroidów (kod ATC A07EB01). Mechanizm działania tej substancji czynnej opiera się na stabilizacji błony komórkowej mastocytów (komórek tucznych). Zgodnie z Charakterystyką Produktu Leczniczego Nalcrom wskazany jest w alergii pokarmowej (gdzie przeprowadzono odpowiednie badania w celu określenia wrażliwości na jeden lub więcej alergenów spożywczych), w połączeniu z ograniczeniem głównych alergenów przyczynowych w diecie. Alternatywne technologie medyczne Zgodnie z opinią ekspertów klinicznych rekomendowanym postępowaniem w AZS są stosowane miejscowo glikokortykosteroidy i inhibitory kalcyneuryny, a także doustnie leki antyhistaminowe i GKS, zaś w przypadku alergii pokarmowej eksperci wymieniają przede wszystkim dietę eliminacyjną. Rekomendacje zagranicznych towarzystw naukowych i organizacji ochrony zdrowia zalecają w przypadku atopowego zapalenia skóry specjalną pielęgnację skóry (głównie używanie emolientów) i bandażowanie (na sucho i na mokro). W miejscowym leczeniu zaleca się stosowanie kortykosteroidów i w wybranych przypadkach inhibitorów kalcyneuryny. W leczeniu atopowego zapalenia skóry, szczególnie w ciężkich przypadkach, zastosowanie może znaleźć także fototerapia i leczenie systemowe. Główne zalecenia w zagranicznych wytycznych w leczeniu alergii pokarmowych dotyczą unikania spożywania uczulających pokarmów (a także tych, które mogą wywołać reakcję krzyżową), zaleca się stosowanie mieszanek zastępczych u małych dzieci, stosowanie leków przeciwhistaminowych w przypadku lekkich objawów alergii pokarmowej, zaś w przypadku ciężkich objawów - podanie adrenaliny. Skuteczność kliniczna Brak jest wysokiej jakości randomizowanych badań klinicznych oceniających stosowanie kromoglikanu sodu w ocenianych wskazaniach. Odnalezione badania o niskiej wiarygodności w odmienny sposób prezentują wyniki, które także częściowo się wykluczają, ale wskazują na miejsce ocenianej technologii w leczeniu AZS i alergii pokarmowej. Należy przy tym zaznaczyć, że zlecenie Ministerstwa Zdrowia dotyczy alergii pokarmowej wieloważnej oraz atopowego zapalenia skóry o ciężkim przebiegu, jednakże zastosowanie tak szczegółowego wyszukiwania w medycznych bazach danych nie było możliwe do realizacji, dlatego też przeprowadzono szerokie wyszukiwanie dotyczące wskazania głównego tj. alergii pokarmowej oraz atopowego zapalenia skóry, a jego wyniki przedstawiono poniżej. Atopowe zapalenie skóry W ramach systematycznego przeglądu dowodów naukowych nie zidentyfikowano przeglądów systematycznych z metaanalizą lub bez, oceniających skuteczność kromoglikanu sodu w leczeniu AZS. Natomiast odnaleziono i włączono do analizy jedną publikację stanowiącą przegląd badań dotyczących skuteczności kromoglikanu sodu w leczeniu AZS u dzieci (Businco 1991), przy czym nie opisano w niej metodologii przeprowadzonego wyszukiwania i selekcji doniesień. Przegląd Businco 1991 obejmował 12 badań, w tym: 5 badań otwartych (Shaw 1975, Molkhou 1976, Cavagni 1981, Harries 1983, Boner 1985), 1 pojedynczo zaślepione (Corrias 1985), 6 podwójnie zaślepionych (Atherton 1982, Molkhou 1982, Giannetti 1984, Graham 1984, Businco 1986, Burks 1988). Populację stanowiły dzieci z AZS - łącznie 281 pacjentów w wieku od 0,5 roku do 15 lat. Czas terapii wahał się w badaniach od 1 tygodnia do 3 miesięcy. Dawkowanie w większości badań 3
4 podawano w mg na dobę ( mg), jednak w trzech badaniach stosowano dawkowanie na kg m.c. na dobę (40 mg). Wyniki przeglądu Businco 1991 wskazują, że cztery z pięciu badań otwartych prezentują pozytywne wyniki terapii SCG w AZS u dzieci, w jednym badaniu nie wskazano ani na skuteczność ani na nieskuteczność terapii. Badania podwójnie zaślepione były pozytywne dla skuteczności SCG w 3 przypadkach i negatywne również w 3 przypadkach. Ponadto do analizy włączono dwa badania pierwotne Badanie Lindskov 1983 stanowiło randomizowaną, podwójnie zaślepioną, kontrolowaną placebo próbę typu cross-over, do której włączano pacjentów z ciężkim i rozpowszechnionym AZS, zarówno dorosłych, jak i dzieci. Włączono 10 dzieci i 14 osób dorosłych. W ocenie subiektywnej (pacjentów/opiekunów), nie zaobserwowano różnic istotnych statystycznie pomiędzy SCG i placebo w zakresie świądu w ciągu dnia i ciężkości egzemy. U dorosłych świąd w nocy był znamiennie zmniejszony (p <0,05) po pierwszych 3 tyg. leczenia SCG w porównaniu z analogicznym okresem w grupie placebo, a także był znamiennie zmniejszony (p <0,05) po kolejnych 3 tyg. leczenia placebo w porównaniu z SCG. W ramach oceny klinicznej nie odnotowano różnic istotnych statystycznie, z wyjątkiem egzemy po 6 tyg. leczenia, gdzie wykazano istotną statystycznie różnicę na korzyć SCG (p <0,05). Badanie Daugbjerg 1984 stanowiło podwójnie zaślepioną, kontrolowaną placebo próbę typu crossover, do której włączano pacjentów ze zróżnicowanym stopniem zaawansowania AZS spowodowanym alergią pokarmową. Włączono 34 pacjentów w wieku od 1 do 23 lat, z czego 16 miało łagodne, 16 umiarkowane, a 2 ciężkie AZS. Subiektywna ocena na podstawie wyniku z dzienniczka obserwacyjnego (diary card symptom scores) wykazała, że generalnie nie było różnic istotnych statystycznie w efektach leczenia, choć zaobserwowano znaczące różnice dla indywidualnych sekwencji leczenia na rzecz placebo. Ocena kliniczna była zgodna z subiektywną: generalnie nie było różnic istotnych statystycznie w efektach leczenia, choć w sekwencji SCG-placebo zaobserwowano znaczące różnice na rzecz placebo. Alergia pokarmowa W ramach systematycznego przeglądu dowodów naukowych nie zidentyfikowano przeglądów systematycznych z metaanalizą lub bez, oceniających skuteczność kromoglikanu sodu w leczeniu alergii pokarmowej. Do analizy klinicznej dla tego wskazania włączono dwa badania pierwotne. Badanie Dannaeus 1977 stanowiło randomizowaną, podwójnie zaślepioną, kontrolowaną placebo próbę typu cross-over, w której porównywano aktywne leczenie kromoglikanem sodu z placebo (glukoza) u dzieci z historią alergii pokarmowej. Do badania włączono 20 pacjentów w wieku 1-15 lat, którzy mieli alergię na wiele pokarmów różnego rodzaju, z czego najczęstszymi była alergia na: jaja (11), ryba (6), owoce i orzechy (10), warzywa (8), mleko (2), czekolada (3), barwniki i penicylina (4). Zarówno w ocenie rodziców, jak i klinicystów, preferowanym okresem leczenia był ten w którym podawano SCG (p < 0,05). Średnie wyniki dla objawów podczas pierwszych dwóch tyg. każdego leczenia nie wykazały istotnej statystycznie różnicy pomiędzy SCG i placebo, ale u 5 dzieci zauważono znaczącą ulgę w objawach skórnych podczas leczenia SCG. Średnie wyniki w objawach dla tygodnia, w którym eksponowano uczestników na alergen, były niższe dla SCG, ale różnica nie była istotna statystycznie. Badaniem prospektywnym Żur 2001 objęto grupę 54 dzieci z rozpoznaniem alergii pokarmowej, w wieku od 6 do 36 miesiąca życia. Grupę dobierano losowo, stosując leczenie kromoglikanem disodowym lub ketotifenem, w zależności od kolejności zgłaszania się do lekarza udzielającego pierwszej porady lekarskiej. 4
5 Po przeprowadzonym leczeniu uzyskano istotną statystycznie poprawę stanu klinicznego pacjentów, zarówno w grupie pacjentów leczonych kromoglikanem, jak i ketotifenem. Raportowano zmianę wartości punktowej SCORE ze średniej 9,68 przed leczeniem na 3,84 po leczeniu kromoglikanem (p < 0,00001). Podobne wyniki, uzyskano w grupie leczonej ketotifenem - zmiana wartości SCORE ze średniej 8,62 przed leczeniem na 3,03 po leczeniu (p < 0,00001). Autorzy dokonali także zbiorczej analizy uzyskanych wyników leczenia u dzieci z różnymi objawami klinicznymi alergii pokarmowej. Średnie wartości SCORE przed leczeniem w stosunku do wartości po leczeniu, zarówno kromoglikanem sodu jak i ketotifenem, w odniesieniu do objawów wielonarządowych i ze strony przewodu pokarmowego różnią się znamiennie statystycznie (p < 0,001 i p < 0,0001). Również u pacjentów z alergicznymi zmianami skórnymi leczonych ketotifenem uzyskano znamienną statystycznie poprawę (p < 0,0002). Jednakże nie wykazano takiej różnicy u dzieci z objawami skórnymi leczonych kromoglikanem (p < 0,14). Skuteczność praktyczna Nie odnaleziono dowodów naukowych dokumentujących skuteczność praktyczną wnioskowanej technologii. Bezpieczeństwo stosowania Zgodnie z Charakterystyką Produktu leczniczego (ChPL) Nalcrom odnotowano w kilku przypadkach nudności, wysypki skórne i bóle stawów. Zdarzenia niepożądane przedstawione w ChPL są zgodne z tymi raportowanymi w badaniach włączonych do analizy. Wpływ na budżet płatnika publicznego Dane Ministerstwa Zdrowia zostały podane łącznie do obydwu wnioskowanych wskazań tj. alergia pokarmowa wieloważna oraz atopowe zapalenie skóry o ciężkim przebiegu. Dane te wskazują, że w 2012 roku zostało wydanych 11 zgód na refundację, zaś w pierwszym półroczu 2013 roku 8 zgód. Wartość zgód wydanych na refundację wyniosła łącznie PLN w 2012 r. i PLN w 2013 r. (pierwsze półrocze). Produkt był importowany z Włoch, Szwajcarii i Wielkiej Brytanii. Omówienie rekomendacji wydanych w innych krajach w odniesieniu do ocenianej technologii Odnaleziono 8 rekomendacji klinicznych dotyczących alergii pokarmowej oraz 12 odnoszących się do leczenia atopowego zapalenia skóry. Żadne odnalezione wytyczne kliniczne nie rekomendowały zastosowania kromoglikanu sodu w postaci doustnej w leczeniu AZS o ciężkim przebiegu oraz alergii pokarmowej wieloważnej. W przypadku AZS, dwie rekomendacje (Ring 2012 i EDF) odnosiły się do stosowania miejscowego stabilizatorów mastocytów (topical mast cell stabillizers), nie rekomendując jednocześnie terapii z uwagi na brak wystarczającej ilości dowodów w postaci randomizowanych badań klinicznych uzasadniających stosowanie stabilizatorów mastocytów w leczeniu świądu w AZS (atopic eczema ich) (poziom 2b, B). Natomiast japońska rekomendacja (JDA 2009) wymienia kromoglikan sodu (bez określenia postaci leku) wśród leków antyalergicznych nie posiadających antyhistaminowego efektu działania. Jednakże autorzy publikacji nie uznają tej terapii za standardowe leczenie. Zaznaczają, że skuteczność terapii niestandardowych jest dochodzona tylko w niektórych ośrodkach oraz większość ich skuteczności nie jest udowodniona naukowo, dlatego autorzy nie przedstawiają ich w wytycznych, które poświęcono podstawowemu leczeniu atopowego zapalenia skóry. W zakresie alergii pokarmowej, jedna rekomendacja singapurskiego Ministerstwa Zdrowia (MoH Singapore 2010) wskazuje, że istnieją ograniczone korzyści ze stosowania m.in. kromoglikanu sodu 5
6 (bez określenia postaci leku) w przypadku alergicznego eozynofilowego zapalenia przełyku oraz eozynofilowego zapalenia żołądka i jelit, jednak nie jest to leczenie z wyboru. (grade D, level 3). Nie odnaleziono żadnej rekomendacji refundacyjnej odnoszącej się do finansowania kromoglikanu sodu (Nalcrom). Niniejszy produkt znaleziono na listach refundacyjnych w następujących krajach: Czechy, Szwajcaria. Podstawa przygotowania rekomendacji Rekomendacja została przygotowana na podstawie zlecenia Ministra Zdrowia z dnia r. (znak: MZ- PLD /AL/13r.), w sprawie zbadania zasadności wydawania zgody na refundację produktu leczniczego Nalcrom (acidum cromoglicicum), kapsułki a 100 mg, we wskazaniu: alergia pokarmowa, wieloważna oraz atopowe zapalenie skóry o ciężkim przebiegu, na podstawie art. 31e ust. 1 ustawy o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych (Dz. U. z 2004 r. Nr 210, poz. 2135, z późn. zm.) i w związku z art. 39 ust. 3 ustawy z dnia 12 maja 2011 r. o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych (Dz. U. Nr 122, poz. 696, z późn. zm.), po uzyskaniu stanowiska Rady Przejrzystości nr 301/2014 z dnia 13 października 2014 r. w sprawie zasadności wydawania zgody na refundację produktu leczniczego Nalcrom (acidum cromoglicicum) we wskazaniach: alergia pokarmowa wieloważna oraz atopowe zapalenie skóry o ciężkim przebiegu. Piśmiennictwo 1. Stanowisko Rady Przejrzystości nr 301/2014 z dnia 13 października 2014 r. w sprawie zasadności wydawania zgody na refundację produktu leczniczego Nalcrom (acidum cromoglicicum) we wskazaniach: alergia pokarmowa wieloważna oraz atopowe zapalenie skóry o ciężkim przebiegu. 2. Raport Nr: AOTM-BP /2014. Nalcrom (acidum cromoglicicum), kapsułki a 100 mg, we wskazaniu: alergia pokarmowa, wieloważna oraz atopowe zapalenie skóry o ciężkim przebiegu. Raport ws. zasadności wydawania zgody na refundację produktu leczniczego. 6
Rada Przejrzystości. Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 29/2012 z dnia 11 czerwca 2012 r. w sprawie zasadności finansowania środka spożywczego specjalnego przeznaczenia
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 29/2012 z dnia 11 czerwca 2012 r. w sprawie zasadności finansowania środka spożywczego specjalnego przeznaczenia
 Rada Przejrzystości działająca przy Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji Stanowisko Rady Przejrzystości nr 95/2016 z dnia 29 sierpnia 2016 roku w sprawie zasadności wydawania zgody
Rada Przejrzystości działająca przy Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji Stanowisko Rady Przejrzystości nr 95/2016 z dnia 29 sierpnia 2016 roku w sprawie zasadności wydawania zgody
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 380/2014 z dnia 29 grudnia 2014 r. w sprawie zasadności objęcia refundacją leku Mimpara (cinacalcetum) w zakresie
Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 380/2014 z dnia 29 grudnia 2014 r. w sprawie zasadności objęcia refundacją leku Mimpara (cinacalcetum) w zakresie
NIETOLERANCJA A ALERGIA POKARMOWA
 NIETOLERANCJA A ALERGIA POKARMOWA Nietolerancja i alergia pokarmowa to dwie mylone ze sobą reakcje organizmu na pokarmy, które dla zdrowych osób są nieszkodliwe. Nietolerancja pokarmowa w objawach przypomina
NIETOLERANCJA A ALERGIA POKARMOWA Nietolerancja i alergia pokarmowa to dwie mylone ze sobą reakcje organizmu na pokarmy, które dla zdrowych osób są nieszkodliwe. Nietolerancja pokarmowa w objawach przypomina
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 5/2012 z dnia 27 lutego 2012 r. w zakresie zakwalifikowania/niezasadności zakwalifikowania leku Valdoxan (agomelatinum)
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 5/2012 z dnia 27 lutego 2012 r. w zakresie zakwalifikowania/niezasadności zakwalifikowania leku Valdoxan (agomelatinum)
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 112/2013 z dnia 26 sierpnia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację produktu
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 112/2013 z dnia 26 sierpnia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację produktu
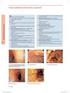
pteronyssinus i Dermatophagoides farinae (dodatnie testy płatkowe stwierdzono odpowiednio u 59,8% i 57,8% pacjentów) oraz żółtko (52,2%) i białko
 8. Streszczenie Choroby alergiczne są na początku XXI wieku są globalnym problemem zdrowotnym. Atopowe zapalenie skóry (AZS) występuje u 20% dzieci i u ok. 1-3% dorosłych, alergiczny nieżyt nosa dotyczy
8. Streszczenie Choroby alergiczne są na początku XXI wieku są globalnym problemem zdrowotnym. Atopowe zapalenie skóry (AZS) występuje u 20% dzieci i u ok. 1-3% dorosłych, alergiczny nieżyt nosa dotyczy
Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej. Szanowny Panie Marszałku,
 Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej Szanowny Panie Marszałku, w odpowiedzi na interpelację nr 9087 Posłów na Sejm RP: Krystyny Sibińskiej, Marii Janyska,
Warszawa,14 lutego 2017r. Pan Marek Kuchciński Marszałek Sejmu Rzeczypospolitej Polskiej Szanowny Panie Marszałku, w odpowiedzi na interpelację nr 9087 Posłów na Sejm RP: Krystyny Sibińskiej, Marii Janyska,
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 18/2013 z dnia 28 stycznia 2013 r. w sprawie zasadności finansowania leku Myozyme (alglukozydaza alfa) w ramach
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 18/2013 z dnia 28 stycznia 2013 r. w sprawie zasadności finansowania leku Myozyme (alglukozydaza alfa) w ramach
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
12 SQ-HDM Grupa farmakoterapeutyczna: Wyciągi alergenowe, kurz domowy; Kod ATC: V01AA03
 SUBSTANCJA CZYNNA (INN) GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC) PODMIOT ODPOWIEDZIALNY NAZWA HANDLOWA PRODUKTU LECZNICZEGO, KTÓREGO DOTYCZY PLAN ZARZĄDZANIA RYZYKIEM 12 SQ-HDM Grupa farmakoterapeutyczna:
SUBSTANCJA CZYNNA (INN) GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC) PODMIOT ODPOWIEDZIALNY NAZWA HANDLOWA PRODUKTU LECZNICZEGO, KTÓREGO DOTYCZY PLAN ZARZĄDZANIA RYZYKIEM 12 SQ-HDM Grupa farmakoterapeutyczna:
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 111/2013 z dnia 26 sierpnia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Zoladex,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 111/2013 z dnia 26 sierpnia 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Zoladex,
Aneks II. Wnioski naukowe
 Aneks II Wnioski naukowe 8 Wnioski naukowe Solu-Medrol 40 mg, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań (zwany dalej Solu-Medrol ) zawiera metyloprednisolon i (jako substancję pomocniczą)
Aneks II Wnioski naukowe 8 Wnioski naukowe Solu-Medrol 40 mg, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań (zwany dalej Solu-Medrol ) zawiera metyloprednisolon i (jako substancję pomocniczą)
Agencja Oceny Technologii Medycznych
 Rekomendacja nr 21/2012 Prezesa Agencji Oceny Technologii Medycznych z dnia 11 czerwca 2011 r. w sprawie objęcia refundacją środka spożywczego specjalnego przeznaczenia żywieniowego Nutramigen 1 LGG, preparat
Rekomendacja nr 21/2012 Prezesa Agencji Oceny Technologii Medycznych z dnia 11 czerwca 2011 r. w sprawie objęcia refundacją środka spożywczego specjalnego przeznaczenia żywieniowego Nutramigen 1 LGG, preparat
Rada Przejrzystości. Uzasadnienie. Przedmiot wniosku. Problem zdrowotny
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 208/2013 z dnia 30 września 2013 r. w sprawie zasadności wydawania zgody na refundację produktu leczniczego Mutaflor
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 208/2013 z dnia 30 września 2013 r. w sprawie zasadności wydawania zgody na refundację produktu leczniczego Mutaflor
Podsumowanie u zarządzania rzyzkiem dla produktu leczniczego Cartexan przeznaczone do publicznej wiadomości
 Podsumowanie u zarządzania rzyzkiem dla produktu leczniczego Cartexan przeznaczone do publicznej wiadomości Omówienie rozpowszechnienia choroby Rosnąca oczekiwana długość życia i starzejące się społeczeństwo
Podsumowanie u zarządzania rzyzkiem dla produktu leczniczego Cartexan przeznaczone do publicznej wiadomości Omówienie rozpowszechnienia choroby Rosnąca oczekiwana długość życia i starzejące się społeczeństwo
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 144/2013 z dnia 21 października 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 144/2013 z dnia 21 października 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego
INTESTA jedyny. oryginalny maślan sodu w chronionej patentem matrycy trójglicerydowej
 INTESTA jedyny oryginalny maślan sodu w chronionej patentem matrycy trójglicerydowej Dlaczego INTESTA? kwas masłowy jest podstawowym materiałem energetycznym dla nabłonka przewodu pokarmowego, zastosowanie,
INTESTA jedyny oryginalny maślan sodu w chronionej patentem matrycy trójglicerydowej Dlaczego INTESTA? kwas masłowy jest podstawowym materiałem energetycznym dla nabłonka przewodu pokarmowego, zastosowanie,
Aneks III. Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 158/2013 z dnia 5 sierpnia 2013 r. w sprawie oceny leku Signifor (pasyreotyd), kod EAN 5909990958238 we wskazaniu
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 158/2013 z dnia 5 sierpnia 2013 r. w sprawie oceny leku Signifor (pasyreotyd), kod EAN 5909990958238 we wskazaniu
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 45/2014 z dnia 28 stycznia 2014 r. w sprawie oceny leku Botox (toksyna botulinowa typu A 100 jednostek) we wskazaniu
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 45/2014 z dnia 28 stycznia 2014 r. w sprawie oceny leku Botox (toksyna botulinowa typu A 100 jednostek) we wskazaniu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 13/2012 z dnia 26 marca 2012 r w zakresie zasadności zakwalifikowania leków Clatra (bilastinum) 20 mg, tabletki,
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 13/2012 z dnia 26 marca 2012 r w zakresie zasadności zakwalifikowania leków Clatra (bilastinum) 20 mg, tabletki,
Dieta eliminacyjna czy prowokacja. dr. Agnieszka Krauze Stadion Narodowy Warszawa
 Dieta eliminacyjna czy prowokacja dr. Agnieszka Krauze Stadion Narodowy Warszawa 14.03.2015 Alergeny pokarmowe w grupie dzieci mleko krowie jaja soja gluten ryby owoce morza orzeszki Naturalny przebieg
Dieta eliminacyjna czy prowokacja dr. Agnieszka Krauze Stadion Narodowy Warszawa 14.03.2015 Alergeny pokarmowe w grupie dzieci mleko krowie jaja soja gluten ryby owoce morza orzeszki Naturalny przebieg
Ulotka dla pacjenta: Informacja dla użytkownika
 Finacea 150 mg/g żel Acidum azelaicum Ulotka dla pacjenta: Informacja dla użytkownika Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla pacjenta. Lek ten jest dostępny bez
Finacea 150 mg/g żel Acidum azelaicum Ulotka dla pacjenta: Informacja dla użytkownika Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla pacjenta. Lek ten jest dostępny bez
ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA
 ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA Poprawki do CHPL oraz ulotki dla pacjenta są ważne od momentu zatwierdzenia Decyzji Komisji. Po zatwierdzeniu Decyzji Komisji,
ANEKS III ZMIANY W CHARAKTERYSTYKACH PRODUKTÓW LECZNICZYCH I ULOTCE DLA PACJENTA Poprawki do CHPL oraz ulotki dla pacjenta są ważne od momentu zatwierdzenia Decyzji Komisji. Po zatwierdzeniu Decyzji Komisji,
Podsumowanie planu zarządzania ryzykiem dla produktu leczniczego Dobenox przeznaczone do publicznej wiadomości.
 VI.2 Plan Zarządzania Ryzykiem dla produktów kwalifikowanych jako "Well established use" zawierających Podsumowanie planu zarządzania ryzykiem dla produktu leczniczego Dobenox przeznaczone do publicznej
VI.2 Plan Zarządzania Ryzykiem dla produktów kwalifikowanych jako "Well established use" zawierających Podsumowanie planu zarządzania ryzykiem dla produktu leczniczego Dobenox przeznaczone do publicznej
Aneks III. Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Warszawa, dnia 29 marca 2012 r. Poz. 348 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 14 marca 2012 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 29 marca 2012 r. Poz. 348 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 14 marca 2012 r. w sprawie sprowadzania z zagranicy środków spożywczych specjalnego
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 29 marca 2012 r. Poz. 348 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 14 marca 2012 r. w sprawie sprowadzania z zagranicy środków spożywczych specjalnego
DEFERAZYROKS W LECZENIU PRZEWLEKŁEGO OBCIĄŻENIA ŻELAZEM W WYNIKU TRANSFUZJI KRWI U DOROSŁYCH
 DEFERAZYROKS W LECZENIU PRZEWLEKŁEGO OBCIĄŻENIA ŻELAZEM W WYNIKU TRANSFUZJI KRWI U DOROSŁYCH ANALIZA WPŁYWU NA SYSTEM OCHRONY ZDROWIA Wersja 1.1 Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/33 02-516 Warszawa
DEFERAZYROKS W LECZENIU PRZEWLEKŁEGO OBCIĄŻENIA ŻELAZEM W WYNIKU TRANSFUZJI KRWI U DOROSŁYCH ANALIZA WPŁYWU NA SYSTEM OCHRONY ZDROWIA Wersja 1.1 Wykonawca: MAHTA Sp. z o.o. ul. Rejtana 17/33 02-516 Warszawa
VOLTAREN MAX Diklofenak dietyloamoniowy 23,2 mg/g Żel
 VOLTAREN MAX Diklofenak dietyloamoniowy 23,2 mg/g Żel Wskazania do stosowania Voltaren MAX jest wskazany do stosowania u dorosłych i młodzieży w wieku powyżej 14 lat. Produkt działa przeciwbólowo, przeciwzapalnie
VOLTAREN MAX Diklofenak dietyloamoniowy 23,2 mg/g Żel Wskazania do stosowania Voltaren MAX jest wskazany do stosowania u dorosłych i młodzieży w wieku powyżej 14 lat. Produkt działa przeciwbólowo, przeciwzapalnie
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 182/2013 z dnia 9 września 2013 r. w sprawie oceny leku Iressa (gefitynib) we wskazaniu leczenie niedrobnokomórkowego
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 182/2013 z dnia 9 września 2013 r. w sprawie oceny leku Iressa (gefitynib) we wskazaniu leczenie niedrobnokomórkowego
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
KOMPLEKSOWA AMBULATORYJNA OPIEKA SPECJALISTYCZNA NAD PACJENTEM Z ALERGIĄ LECZONYM IMMUNOTERAPIĄ
 KOMPLEKSOWA AMBULATORYJNA OPIEKA SPECJALISTYCZNA NAD PACJENTEM Z ALERGIĄ LECZONYM IMMUNOTERAPIĄ Charakterystyka problemu zdrowotnego Alergia uznawana jest za chorobę cywilizacyjną XX wieku. W wielu obserwacjach
KOMPLEKSOWA AMBULATORYJNA OPIEKA SPECJALISTYCZNA NAD PACJENTEM Z ALERGIĄ LECZONYM IMMUNOTERAPIĄ Charakterystyka problemu zdrowotnego Alergia uznawana jest za chorobę cywilizacyjną XX wieku. W wielu obserwacjach
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 127/2013 z dnia 8 lipca 2013 r. w sprawie zasadności finansowania leku Benlysta (belimumab) 120 mg, EAN 5909990881123
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 127/2013 z dnia 8 lipca 2013 r. w sprawie zasadności finansowania leku Benlysta (belimumab) 120 mg, EAN 5909990881123
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
Produkty złożone (combo) stosowane w nadciśnieniu tętniczym a system refundacji leków ocena potencjału oszczędności
 Produkty złożone (combo) stosowane w nadciśnieniu tętniczym a system refundacji leków ocena potencjału oszczędności MIEJ SERCE I PATRZAJ W SERCE... I TĘTNICE HEALTH PROJECT MANAGEMENT 23 maja 2016 r. Nieprzestrzeganie
Produkty złożone (combo) stosowane w nadciśnieniu tętniczym a system refundacji leków ocena potencjału oszczędności MIEJ SERCE I PATRZAJ W SERCE... I TĘTNICE HEALTH PROJECT MANAGEMENT 23 maja 2016 r. Nieprzestrzeganie
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 139/2014 z dnia 2 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Giotrif,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 139/2014 z dnia 2 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Giotrif,
VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości
 VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Szacuje się, że wysokie ciśnienie krwi jest przyczyną
VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Szacuje się, że wysokie ciśnienie krwi jest przyczyną
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 115/2012 z dnia 12 listopada w sprawie zasadności finansowania leku Procoralan (EAN 5909990340439) we wskazaniu:
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 115/2012 z dnia 12 listopada w sprawie zasadności finansowania leku Procoralan (EAN 5909990340439) we wskazaniu:
Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie?
 Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie? lek. med. Marek Dudziński Oddział Hematologii Wojewódzki Szpital Specjalistyczny
Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie? lek. med. Marek Dudziński Oddział Hematologii Wojewódzki Szpital Specjalistyczny
Przedmiot wniosku. Problem zdrowotny
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 135/2013 z dnia 30 września 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację produktu
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 135/2013 z dnia 30 września 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację produktu
Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska
 Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT) Słów kilka o HTA HTA nie jest: nauką o ochronie zdrowia nauką / analizą dot.
Rola i zadania AOTMiT w procesie refundacji leków Aneta Lipińska Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT) Słów kilka o HTA HTA nie jest: nauką o ochronie zdrowia nauką / analizą dot.
Liczba alergików rośnie z roku na rok. Na alergie cierpi prawie ¼ społeczeństwa. czyli 8,5 miliona Polaków!
 Liczba alergików rośnie z roku na rok. Na alergie cierpi prawie ¼ społeczeństwa czyli 8,5 miliona Polaków! Dlaczego tak się dzieje? Rośnie liczba dużych miast. Rośnie też ilość samochodów, bloków mieszkalnych,
Liczba alergików rośnie z roku na rok. Na alergie cierpi prawie ¼ społeczeństwa czyli 8,5 miliona Polaków! Dlaczego tak się dzieje? Rośnie liczba dużych miast. Rośnie też ilość samochodów, bloków mieszkalnych,
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks II Zmiany w drukach informacyjnych produktów leczniczych zarejestrowanych w procedurze narodowej
 Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną immunoglobulinę anty-t limfocytarną pochodzenia króliczego stosowaną u ludzi [rabbit anti-human thymocyte] (proszek
Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną immunoglobulinę anty-t limfocytarną pochodzenia króliczego stosowaną u ludzi [rabbit anti-human thymocyte] (proszek
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 90/2012 z dnia 15 października 2012 r. w sprawie zasadności finansowania leku Primacor (chlorowodorek lerkanidypiny)
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 90/2012 z dnia 15 października 2012 r. w sprawie zasadności finansowania leku Primacor (chlorowodorek lerkanidypiny)
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 141/2013 z dnia 14 października 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 141/2013 z dnia 14 października 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 38/2012 z dnia 27 marca 2012 r. w sprawie objęcia refundacją budesonidu w produktach leczniczych podawanych w leczeniu
Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 38/2012 z dnia 27 marca 2012 r. w sprawie objęcia refundacją budesonidu w produktach leczniczych podawanych w leczeniu
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r. w sprawie minimalnych wymagań, jakie muszą spełniać analizy
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 kwietnia 2012 r. Poz. 388 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2012 r. w sprawie minimalnych wymagań, jakie muszą spełniać analizy
ANKIETA DLA RODZICÓW dotycząca ALERGII oraz NIETOLERANCJI ŻYWIENIOWYCH dla uczestników obozów organizowanych przez SportFun
 NAZWISKO i IMIĘ DZIECKA Data urodzenia dziecka MIEJSCE i TERMIN turnusu TELEFON do rodzica/opiekuna ANKIETA DLA RODZICÓW dotycząca ALERGII oraz NIETOLERANCJI ŻYWIENIOWYCH dla uczestników obozów organizowanych
NAZWISKO i IMIĘ DZIECKA Data urodzenia dziecka MIEJSCE i TERMIN turnusu TELEFON do rodzica/opiekuna ANKIETA DLA RODZICÓW dotycząca ALERGII oraz NIETOLERANCJI ŻYWIENIOWYCH dla uczestników obozów organizowanych
Warszawa / Zalesie Górne, 22.05.2012 r. Sz. Pan Bolesław Piecha Przewodniczący Komisji Zdrowia
 Warszawa / Zalesie Górne, 22.05.2012 r. Sz. Pan Bolesław Piecha Przewodniczący Komisji Zdrowia Dotyczy: Prośba o zgodę na uczestnictwo w posiedzeniu sejmowej komisji zdrowia dotyczącym realizacji świadczeń
Warszawa / Zalesie Górne, 22.05.2012 r. Sz. Pan Bolesław Piecha Przewodniczący Komisji Zdrowia Dotyczy: Prośba o zgodę na uczestnictwo w posiedzeniu sejmowej komisji zdrowia dotyczącym realizacji świadczeń
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA SYLIMAROL 35 mg Produkt przeznaczony dla młodzieży powyżej 12 roku życia i dorosłych. Wielkość opakowania: 30 lub 60 sztuk Należy przeczytać uważnie całą
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA SYLIMAROL 35 mg Produkt przeznaczony dla młodzieży powyżej 12 roku życia i dorosłych. Wielkość opakowania: 30 lub 60 sztuk Należy przeczytać uważnie całą
Anna Kłak. Korzystanie z informacji dostępnych w Internecie z zakresu zdrowia i choroby przez osoby chore na alergię dróg oddechowych i astmę
 Anna Kłak Korzystanie z informacji dostępnych w Internecie z zakresu zdrowia i choroby przez osoby chore na alergię dróg oddechowych i astmę STRESZCZENIE ROZPRAWY DOKTORSKIEJ Wstęp: Świadomość pacjentów
Anna Kłak Korzystanie z informacji dostępnych w Internecie z zakresu zdrowia i choroby przez osoby chore na alergię dróg oddechowych i astmę STRESZCZENIE ROZPRAWY DOKTORSKIEJ Wstęp: Świadomość pacjentów
Warszawa, dnia 29 marca 2012 r. Poz. 349. Rozporządzenie. z dnia 21 marca 2012 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 29 marca 2012 r. Poz. 349 Rozporządzenie Ministra Zdrowia 1) z dnia 21 marca 2012 r. w sprawie sprowadzania z zagranicy produktów leczniczych niezbędnych
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 29 marca 2012 r. Poz. 349 Rozporządzenie Ministra Zdrowia 1) z dnia 21 marca 2012 r. w sprawie sprowadzania z zagranicy produktów leczniczych niezbędnych
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 79/2013 z dnia 1 lipca 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Esbriet
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 79/2013 z dnia 1 lipca 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Esbriet
Warszawa, dnia 11 stycznia 2013 r. Poz. 44 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 20 grudnia 2012 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 stycznia 2013 r. Poz. 44 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 20 grudnia 2012 r. w sprawie wzorów wniosków w zakresie refundacji leku, środka
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 stycznia 2013 r. Poz. 44 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 20 grudnia 2012 r. w sprawie wzorów wniosków w zakresie refundacji leku, środka
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 157/2014 z dnia 23 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację produktu
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 157/2014 z dnia 23 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie zasadności wydawania zgód na refundację produktu
Aneks I. Wnioski naukowe i podstawy do zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy do zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy do zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED.
 POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED Izabela Pieniążek Klasyczne dossier? Rozporządzenie MZ w sprawie MINIMALNYCH
POZA KLASYCZNYM DOSSIER I SPEŁNIANIEM WYMOGÓW FORMALNYCH WYKORZYSTANIE REAL WORLD DATA, PRZEGLĄDY BURDEN OF ILLNESS I UNMET NEED Izabela Pieniążek Klasyczne dossier? Rozporządzenie MZ w sprawie MINIMALNYCH
Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
 18 października 2012 EMA/653433/2012 EMEA/H/A-5(3)/1319 Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
18 października 2012 EMA/653433/2012 EMEA/H/A-5(3)/1319 Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ 1 g płynu do stosowania
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ 1 g płynu do stosowania
ANEKS I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 ANEKS I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
ANEKS I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Metoksyfluran (Penthrox) Lek. Justyna Kasznia
 Metoksyfluran (Penthrox) Lek. Justyna Kasznia Metoksyfluran nowy-stary środek Stosowany w Australii i Nowej Zelandii od 40 lat jako środek p- bólowy Zarejestrowany we wszystkich krajach Europejskich w
Metoksyfluran (Penthrox) Lek. Justyna Kasznia Metoksyfluran nowy-stary środek Stosowany w Australii i Nowej Zelandii od 40 lat jako środek p- bólowy Zarejestrowany we wszystkich krajach Europejskich w
Aneks III Zmiany w charakterystyce produktu leczniczego oraz w ulotce dla pacjenta
 Aneks III Zmiany w charakterystyce produktu leczniczego oraz w ulotce dla pacjenta Uwaga: Niniejsze zmiany do streszczenia charakterystyki produktu leczniczego i ulotki dla pacjenta są wersją obowiązującą
Aneks III Zmiany w charakterystyce produktu leczniczego oraz w ulotce dla pacjenta Uwaga: Niniejsze zmiany do streszczenia charakterystyki produktu leczniczego i ulotki dla pacjenta są wersją obowiązującą
ANEKS II WNIOSKI NAUKOWE I PODSTAWY DO ZMIANY CHARAKTERYSTYK PRODUKTU LECZNICZEGO I ULOTEK DLA PACJENTA PRZEDSTAWIONE PRZEZ EUROPEJSKĄ AGENCJĘ LEKÓW
 ANEKS II WNIOSKI NAUKOWE I PODSTAWY DO ZMIANY CHARAKTERYSTYK PRODUKTU LECZNICZEGO I ULOTEK DLA PACJENTA PRZEDSTAWIONE PRZEZ EUROPEJSKĄ AGENCJĘ LEKÓW 108 WNIOSKI NAUKOWE OGÓLNE PODSUMOWANIE OCENY NAUKOWEJ
ANEKS II WNIOSKI NAUKOWE I PODSTAWY DO ZMIANY CHARAKTERYSTYK PRODUKTU LECZNICZEGO I ULOTEK DLA PACJENTA PRZEDSTAWIONE PRZEZ EUROPEJSKĄ AGENCJĘ LEKÓW 108 WNIOSKI NAUKOWE OGÓLNE PODSUMOWANIE OCENY NAUKOWEJ
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA DIKLONAT P, 10 mg/g, żel (Diclofenacum natricum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona ważne informacje dla pacjenta. Lek ten jest
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA DIKLONAT P, 10 mg/g, żel (Diclofenacum natricum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona ważne informacje dla pacjenta. Lek ten jest
Lek BI w porównaniu z lekiem Humira u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą
 Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 153/2014 z dnia 23 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją lek Selincro, nalmefen,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 153/2014 z dnia 23 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją lek Selincro, nalmefen,
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Biorąc pod uwagę sprawozdanie komitetu PRAC do raportu PSUR dla dexamethasonu (za wyjątkiem
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Biorąc pod uwagę sprawozdanie komitetu PRAC do raportu PSUR dla dexamethasonu (za wyjątkiem
Pełny wykaz substancji pomocniczych, patrz punkt 6.1 Charakterystyki Produktu Leczniczego (ChPL).
 Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
Pewnego razu w gabinecie. Dr hab. med. Andrea Horvath Klinika Pediatrii, WUM
 Pewnego razu w gabinecie. Dr hab. med. Andrea Horvath Klinika Pediatrii, WUM Pewnego razu w gabinecie Niemowlę 10.miesięczne CII PII SN; masa ur. 3600 Wywiad rodzinny bez obciążeń Pewnego razu w gabinecie
Pewnego razu w gabinecie. Dr hab. med. Andrea Horvath Klinika Pediatrii, WUM Pewnego razu w gabinecie Niemowlę 10.miesięczne CII PII SN; masa ur. 3600 Wywiad rodzinny bez obciążeń Pewnego razu w gabinecie
Ulotka dołączona do opakowania: informacja dla pacjenta. Essentiale VITAL, 600 mg, pasta doustna. Phospholipidum essentiale
 Ulotka dołączona do opakowania: informacja dla pacjenta Essentiale VITAL, 600 mg, pasta doustna Phospholipidum essentiale Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta Essentiale VITAL, 600 mg, pasta doustna Phospholipidum essentiale Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta Skinoren Rosacea 150 mg/g żel Acidum azelaicum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Skinoren Rosacea 150 mg/g żel Acidum azelaicum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 5/2014 z dnia 13 stycznia 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Targin,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 5/2014 z dnia 13 stycznia 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Targin,
Olopatadyna 1 mg/ml krople do oczu, roztwór. Abdi Farma, Unipessoal Lda
 Plan zarządzania ryzykiem Olopatadyna 1 mg/ml krople do oczu, roztwór Abdi Farma, Unipessoal Lda Data: 23 maja 2013 r. NINIEJSZY DOKUMENT ZAWIERA INFORMACJE POUFNE. KOPIOWANIE I ROZPOWSZECHNIANIE BEZ PISEMNEGO
Plan zarządzania ryzykiem Olopatadyna 1 mg/ml krople do oczu, roztwór Abdi Farma, Unipessoal Lda Data: 23 maja 2013 r. NINIEJSZY DOKUMENT ZAWIERA INFORMACJE POUFNE. KOPIOWANIE I ROZPOWSZECHNIANIE BEZ PISEMNEGO
Ulotka dołączona do opakowania: informacja dla użytkownika. UNIBEN 1,5 mg/ml, aerozol do stosowania w jamie ustnej (Benzydamini hydrochloridum)
 Ulotka dołączona do opakowania: informacja dla użytkownika UNIBEN 1,5 mg/ml, aerozol do stosowania w jamie ustnej (Benzydamini hydrochloridum) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika UNIBEN 1,5 mg/ml, aerozol do stosowania w jamie ustnej (Benzydamini hydrochloridum) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 77/2013 z dnia 1 lipca 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją środka spożywczego specjalnego
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 77/2013 z dnia 1 lipca 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją środka spożywczego specjalnego
6.2 Podsumowanie planu zarządzania ryzykiem dla produktu leczniczego Mupirocin InfectoPharm przeznaczone do publicznej wiadomości
 6.2 Podsumowanie planu zarządzania ryzykiem dla produktu leczniczego Mupirocin InfectoPharm przeznaczone do publicznej wiadomości 6.2.1 Omówienie rozpowszechnienia choroby Infectopharm posiada pozwolenie
6.2 Podsumowanie planu zarządzania ryzykiem dla produktu leczniczego Mupirocin InfectoPharm przeznaczone do publicznej wiadomości 6.2.1 Omówienie rozpowszechnienia choroby Infectopharm posiada pozwolenie
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Celem Tygodnia Szczepień w Polsce jest podkreślanie roli szczepień powszechnych i indywidualnych poprzez:
 W dniach 22-26 kwietnia obchodzimy, już po raz IX, Europejski Tydzień Szczepień. Jest to inicjatywa Światowej Organizacji Zdrowia (WHO), realizowana i koordynowana na poziomie lokalnym przez poszczególne
W dniach 22-26 kwietnia obchodzimy, już po raz IX, Europejski Tydzień Szczepień. Jest to inicjatywa Światowej Organizacji Zdrowia (WHO), realizowana i koordynowana na poziomie lokalnym przez poszczególne
Annex I. Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia
 Annex I Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia Podsumowanie naukowe Biorąc pod uwagę Raport oceniający komitetu PRAC dotyczący Okresowego Raportu o Bezpieczeństwie
Annex I Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia Podsumowanie naukowe Biorąc pod uwagę Raport oceniający komitetu PRAC dotyczący Okresowego Raportu o Bezpieczeństwie
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA VERTIX, 24 MG, TABLETKI (BETAHISTINI DIHYDROCHLORIDUM)
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA VERTIX, 24 MG, TABLETKI (BETAHISTINI DIHYDROCHLORIDUM) Należy zapoznać się z treścią ulotki przez zastosowaniem leku. - Należy zachować tę ulotkę, aby w
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA VERTIX, 24 MG, TABLETKI (BETAHISTINI DIHYDROCHLORIDUM) Należy zapoznać się z treścią ulotki przez zastosowaniem leku. - Należy zachować tę ulotkę, aby w
chorych na ITP Krzysztof Chojnowski Warszawa, 27 listopada 2009 r.
 Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum)
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona ważne informacje
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona ważne informacje
Agencja Oceny Technologii Medycznych
 Rekomendacja nr 77/2012 Prezesa Agencji Oceny Technologii Medycznych z dnia 8 października 2012 r. w sprawie objęcia refundacją środka spożywczego specjalnego przeznaczenia żywieniowego Neocate Advance,
Rekomendacja nr 77/2012 Prezesa Agencji Oceny Technologii Medycznych z dnia 8 października 2012 r. w sprawie objęcia refundacją środka spożywczego specjalnego przeznaczenia żywieniowego Neocate Advance,
100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix L., folium) (4-8:1). Ekstrahent: etanol 30% (m/m).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
Rosnąca wiedza Polaków na temat mukowiscydozy
 Rosnąca wiedza Polaków na temat mukowiscydozy Blisko dwie trzecie Polaków deklaruje, że słyszało o mukowiscydozie najczęściej występującej chorobie genetycznej. W porównaniu z wiedzą deklarowaną w analogicznym
Rosnąca wiedza Polaków na temat mukowiscydozy Blisko dwie trzecie Polaków deklaruje, że słyszało o mukowiscydozie najczęściej występującej chorobie genetycznej. W porównaniu z wiedzą deklarowaną w analogicznym
Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji
 Rada Przejrzystości działająca przy Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji Opinia Rady Przejrzystości nr 198/2015 z dnia 21 września 2015 r. w sprawie objęcia refundacją leków zawierających
Rada Przejrzystości działająca przy Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji Opinia Rady Przejrzystości nr 198/2015 z dnia 21 września 2015 r. w sprawie objęcia refundacją leków zawierających
wymieniają ryzedronian sodu jako jedną z substancji zalecanych w leczeniu i profilaktyce osteoporozy wywołanej glikokortykosteroidami.
 Rada Przejrzystości działająca przy Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji Opinia Rady Przejrzystości nr 91/2016 z dnia 23 marca 2016 roku w sprawie objęcia refundacją leków zawierających
Rada Przejrzystości działająca przy Prezesie Agencji Oceny Technologii Medycznych i Taryfikacji Opinia Rady Przejrzystości nr 91/2016 z dnia 23 marca 2016 roku w sprawie objęcia refundacją leków zawierających
PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL
 PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO Szanowny Farmaceuto, Należy
PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO Szanowny Farmaceuto, Należy
Zadanie pytania klinicznego (PICO) Wyszukanie i selekcja wiarygodnej informacji. Ocena informacji o metodzie leczenia
 Praktykowanie EBM Krok 1 Krok 2 Krok 3 Krok 4 Zadanie pytania klinicznego (PICO) Wyszukanie i selekcja wiarygodnej informacji Ocena informacji o metodzie leczenia Podjęcie decyzji klinicznej na podstawie
Praktykowanie EBM Krok 1 Krok 2 Krok 3 Krok 4 Zadanie pytania klinicznego (PICO) Wyszukanie i selekcja wiarygodnej informacji Ocena informacji o metodzie leczenia Podjęcie decyzji klinicznej na podstawie
Ulotka dołączona do opakowania: informacja dla użytkownika. ZYX, 5 mg, tabletki powlekane. Levocetirizini dihydrochloridum
 Ulotka dołączona do opakowania: informacja dla użytkownika ZYX, 5 mg, tabletki powlekane Levocetirizini dihydrochloridum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika ZYX, 5 mg, tabletki powlekane Levocetirizini dihydrochloridum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
ETYKIETO-ULOTKA OZNAKOWANIE OPAKOWANIA BEZPOŚREDNIEGO PRODUKTU LECZNICZEGO
 ETYKIETO-ULOTKA OZNAKOWANIE OPAKOWANIA BEZPOŚREDNIEGO PRODUKTU LECZNICZEGO RUTINOSAL C Salicis cortex + Rutosidum + Vitaminum C tabletka, 300 mg + 20 mg + 40 mg Skład tabletki: kora wierzby - 300 mg rutozyd
ETYKIETO-ULOTKA OZNAKOWANIE OPAKOWANIA BEZPOŚREDNIEGO PRODUKTU LECZNICZEGO RUTINOSAL C Salicis cortex + Rutosidum + Vitaminum C tabletka, 300 mg + 20 mg + 40 mg Skład tabletki: kora wierzby - 300 mg rutozyd
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g płynu do stosowania na skórę zawiera 100
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g płynu do stosowania na skórę zawiera 100
w kale oraz innych laboratoryjnych markerów stanu zapalnego (białka C-reaktywnego,
 1. Streszczenie Wstęp: Od połowy XX-go wieku obserwuje się wzrost zachorowalności na nieswoiste choroby zapalne jelit (NChZJ), w tym chorobę Leśniowskiego-Crohna (ChLC), zarówno wśród dorosłych, jak i
1. Streszczenie Wstęp: Od połowy XX-go wieku obserwuje się wzrost zachorowalności na nieswoiste choroby zapalne jelit (NChZJ), w tym chorobę Leśniowskiego-Crohna (ChLC), zarówno wśród dorosłych, jak i
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta tabletki powlekane 100 mg Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Ulotka dołączona do opakowania: informacja dla pacjenta tabletki powlekane 100 mg Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
