Temat lekcji Bogactwa Naturalne Ziemi
|
|
|
- Dorota Niewiadomska
- 9 lat temu
- Przeglądów:
Transkrypt
1 Piotr Chojnacki Anna Kaczmarek Anna Kaleta Jolanta Karpińska Daniel Synówka Wrocław dn. 30 maja 2005r Temat lekcji Bogactwa Naturalne Ziemi Cele główne lekcji: 1. Poznanie bogactw naturalnych ziemi. 2. Sposób powstawania bogactw naturalnych. 3. Omówienie zastosowań w życiu codziennym. Cele operacyjne: Uczeń wie: 1. Co to są surowce mineralne. 2. W jaki sposób powstaje ropa naftowa, gaz ziemny, węgle (kamienny, brunatny). 3. Jak przebiega przeróbka paliw kopalnianych i zna ich zastosowanie. 4. Jaki jest sposób otrzymywania paliw kopalnianych. Uczeń umie: 1. Rozpoznać podstawowe bogactwa naturalne. 2. Wymienić dominujące pierwiastki w danej skale (minerale). Uczeń rozumie: 1. Wpływ spalania paliw na środowisko naturalne. 2. Problem wyczerpania zasobów naturalnych. Czas lekcji: Zajęcia podzielone na trzy jednostki lekcyjne. Piotr Chojnacki 1
2 Wykorzystane metody nauczania: Przekaz słowny. Metoda tekstu przewodniego. Forma mini-wykładu. Ćwiczenia w grupach. Materiały wykorzystywane podczas lekcji: niektóre bogactwa naturalne ziemi np. przykłady skał, minerałów, folia, koperty, kreda. Piotr Chojnacki 2
3 1. JEDNOSTKA LEKCYJNA Faza zasadnicza Faza wstępna Przywitanie uczniów Sprawdzenie obecności Sprawy organizacyjne Podanie tematu lekcji celu ogólnego: Poznanie bogactw naturalnych Ziemi. Surowce mineralne. Zadaje pytanie nr 1: Co rozumiecie pod pojęciem bogactwo naturalne Ziemi? Wypiszcie przykłady w 2-osobowych grupach. Ćwiczenie 1. Nauczyciel podaje polecenie: Pozostańcie w grupach. Spróbujcie sklasyfikować wymienione przez Was bogactwa naturalne Ziemi na: 1. wyczerpywalne, odnawialne 2. wyczerpywane, nieodnawialne 3. niewyczerpywalne Wynik przedstawcie w formie tabelki. Po zakończonym ćwiczeniu nauczyciel sprawdza, poprawność odpowiedzi uczniów, wskazuje ewentualne błędy. Podaje definicję: SUROWCE MINERALNE: minerały i skały wykorzystywane przez człowieka w różnych dziedzinach życia Przywitanie nauczyciela Uczniowie zapisują temat w zeszycie; Wypisują w grupach 2-osobowych: złoża rud metali, sól kamienna, skały gipsowe, skały wapienne, piasek, minerały, kamienie szlachetne, metale, gaz ziemny, ropa naftowa, węgiel kamienny, węgiel brunatny, woda, gleba, las, rośliny, zwierzęta, powietrze, wiatr, energia słoneczna Uczniowie pracują i w formie tabelki przedstawiają swoje propozycje Uczniowie zapisują definicje w zeszycie. 30 minut 5 minut Ćwiczenie 2.Nauczyciel podaje polecenie: Spośród wymienionych na początku lekcji bogactw naturalnych Ziemi wybierzcie surowce mineralne i podzielcie je ze względu na zastosowanie, na: (praca dalej w grupach) 1. energetyczne 2. budowlane 3. chemiczne 4. metalurgiczne 5. zdobnicze Po zakończonym ćwiczeniu nauczyciel sprawdza, poprawność odpowiedzi uczniów, wskazuje ewentualne błędy. Uczniowie pracują i w formie tabelki podają swoje propozycje Piotr Chojnacki 3
4 Faza końcowa Faza zasadnicza cd. Ćwiczenie 3. Nauczyciel omawia ćwiczenie: Na konsoli znajduję się kilka przykładów bogactw naturalnych ziemi. Dostaniecie krateczki z nazwą i oddzielne z wzorem sumarycznym związku. Wasze zadanie polega na przyporządkowaniu nazwy do odpowiedniego wzoru oraz nazwanie występujących w nim pierwiastków. Nauczyciel prosi o przedstawienie wyników i o wspólną ocenę; Mini wykład 1 : W formie mini wykładu nauczyciel przekazuje uczniom cenne informacje z zakresu: SUROWCE MINERALNE.SKAŁY WAPIENNE I GIPSOWE ICH WŁAŚCIWOŚCI I ZASTOSOWANIE Nauczycie, prezentuje folie i daje uczniom ksero folii. Praca domowa (zbiorcza) na koniec 2 jednostki lekcyjnej. Obejmować będzie tą i następną lekcję. Uczniowie pracują w grupach (max 5 osobowych). Przyporządkowują nazwy do poszczególnych bogactw i wzorów i nazywają w nich pierwiastki Uczniowie uważnie słuchają. 10 minut Piotr Chojnacki 4
5 Materiały i odpowiedzi dla nauczyciela do przeprowadzenia lekcji (dołączane do konspektu w ramach 1 jednostki lekcyjnej) Temat: Poznanie bogactw naturalnych Ziemi. Surowce mineralne. Ćwiczenie 1: Klasyfikacja bogactw naturalnych Ziemi na: powietrze woda gleba las zwierzęta rośliny 1. wyczerpywalne, odnawialne 2. wyczerpywalne, nieodnawialne węgiel kamienny węgiel brunatny gaz ziemny ropa naftowa sól kamienna rudy metali skały gipsowe, wapienne, piasek 3. niewyczerpywalne energia słoneczna wiatr Ćwiczenie 2: Klasyfikacja surowców mineralnych ze względu na zastosowanie, na: 1. energetyczne 2. budowlane 3. chemiczne 4. metalurgiczne 5. zdobnicze ropa naftowa gaz ziemy węgiel (kamienny, brunatny) skały wapienne, gipsowe, piasek rudy metali skały wapienne sól kamienna rudy metali metale kamienie szlachetne Ćwiczenie 3: Przyporządkowanie nazw bogactw naturalnych ziemi odpowiednim wzorom sumarycznym. Nazwanie występujących w nich pierwiastków: woda H 2 O H wodór, O tlen sól kamienna NaCl Na sód, Cl chlor węgiel kamienny C C - węgiel skała wapienna CaCO 3 Ca wapń, C-węgiel, O- tlen piasek kwarcowy SiO 2 Si krzem, O-tlen magnetyt Fe 3 O 4 Fe żelazo, O - tlen Piotr Chojnacki 5
6 Mini wykład 1: Surowce mineralne. Skały wapienne i gipsowe - ich właściwości i zastosowanie (folie) - (uczniowie dostaną ksero folii) Skały wapienne: Skały wapienne to wapień, kreda i marmur. Wapień i kreda to skały osadowe, które powstały na dnie mórz i oceanów. Marmur ma zastosowanie głównie jako materiał dekoracyjny i rzeźbiarski. Podstawowym związkiem chemicznym, tworzącym wszystkie skały wapienne, jest minerał, kalcyt, o wzorze sumarycznym CaCO 3 Właściwości i zastosowanie skał wapiennych: Rozkład pod wpływem kwasów: CaCO 3 + 2HCl CaCl 2 + H 2 O + CO 2 Zmętnienie wody wapiennej: Rozkład termiczny: CO 2 + Ca(OH) 2 CaCO 3 + H 2 O o C CaCO 3 CaO + CO 2 Powstały tlenek wapnia CaO to wapno palone (biały proszek). Proces termicznego rozkładu (prażenia) wapieni wykorzystywany jest na skale przemysłową i odbywa się w piecach szybowych zwanych wapiennikami. Poza CaO wydziela się bezbarwny gaz dwutlenek węgla powodujący zmętnienie wody wapiennej. Czysty tlenek wapnia CaO jest białym, krystalicznym ciałem stałym. Jest higroskopijny tzn. ma zdolność pochłaniania wody lub pary wodnej np. z powietrza, dlatego stosowany jest w laboratoriach chemicznych do osuszania niektórych cieczy i gazów. Pochłania również dwutlenek węgla z powietrza, co przedstawia równanie reakcji: CaO + CO 2 CaCO 3 Tlenek wapnia CaO reaguje z wodą bardzo gwałtownie. Naczynie, w którym biegnie reakcja staje się gorące, wydziela się duża ilośc ciepła. Jest to reakcja egzoenergetyczna, która przebiega w sposób przedstawiony równaniem reakcji: CaO + H 2 O Ca(OH) 2 + ciepło wapno gaszone Powstały Ca(OH) 2 - wodorotlenek wapnia zwany jest wapnem gaszonym, a powyższa reakcja nosi nazwę gaszenia wapna palonego. Wapno gaszone jest substancją słabo rozpuszczalną w wodzie. Stężony roztwór ma właściwości żrące, w zwiąku, z czym wapna palonego i wapna gaszonego nie wolno Piotr Chojnacki 6
7 bezpośrednio brać do rąk. Stosuje się go w budownictwie jako składnik zaprawy murarskiej oraz w przemyśle chemicznym do produkcji wielu odczynników chemicznych. Wapno gaszone sprzedawane jest w stanie suchym w workach papierowych jako wapno hydratyzowane. Używa się go również w rolnictwie do odkwaszania gleby oraz do bielenia drzew owocowych owocowych ścian wewnętrznych budynków gospodarczych, ponieważ ma właściwości bakteriobójcze. Wapno gaszone zmieszane z piaskiem i wodą tworzy tzw. zaprawę murarską. Zaprawa jest materiałem plastycznym i stanowi lepiszcze powszechnie stosowane do spajania cegieł i sporządzania tynków. Plastyczna początkowo masa po pewnym czasie tężeje i wysycha jest to proces wiązania zaprawy. Jej twardnienie zachodzi pod wpływem dwutlenku węgla zawartego w powietrzu, zgodnie z równaniem: Ca(OH) 2 + CO 2 CaCO 3 + H 2 O Skały gipsowe: Składnikiem wszystkich skał gipsowych jest siarczan wapnia : CaSO 4. W przyrodzie znane są dwa minerały zawierające CaSO 4 : anhydryt zbudowany z samego CaSO 4 oraz gips krystaliczny lub alabaster o wzorze sumarycznym CaSO 4 * 2 H 2 O (dwuwodny siarczan (VI) wapnia ). Mówi się, że dwuwodny siarczan (VI) wapnia jest solą uwodnioną, czyli hydratem. Właściwości i zastosowanie skał gipsowych: Rozkład termiczny: o C 2 (CaSO 4 * 2 H 2 O) (CaSO 4 ) 2 * H 2 O + 3 H 2 O gips krystaliczny gips palony W wyniku reakcji powstaje biały proszek (szary jeśli jest zanieczyszczony), tzw. gips palony. Gips palony to półhydrat. Jest białym ciałem stałym, nierozpuszczalnym w wodzie. Zmieszany z wodą tworzy półpłynną, szybko twardniejącą masą zaprawę gipsową. W momencie jej twardnienia zachodzi reakcja odwrotna do prażenia gipsu krystalicznego: (CaSO 4 ) 2 *H 2 O + 3 H 2 O 2 (CaSO 4 * 2 H 2 O) Zaprawa gipsowa nie ma właściwości żrących jak zaprawa wapienna, dlatego znalazła zastosowanie w medycynie do sporządzania bandaży chirurgicznych i usztywniania złamanych kości. Stosuje się ją również w budownictwie jako tzw. zaprawę hydrauliczną do wyrównywania ścian lub jako dodatek do cementu. Dodanie gipsu do zaprawy znacznie skraca okres jej wiązania, w związku, z czym do prac np. tynkarskich stosuje się często zaprawy gipsowo wapienne. Gips palony jest wykorzystywany również do wykonywania odlewów różnych modeli plastycznych i w ceramice. Piotr Chojnacki 7
8 Piotr Chojnacki 8
9 2. JEDNOSTKA LEKCYJNA Faza zasadnicza Faza wstępna Przywitanie uczniów Sprawdzenie obecności Sprawy organizacyjne Przypomnienie wiadomości o poznanych bogactwach naturalnych ziemi Podanie tematu lekcji celu ogólnego: "Surowce energetyczne. Sposób ich powstawania i zastosowanie w życiu codziennym Zadaje uczniom pytanie nr 1: Wymieńcie znane Wam surowce energetyczne Nauczyciel definiuje nowe pojęcia: 1. węgiel kamienny- to odmiana zawierająca około 87% pierwiastka węgla. Stosowany jest jako paliwo, np. przy ogrzewaniu mieszkań i w elektrociepłowniach. Zawiera siarkę i podczas jego spalania wydziela się dużo tlenku siarki (IV), który zanieczyszcza powietrze. 2. węgiel brunatny zawiera około 70% pierwiastka węgla. Stosowany jest również jako paliwo, ale podczas spalania wydziela mniejszą ilość ciepła. 3. torf zawiera około 60% pierwiastka węgla. Ma barwę ciemnobrunatną. Występuję najczęściej na dnie bagien, powstaje ze zgniłych roślin. 4. ropa naftowa powstała ze szczątków roślin i zwierzęcych w wyniku procesów gnilnych zachodzących w temperaturze 200 C, pod dużym ciśnieniem. Oleista ciecz barwy żółtej, brunatnej lub czarnej. Przywitanie nauczyciela Uczniowie opowiadają w kilku słowach o poznanych bogactwach. (O czym się dowiedzieli na poprzedniej lekcji.) Uczniowie zapisują temat w zeszycie Uczniowie wspólnie udzielają odpowiedzi: węgiel, ropa naftowa, gaz ziemny Uczniowie notują informacje w zeszycie 30 minut 5 minut 5. gaz ziemny jest gazową mieszaniną jednorodną lekkich węglowodorów głównie związku zwanego metanem. Mini wykład 1: Nauczyciel przedstawia na folii proces powstawania węgla, gazu ziemnego ropy naftowej. Podaje uczniom notatkę do zeszytu. Omawia również przeróbkę paliw kopalnianych. Uczniowie uważnie słuchają i notują Piotr Chojnacki 9
10 Ćwiczenie 1: Nauczyciel omawia ćwiczenie: Rozdaję Wam koperty, w których znajduje się polecenie dotyczące kolejnego ćwiczenia. (Przyporządkuj sposób powstania do odpowiedniego surowca energetycznego). Pracujecie w 5 osobowych grupach. Uczniowie pracują, przyporządkowują dane surowce energetyczne do sposobów ich powstawania Prezentują swoje wyniki; Przykład: Faza końcowa Faza zasadnicza cd. ropa naftowa szczątki roślin i zwierząt węgiel kamienny zawartość węgla 87% węgiel brunatny zawartość węgla 70% ropa naftowa szczątki roślin i zwierząt torf dna bagien, zgniłe rośliny Nauczyciel przedstawia poprawne odpowiedzi do ćwiczenia; Przedstawia wykresy emisji gazów szkodliwych, produktów przemysłu, analizując je. Załącznik z wykresami 2 jednostka lekcyjna ćw Na zakończenie lekcji sprawdza zapamiętaną wiedzę uczniów zadając pytanie: Jakie jest zastosowanie poznanych przez Ciebie bogactw w życiu codziennym i gospodarce człowieka? Zadaje i omawia pracę domową, która obejmuje poprzednią (pierwszą) i aktualną (drugą) jednostkę lekcyjną. W formie pisemnej odpowiedz na pytania: 1.Jakie zagrożenie dla życia człowieka stanowi problem wyczerpania się bogactw pracy domowej: naturalnych ziemi? 2. Moim zdaniem, jednym z najważniejszych surowców mineralnych jest.. Odpowiedź uzasadnij Uczniowie słuchają, sporządzają notatki Uczniowie odpowiadają i wygłaszają swoje opinie, poglądy. Zapisują temat pracy domowej Taki temat pracy domowej pobudza wyobraźnie i własną inwencję ucznia. Pozwala zaznajomić się nauczycielowi z indywidualnym poglądem ucznia na ten temat. Piotr Chojnacki 10
11 Materiały i odpowiedzi dla nauczyciela do przeprowadzenia lekcji (dołączane do konspektu w ramach 2 jednostki lekcyjnej) Temat: Surowce energetyczne. Sposób ich powstawania i zastosowanie w życiu codziennym. ćwiczenie 2: Trendy emisji NO x przedstawione na rysunku 2.5 wskazują na systematyczny spadek emisji tych zanieczyszczeń. W przypadku tlenków azotu przejściowy wzrost krajowej emisji w latach wynika ze wzrostu emisji spalania paliw w sektorze energetyki zawodowej i przemyśle. 10 minut Na rysunkach 2.6 i 2.6a widać również tendencje spadkową zarówno emisji SO 2 jak i CO. O wielkości krajowej emisji tlenku węgla decydują nieefektywne procesy spalania z sektora komunalnego i mieszkaniowego. Przejściowy wzrost krajowej emisji CO w latach i 1999 wynika ze wzrostu ilości paliw w tym sektorze. Piotr Chojnacki 11
12 W przypadku dwutlenku siarki o krajowej emisji decydują procesy spalania paliw we wszystkich trzech sektorach: energetyce zawodowej, komunalnym i mieszkaniowym oraz w przemyśle. Przejściowy wzrost krajowej emisji SO 2 w latach wynika ze wzrostu emisji spalania paliw (głównie węgla) w sektorze energetyki zawodowej. Piotr Chojnacki 12
13 Piotr Chojnacki 13
14 3. JEDNOSTKA LEKCYJNA Przywitanie uczniów Sprawdzenie obecności Przywitanie nauczyciela Podanie tematu lekcji celu ogólnego: Bogactwa naturalne ziemi kłodzkiej - wycieczka Miejsca zwiedzania: Złoty Stok kopalnia złota; Kletno Jaskinia Niedźwiedzia; Lądek Zdrój wystawy marmurów, uzdrowisko (pijalnia wód mineralnych); Nowa Ruda Muzeum górnictwa; Szklary wystawy agatów, kryształów górskich Uczniowie rozpoznają minerały i sprawdzają w praktyce zdobytą wcześniej wiedzę na temat bogactw naturalnych ziemi. Uczniowie poznają z zainteresowaniem proces wydobycia węgla kamiennego. Uczniowie utrwalają zdobytą wiedzę. ZAŁOŻENIA PROGRAMOWE: Uczeń: - potrafi w praktyce rozróżniać minerały; - zna proces wydobycia węgla kamiennego i złota; -potrafi omówić wpływ różnych czynników na występowanie bogactw naturalnych; Wycieczka uczy praktycznego wykorzystania wiedzy zdobytej na zajęciach oraz kształtuje wrażliwość uczniów na problemy nieumiejętnego korzystania z bogactw naturalnych. Piotr Chojnacki 14
Zadanie 3 Zapisz wzory sumaryczne głównych składników przedstawionych skał i minerałów. kalcyt kreda kwarc gips agat
 CZĘŚĆ 1 Zadanie 1 Wyjaśnij pojęcia. wapno palone, hydraty, zaprawa gipsowa, zaprawa wapienna, wietrzenie skał, wapno gaszone, próchnica, degradacja gleby, właściwości sorpcyjne gleby, wapno palone, degradacja
CZĘŚĆ 1 Zadanie 1 Wyjaśnij pojęcia. wapno palone, hydraty, zaprawa gipsowa, zaprawa wapienna, wietrzenie skał, wapno gaszone, próchnica, degradacja gleby, właściwości sorpcyjne gleby, wapno palone, degradacja
Materiały i tworzywa pochodzenia naturalnego
 Materiały i tworzywa pochodzenia naturalnego 1. Przyporządkuj opisom odpowiadające im pojęcia. Wpisz litery (A I) w odpowiednie kratki. 3 p. A. hydraty D. wapno palone G. próchnica B. zaprawa wapienna
Materiały i tworzywa pochodzenia naturalnego 1. Przyporządkuj opisom odpowiadające im pojęcia. Wpisz litery (A I) w odpowiednie kratki. 3 p. A. hydraty D. wapno palone G. próchnica B. zaprawa wapienna
Bogusława Kozub; nauczyciel chemii w Publicznym Gimnazjum nr 5 w Płazie
 Bogusława Kozub; nauczyciel chemii w Publicznym Gimnazjum nr 5 w Płazie Temat: Surowce i tworzywa pochodzenia mineralnego. Temat realizowany metodą projektu. Celem projektu jest zapoznanie się uczniów
Bogusława Kozub; nauczyciel chemii w Publicznym Gimnazjum nr 5 w Płazie Temat: Surowce i tworzywa pochodzenia mineralnego. Temat realizowany metodą projektu. Celem projektu jest zapoznanie się uczniów
Litowce i berylowce- lekcja powtórzeniowa, doświadczalna.
 Doświadczenie 1 Tytuł: Badanie właściwości sodu Odczynnik: Sód metaliczny Szkiełko zegarkowe Metal lekki o srebrzystej barwie Ma metaliczny połysk Jest bardzo miękki, można kroić go nożem Inne właściwości
Doświadczenie 1 Tytuł: Badanie właściwości sodu Odczynnik: Sód metaliczny Szkiełko zegarkowe Metal lekki o srebrzystej barwie Ma metaliczny połysk Jest bardzo miękki, można kroić go nożem Inne właściwości
KLASA II I. WODA I ROZTORY WODNE. - wie gdzie i w jakiej postaci występuje woda w przyrodzie - wie jak powstaje roztwór i z czego się składa
 SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII KLASA II I. WODA I ROZTORY WODNE Ocena dopuszczająca - wie gdzie i w jakiej postaci występuje woda w przyrodzie - wie jak powstaje roztwór i z czego się składa -
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII KLASA II I. WODA I ROZTORY WODNE Ocena dopuszczająca - wie gdzie i w jakiej postaci występuje woda w przyrodzie - wie jak powstaje roztwór i z czego się składa -
Instrukcja dla uczestnika
 II edycja Konkursu Chemicznego Chemik dla uczniów szkół gimnazjalnych rok szkolny 2016/2017 Instrukcja dla uczestnika I etap Konkursu (etap szkolny) 1. Sprawdź, czy arkusz konkursowy, który otrzymałeś
II edycja Konkursu Chemicznego Chemik dla uczniów szkół gimnazjalnych rok szkolny 2016/2017 Instrukcja dla uczestnika I etap Konkursu (etap szkolny) 1. Sprawdź, czy arkusz konkursowy, który otrzymałeś
SCENARIUSZ ZAJĘĆ INTERDYSCYPLINARNYCH
 85 S t r o n a IV. SCENARIUSZ ZAJĘĆ INTERDYSCYPLINARNYCH Temat:. Ściany jako podstawowy element domu, materiały izolacyjne. Czas trwania: 45 min. Cel główny: Uczeń: - potrafi rozpoznać materiały stosowane
85 S t r o n a IV. SCENARIUSZ ZAJĘĆ INTERDYSCYPLINARNYCH Temat:. Ściany jako podstawowy element domu, materiały izolacyjne. Czas trwania: 45 min. Cel główny: Uczeń: - potrafi rozpoznać materiały stosowane
Surowce pochodzenia mineralnego
 strona 1/5 Surowce pochodzenia mineralnego Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Surowce i tworzywa pochodzenia mineralnego: węgiel kamienny, ropa naftowa, gaz
strona 1/5 Surowce pochodzenia mineralnego Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Surowce i tworzywa pochodzenia mineralnego: węgiel kamienny, ropa naftowa, gaz
SPOIWA MINERALNE POLITECHNIKA GDAŃSKA WYDZIAŁ CHEMICZNY KATEDRA INŻYNIERII PROCESOWEJ I TECHNOLOGII CHEMICZNEJ TECHNOLOGIE MATERIAŁÓW BUDOWLANYCH
 POLITECHNIKA GDAŃSKA WYDZIAŁ CHEMICZNY KATEDRA INŻYNIERII PROCESOWEJ I TECHNOLOGII CHEMICZNEJ TECHNOLOGIE MATERIAŁÓW BUDOWLANYCH SPOIWA MINERALNE dr hab. inż. Anna Zielińska-Jurek mgr inż. Zuzanna Bielan
POLITECHNIKA GDAŃSKA WYDZIAŁ CHEMICZNY KATEDRA INŻYNIERII PROCESOWEJ I TECHNOLOGII CHEMICZNEJ TECHNOLOGIE MATERIAŁÓW BUDOWLANYCH SPOIWA MINERALNE dr hab. inż. Anna Zielińska-Jurek mgr inż. Zuzanna Bielan
ROZKŁAD MATERIAŁU Z CHEMII W KLASIE II
 ROZKŁAD MATERIAŁU Z CHEMII W KLASIE II Temat i numer kolejny lekcji Zagadnienia programowe Wymagania: podstawowe (P) ponadpodstawowe (PP) Przykłady metod i form pracy 1. Organizacja pracy na lekcjach chemii.
ROZKŁAD MATERIAŁU Z CHEMII W KLASIE II Temat i numer kolejny lekcji Zagadnienia programowe Wymagania: podstawowe (P) ponadpodstawowe (PP) Przykłady metod i form pracy 1. Organizacja pracy na lekcjach chemii.
Wymagania edukacyjne z chemii Klasa II WODOROTLENKI A ZASADY
 Wymagania edukacyjne z chemii Klasa II WODOROTLENKI A ZASADY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą wymienia rodzaje wskaźników; sprawdza doświadczalnie działanie podaje przykłady
Wymagania edukacyjne z chemii Klasa II WODOROTLENKI A ZASADY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą wymienia rodzaje wskaźników; sprawdza doświadczalnie działanie podaje przykłady
Wodorotlenki O O O O. I n. I. Wiadomości ogólne o wodorotlenkach.
 Wodorotlenki I. Wiadomości ogólne o wodorotlenkach. Wodorotlenki są to związki chemiczne zbudowane z atomu metalu i grupy wodorotlenowej. Wzór ogólny wodorotlenków: wartościowość metalu M n ( ) grupa wodorotlenowa
Wodorotlenki I. Wiadomości ogólne o wodorotlenkach. Wodorotlenki są to związki chemiczne zbudowane z atomu metalu i grupy wodorotlenowej. Wzór ogólny wodorotlenków: wartościowość metalu M n ( ) grupa wodorotlenowa
Wapń i jego związki. -występowanie i otrzymywanie -właściwości fizyczne i chemiczne - ważniejsze związki wapnia
 Wapń i jego związki -występowanie i otrzymywanie -właściwości fizyczne i chemiczne - ważniejsze związki wapnia Wapń występowanie Występowanie: występuje wyłącznie w postaci związanej CaCO 3 w minerałachkalcyt,
Wapń i jego związki -występowanie i otrzymywanie -właściwości fizyczne i chemiczne - ważniejsze związki wapnia Wapń występowanie Występowanie: występuje wyłącznie w postaci związanej CaCO 3 w minerałachkalcyt,
II. CHEMIA NIEORGANICZNA
 pitagoras.d2.pl II. CHEMIA NIEORGANICZNA TLENKI: Tlenki to związki tlenu z innymi pierwiastkami. Tlen w tlenkach ma zawsze II. pierwiastka X I II III IV V VI VII wzór tlenku X 2 O XO X 2 O 3 XO 2 X 2 O
pitagoras.d2.pl II. CHEMIA NIEORGANICZNA TLENKI: Tlenki to związki tlenu z innymi pierwiastkami. Tlen w tlenkach ma zawsze II. pierwiastka X I II III IV V VI VII wzór tlenku X 2 O XO X 2 O 3 XO 2 X 2 O
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap rejonowy rok szkolny 2010/2011 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap rejonowy rok szkolny 2010/2011 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego. II Etap - 18 stycznia 2016
 XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego II Etap - 18 stycznia 2016 Nazwisko i imię ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego II Etap - 18 stycznia 2016 Nazwisko i imię ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
Obliczenia chemiczne
 strona 1/8 Obliczenia chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Wagowe stosunki stechiometryczne w związkach chemicznych i reakcjach chemicznych masa atomowa
strona 1/8 Obliczenia chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Wagowe stosunki stechiometryczne w związkach chemicznych i reakcjach chemicznych masa atomowa
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW. Eliminacje rejonowe II stopień
 POUFNE Pieczątka szkoły 28 stycznia 2016 r. Kod ucznia (wypełnia uczeń) Imię i nazwisko (wypełnia komisja) Czas pracy 90 minut KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 Eliminacje rejonowe
POUFNE Pieczątka szkoły 28 stycznia 2016 r. Kod ucznia (wypełnia uczeń) Imię i nazwisko (wypełnia komisja) Czas pracy 90 minut KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 Eliminacje rejonowe
1. Pochodzenie i klasyfikacja zasobów przyrodniczych... 11
 Spis treści 1. Pochodzenie i klasyfikacja zasobów przyrodniczych... 11 1.1. Rozwój cywilizacji człowieka a korzystanie z zasobów Ziemi... 11 1.2. Czy zasoby naturalne Ziemi mogą ulec wyczerpaniu?... 14
Spis treści 1. Pochodzenie i klasyfikacja zasobów przyrodniczych... 11 1.1. Rozwój cywilizacji człowieka a korzystanie z zasobów Ziemi... 11 1.2. Czy zasoby naturalne Ziemi mogą ulec wyczerpaniu?... 14
WYMAGANIA EDUKACYJNE Z CHEMII 2013/2014
 Uczeń klasy I: WYMAGANIA EDUKACYJNE Z CHEMII 2013/2014 -rozróżnia i nazywa podstawowy sprzęt laboratoryjny -wie co to jest pierwiastek, a co to jest związek chemiczny -wyszukuje w układzie okresowym nazwy
Uczeń klasy I: WYMAGANIA EDUKACYJNE Z CHEMII 2013/2014 -rozróżnia i nazywa podstawowy sprzęt laboratoryjny -wie co to jest pierwiastek, a co to jest związek chemiczny -wyszukuje w układzie okresowym nazwy
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe
 kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe Zadanie
kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe Zadanie
Technologie Materiałów Budowlanych Wykład 3. Mineralne spoiwa budowlane
 Technologie Materiałów Budowlanych Wykład 3 Mineralne spoiwa budowlane Spoiwa mineralne Materiały o właściwościach wiążących, wytwarzane przez wypalenie i sproszkowanie surowców skalnych Po wymieszaniu
Technologie Materiałów Budowlanych Wykład 3 Mineralne spoiwa budowlane Spoiwa mineralne Materiały o właściwościach wiążących, wytwarzane przez wypalenie i sproszkowanie surowców skalnych Po wymieszaniu
Chemia. 3. Która z wymienionych substancji jest pierwiastkiem? A Powietrze. B Dwutlenek węgla. C Tlen. D Tlenek magnezu.
 Chemia Zestaw I 1. Na lekcjach chemii badano właściwości: żelaza, węgla, cukru, miedzi i magnezu. Który z zestawów badanych substancji zawiera tylko niemetale? A Węgiel, siarka, tlen. B Węgiel, magnez,
Chemia Zestaw I 1. Na lekcjach chemii badano właściwości: żelaza, węgla, cukru, miedzi i magnezu. Który z zestawów badanych substancji zawiera tylko niemetale? A Węgiel, siarka, tlen. B Węgiel, magnez,
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE II gimnazjum
 WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE II gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE II gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
2. Podczas spalania 2 objętości pewnego gazu z 4 objętościami H 2 otrzymano 1 objętość N 2 i 4 objętości H 2O. Jaki gaz uległ spalaniu?
 1. Oblicz, ilu moli HCl należy użyć, aby poniższe związki przeprowadzić w sole: a) 0,2 mola KOH b) 3 mole NH 3 H 2O c) 0,2 mola Ca(OH) 2 d) 0,5 mola Al(OH) 3 2. Podczas spalania 2 objętości pewnego gazu
1. Oblicz, ilu moli HCl należy użyć, aby poniższe związki przeprowadzić w sole: a) 0,2 mola KOH b) 3 mole NH 3 H 2O c) 0,2 mola Ca(OH) 2 d) 0,5 mola Al(OH) 3 2. Podczas spalania 2 objętości pewnego gazu
Wymagania programowe na poszczególne oceny. IV. Kwasy. Ocena bardzo dobra. Ocena dostateczna. Ocena dopuszczająca. Ocena dobra [1] [ ]
![Wymagania programowe na poszczególne oceny. IV. Kwasy. Ocena bardzo dobra. Ocena dostateczna. Ocena dopuszczająca. Ocena dobra [1] [ ] Wymagania programowe na poszczególne oceny. IV. Kwasy. Ocena bardzo dobra. Ocena dostateczna. Ocena dopuszczająca. Ocena dobra [1] [ ]](/thumbs/59/43143309.jpg) Wymagania programowe na poszczególne oceny IV. Kwasy Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra [1] [1 + 2] [1 + 2 + 3] [1 + 2 + 3 + 4] wymienia zasady bhp dotyczące obchodzenia
Wymagania programowe na poszczególne oceny IV. Kwasy Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra [1] [1 + 2] [1 + 2 + 3] [1 + 2 + 3 + 4] wymienia zasady bhp dotyczące obchodzenia
Kryteria oceniania z chemii kl VII
 Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Wojewódzki Konkurs Przedmiotowy z Chemii III etap
 KOD Ucznia Wojewódzki Konkurs Przedmiotowy z Chemii III etap Termin: 05. 04. 2004 r Czas pracy: 90 minut Ilość punktów za rozwiązanie zadań Razem Podpis Część I Cześć II Cześć III Zadania zamknięte i otwarte
KOD Ucznia Wojewódzki Konkurs Przedmiotowy z Chemii III etap Termin: 05. 04. 2004 r Czas pracy: 90 minut Ilość punktów za rozwiązanie zadań Razem Podpis Część I Cześć II Cześć III Zadania zamknięte i otwarte
TEST NA EGZAMIN POPRAWKOWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM
 TEST NA EGZAMIN PPRAWKWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM I. Część pisemna: 1. Które z poniższych stwierdzeń jest fałszywe? a.) Kwasy są to związki chemiczne zbudowane z wodoru i reszty kwasowej.
TEST NA EGZAMIN PPRAWKWY Z CHEMII DLA UCZNIA KLASY II GIMNAZJUM I. Część pisemna: 1. Które z poniższych stwierdzeń jest fałszywe? a.) Kwasy są to związki chemiczne zbudowane z wodoru i reszty kwasowej.
WYMAGANIA EDUKACYJNE w klasie II
 WYMAGANIA EDUKACYJNE w klasie II Lp. Treści nauczania (temat lekcji) Liczba godzin na realizację Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej ) Wymagania i kryteria
WYMAGANIA EDUKACYJNE w klasie II Lp. Treści nauczania (temat lekcji) Liczba godzin na realizację Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej ) Wymagania i kryteria
1. Podstawowe prawa i pojęcia chemiczne
 1. PODSTAWOWE PRAWA I POJĘCIA CHEMICZNE 5 1. Podstawowe prawa i pojęcia chemiczne 1.1. Wyraź w gramach masę: a. jednego atomu żelaza, b. jednej cząsteczki kwasu siarkowego. Odp. 9,3 10 23 g; 1,6 10 22
1. PODSTAWOWE PRAWA I POJĘCIA CHEMICZNE 5 1. Podstawowe prawa i pojęcia chemiczne 1.1. Wyraź w gramach masę: a. jednego atomu żelaza, b. jednej cząsteczki kwasu siarkowego. Odp. 9,3 10 23 g; 1,6 10 22
Skały wapienne i ich właściwości
 Skały wapienne i ich właściwości Małgorzata Lech Cele ogólne lekcji: zapoznanie uczniów z rodzajami skał wapiennych, ich pochodzeniem, występowaniem, składem, właściwościami i zastosowaniem, doskonalenie
Skały wapienne i ich właściwości Małgorzata Lech Cele ogólne lekcji: zapoznanie uczniów z rodzajami skał wapiennych, ich pochodzeniem, występowaniem, składem, właściwościami i zastosowaniem, doskonalenie
3. Interakcja człowiek gospodarka. Sprawdzian wiadomości
 1. 2. 3. Interakcja człowiek gospodarka. Sprawdzian wiadomości 1. Cele lekcji i. Cel ogólny Podsumowanie wiadomości dotyczących przemysłu Polski. Uczeń: ii. a) Wiadomości wie, które źródła należą do zasobów
1. 2. 3. Interakcja człowiek gospodarka. Sprawdzian wiadomości 1. Cele lekcji i. Cel ogólny Podsumowanie wiadomości dotyczących przemysłu Polski. Uczeń: ii. a) Wiadomości wie, które źródła należą do zasobów
Scenariusz lekcji chemii w klasie drugiej gimnazjum
 mgr Sylwia Pięta nauczyciel chemii i matematyki Zespół Szkół z Oddziałami Sportowymi nr 1 61-638 Poznań, Os. Pod Lipami 106 Cele lekcji Temat lekcji: Poznajemy sole Formy pracy: Metody pracy: Scenariusz
mgr Sylwia Pięta nauczyciel chemii i matematyki Zespół Szkół z Oddziałami Sportowymi nr 1 61-638 Poznań, Os. Pod Lipami 106 Cele lekcji Temat lekcji: Poznajemy sole Formy pracy: Metody pracy: Scenariusz
I edycja Konkursu Chemicznego im. Ignacego Łukasiewicza dla uczniów szkół gimnazjalnych. rok szkolny 2014/2015 ZADANIA.
 I edycja Konkursu Chemicznego im. Ignacego Łukasiewicza dla uczniów szkół gimnazjalnych rok szkolny 2014/2015 ZADANIA ETAP I (szkolny) Zadanie 1 Wapień znajduje szerokie zastosowanie jako surowiec budowlany.
I edycja Konkursu Chemicznego im. Ignacego Łukasiewicza dla uczniów szkół gimnazjalnych rok szkolny 2014/2015 ZADANIA ETAP I (szkolny) Zadanie 1 Wapień znajduje szerokie zastosowanie jako surowiec budowlany.
CHEMIA KLASA II I PÓŁROCZE
 CHEMIA KLASA II I PÓŁROCZE wymienia zasady bhp dotyczące obchodzenia się z kwasami definiuje pojęcia: elektrolit i nieelektrolit wyjaśnia, co to jest wskaźnik i wymienia trzy przykłady odróżnia kwasy od
CHEMIA KLASA II I PÓŁROCZE wymienia zasady bhp dotyczące obchodzenia się z kwasami definiuje pojęcia: elektrolit i nieelektrolit wyjaśnia, co to jest wskaźnik i wymienia trzy przykłady odróżnia kwasy od
DZIAŁ 3: ROZTWORY WODNE OCENA ŚRÓDROCZNA
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii w klasie II, wynikające z realizowanego programu nauczania chemii w gimnazjum K.M. Pazdro
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii w klasie II, wynikające z realizowanego programu nauczania chemii w gimnazjum K.M. Pazdro
Wymagania edukacyjne na poszczególne oceny z chemii dla klasy II gimnazjum oparte na programie nauczania Chemia Nowa Era
 Wymagania edukacyjne na poszczególne oceny z chemii dla klasy II gimnazjum oparte na programie nauczania Chemia Nowa Era IV. Kwasy Opracowała mgr Agnieszka Para Ocena dopuszczająca [1] wymienia zasady
Wymagania edukacyjne na poszczególne oceny z chemii dla klasy II gimnazjum oparte na programie nauczania Chemia Nowa Era IV. Kwasy Opracowała mgr Agnieszka Para Ocena dopuszczająca [1] wymienia zasady
KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 ... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, Witaj w pierwszym etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, Witaj w pierwszym etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
X Konkurs Chemii Nieorganicznej i Ogólnej rok szkolny 2011/12
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO X Konkurs Chemii Nieorganicznej i Ogólnej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1. (10
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO X Konkurs Chemii Nieorganicznej i Ogólnej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1. (10
KLASA II Dział 6. WODOROTLENKI A ZASADY
 KLASA II Dział 6. WODOROTLENKI A ZASADY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą definiuje wskaźnik; wyjaśnia pojęcie: wodorotlenek; wskazuje metale aktywne i mniej aktywne; wymienia
KLASA II Dział 6. WODOROTLENKI A ZASADY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą definiuje wskaźnik; wyjaśnia pojęcie: wodorotlenek; wskazuje metale aktywne i mniej aktywne; wymienia
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap rejonowy rok szkolny 2009/2010 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap rejonowy rok szkolny 2009/2010 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
H2S, H2SO4, H2SO3, HNO3, H2CO3,
 Wymagania programowe z chemii dla klasy drugiej (na podstawie treści zawartych w podstawie programowej, programie nauczania oraz podręczniku dla klasy drugiej gimnazjum Chemia Nowej Ery). Wyróżnione wymagania
Wymagania programowe z chemii dla klasy drugiej (na podstawie treści zawartych w podstawie programowej, programie nauczania oraz podręczniku dla klasy drugiej gimnazjum Chemia Nowej Ery). Wyróżnione wymagania
Kryteria oceniania z chemii dla klasy drugiej DLA UCZNIÓW Z OBOWIĄZKIEM DOSTOSOWANIA WYMAGAŃ EDUKACYJNYCH
 Kryteria oceniania z chemii dla klasy drugiej DLA UCZNIÓW Z OBOWIĄZKIEM DOSTOSOWANIA WYMAGAŃ EDUKACYJNYCH (na podstawie treści zawartych w podstawie programowej, programie nauczania oraz podręczniku dla
Kryteria oceniania z chemii dla klasy drugiej DLA UCZNIÓW Z OBOWIĄZKIEM DOSTOSOWANIA WYMAGAŃ EDUKACYJNYCH (na podstawie treści zawartych w podstawie programowej, programie nauczania oraz podręczniku dla
Technologie Materiałów Budowlanych Wykład 3. Mineralne spoiwa budowlane cz. II
 Technologie Materiałów Budowlanych Wykład 3 Mineralne spoiwa budowlane cz. II Spoiwa gipsowe surowce naturalne : kamień gipsowy - CaSO 4 *2 H 2 O (95%) anhydryt - CaSO 4 gipsy chemiczne (syntetyczne) gipsy
Technologie Materiałów Budowlanych Wykład 3 Mineralne spoiwa budowlane cz. II Spoiwa gipsowe surowce naturalne : kamień gipsowy - CaSO 4 *2 H 2 O (95%) anhydryt - CaSO 4 gipsy chemiczne (syntetyczne) gipsy
Wymagania z chemii na poszczególne oceny Klasa 2 gimnazjum. Kwasy.
 Wymagania z chemii na poszczególne oceny Klasa 2 gimnazjum Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz: Omawiają przemysłową metodę otrzymywania kwasu
Wymagania z chemii na poszczególne oceny Klasa 2 gimnazjum Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz: Omawiają przemysłową metodę otrzymywania kwasu
Drewno. Zalety: Wady:
 Drewno Drewno to naturalny surowiec w pełni odnawialny. Dzięki racjonalnej gospodarce leśnej w Polsce zwiększają się nie tylko zasoby drewna, lecz także powierzchnia lasów. łatwość w obróbce, lekkość i
Drewno Drewno to naturalny surowiec w pełni odnawialny. Dzięki racjonalnej gospodarce leśnej w Polsce zwiększają się nie tylko zasoby drewna, lecz także powierzchnia lasów. łatwość w obróbce, lekkość i
Wymagania programowe na poszczególne oceny chemia kl. II Gimnazjum Rok szkolny 2015/2016 Wewnętrzna budowa materii
 Wymagania programowe na poszczególne oceny chemia kl. II Gimnazjum Rok szkolny 2015/2016 Wewnętrzna budowa materii Dopuszczający (K) Dostateczny(P) Dobry(R) Bardzo dobry (D) Celujący (W) Uczeń : - wie,
Wymagania programowe na poszczególne oceny chemia kl. II Gimnazjum Rok szkolny 2015/2016 Wewnętrzna budowa materii Dopuszczający (K) Dostateczny(P) Dobry(R) Bardzo dobry (D) Celujący (W) Uczeń : - wie,
IX Powiatowy Konkurs z Chemii. dla uczniów gimnazjum. w roku szkolnym 2011/2012. pod patronatem Jurajskiego Stowarzyszenia Nauczycieli Twórczych.
 IX Powiatowy Konkurs z Chemii dla uczniów gimnazjum w roku szkolnym 2011/2012 pod patronatem Jurajskiego Stowarzyszenia Nauczycieli Twórczych. KOD UCZNIA. Etap szkolny Data: 19. 03. 2012 Czas pracy- 90
IX Powiatowy Konkurs z Chemii dla uczniów gimnazjum w roku szkolnym 2011/2012 pod patronatem Jurajskiego Stowarzyszenia Nauczycieli Twórczych. KOD UCZNIA. Etap szkolny Data: 19. 03. 2012 Czas pracy- 90
Scenariusz lekcji otwartej w klasie drugiej gimnazjum. Opracowała: Marzena Bień
 Scenariusz lekcji otwartej w klasie drugiej gimnazjum Opracowała: Marzena Bień Termin realizacji: 13.03.2008 r. Czas realizacji: 45 minut Temat: Reakcje metali z kwasami. Cel ogólny: Zapoznanie się z jedną
Scenariusz lekcji otwartej w klasie drugiej gimnazjum Opracowała: Marzena Bień Termin realizacji: 13.03.2008 r. Czas realizacji: 45 minut Temat: Reakcje metali z kwasami. Cel ogólny: Zapoznanie się z jedną
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab
 SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab CZĄSTECZKA I RÓWNANIE REKCJI CHEMICZNEJ potrafi powiedzieć co to jest: wiązanie chemiczne, wiązanie jonowe, wiązanie
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab CZĄSTECZKA I RÓWNANIE REKCJI CHEMICZNEJ potrafi powiedzieć co to jest: wiązanie chemiczne, wiązanie jonowe, wiązanie
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLASY II. Ocena Semestr I Semestr II
 WYMAGANIA PROGRAMOWE Z CHEMII DLA KLASY II Ocena Semestr I Semestr II Wymagania konieczne( ocena dopuszczająca ) - zna treść prawa zachowania masy i prawa stałości składu związku chemicznego - potrafi
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLASY II Ocena Semestr I Semestr II Wymagania konieczne( ocena dopuszczająca ) - zna treść prawa zachowania masy i prawa stałości składu związku chemicznego - potrafi
Wymagania programowe na poszczególne oceny. Chemia Kl.2. I. Kwasy
 Wymagania programowe na poszczególne oceny Chemia Kl.2 I. Kwasy Ocena dopuszczająca zna zasady bhp dotyczące obchodzenia się z kwasami definiuje elektrolit, nieelektrolit wyjaśnia pojęcie wskaźnika i wymienia
Wymagania programowe na poszczególne oceny Chemia Kl.2 I. Kwasy Ocena dopuszczająca zna zasady bhp dotyczące obchodzenia się z kwasami definiuje elektrolit, nieelektrolit wyjaśnia pojęcie wskaźnika i wymienia
Przemiany substancji
 Przemiany substancji Poniżej przedstawiono graf pokazujący rodzaje przemian jaki ulegają substancje chemiczne. Przemiany substancji Przemiany chemiczne Przemiany fizyczne Objawy: - zmiania barwy, - efekty
Przemiany substancji Poniżej przedstawiono graf pokazujący rodzaje przemian jaki ulegają substancje chemiczne. Przemiany substancji Przemiany chemiczne Przemiany fizyczne Objawy: - zmiania barwy, - efekty
Skały budujące Ziemię
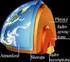 Skały budujące Ziemię Minerały Minerał pierwiastek lub związek chemiczny powstały w przyrodzie w sposób naturalny, jednorodny pod względem chemicznym i fizycznym. Minerały w większości mają budowę krystaliczną.
Skały budujące Ziemię Minerały Minerał pierwiastek lub związek chemiczny powstały w przyrodzie w sposób naturalny, jednorodny pod względem chemicznym i fizycznym. Minerały w większości mają budowę krystaliczną.
MAŁOPOLSKI KONKURS CHEMICZNY. dla uczniów szkół podstawowych. 25 października 2019 r. Etap I (szkolny)
 Kod ucznia MAŁOPOLSKI KONKURS CHEMICZNY dla uczniów szkół podstawowych 25 października 2019 r. Etap I (szkolny) Wypełnia Komisja Etapu Szkolnego Zadanie 1 2 3 4 5 6 7 8 9 10 Maksymalna 2 2 2 1 4 1 2 1
Kod ucznia MAŁOPOLSKI KONKURS CHEMICZNY dla uczniów szkół podstawowych 25 października 2019 r. Etap I (szkolny) Wypełnia Komisja Etapu Szkolnego Zadanie 1 2 3 4 5 6 7 8 9 10 Maksymalna 2 2 2 1 4 1 2 1
Zasady oceniania z chemii w klasie II w roku szkolnym 2015/2016. Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra
 Zasady oceniania z chemii w klasie II w roku szkolnym 2015/2016 I. Kwasy wymienia zasady bhp dotyczące obchodzenia się z kwasami definiuje pojęcia: elektrolit i nieelektrolit wyjaśnia, co to jest wskaźnik
Zasady oceniania z chemii w klasie II w roku szkolnym 2015/2016 I. Kwasy wymienia zasady bhp dotyczące obchodzenia się z kwasami definiuje pojęcia: elektrolit i nieelektrolit wyjaśnia, co to jest wskaźnik
KONKURS Z CHEMII. dla uczniów gimnazjów województwa warmińsko-mazurskiego w roku szkolnym 2017/2018 ETAP WOJEWÓDZKI 22 LUTEGO 2018
 Nr zada nia Licz ba pkt. 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Nr zada nia Licz ba pkt. 15 16 17 18 19 20 SUMA PKT. % KOD UCZNIA... KONKURS Z CHEMII dla uczniów gimnazjów województwa warmińsko-mazurskiego w
Nr zada nia Licz ba pkt. 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Nr zada nia Licz ba pkt. 15 16 17 18 19 20 SUMA PKT. % KOD UCZNIA... KONKURS Z CHEMII dla uczniów gimnazjów województwa warmińsko-mazurskiego w
Instrukcja dla uczestnika. II etap Konkursu. U z u p e ł n i j s w o j e d a n e p r z e d r o z p o c z ę c i e m r o z w i ą z y w a n i a z a d a ń
 III edycja rok szkolny 2017/2018 Uzupełnia Organizator Konkursu Instrukcja dla uczestnika II etap Konkursu Liczba uzyskanych punktów 1. Sprawdź, czy arkusz konkursowy, który otrzymałeś zawiera 12 stron.
III edycja rok szkolny 2017/2018 Uzupełnia Organizator Konkursu Instrukcja dla uczestnika II etap Konkursu Liczba uzyskanych punktów 1. Sprawdź, czy arkusz konkursowy, który otrzymałeś zawiera 12 stron.
grupa a Człowiek i środowisko
 grupa a Człowiek i środowisko................................................. Imię i nazwisko Poniższy test składa się z 18 zadań. Przy każdym poleceniu podano liczbę punktów możliwą do uzyskania za prawidłową
grupa a Człowiek i środowisko................................................. Imię i nazwisko Poniższy test składa się z 18 zadań. Przy każdym poleceniu podano liczbę punktów możliwą do uzyskania za prawidłową
Nauczycielski plan dydaktyczny z chemii klasa: 1 LO, I ZS, 2 TA, 2 TŻ1, 2 TŻ2, 2 TŻR, 2 TI,2 TE1, 2 TE2, zakres podstawowy
 Nauczycielski plan dydaktyczny z chemii klasa: 1 LO, I ZS, 2 TA, 2 TŻ1, 2 TŻ2, 2 TŻR, 2 TI,2 TE1, 2 TE2, zakres podstawowy Temat lekcji Treści nauczania 1. Zapoznanie z przedmiotowym systemem oceniania
Nauczycielski plan dydaktyczny z chemii klasa: 1 LO, I ZS, 2 TA, 2 TŻ1, 2 TŻ2, 2 TŻR, 2 TI,2 TE1, 2 TE2, zakres podstawowy Temat lekcji Treści nauczania 1. Zapoznanie z przedmiotowym systemem oceniania
Kod ucznia: Zadanie Maksymalna ilość
 Warszawa 16 maja 2008r. Międzyszkolny konkurs chemiczny KWAS Etap II międzyszkolny Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Maksymalna ilość 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Liczba uzyskana
Warszawa 16 maja 2008r. Międzyszkolny konkurs chemiczny KWAS Etap II międzyszkolny Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Maksymalna ilość 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Liczba uzyskana
WYMAGANIA NA POSZCZEGÓLNE OCENY Z CHEMII DLA KLASY II. mgr Marta Warecka Lenart
 WYMAGANIA NA POSZCZEGÓLNE OCENY Z CHEMII DLA KLASY II mgr Marta Warecka Lenart (program nauczania chemii Chemia Nowej Ery autorstwa T.Kulawik i M.Litwin) Ocenę dopuszczający otrzymuje uczeń, który w 75%
WYMAGANIA NA POSZCZEGÓLNE OCENY Z CHEMII DLA KLASY II mgr Marta Warecka Lenart (program nauczania chemii Chemia Nowej Ery autorstwa T.Kulawik i M.Litwin) Ocenę dopuszczający otrzymuje uczeń, który w 75%
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych. CHEMIA klasa II.
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa II Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -wymienia zasady bhp
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa II Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -wymienia zasady bhp
ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII
 ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII Zadanie 1. Na rysunku przedstawiono fragment układu okresowego pierwiastków. Dokoocz zdania tak aby były prawdziwe. Wiązanie jonowe występuje w związku chemicznym
ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII Zadanie 1. Na rysunku przedstawiono fragment układu okresowego pierwiastków. Dokoocz zdania tak aby były prawdziwe. Wiązanie jonowe występuje w związku chemicznym
Kalendarz trzecioklasisty CHEMIA
 Kalendarz trzecioklasisty CHEMIA POWTARZAJ RAZEM Z NAMI Miesiąc Wrzesieo Październik Listopad Grudzieo Styczeo Luty Marzec Kwiecieo Zagadnienie do powtórzenia Substancje chemiczne i ich przemiany Atom
Kalendarz trzecioklasisty CHEMIA POWTARZAJ RAZEM Z NAMI Miesiąc Wrzesieo Październik Listopad Grudzieo Styczeo Luty Marzec Kwiecieo Zagadnienie do powtórzenia Substancje chemiczne i ich przemiany Atom
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 POUFNE Pieczątka szkoły 16 styczeń 2010 r. Kod ucznia Wpisuje uczeń po otrzymaniu zadań Imię Wpisać po rozkodowaniu pracy Czas pracy 90 minut Nazwisko KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY
POUFNE Pieczątka szkoły 16 styczeń 2010 r. Kod ucznia Wpisuje uczeń po otrzymaniu zadań Imię Wpisać po rozkodowaniu pracy Czas pracy 90 minut Nazwisko KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY
Chemia nieorganiczna Zadanie Poziom: podstawowy
 Zadanie 1 2 3 4 5 6 7 8 9 10 (Nazwisko i imię) Punkty Razem pkt % Chemia nieorganiczna Zadanie 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 Poziom: podstawowy Punkty Zadanie 1. (1 pkt.) W podanym
Zadanie 1 2 3 4 5 6 7 8 9 10 (Nazwisko i imię) Punkty Razem pkt % Chemia nieorganiczna Zadanie 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 Poziom: podstawowy Punkty Zadanie 1. (1 pkt.) W podanym
SCENARIUSZ LEKCJI CHEMII
 SCENARIUSZ LEKCJI CHEMII Temat: PIERWIASTKI, ICH NAZWY I SYMBOLE Wymagania podstawy programowej uczeń: I.9) posługuje się symbolami pierwiastków ( ): H, C, N, O, Na, Mg, Al, Si, P, S, Cl, K, Ca, Fe, Cu,
SCENARIUSZ LEKCJI CHEMII Temat: PIERWIASTKI, ICH NAZWY I SYMBOLE Wymagania podstawy programowej uczeń: I.9) posługuje się symbolami pierwiastków ( ): H, C, N, O, Na, Mg, Al, Si, P, S, Cl, K, Ca, Fe, Cu,
CHEMIA KL. II GIMNAZJUM. Wymagania ogólne na poszczególne stopnie szkolne:
 CHEMIA KL. II GIMNAZJUM Wymagania ogólne na poszczególne stopnie szkolne: Ocenę celującą na semestr/koniec roku otrzymuje uczeń, który: - posiada wiadomości i umiejętności znacznie wykraczające poza program
CHEMIA KL. II GIMNAZJUM Wymagania ogólne na poszczególne stopnie szkolne: Ocenę celującą na semestr/koniec roku otrzymuje uczeń, który: - posiada wiadomości i umiejętności znacznie wykraczające poza program
SCENARIUSZ LEKCJI prowadzonej pod kątem hospitacji diagnozującej w klasie pierwszej gimnazjum
 Literka.pl Atom i cząsteczka Data dodania: 2010-05-31 11:51:50 Autor: Anna Piwowarczyk Podsumowanie wiadomości o wewnętrznej budowie materii. SCENARIUSZ LEKCJI prowadzonej pod kątem hospitacji diagnozującej
Literka.pl Atom i cząsteczka Data dodania: 2010-05-31 11:51:50 Autor: Anna Piwowarczyk Podsumowanie wiadomości o wewnętrznej budowie materii. SCENARIUSZ LEKCJI prowadzonej pod kątem hospitacji diagnozującej
WYKRYWANIE ZANIECZYSZCZEŃ WODY POWIERZA I GLEBY
 WYKRYWANIE ZANIECZYSZCZEŃ WODY POWIERZA I GLEBY Instrukcja przygotowana w Pracowni Dydaktyki Chemii Zakładu Fizykochemii Roztworów. 1. Zanieczyszczenie wody. Polska nie należy do krajów posiadających znaczne
WYKRYWANIE ZANIECZYSZCZEŃ WODY POWIERZA I GLEBY Instrukcja przygotowana w Pracowni Dydaktyki Chemii Zakładu Fizykochemii Roztworów. 1. Zanieczyszczenie wody. Polska nie należy do krajów posiadających znaczne
Temat 2: Nazewnictwo związków chemicznych. Otrzymywanie i właściwości tlenków
 Zasada ogólna: We wzorze sumarycznym pierwiastki zapisujemy od metalu do niemetalu, natomiast odczytujemy nazwę zaczynając od niemetalu: MgO, CaS, NaF Nazwy związków chemicznych najczęściej tworzymy, korzystając
Zasada ogólna: We wzorze sumarycznym pierwiastki zapisujemy od metalu do niemetalu, natomiast odczytujemy nazwę zaczynając od niemetalu: MgO, CaS, NaF Nazwy związków chemicznych najczęściej tworzymy, korzystając
Scenariusz lekcji otwartej chemia w klasie III w dniu Temat: Kwasy, zasady i sole powtórzenie wiadomości.
 Autor mgr Sławomir Rybiński Scenariusz lekcji otwartej chemia w klasie III w dniu 4.03.2014 Cele realizacja podstawy programowej: - Cele ogólne II. Rozumowanie i zastosowanie nabytej wiedzy do rozwiązywania
Autor mgr Sławomir Rybiński Scenariusz lekcji otwartej chemia w klasie III w dniu 4.03.2014 Cele realizacja podstawy programowej: - Cele ogólne II. Rozumowanie i zastosowanie nabytej wiedzy do rozwiązywania
Powtórzenie wiadomości z kl. I
 Mariola Winiarczyk Zespół Szkolno-Gimnazjalny Rakoniewice Powtórzenie wiadomości z kl. I Na początku kl. I po kilku lekcjach przypominających materiał w każdej klasie przeprowadzam mini konkurs chemiczny.
Mariola Winiarczyk Zespół Szkolno-Gimnazjalny Rakoniewice Powtórzenie wiadomości z kl. I Na początku kl. I po kilku lekcjach przypominających materiał w każdej klasie przeprowadzam mini konkurs chemiczny.
Egzamin gimnazjalny. Chemia. Także w wersji online TRENING PRZED EGZAMINEM. Sprawdź, czy zdasz!
 Egzamin gimnazjalny 1 Chemia TRENING PRZED EGZAMINEM Także w wersji online Sprawdź, czy zdasz! Spis treści Zestaw 1: Substancje i ich właściwości 5 Zestaw 2: Wewnętrzna budowa materii 9 Zestaw 3: Reakcje
Egzamin gimnazjalny 1 Chemia TRENING PRZED EGZAMINEM Także w wersji online Sprawdź, czy zdasz! Spis treści Zestaw 1: Substancje i ich właściwości 5 Zestaw 2: Wewnętrzna budowa materii 9 Zestaw 3: Reakcje
Imię i nazwisko Klasa Punkty (max 12) Ocena
 Rozdział 1. grupa A Imię i nazwisko Klasa Punkty (max 12) Ocena Data Zadanie 1. (1 pkt) Podkreśl właściwości dotyczące ditlenku węgla: gaz, rozpuszczalny w wodzie, bezbarwny, palny, żółty, powoduje zmętnienia
Rozdział 1. grupa A Imię i nazwisko Klasa Punkty (max 12) Ocena Data Zadanie 1. (1 pkt) Podkreśl właściwości dotyczące ditlenku węgla: gaz, rozpuszczalny w wodzie, bezbarwny, palny, żółty, powoduje zmętnienia
KWASY I WODOROTLENKI. 1. Poprawne nazwy kwasów H 2 S, H 2 SO 4, HNO 3, to:
 KWASY I WODOROTLENKI 1. Poprawne nazwy kwasów H 2 S, H 2 SO 4, HNO 3, to: 1. kwas siarkowy (IV), kwas siarkowy (VI), kwas azotowy, 2. kwas siarkowy (VI), kwas siarkowy (IV), kwas azotowy (V), 3. kwas siarkowodorowy,
KWASY I WODOROTLENKI 1. Poprawne nazwy kwasów H 2 S, H 2 SO 4, HNO 3, to: 1. kwas siarkowy (IV), kwas siarkowy (VI), kwas azotowy, 2. kwas siarkowy (VI), kwas siarkowy (IV), kwas azotowy (V), 3. kwas siarkowodorowy,
Warszawski konkurs chemiczny KWAS. Etap I szkolny. Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17
 Warszawa 17 marca 2009r. Warszawski konkurs chemiczny KWAS Etap I szkolny Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Maksymalna ilość punktów 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Liczba
Warszawa 17 marca 2009r. Warszawski konkurs chemiczny KWAS Etap I szkolny Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Maksymalna ilość punktów 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Liczba
WOJEWÓDZKI KONKURS CHEMICZNY
 Kod ucznia Liczba punktów WOJWÓDZKI KONKURS CHMICZNY DLA UCZNIÓW GIMNAZJÓW W ROKU SZKOLNYM 2014/2015 16 STYCZNIA 2015 1. Test konkursowy zawiera 26 zadań. Są to zadania zamknięte i otwarte. Na ich rozwiązanie
Kod ucznia Liczba punktów WOJWÓDZKI KONKURS CHMICZNY DLA UCZNIÓW GIMNAZJÓW W ROKU SZKOLNYM 2014/2015 16 STYCZNIA 2015 1. Test konkursowy zawiera 26 zadań. Są to zadania zamknięte i otwarte. Na ich rozwiązanie
Klasa II : Dział 1. WODA I ROZTWORY WODNE
 Klasa II : Dział 1. WODA I ROZTWORY WODNE Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą Celujący wymienia rodzaje wód; wie, jaką funkcję pełni woda w budowie organizmów; podaje przykłady
Klasa II : Dział 1. WODA I ROZTWORY WODNE Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą Celujący wymienia rodzaje wód; wie, jaką funkcję pełni woda w budowie organizmów; podaje przykłady
Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń:
![Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń: Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń:](/thumbs/70/63524095.jpg) Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018 III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących w przyrodzie podaje, na czym polega obieg wody w przyrodzie wymienia
Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018 III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących w przyrodzie podaje, na czym polega obieg wody w przyrodzie wymienia
Warszawski Konkurs Chemiczny KWAS Etap II Warszawski
 Warszawa dnia 8 maja 2010r. Warszawski Konkurs Chemiczny KWAS Etap II Warszawski Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 Maksymalna ilość punktów Liczba punktów
Warszawa dnia 8 maja 2010r. Warszawski Konkurs Chemiczny KWAS Etap II Warszawski Kod ucznia: Zadanie 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 Maksymalna ilość punktów Liczba punktów
II Etap rejonowy 28 styczeń 2019 r. Imię i nazwisko ucznia: Czas trwania: 60 minut
 XVI Wojewódzki Konkurs z Chemii dla uczniów klas trzecich gimnazjów oraz klas trzecich oddziałów gimnazjalnych prowadzonych w szkołach innego typu województwa świętokrzyskiego w roku szkolnym 2018/2019
XVI Wojewódzki Konkurs z Chemii dla uczniów klas trzecich gimnazjów oraz klas trzecich oddziałów gimnazjalnych prowadzonych w szkołach innego typu województwa świętokrzyskiego w roku szkolnym 2018/2019
Beata Mendak fakultety z chemii II tura PYTANIA Z KLASY PIERWSZEJ
 Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
2.4. ZADANIA STECHIOMETRIA. 1. Ile moli stanowi:
 2.4. ZADANIA 1. Ile moli stanowi: STECHIOMETRIA a/ 52 g CaCO 3 b/ 2,5 tony Fe(OH) 3 2. Ile g stanowi: a/ 4,5 mmol ZnSO 4 b/ 10 kmol wody 3. Obl. % skład Fe 2 (SO 4 ) 3 6H 2 O 4. Obl. % zawartość tlenu
2.4. ZADANIA 1. Ile moli stanowi: STECHIOMETRIA a/ 52 g CaCO 3 b/ 2,5 tony Fe(OH) 3 2. Ile g stanowi: a/ 4,5 mmol ZnSO 4 b/ 10 kmol wody 3. Obl. % skład Fe 2 (SO 4 ) 3 6H 2 O 4. Obl. % zawartość tlenu
Wymagania edukacyjne z chemii dla klasy drugiej
 Na ocenę dopuszczającą uczeń: Wymagania edukacyjne z chemii dla klasy drugiej odczytuje wartościowość pierwiastka z układu okresowego pierwiastków chemicznych; nazywa tlenki zapisane za pomocą wzoru sumarycznego;
Na ocenę dopuszczającą uczeń: Wymagania edukacyjne z chemii dla klasy drugiej odczytuje wartościowość pierwiastka z układu okresowego pierwiastków chemicznych; nazywa tlenki zapisane za pomocą wzoru sumarycznego;
PODSTAWY STECHIOMETRII
 PODSTAWY STECHIOMETRII 1. Obliczyć bezwzględne masy atomów, których względne masy atomowe wynoszą: a) 7, b) 35. 2. Obliczyć masę próbki wody zawierającej 3,01 10 24 cząsteczek. 3. Która z wymienionych
PODSTAWY STECHIOMETRII 1. Obliczyć bezwzględne masy atomów, których względne masy atomowe wynoszą: a) 7, b) 35. 2. Obliczyć masę próbki wody zawierającej 3,01 10 24 cząsteczek. 3. Która z wymienionych
WYZWANIA EKOLOGICZNE XXI WIEKU
 WYZWANIA EKOLOGICZNE XXI WIEKU ZA GŁÓWNE ŹRÓDŁA ZANIECZYSZCZEŃ UWAŻANE SĄ: -przemysł -transport -rolnictwo -gospodarka komunalna Zanieczyszczenie gleb Przyczyny zanieczyszczeń gleb to, np.: działalność
WYZWANIA EKOLOGICZNE XXI WIEKU ZA GŁÓWNE ŹRÓDŁA ZANIECZYSZCZEŃ UWAŻANE SĄ: -przemysł -transport -rolnictwo -gospodarka komunalna Zanieczyszczenie gleb Przyczyny zanieczyszczeń gleb to, np.: działalność
KONSPEKT LEKCJI Z CHEMII KLASA II. opracowała Aldona Pawłowska I ANALIZA MATERIAŁU NAUCZANIA II CELE NAUCZANIA III WYMAGANIA PROGRAMOWE IV TOK LEKCJI
 GIMNAZJUM NR 2 KONSPEKT LEKCJI Z CHEMII KLASA II opracowała Aldona Pawłowska ZAWARTOŚĆ KONSPEKTU: I ANALIZA MATERIAŁU NAUCZANIA II CELE NAUCZANIA III WYMAGANIA PROGRAMOWE IV TOK LEKCJI 1 KONSPEKT LEKCJI
GIMNAZJUM NR 2 KONSPEKT LEKCJI Z CHEMII KLASA II opracowała Aldona Pawłowska ZAWARTOŚĆ KONSPEKTU: I ANALIZA MATERIAŁU NAUCZANIA II CELE NAUCZANIA III WYMAGANIA PROGRAMOWE IV TOK LEKCJI 1 KONSPEKT LEKCJI
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE etap szkolny rok szkolny 2010/2011 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE etap szkolny rok szkolny 2010/2011 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
I. Substancje i ich przemiany
 NaCoBeZU z chemii dla klasy 7 I. Substancje i ich przemiany 1. Zasady bezpiecznej pracy na lekcjach chemii zaliczam chemię do nauk przyrodniczych stosuję zasady bezpieczeństwa obowiązujące w pracowni chemicznej
NaCoBeZU z chemii dla klasy 7 I. Substancje i ich przemiany 1. Zasady bezpiecznej pracy na lekcjach chemii zaliczam chemię do nauk przyrodniczych stosuję zasady bezpieczeństwa obowiązujące w pracowni chemicznej
Uczeń potrafi określić, w jakich dziedzinach surowce mineralne są wykorzystywane przez człowieka.
 Skorupa ziemska widziana oczami chemika 1. Cele lekcji a) Wiadomości Uczeń wie: co to jest skorupa ziemska, jakie pierwiastki wchodzą w skład skorupy ziemskiej, co to są minerały, skały i surowce mineralne,
Skorupa ziemska widziana oczami chemika 1. Cele lekcji a) Wiadomości Uczeń wie: co to jest skorupa ziemska, jakie pierwiastki wchodzą w skład skorupy ziemskiej, co to są minerały, skały i surowce mineralne,
Wymagania edukacyjne z chemii w klasie 2E
 Wymagania edukacyjne z chemii w klasie 2E Woda i roztwory wodne Wymagania na ocenę wymienia rodzaje wód; wie, jaką funkcję pełni woda w budowie organizmów; podaje przykłady roztworów i zawiesin spotykanych
Wymagania edukacyjne z chemii w klasie 2E Woda i roztwory wodne Wymagania na ocenę wymienia rodzaje wód; wie, jaką funkcję pełni woda w budowie organizmów; podaje przykłady roztworów i zawiesin spotykanych
Powietrze i inne gazy. Powietrze jest jednorodną mieszaniną gazów. Mieszanina ta nie posiada barwy, smaku ani zapachu.
 Składniki powietrza Powietrze jest jednorodną mieszaniną gazów. Mieszanina ta nie posiada barwy, smaku ani zapachu. Doświadczenie nr 1 Temat: Badanie składników powietrza. Schemat doświadczenia: Obserwacje:
Składniki powietrza Powietrze jest jednorodną mieszaniną gazów. Mieszanina ta nie posiada barwy, smaku ani zapachu. Doświadczenie nr 1 Temat: Badanie składników powietrza. Schemat doświadczenia: Obserwacje:
WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH
 WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH PODZIAŁ ZWIĄZKÓW NIEORGANICZNYCH Tlenki (kwasowe, zasadowe, amfoteryczne, obojętne) Związki niemetali Kwasy (tlenowe, beztlenowe) Wodorotlenki
WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH PODZIAŁ ZWIĄZKÓW NIEORGANICZNYCH Tlenki (kwasowe, zasadowe, amfoteryczne, obojętne) Związki niemetali Kwasy (tlenowe, beztlenowe) Wodorotlenki
a) Sole kwasu chlorowodorowego (solnego) to... b) Sole kwasu siarkowego (VI) to... c) Sole kwasu azotowego (V) to... d) Sole kwasu węglowego to...
 Karta pracy nr 73 Budowa i nazwy soli. 1. Porównaj wzory sumaryczne soli. FeCl 2 Al(NO 3 ) 3 K 2 CO 3 Cu 3 (PO 4 ) 2 K 2 SO 4 Ca(NO 3 ) 2 CaCO 3 KNO 3 PbSO 4 AlCl 3 Fe 2 (CO 3 ) 3 Fe 2 (SO 4 ) 3 AlPO 4
Karta pracy nr 73 Budowa i nazwy soli. 1. Porównaj wzory sumaryczne soli. FeCl 2 Al(NO 3 ) 3 K 2 CO 3 Cu 3 (PO 4 ) 2 K 2 SO 4 Ca(NO 3 ) 2 CaCO 3 KNO 3 PbSO 4 AlCl 3 Fe 2 (CO 3 ) 3 Fe 2 (SO 4 ) 3 AlPO 4
BADANIE WYNIKÓW NAUCZANIA Z CHEMII KLASA I GIMNAZJUM. PYTANIA ZAMKNIĘTE.
 BADANIE WYNIKÓW NAUCZANIA Z CHEMII KLASA I GIMNAZJUM. PYTANIA ZAMKNIĘTE. 1. Którą mieszaninę można rozdzielić na składniki poprzez filtrację; A. Wodę z octem. B. Wodę z kredą. C. Piasek z cukrem D. Wodę
BADANIE WYNIKÓW NAUCZANIA Z CHEMII KLASA I GIMNAZJUM. PYTANIA ZAMKNIĘTE. 1. Którą mieszaninę można rozdzielić na składniki poprzez filtrację; A. Wodę z octem. B. Wodę z kredą. C. Piasek z cukrem D. Wodę
Chemia Nowej Ery Wymagania programowe na poszczególne oceny dla klasy II
 Chemia Nowej Ery Wymagania programowe na poszczególne oceny dla klasy II Szczegółowe kryteria oceniania po pierwszym półroczu klasy II: III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących
Chemia Nowej Ery Wymagania programowe na poszczególne oceny dla klasy II Szczegółowe kryteria oceniania po pierwszym półroczu klasy II: III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących
SCENARIUSZ LEKCJI CHEMII LUB BIOLOGII Z WYKORZYSTANIEM FILMU SPOSÓB NA IDEALNĄ PIANĘ
 SCENARIUSZ LEKCJI CHEMII LUB BIOLOGII Z WYKORZYSTANIEM FILMU SPOSÓB NA IDEALNĄ PIANĘ SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III.
SCENARIUSZ LEKCJI CHEMII LUB BIOLOGII Z WYKORZYSTANIEM FILMU SPOSÓB NA IDEALNĄ PIANĘ SPIS TREŚCI: I. Wprowadzenie. II. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. III.
