Wykład 10 17/12/2010 ver. 1 (28/12/2010)
|
|
|
- Alojzy Markowski
- 7 lat temu
- Przeglądów:
Transkrypt
1 Wykład 10 17/12/2010 ver. 1 (28/12/2010) Siarka 1. Siarka nie jest pierwiastkiem limitującym wzrost roślin i bakterii. 2. Podlega krążeniu przy udziale różnych grup troficznych mikroorganizmów. 3. Jej przemiany są związane z procesami utleniania i redukcji (od -2 dla S do +6 dla SO 4 ). 4. Siarka występuje w ponad 2000 minerałach w których stanowi od 7 do 53% przez co jest jednym z 13 najpowszechniej występujących pierwiastków w skorupie ziemskiej. Obieg siarki przekształcenia siarki i jej związków zachodzące z udziałem mikroorganizmów są złożone. Największa ilość siarki na Ziemi znajduje się w osadach i skałach głównie w postaci gipsu (CaSO 4 ) i pirytu (FeS 2 ). Główny rezerwuar siarki dla biosfery to siarczany zawarte w oceanach. Znaczenie ma też siarkowodór pochodzenia biologicznego i geochemicznego. 1. Siarczki w warunkach tlenowych ulegają szybkiemu utlenianiu na drodze chemicznej. Utleniają je też chemolitotrofy i fototrofy anoksygenowe,=m 2. Siarka pierwiastkowa jest również utleniana przez w/w grupy bakterii, a w warunkach beztlenowych może stanowić końcowy akceptor dla niektórych archeonów i bakterii. 3. Siarczany stanowią źródło siarki dla wielu organizmów. W czasie mineralizacji związków organicznych dochodzi do desulfuryzacji, a więc uwolnienia z nich H 2 S. 4. Siarczany stanowią końcowy akceptor elektronów w tzw. oddychaniu siarczanowym bakterii redukujących siarczany. 5. Niektóre organizmy syntetyzują też rozmaite organiczne związki siarki. Przemiany siarki w toni wodnej i osadach.
2 Mikroorganizmy: utleniające redukujące związki siarki Bakterie utleniające związki siarki: I. obligatoryjne lub fakultatywne chemoautotrofy II. anoksygenowe fototrofy grupa Konwersja zw. siarki I H 2 S S 0 S 0 SO 4 S 2 O 3 SO 4 II H 2 S S 0 S 0 SO 4 wymagania środowisko rodzaj H 2 S - O 2 Beltlenowe, H 2 S, światło Gorące źródła, gleba, wody kopalniane Osady denne, wody beztlenowe Acidithiobacillus Thiomicrospira Achromatium Beggiatoa Thermothrix Chlorobium Chromatium Ectothiorhodospira Thiopedia Rhodopseudomonas Bezbarwne bakterie siarkowe 1. Utlenianie związków siarki przez bezbarwne bakterie siarkowe a.) bakterie tionowe (utleniające związki siarki i kwasy tionowe) grupa bardzo zróżnicowana fizjologicznie: - obligatoryjne chemolitoautotrofy grupa Typowy gat. Donor e Akceptor e Źródło węgla Produkt Bakterie siarkowe Acidothiobacil lus ferroxidans S 0, S 2 O 3 O 2 CO 2\ SO 4
3 Do obligatoryjnych chemolitotrofów należą także: Thiobacillus thiooxidans (Acidothiobacillus thiooxidans) T. Thioparus T. ferroxidans T. denitryficans - fakultatywne chemolitoautotrofy: rosną chemolitoautotroficznie na podłożu pozbawionym zw. organicznych, a chemoorganoheterotroficznie w obecności tych związków. Thiobacillus novelleus (Starkeya novella) Thiobacillus intermedius (Thiomonas intermedia) Thiomicrospira Sulfolobus (Archea) b.) bakterie siarkowe właściwe (utleniające tylko związki siarki) chemolitoheterotrofy: Beggiatoa, Thiotrix, Thioploca. Charakterystyczną cechą A. ferroxidans jest autotrofizm. Bakterie te to chemoautotrofy, ich źródłem węgla jest wyłącznie zaś źródłem energii tylko utlenianie związków nieorganicznych (np. pirytów). Pałeczki A. ferroxidans to organizmy tlenowe występujące w środowiskach skrajnie niekorzystnych: optymalna temperatura st. C. ph 1,5-3,5 (wybitnie kwasolubne, zdolne do rozmnażania w ph ok. 2) tolerują obecność wysokich stężeń metali ciężkich (np. w wodach kopalnianych) autotrofy CO2 to źródło węgla ( zdolne są do wzrostu przy braku jakichkolwiek związków organicznych). Mikrobiologiczne ługowanie metali bioługowanie trzy gatunki chemolitoautotroficznych bakterii utleniających związki żelaza i siarki są wykorzystywane w procesach bioługowania: Acidithiobacillus ferroxidans, Acidithiobacillus thiooxidans i Leptospirillum ferroxidans. Proces ten polega na wykorzystaniu zdolności niektórych kwasolubnych bakterii utleniających siarkę i/lub żelazo do przeprowadzania nierozpuszczalnych siarczków metali w rozpuszczalne siarczany. Sumarycznie reakcję ługowania można przedstawić następująco: 4FeS O 2 +H 2 O 2Fe 2 (SO 4 ) 3 + 2H 2 SO 4 Schemat utleniania pirytu przez bakterie z rodzaju Aciithiobacillus
4 Reakcja: I. ma charakter abiotyczny (chemiczny) i zachodzi powoli II. to mikrobiologiczne utlenianie Fe(II) do Fe(III) prowadzone przez Acidithiobacillus ferroxidans, jest to reakcja wielokrotnie szybsza od reakcji I, a powstający 2Fe 2 (SO 4 ) 3 jest silnym utleniaczem III powstały Fe 2 (SO 4 ) 3 reaguje z pirytem (dzięki czemu utlenianie pirytu przestaje być ograniczone szybkością reakcji I). W reakcji tej powstaje FeSO4 oraz S 0. IV. siarka elementarna jest utleniana do kwasu siarkowego przez Acidithiobacillus ferroxidans. Bezbarwne bakterie utleniające związki siarki podsumowanie Utleniają: H 2 S, S 0, SO 3, S 2 O 3, S 4 O 6 2 do SO 4 (zakwaszenie środowiska). Niektóre utleniają H 2 S dwuetapowo, najpierw do S 0, którą gromadzą wewnątrz komórek, np. Thiomargerita namibiensis. H 2 S + ½ O 2 S 0 + H 2 O Siarka ta może zostać wykorzystana gdy zabraknie H 2 S w środowisku. S 0 + H 2 O + 1,5 O 2 SO 4 + 2H + Niektóre utleniają także: SCN -, CS 2, (CH 3 )S H 2 S + 2O 2 SO 4 + 2H + Fototrofy anoksygenowe Fotosynteza typ Gatunek anoksygeno typowy wa Purpurowe siarkowe Purpurowe niesiarkowe Zielone siarkowe Zielone niesiarkowe Proteobact eria Proteobact eria Chromatium Barwniki fotosyntet yczne Bchl a lub Bchl b Rhodobacter Bchl a Chlorobi Chlorobium Bchl a i c (chloroso my) Chloroflex i Donor e H 2 S, S 0, S 2 O 3, H 2, H 2, zw. org, niektóre H 2 S H 2 S, S 0, S 2 O 3, H 2, Fe Chloroflexus Bchl a i c H 2 S, H 2, Źródło węgla Sposób wiązania CO2 Cykl Calvina Cykl Calvina Red. cykl kwasów trikarboksylo wych Szlak hydroksyprop ionowy Wzrost w ciemnoś ci i war. tlen. tak tak nie tak Występowanie bezbarwnych bakterii siarkowych 1. występują w: - złożach siarki, - gorących źródłach siarkowych, - kopalniach siarki i kopalniach węgla - w granicznej warstwie między środowiskiem tlenowym i beztlenowym wód (w warstwie beztlenowej bakterie redukujące siarczany wytwarzają H 2 S!!! omg!)
5 2. Bezbarwne bakterie siarkowe biorą udział w: - obiegu siarki - korozji betonu i metali - wykorzystuje się je do oczyszczania ścieków i ługowania metali. 3. Bezbarwne bakterie siarkowe występują jako: a.) bakterie swobodnie żyjące: Beggiatoa, Thiomicrospira, Thiobcillus pożywienie obunogów, krabów, małży. b.) bezbarwne bakterie siarkowe żyją w symbiozie z rurkoczułkowcami. Występują one na dnie oceanów w pobliżu ujść hydrotermalnych, w miejscach pęknięć skorupy ziemskiej (powstających na skutek ruchów płyt tektonicznych). Rurkoczułkowiec Riftia pachyptila (pogonofora) nie ma przewodu pokarmowego ma natomiast specjalny narząd trofosom. Trofosom zawiera endosymbionty (bezbarwne bakterie siarkowe), które wytwarzają związki organiczne z dostarczanych im przez krwioobieg zwierzęcia siarkowodowu, tlenu i dwutlenku węgla. Bezbarwne bakterie siarkowe występują też jako endosymbionty w komórkach skrzeli małża Calyptogena. Czarne kominy 1. Woda wydostająca się z ujść hydrotermalnych ma temperaturę ok. 350 st. C (ogrzała się w wyniku kontaktu z bazaltem i magmą) i zawiera związki nieorganiczne w tym H 2 S i FeS. 2. W chwili kontaktu wody gorącej z zimną siarczki wytrącają się i powstaje czarna chmura a dookoła charakterystyczne stożki tzw. czarne kominy. 3. Powierzchnia tych kominów pokryta jest rurkoczułkowcami (pogonofora) których długość wynosi nawet 1 m!!! (niemożliwe.) Budowa czarnego komina przy ujściu hydrotermalnym. 4. Rurkoczułkowce pokrywają całą powierzchnię kominów. 5. Gorąca woda wydostając się z komina przynosi do otaczających go zimnych wód oceanu siarczki i inne związki pochodzące z leżącej pod dnem oceanu warstwy skał. 6. Niektóre z minerałów wytrącają się tworząc dym, a [p opadnięciu przyczyniają się do powstawania komina. 7. Rurkoczułkowce pobierają siarczki, tlen, dwutlenek węgla i inne związki ze zmieszanych wód. Riftia pachyptila 1. Riftia pachyptila bytuje w temperaturze st. C i wysokim ciśnieniu.
6 2. We krwi rurkoczułkowca wstępuje forma hemoglobiny, która wiąże tlen, siarkowodór i dwutlenek węgla i dostarcza do organu zwanego trofosomem. 3. W trofosomie występują endosymbionty bezbarwne bakterie siarkowe, które uzyskują energię z utleniania siarczków do siarczanów. Źródłem węgla jest dla nich dwutlenek węgla. 4. Tlen, dwutlenek węgla i siarkowodór są dostarczane przez krwioobieg. Budowa Riftia Oddziaływania pokarmowe między komórkami trofosomu i endosymbiontem bakteryjnym. Endosymbiont utlenia HS - do SO 4 z wytworzeniem ATP, niezbędnego do wiązania dwutlenku węgla w związki organiczne [CHO] dostarczane komórkom zwierzęcia. Utlenianie związków siarki przez fototrofy anoksygenowe fototrofy anoksygenowe: nie wytwarzają tlenu, wykorzystują siarkę, nieorganiczne związki siarki, wodór, żelazo(iii) oraz zw. organiczne jako donory elektronów, przeprowadzają fotosyntezę tylko w warunkach beztlenowych lub gdy jest jego bardzo małe stężenie, w głębokich warstwach zbiornków. Należą do nich bakterie: purpurowe siarkowe, purpurowe niesiarkowe, zielone siarkowe, zielone niesiarkowe. 1. Purpurowe bakterie siarkowe (gamma-proteobacteria) Nazwa tej grupy pochodzi od zawartych w ich komórkach karotenoidów nadających im kolor czerwony, purpurowy lub brązowy. Donorem elektronów jest np. H 2 S utleniany do siarki gromadzonej wewnątrz komórek. Wiążą one dwutlenek węgla w cyklu Calvina. Występują w warstwie beztlenowej wód bogatych w siarczki np. Chromatium sp. W ciemności mogą rosnąć w warunkach tlenowych w obecności związków organicznych. 2. Purpurowe bakterie niesiarkowe (alfa-proteobacteria) Określenie niesiarkowe wzięło się stąd iż kiedyś uważano, że nie są one zdolne do wykorzystywania związków siarki jako donorów elektronów. Potem okazało się, że większość z nich może wykorzystywać siarczki, ale stężenie siarczku musi być niższe niż to, przy którym rosną bakterie purpurowe siarkowe. Mogą wykorzystywać wodór i związki organiczne jako donory elektronów, a niektóre także związki siarki np. Rhodobacter sphaeroides.
7 Niezwykle plastyczny metabolizm w zależności od warunków środowiska mogą rosnąć: fotolitoautotroficznie, fotoorganoheterotroficznie albo chemoorganoheterotroficznie. 3. Zielone bakterie siarkowe (typ Chlorobi) - fotolitoautotrofy, niektóre zdolne do fotoorganoheterotrofii, - wykorzystują H 2 S, S 0, S 2 O 3 lub H 2 jako donory elektronów, - wiążą dwutlenek węgla w reduktywnym cyklu kwasów trójkarboksylowych, np. Chlorobium spp. Odkładają siarkę na zewnątrz komórki, mają chlorosomy i zawierają barwniki fotosyntetyczne, - bakterie te nie są zdolne do wzrostu w ciemności w warunkach tlenowych. 4. Bakterie zielone niesiarkowe (typ Chloroflexi zawierający też bakterie niefotosyntetyzujące) - bakterie nitkowate, termofilne, tworzące grube maty w gorących źródłach, - w warunkach beztlenowych w świetle najwydajniej rosną fotoorganoheterotroficznie, - rosną też fotolitoautotroficznie (z wodorem lub siarkowodorem) - wiążą dwutlenek węgla w szlaku hydroksypropionowym unikatowym dla tej grupy bakterii, - w ciemności rosną chemoorganoheterotroficznie. Maksima absorpcji światła (to było na pierwszym zdaje się wykładzie. I tak się nie będziemy uczyć na pamięć jakie długości fali absorbują jakie glony... bez przesady.) Światło a rozmieszczenie bakterii Bakterie fotosyntetyzujące występują poniżej zasięgu występowania fitoplanktonu (głębokie wody, warunki beztlenowe, obecność siarkowodoru). Bakterie fotosyntetyzujące wykorzystują spektrum światła w zakresie: A nm (zielone bakterie siarkowe) B - >800 nm (bakterie purpurowe) Są to długości fali w znikomym stopniu wykorzystywane przez fitoplankton!!
Procesy biotransformacji
 Biohydrometalurgia jest to dział techniki zajmujący się otrzymywaniem metali przy użyciu mikroorganizmów i wody. Ma ona charakter interdyscyplinarny obejmujący wiedzę z zakresu biochemii, geomikrobiologii,
Biohydrometalurgia jest to dział techniki zajmujący się otrzymywaniem metali przy użyciu mikroorganizmów i wody. Ma ona charakter interdyscyplinarny obejmujący wiedzę z zakresu biochemii, geomikrobiologii,
Wykład 5 Biotechnologiczne metody pozyskiwania i ulepszania surowców
 Mikrobiologiczne ługowanie metali z rud, odpadów przemysłowych i osadów ściekowych Niektóre drobnoustroje wykorzystywane w przemysłowych procesach bioługowania Drobnoustrój Typ Metabolizm Optimum ph Zakres
Mikrobiologiczne ługowanie metali z rud, odpadów przemysłowych i osadów ściekowych Niektóre drobnoustroje wykorzystywane w przemysłowych procesach bioługowania Drobnoustrój Typ Metabolizm Optimum ph Zakres
Redukcja związków siarki 1. Mikroorganizmy redukujące utlenione związki siarki (np. SO 4
 Wykład 11 07/01/2011 ver. 1 (08/01/2011) Redukcja związków siarki 1. Mikroorganizmy redukujące utlenione związki siarki (np. SO 4 do H 2 S). Ich rola jest znacznie większa w wodach morskich i oceanach
Wykład 11 07/01/2011 ver. 1 (08/01/2011) Redukcja związków siarki 1. Mikroorganizmy redukujące utlenione związki siarki (np. SO 4 do H 2 S). Ich rola jest znacznie większa w wodach morskich i oceanach
EKOLOGIA OGÓLNA WBNZ 884. Wykład 5 Obieg pierwiastków (Biogeochemia)
 EKOLOGIA OGÓLNA WBNZ 884 Wykład 5 Obieg pierwiastków (Biogeochemia) 2007 Skład chemiczny organizmów Pierwiastki Związki chemiczne Zawartość w organizmach Bakteria Roślina grzyb ryba świnia H O Woda 75
EKOLOGIA OGÓLNA WBNZ 884 Wykład 5 Obieg pierwiastków (Biogeochemia) 2007 Skład chemiczny organizmów Pierwiastki Związki chemiczne Zawartość w organizmach Bakteria Roślina grzyb ryba świnia H O Woda 75
BILANS WĘGLA A ZMIANY GLOBALNE (jeszcze raz)
 BILANS WĘGLA A ZMIANY GLOBALNE (jeszcze raz) Nauka, pseudonauka, ideologia: Bilans węgla w biosferze i zmiany klimatu Wzrost zawartości CO 2 w atmosferze: poza dyskusją Zmiana parametrów efektu cieplarnianego:
BILANS WĘGLA A ZMIANY GLOBALNE (jeszcze raz) Nauka, pseudonauka, ideologia: Bilans węgla w biosferze i zmiany klimatu Wzrost zawartości CO 2 w atmosferze: poza dyskusją Zmiana parametrów efektu cieplarnianego:
WYKRYWANIE ZANIECZYSZCZEŃ WODY POWIERZA I GLEBY
 WYKRYWANIE ZANIECZYSZCZEŃ WODY POWIERZA I GLEBY Instrukcja przygotowana w Pracowni Dydaktyki Chemii Zakładu Fizykochemii Roztworów. 1. Zanieczyszczenie wody. Polska nie należy do krajów posiadających znaczne
WYKRYWANIE ZANIECZYSZCZEŃ WODY POWIERZA I GLEBY Instrukcja przygotowana w Pracowni Dydaktyki Chemii Zakładu Fizykochemii Roztworów. 1. Zanieczyszczenie wody. Polska nie należy do krajów posiadających znaczne
METABOLIZM. Zadanie 1. (3 pkt). Uzupełnij tabelę, wpisując w wolne kratki odpowiednio produkt oddychania tlenowego i produkty fermentacji alkoholowej.
 Zadanie 1. (3 pkt). Uzupełnij tabelę, wpisując w wolne kratki odpowiednio produkt oddychania tlenowego i produkty fermentacji alkoholowej. Zadanie 3. (3 pkt). Schemat mechanizmu otwierania aparatu szparkowego.
Zadanie 1. (3 pkt). Uzupełnij tabelę, wpisując w wolne kratki odpowiednio produkt oddychania tlenowego i produkty fermentacji alkoholowej. Zadanie 3. (3 pkt). Schemat mechanizmu otwierania aparatu szparkowego.
GLOBALNE CYKLE BIOGEOCHEMICZNE obieg siarki
 GLOBALNE CYKLE BIOGEOCHEMICZNE oieg siarki W organizmie ludzkim: mięśnie: 5000-11000 ppm, kości: 500-2400 ppm, krew 1,8 g/l Całkowita zawartość (70 kg): 140 g. Rozpowszechnienie siarki (wagowo) Ziemia
GLOBALNE CYKLE BIOGEOCHEMICZNE oieg siarki W organizmie ludzkim: mięśnie: 5000-11000 ppm, kości: 500-2400 ppm, krew 1,8 g/l Całkowita zawartość (70 kg): 140 g. Rozpowszechnienie siarki (wagowo) Ziemia
prawo czynników ograniczających Justus von Liebig
 prawo czynników ograniczających Justus von Liebig.. względne znaczenie jakiegoś czynnika ograniczającego jest tym większe, im bardziej dany czynnik, w porównaniu z innymi stanowi minimum. FOSFOR FOSFOR
prawo czynników ograniczających Justus von Liebig.. względne znaczenie jakiegoś czynnika ograniczającego jest tym większe, im bardziej dany czynnik, w porównaniu z innymi stanowi minimum. FOSFOR FOSFOR
Komórka organizmy beztkankowe
 Grupa a Komórka organizmy beztkankowe Poniższy test składa się z 12 zadań. Przy każdym poleceniu podano liczbę punktów możliwą do uzyskania za prawidłową odpowiedź. Za rozwiązanie całego testu możesz otrzymać
Grupa a Komórka organizmy beztkankowe Poniższy test składa się z 12 zadań. Przy każdym poleceniu podano liczbę punktów możliwą do uzyskania za prawidłową odpowiedź. Za rozwiązanie całego testu możesz otrzymać
BIOTECHNOLOGIA OGÓLNA
 BIOTECHNOLOGIA OGÓLNA 1. 2. 3. 4. 5. Ogólne podstawy biologicznych metod oczyszczania ścieków. Ścieki i ich rodzaje. Stosowane metody analityczne. Substancje biogenne w ściekach. Tlenowe procesy przemiany
BIOTECHNOLOGIA OGÓLNA 1. 2. 3. 4. 5. Ogólne podstawy biologicznych metod oczyszczania ścieków. Ścieki i ich rodzaje. Stosowane metody analityczne. Substancje biogenne w ściekach. Tlenowe procesy przemiany
FOSFOR. w litosferze. apatyty: Ca 5 (PO 4 ) 3. fluoroapatyty hydroksyapatyty chloroapatyty
 FOSFOR FOSFOR w litosferze apatyty: Ca 5 (PO 4 ) 3 F Ca 5 (PO 4 ) 3 OH Ca 5 (PO 4 ) 3 Cl fluoroapatyty hydroksyapatyty chloroapatyty FOSFOR w litosferze apatyty: Ca 5 (PO 4 ) 3 F Ca 5 (PO 4 ) 3 OH Ca 5
FOSFOR FOSFOR w litosferze apatyty: Ca 5 (PO 4 ) 3 F Ca 5 (PO 4 ) 3 OH Ca 5 (PO 4 ) 3 Cl fluoroapatyty hydroksyapatyty chloroapatyty FOSFOR w litosferze apatyty: Ca 5 (PO 4 ) 3 F Ca 5 (PO 4 ) 3 OH Ca 5
Energia kwantu jest odwrotnie proporcjonalna do długości fali elektromagnetycznej.
 Wykład 3 22/10/2010 ver. 1-A (08/12/2010) Temat: Światło Światło Podstawowym czynnikiem warunkującym istnienie życia na Ziemi jest energia słoneczna. W procesie fotosyntezy zostaje ona zmieniona w energię
Wykład 3 22/10/2010 ver. 1-A (08/12/2010) Temat: Światło Światło Podstawowym czynnikiem warunkującym istnienie życia na Ziemi jest energia słoneczna. W procesie fotosyntezy zostaje ona zmieniona w energię
Metabolizm komórkowy i sposoby uzyskiwania energii
 Metabolizm komórkowy i sposoby uzyskiwania energii Metabolizm całokształt reakcji chemicznych i związanych z nimi przemian energii zachodzący w komórkach. Podstawa wszelakich zjawisk biologicznych. Metabolizm
Metabolizm komórkowy i sposoby uzyskiwania energii Metabolizm całokształt reakcji chemicznych i związanych z nimi przemian energii zachodzący w komórkach. Podstawa wszelakich zjawisk biologicznych. Metabolizm
Zn + S ZnS Utleniacz:... Reduktor:...
 Zadanie: 1 Spaliny wydostające się z rur wydechowych samochodów zawierają znaczne ilości tlenku węgla(ii) i tlenku azotu(ii). Gazy te są bardzo toksyczne i dlatego w aktualnie produkowanych samochodach
Zadanie: 1 Spaliny wydostające się z rur wydechowych samochodów zawierają znaczne ilości tlenku węgla(ii) i tlenku azotu(ii). Gazy te są bardzo toksyczne i dlatego w aktualnie produkowanych samochodach
Wirusy i bakterie. Barbara Lewicka
 Wirusy i bakterie Barbara Lewicka Budowa wirusa HIV a) glikoproteina 120, b) glikoproteina 41, c) lipidowa osłonka zewnętrzna, d) białkowa osłonka rdzenia, e) proteaza, f) kapsyd, g) RNA, h) odwrotna
Wirusy i bakterie Barbara Lewicka Budowa wirusa HIV a) glikoproteina 120, b) glikoproteina 41, c) lipidowa osłonka zewnętrzna, d) białkowa osłonka rdzenia, e) proteaza, f) kapsyd, g) RNA, h) odwrotna
CYKL AZOTU W BIOSFERZE
 CYKL AZOTU W BIOSFERZE Stopień utlenienia związek +5 N 2 O 5 HNO 3, NO 3 - +4 NO 2 N 2 O 4 +3 HNO 2 NO 2 - +2 NO +1 N 2 O 0 N 2 (-1, -2) (NH 2 OH, N 2 H 4 ) -3 NH 3, NH + 4 CH 3 NH 2 Stopień utlenienia
CYKL AZOTU W BIOSFERZE Stopień utlenienia związek +5 N 2 O 5 HNO 3, NO 3 - +4 NO 2 N 2 O 4 +3 HNO 2 NO 2 - +2 NO +1 N 2 O 0 N 2 (-1, -2) (NH 2 OH, N 2 H 4 ) -3 NH 3, NH + 4 CH 3 NH 2 Stopień utlenienia
Geochemia krajobrazu. pod redakcją Urszuli Pokojskiej i Renaty Bednarek
 Geochemia krajobrazu pod redakcją Urszuli Pokojskiej i Renaty Bednarek SPIS TREŚCI Spis treści Spis treści Przedmowa... 11 CZĘŚĆ 1. WIADOMOŚCI WPROWADZAJĄCE Rozdział I. Elementy chemii ogólnej (Urszula
Geochemia krajobrazu pod redakcją Urszuli Pokojskiej i Renaty Bednarek SPIS TREŚCI Spis treści Spis treści Przedmowa... 11 CZĘŚĆ 1. WIADOMOŚCI WPROWADZAJĄCE Rozdział I. Elementy chemii ogólnej (Urszula
Udział drobnoustrojów glebowych w obiegu węgla, azotu i siarki w przyrodzie
 Udział drobnoustrojów glebowych w obiegu węgla, azotu i siarki w przyrodzie Drobnoustroje prowadzące fotosyntezę W glebie występuje co najmniej 13 tysięcy gatunków bakterii, jednak większość z nich jest
Udział drobnoustrojów glebowych w obiegu węgla, azotu i siarki w przyrodzie Drobnoustroje prowadzące fotosyntezę W glebie występuje co najmniej 13 tysięcy gatunków bakterii, jednak większość z nich jest
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 16 stycznia 2015 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 16 stycznia 2015 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 16 stycznia 2015 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Woda. Najpospolitsza czy najbardziej niezwykła substancja Świata?
 Woda Najpospolitsza czy najbardziej niezwykła substancja Świata? Cel wykładu Odpowiedź na pytanie zawarte w tytule A także próby odpowiedzi na pytania typu: Dlaczego woda jest mokra a lód śliski? Dlaczego
Woda Najpospolitsza czy najbardziej niezwykła substancja Świata? Cel wykładu Odpowiedź na pytanie zawarte w tytule A także próby odpowiedzi na pytania typu: Dlaczego woda jest mokra a lód śliski? Dlaczego
BIOCHEMICZNE ZAPOTRZEBOWANIE TLENU
 BIOCHEMICZNE ZAPOTRZEBOWANIE TLENU W procesach samooczyszczania wód zanieczyszczonych związkami organicznymi zachodzą procesy utleniania materii organicznej przy współudziale mikroorganizmów tlenowych.
BIOCHEMICZNE ZAPOTRZEBOWANIE TLENU W procesach samooczyszczania wód zanieczyszczonych związkami organicznymi zachodzą procesy utleniania materii organicznej przy współudziale mikroorganizmów tlenowych.
Biochemia zadymionych komórek
 Biochemia zadymionych komórek Dariusz Latowski Uniwersytet Jagielloński Wydział Biochemii, Biofizyki i Biotechnologii Zakład Fizjologii i Biochemii Roślin Biochemia zadymionych komórek hemia życia zadymionych
Biochemia zadymionych komórek Dariusz Latowski Uniwersytet Jagielloński Wydział Biochemii, Biofizyki i Biotechnologii Zakład Fizjologii i Biochemii Roślin Biochemia zadymionych komórek hemia życia zadymionych
Chemiczne oddziaływanie składowisk odpadów górnictwa węgla kamiennego na środowisko
 Chemiczne oddziaływanie składowisk odpadów górnictwa węgla kamiennego na środowisko Prof. nadzw. dr hab. Andrzej Misiołek Wydział Nauk Technicznych Wyższa Szkoła Zarządzania Ochroną Pracy w Katowicach
Chemiczne oddziaływanie składowisk odpadów górnictwa węgla kamiennego na środowisko Prof. nadzw. dr hab. Andrzej Misiołek Wydział Nauk Technicznych Wyższa Szkoła Zarządzania Ochroną Pracy w Katowicach
-wszystkie substancje (pierwiastki lub zw chem) które biorą udział w reakcji chemicznej nazywamy reagentami
 Zapis reakcji chemicznej co to są przemiany chemiczne oraz w jaki sposób możemy opisać zachodzące reakcje? wokół nas bezustannie zachodzą rozmaite przemiany przemiany podczas których powstaje nowa substancja,
Zapis reakcji chemicznej co to są przemiany chemiczne oraz w jaki sposób możemy opisać zachodzące reakcje? wokół nas bezustannie zachodzą rozmaite przemiany przemiany podczas których powstaje nowa substancja,
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego. II Etap - 18 stycznia 2016
 XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego II Etap - 18 stycznia 2016 Nazwisko i imię ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego II Etap - 18 stycznia 2016 Nazwisko i imię ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
XXIV Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych. Etap II rozwiązania zadań
 XXIV Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych Etap II rozwiązania zadań Zadanie 1 Na podstawie informacji o pierwiastku X i jego solach (B-E) możemy stwierdzić, że jest to żelazo. Najbardziej
XXIV Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych Etap II rozwiązania zadań Zadanie 1 Na podstawie informacji o pierwiastku X i jego solach (B-E) możemy stwierdzić, że jest to żelazo. Najbardziej
CHEMIA. Wymagania szczegółowe. Wymagania ogólne
 CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
PODSTAWY FUNKCJONOWANIA ŚRODOWISKA - CYKLE BIOGEOCHEMICZNE
 PODSTAWY FUNKCJONOWANIA ŚRODOWISKA - CYKLE BIOGEOCHEMICZNE Podstawą funkcjonowania ekosystemu jest przepływ energii i obiegi materii. Obieg materii dotyczy naturalnego krążenia pierwiastków chemicznych,
PODSTAWY FUNKCJONOWANIA ŚRODOWISKA - CYKLE BIOGEOCHEMICZNE Podstawą funkcjonowania ekosystemu jest przepływ energii i obiegi materii. Obieg materii dotyczy naturalnego krążenia pierwiastków chemicznych,
Reakcje chemiczne. Typ reakcji Schemat Przykłady Reakcja syntezy
 Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Biologia środowiska PRACA ZBIOROWA POD KIERUNKIEM: prof. Anny Grabińskiej-Łoniewskiej prof. Marii Łebkowskiej
 Biologia środowiska PRACA ZBIOROWA POD KIERUNKIEM: prof. Anny Grabińskiej-Łoniewskiej prof. Marii Łebkowskiej Prezentowany podręcznik akademicki w przejrzysty i dokładny sposób opisuje wybrane zagadnienia
Biologia środowiska PRACA ZBIOROWA POD KIERUNKIEM: prof. Anny Grabińskiej-Łoniewskiej prof. Marii Łebkowskiej Prezentowany podręcznik akademicki w przejrzysty i dokładny sposób opisuje wybrane zagadnienia
Biologiczne oczyszczanie ścieków
 Biologiczne oczyszczanie ścieków Ściek woda nie nadająca się do użycia do tego samego celu Rodzaje ścieków komunalne, przemysłowe, rolnicze Zużycie wody na jednego mieszkańca l/dobę cele przemysłowe 4700
Biologiczne oczyszczanie ścieków Ściek woda nie nadająca się do użycia do tego samego celu Rodzaje ścieków komunalne, przemysłowe, rolnicze Zużycie wody na jednego mieszkańca l/dobę cele przemysłowe 4700
Pierwiastki bloku d. Zadanie 1.
 Zadanie 1. Zapisz równania reakcji tlenków chromu (II), (III), (VI) z kwasem solnym i zasadą sodową lub zaznacz, że reakcja nie zachodzi. Określ charakter chemiczny tlenków. Charakter chemiczny tlenków:
Zadanie 1. Zapisz równania reakcji tlenków chromu (II), (III), (VI) z kwasem solnym i zasadą sodową lub zaznacz, że reakcja nie zachodzi. Określ charakter chemiczny tlenków. Charakter chemiczny tlenków:
PROCESY BIOGEOCHEMICZNE NA LĄDACH
 PROCESY BIOGEOCHEMICZNE NA LĄDACH Ekosystemy lądowe Ekosystemy wodne Ekosystemy lądowe Ekosystemy wilgotne Ekosystemy wodne Ekosystemy lądowe Ekosystemy wilgotne Ekosystemy wodne skała macierzysta Wietrzenie
PROCESY BIOGEOCHEMICZNE NA LĄDACH Ekosystemy lądowe Ekosystemy wodne Ekosystemy lądowe Ekosystemy wilgotne Ekosystemy wodne Ekosystemy lądowe Ekosystemy wilgotne Ekosystemy wodne skała macierzysta Wietrzenie
Rozwiązania. dla produktu MN dla M = 3 dla N = 1. Stałą równowagi obliczamy z następującego wzoru:
 Rozwiązania Zadanie 1 Efekt cieplny rozpuszczania 272 g Ca SO 4 wynosi: 136 g Ca SO 4 to masa 1 mola 272 g Ca SO 4 to 2 mole. Odpowiedź: Ciepło rozpuszczania odnosi się do 1 mola substancji, stąd 2x(-20,2
Rozwiązania Zadanie 1 Efekt cieplny rozpuszczania 272 g Ca SO 4 wynosi: 136 g Ca SO 4 to masa 1 mola 272 g Ca SO 4 to 2 mole. Odpowiedź: Ciepło rozpuszczania odnosi się do 1 mola substancji, stąd 2x(-20,2
II Etap rejonowy 28 styczeń 2019 r. Imię i nazwisko ucznia: Czas trwania: 60 minut
 XVI Wojewódzki Konkurs z Chemii dla uczniów klas trzecich gimnazjów oraz klas trzecich oddziałów gimnazjalnych prowadzonych w szkołach innego typu województwa świętokrzyskiego w roku szkolnym 2018/2019
XVI Wojewódzki Konkurs z Chemii dla uczniów klas trzecich gimnazjów oraz klas trzecich oddziałów gimnazjalnych prowadzonych w szkołach innego typu województwa świętokrzyskiego w roku szkolnym 2018/2019
TYPY REAKCJI CHEMICZNYCH
 1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
Tlen. Występowanie i odmiany alotropowe Otrzymywanie tlenu Właściwości fizyczne i chemiczne Związki tlenu tlenki, nadtlenki i ponadtlenki
 Tlen Występowanie i odmiany alotropowe Otrzymywanie tlenu Właściwości fizyczne i chemiczne Związki tlenu tlenki, nadtlenki i ponadtlenki Ogólna charakterystyka tlenowców Tlenowce: obejmują pierwiastki
Tlen Występowanie i odmiany alotropowe Otrzymywanie tlenu Właściwości fizyczne i chemiczne Związki tlenu tlenki, nadtlenki i ponadtlenki Ogólna charakterystyka tlenowców Tlenowce: obejmują pierwiastki
Scenariusz lekcji z biologii w szkole ponadgimnazjalnej
 Scenariusz lekcji z biologii w szkole ponadgimnazjalnej Temat lekcji: Formułowanie odpowiedzi związek logiczny między elementami odpowiedzi. Cele kształcenia: 1. Wymagania ogólne: IV. Poszukiwanie, wykorzystanie
Scenariusz lekcji z biologii w szkole ponadgimnazjalnej Temat lekcji: Formułowanie odpowiedzi związek logiczny między elementami odpowiedzi. Cele kształcenia: 1. Wymagania ogólne: IV. Poszukiwanie, wykorzystanie
Spis treści. Przedmowa 9 ROZDZIAŁ I
 Spis treści Przedmowa 9 ROZDZIAŁ I Wybrane zagadnienia z ekologii 11 1.1. Charakterystyka poziomów organizacji biosfery 14 1.1.1. Gatunek 14 1.1.2. Populacja 14 1.1.2.1. Zagęszczenie populacji 15 1.1.2.2.
Spis treści Przedmowa 9 ROZDZIAŁ I Wybrane zagadnienia z ekologii 11 1.1. Charakterystyka poziomów organizacji biosfery 14 1.1.1. Gatunek 14 1.1.2. Populacja 14 1.1.2.1. Zagęszczenie populacji 15 1.1.2.2.
Przemiana materii i energii - Biologia.net.pl
 Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Ogół przemian biochemicznych, które zachodzą w komórce składają się na jej metabolizm. Wyróżnia się dwa antagonistyczne procesy metabolizmu: anabolizm i katabolizm. Szlak metaboliczny w komórce, to szereg
Copyrights LCE LOGOS Centrum Edukacyjne Fotosynteza
 Fotosynteza Fotosynteza jest procesem anabolicznym, czyli z prostych substancji pobranych z otoczenia pod wpływem energii syntetyzowane są złożone substancje organiczne (głównie cukry). Energią niezbędną
Fotosynteza Fotosynteza jest procesem anabolicznym, czyli z prostych substancji pobranych z otoczenia pod wpływem energii syntetyzowane są złożone substancje organiczne (głównie cukry). Energią niezbędną
Elektrochemia - szereg elektrochemiczny metali. Zadania
 Elektrochemia - szereg elektrochemiczny metali Zadania Czym jest szereg elektrochemiczny metali? Szereg elektrochemiczny metali jest to zestawienie metali według wzrastających potencjałów normalnych. Wartości
Elektrochemia - szereg elektrochemiczny metali Zadania Czym jest szereg elektrochemiczny metali? Szereg elektrochemiczny metali jest to zestawienie metali według wzrastających potencjałów normalnych. Wartości
Temat: Czym zajmuje się ekologia?
 Temat: Czym zajmuje się ekologia? Z czym kojarzy Ci się pojęcie ekologia? Termin ekologia pochodzi z języka greckiego i utworzono go z dwóch wyrazów: oikos oznacza dom, środowisko lub miejsce życia; lógos
Temat: Czym zajmuje się ekologia? Z czym kojarzy Ci się pojęcie ekologia? Termin ekologia pochodzi z języka greckiego i utworzono go z dwóch wyrazów: oikos oznacza dom, środowisko lub miejsce życia; lógos
I BIOLOGIA JAKO NAUKA
 I BIOLOGIA JAKO NAUKA Zadanie. Rozwiąż krzyżówkę, a następnie odczytaj i wyjaśnij hasło. 0. Bada skład chemiczny organizmów i zachodzące w nich reakcje.. Zajmuje się procesami dziedziczenia.. Przedmiotem
I BIOLOGIA JAKO NAUKA Zadanie. Rozwiąż krzyżówkę, a następnie odczytaj i wyjaśnij hasło. 0. Bada skład chemiczny organizmów i zachodzące w nich reakcje.. Zajmuje się procesami dziedziczenia.. Przedmiotem
EKOLOGIA OGÓLNA WBNZ 884
 EKOLOGIA OGÓLNA WBNZ 884 Wykład 8 Ekosystemy: ogólne prawidłowości; stabilność i pojęcia pokrewne Życie biosfery = cykl redoks węgla EKOSYSTEM DEPOZYCJA (ocean, osady) energia CO 2 energia REDUKCJA tylko
EKOLOGIA OGÓLNA WBNZ 884 Wykład 8 Ekosystemy: ogólne prawidłowości; stabilność i pojęcia pokrewne Życie biosfery = cykl redoks węgla EKOSYSTEM DEPOZYCJA (ocean, osady) energia CO 2 energia REDUKCJA tylko
I. Pobieranie próbek. Lp. Wykaz czynności Wielkość współczynnika
 Koszty i wykaz badań wykonywanych w Wojewódzkim Inspektoracie Ochrony Środowiska w Poznaniu 1. Stawka podstawowa wynosi 40,41 zł. 2. Wyliczenie kosztów usługi następuje w sposób następujący: koszt usługi
Koszty i wykaz badań wykonywanych w Wojewódzkim Inspektoracie Ochrony Środowiska w Poznaniu 1. Stawka podstawowa wynosi 40,41 zł. 2. Wyliczenie kosztów usługi następuje w sposób następujący: koszt usługi
Budowa atomu. Wiązania chemiczne
 strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
KONKURS CHEMICZNY KLAS TRZECICH GIMNAZJALNYCH ROK SZKOLNY 2011/2012
 IMIĘ I NAZWISKO PUNKTACJA SZKOŁA KLASA NAZWISKO NAUCZYCIELA CHEMII I LICEUM OGÓLNOKSZTAŁCĄCE Inowrocław 19 maja 2012 im. Jana Kasprowicza INOWROCŁAW KONKURS CHEMICZNY KLAS TRZECICH GIMNAZJALNYCH ROK SZKOLNY
IMIĘ I NAZWISKO PUNKTACJA SZKOŁA KLASA NAZWISKO NAUCZYCIELA CHEMII I LICEUM OGÓLNOKSZTAŁCĄCE Inowrocław 19 maja 2012 im. Jana Kasprowicza INOWROCŁAW KONKURS CHEMICZNY KLAS TRZECICH GIMNAZJALNYCH ROK SZKOLNY
WIETRZENIE. Rozpuszczanie polega na łączeniu się minerałów z wodą i doprowadzeniu ich do roztworu. Tego typu wietrzeniu ulegają głównie sole.
 WIETRZENIE Wietrzenie to proces prowadzący do rozpadu lub rozkładu skały RODZAJE WIETRZENIA WIETRZENIE FIZYCZNE = MECHANICZNE v INSOLACJA v ZAMRÓZ (MROZOWE) v SKAŁ ILASTYCH v SOLNE WIETRZENIE CHEMICZNE
WIETRZENIE Wietrzenie to proces prowadzący do rozpadu lub rozkładu skały RODZAJE WIETRZENIA WIETRZENIE FIZYCZNE = MECHANICZNE v INSOLACJA v ZAMRÓZ (MROZOWE) v SKAŁ ILASTYCH v SOLNE WIETRZENIE CHEMICZNE
ph roztworu (prawie) się nie zmieniło. Zawiesina soi ma ph obojętne (lekko kwaśne). Zapach nie zmienił się.
 Ureaza - dodatek krajowy 1. Odniesienie do podstawy programowej (starej) Kształcenie w zakresie podstawowym Odżywianie się człowieka - budowa i funkcja układu pokarmowego, główne składniki pokarmowe i
Ureaza - dodatek krajowy 1. Odniesienie do podstawy programowej (starej) Kształcenie w zakresie podstawowym Odżywianie się człowieka - budowa i funkcja układu pokarmowego, główne składniki pokarmowe i
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe
 kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe Zadanie
kod ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO Uzyskane punkty.. WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2016/2017 eliminacje rejonowe Zadanie
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Eco-Tabs. Nowa technologia w bioremediacji silnie zeutrofizowanych zbiorników wodnych
 TM Eco-Tabs Nowa technologia w bioremediacji silnie zeutrofizowanych zbiorników wodnych Prof. dr hab. Ryszard J. Chróst Zakład Ekologii Mikroorganizmów UW Przyczyny i skutki eutrofizacji wód podlegające
TM Eco-Tabs Nowa technologia w bioremediacji silnie zeutrofizowanych zbiorników wodnych Prof. dr hab. Ryszard J. Chróst Zakład Ekologii Mikroorganizmów UW Przyczyny i skutki eutrofizacji wód podlegające
Skały budujące Ziemię
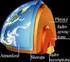 Skały budujące Ziemię Minerały Minerał pierwiastek lub związek chemiczny powstały w przyrodzie w sposób naturalny, jednorodny pod względem chemicznym i fizycznym. Minerały w większości mają budowę krystaliczną.
Skały budujące Ziemię Minerały Minerał pierwiastek lub związek chemiczny powstały w przyrodzie w sposób naturalny, jednorodny pod względem chemicznym i fizycznym. Minerały w większości mają budowę krystaliczną.
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
23 zadania z chemii. Zadanie 1 (0-1) Podstawowymi składnikami substancji zapachowych wielu roślin są estry. Można je przedstawić wzorem ogólnym:
 23 zadania z chemii Zadanie 1 (0-1) Podstawowymi składnikami substancji zapachowych wielu roślin są estry. Można je przedstawić wzorem ogólnym: Estrem jest związek o wzorze: Zadanie 2 (0-1) Elementy kolejki
23 zadania z chemii Zadanie 1 (0-1) Podstawowymi składnikami substancji zapachowych wielu roślin są estry. Można je przedstawić wzorem ogólnym: Estrem jest związek o wzorze: Zadanie 2 (0-1) Elementy kolejki
WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH
 WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH PODZIAŁ ZWIĄZKÓW NIEORGANICZNYCH Tlenki (kwasowe, zasadowe, amfoteryczne, obojętne) Związki niemetali Kwasy (tlenowe, beztlenowe) Wodorotlenki
WŁAŚCIWOŚCI NIEKTÓRYCH PIERWIASTKÓW I ICH ZWIĄZKÓW NIEORGANICZNYCH PODZIAŁ ZWIĄZKÓW NIEORGANICZNYCH Tlenki (kwasowe, zasadowe, amfoteryczne, obojętne) Związki niemetali Kwasy (tlenowe, beztlenowe) Wodorotlenki
Fragmenty Działu 7 z Tomu 1 REAKCJE UTLENIANIA I REDUKCJI
 Fragmenty Działu 7 z Tomu 1 REAKCJE UTLENIANIA I REDUKCJI Zadanie 726 (1 pkt.) V/2006/A1 Konfigurację elektronową atomu glinu w stanie podstawowym można przedstawić następująco: 1s 2 2s 2 2p 6 3s 2 3p
Fragmenty Działu 7 z Tomu 1 REAKCJE UTLENIANIA I REDUKCJI Zadanie 726 (1 pkt.) V/2006/A1 Konfigurację elektronową atomu glinu w stanie podstawowym można przedstawić następująco: 1s 2 2s 2 2p 6 3s 2 3p
Reakcje zachodzące w komórkach
 Reakcje zachodzące w komórkach W każdej sekundzie we wszystkich organizmach żywych zachodzi niezliczona ilość reakcji metabolicznych. Metabolizm (gr. metabole - przemiana) to przemiany materii i energii
Reakcje zachodzące w komórkach W każdej sekundzie we wszystkich organizmach żywych zachodzi niezliczona ilość reakcji metabolicznych. Metabolizm (gr. metabole - przemiana) to przemiany materii i energii
1. Podstawowe prawa i pojęcia chemiczne
 1. PODSTAWOWE PRAWA I POJĘCIA CHEMICZNE 5 1. Podstawowe prawa i pojęcia chemiczne 1.1. Wyraź w gramach masę: a. jednego atomu żelaza, b. jednej cząsteczki kwasu siarkowego. Odp. 9,3 10 23 g; 1,6 10 22
1. PODSTAWOWE PRAWA I POJĘCIA CHEMICZNE 5 1. Podstawowe prawa i pojęcia chemiczne 1.1. Wyraź w gramach masę: a. jednego atomu żelaza, b. jednej cząsteczki kwasu siarkowego. Odp. 9,3 10 23 g; 1,6 10 22
2. Podczas spalania 2 objętości pewnego gazu z 4 objętościami H 2 otrzymano 1 objętość N 2 i 4 objętości H 2O. Jaki gaz uległ spalaniu?
 1. Oblicz, ilu moli HCl należy użyć, aby poniższe związki przeprowadzić w sole: a) 0,2 mola KOH b) 3 mole NH 3 H 2O c) 0,2 mola Ca(OH) 2 d) 0,5 mola Al(OH) 3 2. Podczas spalania 2 objętości pewnego gazu
1. Oblicz, ilu moli HCl należy użyć, aby poniższe związki przeprowadzić w sole: a) 0,2 mola KOH b) 3 mole NH 3 H 2O c) 0,2 mola Ca(OH) 2 d) 0,5 mola Al(OH) 3 2. Podczas spalania 2 objętości pewnego gazu
TWORZYWA BIODEGRADOWALNE
 TWORZYWA BIODEGRADOWALNE Opracowały: Joanna Grzegorzek kl. III a TE Katarzyna Kołdras kl. III a TE Tradycyjne tworzywa sztuczne to materiały składające się z polimerów syntetycznych. Większość z nich nie
TWORZYWA BIODEGRADOWALNE Opracowały: Joanna Grzegorzek kl. III a TE Katarzyna Kołdras kl. III a TE Tradycyjne tworzywa sztuczne to materiały składające się z polimerów syntetycznych. Większość z nich nie
Identyfikacja wybranych kationów i anionów
 Identyfikacja wybranych kationów i anionów ZACHOWAĆ SZCZEGÓLNĄ OSTRORZNOŚĆ NIE ZATYKAĆ PROBÓWKI PALCEM Zadanie 1 Celem zadania jest wykrycie jonów Ca 2+ a. Próba z jonami C 2 O 4 ZACHOWAĆ SZCZEGÓLNĄ OSTRORZNOŚĆ
Identyfikacja wybranych kationów i anionów ZACHOWAĆ SZCZEGÓLNĄ OSTRORZNOŚĆ NIE ZATYKAĆ PROBÓWKI PALCEM Zadanie 1 Celem zadania jest wykrycie jonów Ca 2+ a. Próba z jonami C 2 O 4 ZACHOWAĆ SZCZEGÓLNĄ OSTRORZNOŚĆ
WOJEWÓDZKI KONKURS CHEMICZNY
 Pieczątka szkoły Kod ucznia Liczba punktów WOJEWÓDZKI KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM W ROKU SZKOLNYM 2014/2015 12 LISTOPADA 2014R. 1. Test konkursowy zawiera 26 zadań. Są to zadania zamknięte
Pieczątka szkoły Kod ucznia Liczba punktów WOJEWÓDZKI KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM W ROKU SZKOLNYM 2014/2015 12 LISTOPADA 2014R. 1. Test konkursowy zawiera 26 zadań. Są to zadania zamknięte
Temat 2: Nazewnictwo związków chemicznych. Otrzymywanie i właściwości tlenków
 Zasada ogólna: We wzorze sumarycznym pierwiastki zapisujemy od metalu do niemetalu, natomiast odczytujemy nazwę zaczynając od niemetalu: MgO, CaS, NaF Nazwy związków chemicznych najczęściej tworzymy, korzystając
Zasada ogólna: We wzorze sumarycznym pierwiastki zapisujemy od metalu do niemetalu, natomiast odczytujemy nazwę zaczynając od niemetalu: MgO, CaS, NaF Nazwy związków chemicznych najczęściej tworzymy, korzystając
Instrukcja dla uczestnika. II etap Konkursu. U z u p e ł n i j s w o j e d a n e p r z e d r o z p o c z ę c i e m r o z w i ą z y w a n i a z a d a ń
 III edycja rok szkolny 2017/2018 Uzupełnia Organizator Konkursu Instrukcja dla uczestnika II etap Konkursu Liczba uzyskanych punktów 1. Sprawdź, czy arkusz konkursowy, który otrzymałeś zawiera 12 stron.
III edycja rok szkolny 2017/2018 Uzupełnia Organizator Konkursu Instrukcja dla uczestnika II etap Konkursu Liczba uzyskanych punktów 1. Sprawdź, czy arkusz konkursowy, który otrzymałeś zawiera 12 stron.
Ewa Imbierowicz. Prezentacja i omówienie wyników pomiarów monitoringowych, uzyskanych w trybie off-line
 Projekt MONSUL Analiza czynników wpływających na stan ekologiczny wód Zbiornika Sulejowskiego w oparciu o ciągły monitoring i zintegrowany model 3D zbiornika Ewa Imbierowicz Prezentacja i omówienie wyników
Projekt MONSUL Analiza czynników wpływających na stan ekologiczny wód Zbiornika Sulejowskiego w oparciu o ciągły monitoring i zintegrowany model 3D zbiornika Ewa Imbierowicz Prezentacja i omówienie wyników
X / \ Y Y Y Z / \ W W ... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
2.4. ZADANIA STECHIOMETRIA. 1. Ile moli stanowi:
 2.4. ZADANIA 1. Ile moli stanowi: STECHIOMETRIA a/ 52 g CaCO 3 b/ 2,5 tony Fe(OH) 3 2. Ile g stanowi: a/ 4,5 mmol ZnSO 4 b/ 10 kmol wody 3. Obl. % skład Fe 2 (SO 4 ) 3 6H 2 O 4. Obl. % zawartość tlenu
2.4. ZADANIA 1. Ile moli stanowi: STECHIOMETRIA a/ 52 g CaCO 3 b/ 2,5 tony Fe(OH) 3 2. Ile g stanowi: a/ 4,5 mmol ZnSO 4 b/ 10 kmol wody 3. Obl. % skład Fe 2 (SO 4 ) 3 6H 2 O 4. Obl. % zawartość tlenu
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW
 WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
Substancje o Znaczeniu Biologicznym
 Substancje o Znaczeniu Biologicznym Tłuszcze Jadalne są to tłuszcze, które może spożywać człowiek. Stanowią ważny, wysokoenergetyczny składnik diety. Z chemicznego punktu widzenia głównym składnikiem tłuszczów
Substancje o Znaczeniu Biologicznym Tłuszcze Jadalne są to tłuszcze, które może spożywać człowiek. Stanowią ważny, wysokoenergetyczny składnik diety. Z chemicznego punktu widzenia głównym składnikiem tłuszczów
EKOLOGIA. Początek Wszechświata. Historia Ziemi. Historia świata w pigułce
 EKOLOGIA Historia świata w pigułce 1 Początek Wszechświata ok. 15 mld lat temu: temperatura: + + gęstość: : + + WIELKI WYBUCH 10-12 s: temp. +10 15 K; powstanie cząstek elementarnych i antycząstek 10-5
EKOLOGIA Historia świata w pigułce 1 Początek Wszechświata ok. 15 mld lat temu: temperatura: + + gęstość: : + + WIELKI WYBUCH 10-12 s: temp. +10 15 K; powstanie cząstek elementarnych i antycząstek 10-5
Bliskie spotkania z biologią. METABOLIZM część II. dr hab. Joanna Moraczewska, prof. UKW
 Bliskie spotkania z biologią METABOLIZM część II dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki METABOLIZM KATABOLIZM - rozkład związków chemicznych
Bliskie spotkania z biologią METABOLIZM część II dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki METABOLIZM KATABOLIZM - rozkład związków chemicznych
Biologiczne oczyszczanie wody i ścieków
 Gospodarka energetyczna, wodna i ściekowa Biologiczne oczyszczanie wody i ścieków Biologiczne oczyszczanie ścieków zachodzi w: komorach napowietrzania z osadem czynnym, na złożach biologicznych, glebie
Gospodarka energetyczna, wodna i ściekowa Biologiczne oczyszczanie wody i ścieków Biologiczne oczyszczanie ścieków zachodzi w: komorach napowietrzania z osadem czynnym, na złożach biologicznych, glebie
KONKURS CHEMICZNY,,ROK PRZED MATURĄ
 KONKURS CHEMICZNY,,ROK PRZED MATURĄ ROK SZKOLNY 2007/2008 ETAP SZKOLNY Numer kodowy Suma punktów: Podpisy Komisji: 1.... 2.... 3.... Informacje dla ucznia: 1. Arkusz zawiera 12 zadań. 2. Pisemnych odpowiedzi
KONKURS CHEMICZNY,,ROK PRZED MATURĄ ROK SZKOLNY 2007/2008 ETAP SZKOLNY Numer kodowy Suma punktów: Podpisy Komisji: 1.... 2.... 3.... Informacje dla ucznia: 1. Arkusz zawiera 12 zadań. 2. Pisemnych odpowiedzi
Instrukcja do ćwiczenia WŁAŚCIWOŚCI WYBRANYCH ANIONÓW.
 Instrukcja do ćwiczenia WŁAŚCIWOŚCI WYBRANYCH ANIONÓW. CHEMIA ANIONÓW W ROZTWORACH WODNYCH Celem ćwiczenia jest zapoznanie się z właściwościami chemicznymi wybranych anionów pierwiastków I oraz II okresu
Instrukcja do ćwiczenia WŁAŚCIWOŚCI WYBRANYCH ANIONÓW. CHEMIA ANIONÓW W ROZTWORACH WODNYCH Celem ćwiczenia jest zapoznanie się z właściwościami chemicznymi wybranych anionów pierwiastków I oraz II okresu
 http://muzeum.if.pw.edu.pl/ W jaki sposób Maria Skłodowska-Curie wydzieliła polon i rad z blendy uranowej? Warsztaty metodyczne dla nauczycieli chemii szkół gimnazjalnych i ponadgimnazjalnych 29 stycznia
http://muzeum.if.pw.edu.pl/ W jaki sposób Maria Skłodowska-Curie wydzieliła polon i rad z blendy uranowej? Warsztaty metodyczne dla nauczycieli chemii szkół gimnazjalnych i ponadgimnazjalnych 29 stycznia
Od Wielkiego Wybuchu do Gór Izerskich. Tomasz Mrozek Instytut Astronomiczny UWr Zakład Fizyki Słońca CBK PAN
 Od Wielkiego Wybuchu do Gór Izerskich Tomasz Mrozek Instytut Astronomiczny UWr Zakład Fizyki Słońca CBK PAN Góry Izerskie Góry Izerskie Góry Izerskie Góry Izerskie Góry Izerskie Góry Izerskie Góry Izerskie
Od Wielkiego Wybuchu do Gór Izerskich Tomasz Mrozek Instytut Astronomiczny UWr Zakład Fizyki Słońca CBK PAN Góry Izerskie Góry Izerskie Góry Izerskie Góry Izerskie Góry Izerskie Góry Izerskie Góry Izerskie
Zadania na listopad. Zadanie 1 Meksyk położony jest od Buenos Aires na A. północny wschód B. południowy wschód C. północny zachód D.
 Zadania na listopad Zadania z geografii Meksyk położony jest od Buenos Aires na A. północny wschód B. południowy wschód C. północny zachód D. południowy zachód Zadanie 2 Jeżeli w Lagos jest godzina 12.00
Zadania na listopad Zadania z geografii Meksyk położony jest od Buenos Aires na A. północny wschód B. południowy wschód C. północny zachód D. południowy zachód Zadanie 2 Jeżeli w Lagos jest godzina 12.00
Powodzenia!!! WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII III ETAP. Termin: r. Czas pracy: 90 minut. Liczba otrzymanych punktów
 KOD Ucznia WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII III ETAP Termin: 21.03.2006r. Czas pracy: 90 minut Numer zadania Liczba możliwych punktów 1 6 2 3 3 6 4 7 5 7 6 6 7 6 8 3 9 6 10 8 Razem 58 Liczba otrzymanych
KOD Ucznia WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII III ETAP Termin: 21.03.2006r. Czas pracy: 90 minut Numer zadania Liczba możliwych punktów 1 6 2 3 3 6 4 7 5 7 6 6 7 6 8 3 9 6 10 8 Razem 58 Liczba otrzymanych
ILOŚCIOWE OZNACZANIE SIARCZANÓW W WODZIE WODOCIĄGOWEJ METODĄ MIARECZKOWANIA KONDUKTOMETRYCZNEGO
 ILOŚCIOWE OZNACZANIE SIARCZANÓW W WODZIE WODOCIĄGOWEJ METODĄ MIARECZKOWANIA KONDUKTOMETRYCZNEGO Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu Łódzkiego. 1. Wprowadzenie 1.1.
ILOŚCIOWE OZNACZANIE SIARCZANÓW W WODZIE WODOCIĄGOWEJ METODĄ MIARECZKOWANIA KONDUKTOMETRYCZNEGO Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu Łódzkiego. 1. Wprowadzenie 1.1.
Wanda Wołyńska Instytut Biotechnologii Przemysłu Rolno-Spożywczego Oddział Cukrownictwa. IBPRS Oddział Cukrownictwa Łódź, czerwiec 2013r.
 Wanda Wołyńska Instytut Biotechnologii Przemysłu Rolno-Spożywczego Oddział Cukrownictwa Łódź, 25-26 czerwiec 2013r. 1 Badania fizyko-chemiczne wód i ścieków wykonywane są w różnych celach i w zależności
Wanda Wołyńska Instytut Biotechnologii Przemysłu Rolno-Spożywczego Oddział Cukrownictwa Łódź, 25-26 czerwiec 2013r. 1 Badania fizyko-chemiczne wód i ścieków wykonywane są w różnych celach i w zależności
Analiza czynności życiowych bakterii i określanie roli tych procesów w środowisku przyrodniczym
 Analiza czynności życiowych bakterii i określanie roli tych procesów w środowisku przyrodniczym Salmonella Clostridium Escherischia coli Pseudomonas Bakterie (łac. bacteria, od gr. bakterion pałeczka)
Analiza czynności życiowych bakterii i określanie roli tych procesów w środowisku przyrodniczym Salmonella Clostridium Escherischia coli Pseudomonas Bakterie (łac. bacteria, od gr. bakterion pałeczka)
Oznaczanie żelaza i miedzi metodą miareczkowania spektrofotometrycznego
 Oznaczanie żelaza i miedzi metodą miareczkowania spektrofotometrycznego Oznaczanie dwóch kationów obok siebie metodą miareczkowania spektrofotometrycznego (bez maskowania) jest możliwe, gdy spełnione są
Oznaczanie żelaza i miedzi metodą miareczkowania spektrofotometrycznego Oznaczanie dwóch kationów obok siebie metodą miareczkowania spektrofotometrycznego (bez maskowania) jest możliwe, gdy spełnione są
Plan: 1) krutki opis w ramach wstępu 2) Występowanie 3) Otrzymywanie 4) Właściwości 5) Związki 6) Izotopy 7) Zastosowanie 8) Znaczenie biologiczne
 Mied ź Plan: 1) krutki opis w ramach wstępu 2) Występowanie 3) Otrzymywanie 4) Właściwości 5) Związki 6) Izotopy 7) Zastosowanie 8) Znaczenie biologiczne 1) krutki opis w ramach wstępu Miedź (Cu, łac.
Mied ź Plan: 1) krutki opis w ramach wstępu 2) Występowanie 3) Otrzymywanie 4) Właściwości 5) Związki 6) Izotopy 7) Zastosowanie 8) Znaczenie biologiczne 1) krutki opis w ramach wstępu Miedź (Cu, łac.
Wykłady z Geochemii Ogólnej
 Wykłady z Geochemii Ogólnej III rok WGGiOŚ AGH 2010/11 dr hab. inż. Maciej Manecki A-0 p.24 www.geol.agh.edu.pl/~mmanecki ELEMENTY KOSMOCHEMII Nasza wiedza o składzie materii Wszechświata pochodzi z dwóch
Wykłady z Geochemii Ogólnej III rok WGGiOŚ AGH 2010/11 dr hab. inż. Maciej Manecki A-0 p.24 www.geol.agh.edu.pl/~mmanecki ELEMENTY KOSMOCHEMII Nasza wiedza o składzie materii Wszechświata pochodzi z dwóch
22 marca - Światowy Dzień Wody
 22 marca - Światowy Dzień Wody Bez wody nie ma życia... Woda jako czysty związek wodoru i tlenu (H 2 O) w przyrodzie nie występuje. Jest bardzo rozcieńczonym roztworem soli, kwasów, zasad i gazów. Skład
22 marca - Światowy Dzień Wody Bez wody nie ma życia... Woda jako czysty związek wodoru i tlenu (H 2 O) w przyrodzie nie występuje. Jest bardzo rozcieńczonym roztworem soli, kwasów, zasad i gazów. Skład
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali
 Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
Spis treści. Wstęp... 9
 Spis treści Wstęp... 9 1. Szkło i sprzęt laboratoryjny 1.1. Szkła laboratoryjne własności, skład chemiczny, podział, zastosowanie.. 11 1.2. Wybrane szkło laboratoryjne... 13 1.3. Szkło miarowe... 14 1.4.
Spis treści Wstęp... 9 1. Szkło i sprzęt laboratoryjny 1.1. Szkła laboratoryjne własności, skład chemiczny, podział, zastosowanie.. 11 1.2. Wybrane szkło laboratoryjne... 13 1.3. Szkło miarowe... 14 1.4.
Zastosowanie spektrofotometrii (UV-VIS) do oznaczania Fe(III) i Fe(II) w wodzie
 UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII ANALIZA ŚLADOWYCH ZANIECZYSZCZEŃ ŚRODOWISKA I ROK OŚ II Ćwiczenie 4 Zastosowanie spektrofotometrii (UV-VIS) do oznaczania Fe(III) i Fe(II) w wodzie 1. Wprowadzenie Żelazo
UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII ANALIZA ŚLADOWYCH ZANIECZYSZCZEŃ ŚRODOWISKA I ROK OŚ II Ćwiczenie 4 Zastosowanie spektrofotometrii (UV-VIS) do oznaczania Fe(III) i Fe(II) w wodzie 1. Wprowadzenie Żelazo
************************************************************
 As 2 S 3 + HNO 3 + H 2 O = H 3 AsO 4 + H 2 SO 4 + NO Zn + HNO 3 = Zn(NO 3 ) 2 + NH 4 NO 3 + H 2 O HClO 3 = ClO 2 + HClO 4 + H 2 O KNO 2 + KMnO 4 +? = KNO 3 + MnSO 4 +? Bi 2 S 3 + NO 3 = Bi 3+ + NO + S
As 2 S 3 + HNO 3 + H 2 O = H 3 AsO 4 + H 2 SO 4 + NO Zn + HNO 3 = Zn(NO 3 ) 2 + NH 4 NO 3 + H 2 O HClO 3 = ClO 2 + HClO 4 + H 2 O KNO 2 + KMnO 4 +? = KNO 3 + MnSO 4 +? Bi 2 S 3 + NO 3 = Bi 3+ + NO + S
Moduł: Chemia. Fundamenty. Liczba godzin. Nr rozdziału Tytuł. Temat lekcji. Rozdział 1. Przewodnik po chemii (12 godzin)
 Rozkład materiału z chemii w klasie II LO zakres rozszerzony Chemia. Fundamenty. Krzysztof Pazdro, wyd. Oficyna Edukacyjna Krzysztof Pazdro Sp. z o.o.. nr dopuszczenia 565//0 Chemia. i związki nieorganiczne.
Rozkład materiału z chemii w klasie II LO zakres rozszerzony Chemia. Fundamenty. Krzysztof Pazdro, wyd. Oficyna Edukacyjna Krzysztof Pazdro Sp. z o.o.. nr dopuszczenia 565//0 Chemia. i związki nieorganiczne.
powierzchniowa warstwa skorupy ziemskiej będąca produktem wietrzenia skał, czyli długotrwałego działania na nie wody, powietrza i temperatury, oraz
 powierzchniowa warstwa skorupy ziemskiej będąca produktem wietrzenia skał, czyli długotrwałego działania na nie wody, powietrza i temperatury, oraz działania mikroorganizmów Złożony i długotrwały proces
powierzchniowa warstwa skorupy ziemskiej będąca produktem wietrzenia skał, czyli długotrwałego działania na nie wody, powietrza i temperatury, oraz działania mikroorganizmów Złożony i długotrwały proces
Instrukcja dla uczestnika
 III edycja Konkursu Chemicznego Chemik dla uczniów szkół podstawowych i gimnazjalnych rok szkolny 2017/2018 Instrukcja dla uczestnika I etap Konkursu (etap szkolny) 1. Sprawdź, czy arkusz konkursowy, który
III edycja Konkursu Chemicznego Chemik dla uczniów szkół podstawowych i gimnazjalnych rok szkolny 2017/2018 Instrukcja dla uczestnika I etap Konkursu (etap szkolny) 1. Sprawdź, czy arkusz konkursowy, który
Właściwości wód podziemnych
 Właściwości wód podziemnych Właściwości fizyczne i organoleptyczne wód podziemnych: Temperatura Przeźroczystość. Mętność, Barwa, Radoczynność, Smak, Zapach. Skład chemiczny wód podziemnych zależy od rodzaju
Właściwości wód podziemnych Właściwości fizyczne i organoleptyczne wód podziemnych: Temperatura Przeźroczystość. Mętność, Barwa, Radoczynność, Smak, Zapach. Skład chemiczny wód podziemnych zależy od rodzaju
W probówkach oznaczonych numerami 1-8 znajdują się wodne roztwory (o stężeniu 0,1
 XLVIII OLIMPIADA CHEMICZA Etap II KOMITET GŁÓWY OLIMPIADY CHEMICZEJ Zadanie laboratoryjne W probówkach oznaczonych numerami 1-8 znajdują się wodne roztwory (o stężeniu 0,1 mol/dm 3 ) pojedynczych substancji
XLVIII OLIMPIADA CHEMICZA Etap II KOMITET GŁÓWY OLIMPIADY CHEMICZEJ Zadanie laboratoryjne W probówkach oznaczonych numerami 1-8 znajdują się wodne roztwory (o stężeniu 0,1 mol/dm 3 ) pojedynczych substancji
8. MANGANOMETRIA. 8. Manganometria
 8. MANGANOMETRIA 5 8. Manganometria 8.1. Oblicz ile gramów KMnO 4 zawiera 5 dm 3 roztworu o stężeniu 0,0285 mol dm 3. Odp. 22,5207 g 8.2. W jakiej objętości 0,0205 molowego roztworu KMnO 4 znajduje się
8. MANGANOMETRIA 5 8. Manganometria 8.1. Oblicz ile gramów KMnO 4 zawiera 5 dm 3 roztworu o stężeniu 0,0285 mol dm 3. Odp. 22,5207 g 8.2. W jakiej objętości 0,0205 molowego roztworu KMnO 4 znajduje się
METODY PRZYGOTOWANIA PRÓBEK DO POMIARU STOSUNKÓW IZOTOPOWYCH PIERWIASTKÓW LEKKICH. Spektrometry IRMS akceptują tylko próbki w postaci gazowej!
 METODY PRZYGOTOWANIA PRÓBEK DO POMIARU STOSUNKÓW IZOTOPOWYCH PIERWIASTKÓW LEKKICH Spektrometry IRMS akceptują tylko próbki w postaci gazowej! Stąd konieczność opracowania metod przeprowadzania próbek innych
METODY PRZYGOTOWANIA PRÓBEK DO POMIARU STOSUNKÓW IZOTOPOWYCH PIERWIASTKÓW LEKKICH Spektrometry IRMS akceptują tylko próbki w postaci gazowej! Stąd konieczność opracowania metod przeprowadzania próbek innych
Bliskie spotkania z biologią METABOLIZM. dr hab. Joanna Moraczewska, prof. UKW. Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki
 Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
Bliskie spotkania z biologią METABOLIZM dr hab. Joanna Moraczewska, prof. UKW Instytut Biologii Eksperymetalnej, Zakład Biochemii i Biologii Komórki Metabolizm całokształt przemian biochemicznych i towarzyszących
