Journal Club. Inhibition of mutated, activated BRAF in metastatic melanoma Flaherty KT, Puzanov I, Kim KB i wsp. N Engl J Med 2010; 363:
|
|
|
- Maciej Chmielewski
- 4 lat temu
- Przeglądów:
Transkrypt
1 NOWOTWORY Journal of Oncology 2011 volume 61 Number Journal Club Eribulin monotherapy versus treatment of physician s choice in patients with metastatic breast cancer (EMBRACE): a phase 3 open-label randomised study Cortes J, O Shaughnessy J, Loesch D i wsp. EMBRACE (Eisai Metastatic Breast Cancer Study Assessing Physician s Choice Versus E7389) investigators Lancet 2011; 377: Nowe metody wydłużające czas przeżycia chorych na rozsianego raka piersi po wielu liniach leczenia są bardzo potrzebne. Erybulina jest nie-taksoidowym inhibitorem mikrotubul o nowym sposobie działania. Celem badania było porównanie czasu całkowitego przeżycia chorych leczonych erybuliną z innymi sposobami leczenia. Metody. W otwartym badaniu klinicznym III fazy chore na rozsianego raka piersi przydzielano losowo (2:1) do leczenia erybuliną (1,4 mg/m 2 ), podawaną dożylnie w 2-5 min w dniach 1. i dniowego cyklu lub do innego leczenia wybranego przez lekarza (treatment of physician s choice TPC). Chore włączane do badania otrzymały wcześniej od 2 do 5 linii chemioterapii (2 lub więcej z powodu zaawansowanej choroby), w tym antracykliny i taksoidy, chyba że istniały przeciwwskazania do ich zastosowania. Chore stratyfikowano wg regionu geograficznego, wcześniejszego leczenia kapecytabiną oraz stanu receptora HER2. Badanie nie było zaślepione. Pierwotnym wskaźnikiem końcowej oceny był czas całkowitego przeżycia w analizie zgodnej z intencją leczenia. Badanie zarejestrowano w ClinicalTrials.gov pod numerem NCT Wyniki. 762 chore przydzielono losowo do leczenia (508 erybuliną, 254 TPC). Czas całkowitego przeżycia był znamiennie dłuższy wśród leczonych erybuliną (mediana 13,1 miesięcy 95% CI 11,8-14,3), w porównaniu do TPC (10,6 miesięcy 9,3-12,5; współczynnik ryzyka 0,81, 95% CI 0,66-0,99; p=0,041). Najczęściej występującym działaniem niepożądanym w obu grupach były astenia i zmęczenie (270 [54%] spośród 503 chorych leczonych erybuliną oraz 98 [40%] spośród 247 chorych w grupie TPC) oraz neutropenia (260 [52%] wśród leczonych erybuliną oraz 73 [30%] leczonych TPC). Obwodowa neuropatia była najczęstszym objawem prowadzącym do przerwania leczenia erybuliną; wystąpiła u 24 (5%) spośród 503 chorych. Wnioski. Erybulina znamienne wydłużyła czas całkowitego przeżycia, w porównaniu do TPC u chorych na rozsianego raka piersi po wielu liniach leczenia. Wyniki niniejszego badania pokazują, że nowe leki mogą wydłużyć czas całkowitego przeżycia chorych nieodpowiadających na standardowe leczenia. Inhibition of mutated, activated BRAF in metastatic melanoma Flaherty KT, Puzanov I, Kim KB i wsp. N Engl J Med 2010; 363: Występowanie somatycznych mutacji w genie kodującym serynowo-treoninową kinazę białkową BRAF w większości przypadków czerniaka oferuje potencjalną możliwość celowanego leczenia, skierowanego przeciwko onkogenom. Metody. W wieloośrodkowym badaniu I fazy oceniano efekt eskalacji dawki PLX4032 (znanego także jako RG7204), doustnego inhibitora zmutowanego BRAF, a następnie kontynuowano rozszerzoną fazę badania, z zastosowaniem maksymalnej tolerowanej dawki (rekomendowanej do badania II fazy). Chorzy otrzymywali PLX4032 dwa razy dziennie do progresji choroby. U wszystkich chorych przeprowadzono analizę farmakokinetyczną oraz ocenę odpowiedzi na leczenie. U wybranych chorych wykonano biopsję zmiany przed oraz w trakcie leczenia celem potwierdzenia zahamowania BRAF. Wyniki. 55 chorych (49 z rozpoznaniem czerniaka) włączono do fazy eskalacji dawki, a dodatkowych 32 chorych na rozsianego czerniaka z mutacją BRAF i V600E do rozszerzonej fazy badania. Rekomendowana dawka do badania II fazy wyniosła 960 mg dwa razy dziennie. Eskalacja dawki była ograniczona wysypką, zmęczeniem oraz bólami stawów w stopniu 2. lub 3. W kohorcie chorych leczonych w fazie eskalacji dawki, u 10 spośród 16 chorych na czerniaka z mutacją V600E BRAF, którzy otrzymywali dawkę PLX mg dwa razy dziennie, zaobserwowano częściową remisję, a u 1 chorego całkowitą. W kohorcie rozszerzonej fazy badania u 24 spośród 32 chorych stwierdzono częściową remisję, a u 2 całkowitą. Oszacowany średni czas do progresji wszystkich chorych wyniósł powyżej 7 miesięcy. Wnioski. Zastosowanie PLX4032 u chorych na rozsianego czerniaka, z potwierdzoną mutacją V600E BRAF, skutkowało całkowitą lub częściową remisją u większości chorych.
2 309 Prednisone plus cabazitaxel or mitoxantrone for metastatic castration-resistant prostate cancer progressing after docetaxel treatment: a randomised open-label trial de Bono JS, Oudard S, Ozguroglu M i wsp. Lancet ; 376: Kabazytaksel jest nowoczesnym, wiążącym tubulinę taksoidem, wykazującym przeciwnowotworową aktywność w przypadkach oporności na docetaksel. Oceniono skuteczność oraz bezpieczeństwo zastosowania kabazytakselu w połączeniu z prednizonem, w porównaniu do mitoksantronu z prednizonem, w grupie chorych na rozsianego, opornego na leczenie antyandrogenowe raka stercza z progresją po leczeniu z udziałem docetakselu. Metody. Do otwartego badania III fazy włączono chorych na rozsianego, opornego na leczenie antyandrogenowe raka gruczołu krokowego, uprzednio poddanych hormonoterapii, u których doszło do progresji w trakcie lub po zakończeniu chemioterapii z udziałem docetakselu. Chorych przydzielano losowo do 10 mg prednizonu doustnie, w połączeniu z dożylnym wlewem mitoksantronu 12 mg/m 2 (15-30 minut) lub kabazytakselu 25 mg/m 2 (1h) co 3 tygodnie. Pierwotnym wskaźnikiem końcowej oceny był całkowity czas przeżycia, a wtórnymi czas do progresji oraz bezpieczeństwo leczenia. Analizę przeprowadzono zgodnie z intencją leczenia. Badanie zarejestrowano w ClinicalTrials.gov pod numerem NCT Wyniki. Do badania włączono 755 chorych (377 do grupy z mitoksantronem, 378 z kabazytakselem). Analizę zakończono 25 września 2009 r. Średni czas przeżycia wyniósł 15,1 miesięcy (95% przedział ufności 14,1-16,3) w grupie chorych otrzymujących kabazytaksel i 12,7 miesięcy (11,6-13,7) w grupie leczonej mitoksantronem. Współczynnik ryzyka zgonu chorych otrzymujących kabazytaksel w porównaniu do leczonych mitoksantronem wyniósł 0,70 (95% przedział ufności 0,59-0,83, p<0,0001). Średni czas do progresji wyniósł 2,8 miesięcy (95% przedział ufności 2,4-3,0) w grupie leczonej kabazytakselem i 1,4 miesięcy (1,4-1,7) w grupie otrzymującej mitoksantron (współczynnik ryzyka 0,74, 0,64-0,86, p<0,0001). Najczęstszym klinicznie znamiennym niepożądanym zdarzeniem w stopniu 3. lub wyższym była neutropenia (kabazytaksel 303 [82%] chorych w porównaniu z mitoksantronem 215 [58%]) oraz biegunka (23 [6%] w porównaniu z 1 chorym [<1%]). Gorączka neutropeniczna wystąpiła u 28 (8%) chorych otrzymujących kabazytaksel oraz u 5 (1%) otrzymujących mitoksantron. Wnioski. Zastosowanie kabazytakselu z prednizonem wydłużyło czas całkowitego przeżycia chorych na rozsianego, opornego na leczenie antyandrogenowe raka gruczołu krokowego z progresją podczas lub po chemioterapii z udziałem docetakselu. Randomized trial of radiotherapy plus concurrent-adjuvant chemotherapy vs radiotherapy alone for regionally advanced nasopharyngeal carcinoma Lee AW, Tung SY, Chua DT i wsp. J Natl Cancer Inst 2010;102: Aktualne zalecenia dotyczące leczenia zaawansowanego raka nosowej części gardła przy użyciu jednoczasowej radiochemioterapii zostały oparte na wynikach publikowanego w 1998 r. badania Intergroup W tym badaniu wyniki wyłącznej radioterapii były gorsze niż w innych badaniach. Nie przedstawiono również danych odnośnie późnych powikłań. Konieczna była długoterminowa weryfikacja indeksu terapeutycznego tego schematu leczenia. Metody. Chorych na nierogowaciejącego raka nosowej części gardła w stopniu zaawansowania T1-4N2-3 M0 przydzielono losowo do wyłącznej radioterapii (176 chorych) lub do jednoczesnej radiochemioterapii (172 chorych) z zastosowaniem cisplatyny (100 mg/m 2 ), podawanej w 3 cyklach co 3 tygodnie, z uzupełniającą chemioterapią z użyciem cisplatyny (80 mg/m 2 ) i fluorouracylu (1000 mg/m 2 /d przez 4 dni) w 3 cyklach co 4 tygodnie. Pierwotnymi wskaźnikami końcowej oceny był całkowity czas wolny od niepowodzenia (FFR; czas do wystąpienia pierwszego niepowodzenia w każdej lokalizacji) i czas do progresji. Wtórnymi punktami końcowej oceny był czas całkowitego przeżycia, czas do miejscowo-regionalnego niepowodzenia, czas do odległego niepowodzenia oraz wskaźniki wczesnej oraz późnej toksyczności. Wszystkie testy statystyczne były dwustronne. Wyniki. Obie grupy były dobrze zrównoważone pod względem charakterystyki chorych, czynników zależnych od nowotworu oraz parametrów radioterapii. Dodanie chemioterapii znamiennie zwiększyło udział 5-letnich przeżyć bez niepowodzeń (radiochemioterapia w porównaniu do wyłącznej radioterapii: 67% w porównaniu z 55%; p=0,014) oraz 5-letnich przeżyć wolnych od progresji (radiochemioterapia w porównaniu do wyłącznej radioterapii: 62% w porównaniu z 53%; p=0,035). Skumulowany współczynnik wystąpienia wczesnych powikłań wzrósł o 30% w grupie poddanej chemioterapii (radiochemioterapia w porównaniu z wyłączną radioterapią: 83% w porównaniu z 53%; p<0,001), ale nie obserwowano znamiennego wzrostu 5-letnich późnych powikłań (radiochemioterapia w porównaniu z wyłączną radioterapią: 30% w porównaniu z 24%; p=0,30). Udział zgonów z powodu progresji zmniejszył się o 14% (radiochemioterapia w porównaniu z wyłączną radioterapią: 38% w porównaniu z 24%; p=0,008), ale udział 5-letnich przeżyć był zbliżony w obu grupach (radiochemioterapia w porównaniu z wyłączną radioterapią: 68% w porównaniu do 64%; p=0,22; współczynnik ryzyka dla radiochemioterapii wyniósł 0,81, 95% przedział ufności od 0,58 do 1,13), ponieważ liczba zgonów z powodu toksyczności lub
3 310 przypadkowych przyczyn wzrosła o 7% (radiochemioterapia w porównaniu z wyłączną radioterapią: odpowiednio 1,7% w porównaniu z 0 oraz 8,1% w porównaniu z 3,4%; p=0,015). Wnioski. Skojarzenie radioterapii z jednoczesną i uzupełniającą chemioterapią znamiennie obniżyło liczbę niepowodzeń oraz zgonów związanych z nowotworem, w porównaniu do wyłącznej radioterapii. Nie wykazano znamiennego wzrostu częstości późnych powikłań, ale zwiększona liczba zgonów nie związanych z nowotworem ograniczyła ostateczny potencjalny zysk w całkowitym przeżyciu. Early palliative care for patients with metastatic non-small-cell lung cancer Temel JS, Greer JA, Muzikansky A i wsp. N Engl J Med 2010; 363: U chorych na rozsianego niedrobnokomórkowego raka płuca w terminalnym okresie życia występują nasilone dolegliwości, co może się wiązać ze stosowaniem agresywnego podejścia terapeutycznego. Oceniono wpływ wczesnego podjęcia opieki paliatywnej na oceniane przez chorego punkty końcowe oraz zakres opieki terminalnej w grupie chorych leczonych ambulatoryjnie z nowo rozpoznaną chorobą. Metody. Chorych na nowo rozpoznanego rozsianego niedrobnokomórkowego raka płuca przydzielono losowo do wczesnej opieki paliatywnej, połączonej ze standardowym leczeniem onkologicznym lub wyłącznego leczenia onkologicznego. W oparciu o skalę FACT-L (Functional Assessment of Cancer Therapy-Lung) oraz Hospital Anxiety and Depression Scale oceniano jakość życia oraz samopoczucie w chwili włączenia do badania oraz po 12 tygodniach. Pierwotnym wskaźnikiem oceny końcowej była zmiana jakości życia po 12 tygodniach. Dane na temat terminalnej opieki uzyskiwano z elektronicznych systemów przechowujących dokumentację medyczną (EMR). Wyniki. 27 spośród 151 chorych poddanych randomizacji zmarło w ciągu 12 tygodni, a 107 (86% pozostałych chorych) ukończyło samoocenę. Jakość życia chorych objętych wczesną opieką paliatywną była lepsza, w porównaniu do chorych otrzymujących standardowe leczenie onkologiczne (średnia punktacja w skali FACT-L [zakres od 0 do 136 punktów, z wyższą punktacją wskazującą na lepszą jakość życia] wyniosła 98,0 w porównaniu do 91,5; p=0,03). Dodatkowo mniej chorych w grupie objętej opieką paliatywną, w porównaniu do chorych leczonych wyłącznie onkologicznie, miało objawy depresji (16% w porównaniu z 38%, p=0,01). Mniej chorych spośród objętych wczesną opieką paliatywną wymagało agresywnego leczenia w terminalnym okresie życia, w porównaniu z grupą otrzymujących standardowe leczenie onkologiczne (33% w porównaniu z 54%, p=0,05), a ich średni czas przeżycia był dłuższy (11,6 miesięcy w porównaniu z 8,9 miesięcy, p=0,02). Wnioski. Wdrożenie wczesnej paliatywnej opieki w grupie chorych na rozsianego niedrobnokomórkowego raka płuca znamiennie poprawiło jakość życia oraz samopoczucie chorych. W porównaniu do chorych leczonych wyłącznie onkologicznie, chorzy objęci wczesną opieką paliatywną poddawani byli mniej agresywnej terapii w terminalnym okresie życia i żyli dłużej. Iniparib plus chemotherapy in metastatic triple-negative breast cancer O Shaughnessy J, Osborne C, Pippen JE i wsp. N Engl J Med 2011; 364: W komórkach potrójnie ujemnego raka piersi (triple-negative breast cancer TNBC) występują swoiste zaburzenia naprawy DNA, co stanowi przesłankę do zastosowania w tym nowotworze celowanego leczenia inhibitorami polimerazy poliadp-rybozy (PARP). Metody. W otwartym badaniu II fazy porównano skuteczność i bezpieczeństwo stosowania gemcytabiny z karboplatyną oraz leczenia tym schematem w skojarzeniu z iniparybem, niskocząsteczkowym inhibitorem PARP w grupie chorych na rozsianego potrójnie ujemnego raka piersi. 123 chore przydzielano losowo do leczenia gemcytabiną (1000 mg/m 2 ) i karboplatyną (AUC 2) w dniach 1. i 8. cyklu w skojarzeniu z iniparybem (5,6 mg/ kg w dniach 1., 4., 8., i 11., co 3 tygodnie) lub placebo. Pierwotnym wskaźnikiem końcowej oceny był udział klinicznych korzyści (udział obiektywnych odpowiedzi [całkowitych lub częściowych] oraz stabilizacji choroby 6 miesięcy) oraz bezpieczeństwo leczenia. Dodatkowymi punktami końcowej oceny były: odsetek obiektywnych odpowiedzi, czas do progresji oraz czas całkowitego przeżycia. Wyniki. Skojarzenie gemcytabiny i karboplatyny z iniparybem zwiększyło odsetek klinicznych korzyści z 34% do 56% (p=0,01) i całkowity odsetek odpowiedzi z 32% do 52% (p=0,02). Dodanie iniparybu wydłużyło także średni czas do progresji z 3,6 miesięcy do 5,9 miesięcy (współczynnik ryzyka progresji [HR] 0,59; p=0,01) i średni czas całkowitego przeżycia z 7,7 miesięcy do 12,3 miesięcy (współczynnik ryzyka zgonu 0,57; p=0,01). W obu grupach najczęstszymi działaniami niepożądanymi w stopniu 3. i 4. były: neutropenia, małopłytkowość, niedokrwistość, zmęczenie lub astenia, leukopenia i podwyższona aktywność aminotransferazy alaninowej. Nie zaobserwowano znamiennej różnicy w częstości występowania działań niepożądanych pomiędzy obiema grupami. Wnioski. Dodanie iniparybu do chemioterapii zwiększyło korzyść kliniczną oraz wydłużyło czas przeżycia chorych na rozsianego potrójnie ujemnego raka piersi, bez znamiennego nasilenia toksyczności. Na podstawie tych wyników obecnie prowadzone jest badanie III fazy, w którym będzie oceniany całkowity czas przeżycia oraz czas do progresji. Badanie zarejestrowano na ClinicalTrials.gov pod numerem NCT
4 311 Everolimus for advanced pancreatic neuroendocrine tumors Yao JC, Shah MH, Ito T i wsp. N Engl J Med 2011; 364: W dwóch badaniach II fazy z udziałem chorych na zaawansowany neuroendokrynny nowotwór trzustki potwierdzono aktywność przeciwnowotorową ewerolimusu, doustnego inhibitora kinazy mtor. Oceniono działanie ewerolimusu w prospektywnym badaniu III fazy. Metody. 410 chorych na zaawansowany, neuroendokrynny, dobrze lub średnio zróżnicowany nowotwór trzustki, z potwierdzoną radiologicznie progresją w ciągu ostatnich 12 miesięcy, przydzielono losowo do leczenia ewerolimusem w dawce 10 mg raz dziennie (207 chorych) lub placebo (203 chorych), w skojarzeniu z najlepszym leczeniem objawowym (BSC). Pierwotnym wskaźnikiem oceny końcowej był czas do progresji w analizie typu intention-to-treat. Chorym otrzymującym placebo, po radiologicznym potwierdzeniu progresji, podawano ewerolimus. Wyniki. Mediana czasu do progresji wyniosła 11 miesięcy w grupie leczonej ewerolimusem, w porównaniu do 4,6 miesięcy w grupie otrzymującej placebo (współczynnik ryzyka progresji choroby lub zgonu w grupie z ewerolimusem 0,35; 95% przedział ufności [CI], 0,27 do 0,45; p<0,001), co odpowiadało zmniejszeniu szacowanego ryzyka progresji lub zgonu o 65%. Po 18 miesiącach obserwacji odsetek chorych bez progresji wyniósł odpowiednio 34% (95% przedział ufności 26 do 43) w grupie leczonych ewerolimusem, w porównaniu do 9% (95% przedział ufności, 4 do 16) w grupie otrzymującej placebo. Niepożądane działania związane z lekiem: zapalenie jamy ustnej (u 64% chorych w grupie leczonej ewerolimusem w porównaniu do 17% wśród otrzymujących placebo), wysypka (49% w porównaniu do 10%), biegunka (34% w porównaniu do 10%), zmęczenie (31% w porównaniu do 14%) oraz zakażenia (23% w porównaniu do 6%) głównie górnych dróg oddechowych, wystąpiły głównie w 1. i 2. stopniu nasilenia. Zdarzenia niepożądane w stopniu 3. i 4. występowały częściej w grupie chorych leczonych ewerolimusem: niedokrwistość (6% w porównaniu do 0%) i hiperglikemia (5% w porównaniu do 2%). Średni czas podawania ewerolimusu był 2,3-krotnie dłuższy niż podawanie placebo (38 tygodni w porównaniu do 16 tygodni). Wnioski. W grupie chorych na zaawansowany, neuroendokrynny nowotwór trzustki z progresją po uprzednim leczeniu, zastosowanie ewerolimusu znamiennie wydłużyło czas do progresji w porównaniu z placebo oraz wiązało się z niewielkim odsetkiem poważnych działań niepożądanych. Badanie zarejestrowano na ClinicalTrials.gov pod numerem NCT Induction chemotherapy with cisplatin and fluorouracil alone or in combination with docetaxel in locally advanced squamous-cell cancer of the head and neck: long-term results of the TAX 324 randomised phase 3 trial Lorch JH, Goloubeva O, Haddad R i wsp. Lancet Oncol 2011; 12: Wstępne wyniki badania TAX 324, opublikowane po 2 latach obserwacji, potwierdziły znamienne wydłużenie czasu przeżycia chorych na miejscowo zaawansowane nowotwory głowy i szyi, poddanych indukcyjnej chemioterapii z zastosowaniem docetakselu, cisplatyny i fluorouracylu (TPF), w porównaniu do schematu złożonego wyłącznie z cisplatyny i fluorouracylu (PF). Przedstawiono wyniki po 5 latach obserwacji. Metody. W otwartym badaniu III fazy TAX 324 porównywano zastosowanie 3 cykli indukcyjnej chemioterapii wg schematu TPF (docetaksel 75 mg/m 2, cisplatyna 100 mg/m 2 i fluorouracyl 1000 mg/m 2 /d w ciągłym 24-godzinnym wlewie przez 4 dni) z 3 cyklami PF (cisplatyna 100 mg/m 2 i fluorouracyl 1000 mg/m 2 /d w ciągłym 24-godzinnym wlewie przez 5 dni) u chorych na płaskonabłonkowe nowotwory głowy i szyi w III lub IV stopniu klinicznego zaawansowania. Następnie chorzy byli poddawani trwającej 7 tygodni radioterapii, skojarzonej z podawaną cotygodniowo karboplatyną. Randomizacji dokonywano centralnie przy użyciu techniki minimizacji typu biased-coin. Przy włączaniu do badania chorzy byli stratyfikowani wg lokalizacji ogniska pierwotnego, stanu zajęcia węzłów chłonnych (N0 lub N1 vs N2 lub N3) oraz ośrodka. Dane do niniejszej długoterminowej analizy zbierano od r. Pierwotnymi wskaźnikami oceny końcowej były: czas całkowitego przeżycia oraz czas do progresji. Toksyczność leczenia oceniano na podstawie konieczności wyłonienia tracheotomii oraz zastosowania sondy dożołądkowej. Dane wszystkich 501 chorych (255 TPF, 246 PF) wykorzystano do analizy intention-to-treat. W przypadku 61 chorych, dla których nie posiadano danych z czasu obserwacji, wykorzystano wyniki wstępnej analizy z 2005 r. Badanie zarejestrowano na ClinicalTrials.gov pod numerem NCT Wyniki. Mediana czasu obserwacji wyniosła 72,2 miesięcy (95% CI 68,8-75,5). Czas całkowitego przeżycia był znamiennie dłuższy w grupie chorych leczonych TPF w porównaniu do PF (współczynnik ryzyka [HR] 0,74 95% CI 0,58-0,94). Udział 5-letnich przeżyć wyniósł 52% w grupie chorych otrzymujących TPF oraz 42% wśród otrzymujących PF. Mediana czasu przeżycia wyniosła 70,6 miesięcy (95% CI 49,0-89,0) w grupie leczonej TPF, w porównaniu do 34,8 miesięcy (22,6-48,0) w grupie leczonej PF (p=0,014). Czas do progresji był także znamiennie dłuższy w grupie otrzymującej TPF (średnio 38,1 miesięcy, 95% CI 19,3-66,1), w porówna-
5 312 niu do 13,2 (10,6-20,7; HR 0,75, 95% CI 0,60-0,94). Nie zaobserwowano znamiennej różnicy w częstości założenia sondy dożołądkowej i tracheostomii pomiędzy obiema grupami. W grupie otrzymującej TPF trzech spośród 91 (3%) chorych wymagało założenia sondy dożołądkowej, w porównaniu do 8 spośród 71 (11%) otrzymujących PF. U 6 spośród 92 (7%) chorych leczonych TPF wyłoniono tracheotomię, zaś w grupie leczonej PF tego zabiegu wymagało 8 spośród 71 (11%) chorych. Wnioski. Zastosowanie indukcyjnej chemioterapii wg schematu TPF w grupie chorych na miejscowo zaawansowane nowotwory głowy i szyi wiąże się z wydłużeniem czasu przeżycia. Chorzy kwalifikowani do indukcyjnej chemioterapii powinni być leczeni schematem TPF. Opracowali: Dr n. med. Anna Kowalczyk Dr n. med. Ewa Szutowicz-Zielińska Dr n. med. Anna Wrona Dr n. med. Krzysztof Konopa
Rak piersi. Doniesienia roku Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie
 Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego. Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa
 Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Wydłużenie życia chorych z rakiem płuca - nowe możliwości
 Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Typ histopatologiczny
 Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Warszawa, 31.10.2007r.
 Warszawa, 31.10.2007r. Lek Taxotere otrzymuje pozytywną opinię Komitetu ds. Produktów Leczniczych stosowanych u Ludzi (CHMP), zalecającą rejestrację w Unii Europejskiej do leczenia indukcyjnego miejscowo
Warszawa, 31.10.2007r. Lek Taxotere otrzymuje pozytywną opinię Komitetu ds. Produktów Leczniczych stosowanych u Ludzi (CHMP), zalecającą rejestrację w Unii Europejskiej do leczenia indukcyjnego miejscowo
Piotr Potemski. Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi
 Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Obserwowane są samoistne regresje zmian przerzutowych
Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Obserwowane są samoistne regresje zmian przerzutowych
Katarzyna Pogoda Warszawa, 23 marca 2017 roku
 Chemioterapia doustna i podskórne metody podawania leków w raku piersi. Lepsza jakość życia pacjentek Katarzyna Pogoda Warszawa, 23 marca 2017 roku Rak piersi - heterogenna choroba Stopień zaawansowania
Chemioterapia doustna i podskórne metody podawania leków w raku piersi. Lepsza jakość życia pacjentek Katarzyna Pogoda Warszawa, 23 marca 2017 roku Rak piersi - heterogenna choroba Stopień zaawansowania
Keytruda (pembrolizumab)
 EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
Piotr Potemski. Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi
 Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Konferencje naukowe a praktyka kliniczna Podstawowe
Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Konferencje naukowe a praktyka kliniczna Podstawowe
S T R E S Z C Z E N I E
 STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
NOWOTWORY Journal of Oncology 2009 volume 59 Number 3 243 247. Journal Club
 NOWOTWORY Journal of Oncology 2009 volume 59 Number 3 243 247 Journal Club Standard-dose versus higher-dose prophylactic cranial irradiation (PCI) in patients with limited-stage small-cell lung cancer
NOWOTWORY Journal of Oncology 2009 volume 59 Number 3 243 247 Journal Club Standard-dose versus higher-dose prophylactic cranial irradiation (PCI) in patients with limited-stage small-cell lung cancer
Rak jajnika. Prof. Mariusz Bidziński. Klinika Ginekologii Onkologicznej
 Rak jajnika Prof. Mariusz Bidziński Klinika Ginekologii Onkologicznej Współpraca z firmami: Roche, Astra Zeneca, MSD, Olympus Mutacje w genach BRCA1 i BRCA2 Materiały edukacyjne Astra Zeneca Mutacje w
Rak jajnika Prof. Mariusz Bidziński Klinika Ginekologii Onkologicznej Współpraca z firmami: Roche, Astra Zeneca, MSD, Olympus Mutacje w genach BRCA1 i BRCA2 Materiały edukacyjne Astra Zeneca Mutacje w
Nowotwór złośliwy oskrzela i płuca
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy oskrzela i płuca Bevacizumab Bewacyzumab w skojarzeniu z chemioterapią opartą na pochodnych platyny jest wskazany w leczeniu pierwszego
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy oskrzela i płuca Bevacizumab Bewacyzumab w skojarzeniu z chemioterapią opartą na pochodnych platyny jest wskazany w leczeniu pierwszego
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
Komunikat prasowy. Dodatkowe informacje
 Dane na temat czasu przeżycia całkowitego uzyskane w badaniu LUX-Lung 7 bezpośrednio porównującym leki afatynib i gefitynib, przedstawione na ESMO 2016 W badaniu LUX-Lung 7 zaobserwowano mniejsze ryzyko
Dane na temat czasu przeżycia całkowitego uzyskane w badaniu LUX-Lung 7 bezpośrednio porównującym leki afatynib i gefitynib, przedstawione na ESMO 2016 W badaniu LUX-Lung 7 zaobserwowano mniejsze ryzyko
Journal Club. leczenia chirurgicznego uzupełnionego chemioradioterapią. z wyłącznym leczeniem chirurgicznym, a także skuteczność
 NOWOTWORY Journal of Oncology 2011 volume 61 Number 1 99 104 Journal Club Adjuvant chemotherapy, with or without postoperative radiotherapy, in operable non-small-cell lung cancer: two meta-analyses of
NOWOTWORY Journal of Oncology 2011 volume 61 Number 1 99 104 Journal Club Adjuvant chemotherapy, with or without postoperative radiotherapy, in operable non-small-cell lung cancer: two meta-analyses of
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
Journal Club. Tumor-associated macrophages and survival in classic Hodgkin s lymphoma Steidl C, Lee T, Shah SP i wsp. N Engl J Med 2010; 362: 875-885
 NOWOTWORY Journal of Oncology 2010 volume 60 Number 3 297 301 Journal Club Effect of dutasteride on the risk of prostate cancer Andriole GL, Bostwick DG, Brawley OW i wsp. N Engl J Med 2010; 362: 1192-1202
NOWOTWORY Journal of Oncology 2010 volume 60 Number 3 297 301 Journal Club Effect of dutasteride on the risk of prostate cancer Andriole GL, Bostwick DG, Brawley OW i wsp. N Engl J Med 2010; 362: 1192-1202
Jurnal Club. Human Papillomavirus and survival of patients with oropharyngeal cancer Ang KK, Harris J, Wheeler R i wsp. N Engl J Med 2010; 363: 24-35
 NOWOTWORY Journal of Oncology 2010 volume 60 Number 4 395 399 Jurnal Club Human Papillomavirus and survival of patients with oropharyngeal cancer Ang KK, Harris J, Wheeler R i wsp. N Engl J Med 2010; 363:
NOWOTWORY Journal of Oncology 2010 volume 60 Number 4 395 399 Jurnal Club Human Papillomavirus and survival of patients with oropharyngeal cancer Ang KK, Harris J, Wheeler R i wsp. N Engl J Med 2010; 363:
Leczenie skojarzone w onkologii. Joanna Streb, Oddział Kliniczny Onkologii Szpitala Uniwersyteckiego
 Leczenie skojarzone w onkologii Joanna Streb, Oddział Kliniczny Onkologii Szpitala Uniwersyteckiego Zastosowanie leczenia skojarzonego w onkologii Chemioradioterapia sekwencyjna lub jednoczasowa: Nowotwory
Leczenie skojarzone w onkologii Joanna Streb, Oddział Kliniczny Onkologii Szpitala Uniwersyteckiego Zastosowanie leczenia skojarzonego w onkologii Chemioradioterapia sekwencyjna lub jednoczasowa: Nowotwory
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 36/2012 z dnia 25 czerwca 2012 r. w zakresie usunięcia z wykazu świadczeń gwarantowanych/zmiany poziomu lub sposobu
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 36/2012 z dnia 25 czerwca 2012 r. w zakresie usunięcia z wykazu świadczeń gwarantowanych/zmiany poziomu lub sposobu
Potrójnie ujemne postaci raki piersi, co o nich już wiemy? Katarzyna Pogoda
 Potrójnie ujemne postaci raki piersi, co o nich już wiemy? Katarzyna Pogoda Biologiczne podtypy raka piersi Przebieg choroby TNBC Biologiczny podtyp o większym ryzyku nawrotu choroby. Rozsiew następuje
Potrójnie ujemne postaci raki piersi, co o nich już wiemy? Katarzyna Pogoda Biologiczne podtypy raka piersi Przebieg choroby TNBC Biologiczny podtyp o większym ryzyku nawrotu choroby. Rozsiew następuje
Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną. Klinika Onkologii i Radioterapii
 Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną chemioterapię z udziałem cisplatyny? Jacek Jassem Klinika Onkologii i Radioterapii Gdańskiego ń Uniwersytetu t Medycznego Jaka jest siła
Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną chemioterapię z udziałem cisplatyny? Jacek Jassem Klinika Onkologii i Radioterapii Gdańskiego ń Uniwersytetu t Medycznego Jaka jest siła
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 88/2013 z dnia 29 lipca 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Halaven
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 88/2013 z dnia 29 lipca 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Halaven
czerniak (nowotwór skóry), który rozprzestrzenił się lub którego nie można usunąć chirurgicznie;
 EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
CT colonography versus colonoscopy for the detection of advanced neoplasia Kim DH, Pickhardt PJ, Taylor AJ i wsp. N Engl J Med 2007; 357: 1403-1412
 NOWOTWORY Journal of Oncology 2007 volume 57 Number 6 741 745 Journal Club Chemotherapy plus involved-field radiation in early-stage Hodgkin s disease Fermé C, Eghbali H, Meerwaldt JH i wsp. EORTC GELA
NOWOTWORY Journal of Oncology 2007 volume 57 Number 6 741 745 Journal Club Chemotherapy plus involved-field radiation in early-stage Hodgkin s disease Fermé C, Eghbali H, Meerwaldt JH i wsp. EORTC GELA
Journal Club. Fibulin-3 as a blood and effusion biomarker for pleural mesothelioma
 Journal Club NOWOTWORY Journal of Oncology 2012, volume 62, number 6, 499 503 Polskie Towarzystwo Onkologiczne ISSN 0029-540X www.nowotwory.viamedica.pl Fibulin-3 as a blood and effusion biomarker for
Journal Club NOWOTWORY Journal of Oncology 2012, volume 62, number 6, 499 503 Polskie Towarzystwo Onkologiczne ISSN 0029-540X www.nowotwory.viamedica.pl Fibulin-3 as a blood and effusion biomarker for
C e l. Doksorubicyna w połączeniu z cyklofosfamidem (AC) jest standardowym schematem, stosowanym w uzupełniającym
 NOWOTWORY Journal of Oncology 2008 volume 58 Number 5 485 491 Journal Club Effect of preoperative chemoradiation in addition to preoperative chemotherapy: a randomised trial in stage III non-small-cell
NOWOTWORY Journal of Oncology 2008 volume 58 Number 5 485 491 Journal Club Effect of preoperative chemoradiation in addition to preoperative chemotherapy: a randomised trial in stage III non-small-cell
LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C 34)
 Załącznik B.6. LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C 34) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
Załącznik B.6. LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C 34) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI. Maria Litwiniuk Warszawa 28 maja 2019
 LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI Maria Litwiniuk Warszawa 28 maja 2019 Konflikt interesów Wykłady sponsorowane dla firm: Teva, AstraZeneca, Pfizer, Roche Sponorowanie
LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI Maria Litwiniuk Warszawa 28 maja 2019 Konflikt interesów Wykłady sponsorowane dla firm: Teva, AstraZeneca, Pfizer, Roche Sponorowanie
Terapeutyczne Programy Zdrowotne 2012 Leczenie glejaków mózgu Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r.
 Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
chemioterapią oraz przedoperacyjnej radioterapii z pooperacyjną
 NOWOTWORY Journal of Oncology 2006 volume 56 Number 6 749 753 Jornal Club Chemotherapy with preoperative radiotherapy in rectal cancer Bosset JF, Collette L, Calais G i wsp. EORTC Radiotherapy Group Trial
NOWOTWORY Journal of Oncology 2006 volume 56 Number 6 749 753 Jornal Club Chemotherapy with preoperative radiotherapy in rectal cancer Bosset JF, Collette L, Calais G i wsp. EORTC Radiotherapy Group Trial
Przegląd publikacji z roku 2013 Cancer New England Journal of Medicine Annals of Oncology
 Przegląd publikacji z roku 2013 Cancer New England Journal of Medicine Annals of Oncology Renata Zaucha HOT TOPICS 2014 w Onkologii Ginekologicznej Warszawa Wybrane publikacje 1 Annals of Oncology 2013;
Przegląd publikacji z roku 2013 Cancer New England Journal of Medicine Annals of Oncology Renata Zaucha HOT TOPICS 2014 w Onkologii Ginekologicznej Warszawa Wybrane publikacje 1 Annals of Oncology 2013;
zaawansowanym rakiem nerkowokomórkowym, rodzajem raka nerki, u pacjentów, którzy byli wcześniej leczeni lekami przeciwnowotworowymi;
 EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
Personalizacja leczenia rozsianego raka nerki.
 RAFAŁ STEC Personalizacja leczenia rozsianego raka nerki. Warszawa, 13 października 2018 roku Opis przypadku nr 1. Rozpoznanie Data rozpoznania: 07.11.2007 r. Pacjent: 65 lat, K Dane na temat guza: - Stopień
RAFAŁ STEC Personalizacja leczenia rozsianego raka nerki. Warszawa, 13 października 2018 roku Opis przypadku nr 1. Rozpoznanie Data rozpoznania: 07.11.2007 r. Pacjent: 65 lat, K Dane na temat guza: - Stopień
Nowotwór złośliwy piersi
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy piersi Lapatinib Refundacja z ograniczeniami Lapatinib jest wskazany do leczenia dorosłych pacjentów z rakiem piersi, u których nowotwór
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy piersi Lapatinib Refundacja z ograniczeniami Lapatinib jest wskazany do leczenia dorosłych pacjentów z rakiem piersi, u których nowotwór
ASCO 2017 KURIER ONKOLOGICZNY. Monika Dudzisz-Śledź, Piotr Wysocki
 KURIER ONKOLOGICZNY Monika Dudzisz-Śledź, Piotr Wysocki ASCO 2017 Artykuł jest tłumaczeniem pracy: Dudzisz-Śledź M, Wysocki P. Oncology courier. Oncol Clin Pract 2017; 13: 71 74. DOI: 10.5603/OCP.2017.0012.
KURIER ONKOLOGICZNY Monika Dudzisz-Śledź, Piotr Wysocki ASCO 2017 Artykuł jest tłumaczeniem pracy: Dudzisz-Śledź M, Wysocki P. Oncology courier. Oncol Clin Pract 2017; 13: 71 74. DOI: 10.5603/OCP.2017.0012.
Wybór najistotniejszych publikacji z roku 2013 Lancet (IF-39)/Lancet Oncology (IF-25)/ Oncologist
 Wybór najistotniejszych publikacji z roku 2013 Lancet (IF-39)/Lancet Oncology (IF-25)/ Oncologist (IF-4) Dr n. med. Lubomir Bodnar Klinika Onkologii, Wojskowego Instytutu Medycznego w Warszawie Warszawa
Wybór najistotniejszych publikacji z roku 2013 Lancet (IF-39)/Lancet Oncology (IF-25)/ Oncologist (IF-4) Dr n. med. Lubomir Bodnar Klinika Onkologii, Wojskowego Instytutu Medycznego w Warszawie Warszawa
NOWOTWORY Journal of Oncology 2008 volume 58 Number Journal Club
 NOWOTWORY Journal of Oncology 2008 volume 58 Number 4 391 395 Journal Club Phase III study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapynaive patients with advanced-stage
NOWOTWORY Journal of Oncology 2008 volume 58 Number 4 391 395 Journal Club Phase III study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapynaive patients with advanced-stage
Immunoterapia niedrobnokomórkowego raka płuca. dr n. med. Adam Płużański. Klinika Nowotworów Płuca i Klatki Piersiowej
 Immunoterapia niedrobnokomórkowego raka płuca dr n. med. Adam Płużański Klinika Nowotworów Płuca i Klatki Piersiowej Centrum Onkologii-Instytut im.m Skłodowskiej-Curie w Warszawie Historia prób immunoterapii
Immunoterapia niedrobnokomórkowego raka płuca dr n. med. Adam Płużański Klinika Nowotworów Płuca i Klatki Piersiowej Centrum Onkologii-Instytut im.m Skłodowskiej-Curie w Warszawie Historia prób immunoterapii
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 139/2014 z dnia 2 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Giotrif,
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 139/2014 z dnia 2 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego Giotrif,
Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008.
 załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
Paclitaxel plus bevacizumab versus paclitaxel alone for metastatic breast cancer Miller K, Wang M, Gralow J i wsp. N Engl J Med 2007; 357: 2666-2676
 NOWOTWORY Journal of Oncology 2008 volume 58 Number 1 101 105 Journal Club Bevacizumab plus interferon alfa-2a for treatment of metastatic renal cell carcinoma: a randomised, doubleblind phase III trial
NOWOTWORY Journal of Oncology 2008 volume 58 Number 1 101 105 Journal Club Bevacizumab plus interferon alfa-2a for treatment of metastatic renal cell carcinoma: a randomised, doubleblind phase III trial
NOWOTWORY Journal of Oncology 2007 volume 57 Number 5 621 625 Journal Club
 NOWOTWORY Journal of Oncology 2007 volume 57 Number 5 621 625 Journal Club The value of combined-modality therapy in elderly patients with stage III nonsmall cell lung cancer Schild SE, Mandrekar SJ, Jatoi
NOWOTWORY Journal of Oncology 2007 volume 57 Number 5 621 625 Journal Club The value of combined-modality therapy in elderly patients with stage III nonsmall cell lung cancer Schild SE, Mandrekar SJ, Jatoi
Kobimetynib w leczeniu czerniaka z obecnością mutacji BRAF w świetle zmian w programie lekowym
 Kobimetynib w leczeniu czerniaka z obecnością mutacji BRAF w świetle zmian w programie lekowym Piotr Rutkowski Kobimetynib był drugim selektywnym inhibitorem MEK (po trametynibie) zarejestrowanym do leczenia
Kobimetynib w leczeniu czerniaka z obecnością mutacji BRAF w świetle zmian w programie lekowym Piotr Rutkowski Kobimetynib był drugim selektywnym inhibitorem MEK (po trametynibie) zarejestrowanym do leczenia
RAK NERKOWO-KOMÓRKOWY UOGÓLNIONE STADIUM PRZEWLEKŁA CHOROBA // DŁUGOŚĆ LECZENIA
 RAK NERKOWO-KOMÓRKOWY PRZEWLEKŁA CHOROBA // DŁUGOŚĆ LECZENIA Maciej Krzakowski Centrum Onkologii-Instytut im. Marii Skłodowskiej-Curie Warszawa 1 SYGNAŁOWE SZLAKI // TERAPEUTYCZNE CELE * Oudard i wsp.
RAK NERKOWO-KOMÓRKOWY PRZEWLEKŁA CHOROBA // DŁUGOŚĆ LECZENIA Maciej Krzakowski Centrum Onkologii-Instytut im. Marii Skłodowskiej-Curie Warszawa 1 SYGNAŁOWE SZLAKI // TERAPEUTYCZNE CELE * Oudard i wsp.
Ocena czynników rokowniczych w raku płaskonabłonkowym przełyku w materiale Kliniki Chirurgii Onkologicznej AM w Gdańsku doniesienie wstępne
 Ocena czynników rokowniczych w raku płaskonabłonkowym przełyku w materiale Kliniki Chirurgii Onkologicznej AM w Gdańsku doniesienie wstępne Świerblewski M. 1, Kopacz A. 1, Jastrzębski T. 1 1 Katedra i
Ocena czynników rokowniczych w raku płaskonabłonkowym przełyku w materiale Kliniki Chirurgii Onkologicznej AM w Gdańsku doniesienie wstępne Świerblewski M. 1, Kopacz A. 1, Jastrzębski T. 1 1 Katedra i
Nowe możliwości leczenia ostrej białaczki limfoblastycznej
 Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Leczenie zaawansowanych (nieresekcyjnych i/lub przerzutowych) GIST Nieoperacyjny lub rozsiany GIST jest oporny na konwencjonalną chemioterapię.
 Leczenie zaawansowanych (nieresekcyjnych i/lub przerzutowych) GIST Nieoperacyjny lub rozsiany GIST jest oporny na konwencjonalną chemioterapię. Rola radioterapii nie jest ostatecznie ustalona. Dotychczasowe
Leczenie zaawansowanych (nieresekcyjnych i/lub przerzutowych) GIST Nieoperacyjny lub rozsiany GIST jest oporny na konwencjonalną chemioterapię. Rola radioterapii nie jest ostatecznie ustalona. Dotychczasowe
Dr n. med. Norbert Grząśko w imieniu Polskiej Grupy Szpiczakowej Lublin, 12.04.2008
 Ocena skuteczności i bezpieczeństwa leczenia układem CTD (cyklofosfamid, talidomid, deksametazon) u chorych na szpiczaka plazmocytowego aktualizacja danych Dr n. med. Norbert Grząśko w imieniu Polskiej
Ocena skuteczności i bezpieczeństwa leczenia układem CTD (cyklofosfamid, talidomid, deksametazon) u chorych na szpiczaka plazmocytowego aktualizacja danych Dr n. med. Norbert Grząśko w imieniu Polskiej
NOWOTWORY Journal of Oncology 2011 volume 61 Number Journal Club
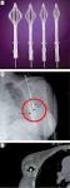 NOWOTWORY Journal of Oncology 2011 volume 61 Number 5 533 538 Journal Club International phase III trial assessing neoadjuvant cisplatin, methotrexate, and vinblastine chemotherapy for muscle-invasive
NOWOTWORY Journal of Oncology 2011 volume 61 Number 5 533 538 Journal Club International phase III trial assessing neoadjuvant cisplatin, methotrexate, and vinblastine chemotherapy for muscle-invasive
Wyniki badania CLARINET w jelitowotrzustkowych nowotworach neuroendokrynnych GEP-NET/NEN bez czynności wydzielniczej
 Wyniki badania CLARINET w jelitowotrzustkowych nowotworach neuroendokrynnych GEP-NET/NEN bez czynności wydzielniczej Jarosław B. Ćwikła UWM Olsztyn i CMKP Warszawa jbcwikla@interia.pl Wieloośrodkowe, randomizowane
Wyniki badania CLARINET w jelitowotrzustkowych nowotworach neuroendokrynnych GEP-NET/NEN bez czynności wydzielniczej Jarosław B. Ćwikła UWM Olsztyn i CMKP Warszawa jbcwikla@interia.pl Wieloośrodkowe, randomizowane
Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce
 Warszawa, 27.01.2016 Seminarium naukowe: Terapie przełomowe w onkologii i hematoonkologii a dostępność do leczenia w Polsce na tle Europy Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce Dr n.
Warszawa, 27.01.2016 Seminarium naukowe: Terapie przełomowe w onkologii i hematoonkologii a dostępność do leczenia w Polsce na tle Europy Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce Dr n.
Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym?
 Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym? Piotr Potemski Klinika Chemioterapii Nowotworów Katedry Onkologii Uniwersytet
Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym? Piotr Potemski Klinika Chemioterapii Nowotworów Katedry Onkologii Uniwersytet
Journal Club. Long-term survival of participants in the Prostate Cancer Prevention Trial
 Journal Club NOWOTWORY Journal of Oncology 2013, volume 63, number 6, 519 524 DOI: 10.5603/NJO.2013.0061 Polskie Towarzystwo Onkologiczne ISSN 0029 540X www.nowotwory.viamedica.pl Pazopanib versus sunitinib
Journal Club NOWOTWORY Journal of Oncology 2013, volume 63, number 6, 519 524 DOI: 10.5603/NJO.2013.0061 Polskie Towarzystwo Onkologiczne ISSN 0029 540X www.nowotwory.viamedica.pl Pazopanib versus sunitinib
Rola mutacji BRCA 1/2 w leczeniu pacjentek z rakiem piersi
 Rola mutacji BRCA /2 w leczeniu pacjentek z rakiem piersi Tadeusz Pieńkowski Klinika Onkologii i Hematologii CSKMSWiA Klinika Onkologii i Hematologii CMKP Warszawa 29 Uszkodzenie genów BRCA i BRCA2 może
Rola mutacji BRCA /2 w leczeniu pacjentek z rakiem piersi Tadeusz Pieńkowski Klinika Onkologii i Hematologii CSKMSWiA Klinika Onkologii i Hematologii CMKP Warszawa 29 Uszkodzenie genów BRCA i BRCA2 może
CHEMIOTERAPIA I RZUTU: IP vs DOSE DENSE?
 CHEMIOTERAPIA I RZUTU: IP vs DOSE DENSE? Dr n. med. Anita Chudecka-Głaz Prof. zw. dr hab. n. med. Izabella Rzepka-Górska Katedra i Klinika Ginekologii Operacyjnej i Onkologii Ginekologicznej Dorosłych
CHEMIOTERAPIA I RZUTU: IP vs DOSE DENSE? Dr n. med. Anita Chudecka-Głaz Prof. zw. dr hab. n. med. Izabella Rzepka-Górska Katedra i Klinika Ginekologii Operacyjnej i Onkologii Ginekologicznej Dorosłych
Dr hab. n. med. Paweł Blecharz
 BRCA1 zależny rak piersi i jajnika odmienności diagnostyczne i kliniczne (BRCA1 dependent breast and ovarian cancer clinical and diagnostic diversities) Paweł Blecharz Dr hab. n. med. Paweł Blecharz Dr
BRCA1 zależny rak piersi i jajnika odmienności diagnostyczne i kliniczne (BRCA1 dependent breast and ovarian cancer clinical and diagnostic diversities) Paweł Blecharz Dr hab. n. med. Paweł Blecharz Dr
Wyniki zasadniczego badania fazy III u pacjentów z rakiem jelita grubego z przerzutami:
 Informacja prasowa Bayer HealthCare Public Relations Al.Jerozolimskie 158 02-326 Warszawa Polska Wyniki zasadniczego badania fazy III u pacjentów z rakiem jelita grubego z przerzutami: Pozytywne dane z
Informacja prasowa Bayer HealthCare Public Relations Al.Jerozolimskie 158 02-326 Warszawa Polska Wyniki zasadniczego badania fazy III u pacjentów z rakiem jelita grubego z przerzutami: Pozytywne dane z
Spis treści. Przedmowa Barbara Czerska... 11 Autorzy... 17 Wykaz skrótów... 19
 Przedmowa Barbara Czerska.................................. 11 Autorzy.................................................... 17 Wykaz skrótów.............................................. 19 Rozdział I.
Przedmowa Barbara Czerska.................................. 11 Autorzy.................................................... 17 Wykaz skrótów.............................................. 19 Rozdział I.
RAK PŁUCA 2016 ROK. Maciej Krzakowski
 RAK PŁUCA 2016 ROK Maciej Krzakowski MEDIANA CZASU PRZEŻYCIA CAŁKOWITEGO 12-24/ 12 2-4/ 12 Leczenie objawowe Chemioterapia 1-lekowa DDP Chemioterapia 2-lekowa DDP+VP16/VBL Chemioterapia 2-lekowa DDP+Leki
RAK PŁUCA 2016 ROK Maciej Krzakowski MEDIANA CZASU PRZEŻYCIA CAŁKOWITEGO 12-24/ 12 2-4/ 12 Leczenie objawowe Chemioterapia 1-lekowa DDP Chemioterapia 2-lekowa DDP+VP16/VBL Chemioterapia 2-lekowa DDP+Leki
LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C-34)
 Załącznik B.6. LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C-34) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
Załącznik B.6. LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C-34) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Pharmaki Generics, 20 mg/0,5 ml, koncentrat i rozpuszczalnik do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Pharmaki Generics, 20 mg/0,5 ml, koncentrat i rozpuszczalnik do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Lek Avastin stosuje się u osób dorosłych w leczeniu następujących rodzajów nowotworów w skojarzeniu z innymi lekami przeciwnowotworowymi:
 EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Computed tomography screening and lung cancer outcomes Bach PB, Jett JR, Pastorino U i wsp. JAMA 2007; 297: 953-961.
 NOWOTWORY Journal of Oncology 2007 volume 57 Number 3 349 353 Journal Club Computed tomography screening and lung cancer outcomes Bach PB, Jett JR, Pastorino U i wsp. JAMA 2007; 297: 953-961. Palący oraz
NOWOTWORY Journal of Oncology 2007 volume 57 Number 3 349 353 Journal Club Computed tomography screening and lung cancer outcomes Bach PB, Jett JR, Pastorino U i wsp. JAMA 2007; 297: 953-961. Palący oraz
Rak pęcherza moczowego - chemioterapia jako element leczenia skojarzonego
 Rak pęcherza moczowego - chemioterapia jako element leczenia skojarzonego Elżbieta Senkus-Konefka Klinika Onkologii i Radioterapii Gdański Uniwersytet Medyczny Kliknij ikonę, aby dodać obraz 888 cystektomii
Rak pęcherza moczowego - chemioterapia jako element leczenia skojarzonego Elżbieta Senkus-Konefka Klinika Onkologii i Radioterapii Gdański Uniwersytet Medyczny Kliknij ikonę, aby dodać obraz 888 cystektomii
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Niedrobnokomórkowy rak płuca podtrzymujące leczenie pemetreksedem
 PRACA PRZEGLĄDOWA Maciej Krzakowski Klinika Nowotworów Płuca i Klatki Piersiowej, Centrum Onkologii Instytut im. Marii Skłodowskiej-Curie w Warszawie Niedrobnokomórkowy rak płuca podtrzymujące leczenie
PRACA PRZEGLĄDOWA Maciej Krzakowski Klinika Nowotworów Płuca i Klatki Piersiowej, Centrum Onkologii Instytut im. Marii Skłodowskiej-Curie w Warszawie Niedrobnokomórkowy rak płuca podtrzymujące leczenie
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Accord 20 mg/1 ml koncentrat do sporządzania roztworu do infuzji Docetaxel Accord 80 mg/4 ml koncentrat do sporządzania
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Accord 20 mg/1 ml koncentrat do sporządzania roztworu do infuzji Docetaxel Accord 80 mg/4 ml koncentrat do sporządzania
 W badaniu 4S (ang. Scandinavian Simvastatin Survivat Study), oceniano wpływ symwastatyny na całkowitą śmiertelność u 4444 pacjentów z chorobą wieńcową i z wyjściowym stężeniem cholesterolu całkowitego
W badaniu 4S (ang. Scandinavian Simvastatin Survivat Study), oceniano wpływ symwastatyny na całkowitą śmiertelność u 4444 pacjentów z chorobą wieńcową i z wyjściowym stężeniem cholesterolu całkowitego
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Teva 20 mg/0,5 ml koncentrat i rozpuszczalnik do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Teva 20 mg/0,5 ml koncentrat i rozpuszczalnik do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Docetaxel-Ebewe, 10 mg/ml, koncentrat do sporządzania roztworu do infuzji
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel-Ebewe, 10 mg/ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml koncentratu do sporządzania
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel-Ebewe, 10 mg/ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml koncentratu do sporządzania
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Produkt leczniczy bez ważnego pozwolenia na dopuszczenie do obrotu
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docefrez 20 mg proszek i rozpuszczalnik do sporządzania koncentratu roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docefrez 20 mg proszek i rozpuszczalnik do sporządzania koncentratu roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda
Rak stercza oporny na kastrację. leczenie ukierunkowane na przerzuty do kości
 Rak stercza oporny na kastrację leczenie ukierunkowane na przerzuty do kości Nowotwór Częstość przerzutów do kości Rak piersi 65 75% Rak stercza 65 75% Niedrobnokomórkowy rak płuca 30 40% Coleman RE. Cancer
Rak stercza oporny na kastrację leczenie ukierunkowane na przerzuty do kości Nowotwór Częstość przerzutów do kości Rak piersi 65 75% Rak stercza 65 75% Niedrobnokomórkowy rak płuca 30 40% Coleman RE. Cancer
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Accord 20 mg/1 ml koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml koncentratu
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Accord 20 mg/1 ml koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml koncentratu
Journal Club. HPV screening for cervical cancer in rural India Sankaranarayanan R, Nene BM, Shastri SS i wsp. N Engl J Med 2009; 360: 1385-1394
 NOWOTWORY Journal of Oncology 2009 volume 59 Number 2 149 153 Journal Club Screening and prostate-cancer mortality in a randomized european study Schröder FH, Hugosson J, Roobol MJ i wsp. N Engl. J Med
NOWOTWORY Journal of Oncology 2009 volume 59 Number 2 149 153 Journal Club Screening and prostate-cancer mortality in a randomized european study Schröder FH, Hugosson J, Roobol MJ i wsp. N Engl. J Med
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Winthrop 20 mg koncentrat i rozpuszczalnik do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Winthrop 20 mg koncentrat i rozpuszczalnik do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI
Lek BI w porównaniu z lekiem Humira u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą
 Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
zaawansowany rak nerki lub rak nerki z przerzutami, w skojarzeniu z interferonem alfa-2a;
 EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Polpharma, 20 mg/1 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml koncentratu zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Polpharma, 20 mg/1 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml koncentratu zawiera
RAK JAJNIKA CZYLI RZECZ O WYBRCA-OWANYCH (WYBRAKOWANYCH) GENACH
 RAK JAJNIKA CZYLI RZECZ O WYBRCA-OWANYCH (WYBRAKOWANYCH) GENACH Dr hab. n. med. Lubomir Bodnar Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie PORUSZANE TEMATY Budowa genów odpowiedzialnych za
RAK JAJNIKA CZYLI RZECZ O WYBRCA-OWANYCH (WYBRAKOWANYCH) GENACH Dr hab. n. med. Lubomir Bodnar Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie PORUSZANE TEMATY Budowa genów odpowiedzialnych za
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Produkt leczniczy bez ważnego pozwolenia na dopuszczenie do obrotu
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Mylan, 20 mg/1 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr koncentratu
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Mylan, 20 mg/1 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr koncentratu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Docetaxel Pfizer, 10 mg/ml, koncentrat do sporządzania roztworu do infuzji
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Pfizer, 10 mg/ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden mililitr koncentratu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Pfizer, 10 mg/ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden mililitr koncentratu
LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4)
 Załącznik B.53. LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Załącznik B.53. LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Teva 20 mg/0,72 ml koncentrat i rozpuszczalnik do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Teva 20 mg/0,72 ml koncentrat i rozpuszczalnik do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
typ 3, sporadyczny; Techniki Obrazowe
 Guz neuroendokrynny żołądka typ 3, sporadyczny; Techniki Obrazowe Mariusz I.Furmanek CSK MSWiA i CMKP Warszawa Ocena wyjściowa, metody strukturalne WHO 2 (rak wysoko zróżnicowany); Endoskopia i/lub EUS;
Guz neuroendokrynny żołądka typ 3, sporadyczny; Techniki Obrazowe Mariusz I.Furmanek CSK MSWiA i CMKP Warszawa Ocena wyjściowa, metody strukturalne WHO 2 (rak wysoko zróżnicowany); Endoskopia i/lub EUS;
Data zakończenia badania klinicznego
 Lp. Numer protokołu badania Nazwa sponsora/cro Skład zespołu badawczego Data rozpoczęcia badania klinicznego w ośrodku Data zakończenia badania klinicznego 1 2 3 6 6 12 1. EMRII200037-014 Otwarte, randomizowane,
Lp. Numer protokołu badania Nazwa sponsora/cro Skład zespołu badawczego Data rozpoczęcia badania klinicznego w ośrodku Data zakończenia badania klinicznego 1 2 3 6 6 12 1. EMRII200037-014 Otwarte, randomizowane,
Efektywna kontrola chorych po leczeniu nowotworów jąder
 Efektywna kontrola chorych po leczeniu nowotworów jąder Marzena Wełnicka-Jaśkiewicz Klinika Onkologii i Radioterapii Gdańskiego Uniwersytetu Medycznego Efektywna kontrola ścisła obserwacja po leczeniu
Efektywna kontrola chorych po leczeniu nowotworów jąder Marzena Wełnicka-Jaśkiewicz Klinika Onkologii i Radioterapii Gdańskiego Uniwersytetu Medycznego Efektywna kontrola ścisła obserwacja po leczeniu
Raki HPV (+) ustnej części gardła. Kiedy i jak deeskalować intensywność leczenia? Dr hab. n. med. Tomasz Rutkowski Lek. Dorota Księżniak-Baran
 Raki HPV (+) ustnej części gardła. Kiedy i jak deeskalować intensywność leczenia? Dr hab. n. med. Tomasz Rutkowski Lek. Dorota Księżniak-Baran Epidemiologia Chaturvedi et al. 2011 Epidemiologia Odsetek
Raki HPV (+) ustnej części gardła. Kiedy i jak deeskalować intensywność leczenia? Dr hab. n. med. Tomasz Rutkowski Lek. Dorota Księżniak-Baran Epidemiologia Chaturvedi et al. 2011 Epidemiologia Odsetek
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 173/2014 z dnia 7 lipca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego obejmującego
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 173/2014 z dnia 7 lipca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego obejmującego
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Mylan, 20 mg/1 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr koncentratu
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Docetaxel Mylan, 20 mg/1 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr koncentratu
Koncentrat jest przezroczystym, bezbarwnym lub jasnożółtym roztworem.
 1. NAZWA PRODUKTU LECZNICZEGO DOCETAXEL KABI, 180 mg/9 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml koncentratu zawiera 20 mg docetakselu (bezwodnego). Fiolka
1. NAZWA PRODUKTU LECZNICZEGO DOCETAXEL KABI, 180 mg/9 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml koncentratu zawiera 20 mg docetakselu (bezwodnego). Fiolka
Koncentrat jest przezroczystym, bezbarwnym lub jasnożółtym roztworem.
 1. NAZWA PRODUKTU LECZNICZEGO DOCETAXEL KABI, 160 mg/8 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml koncentratu zawiera 20 mg docetakselu (bezwodnego). Fiolka
1. NAZWA PRODUKTU LECZNICZEGO DOCETAXEL KABI, 160 mg/8 ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml koncentratu zawiera 20 mg docetakselu (bezwodnego). Fiolka
LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka
Załącznik B.14. LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka
Lublin, 26 maja, 2015 roku
 Lublin, 26 maja, 2015 roku Recenzja pracy doktorskiej lek. Iwony Kubickiej- Mendak pt. Ocena przyczyn niepowodzenia leczenia i ryzyka późnych powikłań brachyterapii LDR i HDR chorych na raka szyjki macicy
Lublin, 26 maja, 2015 roku Recenzja pracy doktorskiej lek. Iwony Kubickiej- Mendak pt. Ocena przyczyn niepowodzenia leczenia i ryzyka późnych powikłań brachyterapii LDR i HDR chorych na raka szyjki macicy
NOWE ZWIĄZKI PRZECIWNOWOTWOROWE Z GRUPY INHIBITORÓW KINAZY TYROZYNOWEJ EGFR STOSOWANE W TERAPII CELOWANEJ. Joanna Rozegnał
 NOWE ZWIĄZKI PRZECIWNOWOTWOROWE Z GRUPY INHIBITORÓW KINAZY TYROZYNOWEJ EGFR STOSOWANE W TERAPII CELOWANEJ Joanna Rozegnał TERAPIA CELOWANA: Jedna z najbardziej nowoczesnych metod leczenia nowotworów Skierowana
NOWE ZWIĄZKI PRZECIWNOWOTWOROWE Z GRUPY INHIBITORÓW KINAZY TYROZYNOWEJ EGFR STOSOWANE W TERAPII CELOWANEJ Joanna Rozegnał TERAPIA CELOWANA: Jedna z najbardziej nowoczesnych metod leczenia nowotworów Skierowana
