Estradiol i dydrogesteron w doustnej terapii hormonalnej okresu menopauzy
|
|
|
- Rafał Szewczyk
- 6 lat temu
- Przeglądów:
Transkrypt
1 Estradiol i dydrogesteron w doustnej terapii hormonalnej okresu menopauzy Estradiol together with dydrogesterone in oral hormonal therapy of the menopausal period Tomasz Pertyński, Grzegorz Stachowiak Klinika Ginekologii i Chorób Menopauzy, Instytut Centrum Zdrowia Matki Polki w Łodzi; kierownik Kliniki: prof. dr hab. med. Tomasz Pertyński Przegląd Menopauzalny 2008; 1: 1 8 Streszczenie Estradiol (E 2 ) i dydrogesteron są stosowane doustnie w terapii hormonalnej (HT) okresu menopauzy od wielu lat. Dostępne obecnie w Polsce preparaty E 2 z dydrogesteronem zapewniają wysoką skuteczność leczniczą zarówno w ciągłej (w tym niskodawkowej), jak i sekwencyjnej HT. To połączenie estrogenu z progestagenem charakteryzuje wyjątkowo korzystny profil farmakologiczny (z korzystnym wpływem na profil lipidowy, gospodarkę węglowodanową, ciśnienie tętnicze czy skórę) oraz wysoki stopień bezpieczeństwa terapeutycznego (wpływ na endometrium i profil krwawień macicznych oraz na tkanki sutka). Ten typ HT winien być jedną z podstawowych opcji terapeutycznych dla kobiet menopauzalnych wymagających leczenia hormonalnego. Słowa kluczowe: estradiol, dydrogesteron, doustna terapia hormonalna, menopauza Summary Estradiol (E 2 ) and dydrogesterone have been present in oral hormone therapy (HT) of the menopausal period for some years. E 2 /dydrogesterone preparations attainable in Poland at present show high therapeutic efficacy both as continuous (including low-dose) and sequential HT. This oestrogen-progestogen combination is characterized by an exceptionally advantageous pharmacological profile (with a favourable influence on lipid profile, carbohydrate metabolism, blood pressure or skin) and high therapeutic safety (an impact on endometrium, uterine bleeding profile and breast tissues). This type of HT should be one of the basic therapeutic options for menopausal women in need of hormonal treatment. Key words: estradiol, dydrogesterone, oral hormone therapy, menopause Mimo że istnieje wiele dróg podawania steroidów płciowych kobietom m.in. drogą przezskórną (plastry, żele), wziewną (inhalacje donosowe), dopochwową (globulki, tabletki i kremy dopochwowe, pierścienie pochwowe), za pomocą iniekcji domięśniowych, implantów podskórnych czy drogą domaciczną (wkładki domaciczne uwalniające hormony) to jedną z dwóch najpopularniejszych form terapii hormonalnej (ang. hormone therapy HT) okresu menopauzy pozostaje nadal tabletka doustna. Podany doustnie estradiol (E 2 podstawowy i najlepszy estrogen w doustnej HT), zanim dostanie się do krążenia ogólnego i osiągnie narząd docelowy, musi być wchłonięty w przewodzie pokarmowym, dostać się do krążenia wrotnego, a następnie do wątroby, by tam z jednej strony sam ulec częściowo przemianom metabolicznym (do krążenia ogólnego przechodzi tylko niewielka część podanej dawki), z drugiej zaś wpłynąć na zmiany metabolizmu komórek wątroby. Po zmetabolizowaniu w przewodzie pokarmowym i wątrobie E 2 przedostaje się do krążenia ogólnego głównie jako estron (E 1 ) i jego siarczan. Wzrost białka SHBG (ang. sex hormone binding globulin) po doustnym podaniu HT to kolejne ograniczenie biodostępności krążącego E 2. Jest to szczególnie widoczne podczas doustnej terapii za pomocą skoniugowanych estrogenów końskich (ang. conjugated equine estrogens CEE), indukującej wzrost stężeń tego białka wiążącego znacznie silniej Adres do korespondencji: prof. dr hab. med. Tomasz Pertyński, Klinika Ginekologii i Chorób Menopauzy, Instytut Centrum Zdrowia Matki Polki, ul. Rzgowska 281/289, Łódź 1
2 W¹troba 2 efekt pierwszego przejścia Krążenie ogólne gł. E 1, siarczan E 1, E 3 Narz¹dy docelowe 3 Drogi żółciowe gł. 16-glukuronid- -3-siarczan-E 3 Kr¹ enie w¹trobowo- -jelitowe Kr¹ enie wrotne Nerki gł. E 3 Jelito cienkie 1 4 1, 2, 3, 4 metabolizm E 2, m.in. sprzęganie z kwasem siarkowym i/lub glukuronowym, przemiana w E 3 (gł. wątroba) Ryc. 1. Metabolizm estradiolu doustna droga podania niż 17β-estradiol [1]. Schemat przemian E 2 po podaniu doustnym przedstawiono na ryc. 1. [2]. Efekt pierwszego przejścia przez wątrobę skutkuje wieloma zmianami metabolicznymi, charakterystycznymi dla doustnej HT. Zaliczyć do nich należy przede wszystkim spadek stężenia cholesterolu całkowitego, spadek stężenia frakcji LDL-cholesterolu, wzrost stężenia frakcji HDL-cholesterolu, wzrost stężenia trójglicerydów, korzystny wpływ na fibrynolizę ustrojową (głównie spadek aktywności i stężenia inhibitora plazminogenu 1 PAI-1), wzrost produkcji angiotensynogenu, wzrost stężenia E 1, wzrost stężenia SHBG, wzrost stężenia CBG (ang. corticosteroid-binding globulin), wzrost stężenia białka C-reaktywnego (ang. C-reactive protein CRP) [3]. Główne skutki metaboliczne obserwowane po doustnym podaniu estradiolu przedstawiono w tab. I [4]. Choć doustna HT wymaga większych niż przezskórna HT dobowych dawek estrogenów (w przypadku E 2 jest to dawka ok. 40 razy większa), a wiele efektów metabolicznych doustnego podania hormonu może być niekorzystnych dla kobiety po menopauzie (np. aktywacja układu RAA i możliwy wzrost ciśnienia tętniczego krwi warto podkreślić, że doustna HT obniża poziom cholesterolu (korzystnie modyfikując jego frakcje) silniej niż plastry oraz efektywniej pobudza fibrynolizę ustrojową, co może mieć istotne implikacje krążeniowe [5, 6]. Niezmiernie ważny w złożonej HT okresu menopauzy jest również wybór odpowiedniego progestagenu. Choć obecnie jedynym wskazaniem do stosowania wstawki progestagennej w ramach HT jest zabezpieczenie błony śluzowej jamy macicy przed rozrostami, a w konsekwencji przed rozwojem adenocarcinoma endometrii, to z jednej strony złożona problematyka stosowania HT u kobiet menopauzalnych (m.in. regulacja zaburzeń miesiączkowania w okresie przedmenopauzy i pomenopauzy, współwystępowanie rozrostów endometrium, endometriozy, mięśniaków macicy, łagodnych zmian sutka czy chorób sercowo-naczyniowych), z drugiej zaś obecność dodatkowych efektów metabolicznych stosowania danego progestagenu (m.in. wpływ na gospodarkę lipidową i węglowodanową oraz hemostazę) wymagają, by wybór ten pozwalał w możliwie najlepszy sposób na indywidualizację terapii i dostosowanie jej do potrzeb każdej pacjentki. Znalezienie (stworzenie) takiego idealnego progestagenu pozwoli uniknąć wielu działań ubocznych charakterystycznych dla tej grupy leków, będących pochodną ich aktywności androgennej, glikokortykoidowej i mineralokortykoidowej czy estrogenowej. Z wielu dostępnych danych wynika, że pomimo wprowadzania coraz doskonalszych progestagenów (np. drospirenonu) jednym z najlepszych (jeśli nie naj- 2
3 lepszym) związkiem z tej grupy leków pozostaje dydrogesteron. Wskazuje na to wyraźnie porównanie profili farmakologicznych dydrogesteronu z innymi progestagenami (tab. II). Dydrogesteron ponadto, podobnie jak szereg nowych progestagenów wprowadzanych obecnie do HT, takich jak np. drospirenon, octan nomegestrolu, promegeston, megeston, trimegeston czy nestoron, należy do grupy selektywnych modulatorów enzymów metabolizmu estrogenów (ang. selective estrogen enzyme modulators SEEM). Progestageny z tej grupy pobudzają aktywność sulfotransferazy w tkance gruczołu sutkowego, hamując jednocześnie aktywność sulfatazy, aromatazy i 17β-dehydrogenazy hydroksysteroidowej. Ten korzystny wpływ na aktywność układów enzymatycznych biorących udział w lokalnej biosyntezie estrogenów prowadzi do zmniejszenia kancerogennej puli hormonów w tkankach sutka [7]. Dydrogesteron w połączeniu z E 2, w ramach doustnej HT okresu menopauzy, jest obecnie dostępny na polskim rynku farmaceutycznym w 3 gotowych, złożonych preparatach hormonalnych: dla miesiączkujących kobiet menopauzalnych w cyklicznej HT tabletki zawierające 2 mg E 2 (przez pierwsze 14 dni) oraz 2 mg E 2 i 10 mg dydrogesteronu (od dnia cyklu) (opakowanie 28 tabl.), dla kobiet po menopauzie w ciągłej HT tabletki zawierające 2 mg E 2 i 10 mg dydrogesteronu (opakowanie 28 tabl.), dla kobiet po menopauzie jako ciągła, niskodawkowa HT tabletki zawierające 1 mg E 2 i 5 mg dydrogesteronu (opakowanie 28 tabl.). Estradiol w połączeniu z dydrogesteronem stosowany wg ww. trzech formuł dawkowania to skuteczna i, co równie ważne, bezpieczna forma leczenia dolegliwości oraz schorzeń okresu menopauzy. E 2 + dydrogesteron a nieprawid³owe krwawienia maciczne Występowanie (meno)metrorrhagia w trakcie stosowania HT jest jedną z głównych przyczyn niskiego compliance. W przypadku cyklicznej HT jest ważne, by charakterystyczne dla niej krwawienia z odstawienia były regularne, nieobfite i niedługie. Inną sprawą jest występowanie acyklicznych krwawień podczas hormonoterapii, mogących sugerować obecność patologii w obrębie endometrium. Cykliczna, doustna HT złożona z dydrogesteronu i E 2 charakteryzuje się dobrą kontrolą krwawień macicznych i niskim odsetkiem kobiet (1,06%) rezygnujących z niej z powodu nieprawidłowych krwawień. Częstość krwawień międzymiesiączkowych podczas tego typu terapii jest niska i oceniana na 4,6 9,8% na cykl, a ponad 60% kobiet nie ma ich w ogóle. Średnia Tab. I. Główne metaboliczne efekty doustnego E 2 [4] Parametr Doustna HT E 1 /E 2 5:1 cholesterol całkowity HDL LDL trójglicerydy aktywacja RAAS angiotensynogen czynnik VII krzepnięcia białko S AT III APCR PAI-1 F 1+2 D-dimery CRP NO IGT leptyna SHBG IGF-1 długość krwawienia wynosiła 5,5 dnia, a samo krwawienie pojawia się z dużą regularnością pomiędzy 13. a 14. dniem cyklu. W przypadku zastosowania jej u kobiet po menopauzie, regularne krwawienia powracają u 86 96% [8]. Jest to zgodne z częstością krwawień z odstawienia u kobiet letnich, występujących podczas innych typów cyklicznej HT [9]. W przypadku ciągłej, niskodawkowej HT złożonej z 1 mg E 2 i różnych dawek dydrogesteronu (5 20 mg/dobę) amenorrhoea po roku terapii utrzymuje się u 75 89% kobiet [10]. Ta dobra skuteczność kontroli krwawień przełomowych powoduje większą akceptację terapii przez pacjentki oraz zmniejsza ogólne koszty leczenia, redukując liczbę wykonywanych dodatkowo badań USG, biopsji aspiracyjnych, abrazji czy histeroskopii. E 2 + dydrogesteron a patologia endometrium Liczne badania epidemiologiczne dowiodły, że stosowanie samych estrogenów bez jednoczesnej substytucji progestagenowej u kobiet z zachowaną macicą daje re- 3
4 Tab. II. Profil farmakologiczny wybranych progestagenów Progestagen Działanie Działanie Działanie Działanie Działanie Działanie progestagenowe antyestrogenowe glukokortykoidowe androgenowe antyandrogenowe antymineralokortykoidowe dydrogesteron + + +/ +/ progesteron + + (+) + drospirenon lewonorgestrel + + (+) norgestimat + + +/ +/ dezogestrel + + +/ (+) megestrol octan nomegestrolu + + (+) + (+) NETA MPA / octan cyproteronu + + (+) + (+) działanie słabe; +/ działanie niepewne zultat w postaci wzrostu ryzyka hiperplazji i raka endometrium [11]. Progestageny wywierają bowiem antyproliferacyjny efekt na błonę śluzową trzonu macicy, poddaną uprzednio działaniu estrogenów, przekształcając proliferacyjnie zmienioną tkankę w amitotyczne, wydzielnicze endometrium [12]. Zastosowanie progestagenów w HT zmniejsza ryzyko hiperplazji i raka błony śluzowej macicy [13]. Doustny progestagen, aby zrównoważyć mitogenny wpływ estrogenu w ciągłej hormonoterapii, musi być podawany codziennie, natomiast w cyklicznej HT przez dni drugiej fazy cyklu [14]. Potwierdzeniem ochronnego wpływu progestagenów na endometrium jest brak mitotycznej aktywności komórek cew gruczołowych w większości z poddanych ocenie histologicznej fragmentów błony śluzowej jamy macicy, pobranych w trakcie takich zabiegów diagnostycznych, jak biopsja pipelle, D&C (ang. dilation and curettage) czy histeroskopia [15]. Trzeba wiedzieć, że HT redukuje, lecz nie eliminuje całkowicie występowania hiperplazji lub raka endometrium [11]. Częstość występowania rozrostu prostego endometrium w trakcie rocznej HT (zarówno cyklicznej, jak i ciągłej) u kobiet z zachowaną macicą jest oceniana odpowiednio na 20% i poniżej 1% [16]. Co więcej, ten korzystny wpływ HT na endometrium utrzymuje się w kolejnych latach terapii. W ciągu 3 lat badania Postmenopausal Estrogen/Progestin Interventions Trial (PEPI Trial) hiperplazję endometrium stwierdzono u mniej niż 1% kobiet przyjmujących HT złożoną z CEE i mikronizowanego progesteronu lub octanu medroksyprogesteronu (MPA), podczas gdy w grupie stosującej wyłącznie CEE aż w 62% przypadków. Należy także podkreślić, że w badaniu tym w grupie kobiet stosujących HT nie było żadnego przypadku rozrostu atypowego, podczas gdy w grupie otrzymującej same estrogeny częstość rozrostu atypowego wynosiła 12% [17]. Także dydrogesteron jest progestagenem skutecznie zabezpieczającym kobiety stosujące HT przed patologią endometrium w trakcie 12 mies. doustnej HT złożonej z E 2 i dydrogesteronu rozrost prosty endometrium został wykryty u 1 ze 146 kobiet (0,7%). U kolejnych 3 kobiet (2,1%) stwierdzono endometrium proliferacyjne, natomiast pozostała grupa (97,2%) charakteryzowała się amitotycznym/wydzielniczym lub atroficznym endometrium [18]. E 2 + dydrogesteron a problematyka raka sutka Wp³yw na insulinopodobny czynnik wzrostu 1 Jest to peptyd strukturalnie i czynnościowo podobny do insuliny. Większość insulinopodobnego czynnika wzrostu 1 (ang. insuline-like growth factor-1 IGF-1) w krążeniu jest pochodzenia wątrobowego, a jego synteza jest stymulowana przez hormon wzrostu (ang. growth hormone GH). Pomiędzy IGF-1 a GH występuje mechanizm ujemnego sprzężenia zwrotnego, a wiele badań populacyjnych dowodzi, iż oś hormonalna IGF-1/GH ma związek z ryzykiem raka sutka [19]. Insulinopodobny czynnik wzrostu 1 jest silnym mitogenem dla komórek raka sutka. Jego wysokie poziomy w krążeniu są związane ze zwiększonym ryzykiem raka sutka u kobiet w okresie premenopauzy [20]. Biodostępność IGF-1 w tkankach jest regulowana przez peptydy wiążące IGF (ang. IGF-binding protein 4
5 IGFPB). Uważa się, że połączony efekt działania E 2 i IGF-1 może stymulować proliferację prawidłowych komórek nabłonkowych i prowadzić do wzrostu ryzyka raka sutka [19]. Estrogenoterapia zmniejsza aktywność krążącego IGF-1 poprzez hamowanie jego syntezy w wątrobie oraz zwiększenie poziomu IGFPB-1, przy czym doustna droga podania hormonów ma większy wpływ na syntezę wątrobową tego białka niż droga przezskórna [21]. Połączenie dydrogesteronu z E 2 w doustnej HT korzystnie obniża poziom IGF-1, niezależnie od jego poziomów wyjściowych. Zjawiska tego nie obserwuje się natomiast w trakcie przezskórnej HT, złożonej z E 2 i octanu noretisteronu (NETA), a w grupie z niskimi wyjściowymi poziomami IGF-1 dochodzi nawet do wzrostu stężenia IGF-1 w trakcie terapii [22]. Octan noretisteronu i MPA przyjmowane w ramach doustnej HT, odmiennie niż dydrogesteron, zmniejszają korzystny wpływ estrogenów na IGF-1 [23]. Wp³yw na bia³ko SHBG Jest to białko nośnikowe dla steroidów płciowych we krwi, a jego stężenie w surowicy reguluje poziomy wolnej frakcji androgenów i estradiolu oraz dostęp tych hormonów do tkanek docelowych. Zaobserwowano związek pomiędzy niskim stopniem wiązania E 2 z SHBG (i niewielkim wzrostem jego wolnej frakcji) a wzrostem częstości raka sutka u kobiet po menopauzie [24]. Wykazano, że oprócz pełnienia funkcji nośnikowej, SHBG łączy się z komórkami tkanek estrogenozależnych [25]. SHBG poprzez aktywację camp hamuje indukowaną przez E 2 proliferację komórek w estrogenozależnym raku sutka [26]. Białko to można uznać za czynnik spustowy, który aktywuje antyestrogenową ścieżkę metaboliczną organizmu. Doustna estrogenoterapia stymuluje, w wyniku efektu pierwszego przejścia, produkcję SHBG w wątrobie, natomiast E 2 podawany przezskórnie nie powoduje wzrostu stężeń tego białka [27]. Progestageny nadające aktywność androgenną zmniejszają korzystny wpływ doustnej HT na poziom SHBG [28]. Efektu takiego nie obserwuje się natomiast w przypadku dydrogesteronu podanie kobietom doustnej, cyklicznej HT złożonej z tego progestagenu i E 2 powoduje znaczący, szybki wzrost stężeń SHBG, którego brak przy przezskórnej HT (E 2 + NETA) [22]. Wp³yw na podzia³y komórkowe i procesy apoptozy Badania epidemiologiczne na dużych populacjach dowiodły niewątpliwego udziału estrogenów w kancerogenezie raka sutka, natomiast ciągle brak jest jasnych danych dotyczących ryzyka wystąpienia tego nowotworu podczas złożonej estrogenowo-progestagenowej HT [29]. Wyniki dostępnych badań nie są jednoznaczne, a część z nich nadal jest w toku [30, 31]. Główne przyczyny takiego stanu to niehomogenne (i trudne do porównania ze sobą) populacje badanych kobiet oraz wielka różnorodność dawek i typów stosowanych hormonów [32]. Z badań in vivo wynika, że komórki nabłonkowe sutka ulegają proliferacji pod wpływem przezskórnej ekspozycji na estradiol, dodanie zaś progesteronu zmniejsza liczbę podziałów komórkowych [33]. Wzrasta też zainteresowanie badaniami in vitro dotyczącymi stymulacji za pomocą steroidów płciowych określonych linii komórkowych raka sutka, które mają bądź nie receptory dla estrogenów. Linią zawierającą receptory estrogenowe (ER+) są komórki MCF-7, natomiast linia raka sutka o nazwie MDA-MB-231 jest ich pozbawiona (ER ). W jednym z takich badań [34] inkubowano komórki obu linii raka sutka z wieloma różnymi związkami chemicznymi, takimi jak dihydrodydrogesteron (główny metabolit dydrogesteronu), E 2, tamoksyfen i cyklofosfamid, oceniając parametry dojrzewania komórkowego (ekspresję mucyny 1), proliferacji (ekspresję cykliny D1) i apoptozy (utratę jądrowego DNA). Ekspresja mucyny 1, proteiny obecnej w komórkach nabłonka gruczołowego, jest nasilona w przypadku wysoko zróżnicowanych komórek nowotworów złośliwych. Wzrost ekspresji mucyny 1 w komórkach raka sutka ER+ obserwowano w przypadku inkubacji z samym E 2 oraz kompleksem tamoksyfen/e 2 /dihydrodydrogesteron, a w komórkach ER podczas inkubacji z kompleksem E 2 /dydrodydrogesteron oraz tamoksyfen/e 2 /dihydrodydrogesteron, co sugeruje korzystny wzrost stopnia dojrzałości tych komórek. Cyklina D1 odgrywa ważną rolę w powstawaniu raka sutka, jest proteiną komórek nabłonka przewodów wyprowadzających. Jej zwiększona ekspresja jest obserwowana w ok. 50% przypadków raka sutka, a nadprodukcja w znamienny sposób koreluje z syntezą estrogenów w tkance guza. Cyklina D1 to znany efektor działania estrogenów w komórkach raka sutka. W komórkach linii MCF-7 synteza mrna cykliny D1 jest indukowana przez estrogeny w ciągu 4 godz. Wykazano, że myszy pozbawione cykliny D1 są odporne na raka sutka indukowanego przez szczurze onkogeny neu i ras [35]. W omawianym badaniu najwyższą ekspresję cykliny D1 w komórkach ER+ stwierdzono po 48 godz. inkubacji w kompleksie tamoksyfen/e 2 /dihydrodydrogesteron, natomiast w przypadku komórek ER najniższa ekspresja tej proteiny była obserwowana po 24 godz. inkubacji w kompleksie E 2 /dihydrodydrogesteron. Oceniano również zależność pomiędzy proliferacją a apoptozą. Najwyższy wskaźnik apoptoza/proliferacja (sugerujący regresję nowotworu) zarówno w komórkach ER+, jak i ER, obserwowano po 144 godz. inkubacji w przypadku tamoksyfenu, który od lat uważany jest za jeden z najsilniejszych reduktorów linii komórkowych raka sutka in vitro. Wzrost tego wskaźnika był obserwowany również w przypadku inkubacji komórek ER+ z kompleksem E 2 /dihydrodydrogesteron (jak się można było spodziewać, zjawisko to nie występowało w trakcie inkubacji z komórkami ER ). W innym badaniu in vitro, porównując wpływ różnych progestagenów i E 2 na apoptozę i proliferację komórek MCF-7 raka sutka, stwierdzono 5
6 (po 144 godz. inkubacji), że stosunek apoptoza/proliferacja jest >1 dla progesteronu, =1 dla dihydrodydrogesteronu, natomiast dla pozostałych badanych progestagenów (MPA, NETA, dienogestu) i 17β-estradiolu <1 (dominacja procesów proliferacyjnych). Co ciekawe, w przypadku inkubacji komórek MCF-7 w środowisku estrogenowo-progestagenowym, najwyższy (i jedyny >1) wskaźnik apoptoza/proliferacja uzyskano w przypadku połączenia E 2 z dihydrodydrogesteronem; dla kombinacji E 2 + progesteron wskaźnik ten wynosił 1, a w pozostałych przypadkach (E 2 + MPA, E 2 + NETA i E 2 + dienogest) był <1 [36]. Przytoczone powyżej dane sugerują, że pewne kombinacje estrogenów i progestagenów stosowane w HT, w tym przede wszystkim doustna hormonoterapia złożona z dydrogesteronu i E 2, mogą wykazywać więcej korzyści niż szkód w działaniu na tkanki sutka oraz rozwój i przebieg raka tego narządu. E 2 + dydrogesteron a problem osteoporozy pomenopauzalnej Według danych WHO ryzyko złamań kostnych u kobiet, które nigdy nie stosowały HT, jest o 100% większe w porównaniu z kobietami stosującymi terapię hormonalną [37]. Od dawna wiadomo, że zastosowanie samych estrogenów korzystnie wpływa na gęstość tkanki kostnej, zapobiegając, a nawet odwracając proces utraty masy tkanki kostnej u kobiet po menopauzie, natomiast konieczność podawania progestagenów może wiązać się z pojawieniem wielu działań niepożądanych, które minimalizują bądź znoszą wpływ estrogenów na dany narząd docelowy [38]. W przypadku dydrogesteronu doustna HT złożona z tego progestagenu i E 2 korzystnie wpływa na metabolizm i gęstość mineralną kości (ang. bone mineral density BMD) w ciągu 6 mies. ciągłej HT złożonej z 2 mg E 2 i dydrogesteronu (w czterech różnych dawkach 2,5 mg, 5 mg, 10 mg i 15 mg) doszło do zahamowania procesów resorpcji w tkance kostnej [39]. Również w przypadku preferowanej obecnie terapii niskodawkowej, E 2 w dawce 1 mg w połączeniu z dydrogesteronem (dawki dobowe 5 mg, 10 mg i 20 mg) spowodował statystycznie znamienny wzrost BMD odcinka lędźwiowego kręgosłupa u kobiet po menopauzie wzrost o 2,4% po 6 mies. i o 3,6% po roku terapii [10]. Wykazany brak zależności pomiędzy dobową dawką dydrogesteronu a uzyskanymi zmianami w parametrach resorpcji kostnej i BMD (zarówno w terapii niskodawkowej, jak i przy stosowaniu 2 mg E 2 dziennie) świadczy o neutralnym wpływie tego progestagenu na metabolizm kostny. Z drugiej strony, skuteczność niskodawkowej HT zawierającej ten progestagen w podwyższaniu BMD kobiet menopauzalnych pozwala na zmniejszenie częstości objawów ubocznych związanych z doustnym przyjmowaniem estrogenów, co jest szczególnie pożądane w grupie kobiet po 60. roku życia. E 2 + dydrogesteron a gospodarka lipidowa Estrogenoterapia u kobiet w okresie menopauzy pozytywnie wpływa na ich profil lipidowy, redukując stężenie cholesterolu całkowitego, zmniejszając stężenie frakcji LDL-cholesterolu oraz podnosząc stężenie frakcji HDL-cholesterolu [40]. Ponieważ jednak u większości kobiet ze względu na obecność endometrium stosowanie samych estrogenów nie jest możliwe, by utrzymać antyaterogenny efekt leczniczy klasycznej HT, dodany progestagen nie powinien znosić korzystnego wpływu estrogenu na lipidy. Aby osiągnąć ten cel, składowa progestagenna HT powinna charakteryzować się możliwie małym efektem androgenowym. Właściwości takie ma dydrogesteron [41]. Cykliczna HT złożona z E 2 i dydrogesteronu (podawanego przez 14 dni w drugiej fazie 28-dniowego cyklu) wywiera korzystny, podobny do estrogenoterapii, wpływ na profil lipidowy [42]. Ciągła HT zawierająca standardową dawkę 2 mg E 2 w połączeniu z różnymi dawkami dydrogesteronu 2,5 15 mg spowodowała już po 3 mies. redukcję stężeń cholesterolu całkowitego, frakcji LDL-cholesterolu i Apo B z towarzyszącym wzrostem stężeń frakcji HDL-cholesterolu iapo A 1. Te korzystne zmiany utrzymały się w kolejnych 3 mies. terapii [39]. Dydrogesteron w porównaniu ze stosowanym powszechnie w naszym kraju w HT octanem medroksyprogesteronu ma zdecydowanie korzystniejszy wpływ na profil lipidowy [43]. Należy o tym zawsze pamiętać, mając na względzie ryzyko wystąpienia powikłań sercowo-naczyniowych podczas HT. Doustna HT złożona z 2 mg E 2 i 10 mg dydrogesteronu okazała się mieć korzystniejszy wpływ na lipidy osocza od hormonoterapii złożonej z 50 µg transdermalnego E 2 wpołączeniu z 10 mg dydrogesteronu oraz od 2,5 mg tibolonu [44]. Porównując wpływ na profil lipidowy dwóch różnych typów cyklicznej HT (doustny E 2 z dydrogesteronem oraz przezskórny E 2 + NETA), stwierdzono, że korzystniej działa tu terapia doustna (spadek stężeń cholesterolu całkowitego i frakcji LDL-cholesterolu, wzrost stężenia frakcji HDL-cholesterolu, brak zmian w stężeniu trójglicerydów) niż przezskórna (spadek stężeń cholesterolu całkowitego i frakcji LDL-cholesterolu, brak zmian w stężeniu frakcji HDL-cholesterolu i trójglicerydów) [22]. Rezultaty ostatnich badań koncentrują się na zastosowaniu dydrogesteronu w niskodawkowej HT. Ich wyniki świadczą, że w przypadku łączenia 1 mg E 2 z różnymi dawkami tego progestagenu (2,5 mg, 5 mg, 10 mg i 20 mg) w ciągłej doustnej HT dochodzi do spadku stężeń cholesterolu całkowitego (redukcja o 4,6 7,6%) i frakcji LDL-cholesterolu (redukcja o 6,3 11,6%) oraz wzrostu stężeń frakcji HDL-cholesterolu (o 4,3 7,4%), apolipoprotein A 1 i B [45]. Podawanie kobietom w okresie menopauzy doustnej ciągłej HT złożonej z E2 i różnych dawek dydrogesteronu (dawka dzienna 2,5 15 mg) powoduje także spadek stężenia Lp(a) [46]. Lipoproteina (a) poprzez swoje strukturalne podobieństwo do plazminogenu konkuruje z nim o miej- 6
7 sca wiązania na włóknach fibryny, a w przypadku dużych stężeń może zmniejszać możliwość wiązania plazminogenu z fibryną. W konsekwencji doprowadza to do osłabienia generowania plazminy, co sprzyja rozwojowi zakrzepicy [47 49]. Dydrogesteron jako progestagenna składowa zarówno cyklicznej, jak i ciągłej HT jest więc dobrą alternatywą dla innych progestagenów, a o jego zastosowaniu należy pamiętać zawsze przy rozpoczynaniu leczenia hormonalnego w grupie kobiet menopauzalnych ze zwiększonym ryzykiem chorób układu krążenia. E 2 + dydrogesteron a gospodarka wêglowodanowa Ciągła, doustna HT złożona z 2 mg E 2 /dobę w połączeniu z 10 mg dydrogesteronu/dobę u kobiet po menopauzie powoduje w ciągu 12 mies. redukcję stężeń glukozy na czczo (p<0,05), zmniejsza poposiłkowe stężenie insuliny (p<0,05), jak również, choć niezamiennie statystycznie, redukuje stężenia (poposiłkowe i na czczo) GLP-1 (ang. glucagon-like peptide-1). Doustna HT znacząco wpływa więc na enteroinsularną oś kobiet menopauzalnych, przyczyniając się do normalizacji poziomów glukozy w surowicy [50]. E 2 + dydrogesteron a nadciœnienie têtnicze Stosowanie przez rok cyklicznej, niskodawkowej HT złożonej z 1 mg E 2 i 10 mg dydrogesteronu (w drugiej fazie cyklu) u zdrowych kobiet menopauzalnych (n=44), z prawidłowym ciśnieniem tętniczym spowodowało znamienny statystycznie spadek ambulatoryjnego skurczowego ciśnienia tętniczego krwi (średnio o 5,4 mm Hg; p<0,01) oraz średniego, dziennego skurczowego ciśnienia tętniczego krwi (średnio o 6,6 mm Hg; p<0,001), przy braku zmian RR w grupie kontrolnej (n=36) [51]. W innym badaniu po roku stosowania HT (2 mg/dobę E mg dydrogesteronu przez 12 dni każdego cyklu) doszło do znamiennego statystycznie spadku zarówno średniego ciśnienia tętniczego krwi, jak również spadku stężeń amin katecholowych adrenaliny i noradrenaliny i wzrostu stężeń nitratów we krwi zdrowych kobiet po menopauzie [52]. Również w przypadku stosowania niskodawkowej HT (1 mg E mg dydrogesteronu przez 14 dni drugiej fazy cyklu) w grupie kobiet z nadciśnieniem tętniczym odnotowano korzystny spadek zarówno średniego ciśnienia tętniczego (o 2,2±0,6 mm Hg; p<0,001), jak i nocnego ciśnienia skurczowego (o 3,0±1,5 mm Hg; p<0,001) oraz ciśnienia rozkurczowego krwi (o 2,0±0,8 mm Hg; p<0,001) [53]. E 2 + dydrogesteron a problem starzenia siê skóry Mimo że proces starzenia się skóry nie jest wskazaniem do zastosowania systemowej HT, to dostępne dane świadczą o wyraźnej poprawie parametrów związanych z tym procesem w trakcie leczenia hormonalnego po 7 cyklach sekwencyjnej HT złożonej z E 2 (2 mg/dobę) i dydrogesteronu (10 mg/dobę od dnia cyklu), zastosowanych u 40 kobiet menopauzalnych, stwierdzono znamienną poprawę elastyczności i uwodnienia skóry (odpowiednio na żuchwie i ramieniu), jak również zwiększenie jej grubości [54]. E 2 + dydrogesteron a objawy wazomotoryczne Kończąc rozważania dotyczące doustnych HT zawierających E 2 i dydrogesteron, należy podkreślić wysoką skuteczność tych terapii w zwalczaniu nasilonych objawów wypadowych okresu menopauzy, będących jak wiadomo podstawowym wskazaniem do zastosowania każdego typu HT. Również w przypadku niskodawkowej, sekwencyjnej HT (1 mg E 2 /dobę + 10 mg dydrogesteronu w II fazie) osiągana jest znacząca poprawa (p=0,001) objawów klimakterycznych 86%, redukcja uderzeń gorąca po 6 cyklach leczniczych (m.in. spadek punktacji w skali Greena, korzystna opinia samych pacjentek o terapii, poprawa jakości ich życia), identyczny, jak w przypadku HT złożonej z CEE (0,625 mg/dobę!) i norgestrelu (0,15 mg/dobę), przy korzystniejszym wpływie na profil lipidowy (wzrost HDL przy E 2 /dydrogesteron, spadek przy CEE/norgestrel) [55]. Podsumowując, wybór doustnej HT złożonej z estradiolu i dydrogesteronu to dobra i bezpieczna opcja terapeutyczna dla wielu kobiet menopauzalnych wymagających leczenia hormonalnego. Piśmiennictwo 1. Yilmazer M, Fenkci V, Fenkci S, et al. Hormone replacement therapy, C-reactive protein, and fibrinogen in healthy postmenopausal women. Maturitas 2003; 46: Lievertz RW. Pharmacology and pharmacokinetics of estrogens. Am J Obstet Gynecol 1987; 156: Bahvanani B. Pharmacology of hormonal therapeutic agents in the menopause comprehensive management. In: The Menopause Comprehensive Management. Eskin BA (ed). The Partenon Publishing Group, New York Crook D. The metabolic consequences of treating postmenopausal women with non-oral hormone replacement therapy. Br J Obstet Gynaecol 1997; 104 (suppl. 16): Corson SL. A decade of experience with transdermal estrogen replacement therapy: overview of key pharmacologic and clinical findings. Int J Fertil 1993; 38: Boyd RA, Zegarac EA, Eldon MA, et al. Pharmacokinetic characterization of 7-day 17β-estradiol transdermal delivery system In healthy postmenopausal women. Pharm Res 1993; 10: S Pasqualini JR. Differential effects of progestins on breast tissue enzymes. Maturitas 2003; 46 (suppl. 1): S Frenczy A, Gelfand MM. Endometrial histology and bleeding patterns in post-menopausal women taking sequential, combined estradiol and dydrogesterone. Maturitas 1997; 26: Bewtra C, Kable WT, Gallagher JC, et al. Endometrial histology and bleeding patterns in menopausal women treated with estrogen and continuous or cyclic progestin. J Reprod Med 1988; 33:
8 10. Stevenson JC, Teter P, Lees B. 17β-estradiol (1 mg/day) continuously combined with dydrogesterone (5, 10 or 20 mg/day) increases bone mineral density in postmenopausal women. Maturitas 2001; 38: Grady D, Gebretsadlk T, Kerlikowske K, et al. Hormone replacement therapy and endometrial risk: a meta-analysis. Obstet Gynecol 1995; 85: Ferenczy A. Anatomy and histology of the uterine corpus. In: Blaustein s Pathology of the Female Genital Tract. Kurman RJ (ed.). Springer-Verlag, New York 1994; Harlap S. The benefits and risk of hormone replacement therapy: an epidemiologic overview. Am J Obstet Gynecol 1992; 166: Cust MP, Hangar KF, Hillard TC, et al. A risk benefit assessment of estrogen therapy in post-menopausal women. Drug Safety 1990; 5: Moyer DL, de Lingeries B, Driguez P, et al. Prevention of endometrial hyperplasia by progesterone during long-term estradiol replacement: influence of bleeding pattern and secretory changes. Fertil Steril 1993; 59: Woodruff JD, Piekar JH for the Menopause Study Group. Incidence of endometrial hyperplasia in post-menopausal women taking conjugated estrogens (Premarin) with medroxyprogesterone acetate or conjugated estrogens alone. Am J Obstet Gynecol 1994; 170: The Post-menopausal Estrogen/Progestin Interventions (PEPI) Trial. Effects of hormone replacement therapy on endometrial histology in post-menopausal women. J Am Med Assoc 1996; 275: Frenczy A, Gelfand MM. Endometrial histology and bleeding patterns in post-menopausal women taking sequential, combined estradiol and dydrogesterone. Maturitas 1997; 26: Pollak M. Insulin-like growth factor physiology and cancer risk. Eur J Cancer 2000; 36: Hankinson SE, Willett WC, Colditz GA, et al. Circulating concentrations of insulin-like growth factor-i and risk of breast cancer. Lancet 1998; 351: Carmina E, Lo Dico F, Carollo F, et al. Serum IGF-I and binding proteins 1 and 3 in postmenopausal women and the effects of estrogen. Menopause 1996; 3: Campagnoli C, Colombo P, De Aloysio D, et al. Positive effects on cardiovascular and breast metabolic markers of oral estradiol and dydrogesterone in comparison with transdermal estradiol and norethisterone acetate. Maturitas 2002; 41: Campagnoli C, Biglia N, Lanza MG, et al. Androgenic progestogens oppose the decrease of insulin-like growth factor I serum level induced by conjugated oestrogens in postmenopausal women. Preliminary report. Maturitas 1994; 19: Nachtigall LE. Sex hormone-binding globulin and breast cancer risk. Prim Care Up-date Ob/Gyns 1999; 6: Fortunati N. Sex hormone-binding globulin: not only a transport protein. What news is around the corner. J Endocrinol Invest 1999; 22: Fortunati N, Fissore F, Fazzari A, et al. Estradiol induction of camp in breast cancer cells mediated by foetal calf serum (FCS) and sex hormone-binding globulin (SHBG). J Steroid Biochem Mol Biol 1999; 70: Campagnoli C, Biglia N, Altare F, et al. Differential effects of oral conjugated estrogens and transdermal estradiol on insulin-like growth 1, growth hormone and sex hormone binding globulin levels. Gynaecol Endocrinol 1993; 7: Miller VT, Muesing RA, LaRosa JC, et al. Effects of conjugated equine estrogens with and without three different progestogens on lipoproteins, high-density lipoprotein subfractions, and apolipoprotein A-1. Obstet Gynecol 1991; 77: Collaborative Group on Hormonal Factors in Breast Cancer, Breast cancer and hormone replacement therapy: collaborative reanalysis of data from 51 epidemiological studies of women with breast cancer and women without breast cancer. Lancet 1997; 350: Magnusson C, Baron JA, Correia R, et al. Breast-cancer risk following long-term oestrogen- and oestrogen-progestin replacement therapy. Int J Cancer 1999; 81: O Meara ES, Rossing MA, Daling JR, et al. Hormone replacement therapy after a diagnosis of breast cancer in relation to recurrence and mortality. J Natl Cancer Inst 2001; 93: Genazziani AR, Gadducci A, Gambacciani M. Controversial issues in climacteric medicine II: hormone replacement therapy and cancer. Climacteric 2001; 4: Chang KJ, Lee TT, Linares-Cruz G, et al. Influences of percutaneous administration of estradiol and progesterone on human breast epithelial cell cycle in vivo. Fertil Steril 1995; 63: Franke HR, Kole S, Ciftci Z, et al. In vitro effects of estradiol, dydrogesterone, tamoxifen and cyclophosphamide on proliferation vs. death in human breast cancer cells. Cancer Lett 2003; 190: Yu Q, Geng Y, Sicinski P. Specific protection against breast cancers by cyklin D 1 ablation. Nature 2001; 411: Franke HK, Hermes I. Differential effects of progestogens on breast cancer lines. Maturitas 2003; 46 (suppl 1): S World Health Organisation. Assessment of fracture risk and its application to screening for postmenopausal osteoporosis. WHO Technical Report Series 843, Hormone replacement therapy. Clinical Synthesis Panel on HRT. Lancet 1999; 354: Voetberg GA, Netelenbos JC, Kenemans P, et al. Estrogen replacement therapy continuously combined with four different dosages of dydrogesterone: effect on calcium and lipid metabolism. J Clin Endocrinol Metab 1994; 79: Lobo RA, Speroff L. International consensus conference on postmenopausal hormone therapy and the cardiovascular system. Fertil Steril 1994; 61: Tausk M. A general summary of dydrogesterone, a derivative of retroprogesterone. In: International encyclopaedia of pharmacology and therapeutics. Tausk M (ed.). Vol. II. Pergamon Press, Oxford, New York 1972; Gelfand M, Fugere P, Bissonnette F. Cardiovascular risk factors during sequentially combined 17β-estradiol and dydrogesterone (Femoston): results from a one-year study in post-menopausal women. Maturitas 1997; 26: Gelfand M, Fugere P, Bissonnette F, et al. Conjugated estrogens combined with sequential dydrogesterone or medroxyprogesterone acetate in postmenopausal women: effects on lipoproteins, glucose tolerance, endometrial histology, and bleeding. Menopause 1997; 4: Hänggi W, Lippuner K, Riesen W, et al. Long-term influence of different postmenopausal hormone replacement regimens on serum lipids and lipoprotein (a): a randomised study. Br J Obstet Gynaecol 1997; 104: Pornel B, Chevallier O, Netelenbos JC. Oral 17β-estradiol (1 mg) continuously combined with dydrogesterone improves the serum lipid profile of postmenopausal women 46. Mijatovic V, Kenemans P, Netelenbos JC, et al. Oral 17β-estradiol continuously combined with dydrogesterone lowers serum lipoprotein (a) concentrations in healthy postmenopausal women. J Clin Endocrinol Metab 1997; 82: Aznar J, Estelles A, Breto M, et al. Euglobin clot lysis induced by tissue-type plasminogen activator is reduced in subjects with increased levels of lipoprotein (a). Thromb Res 1992; 66: Edelberg JM, Pizzo SV. Lipoprotein (a): the link between impaired fibrinolysis and atherosclerosis. Fibrynolysis 1991; 5: Kim SW et al. Prevalence of deep venous thrombosis in patients with chronic spinal cord injury. Arch Phys Med Rehabil 1994; 75: Sztefko K, Rogatko I, Milewicz T, et al. Effect of hormone therapy on the enteroinsular axis. Menopause 2005; 12: Kaya C, Dinçer Cengiz S, Cengiz B, Akgün G. Long-term effects of low-dose 17beta-estradiol plus dydrogesterone on 24-h ambulatory blood pressure in healthy postmenopausal women: A 1-year, randomized, prospective study. Gynecol Endocrinol 2007; 23 (suppl. 1): Maffei S, Mercuri A, Prontera C, et al. Vasoactive biomarkers and oxidative stress in healthy recently postmenopausal women treated with hormone replacement therapy. Climacteric 2006; 9: Kaya C, Dinçer Cengiz S, Cengiz B, Akgün G. The long-term effects of low-dose 17beta-estradiol and dydrogesterone hormone replacement therapy on 24-h ambulatory blood pressure in hypertensive postmenopausal women: a 1-year randomized, prospective study. Climacteric 2006; 9: Sator PG, Sator MO, Schmidt JB, et al. A prospective, randomized, double-blind, placebo-controlled study on the influence of a hormone replacement therapy on skin aging in postmenopausal women. Climacteric 2007; 10: Cieraad D, Conradt C, Jesinger D, Bakowski M. Clinical study comparing the effects of sequential hormone replacement therapy with oestradiol/dydrogesterone and conjugated equine oestrogen/norgestrel on lipids and symptoms. Arch Gynecol Obstet 2006; 274:
PROGESTAGENY W HORMONALNEJ TERAPII ZASTĘPCZEJ
 PROGESTAGENY W HORMONALNEJ TERAPII ZASTĘPCZEJ Rekomendacje w zakresie stosowania progestagenów w hormonalnej terapii zastępczej opracował na posiedzeniu w dniach 14/15.07.2006r. w Gdańsku Zespół Ekspertów
PROGESTAGENY W HORMONALNEJ TERAPII ZASTĘPCZEJ Rekomendacje w zakresie stosowania progestagenów w hormonalnej terapii zastępczej opracował na posiedzeniu w dniach 14/15.07.2006r. w Gdańsku Zespół Ekspertów
Niskie dawki w terapii hormonalnej okresu menopauzy
 Niskie dawki w terapii hormonalnej okresu menopauzy Low doses in hormone therapy of the menopausal period Tomasz Pertyński, Grzegorz Stachowiak Klinika Ginekologii i Chorób Menopauzy Instytutu Centrum
Niskie dawki w terapii hormonalnej okresu menopauzy Low doses in hormone therapy of the menopausal period Tomasz Pertyński, Grzegorz Stachowiak Klinika Ginekologii i Chorób Menopauzy Instytutu Centrum
Terapia Hormonalna Wieku Menopauzalnego. Klinika Endokrynologii Ginekologicznej Warszawski Uniwersytet Medyczny
 Terapia Hormonalna Wieku Menopauzalnego Klinika Endokrynologii Ginekologicznej Warszawski Uniwersytet Medyczny Rekomendacje PTG w sprawie stosowania HT HT nie może być stosowana u wszystkich kobiet w okresie
Terapia Hormonalna Wieku Menopauzalnego Klinika Endokrynologii Ginekologicznej Warszawski Uniwersytet Medyczny Rekomendacje PTG w sprawie stosowania HT HT nie może być stosowana u wszystkich kobiet w okresie
Spodziewany efekt kliniczny wpływu wit. K na kość
 Rola witaminy K2 w prewencji utraty masy kostnej i ryzyka złamań i w zaburzeniach mikroarchitektury Ewa Sewerynek, Michał Stuss Zakład Zaburzeń Endokrynnych i Metabolizmu Kostnego Uniwersytetu Medycznego
Rola witaminy K2 w prewencji utraty masy kostnej i ryzyka złamań i w zaburzeniach mikroarchitektury Ewa Sewerynek, Michał Stuss Zakład Zaburzeń Endokrynnych i Metabolizmu Kostnego Uniwersytetu Medycznego
Klinika Endokrynologii Ginekologicznej WUM
 Klinika Endokrynologii Ginekologicznej WUM } Objawy menopauzalne umiarkowane i nasilone } Objawy atrofii urogenitalnej } Pierwotna niedoczynność jajników: przedwczesna i wczesna menopauza (do co najmniej
Klinika Endokrynologii Ginekologicznej WUM } Objawy menopauzalne umiarkowane i nasilone } Objawy atrofii urogenitalnej } Pierwotna niedoczynność jajników: przedwczesna i wczesna menopauza (do co najmniej
Czym siê kierowaæ w doborze progestagenu do terapii hormonalnej wieku menopauzalnego?
 Czym siê kierowaæ w doborze progestagenu do terapii hormonalnej wieku menopauzalnego? How to choose a progestogen for hormone therapy of the menopausal period? Tomasz Pertyński, Grzegorz Stachowiak Klinika
Czym siê kierowaæ w doborze progestagenu do terapii hormonalnej wieku menopauzalnego? How to choose a progestogen for hormone therapy of the menopausal period? Tomasz Pertyński, Grzegorz Stachowiak Klinika
Wp³yw przezskórnej sekwencyjnej hormonalnej terapii na bezpieczeñstwo endometrium oraz profil krwawieñ u kobiet w okresie oko³omenopauzalnym
 Wp³yw przezskórnej sekwencyjnej hormonalnej terapii na bezpieczeñstwo endometrium oraz profil krwawieñ u kobiet w okresie oko³omenopauzalnym Influence of transdermal sequential hormone therapy on the endometrial
Wp³yw przezskórnej sekwencyjnej hormonalnej terapii na bezpieczeñstwo endometrium oraz profil krwawieñ u kobiet w okresie oko³omenopauzalnym Influence of transdermal sequential hormone therapy on the endometrial
Rola tibolonu w leczeniu dolegliwoœci i schorzeñ okresu menopauzy
 Rola tibolonu w leczeniu dolegliwoœci i schorzeñ okresu menopauzy The role of tibolone in the treatment of ailments and diseases of the menopausal period Grzegorz Stachowiak, Tomasz Pertyński Klinika Ginekologii
Rola tibolonu w leczeniu dolegliwoœci i schorzeñ okresu menopauzy The role of tibolone in the treatment of ailments and diseases of the menopausal period Grzegorz Stachowiak, Tomasz Pertyński Klinika Ginekologii
Korzyści ze stosowania HTZ
 Wprowadzenie do Rekomendacji Zarządu Głównego PTG w sprawie stosowania hormonalnej terapii zastępczej (Stan wiedzy na dzień 10.07.2004 r.- prof. dr hab. n. med. Tomasz Pertyński) Wyniki dużych randomizowanych
Wprowadzenie do Rekomendacji Zarządu Głównego PTG w sprawie stosowania hormonalnej terapii zastępczej (Stan wiedzy na dzień 10.07.2004 r.- prof. dr hab. n. med. Tomasz Pertyński) Wyniki dużych randomizowanych
Czy jest możliwe skuteczne leczenie cukrzycy w grupie chorych otyłych ze znaczną insulinoopornością?
 Jerzy Maksymilian Loba Klinika Chorób Wewnętrznych i Diabetologii Uniwersytet Medyczny w Łodzi Czy jest możliwe skuteczne leczenie cukrzycy w grupie chorych otyłych ze znaczną insulinoopornością? Definicja
Jerzy Maksymilian Loba Klinika Chorób Wewnętrznych i Diabetologii Uniwersytet Medyczny w Łodzi Czy jest możliwe skuteczne leczenie cukrzycy w grupie chorych otyłych ze znaczną insulinoopornością? Definicja
Desogestrel SUBSTANCJE CZYNNE. Grupa farmakoterapeutyczna: progestageny i estrogeny, produkty złożone. GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC)
 SUBSTANCJE CZYNNE Desogestrel GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC) Grupa farmakoterapeutyczna: progestageny i estrogeny, produkty złożone. Kod ATC: G03AC09 PODMIOT ODPOWIEDZIALNY NAZWA HANDLOWA PRODUKTU
SUBSTANCJE CZYNNE Desogestrel GRUPA FARMAKOTERAPEUTYCZNA (KOD ATC) Grupa farmakoterapeutyczna: progestageny i estrogeny, produkty złożone. Kod ATC: G03AC09 PODMIOT ODPOWIEDZIALNY NAZWA HANDLOWA PRODUKTU
STRESZCZENIE. Wstęp. Cele pracy
 STRESZCZENIE Wstęp Hormon wzrostu (GH) jest jednym z najważniejszych hormonów anabolicznych promujących proces wzrastania człowieka. GH działa lipolitycznie, wpływa na metabolizm węglowodanów, białek i
STRESZCZENIE Wstęp Hormon wzrostu (GH) jest jednym z najważniejszych hormonów anabolicznych promujących proces wzrastania człowieka. GH działa lipolitycznie, wpływa na metabolizm węglowodanów, białek i
Wp³yw przezskórnej sekwencyjnej terapii hormonalnej na profil hormonalny i lipidowy w surowicy krwi u kobiet w okresie oko³omenopauzalnym
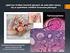 Wp³yw przezskórnej sekwencyjnej terapii hormonalnej na profil hormonalny i lipidowy w surowicy krwi u kobiet w okresie oko³omenopauzalnym The influence of sequential transdermal hormone therapy on serum
Wp³yw przezskórnej sekwencyjnej terapii hormonalnej na profil hormonalny i lipidowy w surowicy krwi u kobiet w okresie oko³omenopauzalnym The influence of sequential transdermal hormone therapy on serum
prof. Grzegorz Stachowiak Stosowanie terapii hormonalnej u kobiet po menopauzie
 prof. Grzegorz Stachowiak Stosowanie terapii hormonalnej u kobiet po menopauzie http://dopobrania.pwn.pl/ Stosowanie terapii hormonalnej u kobiet po menopauzie Grzegorz Stachowiak Klinika Ginekologii i
prof. Grzegorz Stachowiak Stosowanie terapii hormonalnej u kobiet po menopauzie http://dopobrania.pwn.pl/ Stosowanie terapii hormonalnej u kobiet po menopauzie Grzegorz Stachowiak Klinika Ginekologii i
ekarz ginekolog przepisał Pani złożony środek hormonalny Velbienne mini.
 ekarz ginekolog przepisał Pani złożony środek hormonalny Velbienne mini. Niniejszy Poradnik ma jedynie wartość informacyjną. Zawsze rekomendujemy konsultację z Pani lekarzem ginekologiem. Należy dokładnie
ekarz ginekolog przepisał Pani złożony środek hormonalny Velbienne mini. Niniejszy Poradnik ma jedynie wartość informacyjną. Zawsze rekomendujemy konsultację z Pani lekarzem ginekologiem. Należy dokładnie
 ANTYKONCEPCJA DORAŹNA OCTAN ULIPRYSTALU Stanisław Radowicki Konsultant Krajowy w dziedzinie położnictwa i ginekologii Warszawa 24 lutego 2015 r. Fizjologia cyklu miesiączkowego Okno płodności Cykl miesiączkowy
ANTYKONCEPCJA DORAŹNA OCTAN ULIPRYSTALU Stanisław Radowicki Konsultant Krajowy w dziedzinie położnictwa i ginekologii Warszawa 24 lutego 2015 r. Fizjologia cyklu miesiączkowego Okno płodności Cykl miesiączkowy
PRZEGL D MENOPAUZALNY 6/2006
 Porównanie skutecznoœci i tolerancji dwóch doustnych preparatów niskodawkowych zawieraj¹cych 1 mg 17β-estradiolu oraz dydrogesteron lub octan noretisteronu zastosowanych jako z³o ona ci¹g³a terapia hormonalna
Porównanie skutecznoœci i tolerancji dwóch doustnych preparatów niskodawkowych zawieraj¹cych 1 mg 17β-estradiolu oraz dydrogesteron lub octan noretisteronu zastosowanych jako z³o ona ci¹g³a terapia hormonalna
Typ histopatologiczny
 Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Kwasy tłuszczowe EPA i DHA omega-3 są niezbędne dla zdrowia serca i układu krążenia.
 Kwasy tłuszczowe EPA i DHA omega-3 są niezbędne dla zdrowia serca i układu krążenia. Kwasy tłuszczowe omega-3 jak pokazują wyniki wielu światowych badań klinicznych i epidemiologicznych na ludziach, są
Kwasy tłuszczowe EPA i DHA omega-3 są niezbędne dla zdrowia serca i układu krążenia. Kwasy tłuszczowe omega-3 jak pokazują wyniki wielu światowych badań klinicznych i epidemiologicznych na ludziach, są
Terapia hormonalna okresu menopauzy przezskórna droga podania
 DOI: 10.5114/pm.2012.30230 Przegl d menopauzalny 4/2012 Terapia hormonalna okresu menopauzy przezskórna droga podania Menopausal hormone therapy: transdermal route of administration Małgorzata Bińkowska,
DOI: 10.5114/pm.2012.30230 Przegl d menopauzalny 4/2012 Terapia hormonalna okresu menopauzy przezskórna droga podania Menopausal hormone therapy: transdermal route of administration Małgorzata Bińkowska,
diagnostyka różnicowa złośliwych i niezłośliwych zmian w jajnikach nie tylko CA 125 i HE4, ale również wybrane wykładniki gospodarki lipidowej
 diagnostyka różnicowa złośliwych i niezłośliwych zmian w jajnikach nie tylko CA 125 i HE4, ale również wybrane wykładniki gospodarki lipidowej Pracownia Markerów Nowotworowych Zakładu Patologii i Diagnostyki
diagnostyka różnicowa złośliwych i niezłośliwych zmian w jajnikach nie tylko CA 125 i HE4, ale również wybrane wykładniki gospodarki lipidowej Pracownia Markerów Nowotworowych Zakładu Patologii i Diagnostyki
Aneks II. Niniejsza Charakterystyka Produktu Leczniczego oraz ulotka dla pacjenta stanowią wynik procedury arbitrażowej.
 Aneks II Zmiany dotyczące odpowiednich punktów Charakterystyki Produktu Leczniczego oraz ulotki dla pacjenta przedstawione przez Europejską Agencję Leków (EMA) Niniejsza Charakterystyka Produktu Leczniczego
Aneks II Zmiany dotyczące odpowiednich punktów Charakterystyki Produktu Leczniczego oraz ulotki dla pacjenta przedstawione przez Europejską Agencję Leków (EMA) Niniejsza Charakterystyka Produktu Leczniczego
ANNALES UNIVERSITATIS MARIAE CURIE-SKŁODOWSKA LUBLIN - POLONIA VOL.LIX, SUPPL. XIV, 81 SECTIO D 2004
 ANNALES UNIVERSITATIS MARIAE CURIE-SKŁODOWSKA LUBLIN - POLONIA VOL.LIX, SUPPL. XIV, 81 SECTIO D 2004 Zakład Pielęgniarstwa Położniczo Ginekologicznego Akademii Medycznej w Białymstoku * Department of Gynecology
ANNALES UNIVERSITATIS MARIAE CURIE-SKŁODOWSKA LUBLIN - POLONIA VOL.LIX, SUPPL. XIV, 81 SECTIO D 2004 Zakład Pielęgniarstwa Położniczo Ginekologicznego Akademii Medycznej w Białymstoku * Department of Gynecology
S³owa kluczowe: rak sutka, menopauza, estrogeny, przezskórna terapia hormonalna. (Przegl¹d Menopauzalny 2005; 3: 47 52)
 Rak sutka a terapia hormonalna okresu menopauzy Breast cancer versus hormone therapy of the menopausal period Tomasz Pertyñski, Grzegorz Stachowiak W pracy przedstawione zosta³y dane na temat zwi¹zku steroidów
Rak sutka a terapia hormonalna okresu menopauzy Breast cancer versus hormone therapy of the menopausal period Tomasz Pertyñski, Grzegorz Stachowiak W pracy przedstawione zosta³y dane na temat zwi¹zku steroidów
Gdański Uniwersytet Medyczny. Polimorfizm genów receptorów estrogenowych (ERα i ERβ) a rozwój zespołu metabolicznego u kobiet po menopauzie
 Gdański Uniwersytet Medyczny Mgr Karolina Kuźbicka Polimorfizm genów receptorów estrogenowych (ERα i ERβ) a rozwój zespołu metabolicznego u kobiet po menopauzie Rozprawa doktorska Promotor: dr hab. n.
Gdański Uniwersytet Medyczny Mgr Karolina Kuźbicka Polimorfizm genów receptorów estrogenowych (ERα i ERβ) a rozwój zespołu metabolicznego u kobiet po menopauzie Rozprawa doktorska Promotor: dr hab. n.
Transdermalne systemy hormonalne
 Transdermalne systemy hormonalne Gdańsk 2014 Redaktor prowadzący: Olga Strzelec Redakcja: Olga Strzelec Korekta: Teresa Moroz Projekt okładki: Andrzej Owsiany Skład: Tomasz Kowalewski Seria wydawnicza
Transdermalne systemy hormonalne Gdańsk 2014 Redaktor prowadzący: Olga Strzelec Redakcja: Olga Strzelec Korekta: Teresa Moroz Projekt okładki: Andrzej Owsiany Skład: Tomasz Kowalewski Seria wydawnicza
 W badaniu 4S (ang. Scandinavian Simvastatin Survivat Study), oceniano wpływ symwastatyny na całkowitą śmiertelność u 4444 pacjentów z chorobą wieńcową i z wyjściowym stężeniem cholesterolu całkowitego
W badaniu 4S (ang. Scandinavian Simvastatin Survivat Study), oceniano wpływ symwastatyny na całkowitą śmiertelność u 4444 pacjentów z chorobą wieńcową i z wyjściowym stężeniem cholesterolu całkowitego
Klinika Endokrynologii Ginekologicznej, Collegium Medicum Uniwersytetu Jagiellońskiego, Kraków, Polska; 2
 Wpływ drogi podania 17β-estradiolu na stężenie insulinopodobnego czynnika wzrostu-i (IGF-I) i jego białek wiążących 1 i 3 w surowicy krwi u kobiet po menopauzie stosujących octan norethisteronu Influence
Wpływ drogi podania 17β-estradiolu na stężenie insulinopodobnego czynnika wzrostu-i (IGF-I) i jego białek wiążących 1 i 3 w surowicy krwi u kobiet po menopauzie stosujących octan norethisteronu Influence
Przezskórna terapia okresu menopauzy state of the art in 2010
 Przezskórna terapia okresu menopauzy state of the art in 2010 Transdermal hormone therapy of the menopausal period state of the art in 2010 Tomasz Pertyński, Grzegorz Stachowiak Klinika Ginekologii i Chorób
Przezskórna terapia okresu menopauzy state of the art in 2010 Transdermal hormone therapy of the menopausal period state of the art in 2010 Tomasz Pertyński, Grzegorz Stachowiak Klinika Ginekologii i Chorób
Wybór najistotniejszych publikacji z roku 2013 Lancet (IF-39)/Lancet Oncology (IF-25)/ Oncologist
 Wybór najistotniejszych publikacji z roku 2013 Lancet (IF-39)/Lancet Oncology (IF-25)/ Oncologist (IF-4) Dr n. med. Lubomir Bodnar Klinika Onkologii, Wojskowego Instytutu Medycznego w Warszawie Warszawa
Wybór najistotniejszych publikacji z roku 2013 Lancet (IF-39)/Lancet Oncology (IF-25)/ Oncologist (IF-4) Dr n. med. Lubomir Bodnar Klinika Onkologii, Wojskowego Instytutu Medycznego w Warszawie Warszawa
Hormonalna terapia zastêpcza a choroby naczyñ têtniczych
 Hormonalna terapia zastêpcza a choroby naczyñ têtniczych The hormone replacement therapy and the diseases of the arteries Romuald Dębski Klinika Położnictwa i Ginekologii Centrum Medycznego Kształcenia
Hormonalna terapia zastêpcza a choroby naczyñ têtniczych The hormone replacement therapy and the diseases of the arteries Romuald Dębski Klinika Położnictwa i Ginekologii Centrum Medycznego Kształcenia
Wp³yw drogi poda y 17β-estradiolu i rodzaju zastosowanego doustnie gestagenu na stê enie glukozy i insuliny u kobiet po menopauzie
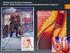 Wp³yw drogi poda y 17β-estradiolu i rodzaju zastosowanego doustnie gestagenu na stê enie glukozy i insuliny u kobiet po menopauzie Influence of route of 17β-oestradiol administration and type of gestagen
Wp³yw drogi poda y 17β-estradiolu i rodzaju zastosowanego doustnie gestagenu na stê enie glukozy i insuliny u kobiet po menopauzie Influence of route of 17β-oestradiol administration and type of gestagen
Hormonalna terapia zastępcza a cukrzyca
 PRACA POGLĄDOWA ISSN 1640 8497 Marek Bolanowski Katedra i Klinika Endokrynologii i Diabetologii Akademii Medycznej we Wrocławiu Hormonalna terapia zastępcza a cukrzyca Hormone replacement therapy and diabetes
PRACA POGLĄDOWA ISSN 1640 8497 Marek Bolanowski Katedra i Klinika Endokrynologii i Diabetologii Akademii Medycznej we Wrocławiu Hormonalna terapia zastępcza a cukrzyca Hormone replacement therapy and diabetes
Substancja pomocnicza o znanym działaniu: butylohydroksytoluen. Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OEKOLP forte 0,5 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka zawiera 0,5 mg estriolu (Estriolum) Substancja pomocnicza
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OEKOLP forte 0,5 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka zawiera 0,5 mg estriolu (Estriolum) Substancja pomocnicza
2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 1,0 mg estriolu (Estriolum) Substancja pomocnicza o znanym działaniu: glikol propylenowy.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OEKOLP 1 mg/g, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 1,0 mg estriolu (Estriolum) Substancja pomocnicza o znanym działaniu:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OEKOLP 1 mg/g, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 1,0 mg estriolu (Estriolum) Substancja pomocnicza o znanym działaniu:
UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA.
 UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA Małgorzata Biskup Czynniki ryzyka sercowo-naczyniowego u chorych na reumatoidalne zapalenie
UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA Małgorzata Biskup Czynniki ryzyka sercowo-naczyniowego u chorych na reumatoidalne zapalenie
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1937274. (96) Data i numer zgłoszenia patentu europejskiego: 05.09.2006 06791828.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1937274 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 0.09.06 06791828.4
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1937274 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 0.09.06 06791828.4
Płocki Zakład Opieki Zdrowotnej, Oddział Ginekologiczno-Położniczy; ordydnator Oddziału: dr med. Romuald Juchnowicz-Bierbasz
 Zmiany patologiczne w jamie macicy u kobiet po menopauzie zale noœæ od czasu trwania menopauzy i przesz³oœci ginekologiczno-po³o niczej, u kobiet z krwawieniami i bez krwawieñ Pathology of uterus cavity
Zmiany patologiczne w jamie macicy u kobiet po menopauzie zale noœæ od czasu trwania menopauzy i przesz³oœci ginekologiczno-po³o niczej, u kobiet z krwawieniami i bez krwawieñ Pathology of uterus cavity
WPŁYW DOPOCHWOWEGO LECZENIA ESTRIOLEM ZMIAN ATROFICZNYCH POCHWY NA GRUBOŚĆ ENDOMETRIUM U KOBIET PO MENOPAUZIE
 Nowiny Lekarskie 2006, 75, 4, 323 327 PATRYCJA GULA, WOJMIR ZIĘTKOWIAK WPŁYW DOPOCHWOWEGO LECZENIA ESTRIOLEM ZMIAN ATROFICZNYCH POCHWY NA GRUBOŚĆ ENDOMETRIUM U KOBIET PO MENOPAUZIE EFFECT OF VAGINAL ESTRIOL
Nowiny Lekarskie 2006, 75, 4, 323 327 PATRYCJA GULA, WOJMIR ZIĘTKOWIAK WPŁYW DOPOCHWOWEGO LECZENIA ESTRIOLEM ZMIAN ATROFICZNYCH POCHWY NA GRUBOŚĆ ENDOMETRIUM U KOBIET PO MENOPAUZIE EFFECT OF VAGINAL ESTRIOL
Wybór drogi podania w terapii hormonalnej okresu menopauzy kiedy warto zamieniæ tabletki na plastry?
 Wybór drogi podania w terapii hormonalnej okresu menopauzy kiedy warto zamieniæ tabletki na plastry? Choosing the route of drug administration for hormone therapy of the menopausal period when is it worth
Wybór drogi podania w terapii hormonalnej okresu menopauzy kiedy warto zamieniæ tabletki na plastry? Choosing the route of drug administration for hormone therapy of the menopausal period when is it worth
Analysis of infectious complications inf children with acute lymphoblastic leukemia treated in Voivodship Children's Hospital in Olsztyn
 Analiza powikłań infekcyjnych u dzieci z ostrą białaczką limfoblastyczną leczonych w Wojewódzkim Specjalistycznym Szpitalu Dziecięcym w Olsztynie Analysis of infectious complications inf children with
Analiza powikłań infekcyjnych u dzieci z ostrą białaczką limfoblastyczną leczonych w Wojewódzkim Specjalistycznym Szpitalu Dziecięcym w Olsztynie Analysis of infectious complications inf children with
S³owa kluczowe: menopauza, hormonalna terapia zastêpcza, progestageny. (Przegl¹d Menopauzalny 2003; 2:12 17)
 Progestageny w hormonalnej terapii zastêpczej nowe perspektywy Progestins in hormonal replacement therapy new perspectives W³odzimierz Baranowski 1, 2, Jacek Tomaszewski 1 W ci¹gu ostatniej dekady wprowadzono
Progestageny w hormonalnej terapii zastêpczej nowe perspektywy Progestins in hormonal replacement therapy new perspectives W³odzimierz Baranowski 1, 2, Jacek Tomaszewski 1 W ci¹gu ostatniej dekady wprowadzono
UNIWERSYTET WARMIŃSKO MAZURSKI W OLSZTYNIE
 UNIWERSYTET WARMIŃSKO MAZURSKI W OLSZTYNIE Katarzyna Myszka Podgórska Ocena częstości występowania zespołu metabolicznego u osób z przypadkowo wykrytymi guzami nadnerczy z prawidłową aktywnością hormonalną
UNIWERSYTET WARMIŃSKO MAZURSKI W OLSZTYNIE Katarzyna Myszka Podgórska Ocena częstości występowania zespołu metabolicznego u osób z przypadkowo wykrytymi guzami nadnerczy z prawidłową aktywnością hormonalną
Kinga Janik-Koncewicz
 Kinga Janik-Koncewicz miażdżyca choroby układu krążenia cukrzyca typu 2 nadciśnienie choroby układu kostnego nowotwory Światowa Organizacja Zdrowia szacuje, że około 7-41% nowotworów jest spowodowanych
Kinga Janik-Koncewicz miażdżyca choroby układu krążenia cukrzyca typu 2 nadciśnienie choroby układu kostnego nowotwory Światowa Organizacja Zdrowia szacuje, że około 7-41% nowotworów jest spowodowanych
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków
 Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
ANTYKONCEPCJA. Warszawski Uniwersytet Medyczny Klinika Endokrynologii Ginekologicznej. lek med Katarzyna Suchta
 ANTYKONCEPCJA Warszawski Uniwersytet Medyczny Klinika Endokrynologii Ginekologicznej lek med Katarzyna Suchta ANTYKONCEPCJA Mianem antykoncepcji określa się świadomie podjęte działania i środki mające
ANTYKONCEPCJA Warszawski Uniwersytet Medyczny Klinika Endokrynologii Ginekologicznej lek med Katarzyna Suchta ANTYKONCEPCJA Mianem antykoncepcji określa się świadomie podjęte działania i środki mające
ANEKS I. Strona 1 z 5
 ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC WETERYNARYJNYCH PRODUKTÓW LECZNICZYCH, GATUNKI ZWIERZĄT, DROGA PODANIA, PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH
ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC WETERYNARYJNYCH PRODUKTÓW LECZNICZYCH, GATUNKI ZWIERZĄT, DROGA PODANIA, PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH
Ulotka dołączona do opakowania: informacja dla pacjenta. Luteina, 50 mg, tabletki dopochwowe Progesteronum
 Ulotka dołączona do opakowania: informacja dla pacjenta Luteina, 50 mg, tabletki dopochwowe Progesteronum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Luteina, 50 mg, tabletki dopochwowe Progesteronum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Rozrosty endometrium: skutecznoϾ leczenia naturalnym mikronizowanym progesteronem podawanym dopochwowo
 Rozrosty endometrium: skutecznoϾ leczenia naturalnym mikronizowanym progesteronem podawanym dopochwowo Endometrial hyperplasia: efficacy of treatment with vaginal tablet containing natural micronized
Rozrosty endometrium: skutecznoϾ leczenia naturalnym mikronizowanym progesteronem podawanym dopochwowo Endometrial hyperplasia: efficacy of treatment with vaginal tablet containing natural micronized
PROVERA, 10 mg, tabletki Okrągłe, białe tabletki z wytłoczonym znakiem Upjohn 50 po jednej stronie i linią podziału po drugiej stronie.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PROVERA, 5 mg, tabletki PROVERA, 10 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda tabletka zawiera 5 mg lub 10 mg medroksyprogesteronu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PROVERA, 5 mg, tabletki PROVERA, 10 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda tabletka zawiera 5 mg lub 10 mg medroksyprogesteronu
Rejestracja przepływów w tętnicach pęcherzowych z zastosowaniem techniki dopplerowskiej u pacjentek z nietrzymaniem moczu
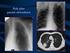 Krzysztof Cendrowski, Włodzimierz Sawicki, Beata Śpiewankiewicz, Jerzy Stelmachów Rejestracja przepływów w tętnicach pęcherzowych z zastosowaniem techniki dopplerowskiej u pacjentek z nietrzymaniem moczu
Krzysztof Cendrowski, Włodzimierz Sawicki, Beata Śpiewankiewicz, Jerzy Stelmachów Rejestracja przepływów w tętnicach pęcherzowych z zastosowaniem techniki dopplerowskiej u pacjentek z nietrzymaniem moczu
Nowe terapie w cukrzycy typu 2. Janusz Gumprecht
 Nowe terapie w cukrzycy typu 2 Janusz Gumprecht Dziś już nic nie jest takie jak było kiedyś 425 000 000 Ilość chorych na cukrzycę w roku 2017 629 000 000 Ilość chorych na cukrzycę w roku 2045 International
Nowe terapie w cukrzycy typu 2 Janusz Gumprecht Dziś już nic nie jest takie jak było kiedyś 425 000 000 Ilość chorych na cukrzycę w roku 2017 629 000 000 Ilość chorych na cukrzycę w roku 2045 International
CHOLESTONE NATURALNA OCHRONA PRZED MIAŻDŻYCĄ. www.california-fitness.pl www.calivita.com
 CHOLESTONE NATURALNA OCHRONA PRZED MIAŻDŻYCĄ Co to jest cholesterol? Nierozpuszczalna w wodzie substancja, która: jest składnikiem strukturalnym wszystkich błon komórkowych i śródkomórkowych wchodzi w
CHOLESTONE NATURALNA OCHRONA PRZED MIAŻDŻYCĄ Co to jest cholesterol? Nierozpuszczalna w wodzie substancja, która: jest składnikiem strukturalnym wszystkich błon komórkowych i śródkomórkowych wchodzi w
Doustne środki antykoncepcyjne a ryzyko wystąpienia zakrzepicy. Dr hab. Jacek Golański Zakład Zaburzeń Krzepnięcia Krwi Uniwersytet Medyczny w Łodzi
 Doustne środki antykoncepcyjne a ryzyko wystąpienia zakrzepicy Dr hab. Jacek Golański Zakład Zaburzeń Krzepnięcia Krwi Uniwersytet Medyczny w Łodzi Żylna choroba zakrzepowozatorowa (ŻChZZ) stanowi ważny
Doustne środki antykoncepcyjne a ryzyko wystąpienia zakrzepicy Dr hab. Jacek Golański Zakład Zaburzeń Krzepnięcia Krwi Uniwersytet Medyczny w Łodzi Żylna choroba zakrzepowozatorowa (ŻChZZ) stanowi ważny
Ulotka dołączona do opakowania: informacja dla pacjenta Luteina, 50 mg, tabletki dopochwowe. Progesteronum
 Ulotka dołączona do opakowania: informacja dla pacjenta Luteina, 50 mg, tabletki dopochwowe Progesteronum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Luteina, 50 mg, tabletki dopochwowe Progesteronum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Jedna tabletka powlekana zawiera 10 mg dydrogesteronu (Dydrogesteronum). Produkt zawiera laktozę jednowodną.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Duphaston 10 mg, tabletki powlekane 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka powlekana zawiera 10 mg dydrogesteronu (Dydrogesteronum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Duphaston 10 mg, tabletki powlekane 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka powlekana zawiera 10 mg dydrogesteronu (Dydrogesteronum).
ESMYA (ulipristal acetate): Poradnik dla lekarza
 ESMYA (ulipristal acetate): Poradnik dla lekarza dotyczący przepisywania leku Esmya STRESZCZENIE Octan uliprystalu jest wskazany do przeprowadzenia jednego cyklu leczenia przedoperacyjnego w przypadku
ESMYA (ulipristal acetate): Poradnik dla lekarza dotyczący przepisywania leku Esmya STRESZCZENIE Octan uliprystalu jest wskazany do przeprowadzenia jednego cyklu leczenia przedoperacyjnego w przypadku
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1933843 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 12.10.2006 06806225.6
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1933843 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 12.10.2006 06806225.6
Liofilizowany ocet jabłkowy 80% (±5%), mikronizowany błonnik jabłkowy 20% (±5%), celulozowa otoczka kapsułki.
 Suplement diety Składniki: Liofilizowany ocet jabłkowy 80% (±5%), mikronizowany błonnik jabłkowy 20% (±5%), celulozowa otoczka kapsułki. Przechowywanie: W miejscu niedostępnym dla małych dzieci. Przechowywać
Suplement diety Składniki: Liofilizowany ocet jabłkowy 80% (±5%), mikronizowany błonnik jabłkowy 20% (±5%), celulozowa otoczka kapsułki. Przechowywanie: W miejscu niedostępnym dla małych dzieci. Przechowywać
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PROVERA, 5 mg, tabletki PROVERA, 10 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda tabletka zawiera 5 mg lub 10 mg medroksyprogesteronu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PROVERA, 5 mg, tabletki PROVERA, 10 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda tabletka zawiera 5 mg lub 10 mg medroksyprogesteronu
Wpływ hormonalnej terapii okresu menopauzalnego na układ sercowo-naczyniowy przesłanki teoretyczne
 Stanowisko Zespołu Ekspertów Polskiego Towarzystwa Ginekologicznego, Polskiego Towarzystwa Kardiologicznego oraz Polskiego Towarzystwa Menopauzy i Andropauzy na temat wpływu terapii hormonalnej okresu
Stanowisko Zespołu Ekspertów Polskiego Towarzystwa Ginekologicznego, Polskiego Towarzystwa Kardiologicznego oraz Polskiego Towarzystwa Menopauzy i Andropauzy na temat wpływu terapii hormonalnej okresu
STRESZCZENIE PRACY DOKTORSKIEJ
 mgr Bartłomiej Rospond POSZUKIWANIE NEUROBIOLOGICZNEGO MECHANIZMU UZALEŻNIENIA OD POKARMU - WPŁYW CUKRÓW I TŁUSZCZÓW NA EKSPRESJĘ RECEPTORÓW DOPAMINOWYCH D 2 W GRZBIETOWYM PRĄŻKOWIU U SZCZURÓW STRESZCZENIE
mgr Bartłomiej Rospond POSZUKIWANIE NEUROBIOLOGICZNEGO MECHANIZMU UZALEŻNIENIA OD POKARMU - WPŁYW CUKRÓW I TŁUSZCZÓW NA EKSPRESJĘ RECEPTORÓW DOPAMINOWYCH D 2 W GRZBIETOWYM PRĄŻKOWIU U SZCZURÓW STRESZCZENIE
Amy Ferris, Annie Price i Keith Harding Pressure ulcers in patients receiving palliative care: A systematic review Palliative Medicine 2019 Apr 24
 Amy Ferris, Annie Price i Keith Harding Pressure ulcers in patients receiving palliative care: A systematic review Palliative Medicine 2019 Apr 24 Cel - przegląd ma na celu określenie częstości występowania
Amy Ferris, Annie Price i Keith Harding Pressure ulcers in patients receiving palliative care: A systematic review Palliative Medicine 2019 Apr 24 Cel - przegląd ma na celu określenie częstości występowania
Rak piersi. Doniesienia roku Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie
 Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI. Maria Litwiniuk Warszawa 28 maja 2019
 LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI Maria Litwiniuk Warszawa 28 maja 2019 Konflikt interesów Wykłady sponsorowane dla firm: Teva, AstraZeneca, Pfizer, Roche Sponorowanie
LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI Maria Litwiniuk Warszawa 28 maja 2019 Konflikt interesów Wykłady sponsorowane dla firm: Teva, AstraZeneca, Pfizer, Roche Sponorowanie
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 PL/EP 1740163 T3 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1740163 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 15.04.2005
PL/EP 1740163 T3 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1740163 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 15.04.2005
Rekomendacje Polskiego Towarzystwa Menopauzy i Andropauzy na temat hormonalnej terapii menopauzy stan wiedzy na grudzieñ 2013 roku
 DOI: 10.5114/pm.2014.41078 Prz Menopauzalny 2014; 18(1): 1-8 Special paper Rekomendacje Polskiego Towarzystwa Menopauzy i Andropauzy na temat hormonalnej terapii menopauzy stan wiedzy na grudzieñ 2013
DOI: 10.5114/pm.2014.41078 Prz Menopauzalny 2014; 18(1): 1-8 Special paper Rekomendacje Polskiego Towarzystwa Menopauzy i Andropauzy na temat hormonalnej terapii menopauzy stan wiedzy na grudzieñ 2013
Terapia hormonalna a choroba zakrzepowo-zatorowa
 Terapia hormonalna a choroba zakrzepowo-zatorowa Hormonal therapy and thromboembolic disease Bartłomiej Barczyński, Jan Kotarski I Katedra i Klinika Ginekologii Onkologicznej i Ginekologii, Uniwersytet
Terapia hormonalna a choroba zakrzepowo-zatorowa Hormonal therapy and thromboembolic disease Bartłomiej Barczyński, Jan Kotarski I Katedra i Klinika Ginekologii Onkologicznej i Ginekologii, Uniwersytet
Materiały edukacyjne. Diagnostyka i leczenie nadciśnienia tętniczego
 Materiały edukacyjne Diagnostyka i leczenie nadciśnienia tętniczego Klasyfikacja ciśnienia tętniczego (mmhg) (wg. ESH/ESC )
Materiały edukacyjne Diagnostyka i leczenie nadciśnienia tętniczego Klasyfikacja ciśnienia tętniczego (mmhg) (wg. ESH/ESC )
Orthogen GmbH. Department of Radiology and Microtherapy University of Witten/Herdecke, Germany
 Orthogen GmbH Biologiczne podstawy stosowania metody Irap IL-1 IL-1 IL-1Ra Podstawy działania Irap IL-1 Ra! TGF-β! PDGF! IGF! HGF! Przygotowywanie autologicznej kondycjonowanej surowicy (ACS) proces Irap
Orthogen GmbH Biologiczne podstawy stosowania metody Irap IL-1 IL-1 IL-1Ra Podstawy działania Irap IL-1 Ra! TGF-β! PDGF! IGF! HGF! Przygotowywanie autologicznej kondycjonowanej surowicy (ACS) proces Irap
VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości
 VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Szacuje się, że wysokie ciśnienie krwi jest przyczyną
VI.2 Podsumowanie planu zarządzania ryzykiem dla produktu Zanacodar Combi przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Szacuje się, że wysokie ciśnienie krwi jest przyczyną
Profil metaboliczny róŝnych organów ciała
 Profil metaboliczny róŝnych organów ciała Uwaga: tkanka tłuszczowa (adipose tissue) NIE wykorzystuje glicerolu do biosyntezy triacylogliceroli Endo-, para-, i autokrynna droga przekazu informacji biologicznej.
Profil metaboliczny róŝnych organów ciała Uwaga: tkanka tłuszczowa (adipose tissue) NIE wykorzystuje glicerolu do biosyntezy triacylogliceroli Endo-, para-, i autokrynna droga przekazu informacji biologicznej.
Mefelor 50/5 mg Tabletka o przedłużonym uwalnianiu. Metoprololtartrat/Felodipi n AbZ 50 mg/5 mg Retardtabletten
 ANEKS I WYKAZ NAZW, POSTACI FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCÓW, POSIADACZY POZWOLEŃ NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH Państwo członkowskie Podmiot
ANEKS I WYKAZ NAZW, POSTACI FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCÓW, POSIADACZY POZWOLEŃ NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH Państwo członkowskie Podmiot
PRZEGL D MENOPAUZALNY 4/2006
 Wp³yw szeœciomiesiêcznej przezskórnej suplementacji 17β-estradiolem wraz z doustn¹ poda ¹ medroksyprogesteronu lub doustnej poda y simwastatyny na poziomy glikemii i insulinemii u kobiet po menopauzie
Wp³yw szeœciomiesiêcznej przezskórnej suplementacji 17β-estradiolem wraz z doustn¹ poda ¹ medroksyprogesteronu lub doustnej poda y simwastatyny na poziomy glikemii i insulinemii u kobiet po menopauzie
Przekwitanie. Klinika Endokrynologii Ginekologicznej Warszawski Uniwersytet Medyczny
 Przekwitanie Klinika Endokrynologii Ginekologicznej Warszawski Uniwersytet Medyczny Menopauza (gr. men- miesiąc, pausis pauza) Definicja wg WHO (1996) ostatnie krwawienie miesiączkowe, po którym w okresie
Przekwitanie Klinika Endokrynologii Ginekologicznej Warszawski Uniwersytet Medyczny Menopauza (gr. men- miesiąc, pausis pauza) Definicja wg WHO (1996) ostatnie krwawienie miesiączkowe, po którym w okresie
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. Orgametril, 5 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Orgametril, 5 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka zawiera 5 mg linestrenolu (Lynestrenolum). Produkt zawiera laktozę.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Orgametril, 5 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka zawiera 5 mg linestrenolu (Lynestrenolum). Produkt zawiera laktozę.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Indivina, 1 mg + 2,5 mg, tabletki Indivina, 1 mg + 5 mg, tabletki Indivina, 2 mg + 5 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Indivina, 1 mg + 2,5 mg, tabletki Indivina, 1 mg + 5 mg, tabletki Indivina, 2 mg + 5 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna
Nowa szansa dla terapii hormonalnej w prewencji kardiologicznej?
 Nowa szansa dla terapii hormonalnej w prewencji kardiologicznej? A new chance for hormone therapy in cardiological prophylaxis? Zdzisława Kornacewicz-Jach Klinika Kardiologii Pomorskiej Akademii Medycznej
Nowa szansa dla terapii hormonalnej w prewencji kardiologicznej? A new chance for hormone therapy in cardiological prophylaxis? Zdzisława Kornacewicz-Jach Klinika Kardiologii Pomorskiej Akademii Medycznej
NIEPRAWIDŁOWE KRWAWIENIA Z DRÓG RODNYCH. Dr n. med. Monika Szymańska
 Dr n. med. Monika Szymańska PRAWIDŁOWE KRWAWIENIE Z Miesiączka Krwawienie maciczne występujące co 25-35 dni Trwające 3-7 dni Utrata krwi 30-80ml Menarche 9-16rż. (Polska 12,8 lat) Menopauza 49-53 rż (Polska
Dr n. med. Monika Szymańska PRAWIDŁOWE KRWAWIENIE Z Miesiączka Krwawienie maciczne występujące co 25-35 dni Trwające 3-7 dni Utrata krwi 30-80ml Menarche 9-16rż. (Polska 12,8 lat) Menopauza 49-53 rż (Polska
Leki antykachektyczne. lek. med. Marta Bijak-Ulejczyk Oddział Anestezjologii i Intensywnej Terapii
 Leki antykachektyczne lek. med. Marta Bijak-Ulejczyk Oddział Anestezjologii i Intensywnej Terapii Grupy leków czyli co mamy środki stymulujące apetyt leki modulujące pracę przewodu pokarmowego leki anaboliczne/antykataboliczne
Leki antykachektyczne lek. med. Marta Bijak-Ulejczyk Oddział Anestezjologii i Intensywnej Terapii Grupy leków czyli co mamy środki stymulujące apetyt leki modulujące pracę przewodu pokarmowego leki anaboliczne/antykataboliczne
Ocena czynników wp³ywaj¹cych na gruboœæ b³ony œluzowej trzonu macicy u kobiet w wieku pomenopauzalnym
 Ocena czynników wp³ywaj¹cych na gruboœæ b³ony œluzowej trzonu macicy u kobiet w wieku pomenopauzalnym An assessment of factors associated with thickness of the endometrium in postmenopausal women Anna
Ocena czynników wp³ywaj¹cych na gruboœæ b³ony œluzowej trzonu macicy u kobiet w wieku pomenopauzalnym An assessment of factors associated with thickness of the endometrium in postmenopausal women Anna
SEMINARIUM 2 15. 10. 2015
 SEMINARIUM 2 15. 10. 2015 Od tłuszczu pokarmowego do lipoprotein osocza, metabolizm, budowa cząsteczek lipoprotein, apolipoproteiny, znaczenie biologiczne, enzymy biorące udział w metabolizmie lipoprotein,
SEMINARIUM 2 15. 10. 2015 Od tłuszczu pokarmowego do lipoprotein osocza, metabolizm, budowa cząsteczek lipoprotein, apolipoproteiny, znaczenie biologiczne, enzymy biorące udział w metabolizmie lipoprotein,
Bezpieczeñstwo zakrzepowo-zatorowe przezskórnej terapii hormonalnej
 Bezpieczeñstwo zakrzepowo-zatorowe przezskórnej terapii hormonalnej Thromboembolic safety of transdermal hormone therapy Grzegorz Stachowiak, Tomasz Pertyński Klinika Menopauzy i Chorób Kobiecych, Instytut
Bezpieczeñstwo zakrzepowo-zatorowe przezskórnej terapii hormonalnej Thromboembolic safety of transdermal hormone therapy Grzegorz Stachowiak, Tomasz Pertyński Klinika Menopauzy i Chorób Kobiecych, Instytut
Hormonalna terapia zastêpcza a cukrzyca
 DOI: 10.5114/pm.2013.33424 Przegl d menopauzalny 1/2013 Hormonalna terapia zastêpcza a cukrzyca Hormonal replacement therapy and the diabetes Ewa Wender-Ożegowska 1, Katarzyna Ożegowska 2, Paweł Gutaj
DOI: 10.5114/pm.2013.33424 Przegl d menopauzalny 1/2013 Hormonalna terapia zastêpcza a cukrzyca Hormonal replacement therapy and the diabetes Ewa Wender-Ożegowska 1, Katarzyna Ożegowska 2, Paweł Gutaj
Wpływ alkoholu na ryzyko rozwoju nowotworów złośliwych
 Wpływ alkoholu na ryzyko rozwoju nowotworów złośliwych Badania epidemiologiczne i eksperymentalne nie budzą wątpliwości spożywanie alkoholu zwiększa ryzyko rozwoju wielu nowotworów złośliwych, zwłaszcza
Wpływ alkoholu na ryzyko rozwoju nowotworów złośliwych Badania epidemiologiczne i eksperymentalne nie budzą wątpliwości spożywanie alkoholu zwiększa ryzyko rozwoju wielu nowotworów złośliwych, zwłaszcza
Zespó³ metaboliczny u kobiet w okresie menopauzy
 Zespó³ metaboliczny u kobiet w okresie menopauzy Metabolic syndrome in women in the menopausal period Grzegorz Stachowiak, Agnieszka Zając, Tomasz Pertyński Klinika Ginekologii i Chorób Menopauzy, Instytut
Zespó³ metaboliczny u kobiet w okresie menopauzy Metabolic syndrome in women in the menopausal period Grzegorz Stachowiak, Agnieszka Zając, Tomasz Pertyński Klinika Ginekologii i Chorób Menopauzy, Instytut
Podmiot odpowiedzialny Wnioskodawca Nazwa własna Moc Postać farmaceutyczna Droga podania Zawartość (stężenie) Vantas 50 mg Implant Podskórne 50 mg
 ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTÓW LECZNICZYCH, DROGA PODANIA, WNIOSKODAWCA, PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH Państwo
ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC PRODUKTÓW LECZNICZYCH, DROGA PODANIA, WNIOSKODAWCA, PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH CZŁONKOWSKICH Państwo
Propozycja algorytmu postępowania w przypadkach krwawień z
 Propozycja algorytmu postępowania w przypadkach krwawień z macicy podczas hormonalnej terapii zastępczej. Tomasz Paszkowski III Katedra i Klinika Ginekologii Akademii Medycznej w Lublinie, kierownik Katedry
Propozycja algorytmu postępowania w przypadkach krwawień z macicy podczas hormonalnej terapii zastępczej. Tomasz Paszkowski III Katedra i Klinika Ginekologii Akademii Medycznej w Lublinie, kierownik Katedry
Najnowsze doniesienia na temat bezpieczeñstwa terapii hormonalnej dla gruczo³u piersiowego
 Najnowsze doniesienia na temat bezpieczeñstwa terapii hormonalnej dla gruczo³u piersiowego The latest data on hormonal therapy safety for breast Romuald Dębski II Klinika Położnictwa i Ginekologii Centrum
Najnowsze doniesienia na temat bezpieczeñstwa terapii hormonalnej dla gruczo³u piersiowego The latest data on hormonal therapy safety for breast Romuald Dębski II Klinika Położnictwa i Ginekologii Centrum
Klinika Endokrynologii Ginekologicznej Collegium Medicum Uniwersytetu Jagiellońskiego w Krakowie, Polska 2
 Ginekol Pol. 2011, 82, 254-258 The somatotropic axis in postmenopausal women during six month of transdermal continuous 17β-estradiol administration combined with oral medroxyprogesterone Zmiany aktywnoêci
Ginekol Pol. 2011, 82, 254-258 The somatotropic axis in postmenopausal women during six month of transdermal continuous 17β-estradiol administration combined with oral medroxyprogesterone Zmiany aktywnoêci
Hormonalna terapia zastêpcza (HTZ) ze szczególnym uwzglêdnieniem estradiolu podawanego przezskórnie
 Hormonalna terapia zastêpcza (HTZ) ze szczególnym uwzglêdnieniem estradiolu podawanego przezskórnie Dr n. med. Wojciech Kluszczyk 1 Dr n. med. Adam Kwieciñski 2 1 Specjalista ginekolog-po³o nik, Szpital
Hormonalna terapia zastêpcza (HTZ) ze szczególnym uwzglêdnieniem estradiolu podawanego przezskórnie Dr n. med. Wojciech Kluszczyk 1 Dr n. med. Adam Kwieciñski 2 1 Specjalista ginekolog-po³o nik, Szpital
Fetuina i osteopontyna u pacjentów z zespołem metabolicznym
 Fetuina i osteopontyna u pacjentów z zespołem metabolicznym Dr n med. Katarzyna Musialik Katedra Chorób Wewnętrznych, Zaburzeń Metabolicznych i Nadciśnienia Tętniczego Uniwersytet Medyczny w Poznaniu *W
Fetuina i osteopontyna u pacjentów z zespołem metabolicznym Dr n med. Katarzyna Musialik Katedra Chorób Wewnętrznych, Zaburzeń Metabolicznych i Nadciśnienia Tętniczego Uniwersytet Medyczny w Poznaniu *W
Leki antykachektyczne. lek. med. Marta Bijak-Ulejczyk Oddział Anestezjologii i Intensywnej Terapii
 Leki antykachektyczne lek. med. Marta Bijak-Ulejczyk Oddział Anestezjologii i Intensywnej Terapii Grupy leków czyli co mamy środki stymulujące apetyt leki modulujące pracę przewodu pokarmowego leki anaboliczne/antykataboliczne
Leki antykachektyczne lek. med. Marta Bijak-Ulejczyk Oddział Anestezjologii i Intensywnej Terapii Grupy leków czyli co mamy środki stymulujące apetyt leki modulujące pracę przewodu pokarmowego leki anaboliczne/antykataboliczne
HORMONY STERYDOWE I PODOBNIE DZIAŁAJĄCE
 HORMONY STERYDOWE I PODOBNIE DZIAŁAJĄCE Są to związki należące do grupy steroidów, które charakteryzują się wykazywaniem istotnych aktywności biologicznych typu hormonalnego. Docierając do komórki docelowej,
HORMONY STERYDOWE I PODOBNIE DZIAŁAJĄCE Są to związki należące do grupy steroidów, które charakteryzują się wykazywaniem istotnych aktywności biologicznych typu hormonalnego. Docierając do komórki docelowej,
Aneks II. Wnioski naukowe i podstawy zmiany warunków pozwoleń na dopuszczenie do obrotu
 Aneks II Wnioski naukowe i podstawy zmiany warunków pozwoleń na dopuszczenie do obrotu 20 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej produktów leczniczych zawierających lewonorgestrel
Aneks II Wnioski naukowe i podstawy zmiany warunków pozwoleń na dopuszczenie do obrotu 20 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej produktów leczniczych zawierających lewonorgestrel
Dr hab. med. Mirosław Dziuk, prof. nadzw. Kierownik Zakładu Medycyny Nuklearnej WIM Warszawa
 Dr hab. med. Mirosław Dziuk, prof. nadzw. Kierownik Zakładu Medycyny Nuklearnej WIM Warszawa ROZPOZNAWANIE: PET - CT W ONKOLOGII poszukiwanie ognisk choroby - wczesne wykrywanie różnicowanie zmian łagodnych
Dr hab. med. Mirosław Dziuk, prof. nadzw. Kierownik Zakładu Medycyny Nuklearnej WIM Warszawa ROZPOZNAWANIE: PET - CT W ONKOLOGII poszukiwanie ognisk choroby - wczesne wykrywanie różnicowanie zmian łagodnych
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Biosteron lekam, 25 mg, tabletki. (Dehydroepiandrosteronum)
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Biosteron lekam, 25 mg, tabletki (Dehydroepiandrosteronum) Należy zapoznać się z treścią ulotki przed zażyciem leku. - Należy zachować tę ulotkę, aby w razie
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Biosteron lekam, 25 mg, tabletki (Dehydroepiandrosteronum) Należy zapoznać się z treścią ulotki przed zażyciem leku. - Należy zachować tę ulotkę, aby w razie
Tyreologia opis przypadku 9
 Kurs Polskiego Towarzystwa Endokrynologicznego Tyreologia opis przypadku 9 partner kursu: (firma nie ma wpływu na zawartość merytoryczną) Tyreologia Opis przypadku European Society of Endocrinology Clinical
Kurs Polskiego Towarzystwa Endokrynologicznego Tyreologia opis przypadku 9 partner kursu: (firma nie ma wpływu na zawartość merytoryczną) Tyreologia Opis przypadku European Society of Endocrinology Clinical
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Fem 7; 50 µg/24 h (1,5 mg), system transdermalny 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy system transdermalny Fem 7 zawiera 1,5 mg estradiolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Fem 7; 50 µg/24 h (1,5 mg), system transdermalny 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy system transdermalny Fem 7 zawiera 1,5 mg estradiolu
