PRZEDSTAWICIELE ZAWODÓW MEDYCZNYCH (HCP) Gedeon Richter Polska Sp. z o.o.
|
|
|
- Mikołaj Górecki
- 6 lat temu
- Przeglądów:
Transkrypt
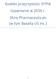
1 PRZEDSTAWICIELE ZAWODÓW MEDYCZNYCH (HCP) Gedeon Richter Polska Sp. z o.o. Imię i nazwisko HCP Umowy cywilno-prawne Łączna kwota wynagrodzenia za usługi Liczba wydarzeń zorganizowanych przez podmioty zewnętrzne, w jakich uczestniczył HCP 1 Krajowe Zagraniczne, na terenie UE Zagraniczne, poza terenem UE Liczba wydarzeń zorganizowanych przez Gedeon Polska Sp. z o.o., w jakich uczestniczył dany HCP 2 Krajowe Zagraniczne, na terenie UE Zagraniczne, poza terenem UE Liczba przypadków zwiedzania zakładów produkcyjnych Gedeon Richter Polska Sp. z o.o. HCP 3 beneficjentów HCP, którzy nie wyrazili Kwota łączna dla HCP, którzy nie wyrazili dla HCP, którzy nie wyrazili dla HCP, którzy nie wyrazili dla HCP, którzy nie wyrazili zgody na dla HCP, którzy nie wyrazili dla HCP, którzy nie wyrazili dla HCP, którzy nie wyrazili zgody na dla HCP, którzy nie wyrazili ,87 PLN Ujawnieniu podlegają wydarzenia, dla których wśród finansowanych świadczeń znalazły się: opłaty rejestracyjne i/lub koszty transportu i/lub zakwaterowania 2 Ujawnieniu podlegają wydarzenia, dla których wśród finansowanych świadczeń znalazły się koszty transportu i/lub zakwaterowania. 3 Ujawnieniu podlegają przypadki zwiedzania, w związku z którymi poniesiono koszty przelotu lub zakwaterowania. 1
2 Nazwa HCO ORGANIZACJE OCHRONY ZDROWIA (HCO) Gedeon Richter Polska Sp. z o.o. Wynagrodzenie za usługi 45 Łączna kwota wynagrodzenia (z wyłączeniem umów związanych z R&D i badaniem rynku) Darowizny/sponsoring Pieniężne Rzeczowe Produktów Warszawski Uniwersytet Medyczny 1 500, , Polskie Towarzystwo Studentów Farmacji 3 000, , Warszawski Uniwersytet Medyczny 1 500, , Naczelna Izba Aptekarska , , Dzień Polskiej Farmacji , , Polskie Towarzystwo Studentów Farmacji 3 000, , Polskie Towarzystwo Studentów Farmacji 6 000, , Wojewódzki Szpital Zespolony im. dr Romana Ostrzyckiego w Koninie przy ul. Szpitalnej 45; Oddział kardiologii Stowarzyszenie na Rzecz Rozwoju Profilaktyki i Leczenia Chorób Kobiecych Katowice, ul. Medyków 14 Fundacja Serce Dziecka im. Diny Radziwiłłowej Warszawą, ul. Relaksowa 59 Polskie Towarzystwo Kardiologiczne Oddział Gdańsk, ul. Dębinki 11 Przekazanie grantów naukowych 640, , , , , , , , Instytut Psychiatrii i Neurologii w Warszawie , , Narodowy Instytut Zdrowia Publicznego Państwowy Zakład Higieny, ul. Chocimska 24, Warszawa Samodzielny Publiczny Specjalistyczny Szpital Zachodni im. Św. Jana Pawła II w Grodzisku Mazowieckim, ul. Daleka , , , , Podsumowanie łączna kwota dla wszystkich HCO Podsumowanie łączna kwota dla wszystkich HCO Podsumowanie łączna kwota dla wszystkich HCO Podsumowanie łączna kwota dla wszystkich HCO Podsumowanie łączna kwota dla wszystkich HCO 4 Wynagrodzenie może obejmować: płatności za usługi doradcze, w tym konsultacje, wykłady, udział w panelu ekspertów. 5 Wynagrodzenie za badania rozwojowe oraz badania rynku są wyłączone z zakresu raportowania na podstawie Kodeksu Etyki. 2
3 , , , ORGANIZACJE PACJENCKIE (PAG) Gedeon Richter Polska Sp. z o.o. Nazwa organizacji Kategoria przekazania wartości Cel/opis przekazania wartości Łączna wartość przekazanych korzyści Polskie Amazonki Ruch Społeczny Sponsoring Cele statutowe ,00 3
4 NOTA METODOLOGICZNA 1. WSTĘP CEL I PODSTAWA RAPORTOWANIA W związku z tym, że Polski Związek Pracodawców Przemysłu Farmaceutycznego (PZPPF) jest sygnatariuszem Kodeksu Etyki Medicines for Europe (dawniej The European Generic and Biosimilar Medicines Association EGA; Europejskie Stowarzyszenie Producentów Leków Generycznych), Przedsiębiorcy zrzeszeni w PZPPF mają również obowiązek ujawnić Transfery Korzyści oraz przygotować notę opisującą metodologię. Niniejsza nota została przygotowana w celu wypełnienia tego obowiązku. Każdy Przedsiębiorca, członek PZPPF, będący sygnatariuszem Kodeksu Etyki, ma za zadanie opublikować notę opisującą metodologię, jaką zastosował podczas przygotowania, ujawnienia i określenia Transferów Korzyści dla każdej ujawnianej kategorii. Nota dotyczy terytorium Polski. 2. ZAKRES DEFINICJI Kodeks Medicines for Europe (EGA) Kodeks postępowania członków Medicines for Europe (dawniej The European Generic and Biosimilar Medicines Association EGA) w relacjach ze środowiskiem służby zdrowia. Kodeks reguluje relacje w odniesieniu do leków na receptę (RX). Leki bez recepty (OTC) są produktami opartymi na wyborze pacjentów, dlatego nie są objęte zakresem Kodeksu Medicines for Europe. Członkowie Medicines for Europe (EGA) Przedsiębiorstwa członkowskie Medicines for Europe (EGA) (w tym podmioty powiązane z przedsiębiorstwami członkowskimi Medicines for Europe (EGA)) oraz krajowe stowarzyszenie należące do Medicines for Europe (EGA) (w tym członkowie podmiotów powiązanych z krajowymi stowarzyszeniami należącymi do Medicines for Europe (EGA)). Osoba wykonująca zawód medyczny (HCP) - Każda osoba fizyczna, która jest lekarzem, osobą wykonującą zawód lekarza, lekarza dentysty, farmaceuty i technika farmacji, pielęgniarki i położnej, ratownika medycznego, diagnosty laboratoryjnego, felczera lub starszego felczera, bądź też każda inna osoba, która w trakcie wykonywania obowiązków służbowych może przepisywać, kupować, dostarczać, zalecać lub podawać produkt leczniczy. Dla uniknięcia wątpliwości, definicja osoby wykonującej zawód medyczny obejmuje: każdego urzędnika lub pracownika agencji rządowej lub innej organizacji (w sektorze publicznym lub prywatnym), który może przepisywać, wydawać, kupować lub podawać produkty lecznicze, oraz każdego pracownika przedsiębiorstwa farmaceutycznego, którego podstawowym wykonywanym zawodem jest zawód praktykującej osoby wykonującej zawód medyczny, jednak nie obejmuje (x) wszelkich innych pracowników przedsiębiorstwa farmaceutycznego oraz (y) hurtowni lub dystrybutora produktów leczniczych. Organizacja ochrony zdrowia (HCO) Każdy podmiot, który jest organizacją medyczną lub naukową, z zakresu ochrony zdrowia lub medycyny, niezależnie od jego formy organizacyjnej lub prawnej. Za organizację ochrony zdrowia nie są uważani przedsiębiorcy prowadzący obrót hurtowy lub detaliczny produktami leczniczymi. Usługi komercyjne świadczone przez apteki i sieci apteczne nie podlegają raportowaniu. Organizacje pacjentów (PO) Organizacje non-profit, które są skoncentrowane na pacjentach, i w których pacjenci lub ich opiekunowie stanowią większość członków organów zarządczych. Organizacje non-profit, w organach w których zasiadają HCP, traktowane są jako organizacje ochrony zdrowia. 4
5 3. ZAKRES PRZEDMIOTOWY PUBLIKACJI Gedeon Richter Polska Sp. z o.o. postanowił o publikacji Raportu przejrzystości ujawniającego transfery zdefiniowanych niżej świadczeń na rzecz HCP, HCO i PO. Z zakresu raportowania wyłączono HCP, którzy są zatrudnieni przez Gedeon Richter Polska Sp. z o.o. na podstawie umowy o pracę, jako pracownicy etatowi. 4. DEFINICJA ŚWIADCZENIA (ang. Transfer of value ) Na potrzeby raportowania przyjęto, że przekazanie świadczenia obejmuje wszelkie Transfery Korzyści do HCP, HCO lub PO obejmujące: a) Transfery pieniężne do HCP (wynagrodzenie za wykonanie usług na podstawie umów cywilno prawnych obejmujących przeprowadzenie wykładu lub prelekcji, pełnienie roli eksperta w panelu doradczym, uczestnictwo w grupie focusowej lub innej usługi doradczej. Wynagrodzenia w związku z pracami badawczo-rozwojowymi luba badaniami rynkowymi są wyłączone z zakresu niniejszego raportowania. b) Wsparcie edukacyjne, organizowanie spotkań oraz wizyty w zakładzie produkcyjnym Gedeon Richter Polska Sp. z o.o. w tym zakresie członkowie Medicines for Europe mają do wyboru dwie opcje ujawniania i mogą zdecydować, którą opcję przyjąć w przypadku ujawniania informacji w tej kategorii: Opcja 1 Liczba wydarzeń, w których udział HCP był sponsorowany. Wsparcie będzie ujawniane w następujących kategoriach i podkategoriach: Wydarzenia naukowe organizowane przez osobę trzecią (w przypadkach, gdy Gedeon Richter Polska Sp. z o.o. pokrył opłaty rejestracyjne, koszty podróży lub zakwaterowania) wraz z podaniem czy jest to wydarzenie odbywające się w kraju, w Europie czy poza Europą. Wizyty w zakładzie produkcyjnym Gedeon Richter Polska Sp. z o.o. (w przypadku, gdy w związku z wizytą poniesiono koszt zakwaterowania w hotelu lub/i podróży lotniczej). Spotkania organizowane przez Gedeon Richter Polska Sp. z o.o. (w przypadku, gdy poniesiono koszt zakwaterowania w hotelu lub/i podróży lotniczej), wraz z podaniem czy jest to wydarzenie odbywające się w kraju, Europie czy poza Europą. Opcja 2 Suma kwot wsparcia udzielonego HCP na poszczególne wydarzenia naukowe. Wsparcie będzie ujawniane w następujących kategoriach i podkategoriach: Wydarzenia naukowe organizowane przez osobę trzecią (w przypadku, gdy Gedeon Richter Polska Sp. z o.o. pokrył opłaty rejestracyjne, koszty podróży lub zakwaterowania), publikacji podlega: i. Nazwa wydarzenia naukowego, ii. Łączna kwota wydana na każde wydarzenie naukowe, iii. Liczba Przedstawicieli Zawodów Medycznych (HCP), którzy otrzymali finansowe wsparcie uczestnictwa w danym wydarzeniu naukowym. Wizyty w zakładzie produkcyjnym Gedeon Richter Polska Sp. z o.o. (w przypadku, gdy w związku z wizytą poniesiono koszt zakwaterowania w hotelu lub/i podróży lotniczej), publikacji podlega: i. Łączna wydatkowana kwota, ii. Liczba Przedstawicieli Zawodów Medycznych (HCP), którzy otrzymali finansowe wsparcie uczestnictwa. 5
6 Spotkania organizowane przez Gedeon Richter Polska Sp. z o.o. lub (w przypadku, gdy poniesiono koszt zakwaterowania w hotelu lub/i podróży lotniczej), publikacji podlega: i. Łączna wydatkowana kwota, ii. Liczba Przedstawicieli Zawodów Medycznych (HCP), którzy otrzymali finansowe wsparcie uczestnictwa. c) Transfery pieniężne do HCO (wynagrodzenie) za wykonanie usług na podstawie umów cywilno prawnych, obejmujących przeprowadzenie wykładu lub prelekcji, pełnienie roli eksperta w panelu doradczym, uczestnictwo w grupie focusowej lub innej usługi doradczej. Wynagrodzenia w związku z pracami badawczo-rozwojowymi lub badaniami rynkowymi są wyłączone z zakresu niniejszego raportowania. d) Darowizny i granty przekazane HCO (w tym darowizny pieniężne, rzeczowe i produktowe). e) Sponsoring działalności PO (w tym darowizny pieniężne i rzeczowe przekazane PO), z informacją o wartości i celu przekazania transferu. 5. WARTOŚĆ ŚWIADCZENIA a) W Raportach świadczenia zostały przedstawione w kwotach netto, bez podatku VAT. b) W sytuacjach, w których rozdzielenie wartości świadczenia byłoby niemożliwe, np. podatek przy przekazaniu świadczenia został pobrany u źródła, ujawniono kwotę świadczenia razem z wartością podatku. c) Darowizny rzeczowe i produktowe zostały przedstawione według detalicznej wartości rynkowej. W przypadku darowizn rzeczowych przyjęto cenę zakupu. d) Wartość świadczeń przedstawiana jest w polskich złotych. W przypadku przekazania świadczenia w walucie obcej, jego wartość została przeliczona na polskie złote według kursu NBP z dnia przekazania świadczenia. e) Wartość świadczeń przekazywanych na podstawie umów wieloletnich została przedstawiona w Raportach w kwocie przypisanej do danego roku kalendarzowego. 6. DATA PRZEKAZANIA ŚWIADCZENIA a) W przypadku świadczeń polegających na dostarczaniu usług dla Gedeon Richter Polska Sp. z o.o. lub udzielaniu przez nie grantów lub darowizn pieniężnych, za datę świadczenia przyjęto datę dokonania zapłaty (wykonania przelewu bankowego). W tym przypadku nie ma znaczenia data faktycznego wykonania usługi (np. wygłoszenia wykładu) lub wykorzystania grantu lub darowizny. b) W przypadku darowizn produktowych lub rzeczowych, za datę przekazania świadczenia przyjęto datę protokołu przekazania. c) W przypadku innych rodzajów świadczeń, np. sponsorowania udziału w wydarzeniach o charakterze naukowym, za datę przekazania świadczenia przyjęto datę pierwszego dnia wydarzenia, które było przedmiotem sponsoringu. 7. ZGODA NA UPUBLICZNIENIE DANYCH W SPOSÓB ZINDYWIDUALIZOWANY Zgoda na udostępnienie danych osobowych HCP w Raporcie Przejrzystości, była zbierana po zakończeniu roku, którego dotyczy raportowanie, tj. ujawnienie danych w Raporcie obejmującym Transfery Korzyści przekazane HCP w 2017 roku były zbierane w 2018 roku. Formularz zgody zawierał wszystkie Transfery podlegające raportowaniu, przekazane HCP w 2017 r. Zgoda lub brak zgody obejmowała wszystkie przekazane Transfery Korzyści. To oznacza, że nie było możliwe wyrażenie zgody przez HCP na ujawnienie danych dotyczących tylko części aktywności, w których brał on udział. 6
7 7.1. Ochrona danych osobowych Zgodnie z pkt 7.3 Kodeksu Medicines for Europe (EGA), EGA przy upublicznianiu Raportu Przejrzystości, zobowiązana jest przestrzegać obowiązujących przepisów prawa dotyczących ochrony danych osobowych. Z przepisów tych wynika obowiązek uzyskania zgody poszczególnych HCP na opublikowanie w Raporcie Przejrzystości ich danych osobowych. Aby zgoda HCP była wiążąca, musi być: udzielona dobrowolnie konkretna jednoznaczna wynikiem świadomej decyzji Ponieważ zgoda jednostki stanowi podstawę do publikacji, HCP zachowują prawo do odmowy ujawnienia swoich danych oraz przysługujące im na mocy przepisów prawo do poprawiania błędów lub usunięcia informacji. Tym samym, transfery do HCP, wobec których spełniono obowiązek informacyjny i którzy wyrazili zgodę na publikację ich danych osobowych, zostali ujęci w Raporcie pod imieniem i nazwiskiem. Transfery do HCP, wobec których spełniono obowiązek informacyjny i którzy nie wyrazili publikację ich danych osobowych, zostali ujęci w Raporcie danych zagregowanych Odmowa zgody i wycofanie zgody Dane dotyczące HCP, którzy odmówili udzielenia publikację, sumuje się i ujawnia w sposób zagregowany bez wskazania imion i nazwisk tych osób. W przypadku wycofania przez HCP upublicznienie danych, Gedeon Richter Polska Sp. z o.o. zobowiązane jest do usunięcia tych danych z Raportu Przejrzystości niezwłocznie. Jeżeli wycofanie stąpiło przed upublicznieniem danych, Gedeon Richter Polska Sp. z o.o. zapewnia, żeby dane dotyczące Transferów Wartości przekazanych danemu HCP w okresie raportowania, udostępnione zostały w formie zbiorczej. Jeżeli wycofanie stąpi po upublicznieniu Raportu Przejrzystości, Gedeon Richter Polska Sp. z o.o. wprowadzi odpowiednie poprawki do Raportu. W takiej sytuacji Gedeon Richter Polska Sp. z o.o. nie ponosi jednak odpowiedzialności za dane pobrane z Raportu upublicznionego przed wycofaniem zgody przez HCP. Zarówno odmowa udzielenia zgody jak i jej późniejsze wycofanie pozostaje bez wpływu na współpracę między HCP a Gedeon Richter Polska Sp. z o.o. Postanowienia o których mowa w pkt stosuje się w przypadku wyboru Opcji 1, o której mowa w pkt PUBLIKACJA DANYCH 7
8 Zgodnie treścią pkt 7.4 Kodeksu Medicines For Europe (EGA), Gedeon Richter Polska Sp. z o.o. powinny ujawniać Transfery Korzyści w taki sposób, aby umożliwić do nich publiczny dostęp. Publikacja Raportu Przejrzystości nastąpi za pośrednictwem strony internetowej zaś dane zagregowane dla wszystkich członków EGA oraz linki do Raportów indywidualnych na centralnej platformie należącej do PZPPF. 9. CZĘSTOTLIWOŚĆ UJAWNIANIA DANYCH Zgodnie z treścią pkt 7.7 Kodeksu Medicines For Europe (EGA), ujawnień należy dokonywać w odstępach rocznych, a każdy okres sprawozdawczy obejmuje pełny rok kalendarzowy. Pierwszym okresem sprawozdawczym będzie rok Ujawnienie powinno nastąpić najpóźniej w ciągu 6 miesięcy od zakończenia danego okresu sprawozdawczego. Oznacza to, że wszystkie podlegające ujawnieniu Transfery Korzyści przekazane w pierwszym okresie sprawozdawczym zostaną ujawnione najpóźniej do 29 czerwca 2018 roku. Kolejne Raporty Przejrzystości będą publikowane raz w roku do 30 czerwca. Raport Przejrzystości z danego okresu sprawozdawczego będzie dostępny w miejscu jego publikacji przez okres 3 lat. 8
NOTA METODOLOGICZNA. 1. Wstęp cel i podstawa raportowania
 NOTA METODOLOGICZNA 1. Wstęp cel i podstawa raportowania W związku z tym, że Polski Związek Pracodawców Przemysłu Farmaceutycznego (PZPPF) jest sygnatariuszem Kodeksu Etyki Medicines for Europe (dawniej
NOTA METODOLOGICZNA 1. Wstęp cel i podstawa raportowania W związku z tym, że Polski Związek Pracodawców Przemysłu Farmaceutycznego (PZPPF) jest sygnatariuszem Kodeksu Etyki Medicines for Europe (dawniej
Raport Przejrzystości Nota metodologiczna
 Raport Przejrzystości 2018 Nota metodologiczna SPIS TREŚCI 1. Wstęp cel i podstawa raportowania... 2 2. Definicje... 3 3. Spółki dokonujące publikacji Raportu Przejrzystości... 3 4. Świadczenia podlegające
Raport Przejrzystości 2018 Nota metodologiczna SPIS TREŚCI 1. Wstęp cel i podstawa raportowania... 2 2. Definicje... 3 3. Spółki dokonujące publikacji Raportu Przejrzystości... 3 4. Świadczenia podlegające
Raport Przejrzystości Nota metodologiczna
 Raport Przejrzystości 2017 Nota metodologiczna SPIS TREŚCI 1. stęp cel i podstawa raportowania... 2 2. Definicje... 3 3. Spółki z Grupy Adamed dokonujące publikacji Raportu Przejrzystości... 4 4. Transfery
Raport Przejrzystości 2017 Nota metodologiczna SPIS TREŚCI 1. stęp cel i podstawa raportowania... 2 2. Definicje... 3 3. Spółki z Grupy Adamed dokonujące publikacji Raportu Przejrzystości... 4 4. Transfery
NOTA METODOLOGICZNA I. WSTĘP
 NOTA METODOLOGICZNA I. WSTĘP Będąc członkiem Polskiego Związku Pracodawców Przemysłu Farmaceutycznego (PZPPF), który jest sygnatariuszem Kodeksu Etyki Europejskiego Stowarzyszenia Firm Generycznych (Medicines
NOTA METODOLOGICZNA I. WSTĘP Będąc członkiem Polskiego Związku Pracodawców Przemysłu Farmaceutycznego (PZPPF), który jest sygnatariuszem Kodeksu Etyki Europejskiego Stowarzyszenia Firm Generycznych (Medicines
NOTA METODOLOGICZNA I. WSTĘP
 NOTA METODOLOGICZNA I. WSTĘP Będąc członkiem Polskiego Związku Pracodawców Przemysłu Farmaceutycznego (PZPPF), który jest sygnatariuszem Kodeksu Etyki Europejskiego Stowarzyszenia Firm Generycznych (Medicines
NOTA METODOLOGICZNA I. WSTĘP Będąc członkiem Polskiego Związku Pracodawców Przemysłu Farmaceutycznego (PZPPF), który jest sygnatariuszem Kodeksu Etyki Europejskiego Stowarzyszenia Firm Generycznych (Medicines
7. ZASADY I WYMAGANIA DOTYCZĄCE PRZEJRZYSTOŚCI Ujawnianie Transferów Korzyści. Transfer Korzyści przekazywanie
 7. ZASADY I WYMAGANIA DOTYCZĄCE PRZEJRZYSTOŚCI 7.1. Ujawnianie Transferów Korzyści Transfer Korzyści przekazywanie Transfer Korzyści obejmuje jakiekolwiek świadczenia pieniężne lub niepieniężne przekazane
7. ZASADY I WYMAGANIA DOTYCZĄCE PRZEJRZYSTOŚCI 7.1. Ujawnianie Transferów Korzyści Transfer Korzyści przekazywanie Transfer Korzyści obejmuje jakiekolwiek świadczenia pieniężne lub niepieniężne przekazane
Data publikacji 28 czerwca 2019 r.
 Metodologia działań firmy Bristol-Myers Squibb (BMS) podejmowanych w związku z Kodeksem Przejrzystości EFPIA dotyczącym świadczeń o określonej wartości na rzecz przedstawicieli zawodów medycznych i organizacji
Metodologia działań firmy Bristol-Myers Squibb (BMS) podejmowanych w związku z Kodeksem Przejrzystości EFPIA dotyczącym świadczeń o określonej wartości na rzecz przedstawicieli zawodów medycznych i organizacji
Data publikacji 30 czerwca 2017 r.
 Metodologia działań firmy Bristol-Myers Squibb (BMS) podejmowanych w związku z Kodeksem Przejrzystości EFPIA dotyczącym świadczeń o określonej wartości na rzecz przedstawicieli zawodów medycznych i organizacji
Metodologia działań firmy Bristol-Myers Squibb (BMS) podejmowanych w związku z Kodeksem Przejrzystości EFPIA dotyczącym świadczeń o określonej wartości na rzecz przedstawicieli zawodów medycznych i organizacji
1. Sposób ustalenia wartości świadczenia a. b. 2. Sposób publikacji informacji o świadczeniach: a. b. 3. Data przekazania świadczenia
 1. Sposób ustalenia wartości świadczenia a. Świadczenia zostały wskazane w kwocie całkowitej poniesionej przez Spółkę. b. Jeżeli dane świadczenie zostało przekazane przez spółkę Angelini Pharma Polska
1. Sposób ustalenia wartości świadczenia a. Świadczenia zostały wskazane w kwocie całkowitej poniesionej przez Spółkę. b. Jeżeli dane świadczenie zostało przekazane przez spółkę Angelini Pharma Polska
Nota metodologiczna do Raportu Przejrzystości - Boehringer Ingelheim Marketing Sp. z o.o.
 Kodeks Przejrzystości Nota metodologiczna do Raportu Przejrzystości - Boehringer Ingelheim Marketing Sp. z o.o. Poniższy dokument to nota metodologiczna, która szczegółowo określa wynikające z Kodeksu
Kodeks Przejrzystości Nota metodologiczna do Raportu Przejrzystości - Boehringer Ingelheim Marketing Sp. z o.o. Poniższy dokument to nota metodologiczna, która szczegółowo określa wynikające z Kodeksu
NOTA METODOLOGICZNA WSTĘP
 NOTA METODOLOGICZNA WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony zdrowia od dawna jest motorem napędowym rozwoju w dziedzinie opieki nad pacjentem i postępu innowacyjnej
NOTA METODOLOGICZNA WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony zdrowia od dawna jest motorem napędowym rozwoju w dziedzinie opieki nad pacjentem i postępu innowacyjnej
Nota metodologiczna Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA (ZPIFF INFARMA)
 Kodeks Przejrzystości Nota metodologiczna Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA (ZPIFF INFARMA) WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony
Kodeks Przejrzystości Nota metodologiczna Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA (ZPIFF INFARMA) WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony
INFARMA (ZPIFF INFARMA)
 Eli Lilly Polska Sp. z o.o. ul. Żwirki i Wigury 18A, 02-092 Warszawa Poland +48 22 306 0944 www.lilly.pl Kodeks Przejrzystości Nota metodologiczna Związku Pracodawców Innowacyjnych Firm Farmaceutycznych
Eli Lilly Polska Sp. z o.o. ul. Żwirki i Wigury 18A, 02-092 Warszawa Poland +48 22 306 0944 www.lilly.pl Kodeks Przejrzystości Nota metodologiczna Związku Pracodawców Innowacyjnych Firm Farmaceutycznych
Nota Metodologiczna spółki MSD Polska dotycząca raportowania danych zgodnie z Kodeksem Przejrzystości ZPIFF INFARMA
 Nota Metodologiczna spółki MSD Polska dotycząca raportowania danych zgodnie z Kodeksem Przejrzystości ZPIFF INFARMA Wprowadzenie MSD Polska Sp. z o.o. (MSD) uważa, że profesjonalne relacje między firmami
Nota Metodologiczna spółki MSD Polska dotycząca raportowania danych zgodnie z Kodeksem Przejrzystości ZPIFF INFARMA Wprowadzenie MSD Polska Sp. z o.o. (MSD) uważa, że profesjonalne relacje między firmami
Data publikacji 30 czerwca 2016 r.
 Nota metodologiczna określająca, wynikające z Kodeksu Przejrzystości, zasady publikacji informacji na temat świadczeń przekazanych w 2015 roku przez firmę Bristol-Myers Squibb (BMS/Spółka) przedstawicielom
Nota metodologiczna określająca, wynikające z Kodeksu Przejrzystości, zasady publikacji informacji na temat świadczeń przekazanych w 2015 roku przez firmę Bristol-Myers Squibb (BMS/Spółka) przedstawicielom
Wzór noty metodologicznej Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA (ZPIFF INFARMA)
 Wzór noty metodologicznej ZPIFF INFARMA 8.12.2015 Kodeks Przejrzystości Wzór noty metodologicznej Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA (ZPIFF INFARMA) WSTĘP Współpraca między
Wzór noty metodologicznej ZPIFF INFARMA 8.12.2015 Kodeks Przejrzystości Wzór noty metodologicznej Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA (ZPIFF INFARMA) WSTĘP Współpraca między
METODOLOGIA. Strona 1 z 7. Nota Metodologiczna Chiesi Poland Sp. z o.o
 METODOLOGIA sposobu udostępnienia przez Chiesi Poland Sp. z o.o. informacji na temat świadczeń przekazanych przez Chiesi Poland Sp. z o.o. i spółki z jej grupy kapitałowej na rzecz Przedstawicieli Zawodów
METODOLOGIA sposobu udostępnienia przez Chiesi Poland Sp. z o.o. informacji na temat świadczeń przekazanych przez Chiesi Poland Sp. z o.o. i spółki z jej grupy kapitałowej na rzecz Przedstawicieli Zawodów
Nota metodologiczna Wprowadzenie Definicje
 Nota metodologiczna Wprowadzenie MSD Polska uważa, że wzajemne oddziaływania pomiędzy firmami farmaceutycznymi oraz Przedstawicielami zawodów medycznych mają istotny i pozytywny wpływ na jakość leczenia
Nota metodologiczna Wprowadzenie MSD Polska uważa, że wzajemne oddziaływania pomiędzy firmami farmaceutycznymi oraz Przedstawicielami zawodów medycznych mają istotny i pozytywny wpływ na jakość leczenia
KODEKS PRZEJRZYSTOŚCI EUROPEJSKIEJ FEDERACJI PRZEMYSŁU FARMACEUTYCZNEGO I STOWARZYSZEŃ EFPIA 2015 r.
 KODEKS PRZEJRZYSTOŚCI EUROPEJSKIEJ FEDERACJI PRZEMYSŁU FARMACEUTYCZNEGO I STOWARZYSZEŃ EFPIA 2015 r. Szanowni Państwo, Pfizer Polska regularnie współpracuje z Przedstawicielami zawodów medycznych (HCPs)
KODEKS PRZEJRZYSTOŚCI EUROPEJSKIEJ FEDERACJI PRZEMYSŁU FARMACEUTYCZNEGO I STOWARZYSZEŃ EFPIA 2015 r. Szanowni Państwo, Pfizer Polska regularnie współpracuje z Przedstawicielami zawodów medycznych (HCPs)
Zasady współpracy z organizacjami ochrony zdrowia i organizatorami wydarzeń naukowych
 16 kwietnia 2015 r. Zasady współpracy z organizacjami ochrony zdrowia i organizatorami wydarzeń naukowych Jednym z celów działalności innowacyjnych firm farmaceutycznych zrzeszonych w Związku Pracodawców
16 kwietnia 2015 r. Zasady współpracy z organizacjami ochrony zdrowia i organizatorami wydarzeń naukowych Jednym z celów działalności innowacyjnych firm farmaceutycznych zrzeszonych w Związku Pracodawców
2018 Metodologia 1. ZOBOWIĄZANIE FIRMY ASTELLAS
 1. ZOBOWIĄZANIE FIRMY ASTELLAS 2018 Metodologia 1.1 Współpraca przedstawicieli zawodów medycznych i organizacji ochrony zdrowia od dawna jest pozytywnym czynnikiem postępu w opiece nad pacjentem oraz w
1. ZOBOWIĄZANIE FIRMY ASTELLAS 2018 Metodologia 1.1 Współpraca przedstawicieli zawodów medycznych i organizacji ochrony zdrowia od dawna jest pozytywnym czynnikiem postępu w opiece nad pacjentem oraz w
2016 Metodologia UDOSTĘPNIANIE INFORMACJI O ŚWIADCZENIACH: STRESZCZENIE METODY
 2016 Metodologia WPROWADZENIE Współpraca przedstawicieli zawodów medycznych i organizacji ochrony zdrowia od dawna jest pozytywnym czynnikiem postępu w opiece nad pacjentem oraz w osiągnięciach innowacyjnej
2016 Metodologia WPROWADZENIE Współpraca przedstawicieli zawodów medycznych i organizacji ochrony zdrowia od dawna jest pozytywnym czynnikiem postępu w opiece nad pacjentem oraz w osiągnięciach innowacyjnej
Zakres przedmiotowy publikacji - Transfer Korzyści raport za 2017 i nota metodologiczna
 W związku z faktem, że każdy Przedsiębiorca, członek PZPPF (jakim jest VIPHARM S.A.), będący sygnatariuszem Kodeksu Medicines For Europe (EGA), ma obowiązek ujawnić Transfery Korzyści i opublikować notę
W związku z faktem, że każdy Przedsiębiorca, członek PZPPF (jakim jest VIPHARM S.A.), będący sygnatariuszem Kodeksu Medicines For Europe (EGA), ma obowiązek ujawnić Transfery Korzyści i opublikować notę
LEO Pharma Sp. z o.o NOTA METODOLOGICZNA
 LEO Pharma Sp. z o.o NOTA METODOLOGICZNA Strona 1 z 8 Kodeks Przejrzystości WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony zdrowia od dawna jest motorem napędowym
LEO Pharma Sp. z o.o NOTA METODOLOGICZNA Strona 1 z 8 Kodeks Przejrzystości WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony zdrowia od dawna jest motorem napędowym
Kodeks Przejrzystości. Nota metodologiczna Boehringer Ingelheim Marketing Sp. z o.o.
 Kodeks Przejrzystości Nota metodologiczna Boehringer Ingelheim Marketing Sp. z o.o. Poniższy dokument to nota metodologiczna, która szczegółowo określa wynikające z Kodeksu Przejrzystości zasady publikacji
Kodeks Przejrzystości Nota metodologiczna Boehringer Ingelheim Marketing Sp. z o.o. Poniższy dokument to nota metodologiczna, która szczegółowo określa wynikające z Kodeksu Przejrzystości zasady publikacji
Kodeks Przejrzystości. Nota metodologiczna Teva Pharmaceuticals Polska Sp. z o.o. WSTĘP
 Kodeks Przejrzystości Nota metodologiczna Teva Pharmaceuticals Polska Sp. z o.o. WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony zdrowia od dawna jest motorem napędowym
Kodeks Przejrzystości Nota metodologiczna Teva Pharmaceuticals Polska Sp. z o.o. WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony zdrowia od dawna jest motorem napędowym
Celgene Sp. z o.o. Nota metodologiczna
 Celgene Sp. z o.o. Nota metodologiczna podsumowująca metodologię przyjętą na potrzeby przygotowania do publicznego udostępnienia informacji o świadczeniach przekazanych przedstawicielom ochrony zdrowia
Celgene Sp. z o.o. Nota metodologiczna podsumowująca metodologię przyjętą na potrzeby przygotowania do publicznego udostępnienia informacji o świadczeniach przekazanych przedstawicielom ochrony zdrowia
LEO Pharma Sp. z o.o NOTA METODOLOGICZNA
 LEO Pharma Sp. z o.o NOTA METODOLOGICZNA Strona 1 z 8 Kodeks Przejrzystości WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony zdrowia od dawna jest motorem napędowym
LEO Pharma Sp. z o.o NOTA METODOLOGICZNA Strona 1 z 8 Kodeks Przejrzystości WSTĘP Współpraca między przedstawicielami zawodów medycznych a organizacjami ochrony zdrowia od dawna jest motorem napędowym
Nota metodologiczna firmy Roche Polska Sp. z o. o.
 Nota metodologiczna firmy Roche Polska Sp. z o. o. Czym jest Kodeks Przejrzystości? Kodeks Przejrzystości jest zbiorem zasad przyjętych przez innowacyjne firmy farmaceutyczne zrzeszone w Europejskiej Federacji
Nota metodologiczna firmy Roche Polska Sp. z o. o. Czym jest Kodeks Przejrzystości? Kodeks Przejrzystości jest zbiorem zasad przyjętych przez innowacyjne firmy farmaceutyczne zrzeszone w Europejskiej Federacji
KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA
 KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA Preambuła Kodeks Przejrzystości stanowi zasady udostępniania opinii publicznej informacji na temat współpracy firm
KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA Preambuła Kodeks Przejrzystości stanowi zasady udostępniania opinii publicznej informacji na temat współpracy firm
2018 TOV. Koszty poniesione w związku z Wydarzeniami. Koszty podróży i zakwaterowania. Opłaty rejestracyjne
 2018 TOV 1. Świadczenia uzyskane przez Przedstawicieli zawodów medycznych ŚWIADCZENIA PRZEKAZANE PRZEZ (Actelion) i spółki z jego grupy kapitałowej z siedzibą poza terytorium Polski Imię i nazwisko Dokładny
2018 TOV 1. Świadczenia uzyskane przez Przedstawicieli zawodów medycznych ŚWIADCZENIA PRZEKAZANE PRZEZ (Actelion) i spółki z jego grupy kapitałowej z siedzibą poza terytorium Polski Imię i nazwisko Dokładny
Nota Metodologiczna UCB
 Nota Metodologiczna UCB Na podstawie Kodeksu Przejrzystości EFPIA (sekcja 3.05) Niniejsza nota opisuje stanowisko UCB dotyczące Kodeksu Przejrzystości EFPIA, z uwzględnieniem różnic wynikających z polskich
Nota Metodologiczna UCB Na podstawie Kodeksu Przejrzystości EFPIA (sekcja 3.05) Niniejsza nota opisuje stanowisko UCB dotyczące Kodeksu Przejrzystości EFPIA, z uwzględnieniem różnic wynikających z polskich
Tytuł: Nota Metodologiczna Sandoz Polska
 Tytuł: Nota Metodologiczna Sandoz Polska Publikacja świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w związku z Kodeksem Przejrzystości
Tytuł: Nota Metodologiczna Sandoz Polska Publikacja świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w związku z Kodeksem Przejrzystości
Kodeks Przejrzystości. Nota metodologiczna Boehringer Ingelheim Marketing Sp. z o.o.
 Kodeks Przejrzystości Nota metodologiczna Boehringer Ingelheim Marketing Sp. z o.o. Poniższy dokument to nota metodologiczna, która szczegółowo określa wynikające z Kodeksu Przejrzystości zasady publikacji
Kodeks Przejrzystości Nota metodologiczna Boehringer Ingelheim Marketing Sp. z o.o. Poniższy dokument to nota metodologiczna, która szczegółowo określa wynikające z Kodeksu Przejrzystości zasady publikacji
Novo Nordisk Pharma Sp. z o.o. Dokument dotyczący metodologii rok 2015 ( Metodologia )
 Novo Nordisk Pharma Sp. z o.o. Dokument dotyczący metodologii rok 2015 ( Metodologia ) Spis treści Preambuła... 3 1. Ogólne podsumowanie... 4 2. i definicje... 6 2 z 13 Preambuła Novo Nordisk Pharma Sp.
Novo Nordisk Pharma Sp. z o.o. Dokument dotyczący metodologii rok 2015 ( Metodologia ) Spis treści Preambuła... 3 1. Ogólne podsumowanie... 4 2. i definicje... 6 2 z 13 Preambuła Novo Nordisk Pharma Sp.
Informacje za 2018 rok
 Nota metodologiczna dotycząca wymogów Grupy LEO w zakresie publikowania informacji o świadczeniach na rzecz przedstawicieli zawodów medycznych i organizacji ochrony zdrowia (w tym wytyczne lokalne spółki
Nota metodologiczna dotycząca wymogów Grupy LEO w zakresie publikowania informacji o świadczeniach na rzecz przedstawicieli zawodów medycznych i organizacji ochrony zdrowia (w tym wytyczne lokalne spółki
Tytuł: Nota Metodologiczna Novartis Poland
 Tytuł: Nota Metodologiczna Novartis Poland dotycząca publikacji świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w 2017 r. w związku
Tytuł: Nota Metodologiczna Novartis Poland dotycząca publikacji świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w 2017 r. w związku
Tytuł: Nota Metodologiczna Alcon Polska Sp. z o.o.
 Tytuł: Nota Metodologiczna Alcon Polska Sp. z o.o. dotycząca publikacji świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w 2016 r. w
Tytuł: Nota Metodologiczna Alcon Polska Sp. z o.o. dotycząca publikacji świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w 2016 r. w
Projekt rozporządzenia Ministra Zdrowia. w sprawie sposobu i zakresu kontroli systemu monitorowania bezpieczeństwa stosowania produktów leczniczych
 Projekt rozporządzenia Ministra Zdrowia w sprawie sposobu i zakresu kontroli systemu monitorowania bezpieczeństwa stosowania produktów leczniczych Przekazany do uzgodnień zewnętrznych w dniu 26 kwietnia
Projekt rozporządzenia Ministra Zdrowia w sprawie sposobu i zakresu kontroli systemu monitorowania bezpieczeństwa stosowania produktów leczniczych Przekazany do uzgodnień zewnętrznych w dniu 26 kwietnia
Nota Metodologiczna Sandoz Polska
 Nota Metodologiczna Sandoz Polska Publikacja świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w związku z Kodeksem Przejrzystości Związku
Nota Metodologiczna Sandoz Polska Publikacja świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w związku z Kodeksem Przejrzystości Związku
Nota Metodologiczna Sandoz Polska
 Nota Metodologiczna Sandoz Polska Publikacja świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w związku z Kodeksem Przejrzystości Związku
Nota Metodologiczna Sandoz Polska Publikacja świadczeń przekazywanych na rzecz Przedstawicieli Zawodów Medycznych ( HCP ) oraz Organizacji Ochrony Zdrowia ( HCO ) w związku z Kodeksem Przejrzystości Związku
AstraZeneca Pharma Poland Sp. z o.o Postępu 14, Warszawa
 Informowanie o korzyściach przekazywanych Pracownikom służby zdrowia oraz Organizacjom ochrony zdrowia Dokument na temat metodologii zgłaszania danych za rok 2016 w 2017 r. AstraZeneca Pharma Poland Sp.
Informowanie o korzyściach przekazywanych Pracownikom służby zdrowia oraz Organizacjom ochrony zdrowia Dokument na temat metodologii zgłaszania danych za rok 2016 w 2017 r. AstraZeneca Pharma Poland Sp.
Kodeks Przejrzystości EFPIA / INFARMA. Nota Metodologiczna
 Kodeks Przejrzystości EFPIA / INFARMA Nota Metodologiczna SANOFI POLSKA Czerwiec 2018 r. SPIS TREŚCI EuDisclose Wprowadzenie... 2 Jakie wymogi przewiduje kodeks przejrzystości EFPIA?... 3 W jaki sposób
Kodeks Przejrzystości EFPIA / INFARMA Nota Metodologiczna SANOFI POLSKA Czerwiec 2018 r. SPIS TREŚCI EuDisclose Wprowadzenie... 2 Jakie wymogi przewiduje kodeks przejrzystości EFPIA?... 3 W jaki sposób
Kodeks Przejrzystości EFPIA / INFARMA. Nota Metodologiczna
 Kodeks Przejrzystości EFPIA / INFARMA Nota Metodologiczna SANOFI POLSKA Czerwiec 2017 r. SPIS TREŚCI EuDisclose SPIS TREŚCI... 1 wprowadzenie... 2 JAKIE WYMOGI PRZEWIDUJE KODEKS PRZEJRZYSTOŚCI EFPIA?...
Kodeks Przejrzystości EFPIA / INFARMA Nota Metodologiczna SANOFI POLSKA Czerwiec 2017 r. SPIS TREŚCI EuDisclose SPIS TREŚCI... 1 wprowadzenie... 2 JAKIE WYMOGI PRZEWIDUJE KODEKS PRZEJRZYSTOŚCI EFPIA?...
Informowanie o korzyś ciach przekazywanych Przedśtawicielom zawodo w medycznych (PZM, ang. HCP) oraz Organizacjom ochrony zdrowia (OOZ, ang.
 Informowanie o korzyś ciach przekazywanych Przedśtawicielom zawodo w medycznych (PZM, ang. HCP) oraz Organizacjom ochrony zdrowia (OOZ, ang. HCO) Dokument na temat metodologii zgłaszania danych za rok
Informowanie o korzyś ciach przekazywanych Przedśtawicielom zawodo w medycznych (PZM, ang. HCP) oraz Organizacjom ochrony zdrowia (OOZ, ang. HCO) Dokument na temat metodologii zgłaszania danych za rok
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2008 r. w sprawie kontroli seryjnej wstępnej produktów leczniczych weterynaryjnych
 Projekt 30.09.08 r. ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2008 r. w sprawie kontroli seryjnej wstępnej produktów leczniczych weterynaryjnych Na podstawie art. 65 ust. 10 ustawy z dnia 6 września 2001
Projekt 30.09.08 r. ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2008 r. w sprawie kontroli seryjnej wstępnej produktów leczniczych weterynaryjnych Na podstawie art. 65 ust. 10 ustawy z dnia 6 września 2001
SZCZEGÓŁOWE PRAWA PACJENTA W PRZEPISACH PRAWNYCH
 SZCZEGÓŁOWE PRAWA PACJENTA W PRZEPISACH PRAWNYCH 1. Prawo do ochrony zdrowia (art. 68 ust. 1 Konstytucji RP). 2. Prawo do równego dostępu do świadczeń opieki zdrowotnej finansowanej ze środków publicznych,
SZCZEGÓŁOWE PRAWA PACJENTA W PRZEPISACH PRAWNYCH 1. Prawo do ochrony zdrowia (art. 68 ust. 1 Konstytucji RP). 2. Prawo do równego dostępu do świadczeń opieki zdrowotnej finansowanej ze środków publicznych,
U S T A W A z dnia 2007 r. o zmianie ustawy Prawo farmaceutyczne oraz o zmianie niektórych innych ustaw 1)
 PROJEKT 26.01.07r. U S T A W A z dnia 2007 r. o zmianie ustawy Prawo farmaceutyczne oraz o zmianie niektórych innych ustaw 1) Art. 1. W ustawie z dnia 6 września 2001 r. Prawo farmaceutyczne (Dz. U. z
PROJEKT 26.01.07r. U S T A W A z dnia 2007 r. o zmianie ustawy Prawo farmaceutyczne oraz o zmianie niektórych innych ustaw 1) Art. 1. W ustawie z dnia 6 września 2001 r. Prawo farmaceutyczne (Dz. U. z
Nota Metodologiczna 2015 r.
 Nota Metodologiczna 2015 r. Dokument określający wynikające z Kodeksu Przejrzystości zasady publikacji informacji na temat świadczeń przekazanych Przedstawicielom Zawodów Medycznych oraz Organizacjom Ochrony
Nota Metodologiczna 2015 r. Dokument określający wynikające z Kodeksu Przejrzystości zasady publikacji informacji na temat świadczeń przekazanych Przedstawicielom Zawodów Medycznych oraz Organizacjom Ochrony
z dnia 12 marca 2008 r. (Dz.U. Nr 57, poz. 347)
 Rozporządzenie Ministra Zdrowia w sprawie określenia szczegółowych zasad i trybu wstrzymywania i wycofywania z obrotu produktów leczniczych i wyrobów medycznych z dnia 12 marca 2008 r. (Dz.U. Nr 57, poz.
Rozporządzenie Ministra Zdrowia w sprawie określenia szczegółowych zasad i trybu wstrzymywania i wycofywania z obrotu produktów leczniczych i wyrobów medycznych z dnia 12 marca 2008 r. (Dz.U. Nr 57, poz.
INFARMA KODEKS. zdrowia i organizatorami wydarzeń naukowych ", który dołączamy do tego listu. Marny nadzieję,
 ZPIFF/86/PSzJ20 15/KK Warszawa, 16 kwietnia 2015 r. Szanowna Pani Małgorzata Majer Prezes Stowarzyszenie Menedżerów Opieki Zdrowotnej Szanowna Pani, Od l stycznia 2015 roku 31 innowacyjne fumy farmaceutyczne
ZPIFF/86/PSzJ20 15/KK Warszawa, 16 kwietnia 2015 r. Szanowna Pani Małgorzata Majer Prezes Stowarzyszenie Menedżerów Opieki Zdrowotnej Szanowna Pani, Od l stycznia 2015 roku 31 innowacyjne fumy farmaceutyczne
Na podstawie art. 47b ust. 3 ustawy z dnia 6 września 2001 r. - Prawo farmaceutyczne (Dz. U. z 2008 r. Nr 45 poz. 271) zarządza się, co następuje:
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia... 2008 r. w sprawie wysokości i sposobu pokrywania kosztów związanych z przeprowadzeniem inspekcji przez inspektorów do spraw wytwarzania Głównego Inspektoratu
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia... 2008 r. w sprawie wysokości i sposobu pokrywania kosztów związanych z przeprowadzeniem inspekcji przez inspektorów do spraw wytwarzania Głównego Inspektoratu
RAPORT PRZEJRZYSTOŚCI 2016
 RAPORT PRZEJRZYSTOŚCI 2016 1. Świadczenia uzyskane przez Przedstawicieli zawodów medycznych ŚWIADCZENIA PRZEKAZANE PRZEZ ACTELION PHARMA POLSKA Sp. z o.o. i spółki z jego grupy kapitałowej z siedzibą poza
RAPORT PRZEJRZYSTOŚCI 2016 1. Świadczenia uzyskane przez Przedstawicieli zawodów medycznych ŚWIADCZENIA PRZEKAZANE PRZEZ ACTELION PHARMA POLSKA Sp. z o.o. i spółki z jego grupy kapitałowej z siedzibą poza
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 marca 2008 r.
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 marca 2008 r. w sprawie określenia szczegółowych zasad i trybu wstrzymywania i wycofywania z obrotu produktów leczniczych i wyrobów medycznych (Dz. U. z dnia
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 marca 2008 r. w sprawie określenia szczegółowych zasad i trybu wstrzymywania i wycofywania z obrotu produktów leczniczych i wyrobów medycznych (Dz. U. z dnia
Gdzie szczepić: ZOZ-Y czy apteki? Propozycje nowych rozwiązań
 Gdzie szczepić: ZOZ-Y czy apteki? Konferencja GRYPA 2013/2014 16 kwietnia 2013 Warszawa Propozycje nowych rozwiązań Dr n. med. Agnieszka Mastalerz-Migas Katedra i Zakład Medycyny Rodzinnej Uniwersytetu
Gdzie szczepić: ZOZ-Y czy apteki? Konferencja GRYPA 2013/2014 16 kwietnia 2013 Warszawa Propozycje nowych rozwiązań Dr n. med. Agnieszka Mastalerz-Migas Katedra i Zakład Medycyny Rodzinnej Uniwersytetu
KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA
 KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA 1 INFARMA KODEKS PRZEJRZYSTOŚCI KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA
KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA 1 INFARMA KODEKS PRZEJRZYSTOŚCI KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA
Autopoprawka do projektu ustawy o zmianie ustawy - Prawo farmaceutyczne oraz o zmianie niektórych innych ustaw (druk sejmowy nr 1775)
 Autopoprawka do projektu ustawy o zmianie ustawy - Prawo farmaceutyczne oraz o zmianie niektórych innych ustaw (druk sejmowy nr 1775) W projekcie ustawy o zmianie ustawy Prawo farmaceutyczne oraz o zmianie
Autopoprawka do projektu ustawy o zmianie ustawy - Prawo farmaceutyczne oraz o zmianie niektórych innych ustaw (druk sejmowy nr 1775) W projekcie ustawy o zmianie ustawy Prawo farmaceutyczne oraz o zmianie
KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA
 KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA KODEKS PRZEJRZYSTOŚCI KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA Preambuła
KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA KODEKS PRZEJRZYSTOŚCI KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA Preambuła
Opiniowanie Kandydatów na kierowników aptek lub hurtowni.
 Katowice 2008-12-17 Opiniowanie Kandydatów na kierowników aptek lub hurtowni. Opiniowanie Kandydatów na kierowników i wydawanie rękojmi należytego prowadzenia apteki lub hurtowni odbywa się w ŚIA według
Katowice 2008-12-17 Opiniowanie Kandydatów na kierowników aptek lub hurtowni. Opiniowanie Kandydatów na kierowników i wydawanie rękojmi należytego prowadzenia apteki lub hurtowni odbywa się w ŚIA według
Kodeks Etyki Związku Pracodawców Aptecznych PharmaNET. Preambuła. Związek Pracodawców Aptecznych PharmaNET oraz jego Członkowie, mając na uwadze:
 Kodeks Etyki Związku Pracodawców Aptecznych PharmaNET Preambuła Związek Pracodawców Aptecznych PharmaNET oraz jego Członkowie, mając na uwadze: funkcję apteki jako placówki zdrowia publicznego, której
Kodeks Etyki Związku Pracodawców Aptecznych PharmaNET Preambuła Związek Pracodawców Aptecznych PharmaNET oraz jego Członkowie, mając na uwadze: funkcję apteki jako placówki zdrowia publicznego, której
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r.
 PROJEKT 29.12.2004 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia...2004 r. zmieniające rozporządzenie w sprawie ustalenia cen urzędowych hurtowych i detalicznych na produkty lecznicze i wyroby medyczne Na
PROJEKT 29.12.2004 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia...2004 r. zmieniające rozporządzenie w sprawie ustalenia cen urzędowych hurtowych i detalicznych na produkty lecznicze i wyroby medyczne Na
STATUT. Samodzielnego Publicznego Zakładu Opieki Zdrowotnej Zespołu Opieki Zdrowotnej w Głuchołazach. Rozdział I Postanowienia ogólne
 Załącznik do Uchwały Nr XV/183/12 Rady Powiatu w Nysie z 27 kwietnia 2012r STATUT Samodzielnego Publicznego Zakładu Opieki Zdrowotnej Zespołu Opieki Zdrowotnej w Głuchołazach Rozdział I Postanowienia ogólne
Załącznik do Uchwały Nr XV/183/12 Rady Powiatu w Nysie z 27 kwietnia 2012r STATUT Samodzielnego Publicznego Zakładu Opieki Zdrowotnej Zespołu Opieki Zdrowotnej w Głuchołazach Rozdział I Postanowienia ogólne
Marketing w handlu - marketing w medycynie i farmacji. Agnieszka Wilk
 Marketing w handlu - marketing w medycynie i farmacji Agnieszka Wilk w.agnieszka@vp.pl Agenda 1. Marketing mix (4 P w farmacji) 2. Struktura marketingu w firmie farmaceutycznej 3. Podstawy regulacji prawnych
Marketing w handlu - marketing w medycynie i farmacji Agnieszka Wilk w.agnieszka@vp.pl Agenda 1. Marketing mix (4 P w farmacji) 2. Struktura marketingu w firmie farmaceutycznej 3. Podstawy regulacji prawnych
Brak uwag w podanym terminie pozwolę sobie potraktować jako rezygnację ze składania uwag i uzgodnienie treści przedmiotowego projektu.
 Warszawa, 14 stycznia 2019 FZP.0210.3.2019.KW/AW Według rozdzielnika Szanowni Państwo, stosownie do postanowień 35, 36 i 38 uchwały nr 190 Rady Ministrów z dnia 29 października 2013 r. Regulamin pracy
Warszawa, 14 stycznia 2019 FZP.0210.3.2019.KW/AW Według rozdzielnika Szanowni Państwo, stosownie do postanowień 35, 36 i 38 uchwały nr 190 Rady Ministrów z dnia 29 października 2013 r. Regulamin pracy
I. Postanowienia ogólne. 1 Zakres regulacji
 Regulamin świadczenia pomocy publicznej w ramach Projektu Małopolski Park Technologii Informacyjnych Ośrodek Innowacyjności Krakowskiego Parku Technologicznego realizowanego w ramach Programu Operacyjnego
Regulamin świadczenia pomocy publicznej w ramach Projektu Małopolski Park Technologii Informacyjnych Ośrodek Innowacyjności Krakowskiego Parku Technologicznego realizowanego w ramach Programu Operacyjnego
Uwaga metodologiczna Gilead w sprawie sprawozdawczości zapewniającej przejrzystość
 Uwaga metodologiczna Gilead w sprawie sprawozdawczości zapewniającej przejrzystość Spis treści 1 Wprowadzenie... 2 2 Definicja Świadczeń... 2 3 Definicja Świadczeń Transgranicznych oraz postępowanie z
Uwaga metodologiczna Gilead w sprawie sprawozdawczości zapewniającej przejrzystość Spis treści 1 Wprowadzenie... 2 2 Definicja Świadczeń... 2 3 Definicja Świadczeń Transgranicznych oraz postępowanie z
USTAWA z dnia 6 września 2001 r.
 Kancelaria Sejmu s. 1/9 USTAWA z dnia 6 września 2001 r. Opracowano na podstawie: Dz.U. z 2001 r. Nr 126, poz. 1382. Przepisy wprowadzające ustawę - Prawo farmaceutyczne, ustawę o wyrobach medycznych oraz
Kancelaria Sejmu s. 1/9 USTAWA z dnia 6 września 2001 r. Opracowano na podstawie: Dz.U. z 2001 r. Nr 126, poz. 1382. Przepisy wprowadzające ustawę - Prawo farmaceutyczne, ustawę o wyrobach medycznych oraz
Opinia do ustawy o zmianie ustawy o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych oraz niektórych innych ustaw.
 Warszawa, 15 września 2014 r. Opinia do ustawy o zmianie ustawy o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych oraz niektórych innych ustaw (druk nr 708) I. Cel i przedmiot ustawy
Warszawa, 15 września 2014 r. Opinia do ustawy o zmianie ustawy o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych oraz niektórych innych ustaw (druk nr 708) I. Cel i przedmiot ustawy
ROZPORZĄDZENIE MINISTRA ZDROWIA1)
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r. w sprawie wymagań, jakim powinna odpowiadać osoba wykwalifikowana odpowiedzialna za jakość i kontrolę serii produktu leczniczego przed wprowadzeniem na rynek
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r. w sprawie wymagań, jakim powinna odpowiadać osoba wykwalifikowana odpowiedzialna za jakość i kontrolę serii produktu leczniczego przed wprowadzeniem na rynek
Forum innowacyjna ochrona zdrowia
 Forum innowacyjna ochrona zdrowia Prawo dziś i jutro Marcin Długosz KAMSOFT S.A. Bezpieczeństwo dystrybucji raportowanie i wymiana danych z systemów informatycznych na rynku farmaceutycznym 2 Zmiany w
Forum innowacyjna ochrona zdrowia Prawo dziś i jutro Marcin Długosz KAMSOFT S.A. Bezpieczeństwo dystrybucji raportowanie i wymiana danych z systemów informatycznych na rynku farmaceutycznym 2 Zmiany w
IPSEN PROGRAM PRZEJRZYSTOŚCI EFPIA NOTA METODOLOGICZNA HISTORIA ZMIAN DOKUMENTU
 IPSEN PROGRAM PRZEJRZYSTOŚCI EFPIA NOTA METODOLOGICZNA HISTORIA ZMIAN DOKUMENTU DATA AUTOR WERSJA PRZYCZYNA ZMIAN 04/09/2015 Laetitia Minel 0.1 Utworzenie 04/01/2016 Laetitia Minel 0.2 Poprawki (przegląd
IPSEN PROGRAM PRZEJRZYSTOŚCI EFPIA NOTA METODOLOGICZNA HISTORIA ZMIAN DOKUMENTU DATA AUTOR WERSJA PRZYCZYNA ZMIAN 04/09/2015 Laetitia Minel 0.1 Utworzenie 04/01/2016 Laetitia Minel 0.2 Poprawki (przegląd
Regulacje prawne w zakresie badań naukowych. dr Monika Urbaniak
 Regulacje prawne w zakresie badań naukowych dr Monika Urbaniak Badania naukowe mogą przyjąć postać badań interwencyjnych i eksperymentów medycznych Pojęcie: badanie nieinterwencyjne oznacza, że wybór terapii
Regulacje prawne w zakresie badań naukowych dr Monika Urbaniak Badania naukowe mogą przyjąć postać badań interwencyjnych i eksperymentów medycznych Pojęcie: badanie nieinterwencyjne oznacza, że wybór terapii
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r. w sprawie warunków wysyłkowej sprzedaży produktów leczniczych wydawanych bez przepisu lekarza 2)
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r. w sprawie warunków wysyłkowej sprzedaży produktów leczniczych wydawanych bez przepisu lekarza 2) Na podstawie art. 68 ust. 3a ustawy z dnia 6 września 2001
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r. w sprawie warunków wysyłkowej sprzedaży produktów leczniczych wydawanych bez przepisu lekarza 2) Na podstawie art. 68 ust. 3a ustawy z dnia 6 września 2001
UCHWAŁA NR XXVII/187/12 RADY POWIATU BRZESKIEGO. z dnia 20 grudnia 2012 r. w sprawie statutu Brzeskiego Centrum Medycznego w Brzegu
 UCHWAŁA NR XXVII/187/12 RADY POWIATU BRZESKIEGO z dnia 20 grudnia 2012 r. w sprawie statutu Brzeskiego Centrum Medycznego w Brzegu Na podstawie art. 42 ust. 4 ustawy z dnia 15 kwietnia 2011 r. o działalności
UCHWAŁA NR XXVII/187/12 RADY POWIATU BRZESKIEGO z dnia 20 grudnia 2012 r. w sprawie statutu Brzeskiego Centrum Medycznego w Brzegu Na podstawie art. 42 ust. 4 ustawy z dnia 15 kwietnia 2011 r. o działalności
STATUT. SZPITALA SPECJALISTYCZNEGO IM. ŚWIĘTEJ RODZINY SAMODZIELNEGO PUBLICZNEGO ZAKŁADU OPIEKI ZDROWOTNEJ (tekst jednolity)
 Załącznik nr 4 do uchwały nr LVII/1487/2017 Rady m.st. Warszawy z dnia 16 listopada 2017 r. STATUT SZPITALA SPECJALISTYCZNEGO IM. ŚWIĘTEJ RODZINY SAMODZIELNEGO PUBLICZNEGO ZAKŁADU OPIEKI ZDROWOTNEJ (tekst
Załącznik nr 4 do uchwały nr LVII/1487/2017 Rady m.st. Warszawy z dnia 16 listopada 2017 r. STATUT SZPITALA SPECJALISTYCZNEGO IM. ŚWIĘTEJ RODZINY SAMODZIELNEGO PUBLICZNEGO ZAKŁADU OPIEKI ZDROWOTNEJ (tekst
KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA
 KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA 1 INFARMA KODEKS PRZEJRZYSTOŚCI KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA
KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA 1 INFARMA KODEKS PRZEJRZYSTOŚCI KODEKS PRZEJRZYSTOŚCI Związku Pracodawców Innowacyjnych Firm Farmaceutycznych INFARMA
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ. Warszawa, dnia 8 października 2019 r. Poz z dnia 11 września 2019 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 8 października 2019 r. Poz. 1905 USTAWA z dnia 11 września 2019 r. 1), 2) o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw Art.
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 8 października 2019 r. Poz. 1905 USTAWA z dnia 11 września 2019 r. 1), 2) o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw Art.
II. Zestawienie wykonanych kontroli w roku 2016.
 II. Zestawienie wykonanych kontroli w roku 2016. L p. Placówki podlegające nadzorowi i kontroli Plan kontroli Wykonanie kontroli Rodzaj wg stanu na dzień 31.12.2016 Ogółem w tym plano wych Planowe Spraw
II. Zestawienie wykonanych kontroli w roku 2016. L p. Placówki podlegające nadzorowi i kontroli Plan kontroli Wykonanie kontroli Rodzaj wg stanu na dzień 31.12.2016 Ogółem w tym plano wych Planowe Spraw
Sylabus A. INFORMACJE OGÓLNE
 Sylabus A. INFORMACJE OGÓLNE Nazwa Komentarz Nazwa Podstawy prawa zdrowia publicznego Kierunek studiów Zdrowie Publiczne Marketing i Zarządzanie Jednostka prowadząca Zakład Zdrowia Publicznego Kierownik
Sylabus A. INFORMACJE OGÓLNE Nazwa Komentarz Nazwa Podstawy prawa zdrowia publicznego Kierunek studiów Zdrowie Publiczne Marketing i Zarządzanie Jednostka prowadząca Zakład Zdrowia Publicznego Kierownik
Nota metodologiczna Kodeksy dotyczące ujawniania danych EFPIA i lokalnych stowarzyszeń branżowych
 Nota metodologiczna Kodeksy dotyczące ujawniania danych EFPIA i lokalnych stowarzyszeń branżowych SPIS TREŚCI SPIS TREŚCI... 2 1. WPROWADZENIE... 4 2. ZAKRES... 4 3. DEFINICJE... 5 4. GROMADZENIE DANYCH
Nota metodologiczna Kodeksy dotyczące ujawniania danych EFPIA i lokalnych stowarzyszeń branżowych SPIS TREŚCI SPIS TREŚCI... 2 1. WPROWADZENIE... 4 2. ZAKRES... 4 3. DEFINICJE... 5 4. GROMADZENIE DANYCH
Projekt, 07.03.2014 R. z dnia..2014 r.
 Projekt, 07.03.2014 R. R O Z P O R Z Ą D Z E N I E M I N I S T R A Z D R O W I A 1) z dnia..2014 r. w sprawie wykazu świadczeń opieki zdrowotnej wymagających uprzedniej zgody dyrektora oddziału wojewódzkiego
Projekt, 07.03.2014 R. R O Z P O R Z Ą D Z E N I E M I N I S T R A Z D R O W I A 1) z dnia..2014 r. w sprawie wykazu świadczeń opieki zdrowotnej wymagających uprzedniej zgody dyrektora oddziału wojewódzkiego
Polska-Katowice: Produkty farmaceutyczne 2019/S Ogłoszenie o zamówieniu. Dostawy
 1 / 6 Niniejsze ogłoszenie w witrynie : udl?uri=:notice:138195-2019:text:pl:html Polska-Katowice: Produkty farmaceutyczne 2019/S 060-138195 Ogłoszenie o zamówieniu Dostawy Legal Basis: Dyrektywa 2014/24/UE
1 / 6 Niniejsze ogłoszenie w witrynie : udl?uri=:notice:138195-2019:text:pl:html Polska-Katowice: Produkty farmaceutyczne 2019/S 060-138195 Ogłoszenie o zamówieniu Dostawy Legal Basis: Dyrektywa 2014/24/UE
Wymiana doświadczeń Piotr Banasiewicz Wydział Informacji i Współpracy z Regionami
 Wymiana doświadczeń Piotr Banasiewicz Wydział Informacji i Współpracy z Regionami Warszawa, 2017-04-21 PORTFOLIO PROJEKTÓW CSIOZ Platforma udostępniania on-line przedsiębiorcom usług i zasobów cyfrowych
Wymiana doświadczeń Piotr Banasiewicz Wydział Informacji i Współpracy z Regionami Warszawa, 2017-04-21 PORTFOLIO PROJEKTÓW CSIOZ Platforma udostępniania on-line przedsiębiorcom usług i zasobów cyfrowych
ZASADY UDZIELANIA ŚWIADCZEŃ ZDROWOTNYCH W OPARCIU O PRZEPISY DYREKTYWY TRANSGRANICZNEJ
 ZASADY UDZIELANIA ŚWIADCZEŃ ZDROWOTNYCH W OPARCIU O PRZEPISY DYREKTYWY TRANSGRANICZNEJ DYREKTYWA PE I RADY 2011/24/UE Z DNIA 9 MARCA 2011 R. W SPRAWIE STOSOWANIA PRAW PACJENTÓW W TRANSGRANICZNEJ OPIECE
ZASADY UDZIELANIA ŚWIADCZEŃ ZDROWOTNYCH W OPARCIU O PRZEPISY DYREKTYWY TRANSGRANICZNEJ DYREKTYWA PE I RADY 2011/24/UE Z DNIA 9 MARCA 2011 R. W SPRAWIE STOSOWANIA PRAW PACJENTÓW W TRANSGRANICZNEJ OPIECE
2. Rozporządzenie wchodzi w życie po upływie 14 dni od dnia ogłoszenia 3).
 24.12.2013 r. ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia.. r. w sprawie wzoru wniosku o zmianę zezwolenia na wytwarzanie lub import produktu leczniczego i badanego produktu leczniczego Na podstawie art.
24.12.2013 r. ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia.. r. w sprawie wzoru wniosku o zmianę zezwolenia na wytwarzanie lub import produktu leczniczego i badanego produktu leczniczego Na podstawie art.
Kodeks przejrzystości EFPIA Ujawnianie w 2016 r. Shire Pharmaceuticals (w tym Baxalta US Inc.)
 Kodeks przejrzystości EFPIA Ujawnianie w 2016 r. Shire Pharmaceuticals (w tym Baxalta US Inc.) 1 Część 1: Podejście do sprawozdawczości w odniesieniu do danych z 2016 r. W dniu 3 czerwca 2016 r. spółka
Kodeks przejrzystości EFPIA Ujawnianie w 2016 r. Shire Pharmaceuticals (w tym Baxalta US Inc.) 1 Część 1: Podejście do sprawozdawczości w odniesieniu do danych z 2016 r. W dniu 3 czerwca 2016 r. spółka
mgr DOROTA GRAŻYNA GNIEWOSZ Trutnov, 9 listopada 2016 r. CZ /0.0/0.0/15_005/000051
 mgr DOROTA GRAŻYNA GNIEWOSZ Trutnov, 9 listopada 2016 r. to zespół osób i instytucji mający za zadanie zapewnić opiekę zdrowotną ludności. Polski system opieki zdrowotnej oparty jest na modelu ubezpieczeniowym,
mgr DOROTA GRAŻYNA GNIEWOSZ Trutnov, 9 listopada 2016 r. to zespół osób i instytucji mający za zadanie zapewnić opiekę zdrowotną ludności. Polski system opieki zdrowotnej oparty jest na modelu ubezpieczeniowym,
Informacja o polityce prywatności dla pracowników służby zdrowia. Data: 1 lutego 2019 r
 Informacja o polityce prywatności dla pracowników służby zdrowia Data: 1 lutego 2019 r Biogen Poland Sp. z o.o. ( Biogen ) wchodzi w kontakty z pracownikami służby zdrowia ( HCP ) na wiele sposobów. Niniejsza
Informacja o polityce prywatności dla pracowników służby zdrowia Data: 1 lutego 2019 r Biogen Poland Sp. z o.o. ( Biogen ) wchodzi w kontakty z pracownikami służby zdrowia ( HCP ) na wiele sposobów. Niniejsza
Raport Konsultanta Wojewódzkiego w dziedzinie Psychologia Kliniczna za rok 2015
 Aleksandra Kühn-Dymecka Instytut Psychiatrii i Neurologii 02-957 Warszawa Al. Sobieskiego 9 Email dymecka@ipin.edu.pl tel., 224582534 Warszawa 01-02-2016 r Raport Konsultanta Wojewódzkiego w dziedzinie
Aleksandra Kühn-Dymecka Instytut Psychiatrii i Neurologii 02-957 Warszawa Al. Sobieskiego 9 Email dymecka@ipin.edu.pl tel., 224582534 Warszawa 01-02-2016 r Raport Konsultanta Wojewódzkiego w dziedzinie
Wydział Farmaceutyczny
 Fakultet przygotowany w ramach projektu WUM AID Akademia Innowacyjnej Dydaktyki Warszawskiego Uniwersytetu Medycznego współfinansowanego ze środków Europejskiego Funduszu Społecznego w ramach POWER 2014-2020
Fakultet przygotowany w ramach projektu WUM AID Akademia Innowacyjnej Dydaktyki Warszawskiego Uniwersytetu Medycznego współfinansowanego ze środków Europejskiego Funduszu Społecznego w ramach POWER 2014-2020
UMOWA Nr... o upoważnieniu do wystawiania recept na leki i wyroby medyczne podlegające refundacji
 Załącznik do Zarządzenia Prezesa Narodowego Funduszu Zdrowia Nr 41/2004 z dnia 25 listopada 2004 UMOWA Nr... o upoważnieniu do wystawiania recept na leki i wyroby medyczne podlegające refundacji zawarta
Załącznik do Zarządzenia Prezesa Narodowego Funduszu Zdrowia Nr 41/2004 z dnia 25 listopada 2004 UMOWA Nr... o upoważnieniu do wystawiania recept na leki i wyroby medyczne podlegające refundacji zawarta
I spotkanie Studenckiego Koła Naukowego Prawa Medycznego Warszawskiego Uniwersytetu Medycznego. Podsumowanie
 I spotkanie Studenckiego Koła Naukowego Prawa Medycznego Warszawskiego Uniwersytetu Medycznego Podsumowanie Wiedza i postawy studentów Warszawskiego Uniwersytetu Medycznego wobec rozszerzenia uprawień
I spotkanie Studenckiego Koła Naukowego Prawa Medycznego Warszawskiego Uniwersytetu Medycznego Podsumowanie Wiedza i postawy studentów Warszawskiego Uniwersytetu Medycznego wobec rozszerzenia uprawień
KATALOG AKTÓW PRAWNYCH ODNOSZĄCYCH SIĘ DO SZPITALA POWIATOWEGO W WOŁOMINIE SAMODZIELNEGO ZESPOŁU PUBLICZNYCH ZAKŁADÓW OPIEKI ZDROWOTNEJ
 KATALOG AKTÓW PRAWNYCH ODNOSZĄCYCH SIĘ DO SZPITALA POWIATOWEGO W WOŁOMINIE SAMODZIELNEGO ZESPOŁU PUBLICZNYCH ZAKŁADÓW OPIEKI ZDROWOTNEJ PRZEPISY OGÓLNE Dz.U.98.21.94 -j.t. ustawa 1974.06.26 Kodeks pracy.
KATALOG AKTÓW PRAWNYCH ODNOSZĄCYCH SIĘ DO SZPITALA POWIATOWEGO W WOŁOMINIE SAMODZIELNEGO ZESPOŁU PUBLICZNYCH ZAKŁADÓW OPIEKI ZDROWOTNEJ PRZEPISY OGÓLNE Dz.U.98.21.94 -j.t. ustawa 1974.06.26 Kodeks pracy.
PROJEKT Opłata ryczałtowa za lek podstawowy wynosi 3,20 zł. Opłata ryczałtowa za lek recepturowy wynosi 5 zł.
 Projekt rozporządzenia Ministra Zdrowia w sprawie wykazu leków, które mogą być traktowane jako surowce farmaceutyczne, wysokości opłaty ryczałtowej za leki podstawowe i recepturowe, ilości leku recepturowego,
Projekt rozporządzenia Ministra Zdrowia w sprawie wykazu leków, które mogą być traktowane jako surowce farmaceutyczne, wysokości opłaty ryczałtowej za leki podstawowe i recepturowe, ilości leku recepturowego,
Wymogi Europejskiej Federacji Producentów Leków i Stowarzyszeń Farmaceutycznych (EFPIA) w zakresie przejrzystości i ujawniania danych dotyczących
 Wymogi Europejskiej Federacji Producentów Leków i Stowarzyszeń Farmaceutycznych (EFPIA) w zakresie przejrzystości i ujawniania danych dotyczących współpracy z pracownikami służby zdrowia i organizacjami
Wymogi Europejskiej Federacji Producentów Leków i Stowarzyszeń Farmaceutycznych (EFPIA) w zakresie przejrzystości i ujawniania danych dotyczących współpracy z pracownikami służby zdrowia i organizacjami
Aspekty prawne Farmacji Szpitalnej. mgr Ewa Steckiewicz- Bartnicka wojewódzki konsultant w dziedzinie Farmacji Szpitalnej
 Aspekty prawne Farmacji Szpitalnej mgr Ewa Steckiewicz- Bartnicka wojewódzki konsultant w dziedzinie Farmacji Szpitalnej Podstawy prawne Ustawa z dnia 6 września 2001r. - Prawo farmaceutyczne ( Dz.U.2016.2142
Aspekty prawne Farmacji Szpitalnej mgr Ewa Steckiewicz- Bartnicka wojewódzki konsultant w dziedzinie Farmacji Szpitalnej Podstawy prawne Ustawa z dnia 6 września 2001r. - Prawo farmaceutyczne ( Dz.U.2016.2142
Polityka ochrony danych osobowych
 Polityka ochrony danych osobowych Art. 1 Administratorem Pana/Pani danych osobowych, a w tym dokumentacji medycznej, jest Wojciech J. Baranowski. Art. 2 W celu uzyskania bardziej szczegółowych informacji
Polityka ochrony danych osobowych Art. 1 Administratorem Pana/Pani danych osobowych, a w tym dokumentacji medycznej, jest Wojciech J. Baranowski. Art. 2 W celu uzyskania bardziej szczegółowych informacji
