JOURNAL OF CLINICAL ONCOLOGY
|
|
|
- Emilia Pawlik
- 8 lat temu
- Przeglądów:
Transkrypt
1 TOM 25 NUMER GRUDNIA 2007 JOURNAL OF CLINICAL ONCOLOGY PRACA ORYGINALNA Alemtuzumab w porównaniu z chlorambucilem jako leczenie pierwszej linii w przewlekłej białaczce limfocytowej Peter Hillmen, Aleksander B. Skotnicki, Tadeusz Robak, Branimir Jaksic, Anna Dmoszynska, Jingyang Wu, Cynthia Sirard i Jiri Mayer Leeds Teaching Hospitals NHS Trust, Leeds, United Kingdom; Jagiellionian University Collegium Medicum, Krakow; Kopernik Memorial Hospital, Lodz; Clinical Hospital No 1, Lublin, Poland; Clinical Hospital Merkur, Zagreb, Croatia; Genzyme Corp, Cambridge, MA; and the University Hospital Brno, Brno, Czech Republic. Otrzymano 5 czerwca 2007; zaakceptowano 8 sierpnia Opublikowano przed drukiem na stronie internetowej 5 listopada WspieraneprzezGenzymeCorp,Cambridge, MA. Częściowo zaprezentowano na 48. dorocznym spotkaniu Amerykańskiego Towarzystwa Hematologii, 9-12 Grudnia, 2006 roku, Orlando, FL. Oświadczenie autorów na temat potencjalnych konfliktów interesów oraz wkład poszczególnych autorów zamieszczono na końcu artykułu. Prośby o przedruki należy adresować: Peter Hillmen, MD, PhD, Leeds Teaching Hospitals National Health Service Trust, Leeds General Infirmary, Leeds, United Kingdom; peter.hillmen@nhs.net by American Society of Clinical Oncology X/07/ /$20.00 S T R E S Z C Z E N I E Cel Badanie randomizowane przeprowadzono, aby ocenić skuteczność i bezpieczeństwo dożylnego alemtuzumabu w porównaniu z chlorambucilem stosowanym jako leczenie pierwszej linii w przewlekłej białaczce limfocytowej (chronic lymphocytic leukemia, CLL). Chorzy i metody Pacjenci otrzymywali alemtuzumab (30 mg trzy razy w tygodniu, do 12 tygodni) lub chlorambucil (40 mg/m 2 co 28 dni, do 12 miesięcy). Głównym punktem końcowym było przeżycie wolne od progresji (progression-free survival, PFS). Drugorzędne punkty końcowe obejmowały całkowity odsetek odpowiedzi (overall response rate, ORR), całkowitych remisji (complete response, CR), czas do leczenia alternatywnego, bezpieczeństwo i całkowite przeżycie chorych. Wyniki W sposób randomizowany podzielono 297 pacjentów na dwie grupy, 149 przydzielono do leczenia alemtuzumabem i 148 do leczenia chlorambucilem. Alemtuzumab dawał lepsze PFS, z 42% obniżeniem ryzyka progresji lub zgonu (iloraz hazardu [hazard ratio, HR] = 0,58; P = 0,0001), a mediana czasu do leczenia alternatywnego wyniosła 23,3 względem 14,7 miesiąca dla chlorambucilu (HR = 0,54; P = 0,0001). ORR osiągnął 83% dla alemtuzumabu (24% CR) względem 55% dla chlorambucilu (2% CR); różnice w ORR i CR były wysoce istotne statystycznie (P! 0,0001). Eliminacja minimalnej choroby resztkowej nastąpiła u 11 spośród 36 pacjentów z całkowitą odpowiedzią dla alemtuzumabu, w grupie chlorambucilu nie było żadnego takiego pacjenta. Profil niepożądanych zdarzeń był podobny, z wyjątkiem większej liczby zdarzeń związanych z infuzją i wirusem cytomegalii (CMV) dla alemtuzumabu oraz większą częstością nudności i wymiotów dla chlorambucilu. Zdarzenia związane z CMV nie miały istotnego wpływu na skuteczność leczenia. Wniosek Zastosowanie alemtuzumabu jako leczenia pierwszej linii pacjentów z CLL w porównaniu z chlorambucilem wiązało się z istotną poprawą PFS, czasu do leczenia alternatywnego, ORR, CR, remisją bez minimalnej choroby resztkowej z przewidywalną i dającą się kontrolować toksycznością. J Clin Oncol 25: przez Amerykańskie Towarzystwo Onkologii Klinicznej. DOI: /JCO WSTĘP Różnorodność molekularna przewlekłej białaczki limfocytowej (chronic lymphocytic leukemia, CLL) wiąże się z długotrwałym przeżyciem części pacjentów, podczas gdy inni mają bardzo złe rokowanie. 1 Opcje terapii pierwszej linii obejmują chlorambucil, 2,3 jedyny lek zatwierdzony przez amerykańską Agencję ds. Żywności i Leków (Food And Drug Administration) do stosowania w pierwszej linii leczenia CLL (aż do ostatnio zarejestrowanego alemtuzumabu) i analog purynowy fludarabina. 4,5 Chemioterapia wielolekowa w CLL przyniosła poprawę odsetka odpowiedzi i przeżycia wolnego od progresji (progression-free survival, PFS), ale nie całkowitego przeżycia. 6,7 Eliminacja wykrywalnej minimalnej choroby resztkowej (minimal residual disease, MRD) wpływała na przedłużenie czasu przeżycia. 8 Nowe strategie leczenia CLL będą obejmować najaktywniejsze leki i będą dobierane pod względem molekularnych cech choroby specyficznych dla danego pacjenta. Według hierarchicznego modelu Döhnera 1 największy postęp choroby i wyniki leczenia korelują z delecjami 17p (lokalizacja genu p53) i 11q. Mutacje p53 w CLL związane są z opornością na chemioterapię, szczególnie na analogi puryn, oraz ze skróconym czasem przeżycia Dzieje się tak 207
2 Hillmen i wsp. najprawdopodobniej dlatego, że leki te indukują apoptozę poprzez szlaki zależne od p Istotne jest, aby zidentyfikować terapie CLL, które działają szlakami niezależnymi od p53 i mogą wyeliminować MRD. Alemtuzumab jest rekombinowanym, humanizowanym przeciwciałem monoklonalnym skierowanym przeciwko CD52, białku powierzchniowemu wykazującemu wysoką ekspresję na większości normalnych i nowotworowych limfocytach B i T, 14 ale nie na hematopoetycznych komórkach macierzystych. 15 U pacjentów po wznowie lub z oporną CLL po leczeniu fludarabiną i lekami alkilującymi alemtuzumab indukował całkowity odsetek odpowiedzi (overall response rate, ORR) rzędu 33%, w tym całkowitą odpowiedź (complete response, CR) u niektórych pacjentów, z dodatkowymi korzyściami klinicznymi u pacjentów ze stabilną chorobą. 16 Najczęstszymi toksycznościami były ostre reakcje 1. i 2. stopnia związane z infuzją, cytopenie i skłonność do infekcji związana z cytopeniami. Alemtuzumab wykazuje skuteczność u pacjentów z CLL oporną na fludarabinę i delecjami chromosomu 17p lub mutacjami genu p U niektórych pacjentów z CLL alemtuzumab eliminował MRD, co wiązało się z wydłużeniem czasu przeżycia. 8,20,21 Badanie fazy II z alemtuzumabem podawanym podskórnie w pierwszej linii leczenia CLL wykazało poprawę profilu bezpieczeństwa i ORR rzędu 87%, w tym 19% CR. 22,23 CAM307 był międzynarodowym, randomizowanym, otwartym badaniem fazy III porównującym alemtuzumab z chlorambucilem u wcześniej nieleczonych pacjentów z CLL wymagających rozpoczęcia leczenia. Pierwotnym punktem końcowym CAM307 był PFS. Drugorzędowe punkty końcowe obejmowały odsetek odpowiedzi, czas do alternatywnego leczenia, całkowite przeżycie i bezpieczeństwo. CHORZY I METODY Chorzy Pacjenci kwalifikujący się do badań mieli skończone 18 lat i potwierdzone rozpoznanie B-komórkowej CLL za pomocą cytometrii przepływowej, stopnia od I do IV wg Rai z progresją potwierdzoną wg kryteriów Grupy Roboczej Narodowego Instytutu Raka (National Cancer Institute Working Group, NCI- WG) z 1996 roku, 24 bez wcześniejszej chemioterapii dla CLL, z przewidywalnym przeżyciem co najmniej 12 tygodni, stanem sprawności 0 do 2 wg WHO oraz prawidłową czynnością nerek i wątroby. Kryteria wykluczenia obejmowały przewlekłe doustne stosowanie kortykosteroidów, małopłytkowość autoimmunologiczną, wcześniejszy przeszczep szpiku kostnego, CLL z zajęciem ośrodkowego układu nerwowego, dodatni test ilościowej reakcji łańcuchowej polimerazy (polymerase chain reaction, PCR)wkierunku wirusa cytomegalii (cytomegalovirus, CMV), dodatni test na HIV i obecność aktywnej infekcji. Analizę cytogenetyczną przed leczeniem prowadzono za pomocą fluorescencyjnej hybrydyzacji in situ na materiale pochodzącym z krwi obwodowej. Wyniki analizy cytogenetycznej nie były kryteriami włączenia do badań ani do stratyfikacji. Wszyscy pacjenci udzielili pisemnej świadomej zgody. Plan leczenia Pacjenci zostali w sposób randomizowany przydzieleni do ramienia z alemtuzumabem lub chlorambucilem (Ryc. A1, dostępna wyłącznie on-line). Przydzielenie do ramion leczenia było zrównoważone pomiędzy ośrodkami badań, wg stadium Rai (I i II względem III/IV), stanu sprawności (0 do 1 względem 2), wieku (! 65 względem " 65 lat), płci i maksymalnego rozmiaru węzłów chłonnych (niemacalne lub! 5 względem " 5 cm). Dawka alemtuzumabu była codziennie zwiększana (3, 10 i 30 mg) do czasu uzyskania tolerancji w dawce dożylnej (i.v.) 30 mg w ciągu 2 godzin. Następnie pacjenci otrzymywali alemtuzumab 30 mg 3 razy w tygodniu nie dłużej niż 12 tygodni, włączając w to fazę zwiększania dawki. Premedykacja przed alemtuzumabem składała się z difenhydraminy i acetaminofenu lub paracetamolu doustnie (paracetamol orally, PO) na 30 min przed podaniem, z dodatkową meperydyną lub hydrokortyzonem i.v. w razie potrzeby. W czasie pierwszego miesiąca leczenia pacjenci otrzymywali allopurinol w dniach od 1 do 13. Chorzy otrzymywali profilaktycznie trimetoprim/sulfametoksazol i famcyklowir (lub leki równoważne) podczas leczenia i przez co najmniej 2 miesiące po ostatniej dawce alemtuzumabu, aż liczba komórek CD4 + przekroczyła 200 komórek/\l. Stosowanie alemtuzumabu przerywano podczas ciężkich infekcji lub w przypadku wystąpienia toksyczności płucnej, nerkowej bądź wątrobowej co najmniej 3. stopnia. Dodatni wynik testu PCR w kierunku CMV prowadził do przerwania terapii z następczym powtórzeniem testu CMV PCR tydzień później. Leczenie wznawiano u pacjentów bez objawów, gdy powtórzony test był ujemny. Dodatni kontrolny test PCR i/lub objawy typowe dla aktywnego zakażenia CMV prowadziły do przerwania leczenia i terapii gancyklowirem i.v. lub równoważnej. Leczenia zaprzestawano, gdy opóźnienie przekraczało 4 tygodnie. Pacjenci leczeni w ramieniu z chlorambucilem otrzymywali dawkę 40 mg/m 2 PO co 28 dni, nie więcej niż 12 cykli, z allopurinolem PO w dniach od 1 to 8 w ciągu pierwszych trzech cykli. Nie było wymagane profilaktyczne stosowanie antybiotyków. Leczenie przerywano w przypadku wystąpienia toksycznościconajmniej3.stopnia,zredukcjądawkichlorambucilu o 50%, gdy dawkę podano ponownie po przerwie związanej z toksycznością co najmniej 3. stopnia, w tym w postaci toksyczności płucnej, nerkowej, wątrobowej bądź innej toksyczności niehematologicznej. W obu ramionach zaprzestawano leczenia, gdy u pacjenta zaobserwowano progresję choroby, nieakceptowalną toksyczność, niedokrwistość autoimmunologiczną lub autoimmunologiczną małopłytkowość. Następcze leczenie pozostawiono do decyzji lekarza prowadzącego. Ocena podczas badania Pacjentów oceniano, przeprowadzając badanie fizykalne, badania laboratoryjne i rtg klatki piersiowej (wyłącznie w trakcie leczenia) wg wskazań, a następnie w odstępach miesięcznych aż do progresji choroby, podania terapii alternatywnej lub przez 18 miesięcy od pierwszej dawki. Następnie pacjentów kontrolowano co 3 miesiące w celu oceny ewentualnej progresji choroby i całkowitego czasu przeżycia. Niezależny panel oceniający odpowiedź, nieznający przydzielonego leczenia, potwierdzał rozpoznanie CLL i stadium Rai oraz oceniał odpowiedź i datę progresji choroby u każdego pacjenta. Zdarzenia niepożądane (adverse event, AE) były stopniowane wg Common Toxicity Criteria (CTC) Narodowego Instytutu Raka (National Cancer Institute, NCI) wersja JOURNAL OF CLINICAL ONCOLOGY
3 Alemtuzumab z porównaniu z chlorambucilem jako leczenie pierwszej linii w CLL W ramieniu z alemtuzumabem badanie CMV metodą PCR wykonywano raz w tygodniu w czasie leczenia i co 2 tygodnie przez 2 miesiące od zakończenia terapii. W ramieniu z chlorambucilem badanie CMV metodą PCR wykonywano raz w miesiącu w czasie leczenia, po jego zakończeniu i miesiąc później. Bezpośredni i pośredni test Coombsa wykonywano przed rozpoczęciem leczenia, co miesiąc w trakcie badania oraz w chwili zakończenia terapii dla obu ramion. Cytometria przepływowa i analizy cytogenetyczne Cytometrię przepływową przeprowadzano na materiale pobranym z krwi obwodowej przed i w czasie badania w celu monitorowania odpowiedzi, a także w sytuacji, kiedy było to możliwe w szpiku kostnym przed leczeniem i w powtórnych badaniach. Przed rozpoczęciem badania wykonywano analizę interfazowej hybrydyzacji in situ z zastosowaniem 13 sond DNA dla wykrycia aberracji chromosomowych w obrębie 17p13.1 (p53), 13q14 (RB1, D13S319 i D13S25), 11q22-11q23 (ATM i MLL), 6q27 (subtelomeryczne), 6q21 (chromosom 6q21/sonda koktajlowa alpha satelity 6), trisomii 8q24 (c-myc), trisomii 12q13 (CEP12) i translokacji obejmujących locus genu kodującego łańcuchy ciężkie immunoglobulin (IGH, 14q32.33). Analizy cytogenetyczne i MRD były przeprowadzane w laboratoriach centralnych. Kryteria odpowiedzi i ocena pełnej odpowiedzi Kryteria odpowiedzi i progresji zostały zdefiniowane wg kryteriów odpowiedzi dla CLL opracowanych przez Grupę Roboczą sponsorowaną przez NCI. 24 Pacjenci z kliniczną CR mieli potwierdzający aspirat i biopsję szpiku kostnego 8 tygodni po zakończeniu leczenia. Ocenę MRD przeprowadzano metodą czterokolorowej cytometrii przepływowej (CD5 + /CD19 + /CD52 + / Ś + lub Ť + ) we krwi obwodowej lub szpiku kostnym. Analiza statystyczna Planowana liczebność badanej grupy wynosiła 284 pacjentów (142 w każdym z ramion), co pozwalałoby wykryć 50% wzrost mediany PFS w którymkolwiek z ramion (iloraz hazardu [hazard ratio, HR] = 0,667) z mocą 80% i R = 0,05 (dwustronnie). Wcześniej planowana analiza przejściowa została wykonana po 95 progresjach, a analiza końcowa została przeprowadzona przy poziomie istotności 0,048 z zastosowaniem metody O Briena- Fleminga, aby zapewnić całkowity poziom istotności 0,05. Wszyscy pacjenci rozdzieleni w sposób randomizowany zostali wzięci pod uwagę w analizie skuteczności zgodnie z zasadą zamiaru leczenia. Bezpieczeństwo analizowano dla wszystkich pacjentów, którzy otrzymali co najmniej jedną dawkę badanego leku. Wszystkie rozkłady czasu do zdarzenia były szacowane metodą Kaplana-Meiera, wyrażane w miesiącach i porównywane za pomocą stratyfikowanego (stadium Rai I do II względem III do IV) testu log-rank. HR było obliczane za pomocą modelu Coxa stratyfikowanego dla stadium Rai. Odsetki odpowiedzi porównywano z zastosowaniem testu 2 lub dokładnego testu Fishera, w zależności od tego, który był właściwy. PFS oceniono od daty randomizacji do pierwszego obiektywnego udokumentowania progresji choroby lub zgonu. Czas do leczenia alternatywnego zdefiniowano od daty randomizacji do daty pierwszego alternatywnego leczenia lub zgonu spowodowanego jakąkolwiek przyczyną. Ogółem 191 zdarzeń progresji choroby lub zgonu (82 w ramieniu z alemtuzumabem i 109 w ramieniu z chlorambucilem) uwzględniono w końcowej analizie PFS. Wszystkie analizy skuteczności przeprowadzał niezależny panel oceniający kryteria włączenia do badań, odpowiedzi i daty progresji. WYNIKI Pacjenci Od grudnia 2001 roku do lipca 2004 roku do badań włączono 297 pacjentów i w sposób randomizowany przydzielono do leczenia alemtuzumabem (n = 149) lub chlorambucilem (n = 148) w 44 ośrodkach (dziewięć w USA i 35 w Europie). Trzech pacjentów (dwóch przydzielonych do alemtuzumabu i jeden do chlorambucilu) wycofało zgodę przed podaniem leczenia i nie wzięto ich pod uwagę w analizie bezpieczeństwa. Podstawowe cechy demograficzne i choroby były zrównoważone pomiędzy grupami (Tabela 1). Wyniki uzyskane od 282 pacjentów użyto do analizy podgrup cytogenetycznych. Czas trwania leczenia Jednakowa liczba pacjentów (n = 147) w obu ramionach otrzymała co najmniej jedno podanie leku objętego badaniami. Mediana długości ekspozycji na alemtuzumab wyniosła 11,7 tygodnia (zakres, od 0 do 33 tygodni), włączając w to przerwy w leczeniu, a mediana dawki kumulacyjnej osiągnęła 956 mg (zakres, od 2 do 1645 mg). Niemal wszyscy pacjenci, 143 (97,3%) ze 147, otrzymali alemtuzumab w dawce zamierzonej 30 mg, a 85,7% osiągnęło ten cel w okresie 5 dni kalendarzowych. Większość pacjentów (71,4%) była leczona 21 lub więcej dawkami alemtuzumabu 30 mg. Mediana długości ekspozycji na chlorambucil wyniosła 28,3 tygodnia (zakres, od 4 do 59 tygodni), z medianą dawki kumulacyjnej w wysokości 515 mg (zakres, od 60 do 1168 mg) i medianą siedmiu podanych cykli (zakres, od jednego do 12 cykli). Skuteczność PFS. Wykazano wyższość alemtuzumabu nad chlorambucilem w zakresie PFS (stratyfikowany log-rank P = 0,0001). Po uwzględnieniu stadium zaawansowania wg Rai (I do II względem III/IV), HR dla PFS wyniósł 0,58 (95% CI, od 0,43 do 0,77), dla 42% obniżenia ryzyka progresji choroby lub zgonu (Ryc. 1A). Lepsza odpowiedź wydawała się korelować z dłuższym PFS u pacjentów leczonych alemtuzumabem (Ryc. 1B). Odsetki odpowiedzi Odsetki ORR i CR były istotnie wyższe (P! 0,0001) dla alemtuzumabu (Tabela 2). W analizie podgrupy chorych z zamiarem leczenia MRD była niewykrywalna u 11 spośród 36 pacjentów w CR po alemtuzumabie. Czas do leczenia alternatywnego Pacjenci otrzymujący alemtuzumab wykazali dłuższą medianę czasu do leczenia alternatywnego w porównaniu z chorymi, którzy otrzymywali chlorambucil (stratyfikowany log-rank P = 0,0001), pomimo krótszego czasu trwania leczenia. Mediana czasu do leczenia alternatyw
4 Hillmen i wsp. Tabela 1. Charakterystyka początkowa pacjentów i cytogenetyka Cecha Alemtuzumab (n = 149) Chlorambucil (n = 148) pacjentów % pacjentów % Wiek, lata Mediana 59,0 60,0 Zakres Płeć Mężczyźni , ,3 Kobiety 43 28, ,7 Grupa stadium Rai (IRRP) 0 lub brak* 6 4,0 3 2,0 I-II 93 62, ,9 III/IV 50 33, ,1 Czas od pierwszego rozpoznania do randomizowanego przydziału, miesiące Mediana 9,38 7,85 Zakres 0,5-167,4 0,1-224,8 Maksymalny rozmiar węzłów chłonnych, cm! , ,3 " , ,0 Bez powiększonych węzłów chłonnych 8 5,4 10 6,8 Palpacyjna hepatomegalia 43 28, ,2 Palpacyjna splenomegalia 53 35, ,8 Stan sprawności wg WHO ,4 5 3,4 Nocne poty 64 43, ,6 Ubytek masy ciała 10% 9 6, ,8 Gorączka 1 0,7 2 1,4 Hierarchiczna podgrupa cytogenetyczna 17p13.1 (p53) 11 7,7 10 7,2 Jakakolwiek delecja 11q 23 16, ,3 Trisomia 12 (ale nie delecja 11p lub 17p) 24 16,8 10 7,2 Normalny 25 17, ,7 Wyłącznie delecja 13q 33 23, ,5 Różne inne kombinacje 27 18, ,1 Skróty: IRRP niezależny panel oceniający odpowiedź; CLL przewlekła białaczka limfocytowa. *Pacjenci byli ocenieni jako stadium Rai 0 (n = 5) lub diagnoza B-komórkowej CLL nie została potwierdzona (n = 4) przez IRRP. Jeden z pacjentów został omyłkowo randomizowany przed potwierdzeniem rozpoznania CLL. Według metody hierarchicznego modelu Döhnera i wsp., 1 n = 143 dla grupy z alemtuzumabem i n = 139 dla grupy z chlorambucilem. nego wyniosła 23,3 miesiąca (95% CI, od 20,7 do 31,0 miesięcy) dla alemtuzumabu, z medianą 11,7 tygodnia terapii i 14,7 miesiąca (95% CI, od 12,6 do 16,8 miesiąca) dla chlorambucilu, z medianą 28,3 tygodnia terapii. Tak więc leczenie alemtuzumabem było związane z okresem około 88 tygodni wolnych od leczenia w porównaniu z 36 tygodniami dla chlorambucilu. Wyniki leczenia w zależności od grupy cytogenetycznej i czynnika stratyfikacji Aberracje chromosomowe zostały podzielone wg hierarchicznego modelu Döhnera. 1 Tabela 3 zawiera wyniki skuteczności w zależności od aberracji genetycznej, a Tabela 4 ilustruje wyniki skuteczności w zależności od czynnika stratyfikacji. Całkowite przeżycie Mediana całkowitego przeżycia nie została osiągnięta dla żadnego z ramion. Po medianie czasu obserwacji wynoszącej 24,6 miesiąca, 84% pacjentów przeżyło w każdym z ramion w punkcie odcięcia danych lub w dniu ostatniej kontrolnej wizyty. Nie oczekuje się dalszych informacji na temat całkowitego przeżycia. Bezpieczeństwo AE. AE podczas leczenia i w ciągu 30 dni od ostatniej dawki badania podsumowano w Tabeli 5. Zdarzenia związane z infuzją w ramieniu z alemtuzumabem obejmowały gorączkę, dreszcze, nudności, spadki ciśnienia, pokrzywkę, duszność, wysypkę, wymioty i objawy bronchospastyczne, które miały mniejsze nasilenie po pierwszym tygodniu leczenia. Szesnastu pacjentów (11%) leczonych alemtuzumabem i 26 pacjentów (18%) leczonych chlorambucilem miało niedokrwistość 3 do 4 stopnia, z medianą czasu ujawnienia się odpowiednio po 4,4 i 8,1 tygodnia. Sześćdziesięciu pacjentów (41%) otrzymujących alemtuzumab i 36 pacjentów (25%) otrzymujących chlorambucil miało neu- 210 JOURNAL OF CLINICAL ONCOLOGY
5 Alemtuzumab z porównaniu z chlorambucilem jako leczenie pierwszej linii w CLL Ryc. 1. (A) Oszacowane metodą Kaplana-Meiera przeżycie wolne od progresji (PFS) na podstawie wyników niezależnego panelu oceniającego odpowiedź. Ogólnie mediana PFS wyniosła 14,6 miesiąca (95% CI, od 12,3 do 21,7 miesiąca) dla pacjentów w ramieniu z alemtuzumabem i 11,7 miesiąca (95% CI, od 9,9 do 13,2 miesiąca) dla pacjentów w ramieniu z chlorambucilem (stratyfikowane log-rank P = 0,0001). Mediana okresu obserwacji wyniosła 24,5 miesiąca dla alemtuzumabu i 24,9 miesiąca dla chlorambucilu. (B) Oszacowane metodą Kaplana-Meiera PFS wg odpowiedzi w ramieniu z alemtuzumabem. Przy medianie okresu obserwacji wynoszącej 2 lata progresja nastąpiła tylko u jednego pacjenta CRm. CR całkowita remisja; MRD minimalna choroba resztkowa; CRm+ MRD ujemna CR; CRm+ MRD dodatnia CR; PR częściowa remisja. tropenię 3 do 4 stopnia (P = 0,0041), z medianą czasu ujawnienia się odpowiednio po 4,4 i 3,7 tygodnia. Osiemnastu pacjentów (12%) otrzymujących alemtuzumab i 17 Kategoria odpowiedzi Tabela 2. Odpowiedź na leczenie wg IRRP Alemtuzumab Chlorambucil (n = 149) (n = 148) P Ogólna odpowiedź , ,4! 0,0001 CR 36 24,2 3 2,0! 0,0001 MRD-ujemna* 11 7, ,0008 Częściowa odpowiedź 88 59, ,4 Stabilna choroba 9 6, ,4 Progresja choroby 5 3, ,2 Nie do oceny 11 7,4 6 4,1 Skróty: IRRP niezależny panel oceniający odpowiedź; CR całkowita remisja; MRD minimalna choroba resztkowa. *Dwóch chorych MRD-CR zostało ocenionych przez IRRP jako stadium 0 Rai na początku badania. pacjentów (12%) otrzymujących chlorambucil miało małopłytkowość 3 do 4 stopnia, z medianą czasu ujawnienia się odpowiednio po 1,3 i 7,9 tygodnia. W ramieniu z alemtuzumabem u czterech (33%) spośród 12 pacjentów z początkowo dodatnim bezpośrednim testem Coombsa doszło podczas leczenia do konwersji do wyniku ujemnego, a czterech (3%) spośród 132 pacjentów z początkowo ujemnym bezpośrednim testem Coombsa miało wynik dodatni w trakcie leczenia. W ramieniu z chlorambucilem u jednego (7%) spośród 15 pacjentów z początkowo dodatnim bezpośrednim testem Coombsa doszło podczas leczenia do konwersji do wyniku ujemnego, a ośmiu (6%) spośród 125 pacjentów z początkowo ujemnym bezpośrednim testem Coombsa miało wynik dodatni w trakcie leczenia. W ramieniu z alemtuzumabem u jednego pacjenta rozwinęła się niedokrwistość hemolityczna (związana z chorobą nowotworową) 4 miesiące po ostatniej dawce badanego leku. W ramieniu z chlorambucilem u dwóch pacjentów rozwinęła się niedokrwistość hemolityczna (w jednym przypadku związana z badanym le
6 Hillmen i wsp. Delecja chorych Tabela 3. ORR i PFS dla ramion leczenia wg anomalii cytogenetycznych Alemtuzumab Chlorambucil ORR ORR P Mediana PFS (miesiące) chorych Mediana PFS (miesiące) ORR PFS del 17p , ,2 0,0805 0,4066 del 11q (bez del 17p) , ,5! 0,0001 0,4338 Trisomia 12 (bez del 17p, , ,9 1,0000 0,0915 bez del 11q) Prawidłowa , ,3 0,3238 0,5582 Wyłącznie 13q , ,0 0,0087 0,0170 del 17p lub del 11q , ,7! 0,0001 0,1602 UWAGA. Dane przedstawione wg hierarchicznego modelu Döhnera i wsp. 1 plus dodatkowa analiza łącząca del 17p i del 11q. Skróty: ORR ogólny odsetek odpowiedzi; PFS przeżycie wolne od progresji; del delecja. kiem, w drugim z chorobą nowotworową) podczas otrzymywania leku. Chociaż neutropenie 3 do 4 stopnia były częstsze w ramieniu z alemtuzumabem, gorączka neutropeniczna (4,8% w grupie alemtuzumabu i 2,7% w grupie chlorambucilu) i bakteriemia/posocznica (odpowiednio 3% i 1,4%) występowały równie rzadko. Czynniki wzrostu zastosowano u 9,5% pacjentów otrzymujących alemtuzumab i 4,1% otrzymujących chlorambucil. Poważne AE i zaprzestanie leczenia wynikające z AE Ciężkie AE związane z lekami były częstsze w ramieniu z alemtuzumabem (26,5% względem 6,8%), ale w niektórych instytucjach zgłaszano bezobjawowy dodatni test PCR CMV jako ciężki AE, ponieważ rutynowa praktyka medyczna lub warunki socjalne wymagały przyjęcia do szpitala do leczenia gancyklowirem dożylnie. Biorąc pod uwagę ciężkie AE związane z lekami, jedynym zdarzeniem występującym częściej u pacjentów otrzymujących alemtuzumab były zdarzenia z CMV. AE związane z lekami, które prowadziły do całkowitego zaprzestania podawania badanego leku, stwierdzono u 19,7% pacjentów otrzymujących alemtuzumab i 4,1% pacjentów otrzymujących chlorambucil. W ramieniu z alemtuzumabem 17 pacjentów zakończyło badanie z powodu toksyczności 3/4 stopnia związanej z lekami, w tym 6 z powodu CMV 3. stopnia, 1 gruźlicy, 1 odoskrzelowego zapalenia płuc, 2 neutropenii, 1 małopłytkowości i po jednym z powodu pokrzywki, spadku ciśnienia tętniczego z bradykardią zatokową, zatrzymania akcji serca (z natychmiastowym wznowieniem), duszności i nadwrażliwości, skurczu oskrzeli i migotania przedsionków. W ramieniu z chlorambucilem pięciu pacjentów zakończyło badanie z powodu 3/4 stopnia AE związanych z lekami, w tym 2 z powodu małopłytkowości 3. stopnia, 1 leukopenii 3. stopnia, 1 zapalenia mózgu wywołanego przez Listeria monocytogenes i 1 z powodu zapalenia płuc. Czynnik chorych Tabela 4. ORR i PFS dla ramion leczenia wg czynnika stratyfikacji Alemtuzumab Chlorambucil ORR ORR P Mediana PFS (miesiące) chorych Mediana PFS (miesiące) ORR PFS Wiek, lata " , ,5 0,0409 0,2131! , ,7! 0,0001! 0,0001 Płeć Mężczyźni , ,0! 0,0001 0,0020 Kobiety , ,7 1,0000 0,0221 Maksymalny rozmiar węzłów, cm " , ,8 0,0125 0,2195! , ,5! 0,0001 0,0003 Stan sprawności , ,0! 0,0001 0, , ,5 0,1667 0,4245 Skróty: ORR ogólny odsetek odpowiedzi; PFS przeżycie wolne od progresji. 212 JOURNAL OF CLINICAL ONCOLOGY
7 Alemtuzumab z porównaniu z chlorambucilem jako leczenie pierwszej linii w CLL Zdarzenia niepożądane Tabela 5. Toksyczności zgłaszane przez " 10% chorych Alemtuzumab (n = 147) Chlorambucil (n = 147) Wszystkie stopnie Stopnie 3/4 Wszystkie stopnie Stopnia 3 Związane z infuzją Gorączka 94 63,9 12 8,2 5 3,4 Dreszcze 73 49,7 5 3,4 Pokrzywka 22 15,0 3 2,0 1 0,7 Spadki ciśnienia 21 14,3 2 1,4 Wysypka 18 12,2 1 0,7 1 0,7 Zakażenie CMV* Bezobjawowa CMV z dodatnim PCR 77 52,4 6 4,1 11 7,5 Objawowe zakażenie CMV 23 15,6 6 4,1 Nudności 19 12, ,7 1 0,7 Wymioty 10 6, ,4 1 0,7 UWAGA. Toksyczności są związane z leczeniem, z wyjątkiem zdarzeń z CMV, które były zgłaszane bez względu na związek. Stopnie odpowiadają Common Toxicity Criteria National Cancer Institute wersja 2.0 Skróty: CMV wirus cytomegalii; PCR reakcja łańcuchowa polimerazy. Czterech pacjentów zmarło w trakcie leczenia lub w ciągu 30 dni od ostatniej dawki badanego leku, jeden (0,6%) w ramieniu z alemtuzumabem z powodu infekcji Candida albicans niezwiązanej z leczeniem i trzech (2,0%) w ramieniu z chlorambucilem, jeden z powodu zapalenia mózgu Listeria monocytogenes związanego z leczeniem, jeden z powodu nagłego zgonu z innych przyczyn i jeden z powodu niewydolności krążeniowej. W żadnym z ramion nie było przypadków transformacji Richtera. CMV Chociaż żaden z pacjentów otrzymujących chlorambucil nie miał PCR-dodatniej CMV przebiegającej z objawami klinicznymi, 15,6% pacjentów otrzymujących alemtuzumab miało objawowe zakażenie CMV, bez zajęcia narządów końcowych. Podczas leczenia 52,4% pacjentów otrzymujących alemtuzumab i 7,5% pacjentów przyjmujących chlorambucil miało dodatni wynik CMV PCR, bez klinicznych objawów infekcji. Wśród 23 pacjentów z PCR-dodatnim objawowym zakażeniem CMV leczenie zostało przerwane u 21 chorych; wszyscy z wyjątkiem jednego otrzymali leki przeciwwirusowe i wszyscy wyzdrowieli. Wśród 78 bezobjawowych pacjentów leczonych alemtuzumabem, którzy mieli jeden lub więcej dodatnich wyników PCR w kierunku CMV (w tym jeden po zakończeniu leczenia), leczenie przerwano u 47 chorych, a 36 otrzymało leki przeciwwirusowe. Skuteczność leczenia alemtuzumabem została utrzymana u pacjentów z bezobjawowym lub objawowym dodatnim wynikiem PCR w kierunku CMV. U pacjentów z objawową CMV, ORR wyniósł 83% z 26% CR, a u pacjentów z bezobjawową CMV ORR osiągnął 92% z 29% CR. Mediana PFS dla wszystkich CMV PCR-dodatnich pacjentów wyniosła 14,6 miesiąca, podobnie jak dla całego ramienia badawczego i wszyscy pacjenci wyzdrowieli bez żadnych następstw choroby infekcyjnej. DYSKUSJA Wyniki tego badania wykazują przewagę leczenia pierwszej linii u pacjentów z CLL za pomocą alemtuzumabu w porównaniu z chlorambucilem. Leczenie alemtuzumabem dawało istotnie statystycznie dłuższy PFS, wyższy ORR i CR, MRD-ujemne CR i dłuższy czas do leczenia alternatywnego, czemu towarzyszył przewidywalny i dający się kontrolować profil bezpieczeństwa. Obecnie za najbardziej skuteczne leczenie pierwszej linii w CLL uważa się skojarzone zastosowanie fludarabiny, cyklofosfamidu i rytuksymabu Odsetek odpowiedzi na alemtuzumab jako pojedynczego leku, wykazany w tym badaniu (24% CR, 59% odpowiedzi częściowej [PR]), jest wyższy niż dla monoterapii fludarabiną 5 (20% CR, 43% PR) i rytuksymabem 30 (9% CR, 49% PR) w podobnych populacjach pacjentów. Tym samym czyni to alemtuzumab dobrym kandydatem do dalszych badań nad jego skojarzonym podawaniem z innymi lekami. Inne badania sugerowały, że alemtuzumab wykazuje aktywność u pacjentów z nieprawidłowościami cytogenetycznymi wysokiego ryzyka, w tym delecją 17p lub 11q, którzy z reguły źle odpowiadają na inne terapie Alemtuzumab eliminuje także MRD u niektórych pacjentów zgodnie z wcześniejszymi doniesieniami. 8,20,21,31 Skuteczność alemtuzumabu wykazana w tym badaniu potwierdza hipotezę, że lek ten jest aktywny u źle rokujących pacjentów. Wyniki te wymagają jednak potwierdzenia w przyszłych badaniach klinicznych. Przedstawione dane sugerują również, że alemtuzumab w leczeniu pierwszej linii ma lepszy profil bezpieczeństwa niż w przypadku jego zastosowania w bardziej zaawansowanej chorobie. Najczęstszymi AE były zdarzenia związane z infuzją leku i charakteryzowały się one stopniem nasilenia od lekkiego do średniego, dawały się 213
8 Hillmen i wsp. opanować, a ich częstość zmniejszała się z następnymi dawkami. Ostatnie badania wykazały, że zdarzenia związane z infuzją mogą być ograniczone po podskórnym podaniu alemtuzumabu. 22,32 Częstość występowania niedokrwistości, małopłytkowości, gorączki neutropenicznej i objawowych infekcji (innych niż CMV) była porównywalna z chlorambucilem; rzadko stosowano krwiotwórcze czynniki wzrostu. Porównując do ramienia z chlorambucilem, więcej pacjentów w grupie z alemtuzumabem, którzy przystąpili do badań z dodatnim testem Coombsa, uzyskało konwersję do wyniku ujemnego. W grupie chorych leczonych alemtuzumabem nie odnotowano żadnego zgonu będącego następstwem leczenia. Zarówno objawowe infekcje CMV, jak i bezobjawowe dodatnie wyniki CMV PCR, które częściej występowały w grupie alemtuzumabu, zostały skutecznie opanowane standardowym leczeniem i wydawały się nie wpływać na uzyskanie odpowiedzi na alemtuzumab. Wytyczne postępowania leczniczego w przypadku reaktywacji CMV u pacjentów leczonych alemtuzumabem zostały wcześniej opublikowane. 33 W przypadku wznowy lub choroby opornej na leczenie, kombinacje alemtuzumab/fludarabina, 34,35 alemtuzumab/rytuksymab 36,37 i cyklofosfamid/fludarabina/alemtuzumab/rytuksymab 38 pozwalały na uzyskanie obiecujących wyników. Wstępne wyniki badań alemtuzumabu jako leczenia podtrzymującego 39 lub terapii konsolidującej 20,31,40-43 są także zachęcające. Duża aktywność pojedynczego leku i dający się opanować profil bezpieczeństwa alemtuzumabu w pierwszej linii uzasadniają dalsze badania w połączeniu z innymi lekami jako leczenia konsolidującego i eliminującego MRD. Przedstawione dane wskazują, że alemtuzumab może być najaktywniejszym pojedynczym lekiem w terapii chorych na CLL. Wydaje się też, że odgrywa ważną rolę w leczeniu chorych cechujących się źle rokującymi zaburzeniami cytogenetycznymi i przyczynia się do eliminacji MRD. Pojawienie się ulepszonej stratyfikacji do grup rokowniczych, bardziej czułych i praktycznych testów do wykrywania MRD oraz strategii leczniczych, które obejmują najaktywniejsze leki, takie jak alemtuzumab, powinien skutkować istotnym postępem w leczeniu CLL. PIŚMIENNICTWO 1. Döhner H, Stilgenbauer S, Benner A, et al: Genomic aberrations and survival in chronic lymphocytic leukemia. N Engl J Med 343: , Chemotherapeutic options in chronic lymphocytic leukemia: A meta-analysis of the randomized trials: CLL Trialists Collaborative Group. J Natl Cancer Inst 91: , Robak T, Blonski JZ, Kasznicki M, et al: Cladribine with prednisone versus chlorambucil with prednisone as first-line therapy in chronic lymphocytic leukemia: Report of a prospective, randomized, multicenter trial. Blood 96: , Johnson S, Smith AG, Loffler H, et al: Multicentre prospective randomised trial of fludarabine versus cyclophosphamide, doxorubicin, and prednisone (CAP) for treatment of advanced-stage chronic lymphocytic leukaemia: The French Cooperative Group on CLL. Lancet 347: , Rai KR, Peterson BL, Appelbaum FR, et al: Fludarabine compared with chlorambucil as primary therapy for chronic lymphocytic leukemia. N Engl J Med 343: , Steurer M, Pall G, Richards S, et al: Purine antagonists for chronic lymphocytic leukaemia. Cochrane Database Syst Rev 3:CD004270, Zhu Q, Tan DC, Samuel M, et al: Fludarabine in comparison to alkylator-based regimen as induction therapy for chronic lymphocytic leukemia: A systematic review and meta-analysis. Leuk Lymphoma 45: , Moreton P, Kennedy B, Lucas G, et al: Eradication of minimal residual disease in B-cell chronic lymphocytic leukemia after alemtuzumab therapy is associated with prolonged survival. J Clin Oncol 23: , Wattel E, Preudhomme C, Hecquet B, et al: p53 mutations are associated with resistance to chemotherapy and short survival in hematologic malignancies. Blood 84: , Döhner H, Fischer K, Bentz M, et al: p53 gene deletion predicts for poor survival and non-response to therapy with purine analogs in chronic B-cell leukemias. Blood 85: , Cordone I, Masi S, Mauro FR, et al: p53 expression in B-cell chronic lymphocytic leukemia: A marker of disease progression and poor prognosis. Blood 91: , Lens D, Dyer MJ, Garcia-Marco JM, et al: p53 abnormalities in CLL are associated with excess of prolymphocytes and poor prognosis. Br J Haematol 99: , Levine AJ: p53, the cellular gatekeeper for growth and division. Cell 88: , Treumann A, Lifely MR, Schneider P, et al: Primary structure of CD52. J Biol Chem 270: , Gilleece MH, Dexter TM: Effect of Campath-1H antibody on human hematopoietic progenitors in vitro. Blood 82: , Keating MJ, Flinn I, Jain V, et al: Therapeutic role of alemtuzumab (Campath-1H) in patients who have failed fludarabine: Results of a large international study. Blood 99: , Stilgenbauer S, Döhner H: Campath-1Hinduced complete remission of chronic lymphocytic leukemia despite p53 gene mutation and resistance to chemotherapy. N Engl J Med 347: , Lozanski G, Heerema NA, Flinn IW, et al: Alemtuzumab is an effective therapy for chronic lymphocytic leukemia with p53 mutations and deletions. Blood 103: , Osuji NC, Del GI, Matutes E, et al: The efficacy of alemtuzumab for refractory chronic lymphocytic leukemia in relation to cytogenetic abnormalities of p53. Haematologica 90: , O Brien SM, Kantarjian HM, Thomas DA, et al: Alemtuzumab as treatment for residual disease after chemotherapy in patients with chronic lymphocytic leukemia. Cancer 98: , Montillo M, Schinkoethe T, Elter T: Eradication of minimal residual disease with alemtuzumab in B-cell chronic lymphocytic leukemia (B-CLL) patients: The need for a standard method of detection and the potential impact of bone marrow clearance on disease outcome. Cancer Invest 23: , Lundin J, Kimby E, Bjorkholm M, et al: Phase II trial of subcutaneous anti-cd52 monoclonal antibody alemtuzumab (Campath-1H) as first-line treatment for patients with B-cell chronic lymphocytic leukemia (B- CLL). Blood 100: , Karlsson C, Norin S, Kimby E, et al: Alemtuzumab as first-line therapy for B-cell chronic lymphocytic leukemia: Long-term follow-up of clinical effects, infectious complications and risk of Richter transformation. Leukemia 20: , Cheson BD, Bennett JM, Grever M, et al: National Cancer Institute-sponsored Working Group guidelines for chronic lymphocytic leukemia: Revised guidelines for diagnosis and treatment. Blood 87: , Eichhorst BF, Busch R, Hopfinger G, et al: Fludarabine plus cyclophosphamide versus fludarabine alone in first-line therapy of younger patients with chronic lymphocytic leukemia. Blood 107: , Flinn IW, Neuberg DS, Grever MR, et al: Phase III trial of fludarabine plus cyclophosphamide compared with fludarabine for patients with previously untreated chronic lymphocytic leukemia: US Intergroup Trial E2997. J Clin Oncol 25: , Byrd JC, Peterson BL, Morrison VA, et al: Randomized phase 2 study of fludarabine with concurrent versus sequential treatment with rituximab in symptomatic, untreated patients with B-cell chronic lymphocytic leukemia: Results from Cancer and Leukemia Group B 9712 (CALGB 9712). Blood 101: 6-14, Keating MJ, O Brien S, Albitar M, et al: Early results of a chemoimmunotherapy regimen of fludarabine, cyclophosphamide, and rituximab as initial therapy for chronic lymphocytic leukemia. J Clin Oncol 23: , Byrd JC, Rai K, Peterson BL, et al: Addition of rituximab to fludarabine may prolong progression-free survival and overall survival in patients with previously untreated chronic lymphocytic leukemia: An updated retrospective comparative analysis of CALGB 9712 and CALGB Blood 105:49-53, Hainsworth JD, Litchy S, Barton JH, et al: Single-agent rituximab as first-line and maintenance treatment for patients with chronic lymphocytic leukemia or small lymphocytic lymphoma: A phase II trial of the Minnie Pearl Cancer Res Network. J Clin Oncol 21: , Montillo M, Tedeschi A, Miqueleiz S, et al: Alemtuzumab as consolidation after a response to 214 JOURNAL OF CLINICAL ONCOLOGY
9 Alemtuzumab z porównaniu z chlorambucilem jako leczenie pierwszej linii w CLL fludarabine is effective in purging residual disease in patients with chronic lymphocytic leukemia. J Clin Oncol 24: , Montillo M, Cafro AM, Tedeschi A, et al: Safety and efficacy of subcutaneous Campath-1H for treating residual disease in patients with chronic lymphocytic leukemia responding to fludarabine. Haematologica 87: , O Brien SM, Keating MJ, Mocarski ES: Updated guidelines on the management of cytomegalovirus reactivation in patients with chronic lymphocytic leukemia treated with alemtuzumab. Clin Lymphoma Myeloma 7: , Elter T, Borchmann P, Schulz H, et al: Fludarabine in combination with alemtuzumab is effective and feasible in patients with relapsed or refractory B-cell chronic lymphocytic leukemia: Results of a phase II trial. J Clin Oncol 23: , Kennedy B, Rawstron A, Carter C, et al: Campath-1H and fludarabine in combination are highly active in refractory chronic lymphocytic leukemia. Blood 99: , Faderl S, Thomas DA, O Brien S, et al: Experience with alemtuzumab plus rituximab in patients with relapsed and refractory lymphoid malignancies. Blood 101: , Nabhan C, Patton D, Gordon LI, et al: A pilot trial of rituximab and alemtuzumab combination therapy in patients with relapsed and/or refractory chronic lymphocytic leukemia (CLL). Leuk Lymphoma 45: , Wierda W, Faderl S, O Brien S, et al: Combined cyclophosphamide, fludarabine, alemtuzumab, and rituximab (CFAR) is active for relapsed and refractory patients with CLL. Blood 104, 2004 (abstr 340) 39. Thieblemont C, Bouafia F, Hornez E, et al: Maintenance therapy with a monthly injection of alemtuzumab prolongs response duration in patients with refractory B-cell chronic lymphocytic leukemia/small lymphocytic lymphoma (B-CLL/SLL). Leuk Lymphoma 45: , Rai K, Byrd J, Peterson BL, et al: Subcutaneous alemtuzumab following fludarabine for previously untreated patients with chronic lymphocytic leukemia (CLL): CALGB Study Blood 102, 2003 (abstr 2506) 41. Wendtner CM, Ritgen M, Schweighofer CD, et al: Consolidation with alemtuzumab in patients with chronic lymphocytic leukemia (CLL) in first remission: Experience on safety and efficacy within a randomized multicenter phase III trial of the German CLL Study Group (GCLLSG). Leukemia 18: , Liggett WH, Hainsworth JD, Spigel DR, et al: Fludarabine/rituximab (FR) followed by alemtuzumab as first-line treatment for patients with chronic lymphocytic leukemia (CLL) or small lymphocytic lymphoma (SLL): A Minnie Pearl Cancer Res Network phase II trial. J Clin Oncol 23:574s, 2005 (abstr 6556) 43. Wierda WG, Kipps TJ, Keating MJ, et al: Self-administered, subcutaneous (SQ) alemtuzumab to eliminate residual disease in patients (pts) with CLL. Blood 108, 2006 (abstr 2839) Oświadczenie autorów na temat potencjalnych konfliktów interesów Chociaż wszyscy autorzy wypełnili deklaracje jawności, następujący autorzy wskazali występowanie korzyści finansowej. Zależności oznaczone literą U to takie, w przypadku których nie otrzymano wynagrodzenia, zależności oznaczone literą C to te, w przypadku których autorzy otrzymali wynagrodzenie. Szczegółowy opis tych kategorii oraz więcej informacji na temat polityki ASCO dotyczącej konfliktów interesów znajduje się w deklaracji oświadczenia autorów i Oświadczenia o możliwym konflikcie interesów w części informacji dla autorów. Autorzy Zatrudnienie Rola konsultanta lub doradcy Akcje giełdowe Jingyang Wu Genzyme Corp (C) Genzyme Corp Cynthia Sirard Genzyme Corp (C) Genzyme Corp Honoraria Peter Hillmen Bayer Schering Pharma Genzyme Corp Jiri Mayer Aleksander B. Skotnicki Tadeusz Robak Branimir Jaksic Anna Dmoszynska Berlex (C) Fundusze badawcze Świadectwa Inne Genzyme Corp Genzyme Corp Genzyme Corp Genzyme Corp Wkład poszczególnych autorów Pomysł i projekt badania: Peter Hillmen, Aleksander B. Skotnicki, Tadeusz Robak Dostarczenie próbek lub umożliwienie dostępu do chorych: Peter Hillmen, Aleksander B. Skotnicki, Tadeusz Robak, Branimir Jaksic, Anna Dmoszynska, Jiri Mayer Zbieranie i gromadzenie danych: Peter Hillmen, Aleksander B. Skotnicki, Tadeusz Robak, Branimir Jaksic, Anna Dmoszynska, Jingyang Wu, Cynthia Sirard, Jiri Mayer Analiza i interpretacja danych: Peter Hillmen, Aleksander B. Skotnicki, Tadeusz Robak, Jingyang Wu, Cynthia Sirard, Jiri Mayer Pisanie manuskryptu: Peter Hillmen, Jingyang Wu, Cynthia Sirard Ostateczna akceptacja manuskryptu: Peter Hillmen, Aleksander B. Skotnicki, Tadeusz Robak, Branimir Jaksic, Anna Dmoszynska, Jingyang Wu, Cynthia Sirard, Jiri Mayer 215
Przewlekła białaczka limfocytowa
 Przewlekła białaczka limfocytowa Ewa Lech-Marańda Klinika Hematologii Instytutu Hematologii i Transfuzjologii Klinika Hematologii i Transfuzjologii CMKP Przewlekła białaczka limfocytowa (CLL) Początek
Przewlekła białaczka limfocytowa Ewa Lech-Marańda Klinika Hematologii Instytutu Hematologii i Transfuzjologii Klinika Hematologii i Transfuzjologii CMKP Przewlekła białaczka limfocytowa (CLL) Początek
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka szpikowa
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka szpikowa
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Dziennik Urzędowy Ministra Zdrowia 618 Poz. 51 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dziennik Urzędowy Ministra Zdrowia 618 Poz. 51 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Nowe możliwości leczenia ostrej białaczki limfoblastycznej
 Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Polskie doświadczenia kliniczne z bendamustyną
 Polskie doświadczenia kliniczne z bendamustyną Iwona Hus Klinika Hematoonkologii i Transplantacji Szpiku UM w Lublinie XXIII Zjazd PTHiT Wrocław 2009 Bendamustyna w leczeniu PBL monoterapia Efficacy of
Polskie doświadczenia kliniczne z bendamustyną Iwona Hus Klinika Hematoonkologii i Transplantacji Szpiku UM w Lublinie XXIII Zjazd PTHiT Wrocław 2009 Bendamustyna w leczeniu PBL monoterapia Efficacy of
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Dziennik Urzędowy Ministra Zdrowia 624 Poz. 71 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dziennik Urzędowy Ministra Zdrowia 624 Poz. 71 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Ocena immunologiczna i genetyczna białaczkowych komórek macierzystych
 Karolina Klara Radomska Ocena immunologiczna i genetyczna białaczkowych komórek macierzystych Streszczenie Wstęp Ostre białaczki szpikowe (Acute Myeloid Leukemia, AML) to grupa nowotworów mieloidalnych,
Karolina Klara Radomska Ocena immunologiczna i genetyczna białaczkowych komórek macierzystych Streszczenie Wstęp Ostre białaczki szpikowe (Acute Myeloid Leukemia, AML) to grupa nowotworów mieloidalnych,
Rak piersi. Doniesienia roku Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie
 Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Skuteczność schematu bendamustyna i rytuksymab w leczeniu nawrotowej postaci przewlekłej białaczki limfocytowej
 OPIS PRZYPADKU Hematologia 2010, tom 1, nr 4, 359 363 Copyright 2010 Via Medica ISSN 2081 0768 Skuteczność schematu bendamustyna i rytuksymab w leczeniu nawrotowej postaci przewlekłej białaczki limfocytowej
OPIS PRZYPADKU Hematologia 2010, tom 1, nr 4, 359 363 Copyright 2010 Via Medica ISSN 2081 0768 Skuteczność schematu bendamustyna i rytuksymab w leczeniu nawrotowej postaci przewlekłej białaczki limfocytowej
LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka
Załącznik B.14. LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0)
 Załącznik B.65. LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia dazatynibem ostrej białaczki limfoblastycznej z obecnością chromosomu
Załącznik B.65. LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia dazatynibem ostrej białaczki limfoblastycznej z obecnością chromosomu
Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie
 brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
Białaczka limfatyczna
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
Typ histopatologiczny
 Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008.
 załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
Wydłużenie życia chorych z rakiem płuca - nowe możliwości
 Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Personalizacja leczenia w hematoonkologii dziecięcej
 MedTrends 2016 Europejskie Forum Nowoczesnej Ochrony Zdrowia Zabrze, 18-19 marca 2016 r. Personalizacja leczenia w hematoonkologii dziecięcej Prof. dr hab. n. med. Tomasz Szczepański Katedra i Klinika
MedTrends 2016 Europejskie Forum Nowoczesnej Ochrony Zdrowia Zabrze, 18-19 marca 2016 r. Personalizacja leczenia w hematoonkologii dziecięcej Prof. dr hab. n. med. Tomasz Szczepański Katedra i Klinika
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego. Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa
 Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Dr n. med. Norbert Grząśko w imieniu Polskiej Grupy Szpiczakowej Lublin, 12.04.2008
 Ocena skuteczności i bezpieczeństwa leczenia układem CTD (cyklofosfamid, talidomid, deksametazon) u chorych na szpiczaka plazmocytowego aktualizacja danych Dr n. med. Norbert Grząśko w imieniu Polskiej
Ocena skuteczności i bezpieczeństwa leczenia układem CTD (cyklofosfamid, talidomid, deksametazon) u chorych na szpiczaka plazmocytowego aktualizacja danych Dr n. med. Norbert Grząśko w imieniu Polskiej
Komunikat prasowy. Dodatkowe informacje
 Dane na temat czasu przeżycia całkowitego uzyskane w badaniu LUX-Lung 7 bezpośrednio porównującym leki afatynib i gefitynib, przedstawione na ESMO 2016 W badaniu LUX-Lung 7 zaobserwowano mniejsze ryzyko
Dane na temat czasu przeżycia całkowitego uzyskane w badaniu LUX-Lung 7 bezpośrednio porównującym leki afatynib i gefitynib, przedstawione na ESMO 2016 W badaniu LUX-Lung 7 zaobserwowano mniejsze ryzyko
Aneks II Zmiany w drukach informacyjnych produktów leczniczych zarejestrowanych w procedurze narodowej
 Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną immunoglobulinę anty-t limfocytarną pochodzenia króliczego stosowaną u ludzi [rabbit anti-human thymocyte] (proszek
Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną immunoglobulinę anty-t limfocytarną pochodzenia króliczego stosowaną u ludzi [rabbit anti-human thymocyte] (proszek
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe Od czasu dopuszczenia produktu Esmya do obrotu zgłoszono cztery przypadki poważnego uszkodzenia wątroby prowadzącego do transplantacji wątroby. Ponadto zgłoszono
Aneks IV Wnioski naukowe 1 Wnioski naukowe Od czasu dopuszczenia produktu Esmya do obrotu zgłoszono cztery przypadki poważnego uszkodzenia wątroby prowadzącego do transplantacji wątroby. Ponadto zgłoszono
Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych
 Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych Jadwiga Dwilewicz-Trojaczek Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa
Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych Jadwiga Dwilewicz-Trojaczek Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa
Terapeutyczne Programy Zdrowotne 2012 Leczenie glejaków mózgu Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r.
 Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
S T R E S Z C Z E N I E
 STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną. Klinika Onkologii i Radioterapii
 Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną chemioterapię z udziałem cisplatyny? Jacek Jassem Klinika Onkologii i Radioterapii Gdańskiego ń Uniwersytetu t Medycznego Jaka jest siła
Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną chemioterapię z udziałem cisplatyny? Jacek Jassem Klinika Onkologii i Radioterapii Gdańskiego ń Uniwersytetu t Medycznego Jaka jest siła
Piotr Potemski. Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi
 Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Obserwowane są samoistne regresje zmian przerzutowych
Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Obserwowane są samoistne regresje zmian przerzutowych
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
Bendamustyna w leczeniu opornych postaci szpiczaka mnogiego
 Bendamustyna w leczeniu opornych postaci szpiczaka mnogiego Iwona Hus, Joanna Mańko Klinika Hematonkologii i Transplantacji Szpiku Uniwersytetu Medycznego w Lublinie Nałęczów 22 listopada 2008 Bendamustyna
Bendamustyna w leczeniu opornych postaci szpiczaka mnogiego Iwona Hus, Joanna Mańko Klinika Hematonkologii i Transplantacji Szpiku Uniwersytetu Medycznego w Lublinie Nałęczów 22 listopada 2008 Bendamustyna
Porównanie skuteczności leków adiuwantowych. w neuropatycznym bólu nowotworowym1
 Porównanie skuteczności leków adiuwantowych w neuropatycznym bólu nowotworowym1 Badanie1 New Delhi Cel Metoda Porównanie pregabaliny z amitryptyliną* i gabapentyną pod względem skuteczności klinicznej
Porównanie skuteczności leków adiuwantowych w neuropatycznym bólu nowotworowym1 Badanie1 New Delhi Cel Metoda Porównanie pregabaliny z amitryptyliną* i gabapentyną pod względem skuteczności klinicznej
ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH
 ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH 1 Państwo Członkowskie UE/EOG Austria Belgia Dania Finlandia Francja Irlandia
ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH 1 Państwo Członkowskie UE/EOG Austria Belgia Dania Finlandia Francja Irlandia
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
Superior efficacy of nilotinib vs imatinib in patients with chronic myeloid leukemia in chronic phase. ENESTnd and ENESTcmr current results analysis
 Większa skuteczność nilotynibu niż imatynibu w leczeniu przewlekłej białaczki szpikowej w fazie przewlekłej. Analiza aktualnych wyników badania ENESTnd i ENESTcmr Superior efficacy of nilotinib vs imatinib
Większa skuteczność nilotynibu niż imatynibu w leczeniu przewlekłej białaczki szpikowej w fazie przewlekłej. Analiza aktualnych wyników badania ENESTnd i ENESTcmr Superior efficacy of nilotinib vs imatinib
LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C 34)
 Załącznik B.6. LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C 34) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
Załącznik B.6. LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C 34) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
 Załącznik nr 10 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny:
Załącznik nr 10 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny:
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Rysunek. Układ limfatyczny.
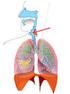 Informacja dotyczy rodzaju chłoniaka nieziarniczego zwanego chłoniakiem z małych limfocytów B. Warto również przeczytać informacje na temat przewlekłej białaczki limfocytowej (CLL), która jest podobnym
Informacja dotyczy rodzaju chłoniaka nieziarniczego zwanego chłoniakiem z małych limfocytów B. Warto również przeczytać informacje na temat przewlekłej białaczki limfocytowej (CLL), która jest podobnym
MabThera. w leczeniu podtrzymującym chorych na chłoniaka grudkowego. Dr hab. med. Maciej Machaczka, Prof. UR
 MabThera w leczeniu podtrzymującym chorych na chłoniaka grudkowego Dr hab. med. Maciej Machaczka, Prof. UR Senior Consultant and Research Scientist Hematology Center Karolinska and Karolinska Institutet
MabThera w leczeniu podtrzymującym chorych na chłoniaka grudkowego Dr hab. med. Maciej Machaczka, Prof. UR Senior Consultant and Research Scientist Hematology Center Karolinska and Karolinska Institutet
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 90/2011 Prezesa Agencji Oceny Technologii Medycznych z dnia 19 grudnia 2011 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 90/2011 Prezesa Agencji Oceny Technologii Medycznych z dnia 19 grudnia 2011 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych
chorych na ITP Krzysztof Chojnowski Warszawa, 27 listopada 2009 r.
 Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym?
 Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym? Piotr Potemski Klinika Chemioterapii Nowotworów Katedry Onkologii Uniwersytet
Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym? Piotr Potemski Klinika Chemioterapii Nowotworów Katedry Onkologii Uniwersytet
Lek BI w porównaniu z lekiem Humira u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą
 Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20)
 Dziennik Urzędowy Ministra Zdrowia 511 Poz. 42 Załącznik B.4. LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie zaawansowanego
Dziennik Urzędowy Ministra Zdrowia 511 Poz. 42 Załącznik B.4. LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie zaawansowanego
Ulotka dołączona do opakowania: informacja dla użytkownika. Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji
 Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Przewlekła białaczka limfocytowa
 PRACA PRZEGLĄDOWA Krzysztof Warzocha Klinika Hematologii Instytutu Hematologii i Transfuzjologii Przewlekła białaczka limfocytowa Chronic lymphocytic leukemia Adres do korespondencji: prof. dr hab. med.
PRACA PRZEGLĄDOWA Krzysztof Warzocha Klinika Hematologii Instytutu Hematologii i Transfuzjologii Przewlekła białaczka limfocytowa Chronic lymphocytic leukemia Adres do korespondencji: prof. dr hab. med.
Rak jajnika. Prof. Mariusz Bidziński. Klinika Ginekologii Onkologicznej
 Rak jajnika Prof. Mariusz Bidziński Klinika Ginekologii Onkologicznej Współpraca z firmami: Roche, Astra Zeneca, MSD, Olympus Mutacje w genach BRCA1 i BRCA2 Materiały edukacyjne Astra Zeneca Mutacje w
Rak jajnika Prof. Mariusz Bidziński Klinika Ginekologii Onkologicznej Współpraca z firmami: Roche, Astra Zeneca, MSD, Olympus Mutacje w genach BRCA1 i BRCA2 Materiały edukacyjne Astra Zeneca Mutacje w
UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA.
 UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA Małgorzata Biskup Czynniki ryzyka sercowo-naczyniowego u chorych na reumatoidalne zapalenie
UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA Małgorzata Biskup Czynniki ryzyka sercowo-naczyniowego u chorych na reumatoidalne zapalenie
Leczenie systemowe raka nie-jasnokomórkowego
 Leczenie systemowe raka nie-jasnokomórkowego Piotr Tomczak Uniwersytet Medyczny w Poznaniu Klinika Onkologii Jastrzębia Góra Nie-jasnokomórkowy rak nerki (ncc RCC) niejednorodna grupa o zróżnicowanej histologii
Leczenie systemowe raka nie-jasnokomórkowego Piotr Tomczak Uniwersytet Medyczny w Poznaniu Klinika Onkologii Jastrzębia Góra Nie-jasnokomórkowy rak nerki (ncc RCC) niejednorodna grupa o zróżnicowanej histologii
Leczenie przewlekłej białaczki limfatycznej na podstawie aktualnych wyników badań klinicznych
 P R A C A P R Z E G L Ą D O W A Anna Szmigielska-Kapłon, Tadeusz Robak Klinika Hematologii Uniwersytetu Medycznego w Łodzi Leczenie przewlekłej białaczki limfatycznej na podstawie aktualnych wyników badań
P R A C A P R Z E G L Ą D O W A Anna Szmigielska-Kapłon, Tadeusz Robak Klinika Hematologii Uniwersytetu Medycznego w Łodzi Leczenie przewlekłej białaczki limfatycznej na podstawie aktualnych wyników badań
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 765 Poz. 42 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 765 Poz. 42 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
LECZENIE CHOROBY GAUCHERA ICD-10 E
 załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
prof. Joanna Chorostowska-Wynimko Zakład Genetyki i Immunologii Klinicznej Instytut Gruźlicy i Chorób Płuc w Warszawie
 prof. Joanna Chorostowska-Wynimko Zakład Genetyki i Immunologii Klinicznej Instytut Gruźlicy i Chorób Płuc w Warszawie Sekwencyjność występowania zaburzeń molekularnych w niedrobnokomórkowym raku płuca
prof. Joanna Chorostowska-Wynimko Zakład Genetyki i Immunologii Klinicznej Instytut Gruźlicy i Chorób Płuc w Warszawie Sekwencyjność występowania zaburzeń molekularnych w niedrobnokomórkowym raku płuca
Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce
 Warszawa, 27.01.2016 Seminarium naukowe: Terapie przełomowe w onkologii i hematoonkologii a dostępność do leczenia w Polsce na tle Europy Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce Dr n.
Warszawa, 27.01.2016 Seminarium naukowe: Terapie przełomowe w onkologii i hematoonkologii a dostępność do leczenia w Polsce na tle Europy Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce Dr n.
LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2
 załącznik nr 11 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
załącznik nr 11 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
Promotor: prof. dr hab. Katarzyna Bogunia-Kubik Promotor pomocniczy: dr inż. Agnieszka Chrobak
 INSTYTUT IMMUNOLOGII I TERAPII DOŚWIADCZALNEJ IM. LUDWIKA HIRSZFELDA WE WROCŁAWIU POLSKA AKADEMIA NAUK mgr Milena Iwaszko Rola polimorfizmu receptorów z rodziny CD94/NKG2 oraz cząsteczki HLA-E w patogenezie
INSTYTUT IMMUNOLOGII I TERAPII DOŚWIADCZALNEJ IM. LUDWIKA HIRSZFELDA WE WROCŁAWIU POLSKA AKADEMIA NAUK mgr Milena Iwaszko Rola polimorfizmu receptorów z rodziny CD94/NKG2 oraz cząsteczki HLA-E w patogenezie
Aneks. Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków
 Aneks Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Produkt leczniczy Folotyn roztwór
Aneks Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Produkt leczniczy Folotyn roztwór
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 719 Poz. 27 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem
Dziennik Urzędowy Ministra Zdrowia 719 Poz. 27 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM I EPOPROSTENOLEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia sildenafilem
LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48)
 Dziennik Urzędowy Ministra Zdrowia 492 Poz. 66 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Dziennik Urzędowy Ministra Zdrowia 492 Poz. 66 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
POSTĘPY W LECZENIU PBL
 POSTĘPY W LECZENIU PBL Klinika Chorób Wewnętrznych i Hematologii Wojskowy Instytut Medyczny Prof. dr hab. med. Piotr Rzepecki Terapia przełomowa Pojęcie terapii przełomowych w hematoonkologii zostało wprowadzone
POSTĘPY W LECZENIU PBL Klinika Chorób Wewnętrznych i Hematologii Wojskowy Instytut Medyczny Prof. dr hab. med. Piotr Rzepecki Terapia przełomowa Pojęcie terapii przełomowych w hematoonkologii zostało wprowadzone
Radioterapia stereotaktyczna. Rafal Dziadziuszko Gdański Uniwersytet Medyczny
 Radioterapia stereotaktyczna przerzutów do OUN Rafal Dziadziuszko Gdański Uniwersytet Medyczny Urządzenia do RT stereotaktycznej - nóż gamma Urządzenia do RT stereotaktycznej - nóż gamma Urządzenia do
Radioterapia stereotaktyczna przerzutów do OUN Rafal Dziadziuszko Gdański Uniwersytet Medyczny Urządzenia do RT stereotaktycznej - nóż gamma Urządzenia do RT stereotaktycznej - nóż gamma Urządzenia do
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
wolna od leczenia? (TFR ang. Treatment Free Remission)
 Czy można bezpiecznie przerwać leczenie przewlekłej białaczki szpikowej Czym jest remisja wolna od leczenia (TFR ang. Treatment Free Remission) KILKA INFORMACJI NA POCZąTEK... Remisja wolna od leczenia
Czy można bezpiecznie przerwać leczenie przewlekłej białaczki szpikowej Czym jest remisja wolna od leczenia (TFR ang. Treatment Free Remission) KILKA INFORMACJI NA POCZąTEK... Remisja wolna od leczenia
WZW TYPU B CO POWINIENEŚ WIEDZIEĆ? CZY WYKORZYSTAŁEŚ WSYSTKIE DOSTĘPNE ŚRODKI ABY USTRZEC SIĘ PRZED WIRUSOWYM ZAPALENIEM WĄTROBY TYPU B?
 WZW TYPU B CO POWINIENEŚ WIEDZIEĆ? CZY WYKORZYSTAŁEŚ WSYSTKIE DOSTĘPNE ŚRODKI ABY USTRZEC SIĘ PRZED WIRUSOWYM ZAPALENIEM WĄTROBY TYPU B? ZDOBĄDŹ INFORMACJE! ZASZCZEP SIĘ! ZDOBĄDŹ OCHRONĘ! szczepionka przeciw
WZW TYPU B CO POWINIENEŚ WIEDZIEĆ? CZY WYKORZYSTAŁEŚ WSYSTKIE DOSTĘPNE ŚRODKI ABY USTRZEC SIĘ PRZED WIRUSOWYM ZAPALENIEM WĄTROBY TYPU B? ZDOBĄDŹ INFORMACJE! ZASZCZEP SIĘ! ZDOBĄDŹ OCHRONĘ! szczepionka przeciw
Praktyczne stosowanie terapii celowanej w hematologii aktualne problemy
 Prof. Andrzej Hellmann Katedra i Klinika Hematologii i Transplantologii Gdański Uniwersytet Medyczny Praktyczne stosowanie terapii celowanej w hematologii aktualne problemy Seminarium Edukacyjne Innowacje
Prof. Andrzej Hellmann Katedra i Klinika Hematologii i Transplantologii Gdański Uniwersytet Medyczny Praktyczne stosowanie terapii celowanej w hematologii aktualne problemy Seminarium Edukacyjne Innowacje
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 144/2013 z dnia 21 października 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 144/2013 z dnia 21 października 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego
Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie?
 Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie? lek. med. Marek Dudziński Oddział Hematologii Wojewódzki Szpital Specjalistyczny
Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie? lek. med. Marek Dudziński Oddział Hematologii Wojewódzki Szpital Specjalistyczny
Standard leczenia, jakiego oczekują pacjenci z przewlekłą białaczką limfocytową. Aleksandra Rudnicka rzecznik PKPO
 Standard leczenia, jakiego oczekują pacjenci z przewlekłą białaczką limfocytową Aleksandra Rudnicka rzecznik PKPO Wspólny głos ponad 100 tysięcy pacjentów onkologicznych! 45 organizacje wspólnie działają
Standard leczenia, jakiego oczekują pacjenci z przewlekłą białaczką limfocytową Aleksandra Rudnicka rzecznik PKPO Wspólny głos ponad 100 tysięcy pacjentów onkologicznych! 45 organizacje wspólnie działają
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Znaczenie PFS oraz OS w analizach klinicznych w onkologii
 Znaczenie PFS oraz OS w analizach klinicznych w onkologii experience makes the difference Magdalena Władysiuk, lek. med., MBA Cel terapii w onkologii/hematologii Kontrola rozwoju choroby Kontrola objawów
Znaczenie PFS oraz OS w analizach klinicznych w onkologii experience makes the difference Magdalena Władysiuk, lek. med., MBA Cel terapii w onkologii/hematologii Kontrola rozwoju choroby Kontrola objawów
Dlaczego potrzebne było badanie?
 Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z chorobą Alzheimera we wczesnym stadium Jest to podsumowanie badania klinicznego przeprowadzonego z udziałem pacjentów
Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z chorobą Alzheimera we wczesnym stadium Jest to podsumowanie badania klinicznego przeprowadzonego z udziałem pacjentów
Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010
 Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010 1. Leczeniem powinni być objęci chorzy z ostrym, przewlekłym zapaleniem wątroby oraz wyrównaną
Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010 1. Leczeniem powinni być objęci chorzy z ostrym, przewlekłym zapaleniem wątroby oraz wyrównaną
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE SZPICZAKA PLAZMATYCZNO KOMÓRKOWEGO (PLAZMOCYTOWEGO) (ICD-10 C 90)
 Załącznik B.13. LECZENIE SZPICZAKA PLAZMATYCZNO KOMÓRKOWEGO (PLAZMOCYTOWEGO) (ICD-10 C 90) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia bortezomibem 1.1 Leczenie bortezomibem nowo zdiagnozowanych
Załącznik B.13. LECZENIE SZPICZAKA PLAZMATYCZNO KOMÓRKOWEGO (PLAZMOCYTOWEGO) (ICD-10 C 90) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia bortezomibem 1.1 Leczenie bortezomibem nowo zdiagnozowanych
Dlaczego potrzebne było badanie?
 Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z łagodną postacią choroby Alzheimera oraz trudności z funkcjonowaniem psychicznym Jest to podsumowanie badania klinicznego
Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z łagodną postacią choroby Alzheimera oraz trudności z funkcjonowaniem psychicznym Jest to podsumowanie badania klinicznego
LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C-34)
 Załącznik B.6. LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C-34) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
Załącznik B.6. LECZENIE NIEDROBNOKOMÓRKOWEGO RAKA PŁUCA (ICD-10 C-34) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH
Optymalizacja strategii leczenia pierwszej linii przewlekłej białaczki limfocytowej
 P R A C A P R Z E G L Ą D O W A Krzysztof Warzocha Klinika Hematologii Instytutu Hematologii i Transfuzjologii w Warszawie Optymalizacja strategii leczenia pierwszej linii przewlekłej białaczki limfocytowej
P R A C A P R Z E G L Ą D O W A Krzysztof Warzocha Klinika Hematologii Instytutu Hematologii i Transfuzjologii w Warszawie Optymalizacja strategii leczenia pierwszej linii przewlekłej białaczki limfocytowej
Warszawa, 16-17.03.201217.03.2012 PLRG / PALG 16-17.03.2012
 Przegląd badań klinicznych PLRG Konferencja PLRG i PALG Warszawa, 16-17.03.201217.03.2012 Janusz Szczepanik CRO Quantum Satis 1 Badania kliniczne PLRG PLRG R-CVP/CHOP (PLRG4) HOVON 68 CLL Watch and Wait
Przegląd badań klinicznych PLRG Konferencja PLRG i PALG Warszawa, 16-17.03.201217.03.2012 Janusz Szczepanik CRO Quantum Satis 1 Badania kliniczne PLRG PLRG R-CVP/CHOP (PLRG4) HOVON 68 CLL Watch and Wait
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
NON-HODGKIN S LYMPHOMA
 NON-HODGKIN S LYMPHOMA Klinika Hematologii, Nowotworów Krwi i Transplantacji Szpiku We Wrocławiu Aleksandra Bogucka-Fedorczuk DEFINICJA Chłoniaki Non-Hodgkin (NHL) to heterogeniczna grupa nowotworów charakteryzująca
NON-HODGKIN S LYMPHOMA Klinika Hematologii, Nowotworów Krwi i Transplantacji Szpiku We Wrocławiu Aleksandra Bogucka-Fedorczuk DEFINICJA Chłoniaki Non-Hodgkin (NHL) to heterogeniczna grupa nowotworów charakteryzująca
Wirus zapalenia wątroby typu B
 Wirus zapalenia wątroby typu B Kliniczne następstwa zakażenia odsetek procentowy wyzdrowienie przewlekłe zakażenie Noworodki: 10% 90% Dzieci 1 5 lat: 70% 30% Dzieci starsze oraz 90% 5% - 10% Dorośli Choroby
Wirus zapalenia wątroby typu B Kliniczne następstwa zakażenia odsetek procentowy wyzdrowienie przewlekłe zakażenie Noworodki: 10% 90% Dzieci 1 5 lat: 70% 30% Dzieci starsze oraz 90% 5% - 10% Dorośli Choroby
Radioterapia w leczeniu raka pęcherza moczowego - zalecenia
 Radioterapia w leczeniu raka pęcherza moczowego - zalecenia Radioterapia w leczeniu raka pęcherza moczowego może być stosowana łącznie z leczeniem operacyjnym chemioterapią. Na podstawie literatury anglojęzycznej
Radioterapia w leczeniu raka pęcherza moczowego - zalecenia Radioterapia w leczeniu raka pęcherza moczowego może być stosowana łącznie z leczeniem operacyjnym chemioterapią. Na podstawie literatury anglojęzycznej
LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Dziennik Urzędowy Ministra Zdrowia 615 Poz. 27 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Dziennik Urzędowy Ministra Zdrowia 615 Poz. 27 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Zadanie pytania klinicznego (PICO) Wyszukanie i selekcja wiarygodnej informacji. Ocena informacji o metodzie leczenia
 Praktykowanie EBM Krok 1 Krok 2 Krok 3 Krok 4 Zadanie pytania klinicznego (PICO) Wyszukanie i selekcja wiarygodnej informacji Ocena informacji o metodzie leczenia Podjęcie decyzji klinicznej na podstawie
Praktykowanie EBM Krok 1 Krok 2 Krok 3 Krok 4 Zadanie pytania klinicznego (PICO) Wyszukanie i selekcja wiarygodnej informacji Ocena informacji o metodzie leczenia Podjęcie decyzji klinicznej na podstawie
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
czerniak (nowotwór skóry), który rozprzestrzenił się lub którego nie można usunąć chirurgicznie;
 EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32.a. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE
Załącznik B.32.a. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE
IL-4, IL-10, IL-17) oraz czynników transkrypcyjnych (T-bet, GATA3, E4BP4, RORγt, FoxP3) wyodrębniono subpopulacje: inkt1 (T-bet + IFN-γ + ), inkt2
 Streszczenie Mimo dotychczasowych postępów współczesnej terapii, przewlekła białaczka limfocytowa (PBL) nadal pozostaje chorobą nieuleczalną. Kluczem do znalezienia skutecznych rozwiązań terapeutycznych
Streszczenie Mimo dotychczasowych postępów współczesnej terapii, przewlekła białaczka limfocytowa (PBL) nadal pozostaje chorobą nieuleczalną. Kluczem do znalezienia skutecznych rozwiązań terapeutycznych
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r.
 Dziennik Ustaw Nr 269 15678 Poz. 1593 1593 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na podstawie
Dziennik Ustaw Nr 269 15678 Poz. 1593 1593 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na podstawie
Wyniki badania CLARINET w jelitowotrzustkowych nowotworach neuroendokrynnych GEP-NET/NEN bez czynności wydzielniczej
 Wyniki badania CLARINET w jelitowotrzustkowych nowotworach neuroendokrynnych GEP-NET/NEN bez czynności wydzielniczej Jarosław B. Ćwikła UWM Olsztyn i CMKP Warszawa jbcwikla@interia.pl Wieloośrodkowe, randomizowane
Wyniki badania CLARINET w jelitowotrzustkowych nowotworach neuroendokrynnych GEP-NET/NEN bez czynności wydzielniczej Jarosław B. Ćwikła UWM Olsztyn i CMKP Warszawa jbcwikla@interia.pl Wieloośrodkowe, randomizowane
LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0)
 Załącznik B.22. LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0) WIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii dokonuje Zespół Koordynacyjny ds. Chorób Ultrarzadkich powoływany przez Prezesa Narodowego
Załącznik B.22. LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0) WIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii dokonuje Zespół Koordynacyjny ds. Chorób Ultrarzadkich powoływany przez Prezesa Narodowego
LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0)
 Dziennik Urzędowy Ministra Zdrowia 731 Poz. 66 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Dziennik Urzędowy Ministra Zdrowia 731 Poz. 66 Załącznik B.68. LECZENIE TĘTNICZEGO NADCIŚNIENIA PŁUCNEGO SILDENAFILEM, EPOPROSTENOLEM I MACYTENTANEM (TNP) (ICD-10 I27, I27.0) ŚWIADCZENIOBIORCY I. Terapia
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 8/2011 Prezesa Agencji Oceny Technologii Medycznych z dnia 28 lutego 2011 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych albo
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 8/2011 Prezesa Agencji Oceny Technologii Medycznych z dnia 28 lutego 2011 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych albo
