|
|
|
- Irena Jóźwiak
- 8 lat temu
- Przeglądów:
Transkrypt
1 SPRAWEUONO PoD IMGLĘDEM MERVTCIRYEEsSYM CHAMKTERYSTYKA PRODUKTU LECZNICZEGO -tl3-0i 20n7 {. NAZWA WŁASNA PRoDUKTU LEczNlczEGo,b CAPD/DPCA 2 Roztwór do dia izyotzewnowej CAPD/DPCA 3 Roztwór do dializy otvewnowej CAPD/DPCA 4 Roztwórdo dializyotzewnowej 2. SKŁAD JAKoŚcloWY l lloścpwy 1 litrzawiera: Sodu chlorek Sodu mlecean Wapniachlorekdwuwodnv Maqnezuch oreksześciowodnv Glukoza iednowodna (co odpowiadaqlukozie Na+ Ca++ Mo++ cr- Mleczan Teoretvcznaosmo arność ph substancj czynnych CAPD/DPCA o q o o q {15,0g) 134 mmolfl 1.75mmol/l 0.5 mm l 103.5mmo ń $5 mmolll 358 mosmll 5,5 CAPD/DPCA o 3.925q q q CAPD/DPCA 4 (42,5g) 134 mmolll 1.75mmolll 0.5 mmolll 103.5mmolfl 35 mmolfl 511 mosmll 5,5 Q2.73s\ 134 mmol/l 1.75mmolll 0.5 mmol/l 103:5mmol/l 35 mmolll 401 mosmll 5, q 5,786s 3.925s o o 25.0 q 3. POSTAC FARMACEUTYCZNA Roztwórdo dializyotzewnowej 4. szczecótowe DANEKL NtczNE 4.{ Wskazania do stosowania Schyłkowaprzew ekła niewydo ność nereko różnejetio ogii. 4'2 4.2 Davvkowowanie e i sposób podawania Ciqgłaambulatoryjnadialłzaotzewnowa (CADO) o i enie jest wskazaneinaczej,na jednqwymianstosujesi 2000 ml roztworu.jeś ina początku eczeniadiaiiząotzewnowąu p,łtjentawystąpiądolegliwości typu rozpierania, pojedynczejwymiany powinnabyćczasowozmniejszona objtość do ml. U dzieciw za ezności od wieku,wzrostui niasy ciałazaleca si stosowaćwlewo objtości od 500 m do 1500m (3040 m /kgmasyciała)na iednąwymian. U dorosłycho dużejmasie ciałai (lub)u pacjentówdobrzetolerujących wiksząobjtośćmożna. jednąwymian. stosowaćnawet ml roztworuna MINTSTERSTWU LI.. it Lekowsl PolitYki Departament WarszawP ul. lmiodowa1'
2 Automatycznadializa otnewnowa (ADO) Jeśliprowadzisi dializotzewnowąprzerywaną ubciągę cyk icznąz uiyciemaparatudo automatycznejdia izyotzewnowej (cyk eras eep-safe),stosujesi worki o wikszejobjtości (5000m ),które umożliwiają wykonaniewicejniżjednejwymianyroztworu'cykler s eep.safe przeprowadzawymianyroztworuzgodniez pzepisem zabieguzapisanymw jego pamici. Sposób posęporłania: Ciqgłaambulatoryjna dializa otrzewnowa (CADż) Czas zaleganiaroztworuwynosi4.8 godzin,objtośó 2000 m wymienianajest cztery razyna dob (podanewańościsątylko orientacyjne, gdyźdawkowaniemusi byćusta oneindywidua nie d akażdegopacjenta). Roztwórgotowydo użyciana ezynajpierwpodgzać do temperaturyciała,a nastpnie wprowadzaćdo jamy otzewnowejza pomocącewnikaotzewnowegow czasie 5.20 minut' odpowiedniadawkaroztworupowinnapozostaćw jamie bzusznej przezokresod 4 do 8 godzin (czas równoważenia otzewnowego),a nastpniezostaćzdrenowanaizastąpionanowym roztworem. Automatycznadializa otnewnowa (ADO) Końcówkiworkówprzeznaczanychdo użyciaz cykleremsleep.safeizgodnychz pzepisem dializynaieżyumieścić w prowadnikachcyklera.cyk erautomatycznie wykonaich połączenie z drenamizestawu S eep Safe. Nastpnieautomatyczniezostaną sprawdzonekody paskowe końcówekworków,a w razie podłączenia workówniezgodnychz pzepisem dializyzapisanymw pamicicyklera,pojawisi alarm'pa zakanczeniusprawdzania,zestawdrenówmożnapołączyć z drenemłączącympacjentai rozpoeąć zabieg. Roztwór do dializyzbstaje automatycznie podgzany do temperaturyciałaprzez cyk ersleep.safe podczas przeplywudo jamy otzewnowej. Czas zpleganiai stżenieglukozyzostająwybraneprzezcyk erzgodnió z lve-pisem ekarskim znajdującymsi w pamiciaparatu(dalszeszczegółyzamieszczonesąw instiukcjiużytkowania cyklerasleep-safe). W za eznościod stanu nawodnienia isężenia e ektrolitów,oapd/dpca 2 jest uźywanyw połqczeniuz innym roztworemdo dializy otzewnowej, o wyzszym stżeniug ukozy(ten.o wyzszej osmolarności} ubo innym potasulub sodu. st.źeniu W zaleznościod stanu Wza eżnościod stanu nawodnieniaistzenia nawodnienia istzenia e ektrolitów,oapdidpca 3 jest elektrolitow,capdidpca 4 użyłranywpołąeeniu z innym jest używanyw potączeniu roztworemdo dializy z innymroztworemdo dializy otrzewnowej,o nizszym otrzewnowejo niższymlub stżeniug qkozy(tzn.o nizszej wyższymsężeniuglukozy osmo amości} ubo innym (tzn.o nizszej lub wyzszej sężeniupotasu ubsodu. osmo arności) ubo innym W eelu ochronyotrzewnej stżeniupotasulub sodu' i unikniciaodwodnienia' ie stżeniaglukozy,takie jak w CAPDTDPCA 3, nalezy stosowacmoż iwienajzadziej. Na ogółwystarcza. lub 2 wymianyz wysokimistżeniami g ukozy'do pozostałychwymian uźywasi nizszego stżenia glukozy. zdrowia K[Ęlł$.Two polityki uepanament Lekowej i Farmacli 00-gS2 Warszawa rrl.miodnwa1f
3 pzepisanej dawkipowinnabyćwykonywanacodzienniei kontynuowana Dia izaz zastosowaniern tak długo,jak dfugowskazanajest terapianerkozastpcza. 4.3 Przeciwvvskazania P zeciww skazania dia opisywanych roztworów: Dla CAPD/DPCA2,3 i 4: hipokaliemia, hiperkalcemia D acapd/dpca 3 (dodatkowo): hipowo emia, niedociśnienie ttnicze P zeciww skazania ogól ne dla dializy otnewnowej: pzypadkach: Zabiegowidia izyotzewnowejnie wolno poddawaćpacjentóww nastpujących - choroby'które mogąuszkadzaćpowłokibzucha ubjam otrzewnowątakiejak: niedawnopzebyte urazyjamy bzusznej, oparzenia powtokbzusznych, inne roz egłe stanyzapa neskóry powłokbzucha (dermatitis) w oko icyujściacewnika,zapalenie perforacja powłok otzewnej; brzucha;przebyteoperacjejamy bzuszneiz pozostawieniem zrostów;chorobyzapalne jelit(chorobacrohna,wzodziejącezapa eniajelitagrubego,zapa enia guzyjamy bzusznej; niedawnopzebyte operacjejamy bzusznej, pzepuk ina uchyłka); je ita;wewntzne lub zewntzne pzetoki bzuszne; brzuszna,niedrozność - chorobypłuc(zwłaszczazapaleniepłuc); - posocznica; - kwasica mleczanowa;.wyniszczenieoraz poważnautratamasy ciała,ałłaszczaw pzypadkach, gdy nie ma moż iwości odpowiedniegożywienia;. w rzadkichpzypadkach mocznicy,któę nie moznadłuzejopanowaóstosowaniemdializy otzewnowej;. skęna hiper ipidemia; - u pacjentów,któzy z powodówfizycznychlub umysłowych są niezdolnido vvykonania dializy : ] otzewnowej zgodnie z instrukcjąlekarza' 4.4' Specialne ostrzeżenia.iśrodkiostrożności.dotyczącestbsowafiie.-.,..w nastpstwiezabuzeń elektrolitowych, np' spowodowanychprzezwymiotylub biegunk, koniecznemoźebyó czasowezastosowanieroztworudo dializyotzewnowejaawieęącego potas. W pzypadku hiperkalcemii, np. wynikającej z eczeniaduzymidawkamiśrodków wiązących fosforanyzawierającychwapń, i ( ub)witaminąd, wskazane możebyć pzejściowe ubstałe zastosowanieroztworudo dia izyo mniejszejzawańościwapnia. objtośówymianyroztworupowinnabyćzmniejszonau dzieci,odpowiedniodo wieku,wzrostu i masy ciała(patz takżepunkt4.2).u pacjentóww podeszłym wiekupzed rozpoczciem eczeniana eżyvtziąćpod uwagwikszą czstośćwystpowaniapzepuk in. Należyprowadzićdokładnyrejestrrównowagipłynowej i masy ciała,aby uniknąóodwodnienia ub pzewodnieniaz ich potencjalniegroźnymi d ażycianastpstwami. lstotnejest równiezregularne wykonywaniebadaniapzedmiotowegooraz monitorowanie kreaęniny stżeńe ektrolitów, i mocznika,białekw surowicy,cukruwe knvi,oraz W razie koniecznościinnychparametrów (np' gazów knnri, aboratoryjnych równowagikwasowo.zasadowej). U chorychna cukzyc należydostosowaćdobowądawkinsulłnydo zwikszonejilości pzyjmowanejg ukozy.koniecznajest regu arnakontro astżeniaglukozywe krwi.' Aby zmniejszyćryzykoinfekcji,podczas wymianyroztworudia izacyjnegonależyzachować warunkiaseptyczne. Poclczastransportuod producentado ośrodka dializ lub podczas pzechowywaniatn'.'łąapitalu p astikoweopakowaniamogąulec uszkodzeniu.w takimpzypad,ln.l istniejemoż iwe.ść zakażenia grzybiczego ubbaktmyjnegoi rozwojumikroorganizmóww roztworzedo dia izy.w.wią3kuz tym,pzed podłączenłem workai użyciemroztworudia izacyjnego na eżydokładnie:;piswdzić, czy opakowanienie }estuszkodzone.należyzutrócićuwagna każde,nawetniewi*łkie, uszkodzenietączników,zamknić,spoin oraznarożnikówopakowania,ze wzg duna możliwośó zanieczyszczenia. ŁtIN sterstwozdrowia Uepanamen Połityki LekoĘ i Farmacji 00-9SZ Warszawa ul. Miodowa15
4 nadajesi do użyciatylko Roztwórdia izacyjny Nie wolno używaćworkówz mtnązawańością' Medy, gdy opakowanieizamkniciasą nieuszkodzone.jeśliistniejepohzeba,należypobrać próbkido badań,w tym mikrobio ogicznych. Roztworydo dializy CAPD/DPCA 2, 3 i 4 możnastosowaćty kovutedy,gdy są przezraczyste,a jest nieuszkodzone. opakowanie Wszelkiepozostałości roztworu na eżywyzucić. Roztworówdo dia izy otruewnowejgapd/dpga 2, 3 i 4 nie wo no stosować do infuzii doży nych. 4.S lnterakcjez innymi lekami i inne rodzaje interakcji \.' podawane ekimogąpzenikać do roztworu Na eżyplzyjąćjako ogó nązasad,ze równocześnie i byó usuwanez organizmu;d ategokoniecznemożebyćdostosowaniedawki. dia izacyjnego Podczas równoczesnegopodawaniazwiązkówwapnialub witaminyd na eżywziąćpod uwagmoz iwość hiperka cemii. ZastosowanieśrodkóW nerek,jednakmoże moczopdnychmożewspomóc resztkowączynnośó równieżpowodowaćzabuueniarównowagiwodnejie ektro itowej. W trakcie eczeniapreparataminaparstnicyszczególnieuważniepowinnobyćmonitorowane na te leki. stżeniepotasuw surowicy,gdyźhipokaliemiapowodujezwikszonąwrażliwość 4.6 Giążalub laktacja Dia izaotzewnowamożebyćwykonywanaty kow późnymokresieciąży,po wnik iwym rozważeniukorzyścii ryzyka' 4'7 Wpływna zdo nośóprowadzenia pojazdówmechanicznych i obsługiwania urządzeń mechanicznychw ruchu Nie obsenłowanozadnegowpływucapd/dpca 2, g i 4 na zdolnośćprowadzeniapojazdów mechanicznychi obsługiwania uządzeń mechanicznychw ruchu. 4.8 Działanianiepożądane \- OAPD/DPOA2,3 i 4 są roztworami e ektrolitów o składziew znacznejmieze podobnymdo wystpującego We knrvi.mozliwedziałanianiepożądanemogąwynikaća ba ztechnikidializy przez roztwórdia izacyjny. otrzewnowej,albo byćvtlywołane Działania niepożqdane wynikajqce z techniki.dializy otrzewnowej: Do czstychpowikłańkazdejdia izyotrzewnowej, równieżz zastosowaniemcapd/dpoa 2,3 i 4 należyzapa enieotrzewnejorazzakażeniew miejscuujściaiw świet e cewnika.nie eczone zapa enieotzewnej możeprowadzićdo posocznicy.oznakamizaczynającegosi zapa enia otzewnej są zmtnieniedializatu,bóle bzucha araz garączka.należyoznaczyćrodzaiczynnika etio ogicznego oraz iczb eukocytóww dia izacie.brak podwyższenia liczbyleukocytów,przy a jednoczesnymwystpowaniuinnychobjawów,nie wyk uczazapa eniaotzewnej. Na eży i niezwłocznie podjącodpowiednie eczenie[dootrzewnowe i'(lub)ogólne]zgodnez obecnym ' stanemwiedzy,stosującleki skutecznewobec pżypuszcza negopatogenu,nawetpzed.'ł uzyskaniemwynikuposiewu.po uzyskaniuwynikubadaniamfrkrobio ogicznego eczeniena eży odpowiedniodostosować'. W czasiedializyotzewnowejnie możnauniknąówzg dnych stratbiałka(5-15g/dob) i aminokwasów(1,2-3,4g/dob);dochodzitakżedo utratywitaminrozpuszaza nych w wodzie. Stratytych substancjina eżyuzupełniaóodpowiednimidostawamizpożywieniem. Do wystąpienia hipoproteinemiimożedojśćw wynikuniewyrównaniastrat białrgk odrowiedg11ffiwo zdrowia repanament potityki Lekowg i er*rfr Warszawa uf Miorjowa15
5 pzenikania przez błonotzewnej możeulec zmianiew trakciedługotnrvałego Charakterystyka eczeniadializamiotrzewnowymi, co objawia.sipleruvotnie utratązdolności ultrafiltracji. pzypadkach W ciżkich na eżyzaprzestać eczeniadia izamiotzewnowymiiwdrożyć hemodializy. jamy bzusznej), Ponadtomogąwystąpió:uczucierozpieraniai pełności (dolegliwościwewnątz utrudnionywlew i Wypływ roztworu,pzepukliny,bóle barków,dusznośówskutekuniesienia przepony,biegunkii zaparcia. Działanianiepoiqdane zwiqzane z raztwaremda dializy: Roztwórdo dia izymożespowodowaćzabuzenia równowagiptynówielektro itów,np. hipokaiiemi. Jeślizwikszonajest podażwapnia,np. popżez jednoczesnestosowaniezawierających wapń preparatówwiążącychfosforany,możedojśćdo hiperka cemii.zaburzeniagospodarki e ektro itowej możnawyrównaćzmieniającstosowanypłyndo dializy (w pzypadku hiperka cemii) lub zmieniającsposób odżywiania(w przypadkuhipoka iemii). Spośródzabulzeń gospodarkiwodnejmożedojśódopaewodnienia ubodwodnienia.znaczne. odwodnienie(szczególniepodczas eceeniaz zastosowaniemroztworówo dużymstżeniu g ukozy)możedawaćobjawyniskiegociśnieniattniczegokrwi,przyspieszonejczynńościserca, zawrotówgłowyi kurczów miśni.pzewodnienie prowadzido zwikszeniamasy ciała,wysokiego ciśnienia ttniczegokrwi,obzków kończyndolnychiduszności. Mogąwystąpićlub ulec nasi eniuzaburzeniaprzemianytfuszczowej(dys.i hiperlipidemia). Nastpstwemciągłegowchłanianiag ukoz;z roztworudializacyjnegomożebyć rzadko jeś iw diecie pacjentanie unzg dnisi zwiets111ei podażyka orii. wystpującaotyłość, 4.9 Przedawkowanie Dotychczasnie zgłaszanonagłychwypadków specyficznychd a roztworu. W peypadku przedawkowaniainadmiema objtość roztworu)możnaw szybki spósoo usunąć. roztwórz jamyotzewnowej do worka drenażowego' W pzypadku zbyt czstychwymianroztworunastąpićmoźeodwodnieniei (lub)zabuzenia gospodarkielektrolitowej. Jeże izapomniano wymienićpłyn,z 'egutyeas zaleganianastpnejwymianyskraca si tak, żebyzostałautrzymanacałkowita ilośćroztworuprzepisanegona dob (np'4 x 2000 m )' Niewłaściwe stosowaniewymianmożeprowadziódo przewodnienialub odwodnieniai zabuzeń elektrolitowych. Najbardziejprawdopodobnymnastpstwempzedawkowania roztworówoapd/dpca 2, 3 i 4 jest odwodnienie. Stosowaniezbyt małychdawekroztworulub zaprzestanieleczeniamożeprowadzićdo zagrażąącegozyciu pzewodnienia z obwodowyrniobzkami i dekompensacjąkrąienia, oraz do objawówmocznicy,które równieżsągroźned ażycia. Stosujesi ogólnie przyjtezasady medycynyratunkoweji intensywnejopieki'pacjentmoże wymagaćleczeniahemodializąz nagłychwskazań. : 5. YltŁAŚcwośg FAR! AKoLoGlczNE 5'{ Właściwości {armakodynamiczne Grupafarmakoterapeutyczna: roztworydo dializyotzewnornrej; roztworyhipertoniczne; kodatc: B05DB. OAPD/DPCA 2,3,,i4 są roztworamietektrolitówbuforowanyrni m eczanem,zawieąącymi g ukoz,przeznac'zonymido stosowaniadootzewnowego w eczeniudia iząotrzewnową(do) krańcowejniewydo ności nereko różnejetiologii'.l3j]:"ffi "***ffi :'tr.#'."j#nti:#$la;"t[h#i,.s# ffffifu
6 Technikadia izyotzewnowejopierasi na wykozystaniubłonyotzewnowejjako półpzepuszcza nejbłonyumozliwiającejwymiansubstancjirozpuszczonychoraz wody pomidzykrwiąi roztworemdializacyjnym.odbywa si to na skutekzjawiskdyfuzjii konwekcji. Zawańośćelektro itóww roztworzejest zasadniczo taka sama jak w fizjo ogicznejsurowicy,skład potasu)do stosowaniau pacjentów zostałjednakdostosowany(np.pod wzgldemzawartości leczenienerkozastpczedziki wymianiesubstancji chorychna mocznic,tak aby umoźliwić ipłynówpftez otzewną. Substancje,które norma niezostająusunitez moczem,takiejak mocznik,kreaęnina,fosforany nieorganiczne,kwas moczowy,inne substancjerozpuszczoneoraz woda,sa usuwanez organizmudo roztworudializacyjnego. Homeostazastanunawodnieniajest utrzymywanapoprzezpodawanieroztworówo różnym sężeniuglukozy,co wpfywana usuwaniepłynów(u trafi tracja). KwasicametabolicznaMórna do schyłkowej niewydolności nerekjest wyrównywanaza pomocą mleczanuzawartegow roztwoze do dializy.w wynikumetabolizmumleczanupowstaje wodorowg an. iwościfarmakokinetyczne 5.2 Właśc \-' \- ProduĘ pzemiany materiigromadzące si podczas mocznicy(np.mocznik,kreatynina,kwas moczowy),nieorganicznefosforanyoraze ektro Ę,jak sód, potas,wapń i magnezsą usuwane z organizmudo roztworudializacyjnegodzikidyfuzjii (lub)konwekcji. Glukozaw roztworachcapd/dpoa 2, 3 i4 stosowanajako środekosmotyczny,wchłaniasi powo i,zmniejszającgradientdyfuzjimidzy roztworemdia izacyjnyma płynem jest najwikszana początkuczasu zalegania, osiągając zewnątzkomórkowym.u trafi tracja glukozy maksimumpo upływieok' dwóch do tzech godzin.późniejnastpujer1ychłanianie z postpującym spadkiemultrafiltracji Po 4 godzinachilośću trafittratu wynoslśrednio100 m przy stzeniuglukozyrównym1,5o/o, przy prry 400 ml 2,34/oi 800 ml 4,25o/o glukozyzawarlejwrozhnroze P.9!czaszaleganiaWzez 6 godzinwchłonite zostaje60 do 80o/o dializacyjnym. L-m eczanstosowanyjako środekbuforującyzostaje wchłonityniema całkowiciepo 6 godzinachokresuza egania.u pacjentówz prawidłową m eczanzostaje czynnościąwątroby szybkozmetabo izowany, na co wskazująprawidłowe rnetabolitów. stżeniapośrednich TranspońWapniaza eiy od stźeniaglukozyw roztworzedializacyjnym, od objtościw ewu, stżeniawapniazjonizowanegow surowicyistżeniawapniaw roztworzedializacyjnym. mwyższesężenieg ukozy,objtość w ewui stżeniewapnia zjonizowanegow surowicyi im niższestżeniewapniaw rozt.t,torze dia izacyjnym, tymwikszyjest stopieńpzenikania wapnia od pacjentado roztworudializacyjnego. 5.3 Przedklinicznedane o bezpieczeństwie Ponieważwszystkieskładnikisą substancjamifizjologicznymi, nie pzeprowadzonobadań toksykologicznych' Klinicznestosowanieroztworówdo dializyotzewnowejo podobnymskładzie nie wskazywałona poważneryzykotoksyczności. 6. DANE FARMACEUTYCZNE 6.1 Wykaz substaqcji pomocniczych kwassolny sodu wodorotlenek woda do wstzykiwań,, Niezgodności farmaceuęczne Ze wzglduna ryzykoniezgodności izakażenia,do roztworudo dializyotzewnowejleki można MINISTERSTWO ZDROWIA Depańamen{ Po ityki Lekow$ i Farmacji 00"952 Warszawa ul. Mtodowa15
7 ó łą ł ó Ż ć ć ż ś ś ż ś ć ż ó Ć ść łą łą ł ść łą ł ść śó Ę ą ł ś ż ż ł ć ż ś ść ć ą ć ś ś ćłą ą ó ó ąć ś ó ś ć ż ś ć ń ó łą ą
8 ó ąó ą Ę ć ń ó łą ą ć łą ą ł Ć ś Ź ż ł ć łą ń łą ą ń ó łą ą ą łą łą ó ń ó łą ą ć ń ó łą ą ą łą ąć ń ć ąć Łą ó Ó ó ą ą ż ż ą
9 Ż ć ż ś ść ń ł ż ć ó ó ś ć ż ó ąć ąć ł ż ć ń ż Ą Ą ł Ą ł ł ł ń Ę Ą
 Ł Ę Ę Ę Ł Ś Ś ś ł śó Ć Żć Ó Ół ł ŚÓ Óż ł ą śó ść ą Ą Ó Ciqgłaambulataryjnadializa otzewnowa (cado) o i]e nie jest wskazaneinaczej,stosujesi 2000 m roztworuna jednqwymian,cztery razyna dob,co odpowiadadobowejdawce8000
Ł Ę Ę Ę Ł Ś Ś ś ł śó Ć Żć Ó Ół ł ŚÓ Óż ł ą śó ść ą Ą Ó Ciqgłaambulataryjnadializa otzewnowa (cado) o i]e nie jest wskazaneinaczej,stosujesi 2000 m roztworuna jednqwymian,cztery razyna dob,co odpowiadadobowejdawce8000
1. Nazwa własna produktu leczniczego Physioneal 40 z glukozą 3,86% w/v 38,6 mg/ml roztwór do dializy otrzewnowej
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. Nazwa własna produktu leczniczego Physioneal 40 z glukozą 3,86% w/v 38,6 mg/ml roztwór do dializy otrzewnowej 2. Skład jakościowy i ilościowy Przed zmieszaniem 1000
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. Nazwa własna produktu leczniczego Physioneal 40 z glukozą 3,86% w/v 38,6 mg/ml roztwór do dializy otrzewnowej 2. Skład jakościowy i ilościowy Przed zmieszaniem 1000
Dializa otrzewnowa. stay safe CAPD/DPCA Podręcznik Szkoleniowy
 Dializa otrzewnowa stay safe CAPD/DPCA Podręcznik Szkoleniowy System zapewniający maksymalne bezpieczeństwo stay safe nowa generacja systemów CADO system stay safe jest przyjazny dla środowiska Nowa generacja
Dializa otrzewnowa stay safe CAPD/DPCA Podręcznik Szkoleniowy System zapewniający maksymalne bezpieczeństwo stay safe nowa generacja systemów CADO system stay safe jest przyjazny dla środowiska Nowa generacja
2,5 mmol/l 198 mmol/l 1,0 mmol/l 207 mmol/l. 70 mmol/l 70 mmol/l. 83,25 mmol/l. 134 mmol/l 0,5 mmol/l 103,5 mmol/l 34 mmol/l
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO bicavera z 1,5% glukozą i wapniem 1,25 mmol/l 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Roztwór bicavera z 1,5% glukozą i wapniem 1,25 mmol/l dostarczany
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO bicavera z 1,5% glukozą i wapniem 1,25 mmol/l 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Roztwór bicavera z 1,5% glukozą i wapniem 1,25 mmol/l dostarczany
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Nutrineal PD4 (z 1,1% roztworem aminokwasów), Zestaw do dializy otrzewnowej. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 litr roztworu zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Nutrineal PD4 (z 1,1% roztworem aminokwasów), Zestaw do dializy otrzewnowej. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 litr roztworu zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
Ulotka dołączona do opakowania: informacja dla pacjenta. bicavera z 2,3% glukozą i wapniem 1,25 mmol/l
 Ulotka dołączona do opakowania: informacja dla pacjenta bicavera z 2,3% glukozą i wapniem 1,25 mmol/l Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta bicavera z 2,3% glukozą i wapniem 1,25 mmol/l Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kg proszku do sporządzania roztworu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kg proszku do sporządzania roztworu
Duosol zawierający 4 mmol/l potasu
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 NAZWA PRODUKTU LECZNICZEGO Duosol zawierający 4 mmol/l potasu 2 SKŁAD JAKOŚCIOWY I ILOŚCIOWY Mniejsza komora Roztwór elektrolitów 555 ml na Większa komora Roztwór
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 NAZWA PRODUKTU LECZNICZEGO Duosol zawierający 4 mmol/l potasu 2 SKŁAD JAKOŚCIOWY I ILOŚCIOWY Mniejsza komora Roztwór elektrolitów 555 ml na Większa komora Roztwór
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Accusol 35. Accusol 35
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Accusol 35 Potassium 4 mmol/l Roztwór do hemofiltracji, hemodializy i hemodiafiltracji. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Skład Komora duża
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Accusol 35 Potassium 4 mmol/l Roztwór do hemofiltracji, hemodializy i hemodiafiltracji. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Skład Komora duża
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO 0,9% Sodium Chloride Braun, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera Chlorek sodu Stężenia elektrolitów:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO 0,9% Sodium Chloride Braun, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera Chlorek sodu Stężenia elektrolitów:
Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego
 C H A R A K T E R Y S T Y K A P R O D U K T U L E C Z N I C Z E G O 1. NAZWA PRODUKTU LECZNICZEGO Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1
C H A R A K T E R Y S T Y K A P R O D U K T U L E C Z N I C Z E G O 1. NAZWA PRODUKTU LECZNICZEGO Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO EXTRANEAL Zestaw do dializy otrzewnowej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH Jałowy płyn do dializy otrzewnowej
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO EXTRANEAL Zestaw do dializy otrzewnowej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH Jałowy płyn do dializy otrzewnowej
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. PŁYN FIZJOLOGICZNY WIELOELEKTROLITOWY IZOTONICZNY FRESENIUS, roztwór do infuzji
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PŁYN FIZJOLOGICZNY WIELOELEKTROLITOWY IZOTONICZNY FRESENIUS, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml roztworu zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PŁYN FIZJOLOGICZNY WIELOELEKTROLITOWY IZOTONICZNY FRESENIUS, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml roztworu zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Microlaxregula, 5,9 g, proszek do sporządzania roztworu doustnego. Makrogol 3350.. 5,9 g w jednej saszetce.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 NAZWA PRODUKTU LECZNICZEGO Microlaxregula, 5,9 g, proszek do sporządzania roztworu doustnego 2 SKŁAD JAKOŚCIOWY I ILOŚCIOWY Makrogol 3350.. 5,9 g w jednej saszetce.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 NAZWA PRODUKTU LECZNICZEGO Microlaxregula, 5,9 g, proszek do sporządzania roztworu doustnego 2 SKŁAD JAKOŚCIOWY I ILOŚCIOWY Makrogol 3350.. 5,9 g w jednej saszetce.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
Pełny wykaz substancji pomocniczych, patrz punkt 6.1
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Physioneal 40 z glukozą 2,27% w/v 22,7 mg/ml Roztwór do dializy otrzewnowej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Przed zmieszaniem 1000 ml
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Physioneal 40 z glukozą 2,27% w/v 22,7 mg/ml Roztwór do dializy otrzewnowej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Przed zmieszaniem 1000 ml
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO Accusol 35 Potassium 4 mmol/l Roztwór do hemofiltracji, hemodializy i hemodiafiltracji. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO Accusol 35 Potassium 4 mmol/l Roztwór do hemofiltracji, hemodializy i hemodiafiltracji. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI
DIANEAL PD4 (glukoza 2,27%) zestaw do dializy otrzewnowej; 22,7 mg/ml
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIANEAL PD4 (glukoza 2,27%) zestaw do dializy otrzewnowej; 22,7 mg/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Glukoza bezwodna (Ph. Eur.) (w postaci
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIANEAL PD4 (glukoza 2,27%) zestaw do dializy otrzewnowej; 22,7 mg/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Glukoza bezwodna (Ph. Eur.) (w postaci
Produkt stosowany pomocniczo w dolegliwościach związanych ze stanami zapalnymi stawów oraz w stanach bólowych po stłuczeniach.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. Nazwa produktu leczniczego Pasta borowinowa lecznicza 2. Skład jakościowy i ilościowy Borowina 3. Postać farmaceutyczna Pasta na skórę 4. Szczegółowe dane kliniczne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. Nazwa produktu leczniczego Pasta borowinowa lecznicza 2. Skład jakościowy i ilościowy Borowina 3. Postać farmaceutyczna Pasta na skórę 4. Szczegółowe dane kliniczne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Rehydron, proszek do przygotowywania roztworu 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 saszetka zawiera: Glukoza bezwodna 6,75 g Chlorek sodu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Rehydron, proszek do przygotowywania roztworu 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 saszetka zawiera: Glukoza bezwodna 6,75 g Chlorek sodu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ADDAMEL N, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml koncentratu zawiera: Substancje czynne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ADDAMEL N, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml koncentratu zawiera: Substancje czynne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO SOLUVIT N, proszek do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH 1 fiolka zawiera: Substancje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO SOLUVIT N, proszek do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH 1 fiolka zawiera: Substancje
CHOROBY WEWNĘTRZNE CHOROBY UKŁADU MOCZOWEGO
 CHOROBY WEWNĘTRZNE CHOROBY UKŁADU MOCZOWEGO Dariusz Moczulski Klinika Chorób Wewnętrznych i Nefrodiabetologii Uniwersytecki Szpital Kliniczny im. WAM ul. Żeromskiego 113, Łódź Zaburzenia gospodarki wodno
CHOROBY WEWNĘTRZNE CHOROBY UKŁADU MOCZOWEGO Dariusz Moczulski Klinika Chorób Wewnętrznych i Nefrodiabetologii Uniwersytecki Szpital Kliniczny im. WAM ul. Żeromskiego 113, Łódź Zaburzenia gospodarki wodno
Linie krwi do aparatu do hemodializy Braun Dialog
 Załącznik nr 1 do SIWZ Pakiet nr 1 Linie krwi do aparatu do hemodializy Braun Dialog Linia krwi (2 wkłucia 1 pompa) ze sterylnym workiem kpl. 12 500 RAZEM 12 500 Pakiet nr 2 Linie krwi do aparatu do hemodializy
Załącznik nr 1 do SIWZ Pakiet nr 1 Linie krwi do aparatu do hemodializy Braun Dialog Linia krwi (2 wkłucia 1 pompa) ze sterylnym workiem kpl. 12 500 RAZEM 12 500 Pakiet nr 2 Linie krwi do aparatu do hemodializy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NATRIUM CHLORATUM 0,9 % FRESENIUS, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 9,0 mg sodu chlorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NATRIUM CHLORATUM 0,9 % FRESENIUS, 9 mg/ml, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 9,0 mg sodu chlorku
Ulotka dołączona do opakowania: Informacja dla użytkownika. ACCUSOL 35 Potassium 4 mmol/l, roztwór do hemofiltracji, hemodializy i hemodiafiltracji
 Ulotka dołączona do opakowania: Informacja dla użytkownika ACCUSOL 35 Potassium 4 mmol/l, roztwór do hemofiltracji, hemodializy i hemodiafiltracji Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: Informacja dla użytkownika ACCUSOL 35 Potassium 4 mmol/l, roztwór do hemofiltracji, hemodializy i hemodiafiltracji Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Gaviscon Advance, (1000 mg mg)/10 ml, zawiesina doustna
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon Advance, (1000 mg + 200 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu leczniczego zawiera 100 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon Advance, (1000 mg + 200 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu leczniczego zawiera 100 mg
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH
 WOREK 10 KG 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY proszek do sporządzania roztworu na skórę produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Co zawiera Ciechociński szlam leczniczy
WOREK 10 KG 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY proszek do sporządzania roztworu na skórę produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Co zawiera Ciechociński szlam leczniczy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sterofundin ISO, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml produktu leczniczego Sterofundin ISO, roztwór do infuzji zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sterofundin ISO, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml produktu leczniczego Sterofundin ISO, roztwór do infuzji zawiera:
Pakiet nr 1 Linie krwi do aparatu do hemodializy Braun Dialog
 Załącznik nr 1 do SIWZ Pakiet nr 1 Linie krwi do aparatu do hemodializy Braun Dialog 1. Linia krwi (2 wkłucia 1 pompa) ze sterylnym workiem kpl. 11 300 sterylizacja dowolna z wyjątkiem tlenku etylenu.
Załącznik nr 1 do SIWZ Pakiet nr 1 Linie krwi do aparatu do hemodializy Braun Dialog 1. Linia krwi (2 wkłucia 1 pompa) ze sterylnym workiem kpl. 11 300 sterylizacja dowolna z wyjątkiem tlenku etylenu.
Fresenius Kabi Polska Sp. z o.o. CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO SOLUTIO RINGERI LACTATE FRESENIUS, roztwór do infuzji 2. SKŁAD ILOŚCIOWY I JAKOŚCIOWY 1 ml roztworu zawiera 6,01 mg chlorku sodu (Natrii
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO SOLUTIO RINGERI LACTATE FRESENIUS, roztwór do infuzji 2. SKŁAD ILOŚCIOWY I JAKOŚCIOWY 1 ml roztworu zawiera 6,01 mg chlorku sodu (Natrii
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA HANDLOWA LEKU GOTOWEGO SALICYLOL 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH (W PRZELICZENIU NA 100g)
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA HANDLOWA LEKU GOTOWEGO SALICYLOL 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH (W PRZELICZENIU NA 100g)
DIANEAL PD4 (glukoza 2,27%) zestaw do dializy otrzewnowej; 22,7 mg/ml. Stężenie (glukoza) 1,36% w/v 13,6 mg/ml 15,00 13,60
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIANEAL PD4 (glukoza 2,27%) zestaw do dializy otrzewnowej; 22,7 mg/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Glukoza bezwodna (Ph. Eur.) 2,27%
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIANEAL PD4 (glukoza 2,27%) zestaw do dializy otrzewnowej; 22,7 mg/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Glukoza bezwodna (Ph. Eur.) 2,27%
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. PRIMENE 10% roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PRIMENE 10% roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml roztworu do infuzji zawiera: L-Izoleucyna... L-Leucyna... L-Walina...
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PRIMENE 10% roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml roztworu do infuzji zawiera: L-Izoleucyna... L-Leucyna... L-Walina...
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
Ulotka dołączona do opakowania: informacja dla użytkownika. PŁYN FIZJOLOGICZNY WIELOELEKTROLITOWY IZOTONICZNY FRESENIUS roztwór do infuzji
 Ulotka dołączona do opakowania: informacja dla użytkownika PŁYN FIZJOLOGICZNY WIELOELEKTROLITOWY IZOTONICZNY roztwór do infuzji Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika PŁYN FIZJOLOGICZNY WIELOELEKTROLITOWY IZOTONICZNY roztwór do infuzji Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika PHYSIONEAL 40 z glukozą 1,36% w/v 13,6 mg/ml, roztwór do dializy otrzewnowej PHYSIONEAL 40 z glukozą 2,27% w/v 22,7 mg/ml, roztwór do dializy
Ulotka dołączona do opakowania: informacja dla użytkownika PHYSIONEAL 40 z glukozą 1,36% w/v 13,6 mg/ml, roztwór do dializy otrzewnowej PHYSIONEAL 40 z glukozą 2,27% w/v 22,7 mg/ml, roztwór do dializy
Ulotka dołączona do opakowania: informacja dla użytkownika. Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych
 Ulotka dołączona do opakowania: informacja dla użytkownika Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. Aqua pro injectione Baxter 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Aqua pro injectione Baxter 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ Każdy worek zawiera wodę do wstrzykiwań 100% m/v 3. POSTAĆ
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Aqua pro injectione Baxter 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ Każdy worek zawiera wodę do wstrzykiwań 100% m/v 3. POSTAĆ
Ulotka dołączona do opakowania: Informacja dla użytkownika. NUTRINEAL PD4 CLEAR-FLEX, roztwór do dializy otrzewnowej
 Ulotka dołączona do opakowania: Informacja dla użytkownika NUTRINEAL PD4 CLEAR-FLEX, roztwór do dializy otrzewnowej Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: Informacja dla użytkownika NUTRINEAL PD4 CLEAR-FLEX, roztwór do dializy otrzewnowej Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1000 ml produktu leczniczego Sterofundin ISO, roztwór do infuzji zawiera:
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sterofundin ISO, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml produktu leczniczego Sterofundin ISO, roztwór do infuzji zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sterofundin ISO, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml produktu leczniczego Sterofundin ISO, roztwór do infuzji zawiera:
 ę Ę Ę Ł Ę Ł Ś Ś ż ł ł Ż ż ą ń ł ł ł ę ą Ł łł ą ś ą ż ę ć ś ł Ą ś ą ę ę ę ę ę łż ą ę ą ę ż ą ę ść ł ć ę Ż ś ś Ł ł ż ł ł ą ą ł ś ł Ę ć ł łł ń Paejenci w podeszłymwiehł U pacjentoww podesąm wieku za ecaty
ę Ę Ę Ł Ę Ł Ś Ś ż ł ł Ż ż ą ń ł ł ł ę ą Ł łł ą ś ą ż ę ć ś ł Ą ś ą ę ę ę ę ę łż ą ę ą ę ż ą ę ść ł ć ę Ż ś ś Ł ł ż ł ł ą ą ł ś ł Ę ć ł łł ń Paejenci w podeszłymwiehł U pacjentoww podesąm wieku za ecaty
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Nutrineal PD4 (z 1,1% roztworem aminokwasów) Roztwór do dializy otrzewnowej. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 litr roztworu zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Nutrineal PD4 (z 1,1% roztworem aminokwasów) Roztwór do dializy otrzewnowej. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 litr roztworu zawiera:
Zał. Nr 3. Pak Nr 1 Dreny Dializacyjne Linii Krwi. Cena 1 szt. brutto. Cena 1 szt netto. Ilość szt. Stawk a VAT. Wartość brutto
 Pak Nr 1 Dreny Dializacyjne Linii Krwi Lp Artykuł J/m Ilość szt. 1 szt Stawk a VAT 1 szt. Producent nr katalogowy Nr certyfikatu + nr str. w ofercie 1 Dreny Dializacyjne Linii Krwi Szt 32.000 Dreny dializacyjne
Pak Nr 1 Dreny Dializacyjne Linii Krwi Lp Artykuł J/m Ilość szt. 1 szt Stawk a VAT 1 szt. Producent nr katalogowy Nr certyfikatu + nr str. w ofercie 1 Dreny Dializacyjne Linii Krwi Szt 32.000 Dreny dializacyjne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Vaminolact, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml roztworu zawiera: Substancje czynne: L-alanina L-arginina L-asparaginowy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Vaminolact, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml roztworu zawiera: Substancje czynne: L-alanina L-arginina L-asparaginowy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PŁYN RINGERA FRESENIUS, (8,6 mg + 0,3 mg + 0,33 mg)/ml, roztwór do infuzji (Natrii chloridum + Kalii chloridum + Calcii chloridum dihydricum)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PŁYN RINGERA FRESENIUS, (8,6 mg + 0,3 mg + 0,33 mg)/ml, roztwór do infuzji (Natrii chloridum + Kalii chloridum + Calcii chloridum dihydricum)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Gaviscon o smaku mięty, (500 mg mg mg)/10 ml, zawiesina doustna
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda dawka 10 ml produktu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda dawka 10 ml produktu
CALCIUM RESONIUM, 1,2 g jonów wapnia/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CALCIUM RESONIUM, 1,2 g jonów wapnia/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CALCIUM RESONIUM, 1,2 g jonów wapnia/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PHYSIONEAL 40 CLEAR-FLEX, glukoza 13,6 mg/ml, roztwór do dializy otrzewnowej PHYSIONEAL 40 CLEAR-FLEX, glukoza 22,7 mg/ml, roztwór do
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PHYSIONEAL 40 CLEAR-FLEX, glukoza 13,6 mg/ml, roztwór do dializy otrzewnowej PHYSIONEAL 40 CLEAR-FLEX, glukoza 22,7 mg/ml, roztwór do
Aminomel 10E 12,5E Substancje czynne: L-izoleucyna 5,85 g 7,31 g L-leucyna 6,24 g 7,80 g L-lizyny octan (w przeliczeniu na L-lizynę)
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO AMINOMEL 10E roztwór do infuzji. AMINOMEL 12,5E roztwór do infuzji. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml roztworu do infuzji zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO AMINOMEL 10E roztwór do infuzji. AMINOMEL 12,5E roztwór do infuzji. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml roztworu do infuzji zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg sodu kromoglikanu (Natrii cromoglicas).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg sodu kromoglikanu (Natrii cromoglicas).
www.dializadomowa.pl
 12 marca 2009 r Informacja prasowa Przewlekła choroba nerek prowadzi do nieodwracalnej niewydolności tego organu. Jedyną możliwością utrzymania chorego przy życiu jest leczenie nerkozastępcze. Dializowanie
12 marca 2009 r Informacja prasowa Przewlekła choroba nerek prowadzi do nieodwracalnej niewydolności tego organu. Jedyną możliwością utrzymania chorego przy życiu jest leczenie nerkozastępcze. Dializowanie
FORMULARZ ASORTYMENTOWO CENOWY PAKIET I. Zamawiający nie dopuszcza możliwości składania ofert częściowych w przedmiotowym pakiecie
 PAKIET I Zamawiający nie dopuszcza możliwości składania ofert częściowych w przedmiotowym pakiecie Przedmiot zamówienia: Materiały do wykonywania ciągłej hemodializy z regionalną antykoagulacją cytrynianową
PAKIET I Zamawiający nie dopuszcza możliwości składania ofert częściowych w przedmiotowym pakiecie Przedmiot zamówienia: Materiały do wykonywania ciągłej hemodializy z regionalną antykoagulacją cytrynianową
 Ł Ś Ś ńó ą ę ęż ł Ę ą ł ół ą ą ł ł ł ł ł ł ę ó Ół ę łą ś ą ó ó ś ę ę ś ę ó ę ą ż ć ż ś ł ó ą ł ą ł ł ę ęś ę ł ę ł Aby uzyskać zvtięantemaksymalnejilościfosforanóvr,osvaren naleę przyjmowac wyłącznierazemz
Ł Ś Ś ńó ą ę ęż ł Ę ą ł ół ą ą ł ł ł ł ł ł ę ó Ół ę łą ś ą ó ó ś ę ę ś ę ó ę ą ż ć ż ś ł ó ą ł ą ł ł ę ęś ę ł ę ł Aby uzyskać zvtięantemaksymalnejilościfosforanóvr,osvaren naleę przyjmowac wyłącznierazemz
 ń Ł Ó Ś ś ś ŁĄ Ś Ł Ś Ś ń Ś ś Ę Ę ń Ł Ó ń ś ń ś ś ś ś ś ś ś ś ś ś ś ś ś ź Ś ń ś ś Ź ś Ó ś ś ś ś ń ś ń Ó Ż ś ś ś ś ś ś ś ś ś ś ń ś ś ś ś ś ś ś Ż ś ś ś ś ś Ż Ź ś Ż ń ń ś ś Ź ś ś Ł Ś ś Ę Ż ś ś Ż ś ś ś ś ś
ń Ł Ó Ś ś ś ŁĄ Ś Ł Ś Ś ń Ś ś Ę Ę ń Ł Ó ń ś ń ś ś ś ś ś ś ś ś ś ś ś ś ś ź Ś ń ś ś Ź ś Ó ś ś ś ś ń ś ń Ó Ż ś ś ś ś ś ś ś ś ś ś ń ś ś ś ś ś ś ś Ż ś ś ś ś ś Ż Ź ś Ż ń ń ś ś Ź ś ś Ł Ś ś Ę Ż ś ś Ż ś ś ś ś ś
 Ś Ń Ż Ś ż Ś ć Ść Ó Ó Ó Ż Ż ć Ż Ó Ż Ż Ż Ś ć Ż Ś Ó Ó ć ć Ż Ż Ś Ś Ą Ś Ż Ó Ź Ż ć Ó Ź Ó Ś ć ć ć ć ż ć Ć Ż Ć ć ć Ż Ś Ó Ó ć ć Ć Ś Ó Ż Ó Ó ż Ż Ż ŚÓ Ż Ż Ą Ó Ż Ż ć Ść Ś Ż Ż Ź Ż Ż ć Ó Ó Ś Ś Ó Ż Ż Ż Ś Ż Ż ć Ż ć Ż
Ś Ń Ż Ś ż Ś ć Ść Ó Ó Ó Ż Ż ć Ż Ó Ż Ż Ż Ś ć Ż Ś Ó Ó ć ć Ż Ż Ś Ś Ą Ś Ż Ó Ź Ż ć Ó Ź Ó Ś ć ć ć ć ż ć Ć Ż Ć ć ć Ż Ś Ó Ó ć ć Ć Ś Ó Ż Ó Ó ż Ż Ż ŚÓ Ż Ż Ą Ó Ż Ż ć Ść Ś Ż Ż Ź Ż Ż ć Ó Ó Ś Ś Ó Ż Ż Ż Ś Ż Ż ć Ż ć Ż
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1. NAZWA PRODUKTU LECZNICZEGO Prismasol 2 mmol/l potasu, roztwór do hemodializy /hemofiltracji
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Prismasol 2 mmol/l potasu, roztwór do hemodializy /hemofiltracji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Produkt leczniczy Prismasol 2 mmol/l
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Prismasol 2 mmol/l potasu, roztwór do hemodializy /hemofiltracji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Produkt leczniczy Prismasol 2 mmol/l
100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix L., folium) (4-8:1). Ekstrahent: etanol 30% (m/m).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO bezpotasowy roztwór do hemofiltracji 2 mmol/l roztwór do hemofiltracji 3 mmol/l roztwór do hemofiltracji 4 mmol/l roztwór do hemofiltracji
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO bezpotasowy roztwór do hemofiltracji 2 mmol/l roztwór do hemofiltracji 3 mmol/l roztwór do hemofiltracji 4 mmol/l roztwór do hemofiltracji
Fresenius Kabi Polska Sp. z o.o. CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PŁYN FIZJOLOGICZNY WIELOELEKTROLITOWY IZOTONICZNY FRESENIUS, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY mg/1000 ml jony mmol/1000
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PŁYN FIZJOLOGICZNY WIELOELEKTROLITOWY IZOTONICZNY FRESENIUS, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY mg/1000 ml jony mmol/1000
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. RERE-SO-0050 Rev 00 Annex C SmPC Biphozyl (revised version)
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Biphozyl, roztwór do hemodializy/do hemofiltracji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Biphozyl jest dostępny w dwukomorowym worku.
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Biphozyl, roztwór do hemodializy/do hemofiltracji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Biphozyl jest dostępny w dwukomorowym worku.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GELOPLASMA, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Żelatyna w postaci zmodyfikowanej płynnej żelatyny* ilość wyrażona jako
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GELOPLASMA, roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Żelatyna w postaci zmodyfikowanej płynnej żelatyny* ilość wyrażona jako
Miejscowe oczyszczanie skóry: Wetrzeć niewielką ilość emulsji do kąpieli w zwilżoną uprzednio skórę, a następnie spłukać wodą i osuszyć ręcznikiem.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 634 mg/g, emulsja do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g emulsji do kąpieli zawiera 634 mg parafiny ciekłej, lekkiej (Paraffinum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 634 mg/g, emulsja do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g emulsji do kąpieli zawiera 634 mg parafiny ciekłej, lekkiej (Paraffinum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Każdy pojemnik jednodawkowy zawiera roztwór sodu kromoglikanu o stężeniu 20 mg/ml.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Alleoptical, 20 mg/ml, krople do oczu, roztwór w pojemniku jednodawkowym. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy pojemnik jednodawkowy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Alleoptical, 20 mg/ml, krople do oczu, roztwór w pojemniku jednodawkowym. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy pojemnik jednodawkowy
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH
 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH BUTELKA 500 ML 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI ŁUG LECZNICZY roztwór, produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Skład 1 l roztworu
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH BUTELKA 500 ML 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI ŁUG LECZNICZY roztwór, produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Skład 1 l roztworu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Patentex Oval N, 75 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka (3,15 g) zawiera: Nonoksynol-9 (INN) 75 mg Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Patentex Oval N, 75 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka (3,15 g) zawiera: Nonoksynol-9 (INN) 75 mg Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NERVOMIX Forte, kapsułka twarda 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera: Substancje czynne: Valerianae radix 210 mg, Lupuli
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NERVOMIX Forte, kapsułka twarda 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera: Substancje czynne: Valerianae radix 210 mg, Lupuli
Ulotka dołączona do opakowania: informacja dla użytkownika. Biphozyl, roztwór do hemodializy/do hemofiltracji Produkt złożony
 Ulotka dołączona do opakowania: informacja dla użytkownika Biphozyl, roztwór do hemodializy/do hemofiltracji Produkt złożony Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika Biphozyl, roztwór do hemodializy/do hemofiltracji Produkt złożony Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: Informacja dla użytkownika
 Ulotka dołączona do opakowania: Informacja dla użytkownika DIANEAL PD4 (glukoza 1,36%) zestaw do dializy otrzewnowej; 13,6 mg/ml DIANEAL PD4 (glukoza 2,27%) zestaw do dializy otrzewnowej; 22,7 mg/ml DIANEAL
Ulotka dołączona do opakowania: Informacja dla użytkownika DIANEAL PD4 (glukoza 1,36%) zestaw do dializy otrzewnowej; 13,6 mg/ml DIANEAL PD4 (glukoza 2,27%) zestaw do dializy otrzewnowej; 22,7 mg/ml DIANEAL
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. Bocheńska Lecznicza Sól Jodowo-Bromowa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Bocheńska Lecznicza Sól Jodowo-Bromowa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Produkt leczniczy zawiera sól jodowo-bromową, w tym jodki nie mniej
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Bocheńska Lecznicza Sól Jodowo-Bromowa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Produkt leczniczy zawiera sól jodowo-bromową, w tym jodki nie mniej
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
ZESTAWIENIE PARAMETRÓW TECHNICZNYCH
 Załącznik nr 6 ZESTAWIENIE PARAMETRÓW TECHNICZNYCH L.p. Nazwa wyrobu medycznego Przedmiot zamówienia: osprzęt do wykonywania ciągłych terapii nerkozastępczych Cena Wartość Opis przedmiotu zamówienie J.m.
Załącznik nr 6 ZESTAWIENIE PARAMETRÓW TECHNICZNYCH L.p. Nazwa wyrobu medycznego Przedmiot zamówienia: osprzęt do wykonywania ciągłych terapii nerkozastępczych Cena Wartość Opis przedmiotu zamówienie J.m.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Baycox 2,5%, 2,5 g/100 ml, roztwór doustny dla kur i indyków 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Toltrazuryl
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Baycox 2,5%, 2,5 g/100 ml, roztwór doustny dla kur i indyków 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Toltrazuryl
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2316460 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 12.05.2005 11001347.1
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2316460 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 12.05.2005 11001347.1
Aneks III. Zmiany do odpowiednich części Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta.
 Aneks III Zmiany do odpowiednich części Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta. Uwaga: Poszczególne punkty Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta są wynikiem zakończenia
Aneks III Zmiany do odpowiednich części Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta. Uwaga: Poszczególne punkty Charakterystyki Produktu Leczniczego i Ulotki dla pacjenta są wynikiem zakończenia
RESONIUM A, 1,42 g jonów sodu/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO RESONIUM A, 1,42 g jonów sodu/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 15 g proszku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO RESONIUM A, 1,42 g jonów sodu/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 15 g proszku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Espumisan 100 mg/ml, krople doustne, emulsja 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancja czynna: symetykon 1 ml zawiera 100 mg symetykonu.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Espumisan 100 mg/ml, krople doustne, emulsja 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancja czynna: symetykon 1 ml zawiera 100 mg symetykonu.
Ulotka dołączona do opakowania: informacja dla użytkownika. Aminoven Infant 10%, roztwór do infuzji
 Ulotka dołączona do opakowania: informacja dla użytkownika Aminoven Infant 10%, roztwór do infuzji Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla użytkownika Aminoven Infant 10%, roztwór do infuzji Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Lactulosum Aflofarm, 7,5 g/15 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 15 ml syropu zawiera 7,5 g laktulozy ciekłej (Lactulosum liquidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Lactulosum Aflofarm, 7,5 g/15 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 15 ml syropu zawiera 7,5 g laktulozy ciekłej (Lactulosum liquidum).
Fresenius Kabi Polska Sp. z o.o. CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GLUCOSUM 5% ET NATRIUM CHLORATUM 0,9% 2:1 FRESENIUS, (33,3 mg + 3,0 mg)/ml, roztwór do infuzji 2. SKŁAD ILOŚCIOWY I JAKOŚCIOWY 1 ml roztworu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GLUCOSUM 5% ET NATRIUM CHLORATUM 0,9% 2:1 FRESENIUS, (33,3 mg + 3,0 mg)/ml, roztwór do infuzji 2. SKŁAD ILOŚCIOWY I JAKOŚCIOWY 1 ml roztworu
BIONORICA Polska Sp z o.o. CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Lunapret 1
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO Lunapret 1 1. NAZWA PRODUKTU LECZNICZEGO Lunapret Valerianae radicis extractum siccum + Lupuli strobili extractum siccum tabletki powlekane, 250 mg + 60 mg 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO Lunapret 1 1. NAZWA PRODUKTU LECZNICZEGO Lunapret Valerianae radicis extractum siccum + Lupuli strobili extractum siccum tabletki powlekane, 250 mg + 60 mg 2. SKŁAD
Wszyscy uczestnicy postępowania. Znak: P-M/Z/ / /11 Data: r.
 Wszyscy uczestnicy postępowania Znak: P-M/Z/ / /11 Data: 12.10.2011 r. Dotyczy: postępowania w trybie przetargu nieograniczonego powyżej 193 000 euro na dostawę leków i środków farmaceutycznych (Znak Postępowania:
Wszyscy uczestnicy postępowania Znak: P-M/Z/ / /11 Data: 12.10.2011 r. Dotyczy: postępowania w trybie przetargu nieograniczonego powyżej 193 000 euro na dostawę leków i środków farmaceutycznych (Znak Postępowania:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. INJ. NATRII CHLORATI 10% POLPHARMA, 100 mg/ml, koncentrat do sporządzania roztworu do infuzji
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO INJ. NATRII CHLORATI 10% POLPHARMA, 100 mg/ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml koncentratu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO INJ. NATRII CHLORATI 10% POLPHARMA, 100 mg/ml, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml koncentratu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Osteogenon, 830 mg, tabletki powlekane 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 tabletka powlekana zawiera 830 mg kompleksu osseiny i hydroksyapatytu,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Osteogenon, 830 mg, tabletki powlekane 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 tabletka powlekana zawiera 830 mg kompleksu osseiny i hydroksyapatytu,
6,00 g 6,40 g 10,27 g. 4,59 g 5,53 g 5,13 g 2,05 g 5,13 g 3,02 g 3,88 g 2,59 g 2,16 g 1,29 g 1,66 g 2,59 0,54 g. 0,37 g
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Aminomel Nephro roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml roztworu zawiera: L-izoleucyna L-leucyna L-lizyny octan (odpowiada
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Aminomel Nephro roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1000 ml roztworu zawiera: L-izoleucyna L-leucyna L-lizyny octan (odpowiada
Zastosowanie antykoagulacji cytrynianowej w ciągłej terapii nerkozastępczej u niemowląt z ostrym uszkodzeniem nerek.
 Zastosowanie antykoagulacji cytrynianowej w ciągłej terapii nerkozastępczej u niemowląt z ostrym uszkodzeniem nerek. Klinka Kardiologii i Nefrologii Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu
Zastosowanie antykoagulacji cytrynianowej w ciągłej terapii nerkozastępczej u niemowląt z ostrym uszkodzeniem nerek. Klinka Kardiologii i Nefrologii Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Moxalole, 13,125 g + 350,7 mg + 46,6 mg + 178,5 mg, proszek do sporządzania roztworu doustnego
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Moxalole, 13,125 g + 350,7 mg + 46,6 mg + 178,5 mg, proszek do sporządzania roztworu doustnego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda saszetka
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Moxalole, 13,125 g + 350,7 mg + 46,6 mg + 178,5 mg, proszek do sporządzania roztworu doustnego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda saszetka
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Syrop tymiankowy Labima, 110 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Płynny wyciąg z ziela tymianku (Thymi extractum fluidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Syrop tymiankowy Labima, 110 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Płynny wyciąg z ziela tymianku (Thymi extractum fluidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Skład produktu leczniczego NUTRYELT wyrażony w ilości soli na ampułkę (10 ml) i na litr.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Skład produktu leczniczego wyrażony w ilości soli na ampułkę
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Skład produktu leczniczego wyrażony w ilości soli na ampułkę
, , , , 0
 S T E R O W N I K G R E E N M I L L A Q U A S Y S T E M 2 4 V 4 S E K C J I G B 6 9 6 4 C, 8 S E K C J I G B 6 9 6 8 C I n s t r u k c j a i n s t a l a c j i i o b s ł u g i P r z e d r o z p o c z ę
S T E R O W N I K G R E E N M I L L A Q U A S Y S T E M 2 4 V 4 S E K C J I G B 6 9 6 4 C, 8 S E K C J I G B 6 9 6 8 C I n s t r u k c j a i n s t a l a c j i i o b s ł u g i P r z e d r o z p o c z ę
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sanosvit Calcium, 114 mg jonów wapnia (Ca 2+ )/ 5 ml, syrop. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 5 ml syropu zawiera substancje czynne: Glukonolaktobionian
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sanosvit Calcium, 114 mg jonów wapnia (Ca 2+ )/ 5 ml, syrop. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 5 ml syropu zawiera substancje czynne: Glukonolaktobionian
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO FORTRANS, 74 g, proszek do sporządzania roztworu doustnego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Makrogol 4000 * Sodu siarczan bezwodny. Sodu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO FORTRANS, 74 g, proszek do sporządzania roztworu doustnego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Makrogol 4000 * Sodu siarczan bezwodny. Sodu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum Plus (525 mg + 60 mg + 20 mg)/g, roztwór do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g roztworu do kąpieli zawiera 525 mg parafiny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum Plus (525 mg + 60 mg + 20 mg)/g, roztwór do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g roztworu do kąpieli zawiera 525 mg parafiny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 20 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 20 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Supliven, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Supliven zawiera: 1 ml 1 ampułka (10 ml) chromu(iii)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Supliven, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Supliven zawiera: 1 ml 1 ampułka (10 ml) chromu(iii)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. CALCIUM RESONIUM 1,2 g jonów wapnia/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CALCIUM RESONIUM 1,2 g jonów wapnia/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CALCIUM RESONIUM 1,2 g jonów wapnia/15 g, proszek doustny lub do sporządzania zawiesiny doodbytniczej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Znaczenie równowagi mineralnej Dla pacjentów dializowanych otrzewnowo
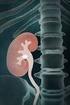 Znaczenie równowagi mineralnej Dla pacjentów dializowanych otrzewnowo Str. 1 Dlaczego dializa jest ważna? Dializa pomaga: 1. Usuwać produkty przemiany materii Zdrowe nerki filtrują krew, usuwając z niej
Znaczenie równowagi mineralnej Dla pacjentów dializowanych otrzewnowo Str. 1 Dlaczego dializa jest ważna? Dializa pomaga: 1. Usuwać produkty przemiany materii Zdrowe nerki filtrują krew, usuwając z niej
Ulotka dołączona do opakowania: informacja dla użytkownika. Benelyte, roztwór do infuzji Produkt złożony
 Ulotka dołączona do opakowania: informacja dla użytkownika, roztwór do infuzji Produkt złożony Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne
Ulotka dołączona do opakowania: informacja dla użytkownika, roztwór do infuzji Produkt złożony Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne
