CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
|
|
|
- Dominik Ignacy Jaworski
- 6 lat temu
- Przeglądów:
Transkrypt
1 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Starelltec Alergia, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 1 mg olopatadyny (w postaci olopatadyny chlorowodorku). Każda kropla roztworu zawiera 0,03 mg olopatadyny (w postaci olopatadyny chlorowodorku). Pełny wykaz substancji pomocniczych, patrz punkt POSTAĆ FARMACEUTYCZNA Krople do oczu, roztwór Przezroczysty, bezbarwny lub prawie bezbarwny roztwór. Osmolalność: mosmol/kg ph: 6,7-7,3 4. SZCZEGÓŁOWE DANE KLINICZNE 4.1 Wskazania do stosowania Leczenie objawów ocznych u pacjentów z rozpoznanym sezonowym alergicznym zapaleniem spojówek. Produkt może być stosowany tylko u osób dorosłych. 4.2 Dawkowanie i sposób podawania Dawkowanie Dorośli Produkt Starelltec Alergia podaje się po jednej kropli do worka spojówkowego chorego oka (oczu) dwa razy na dobę (z zachowaniem 8 godzin przerwy pomiędzy zakropleniem kolejnych dawek). W przypadku braku poprawy lub pogorszenia się objawów w ciągu trzech dni od rozpoczęcia stosowania produktu leczniczego należy skonsultować się z lekarzem. Czas leczenia wynosi do dwóch tygodni. O ile jest to niezbędne, leczenie można kontynuować przez okres do czterech miesięcy po konsultacji lekarskiej. Stosowanie u pacjentów w podeszłym wieku Nie ma konieczności zmiany dawkowania u pacjentów w podeszłym wieku. Dzieci i młodzież Produktu Starelltec Alergia nie należy stosować u dzieci i młodzieży w wieku poniżej 18 lat. Stosowanie u pacjentów z zaburzeniami czynności wątroby i nerek Olopatadyny w postaci kropli do oczu nie badano u pacjentów z chorobami nerek lub wątroby. Nie należy jednak spodziewać się, aby u pacjentów z zaburzeniami czynności nerek lub wątroby istniała konieczność dostosowania dawkowania (patrz punkt 5.2). 1
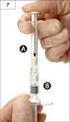
2 Sposób podawania Do stosowania wyłącznie do oka. Produkt Starelltec Alergia to sterylny roztwór, który nie zawiera środków konserwujących. Przed zakropleniem kropli do oczu: - W przypadku pierwszego użycia, przed podaniem kropli do oka, pacjent powinien wypróbować użycie butelki z kroplomierzem, ściskając ją powoli, aż jedna kropla zostanie wypuszczona z butelki, z dala od oka. - Jeżeli pacjent jest pewny, że może zakroplić pojedynczą kroplę, powinien przyjąć najbardziej komfortową pozycję do jego zakroplenia (może siedzieć, leżeć na plecach albo stanąć przed lustrem). Instrukcja stosowania: 1. Przed zakropleniem produktu pacjent powinien dokładnie umyć ręce. 2. Jeśli opakowanie lub butelka są uszkodzone, produktu nie należy stosować. 3. Przed pierwszym użyciem kropli należy odkręcić zakrętkę po upewnieniu się, że pierścień gwarancyjny na zakrętce jest nieprzerwany. Podczas odkręcania pacjent odczuje lekki opór, dopóki pierścień się nie przerwie. 4. Jeśli pierścień gwarancyjny jest poluzowany, należy usunąć go przed zastosowaniem produktu, ponieważ może wpaść do oka i wywołać obrażenia. 5. Pacjent powinien odchylić głowę do tyłu, a następnie palcem delikatnie odciągnąć powiekę ku dołowi, tak by między gałką oczną a powieką utworzyła się kieszonka. (Należy unikać kontaktu końcówki kroplomierza z okiem, powiekami czy palcami.) 6. Zakroplić jedną kroplę naciskając powoli butelkę. Butelkę należy delikatnie ścisnąć w środkowej części, tak aby kropla dostała się do oka pacjenta. Należy pamiętać, że może być kilka sekund opóźnienia pomiędzy ściśnięciem butelki, a uwolnieniem kropli. Pacjent nie powinien zbyt mocno ściskać butelki. Należy poinformować pacjenta, aby skonsultował się z farmaceutą w przypadku jakichkolwiek wątpliwości dotyczących stosowania leku. 7. Jeśli lekarz zaleci stosowanie kropli do drugiego oka, należy powtórzyć czynności z punktu 5. i Po użyciu a przed zamknięciem butelki, w celu usunięcia pozostałości płynu z końcówki należy wstrząsnąć butelkę w dół nie dotykając końcówki kroplomierza w celu usunięcia płynu pozostałego na końcówce kroplomierza. Jest to konieczne w celu zapewnienia możliwości zakroplenia kolejnych kropli. Bezpośrednio po użyciu dokładnie zakręcić butelkę. W razie jednoczesnego stosowania innych podawanych do oka produktów leczniczych, należy zachować odstęp pięciu minut pomiędzy podaniem kolejnych produktów. Maści do oczu należy stosować na końcu. 4.3 Przeciwwskazania Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania Starelltec Alergia jest produktem przeciwalergicznym i przeciwhistaminowym, który mimo podawania miejscowego podlega wchłanianiu ogólnoustrojowemu. W razie wystąpienia objawów ciężkich reakcji niepożądanych lub nadwrażliwości produkt należy odstawić. Brak poprawy lub pogorszenie się objawów w ciągu trzech dni od rozpoczęcia stosowania produktu leczniczego wymaga konsultacji z lekarzem. 2
3 Nie badano stosowania produktu Starelltec Alergia u pacjentów noszących soczewki kontaktowe. Pacjentów należy poinformować, aby wyjmowali soczewki kontaktowe z oka przed zakropleniem produktu i odczekali co najmniej 15 minut przed ich ponownym założeniem. 4.5 Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji Nie przeprowadzono badań dotyczących interakcji z innymi produktami leczniczymi. Wyniki badań in vitro wykazały, że olopatadyna nie hamuje reakcji metabolicznych przebiegających z udziałem izoenzymów 1A2, 2C8, 2C9, 2C19, 2D6, 2E1 i 3A4 cytochromu P-450. Wyniki te wskazują, że nie jest prawdopodobne, aby olopatadyna wchodziła w interakcje metaboliczne z innymi jednocześnie podawanymi substancjami czynnymi. 4.6 Wpływ na płodność, ciążę i laktację Ciąża Brak danych lub istnieją tylko ograniczone dane dotyczące stosowania do oka olopatadyny u kobiet w okresie ciąży. Badania na zwierzętach wykazały szkodliwy wpływ na reprodukcję po podaniu ogólnym (patrz punkt 5.3). Nie zaleca się stosowania olopatadyny u kobiet w ciąży i u kobiet w wieku rozrodczym nie stosujących odpowiednich metod zapobiegania ciąży. Karmienie piersią Badania na zwierzętach wykazały, że olopatadyna przenika do mleka po podaniu doustnym (informacja szczegółowa, patrz punkt 5.3). Nie można wykluczyć zagrożenia dla noworodków/niemowląt. Nie należy stosować produktu leczniczego Starelltec Alergia w okresie karmienia piersią. Płodność Nie przeprowadzono badań mających na celu ocenę wpływu miejscowego podania do oka olopatadyny na płodność u ludzi. 4.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn Produkt leczniczy Starelltec Alergia nie ma wpływu lub wywiera nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn. Podobnie jak w przypadku stosowania wszystkich kropli do oczu, przemijające niewyraźne widzenie lub inne zaburzenia widzenia mogą wpływać na zdolność prowadzenia pojazdów i obsługiwania maszyn. Jeśli po zastosowaniu kropli do oczu wystąpi niewyraźne widzenie, należy odczekać do momentu uzyskania pełnej ostrości widzenia przed prowadzeniem pojazdów lub obsługiwaniem maszyn. 4.8 Działania niepożądane Podsumowanie profilu bezpieczeństwa W badaniach klinicznych prowadzonych z udziałem 1680 pacjentów, olopatadynę podawano jeden do czterech razy na dobę do obu oczu, przez okres do czterech miesięcy. Produkt stosowano w monoterapii lub jako leczenie uzupełniające do stosowania loratadyny w dawce 10 mg. Można przyjąć, że u około 4,5% pacjentów wystąpiły działania niepożądane związane ze stosowaniem olopatadyny, jednak tylko 1,6% pacjentów przerwało udział w badaniach klinicznych z powodu działań niepożądanych. W badaniach klinicznych nie notowano żadnych, okulistycznych ani 3
4 ogólnoustrojowych, ciężkich działań niepożądanych, związanych ze stosowaniem olopatadyny. Najczęściej zgłaszanym działaniem niepożądanym związanym z leczeniem był ból oka, notowany z ogólną ścią 0,7%. Tabelaryczne zestawienie działań niepożądanych W badaniach klinicznych i po wprowadzeniu do obrotu zgłaszano następujące działania niepożądane, które sklasyfikowano zgodnie z następującą konwencją: bardzo ( 1/10), ( 1/100 do <1/10), niezbyt ( 1/1 000 do <1/100), rzadko ( 1/ do <1/1 000), bardzo rzadko (<1/10 000), ść nieznana (ść nie może być określona na podstawie dostępnych danych). W obrębie każdej grupy o określonej ści występowania objawy niepożądane są wymienione zgodnie ze zmniejszającym się nasileniem. Klasyfikacja Układów i Częstość Działania niepożądane Narządów Zakażenia i zarażenia Niezbyt nieżyt błony śluzowej nosa pasożytnicze Zaburzenia układu Nieznana nadwrażliwość, obrzęk twarzy immunologicznego Zaburzenia układu nerwowego Często bóle głowy, zaburzenia smaku Niezbyt zawroty głowy, obniżenie czucia dotyku Nieznana senność Zaburzenia oka Często ból oka, podrażnienie oka, suchość oka, nietypowe odczucia wewnątrz oka Niezbyt nadżerki rogówki, nieprawidłowości nabłonka rogówki, choroby nabłonka rogówki, punktowe zapalenie rogówki, zapalenie rogówki, plamki na rogówce, wydzielina z oka, światłowstręt, niewyraźne widzenie, zmniejszona ostrość widzenia, kurcz powiek, dyskomfort w oku, świąd oka, grudki na spojówkach, choroby spojówek, uczucie obecności ciała obcego w oczach, zwiększone łzawienie, zaczerwienienie powiek, obrzęk powiek, choroby powiek, przekrwienie spojówek Nieznana obrzęk rogówki, obrzęk oka, zapalenie spojówek, rozszerzenie źrenicy, zaburzenia widzenia, strupki na brzegach powiek Zaburzenia układu Często suchość błony śluzowej nosa oddechowego, Nieznana duszność, zapalenie zatok klatki piersiowej i śródpiersia Zaburzenia żołądka i jelit Nieznana nudności, wymioty Zaburzenia skóry i tkanki podskórnej Niezbyt kontaktowe zapalenie skóry, uczucie pieczenia skóry, suchość skóry Nieznana zapalenie skóry, rumień Zaburzenia ogólne i stany Często zmęczenie w miejscu podania Nieznana astenia, złe samopoczucie U pacjentów ze znacznie uszkodzoną rogówką bardzo rzadko obserwowano zwapnienie rogówki związane ze stosowaniem kropli do oczu zawierających fosforany. 4
5 Zgłaszanie podejrzewanych działań niepożądanych Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych Al. Jerozolimskie 181C Warszawa Tel.: Faks: ndl@urpl.gov.pl Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu. 4.9 Przedawkowanie Nie są dostępne dane na temat przypadkowego lub zamierzonego przedawkowania olopatadyny u ludzi poprzez jej przyjęcie drogą doustną. Olopatadyna wykazuje małą toksyczność ostrą dla zwierząt. Przypadkowe połknięcie całej zawartości butelki z olopatadyną może spowodować ogólnoustrojowe narażenie pacjenta na maksymalnie 5 mg olopatadyny. Zakładając 100% wchłanianie, taka ekspozycja w przypadku dziecka o masie ciała 10 kg odpowiadałaby przyjęciu dawki 0,5 mg/kg mc. U psów obserwowano wydłużenie odstępu QTc tylko w przypadku ekspozycji na olopatadynę znacznie przekraczającej maksymalną ekspozycję uzyskiwaną u ludzi, co wskazuje na niewielkie znaczenie tych obserwacji dla stosowania leku w warunkach klinicznych. Olopatadynę podawano doustnie w dawce 5 mg dwa razy na dobę przez 2,5 dnia grupie 102 młodych i starszych zdrowych ochotników obu płci; nie zanotowano przy tym znaczącego wydłużenia odstępu QTc w porównaniu z placebo. Zakres stężeń maksymalnych olopatadyny w osoczu w stanie stacjonarnym obserwowany w tym badaniu (35 do 127 ng/ml) wyznacza co najmniej 70-krotny przedział bezpieczeństwa dla olopatadyny stosowanej miejscowo z punktu widzenia wpływu na repolaryzację serca. W razie przedawkowania należy wdrożyć odpowiednie monitorowanie i postępowanie lecznicze. W razie miejscowego przedawkowania produktu leczniczego Starelltec Alergia nadmiar produktu można wypłukać z oka (oczu) letnią wodą. 5. WŁAŚCIWOŚCI FARMAKOLOGICZNE 5.1 Właściwości farmakodynamiczne Grupa farmakoterapeutyczna: produkty okulistyczne; obkurczające naczynia i przeciwalergiczne; inne leki przeciwalergiczne, kod ATC: S01GX 09 Olopatadyna jest silnym i wybiórczym przeciwalergicznym/przeciwhistaminowym produktem leczniczym, który wywiera efekty lecznicze na drodze wielu różnych mechanizmów działania. Olopatadyna antagonizuje działanie histaminy (podstawowego mediatora odpowiedzi alergicznej u ludzi) i zapobiega indukowanemu histaminą wytwarzaniu cytokin przez ludzkie komórki nabłonka spojówki. Dane uzyskane z badań in vitro sugerują, że może ona wpływać na ludzkie komórki tuczne spojówki hamując wytwarzanie mediatorów zapalenia. Sugeruje się, że u pacjentów z drożnym przewodem nosowo-łzowym miejscowe podanie olopatadyny do oka zmniejsza nasilenie przedmiotowych i podmiotowych objawów ze strony nosa, które współistnieją z sezonowym alergicznym zapaleniem spojówek. Olopatadyna nie powoduje klinicznie znaczących zmian średnicy źrenicy. 5
6 5.2 Właściwości farmakokinetyczne Wchłanianie Olopatadyna, podobnie jak inne miejscowo podawane produkty lecznicze, jest wchłaniana ogólnoustrojowo. Ogólnoustrojowe wchłanianie olopatadyny podawanej miejscowo jest jednak minimalne; stężenia występujące w osoczu mieszczą się w zakresie od poniżej granicy oznaczalności (<0,5 ng/ml) do 1,3 ng/ml. Stężenia te są od 50 do 200 razy mniejsze od stężeń uzyskiwanych po podawaniu dobrze tolerowanych dawek doustnych. Eliminacja Z badań farmakokinetycznych prowadzonych po podawaniu doustnym wynika, że okres półtrwania olopatadyny w osoczu wynosi w przybliżeniu 8 do 12 godzin, a eliminacja odbywa się głównie poprzez wydzielanie nerkowe. Około 60-70% dawki wydala się z moczem w postaci niezmienionej. W moczu wykryto obecność dwóch metabolitów występujących w małych stężeniach: monodemetyloolopatadyny i N-tlenku olopatadyny. Ponieważ olopatadyna wydala się przez nerki głównie w postaci niezmienionej, zaburzenie czynności nerek zmienia farmakokinetykę olopatadyny powodując u pacjentów z ciężkim zaburzeniem czynności nerek (średni klirens kreatyniny 13,0 ml/min) 2,3-krotne zwiększenie stężeń maksymalnych w osoczu w porównaniu ze zdrowymi dorosłymi. Po doustnym podaniu dawki 10 mg pacjentom poddawanym hemodializie (nie wydalającym moczu), stężenia olopatadyny w osoczu były znacząco mniejsze w dniu wykonywania hemodializy niż w dniach, w których nie przeprowadzano tego zabiegu, co sugeruje, że olopatadyna może być usuwana z organizmu poprzez hemodializę. Badania porównujące farmakokinetykę olopatadyny podawanej doustnie w dawce 10 mg młodym ochotnikom (średnia wieku 21 lat) i ochotnikom w wieku podeszłym (średnia wieku 74 lata) nie wykazały żadnych znaczących różnic w stężeniach w osoczu (AUC), wiązaniu z białkami lub wydalaniu w moczu nie zmienionego leku i jego metabolitów. Badanie wpływu zaburzenia czynności nerek na farmakokinetykę olopatadyny po podaniu doustnym przeprowadzono u pacjentów z ciężkim zaburzeniem czynności nerek. Wyniki wskazują, że w tej populacji po podaniu olopatadyny można spodziewać się nieco większych stężeń w osoczu. Ponieważ stężenia olopatadyny w osoczu po miejscowym podaniu do oka są 50 do 200 razy mniejsze niż po podaniu dobrze tolerowanych dawek doustnych, nie wydaje się, aby istniała konieczność zmiany dawkowania u pacjentów w podeszłym wieku lub u pacjentów z zaburzoną czynnością nerek. Metabolizm wątrobowy ma mniejsze znaczenie dla eliminacji olopatadyny. U pacjentów z zaburzoną czynnością wątroby zmiana dawkowania olopatadyny nie wydaje się konieczna. 5.3 Przedkliniczne dane o bezpieczeństwie Dane niekliniczne, wynikające z konwencjonalnych badań farmakologicznych dotyczących bezpieczeństwa, badań toksyczności po podaniu wielokrotnym, genotoksyczności, rakotwórczości oraz toksycznego wpływu na rozród i rozwój potomstwa, nie ujawniają szczególnego zagrożenia dla człowieka. Badania na zwierzętach wykazały zmniejszony wzrost potomstwa karmionego mlekiem matek, które otrzymywały ogólnoustrojowe dawki olopatadyny znacznie przekraczające maksymalne zalecane dla człowieka dawki podawane do oka. Olopatadynę wykryto w mleku karmiących samic szczura po podaniu doustnym. 6. DANE FARMACEUTYCZNE 6.1 Wykaz substancji pomocniczych Sodu chlorek Disodu fosforan dwunastowodny 6
7 Polisorbat 80 Kwas solny rozcieńczony (do ustalenia ph) Woda wysokooczyszczona 6.2 Niezgodności farmaceutyczne Nie dotyczy. 6.3 Okres ważności 2 lata Okres ważności po pierwszym otwarciu butelki: 90 dni. 6.4 Specjalne środki ostrożności podczas przechowywania Przechowywać w temperaturze poniżej 30 C. 6.5 Rodzaj i zawartość opakowania Opakowanie to białe butelki 5 ml (LDPE), z wielodawkowym kroplomierzem (HDPE) zapobiegającym zanieczyszczeniu roztworu bakteriami dzięki systemowi składającemu się z silikonowej membrany i filtrowaniu powietrza zasysanego do butelki, z zakrętką z HDPE z pierścieniem gwarancyjnym, w tekturowym pudełku. 1 x 5 ml butelka 6.6 Specjalne środki ostrożności dotyczące usuwania Bez specjalnych wymagań. 7. PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU Warszawskie Zakłady Farmaceutyczne Polfa S.A. ul. Karolkowa 22/ Warszawa 8. NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU Pozwolenie nr DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: r. 10. DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO r. Charakterystyka Produktu Leczniczego zgodna z Decyzją Prezesa URPL z dn r. 7
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Olopatadine Zentiva, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Olopatadine Zentiva, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Nolodon, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci olopatadyny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Nolodon, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci olopatadyny
Leczenie ocznych objawów przedmiotowych i podmiotowych sezonowego alergicznego zapalenia spojówek.
 1. NAZWA PRODUKTU LECZNICZEGO Oftahist, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci chlorowodorku). Substancje pomocnicze: chlorek
1. NAZWA PRODUKTU LECZNICZEGO Oftahist, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci chlorowodorku). Substancje pomocnicze: chlorek
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO OPATANOL 1 mg/ml krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO OPATANOL 1 mg/ml krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci
Ulotka dołączona do opakowania: informacja dla pacjenta. Starelltec Alergia, 1 mg/ml, krople do oczu, roztwór. Olopatadinum
 Ulotka dołączona do opakowania: informacja dla pacjenta Starelltec Alergia, 1 mg/ml, krople do oczu, roztwór Olopatadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta Starelltec Alergia, 1 mg/ml, krople do oczu, roztwór Olopatadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg sodu kromoglikanu (Natrii cromoglicas).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg sodu kromoglikanu (Natrii cromoglicas).
Substancje pomocnicze o znanym działaniu: benzalkoniowy chlorek 0,1 mg
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ALERPALUX, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci olopatadyny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ALERPALUX, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci olopatadyny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Artelac, 3,2 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3,2 mg hypromelozy (Hypromellosum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Artelac, 3,2 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3,2 mg hypromelozy (Hypromellosum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 20 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 20 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Każdy pojemnik jednodawkowy zawiera roztwór sodu kromoglikanu o stężeniu 20 mg/ml.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Alleoptical, 20 mg/ml, krople do oczu, roztwór w pojemniku jednodawkowym. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy pojemnik jednodawkowy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Alleoptical, 20 mg/ml, krople do oczu, roztwór w pojemniku jednodawkowym. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy pojemnik jednodawkowy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Cusicrom 4%, 40 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 40 mg kromoglikanu disodu. Substancja
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Cusicrom 4%, 40 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 40 mg kromoglikanu disodu. Substancja
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ESPUMISAN, 40 mg, kapsułki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda kapsułka zawiera 40 mg symetykonu. Substancje pomocnicze o znanym działaniu:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ESPUMISAN, 40 mg, kapsułki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda kapsułka zawiera 40 mg symetykonu. Substancje pomocnicze o znanym działaniu:
Ulotka dołączona do opakowania: informacja dla pacjenta. Nolodon, 1 mg/ml, krople do oczu, roztwór. Olopatadinum
 Ulotka dołączona do opakowania: informacja dla pacjenta Nolodon, 1 mg/ml, krople do oczu, roztwór Olopatadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
Ulotka dołączona do opakowania: informacja dla pacjenta Nolodon, 1 mg/ml, krople do oczu, roztwór Olopatadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml produktu zawiera 0,345 mg wodorofumaranu ketotifenu, co odpowiada 0,25 mg ketotifenu (Ketotifenum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zaditen, 0,25 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu zawiera 0,345 mg wodorofumaranu ketotifenu,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zaditen, 0,25 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu zawiera 0,345 mg wodorofumaranu ketotifenu,
Oftahist, 1 mg/ml, krople do oczu, roztwór Olopatadyna
 Ulotka dołączona do opakowania: informacja dla użytkownika Oftahist, 1 mg/ml, krople do oczu, roztwór Olopatadyna Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika Oftahist, 1 mg/ml, krople do oczu, roztwór Olopatadyna Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 3 mg Hypromellosum (hypromelozy) i 1 mg Dextranum (dekstranu 70).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Tears Naturale II, (3 mg + 1 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3 mg Hypromellosum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Tears Naturale II, (3 mg + 1 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3 mg Hypromellosum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kg proszku do sporządzania roztworu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kg proszku do sporządzania roztworu
Miejscowe oczyszczanie skóry: Wetrzeć niewielką ilość emulsji do kąpieli w zwilżoną uprzednio skórę, a następnie spłukać wodą i osuszyć ręcznikiem.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 634 mg/g, emulsja do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g emulsji do kąpieli zawiera 634 mg parafiny ciekłej, lekkiej (Paraffinum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 634 mg/g, emulsja do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g emulsji do kąpieli zawiera 634 mg parafiny ciekłej, lekkiej (Paraffinum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Cholestil Max, 200 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 tabletka zawiera 200 mg hymekromonu (Hymecromonum) Pełny wykaz substancji
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Cholestil Max, 200 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 tabletka zawiera 200 mg hymekromonu (Hymecromonum) Pełny wykaz substancji
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g płynu do stosowania na skórę zawiera 100
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g płynu do stosowania na skórę zawiera 100
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 10 mg substancji czynnej klotrymazolu (Clotrimazolum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Fungotac 10 mg/ml, krople do uszu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg substancji czynnej klotrymazolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Fungotac 10 mg/ml, krople do uszu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg substancji czynnej klotrymazolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ 1 g płynu do stosowania
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ 1 g płynu do stosowania
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Patentex Oval N, 75 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka (3,15 g) zawiera: Nonoksynol-9 (INN) 75 mg Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Patentex Oval N, 75 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka (3,15 g) zawiera: Nonoksynol-9 (INN) 75 mg Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CONDYLINE, 5 mg/ml, roztwór na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu na skórę zawiera 5 mg podofilotoksyny (Podophyllotoxinum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CONDYLINE, 5 mg/ml, roztwór na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu na skórę zawiera 5 mg podofilotoksyny (Podophyllotoxinum).
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO EMADINE 0,5 mg/ml, krople do oczu, roztwór, pojemnik jednodawkowy. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO EMADINE 0,5 mg/ml, krople do oczu, roztwór, pojemnik jednodawkowy. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera
100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix L., folium) (4-8:1). Ekstrahent: etanol 30% (m/m).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
Ulotka dołączona do opakowania: informacja dla pacjenta. Bimifree, 0,3 mg/ml, krople do oczu, roztwór Bimatoprost
 Ulotka dołączona do opakowania: informacja dla pacjenta Bimifree, 0,3 mg/ml, krople do oczu, roztwór Bimatoprost Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta Bimifree, 0,3 mg/ml, krople do oczu, roztwór Bimatoprost Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta. Tobrosopt-DEX, (3 mg + 1 mg)/ml, krople do oczu, zawiesina Tobramycinum + Dexamethasonum
 Ulotka dołączona do opakowania: informacja dla pacjenta Tobrosopt-DEX, (3 mg + 1 mg)/ml, krople do oczu, zawiesina Tobramycinum + Dexamethasonum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla pacjenta Tobrosopt-DEX, (3 mg + 1 mg)/ml, krople do oczu, zawiesina Tobramycinum + Dexamethasonum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Syrop tymiankowy Labima, 110 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Płynny wyciąg z ziela tymianku (Thymi extractum fluidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Syrop tymiankowy Labima, 110 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Płynny wyciąg z ziela tymianku (Thymi extractum fluidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 czopek zawiera 400 mg tribenozydu (Tribenosidum) i 40 mg lidokainy (Lidocainum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Procto-Glyvenol, 400 mg + 40 mg, czopki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 czopek zawiera 400 mg tribenozydu (Tribenosidum) i 40 mg lidokainy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Procto-Glyvenol, 400 mg + 40 mg, czopki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 czopek zawiera 400 mg tribenozydu (Tribenosidum) i 40 mg lidokainy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIFADOL 0,1% 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml zawiera 1 mg diklofenaku sodowego (Diclofenacum natricum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIFADOL 0,1% 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml zawiera 1 mg diklofenaku sodowego (Diclofenacum natricum).
Ulotka dla pacjenta: informacja dla użytkownika. Nodofree, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 Ulotka dla pacjenta: informacja dla użytkownika Nodofree, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dla pacjenta: informacja dla użytkownika Nodofree, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Toselix, 0,8 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml syropu zawiera 0,8 mg butamiratu cytrynianu (Butamirati citras). 5 ml syropu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Toselix, 0,8 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml syropu zawiera 0,8 mg butamiratu cytrynianu (Butamirati citras). 5 ml syropu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TROPICAMIDUM WZF 1%, 10 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg tropikamidu (Tropicamidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TROPICAMIDUM WZF 1%, 10 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg tropikamidu (Tropicamidum).
Ulotka dołączona do opakowania: informacja dla pacjenta. Olopatadine Zentiva, 1 mg/ml, krople do oczu, roztwór Olopatadinum
 Ulotka dołączona do opakowania: informacja dla pacjenta Olopatadine Zentiva, 1 mg/ml, krople do oczu, roztwór Olopatadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta Olopatadine Zentiva, 1 mg/ml, krople do oczu, roztwór Olopatadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO EMADINE 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 0,5 mg emedastyny (w postaci
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO EMADINE 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 0,5 mg emedastyny (w postaci
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA HANDLOWA LEKU GOTOWEGO SALICYLOL 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH (W PRZELICZENIU NA 100g)
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA HANDLOWA LEKU GOTOWEGO SALICYLOL 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH (W PRZELICZENIU NA 100g)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1.NAZWA PRODUKTU LECZNICZEGO Transpulmin S, (10 g + 3 g)/100 g, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 100 mg olejku eukaliptusowego (Eucalypti aetheroleum)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1.NAZWA PRODUKTU LECZNICZEGO Transpulmin S, (10 g + 3 g)/100 g, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 100 mg olejku eukaliptusowego (Eucalypti aetheroleum)
Produktu nie należy stosować pod opatrunkiem okluzyjnym lub w postaci okładów.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Amol, produkt złożony, płyn doustny, płyn na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g produktu zawiera: Mentholum (mentol) 17,23 mg Citronellae
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Amol, produkt złożony, płyn doustny, płyn na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g produktu zawiera: Mentholum (mentol) 17,23 mg Citronellae
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO EMADINE 0,5 mg/ml, krople do oczu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 0,5 mg emedastyny (w postaci
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO EMADINE 0,5 mg/ml, krople do oczu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 0,5 mg emedastyny (w postaci
Ulotka dołączona do opakowania: informacja dla pacjenta. ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum
 Ulotka dołączona do opakowania: informacja dla pacjenta ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta. DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum
 Ulotka dołączona do opakowania: informacja dla pacjenta DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NIZAX ACTIV, 20 mg/g, szampon leczniczy 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g szamponu leczniczego zawiera 20 mg ketokonazolu (Ketoconazolum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NIZAX ACTIV, 20 mg/g, szampon leczniczy 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g szamponu leczniczego zawiera 20 mg ketokonazolu (Ketoconazolum).
Ulotka dołączona do opakowania: informacja dla użytkownika. Olopatadyna Abdi, 1 mg/ml, krople do oczu, roztwór Olopatadyna
 Ulotka dołączona do opakowania: informacja dla użytkownika Olopatadyna Abdi, 1 mg/ml, krople do oczu, roztwór Olopatadyna Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika Olopatadyna Abdi, 1 mg/ml, krople do oczu, roztwór Olopatadyna Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika. Tears Naturale II (3 mg + 1 mg)/ml, krople do oczu, roztwór Hypromellosum + Dextranum
 Ulotka dołączona do opakowania: informacja dla użytkownika Tears Naturale II (3 mg + 1 mg)/ml, krople do oczu, roztwór Hypromellosum + Dextranum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika Tears Naturale II (3 mg + 1 mg)/ml, krople do oczu, roztwór Hypromellosum + Dextranum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Substancja pomocnicza o znanym działaniu: benzalkoniowy chlorek, roztwór.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml zawiera 1 mg diklofenaku sodowego (Diclofenacum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml zawiera 1 mg diklofenaku sodowego (Diclofenacum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO BETADRIN, (1 mg + 0,33 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera jako substancje czynne:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO BETADRIN, (1 mg + 0,33 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera jako substancje czynne:
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta BETADRIN, (1 mg + 0,33 mg)/ml, krople do oczu, roztwór Diphenhydramini hydrochloridum + Naphazolini nitras Należy uważnie zapoznać się z treścią
Ulotka dołączona do opakowania: informacja dla pacjenta BETADRIN, (1 mg + 0,33 mg)/ml, krople do oczu, roztwór Diphenhydramini hydrochloridum + Naphazolini nitras Należy uważnie zapoznać się z treścią
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Zineryt 40 mg/ml + 12 mg/ml, proszek i rozpuszczalnik do sporządzania roztworu do stosowania na skórę
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zineryt 40 mg/ml + 12 mg/ml, proszek i rozpuszczalnik do sporządzania roztworu do stosowania na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zineryt 40 mg/ml + 12 mg/ml, proszek i rozpuszczalnik do sporządzania roztworu do stosowania na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelamed, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,5 mg azelastyny chlorowodorku. Każda
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelamed, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,5 mg azelastyny chlorowodorku. Każda
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO LORATADYNA GALENA, 10 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka zawiera 10 mg loratadyny (Loratadinum). Pełny wykaz
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO LORATADYNA GALENA, 10 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka zawiera 10 mg loratadyny (Loratadinum). Pełny wykaz
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Substancje pomocnicze o znanym działaniu: alkohol cetostearylowy, glikol propylenowy, kwas benzoesowy.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hascoderm, 200 mg/g, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 200 mg kwasu azelainowego (Acidum azelaicum). Substancje pomocnicze
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hascoderm, 200 mg/g, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 200 mg kwasu azelainowego (Acidum azelaicum). Substancje pomocnicze
4.4 Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO BATRAFEN, 10 mg/ml, płyn na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml płynu na skórę zawiera 10 mg cyklopiroksu z olaminą (Ciclopiroxi
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO BATRAFEN, 10 mg/ml, płyn na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml płynu na skórę zawiera 10 mg cyklopiroksu z olaminą (Ciclopiroxi
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. sodu glutaminian (E 621)
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Broncho-Vaxom dla dzieci, 3,5 mg, granulat do sporządzania zawiesiny doustnej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (saszetka) zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Broncho-Vaxom dla dzieci, 3,5 mg, granulat do sporządzania zawiesiny doustnej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (saszetka) zawiera:
Ulotka dołączona do opakowania: informacja dla pacjenta. Vidisic 2 mg/g, żel do oczu, Carbomerum
 Ulotka dołączona do opakowania: informacja dla pacjenta Vidisic 2 mg/g, żel do oczu, Carbomerum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne
Ulotka dołączona do opakowania: informacja dla pacjenta Vidisic 2 mg/g, żel do oczu, Carbomerum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Viru-POS, 30 mg/g, maść do oczu 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g maści zawiera 30 mg acyklowiru (Aciclovirum) Pełny wykaz substancji
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Viru-POS, 30 mg/g, maść do oczu 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g maści zawiera 30 mg acyklowiru (Aciclovirum) Pełny wykaz substancji
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
Pełny wykaz substancji pomocniczych, patrz punkt 6.1 Charakterystyki Produktu Leczniczego (ChPL).
 Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO XYLOMETAZOLIN WZF, 0,05%, 0,5 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,5 mg ksylometazoliny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO XYLOMETAZOLIN WZF, 0,05%, 0,5 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,5 mg ksylometazoliny
Tradycyjny produkt leczniczy roślinny przeznaczony do stosowania w określonych wskazaniach wynikających wyłącznie z jego długotrwałego stosowania.
 1. NAZWA PRODUKTU LECZNICZEGO Avioplant 250 mg kapsułki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera 250 mg sproszkowanego kłącza imbiru (Zingiber officinale Roscoe, rhizoma). Substancja pomocnicza
1. NAZWA PRODUKTU LECZNICZEGO Avioplant 250 mg kapsułki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera 250 mg sproszkowanego kłącza imbiru (Zingiber officinale Roscoe, rhizoma). Substancja pomocnicza
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CYCLONAMINE, 250 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka zawiera 250 mg etamsylatu (Etamsylatum). Substancja pomocnicza
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CYCLONAMINE, 250 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka zawiera 250 mg etamsylatu (Etamsylatum). Substancja pomocnicza
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. NAZWA PRODUKTU LECZNICZEGO Polyvaccinum mite, krople do nosa, zawiesina. Nieswoista szczepionka bakteryjna.. SKŁAD JAKOŚCIOWY I ILOŚCIOWY ml szczepionki zawiera inaktywowane
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. NAZWA PRODUKTU LECZNICZEGO Polyvaccinum mite, krople do nosa, zawiesina. Nieswoista szczepionka bakteryjna.. SKŁAD JAKOŚCIOWY I ILOŚCIOWY ml szczepionki zawiera inaktywowane
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Substancje pomocnicze o znanym działaniu: czerwień koszenilowa (E 124), metylu parahydroksybenzoesan, sód.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Flegamax, 50 mg/ml, roztwór doustny 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu doustnego zawiera 50 mg karbocysteiny (Carbocisteinum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Flegamax, 50 mg/ml, roztwór doustny 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu doustnego zawiera 50 mg karbocysteiny (Carbocisteinum).
Ulotka dołączona do opakowania: informacja dla pacjenta. CIPRONEX 0,3%, 3 mg/ml, krople do oczu, roztwór Ciprofloxacinum
 Ulotka dołączona do opakowania: informacja dla pacjenta CIPRONEX 0,3%, 3 mg/ml, krople do oczu, roztwór Ciprofloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta CIPRONEX 0,3%, 3 mg/ml, krople do oczu, roztwór Ciprofloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Catalin, 0,75 mg, tabletka i rozpuszczalnik do sporządzania kropli do oczu
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Catalin, 0,75 mg, tabletka i rozpuszczalnik do sporządzania kropli do oczu 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 tabletka zawiera 0,75 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Catalin, 0,75 mg, tabletka i rozpuszczalnik do sporządzania kropli do oczu 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 tabletka zawiera 0,75 mg
Ulotka dołączona do opakowania: informacja dla użytkownika. Ofloxamed, 3 mg/ml, krople do oczu, roztwór. Ofloxacinum
 Ulotka dołączona do opakowania: informacja dla użytkownika Ofloxamed, 3 mg/ml, krople do oczu, roztwór Ofloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika Ofloxamed, 3 mg/ml, krople do oczu, roztwór Ofloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NERVOMIX Forte, kapsułka twarda 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera: Substancje czynne: Valerianae radix 210 mg, Lupuli
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NERVOMIX Forte, kapsułka twarda 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera: Substancje czynne: Valerianae radix 210 mg, Lupuli
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ATUSSAN MITE 0,8 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml syropu zawiera 0,8 mg butamiratu cytrynianu. 5 ml syropu zawiera 4,0
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ATUSSAN MITE 0,8 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml syropu zawiera 0,8 mg butamiratu cytrynianu. 5 ml syropu zawiera 4,0
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Uro-Vaxom 6 mg, kapsułki, twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka twarda zawiera: liofilizat OM-89 w tym: liofilizowany lizat
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Uro-Vaxom 6 mg, kapsułki, twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka twarda zawiera: liofilizat OM-89 w tym: liofilizowany lizat
Ulotka dołączona do opakowania: informacja dla pacjenta. Floxamic Neo, 5 mg/ml, krople do oczu, roztwór Moxifloxacinum
 Ulotka dołączona do opakowania: informacja dla pacjenta Floxamic Neo, 5 mg/ml, krople do oczu, roztwór Moxifloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta Floxamic Neo, 5 mg/ml, krople do oczu, roztwór Moxifloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Hepa Merz 3000, 3 g/5 g, granulat do sporządzania roztworu doustnego
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hepa Merz 3000, 3 g/5 g, granulat do sporządzania roztworu doustnego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancja czynna: L-ornityny L-asparaginian
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hepa Merz 3000, 3 g/5 g, granulat do sporządzania roztworu doustnego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancja czynna: L-ornityny L-asparaginian
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastin COMOD, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05 % roztwór chlorowodorku azelastyny (0,50 mg/ml).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastin COMOD, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05 % roztwór chlorowodorku azelastyny (0,50 mg/ml).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum Plus (525 mg + 60 mg + 20 mg)/g, roztwór do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g roztworu do kąpieli zawiera 525 mg parafiny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum Plus (525 mg + 60 mg + 20 mg)/g, roztwór do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g roztworu do kąpieli zawiera 525 mg parafiny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. Azelastin POS, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastin POS, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05 % roztwór chlorowodorku azelastyny (0,50 mg/ml).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastin POS, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05 % roztwór chlorowodorku azelastyny (0,50 mg/ml).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Claritine, 1 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml syropu zawiera 1 mg Loratadinum (loratadyny). Substancje pomocnicze:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Claritine, 1 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml syropu zawiera 1 mg Loratadinum (loratadyny). Substancje pomocnicze:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zineryt 40 mg/ml + 12 mg/ml, proszek i rozpuszczalnik do sporządzania roztworu do stosowania na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zineryt 40 mg/ml + 12 mg/ml, proszek i rozpuszczalnik do sporządzania roztworu do stosowania na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Septofar Miód i Cytryna, 0,6 mg + 1,2 mg, pastylki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda pastylka twarda zawiera: Amylometakrezol
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Septofar Miód i Cytryna, 0,6 mg + 1,2 mg, pastylki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda pastylka twarda zawiera: Amylometakrezol
Ulotka dołączona do opakowania: informacja dla pacjenta. LORATADYNA GALENA, 10 mg, tabletki Loratadinum
 Ulotka dołączona do opakowania: informacja dla pacjenta LORATADYNA GALENA, 10 mg, tabletki Loratadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta LORATADYNA GALENA, 10 mg, tabletki Loratadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku (Oxymetazolini hydrochloridum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OXALIN 0,025%; 0,25 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OXALIN 0,025%; 0,25 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku
Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego
 C H A R A K T E R Y S T Y K A P R O D U K T U L E C Z N I C Z E G O 1. NAZWA PRODUKTU LECZNICZEGO Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1
C H A R A K T E R Y S T Y K A P R O D U K T U L E C Z N I C Z E G O 1. NAZWA PRODUKTU LECZNICZEGO Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ATROPINUM SULFURICUM WZF 1%, 10 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg Atropini sulfas
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ATROPINUM SULFURICUM WZF 1%, 10 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg Atropini sulfas
Ulotka dołączona do opakowania: informacja dla pacjenta. TROPICAMIDUM WZF 0,5%, 5 mg/ml, krople do oczu, roztwór Tropicamidum
 Ulotka dołączona do opakowania: informacja dla pacjenta TROPICAMIDUM WZF 0,5%, 5 mg/ml, krople do oczu, roztwór Tropicamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta TROPICAMIDUM WZF 0,5%, 5 mg/ml, krople do oczu, roztwór Tropicamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO LORATADYNA GALENA, 10 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka zawiera 10 mg loratadyny (Loratadinum). Pełny wykaz
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO LORATADYNA GALENA, 10 mg, tabletki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka zawiera 10 mg loratadyny (Loratadinum). Pełny wykaz
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1. NAZWA PRODUKTU LECZNICZEGO 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GLIMBAX 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,74 mg Diclofenacum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GLIMBAX 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,74 mg Diclofenacum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Każdy ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku (Oxymetazolini hydrochloridum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OXALIN 0,025%; 0,25 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OXALIN 0,025%; 0,25 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml kropli zawiera 0,5 mg chlorowodorku azelastyny (Azelastini
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml kropli zawiera 0,5 mg chlorowodorku azelastyny (Azelastini
Ulotka dla pacjenta: informacja dla użytkownika. NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 Ulotka dla pacjenta: informacja dla użytkownika NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dla pacjenta: informacja dla użytkownika NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta. Zaditen, 0,25 mg/ml, krople do oczu, roztwór. Ketotifenum
 Ulotka dołączona do opakowania: informacja dla pacjenta Zaditen, 0,25 mg/ml, krople do oczu, roztwór Ketotifenum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta Zaditen, 0,25 mg/ml, krople do oczu, roztwór Ketotifenum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynianu (Butamirati citras).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod, 5 mg/ml, krople doustne, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynianu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod, 5 mg/ml, krople doustne, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynianu
Liczba alergików rośnie z roku na rok. Na alergie cierpi prawie ¼ społeczeństwa. czyli 8,5 miliona Polaków!
 Liczba alergików rośnie z roku na rok. Na alergie cierpi prawie ¼ społeczeństwa czyli 8,5 miliona Polaków! Dlaczego tak się dzieje? Rośnie liczba dużych miast. Rośnie też ilość samochodów, bloków mieszkalnych,
Liczba alergików rośnie z roku na rok. Na alergie cierpi prawie ¼ społeczeństwa czyli 8,5 miliona Polaków! Dlaczego tak się dzieje? Rośnie liczba dużych miast. Rośnie też ilość samochodów, bloków mieszkalnych,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Claritine, 1 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml syropu zawiera 1 mg Loratadinum (loratadyny). Substancja pomocnicza
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Claritine, 1 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml syropu zawiera 1 mg Loratadinum (loratadyny). Substancja pomocnicza
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynian (Butamirati citras).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod, 5 mg/ml, krople doustne, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynian
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod, 5 mg/ml, krople doustne, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynian
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 0,15 mg polisulfonianu sodowego azapentacenu (Azapentaceni natrii polysulfonas).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO QUINAX, 0,15 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,15 mg polisulfonianu sodowego azapentacenu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO QUINAX, 0,15 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,15 mg polisulfonianu sodowego azapentacenu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Relestat 0,5 mg/ml, krople do oczu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml kropli do oczu zawiera 0,5 mg chlorowodorku epinastyny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Relestat 0,5 mg/ml, krople do oczu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml kropli do oczu zawiera 0,5 mg chlorowodorku epinastyny
