Spektroskopia Analiza rotacyjna widma cząsteczki N 2. Cel ćwiczenia: Wyznaczenie stałych rotacyjnych i odległości między atomami w cząsteczce N 2
|
|
|
- Aneta Urbańska
- 5 lat temu
- Przeglądów:
Transkrypt
1 Spektroskopia Analiza rotacyjna widma cząsteczki N 2 Cel ćwiczenia: Wyznaczenie stałych rotacyjnych i odległości między atomami w cząsteczce N 2 w stanach B 2 v=0 oraz X 2 v=0. System B 2 u - X 2 g cząsteczki N 2 leżący w zakresie nm jest najbardziej charakterystycznym systemem, spośród około dziesięciu systemów pasm tej cząsteczki. Energia jonizacji cząsteczki N 2 wynosi 15,58 ev, zaś energia potrzebna do wzbudzenia stanów oscylacyjnych stanu B 2 (v 0) musi być 3,2 ev. Dlatego w widmach tylko niektórych rodzajów plazm obserwuje się pasma systemu B-X wymagające całkowitej energii wzbudzenia rzędu ev. Najczęściej wzbudzane i obserwowane są pasma 1-0, 0-0, 1-1 oraz 0-1. Najbardziej intensywne pasmo tego systemu z charakterystyczną głowicą odpowiadające przejściu oscylacyjnemu 0-0, leży przy 391,4 nm i jest cieniowane w kierunku fioletu. Cząsteczka N 2 jest lekką molekułą i nawet przy niskiej rozdzielczości widma można zauważyć fragmenty struktury rotacyjnej tego pasma (linie rotacyjne). Stan elektronowy 2 Zgodnie z notacją spektroskopową zapis stanu elektronowego 2 oznacza, że mamy do czynienia z cząsteczką zawierającą jeden niesparowany elektron (spinowa liczba kwantowa S = ½, stąd multipletowość stanu elektronowego 2S 1 = 2) a rzut wypadkowego orbitalnego momentu pędu elektronów na oś cząsteczki wynosi zero (liczba kwantowa = 0). Różne przypadki sprzężeń między ruchem elektronów i ruchem rotacyjnym cząsteczek zostały opisane i zaklasyfikowane przez Hunda do jednej z pięciu przypadków (a - e). W stanie 2 wypadkowy moment orbitalnego momentu pędu i rotacji N = Λ R sprzęga się ze spinowym momentem pędu elektronów S tworząc wypadkowy moment pędu cząsteczki J = N S (przypadek b Hunda, rys. 1). Rys. 1.Sprzężenie wektorów momentów pędu w przypadku Hunda b.
2 Jeżeli S = ½, wówczas każdy poziom rotacyjny o N 1 rozszczepia się na dwa podpoziomy o J = N ½ oraz J = N ½, o energiach odpowiednio: J = N ½ F 1 (N) = BvN(N 1) ½ N DvN 2 (N1) 2... (1) J = N ½ F 2 (N) =BvN(N 1) ½ (N1) DvN 2 (N1) 2... (2) gdzie jest stałą rozszczepienia, Bv i Dv to stałe rotacyjne związane z poziomem oscylacyjnym o kwantowej liczbie oscylacji v. Stała rozszczepienia i stała D są znacznie mniejsze niż stała B. Wraz ze wzrostem liczby kwantowej N rozszczepienie poziomów wzrasta liniowo: F 1 (N) F 2 (N) = (N ½). (3) We wzorach (1-3) zastosowano oznaczenie termu rotacyjnego literą F. Przejście 2 2. Rozważmy strukturę widma związanego z przejściem pomiędzy różnymi poziomami rotacyjnymi przejścia wibronowego między dwoma stanami 2 (cząsteczka N 2 ). Zgodnie z ogólnymi regułami wyboru, dla liczby kwantowej J dozwolone są przejścia J = 0, 1, z wyjątkiem J = 0 J = 0. Możliwą zmianę liczby kwantowej N określają reguły wyboru dla przypadku Hunda (b): dozwolone są przejścia rotacyjne, dla których N = 1, z dodatkowym warunkiem: N = 0 jest wzbronione. Przy niezbyt dużej rozdzielczości widma emisyjnego nie obserwuje się opisanych wyżej efektów rozszczepienia poziomów rotacyjnych stanów 2 i wówczas J = N = 1. Widoczna jest wówczas struktura rotacyjna złożona z linii rotacyjnych, dla których J = 1 (gałąź P) i J = 1 (gałąź R). W widmie zarejestrowanym przy dużej rozdzielczości widoczna jest subtelna struktura rotacyjna pasma wibronowego wynikająca z rozszczepienia poziomów rotacyjnych. Na każde przejście N N 1 składają się trzy składowe podporządkowane regule J = 0, 1. Subtelna struktura rotacyjna składa się zatem z dubletu gałęzi P, dla której N = 1 i dubletu gałęzi R, dla której N = 1 oraz z dwóch gałęzi Q tzw. satelickich, związanych z J = 0. W analizowanym widmie cząsteczki N 2 intensywności linii gałęzi satelickich Q są znacznie mniejsze niż intensywności linii gałęzi P i R i praktycznie nie są obserwowane. Liczby falowe odpowiadające liniom gałęzi R i P oznacza się odpowiednio R 1 (N), R 2 (N) i P 1 (N), P 2 (N). Liczby kwantowe N odpowiadają rotacyjnym liczbom kwantowym niższego stanu wibronowego. Indeksy 1 i 2 oznaczają składowe dubletu odpowiednio o J = N ½ oraz J = N ½. Stosując ten zapis, liczby falowe 2
3 linii tworzących cztery główne gałęzie omawianej struktury rotacyjnej (dla stosunkowo niskich wartości N < 70) określają następujące równania: R 1 (N) = ~ 0 F 1 (N1) F 1 (N) = ~ 0 2B (N1) (B - B )N(N1) 4D (N1) 3 (D - D )N 2 (N1) 2 1/2( - )N (4) R 2 (N) = ~ 0 F 2 (N1) F 2 (N) = ~ 0 2B (N1) (B - B )N(N1) 4D (N1) 3 - (D - D )N 2 (N1) 2-1/2( - )N (5) P 1 (N) = ~ 0 F 1 (N 1) F 1 (N) = ~ 0 (B - B )N 2 - (B B )N 2(D D )N 3 - (D - D )N 4 1/2( - )N (6) P 2 (N) = ~ 0 F 2 (N 1) F 2 (N) = ~ 0 (B - B )N 2 - (B B )N 2(D D )N 3 - (D - D )N 4-1/2( - )N (7) gdzie ~ 0 to tzw. linia zerowa danego pasma wibronowego. Znaki prim i bis odnoszą się odpowiednio do wyższego i niższego stanu energetycznego. Linie rotacyjne danej gałęzi, związane z takimi samymi wartościami N, np. R 1 (N) i R 2 (N), leżą zwykle bardzo blisko siebie. W rezultacie, rozszczepienie linii rotacyjnych danej gałęzi jest widoczne dopiero przy dużej rozdzielczości aparatury rejestrującej widmo i dla wysokich wartości N, gdyż rozszczepienie linii wzrasta ze wzrostem liczby kwantowej N (analogicznie jak rozszczepienie termów). Głowicę pasma przy 391,43 nm tworzą linie gałęzi P 1 i P 2 (cieniowanie pasma w kierunku UV), przesuwające się początkowo od linii zerowej w kierunku fal dłuższych a następnie krótszych. Linie rotacyjne gałęzi R 1 oraz R 2 przesuwają się systematycznie od linii zerowej pasma w kierunku fal krótszych. Brak wyraźnej gałęzi Q wskazuje jednoznacznie, że przejście elektronowe jest typu -. Ciągi linii R i P zaczynają się rozszczepiać na dwie składowe R 1 i R 2 oraz P 1 i P 2 po przekroczeniu pewnych wartości N. Widmo N 2 zarejestrowane przy niskiej i wysokiej rozdzielczości przedstawiają rysunki 2 i 3. Przy wartości = 389,55 nm można zaobserwować w widmie głowicę pasma 1-1 oraz ciągi linii rotacyjnych R i P pochodzących od tego pasma, o znacznie niższej intensywności niż te związane z przejściem 0-0. Linie rotacyjne pasma 1-1 nie są rozszczepione na składowe ale dobrze mierzalne. Interferencje z liniami pasma 0-0 są bardzo nieliczne co pozwala na dokładny pomiar położenia linii pasma
4 100,00 90,00 80,00 70,00 60,00 50,00 Linie R i P pasm 0-0 i 1-1 Linie R i P pasma 0-0 Rys.2. Pasmo 0-0 i 1-1 systemu B 2 u - X 2 g cząsteczki N 2 40,00 30,00 20,00 10,00 Rys.1. Widmo elektronowo-oscylacyjno-rotacyjne pasm 0-0 i 1-1 systemu B 2 u - X 2 g 0, , , , , , , , ,00 Rys.1. Widmo elektronowo-oscylacyjno-rotacyjne pasm 0-0 i 1-1 systemu B 2 u - X 2 g 100,00 90,00 80,00 70,00 60,00 50,00 40,00 30,00 20,00 10,00 0, , , , , , , , , , , , Rys.2. Fragment struktury rotacyjnej pasm 0-0 i 1-1 systemu B 2 u - X 2 g zarejestrowany w warunkach wysokiej rozdzielczości widma R21 P48 R20 P47 Rys.3. Fragment rozdzielonej struktury rotacyjnej pasm 0-0 i 1-1 systemu B 2 u - X 2 g wraz z zaznaczeniem linii rotacyjnych gałęzi R(N) i P(N) Zależność między stałą rotacyjną B e i równowagową odległością miedzy atomami r e azotu w cząsteczce dimeru może być wykorzystana do obliczenia odległości między atomami w tej cząsteczce w stanach oscylacyjnych υ=0 obu stanów elektronowych zgodnie z równaniem : B 0 h (8) c r0 Korzystając z równań na liczby falowe linii gałęzi R 1 i R 2 oraz P 1 i P 2 można wyznaczyć rozszczepienie linii w gałęziach R i P a następnie wartość 0-0 : 12 (P) = P 1 (N) P 2 (N) = ( - ) N 1/2 ( ) (9) 12 (R) = R 1 (N) R 2 (N) = ( - ) N 1/2 (3 - ) (10) Standardowa niepewność pomiaru liczb falowych R i P, przy stosunkowo niskiej rozdzielczości, jest często rzędu wielkości stałych i co pozwala jedynie na ewentualne wyznaczenie różnicy ( - ). 4
5 Obliczenia wykonane przy wykorzystaniu sumy: 12 (P) 12 (R)] = ( - ) (2N 1) i z uwzględnieniem liczb falowych tylko tych linii rotacyjnych R i P, które były rozszczepione na składowe P 1 i P 2 oraz R 1 i R 2, pozwalają na oszacowanie różnicy ( - ). Dane literaturowe [2] podają stałą 0 oraz wartość różnicy 0-0 co oznacza że nawet dysponując wyższymi wartościami N trudno jest jednocześnie i bezpośrednio wyznaczyć wartości stałych 0 oraz 0. Wykonanie ćwiczenia Do analizy przygotowano zarejestrowane przy różnej rozdzielczości i w różnych temperaturach pasmo 0-0 systemu B-X cząsteczki N 2 w zakresie nm. W otrzymanym widmie należy zidentyfikować tylko główne ciągi linii rotacyjnych R 1, R 2, P 1 i P 2 (gałęzie satelickie nie pojawiają się lub są bardzo słabe w warunkach eksperymentu). Długości fali mierzone w powietrzu ( air ) należy przeliczyć na długości fali w próżni ( vac ) a te z kolei na liczby falowe w cm -1 ( vac = air ; dla air =380 nm =0,107 nm, dla air =390 nm =0,113 nm). Analizując widmo w pobliżu linii zerowej pasma oraz na podstawie rys. 3 należy zidentyfikować linie rotacyjne R(N) i P(N) przypisując im odpowiednie liczby kwantowe N. Weryfikację poprawnej identyfikacji należy przeprowadzić stosując odpowiednie kombinacje linii R(N) i P(N) (tzw. różnice międzygałęziowe R(N) P(N) oraz R(N-1) P(N1): Δ 2 F = F(N1) F(N) (11) Δ 2 F = R(N) P(N) = (4B - 6D )(N1/2) 8D (N1/2) 3 ± 1/2γ (11a) Δ 2 F = R(N-1) P(N1) = (4B - 6D )(N1/2) 8D (N1/2) 3 ± 1/2γ (11b) Stałe rotacyjne i ich odchylenia/niepewności standardowe należy obliczyć posługując się standardową metodą najmniejszych kwadratów i równaniami (4-7 oraz 11). Do wyznaczenia stałych w takich przypadkach z reguły stosuje się regresję liniową wielokrotną. Finalne obliczenia można wykonać korzystając ze standardowego oprogramowania arkusza kalkulacyjnego EXEL. W przypadku gdy rozszczepienie linii P i R jest niewielkie, widoczne dopiero przy najwyższych obserwowanych w doświadczeniu liczbach kwantowych N i niezbyt dobrze mierzalne (w warunkach przeprowadzonego eksperymentu), a przede wszystkim ze względu na bardzo silne wzajemne skorelowanie stałych rozszczepienia obu stanów, obliczenia 5
6 końcowe można wykonać z pominięciem stałych rozszczepienia 0 oraz 0. Gdy rozszczepienia są widoczne i dobrze mierzalne należy oszacować 0 oraz 0 oraz obliczyć wartość różnicy Δγ = 0-0. Obliczone wartości stałych 00, B, D, B, D oraz Δγ wraz ich standardowymi niepewnościami pomiaru należy przedstawić w tabeli. Należy również obliczyć, korzystając z zależności (8), odległość między atomami azotu w cząsteczce N 2 w stanach oscylacyjnych υ=0 obu kombinujących stanów elektronowych. Tabela 1. Przykładowa tabela z wynikami eksperymentalnymi : Stałe rotacyjne cząsteczki N 2 wyznaczone z pasma 0-0 systemu B-X [w cm -1 ] Stała stan X 2 stan B ,010,02 B 0 1,9226(4) 2,0748(4) D 0 x10 6 6,2(2) 5,9(2) r 0 [w nm] 0,1166 0, ,01 Sprawozdanie powinno zawierać: jedną (!) tabelę z liczbami falowymi zidentyfikowanych linii gałęzi R i P dla odpowiednich wartości N (patrz tabela 2), wykresy Δ 2 F i Δ 2 F w zależności od N1/2, dane do obliczenia ( - ), sposób wykonania obliczeń oraz tabelę z wynikami. W sprawozdaniu należy przedyskutować uzyskane wyniki oraz porównać uzyskane wartości z danymi literaturowymi. Przykładowe wyniki pomiarów (liczby falowe linii rotacyjnych i związane z nimi liczby kwantowe N stanu niższego) zestawiono w tabeli 2. Tabela 2. Wyznaczone liczby falowe ( w cm -1 ) linii rotacyjnych pasma 0-0 systemu B-X cząsteczki N 2 N R 1 (N) R 2 (N) P 1 (N) P 2 (N) , , , , , , , , , , , , , , , , , , , , , , , ,20 6
7 , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , ,43 Literatura cytowana: 1. Herzberg G., Molecular spectra and molecular structure. I. Spectra of diatomic molecules. D. van Nostrand Company, Inc. Princeton Hubert K.P., Herzberg G., Molecular Spectra and Molecular Structure. IV. Constants of diatomic molecules, D. van Nostrand, NJ, 1979 Materiał, którego znajomość obowiązuje przy realizacji ćwiczenia i będzie sprawdzany przed przystąpieniem do ćwiczenia: - struktura elektronowa cząsteczek dwuatomowych, energia cząsteczek dwuatomowych (elektronowa, oscylacyjna, rotacyjna) - klasyfikacja stanów elektronowych cząsteczek dwuatomowych, zapis termów - widmo elektronowe cząsteczek dwuatomowych (intensywność przejść, reguły wyboru, reguła Francka-Condona) - struktura rotacyjna pasm elektronowo-oscylacyjnych (gałęzie, cieniowanie, diagramy Fortrata. Literatura: 1. Chemia fizyczna. 2. Fizykochemia molekularna. Praca zbiorowa pod red. L. Komorowskiego i J. Lipińskiego, Wydawnictwo Naukowe PWN, Warszawa Sadlej J., Spektroskopia molekularna. WN-T, Warszawa 2002, rozdział Kołos W., Sadlej J., Atom i cząsteczka, WN-T Warszawa 2007, rozdział 4 (4.1, 4.6 i 4.7) 7
SPEKTROSKOPIA MOLEKULARNA 2015/16 nazwa przedmiotu SYLABUS A. Informacje ogólne
 SPEKTROSKOPIA MOLEKULARNA 2015/16 nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
SPEKTROSKOPIA MOLEKULARNA 2015/16 nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
ANALITYKA W KONTROLI JAKOŚCI
 ANALITYKA W KONTROLI JAKOŚCI ANALIZA ŚLADÓW METODA ICP-OES Optyczna spektroskopia emisyjna ze wzbudzeniem w indukcyjnie sprzężonej plazmie WYKŁAD 4 Rodzaje widm i mechanizm ich powstania PODSTAWY SPEKTROSKOPII
ANALITYKA W KONTROLI JAKOŚCI ANALIZA ŚLADÓW METODA ICP-OES Optyczna spektroskopia emisyjna ze wzbudzeniem w indukcyjnie sprzężonej plazmie WYKŁAD 4 Rodzaje widm i mechanizm ich powstania PODSTAWY SPEKTROSKOPII
Wyznaczanie temperatury gazu z wykorzystaniem widm emisyjnych molekuł dwuatomowych
 Wyznaczanie temperatury gazu z wykorzystaniem widm emisyjnych molekuł dwuatomowych Opracował: Hubert Lange Aby przygotować się do ćwiczenia należy przeczytać i zrozumieć materiał w książce:. adlej, pektroskopia
Wyznaczanie temperatury gazu z wykorzystaniem widm emisyjnych molekuł dwuatomowych Opracował: Hubert Lange Aby przygotować się do ćwiczenia należy przeczytać i zrozumieć materiał w książce:. adlej, pektroskopia
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego
 Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR
 Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR Szczególnym i bardzo charakterystycznym rodzajem oddziaływań międzycząsteczkowych jest wiązanie wodorowe. Powstaje ono między molekułami,
Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR Szczególnym i bardzo charakterystycznym rodzajem oddziaływań międzycząsteczkowych jest wiązanie wodorowe. Powstaje ono między molekułami,
Diagnostyka plazmy - spektroskopia molekularna. Ewa Pawelec wykład dla pracowni specjalistycznej
 Diagnostyka plazmy - spektroskopia molekularna Ewa Pawelec wykład dla pracowni specjalistycznej Plazma Różne rodzaje plazmy: http://www.ipp.cas.cz/mi/index.html http://www.pro-fusiononline.com/welding/plasma.htm
Diagnostyka plazmy - spektroskopia molekularna Ewa Pawelec wykład dla pracowni specjalistycznej Plazma Różne rodzaje plazmy: http://www.ipp.cas.cz/mi/index.html http://www.pro-fusiononline.com/welding/plasma.htm
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Zad Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji.
 Zad. 1.1. Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji. Zad. 1.1.a. Funkcja: ϕ = sin2x Zad. 1.1.b. Funkcja: ϕ = e x 2 2 Operator: f = d2 dx
Zad. 1.1. Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji. Zad. 1.1.a. Funkcja: ϕ = sin2x Zad. 1.1.b. Funkcja: ϕ = e x 2 2 Operator: f = d2 dx
II.6 Atomy w zewnętrznym polu magnetycznym
 II.6 Atomy w zewnętrznym polu magnetycznym 1. Kwantowanie przestrzenne w zewnętrznym polu magnetycznym. Model wektorowy raz jeszcze 2. Zjawisko Zeemana Normalne zjawisko Zeemana i jego wyjaśnienie w modelu
II.6 Atomy w zewnętrznym polu magnetycznym 1. Kwantowanie przestrzenne w zewnętrznym polu magnetycznym. Model wektorowy raz jeszcze 2. Zjawisko Zeemana Normalne zjawisko Zeemana i jego wyjaśnienie w modelu
SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE
 SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE Promieniowanie o długości fali 2-50 μm nazywamy promieniowaniem podczerwonym. Absorpcja lub emisja promieniowania z tego zakresu jest
SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE Promieniowanie o długości fali 2-50 μm nazywamy promieniowaniem podczerwonym. Absorpcja lub emisja promieniowania z tego zakresu jest
SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE
 1 SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE 2 Promieniowanie o długości fali 2-50 μm nazywamy promieniowaniem podczerwonym. Absorpcja lub emisja promieniowania z tego zakresu jest
1 SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE 2 Promieniowanie o długości fali 2-50 μm nazywamy promieniowaniem podczerwonym. Absorpcja lub emisja promieniowania z tego zakresu jest
Optyczna spektroskopia oscylacyjna. w badaniach powierzchni
 Optyczna spektroskopia oscylacyjna w badaniach powierzchni Zalety oscylacyjnej spektroskopii optycznej uŝycie fotonów jako cząsteczek wzbudzających i rejestrowanych nie wymaga uŝycia próŝni (moŝliwość
Optyczna spektroskopia oscylacyjna w badaniach powierzchni Zalety oscylacyjnej spektroskopii optycznej uŝycie fotonów jako cząsteczek wzbudzających i rejestrowanych nie wymaga uŝycia próŝni (moŝliwość
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków).
 Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
TEORIA PASMOWA CIAŁ STAŁYCH
 TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
Wyznaczanie energii dysocjacji molekuły jodu (I 2 )
 S1 Wyznaczanie energii dysocjacji molekuły jodu (I 2 ) 1 Cel ćwiczenia Bezpośrednim celem ćwiczenia jest wyznaczenie energii dysocjacji molekuły I 2. W trakcie przygotowywania doświadczenia oraz realizacji
S1 Wyznaczanie energii dysocjacji molekuły jodu (I 2 ) 1 Cel ćwiczenia Bezpośrednim celem ćwiczenia jest wyznaczenie energii dysocjacji molekuły I 2. W trakcie przygotowywania doświadczenia oraz realizacji
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Spektroskopia molekularna. Spektroskopia w podczerwieni
 Spektroskopia molekularna Ćwiczenie nr 4 Spektroskopia w podczerwieni Spektroskopia w podczerwieni (IR) jest spektroskopią absorpcyjną, która polega na pomiarach promieniowania elektromagnetycznego pochłanianego
Spektroskopia molekularna Ćwiczenie nr 4 Spektroskopia w podczerwieni Spektroskopia w podczerwieni (IR) jest spektroskopią absorpcyjną, która polega na pomiarach promieniowania elektromagnetycznego pochłanianego
Atom wodoru w mechanice kwantowej. Równanie Schrödingera
 Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
ZASADY ZALICZENIA PRZEDMIOTU MBS
 ZASADY ZALICZENIA PRZEDMIOTU MBS LABORATORIUM - MBS 1. ROZWIĄZYWANIE WIDM kolokwium NMR 25 kwietnia 2016 IR 30 maja 2016 złożone 13 czerwca 2016 wtorek 6.04 13.04 20.04 11.05 18.05 1.06 8.06 coll coll
ZASADY ZALICZENIA PRZEDMIOTU MBS LABORATORIUM - MBS 1. ROZWIĄZYWANIE WIDM kolokwium NMR 25 kwietnia 2016 IR 30 maja 2016 złożone 13 czerwca 2016 wtorek 6.04 13.04 20.04 11.05 18.05 1.06 8.06 coll coll
KARTA PRZEDMIOTU. wykazuje umiejętności nabyte w trakcie ćwiczeń. 75 godziny 30 uczestnictwo w zajęciach 30. nakład
 1 3 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 3 wiedza Symbole efektów kształcenia K_U01 3 umiejętności K_K01 11 kompetencje
1 3 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 3 wiedza Symbole efektów kształcenia K_U01 3 umiejętności K_K01 11 kompetencje
METODY SPEKTROSKOPOWE II. UV-VIS od teorii do praktyki Jakub Grynda Katedra Technologii Leków i Biochemii
 METODY SPEKTROSKOPOWE II UV-VIS od teorii do praktyki Jakub Grynda Katedra Technologii Leków i Biochemii Pokój nr 1 w Chemii B Godziny konsultacji: Poniedziałek 11-13 E-mail: jakub.grynda@gmail.com PLAN
METODY SPEKTROSKOPOWE II UV-VIS od teorii do praktyki Jakub Grynda Katedra Technologii Leków i Biochemii Pokój nr 1 w Chemii B Godziny konsultacji: Poniedziałek 11-13 E-mail: jakub.grynda@gmail.com PLAN
Atomy w zewnętrznym polu magnetycznym i elektrycznym
 Atomy w zewnętrznym polu magnetycznym i elektrycznym 1. Kwantowanie przestrzenne momentów magnetycznych i rezonans spinowy 2. Efekt Zeemana (normalny i anomalny) oraz zjawisko Paschena-Backa 3. Efekt Starka
Atomy w zewnętrznym polu magnetycznym i elektrycznym 1. Kwantowanie przestrzenne momentów magnetycznych i rezonans spinowy 2. Efekt Zeemana (normalny i anomalny) oraz zjawisko Paschena-Backa 3. Efekt Starka
Pomiar widm emisyjnych He, Na, Hg, Cd oraz Zn
 Ćwiczenie 33 Pomiar widm emisyjnych He, Na, Hg, Cd oraz Zn 33.1. Zasada ćwiczenia W ćwiczeniu mierzone są widma emisyjne atomów helu(he), sodu(na), rtęci (Hg), kadmu(cd) i cynku(zn). Pomiar widma helu
Ćwiczenie 33 Pomiar widm emisyjnych He, Na, Hg, Cd oraz Zn 33.1. Zasada ćwiczenia W ćwiczeniu mierzone są widma emisyjne atomów helu(he), sodu(na), rtęci (Hg), kadmu(cd) i cynku(zn). Pomiar widma helu
Temat: Promieniowanie atomu wodoru (teoria)
 Temat: Promieniowanie atomu wodoru (teoria) Zgodnie z drugim postulatem Bohra elektron poruszając się po dozwolonej orbicie nie wypromieniowuje energii. Promieniowanie zostaje wyemitowane, gdy elektron
Temat: Promieniowanie atomu wodoru (teoria) Zgodnie z drugim postulatem Bohra elektron poruszając się po dozwolonej orbicie nie wypromieniowuje energii. Promieniowanie zostaje wyemitowane, gdy elektron
Liczby kwantowe elektronu w atomie wodoru
 Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR
 Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR 1. Wstęp Związki karbonylowe zawierające w położeniu co najmniej jeden atom wodoru mogą ulegać enolizacji przez przesunięcie protonu
Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR 1. Wstęp Związki karbonylowe zawierające w położeniu co najmniej jeden atom wodoru mogą ulegać enolizacji przez przesunięcie protonu
Spektroskopia. Spotkanie pierwsze. Prowadzący: Dr Barbara Gil
 Spektroskopia Spotkanie pierwsze Prowadzący: Dr Barbara Gil Temat rozwaŝań Spektroskopia nauka o powstawaniu i interpretacji widm powstających w wyniku oddziaływań wszelkich rodzajów promieniowania na
Spektroskopia Spotkanie pierwsze Prowadzący: Dr Barbara Gil Temat rozwaŝań Spektroskopia nauka o powstawaniu i interpretacji widm powstających w wyniku oddziaływań wszelkich rodzajów promieniowania na
Przejścia promieniste
 Przejście promieniste proces rekombinacji elektronu i dziury (przejście ze stanu o większej energii do stanu o energii mniejszej), w wyniku którego następuje emisja promieniowania. E Długość wyemitowanej
Przejście promieniste proces rekombinacji elektronu i dziury (przejście ze stanu o większej energii do stanu o energii mniejszej), w wyniku którego następuje emisja promieniowania. E Długość wyemitowanej
0900 FS2 2 FAC. Fizyka atomu i cząsteczki FT 8. WYDZIAŁ FIZYKI UwB KOD USOS: Karta przedmiotu. Przedmiot moduł ECTS. kierunek studiów: FIZYKA 2 st.
 WYDZIAŁ FIZYKI UwB KOD USOS: 0900 FS2 2 FAC Karta przedmiotu Przedmiot moduł ECTS Fizyka atomu i cząsteczki FT 8 kierunek studiów: FIZYKA 2 st. specjalność: FIZYKA TEORETYCZNA Formy zajęć wykład konwersatorium
WYDZIAŁ FIZYKI UwB KOD USOS: 0900 FS2 2 FAC Karta przedmiotu Przedmiot moduł ECTS Fizyka atomu i cząsteczki FT 8 kierunek studiów: FIZYKA 2 st. specjalność: FIZYKA TEORETYCZNA Formy zajęć wykład konwersatorium
Spis treści. Przedmowa redaktora do wydania czwartego 11
 Mechanika kwantowa : teoria nierelatywistyczna / Lew D. Landau, Jewgienij M. Lifszyc ; z jęz. ros. tł. Ludwik Dobrzyński, Andrzej Pindor. - Wyd. 3. Warszawa, 2012 Spis treści Przedmowa redaktora do wydania
Mechanika kwantowa : teoria nierelatywistyczna / Lew D. Landau, Jewgienij M. Lifszyc ; z jęz. ros. tł. Ludwik Dobrzyński, Andrzej Pindor. - Wyd. 3. Warszawa, 2012 Spis treści Przedmowa redaktora do wydania
III.1 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy
 III.1 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy r. akad. 2004/2005 1. Atom helu: struktura poziomów, reguły wyboru, 2. Zakaz Pauliego, 3. Moment pędu w atomach wieloelektronowych:
III.1 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy r. akad. 2004/2005 1. Atom helu: struktura poziomów, reguły wyboru, 2. Zakaz Pauliego, 3. Moment pędu w atomach wieloelektronowych:
II.1 Serie widmowe wodoru
 II.1 Serie widmowe wodoru Jan Królikowski Fizyka IVBC 1 II.1 Serie widmowe wodoru W obszarze widzialnym wystepują 3 silne linie wodoru: H α (656.3 nm), H β (486.1 nm) i H γ (434.0 nm) oraz szereg linii
II.1 Serie widmowe wodoru Jan Królikowski Fizyka IVBC 1 II.1 Serie widmowe wodoru W obszarze widzialnym wystepują 3 silne linie wodoru: H α (656.3 nm), H β (486.1 nm) i H γ (434.0 nm) oraz szereg linii
Stara i nowa teoria kwantowa
 Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE.
 1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
Badanie dynamiki rekombinacji ekscytonów w zawiesinach półprzewodnikowych kropek kwantowych PbS
 Badanie dynamiki rekombinacji ekscytonów w zawiesinach półprzewodnikowych kropek kwantowych PbS 1. Absorpcja i emisja światła w układzie dwupoziomowym. Absorpcję światła można opisać jako proces, w którym
Badanie dynamiki rekombinacji ekscytonów w zawiesinach półprzewodnikowych kropek kwantowych PbS 1. Absorpcja i emisja światła w układzie dwupoziomowym. Absorpcję światła można opisać jako proces, w którym
ĆWICZENIE 3 REZONANS AKUSTYCZNY
 ĆWICZENIE 3 REZONANS AKUSTYCZNY W trakcie doświadczenia przeprowadzono sześć pomiarów rezonansu akustycznego: dla dwóch różnych gazów (powietrza i CO), pięć pomiarów dla powietrza oraz jeden pomiar dla
ĆWICZENIE 3 REZONANS AKUSTYCZNY W trakcie doświadczenia przeprowadzono sześć pomiarów rezonansu akustycznego: dla dwóch różnych gazów (powietrza i CO), pięć pomiarów dla powietrza oraz jeden pomiar dla
Spektroskopowe metody identyfikacji związków organicznych
 Spektroskopowe metody identyfikacji związków organicznych Wstęp Spektroskopia jest metodą analityczną zajmującą się analizą widm powstających w wyniku oddziaływania promieniowania elektromagnetycznego
Spektroskopowe metody identyfikacji związków organicznych Wstęp Spektroskopia jest metodą analityczną zajmującą się analizą widm powstających w wyniku oddziaływania promieniowania elektromagnetycznego
Wyznaczanie zależności współczynnika załamania światła od długości fali światła
 Ćwiczenie O3 Wyznaczanie zależności współczynnika załamania światła od długości fali światła O3.1. Cel ćwiczenia Celem ćwiczenia jest zbadanie zależności współczynnika załamania światła od długości fali
Ćwiczenie O3 Wyznaczanie zależności współczynnika załamania światła od długości fali światła O3.1. Cel ćwiczenia Celem ćwiczenia jest zbadanie zależności współczynnika załamania światła od długości fali
Wykład 6 Spektroskopia oscylacyjna. Model oscylatora harmonicznego i anharmonicznego cząsteczki dwuatomowej
 Wykład 6 Spektroskopia oscylacyjna Model oscylatora armonicznego i anarmonicznego cząsteczki dwuatomowej W6. Spektroskopia oscylacyjna Widmo oscylacyjne cząsteczki CO w azie gazowej O czym nas inormuje
Wykład 6 Spektroskopia oscylacyjna Model oscylatora armonicznego i anarmonicznego cząsteczki dwuatomowej W6. Spektroskopia oscylacyjna Widmo oscylacyjne cząsteczki CO w azie gazowej O czym nas inormuje
Fizyka 3.3 WYKŁAD II
 Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 4 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2013/14
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 4 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2013/14
WFiIS. Wstęp teoretyczny:
 WFiIS PRACOWNIA FIZYCZNA I i II Imię i nazwisko: 1. 2. TEMAT: ROK GRUPA ZESPÓŁ NR ĆWICZENIA Data wykonania: Data oddania: Zwrot do poprawy: Data oddania: Data zliczenia: OCENA Cel ćwiczenia: Wyznaczenie
WFiIS PRACOWNIA FIZYCZNA I i II Imię i nazwisko: 1. 2. TEMAT: ROK GRUPA ZESPÓŁ NR ĆWICZENIA Data wykonania: Data oddania: Zwrot do poprawy: Data oddania: Data zliczenia: OCENA Cel ćwiczenia: Wyznaczenie
II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym
 II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym Jan Królikowski Fizyka IVBC 1 II.4.1 Ogólne własności wektora kwantowego momentu pędu Podane poniżej własności kwantowych wektorów
II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym Jan Królikowski Fizyka IVBC 1 II.4.1 Ogólne własności wektora kwantowego momentu pędu Podane poniżej własności kwantowych wektorów
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Metody analizy pierwiastków z zastosowaniem wtórnego promieniowania rentgenowskiego. XRF, SRIXE, PIXE, SEM (EPMA)
 Metody analizy pierwiastków z zastosowaniem wtórnego promieniowania rentgenowskiego. XRF, SRIXE, PIXE, SEM (EPMA) Promieniowaniem X nazywa się promieniowanie elektromagnetyczne o długości fali od około
Metody analizy pierwiastków z zastosowaniem wtórnego promieniowania rentgenowskiego. XRF, SRIXE, PIXE, SEM (EPMA) Promieniowaniem X nazywa się promieniowanie elektromagnetyczne o długości fali od około
Stany atomu wieloelektronowego o określonej energii. być przypisywane elektrony w tym stanie atomu.
 Notatki do wyk ladu VI Stany atomu wieloelektronowego o określonej energii. Konfiguracja elektronowa atomu - zbiór spinorbitali, wykorzystywanych do konstrukcji funkcji falowej dla danego stanu atomu;
Notatki do wyk ladu VI Stany atomu wieloelektronowego o określonej energii. Konfiguracja elektronowa atomu - zbiór spinorbitali, wykorzystywanych do konstrukcji funkcji falowej dla danego stanu atomu;
Spektroskopia charakterystycznych strat energii elektronów EELS (Electron Energy-Loss Spectroscopy)
 Spektroskopia charakterystycznych strat energii elektronów EELS (Electron Energy-Loss Spectroscopy) Oddziaływanie elektronów ze stałą, krystaliczną próbką wstecznie rozproszone elektrony elektrony pierwotne
Spektroskopia charakterystycznych strat energii elektronów EELS (Electron Energy-Loss Spectroscopy) Oddziaływanie elektronów ze stałą, krystaliczną próbką wstecznie rozproszone elektrony elektrony pierwotne
PRACOWNIA PODSTAW SPEKTROSKOPII MOLEKULARNEJ
 PRACOWNIA PODSTAW SPEKTROSKOPII MOLEKULARNEJ Kierowniczka pracowni: dr hab. Magdalena Pecul-Kudelska, (pok. 417), e-mail mpecul@chem.uw.edu.pl, tel 0228220211 wew 501; Spis ćwiczeń i osoby prowadzące 1.
PRACOWNIA PODSTAW SPEKTROSKOPII MOLEKULARNEJ Kierowniczka pracowni: dr hab. Magdalena Pecul-Kudelska, (pok. 417), e-mail mpecul@chem.uw.edu.pl, tel 0228220211 wew 501; Spis ćwiczeń i osoby prowadzące 1.
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
WYKŁAD 5 Zastosowanie teorii grup w analizie widm oscylacyjnych
 WYKŁAD 5 Zastosowanie teorii grup w analizie widm oscylacyjnych Prof. dr hab. Halina Abramczyk Dr inż. Beata Brożek-Płuska POLITECHNIKA ŁÓDZKA Wydział Chemiczny, Instytut Techniki Radiacyjnej Laboratorium
WYKŁAD 5 Zastosowanie teorii grup w analizie widm oscylacyjnych Prof. dr hab. Halina Abramczyk Dr inż. Beata Brożek-Płuska POLITECHNIKA ŁÓDZKA Wydział Chemiczny, Instytut Techniki Radiacyjnej Laboratorium
OGÓLNE PODSTAWY SPEKTROSKOPII
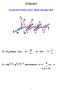 WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
Pasmowa teoria przewodnictwa. Anna Pietnoczka
 Pasmowa teoria przewodnictwa elektrycznego Anna Pietnoczka Wpływ rodzaju wiązań na przewodność próbki: Wiązanie jonowe - izolatory Wiązanie metaliczne - przewodniki Wiązanie kowalencyjne - półprzewodniki
Pasmowa teoria przewodnictwa elektrycznego Anna Pietnoczka Wpływ rodzaju wiązań na przewodność próbki: Wiązanie jonowe - izolatory Wiązanie metaliczne - przewodniki Wiązanie kowalencyjne - półprzewodniki
ĆWICZENIE 1 WYZNACZANIE DŁUGOŚCI FALI ZA POMOCĄ SPEKTROSKOPU
 ĆWICZENIE WYZNACZANIE DŁUGOŚCI FALI ZA POMOCĄ SPEKTROSKOPU Jeżeli gazy zaczynają świecić, na przykład w wyniku podgrzania, to możemy zaobserwować charakterystyczne kolorowe prążki podczas obserwacji tzw.
ĆWICZENIE WYZNACZANIE DŁUGOŚCI FALI ZA POMOCĄ SPEKTROSKOPU Jeżeli gazy zaczynają świecić, na przykład w wyniku podgrzania, to możemy zaobserwować charakterystyczne kolorowe prążki podczas obserwacji tzw.
Jan Drzymała ANALIZA INSTRUMENTALNA SPEKTROSKOPIA W ŚWIETLE WIDZIALNYM I PODCZERWONYM
 Jan Drzymała ANALIZA INSTRUMENTALNA SPEKTROSKOPIA W ŚWIETLE WIDZIALNYM I PODCZERWONYM Światło słoneczne jest mieszaniną fal o różnej długości i różnego natężenia. Tylko część promieniowania elektromagnetycznego
Jan Drzymała ANALIZA INSTRUMENTALNA SPEKTROSKOPIA W ŚWIETLE WIDZIALNYM I PODCZERWONYM Światło słoneczne jest mieszaniną fal o różnej długości i różnego natężenia. Tylko część promieniowania elektromagnetycznego
Badanie widma fali akustycznej
 Politechnika Łódzka FTIMS Kierunek: Informatyka rok akademicki: 00/009 sem.. grupa II Termin: 10 III 009 Nr. ćwiczenia: 1 Temat ćwiczenia: Badanie widma fali akustycznej Nr. studenta: 6 Nr. albumu: 15101
Politechnika Łódzka FTIMS Kierunek: Informatyka rok akademicki: 00/009 sem.. grupa II Termin: 10 III 009 Nr. ćwiczenia: 1 Temat ćwiczenia: Badanie widma fali akustycznej Nr. studenta: 6 Nr. albumu: 15101
Kulka krąży wokół jądra po orbicie, o ustalonych parametrach, które mogą się zmieniać tylko skokowo, kiedy elektron przeskakuje na inną orbitę.
 Widmo elektronowe Elektrony w molekule poruszają się wokół jąder, mają więc pewną energię kinetyczną. Ponieważ znajdują się one w polu sil elektrostatycznych przyciągania przez jądra i odpychania przez
Widmo elektronowe Elektrony w molekule poruszają się wokół jąder, mają więc pewną energię kinetyczną. Ponieważ znajdują się one w polu sil elektrostatycznych przyciągania przez jądra i odpychania przez
Atom wodoru. Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu:
 ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
Efekt fotoelektryczny
 Ćwiczenie 82 Efekt fotoelektryczny Cel ćwiczenia Celem ćwiczenia jest obserwacja efektu fotoelektrycznego: wybijania elektronów z metalu przez światło o różnej częstości (barwie). Pomiar energii kinetycznej
Ćwiczenie 82 Efekt fotoelektryczny Cel ćwiczenia Celem ćwiczenia jest obserwacja efektu fotoelektrycznego: wybijania elektronów z metalu przez światło o różnej częstości (barwie). Pomiar energii kinetycznej
POMIAR PRĘDKOŚCI DŹWIĘKU METODĄ REZONANSU I METODĄ SKŁADANIA DRGAŃ WZAJEMNIE PROSTOPADŁYCH
 Ćwiczenie 5 POMIR PRĘDKOŚCI DŹWIĘKU METODĄ REZONNSU I METODĄ SKŁDNI DRGŃ WZJEMNIE PROSTOPDŁYCH 5.. Wiadomości ogólne 5... Pomiar prędkości dźwięku metodą rezonansu Wyznaczanie prędkości dźwięku metodą
Ćwiczenie 5 POMIR PRĘDKOŚCI DŹWIĘKU METODĄ REZONNSU I METODĄ SKŁDNI DRGŃ WZJEMNIE PROSTOPDŁYCH 5.. Wiadomości ogólne 5... Pomiar prędkości dźwięku metodą rezonansu Wyznaczanie prędkości dźwięku metodą
WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab.
 WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab. Halina Abramczyk POLITECHNIKA ŁÓDZKA Wydział Chemiczny
WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab. Halina Abramczyk POLITECHNIKA ŁÓDZKA Wydział Chemiczny
PRACOWNIA PODSTAW BIOFIZYKI
 PRACOWNIA PODSTAW BIOFIZYKI Ćwiczenia laboratoryjne dla studentów III roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Badanie wygaszania fluorescencji SPQ przez jony chloru
PRACOWNIA PODSTAW BIOFIZYKI Ćwiczenia laboratoryjne dla studentów III roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Badanie wygaszania fluorescencji SPQ przez jony chloru
PRACOWNIA CHEMII. Wygaszanie fluorescencji (Fiz4)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
Widmo sodu, serie. p główna s- ostra d rozmyta f -podstawowa
 Widmo sodu, serie p główna s- ostra d rozmyta f -podstawowa Przejścia dozwolone w Na Reguły wyboru: l =± 1 Diagram Grotriana dla sodu, z lewej strony poziomy energetyczne wodoru; należy zwrócić uwagę,
Widmo sodu, serie p główna s- ostra d rozmyta f -podstawowa Przejścia dozwolone w Na Reguły wyboru: l =± 1 Diagram Grotriana dla sodu, z lewej strony poziomy energetyczne wodoru; należy zwrócić uwagę,
Podczerwień bliska: cm -1 (0,7-2,5 µm) Podczerwień właściwa: cm -1 (2,5-14,3 µm) Podczerwień daleka: cm -1 (14,3-50 µm)
 SPEKTROSKOPIA W PODCZERWIENI Podczerwień bliska: 14300-4000 cm -1 (0,7-2,5 µm) Podczerwień właściwa: 4000-700 cm -1 (2,5-14,3 µm) Podczerwień daleka: 700-200 cm -1 (14,3-50 µm) WIELKOŚCI CHARAKTERYZUJĄCE
SPEKTROSKOPIA W PODCZERWIENI Podczerwień bliska: 14300-4000 cm -1 (0,7-2,5 µm) Podczerwień właściwa: 4000-700 cm -1 (2,5-14,3 µm) Podczerwień daleka: 700-200 cm -1 (14,3-50 µm) WIELKOŚCI CHARAKTERYZUJĄCE
Estymacja wektora stanu w prostym układzie elektroenergetycznym
 Zakład Sieci i Systemów Elektroenergetycznych LABORATORIUM INFORMATYCZNE SYSTEMY WSPOMAGANIA DYSPOZYTORÓW Estymacja wektora stanu w prostym układzie elektroenergetycznym Autorzy: dr inż. Zbigniew Zdun
Zakład Sieci i Systemów Elektroenergetycznych LABORATORIUM INFORMATYCZNE SYSTEMY WSPOMAGANIA DYSPOZYTORÓW Estymacja wektora stanu w prostym układzie elektroenergetycznym Autorzy: dr inż. Zbigniew Zdun
Struktura elektronowa czasteczek. przybliżenie Borna-Oppenheimera. równania Schrödingera dla elektronów przy ustalonym po lożeniu jader
 Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR
 PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR WSTĘP Metody spektroskopowe Spektroskopia bada i teoretycznie wyjaśnia oddziaływania pomiędzy materią będącą zbiorowiskiem
PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR WSTĘP Metody spektroskopowe Spektroskopia bada i teoretycznie wyjaśnia oddziaływania pomiędzy materią będącą zbiorowiskiem
ĆWICZENIE 3 LUMINOFORY ORGANICZNE I NIEORGANICZNE.
 Laboratorium specjalizacyjne A ĆWICZENIE 3 LUMINOFORY ORGANICZNE I NIEORGANICZNE. Zagadnienia: Podział luminoforów: fluorofory oraz fosfory Luminofory organiczne i nieorganiczne Różnorodność stanów wzbudzonych
Laboratorium specjalizacyjne A ĆWICZENIE 3 LUMINOFORY ORGANICZNE I NIEORGANICZNE. Zagadnienia: Podział luminoforów: fluorofory oraz fosfory Luminofory organiczne i nieorganiczne Różnorodność stanów wzbudzonych
Ćwiczenie M-2 Pomiar przyśpieszenia ziemskiego za pomocą wahadła rewersyjnego Cel ćwiczenia: II. Przyrządy: III. Literatura: IV. Wstęp. l Rys.
 Ćwiczenie M- Pomiar przyśpieszenia ziemskiego za pomocą wahadła rewersyjnego. Cel ćwiczenia: pomiar przyśpieszenia ziemskiego przy pomocy wahadła fizycznego.. Przyrządy: wahadło rewersyjne, elektroniczny
Ćwiczenie M- Pomiar przyśpieszenia ziemskiego za pomocą wahadła rewersyjnego. Cel ćwiczenia: pomiar przyśpieszenia ziemskiego przy pomocy wahadła fizycznego.. Przyrządy: wahadło rewersyjne, elektroniczny
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Ćwiczenie 1. Zagadnienia: spektroskopia absorpcyjna, prawa absorpcji, budowa i działanie. Wstęp. Część teoretyczna.
 Ćwiczenie 1 Metodyka poprawnych i dokładnych pomiarów absorbancji, wyznaczenie małych wartości absorbancji. Czynniki wpływające na mierzone widma absorpcji i wartości absorbancji dla wybranych długości
Ćwiczenie 1 Metodyka poprawnych i dokładnych pomiarów absorbancji, wyznaczenie małych wartości absorbancji. Czynniki wpływające na mierzone widma absorpcji i wartości absorbancji dla wybranych długości
Jak analizować widmo IR?
 Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
EFEKT SOLWATOCHROMOWY. WYZNACZANIE MOMENTU DIPOLOWEGO CZĄSTECZKI W STANIE WZBUDZONYM METODĄ SOLWATOCHROMOWĄ
 Ćwiczenie EFEKT SOLWATOCHROMOWY. WYZNACZANIE MOMENTU DIPOLOWEGO CZĄSTECZKI W STANIE WZBUDZONYM METODĄ SOLWATOCHROMOWĄ Zagadnienia: typy przejść elektronowych, orbitale atomowe (s, p, d) i molekularne (σ,
Ćwiczenie EFEKT SOLWATOCHROMOWY. WYZNACZANIE MOMENTU DIPOLOWEGO CZĄSTECZKI W STANIE WZBUDZONYM METODĄ SOLWATOCHROMOWĄ Zagadnienia: typy przejść elektronowych, orbitale atomowe (s, p, d) i molekularne (σ,
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Skręcenie wektora polaryzacji w ośrodku optycznie czynnym
 WFiIS PRACOWNIA FIZYCZNA I i II Imię i nazwisko: 1.. TEMAT: ROK GRUPA ZESPÓŁ NR ĆWICZENIA ata wykonania: ata oddania: Zwrot do poprawy: ata oddania: ata zliczenia: OCENA Cel ćwiczenia: Celem ćwiczenia
WFiIS PRACOWNIA FIZYCZNA I i II Imię i nazwisko: 1.. TEMAT: ROK GRUPA ZESPÓŁ NR ĆWICZENIA ata wykonania: ata oddania: Zwrot do poprawy: ata oddania: ata zliczenia: OCENA Cel ćwiczenia: Celem ćwiczenia
2. Metody, których podstawą są widma atomowe 32
 Spis treści 5 Spis treści Przedmowa do wydania czwartego 11 Przedmowa do wydania trzeciego 13 1. Wiadomości ogólne z metod spektroskopowych 15 1.1. Podstawowe wielkości metod spektroskopowych 15 1.2. Rola
Spis treści 5 Spis treści Przedmowa do wydania czwartego 11 Przedmowa do wydania trzeciego 13 1. Wiadomości ogólne z metod spektroskopowych 15 1.1. Podstawowe wielkości metod spektroskopowych 15 1.2. Rola
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Pracownia Fizyczna ćwiczenie PF-10: Badanie widm emisyjnych za pomocą spektroskopu pryzmatycznego
 Pracownia Fizyczna ćwiczenie PF-10: Badanie widm emisyjnych za pomocą spektroskopu pryzmatycznego Instytut Fizyki im. Mariana Smoluchowskiego Uniwersytet Jagielloński 1 Cel ćwiczenia Celem ćwiczenia jest
Pracownia Fizyczna ćwiczenie PF-10: Badanie widm emisyjnych za pomocą spektroskopu pryzmatycznego Instytut Fizyki im. Mariana Smoluchowskiego Uniwersytet Jagielloński 1 Cel ćwiczenia Celem ćwiczenia jest
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
O 2 O 1. Temat: Wyznaczenie przyspieszenia ziemskiego za pomocą wahadła rewersyjnego
 msg M 7-1 - Temat: Wyznaczenie przyspieszenia ziemskiego za pomocą wahadła rewersyjnego Zagadnienia: prawa dynamiki Newtona, moment sił, moment bezwładności, dynamiczne równania ruchu wahadła fizycznego,
msg M 7-1 - Temat: Wyznaczenie przyspieszenia ziemskiego za pomocą wahadła rewersyjnego Zagadnienia: prawa dynamiki Newtona, moment sił, moment bezwładności, dynamiczne równania ruchu wahadła fizycznego,
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Rozkład normalny, niepewność standardowa typu A
 Podstawy Metrologii i Technik Eksperymentu Laboratorium Rozkład normalny, niepewność standardowa typu A Instrukcja do ćwiczenia nr 1 Zakład Miernictwa i Ochrony Atmosfery Wrocław, listopad 2010 r. Podstawy
Podstawy Metrologii i Technik Eksperymentu Laboratorium Rozkład normalny, niepewność standardowa typu A Instrukcja do ćwiczenia nr 1 Zakład Miernictwa i Ochrony Atmosfery Wrocław, listopad 2010 r. Podstawy
Monochromatyzacja promieniowania molibdenowej lampy rentgenowskiej
 Uniwersytet Śląski Instytut Chemii Zakładu Krystalografii ul. Bankowa 14, pok. 133, 40 006 Katowice tel. (032)359 1503, e-mail: izajen@wp.pl, opracowanie: dr Izabela Jendrzejewska Laboratorium z Krystalografii
Uniwersytet Śląski Instytut Chemii Zakładu Krystalografii ul. Bankowa 14, pok. 133, 40 006 Katowice tel. (032)359 1503, e-mail: izajen@wp.pl, opracowanie: dr Izabela Jendrzejewska Laboratorium z Krystalografii
SPEKTROSKOPIA ROTACYJNA
 SPEKTROSKOPIA ROTACYJNA Co to jest spektroskopia mikrofalowa Obejmuje obszar częstości od 3GHz do 300GHz czyli od 0.1 do 10 cm -1 Wykrywa przejścia pomiędzy skwantowanymi poziomami energetycznymi obracającej
SPEKTROSKOPIA ROTACYJNA Co to jest spektroskopia mikrofalowa Obejmuje obszar częstości od 3GHz do 300GHz czyli od 0.1 do 10 cm -1 Wykrywa przejścia pomiędzy skwantowanymi poziomami energetycznymi obracającej
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Kwantowe własności promieniowania, ciało doskonale czarne, zjawisko fotoelektryczne zewnętrzne.
 Kwantowe własności promieniowania, ciało doskonale czarne, zjawisko fotoelektryczne zewnętrzne. DUALIZM ŚWIATŁA fala interferencja, dyfrakcja, polaryzacja,... kwant, foton promieniowanie ciała doskonale
Kwantowe własności promieniowania, ciało doskonale czarne, zjawisko fotoelektryczne zewnętrzne. DUALIZM ŚWIATŁA fala interferencja, dyfrakcja, polaryzacja,... kwant, foton promieniowanie ciała doskonale
Transport elektronów w biomolekułach
 Transport elektronów w biomolekułach Równanie Arrheniusa, energia aktywacji Większość reakcji chemicznych zachodzi ze stałą szybkości (k) zaleŝną od temperatury (T) i energii aktywacji ( G*) tej reakcji,
Transport elektronów w biomolekułach Równanie Arrheniusa, energia aktywacji Większość reakcji chemicznych zachodzi ze stałą szybkości (k) zaleŝną od temperatury (T) i energii aktywacji ( G*) tej reakcji,
Pracownia fizyczna dla szkół
 Imię i Nazwisko Widma świecenia pierwiastków opracowanie: Zofia Piłat Cel doświadczenia Celem doświadczenia jest zaobserwowanie widm świecących gazów atomowych i zidentyfikowanie do jakich pierwiastków
Imię i Nazwisko Widma świecenia pierwiastków opracowanie: Zofia Piłat Cel doświadczenia Celem doświadczenia jest zaobserwowanie widm świecących gazów atomowych i zidentyfikowanie do jakich pierwiastków
SF5. Spektroskopia absorpcyjna i emisyjna cząsteczek organicznych
 SF5 Spektroskopia absorpcyjna i emisyjna cząsteczek organicznych Każda cząsteczka ma charakterystyczny dla siebie układ poziomów energetycznych elektronowych, oscylacyjnych i rotacyjnych, przy czym tych
SF5 Spektroskopia absorpcyjna i emisyjna cząsteczek organicznych Każda cząsteczka ma charakterystyczny dla siebie układ poziomów energetycznych elektronowych, oscylacyjnych i rotacyjnych, przy czym tych
Pochodna i różniczka funkcji oraz jej zastosowanie do obliczania niepewności pomiarowych
 Pochodna i różniczka unkcji oraz jej zastosowanie do obliczania niepewności pomiarowych Krzyszto Rębilas DEFINICJA POCHODNEJ Pochodna unkcji () w punkcie określona jest jako granica: lim 0 Oznaczamy ją
Pochodna i różniczka unkcji oraz jej zastosowanie do obliczania niepewności pomiarowych Krzyszto Rębilas DEFINICJA POCHODNEJ Pochodna unkcji () w punkcie określona jest jako granica: lim 0 Oznaczamy ją
Chemia kwantowa. Pytania egzaminacyjne. 2010/2011: 1. Przesłanki doświadczalne mechaniki kwantowej.
 1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
Spektroskopia magnetyczna
 Spektroskopia magnetyczna Literatura Zbigniew Kęcki, Podstawy spektroskopii molekularnej, PWN W- wa 1992 lub nowsze wydanie Przypomnienie 1) Mechanika ruchu obrotowego - moment bezwładności, moment pędu,
Spektroskopia magnetyczna Literatura Zbigniew Kęcki, Podstawy spektroskopii molekularnej, PWN W- wa 1992 lub nowsze wydanie Przypomnienie 1) Mechanika ruchu obrotowego - moment bezwładności, moment pędu,
Atomy mają moment pędu
 Atomy mają moment pędu Model na rysunku jest modelem tylko klasycznym i jak wiemy z mechaniki kwantowej, nie odpowiada dokładnie rzeczywistości Jednakże w mechanice kwantowej elektron nadal ma orbitalny
Atomy mają moment pędu Model na rysunku jest modelem tylko klasycznym i jak wiemy z mechaniki kwantowej, nie odpowiada dokładnie rzeczywistości Jednakże w mechanice kwantowej elektron nadal ma orbitalny
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Wykład Budowa atomu 1
 Wykład 30. 11. 2016 Budowa atomu 1 O atomach Trochę historii i wprowadzenie w temat Promieniowanie i widma Doświadczenie Rutherforda i odkrycie jądra atomowego Model atomu wodoru Bohra sukcesy i ograniczenia
Wykład 30. 11. 2016 Budowa atomu 1 O atomach Trochę historii i wprowadzenie w temat Promieniowanie i widma Doświadczenie Rutherforda i odkrycie jądra atomowego Model atomu wodoru Bohra sukcesy i ograniczenia
Rozmycie pasma spektralnego
 Rozmycie pasma spektralnego Rozmycie pasma spektralnego Z doświadczenia wiemy, że absorpcja lub emisja promieniowania przez badaną substancję występuje nie tylko przy częstości rezonansowej, tj. częstości
Rozmycie pasma spektralnego Rozmycie pasma spektralnego Z doświadczenia wiemy, że absorpcja lub emisja promieniowania przez badaną substancję występuje nie tylko przy częstości rezonansowej, tj. częstości
