Laboratorium Biologii i Mikrobiologii
|
|
|
- Renata Król
- 8 lat temu
- Przeglądów:
Transkrypt
1 dr Mariola Chomczyńska dr Agnieszka Rożej Laboratorium Biologii i Mikrobiologii II rok studiów stacjonarnych I-go stopnia 30 godz. Lp. Wykaz ćwiczeń 1 Zasady mikroskopowania 2 Budowa komórki prokariotycznej i eukariotycznej 3 Metabolizm organizmów 4 Występowanie drobnoustrojów w środowisku wodnym, glebie i powietrzu 5 Występowanie drobnoustrojów w środowisku wodnym, glebie i powietrzu cd. 6 Biologiczne badanie wód rola bioindykatorów w określaniu jakości środowiska 7 Biocenoza osadu czynnego 8 Zajęcia zaliczeniowe
2 Ćwiczenie 1 Zasady mikroskopowania Cel ćwiczeń: Poznanie zasad mikroskopowania, nabycie umiejętności mierzenia wielkości obiektów mikroskopowych. Zagadnienia teoretyczne: 1. Rodzaje i przykłady zastosowań mikroskopów 2. Budowa i zasada działania zwykłego mikroskopu świetlnego 3. Powiększenie i zdolność rozdzielcza mikroskopu, immersja 4. Sposoby mierzenia obiektów mikroskopowych Materiały: preparaty mikroskopowe trwałe, owoce jarzębiny, liść kapusty, liść spichrzowy cebuli, sól fizjologiczna Aparatura i szkło: mikroskop świetlny, szkiełka podstawowe i nakrywkowe Wykonanie ćwiczenia: 1. Przygotowanie preparatu mikroskopowego W celu przygotowania preparatu należy: - umyć szkiełko podstawowe i osuszyć bibułą, - nanieść kroplę soli fizjologicznej na szkiełko podstawowe, - wprowadzić niewielki i cienki fragment tkanki (np. skórka z wewnętrznej strony liścia cebuli, skórka z owocu jarzębiny) do kropli soli fizjologicznej, - całość przykryć szkiełkiem nakrywkowym. 2. Skalowanie okularu mikrometrycznego W celu wyskalowania okularu mikrometrycznego należy: - umieścić na stoliku mikroskopu mikrometr przedmiotowy, - włożyć na miejsce jednego z okularów okular mikrometryczny, - patrząc przez okular mikrometryczny znaleźć obraz skali mikrometru przedmiotowego, - ustawić skalę mikrometru przedmiotowego i numerowaną skalę okularu mikrometrycznego równolegle do siebie, - ustawić podziałkę śruby mikrometrycznej okularu mikrometrycznego w pozycji 0, - przesunąć ostrożnie mikrometr przedmiotowy tak aby wybrana długa działka skali mikrometru przedmiotowego (ale nie pierwsza) pokryła się z przecięciem krzyża okularu mikrometrycznego, - przesunąć krzyż na następną długą działkę skali mikrometru przedmiotowego kręcąc śrubą mikrometryczną okularu mikrometrycznego (tj. przesunąć krzyż na odcinku 100 µm), - odczytać ilość działek ze skali śruby okularu mikrometrycznego (uwzględniając jednocześnie ewentualne pełne obroty śruby) odpowiadających przesunięciu krzyża na odcinku 100 µm, - uzyskane dane wykorzystać do ułożenia proporcji i wykonać potrzebne obliczenia:
3 100 µm a działek skali śruby mikrometrycznej x µm 1 działka skali śruby mikrometrycznej, - wyskalować okular mikrometryczny dla obiektywów o powiększeniu 5x, 10x i 40x. 3. Pomiar wielkości komórek w przygotowanym preparacie Aby dokonać pomiaru wielkości wybranej komórki należy: - włożyć na miejsce jednego z okularów mikroskopu okular mikrometryczny, - znaleźć obraz preparatu w mikroskopie przy danym powiększeniu obiektywu, - wyzerować skalę śruby mikrometrycznej i ustawić przecięcie krzyża w miejscu od którego pomiar będzie się zaczynał, - kręcąc śrubą mikrometryczną okularu mikrometrycznego przesunąć krzyż nici do miejsca, gdzie pomiar będzie zakończony, - odczytać ilość działek ze skali śruby okularu mikrometrycznego odpowiadającą przesunięciu krzyża na mierzonym odcinku, - przeliczyć liczbę działek na mikrometry zgodnie z wcześniejszą kalibracją okularu mikrometrycznego dla danego powiększenia obiektywu. Literatura: 1. Różalski A.: Ćwiczenia z mikrobiologii ogólnej, cz.1 i cz.2, Wydawnictwo Uniwersytetu Łódzkiego, Łódź Libudzisz Z., Kowal K., Żakowska Z.: Mikrobiologia techniczna, t.1, Wydawnictwo Naukowe PWN, Warszawa Zmysłowska I.: Mikrobiologia ogólna i środowiskowa, Wydawnictwo Uniwersytetu Warmińsko-Mazurskiego, Olsztyn 2002.
4 Ćwiczenie 2 Budowa komórki prokariotycznej i eukariotycznej Cel ćwiczeń: Poznanie szczegółów budowy komórki prokariotycznej, eukariotycznej, roślinnej i zwierzęcej z jednoczesnym uwzględnieniem funkcji organelli komórkowych. Zagadnienia teoretyczne: 1. Struktura komórki prokariotycznej (z uwzględnieniem budowy i funkcji rzęsek, fimbrii i otoczki) 2. Metoda barwienia bakterii wg Grama budowa ściany komórkowej u bakterii Gramdodatnich i Gram-ujemnych 3. Struktura komórki eukariotycznej różnice w budowie komórki roślinnej i zwierzęcej 4. Funkcje organelli komórkowych Materiały: hodowle bakterii właściwych z rodzajów: Escherichia, Bacillus, skórka z wewnętrznej strony liścia spichrzowego cebuli lub liścia trzykrotki, zawiesina drożdży (Sacharomyces cerevisiae), sól fizjologiczna, 5% r-ór NaCl, r-ór fioletu krystalicznego, etanol (70%), płyn Lugola, fuksyna fenolowa, błękit metylenowy, gotowe preparaty bakterii: Escherichia coli, Bacillus megaterium, Micrococcus luteus, Clostridium sporogenes Aparatura i szkło: mikroskop świetlny, szkiełka podstawowe i nakrywkowe Wykonanie ćwiczenia: Obserwacje mikroskopowe przeprowadzić za pomocą zwykłego mikroskopu optycznego przy użyciu obiektywu suchego 40x oraz immersyjnego o powiększeniu 100x. 1. Morfologia komórek bakteryjnych Obserwacja utrwalonych preparatów mikroskopowych następujących gatunków bakterii: 1. Escherichia coli 2. Bacillus megaterium 3. Micrococcus luteus 4. Clostridium sporogenes 2. Preparat przyżyciowy zwykły: - na odtłuszczonym szkiełku podstawowym umieścić kroplę 0,85% roztworu NaCl (sól fizjologiczna), do którego za pomocą ezy bakteriologicznej, wysterylizowanej w płomieniu palnika, wprowadzić 24-godzinną hodowlę bakterii ze skosu agarowego, - preparat przykryć szkiełkiem nakrywkowym. 3. Plazmoliza w komórkach skórki z wewnętrznej strony łuski cebuli i liścia trzykrotki: - umyć szkiełko podstawowe, - nanieść na szkiełko kroplę soli fizjologicznej, - wprowadzić niewielki fragment skórki (cebuli lub trzykrotki) do kropli,
5 - całość przykryć szkiełkiem nakrywkowym, a obok szkiełka - z lewej strony nanieść kroplę stężonego roztworu NaCl - z prawej strony położyć pasek bibuły, - obserwować preparat przy powiększeniu obiektywu 10x (40x), jednocześnie absorbując wodę z preparatu za pomocą paska bibuły, - narysować etapy plazmolizy. 4. Barwienie bakterii metodą Grama: - wykonać rozmaz 24-godzinnej hodowli bakterii na szkiełku podstawowym, - wysuszyć preparat w temperaturze pokojowej, a następnie utrwalić, przeprowadzając preparat przez płomień palnika zawiesiną zwróconą ku górze, - zalać preparat roztworem fioletu krystalicznego na 2 min, spłukać wodą, zalać płynem Lugola na 1 min., - zanurzyć preparat w 70% alkoholu etylowym na 30 sek., spłukać wodą, - dobarwić preparat roztworem fuksyny zasadowej przez sek., spłukać dokładnie wodą i wysuszyć na powietrzu, - wykonać obserwacje mikroskopowe bakterii za pomocą obiektywu immersyjnego o powiększeniu 100x. W wyniku barwienia bakterie Gram-dodatnie zostają zabarwione na fioletowo, a bakterie Gram-ujemne na różowo. 5. Obserwacja komórek drożdży (Sacharomyces cerevisiae) preparat przyżyciowy: - na odtłuszczone szkiełko podstawowe nanieść kroplę hodowli płynnej S. cerevisiae (w przypadku hodowli na podłożu stałym drobnoustroje zawieszamy w 0,85% NaCl) i kroplę barwnika błękitu metylenowego 1: Całość przykryć szkiełkiem nakrywkowym, - oglądać preparat pod mikroskopem stosując powiększenie 100x i 400x, - obliczyć zawartość procentową komórek martwych drożdży: policzyć komórki zabarwione na niebiesko przypadające na 100 komórek drożdży. Wynik barwienia: zabarwieniu ulegają komórki martwe, w których błona komórkowa, warunkująca barierę półprzepuszczalności traci właściwości wybiórcze i nie jest selektywna. Błękit metylenowy w środowisku wzrostu, w wyniku działania dehydrogenaz drożdży, przechodzi w formę zredukowaną, bezbarwny leukobłękit. Literatura: 1. Kunicki-Goldfinger W. J. H.: Życie bakterii, Wydawnictwo Naukowe PWN, Warszawa Różalski A.: Ćwiczenia z mikrobiologii ogólnej, cz.1 i cz.2, Wydawnictwo Uniwersytetu Łódzkiego, Łódź Zmysłowska I.: Mikrobiologia ogólna i środowiskowa, Wydawnictwo Uniwersytetu Warmińsko-Mazurskiego, Olsztyn Solomon E.P., Berg L.R., Martin D.W., Villee C.A.: Biologia, Oficyna Wydawnicza Multico, Warszawa Czubaj A.: Biologia, Państwowe Wydawnictwa Rolnicze i Leśne, Warszawa 1999.
6 Ćwiczenie 3 Metabolizm organizmów Cel ćwiczeń: Zapoznanie się z przebiegiem podstawowych procesów metabolicznych towarzyszących neutralizacji zanieczyszczeń i wykorzystywanych w rozwiązaniach technologicznych inżynierii środowiska. Zagadnienia teoretyczne: 1. Typy odżywiania się organizmów źródła makroelementów i mikroelementów 2. Sposoby zdobywania energii oddychanie tlenowe, beztlenowe, fermentacja 3. Rodzaje substratów energetycznych wykorzystywanych przez organizmy żywe 4. Asymilacja dwutlenku węgla: fotosynteza bakteryjna i roślinna, chemosynteza 5. Fosforylacja substratowa, oksydatywna, fotooksydacja Materiały: podłoża stałe, różnicujące: McConkey agar, ENDO agar, agar odżywczy + purpura bromokrezolowa + różne źródła węgla (glukoza, glicerol, mannitol, cytrynian Na, laktoza), agar odżywczy + skrobia, podłoża płynne: bulion odżywczy + laktoza + purpura bromokrezolowa, szczepy bakteryjne: Escherichia coli, Enterobacter aerogenes, Serratia marcescens, Pseudomonas fluorescens, Bacillus subtilis, Sarcina lutea, zielona masa roślinna (natka pietruszki lub in.), 96% alkohol etylowy, płyn rozwijający: toluen: eter: aceton (10:2,5:2), moczarka kanadyjska, ziemia ogrodowa, 50mM KOH, 50mM HCl, glukoza, oranż metylowy. Aparatura i szkło: probówki (20 i 60cm 3 ), płytki Petriego, zlewki (50 i 500cm 3 ), słoiki 1L Twist, kolby stożkowe (100 i 500cm 3 ), biureta, moździerz porcelanowy, piasek, bibuła filtracyjna, cylindry miarowe (50 i 100cm 3 ), bagietki z gumką recepturką, linijka z podziałką, termometr Wykonanie ćwiczenia: 1. Identyfikacja szczepów bakteryjnych: W celu identyfikacji szczepów należy: - dokonać obserwacji wzrostu, wyglądu i barwy wyrosłych kolonii szczepów bakterii na stałych podłożach różnicujących, zmiany barwy podłoża stałego i płynnego w przypadku zdolności poszczególnych szczepów bakterii do rozkładu zawartych w podłożu źródeł węgla, - rozpoznać szczepy bakterii na podstawie wyżej wymienionych cech na płytkach z numerowanymi posiewami. 2. Wpływ natężenia światła i temperatury na proces fotosyntezy Pomiary intensywności fotosyntezy oparte są na oznaczaniu wymiany gazowej roślin i polegają na określeniu ilości pobranego dwutlenku węgla lub wydzielonego tlenu. Do tego celu służą metody chemiczne bądź gazometryczne. Do nich m.in. zalicza się półilościową metodę polegającą na liczeniu pęcherzyków tlenu wydzielonego przez fotosyntetyzujące gałązki roślin wodnych.
7 Przebieg ćwiczenia: - gałązkę moczarki kanadyjskiej umieścić w pętli gumki recepturowej przymocowanej do szklanej bagietki i zanurzyć (wierzchołkiem do dołu) w probówce (lub cylindrze) z wodą wodociągową wzbogaconą kilkoma kroplami mineralnej wody gazowanej, - całość umieścić w kolbie stożkowej napełnionej wodą, - ustalić 2 punkty w odległości 2 i 45 cm między źródłem światła a rośliną, - w każdym punkcie kolejno umieścić moczarkę i określić ilość wydzielanych pęcherzyków tlenu; pomiary wykonywać w ciągu 2 minut po 4 minutach adaptacji roślin do warunków świetlnych, trzykrotnie dla każdej odległości od źródła światła, - wyniki badań zestawić w tabeli, Tabela 1. Wpływ natężenia światła na proces fotosyntezy odległość od źródła światła ilość pęcherzyków O 2 w ciągu 2 minut powtórzenia (cm) średnia do dwu kolb stożkowych napełnionych wodą wodociągową o temperaturze 5 o C i 25 o C wstawiać kolejno probówkę z zanurzoną w wodzie gałązką moczarki kanadyjskiej, - po odczekaniu 4 minut, w celu adaptacji moczarki do warunków temperaturowych, liczyć wydzielane pęcherzyki tlenu przez 2 minuty, - pomiar w każdej temperaturze powtórzyć trzykrotnie, - wyniki badań zestawić w tabeli, Tabela 2. Wpływ temperatury na proces fotosyntezy temperatura ( o C) ilość pęcherzyków O 2 w ciągu 2 minut powtórzenia średnia Wyodrębnianie i rozdzielanie barwników asymilacyjnych Reakcje fotosyntezy zachodzą w specjalnych strukturach komórkowych zawierających barwniki fotosyntetyczne. U fotosyntetyzujących Procaryota odbywają się one w wypustkach błon plazmatycznych, zaś w komórkach Eucaryota w chloroplastach. Barwniki związane z fotosyntezą zalicza się do trzech głównych klas: chlorofili, karotenoidów i fikobilin. Chlorofile i karotenoidy są związkami dobrze rozpuszczalnymi w rozpuszczalnikach organicznych, a fikobiliny dobrze rozpuszczają się w wodzie. Przebieg ćwiczenia: - masę roślinną rozetrzeć w moździerzu z piaskiem; uzyskaną miazgę wymieszać z 96% alkoholem etylowym z dodatkiem acetonu; po ponownym utarciu mieszaninę przesączyć przez sączek bibułowy; ekstrakt chronić przed światłem. - przygotować pasek bibuły filtracyjnej o wymiarach 2x20 cm i bibuły chromatograficznej; nanieść kolejno kroplami w jednym miejscu (3 cm od dolnej krawędzi bibuły) wyciąg barwników; po każdym naniesieniu kropli pasek bibuły wysuszyć, - do cylindra wlać płyn rozwijający (warstwa 1-1,5 cm); pasek bibuły z naniesionymi barwnikami umieścić w cylindrze tak, aby końcem dotykał płynu rozwijającego; cylinder
8 szczelnie przykryć; rozdział barwników prowadzić pod włączonym dygestorium!; po 30 minutach wyjąć pasek bibuły, dokładnie wysuszyć i rozpoznać barwniki. 4. Oznaczanie aktywności oddechowej mikroorganizmów glebowych indukowanej substratem (glukozą) Występujące w glebie mikroorganizmy oraz zwierzęta bezkręgowe pobierają w procesie oddychania z powietrza glebowego tlen, a wydzielają dwutlenek węgla, co można wykazać doświadczalnie. Zazwyczaj ok. 10% mikroorganizmów glebowych zachowuje aktywność. Pozostałe 90% znajduje się w stanie uśpienia lub życia utajonego. Po wprowadzeniu do gleby odpowiednich składników pokarmowych, stężenie aktywnych komórek rośnie. Miarą aktywności oddechowej organizmów jest ilość wydzielonego dwutlenku węgla. W trakcie ćwiczenia wydzielany CO 2 (produkt oddychania) ulega absorpcji w roztworze KOH, stosownie do reakcji: KOH + CO 2 K + + HCO 3 - Nadmiar KOH jest określony ilościowo za pomocą miareczkowania HCl. Przebieg ćwiczenia: - do dwóch słojów litrowych wprowadzić po 400g żyznej ziemi ogrodowej; do jednego z nich dodać 4g glukozy i wymieszać dokładnie cukier z ziemią, - do słojów wstawić małe zlewki zawierające po 20ml KOH (50mM); słoje szczelnie zakręcić i pozostawić na 24h, - po inkubacji wyjąć zlewki, zawartość przelać do kolb stożkowych o pojemności 100ml; dodać 2-3 krople wskaźnika ph oranżu metylowego; nadmiar KOH miareczkować 50mM HCl do zmiany barwy z żółtej na czerwoną, - ilość wydzielonego CO 2 obliczyć ze wzoru: ( V V y = 0 ) m gdzie: y - aktywność oddechowa gleby [mm CO 2 / g gleby/ doba], V 0 - objętość KOH użyta do absorpcji CO 2 [ml], V - objętość KOH nie zobojętniona przez HCO 3 - [ml], odpowiadająca objętości HCl zużytego do miareczkowania, m - masa próbki gleby w słoju [g], - porównać aktywność oddechową mikroorganizmów glebowych indukowaną i nie indukowaną dodatkiem glukozy. Literatura: 1. Kunicki-Goldfinger W.: Życie bakterii, Wydawnictwo Naukowe PWN, Warszawa Różalski A.: Ćwiczenia z mikrobiologii ogólnej, cz.1 i cz.2, Wydawnictwo Uniwersytetu Łódzkiego, Łódź Schlegel H.: Mikrobiologia ogólna, Wydawnictwo Naukowe PWN, Warszawa Zmysłowska I.: Mikrobiologia ogólna i środowiskowa, Wydawnictwo Uniwersytetu Warmińsko-Mazurskiego, Olsztyn Solomon E.P., Berg L.R., Martin D.W., Villee C.A.: Biologia, Oficyna Wydawnicza Multico, Warszawa Uziak Z.: Przewodnik do ćwiczeń z fizjologii roślin, Wydawnictwo Akademii Rolniczej, Lublin 1985.
9 Ćwiczenie 4 Występowanie drobnoustrojów w środowisku wodnym, glebie i powietrzu Cel ćwiczeń: Zapoznanie się z warunkami występowania drobnoustrojów w wodzie Poznanie metod oznaczania mikrobiologicznego zanieczyszczenia wody Zagadnienia teoretyczne: 1. Metody liczenia drobnoustrojów 2. Czynniki decydujące o występowaniu drobnoustrojów w wodzie 3. Wskaźniki stanu sanitarnego wody (miano i wskaźnik coli) 4. Metody oznaczania mikrobiologicznego zanieczyszczenia wody Materiały: sól fizjologiczna, podłoże ENDO, fiolet krystaliczny, agar odżywczy, hodowla Escherichia coli, hodowla Bacillus subtilis Aparatura i szkło: mikroskop świetlny z obiektywem immersyjnym, komora Thoma, probówki, płytki Petriego Wykonanie ćwiczenia: 1. Oznaczanie liczby bakterii metodą Wrighta Metoda ta oparta jest na ustaleniu liczby drobnoustrojów w porównaniu do znanej liczby komórek drożdży. Oznaczenie liczby komórek drożdży w l mm 3 wykonuje się za pomocą hemocytometru Thoma (lub Bürkera). Komora Thoma ma głębokość 0,1 mm; na jej dnie znajduje się siatka składająca się z 16 dużych kwadratów, każdy z nich podzielony jest na 16 małych; wymiary jednej małej komory wynoszą: wysokość - 1/10 mm, szerokość - 1/20 mm, długość - 1/20 mm; tak więc powierzchnia małej komory wynosi 1/400 mm 2, a jej objętość 1/4000 mm 3. Po przygotowaniu zawiesiny drożdży wprowadza się ją do komory Thoma. Następnie pod mikroskopem liczy się komórki drożdży w 5 dużych tj. w 80 małych kwadracikach komory. Liczbę komórek drożdży (Y) w 1 mm 3 ustala się według wzoru: liczba komórek rozcienczenie 4000 Y = 80 Dla ustalenia liczby badanych drobnoustrojów, w tym wypadku, B. subtilis należy: - skos z hodowlą B. subtilis zmyć 3 cm 3 0,85% NaCl; zawiesinę bakterii rozcieńczyć trzykrotnie, - zmieszać 0,5 cm 3 zawiesiny drożdży i 0,5 cm 3 zawiesiny bakteryjnej, - sporządzić rozmaz na szkiełku podstawowym, wysuszyć go a następnie utrwalić w płomieniu palnika, - utrwalony rozmaz barwić r-rem fioletu krystalicznego przez 2 minuty, - fiolet zmyć wodą destylowaną i preparat wysuszyć, - używając mikroskopu zliczyć liczbę komórek drożdży i bakterii w 20 polach widzenia, - obliczyć liczbę komórek bakteryjnych według wzoru:
10 Liczba bakterii w l cm 3 = liczba bakterii Y 1000, liczba drozdzy gdzie: (Y) - liczba komórek drożdży w l mm 3, przelicznik na l cm Oznaczanie liczby bakterii metodą płytkową W metodzie płytkowej liczbę komórek bakterii w badanej próbce określa się na podstawie liczby koloni wyrosłych po okresie inkubacji na podłożu odżywczym. Dla ustalenia liczby bakterii tj. E. coli należy: - sporządzić zawiesinę bakterii E. coli zmywając hodowlę ze skosu 3 cm 3 0,85% NaCl, - przygotować rozcieńczenia wg schematu na rys. 1, Rys. 1. Schemat rozcieńczeń zawiesiny bakterii - wysiać po 1 cm 3 zawiesiny E. coli - na 2 płytki z podłożem ENDO z rozcieńczeń: 10-7, 10-8 i 10-9, - hodowle inkubować przez noc w temperaturze 37 C, - po okresie inkubacji zliczyć wyrosłe kolonie na podłożach odżywczych, - liczbę komórek w zawiesinie wyjściowej obliczyć mnożąc liczbę wyrosłych koloni przez dane rozcieńczenie. 3. Oznaczanie bakterii grupy coli metodą fermentacyjną probówkową badania wstępne W metodzie tej określana jest najbardziej prawdopodobna liczba bakterii grupy coli w 100 cm 3 badanej próbki (NPL) przy pomocy tablic sporządzonych na podstawie rachunku prawdopodobieństwa. Aby ustalić liczbę komórek bakterii należy: przygotować pożywkę z laktozą i purpurą bromokrezolową (pożywka LBP) przygotować rozcieńczenia badanej wody: 10-1, 10-2, 10-3, 10-4, 10-5
11 z każdego rozcieńczenia wysiać bakterie - po l ml - do 2 probówek zawierających po 9 ml pożywki hodowle inkubować przez 24 godzin w temperaturze 37 C po okresie inkubacji odczytać wyniki: za wynik dodatni przyjąć wystąpienie pęcherzyków gazu przy wstrząsaniu pożywki i jednoczesne zmętnienie oraz zakwaszenie podłoża (objawiające się zmianą barwy pożywki); za wynik ujemny przyjąć brak gazu i brak zakwaszenia podłoża odczytać NPL dla 2-probówkowego systemu posiewu z tablic rachunku prawdopodobieństwa Literatura: 1. Różalski A.: Ćwiczenia z mikrobiologii ogólnej, cz. 1 i cz.2, Wydawnictwo Naukowe PWN, Warszawa Schlegel H.: Mikrobiologia ogólna, Wydawnictwo Naukowe PWN, Warszawa Zmysłowska I.: Mikrobiologia ogólna i środowiskowa, Wydawnictwo Uniwersytetu Warmińsko-Mazurskiego, Olsztyn Libudzisz Z., Kowal K., Żakowska Z.: Mikrobiologia techniczna, t.1, Wydawnictwo Naukowe PWN, Warszawa Normy: PN-EN ISO 6222:2004, PN-EN ISO :2004, PN-EN ISO :2004, PN- EN ISO :2004/Ap2005, PN-EN ISO :2002, PN-ISO 8199:2001, PN-75/C arkusz 05, PN-77/C arkusz 07, PN-89/Z , PN-89/Z , PN-89/Z
12 Ćwiczenie 5 Występowanie drobnoustrojów w wodzie, glebie i powietrzu cd. Cel ćwiczeń: Zapoznanie się z warunkami występowania drobnoustrojów w glebie i powietrzu Poznanie metod oznaczania mikrobiologicznego zanieczyszczenia gleby i powietrza Zagadnienia teoretyczne: 1. Czynniki decydujące o występowaniu drobnoustrojów w glebie i powietrzu 2. Lokalizacja występowania drobnoustrojów w glebie 3. Pojęcie bioaerozolu 4. Wskaźniki stanu sanitarnego gleb (miano i wskaźnik coli); organizmy wskaźnikowe w powietrzu (Pseudomonas fluorescens, promieniowce, gronkowce) 5. Metody oznaczania mikrobiologicznego zanieczyszczenia gleby i powietrza Materiały: sól fizjologiczna, ziemia ogrodowa, 1% woda peptonowa, odczynnik Nesslera, agar odżywczy, podłoże TSA Aparatura i szkło: mikroskop świetlny z obiektywem immersyjnym, probówki, płytki Petriego Wykonanie ćwiczenia: 1. Oznaczanie miana bakterii amonifikacyjnych w próbce gleby metodą NPL Przebieg ćwiczenia: - 1g świeżej masy gleby zawiesić w 9 cm 3 płynu fizjologicznego (rozcieńczenie 10-1 ), wytrząsać kilka minut, - wykonać szereg rozcieńczeń: do szeregu probówek zawierających 4,5 cm 3 płynu fizjologicznego dodawać po 0,5 cm 3 poprzedniego rozcieńczenia (rozcieńczenia 10-2, 10-3, 10-4, 10-5, 10-6 ), - z każdego rozcieńczenia wysiać po l cm 3 do dwóch probówek z 9 cm 3 wody peptonowej, - hodowlę inkubować 7 dni w temp. 26 C, - po okresie inkubacji wykonać obserwacje wzrostu bakterii (zmętnienie, obecność kożucha, osadu), a także oznaczenia odczynu ph podłoża oraz obecności amoniaku - odczynnikiem Nesslera, - odczyn podłoża sprawdzić zanurzając krótki fragment paska wskaźnikowego w pożywce, - do probówek dodać po 0,2 cm 3 odczynnika Nesslera; pomarańczowa barwa świadczy o obecności amoniaku, - stwierdzenie wzrostu bakterii, obecności amoniaku i alkalizacji podłoża do ph ok. 8,0-9,0 świadczy o zaszłym procesie amonifikacji; wynik oznaczenia podać jako NPL i miano bakterii amonifikacyjnych (wielkość NPL i miana odczytuje się tablic opracowanych na podstawie rachunku prawdopodobieństwa). 2. Oznaczanie ogólnej liczby bakterii w powietrzu metodą sedymentacyjną Przebieg ćwiczenia: - przygotować trzy płytki Petriego z agarem odżywczym, - ustawić płytki w miejscu poboru próbki powietrza, zdjąć wieczka i poddać płytki ekspozycji, przez 10 minut; w tym czasie drobnoustroje sedymentują na powierzchnię pożywki, - płytki zakryć, inkubować 24h w temp. 37 C,
13 - policzyć kolonie wyrosłe na płytkach, obliczyć liczbę bakterii w 1m 3 powietrza wg wzoru: A 5 a π r t = 2 gdzie: a - średnia liczba kolonii bakterii na płytce, r - promień płytki Petriego [cm], t - czas ekspozycji [min], - zinterpretować wynik oceniając stopień zanieczyszczenia powietrza zgodnie z odpowiednią normą. 3. Oznaczanie ogólnej liczby bakterii w powietrzu metodą zderzeniową z użyciem impaktora Andersena Przebieg ćwiczenia: przygotować 6 płytek Petriego zawierających podłoże TSA, po zdjęciu przykrywek, szalki (odpowiednio oznakowane) umieścić w segmentach impaktora (urządzenie pozwala na pobieranie prób frakcji bioaerozolu o różnych rozmiarach cząstek: >7 µm, 7,0-4,7µm, 4,7-3,3µm, 3,3-2,1µm, 2,1-1,1µm, 1,1-0,65µm), włączyć pompę próżniową dla zapewnienia przepływu powietrza przez impaktor, jednocześnie rozpocząć pomiar czasu poboru próby powietrza, po zakończeniu poboru próby powietrza zanotować czas, a następnie wyjąć szalki z impaktora, i umieścić na nich przykrywki, szalki Petriego umieścić w inkubatorze w temperaturze 37 o C na 24 godziny, po zakończeniu okresu inkubacji zliczyć wyrosłe kolonie, skorygować liczbę koloni zgodnie z tabelą korelacji Andersena i określić liczbę jednostek koloniotworczych w 1m 3 powietrza wg. wzoru: CFU [m 3 ] = Objętość powietrza [m 3 ] = 10 liczba kolonii obj. powietrza 4 28,3 x czas pomiaru 1000 Literatura: 1. Różalski A.: Ćwiczenia z mikrobiologii ogólnej, cz. 1 i cz. 2, Wydawnictwo Naukowe PWN, Warszawa Schlegel H.: Mikrobiologia ogólna, Wydawnictwo Naukowe PWN, Warszawa Zmysłowska I.: Mikrobiologia ogólna i środowiskowa, Wydawnictwo Uniwersytetu Warmińsko-Mazurskiego, Olsztyn Libudzisz Z., Kowal K., Żakowska Z.: Mikrobiologia techniczna, t.1, Wydawnictwo Naukowe PWN, Warszawa Normy: PN-EN ISO 6222:2004, PN-EN ISO :2004, PN-EN ISO :2004, PN- EN ISO :2004/Ap2005, PN-EN ISO :2002, PN-ISO 8199:2001, PN-75/C arkusz 05, PN-77/C arkusz 07, PN-89/Z , PN-89/Z , PN-89/Z
14 Ćwiczenie 6 Biologiczne badanie wód rola bioindykatorów w określaniu jakości środowiska Cel ćwiczeń: Zapoznanie się z możliwością monitoringu jakości środowiska za pomocą organizmów żywych. Nabycie umiejętności rozpoznawania wybranych przedstawicieli grzybów, glonów, pierwotniaków, nicieni, wrotków, pierścienic. Zagadnienia teoretyczne: 1. Klasyfikacja wód zgodna z Ramową Dyrektywą Wodną (2000/60/WE). Stan ekologiczny wód. Elementy jakości wód 2. Charakterystyka bakterii, grzybów, glonów, pierwotniaków, nicieni, wrotków, pierścienic i owadów 3. Pojęcie bioindykacji 4. Saprobowość i trofizm system saprobów Kolkwitza-Marrsona oraz metody oceny stanu ekologicznego wód płynących zgodne z Ramową Dyrektywą Wodną 5. Proces samooczyszczania wód rola organizmów żywych Materiały: próbki planktonu pobrane ze zbiorników wodnych różniących się przynależnością do stref saprobowych Aparatura i szkło: mikroskop świetlny, szkiełka podstawowe, szkiełka nakrywkowe Wykonanie ćwiczenia: 1. Analiza planktonu metodą Pantlego i Bucka Przebieg ćwiczenia: - nanieść badaną próbkę planktonu na szkiełko podstawowe i przykryć szkiełkiem nakrywkowym, - ustawić wyraźny obraz przygotowanego preparatu w mikroskopie, - przeglądając 20 pól widzenia zliczać osobniki poszczególnych gatunków, - określić przynależność saprobową poszczególnych gatunków na podstawie wykazu organizmów wskaźnikowych, - przypisać zdiagnozowanym gatunkom wartość saprobowości s według danych podanych w tabeli 1, Tabela 1. Wartości saprobowości s strefa saprobowości znak umowny strefy wartość saprobowości - s ksenosaprobowa x 0 oligosaprobowa o 1 betamezosaprobowa b 2 alfamezosaprobowa a 3 polisaprobowa p 4
15 - obliczyć udziały procentowe poszczególnych gatunków, - przypisać poszczególnym gatunkom częstotliwość względną h według danych zawartych w tabeli 2, Tabela 2. Wartości częstotliwości względnej h liczba osobników danego gatunku w % częstotliwość względna h ogólnej ilości osobników < uzyskane dane zestawić według przykładu podanego w tabeli 3, gatunek Tabela 3. Analiza planktonu metodą Pantlego i Bucka liczba osobników osobniki danego gatunku w % wskaźnik s wskaźnik h s h a b c d suma obliczyć wartość wskaźnika saprobowości S według wzoru: s h S =, h - podać interpretację obliczonego wskaźnika S tj. zakwalifikować zbiornik, z którego pobrano próbę planktonu, do danej strefy saprobowości według danych przedstawionych w tabeli 4. Tabela 4. Określanie stref saprobowości za pomocą wskaźnika saprobowości S zakres wartości wskaźnika - S zaliczenie do strefy 1,0-1,5 oligosaprobowa 1,5-2,5 betamezosaprobowa 2,5-3,5 alfamezosaprobowa 3,5-4,0 polisaprobowa - wymienione wyżej czynności powtórzyć dla kolejnej próby planktonu pochodzącej ze zbiornika o odmiennej przynależności do stref saprobowych.
16 Literatura: 1. Turoboyski L.: Hydrobiologia techniczna, Państwowe Wydawnictwo Naukowe, Warszawa Kocwowa E.: Biologia w ochronie zdrowia i środowiska, Państwowe Wydawnictwo Naukowe, Warszawa Bobrowski M.M.: Podstawy biologii sanitarnej, Wydawnictwo Ekonomia i Środowisko, Białystok Kańska Z., Grabińska-Łoniewska A., Łebkowska M., Rzechowska E.: Ćwiczenia laboratoryjne z biologii sanitarnej. Część 1. Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa Kańska Z., Grabińska-Łoniewska A., Łebkowska M., Rzechowska E.: Ćwiczenia laboratoryjne z biologii sanitarnej. Część 2. Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa Jura C.: Bezkręgowce, Wydawnictwo Naukowe PWN, Warszawa Ramowa Dyrektywa Wodna (2000/60/WE).
17 Ćwiczenie 7 Biocenoza osadu czynnego Cel ćwiczenia: Zapoznanie się ze strukturą i funkcjonowaniem osadu czynnego oraz jego rolą w biologicznym oczyszczaniu ścieków. Zagadnienia teoretyczne: 1. Podstawy biologicznego oczyszczania ścieków metodą osadu czynnego 2. Morfologia osadu czynnego 3. Grupy morfologiczno-funkcjonalne organizmów w osadzie czynnym 4. Funkcje organizmów w osadzie czynnym Materiały: osad czynny z miejskiej oczyszczalni ścieków Aparatura i szkło: mikroskop świetlny, szkiełka podstawowe Wykonanie ćwiczenia: 1. Ogólna ocena osadu czynnego Przebieg ćwiczenia: - nanieść badaną próbkę osadu na szkiełko podstawowe, umieścić preparat na stoliku mikroskopu, obserwacje prowadzić pasami przy powiększeniu obiektywu 10x i 40x, - przy prowadzeniu obserwacji za pomocą obiektywu o 10x powiększeniu zaobserwować kształt, budowę i wielkość kłaczków osadu, określić zagęszczenie bakterii nitkowatych (indeks FI od 0 do 5) i przedstawicieli Protozoa i Metazoa (skala 0-3) reprezentujących: orzęski, wiciowce, ameby nagie, ameby skorupkowe, słonecznice, wrotki, nicienie, skąposzczety (podczas analizy, w razie potrzeby, posłużyć się tablicami z rysunkami schematycznymi organizmów osadu czynnego), - przy prowadzeniu obserwacji za pomocą obiektywu o 40x powiększeniu zaobserwować budowę i wielkość pierwotniaków oraz spójność kłaczków osadu, określić zagęszczenie bakterii nie związanych z kłaczkami tj. rozproszonych (skala 0-3), śrubowców Spirillae (skala 0-3) i krętków Spirochaetae (skala 0-3), - wyniki analizy zestawić w tabeli 1, - ocenić jakość osadu na podstawie tabeli 2.
18 Tabela 1. Formularz analizy mikroskopowej osadu czynnego parametr wartość indeksu bakterie nitkowate a skupienia zooglealne b pierwotniaki i bezkręgowce w tym b : orzęski wiciowce ameby nagie ameby skorupkowe słonecznice wrotki nicienie skąposzczety bakterie rozproszone c śrubowce b krętki b a skala 0-5 b skala 0-3 (brak liczne komórki/kolonie w preparacie) c skala 0-3 (brak liczne komórki/kolonie w polu widzenia) charakterystyka kłaczków: zwarte () otwarte () mocne () słabe () regularne () nieregularne () Tabela 2. Ocena jakości osadu jakość dobra średnia zła indeks nitek < bakterie wolnożyjące > 3 śrubowce 0 1 > 2 orzęski/ameby skorupkowe 1 < 1 0 wiciowce/ameby nagie struktura kłaczków zwarte mocne regularne otwarte słabe nieregularne Literatura 1. Kańska Z., Grabińska-Łoniewska A., Łebkowska M., Rzechowska E.: Ćwiczenia laboratoryjne z biologii sanitarnej. Część 1, Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa Eikelboom D.H., van Buijsen H.J.J.: Podręcznik mikroskopowego badania osadu czynnego, Wydawnictwo Seidel-Przywecki, Szczecin Bobrowski M.M.: Podstawy biologii sanitarnej, Wydawnictwo Ekonomia i Środowisko, Białystok Zmysłowska I.: Mikrobiologia ogólna i środowiskowa, Wydawnictwo Uniwersytetu Warmińsko-Mazurskiego, Olsztyn Błaszczyk M.K.: Mikroorganizmy w ochronie środowiska, Wydawnictwo Naukowe PWN, Warszawa Libudzisz Z., Kowal K., Żakowska Z.: Mikrobiologia techniczna, t.2, Wydawnictwo Naukowe PWN, Warszawa
Ćwiczenie 4-5 Mikrobiologiczne kryteria oceny sanitarnej wody
 ĆWICZENIA Z GOSPODARKI ENERGETYCZNEJ, WODNEJ I ŚCIEKOWEJ CZĘŚĆ MIKROBIOLOGICZNA Ćwiczenie 4-5 Mikrobiologiczne kryteria oceny sanitarnej wody Część teoretyczna: 1. Kryteria jakości sanitarnej wody przeznaczonej
ĆWICZENIA Z GOSPODARKI ENERGETYCZNEJ, WODNEJ I ŚCIEKOWEJ CZĘŚĆ MIKROBIOLOGICZNA Ćwiczenie 4-5 Mikrobiologiczne kryteria oceny sanitarnej wody Część teoretyczna: 1. Kryteria jakości sanitarnej wody przeznaczonej
liczba godzin 2 MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA półpłynne stałe
 MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA Ćwiczenie 6 i 7 6 Fizjologia drobnoustrojów Wymagania metaboliczne bakterii. Rodzaje podłóż mikrobiologicznych.
MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA Ćwiczenie 6 i 7 6 Fizjologia drobnoustrojów Wymagania metaboliczne bakterii. Rodzaje podłóż mikrobiologicznych.
Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku chemia kosmetyczna
 1 Zakład Mikrobiologii UJK Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku chemia kosmetyczna 2 Zakład Mikrobiologii UJK Zakres materiału (zagadnienia)
1 Zakład Mikrobiologii UJK Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku chemia kosmetyczna 2 Zakład Mikrobiologii UJK Zakres materiału (zagadnienia)
Do jednego litra medium dodać 10,0 g skrobi ziemniaczanej lub kukurydzianej i mieszać do uzyskania zawiesiny. Sterylizować w autoklawie.
 Ćwiczenie 3. Izolacja laseczek przetrwalnikujących z gleby Cel ćwiczenia: Izolacja i testowanie przydatności biotechnologicznej laseczek z rodzaju Bacillus występujących w glebie. Odczynniki i podłoża:
Ćwiczenie 3. Izolacja laseczek przetrwalnikujących z gleby Cel ćwiczenia: Izolacja i testowanie przydatności biotechnologicznej laseczek z rodzaju Bacillus występujących w glebie. Odczynniki i podłoża:
BIOLOGIA KOMÓRKI KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO- FAZOWYM; BARWIENIA CYTOCHEMICZNE KOMÓREK
 BIOLOGIA KOMÓRKI KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO- FAZOWYM; BARWIENIA CYTOCHEMICZNE KOMÓREK KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO-FAZOWYM;
BIOLOGIA KOMÓRKI KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO- FAZOWYM; BARWIENIA CYTOCHEMICZNE KOMÓREK KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO-FAZOWYM;
ISBN
 1 2 Recenzent wydania pierwszego: dr hab. RYSZARD GOŁDYN, prof. Uniwersytetu im. Adama Mickiewicza Poszczególne ćwiczenia napisali: dr MICHAŁ MICHAŁKIEWICZ wprowadzenie, ćwiczenia 4, 6-12 mgr MAŁGORZATA
1 2 Recenzent wydania pierwszego: dr hab. RYSZARD GOŁDYN, prof. Uniwersytetu im. Adama Mickiewicza Poszczególne ćwiczenia napisali: dr MICHAŁ MICHAŁKIEWICZ wprowadzenie, ćwiczenia 4, 6-12 mgr MAŁGORZATA
ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN
 ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN CZĘŚĆ TEORETYCZNA Mechanizmy promujące wzrost rośli (PGP) Metody badań PGP CZĘŚĆ PRAKTYCZNA 1. Mechanizmy promujące wzrost roślin. Odczyt. a) Wytwarzanie
ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN CZĘŚĆ TEORETYCZNA Mechanizmy promujące wzrost rośli (PGP) Metody badań PGP CZĘŚĆ PRAKTYCZNA 1. Mechanizmy promujące wzrost roślin. Odczyt. a) Wytwarzanie
ĆWICZENIE 5 Barwniki roślinne. Ekstrakcja barwników asymilacyjnych. Rozpuszczalność chlorofilu
 ĆWICZENIE 5 Barwniki roślinne Ekstrakcja barwników asymilacyjnych 400 mg - zhomogenizowany w ciekłym azocie proszek z natki pietruszki 6 ml - etanol 96% 2x probówki plastikowe typu Falcon na 15 ml 5x probówki
ĆWICZENIE 5 Barwniki roślinne Ekstrakcja barwników asymilacyjnych 400 mg - zhomogenizowany w ciekłym azocie proszek z natki pietruszki 6 ml - etanol 96% 2x probówki plastikowe typu Falcon na 15 ml 5x probówki
Interpretacja wyników analiz ilości i obecności drobnoustrojów zgodnie z zasadami badań mikrobiologicznych żywności i pasz?
 Wydział Biotechnologii i Nauk o Żywności Seminarium STC 2018 Interpretacja wyników analiz ilości i obecności drobnoustrojów zgodnie z zasadami badań mikrobiologicznych żywności i pasz? Dr inż. Agnieszka
Wydział Biotechnologii i Nauk o Żywności Seminarium STC 2018 Interpretacja wyników analiz ilości i obecności drobnoustrojów zgodnie z zasadami badań mikrobiologicznych żywności i pasz? Dr inż. Agnieszka
III. Fizjologia bakterii i zasady diagnostyki bakteriologicznej
 III. Fizjologia bakterii i zasady diagnostyki bakteriologicznej Ćwiczenie 1. Rodzaje pożywek i ich zastosowanie a. Podłoże stałe - proste Agar zwykły (AZ) b. Podłoża wzbogacone Agar z dodatkiem 5% odwłóknionej
III. Fizjologia bakterii i zasady diagnostyki bakteriologicznej Ćwiczenie 1. Rodzaje pożywek i ich zastosowanie a. Podłoże stałe - proste Agar zwykły (AZ) b. Podłoża wzbogacone Agar z dodatkiem 5% odwłóknionej
XIX. Pałeczki Gram-ujemne część I - ćwiczenia praktyczne
 XIX. Pałeczki Gram-ujemne część I - ćwiczenia praktyczne Ćwiczenie 1. Wykonanie preparatu mikroskopowego barwionego metodą Grama Opis preparatu: Ćwiczenie 2. Ocena wzrostu szczepów na podłożach stałych
XIX. Pałeczki Gram-ujemne część I - ćwiczenia praktyczne Ćwiczenie 1. Wykonanie preparatu mikroskopowego barwionego metodą Grama Opis preparatu: Ćwiczenie 2. Ocena wzrostu szczepów na podłożach stałych
HYDROLIZA SOLI. ROZTWORY BUFOROWE
 Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
Ćwiczenie 1 Morfologia I fizjologia bakterii
 Ćwiczenie 1 Morfologia I fizjologia bakterii 1. Barwienie złożone - metoda Grama Przygotowanie preparatu: odtłuszczone szkiełko podstawowe, nałożenie bakterii ( z hodowli płynnej 1-2 oczka ezy lub ze stałej
Ćwiczenie 1 Morfologia I fizjologia bakterii 1. Barwienie złożone - metoda Grama Przygotowanie preparatu: odtłuszczone szkiełko podstawowe, nałożenie bakterii ( z hodowli płynnej 1-2 oczka ezy lub ze stałej
RAPORT Z BADAŃ 01369/2015/D/AGST. Blirt S.A Gdańsk, ul. Trzy Lipy 3/1.38. Dział DNA-Gdańsk. Nr zlecenia
 Strona1/7 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 01369/2015/D/AGST NAZWA I ADRES KLIENTA Zenon Koszorz Ground-Therm Sp z o.o. Ul. Stepowa 30 44-105 Gliwice
Strona1/7 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 01369/2015/D/AGST NAZWA I ADRES KLIENTA Zenon Koszorz Ground-Therm Sp z o.o. Ul. Stepowa 30 44-105 Gliwice
CHROMATOGRAFIA BARWNIKÓW ROŚLINNYCH
 POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 1 CHROMATOGRAFIA BARWNIKÓW ROŚLINNYCH I. Wiadomości teoretyczne W wielu dziedzinach nauki i techniki spotykamy się z problemem
POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 1 CHROMATOGRAFIA BARWNIKÓW ROŚLINNYCH I. Wiadomości teoretyczne W wielu dziedzinach nauki i techniki spotykamy się z problemem
Zakład Biologii Sanitarnej i Ekotechniki ĆWICZENIE 9 FITOROMEDIACJA I MIKROBIOLOGICZNA REMEDIACJA ŚRODOWISK SKAŻONYCH
 ĆWICZENIE 9 FITOROMEDIACJA I MIKROBIOLOGICZNA REMEDIACJA ŚRODOWISK SKAŻONYCH /Opiekun merytoryczny: dr hab. Teodora M. Traczewska, prof. nadzw. PWr modyfikacja: dr inż. Agnieszka Trusz-Zdybek i mgr inż.
ĆWICZENIE 9 FITOROMEDIACJA I MIKROBIOLOGICZNA REMEDIACJA ŚRODOWISK SKAŻONYCH /Opiekun merytoryczny: dr hab. Teodora M. Traczewska, prof. nadzw. PWr modyfikacja: dr inż. Agnieszka Trusz-Zdybek i mgr inż.
VII. Fizjologia bakterii - ćwiczenia praktyczne
 VII. Fizjologia bakterii - ćwiczenia praktyczne Ćwiczenie 1. Rodzaje pożywek i ich zastosowanie a. Podłoże stałe - proste Agar zwykły (AZ) b. Podłoża wzbogacone Agar z dodatkiem 5% odwłóknionej krwi baraniej
VII. Fizjologia bakterii - ćwiczenia praktyczne Ćwiczenie 1. Rodzaje pożywek i ich zastosowanie a. Podłoże stałe - proste Agar zwykły (AZ) b. Podłoża wzbogacone Agar z dodatkiem 5% odwłóknionej krwi baraniej
woda do 1000 ml ph=6,9-7,1. Po sterylizacji dodać nystatynę (końcowe stężenie ok. 50 μg/ml). Agar z wyciągiem glebowym i ekstraktem drożdżowym (YS)
 Ćwiczenie 1, 2, 3, 4 Skrining ze środowiska naturalnego: selekcja promieniowców zdolnych do produkcji antybiotyków. Testowanie zdolności do syntezy antybiotyków przez wyselekcjonowane szczepy promieniowców
Ćwiczenie 1, 2, 3, 4 Skrining ze środowiska naturalnego: selekcja promieniowców zdolnych do produkcji antybiotyków. Testowanie zdolności do syntezy antybiotyków przez wyselekcjonowane szczepy promieniowców
mgr Sławomir Sułowicz Katedra Mikrobiologii UŚ
 mgr Sławomir Sułowicz Katedra Mikrobiologii UŚ 1) Analiza sanitarna wody 2) Analiza mikrobiologiczna gleby 3) Analiza sanitarna powietrza 4) Charakterystyka szczepów bakterii opornych na antybiotyki, wyizolowanych
mgr Sławomir Sułowicz Katedra Mikrobiologii UŚ 1) Analiza sanitarna wody 2) Analiza mikrobiologiczna gleby 3) Analiza sanitarna powietrza 4) Charakterystyka szczepów bakterii opornych na antybiotyki, wyizolowanych
II. OZNACZANIE LICZBY BAKTERII Z GRUPY COLI I BAKTERII Z GRUPY COLI TYP FEKALNY METODĄ PŁYTKOWĄ W ŻYWNOŚCI I INNYCH PRODUKTACH wg PN-ISO 4832: 2007
 Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Temat: Żywność jako środowisko życia mikroorganizmów.
Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Temat: Żywność jako środowisko życia mikroorganizmów.
Laboratorium 3 Toksykologia żywności
 Laboratorium 3 Toksykologia żywności Literatura zalecana: Orzeł D., Biernat J. (red.) 2012. Wybrane zagadnienia z toksykologii żywności. Wydawnictwo Uniwersytetu Przyrodniczego we Wrocławiu. Wrocław. Str.:
Laboratorium 3 Toksykologia żywności Literatura zalecana: Orzeł D., Biernat J. (red.) 2012. Wybrane zagadnienia z toksykologii żywności. Wydawnictwo Uniwersytetu Przyrodniczego we Wrocławiu. Wrocław. Str.:
KARTA PRZEDMIOTU. (pieczęć wydziału) Z1-PU7 WYDANIE N1 Strona 8 z 9
 Załącznik Nr 5 do Zarz. Nr 33/11/12 KARTA PRZEDMIOTU (pieczęć wydziału) Z1-PU7 WYDANIE N1 Strona 8 z 9 1. Nazwa przedmiotu: Mikrobiologia ogólna 2. Kod przedmiotu: 3. Karta przedmiotu ważna od roku akademickiego:
Załącznik Nr 5 do Zarz. Nr 33/11/12 KARTA PRZEDMIOTU (pieczęć wydziału) Z1-PU7 WYDANIE N1 Strona 8 z 9 1. Nazwa przedmiotu: Mikrobiologia ogólna 2. Kod przedmiotu: 3. Karta przedmiotu ważna od roku akademickiego:
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Mikrobiologia Microbiology Kod Punktacja ECTS* 4 Koordynator dr Tomasz Bator Zespół dydaktyczny dr Tomasz Bator dr Magdalena Greczek-Stachura Opis kursu (cele kształcenia)
KARTA KURSU Nazwa Nazwa w j. ang. Mikrobiologia Microbiology Kod Punktacja ECTS* 4 Koordynator dr Tomasz Bator Zespół dydaktyczny dr Tomasz Bator dr Magdalena Greczek-Stachura Opis kursu (cele kształcenia)
SPRAWOZDANIE Z ĆWICZEŃ Z HIGIENY, TOKSYKOLOGII I BEZPIECZEŃSTWA ŻYWNOŚCI
 Data.. Imię, nazwisko, kierunek, grupa SPRAWOZDANIE Z ĆWICZEŃ Z HIGIENY, TOKSYKOLOGII I BEZPIECZEŃSTWA ŻYWNOŚCI OCENA JAKOŚCI WODY DO PICIA Ćwiczenie 1. Badanie właściwości fizykochemicznych wody Ćwiczenie
Data.. Imię, nazwisko, kierunek, grupa SPRAWOZDANIE Z ĆWICZEŃ Z HIGIENY, TOKSYKOLOGII I BEZPIECZEŃSTWA ŻYWNOŚCI OCENA JAKOŚCI WODY DO PICIA Ćwiczenie 1. Badanie właściwości fizykochemicznych wody Ćwiczenie
Instrukcja do ćwiczeń
 Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Instrukcja do ćwiczeń Temat: Woda jako
Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Instrukcja do ćwiczeń Temat: Woda jako
Biologia komórki. Skrypt do ćwiczeń dla studentów Bioinformatyki i Biologii Systemów. (część mikrobiologiczna)
 Biologia komórki Skrypt do ćwiczeń dla studentów Bioinformatyki i Biologii Systemów (część mikrobiologiczna) przygotowany przez zespół pracowników Zakładu Genetyki Bakterii INSTYTUT MIKROBIOLOGII WYDZIAŁ
Biologia komórki Skrypt do ćwiczeń dla studentów Bioinformatyki i Biologii Systemów (część mikrobiologiczna) przygotowany przez zespół pracowników Zakładu Genetyki Bakterii INSTYTUT MIKROBIOLOGII WYDZIAŁ
II. ODŻELAZIANIE LITERATURA. Zakres wiadomości obowiązujących do zaliczenia przed przystąpieniem do wykonania. ćwiczenia:
 II. ODŻELAZIANIE LITERATURA 1. Akty prawne: Aktualne rozporządzenie dotyczące jakości wody do picia i na potrzeby gospodarcze. 2. Chojnacki A.: Technologia wody i ścieków. PWN, Warszawa 1972. 3. Hermanowicz
II. ODŻELAZIANIE LITERATURA 1. Akty prawne: Aktualne rozporządzenie dotyczące jakości wody do picia i na potrzeby gospodarcze. 2. Chojnacki A.: Technologia wody i ścieków. PWN, Warszawa 1972. 3. Hermanowicz
TWARDOŚĆ WODY. Ca(HCO 3 ) HCl = CaCl 2 + 2H 2 O + 2CO 2. Mg(HCO 3 ) 2 + 2HCl = MgCl 2 + 2H 2 O + 2CO 2
 TWARDOŚĆ WODY Ćwiczenie 1. Oznaczanie twardości przemijającej wody wodociągowej Oznaczenie twardości przemijającej wody polega na miareczkowaniu określonej ilości badanej wody roztworem kwasu solnego o
TWARDOŚĆ WODY Ćwiczenie 1. Oznaczanie twardości przemijającej wody wodociągowej Oznaczenie twardości przemijającej wody polega na miareczkowaniu określonej ilości badanej wody roztworem kwasu solnego o
Laboratorium 1. Izolacja i wykrywanie trucizn cz. 1
 Laboratorium 1 Izolacja i wykrywanie trucizn cz. 1 Literatura zalecana: Bajguz A., Piotrowska A. 2005. Ćwiczenia z toksykologii środowiska. Wydawnictwo Uniwersytetu w Białymstoku, Białystok. Str. 15 17,
Laboratorium 1 Izolacja i wykrywanie trucizn cz. 1 Literatura zalecana: Bajguz A., Piotrowska A. 2005. Ćwiczenia z toksykologii środowiska. Wydawnictwo Uniwersytetu w Białymstoku, Białystok. Str. 15 17,
Zakład Biologii Sanitarnej i Ekotechniki ĆWICZENIE 3
 ĆWICZENIE 3 ROLA ORGANIZMÓW AUTOTROFICZNYCH W ŚRODOWISKU. DROBNOUSTROJE FOTO- I CHEMOSYNTETYZUJĄCE I ICH ROLA W INŻYNIERII ŚRODOWISKA /Opiekun merytoryczny: dr hab. Teodora M. Traczewska, prof. nadzw.
ĆWICZENIE 3 ROLA ORGANIZMÓW AUTOTROFICZNYCH W ŚRODOWISKU. DROBNOUSTROJE FOTO- I CHEMOSYNTETYZUJĄCE I ICH ROLA W INŻYNIERII ŚRODOWISKA /Opiekun merytoryczny: dr hab. Teodora M. Traczewska, prof. nadzw.
XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych. a. Candida albicans preparat z hodowli barwiony metoda Grama
 XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych a. Candida albicans preparat z hodowli barwiony metoda Grama Opis preparatu: b. Saccharomyces cerevisiae preparat z hodowli
XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych a. Candida albicans preparat z hodowli barwiony metoda Grama Opis preparatu: b. Saccharomyces cerevisiae preparat z hodowli
Zapisz równanie zachodzącej reakcji. Wskaż pierwiastki, związki chemiczne, substraty i produkty reakcji.
 test nr 2 Termin zaliczenia zadań: IIIa - 29 października 2015 III b - 28 października 2015 zad.1 Reakcja rozkładu tlenku rtęci(ii) 1. Narysuj schemat doświadczenia, sporządź spis użytych odczynników,
test nr 2 Termin zaliczenia zadań: IIIa - 29 października 2015 III b - 28 października 2015 zad.1 Reakcja rozkładu tlenku rtęci(ii) 1. Narysuj schemat doświadczenia, sporządź spis użytych odczynników,
RAPORT Z BADAŃ 164/Z/20110825/D/JOGA. Dostarczony materiał: próbki tworzyw sztucznych. Ilość próbek: 1. Rodzaj próbek: tworzywo
 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 164/Z/20110825/D/JOGA NAZWA I ADRES KLIENTA GROUND-Therm spółka z o.o. ul. Stepowa 30 44-105 Gliwice Tytuł zlecenia:
Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 164/Z/20110825/D/JOGA NAZWA I ADRES KLIENTA GROUND-Therm spółka z o.o. ul. Stepowa 30 44-105 Gliwice Tytuł zlecenia:
Ćwiczenie 8, 9, 10 Kontrola mikrobiologiczna środowiska pracy
 MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA Ćwiczenie 8, 9, 10 Kontrola mikrobiologiczna środowiska pracy liczba godzin 8 Badanie mikrobiologicznej czystości
MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA Ćwiczenie 8, 9, 10 Kontrola mikrobiologiczna środowiska pracy liczba godzin 8 Badanie mikrobiologicznej czystości
WYŻEJ OPISANA CZĘŚĆ DOŚWIADCZENIA JEST PRZYGOTOWANA EOZYNA ŻÓŁTAWA
 ĆWICZENIE 6 Gospodarka wodna Szybkość dyfuzji barwników organicznych w żelatynie Materiał: a/ odczynniki: 20 % roztwór żelatyny, tusz, 1-2 mm roztwory eozyny żółtawej, błękitu metylenowego, oranżu metylowego
ĆWICZENIE 6 Gospodarka wodna Szybkość dyfuzji barwników organicznych w żelatynie Materiał: a/ odczynniki: 20 % roztwór żelatyny, tusz, 1-2 mm roztwory eozyny żółtawej, błękitu metylenowego, oranżu metylowego
ĆWICZENIE 7 Transpiracja
 ĆWICZENIE 7 Transpiracja Oznaczanie rozwartości aparatów szparkowych metodą infiltracji a/ rośliny: liście trzykrotki b/ odczynniki: toluen, etanol, woda destylowana c/ inny sprzęt: zakraplacze, szalki
ĆWICZENIE 7 Transpiracja Oznaczanie rozwartości aparatów szparkowych metodą infiltracji a/ rośliny: liście trzykrotki b/ odczynniki: toluen, etanol, woda destylowana c/ inny sprzęt: zakraplacze, szalki
OZNACZANIE WŁAŚCIWOŚCI BUFOROWYCH WÓD
 OZNACZANIE WŁAŚCIWOŚCI BUFOROWYCH WÓD POWIERZCHNIOWYCH WPROWADZENIE Właściwości chemiczne wód występujących w przyrodzie odznaczają się dużym zróżnicowaniem. Zależą one między innymi od budowy geologicznej
OZNACZANIE WŁAŚCIWOŚCI BUFOROWYCH WÓD POWIERZCHNIOWYCH WPROWADZENIE Właściwości chemiczne wód występujących w przyrodzie odznaczają się dużym zróżnicowaniem. Zależą one między innymi od budowy geologicznej
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Podstawy mikrobiologii z immunologią Basics of microbiology and immunology Kod Punktacja ECTS* 4 Koordynator dr Tomasz Bator Zespół dydaktyczny dr hab. Magdalena Greczek-
KARTA KURSU Nazwa Nazwa w j. ang. Podstawy mikrobiologii z immunologią Basics of microbiology and immunology Kod Punktacja ECTS* 4 Koordynator dr Tomasz Bator Zespół dydaktyczny dr hab. Magdalena Greczek-
1.1 Reakcja trójchlorkiem antymonu
 ĆWICZENIE IV - WYKRYWANIE WITAMIN Odczynniki: - chloroform bezwodny, - bezwodnik kwasu octowego, - trójchlorek antymonu roztwór nasycony w chloroformie, - 1,3-dichlorohydryna gliceryny - żelazicyjanek
ĆWICZENIE IV - WYKRYWANIE WITAMIN Odczynniki: - chloroform bezwodny, - bezwodnik kwasu octowego, - trójchlorek antymonu roztwór nasycony w chloroformie, - 1,3-dichlorohydryna gliceryny - żelazicyjanek
Temat: Analiza sanitarna wody
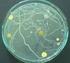 Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Diagnostyka mikrobiologiczna Analityka medyczna III rok Instrukcja do ćwiczeń Temat: Analiza sanitarna
Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Diagnostyka mikrobiologiczna Analityka medyczna III rok Instrukcja do ćwiczeń Temat: Analiza sanitarna
BIOCHEMICZNE ZAPOTRZEBOWANIE TLENU
 BIOCHEMICZNE ZAPOTRZEBOWANIE TLENU W procesach samooczyszczania wód zanieczyszczonych związkami organicznymi zachodzą procesy utleniania materii organicznej przy współudziale mikroorganizmów tlenowych.
BIOCHEMICZNE ZAPOTRZEBOWANIE TLENU W procesach samooczyszczania wód zanieczyszczonych związkami organicznymi zachodzą procesy utleniania materii organicznej przy współudziale mikroorganizmów tlenowych.
ĆWICZENIE 2 WSPÓŁOZNACZANIE WODOROTLENKU I WĘGLANÓW METODĄ WARDERA. DZIAŁ: Alkacymetria
 ĆWICZENIE 2 WSPÓŁOZNACZANIE WODOROTLENKU I WĘGLANÓW METODĄ WARDERA DZIAŁ: Alkacymetria ZAGADNIENIA Prawo zachowania masy i prawo działania mas. Stała równowagi reakcji. Stała dysocjacji, stopień dysocjacji
ĆWICZENIE 2 WSPÓŁOZNACZANIE WODOROTLENKU I WĘGLANÓW METODĄ WARDERA DZIAŁ: Alkacymetria ZAGADNIENIA Prawo zachowania masy i prawo działania mas. Stała równowagi reakcji. Stała dysocjacji, stopień dysocjacji
VIII. Pałeczki Gram-ujemne z rodziny Enterobacteriaceae
 VIII. Pałeczki Gram-ujemne z rodziny Enterobacteriaceae Ćwiczenie 1. Wykonanie preparatu mikroskopowego barwionego metodą Grama Opis preparatu: Ćwiczenie 2. Ocena wzrostu szczepów na podłożach stałych
VIII. Pałeczki Gram-ujemne z rodziny Enterobacteriaceae Ćwiczenie 1. Wykonanie preparatu mikroskopowego barwionego metodą Grama Opis preparatu: Ćwiczenie 2. Ocena wzrostu szczepów na podłożach stałych
Macie zdobyć informacje na temat chloroplastów. W tym celu przeczytajcie instrukcję, podzielcie się zadaniami i wykonajcie je.
 Barbara Jednorowicz - Plastydy organella charakterystyczne wyłącznie dla komórek roślinnych. Konspekt zajęć pozalekcyjnych z biologii Załącznik Instrukcja dla grupy I Macie zdobyć informacje na temat chloroplastów.
Barbara Jednorowicz - Plastydy organella charakterystyczne wyłącznie dla komórek roślinnych. Konspekt zajęć pozalekcyjnych z biologii Załącznik Instrukcja dla grupy I Macie zdobyć informacje na temat chloroplastów.
Ciągły proces otrzymywania bikarbonatu metodą Solvay a
 Ciągły proces otrzymywania bikarbonatu metodą Solvay a WYMAANIA 1. Podstawy teoretyczne procesu otrzymywania sody metodą Solvay a. 2. Schemat technologiczny metody Solvay a operacje jednostkowe.. Surowce
Ciągły proces otrzymywania bikarbonatu metodą Solvay a WYMAANIA 1. Podstawy teoretyczne procesu otrzymywania sody metodą Solvay a. 2. Schemat technologiczny metody Solvay a operacje jednostkowe.. Surowce
X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria
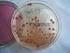 X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria Maczugowce (rodzaj Corynebacterium) Ćwiczenie 1. Wykonanie preparatu
X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria Maczugowce (rodzaj Corynebacterium) Ćwiczenie 1. Wykonanie preparatu
Inżynieria Środowiska I stopień Ogólnoakademicki. niestacjonarne. dr hab. inż. Lidia Dąbek, prof. PŚk. Dr hab. Lidia Dąbek, prof. PŚk.
 KARTA MODUŁU / KARTA PRZEDMIOTU Kod modułu Nazwa modułu Biologia i ekologia 1 Nazwa modułu w języku angielskim Biology and ecology Obowiązuje od roku akademickiego 2012/2013 A. USYTUOWANIE MODUŁU W SYSTEMIE
KARTA MODUŁU / KARTA PRZEDMIOTU Kod modułu Nazwa modułu Biologia i ekologia 1 Nazwa modułu w języku angielskim Biology and ecology Obowiązuje od roku akademickiego 2012/2013 A. USYTUOWANIE MODUŁU W SYSTEMIE
OSTRACODTOXKIT F Procedura testu
 OSTRACODTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI SKONCENTROWANYCH SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 PRZELAĆ ZAWARTOŚĆ 5 FIOLEK
OSTRACODTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI SKONCENTROWANYCH SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 PRZELAĆ ZAWARTOŚĆ 5 FIOLEK
Komórka organizmy beztkankowe
 Grupa a Komórka organizmy beztkankowe Poniższy test składa się z 12 zadań. Przy każdym poleceniu podano liczbę punktów możliwą do uzyskania za prawidłową odpowiedź. Za rozwiązanie całego testu możesz otrzymać
Grupa a Komórka organizmy beztkankowe Poniższy test składa się z 12 zadań. Przy każdym poleceniu podano liczbę punktów możliwą do uzyskania za prawidłową odpowiedź. Za rozwiązanie całego testu możesz otrzymać
II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne. Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową
 II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową Zasada metody: Krążki bibułowe nasycone odpowiednimi ilościami antybiotyków
II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową Zasada metody: Krążki bibułowe nasycone odpowiednimi ilościami antybiotyków
SYLABUS. Wydział Biologiczno - Rolniczy. Katedra Biotechnologii i Mikrobiologii
 SYLABUS 1.1. PODSTAWOWE INFORMACJE O PRZEDMIOCIE/MODULE Nazwa przedmiotu/ modułu Mikrobiologia Kod przedmiotu/ modułu* Wydział (nazwa jednostki prowadzącej kierunek) Nazwa jednostki realizującej przedmiot
SYLABUS 1.1. PODSTAWOWE INFORMACJE O PRZEDMIOCIE/MODULE Nazwa przedmiotu/ modułu Mikrobiologia Kod przedmiotu/ modułu* Wydział (nazwa jednostki prowadzącej kierunek) Nazwa jednostki realizującej przedmiot
Ćwiczenie 11. Temat: Wskaźniki higieniczne żywności.
 Ćwiczenie 11 Temat: Wskaźniki higieniczne żywności. Wskaźniki higieniczne żywności są to grupy bakterii dostające się do żywności w wyniku niewłaściwej higieny produkcji i braku higieny osobistej pracowników.
Ćwiczenie 11 Temat: Wskaźniki higieniczne żywności. Wskaźniki higieniczne żywności są to grupy bakterii dostające się do żywności w wyniku niewłaściwej higieny produkcji i braku higieny osobistej pracowników.
RAPORT Z BADAŃ REALIZOWANYCH W RAMACH OCENY STĘŻENIA BIOAEROZOLU ZANIECZYSZCZAJĄCEGO POWIETRZE NA PODSTAWIE LICZEBNOŚCI WYBRANYCH GRUP DROBNOUSTROJÓW
 Mysłowice, 22.03.2016 r. RAPORT Z BADAŃ REALIZOWANYCH W RAMACH OCENY STĘŻENIA BIOAEROZOLU ZANIECZYSZCZAJĄCEGO POWIETRZE NA PODSTAWIE LICZEBNOŚCI WYBRANYCH GRUP DROBNOUSTROJÓW Zleceniodawca: Stowarzyszenie
Mysłowice, 22.03.2016 r. RAPORT Z BADAŃ REALIZOWANYCH W RAMACH OCENY STĘŻENIA BIOAEROZOLU ZANIECZYSZCZAJĄCEGO POWIETRZE NA PODSTAWIE LICZEBNOŚCI WYBRANYCH GRUP DROBNOUSTROJÓW Zleceniodawca: Stowarzyszenie
Ćwiczenie 1. Technika ważenia oraz wyznaczanie błędów pomiarowych. Ćwiczenie 2. Sprawdzanie pojemności pipety
 II. Wagi i ważenie. Roztwory. Emulsje i koloidy Zagadnienia Rodzaje wag laboratoryjnych i technika ważenia Niepewność pomiarowa. Błąd względny i bezwzględny Roztwory właściwe Stężenie procentowe i molowe.
II. Wagi i ważenie. Roztwory. Emulsje i koloidy Zagadnienia Rodzaje wag laboratoryjnych i technika ważenia Niepewność pomiarowa. Błąd względny i bezwzględny Roztwory właściwe Stężenie procentowe i molowe.
ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1)
 ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1) z dnia 6 listopada 2002 r. w sprawie metodyk referencyjnych badania stopnia biodegradacji substancji powierzchniowoczynnych zawartych w produktach, których stosowanie
ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1) z dnia 6 listopada 2002 r. w sprawie metodyk referencyjnych badania stopnia biodegradacji substancji powierzchniowoczynnych zawartych w produktach, których stosowanie
ZASADY BADAŃ BAKTERIOLOGICZNYCH
 ZASADY BADAŃ BAKTERIOLOGICZNYCH Joanna Kądzielska Katedra Mikrobiologii Lekarskiej Warszawski Uniwersytet Medyczny METODY HODOWLI BAKTERII METODY MIKROSKOPOWE MORFOLOGIA BAKTERII TOK BADANIA DIAGNOSTYCZNEGO
ZASADY BADAŃ BAKTERIOLOGICZNYCH Joanna Kądzielska Katedra Mikrobiologii Lekarskiej Warszawski Uniwersytet Medyczny METODY HODOWLI BAKTERII METODY MIKROSKOPOWE MORFOLOGIA BAKTERII TOK BADANIA DIAGNOSTYCZNEGO
Protokoły do zajęć praktycznych z mikrobiologii ogólnej i żywności dla studentów kierunku: Dietetyka
 Protokoły do zajęć praktycznych z mikrobiologii ogólnej i żywności dla studentów kierunku: Dietetyka Protokół I, zajęcia praktyczne 1. Demonstracja wykonania preparatu barwionego metodą Grama (wykonuje
Protokoły do zajęć praktycznych z mikrobiologii ogólnej i żywności dla studentów kierunku: Dietetyka Protokół I, zajęcia praktyczne 1. Demonstracja wykonania preparatu barwionego metodą Grama (wykonuje
GOSPODARKA ODPADAMI. Oznaczanie metodą kolumnową wskaźników zanieczyszczeń wymywanych z odpadów
 GOSPODARKA ODPADAMI Ćwiczenie nr 5 Oznaczanie metodą kolumnową wskaźników zanieczyszczeń wymywanych z odpadów I. WPROWADZENIE Nieodpowiednie składowanie odpadków na wysypiskach stwarza możliwość wymywania
GOSPODARKA ODPADAMI Ćwiczenie nr 5 Oznaczanie metodą kolumnową wskaźników zanieczyszczeń wymywanych z odpadów I. WPROWADZENIE Nieodpowiednie składowanie odpadków na wysypiskach stwarza możliwość wymywania
Izolacja barwników roślinnych.
 SCENARIUSZ ZAJĘĆ KOŁA NAUKOWEGO BIOLOGICZNO - CHEMICZNEGO prowadzonego w ramach projektu Uczeń OnLine 1. Autor: Maria Szamraj 2. Grupa docelowa: Gimnazjum nr 2 w Bydgoszczy 3. Liczba godzin: 3 godziny
SCENARIUSZ ZAJĘĆ KOŁA NAUKOWEGO BIOLOGICZNO - CHEMICZNEGO prowadzonego w ramach projektu Uczeń OnLine 1. Autor: Maria Szamraj 2. Grupa docelowa: Gimnazjum nr 2 w Bydgoszczy 3. Liczba godzin: 3 godziny
GOSPODARKA ODPADAMI. Oznaczanie metodą kolumnową wskaźników zanieczyszczeń wymywanych z odpadów
 GOSPODARKA ODPADAMI Ćwiczenie nr 5 Oznaczanie metodą kolumnową wskaźników zanieczyszczeń wymywanych z odpadów I. WPROWADZENIE: Nieodpowiednie składowanie odpadków na wysypiskach stwarza możliwość wymywania
GOSPODARKA ODPADAMI Ćwiczenie nr 5 Oznaczanie metodą kolumnową wskaźników zanieczyszczeń wymywanych z odpadów I. WPROWADZENIE: Nieodpowiednie składowanie odpadków na wysypiskach stwarza możliwość wymywania
KARTA KURSU. Mikroorganizmy środowisk wodnych. Microorganisms of the aquatic environments. Kod Punktacja ECTS* 2
 Załącznik nr 4 do Zarządzenia Nr.. KARTA KURSU Nazwa Nazwa w j. ang. Mikroorganizmy środowisk wodnych Microorganisms of the aquatic environments Kod Punktacja ECTS* 2 Koordynator Dr Grzegorz Migdałek Zespół
Załącznik nr 4 do Zarządzenia Nr.. KARTA KURSU Nazwa Nazwa w j. ang. Mikroorganizmy środowisk wodnych Microorganisms of the aquatic environments Kod Punktacja ECTS* 2 Koordynator Dr Grzegorz Migdałek Zespół
FORMULARZ CENOWY. Data:... Nazwa wykonawcy:... Siedziba wykonawcy:... Przedstawia zestawienie cenowe dla oferowanego przedmiotu zamówienia:
 1/PN/2013 Załącznik nr 2 B FORMULARZ CENOWY Data:... Nazwa wykonawcy:...... Siedziba wykonawcy:...... Przedstawia zestawienie cenowe dla oferowanego przedmiotu zamówienia: Lp. Rodzaj Norma Ilość Cena jednostkowa
1/PN/2013 Załącznik nr 2 B FORMULARZ CENOWY Data:... Nazwa wykonawcy:...... Siedziba wykonawcy:...... Przedstawia zestawienie cenowe dla oferowanego przedmiotu zamówienia: Lp. Rodzaj Norma Ilość Cena jednostkowa
KATEDRA INŻYNIERII CHEMICZNEJ I PROCESOWEJ INSTRUKCJE DO ĆWICZEŃ LABORATORYJNYCH LABORATORIUM INŻYNIERII CHEMICZNEJ, PROCESOWEJ I BIOPROCESOWEJ
 KATEDRA INŻYNIERII CHEMICZNEJ I PROCESOWEJ INSTRUKCJE DO ĆWICZEŃ LABORATORYJNYCH LABORATORIUM INŻYNIERII CHEMICZNEJ, PROCESOWEJ I BIOPROCESOWEJ Absorpcja Osoba odiedzialna: Donata Konopacka - Łyskawa dańsk,
KATEDRA INŻYNIERII CHEMICZNEJ I PROCESOWEJ INSTRUKCJE DO ĆWICZEŃ LABORATORYJNYCH LABORATORIUM INŻYNIERII CHEMICZNEJ, PROCESOWEJ I BIOPROCESOWEJ Absorpcja Osoba odiedzialna: Donata Konopacka - Łyskawa dańsk,
Projekt Uchylamy rąbka tajemnicy mikroświata
 Projekt Uchylamy rąbka tajemnicy mikroświata Zajęcia realizowane metodą przewodniego tekstu Cel główny: Budowa, funkcje i różnorodność komórek organizmów. Treści kształcenia zajęć interdyscyplinarnych:
Projekt Uchylamy rąbka tajemnicy mikroświata Zajęcia realizowane metodą przewodniego tekstu Cel główny: Budowa, funkcje i różnorodność komórek organizmów. Treści kształcenia zajęć interdyscyplinarnych:
WYZNACZANIE WSPÓŁCZYNNIKA ZAŁAMANIA ŚWIATŁA METODĄ SZPILEK I ZA POMOCĄ MIKROSKOPU
 WYZNACZANIE WSPÓŁCZYNNIKA ZAŁAMANIA ŚWIATŁA METODĄ SZPILEK I ZA POMOCĄ MIKROSKOPU Cel ćwiczenia: 1. Zapoznanie z budową i zasadą działania mikroskopu optycznego. 2. Wyznaczenie współczynnika załamania
WYZNACZANIE WSPÓŁCZYNNIKA ZAŁAMANIA ŚWIATŁA METODĄ SZPILEK I ZA POMOCĄ MIKROSKOPU Cel ćwiczenia: 1. Zapoznanie z budową i zasadą działania mikroskopu optycznego. 2. Wyznaczenie współczynnika załamania
ĆWICZENIE I - BIAŁKA. Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi.
 ĆWICZENIE I - BIAŁKA Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi. Odczynniki: - wodny 1% roztwór siarczanu(vi) miedzi(ii), - 10% wodny
ĆWICZENIE I - BIAŁKA Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi. Odczynniki: - wodny 1% roztwór siarczanu(vi) miedzi(ii), - 10% wodny
Odczyn roztworu Skala ph. Piotr Zawadzki i Aleksandra Jarocka
 Odczyn roztworu Skala ph Piotr Zawadzki i Aleksandra Jarocka Wskaźniki a odczyn Ph Wskaźniki, to związki, które w zależności od odczynu roztworu zmieniają barwę. Najczęściej spotykanymi w naszym otoczeniu
Odczyn roztworu Skala ph Piotr Zawadzki i Aleksandra Jarocka Wskaźniki a odczyn Ph Wskaźniki, to związki, które w zależności od odczynu roztworu zmieniają barwę. Najczęściej spotykanymi w naszym otoczeniu
Ćwiczenie 14. Technologie z udziałem bakterii kwasu mlekowego: wykorzystanie fermentacji mlekowej, masłowej i propionowej
 Ćwiczenie 14. Technologie z udziałem bakterii kwasu mlekowego: wykorzystanie fermentacji mlekowej, masłowej i propionowej Cel ćwiczenia: Analiza mikrobiologiczno-biochemiczna fermentowanych produktów spożywczych.
Ćwiczenie 14. Technologie z udziałem bakterii kwasu mlekowego: wykorzystanie fermentacji mlekowej, masłowej i propionowej Cel ćwiczenia: Analiza mikrobiologiczno-biochemiczna fermentowanych produktów spożywczych.
Ćwiczenie 9. Temat: Metody ilościowe w mikrobiologicznych badaniach żywności Cz.1
 Ćwiczenie 9 Temat: Metody ilościowe w mikrobiologicznych badaniach żywności Cz.1 Pobieranie prób do badań Próbka pobrana do badań mikrobiologicznych powinna być reprezentatywna tzn. powinna odzwierciedlać
Ćwiczenie 9 Temat: Metody ilościowe w mikrobiologicznych badaniach żywności Cz.1 Pobieranie prób do badań Próbka pobrana do badań mikrobiologicznych powinna być reprezentatywna tzn. powinna odzwierciedlać
Zakład Biologii Sanitarnej i Ekotechniki ĆWICZENIE 2 BUDOWA I FUNKCJE ENZYMÓW. ZASTOSOWANIE BADAŃ ENZYMATYCZNYCH W INŻYNIERII ŚRODOWISKA.
 ĆWICZENIE 2 BUDOWA I FUNKCJE ENZYMÓW. ZASTOSOWANIE BADAŃ ENZYMATYCZNYCH W INŻYNIERII ŚRODOWISKA. /Opiekun merytoryczny: dr hab. Teodora M. Traczewska, prof. nadzw. PWr modyfikacja: dr inż. Agnieszka Trusz-Zdybek
ĆWICZENIE 2 BUDOWA I FUNKCJE ENZYMÓW. ZASTOSOWANIE BADAŃ ENZYMATYCZNYCH W INŻYNIERII ŚRODOWISKA. /Opiekun merytoryczny: dr hab. Teodora M. Traczewska, prof. nadzw. PWr modyfikacja: dr inż. Agnieszka Trusz-Zdybek
ĆWICZENIE NR 3 BADANIE MIKROBIOLOGICZNEGO UTLENIENIA AMONIAKU DO AZOTYNÓW ZA POMOCĄ BAKTERII NITROSOMONAS sp.
 ĆWICZENIE NR 3 BADANIE MIKROBIOLOGICZNEGO UTLENIENIA AMONIAKU DO AZOTYNÓW ZA POMOCĄ BAKTERII NITROSOMONAS sp. Uwaga: Ze względu na laboratoryjny charakter zajęć oraz kontakt z materiałem biologicznym,
ĆWICZENIE NR 3 BADANIE MIKROBIOLOGICZNEGO UTLENIENIA AMONIAKU DO AZOTYNÓW ZA POMOCĄ BAKTERII NITROSOMONAS sp. Uwaga: Ze względu na laboratoryjny charakter zajęć oraz kontakt z materiałem biologicznym,
BIOTECHNOLOGIA OGÓLNA
 BIOTECHNOLOGIA OGÓLNA 1. 2. 3. 4. 5. Ogólne podstawy biologicznych metod oczyszczania ścieków. Ścieki i ich rodzaje. Stosowane metody analityczne. Substancje biogenne w ściekach. Tlenowe procesy przemiany
BIOTECHNOLOGIA OGÓLNA 1. 2. 3. 4. 5. Ogólne podstawy biologicznych metod oczyszczania ścieków. Ścieki i ich rodzaje. Stosowane metody analityczne. Substancje biogenne w ściekach. Tlenowe procesy przemiany
ĆWICZENIE 3. Cukry mono i disacharydy
 ĆWICZENIE 3 Cukry mono i disacharydy Reakcja ogólna na węglowodany (Reakcja Molischa) 1 ml 1% roztworu glukozy 1 ml 1% roztworu fruktozy 1 ml 1% roztworu sacharozy 1 ml 1% roztworu skrobi 1 ml wody destylowanej
ĆWICZENIE 3 Cukry mono i disacharydy Reakcja ogólna na węglowodany (Reakcja Molischa) 1 ml 1% roztworu glukozy 1 ml 1% roztworu fruktozy 1 ml 1% roztworu sacharozy 1 ml 1% roztworu skrobi 1 ml wody destylowanej
Inżynieria Środowiska I stopień Ogólnoakademicki. stacjonarne. Katedra Inżynierii i Ochrony Środowiska. Dr hab. Lidia Dąbek, prof. PŚk.
 KARTA MODUŁU / KARTA PRZEDMIOTU Kod modułu Nazwa modułu Biologia i ekologia Nazwa modułu w języku angielskim Biology and ecology Obowiązuje od roku akademickiego 2012/2013 A. USYTUOWANIE MODUŁU W SYSTEMIE
KARTA MODUŁU / KARTA PRZEDMIOTU Kod modułu Nazwa modułu Biologia i ekologia Nazwa modułu w języku angielskim Biology and ecology Obowiązuje od roku akademickiego 2012/2013 A. USYTUOWANIE MODUŁU W SYSTEMIE
Systemy Ochrony Powietrza Ćwiczenia Laboratoryjne
 POLITECHNIKA POZNAŃSKA INSTYTUT INŻYNIERII ŚRODOWISKA PROWADZĄCY: mgr inż. Łukasz Amanowicz Systemy Ochrony Powietrza Ćwiczenia Laboratoryjne 3 TEMAT ĆWICZENIA: Badanie składu pyłu za pomocą mikroskopu
POLITECHNIKA POZNAŃSKA INSTYTUT INŻYNIERII ŚRODOWISKA PROWADZĄCY: mgr inż. Łukasz Amanowicz Systemy Ochrony Powietrza Ćwiczenia Laboratoryjne 3 TEMAT ĆWICZENIA: Badanie składu pyłu za pomocą mikroskopu
1. Demonstracja preparatów bakteryjnych barwionych metodą negatywną ukazujących kształty komórek bakteryjnych.
 Ćwiczenie 1. Mikrobiologia ogólna - Budowa komórki bakteryjnej. Metody barwienia preparatów bakteryjnych. Wzrost drobnoustrojów w warunkach laboratoryjnych. Uzyskiwanie czystej hodowli. Identyfikowanie
Ćwiczenie 1. Mikrobiologia ogólna - Budowa komórki bakteryjnej. Metody barwienia preparatów bakteryjnych. Wzrost drobnoustrojów w warunkach laboratoryjnych. Uzyskiwanie czystej hodowli. Identyfikowanie
STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI
 Ćwiczenie 8 Semestr 2 STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI Obowiązujące zagadnienia: Stężenie jonów wodorowych: ph, poh, iloczyn jonowy wody, obliczenia rachunkowe, wskaźniki
Ćwiczenie 8 Semestr 2 STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI Obowiązujące zagadnienia: Stężenie jonów wodorowych: ph, poh, iloczyn jonowy wody, obliczenia rachunkowe, wskaźniki
Mikrobiologia II rok Towaroznawstwo i Dietetyka. Ćwiczenie 10
 Część teoretyczna: Mikrobiologia II rok Towaroznawstwo i Dietetyka Ćwiczenie 10 I. MIKROFLORA WODY Mikroflora autochtoniczna to drobnoustroje naturalnie bytujące i rozmnażające się w środowisku wodnym.
Część teoretyczna: Mikrobiologia II rok Towaroznawstwo i Dietetyka Ćwiczenie 10 I. MIKROFLORA WODY Mikroflora autochtoniczna to drobnoustroje naturalnie bytujące i rozmnażające się w środowisku wodnym.
Temat 1: Morfologia komórki i kolonii. Barwienie pozytywne proste i barwienie negatywne
 Temat 1: Morfologia komórki i kolonii. Barwienie pozytywne proste i barwienie negatywne Literatura: 1. Kocwowa E.: Ćwiczenia z mikrobiologii ogólnej dla wyższych szkół technicznych. PWN 1984, str. 32-49
Temat 1: Morfologia komórki i kolonii. Barwienie pozytywne proste i barwienie negatywne Literatura: 1. Kocwowa E.: Ćwiczenia z mikrobiologii ogólnej dla wyższych szkół technicznych. PWN 1984, str. 32-49
Zakład Technologii Wody, Ścieków i Odpadów
 Zakład Technologii Wody, Ścieków i Odpadów Katedra Inżynierii Sanitarnej. Wydział Budownictwa i Architektury Semestr zimowy 2017/18 harmonogram zajęć przedmiotów z formą zajęć laboratoryjnych Chemia Budowlana
Zakład Technologii Wody, Ścieków i Odpadów Katedra Inżynierii Sanitarnej. Wydział Budownictwa i Architektury Semestr zimowy 2017/18 harmonogram zajęć przedmiotów z formą zajęć laboratoryjnych Chemia Budowlana
Hodowlą nazywamy masę drobnoustrojów wyrosłych na podłożu o dowolnej konsystencji.
 Wzrost mikroorganizmów rozumieć można jako: 1. Wzrost masy i rozmiarów pojedynczego osobnika, tj. komórki 2. Wzrost biomasy i liczebności komórek w środowisku, tj. wzrost liczebności populacji Hodowlą
Wzrost mikroorganizmów rozumieć można jako: 1. Wzrost masy i rozmiarów pojedynczego osobnika, tj. komórki 2. Wzrost biomasy i liczebności komórek w środowisku, tj. wzrost liczebności populacji Hodowlą
Ćwiczenie 4. Identyfikacja wybranych cukrów w oparciu o niektóre reakcje charakterystyczne
 Klasyczna Analiza Jakościowa Organiczna, Ćw. 4 - Identyfikacja wybranych cukrów Ćwiczenie 4 Identyfikacja wybranych cukrów w oparciu o niektóre reakcje charakterystyczne Zagadnienia teoretyczne: 1. Budowa
Klasyczna Analiza Jakościowa Organiczna, Ćw. 4 - Identyfikacja wybranych cukrów Ćwiczenie 4 Identyfikacja wybranych cukrów w oparciu o niektóre reakcje charakterystyczne Zagadnienia teoretyczne: 1. Budowa
ĆWICZENIE 2 KONDUKTOMETRIA
 ĆWICZENIE 2 KONDUKTOMETRIA 1. Oznaczanie słabych kwasów w sokach i syropach owocowych metodą miareczkowania konduktometrycznego Celem ćwiczenia jest ilościowe oznaczenie zawartości słabych kwasów w sokach
ĆWICZENIE 2 KONDUKTOMETRIA 1. Oznaczanie słabych kwasów w sokach i syropach owocowych metodą miareczkowania konduktometrycznego Celem ćwiczenia jest ilościowe oznaczenie zawartości słabych kwasów w sokach
CHROMATOGRAFIA ADSORPCYJNA I PODZIAŁOWA. 1. Rozdział barwników roślinnych metodą chromatografii adsorpcyjnej (techniką kolumnową)
 Ćwiczenie nr 7 CHROMATOGRAFIA ADSORPCYJNA I PODZIAŁOWA 1. Rozdział barwników roślinnych metodą chromatografii adsorpcyjnej (techniką kolumnową) Zasada: Barwniki roślinne charakteryzują się różnym powinowactwem
Ćwiczenie nr 7 CHROMATOGRAFIA ADSORPCYJNA I PODZIAŁOWA 1. Rozdział barwników roślinnych metodą chromatografii adsorpcyjnej (techniką kolumnową) Zasada: Barwniki roślinne charakteryzują się różnym powinowactwem
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Izoterma rozpuszczalności w układzie trójskładnikowym
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Izoterma rozpuszczalności w układzie trójskładnikowym ćwiczenie nr 28 Zakres zagadnień obowiązujących do ćwiczenia 1. Stan równowagi układu i rodzaje równowag
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Izoterma rozpuszczalności w układzie trójskładnikowym ćwiczenie nr 28 Zakres zagadnień obowiązujących do ćwiczenia 1. Stan równowagi układu i rodzaje równowag
Oznaczanie SO 2 w powietrzu atmosferycznym
 Ćwiczenie 6 Oznaczanie SO w powietrzu atmosferycznym Dwutlenek siarki bezwodnik kwasu siarkowego jest najbardziej rozpowszechnionym zanieczyszczeniem gazowym, występującym w powietrzu atmosferycznym. Głównym
Ćwiczenie 6 Oznaczanie SO w powietrzu atmosferycznym Dwutlenek siarki bezwodnik kwasu siarkowego jest najbardziej rozpowszechnionym zanieczyszczeniem gazowym, występującym w powietrzu atmosferycznym. Głównym
OCHRONA ŚRODOWISKA W ENERGETYCE NEUTRALIZACJA ŚCIEKÓW
 KIiChŚ OCHRONA ŚRODOWISKA W ENERGETYCE NEUTRALIZACJA ŚCIEKÓW Ćwiczenie nr 2 I WPROWADZENIE Reakcja zobojętniania (neutralizacji) - jest to proces chemiczny, mający na celu doprowadzenie odczynu cieczy
KIiChŚ OCHRONA ŚRODOWISKA W ENERGETYCE NEUTRALIZACJA ŚCIEKÓW Ćwiczenie nr 2 I WPROWADZENIE Reakcja zobojętniania (neutralizacji) - jest to proces chemiczny, mający na celu doprowadzenie odczynu cieczy
WYMAGANIA EDUKACYJNE Z BIOLOGII KLASA 5 DOBRY. DZIAŁ 1. Biologia jako nauka ( 4godzin)
 WYMAGANIA EDUKACYJNE Z BIOLOGII KLASA 5 DOPUSZCZAJĄCY DOSTATECZNY DOBRY BARDZO DOBRY CELUJĄCY DZIAŁ 1. Biologia jako nauka ( 4godzin) wskazuje biologię jako naukę o organizmach wymienia czynności życiowe
WYMAGANIA EDUKACYJNE Z BIOLOGII KLASA 5 DOPUSZCZAJĄCY DOSTATECZNY DOBRY BARDZO DOBRY CELUJĄCY DZIAŁ 1. Biologia jako nauka ( 4godzin) wskazuje biologię jako naukę o organizmach wymienia czynności życiowe
OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE
 OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE WPROWADZENIE Przyswajalność pierwiastków przez rośliny zależy od procesów zachodzących między fazą stałą i ciekłą gleby oraz korzeniami roślin. Pod względem stopnia
OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE WPROWADZENIE Przyswajalność pierwiastków przez rośliny zależy od procesów zachodzących między fazą stałą i ciekłą gleby oraz korzeniami roślin. Pod względem stopnia
I. Pobieranie próbek. Lp. Wykaz czynności Wielkość współczynnika
 Koszty i wykaz badań wykonywanych w Wojewódzkim Inspektoracie Ochrony Środowiska w Poznaniu 1. Stawka podstawowa wynosi 40,41 zł. 2. Wyliczenie kosztów usługi następuje w sposób następujący: koszt usługi
Koszty i wykaz badań wykonywanych w Wojewódzkim Inspektoracie Ochrony Środowiska w Poznaniu 1. Stawka podstawowa wynosi 40,41 zł. 2. Wyliczenie kosztów usługi następuje w sposób następujący: koszt usługi
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2018 CZĘŚĆ PRAKTYCZNA
 Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2018 Nazwa kwalifikacji: Wykonywanie badań analitycznych Oznaczenie kwalifikacji: A.60 Numer zadania: 02
Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2018 Nazwa kwalifikacji: Wykonywanie badań analitycznych Oznaczenie kwalifikacji: A.60 Numer zadania: 02
Obserwacje, doświadczenia, hodowle - aktywny uczeń na lekcjach biologii w klasie piątej
 Obserwacje, doświadczenia, hodowle - aktywny uczeń na lekcjach biologii w klasie piątej Anna Kimak-Cysewska 2018 Samodzielne przeprowadzenie nawet bardzo prostego doświadczenia lub obserwacji dostarcza
Obserwacje, doświadczenia, hodowle - aktywny uczeń na lekcjach biologii w klasie piątej Anna Kimak-Cysewska 2018 Samodzielne przeprowadzenie nawet bardzo prostego doświadczenia lub obserwacji dostarcza
Koncepcja pedagogiczna dla kształcenia zawodowego
 Koncepcja pedagogiczna dla kształcenia zawodowego Szkoła Zespół Szkół Chemicznych Włocławek (PL) Obszar Kształcenie zawodowe Kierunki kształcenia zawodowego Technik ochrony środowiska Obszar działań Praca
Koncepcja pedagogiczna dla kształcenia zawodowego Szkoła Zespół Szkół Chemicznych Włocławek (PL) Obszar Kształcenie zawodowe Kierunki kształcenia zawodowego Technik ochrony środowiska Obszar działań Praca
Z BADAŃ ODDZIAŁYWANIA WYBRANYCH MIKROORGANIZMÓW NA KOMPOZYTY PP Z BIOCYDEM SEANTEX
 SPRAWOZDANIE Z BADAŃ ODDZIAŁYWANIA WYBRANYCH MIKROORGANIZMÓW NA KOMPOZYTY PP Z BIOCYDEM SEANTEX /zlecenie 514010/ wykonane w WOJSKOWYM INSTYTUCIE CHEMII I RADIOMETRII w Warszaawie 1. Materiały i metody
SPRAWOZDANIE Z BADAŃ ODDZIAŁYWANIA WYBRANYCH MIKROORGANIZMÓW NA KOMPOZYTY PP Z BIOCYDEM SEANTEX /zlecenie 514010/ wykonane w WOJSKOWYM INSTYTUCIE CHEMII I RADIOMETRII w Warszaawie 1. Materiały i metody
ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW
 UNIWERSYTET MARII CURIE-SKŁODOWSKIEJ WYDZIAŁ BIOLOGII I BIOTECHNOLOGII ZAKŁAD BIOLOGII MOLEKULARNEJ ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW dla studentów I roku II 0 biotechnologii medycznej
UNIWERSYTET MARII CURIE-SKŁODOWSKIEJ WYDZIAŁ BIOLOGII I BIOTECHNOLOGII ZAKŁAD BIOLOGII MOLEKULARNEJ ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW dla studentów I roku II 0 biotechnologii medycznej
1 Zakład Mikrobiologii UJK. Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku biologia
 1 Zakład Mikrobiologii UJK Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku biologia 2 Zakład Mikrobiologii UJK Organizacja zajęć laboratoryjnych
1 Zakład Mikrobiologii UJK Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku biologia 2 Zakład Mikrobiologii UJK Organizacja zajęć laboratoryjnych
PRZEWODNIK PO PRZEDMIOCIE
 Nazwa przedmiotu: Biologia I Biology I Kierunek: Inżynieria Środowiska Kod przedmiotu: Rodzaj przedmiotu: Poziom kształcenia: Semestr: II podstawowy, moduł 3 I stopnia Rodzaj zajęć: wykład, laboratorium
Nazwa przedmiotu: Biologia I Biology I Kierunek: Inżynieria Środowiska Kod przedmiotu: Rodzaj przedmiotu: Poziom kształcenia: Semestr: II podstawowy, moduł 3 I stopnia Rodzaj zajęć: wykład, laboratorium
OPRACOWAŁA : Klaudia Barczyńska
 OPRACOWAŁA : Klaudia Barczyńska 1 Przedmiotem normy są metody oznaczania zawartości chlorofilu w organizmach zielonych zasiedlających wody powierzchniowe. Zawartość chlorofilu a jest wskaźnikiem biomasy
OPRACOWAŁA : Klaudia Barczyńska 1 Przedmiotem normy są metody oznaczania zawartości chlorofilu w organizmach zielonych zasiedlających wody powierzchniowe. Zawartość chlorofilu a jest wskaźnikiem biomasy
Równowagi w roztworach elektrolitów
 Do doświadczeń stosować suche szkło i sprzęt laboratoryjny. Po użyciu szkło i sprzęt laboratoryjny należy wstępnie opłukać, a po zakończonych eksperymentach dokładnie umyć (przy użyciu detergentów) i pozostawić
Do doświadczeń stosować suche szkło i sprzęt laboratoryjny. Po użyciu szkło i sprzęt laboratoryjny należy wstępnie opłukać, a po zakończonych eksperymentach dokładnie umyć (przy użyciu detergentów) i pozostawić
VI. ZMIĘKCZANIE WODY METODĄ JONOWYMIENNĄ
 I. ZMIĘKCZANIE WODY METODĄ JONOWYMIENNĄ LITERATURA 1. Akty prawne: Aktualne rozporządzenie dotyczące jakości wody do picia i na potrzeby gospodarcze. 2. Chojnacki A.: Technologia wody i ścieków. PWN, Warszawa
I. ZMIĘKCZANIE WODY METODĄ JONOWYMIENNĄ LITERATURA 1. Akty prawne: Aktualne rozporządzenie dotyczące jakości wody do picia i na potrzeby gospodarcze. 2. Chojnacki A.: Technologia wody i ścieków. PWN, Warszawa
