Wykaz ważniejszych skrótów występujących w tekście
|
|
|
- Anna Jaworska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Wykaz ważniejszych skrótów występujących w tekście ABCDE Airway, Breathing, Circulation, Disability, Exposure drogi oddechowe, oddychanie, krążenie, ocena neurologiczna, ocena kliniczna ACD-CPR Active Compression-Decompression Cardiopulmonary Resuscitation RKO za pomocą aktywnej kompresji i dekompresji klatki piersiowej ACS Acute Coronary Syndrome ostry zespół wieńcowy (OZW) AED Automated External Defibrillator automatyczny defibrylator zewnętrzny AF Atrial Fibrillation migotanie przedsionków ALS Advanced Life Support Course for Providers Specjalistyczne zabiegi resuscytacyjne u osób dorosłych (kurs certyfikowany przez ERC) AMI Acute Myocardial Infarction ostry zawał mięśnia sercowego ASA Acetylsalicylic Acid kwas acetylosalicylowy AVNRT Atrio-Ventricular Nodal Re-entry Tachycardia częstoskurcz nadkomorowy z węzła przedsionkowo-komorowego (re-entry) AVRT Atrio-Ventricular Re-entry Tachycardia częstoskurcz nadkomorowy (re-entry) BLS Basic Life Support podstawowe zabiegi resuscytacyjne BLS/AED Podstawowe zabiegi resuscytacyjne i automatyczna defibrylacja zewnętrzna (kurs certyfikowany przez ERC) BMV Bag-Mask-Ventilation wentylacja workiem samoroz pręża l- nym CCOT Critical Care Outreach Team konsultacyjny zespół intensywnej terapii COI Conflict of Interests konflikt interesów CoSTR Consensus on CPR Science with Treatment Recommendations Konsensus w sprawie dowodów naukowych w resuscytacji krążeniowo-oddechowej z rekomendacjami postępowania CPB Cardiopulmonary Bypass krążenie pozaustrojowe CPR Cardiopulmonary Resuscitation resuscytacja krążeniowo- -oddechowa (RKO) CPU Chest Pain observation Unit oddział obserwacyjny pacjentów z bólem w klatce piersiowej CSN centralny system nerwowy CV Compression Ventilation ratio stosunek liczby uciśnięć klatki piersiowej (C) do liczby oddechów ratunkowych (V) DNAR Do Not Attempt Resuscitation decyzja o niepodejmowaniu resuscytacji EC Educator Candidate kandydat na edukatora ERC ECLS Extracorporeal Life Support pozaustrojowe metody wspomagania układu krążenia ECMO Extracorporeal membrane oxygenation pozaustrojowe natlenianie krwi EIT Education, Implementation and Team grupa robocza ds. edukacji, implementacji i zespołów EMC Educator Master Class Europejski kurs dla edukatorów (kurs certyfikowany przez ERC) EMS Emergency Medical System system ratownictwa medycznego (pogotowie ratunkowe) EMT Emergency Medical Technician ratownik, technik medyczny, paramedyk EPLS European Paediatric Life Support Specjalistyczne zabiegi resuscytacyjne u dzieci (kurs certyfikowany przez ERC) EPILS European Paediatric Immediate Life Support Natychmiastowa pomoc w stanach zagrożenia życia u dzieci (kurs certyfikowany przez ERC) ERC European Resuscitation Council Europejska Rada Resuscytacji ETCO 2 end-tidal CO 2 końcowo-wydechowe stężenie dwutlenku węgla EWS Early Warning Score skala wczesnego ostrzegania FBAO Foreign Body Airway Obstruction niedrożność dróg oddechowych spowodowana ciałem obcym GIC Generic Instructor Course Europejski kurs instruktorski (certyfikowany przez ERC) IAC-CPR ICD ILCOR ILS im io IP ITD iv LBBB LMA LQTS LT MAS MET MILS NLS NLPZ NSTEMI NTS NZK ODD OIT OZW PCI PEA PEEP PPCI PR RKO ROSC RRT RSVP SAD SARS SBAR sc SCD SOR SP STEMI SVT UAP VF VT VF/VT ZRM Interposed Abdominal Compression Cardiopulmonary Resuscitation RKO za pomocą naprzemiennego uciskania jamy brzusznej Implantable Cardioverter Defibrillator wszczepialny kardiowerter-defibrylator International Liaison Committee on Resuscitation Międzynarodowy Komitet Łącznikowy ds. Resuscytacji Immediate Life Support Natychmiastowa pomoc w stanach zagrożenia życia (kurs certyfikowany przez ERC) intramuscular domięśniowa droga podaży leków intraosseous doszpikowa droga podaży leków Instructor Potential kandydat na instruktora ERC Impedance Threshold Device zastawka oporowa intravenous dożylna droga podaży leków Left Bundle Branch Block blok lewej odnogi pęczka Hisa Laryngeal Mask Airway maska krtaniowa Long QT Syndrome zespół wydłużonego QT Laryngeal Tube rurka krtaniowa Meconium Aspiration Syndrome zespół aspiracji smółki Medical Emergency Team zespół do stanów nagłych Manual In-Line Stabilisation ręczna stabilizacja w osi głowy i szyi Newborn Life Support Zabiegi resuscytacyjne u noworodka (kurs certyfikowany przez ERC) niesteroidowe leki przeciwzapalne Non-ST Elevation Myocardial Infarction zawał mięśnia sercowego bez uniesienia odcinka ST Non-technical Skills umiejętności pozatechniczne nagłe zatrzymanie krążenia Oesophageal Detector Device detektor przełykowy Oddział Intensywnej Terapii ostry zespół wieńcowy Percutaneous Coronary Intervention przezskórna interwencja wieńcowa Pulseless Electrical Activity aktywność elektryczna bez tętna Positive End Expiratory Pressure dodatnie ciśnienie końcowowydechowe Primary PCI pierwotna PCI Pogotowie Ratunkowe resuscytacja krążeniowo-oddechowa (Cardiopulmonary Resuscitation CPR) Return of Spontaneous Circulation przywrócenie spontanicznego krążenia krwi Rapid Response Team zespół szybkiego reagowania Reason, Story, Vital-signs, Plan przyczyna, historia, oznaki życia, plan Supraglottic Airway Device nadgłośniowe przyrządy do udrażniania dróg oddechowych Severe Acute Respiratory distress Syndrome ostry zespół niewydolności oddechowej Situation-Background-Assessment-Recommendation sytuacja, podstawowe dane, ocena, rekomendacje (system raportowania stanu pacjenta) subcutaneous podskórna droga podaży leków Sudden Cardiac Death nagła śmierć sercowa Szpitalny Oddział Ratunkowy syndrom poresuscytacyjny (post-cardiac arrest syndrome) ST Elevation Myocardial Infarction zawał mięśnia sercowego z uniesieniem odcinka ST Supra-Ventricular Tachycardia częstoskurcz nadkomorowy Unstable Angina Pectoris niestabilna choroba wieńcowa Ventricular Fibrillation migotanie komór Ventricular Tachykardia częstoskurcz komorowy migotanie komór lub częstoskurcz komorowy bez tętna Zespół Ratownictwa Medycznego
2 Publikacja przygotowana przez Europejską Radę Resuscytacji (ERC) przy współpracy z Polską Radą Resuscytacji (PRR). Tekst tłumaczony przez Polską Radę Resuscytacji. Wiedza i praktyka w zakresie resuscytacji krążeniowo-oddechowej to stale zmieniająca się dziedzina medycyny. W miarę rozwoju wiedzy oraz postępu w nauce i doświadczeniu klinicznym zmienia się w sposób ciągły również praktyka medycz na oraz sposób stosowania leków. Czytelnik tego podręcznika jest zobowiązany do zapoznania się z aktualnymi wiado mościami na temat przedstawionych sposobów postępowania i farmakoterapii ze szczególnym uwzględnieniem informacji producentów na temat dawek, czasu i drogi podawania oraz efektów ubocznych stosowanych leków. Na każdej z osób praktykujących medycynę resuscytacji spoczywa osobista odpowiedzialność za stosowane metody lecznicze, których uży cie powinno być oparte na gruntownej wiedzy i umiejętnościach praktycznych z zachowaniem niezbędnych warunków bez pieczeństwa własnego i pacjenta. Wydawcy oraz redaktorzy niniejszego opracowania nie ponoszą odpowiedzialności za szkody, które mogłyby być w jakikolwiek sposób związane z materiałem zawartym w tej książce. Bibliografia do wszystkich rozdziałów została w całości powtórzona za wydaniem oryginalnym. REDAKTOR NAUKOWY WYDANIA POLSKIEGO prof. dr hab. Janusz Andres TŁUMACZENIE Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Elżbieta Dobrowolska, Edyta Drab, Bartosz Frączek, Anna Jarosz, Piotr Kolęda, Paweł Krawczyk, Rafał Surmacz, Jurij Szymański, Grzegorz Zając KOREKTA MERYTORYCZNA Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Bartosz Frączek, Paweł Krawczyk ADIUSTACJA I KOREKTA WYDAWNICZA Danuta Ambrożewicz PROJEKT OKŁADKI Polska Rada Resuscytacji wg plakatu V Międzynarodowego Kongresu Polskiej Rady Resuscytacji autorstwa Mieczysława Górowskiego Publikację wydano ze środków Polskiej Rady Resuscytacji. Copyright by European Resuscitation Council (ERC), 2010 Copyright for the Polish edition by Polska Rada Resuscytacji, Kraków 2010 Copyright for the Polish translation by Polska Rada Resuscytacji, Kraków 2010 Wszystkie prawa zastrzeżone. Żadna część poniższej publikacji nie może być kopiowana i przechowywana w jakimkol wiek mechanicznym systemie kopiowania danych, włączając fotokopie, kserokopie, nagrania i inne, bez uprzedniej pisem nej zgody PRR (dotyczy terenu Rzeczpospolitej Polskiej). Wszystkie prośby o możliwość wykorzystania materiałów zawartych w tej publikacji należy kierować do ERC. ISBN KOORDYNATOR STRONY ORAZ WERSJI ELEKTRONICZNEJ Wytycznych resuscytacji 2010 Wiesław Pyrczak prc@prc.krakow.pl ADRES DO KORESPONDENCJI ADRES DO KORESPONDENCJI W POLSCE ERC Secretariat VZW Polska Rada Resuscytacji Drie Eikenstraat 661 ul. Radziwiłłowska 4, Kraków BE-2650 EDEGEM tel fax Belgium biuro@prc.krakow.pl tel fax Koordynator kursów info@erc.edu Tomasz Galewicz kursy@prc.krakow.pl SKŁAD I PRZYGOTOWANIE DO DRUKU FALL ul. Garczyńskiego 2, Kraków tel ; fall@fall.pl
3 Podsumowanie Komitetu Wykonawczego ERC 1 Jerry P. Nolan a, *, Jasmeet Soar b, David A. Zideman c, Dominique Biarent d, Leo L. Bossaert e, Charles Deakin f, Rudolph W. Koster g, Jonathan Wyllie h, Bernd Böttiger i, on behalf of the ERC Guidelines Writing Group a Anaesthesia and Intensive Care Medicine, Royal United Hospital, Bath, UK b Anaesthesia and Intensive Care Medicine, Southmead Hospital, North Bristol NHS Trust, Bristol, UK c Imperial College Healthcare NHS Trust, London, UK d Paediatric Intensive Care and Emergency Medicine, Université Libre de Bruxelles, Queen Fabiola Children s University Hospital, Brussels, Belgium e Cardiology and Intensive Care, University of Antwerp, Antwerp, Belgium f Cardiac Anaesthesia and Critical Care, Southampton University Hospital NHS Trust, Southampton, UK g Department of Cardiology, Academic Medical Center, Amsterdam, The Netherlands h Neonatology and Paediatrics, The James Cook University Hospital, Middlesbrough, UK i Anästhesiologie und Operative Intensivmedizin, Universitätsklinikum Köln, Köln, Germany Wprowadzenie Poniższa publikacja Wytycznych resuscytacji krążeniowo- -oddechowej Europejskiej Rady Resuscytacji uaktualnia wytyczne opublikowane w 2005 roku i jest kontynuacją ustanowionego pięcioletniego cyklu zmian wytycznych 1. Podobnie jak Wytyczne 2005, tak i obecne są oparte na najbardziej aktualnym dokumencie CoSTR (Consensus on CPR Science with Treatment Recommendations) 2, który systematyzuje wyniki prac naukowych dotyczących szerokiego zakresu tematów związanych z resuscytacją krążeniowo-oddechową (RKO). Wiedza o resuscytacji ciągle się rozwija, dlatego wytyczne postępowania klinicznego muszą być regularnie uaktualniane, by odzwierciedlały ten postęp i wskazywały personelowi medycznemu najlepszy sposób postępowania. W pięcioletnich okresach pomiędzy kolejnymi aktualizacjami wytycznych publikowane są stwierdzenia doradcze dotyczące nowych terapii mogących znacząco wpływać na wyniki leczenia 3. Niniejsze podsumowanie przedstawia podstawowe algorytmy postępowania w resuscytacji dzieci, dorosłych, a także zwraca uwagę na główne zmiany w wytycznych od roku Szczegółowe informacje są zawarte w dziewięciu pozostałych rozdziałach Wytycznych Rozdziały Wytycznych 2010: 1. Podsumowanie Komitetu Wykonawczego ERC. 2. Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja Zaawansowane zabiegi resuscytacyjne u osób dorosłych Postępowanie wstępne w ostrych zespołach wieńcowych Zaawansowane zabiegi resuscytacyjne u dzieci 8. * Corresponding author. jerry.nolan@btinternet.com ( J.P. Nolan). 7. Resuscytacja noworodków bezpośrednio po urodzeniu Zatrzymanie krążenia postępowanie w sytuacjach szczególnych: zaburzenia elektrolitowe, zatrucia, tonięcie, przypadkowa hipotermia, hipertermia, astma, anafilaksja, zabiegi kardiochirurgiczne, urazy, ciąża, porażenie prądem Zasady edukacji w resuscytacji Etyka resuscytacji oraz problemy końca życia 12. Poniższe wytyczne nie definiują jedynego sposobu przeprowadzania resuscytacji. W większości odzwierciedlają szeroko akceptowany pogląd, jak resuscytacja powinna być przeprowadzona zarówno bezpiecznie, jak i skutecznie. Publikacja nowych, zaktualizowanych rekomendacji leczniczych nie oznacza, że dotychczasowe postępowanie jest niebezpieczne czy nieefektywne. Podsumowanie głównych zmian w porównaniu z Wytycznymi 2005 Podstawowe zabiegi resuscytacyjne Zmiany w wytycznych dotyczące podstawowych zabiegów resuscytacyjnych (Basic Life Support BLS) w zestawieniu z Wytycznymi 2005 obejmują 4,13 : Dyspozytorzy powinni być przeszkoleni w zakresie zbierania informacji od osób wzywających pomocy zgodnie z precyzyjnym protokołem. Informacje te powinny być ukierunkowane na rozpoznawanie stanu nieprzytomności i jakości oddychania. Stwierdzenie braku oddechu lub niewłaściwego toru oddechowego w zestawieniu z brakiem przytomności powinny skutkować wdrożeniem właściwego protokołu związanego z podejrzeniem zatrzymania krążenia. Podkreśla się wagę rozpoznania pojedynczych westchnięć (gasping) jako objawu zatrzymania krążenia. Wszystkie osoby udzielające pomocy, niezależnie od stopnia wyszkolenia, powinny wykonywać uciśnięcia klatki u poszkodowanych z zatrzymaniem krążenia. Kluczową interwencją, na które Wytyczne nadal kładą
4 6 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 nacisk, jest wysoka jakość uciśnięć klatki piersiowej. Celem powinno być osiągnięcie głębokości przynaj mniej 5 cm i częstości przynajmniej 100 uciśnięć na minutę. Należy przy tym pamiętać, by klatka piersiowa powróciła do pierwotnego kształtu oraz by minimalizować przerwy w uciskaniu klatki piersiowej. Osoby przeszkolone powinny wykonywać uciśnięcia klatki piersiowej i wentylację w sekwencji 30 : 2. Gdy BLS wykonuje osoba nieprzeszkolona, zachęca się do zastosowania telefonicznego instruktażu prowadzenia RKO z wyłącznym uciskaniem klatki piersiowej. Podczas resuscytacji krążeniowo-oddechowej (RKO) zachęca się do stosowania narzędzi pozwalających na uzyskanie natychmiastowej informacji zwrotnej dla ratowników. Dane gromadzone w tych urządzeniach mogą być użyte w celu monitorowania i poprawy jakości wykonywania RKO, jak również dostarczają zawodowym ratownikom informacji zwrotnych przydatnych w trakcie sesji debriefingowych. Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i elektrostymulacja5, 14 Najważniejsze zmiany dotyczące elektroterapii w Wytycznych 2010 Europejskiej Rady Resuscytacji: Podkreśla się potrzebę wczesnego, nieprzerwanego wykonywania uciśnięć klatki piersiowej. Znacznie większy nacisk kładzie się na minimalizowanie przerw bezpośrednio przed i po defibrylacji. Zaleca się kontynuowanie uciskania klatki piersiowej w trakcie ładowania defibrylatora (przydatne szczególnie przy zastosowaniu elektrod samoprzylepnych przyp. tłum.). Podkreśla się rolę natychmiastowego ponownego podjęcia uciskania klatki piersiowej po wykonanej defibrylacji; w zestawieniu z ciągłym prowadzeniem uciśnięć klatki piersiowej podczas ładowania defibrylatora wykonanie defibrylacji powinno być osiągalne z przerwaniem uciskania klatki piersiowej na czas nie dłuższy niż 5 sekund. Nadal najważniejsze jest bezpieczeństwo ratownika. Wytyczne zwracają również uwagę, że zagrożenie dla ratownika podczas defibrylacji jest bardzo małe, szczególnie, gdy ma założone rękawiczki. Obecnie kładzie się nacisk na szybkie sprawdzenie bezpieczeństwa w celu zminimalizowania przerwy przed defibrylacją. Podczas leczenia pozaszpitalnego zatrzymania krążenia, w czasie gdy defibrylator jest przygotowywany, podłączany i ładowany, zespoły pogotowia ratunkowego powinny zapewnić wysokiej jakości RKO, ale nie jest już zalecane rutynowe stosowanie zdefiniowanego okresu RKO (np. 2 lub 3 minut) przed oceną rytmu i dostarczeniem wyładowania. Dla tych systemów opieki przedszpitalnej, w których wprowadzono zdefiniowany okres RKO przed defibrylacją, wobec braku przekonujących danych potwierdzających bądź wykluczających stosowanie tego typu postępowania, zasadne jest kontynuowanie tej praktyki. Można rozważyć zastosowanie do trzech defibrylacji pod rząd, gdy zatrzymanie krążenia w rytmach do defibrylacji (VF/VT) wystąpi podczas cewnikowania serca lub we wczesnym okresie pooperacyjnym po zabiegach kardiochirurgicznych. Strategia trzech wyładowań może być również rozważona jako wstępne postępowanie w zauważonym zatrzymaniu krążenia, gdy pacjent jest już podłączony do defibrylatora manualnego. Zachęca się do kontynuacji rozwoju programów AED istnieje potrzeba dalszego rozpowszechniania automatycznych defibrylatorów zewnętrznych zarówno w miejscach publicznych, jak i obszarach mieszkalnych. Zaawansowane zabiegi resuscytacyjne u osób dorosłych Najważniejsze zmiany w Wytycznych 2010 dotyczące zaawansowanych zabiegów resuscytacyjnych (Advanced Life Support ALS) u osób dorosłych 6,15 : Zwiększenie nacisku na istotę minimalizowania przerw w wysokiej jakości uciśnięciach klatki piersiowej prowadzonych podczas wszystkich interwencji ALS. Uciśnięcia klatki piersiowej zatrzymywane są na krótko, jedynie by umożliwić istotne interwencje. Zwiększenie nacisku na zastosowanie systemów obserwuj i reaguj ( track and trigger ), by uchwycić pogorszenie się stanu zdrowia pacjenta i umożliwić wdrożenie leczenia w celu prewencji wewnątrzszpitalnego zatrzymania krążenia. Zwrócenie uwagi na niepokojące objawy ryzyka nagłej śmierci sercowej poza szpitalem. Rezygnacja z zalecenia dotyczącego zdefiniowanego okresu RKO przed defibrylacją pozaszpitalną w przebiegu niezauważonego przez służby ratownicze zatrzymania krążenia. Kontynuacja uciśnięć klatki piersiowej podczas ładowania defibrylatora pozwoli to zminimalizować przerwę przed defibrylacją. Zmniejszenie znaczenia uderzenia przedsercowego. Zastosowanie do trzech pod rząd defibrylacji w przypadku migotania komór, częstoskurczu komorowego bez tętna (VF/VT) występujących podczas cewnikowania serca lub bezpośrednio w okresie pooperacyjnym w kardiochirurgii. Nie jest już zalecane podawanie leków przez rurkę intubacyjną jeżeli dostęp dożylny nie jest możliwy do uzyskania, leki powinno się podawać doszpikowo (intraosseous io). W leczeniu zatrzymania krążenia w rytmach do defibrylacji (VF/VT) należy podać 1 mg adrenaliny po wykonaniu trzeciej defibrylacji i podjęciu uciskania klatki piersiowej, a następnie co 3 5 minut (co drugą pętlę RKO). Amiodaron w dawce 300 mg jest także podawany po trzeciej defibrylacji. Atropina nie jest już zalecana do rutynowego stosowania w przypadku asystolii lub czynności elektrycznej bez tętna (Pulseless Electrical Activity PEA). Zmniejszenie nacisku na wczesną intubację dotchawiczą, za wyjątkiem sytuacji, gdy może być ona wykonana przez dobrze wyszkolone osoby, z minimalną tylko przerwą w uciśnięciach klatki piersiowej. Zwiększenie nacisku na zastosowanie kapnografii w celu potwierdzenia i monitorowania położenia rurki dotchawiczej oraz jakości RKO, a także jako wczesnego
5 Podsumowanie Komitetu Wykonawczego ERC 7 wskaźnika powrotu spontanicznego krążenia (Return of Spontaneous Circulation ROSC). Zwrócenie uwagi na potencjalne znaczenie obrazowania ultrasonograficznego podczas ALS. Rozpoznanie potencjalnej szkody powodowanej przez hiperoksemię po ROSC. Gdy osiągnięty zostanie ROSC i można wiarygodnie monitorować saturację krwi tętniczej (SaO 2 ) poprzez pulsoksymetrię i/lub gazometrię, wdechowe stężenie tlenu powinno być miareczkowane tak, by osiągnąć saturację (SaO 2 ) 94 98%. Zwrócenie większej uwagi na szczegółowe leczenie zespołu objawów występujących po zatrzymaniu krążenia syndrom poresuscytacyjny (SP) (post-cardiac arrest syndrome). Podkreślenie faktu, iż wdrożenie zrozumiałych, przejrzystych protokołów leczenia pacjentów po zatrzymaniu krążenia może poprawić przeżycie po ROSC. Zwiększenie nacisku na zastosowanie pierwotnej przezskórnej interwencji wieńcowej w określonej grupie pacjentów z utrzymującym się ROSC (włączając w to pacjentów pozostających w stanie śpiączki). Rewizja zaleceń dotyczących kontroli poziomu glikemii: u osób dorosłych z utrzymującym się ROSC należy wdrożyć leczenie, gdy poziom glukozy we krwi jest >10 mmol/l (>180 mg/dl). Jednocześnie powinno się unikać hipoglikemii. Zastosowanie terapeutycznej hipotermii u pacjentów pozostających w stanie śpiączki po zatrzymaniu krążenia w pierwotnych rytmach nie do defibrylacji, jak i w rytmach do defibrylacji, przy czym należy zauważyć niższy poziom dowodów naukowych na zastosowanie hipotermii w grupie pacjentów z zatrzymaniem krążenia w rytmach nie do defibrylacji. Podkreślenie faktu, iż wiele zaakceptowanych czynników przewidujących/prognozujących niekorzystny wynik leczenia pacjentów pozostających w stanie śpiączki po NZK jest niewiarygodnych, szczególnie gdy zastosowano terapeutyczną hipotermię. Wstępne postępowanie w ostrych zespołach wieńcowych Zmiany w postępowaniu w ostrych zespołach wieńcowych od czasu opublikowania Wytycznych 2005 obejmują poniższe 7,16 : Termin zawał mięśnia sercowego bez uniesienia odcinka ST ostry zespół wieńcowy (Non-ST-Elevation Myocardial Infarction-Acute Coronary Syndrome NSTEMI - -ACS) został wprowadzony dla określenia zarówno NSTEMI, jak i niestabilnej dusznicy bolesnej, ponieważ diagnostyka różnicowa jest zależna od biomarkerów, jakie można oznaczyć dopiero po kilku godzinach, podczas gdy decyzje o wdrożeniu leczenia opierają się o obecne aktualnie objawy kliniczne. Wywiad, badanie fizykalne, biomarkery, kryteria EKG i skale ryzyka nie są wiarygodnymi kryteriami identyfikacji pacjentów, którzy mogą być wcześnie i bezpiecznie wypisani ze szpitala. Rolą oddziałów przyjmujących pacjentów celem obserwacji dolegliwości bólowych w klatce piersiowej (Chest Pain Observation Units CPUs) jest identyfikacja, poprzez zastosowanie powtarzanego badania fizykalnego, EKG i ocenę biomarkerów, tych pacjentów, którzy wymagają przyjęcia do szpitala i leczenia inwazyjnego. Może to wymagać zastosowania testów prowokacyjnych, a w określonej grupie pacjentów badań obrazowych, takich jak tomografia komputerowa serca, rezonans magnetyczny itd. Należy unikać niesteroidowych leków przeciwzapalnych (NLPZ). Nitratów nie powinno się stosować w celach diagnostycznych. Suplementację tlenu powinno się stosować jedynie u pacjentów z hipoksemią, dusznością lub zastojem płucnym. Hiperoksemia może być szkodliwa w przebiegu niepowikłanego zawału. Wprowadzono liberalizację wytycznych leczenia kwasem acetylosalicylowym (ASA): ASA może być obecnie podany przez świadków zdarzenia, także bez zaleceń dyspozytora. Zweryfikowano wytyczne nowej terapii przeciwpłytkowej, przeciwtrombinowej dla pacjentów ze STEMI i NSTEMI-ACS w oparciu o wybraną strategię terapeutyczną. Nie jest zalecane stosowanie inhibitorów glikoproteiny IIb/IIIa przed wykonaniem angiografii/przezskórnej interwencji wieńcowej (PCI). Uaktualniono strategię reperfuzyjną dla zawału mięśnia sercowego z uniesieniem odcinka ST: Preferowanym sposobem leczenia jest pierwotna przezskórna interwencja wieńcowa (Primary PCI) wykonywana we właściwym przedziale czasowym przez doświadczony zespół. Zespół pogotowia ratunkowego może pominąć najbliższy szpital, aby PPCI mogło być wykonane bez zbytecznego opóźnienia. Akceptowalne opóźnienie pomiędzy rozpoczęciem fibrynolizy a pierwszym wypełnieniem balonu jest zmienne i wynosi od ok minut w zależności od lokalizacji zawału, wieku pacjenta i czasu trwania objawów. Ratunkowa PCI (rescue PCI) powinna być podjęta w przypadku nieskutecznej fibrynolizy. Nie jest zalecana strategia rutynowej PCI bezpośrednio po fibrynolizie (facilitated PCI). Pacjenci, u których wykonano skuteczną fibrynolizę, a znajdujący się w szpitalach nieposiadających możliwości wykonania PCI, powinni być przesłani celem wykonania angiografii i ewentualnej PCI optymalnie w ciągu 6 24 godzin po fibrynolizie (strategia farmako-iwazyjna). Angiografia i w razie potrzeby PCI mogą być zasadne u pacjentów po ROSC i mogą być częścią wystandaryzowanego protokołu postępowania po zatrzymaniu krążenia. Aby osiągnąć powyższe zamierzenia, pomocne jest stworzenie sieci obejmujących swoim działaniem pogotowie ratunkowe oraz szpitale posiadające i nieposiadające możliwości wykonania PCI. 1
6 8 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Zalecenia stosowania beta-blokerów są bardziej restrykcyjne: brak jest dowodów pozwalających na rutynowe stosowanie beta-blokerów drogą dożylną za wyjątkiem szczególnych sytuacji, takich jak tachyarytmie. W przeciwnym razie terapia beta-blokerem powinna być rozpoczynana z zastosowaniem niskich dawek jedynie wtedy, gdy stan pacjenta jest stabilny. Wytyczne profilaktycznego zastosowania leków antyarytmicznych, inhibitorów enzymu konwertującego angiotensynę/blokerów receptora angiotensyny oraz statyn pozostają bez zmian. Zabiegi resuscytacyjne u dzieci Najważniejsze zmiany w nowych wytycznych postępowania resuscytacyjnego w pediatrii obejmują 8,17 : Rozpoznanie zatrzymania krążenia osoby z wykształceniem medycznym nie mogą w sposób wiarygodny ocenić obecności bądź braku tętna u niemowlęcia lub dziecka w czasie poniżej 10 sek. Powinni oni poszukiwać oznak życia, a jeżeli są pewni techniki badania, mogą włączyć ocenę tętna do diagnostyki zatrzymania krążenia i zadecydować, czy powinni rozpocząć uciśnięcia klatki piersiowej, czy nie. Decyzja o rozpoczęciu RKO musi być podjęta w czasie krótszym niż 10 sek. W zależności od wieku dziecka tętno można badać na tętnicy szyjnej (dzieci), ramiennej (niemowlęta) lub udowej (dzieci i niemowlęta). Stosunek uciśnięć klatki piersiowej do wentylacji (Compression Ventilation ratio CV) u dzieci zależy od tego, czy pomocy udziela jeden, czy więcej ratowników. Ratowników bez wykształcenia medycznego, którzy zwykle nauczani są działania w pojedynkę, należy instruować, aby wykonywali 30 uciśnięć klatki piersiowej i 2 oddechy ratownicze, czyli tak samo, jak w wytycznych dla dorosłych, co umożliwia każdemu, kto został przeszkolony w zakresie BLS, prowadzenie resuscytacji dzieci przy minimum dodatkowych informacji. Ratownicy mający zawodowy obowiązek udzielania pomocy powinni się uczyć i stosować CV 15 : 2, jednak mogą użyć stosunku 30 : 2, jeśli działają w pojedynkę, szczególnie, gdy nie udaje się im osiągnąć wystarczającej liczby uciśnięć. Wentylacja pozostaje nadal bardzo istotnym elementem RKO w zatrzymaniu krążenia spowodowanym asfiksją. Ratowników, którzy nie są w stanie lub nie chcą prowadzić wentylacji usta usta, należy zachęcać do wykonywania przynajmniej RKO z wyłącznym uciskaniem klatki piersiowej. Podkreśla się znaczenie jakości uciśnięć, które powinny być wykonywane na odpowiednią głębokość, z możliwie najmniejszymi przerwami, aby zminimalizować czas bez przepływu. U wszystkich dzieci należy uciskać klatkę piersiową na co najmniej 1/3 jej wymiaru przednio-tylnego (tj. około 4 cm u niemowląt i około 5 cm u dzieci). Podkreśla się też znaczenie następującego po uciśnięciu całkowitego zwolnienia nacisku. Zarówno u niemowląt, jak i u dzieci częstość uciśnięć powinna wynosić co najmniej 100/min, ale nie więcej niż 120/ min. Technika ich wykonywania u niemowląt obejmuje uciskanie dwoma palcami w przypadku jednego ratownika lub objęcie dłońmi klatki piersiowej i uciskanie dwoma kciukami, jeśli ratowników jest dwóch lub więcej. U starszych dzieci, w zależności od decyzji ratownika, można zastosować technikę uciskania jedną lub dwoma rękami. Automatyczne defibrylatory zewnętrzne (AED) są bezpieczne i skuteczne, gdy stosuje się je u dzieci powyżej 1. roku życia. Specjalne elektrody pediatryczne lub oprogramowanie zmniejszają energię urządzenia do J i są rekomendowane dla dzieci w wieku 1 8 lat. Jeżeli nie jest dostępne takie urządzenie ani dostosowywane manualnie, u dzieci powyżej 1. roku życia można użyć niezmodyfikowanego AED, jak u dorosłych. Istnieją doniesienia o przypadkach skutecznego zastosowania AED u dzieci poniżej 1. roku życia; w rzadkich przypadkach występowania rytmów do defibrylacji u dzieci poniżej 1. roku życia użycie AED jest uzasadnione (najlepiej z modyfikacją energii). Aby skrócić czas bez przepływu, używając manualnego defibrylatora, należy kontynuować uciśnięcia klatki piersiowej podczas umieszczania i ładowania łyżek lub elektrod samoprzylepnych (jeżeli wielkość klatki piersiowej dziecka na to pozwoli). Po naładowaniu defibrylatora należy przerwać na krótko uciskanie klatki piersiowej w celu wykonania defibrylacji. Dla uproszczenia i spójności z wytycznymi BLS i ALS u dorosłych, do defibrylacji u dzieci rekomendowana jest strategia pojedynczych wyładowań energią 4 J/kg bez jej zwiększania (najlepiej z użyciem defibrylatora dwufazowego, ale jednofazowy jest dopuszczalny). Można bezpiecznie używać rurek z mankietem u niemowląt i małych dzieci. Średnicę rurki należy dobrać korzystając z właściwej formuły. Bezpieczeństwo i znaczenie stosowania ucisku na chrząstkę pierścieniowatą podczas intubacji tchawicy nie zostały jasno określone. Dlatego, jeśli ten manewr upośledza wentylację lub opóźnia bądź utrudnia intubację, należy go zmodyfikować lub zaprzestać. Monitorowanie końcowo-wydechowego stężenia dwutlenku węgla (CO 2 ), najlepiej za pomocą kapnografu, jest pomocne w potwierdzaniu prawidłowego położenia rurki intubacyjnej i rekomendowane podczas RKO do pomocy w jej ocenie i optymalizacji jakości. Po ROSC należy tak miareczkować stężenie tlenu w mieszaninie oddechowej, aby ograniczyć ryzyko hiperoksemii. Wdrożenie systemu szybkiego reagowania w oddziałach pediatrycznych może zredukować częstość zatrzymań krążenia i oddychania oraz śmiertelność szpitalną. Nowe zagadnienia w Wytycznych 2010 obejmują postępowanie w patologiach kanałów jonowych i niektórych nowych sytuacjach szczególnych: urazach, korekcji serca jednokomorowego przed i po pierwszym etapie, po korekcji metodą Fontana, nadciśnieniu płucnym. Resuscytacja noworodków bezpośrednio po urodzeniu Poniżej przedstawiono najistotniejsze zmiany, które pojawiły się w 2010 r. w wytycznych resuscytacji noworodków 9,18 :
7 Podsumowanie Komitetu Wykonawczego ERC 9 U wydolnych noworodków aktualnie zaleca się opóźnienie klemowania pępowiny o co najmniej jedną minutę od momentu urodzenia się dziecka (zakończenia drugiego okresu porodu). Dotychczas nie zgromadzono wystarczającej ilości danych pozwalających na wskazanie zalecanego czasu zaklemowania pępowiny u noworodków urodzonych w ciężkiej zamartwicy. U noworodków urodzonych o czasie podczas resuscytacji bezpośrednio po urodzeniu należy używać powietrza. Jeżeli pomimo efektywnej wentylacji oksygenacja (optymalnie oceniana za pomocą oksymetru) nie jest akceptowalna, należy rozważyć użycie wyższego stężenia tlenu. Wcześniaki poniżej 32. tygodnia ciąży oddychając powietrzem, mogą nie osiągnąć takiej samej przezskórnej saturacji jak noworodki urodzone o czasie. Dlatego należy rozważnie podawać mieszaninę tlenu z powietrzem pod kontrolą pulsoksymetru. Jeżeli mieszanina tlenu z powietrzem nie jest dostępna, należy zastosować to, co jest dostępne. Wcześniaki poniżej 28. tygodnia ciąży natychmiast po urodzeniu i bez osuszania należy całkowicie owinąć folią spożywczą lub workiem plastikowym do poziomu szyi. Zabiegi pielęgnacyjne i stabilizacja powinny się odbywać pod promiennikiem ciepła. Noworodki powinny pozostawać owinięte folią dopóki ich temperatura nie zostanie sprawdzona po przyjęciu na oddział. W takich przypadkach temperatura na sali porodowej powinna wynosić przynajmniej 26 C. Rekomendowany stosunek uciśnięć klatki piersiowej do wentylacji w trakcie resuscytacji noworodków wynosi 3 : 1. Nie zaleca się odsysania smółki z nosa i ust po urodzeniu główki dziecka (gdy główka jest jeszcze w kroczu). Jeśli urodzone dziecko jest wiotkie, nie oddycha i obecna jest smółka, zasadne jest wykonać szybką inspekcję jamy ustno-gardłowej i usunąć potencjalną przyczynę niedrożności. Jeżeli na miejscu znajduje się osoba posiadająca specjalistyczne umiejętności, przydatna może być intubacja i odessanie tchawicy. Jednakże jeśli próba intubacji przedłuża się lub jest nieskuteczna, należy rozpocząć wentylację maską twarzową, szczególnie gdy utrzymuje się bradykardia. Gdy podawana jest adrenalina, rekomenduje się drogę dożylną i stosuje dawkę μg/kg. Jeżeli wykorzystywany jest dostęp dotchawiczy, aby osiągnąć efekt porównywalny do dawki 10 μg/kg dożylnie, prawdo podobnie potrzebna będzie dawka co najmniej μg/kg. Wykrycie obecności dwutlenku węgla w wydychanym powietrzu w połączeniu z oceną kliniczną jest zalecane jako najbardziej wiarygodna metoda potwierdzenia położenia rurki intubacyjnej u noworodków z zachowanym spontanicznym krążeniem. U noworodków urodzonych o czasie lub prawie o czasie, rozwijających umiarkowaną lub ciężką encefalopatię hipoksyczno-ischemiczną, należy, o ile to możliwe, zastosować terapeutyczną hipotermię. Takie postępowanie nie modyfikuje przebiegu natychmiastowych zabiegów resuscytacyjnych, ale jest ważne w opiece poresuscytacyjnej. Zasady edukacji w resuscytacji Poniżej przedstawiono kluczowe kwestie wskazane przez grupę roboczą ds. edukacji, implementacji i zespołów (EIT Education, Implementation and Teams) International Liasion Committee on Resuscitation podczas procesu oceny dowodów naukowych Wytycznych ,19 : Aby zapewnić wiarygodną ocenę osiągnięcia założonych celów nauczania, należy przeprowadzać ewaluację metod edukacyjnych. Celem jest upewnienie się, że osoby szkolone posiądą i zachowają umiejętności i wiedzę, które umożliwią im prawidłowe działanie podczas zatrzymania krążenia i poprawią wyniki leczenia pacjentów. Krótkie wideo lub komputerowe kursy samokształcące, z minimalnym udziałem instruktora lub bez niego, w połączeniu z ćwiczeniami praktycznymi można rozważyć jako efektywną alternatywę dla kursów podstawowych zabiegów resuscytacyjnych (BLS-AED) prowadzonych przez instruktorów. Ideałem byłoby, gdyby wszyscy obywatele zostali przeszkoleni w zakresie standardowej RKO, obejmującej uciskanie klatki piersiowej i wentylację. W niektórych sytuacjach jednak dopuszczalne jest szkolenie polegające na nauczaniu RKO z wyłącznym uciskaniem klatki piersiowej (np. dostosowane do sytuacji szkolenie w bardzo ograniczonym czasie). Osoby w ten sposób przeszkolone należy zachęcać, aby uczyły się pełnej RKO. Wiedza i umiejętności z zakresu podstawowych i zaawansowanych zabiegów resuscytacyjnych pogarszają się już po upływie 3 6 miesięcy od szkolenia. Częsta ocena pomoże zidentyfikować osoby wymagające szkoleń przypominających w celu utrzymania wiedzy i umiejętności. Podczas szkoleń z zakresu RKO, niezależnie od wyszkolenia medycznego uczestników, należy rozważyć stosowanie urządzeń dających natychmiastową informację zwrotną w celu poprawy nabywania i utrzymania umiejętności praktycznych. Zwiększony nacisk na rozwijanie umiejętności pozatechnicznych (Non-technical Skills NTS), takich jak kierowanie zespołem, praca zespołowa, podział obowiązków i umiejętność komunikacji, pomoże poprawić jakość RKO i opieki nad pacjentem. Odprawy dla zespołów i przygotowywanie się do resuscytacji oraz omawianie jej w oparciu o analizę postępowania podczas symulowanej lub rzeczywistej resuscytacji należy wykorzystywać jako narzędzie pomocne w doskonaleniu działań zespołów resuscytacyjnych i osób indywidualnych. Liczba badań naukowych dotyczących wpływu szkoleń z zakresu resuscytacji na wyniki końcowe leczenia pacjentów jest ograniczona. Chociaż obserwacje z wykorzystaniem manekinów są przydatne, należy zachęcać badaczy, aby analizowali i publikowali wyniki dotyczące wpływu metod edukacyjnych na efekty leczenia pacjentów. 1
8 10 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Epidemiologia i wyniki leczenia pacjentów po zatrzymaniu krążenia Choroba niedokrwienna serca jest główną przyczyną zgonów na świecie 20. W Europie choroby układu sercowo-naczyniowego są odpowiedzialne za około 40% wszystkich zgonów w grupie osób poniżej 75. roku życia 21. Nagłe zatrzymanie krążenia (NZK) jest odpowiedzialne za ponad 60% zgonów z powodu choroby niedokrwiennej serca u osób dorosłych 22. Dane zbiorcze pochodzące z analizy 37 populacji europejskich wskazują, że roczna częstość pozaszpitalnego zatrzymania krążenia u pacjentów leczonych przez pogotowie ratunkowe wynosi 38 na mieszkańców niezależnie od mechanizmu zatrzymania krąże nia 22a. Z danych tych wynika, że roczna częstość zatrzymania krążenia w mechanizmie migotania komór (VF) leczonych przez pogotowie ratunkowe wynosi 17 na , a przeżycie do wypisu ze szpitala wynosi 10,7% dla wszystkich mechanizmów i 21,2% dla NZK w mechanizmie VF. Niedawno opublikowane dane z 10 ośrodków północnoamerykańskich są zaskakująco zgodne z przedstawionymi powyżej: mediana częstości przeżycia do wypisu ze szpitala wynosiła 8,4% dla wszystkich zatrzymań krążenia leczonych przez pogotowie ratunkowe, niezależnie od mechanizmu, i 22,0% dla VF 23. Istnieją dowody świadczące o wzroście przeżywalności długoterminowej po zatrzymaniu krążenia 24,25. Analizując pierwszy oceniony rytm serca u osób z pozaszpitalnym zatrzymaniem krążenia, VF występowało u ok %. Odsetek ten zmniejszył się w ciągu ostatnich 20 lat Prawdopodobnie w momencie utraty przytomności znacznie więcej osób ma VF lub częstoskurcz komorowy (Ventricular Tachycardia VT), ale zanim personel pogotowia zarejestruje pierwszy zapis czynności elektrycznej serca (EKG), rytm pogarsza się do asystolii 31,32. Jeżeli rytm zostanie zarejestrowany bezpośrednio po utracie przytomności, szczególnie za pomocą AED dostępnego na miejscu zdarzenia, odsetek pacjentów z VF może wynieść nawet % 34. Doniesienia na temat częstości epizodów wewnątrzszpitalnego zatrzymania krążenia są bardziej zróżnicowane i utrzymują się w granicach 1 5 na 1000 przyjęć do szpitala 35. Ostatnie dane pochodzące z American Heart Association s National Registry of CPR wskazują, że odsetek przeżyć do wypisu ze szpitala po wewnątrzszpitalnym zatrzymaniu krążenia wynosi 17,6% (wszystkie mechanizmy) 36. W 25% przypadków wstępny rytm stanowi VF lub VT bez tętna i spośród nich 37% pacjentów przeżywa do wypisu ze szpitala, a jeśli wstępny rytm stanowi PEA lub asystolia 11,5%. Międzynarodowy konsensus naukowy w dziedzinie resuscytacji krążeniowo- -oddechowej (International Consensus on Cardiopulmonary Science) W skład International Liaison Committee on Resuscitation (ILCOR) wchodzą przedstawiciele American Heart Association (AHA), European Resuscitation Council (ERC), Heart and Stroke Foundation of Canada (HSFC), Australian and New Zealand Committee on Resuscitation (ANZ COR), Resuscitation Council of Southern Africa (RCSA), Inter-American Heart Foundation (IAHF) i Resuscitation Council of Asia (RCA). Od roku 2000 badacze z organizacji członkowskich ILCOR oceniali wiedzę z zakresu resuscytacji w pięcioletnich cyklach. Wnioski i zalecenia z 2005 International Consensus Conference on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care with Treatment Recommendations zostały opublikowane pod koniec 2005 roku 37,38. Ostatnia konferencja International Consensus Conference odbyła się w Dallas w styczniu 2010 roku, a wnioski i zalecenia opublikowane w wyniku tego procesu stanowią podstawy aktualnych Wytycznych 2010 ERC 2. Każda z sześciu grup roboczych ILCOR (ds. podstawowych zabiegów resuscytacyjnych [BLS]; ds. zaawansowanych zabiegów resuscytacyjnych [ALS]; ds. ostrych zespołów wieńcowych [ACS]; ds. zabiegów resuscytacyjnych w pediatrii [PLS]; ds. zabiegów resuscytacyjnych u noworodków [NLS]; ds. edukacji, implementacji i zespołów [EIT]) zidentyfikowała zagadnienia wymagające oceny dowodów naukowych i zaprosiła międzynarodowych ekspertów do ich recenzji. Analiza piśmiennictwa opierała się na ustandaryzowanym arkuszu roboczym stanowiącym matrycę, która zawierała specjalnie stworzony system oceny do określenia poziomu istotności naukowej każdego badania 39. Gdy było to możliwe, zapraszano dwóch ekspertów recenzujących, aby dokonali niezależnej oceny każdego zagadnienia. W International Consensus Conference 2010 wzięło udział 313 ekspertów z 30 krajów. W ciągu trzech lat poprzedzających konferencję 356 autorów arkuszy roboczych przeanalizowało dokładnie tysiące publikacji dotyczących 277 określonych zagadnień z dziedziny resuscytacji. Każde zagadnienie zostało opracowane w standardowym formacie PICO Population, Intervention, Comparison Outcome (populacja, interwencja, porównanie wyników oraz końcowe/odległe wyniki leczenia) 2. Każde proponowane stwierdzenie naukowe było podsumowaniem opinii ekspertów opartej na wszystkich istotnych danych naukowych dotyczących danego zagadnienia, a odpowiednie grupy robocze opracowywały konsensus dotyczący zaleceń terapeutycznych (treatment recommendations). Ostateczne sformułowanie stwierdzeń naukowych oraz opracowanie zaleceń terapeutycznych nastąpiło po dodatkowej analizie przez organizacje członkowskie ILCOR i kolegium redakcyjne 2. Ogólne zasady postępowania dotyczące konfliktu interesów (COI Conflict of Interest) stworzone dla 2005 International Consensus Conference 40 zostały dokładnie zrewidowane w roku Przedstawiciele producentów i przemysłu nie brali udziału w konferencji w roku 2005 ani w roku Od nauki do wytycznych Podobnie jak w roku 2005, organizacje tworzące ILCOR będą publikowały własne wytyczne resuscytacji, spójne z wiedzą zawartą w dokumencie uzgodnieniowym z uwzględnieniem geograficznych, ekonomicznych i systemowych różnic dotyczących praktyki oraz dostępności urządzeń medycznych i leków. Wytyczne resuscytacji 2010 ERC wywodzą się z do-
9 Podsumowanie Komitetu Wykonawczego ERC 11 kumentu 2010 Consensus on Science with Treatment Recommendations (CoSTR), ale prezentują konsensus osiągnięty przez Komitet Wykonawczy ERC. Komitet Wykonawczy ERC uważa, że te nowe zalecenia są najbardziej efektywne i najłatwiejsze do przyswojenia oraz przemawia za nimi aktualna wiedza, badania naukowe i doświadczenie. Nieuchronnie, nawet w Europie, różnice w dostępności leków, sprzętu i personelu wymogą adaptację tych wytycznych na poziomie lokalnym, regionalnym i krajowym. Wiele zaleceń z Wytycznych resuscytacji 2005 ERC nie ulega zmianie w roku 2010, ponieważ nie opublikowano nowych badań albo nowe wyniki jedynie potwierdziły dostępne wcześniej dowody naukowe. Łańcuch przeżycia Działania wpływające na przeżycie osoby z nagłym zatrzymaniem krążenia zwane są łańcuchem przeżycia (ryc. 1.1). Pierwsze ogniwo tego łańcucha wskazuje znaczenie prewencji NZK i identyfikacji osób, u których istnieje ryzyko zatrzymania krążenia oraz wezwanie pomocy w nadziei, że wczesne leczenie może zapobiec zatrzymaniu krążenia. Środkowe ogniwa przedstawiają połączenie RKO i defibrylacji jako najważniejszych elementów wczesnego etapu resuscytacji, której celem jest przywrócenie życia. Natychmiastowe podjęcie RKO może podwoić lub potroić przeżycie w pozaszpitalnym zatrzymaniu krążenia w mechanizmie VF Lepiej prowadzić RKO z wyłącznym uciskaniem klatki piersiowej, niż w ogóle nie podejmować RKO 46,47. W przypadku pozaszpitalnych zatrzymań krążenia w mechanizmie VF, RKO i defibrylacja w ciągu 3 5 minut od utraty przytomności mogą zwiększyć przeżycie do 49 75% Każda minuta opóźnienia przed defibrylacją zmniejsza prawdopodobieństwo przeżycia do wypisu ze szpitala o 10 12% 42,56. Ostatnie ogniwo łańcucha przeżycia, efektywna opieka poresuscytacyjna, ma na celu zachowanie funkcji, w szczególności mózgu i serca. Obecnie w warunkach szpitalnych powszechnie uznaje się wagę wczesnego rozpoznania krytycznie chorych pacjentów i aktywacji zespołu resuscytacyjnego z leczeniem ukierunkowanym na zapobieganie zatrzymaniu krążenia 6. W ciągu ostatnich kilku lat rośnie znaczenie leczenia w fazie poresuscytacyjnej, przedstawione w czwartym ogniwie łańcucha przeżycia 3. Różnice postępowania w tej fazie mogą być przyczyną obserwowanej między szpitalami zmienności wyników leczenia po zatrzymaniu krążenia BLS u osób dorosłych kolejność postępowania W poniższym rozdziale termin poszkodowany odnosi się zarówno do kobiet, jak i mężczyzn. Podstawowe zabiegi resuscytacyjne polegają na wykonaniu następującej sekwencji działań (ryc. 1.2): 1. Upewnij się, że ty, poszkodowany i wszyscy świadkowie zdarzenia jesteście bezpieczni. 2. Sprawdź reakcję poszkodowanego: delikatnie potrząśnij za ramiona i głośno zapytaj: Czy wszystko w porządku? 3a. Jeżeli reaguje: zostaw poszkodowanego w pozycji, w której go zastałeś, o ile nie zagraża mu żadne niebezpieczeństwo, dowiedz się jak najwięcej o stanie poszkodowanego i wezwij pomoc, jeśli będzie potrzebna, regularnie oceniaj jego stan. 3b. Jeżeli nie reaguje: głośno zawołaj o pomoc, odwróć poszkodowanego na plecy, a następnie udrożnij jego drogi oddechowe, wykonując odgięcie głowy i uniesienie żuchwy, umieść jedną rękę na czole poszkodowanego i delikatnie odegnij jego głowę do tyłu, opuszki palców drugiej ręki umieść na żuchwie poszkodowanego, a następnie unieś ją w celu udrożnienia dróg oddechowych. 4. Utrzymując drożność dróg oddechowych wzrokiem, słuchem i dotykiem oceń oddech: oceń wzrokiem ruchy klatki piersiowej, 1 Ryc Łańcuch przeżycia
10 12 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Podstawowe zabiegi resuscytacyjne u osób dorosłych Głośno wołaj o pomoc Udrożnij drogi oddechowe i sprawdź oddech NIE ODDYCHA PRAWIDŁOWO? Ryc Algorytm BLS u dorosłych sekwencja postępowania nasłuchuj przy ustach poszkodowanego szmerów oddechowych, staraj się wyczuć ruch powietrza na swoim policzku, podejmij decyzję, czy oddech jest prawidłowy, nieprawidłowy lub nieobecny. W pierwszych minutach zatrzymania krążenia poszkodowany może słabo oddychać lub wykonywać nieregularne, wolne i głośne westchnięcia (gasping). Nie należy ich mylić z prawidłowym oddechem. Na ocenę prawidłowego oddechu za pomocą wzroku, słuchu i dotyku przeznacz nie więcej niż 10 sekund. W przypadku jakichkolwiek wątpliwości dotyczących prawidłowego oddechu działaj tak, jakby był nieprawidłowy. 5a. Jeżeli oddech jest prawidłowy: ułóż poszkodowanego w pozycji bezpiecznej (patrz poniżej), wyślij kogoś lub sam udaj się po pomoc zadzwoń pod numer 112 lub lokalny numer ratunkowy (999 przyp. tłum.), aby wezwać karetkę pogotowia, regularnie oceniaj, czy oddech nadal jest prawidłowy. 5b. Jeżeli oddech poszkodowanego jest nieprawidłowy lub nieobecny: poproś kogoś o wezwanie pomocy oraz znalezienie i przyniesienie AED, jeśli jest dostępne. Jeżeli jesteś sam, użyj telefonu komórkowego w celu wezwania pogotowia ratunkowego. Pozostaw poszkodowanego tylko wtedy, gdy nie ma innej możliwości wezwania pomocy. rozpocznij uciśnięcia klatki piersiowej poszkodowanego zgodnie z poniższym opisem: uklęknij obok poszkodowanego, ułóż nadgarstek jednej ręki na środku jego klatki piersiowej (dolna połowa mostka poszkodowanego), ułóż nadgarstek drugiej dłoni na grzbiecie dłoni leżącej na klatce piersiowej poszkodowanego, spleć palce obu dłoni i upewnij się, że nacisk nie będzie kierowany na żebra poszkodowanego. Utrzymuj ramiona wyprostowane. Nie uciskaj górnej części brzucha ani dolnego końca mostka, ustaw się pionowo nad klatką piersiową poszkodowanego i uciskaj mostek na głębokość nie mniejszą niż 5 cm (ale nie przekraczaj 6 cm), po każdym uciśnięciu zwolnij nacisk na klatkę piersiową nie odrywając rąk od mostka. Powtarzaj uciśnięcia z częstotliwością co najmniej 100/min (ale nie przekraczając 120/min), czas uciśnięcia i zwalniania ucisku na mostek powinny być równe. 6a. Połącz uciśnięcia klatki piersiowej z oddechami ratowniczymi: po wykonaniu 30 uciśnięć klatki piersiowej ponownie udrożnij drogi oddechowe poszkodowanego, odchylając jego głowę i unosząc żuchwę, zaciśnij skrzydełka nosa poszkodowanego, używając palca wskazującego i kciuka dłoni umieszczonej na jego czole, pozostaw usta poszkodowanego lekko otwarte, jednocześnie utrzymując uniesienie żuchwy, weź normalny wdech i obejmij szczelnie usta poszkodowanego swoimi ustami, upewniając się, że nie ma przecieku powietrza, wdmuchuj powietrze do ust poszkodowanego jednostajnie przez około 1 sekundę, jak przy normalnym oddychaniu, obserwując jednocześnie, czy klatka piersiowa się unosi jest to skuteczny oddech ratowniczy, utrzymując odgięcie głowy i uniesienie żuchwy, odsuń swoje usta od ust poszkodowanego i obserwuj, czy podczas wydechu opada jego klatka piersiowa, jeszcze raz nabierz powietrza i wdmuchnij je do ust poszkodowanego, dążąc do wykonania dwóch skutecznych oddechów ratowniczych. Dwa oddechy ratownicze nie powinny w sumie trwać dłużej niż 5 sekund. Następnie bez opóźnienia ułóż ponownie dłonie w prawidłowej pozycji na mostku poszkodowanego i wykonaj kolejnych 30 uciśnięć klatki piersiowej, kontynuuj uciśnięcia klatki piersiowej i oddechy ratownicze w stosunku 30 : 2, przerwij swoje działania w celu sprawdzenia stanu poszkodowanego tylko wtedy, gdy zaczyna reagować: poruszy się, otworzy oczy lub zacznie prawidłowo oddychać. W przeciwnym razie nie przerywaj resuscytacji.
11 Podsumowanie Komitetu Wykonawczego ERC 13 Jeżeli pierwszy oddech ratowniczy nie spowoduje uniesienia się klatki piersiowej, jak przy prawidłowym oddychaniu, przed podjęciem kolejnej próby wykonaj następujące czynności: sprawdź jamę ustną poszkodowanego i usuń wszystkie ciała obce, potwierdź właściwe odchylenie głowy i uniesienie żuchwy, nie podejmuj więcej niż 2 próby wentylacji przed ponownym podjęciem uciśnięć klatki piersiowej. Jeżeli na miejscu zdarzenia jest więcej niż jeden ratownik, ratownicy powinni się zmieniać podczas prowadzenia RKO co 2 minuty, aby zapobiec zmęczeniu. Podczas zmian ratowników należy minimalizować przerwy w uciśnięciach klatki piersiowej. 6b. RKO z wyłącznym uciskaniem klatki piersiowej może być zastosowana uwzględniając poniższe: jeżeli ratownik nie posiada przeszkolenia lub nie chce wykonywać oddechów ratowniczych, jeżeli prowadzona jest RKO z wyłącznym uciskaniem klatki piersiowej, powinna ona być wykonywana bez przerw, z częstotliwością co najmniej 100/min (ale nie przekraczając 120/min). 7. Nie przerywaj resuscytacji do momentu: przybycia wykwalifikowanych służb medycznych i przejęcia przez nie działania, gdy poszkodowany zacznie reagować: poruszy się, otworzy oczy lub zacznie prawidłowo oddychać, wyczerpania własnych sił. Rozpoznanie zatrzymania krążenia i oddychania Sprawdzanie tętna na tętnicy szyjnej (lub innej tętnicy) nie jest dokładną metodą potwierdzania obecności lub braku krążenia zarówno dla ratowników bez wykształcenia medycznego, jak i personelu medycznego Zarówno personel medyczny, jak i ratownicy bez wykształcenia medycznego mają trudności z określeniem obecności prawidłowego oddechu lub jego braku u nieprzytomnych poszkodowanych 67,68. Może to być wynikiem wykonywania przez poszkodowanego pojedynczych (agonalnych) westchnięć (gasping), występujących u blisko 40% poszkodowanych w ciągu pierwszych minut zatrzymania krążenia 69. Dlatego ratowników bez wykształcenia medycznego należy nauczać, by rozpoczynali RKO, gdy poszkodowany jest nieprzytomny (nie reaguje) i nie oddycha prawidłowo. W trakcie szkolenia należy podkreślać, iż agonalne westchnięcia stanowią wskazanie do natychmiastowego rozpoczęcia RKO. Wstępne oddechy ratownicze U osób dorosłych wymagających RKO jako pierwotną przyczynę zatrzymania krążenia zakłada się a priori chorobę serca. RKO należy rozpoczynać od uciśnięć klatki piersiowej, a nie od wykonywania wstępnych oddechów ratowniczych. Nie należy tracić czasu na poszukiwanie ciał obcych podczas inspekcji jamy ustnej, chyba że oddech ratunkowy nie spowoduje uniesienia się klatki piersiowej. Wentylacja Podczas RKO optymalna objętość oddechowa, częstość oddechów, jak i stężenie tlenu w mieszaninie oddechowej niezbędne dla osiągnięcia właściwego utlenowania i eliminacji CO 2 nie są w pełni poznane. W trakcie RKO przepływ krwi przez płuca jest znacznie zmniejszony, dlatego właściwy stosunek wentylacji do perfuzji może być osiągnięty przy objętości i częstości oddechu mniejszych niż prawidłowe 70. Hiperwentylacja jest szkodliwa, ponieważ zwiększa ciśnienie w klatce piersiowej, przez co obniża powrót krwi żylnej do serca, redukując jego rzut. Z kolei przerwy w uciskaniu klatki piersiowej obniżają przeżywalność 71. Ratownicy powinni wykonywać każdy wdech w ciągu około 1 sekundy, z objętością wystarczającą do spowodowania widocznego uniesienia się klatki piersiowej. Równocześnie należy unikać szybkich i forsownych wdechów. Czas konieczny do wykonania dwóch oddechów ratowniczych nie powinien przekraczać 5 sekund. To zalecenie dotyczy wszystkich technik wentylacji w trakcie RKO, zarówno usta usta, jaki i za pomocą worka samorozprężalnego z maską twarzową, niezależnie od podaży tlenu. Uciśnięcia klatki piersiowej Uciśnięcia klatki piersiowej generują niewielki, ale krytycznie ważny przepływ krwi przez mózg i mięsień sercowy, zwiększając prawdopodobieństwo skutecznej defibrylacji. Optymalna technika uciśnięć klatki piersiowej obejmuje: częstotliwość uciśnięć co najmniej 100/min i głębokość uciśnięć co najmniej 5 cm (u osoby dorosłej), ale nie przekraczając 6 cm, powrót klatki piersiowej do wyjściowego kształtu po każdym jej uciśnięciu 72,73 oraz porównywalny czas fazy kompresji i relaksacji. Aby uzyskać rekomendowaną częstość i głębokość uciśnięć, ratownik może być wspomagany uzyskiwaną na bieżąco informacją zwrotną przekazywaną przez urządzenia wbudowane w AED, defibrylatory manualne lub będące oddzielnym sprzętem używanym w trakcie resuscytacji. RKO z wyłącznym uciskaniem klatki piersiowej Niezależnie od wykształcenia medycznego ratownicy przyznają, że niechętnie podjęliby wentylację usta usta, szczególnie u nieznanych osób z zatrzymaniem krążenia 74,75. Doświadczenia na zwierzętach pokazały, iż wyłączne uciśnięcia klatki piersiowej mogą być w pierwszych minutach zatrzymania krążenia tak samo efektywne, jak te prowadzone w połączeniu z wentylacją, pod warunkiem że przyczyną zatrzymania krążenia nie była asfiksja 76,77. Jeżeli drogi oddechowe są udrożnione, pojedyncze westchnienia (gasping) i bierne odkształcenie klatki piersiowej po jej uciśnięciu powodują niewielką wymianę powietrza, ale dotyczy ona wyłącznie przestrzeni martwej 69, Badania na zwierzętach i modele matematyczne wykazały, że podczas uciskania klatki piersiowej bez wykonywania oddechów ratowniczych znajdujące się we krwi tętniczej rezerwy tlenu wyczerpują się po 2 4 minutach 81,82. Przeżywalność dorosłych z zatrzymaniem krążenia niespowodowanym asfiksją, kiedy podjęto RKO z wyłącznym uciskaniem klatki piersiowej, jest znacząco wyższa w porównaniu z grupą, w której RKO nie została podjęta 46,47. Kilka badań dotyczących zatrzymań krążenia u ludzi sugeruje równorzędność RKO z wyłącznym uciskaniem klatki piersiowej w porównaniu z resuscytacją prowadzoną wraz z oddechami ratowniczymi. Równocześnie żadne z tych badań nie wyklucza możliwości, że RKO z wyłącznym uciskaniem 1
12 14 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 klatki piersiowej jest mniej skuteczna 47,83. RKO z wyłącznym uciskaniem klatki piersiowej może być skuteczna tylko w pierwszych kilku minutach po utracie przytomności. RKO z wyłącznym uciskaniem klatki piersiowej nie jest tak skuteczna, jak standardowa RKO w przypadkach zatrzymań krążenia spowodowanych inną przyczyną niż choroba serca (np. tonięcie, uduszenie) u dorosłych oraz dzieci 84,85. Prowadzenie RKO polegającej na uciskaniu klatki piersiowej w połączeniu z oddechami ratowniczymi jest metodą z wyboru zarówno dla personelu medycznego, jak i osób przeszkolonych. Pozostałe osoby udzielające pomocy powinny być zachęcane do prowadzenia RKO z wyłącznym uciskaniem klatki piersiowej w sytuacji, gdy nie mogą lub nie chcą podejmować oddechów ratowniczych, lub kiedy wykonują resuscytację instruowani telefonicznie przez dyspozytora pogotowia ratunkowego. Zagrożenia dla ratownika Wysiłek fizyczny Częstość występowania niepożądanych reakcji u ratowników podczas szkoleń, jak i rzeczywistej RKO (skurcze mięśniowe, bóle pleców, uczucie duszności, hiperwentylacja) jest bardzo mała 86. Kilka badań z wykorzystaniem manekinów wykazało, że w wyniku wyczerpania ratownika głębokość uciśnięć klatki piersiowej może zacząć spadać już po dwóch minutach prowadzenia resuscytacji 87. Dlatego ratownicy powinni się zmieniać co dwie minuty, aby zapobiec spadkowi jakości uciśnięć klatki piersiowej, który wynika ze zmęczenia ratownika. Zmiana ratownika nie powinna przerywać uciskania klatki piersiowej. Zagrożenia w czasie defibrylacji Duże randomizowane badania nad programami publicznego dostępu do defibrylacji pokazały, że AED mogą być używane bezpiecznie przez ratowników niezależnie od ich poziomu wyszkolenia 88. Systematyczny przegląd wszystkich dostępnych źródeł wykazał tylko osiem prac opisujących w sumie 29 przypadków powikłań związanych z wykonywaniem defibrylacji 89. Tylko jedno z tych zdarzeń zostało opisane po 1997 roku 90. Przenoszenie chorób Opisano bardzo mało przypadków, kiedy prowadzenie RKO wiązało się z transmisją choroby. Trzy badania przeprowadzone w kontrolowanych warunkach laboratoryjnych wykazały skuteczność sprzętu ochronnego w ograniczaniu transmisji bakterii podczas RKO 91,92. Jednak bardzo niskie ryzyko zakażenia uzasadnia prowadzenie oddechów ratowniczych bez tego typu narzędzi. Jeżeli wiadomo, że poszkodowany ma ciężką infekcję, zaleca się stosowanie odpowiednich środków ostrożności. Pozycja bezpieczna Istnieje kilka wariantów pozycji bezpiecznej, każdy z nich ma swoje zalety. Żadna z pozycji nie jest idealna dla wszystkich poszkodowanych 93,94. Pozycja powinna być stabilna, jak najbliższa ułożeniu na boku z podparciem głowy i brakiem ucisku na klatkę piersiową, by nie utrudniać oddechu 95. Niedrożność dróg oddechowych spowodowana ciałem obcym (zadławienie) Niedrożność dróg oddechowych spowodowana ciałem obcym (Foreign-Body Airway Obstruction FBAO) jest rzadką, potencjalnie uleczalną przyczyną przypadkowej śmierci 96. Objawy pozwalające na różnicowanie łagodnej i ciężkiej niedrożności zostały przedstawione w tabeli 1.1. Sekwencję postępowania w zadławieniu u osób dorosłych przedstawiono na ryc Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja, elektrostymulacja Automatyczne defibrylatory zewnętrzne Automatyczne defibrylatory zewnętrzne (AED) są bezpieczne i efektywne w użyciu zarówno przez ratowników bez wykształcenia medycznego, jak i osoby z wykształceniem medycznym (w warunkach wewnątrz- i pozaszpitalnych). Użycie AED przez ratowników bez wykształcenia medycznego daje możliwość wykonania defibrylacji wiele minut przed przybyciem pomocy medycznej. Sekwencja użycia AED Algorytm ERC użycia AED przedstawiono na ryc Upewnij się, że ty, poszkodowany i pozostali świadkowie zdarzenia jesteście bezpieczni. 2. Postępuj zgodnie z algorytmem BLS dla osób dorosłych: jeśli poszkodowany jest nieprzytomny i nie oddycha prawidłowo, poproś kogoś o wezwanie pomocy i o znalezienie i przyniesienie AED, jeśli jest dostępne; jeżeli jesteś sam, użyj telefonu komórkowego w celu wezwania pogotowia ratunkowego pozostaw poszkodowanego tylko, jeżeli nie ma innej możliwości wezwania pomocy. Tabela 1.1. Różnicowanie ciężkiej i łagodnej niedrożności dróg oddechowych spowodowanej ciałem obcym (FBAO) a Objaw Łagodna niedrożność Ciężka niedrożność Czy się zadławiłeś? Inne objawy Tak Może mówić, kaszleć, oddychać Nie może mówić, może kiwać głową Nie może oddychać / świsty oddechowe / ciche próby kaszlu / nieprzytomny a Ogólne objawy FBAO: objawy występują podczas jedzenia; poszkodowany może trzymać się za szyję.
13 Podsumowanie Komitetu Wykonawczego ERC 15 Postępowanie w zadławieniu u dorosłych 1 poszkodowanego i wystąpienia nieefektywnego kaszlu Ryc Algorytm postępowania w zadławieniu u dorosłych 3. Rozpocznij RKO zgodnie z algorytmem BLS dla osób dorosłych. Jeżeli jesteś sam, a AED jest bezpośrednio dostępne, użyj go. 4. Gdy tylko pojawi się AED: włącz go i naklej elektrody na odsłoniętą klatkę piersiową poszkodowanego; jeżeli jest więcej niż jeden ratownik, RKO powinna być kontynuowana podczas naklejania elektrod; natychmiast rozpocznij postępowanie zgodnie z poleceniami głosowymi/wizualnymi; upewnij się, że nikt nie dotyka poszkodowanego podczas analizy rytmu przez AED. 5a. Jeżeli wyładowanie jest wskazane: upewnij się, że nikt nie dotyka poszkodowanego; naciśnij przycisk wyładowania zgodnie z poleceniem; natychmiast rozpocznij RKO 30 : 2; kontynuuj postępowanie zgodnie z poleceniami głosowymi/wizualnymi. 5b. Jeżeli wyładowanie nie jest wskazane: natychmiast podejmij RKO, używając sekwencji 30 uciśnięć do 2 oddechów ratowniczych; kontynuuj postępowanie zgodnie z poleceniami głosowymi/wizualnymi. 6. Kontynuuj działania zgodnie z poleceniami AED do czasu: przybycia wykwalifikowanych służb medycznych i przejęcia przez nie działania; gdy poszkodowany zacznie reagować: poruszy się, otworzy oczy lub zacznie prawidłowo oddychać; wyczerpania własnych sił. Programy publicznego dostępu do defibrylacji Wprowadzanie programów AED powinno być szczególnie rozważane w miejscach publicznych, takich jak lotniska 52, centra sportowe, biura, kasyna 55 oraz w samolotach 53, gdzie zatrzymanie krążenia jest z reguły zauważone, a przeszkoleni ratownicy szybko przybywają na miejsce zdarzenia. Badania opisujące programy AED dla ratowników bez wykształcenia medycznego, ale z bardzo krótkim czasem dotarcia do poszkodowanego oraz badania prowadzone bez próby kontrolnej, w których udzielającymi pierwszej pomocy byli policjanci 97,98, wykazały przeżywalność NZK na poziomie 49% 74%. Dotychczas nie wykorzystano pełnego potencjału AED, ponieważ w większości przypadków używa się ich w miejscach publicznych, a w 60 80% do NZK dochodzi w domach prywatnych. Programy publicznego dostępu do defibrylacji (Public Access Defibrillation PAD) i programy AED dla służb kwalifikowanej pierwszej pomocy mogą zwiększyć ilość osób, którym świadkowie udzielą pierwszej pomocy oraz wykonają wczesną defibrylację, dzięki czemu zwiększy się przeżywalność w pozaszpitalnym NZK 99. Ostatnie ogólnokrajowe badania w Japonii i USA 33,100 wykazały, że gdy AED było dostępne, wykonywano defibrylację znacznie wcześniej, co zwiększało szansę przeżycia poszkodowanego. Programy AED, w których te urządzenia były dostępne w obrębie osiedli mieszkalnych, nie zostały jeszcze ocenione. Udowodniono, iż umieszczanie AED w domach prywatnych, nawet u osób ze zwiększonym ryzykiem NZK, jest nieefektywne 101. Użycie AED w warunkach wewnątrzszpitalnych Do czasu 2010 Consensus on CPR Science Conference nie opublikowano żadnych randomizowanych badań porównujących wewnątrzszpitalne użycie AED z defibrylatorami manualnymi. Dwa badania o niższym stopniu wiarygodności, oceniające wewnątrzszpitalne zatrzymania krążenia w rytmach defibrylacyjnych u osób dorosłych wykazały wyższą przeżywalność do wypisu ze szpitala, gdy funkcjonował program AED w porównaniu z wyłącznym użyciem defibrylatora manualnego 102,103. Mimo ograniczonych dowodów powinno się rozważyć umieszczanie AED w oddziałach szpitalnych celem umożliwienia jak najszybszej defibrylacji (<3 min od utraty przytomności) szczególnie w miejscach,
14 16 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Postępowanie z użyciem AED reagować: poruszać się, otwierać oczy, oddychać prawidłowo Ryc Algorytm postępowania z użyciem AED gdzie personel medyczny nie posiada umiejętności rozpoznawania rytmów lub używa defibrylatorów bardzo rzadko. W takich miejscach powinno się wdrożyć efektywny system szkoleń i szkoleń przypominających 104. Należy przeszkolić taką ilość personelu, która umożliwi wykonanie defibrylacji w każdym miejscu w szpitalu przed upływem trzech minut od utraty przytomności. W szpitalach powinno się monitorować czas od utraty przytomności do wykonania pierwszej defibrylacji, jak również odległe wyniki resuscytacji. Porównanie defibrylacji manualnej z trybem półautomatycznym Wiele AED posiada zarówno tryb manualny, jak i półautomatyczny, niewiele jednak badań porównało te dwie opcje. Wykazano, iż użycie trybu półautomatycznego skraca czas do wykonania pierwszej defibrylacji w warunkach tak wewnątrzszpitalnych 105, jak pozaszpitalnych 106, zwiększa częstość konwersji VF 106 oraz zmniejsza ilość defibrylacji bez wskazań 107. Równocześnie użycie trybu półautomatycznego skraca czas wykonywania uciśnięć klatki piersiowej 107,108, głównie ze względu na dłuższy czas konieczny do automatycznej oceny rytmu przed defibrylacją. Mimo tych odmienności żadne badanie nie wykazało różnicy w osiągnięciu ROSC, przeżywalności czy częstości wypisów ze szpitala 105,106,109. Użycie właściwego trybu defibrylacji tak, by była ona najefektywniejsza, będzie zależeć od organizacji systemu ratownictwa, umiejętności, wyszkolenia oraz zdolności rozpoznawania rytmów przez udzielających pomocy. Krótsza przerwa przed wykonaniem defibrylacji, jak i całkowity czas bez uciśnięć klatki piersiowej zwiększają perfuzję życiowo ważnych narządów oraz możliwość osiągnięcia ROSC 71,110,111. W trakcie używania defibrylatorów manualnych, jak i niektórych AED możliwe jest wykonywanie uciśnięć klatki piersiowej podczas ładowania urządzenia, przez co przerwa przed wykonaniem defibrylacji może zostać skrócona do czasu poniżej 5 sekund. Przeszkoleni ratownicy mogą wykonywać wyładowanie w trybie manualnym, wymaga to jednak bezwzględnie częstego szkolenia zespołowego oraz umiejętności rozpoznawania rytmów serca. Postępowanie przed defibrylacją Skracanie przerwy przed wykonaniem defibrylacji Czas pomiędzy przerwaniem uciśnięć klatki piersiowej a wykonaniem defibrylacji (przerwa przeddefibrylacyjna) musi być absolutnie skrócony do minimum; nawet
15 Podsumowanie Komitetu Wykonawczego ERC sekundowa przerwa zmniejsza szanse na skuteczność defibrylacji 71,110,112. Przerwa przeddefibrylacyjna może być z łatwością skrócona poniżej 5 sekund poprzez kontynuację uciśnięć klatki piersiowej w trakcie ładowania defibrylatora oraz pod warunkiem sprawnej pracy zespołu koordynowanej przez lidera posiadającego umiejętność efektywnej komunikacji. Ocena bezpieczeństwa, by upewnić się, że nikt nie dotyka poszkodowanego podczas defibrylacji, powinna być przeprowadzona szybko, ale i skutecznie. Ryzyko przypadkowego porażenia prądem jest minimalizowane jeszcze bardziej, gdy wszyscy ratownicy mają założone rękawiczki 113. Przerwa po defibrylacji powinna być zminimalizowana przez jak najszybsze podjęcie uciśnięć klatki piersiowej (patrz poniżej). Cała procedura defibrylacji powinna być przeprowadzona tak, aby przerwa w uciśnięciach klatki piersiowej trwała mniej niż 5 sekund. Porównanie elektrod samoprzylepnych z łyżkami defibrylatora Użycie elektrod samoprzylepnych celem monitorowania czy defibrylacji posiada praktyczne zalety w stosunku do łyżek defibrylatora Są one bezpieczniejsze i bardziej efektywne w porównaniu ze standardowymi łyżkami defibrylatora 119. Analiza kształtu fali migotania Możliwe jest, z różną wiarygodnością, przewidywanie efektywności defibrylacji na podstawie kształtu fali migotania Jeśli w badaniach prospektywnych uda się określić optymalny kształt fali migotania oraz optymalny czas dostarczenia wyładowania, powinno być możliwe zapobieżenie dostarczania nieefektywnych wyładowań wysoką energią, a tym samym zminimalizowanie uszkodzenia miokardium. Takie technologie są wciąż badane i znajdują się na różnym etapie rozwoju, jednak ich dotychczasowa czułość i specyficzność jest niewystarczająca, by wprowadzić analizę kształtu fali VF do praktyki klinicznej. RKO przed defibrylacją W kilku badaniach sprawdzono, czy RKO wykonywane przed defibrylacją przynosi korzyści, zwłaszcza u pacjentów, u których doszło do niezauważonego zatrzymania krążenia, bądź u pacjentów z wydłużonym czasem od utraty przytomności do rozpoczęcia resuscytacji. Dostępne podczas opracowywania Wytycznych resuscytacji 2005 dane wskazywały, iż zasadne może być podjęcie przez zespół ratownictwa medycznego około 2 minut RKO przed defibrylacją u pacjentów z przedłużoną utratą przytomności (>5 minut) 140. Te rekomendacje były oparte na badaniach klinicznych. Wykazały one, że u dorosłych z pozaszpitalnym zatrzymaniem krążenia w mechanizmie VF lub VT, u których czas dotarcia do pacjenta (response time) przekroczył 4 5 minut, okres 1,5- do 3-minutowej RKO przed wykonaniem defibrylacji zwiększał częstość ROSC, przeżywalność do wypisu ze szpitala 141,142, a także przeżywalność jednoroczną 142 w porównaniu do defibrylacji wykonanej natychmiast po przybyciu zespołu. Ostatnio przeprowadzone dwa randomizowane, kontrolowane badania kliniczne wykazały, że okres 1,5- do 3-minutowej RKO prowadzonej przez zespół ratownictwa medycznego przed wykonaniem defibrylacji u pacjentów z pozaszpitalnym VF czy VT bez tętna, bez względu na czas rozpoczęcia reanimacji, nie poprawia ROSC czy przeżywalności do wypisu ze szpitala 143,144. Cztery pozostałe badania również nie wykazały znaczącego wzrostu częstości ROSC czy przeżywalności do wypisu ze szpitala przy wprowadzeniu wstępnego RKO przed wykonaniem defibrylacji 141,142,145,146, z wyjątkiem jednego, w którym uzyskano częstszą poprawę stanu neurologicznego 30 dni oraz rok od epizodu zatrzymania krążenia 145. Zostało jednak wykazane, że wykonywanie uciśnięć klatki piersiowej podczas podłączania i ładowania defibrylatora zwiększa prawdopodobieństwo przeżycia NZK 147. W każdym przypadku niezauważonego zatrzymania krążenia zespół ratownictwa medycznego powinien prowadzić dobrej jakości uciśnięcia klatki piersiowej podczas uruchamiania, podłączania i ładowania defibrylatora, jednak niezalecany jest jakikolwiek określony czas wykonywania RKO przed analizą rytmu i wykonaniem defibrylacji (np. 2 czy 3 minuty). Niektóre zespoły ratownictwa medycznego wypracowały standardową procedurę prowadzenia uciśnięć klatki piersiowej przez ustalony czas przed wykonaniem defibrylacji; ze względu na brak przekonujących danych potwierdzających bądź negujących tę strategię zasadne wydaje się kontynuowanie tej praktyki. Wykonanie defibrylacji Porównanie pojedynczej defibrylacji z sekwencją trzech defibrylacji Przerwy w uciskaniu klatki piersiowej zmniejszają szansę na konwersję VF do innego rytmu 71. Badania wykazały, iż całkowity czas bez wykonywania uciśnięć klatki piersiowej jest znacznie krótszy przy stosowaniu pojedynczych defibrylacji, niż przy stosowaniu sekwencji trzech defibrylacji 148. Niektóre badania , jednak nie wszystkie 148,152, sugerują znaczną poprawę przeżywalności przy zastosowaniu strategii pojedynczych defibrylacji. Gdy defibrylacja jest wskazana, należy wykonać pojedynczą defibrylację i natychmiast podjąć uciśnięcia klatki piersiowej. Nie powinno się opóźniać rozpoczęcia RKO poświęcając czas na ocenę rytmu czy sprawdzanie tętna bezpośrednio po defibrylacji. Należy kontynuować RKO (30 uciśnięć : 2 wdechy) przez dwie minuty aż do kolejnej analizy rytmu i wykonania kolejnej defibrylacji (jeśli wskazana) (zob. rozdział 4. Zaawansowane zabiegi resuscytacyjne) 6. Należy rozważyć dostarczenie do trzech wyładowań z rzędu przed rozpoczęciem uciśnięć klatki piersiowej, jeśli VF/VT wystąpi podczas cewnikowania serca lub we wczesnym okresie pooperacyjnym w zabiegach kardiochirurgicznych (gdy uciśnięcia klatki piersiowej mogłyby uszkodzić szwy naczyniowe) (zob. rozdział 8, dotyczący sytuacji szczególnych) 10. Ta strategia potrójnej defibrylacji może być również rozważona przy zauważonym zatrzymaniu krążenia w VF/VT u pacjentów podłączonych już do defibrylatora manualnego. Mimo że nie ma danych potwierdzających skuteczność tej strategii w wymienionych sytuacjach, mało prawdopodobnym jest, by uciśnięcia klatki piersiowej poprawiły i tak bardzo wysoką szansę na powrót spontanicznego krążenia, gdy wykonuje się defibrylację wcześnie w fazie elektrycznej, natychmiast po pojawieniu się VF. 1
16 18 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Kształt fal energii defibrylacji Defibrylatory jednofazowe zostały już wycofane z produkcji, mimo to wiele z nich pozostanie w użytku jeszcze przez kilka lat. Zastępuje się je defibrylatorami dwufazowymi. Porównanie defibrylacji jednofazowej i dwufazowej Fale dwufazowe efektywniej leczą komorowe zaburzenia rytmu przy niższych wartościach energii, wykazują większą skuteczność pierwszego wyładowania w porównaniu z falą jednofazową oraz większą skuteczność pierwszej defibrylacji dla długotrwającego VF/VT Żadne randomizowane badania nie wykazały przewagi którejkolwiek z fal, kiedy oceniano stopień ubytków neurologicznych przy wypisie ze szpitala. Fale dwufazowe mają przewagę nad jednofazowymi podczas planowych kardiowersji migotania przedsionków, wykazują większą ogólną skuteczność przy użyciu niższej energii, zmniejszając przez to ciężkość oparzeń skóry , dlatego są falą z wyboru dla tej procedury. Wartości energii (prądu defibrylacji) Nieznana jest optymalna wartość energii zarówno dla fali jednofazowej, jak i dwufazowej. Rekomendacje dla wartości energii opierają się na porozumieniu powstałym po dokładnej analizie obowiązującej literatury. Pierwsza defibrylacja Od czasu publikacji Wytycznych 2005 nie pojawiły się żadne badania określające optymalną wartość energii dla fali jednofazowej. Przez ostatnie pięć lat ukazało się bardzo niewiele badań nad falami dwufazowymi, które mogłyby udoskonalić Wytyczne Nie ma dowodów, by konkretny kształt fali dwufazowej czy model urządzenia był bardziej efektywny od pozostałych. Skuteczność pierwszego wyładowania przy użyciu fali dwufazowej ściętej wykładniczo (BTE), energią J została określona na poziomie 86 98% 153,154, Skuteczność fali dwufazowej rektalinearnej (RLB) podczas pierwszej defibrylacji przy użyciu energii 120 J wynosi 85% (dane przekazane ustnie przez personel, niepublikowane) 155. Dwa badania wykazały równoważność niższej i wyższej wartości energii początkowej defibrylacji dwufazowej 163,164. Mimo że badania u ludzi nie wykazały uszkodzeń (podwyższenie biomarkerów, zmiany w EKG, zmiany frakcji wyrzutowej) spowodowanych którąkolwiek z fal dwufazowych o energii do 360 J 163,165, niektóre badania na zwierzętach sugerują zwiększone ryzyko uszkodzeń wraz ze wzrostem energii Energia dwufazowa wyładowania początkowego nie powinna być niższa niż 120 J dla fali RLB oraz 150 J dla fali BTE. Idealnie energia pierwszej defibrylacji dla każdej fali dwufazowej powinna wynosić co najmniej 150 J. Druga i kolejne defibrylacje Wytyczne 2005 zalecały, by do defibrylacji używać stałej lub stopniowo zwiększanej energii i nie ma dowodów naukowych, aby te zalecenia zmienić. Kardiowersja Gdy kardiowersja jest wykonywana w przedsionkowych lub komorowych zaburzeniach rytmu, konieczna jest synchronizacja wyładowania z załamkiem R elektrokardiogramu, a nie z załamkiem T: dostarczenie wyładowania w trakcie refrakcji względnej cyklu serca może doprowadzić do migotania komór 170. Do kardiowersji AF skuteczniejsze są fale dwufazowe niż jednofazowe Rozpoczynanie kardiowersji od wysokich energii nie poprawia jej skuteczności, w porównaniu z niższymi energiami 156, W oparciu o aktualne dane rozsądne jest rozpoczynanie od zsynchronizowanego wyładowania o energii J i zwiększanie jej w razie konieczności. Trzepotanie przedsionków oraz napadowy częstoskurcz nadkomorowy wymagają niższych wartości energii kardiowersji w porównaniu z migotaniem przedsionków 175. Należy rozpocząć od wyładowania energią 100 J dla defibrylatorów jednofazowych lub J dla defibrylatorów dwufazowych. Kolejne wyładowania wykonuje się stopniowo zwiększając energię 177. Energia potrzebna do kardiowersji VT zależy od morfologii i częstości arytmii 178. Do pierwszej kardiowersji energią dwufazową należy wybrać J. Jeśli pierwsze wyładowanie nie spowodowało powrotu rytmu zatokowego, do kolejnych kardiowersji należy rozważyć stopniowe zwiększanie energii 178. Elektrostymulacja Stymulację należy rozważyć u pacjentów z objawową bradykardią oporną na leki cholinergiczne lub inne sposoby leczenia (zob. rozdział 4. Zaawansowane zabiegi resuscytacyjne) 6. Natychmiastowa stymulacja jest wskazana szczególnie, jeżeli blok występuje na poziomie pęczka Hisa lub poniżej. Jeżeli stymulacja przezskórna jest nieefektywna, należy rozważyć stymulację elektrodą endokawitarną. Wszczepialne kardiowertery-defibrylatory Kardiowertery-defibrylatory (ICD) są wszczepiane pacjentom, u których występuje ryzyko lub którzy przebyli zagrażające życiu defibrylacyjne zaburzenia rytmu. Jeżeli urządzenie wykryje rytm wymagający wyładowania, impuls o energii około 40 J zostanie dostarczony za pośrednictwem elektrody umieszczonej w prawej komorze serca. Po wykryciu VF/VT ICD wykona nie więcej niż osiem wyładowań, ale jeśli rozpozna nowy epizod VF/VT, może się uruchomić na nowo. Wyładowanie ICD może spowodować skurcz mięśni piersiowych, ponadto opisano przypadki porażenia prądem ratowników udzielających pomocy 179. Ze względu na niską energię wyładowania mało prawdopodobne jest, aby ICD stanowiły zagrożenie dla ratownika, rozsądnym jest jednak stosowanie rękawiczek i minimalizowanie kontaktu z pacjentem podczas wyładowania. Zaawansowane zabiegi resuscytacyjne u osób dorosłych Zapobieganie wewnątrzszpitalnemu zatrzymaniu krążenia Wczesne rozpoznanie pogorszenia stanu pacjenta i prewencja zatrzymania krążenia stanowi pierwsze ogniwo łańcucha przeżycia 180. Mniej niż 20% pacjentów, u których doszło do wewnątrzszpitalnego zatrzymania krążenia, przeżyje do momentu wypisania ze szpitala 36,181,182. Prewencja we-
17 Podsumowanie Komitetu Wykonawczego ERC 19 wnątrzszpitalnego zatrzymania krążenia wymaga edukacji personelu medycznego, monitorowania pacjentów, rozpoznania pogorszenia stanu pacjenta oraz stworzenia systemu wzywania pomocy i skutecznej odpowiedzi na jej wezwanie 183. Problem Zatrzymanie krążenia występujące u pacjentów przebywających na oddziałach nieposiadających monitorowania nie jest zwykle ani zdarzeniem nagłym, ani spowodowanym przyczynami pierwotnie kardiologicznymi 184. W tej grupie pacjentów występuje zwykle wolne i postępujące pogorszenie stanu ogólnego, włączając w to hipoksemię i hipotensję, które są niezauważone przez personel medyczny lub pozostają rozpoznane, ale nieadekwatnie leczone U wielu z tych pacjentów dochodzi do niemonitorowanego zatrzymania krążenia, a leżący u jego podstaw rytm jest zwykle nie do defibrylacji 182,188. Liczba pacjentów przeżywających do wypisania ze szpitala jest mała 36,181,188. Edukacja dotycząca postępowania w stanach nagłych Edukacja personelu medycznego jest istotnym elementem implementacji systemu zapobiegania zatrzymaniu krążenia 189. W badaniu australijskim praktycznie cała poprawa dotycząca częstości występowania wewnątrzszpitalnego zatrzymania krążenia nastąpiła w czasie fazy edukacji związanej z wprowadzeniem zespołów resuscytacyjnych (MET) 190,191. Monitorowanie i rozpoznawanie pacjenta w ciężkim stanie W celu ułatwienia wczesnego wykrycia ciężkiego schorzenia u każdego pacjenta powinno się zaplanować schemat monitorowania podstawowych parametrów życiowych określający, jakie parametry i jak często powinny być oceniane 192. Aktualnie w wielu szpitalach, w celu identyfikacji pacjentów wymagających poszerzonego monitorowania, leczenia lub konsultacji specjalistycznej, stosowane są skale wczesnego ostrzegania (Early Warning Scores EWS) lub kryteria wezwania zespołu resuscytacyjnego (strategia track and trigger ) Postępowanie z pacjentem w ciężkim stanie Pacjetów w ciężkim stanie lub tym stanem zagrożonych zazwyczaj leczy zespół resuscytacyjny (Medical Emergency Team MET), zespół szybkiego reagowania (Rapid Response Team RRT) lub konsultacyjny zespół intensywnej terapii (Critical Care Outreach Team CCOT) Zespoły te współistnieją lub zamieniły tradycyjne zespoły resuscytacyjne, które typowo leczyły pacjentów, u których już doszło do zatrzymania krążenia. MET/RRT zwykle składają się z personelu lekarskiego i pielęgniarskiego pracującego na oddziałach intensywnej terapii i oddziałach ogólnych. Zespoły te są wzywane, gdy zostają spełnione określone kryteria wezwania. CCOT są zwykle złożone z personelu pielęgniarskiego działającego pojedynczo lub w zespołach 201. Ostatnie metaanalizy wykazały, że wdrożenie systemów RRT/ MET wiąże się z redukcją zatrzymań krążenia występujących poza OIT, lecz nie wykazano zmniejszenia śmiertelności wewnątrzszpitalnej 202. Zespoły resuscytacyjne odgrywają ważną rolę w poprawie decyzyjności dotyczącej końca życia i niepodejmowania resuscytacji (Do-Not-Attempt Resuscitation DNAR), co przynajmniej częściowo wyjaśnia zmniejszenie częstości występowania zatrzymania krążenia Wytyczne dotyczące zapobiegania wewnątrzszpitalnym zatrzymaniom krążenia Szpitale powinny wprowadzić system opieki obejmujący: (a) szkolenie personelu medycznego dotyczące objawów świadczących o pogarszaniu się stanu ogólnego pacjenta i zasadności wdrożenia szybkiego działania w celu jego poprawy, (b) właściwe i regularne monitorowanie podstawowych parametrów życiowych pacjenta, (c) przejrzyste wytyczne (np. poprzez kryteria wezwania lub skale wczesnego ostrzegania), by pomóc personelowi medycznemu we wczesnym rozpoznaniu pogorszenia stanu pacjenta, (d) prosty, jednolity system wzywania pomocy oraz (e) właściwą i zastosowaną o czasie odpowiedź na wezwanie pomocy 183. Poniższe strategie mogą zapobiec możliwym do uniknięcia wewnątrzszpitalnym zatrzymaniom krążenia: 1. Opiekę nad pacjentami krytycznie chorymi lub zagrożonymi pogorszeniem się stanu zdrowia należy prowadzić na właściwych oddziałach, gdzie jej poziom jest dostosowany do ciężkości stanu chorego. 2. Krytycznie chorzy pacjenci potrzebują regularnej obserwacji: każdy pacjent powinien posiadać udokumentowany plan monitorowania, definiujący jak często i jakie parametry życiowe powinny być monitorowane w zależności od ciężkości stanu pacjenta, prawdopodobieństwa pogorszenia jego stanu i wystąpienia zatrzymania krążenia. Ostatnio zaleca się monitorowanie prostych fizjologicznych zmiennych obejmujących tętno, ciśnienie tętnicze, częstość oddychania, poziom świadomości, temperaturę i saturację (SpO 2 ) 192, W celu identyfikacji pacjentów w krytycznym stanie i/lub zagrożonych pogorszeniem stanu ogólnego i zatrzymaniem krążenia należy zastosować system obserwuj i reaguj ( track and trigger ) (kryteria wezwania lub systemy wczesnego ostrzegania). 4. Należy stosować system karty pacjenta umożliwiający regularne pomiary i dokumentowanie wartości podstawowych parametrów życiowych oraz skal wczesnego ostrzegania jeśli są używane. 5. Należy opracować jasne i swoiste reguły postępowania klinicznego w odpowiedzi na nieprawidłowości parametrów fizjologicznych pacjenta, oparte na systemie obserwuj i reaguj. Powinny one zawierać zalecenia dotyczące dalszego leczenia i określać zakres obowiązków personelu lekarskiego i pielęgniarskiego. 6. W szpitalu powinien obowiązywać jasno określony schemat postępowania w stanach nagłych. Może to być wezwanie zespołu konsultującego lub zespołu resuscytacyjnego (np. MET, RRT) zdolnego do adekwatnego w czasie działania w odpowiedzi na nagłe pogorszenie stanu ogólnego identyfikowanego za pomocą systemu obserwuj i reaguj lub innych wskaźników. Zespół musi być dostępny 24 godziny na dobę i posiadać w swoim składzie osoby z odpowiednimi umiejętnościami postępowania w stanach nagłych. 7. Należy przeszkolić cały personel medyczny w zakresie rozpoznawania, monitorowania i postępowania z pa- 1
18 20 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 cjentami w stanie ciężkim. Dotyczy to również działań podejmowanych podczas oczekiwania na bardziej doświadczoną pomoc. Należy upewnić się, że personel zna swoją rolę działając w systemie szybkiej odpowiedzi. 8. Szpitale muszą umożliwić personelowi wszystkich dyscyplin wezwanie pomocy, gdy rozpoznają pacjenta zagrożonego pogorszeniem stanu zdrowia lub wystąpieniem zatrzymania krążenia. Personel powinien być przeszkolony w użyciu uporządkowanych narzędzi komunikacyjnych (np. Situation-Background-Assessment- Recommendation SBAR) 208 w celu skutecznego przekazania informacji pomiędzy lekarzami, pielęgniarkami i innymi pracownikami ochrony zdrowia. 9. Należy rozpoznać pacjentów, u których zatrzymanie krążenia i oddychania jest przewidywalnym zdarzeniem związanym z końcem życia i u których podejmowanie RKO jest niewłaściwe, a także zidentyfikować pacjentów, którzy nie życzą sobie wdrożenia RKO. Szpitale powinny posiadać strategię dotyczącą DNAR, opartą na krajowych wytycznych, zrozumiałą dla całego personelu medycznego. 10. Należy zapewnić audyt przypadków zatrzymania krążenia, fałszywych rozpoznań zatrzymania krążenia, nieoczekiwanych zgonów i nieplanowanych przyjęć do OIT, w oparciu o dostępne bazy danych. Audytem powinny zostać również objęte zdarzenia poprzedzające zatrzymanie krążenia oraz wdrożone postępowanie. Zapobieganie pozaszpitalnej nagłej śmierci sercowej Choroba wieńcowa jest najczęstszą przyczyną nagłej śmierci sercowej (Sudden Cardiac Death SCD). Przyczynami większości pozostałych epizodów SCD są kardiomiopatia niezwiązana z niedokrwieniem oraz wady zastawkowe. Niewielki odsetek SCD jest spowodowany wrodzonymi zaburzeniami (np. zespół Brugadów, kardiomiopatia przerostowa) lub wrodzonymi chorobami serca. Większość przypadków SCD jest poprzedzona wywiadem dotyczącym choroby serca i objawami ostrzegającymi, najczęściej bólem w klatce piersiowej, około godziny przed zatrzymaniem krążenia 209. Do tej pory zdrowe dzieci lub młodzi dorośli z SCD mogli także prezentować objawy niepokojące (np. zasłabnięcie/ utrata przytomności, ból w klatce piersiowej i kołatanie serca), które powinny były zaalarmować pracowników ochrony zdrowia i skłonić do poszukiwania opinii eksperta w celu zapobieżenia zatrzymaniu krążenia Resuscytacja przedszpitalna Personel systemu ratownictwa medycznego Systemy ratownictwa medycznego w Europie różnią się między sobą zarówno strukturą, jak i działaniem. Niektóre kraje rozwinęły przedszpitalne systemy oparte niemal wyłącznie na ratownikach i technikach medycznych (Emergency Medical Technician EMT), podczas gdy w innych krajach w mniejszym lub większym stopniu w opiece przedszpitalnej zatrudniani są lekarze. Badania porównujące wyniki resuscytacji pomiędzy systemami zatrudniającymi lekarzy i inny personel medyczny są trudne do interpretacji z powodu skrajnie wysokiej zmienności w systemach, niezależnie od składu personelu medycznego 23. Ze względu na niespójność powyższych danych włączenie bądź wyłączenie lekarzy z personelu medycznego udzielającego pomocy w przedszpitalnych zatrzymaniach krążenia w znacznej mierze będzie zależało od lokalnego protokołu. Zasady kończenia resuscytacji Jedno wysokiej jakości, prospektywne badanie wykazało, że wprowadzenie zasady kończenia resuscytacji w oparciu o przyjęte kryteria na poziomie podstawowych zabiegów resuscytacyjnych prowadzonych przez techników medycznych (defibrillation only EMT) jest związane z wysokim prawdopodobieństwem zgonu 219. Zasada ta zaleca zakończenie resuscytacji w sytuacji braku ROSC, braku defibrylacji i w sytuacji, kiedy zatrzymanie krążenia nie wystąpiło w obecności zespołu pogotowia ratunkowego. Prospektywnie walidowana zasada kończenia resuscytacji na poziomie podstawowych zabiegów resuscytacyjnych może być zastosowana jako wskazówka do podjęcia decyzji o zakończeniu przedszpitalnej RKO u osób dorosłych. Wymaga to jednak jej prospektywnego sprawdzenia w systemach ratownictwa medycznego podobnych do tego, w jakim zaproponowano jej wdrożenie. Wprowadzanie odpowiednich zasad działania w zależności od poziomu udzielanej opieki, włączając pomoc wewnątrzszpitalną, może być pomocne w zmniejszeniu różnorodności w zakresie podejmowanych decyzji, jakkolwiek zasady te powinny być prospektywnie walidowane przed ich implementacją. Resuscytacja wewnątrzszpitalna Podział postępowania w przypadku wystąpienia zatrzymania krążenia w szpitalu na podstawowe i zaawansowane zabiegi resuscytacyjne jest arbitralny, gdyż prowadzenie resuscytacji jest procesem ciągłym i opiera się na zdrowym rozsądku. Społeczeństwo oczekuje, że personel medyczny podejmie i prawidłowo wykona resuscytację krążeniowo- -oddechową. W przypadku wszystkich wewnątrzszpitalnych zatrzymań krążenia należy upewnić się, że: zatrzymanie krążenia i oddychania zostanie natychmiast rozpoznane, pomoc jest osiągalna pod standardowym numerem telefonu, natychmiast rozpocznie się RKO z wykorzystaniem przyrządów do udrażniania dróg oddechowych, jeśli będą wskazane, oraz jak najszybszym wykonaniem defibrylacji na pewno w ciągu 3 minut. We wszystkich miejscach klinicznych szpitala powinien być natychmiast dostępny sprzęt i leki umożliwiające prowadzenie resuscytacji. W idealnych warunkach sprzęt do RKO, włączając w to defibrylator, oraz leki i sposób ich rozmieszczenia powinny być ujednolicone w całym szpitalu 220,221. Zespół resuscytacyjny może być tradycyjnym zespołem wzywanym jedynie w sytuacji rozpoznania zatrzymania krążenia. Alternatywnie szpitale mogą stosować strategie rozpoznawania pacjentów, u których występuje ryzyko zatrzymania krążenia i wzywać zespół (np. MET lub RRT) przed jego wystąpieniem. Algorytm wstępnego postępowania w przypadku zatrzymania krążenia w szpitalu ilustruje ryc. 1.5.
19 Podsumowanie Komitetu Wykonawczego ERC 21 Resuscytacja wewnątrzszpitalna Pacjent nieprzytomny/w ciężkim stanie 1 Zawołaj o POMOC i oceń stan pacjenta Nie Oznaki życia? Tak Wezwij zespół resuscytacyjny RKO 30 : 2 używając sprzętu do udrażniania dróg oddechowych i stosując tlen Przyklej elektrody/podłącz monitor Oceń ABCDE Rozpoznaj i lecz przyczyny Tlen, monitorowanie, dostęp dożylny Wezwij zespół resuscytacyjny, jeśli wskazane Zaawansowane zabiegi resuscytacyjne, gdy przybędzie zespół resuscytacyjny Przekaż pacjenta zespołowi resuscytacyjnemu Ryc Algorytm postępowania w wewnątrzszpitalnym zatrzymaniu krążenia Podczas gdy jedna osoba rozpoczyna RKO, pozostałe wzywają zespół resuscytacyjny, gromadzą potrzebny sprzęt i defibrylator. Jeżeli działa tylko jedna osoba, oznacza to konieczność pozostawienia pacjenta. Wykonaj 30 uciśnięć klatki piersiowej, a po nich 2 oddechy. Minimalizuj przerwy i zapewnij wysokiej jakości uciskanie klatki piersiowej. Wykonywanie dobrej jakości uciśnięć klatki piersiowej przez dłuższy czas jest męczące; zapewniając tylko minimalne przerwy, staraj się zmieniać osobę wykonującą uciśnięcia co 2 minuty. Utrzymuj drożność dróg oddechowych i prowadź wentylację płuc, stosując odpowiedni, natychmiast dostępny sprzęt. Zwykle do dyspozycji jest maska kieszonkowa jej użycie może być uzupełnione rurką ustno-gardłową. Alternatywnie, w zależności od lokalnych zaleceń, można zastosować nadgłośniowe urządzenia do udrożnienia dróg oddechowych (Supraglottic Airway Device SAD), worek samorozprężalny lub worek samorozprężalny z maską twarzową. Intubację tchawicy powinny wykonywać tylko osoby przeszkolone w tym zakresie, kompetentne i doświadczone. Rutynowo powinien być dostępny kapnograf z możliwością rejestracji krzywej w celu potwierdzenia właściwego położenia rurki intubacyjnej (w przypadku zachowanego rzutu serca) i późniejszego monitorowania zaintubowanego pacjenta. Wdech wykonuj przez jedną sekundę i podaj objętość, która spowoduje prawidłowe uniesienie klatki piersiowej. Tak szybko, jak to możliwe, podaj tlen. Od momentu intubacji tchawicy lub zastosowania SAD wykonuj uciśnięcia klatki piersiowej nieprzerwanie (z wyjątkiem defibrylacji i oceny tętna, gdy są wskazane), z częstością przynajmniej 100/min i wentyluj płuca z częstością ok. 10 oddechów/min. Unikaj hiperwentylacji (zarówno zbyt dużej częstości oddechów, jak i objętości oddechowej), która może pogorszyć wynik leczenia. Jeżeli sprzęt do udrażniania dróg oddechowych i wentylacji jest niedostępny, rozważ prowadzenie wentylacji usta usta. Jeżeli są przeciwwskazania kliniczne do wentylacji usta usta, albo masz opory lub nie możesz jej prowadzić, wykonuj uciśnięcia klatki piersiowej dopóki nie przybędzie pomoc lub dostępny będzie sprzęt do udrażniania dróg oddechowych. Gdy dostępny będzie defibrylator, przyłóż łyżki do klatki piersiowej pacjenta i oceń rytm. Jeżeli są dostępne elektrody samoprzylepne, naklej je nie przerywając uciśnięć klatki piersiowej. Zastosowanie samoprzylepnych elektrod lub wykonanie szybkiej oceny rytmu za pomocą łyżek quick look umożliwia szybszą ocenę rytmu w porównaniu z zastosowaniem elektrod EKG 222. Przerwa na ocenę rytmu powinna być krótka. Używając manualnego defibrylatora, jeśli jest obecny rytm do defibrylacji (VF/VT), naładuj go, podczas
20 22 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 gdy drugi ratownik wykonuje nieprzerwanie uciśnięcia klatki piersiowej. Gdy defibrylator jest naładowany, przerwij uciśnięcia klatki piersiowej, potwierdź, że nikt nie dotyka pacjenta i wykonaj defibrylację. W przypadku użycia AED stosuj się do audio-wizualnych zaleceń urządzenia. Natychmiast po defibrylacji podejmij uciśnięcia klatki piersiowej. Minimalizuj przerwy w uciśnięciach klatki piersiowej. Używając defibrylatora manualnego można zredukować przerwy pomiędzy zaprzestaniem uciśnięć i ich ponownym podjęciem do 5 sekund. Kontynuuj zabiegi resuscytacyjne do czasu przybycia zespołu resuscytacyjnego lub do momentu pojawienia się oznak życia u pacjenta. Stosuj się do zaleceń głosowych, jeśli używasz AED. Jeżeli stosujesz defibrylator manualny, postępuj zgodnie z uniwersalnym algorytmem zaawansowanych zabiegów resuscytacyjnych. Po rozpoczęciu resuscytacji, jeśli jest wystarczająco dużo personelu, przygotuj kaniule dożylne i leki, które z dużym prawdopodobieństwem zostaną użyte przez zespół resuscytacyjny (np. adrenalina). Wyznacz jedną osobę odpowiedzialną za przekazanie informacji kierownikowi zespołu resuscytacyjnego. Zastosuj uporządkowane narzędzie do przekazania informacji o pacjencie (np. SBAR, RSVP) 208,223. Przygotuj dokumentację pacjenta. Jakość uciśnięć klatki piersiowej podczas resuscytacji w szpitalu jest często niezadowalająca 224,225. Istota nieprzerywanego uciskania klatki piersiowej nie może być przeceniona. Nawet krótkie przerwy w uciśnięciach klatki piersiowej mają katastrofalny wpływ na wynik leczenia i dlatego w trakcie działań resuscytacyjnych utrzymanie ciągłego i skutecznego uciskania klatki piersiowej musi zostać zapewnione. Kierownik zespołu powinien kontrolować jakość prowadzonych zabiegów resuscytacyjnych i jeżeli jest ona zła zmieniać ratowników. Ciągłe monitorowanie ETCO 2 może być zastosowane w celu oceny jakości RKO. Chociaż optymalna wartość docelowa ETCO 2 podczas RKO nie została określona, to istnieje związek wartości ETCO 2 poniżej 10 mm Hg (1,4kPa) z niepowodzeniem w osiągnięciu ROSC i może wskazywać, że jakość uciśnięć klatki piersiowej powinna być poprawiona. Jeżeli jest to możliwe, osoby wykonujące uciskanie klatki piersiowej powinny zmieniać się co 2 minuty, jednak nie powodując dłuższych przerw. Algorytm zaawansowanych zabiegów resuscytacyjnych ALS Chociaż algorytm postępowania w zatrzymaniu krążenia (ryc. 1.6) stosuje się do każdego zatrzymania krążenia, to dodatkowe interwencje mogą być wskazane w sytuacji wystąpienia zatrzymania krążenia w przebiegu szczególnych okoliczności (zob. rozdział 8) 10. Do interwencji, które bezsprzecznie wpływają na poprawę przeżycia po zatrzymaniu krążenia, należą natychmiastowe i skuteczne podjęcie BLS przez świadków zdarzenia, prowadzenie nieprzerwanych, wysokiej jakości uciśnięć klatki piersiowej oraz wczesna defibrylacja w przypadku VF/ VT. Wykazano, że zastosowanie adrenaliny zwiększa ilość ROSC, ale nie udowodniono, by jakikolwiek lek stosowany w resuscytacji lub sprzęt do zaawansowanego udrażniania dróg oddechowych zwiększał przeżywalność do momentu wypisania ze szpitala po zatrzymaniu krążenia Dlatego też leki i zaawansowany sprzęt do udrażniania dróg oddechowych, mimo że należą do interwencji ALS, mają drugorzędne znaczenie w zestawieniu z wczesną defibrylacją i prowadzeniem nieprzerwanych, wysokiej jakości uciśnięć klatki piersiowej. Jak w poprzednich wytycznych, algorytm ALS wyróżnia rytmy do defibrylacji i rytmy nie do defibrylacji. Każda pętla algorytmu jest podobna, RKO powinna być wykonywana przez całe 2 minuty, aż do oceny rytmu i, jeżeli wskazane, oceny tętna. Adrenalina 1 mg podawana jest co 3 5 minut, dopóki nie osiągnie się ROSC. Czas podawania pierwszej dawki adrenaliny opisano poniżej. Rytmy do defibrylacji (migotanie komór/częstoskurcz komorowy bez tętna VF/VT) VF/VT jest pierwszym monitorowanym rytmem w około 25% zatrzymań krążenia, zarówno w szpitalu 36, jak i poza nim 24,25,146. VF/VT występuje również na pewnym etapie w 25% zatrzymań krążenia, kiedy pierwotnie udokumentowanym rytmem była asystolia lub PEA 36. Po potwierdzeniu zatrzymania krążenia należy wezwać pomoc (włączając w to dostarczenie defibrylatora) i rozpocząć RKO, zaczynając od uciśnięć klatki piersiowej w sekwencji 30 uciśnięć : 2 wdechy. Gdy tylko zostanie dostarczony defibrylator, należy kontynuować uciskanie klatki piersiowej, jednoczasowo przyklejając elektrody samoprzylepne lub przykładając łyżki do klatki piersiowej. Następnie należy ocenić rytm i leczyć zgodnie z algorytmem ALS. Gdy potwierdzone zostanie VF/VT, naładuj defibrylator, podczas gdy drugi ratownik wykonuje uciśnięcia klatki piersiowej. Gdy defibrylator jest naładowany, należy przerwać uciskanie klatki piersiowej, szybko upewnić się, że żaden z ratowników nie dotyka pacjenta, a następnie wykonać jedno wyładowanie (360 J dla defibrylatorów jednofazowych lub J dla dwufazowych). Należy minimalizować opóźnienie pomiędzy zaprzestaniem uciskania klatki piersiowej a defibrylacją (przerwa przeddefibrylacyjna). Nawet 5 10 sekund opóźnienia zmniejszy szansę na skuteczną defibrylację 71,110. Bezpośrednio po wyładowaniu, bez ponownej oceny rytmu czy badania tętna, podejmij zabiegi resuscytacyjne (CV 30 : 2), rozpoczynając od uciśnięć klatki piersiowej. Nawet gdy defibrylacja się powiedzie i przywróci rytm perfuzyjny, potrzeba czasu, by pojawiło się krążenie 230, a stwierdzenie tętna bezpośrednio po defibrylacji jest bardzo rzadkie 231. Ponadto opóźnienie wywołane oceną tętna w sytuacji, gdy rytm perfuzyjny nie został przywrócony, będzie negatywnie oddziaływać na mięsień sercowy 232. Kontynuuj RKO przez 2 minuty, a następnie przerwij ją na krótko, aby sprawdzić rytm na monitorze. Jeżeli nadal utrzymuje się VF/VT, wykonaj drugie wyładowanie (360 J dla defibrylatorów jednofazowych lub 150
21 Podsumowanie Komitetu Wykonawczego ERC 23 Zaawansowane zabiegi resuscytacyjne Nie reaguje? Brak oddechu lub tylko pojedyncze westchnięcia 1 Wezwij zespół resuscytacyjny RKO 30 : 2 Minimalizuj przerwy Oceń rytm (VF/VT bez tętna) (PEA/asystolia) Powrót spontanicznego krążenia Natychmiast podejmij RKO przez 2 min Minimalizuj przerwy NATYCHMIASTOWA OPIEKA PORESUSCYTACYJNA Zastosuj schemat ABCDE Kontroluj wentylację i oksygenację Wykonaj 12-odprowadzeniowe EKG Lecz przyczynę zatrzymania krążenia Kontroluj temperaturę/zastosuj terapeutyczną hipotermię Natychmiast podejmij RKO przez 2 min Minimalizuj przerwy PODCZAS RKO Zapewnij wysokiej jakości uciśnięcia klatki piersiowej: częstość, głębokość, właściwe odkształcenie Zaplanuj działanie, zanim przerwiesz RKO Podaj tlen Rozważ zaawansowane drogi oddechowe i kapnografię Nie przerywaj uciskania klatki piersiowej po zabezpieczeniu dróg oddechowych Dostęp donaczyniowy (dożylny, doszpikowy) Podaj adrenalinę co 3 5 min Lecz odwracalne przyczyny ODWRACALNE PRZYCZYNY Hipoksja Hipowolemia Hipo-/hiperkaliemia/zaburzenia metaboliczne Hipotermia Zaburzenia zatorowo-zakrzepowe Tamponada osierdzia Zatrucia Odma prężna Ryc Algorytm zaawansowanych zabiegów resuscytacyjnych ALS 360 J dla dwufazowych) i niezwłocznie po wyładowaniu podejmij RKO (CV 30 : 2) bez ponownej oceny rytmu czy tętna, zaczynając od uciśnięć klatki piersiowej. Kontynuuj RKO przez 2 minuty, potem przerwij na krótko zabiegi resuscytacyjne, aby ocenić rytm. Gdy utrzymuje się VF/VT, wykonaj trzecie wyładowanie (360 J dla defibrylatorów jednofazowych lub J dla dwufazowych) i niezwłocznie po nim powróć do RKO (CV 30 : 2) bez ponownej oceny rytmu czy tętna. Jeśli udało się uzyskać dostęp dożylny lub doszpikowy, podaj 1 mg adrenaliny i 300 mg amiodaronu, gdy tylko rozpocznie się na nowo uciskanie klatki piersiowej. Jeśli nie uda się uzyskać ROSC, wykonując trzecią defibrylację, adrenalina poprawi przepływ krwi w miokardium i może zwiększyć szansę na skuteczną defibrylację przy kolejnej próbie. W badaniach na zwierzętach szczytowe stężenie osoczowe adrenaliny oznaczane było 90 sekund po obwodowym podaniu leku 233. Jeśli dojdzie do ROSC po trzeciej defibrylacji, to jest możliwe, że bolus adrenaliny doprowadzi do tachykardii i nadciśnienia i może spowodować nawrót VF. Jednakże naturalnie występujący poziom adrenaliny w osoczu jest wysoki bezpośrednio po ROSC 234 i jak dotąd nie analizowano dodatkowego ryzyka związanego z egzogenną
22 24 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 podażą adrenaliny. Przerwanie uciskania klatki piersiowej w trakcie trwania pętli RKO, by sprawdzić czy nie ma rytmu mogącego dawać perfuzję, prawdopodobnie jest także szkodliwe. Zastosowanie wykresu kapnografii może pomóc zidentyfikować ROSC bez potrzeby przerywania uciskania klatki piersiowej i może być pomocne w uniknięciu podania adrenaliny w bolusie po jego osiągnięciu. Dwa prospektywne badania przeprowadzone z udziałem pacjentów wykazały znaczący wzrost ETCO 2 towarzyszący powrotowi spontanicznego krążenia 235,236. Po każdej 2-minutowej pętli RKO, jeśli rytm zmienia się w asystolię lub PEA, zastosuj postępowanie jak w rytmach nie do defibrylacji patrz niżej. Jeżeli obecny jest rytm nie do defibrylacji i jest on uporządkowany (zespoły QRS są regularne lub wąskie), należy ocenić tętno. Ocena rytmu powinna być krótka, a ocena tętna wykonywana tylko wtedy, gdy jest obecny uporządkowany rytm. Jeżeli jest jakakolwiek wątpliwość dotycząca obecności tętna w przypadku stwierdzenia uporządkowanego rytmu serca, należy podjąć ponownie RKO. Jeżeli doszło do ROSC, rozpocznij opiekę poresuscytacyjną. Niezależnie od rytmu w zatrzymaniu krążenia należy podawać kolejne dawki 1 mg adrenaliny co 3 5 minut do momentu ROSC. W praktyce polega to na podawaniu 1 mg adrenaliny co dwie pętle algorytmu. Jeżeli w trakcie RKO powrócą oznaki życia (celowe ruchy, prawidłowy oddech, kaszel), należy ocenić rytm na monitorze. W przypadku stwierdzenia uporządkowanego rytmu serca należy ocenić tętno. Gdy jest obecne, kontynuuj opiekę poresuscytacyjną i/lub leczenie zaburzeń rytmu występujących w okresie około zatrzymania krążenia. W przypadku braku tętna podejmij ponownie RKO. Wykonywanie RKO w sekwencji CV 30 : 2 jest męczące. Należy zmieniać osobę wykonującą uciśnięcia klatki piersiowej co 2 minuty, pamiętając o minimalizowaniu przerw w uciśnięciach. Uderzenie przedsercowe Pojedyncze uderzenie przedsercowe ma bardzo małą skuteczność konwersji rytmu defibrylacyjnego i powodzenie tej procedury jest możliwe jedynie wtedy, gdy wykonuje się ją w ciągu pierwszych kilku sekund od wystąpienia rytmu do defibrylacji 240. Bardziej prawdopodobna jest konwersja VT niż VF. Wykonanie uderzenia przedsercowego nie może opóźniać wezwania pomocy czy dostarczenia defibrylatora. Jest to więc terapia właściwa jedynie w sytuacji, gdy kilka osób personelu medycznego jest obecnych przy pacjencie, u którego zauważono monitorowane zatrzymanie krążenia, a defibrylator nie jest natychmiast dostępny 241. W praktyce jest to możliwe jedynie w miejscach o wzmożonym nadzorze, takich jak oddział ratunkowy lub OIT 239. Drogi oddechowe i wentylacja Podczas leczenia uporczywego VF zapewnij dobrą jakość uciśnięć klatki piersiowej pomiędzy kolejnymi defibrylacjami. Rozważ odwracalne przyczyny (4 H i 4 T) i lecz je, gdy występują. Sprawdź położenie łyżek/elektrod, ich kontakt ze skórą, zapewnij dobre przewodzenie impulsu (podkładki żelowe). Intubacja tchawicy jest najpewniejszym sposobem udrożnienia dróg oddechowych, ale powinna być wykonana tylko przez personel stosownie przeszkolony i posiadający doświadczenie w tym zakresie. Osoby te powinny podejmować próby laryngoskopii podczas uciśnięć klatki piersiowej. Krótka przerwa w uciskaniu klatki piersiowej może być potrzebna na wprowadzenie rurki między struny głosowe, ale nie powinno to trwać dłużej niż 10 sekund. Alternatywnie, ażeby uniknąć przerw w uciskaniu klatki piersiowej, intubację można odroczyć do czasu powrotu spontanicznego krążenia. Żadne badanie nie wykazało, że intubacja zwiększa przeżywalność w zatrzymaniu krążenia. Po intubacji potwierdź właściwe położenie rurki i właściwie ją umocuj. Prowadź wentylację z częstością 10 oddechów/min; unikaj hiperwentylacji. Od momentu intubacji tchawicy prowadź uciskanie klatki piersiowej z częstością 100/min, bez przerw na wentylację. Jeśli nie ma osób przeszkolonych w zakresie intubacji, alternatywę stanowią nadgłośniowe przyrządy do udrażniania dróg oddechowych (np. maska krtaniowa, zob. rozdział 4e). Od chwili udrożnienia dróg oddechowych jednym z powyższych przyrządów należy podjąć próbę uciskania klatki piersiowej bez przerw na wentylację. Jeśli pojawi się nadmierny przeciek upośledzający wentylację, resuscytację należy prowadzić z przerwami na oddechy, utrzymując stosunek CV 30 : 2. Dostęp donaczyniowy Zapewnij dostęp do żyły, jeśli dotychczas nie został wykonany. W porównaniu z dostępem centralnym kaniulacja żyły obwodowej jest szybsza, prostsza do wykonania i bezpieczniejsza. Po podaniu leku do kaniuli obwodowej należy ją przepłukać co najmniej 20 ml płynu. Jeżeli uzyskanie dostępu do żyły jest trudne albo niemożliwe, rozważ drogę doszpikową (io). Leki podane doszpikowo osiągają pożądane stężenie w osoczu w czasie porównywalnym z lekami podanymi do żyły centralnej 242. Dostępne ostatnio mechaniczne urządzenia do wykonywania dostępu doszpikowego ułatwiają wykonanie tej procedury 243. Stężenie, jakie osiągnie w surowicy lek podany dotchawiczo, jest nieprzewidywalne, a optymalna dawka dotchawicza większości leków jest nieznana. Dlatego dostęp ten nie jest już zalecany. Leki Adrenalina Pomimo powszechnego stosowania adrenaliny podczas resuscytacji i licznych badań z wykorzystaniem wazopresyny, nie ma badań kontrolnych z zastosowaniem placebo, które wykazałyby, że rutynowe podanie jakiegokolwiek leku wazopresyjnego na którymkolwiek z etapów zatrzymania krążenia u ludzi poprawia przeżycie bez uszkodzeń neurologicznych do wypisu ze szpitala. Mimo braku danych z badań z udziałem ludzi stosowanie adrenaliny jest wciąż zalecane, głównie na podstawie wyników badań na zwierzętach i zwiększonej krótkoterminowej przeżywalności pacjentów 227, 228. Optymalna dawka adrenaliny nie jest znana i nie ma żadnych danych, które uzasadniają stosowanie powtarzalnych dawek tego leku. Istnieje niewiele danych dotyczących farmakokinetyki adrenaliny podczas RKO. Optymalny
23 Podsumowanie Komitetu Wykonawczego ERC 25 czas trwania RKO oraz liczba defibrylacji, jaka powinna być wykonana przed podaniem leków, nie są znane. Obecnie jest zbyt mało dowodów przemawiających za lub przeciw stosowaniu jakiegokolwiek innego wazopresora jako alternatywy lub w zestawieniu z adrenaliną, niezależnie od rytmu zatrzymania krążenia w perspektywie poprawy przeżycia i neurologicznego wyniku leczenia u pacjentów z zatrzymaniem krążenia. Opierając się na ustaleniach ekspertów, w leczeniu VF/VT adrenalinę należy podać po trzeciej defibrylacji, gdy ponownie podjęto uciskanie klatki piersiowej. Lecząc zatrzymanie krążenia, należy powtarzać dawkę adrenaliny co 3 5 minut (co drugą pętlę). Nie należy przerywać RKO w celu podania leków. Leki antyarytmiczne Nie ma dowodów, że rutynowa podaż jakiegokolwiek leku antyarytmicznego w czasie zatrzymania krążenia u ludzi zwiększa przeżycie do wypisu ze szpitala. W porównaniu z placebo 244 i lidokainą 245 zastosowanie amiodaronu w opornym na defibrylację migotaniu komór poprawia krótkoterminowe wyniki przeżycia do przyjęcia do szpitala. Opierając się na ustaleniach ekspertów, przyjmuje się, że jeśli VF/VT utrzymuje się po trzech defibrylacjach, należy podać 300 mg amiodaronu w bolusie. W nawracającym lub opornym VF/ VT można podać kolejną dawkę 150 mg amiodaronu, a następnie włączyć wlew 900 mg w ciągu 24 godzin. Jeśli amiodaron jest niedostępny, alternatywę stanowi lidokaina 1 mg/ kg, ale nie należy stosować lidokainy, gdy już podano amiodaron. Magnez Rutynowe stosowanie magnezu w zatrzymaniu krążenia nie poprawia przeżycia i nie jest rekomendowane, chyba że podejrzewa się torsades de pointes (patrz zaburzenia rytmu towarzyszące zatrzymaniu krążenia). Wodorowęglan sodu Rutynowe podawanie wodorowęglanu sodu podczas zatrzymania krążenia i RKO lub po ROSC nie jest zalecane. Należy podać wodorowęglanu sodu (50 mmol), jeśli zatrzymanie krążenia związane jest z hiperkaliemią lub zatruciem trójcyklicznymi lekami antydepresyjnymi. Dawkę należy powtarzać adekwatnie do sytuacji klinicznej i powtarzanych wyników badania gazometrii krwi tętniczej. Rytmy nie do defibrylacji (PEA Pulseless Electrical Activity i asystolia) Aktywność elektryczna bez tętna (PEA) jest definiowana jako zatrzymanie krążenia, w którym aktywności elektrycznej serca nie towarzyszy obecność fali tętna. PEA często jest powodowana przez odwracalne przyczyny i można ją leczyć, gdy te przyczyny zostaną zidentyfikowane i skorygowane. Szanse przeżycia pacjenta z NZK w mechanizmie asystolii lub PEA są niewielkie, chyba że rozpozna się i skutecznie skoryguje odwracalną przyczynę. Jeżeli pierwszym monitorowanym rytmem jest PEA lub asystolia, należy rozpocząć RKO 30 : 2 i podać adrenalinę tak szybko, jak tylko uda się uzyskać dostęp do żyły. Jeśli jest to asystolia, należy sprawdzić, nie przerywając RKO, czy elektrody są dobrze podpięte. Jak tylko uda się zabezpieczyć drożność dróg oddechowych w sposób zaawansowany, należy prowadzić uciśnięcia klatki piersiowej bez przerw na wentylację. Po 2 minutach RKO należy sprawdzić ponownie rytm. Jeżeli jest obecna asystolia, natychmiast wróć do RKO. Gdy pojawił się zorganizowany rytm, zbadaj tętno. Jeśli nie ma tętna (lub gdy są co do tego jakiekolwiek wątpliwości), prowadź dalej RKO. Jak tylko uzyska się dostęp donaczyniowy (iv, io), należy podać 1 mg adrenaliny i powtarzać co drugą pętlę (tj. co 3 5 minut). Jeśli tętno jest obecne, rozpocznij opiekę poresuscytacyjną. Gdy podczas zabiegów resuscytacyjnych wystąpią oznaki życia, oceń rytm i zbadaj tętno. Jeśli podczas leczenia asystolii czy PEA po 2 minutach RKO rytm zmieni się w VF, postępuj zgodnie z algorytmem dla rytmów do defibrylacji. W przeciwnym razie prowadź dalej RKO i podawaj adrenalinę co 3 5 minut, jeżeli nadal brak tętna. Jeżeli VF zostanie zidentyfikowane na monitorze podczas wykonywania 2-minutowej pętli RKO, należy przed oceną rytmu i wykonaniem defibrylacji, jeżeli wskazana, dokończyć pętlę RKO. Strategia ta minimalizuje przerwy w uciśnięciach klatki piersiowej. Atropina Asystolia podczas zatrzymania krążenia jest raczej spowodowana pierwotną patologią serca niż nadmiernym napięciem nerwu błędnego. Nie ma żadnych dowodów na korzyści płynące z rutynowego podawania atropiny w leczeniu asystolii lub PEA. Kilka ostatnio przeprowadzonych badań nie wykazało korzyści ze stosowania atropiny w resuscytacji w szpitalu jak i poza nim 226, Rutynowe podawanie atropiny w asystolii i PEA nie jest obecnie zalecane. Potencjalnie odwracalne przyczyny zatrzymania krążenia Podczas każdego zatrzymania krążenia muszą być wzięte pod uwagę potencjalne przyczyny lub stany, w stosunku do których istnieje swoiste leczenie. Aby ułatwić zapamiętanie, podzielono je na 2 grupy po 4, w zależności od litery, na jaką się zaczynają (w języku angielskim): H lub T. Więcej szczegółów dotyczących wielu z nich znajduje się w rozdziale Fibrynoliza podczas RKO Terapia fibrynolityczna nie powinna być rutynowo stosowana w zatrzymaniu krążenia 257. Należy ją rozważyć, gdy zatrzymanie krążenia jest spowodowane przez udowodniony lub podejrzewany ostry zator tętnicy płucnej. Po zastosowaniu fibrynolizy w czasie RKO w przebiegu zatoru tętnicy płucnej opisywano przeżycia i dobre neurologiczne wyniki leczenia u pacjentów, którzy wymagali RKO trwającej ponad 60 minut. Jeżeli podawany jest lek fibrynolityczny, należy rozważyć wykonywanie RKO przynajmniej minut przed zakończeniem resuscytacji 258,259. Trwająca resuscytacja nie jest przeciwwskazaniem dla fibrynolizy. Płynoterapia Hipowolemia jest jedną z potencjalnie odwracalnych przyczyn zatrzymania krążenia. W przypadku podejrzenia hipowolemii należy szybko przetaczać płyny. Nie wykazano ewidentnych korzyści ze stosowania koloidów we wstępnej 1
24 26 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 fazie resuscytacji, należy więc używać roztworu soli fizjologicznej lub roztworu Hartmanna (izotoniczny roztwór elektrolitowy buforowany mleczanem przyp. tłum.). Rutynowa płynoterapia podczas zatrzymania krążenia o kardiologicznej przyczynie jest kontrowersyjna. Należy zapewnić normowolemię, pamiętając, że przy braku hipowolemii podaż nadmiernej objętości płynów może być szkodliwa 260. Zastosowanie obrazowania ultrasonograficznego podczas zaawansowanych zabiegów resuscytacyjnych Przeprowadzono kilka badań oceniających zastosowanie ultrasonografii podczas zatrzymania krążenia w celu identyfikacji potencjalnie odwracalnych przyczyn. Chociaż żadne z nich nie wykazało, że zastosowanie tych metod poprawiło ostateczny wynik leczenia, nie ma wątpliwości, że za pomocą echokardiografii można zidentyfikować odwracalne przyczyny zatrzymania krążenia (np. tamponada worka osierdziowego, zatorowość płucna, rozwarstwienie aorty, hipowolemia, odma opłucnowa) Ultrasonografia, jeśli jest dostępna w rękach przeszkolonego klinicysty, może być pomocna w diagnozowaniu i leczeniu potencjalnie odwracalnych przyczyn zatrzymania krążenia. Zastosowanie ultrasonografii w trakcie ALS wymaga odpowiedniego przeszkolenia, tak by przerwy w uciskaniu klatki piersiowej były minimalne. Zalecana jest projekcja podmostkowa 261,267,269. Przyłożenie głowicy bezpośrednio przed przerwaniem uciskania klatki piersiowej, w celu planowanej oceny rytmu, umożliwia sprawnemu ultrasonografiście uzyskać obraz w ciągu 10 sekund przeznaczonych na ocenę rytmu i/lub tętna. Brak ruchów serca stwierdzonych w ultrasonografii podczas resuscytacji pacjentów z zatrzymaniem krążenia jest czynnikiem predykcyjnym wystąpienia zgonu , jakkolwiek brak jest doniesień na temat czułości i swoistości tej metody. Drożność dróg oddechowych i wentylacja U pacjentów wymagających resuscytacji często występuje niedrożność dróg oddechowych. Zwykle jest ona wtórna do utraty przytomności, ale niekiedy stanowi pierwotną przyczynę zatrzymania krążenia. Kluczowa jest natychmiastowa ocena pacjenta, połączona z zapewnieniem drożności dróg oddechowych i wentylacji płuc. Aby poprawić drożność dróg oddechowych w przypadku, gdy przyczyną niedrożności jest język lub inne struktury górnych dróg oddechowych, stosuje się 3 rękoczyny: odgięcie głowy, uniesienie żuchwy i wysunięcie żuchwy. Pomimo zupełnego braku opublikowanych danych dotyczących zastosowania rurek ustno- i nosowo-gardłowych podczas RKO, są one wciąż pomocne, a czasem niezbędne by utrzymać drożność dróg oddechowych szczególnie w przypadku długotrwałej resuscytacji. Podczas RKO tlen należy podać zawsze, jeśli tylko jest dostępny. Brak jest danych określających optymalną wartość saturacji krwi tętniczej (SaO 2 ) podczas RKO. Istnieją dane z badań na zwierzętach 273 oraz pewne obserwacyjne dane kliniczne wskazujące związek pomiędzy wysokimi wartościami SaO 2 po ROSC i niepomyślnym wynikiem leczenia 274. Początkowo należy podać jak najwyższe możliwe stężenie tlenu. Jak tylko możliwa będzie wiarygodna ocena wysycenia tlenem krwi tętniczej za pomocą pulsoksymetru lub gazometrii, powinno się miareczkować wdechowe stężenie tlenu tak, aby osiągnąć SaO %. Alternatywne przyrządy do udrażniania dróg oddechowych a intubacja dotchawicza Nie ma wystarczających danych, by zalecić lub odrzucić zastosowanie jakiejkolwiek techniki udrożnienia dróg oddechowych i zapewnienia wentylacji u osób dorosłych w zatrzymaniu krążenia. Pomimo to intubacja dotchawicza jest ogólnie uważana za optymalny sposób zabezpieczania dróg oddechowych w czasie zatrzymania krążenia. Powinna ona być wykonywana jedynie, gdy dostępny jest wyszkolony personel potrafiący zastosować tę technikę w pewny i sprawny sposób. Istnieją dowody, że gdy intubacja wykonywana jest przez osoby bez wystarczającego przeszkolenia i doświadczenia, częstość występujących powikłań jest nieaakceptowalnie wysoka 275. U pacjentów z pozaszpitalnym zatrzymaniem krążenia wiarygodnie udokumentowane występowanie nierozpoznanej intubacji przełyku wynosiło od 0,5 do 17% (lekarze medycyny ratunkowej: 0,5% 276 ; ratownicy medyczni: 2,4% 277, 6% 278,279, 9% 280, 17% 281 ). Przedłużone próby intubacji są szkodliwe. Zaprzestanie uciskania klatki piersiowej na czas intubacji upośledza przepływ wieńcowy i mózgowy. W badaniu oceniającym przedszpitalną intubację wykonywaną przez ratowników medycznych w 100 zatrzymaniach krążenia całkowity czas trwania przerw w RKO związanych w próbami intubacji wynosił 110 s (IQR s; range s), a w 25% przypadków wynosił ponad 3 minuty 282. Próby intubacji były odpowiedzialne za 25% wszystkich przerw w RKO. Personel ochrony zdrowia, który podejmuje próbę pozaszpitalnej intubacji, powinien brać udział w planowym, monitorowanym programie szkoleniowym, opartym na zrozumiałych kryteriach nabywania umiejętności, umożliwiającym ich odnawianie w regularny sposób. Personel posiadający umiejętności w zakresie zaawansowanych technik udrażniania dróg oddechowych powinien być w stanie wykonać laryngoskopię bez przerywania uciśnięć klatki piersiowej. Krótka przerwa może być wymagana w celu wsunięcia rurki między struny głosowe. Żadna próba intubacji nie powinna powodować przerwania uciśnięć klatki piersiowej na dłużej niż 10 sekund. Po intubacji należy potwierdzić właściwe położenie rurki i odpowiednio ją zabezpieczyć. Rozważa się alternatywne wykorzystanie kilku innych przyrządów do udrażniania dróg oddechowych w czasie RKO. Opublikowano kilka badań, w których oceniano zastosowanie Combitube, classic LMA, rurki krtaniowej (LT) czy I-gel w czasie RKO, ale żadne z nich nie było wystarczająco silne statystycznie, by określić przeżywalność w NZK, jako pierwotny punkt końcowy badania. Większość badaczy analizowała, z jaką częstością skutecznie udrażniano drogi oddechowe i wentylowano pacjentów. Nadgłośniowe przyrządy udrażniające pozwalają na łatwiejsze niż rurka intubacyjna zabezpieczenie dróg oddechowych i w przeciwieństwie do niej mogą być zastosowane, w większości przypadków, bez przerywania uciśnięć klatki piersiowej 283. Potwierdzenie właściwego położenia rurki dotchawiczej Nierozpoznana intubacja przełyku jest najpoważniejszym powikłaniem w trakcie prób intubacji tchawicy. Ruty-
25 Podsumowanie Komitetu Wykonawczego ERC 27 nowe stosowanie pierwotnych i wtórnych technik potwierdzających właściwe położenie rurki dotchawiczej powinno zmniejszyć takie ryzyko. Do pierwotnej oceny należy obserwacja symetrycznego poruszania się klatki piersiowej, osłuchiwanie pól płucnych obustronnie w liniach pachowych (szmery oddechowe powinny być symetryczne i dobrze słyszalne) i osłuchiwanie nadbrzusza (brak szmerów). Kliniczne objawy właściwego umieszczenia rurki nie są całkowicie wiarygodne. Wtórne potwierdzenie położenia rurki dotchawiczej na podstawie wydychanego dwutlenku węgla albo detektora przełykowego powinno zmniejszyć ryzyko nierozpoznanej intubacji przełyku, ale wiarygodność tych metod jest zmienna i dlatego powinny one być stosowane jako dodatek do innych technik 284. Żadna z wtórnych technik nie pozwala stwierdzić, czy rurka jest umieszczona prawidłowo w tchawicy, czy też zbyt głęboko, w głównym oskrzelu. Dokładność kolorymetrycznych detektorów CO 2, detektorów przełykowych i kapnometrów niepokazujących krzywej CO 2 nie przewyższa osłuchiwania klatki piersiowej i bezpośredniej oceny wzrokowej potwierdzającej położenie rurki w tchawicy u poszkodowanych z zatrzymaniem krążenia. Najbardziej czułym i swoistym urządzeniem potwierdzającym położenie rurki w tchawicy u osób z zatrzymaniem krążenia jest kapnografia z możliwością uzyskania krzywej CO 2. Powinna ona uzupełniać kliniczne metody tej oceny (osłuchiwanie i wzrokowe potwierdzenie obecności rurki między strunami głosowymi). Dostępne są przenośne monitory umożliwiające za pomocą kapnografii wstępne potwierdzenie, jak również ciągły monitoring położenia rurki intubacyjnej, które mogą być użyte niezależnie od lokalizacji zdarzenia: pozaszpitalnie, w oddziale ratunkowym czy w różnych lokalizacjach szpitalnych, gdzie wykonywana jest intubacja. W przypadku braku tego typu urządzeń zastosowanie nadgłośniowych przyrządów udrażniających drogi oddechowe może być preferowane, gdy zaistnieje potrzeba użycia zaawansowanych technik. Techniki i urządzenia do prowadzenia RKO Standardowo wykonywana, manualna RKO w najlepszym wypadku powoduje jedynie 30% prawidłowej perfuzji wieńcowej i mózgowej 285. Istnieje kilka technik i urządzeń stosowanych w czasie RKO, które mogą w wybranych przypadkach poprawić hemodynamikę i krótkoterminową przeżywalność pod warunkiem, że zostaną zastosowane przez właściwie przeszkolony personel. Powodzenie danej techniki lub urządzenia zależy od edukacji i wyszkolenia ratowników oraz dostępności zasobów również ludzkich. W określonych grupach ratowników te nowatorskie techniki i urządzenia mogą być lepsze od standardowej RKO. Trzeba zwrócić jednak uwagę, że urządzenie lub technika zapewniająca dobrej jakości RKO, kiedy używane są przez wysoce wykwalifikowany personel lub w warunkach testowych, mogą skutkować niską jakością i częstymi przerwami w RKO, gdy zostaną użyte w niekontrolowanych warunkach klinicznych 286. Pomimo braku rekomendacji dla rutynowego użycia jakiegokolwiek urządzenia wspomagającego krążenie zamiast manualnej RKO, niektóre z nich są stosowane rutynowo zarówno w szpitalach, jak i poza nimi. Jeżeli dobrze wyszkoleni ratownicy stosują urządzenia do prowadzenia RKO, rozważnym jest, by było to prowadzone pod nadzorem, aby zapewnić, że zastosowanie urządzenia nie wpływa negatywnie na przeżycie. Chociaż manualne wykonywanie uciskania klatki piersiowej jest często bardzo niskiej jakości , nie wykazano, by którekolwiek z urządzeń było jednoznacznie lepsze. Zastawka oporowa (Impedance Threshold Device ITD) ITD jest to zastawka oporowa, która ogranicza możliwość wejścia powietrza do klatki piersiowej podczas fazy relaksacji pomiędzy uciśnięciami. Zmniejsza to ciśnienie wewnątrz klatki piersiowej, zwiększając powrót krwi żylnej do serca. Ostatnie metaanalizy dotyczące zastosowania ITD u pacjentów z pozaszpitalnym zatrzymaniem krążenia wykazały wzrost częstości ROSC i krótkoterminowego przeżycia, ale bez poprawy w przeżyciu do wypisu ze szpitala czy zmniejszeniu częstości występowania powikłań neurologicznych 290. Wobec braku danych wskazujących, że ITD zwiększa przeżywalność do wypisu ze szpitala jej rutynowe użycie w zatrzymaniu krążenia nie jest zalecane. Lund University Cardiac Arrest System (LUCAS) Lund University Cardiac Arrest System jest uciskającym mostek urządzeniem zasilanym gazem. Zawiera ono w sobie przyssawkę do aktywnej dekompresji. Badania na zwierzętach wykazały, że RKO z wykorzystaniem urządzenia LUCAS poprawia parametry hemodynamiczne i krótkoterminową przeżywalność 291,292. Nie opublikowano jeszcze wyników badań z randomizacją dotyczących ludzi, porównujących standardową RKO z RKO przy użyciu LUCAS. Load-Distributing Band CPR (AutoPulse) Load-Distributing Band (LDB) jest urządzeniem opasującym klatkę piersiową, składającym się z pneumatycznie zasilanego pasa ściskającego i deski. Chociaż zastosowanie w RKO LDB poprawia parametry hemodynamiczne , to wyniki badań klinicznych są sprzeczne. Jedno wieloośrodkowe randomizowane badanie z grupą kontrolną dotyczące zastosowania urządzenia przez służby ratownicze na ponad 1000 dorosłych pacjentów z pozaszpitalnym zatrzymaniem krążenia, wykazało brak poprawy przeżywalności ocenianej w 4 godziny od ROSC i gorszy neurologiczny wynik leczenia 296. Nierandomizowane badanie kliniczne wykazało wzrost przeżywalności do wypisu ze szpitala w pozaszpitalnym zatrzymaniu krążenia 297. LUCAS i AutoPulse w leczeniu zatrzymania krążenia Obecnie prowadzone są dwa duże wieloośrodkowe badania prospektywne z randomizacją, mające na celu ocenę skuteczności urządzeń AutoPulse i LUCAS. Wyniki tych badań są oczekiwane z zainteresowaniem. W warunkach szpitalnych urządzenia mechaniczne okazały się skuteczne w leczeniu pacjentów poddawanych PCI 298,299 oraz TK 300, a także podczas przedłużonych prób resuscytacji (np. w przypadku hipotermii 301,302, zatrucia, podczas trombolizy u pacjentów z zatorem tętnicy płucnej czy przedłużonego transportu itp.), czyli w sytuacjach, gdzie zmęczenie ratownika może zmniejszyć skuteczność manualnego uciskania klatki piersiowej. W warunkach przedszpitalnych urządzenia te mogą 1
26 28 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 odgrywać ważną rolę w sytuacjach, gdy konieczne jest wydobywanie pacjentów, resuscytacja prowadzona jest w ograniczonych przestrzeniach, wymagane jest przewiezienie pacjenta, co często uniemożliwia skuteczne uciskanie klatki piersiowej przez ratownika. Podczas transportu do szpitala jakość manualnie wykonywanej RKO jest często niezadowalająca. Przyrządowa RKO pozwala na utrzymanie dobrej jakości resuscytacji podczas transportu karetką do szpitala 303,304. Zaletą urządzeń mechanicznych jest możliwość wykonania defibrylacji bez przerw w uciskaniu klatki piersiowej. Rola opisanych urządzeń we wszystkich sytuacjach klinicznych wymaga dalszej oceny. Zaburzenia rytmu towarzyszące zatrzymaniu krążenia Prawidłowe rozpoznanie i leczenie zaburzeń rytmu u pacjentów w stanie krytycznym może zapobiec wystąpieniu epizodu zatrzymania krążenia lub jego nawrotowi po skutecznej resuscytacji. Algorytmy postępowania opisane w tym rozdziale skonstruowano w sposób umożliwiający osobom po szkoleniu ALS, niekoniecznie specjalistom, skuteczne i bezpieczne leczenie pacjenta w stanie zagrożenia życia. Jeżeli życie pacjenta nie jest bezpośrednio zagrożone, sposoby postępowania są różne, włączając w to podaż leków (doustnie lub parenteralnie), w stosowaniu których niespecjalista może mieć mniejsze doświadczenie. W tej sytuacji istnieje możliwość poszukania pomocy kardiologa lub doświadczonego w danej dziedzinie lekarza. Ocena wstępna i leczenie pacjenta z arytmią powinny przebiegać zgodnie ze schematem ABCDE. Kluczowe elementy tego procesu obejmują poszukiwanie objawów niepokojących, podanie wysokiego przepływu tlenu, uzyskanie dostępu dożylnego oraz wdrożenie monitorowania (EKG, pomiar ciśnienia tętniczego, SpO 2 ). Jeżeli tylko jest to możliwe, należy wykonać 12-odprowadzeniowe EKG. Pomoże to dokładnie ocenić rytm przed leczeniem bądź retrospektywnie. Należy wyrównywać wszelkie zaburzenia elektrolitowe (np. K +, Mg 2+, Ca 2+ ). Planując leczenie, należy rozważyć przyczynę i charakter arytmii. W rozpoznawaniu i leczeniu wszystkich zaburzeń rytmu brane są pod uwagę dwa czynniki: stan pacjenta (stabilny czy niestabilny) oraz charakter arytmii. Leki antyarytmiczne charakteryzują się wolniejszym początkiem działania i są mniej skuteczne niż kardiowersja elektryczna w konwersji tachykardii do rytmu zatokowego. Z tego względu leki te powinny być zarezerwowane wyłącznie dla stabilnych pacjentów bez objawów niepokojących. Natomiast kardiowersja elektryczna zwykle jest preferowana w leczeniu pacjentów niestabilnych, wykazujących takie objawy. Objawy niepokojące W przypadku większości zaburzeń rytmu obecność lub brak niepokojących objawów determinuje właściwy sposób leczenia. Poniżej wymienione objawy wskazują pacjentów, u których niestabilność hemodynamiczna powodowana jest arytmią: 1. Wstrząs objawiający się bladością powłok, nadmierną potliwością, zimną i lepką skórą kończyn (zwiększona aktywność układu sympatycznego), zaburzonym stanem świadomości (zmniejszony przepływ mózgowy) i hipotensją (np. skurczowe ciśnienie krwi <90 mm Hg). 2. Omdlenie/utrata przytomności w następstwie zredukowanego przepływu mózgowego. 3. Niewydolność krążenia zaburzenia rytmu, redukując przepływ wieńcowy, upośledzają pracę mięśnia sercowego. W ostrych epizodach może się to objawiać obrzękiem płuc (niewydolność lewej komory) i/lub nadmiernie wypełnionymi żyłami szyjnymi i powiększeniem wątroby (niewydolność prawej komory). 4. Niedokrwienie mięśnia sercowego występuje, gdy zużycie tlenu w sercu przewyższa jego dostarczanie. Niedokrwienie mięśnia sercowego może manifestować się jako ból w klatce piersiowej (dusznica) lub przebiegać bez bólu, jako izolowana zmiana w 12-odprowadzeniowym EKG (ciche niedokrwienie). Obecność niedokrwienia jest szczególnie ważna, gdy pacjent ma wyjściowo chorobę niedokrwienną lub wadę strukturalną serca. W tych przypadkach może pociągnąć to za sobą dalsze, zagrażające życiu komplikacje z zatrzymaniem krążenia włącznie. Możliwości terapii Po rozpoznaniu rytmu oraz obecności lub braku objawów niepokojących natychmiastowe postępowanie obejmuje dwie opcje terapeutyczne: 1. Elektryczna (kardiowersja, stymulacja serca) 2. Farmakologiczna (leki antyarytmiczne i inne). Częstoskurcze Jeżeli pacjent jest niestabilny Jeżeli pacjent jest niestabilny, pogarsza się jego stan i występują objawy niepokojące lub symptomy opisane powyżej, będące następstwem tachykardii, należy natychmiast wykonać kardiowersję (ryc. 1.7). U pacjentów bez obciążeń kardiologicznych rzadko występują niepokojące objawy, gdy czynność komór jest <150/min. U osób z upośledzoną funkcją mięśnia sercowego lub istotnymi schorzeniami towarzyszącymi niepożądane objawy i niestabilność mogą się rozwinąć już przy niższej czynności serca. Jeżeli kardiowersja nie przywróci rytmu zatokowego i pacjent nadal pozostaje niestabilny, należy podać dożylnie 300 mg amiodaronu w ciągu minut i ponowić próbę elektrycznej kardiowersji. Po wysycającej dawce można kontynuować wlew tego leku 900 mg przez 24 godziny. Jeżeli pacjent jest stabilny Jeżeli pacjent, u którego występuje częstoskurcz, jest stabilny i jego stan się nie pogarsza (nie ma żadnych niepokojących objawów), właściwe wydaje się wdrożenie leczenia farmakologicznego (ryc. 1.7). Stymulacja nerwu błędnego może być właściwa jako wstępne leczenie w przypadku częstoskurczu nadkomorowego. Bradykardia Bradykardię definiuje się jako czynność serca <60/min. Stan pacjenta, u którego stwierdzono wolną czynność serca, należy ocenić w oparciu o schemat ABCDE. Należy wziąć
27 Podsumowanie Komitetu Wykonawczego ERC 29 1 Postępowanie w przypadku tachykardii (z tętnem) Oceń, stosując schemat ABCDE Podaj tlen, zapewnij dostęp dożylny Monitoruj EKG, ciśnienie krwi, SpO 2, wykonaj 12-odprowadzeniowe EKG Rozpoznaj i lecz odwracalne przyczyny (np. zaburzenia elektrolitowe) Kardiowersja* Do 3 prób Niestabilny Oceń, czy występują objawy niepokojące 1. Wstrząs 2. Omdlenie 3. Niedokrwienie mięśnia sercowego 4. Niewydolność serca Stabilny Czy zespoły QRS są wąskie (<0,12 sek)? Amiodaron 300 mg iv w ciągu min i kolejna kardiowersja; następnie: Amiodaron 900 mg w ciągu 24 h Szerokie Wąskie * Kardiowersja powinna być zawsze wykonywana po zastosowaniu sedacji lub znieczulenia ogólnego. Niemiarowe Szerokie Czy zespoły QRS są miarowe? Miarowe Miarowy Wąskie Czy rytm jest miarowy? Niemiarowy Poproś o pomoc specjalistę Zastosuj stymulację nerwu błędnego Adenozyna 6 mg iv, szybki bolus; jeżeli nieskuteczna, podaj 12 mg; jeżeli nieskuteczna, podaj kolejne 12 mg Stale monitoruj rytm sreca Niemiarowy częstoskurcz z wąskimi QRS Prawdopodobnie migotanie przedsionków Kontroluj rytm komór: ß-bloker lub diltiazem Rozważ digoksynę lub amiodaron przy objawach niewydolności serca Włącz leki p/zakrzepowe, gdy >48 h Możliwe przyczyny: AF z blokiem odnogi lecz jak częstoskurcz z wąskimi QRS AF w zespole preekscytacji rozważ amiodaron (np. torsades de pointes podaj magnez 2 g w ciągu 10 min) Jeżeli częstoskurcz komorowy (lub nie masz pewności): Amiodaron 300 mg iv w ciągu min, następnie 900 mg w ciągu 24 h Jeśli wcześniej stwierdzono SVT z blokiem odnogi: Podaj adenozynę jak dla miarowych częstoskurczów z wąskimi QRS Przywrócono rytm zatokowy? Tak Prawdopodobnie PSVT w mechanizmie re-entry: Wykonaj 12-odprowadzeniowe EKG przy rytmie zatokowym Jeśli nawraca, podaj ponownie adenozynę i rozważ profilaktyczne leczenie antyarytmiczne Nie Poproś o pomoc specjalistę Prawdopodobnie trzepotanie przedsionków Kontroluj rytm serca (np. β-bloker) Ryc Algorytm postępowania w tachykardii
28 30 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 pod uwagę potencjalne przyczyny wywołujące bradykardię i poszukiwać objawów niepokojących. W przypadku istnienia objawów niepokojących należy wdrożyć leczenie. Należy leczyć każdą rozpoznaną w trakcie wstępnej oceny potencjalnie odwracalną przyczynę bradykardii. Wstępne postępowanie opiera się na podawaniu leków, a stymulacja serca jest zarezerwowana dla pacjentów, u których nie uzyskano odpowiedzi na leczenie farmakologiczne lub z towarzyszącymi czynnikami ryzyka wystąpienia asystolii (ryc. 1.8). Opieka poresuscytacyjna Przywrócenie spontanicznego krążenia (ROSC) jest tylko pierwszym krokiem w kierunku osiągnięcia celu, jakim jest powrót do stanu zdrowia sprzed zatrzymania krążenia. W skład zespołu objawów występujących po zatrzymaniu krążenia syndrom poresuscytacyjny (SP) (post-cardiac arrest syndrome) wchodzą występujące po zatrzymaniu krążenia uszkodzenie mózgu, dysfunkcja mięśnia sercowego, efekt systemowego niedokrwienia/reperfuzji oraz przewlekle trwające procesy chorobowe, mogące komplikować okres poresuscytacyjny 3. Nasilenie objawów jest zależne od czasu trwania i przyczyny zatrzymania krążenia. W przypadku epizodów krótkotrwałych zespół ten może w ogóle nie wystąpić. Uszkodzenie mózgu po zatrzymaniu krążenia objawia się występowaniem śpiączki, drgawek, mioklonii, zaburzeń poznawczych o różnym stopniu nasilenia oraz śmiercią mózgu. Wśród pacjentów, którzy przeżyli do przyjęcia na OIT, ale zmarli podczas hospitalizacji, uszkodzenie mózgu było przyczyną śmierci u 68% w przypadku pozaszpitalnego zatrzymania krążenia oraz u 23% po epizodzie wewnątrzszpitalnym 227,305. Uszkodzenie mózgu po zatrzymaniu krążenia może być nasilone przez zaburzenia w obrębie mikrokrążenia, upośledzenie autoregulacji przepływu mózgowego, hiperkarbię, hiperoksję, podwyższoną temperaturę ciała, hiperglikemię i drgawki. Znaczna dysfunkcja mięśnia sercowego występuje często po zatrzymaniu krąże- Postępowanie w przypadku bradykardii Oceń, stosując schemat ABCDE Podaj tlen, zapewnij dostęp dożylny Monitoruj EKG, ciśnienie krwi, SpO 2, wykonaj 12-odprowadzeniowe EKG Rozpoznaj i lecz odwracalne przyczyny (np. zaburzenia elektrolitowe) Tak Oceń, czy występują objawy niepokojące: 1. Wstrząs 2. Omdlenie 3. Niedokrwienie mięśnia sercowego 4. Niewydolność serca Nie Atropina 500 μg iv Pozytywna odpowiedź? Tak Nie W międzyczasie: Atropina 500 μg iv powtarzaj do max dawki 3 mg Izoprenalina 5 μg/min Adrenalina 2 10 μg/min Alternatywne leki* LUB Stymulacja przezskórna Tak Ryzyko asystolii? Ostatnio przebyty epizod asystolii Blok AV Mobitz II Całkowity blok serca z szerokimi zespołami QRS Pauzy komorowe >3 sek Nie Poproś o pomoc specjalistę Podejmij działania w celu założenia stymulacji wewnętrznej Obserwuj * Alternatywne leki: Aminofilina Dopamina Glukagon (przy przedawkowaniu β-blokerów lub blokerów kanałów wapniowych) Glycopyrolate można stosować zamiast atropiny Ryc Algorytm postępowania w przypadku bradykardii
29 Podsumowanie Komitetu Wykonawczego ERC 31 nia, ale typowo ustępuje po 2 3 dniach 306,307. Występujące w przebiegu zatrzymania krążenia niedokrwienie i reperfuzja dotycząca całego organizmu aktywuje układ immunologiczny oraz krzepnięcia, co sprzyja wystąpieniu niewydolności wielonarządowej i zwiększonemu ryzyku infekcji 308,309. Zatem SP posiada wiele cech wspólnych z sepsą, w tym spadek objętości wewnątrznaczyniowej i wazodylatację 310,311. Drogi oddechowe i oddychanie Zarówno hipoksemia, jak i hiperkapnia mogą zwiększać prawdopodobieństwo kolejnego epizodu zatrzymania krążenia oraz nasilić wtórne uszkodzenie mózgu. W kilku badaniach z udziałem zwierząt wykazano, że hiperoksemia wywołuje stres oksydacyjny oraz powoduje uszkodzenie neuronów dotkniętych niedokrwieniem 273, Analiza baz danych pacjentów po zatrzymaniu krążenia wykazała, że hiperoksemia występująca po resuscytacji wiąże się z gorszymi wynikami leczenia w zestawieniu z normo- i hipoksemią 274. W praktyce klinicznej należy użyć, gdy tylko są dostępne, wiarygodnych metod monitorowania saturacji krwi tętniczej (gazometria i/lub pulsoksymetria). Praktyczne wydaje się miareczkowanie stężenia tlenu w mieszaninie oddechowej w celu utrzymania saturacji krwi tętniczej na poziomie 94 98%. Należy rozważyć intubację dotchawiczą, sedację i kontrolowaną wentylację u każdego pacjenta z upośledzoną funkcją CSN. Nie ma danych określających docelowy poziom CO 2 w krwi tętniczej po resuscytacji, lecz wydaje się zasadne prowadzenie odpowiedniej wentylacji, monitorowania końcowo-wydechowego poziomu PCO 2 oraz gazometrii krwi tętniczej w celu osiągnięcia normokarbii. Krążenie Uważa się, że pacjenci po zatrzymaniu krążenia w przebiegu zawału mięśnia sercowego z uniesieniem odcinka ST (STEMI) powinni mieć wykonaną wczesną angiografię naczyń wieńcowych oraz PCI, jakkolwiek ból w klatce piersiowej i/lub uniesienie odcinka ST są słabymi czynnikami predykcyjnymi ostrej okluzji naczyń wieńcowych w tej grupie 316. Interwencje te należy rozważyć u wszystkich pacjentów po NZK, u których podejrzewa się chorobę wieńcową Wyniki kilku badań wskazują, że równoczesne stosowanie hipotermii terapeutycznej i PCI jest właściwe i bezpieczne u pacjentów po zatrzymaniu krążenia spowodowanym ostrym zawałem mięśnia sercowego 317, Dysfunkcja mięśnia sercowego po zatrzymaniu krążenia prowadzi do niestabilności hemodynamicznej, co objawia się hipotensją, niskimi wartościami wskaźnika sercowego oraz zaburzeniami rytmu 306. Jeśli resuscytacja płynowa i leki wazoaktywne są niewystarczające, by utrzymać perfuzję, należy rozważyć zastosowanie kontrapulsacji wewnątrzaortalnej 317,325. Wobec braku ostatecznych danych należy dążyć do osiągnięcia właściwego poziomu średniego ciśnienia tętniczego pozwalającego na uzyskanie odpowiedniej diurezy (1 ml/kg/h) i prawidłowego lub malejącego poziomu mleczanów surowicy. W tych działaniach należy brać pod uwagę ciśnienie tętnicze krwi typowe dla danego pacjenta, przyczynę zatrzymania krążenia oraz ciężkość dysfunkcji mięśnia sercowego 3. Powikłania neurologiczne optymalizacja terapii Kontrola drgawek Drgawki i/lub mioklonie występują u 5 15% dorosłych pacjentów po ROSC i około 10 40% spośród pozostających w stanie śpiączki 58, Drgawki trzykrotnie zwiększają metabolizm mózgowy 331 i mogą powodować uszkodzenie CSN. Powinny one być szybko i skutecznie leczone za pomocą benzodiazepin, fenytoiny, walproinianu sodu, propofolu lub barbituranów. Żadne z przeprowadzonych badań bezpośrednio nie odnosiło się do profilaktycznego zastosowania leków przeciwdrgawkowych u dorosłych pacjentów po zatrzymaniu krążenia. Kontrola glikemii Istnieje silny związek pomiędzy wysokim poziomem glikemii u pacjentów po resuscytacji a niekorzystnym rokowaniem neurologicznym 58, Duże badanie z randomizacją wykazało, że intensywna kontrola glikemii (4,5 6,0 mmol/l) w porównaniu do kontroli konwencjonalnej (10 mmol/l i mniej) u pacjentów OIT wiąże się ze zwiększoną 90-dniową śmiertelnością w pierwszej grupie 339. Inne niedawno opublikowane badanie oraz 2 metaanalizy badań porównujących ścisłą i konwencjonalną kontrolę glikemii u ciężko chorych pacjentów wykazały brak istotnej różnicy w śmiertelności, natomiast intensywna kontrola glikemii wiązała się z częstszym występowaniem epizodów hipoglikemii Znaczna hipoglikemia wiąże się ze zwiększoną śmiertelnością w grupie ciężko chorych pacjentów 343. Pacjenci pozostający w stanie śpiączki są szczególnie narażeni na nierozpoznanie hipoglikemii. Udowodniono, iż nieutrzymywanie założonego poziomu glukozy i wahania jej wartości mają wpływ na śmiertelność 344. W oparciu o dostępne dane, poziom glukozy po ROSC powinien być utrzymywany 10 mmol/l (180 mg/dl) 345. Należy unikać hipoglikemii. Nie należy stosować intensywnej kontroli glikemii u dorosłych pacjentów po ROSC, z uwagi na zwiększone ryzyko wystąpienia hipoglikemii. Kontrola temperatury Leczenie podwyższonej temperatury Okres hipertermii (hiperpyreksji) występuje często w ciągu pierwszych 48 godzin po zatrzymaniu krążenia Kilka badań wykazało związek pomiędzy wystąpieniem podwyższonej temperatury po zatrzymaniu krążenia i złym rokowaniem 58,346, Brak jest badań z randomizacją i grupą kontrolną oceniających efekt leczenia pyreksji (definiowanej jako temperatura ciała 37,6 C) u pacjentów po zatrzymaniu krążenia. Mimo że nie udowodniono wpływu temperatury na wyniki leczenia, wydaje się zasadnym leczenie każdego epizodu hipertermii po zatrzymaniu krążenia stosując leki przeciwgorączkowe lub aktywne ochładzanie. Terapeutyczna hipotermia W oparciu o wyniki badań z udziałem zwierząt i ludzi uważa się, że umiarkowana hipotermia ma działanie neuroprotekcyjne i poprawia wyniki leczenia po okresie uogólnionej hipoksji i niedokrwienia mózgu 352,353. Schłodzenie 1
30 32 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 hamuje aktywność licznych szlaków metabolicznych prowadzących do opóźnionej śmierci komórki, włączając w to apoptozę (zaprogramowana śmierć komórki). Hipotermia zmniejsza metabolizm mózgowy tlenu (Cerebral Metabolic Rate for Oxygen CMRO 2 ) o około 6% na każdy stopień obniżonej temperatury 354, a to z kolei hamuje uwalnianie aminokwasów pobudzających i wolnych rodników 352. Hipotermia blokuje wewnątrzkomórkowe następstwa działania toksyn pobudzających (wysokie stężenie jonów wapnia i glutaminianu) i redukuje odpowiedź zapalną związaną z występowaniem syndromu poresuscytacyjnego. Wszystkie badania poświęcone hipotermii terapeutycznej po zatrzymaniu krążenia obejmowały jedynie pacjentów w stanie śpiączki. Istnieją silne dowody świadczące o przydatności indukowanej hipotermii u pozostających w stanie śpiączki pacjentów po pozaszpitalnym zatrzymaniu krążenia w mechanizmie VF. Jedno badanie kliniczne z randomizacją 355 i jedno badanie z pseudorandomizacją 356 wykazały poprawę neurologicznych wyników leczenia przy wypisie ze szpitala lub po upływie 6 miesięcy u dorosłych pacjentów pozostających w stanie śpiączki po resuscytacji z powodu pozaszpitalnego zatrzymania krążenia (VF). Schładzanie pacjentów rozpoczynano w ciągu kilku minut lub godzin po ROSC, a następnie utrzymywano przez godziny na poziomie C. Ekstrapolacja tych wyników na epizody zatrzymania krążenia wywołane innymi przyczynami (inne mechanizmy, wewnątrzszpitalne zatrzymanie krążenia, pacjenci pediatryczni) wydaje się rozsądna, ale oparta jest na danych o niższej wiarygodności 317, Praktyczne stosowanie hipotermii terapeutycznej zostało podzielone na trzy fazy: indukcja, podtrzymanie i ponowne ogrzanie 364. Badania na zwierzętach wykazały, że wczesne stosowanie hipotermii po ROSC wiąże się z lepszymi wynikami końcowymi 365. Do indukcji hipotermii mogą być stosowane techniki zewnętrzne i/lub wewnętrzne. Wlew 30 ml/kg roztworu soli fizjologicznej lub roztworu Hartmanna o temperaturze 4 C obniża głęboką temperaturę ciała o około 1,5 C. Inne metody indukcji i/lub podtrzymywania hipotermii obejmują stosowanie: worków z lodem i/lub mokrych ręczników, chłodzących kocy lub okładów z obiegiem zimnej wody lub powietrza, pokrytych żelem materacy z obiegiem wody, wewnątrznaczyniowych wymienników ciepła, krążenia pozaustrojowego. W fazie podtrzymania hipotermii należy stosować metodę umożliwiającą skuteczną kontrolę temperatury. Można to osiągnąć stosując techniki zewnętrzne i/lub wewnętrzne, dające ciągłą informację zwrotną, co pozwala uzyskać zamierzoną temperaturę docelową. Podczas fazy ogrzewania, podobnie jak w fazie schładzania, stężenia osoczowe elektrolitów, objętość wewnątrznaczyniowa i aktywność metaboliczna mogą ulegać gwałtownym zmianom. Z tego powodu ogrzewanie musi następować wolno. Optymalna szybkość ogrzewania nie jest znana, ale obecnie osiągnięty konsensus zakłada, że powinna ona wynosić około 0,25 0,5 C w ciągu godziny 362. Należy być przygotowanym na wystąpienie dobrze poznanych fizjologicznych efektów związanych z hipotermią 364. Rokowanie Przyczyną dwóch trzecich zgonów pacjentów z pozaszpitalnym zatrzymaniem krążenia, którzy zmarli po przyjęciu na OIT, było uszkodzenie neurologiczne, niezależnie od tego, czy zastosowano hipotermię terapeutyczną 227, czy nie 305. W przypadku wewnątrzszpitalnych zatrzymań krążenia przyczyna ta odpowiadała za jedną czwartą zgonów pacjentów przyjętych do OIT. Poszukiwane są metody, jakie można zastosować u indywidualnych pacjentów w celu prognozowania neurologicznych wyników leczenia bezpośrednio po ROSC. Wiele badań koncentruje się na prognozowaniu wystąpienia niekorzystnych odległych wyników leczenia (stan wegetatywny lub zgon), w oparciu o badanie kliniczne lub testy laboratoryjne wskazujące na istnienie nieodwracalnego uszkodzenia mózgu. Mają one na celu pomóc klinicystom w podjęciu decyzji o ograniczaniu bądź zaprzestaniu uporczywej terapii. Warunkiem zastosowania tych testów prognostycznych powinna być 100-procentowa swoistość lub wskaźnik wyników fałszywie dodatnich (False Positive Rate FPR) na poziomie zero, tzn. rozpoznanie pacjentów, którzy ostatecznie uzyskają dobre długoterminowe wyniki leczenia pomimo wstępnego złego rokowania. Testy kliniczne Nie ma neurologicznych objawów, za pomocą których można wiarygodnie przewidzieć niekorzystny wynik leczenia (Cerebral Performance Category CPC: 3, 4 lub zgon) w ciągu pierwszych 24 godzin po zatrzymaniu krążenia. U pacjentów dorosłych pozostających w stanie śpiączki po zatrzymaniu krążenia, którzy nie byli leczeni za pomocą hipotermii terapeutycznej i wykluczono u nich czynniki wpływające na wiarygodną ocenę (takie jak hipotensja, leki uspakajające lub zwiotczające), brak zarówno reakcji źrenic na światło, jak i odruchów rogówkowych w okresie 72 godzin uważa się za wiarygodne czynniki prognostyczne niepomyślnego wyniku leczenia (FPR 0%, 95% CI 0 9%) 330. Mniej wiarygodne jest stwierdzenie braku odruchów przedsionkowo-ocznych w okresie 24 godzin (FPR 0%, 95% CI 0 14%) 366,367 oraz odpowiedzi motorycznej wg skali GCS równej lub niższej od 2 72 godzin (FPR 5%, 95% CI 2 9%) 330. Inne objawy kliniczne, w tym mioklonie, nie mogą być zaliczane do czynników wskazujących na niepomyślne rokowania. Obecność mioklonii u pacjentów dorosłych silnie wiąże się ze złym rokowaniem 329,330, , jakkolwiek opisywano rzadkie przypadki dobrych neurologicznych wyników leczenia w tej grupie pacjentów, co powoduje, że postawienie właściwej diagnozy w tych przypadkach jest problematyczne Markery biochemiczne Nie ma dowodów, by osoczowe (neuronospecyficzna enolaza, białko S-100) i obecne w płynie mózgowo-rdzeniowym biomarkery były przydatne jako jedyne narzędzie rokownicze u pacjentów w stanie śpiączki po zatrzymaniu krążenia bez względu na to, czy zastosowano hipotermię terapeutyczną, czy nie. Elementami ograniczającymi przydatność tych parametrów jest mała liczebność badanej populacji pacjentów i/lub brak jednolitych wartości odcięcia dla prognozowania niekorzystnych wyników leczenia.
31 Podsumowanie Komitetu Wykonawczego ERC 33 Badania elektrofizjologiczne Żadne z badań elektrofizjologicznych nie pozwala w sposób wiarygodny przewidzieć wyniku leczenia u pacjentów pozostających w śpiączce w ciągu pierwszych 24 godzin po zatrzymaniu krążenia. W przypadku oceny somatosensorycznych potencjałów wywołanych, obustronny brak odpowiedzi korowej N20 na stymulację nerwu pośrodkowego u pacjentów w śpiączce po zatrzymaniu krążenia i nieleczonych za pomocą hipotermii terapeutycznej, wiąże się ze złym rokowaniem (zgon lub CPC: 3, 4) z FPR równym 0,7% (95% CI: 0,1 3,7) 376. Badania obrazowe Badano wiele metod obrazowania pod kątem ich przydatności w ocenie rokowania wyników leczenia u dorosłych pacjentów po zatrzymaniu krążenia. W tym gronie znalazły się MRI, TK, SPECT, angiografia naczyń mózgowych, Doppler przezczaszkowy, badania z zakresu medycyny nuklearnej, NIRS (Near Infra-Red Spectroscopy) 15. Brak jest aktualnie wiarygodnych danych popierających zastosowanie jakichkolwiek metod obrazowania w celu oceny rokowania u pozostających w stanie śpiączki pacjentów, którzy przeżyli zatrzymanie krążenia. Wpływ hipotermii terapeutycznej na rokowanie Istnieje niewystarczająca ilość dowodów potwierdzających przydatność stosowania określonego sposobu prognozowania niepomyślnych wyników leczenia u pacjentów po zatrzymaniu krążenia leczonych za pomocą hipotermii terapeutycznej. Do chwili obecnej nie uznano, aby jakikolwiek neurologiczny objaw kliniczny, badanie elektrofizjologiczne, biomarkery lub badanie obrazowe pozwalały w sposób wiarygodny określić neurologiczny wynik leczenia w ciągu pierwszych 24 godzin po zatrzymaniu krążenia. W oparciu o ograniczoną liczbę dostępnych dowodów uważa się, że obustronny brak odpowiedzi korowej N20 na stymulację nerwu pośrodkowego 24 godzin po zatrzymaniu krążenia (FPR 0%, 95% CI: 0 69%) oraz brak zarówno reakcji źrenic na światło, jak i odruchów rogówkowych w okresie 3 dni od zatrzymania krążenia (FPR 0%, 95% CI 0 48%) uważa się za potencjalnie wiarygodne czynniki prognozujące złe rokowanie u pacjentów leczonych za pomocą hipotermii 368,377. Istnieje również ograniczona ilość danych wskazujących, że funkcje motoryczne określone wg skali GCS 2 w okresie 3 dni po ROSC (FPR 14%, 95% CI 3 44%) 368 oraz obecność stanu padaczkowego (FPR 7% [95% CI 1 25%] do 11,5% [95% CI 3 31%]) 378,379 są potencjalnie niewiarygodnymi czynnikami prognozującymi niepomyślne rokowanie u pacjentów leczonych za pomocą hipotermii. Mając na względzie ograniczoną ilość dostępnych dowodów, decyzja o zaprzestaniu uporczywej terapii nie powinna opierać się wyłącznie o wyniki pojedynczych narzędzi prognostycznych. Przeszczepianie narządów Możliwe jest skuteczne przeszczepianie narządów od pacjentów po śmierci sercowej (cardiac death) 380. Ta grupa pacjentów daje niewykorzystywaną możliwość zwiększenia ilości potencjalnych dawców. Pozyskiwanie organów od dawców z niebijącym sercem (non-heart beating donors) jest klasyfikowane jako kontrolowane i niekontrolowane 381. Donacja kontrolowana następuje w wyniku wcześniej zaplanowanego zaprzestania leczenia u pacjentów po śmiertelnych urazach/chorobach. Donacja niekontrolowana dotyczy sytuacji, kiedy dochodzi do pobrania narządów od pacjenta przewiezionego do szpitala i stwierdzeniu zgonu z powodu nieodwracalnego zatrzymania krążenia (brought in dead) lub w trakcie trwania czynności resuscytacyjnych, które nie dają efektu w postaci powrotu spontanicznego krążenia. Centra leczenia pacjentów po zatrzymaniu krążenia Istnieje duża zmienność dotycząca przeżywalności pacjentów w szpitalach zajmujących się leczeniem chorych po zatrzymaniu krążenia Istnieją słabe dowody (low-level), że OIT przyjmujące rocznie ponad 50 pacjentów po zatrzymaniu krążenia osiągają lepsze wskaźniki przeżycia niż OIT przyjmujące rocznie mniej niż 20 pacjentów 61. Istnieją pośrednie dowody mówiące o wpływie regionalnych systemów opieki kardiologicznej na poprawę wyników leczenia u pacjentów po zawale mięśnia sercowego z uniesieniem odcinka ST (STEMI) Z powyższych danych wynika, że specjalistyczne centra i systemy opieki ukierunkowane na leczenie pacjentów po zatrzymaniu krążenia mogą okazać się skuteczne, ale, jak do tej pory, nie udało się zgromadzić bezpośrednich dowodów potwierdzających tę hipotezę Wstępne postępowanie w ostrych zespołach wieńcowych Wprowadzenie W wielu krajach europejskich częstość występowania ostrego zawału mięśnia sercowego z uniesieniem odcinka ST (Acute Myocardial Infarction AMI) zmniejsza się 408 podczas gdy zwiększa się częstość występowania ostrego zespołu wieńcowego bez uniesienia odcinka ST (NSTEMI- -OZW) 409,410. Chociaż dzięki nowoczesnej terapii reperfuzyjnej i poprawie wtórnej profilaktyki udało się znacznie zmniejszyć wewnątrzszpitalną śmiertelność z powodu STEMI, całkowita śmiertelność w ciągu 28 dni pozostaje praktycznie niezmienna, ponieważ dwie trzecie pacjentów umiera przed przyjęciem do szpitala, głównie z powodu ciężkich zaburzeń rytmu wywołanych przez niedokrwienie 411. Dlatego najlepszym sposobem poprawy przeżywalności w przebiegu ostrego niedokrwienia jest ograniczenie opóźnienia pomiędzy pojawieniem się objawów a pierwszym kontaktem z personelem medycznym oraz rozpoczęcie celowanego leczenia we wczesnej, przedszpitalnej, fazie choroby. Termin ostre zespoły wieńcowe (OZW) zawiera w sobie trzy różne jednostki chorobowe z ostrymi objawami choroby wieńcowej: zawał mięśnia sercowego z uniesieniem odcinka ST (ST Elevation Myocardial Infarction STEMI), zawał mięśnia sercowego bez uniesienia odcinka ST (non- -ST Elevation Myocardial Infarction NSTEMI) oraz niestabilną dusznicę bolesną (Ustable Angina Pectoris UAP). Zawał mięśnia sercowego bez uniesienia odcinka ST oraz UAP zwykle określa się łącznie mianem NSTEMI-OZW. 1
32 34 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Częstą przyczyną OZW jest pęknięcie lub erozja blaszki miażdżycowej 412. Zmiany elektrokardiograficzne (brak lub obecność uniesienia odcinka ST) różnicuje STEMI od NSTEMI-OZW. Te ostatnie mogą przebiegać z obniżeniem lub niespecyficznymi zmianami odcinka ST, a nawet prawidłowym zapisem EKG. W przypadku braku uniesienia odcinka ST wzrost stężenia markerów uszkodzenia mięśnia sercowego w surowicy, szczególnie troponin T lub I jako najbardziej specyficznych wskaźników martwicy mięśnia sercowego, wskazuje na obecność NSTEMI. OZW są najczęstszą przyczyną poważnych zaburzeń rytmu serca prowadzących do nagłej śmierci sercowej. Celem terapeutycznym jest leczenie ostrych, zagrażających życiu stanów, takich jak migotanie komór (VF), skrajna bradykardia, jak również utrzymanie funkcji lewej komory oraz zapobieganie wystąpieniu niewydolności krążenia poprzez minimalizację obszaru uszkodzenia mięśnia sercowego. Aktualne wytyczne dotyczą pierwszych godzin od wystąpienia objawów. Postępowanie przedszpitalne i wstępne leczenie w obrębie szpitalnego oddziału ratunkowego (SOR) może się różnić w zależności od lokalnych możliwości, protokołów i uwarunkowań. Dane dotyczące sposobu postępowania przedszpitalnego są zwykle ekstrapolowane z badań nad wstępnym leczeniem pacjentów zaraz po przyjęciu ich do szpitala; istnieje jedynie kilka wartościowych badań dotyczących oceny postępowania przed przyjęciem pacjenta do szpitala. Wyczerpujące wytyczne dotyczące diagnostyki i leczenia OZW, z uniesieniem lub bez uniesienia odcinka ST, zostały opublikowane przez European Society of Cardiology i American College of Cardiology / American Heart Association. Aktualne rekomendacje pozostają z nimi w zgodzie (ryc. 1.9 i ryc. 1.10) 413,414. Rozpoznanie i ocena ryzyka w ostrych zespołach wieńcowych Zagrożeni pacjenci i ich rodziny powinni umieć rozpoznać charakterystyczne objawy, takie jak ból w klatce piersiowej promieniujący do innych obszarów górnej połowy ciała, któremu często towarzyszą: duszność, potliwość, nudności, wymioty lub utrata przytomności. Powinni oni także rozumieć potrzebę wczesnego wezwania pogotowia ratunkowego, a najlepiej by byli oni przeszkoleni w zakresie wykonywania BLS. Dalszego opracowania wymagają metody mające na celu zwiększanie znajomości różnych rodzajów OZW oraz poprawy częstości rozpoznawania OZW w szczególnie narażonych grupach pacjentów. Dyspozytorzy Pogotowia Ratunkowego muszą umieć rozpoznawać OZW zadając odpowiednie pytania. Objawy OZW Typowe objawy towarzyszące OZW to promieniujący ból w klatce piersiowej, duszność oraz wzmożona potliwość, jednakże u pacjentów w podeszłym wieku, kobiet lub u chorujących na cukrzycę mogą wystąpić nietypowy obraz lub objawy niespecyficzne 415,416. Żaden z tych objawów nie może być jedyną podstawą rozpoznania OZW. 12-odprowadzeniowe EKG 12-odprowadzeniowe EKG jest kluczowym badaniem dla oceny OZW. W przypadku STEMI, wskazuje ono potrzebę pilnej terapii reperfuzyjnej (np. pierwotnej przezskórnej interwencji wieńcowej lub prowadzonej przedszpitalnie fibrynolizy). Kiedy podejrzewany jest OZW, 12-odprowadzeniowe EKG powinno być wykonane i ocenione najszybciej jak to jest możliwe po pierwszym kontakcie pacjenta z personelem medycznym, celem wcześniejszego postawie- Ryc Definicje ostrych zespołów wieńcowych (OZW) (STEMI zawał mięśnia sercowego z uniesieniem odcinka ST; NSTEMI zawał mięśnia sercowego bez uniesienia odcinka ST; UAP niestabilna choroba wieńcowa)
33 Podsumowanie Komitetu Wykonawczego ERC 35 1 # Zgodnie ze stratyfikacją ryzyka * Prasugrel, w dawce wysycającej 60 mg, może być stosowany jako alternatywa dla klopidogrelu u pacjentów ze STEMI oraz planowaną PPCI, jeśli nie mają udaru lub TIA w wywiadzie. W momencie opracowania wytycznych tikagrelor nie został jeszcze zaakceptowany jako alternatywa dla klopidogrelu. Ryc Algorytm leczenia ostrych zespołów wieńcowych (PCI = przezskórna interwencja wieńcowa; UFH = heparyna niefrakcjonowana) nia rozpoznania oraz przeprowadzenia kwalifikacji pacjenta. EKG wykonane w warunkach przedszpitalnych lub SOR ma dużą wartość diagnostyczną, jeśli jest interpretowane przez przeszkolony personel medyczny 417. Zapis 12-odprowadzeniowego EKG wykonany w warunkach przedszpitalnych umożliwia wczesne zawiadomienie ośrodka przyjmującego pacjenta oraz przyspiesza decyzje terapeutyczne. Ratownicy medyczni oraz pielęgniarki powinni być szkoleni w rozpoznawaniu STEMI bez bezpośredniego wsparcia lekarza tak długo, jak długo zapewnia się ścisłą kontrolę nad jakością takiego działania. Jeśli interpretacja wykonanego przedszpitalnie EKG nie jest możliwa na miejscu, powinno się dokonać interpretacji komputerowej 418,419 lub przesłać zapis EKG (teletransmisja). Biomarkery W przypadku charakterystycznego wywiadu brak uniesień odcinka ST w 12-odprowadzeniowym EKG oraz podwyższony poziom markerów martwicy mięśnia sercowego (troponiny T, troponiny I, CK, CK-MB, mioglobiny) świadczy o obecności NSTEMI i pozwala na różnicowanie ze STEMI oraz niestabilną dusznicą bolesną. Preferowanym markerem są specyficzne dla mięśnia sercowego troponiny. Podwyższone poziomy troponiny są szczególnie przydatne w identyfikacji pacjentów z grupy zwiększonego ryzyka niepomyślnego przebiegu choroby 420. Zasady podejmowania decyzji o wczesnym wypisie Podjęto próby połączenia danych z wywiadu, badania fizykalnego oraz powtarzanych zapisów EKG i oznaczeń markerów biochemicznych, celem stworzenia zasad klinicznych, które pomogłyby w oddziale ratunkowym zróżnicować pacjentów z podejrzewanym OZW. Jednakże żadna z tych zasad nie jest odpowiednia i wystarczająca do rozpoznania w SOR pacjenta z bólem w klatce piersiowej i podejrzeniem OZW, którego można bezpiecznie wypisać 421. Protokoły obserwacji pacjentów z bólem w klatce piersiowej Dla pacjentów oddziału ratunkowego z wywiadem charakterystycznym w kierunku OZW, ale prawidłowymi badaniami wstępnymi, bezpiecznym i skutecznym rozwiązaniem mogą być oddziały obserwacyjne dla pacjentów z bólem w klatce piersiowej. Mogą one przyczynić się do ograniczenia czasu pobytu w szpitalu, ilości przyjęć do szpitala oraz obniżenia kosztów ponoszonych przez służbę zdrowia, a także poprawy skuteczności diagnostycznej oraz jakości życia 422. Nie ma
34 36 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 bezpośrednich dowodów wskazujących na to, że oddziały obserwacyjne dla pacjentów z bólem w klatce piersiowej lub protokoły obserwacji zmniejszają częstość niekorzystnych wyników leczenia zdarzeń sercowo-naczyniowych, w szczególności śmiertelności u pacjentów z objawami sugerującymi OZW. Objawowe leczenie ostrych zespołów wieńcowych Triazotan glicerolu jest skutecznym lekiem w przypadku wieńcowego bólu w klatce piersiowej, wywołującym również korzystny efekt hemodynamiczny poprzez poszerzenie łożyska żylnego, rozkurcz tętnic wieńcowych oraz w mniejszym stopniu, tętnic obwodowych. Można rozważyć podanie triazotanu glicerolu, gdy skurczowe ciśnienie tętnicze jest wyższe niż 90 mm Hg oraz gdy występują dolegliwości bólowe w klatce piersiowej. Podanie triazotanu glicerolu może również być korzystne w leczeniu ostrego zastoju w krążeniu płucnym. Nie należy stosować nitratów u pacjentów z niskim ciśnieniem krwi ( 90 mm Hg skurczowego ciśnienia krwi), zwłaszcza gdy towarzyszy temu bradykardia, oraz u pacjentów z zawałem dolnej ściany mięśnia sercowego i podejrzeniem zawału prawej komory. Użycie nitratów w tych przypadkach może spowodować znaczne obniżenie ciśnienia krwi oraz rzutu serca. Morfina jest lekiem z wyboru w przypadku zwalczania bólu opornego na działanie nitratów, a dzięki jej działaniu uspokajającemu użycie leków sedatywnych w większości przypadków nie jest konieczne. Jako lek zwiększający pojemność łożyska żylnego może ona przynieść dodatkowe korzyści w przypadku zastoju w krążeniu płucnym. Morfinę należy podawać w dawkach 3 5 mg dożylnie, powtarzanych co kilka minut, aż do ustąpienia bólu. W leczeniu przeciwbólowym powinno się unikać niesteroidowych leków przeciwzapalnych (NSAIDs) ze względu na ich działanie prozakrzepowe 423. Monitorowanie saturacji krwi tętniczej (SaO 2 ) przy pomocy pulsoksymetru pomaga ocenić potrzebę stosowania tlenoterapii. Tylko pacjenci z hipoksemią wymagają leczenia tlenem. Niektóre dane wskazują, że tlen w dużych przepływach może być szkodliwy dla pacjentów z niepowikłanym zawałem mięśnia sercowego Należy dążyć do utrzymywania saturacji krwi pomiędzy 94 a 98% lub 88 92%, jeśli pacjent narażony jest na ryzyko niewydolności oddechowej związanej z hiperkapnią 427. Przyczynowe leczenie ostrych zespołów wieńcowych Inhibitory agregacji płytek Ponieważ aktywacja i agregacja płytek są głównymi procesami wyzwalającymi OZW, hamowanie agregacji płytek jest jednym z najważniejszych elementów wstępnego leczenia zespołów wieńcowych, jak również są istotne w prewencji wtórnej. Kwas acetylosalicylowy (ASA) Dane z dużych, randomizowanych badań klinicznych wykazują zmniejszoną śmiertelność u pacjentów przyjętych do szpitala z rozpoznaniem OZW, którym podawano mg kwasu acetylosalicylowego (Acetylsalicylic Acid ASA). Kilka prac sugeruje zmniejszoną śmiertelność, gdy ASA podawano wcześniej 428,429. Dlatego zaleca się jak najwcześniejsze podanie ASA wszystkim pacjentom z podejrzeniem OZW, za wyjątkiem osób z prawdziwą alergią na ten lek. ASA może być podany przez personel medyczny, świadka zdarzenia lub wzięty za poradą dyspozytora pogotowia, zależnie od lokalnych standardów postępowania. Wstępna dawka ASA podana doustnie (do rozgryzienia) wynosi mg. Inne formy ASA (rozpuszczalna, dożylna) mogą być równie skuteczne co rozgryzione tabletki. Inhibitory receptorów ADP Tienopirydyny (klopidogrel, prasugrel) oraz cyklo-pentylo-triazolo-pirymidyna, tikagrelor, hamują nieodwracalnie receptor ADP, co powoduje dalsze hamowanie agregacji płytek, zainicjowane przez ASA. Klopidogrel podany oprócz heparyny i ASA pacjentom z dużym ryzykiem NSTEMI-OZW poprawia wyniki leczenia 430,431. Dlatego też klopidogrel w połączeniu z ASA oraz lekiem przeciwkrzepliwym powinien być podany tak szybko, jak to jest możliwe, wszystkim pacjentom z NSTEMI- -OZW. Jeśli wybiera się leczenie zachowawcze, należy podać dawkę wysycającą 300 mg; przy planowanym PCI preferowana może być dawka 600 mg. Klopidogrel można zastąpić przez prasugrel lub tikagrelor. Chociaż nie ma żadnego dużego badania dotyczącego wstępnego stosowania klopidogrelu u pacjentów z objawami STEMI i planowanym PCI, takie postępowanie jest prawdopodobnie korzystne. Ponieważ im większa dawka, tym lepsze jest hamowanie płytek, pacjentom ze STEMI oraz planowaną PCI zaleca się podanie dawki wysycającej 600 mg tak szybko, jak to jest możliwe. Prasugrel lub tikagrelol mogą być podane zamiast klopidogrelu przed planowaną PCI. Pacjenci ze STEMI leczeni fibrynolizą powinni mieć podawany klopidogrel (300 mg w dawce wysycającej przed 75. rokiem życia oraz 75 mg bez dawki wysycającej po 75. roku życia) w połączeniu z ASA oraz lekiem przeciwkrzepliwym. Inhibitory glikoproteiny (Gp) IIB/IIIA Blokowanie receptora glikoproteiny (Gp) IIB/IIIA jest wspólnym etapem końcowym hamowania agregacji płytek. Eptifibatyd oraz tirofiban hamują receptor Gp IIB/IIIA w sposób odwracalny, podczas gdy abciksymab prowadzi do nieodwracalnej blokady. Obecnie nie ma wystarczających danych popierających rutynowe leczenie wstępne pacjentów ze STEMI lub NSTEMI-OZW inhibitorami Gp IIB/IIIA. Antytrombiny Heparyna niefrakcjonowana (Unfractionated Heparin UFH) jest pośrednim inhibitorem trombiny i w połączeniu z ASA wykorzystuje się ją jako uzupełnienie terapii fibrynolitycznej lub pierwotnej PCI. Stanowi ona istotną część leczenia niestabilnej dusznicy bolesnej lub STEMI. Obecnie dostępnych jest kilka alternatywnych antytrombin stosowanych w leczeniu pacjentów z OZW. W porównaniu z heparyną niefrakcjonowaną leki te mają bardziej specyficzną aktywność czynnika Xa (heparyny drobnocząsteczkowe [LMWH Low Molecular Weight Heparins], fondaparynuks) lub są bezpośrednimi inhibitorami trombiny (biwalirudyna). Zasadniczo przy stosowaniu nowszych antytrombin nie ma
35 Podsumowanie Komitetu Wykonawczego ERC 37 konieczności monitorowania układu krzepnięcia, jak również istnieje mniejsze ryzyko wystąpienia trombocytopenii. W porównaniu z niefrakcjonowaną heparyną enoksaparyna podana w ciągu pierwszych godzin od epizodu NSTEMI-OZW obniża łącznie całkowitą śmiertelność, częstość zawału mięśnia sercowego oraz potrzebę pilnej rewaskularyzacji 432,433. U pacjentów, u których zaplanowano konserwatywne wstępne zaopatrzenie, fondaparinuks oraz enoksaparyna stanowią rozsądną alternatywę dla UFH. U pacjentów ze zwiększonym ryzykiem krwawienia rozważ podanie fondaparinuksu lub biwalirudyny, które w porównaniu do UFH niosą ze sobą mniejsze ryzyko krwawienia U pacjentów, u których zaplanowano leczenie inwazyjne, enoksaparyna lub biwalirudyna stanowią rozsądną alternatywę dla UFH. Kilka randomizowanych badań przeprowadzonych u pacjentów ze STEMI poddawanych fibrynolizie udowodniło, że dodatkowe leczenie enoksaparyną zamiast UFH skutkuje lepszymi wynikami klinicznymi (niezależnie od stosowanego leku fibrynolitycznego), a jednocześnie nieznacznie zwiększonym ryzykiem krwawienia u pacjentów starszych ( 75. roku życia) oraz z niską masą ciała (masa ciała <60 kg) Enoksaparyna stanowi bezpieczną i efektywną alternatywę dla UFH w czasie aktualnie stosowanej PPCI (np. z szerokim zastosowaniem tienopirydyny oraz/lub blokera receptora Gp IIB/IIIA) 440,441. Nie ma wystarczających danych, by zalecić stosowanie innej niż enoksaparyna LMWH do PPCI u pacjentów ze STEMI. Biwalirudyna jest także bezpieczną alternatywą dla UFH w STEMI i planowanej PCI. Strategie leczenia i system opieki Prowadzono badania nad kilkoma rodzajami strategii, których celem była poprawa przedszpitalnej opieki nad pacjentami z OZW. Wszystkie one mają zasadniczo na celu szybkie identyfikacje pacjentów ze STEMI, tak aby skrócić opóźnienie w leczeniu reperfuzyjnym. Ponadto opracowano kryteria przeprowadzania kwalifikacji pacjentów i wyodrębnienia chorych wysokiego ryzyka z NSTEMI-OZW, którzy wymagają transportu do ośrodka najwyższego stopnia referencyjności przeprowadzającego PCI w systemie całodobowym. W tym kontekście podczas wstępnej opieki nad pacjentem konieczne jest podjęcie kilku dodatkowych decyzji ponad podstawowe czynności diagnostyczne oraz ocenę 12-odprowadzeniowego EKG. Te decyzje odnoszą się do: 1. Strategii reperfuzyjnej u pacjentów ze STEMI, np. PPCI lub (przed)szpitalna fibrynoliza. 2. Ominięcia najbliższego, ale nieoferującego PCI szpitala oraz podjęcie kroków mających na celu skrócenie opóźnienia interwencji, jeśli zadecydowano o przeprowadzeniu PPCI. 3. Procedur w warunkach szczególnych, np. u pacjentów skutecznie zresuscytowanych po nieurazowym zatrzymaniu krążenia, pacjentów we wstrząsie lub pacjentów z NSTEMI-OZW, którzy są niestabilni lub mają objawy świadczące o wysokim ryzyku. Terapia reperfuzyjna u pacjentów z objawami STEMI U wszystkich pacjentów z rozpoznanym STEMI terapia reperfuzyjna powinna być rozpoczęta tak szybko, jak to tylko możliwe, bez względu na wybór metody, w czasie nie dłuższym niż 12 godzin od wystąpienia objawów 414, Reperfuzję można uzyskać poprzez fibrynolizę, PPCI lub kombinację obu metod. Korzyści z leczenia reperfuzyjnego zmniejszają się z czasem, który upłynął od wystąpienia objawów. Fibrynoliza jest najbardziej skuteczna, jeżeli terapię rozpocznie się w ciągu pierwszych 2 do 3 godzin od wystąpienia objawów; skuteczność PPCI w mniejszym stopniu zależy od czasu 445. W przypadku STEMI lub objawów OZW z podejrzeniem świeżego LBBB w zapisie EKG korzystne jest podawanie fibrynolityków przed przyjęciem do szpitala. Leczenie fibrynolityczne może być bezpiecznie wdrożone przez przeszkolonych ratowników medycznych, pielęgniarki lub lekarzy przy wykorzystaniu odpowiednich protokołów postępowania Skuteczność tego leczenia jest najwyższa w pierwszych 3 godzinach od wystąpienia objawów 452. U pacjentów z objawami OZW i zmianami o charakterze STEMI w zapisie EKG (lub obecnością świeżego LBBB, czy potwierdzonym zawałem ściany tylnej), którzy zgłaszają się bezpośrednio na oddział ratunkowy, należy jak najszybciej rozpocząć leczenie fibrynolityczne, chyba że możliwa jest natychmiastowa PPCI. Personel medyczny stosujący fibrynolizę musi mieć świadomość istniejącego ryzyka oraz przeciwwskazań do jej wdrożenia. Pierwotna interwencja przezskórna Angioplastyka wieńcowa, z implantacją stentu lub bez, stała się leczeniem z wyboru u pacjentów ze STEMI, ponieważ w kilku badaniach i metaanalizach wykazano wyższość tego sposobu postępowania nad fibrynolizą w obniżaniu częstości występowania zgonu, udaru oraz powtórnego zawału 453,454 jako łącznego punktu końcowego. Fibrynoliza a pierwotna PCI Kilka raportów i przeglądów porównujących leczenie fibrynolityczne (w tym przedszpitalne podanie leku) z PPCI wskazywało na lepsze przeżycie, jeśli fibrynolizę rozpoczęto do 2 godzin od wystąpienia objawów, a następnie przeprowadzono ratunkową lub opóźnioną PCI Jeśli w odpowiednim przedziale czasu nie da się przeprowadzić PPCI, należy niezależnie od potrzeby pilnego przeniesienia pacjenta do innego ośrodka, rozważyć natychmiastową fibrynolizę, o ile nie ma do niej przeciwwskazań. U pacjentów we wstrząsie ze STEMI leczeniem z wyboru jest pierwotna PCI (lub zabieg pomostowania aortalno-wieńcowego). W tych wypadkach fibrynolizę powinno się rozważyć wyłącznie, jeśli ma miejsce znaczące opóźnienie PCI. Kwalifikacja pacjentów oraz przekazywanie ich do innego ośrodka celem wykonania pierwotnej PCI Ryzyko zgonu, ponownego zawału albo udaru jest obniżone, jeżeli pacjenci ze STEMI są natychmiastowo przekazywani z ośrodków o niższej referencyjności do ośrodków mogących wykonać PPCI 383,454,458. W grupie młodszych pacjentów z zawałem ściany przedniej, u których czas od wystąpienia objawów wynosi poniżej 2 3 godzin, nie wyjaśniono, czy więcej korzyści przyniesie przedszpitalna fibrynoliza, czy pierwotna PCI 459. Uzasadnione jest przekazywanie pacjentów ze STEMI celem wykonania pierwotnej PCI wtedy, gdy czas od wystąpienia objawów mieści się w przedziale od 3 12 godzin, a transport jest natychmiast dostępny. 1
36 38 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Połączenie fibrynolizy i przezskórnej interwencji wieńcowej Aby przywrócić wieńcowy przepływ krwi oraz perfuzję mięśnia sercowego, można w różnych połączeniach stosować fibrynolizę oraz PCI. Istnieje kilka sposobów na połączenie tych dwóch rodzajów terapii. Torowana PCI określa PCI przeprowadzoną natychmiast po fibrynolizie, podejście farmakologiczno-inwazyjne odnosi się do PCI planowo przeprowadzonej w czasie 3 do 24 godzin po fibrynolizie, a ratunkowa PCI to PCI przeprowadzana po nieudanej próbie leczenia reperfuzyjnego (określanej jako <50% normalizacji uniesienia odcinka ST po 60 do 90 minutach od zakończenia terapii fibrynolitycznej). Te strategie różnią się od standardowego podejścia, w którym angiografię i interwencję wykonuje się w kilka dni po udanej fibrynolizie. Kilka badań i metaanaliz wskazuje na gorsze wyniki leczenia, jeśli rutynowo przeprowadza się PCI zaraz po fibrynolizie lub tak szybko, jak to jest możliwe 458,460. Dlatego nie poleca się przeprowadzania planowo torowanej PCI, nawet jeśli mogą być podgrupy pacjentów, dla których takie postępowanie byłoby korzystne 461. U pacjentów z nieudaną fibrynolizą, rozpoznaną na podstawie objawów klinicznych oraz/lub niedostatecznej normalizacji odcinka ST, powinno się niezwłocznie wykonać angiografię oraz PCI 462. W przypadku klinicznie skutecznej fibrynolizy (rozpoznanej na podstawie objawów klinicznych i normalizacji odcinka ST >50%) zaobserwowano poprawę rokowania, jeśli angiografię wykonano kilka godzin po fibrynolizie (podejście farmakologiczno-inwazyjne). Po zakończonej fibrynolizie ten sposób leczenia wymaga wczesnego przekazania pacjenta do ośrodka wykonującego angiografię i PCI 463,464. Reperfuzja po skutecznej resuscytacji Choroba niedokrwienna serca jest najczęstszą pozaszpitalną przyczyną zatrzymania krążenia. Wielu z tych pacjentów będzie miało objawy ostrej niedrożności tętnicy wieńcowej z objawami STEMI w zapisie EKG, jednakże zatrzymanie krążenia w przebiegu choroby niedokrwiennej serca może mieć miejsce także w przypadku braku tych zmian. U pacjentów ze STEMI lub świeżym blokiem lewej odnogi pęczka Hisa (LBBB) w EKG, występującymi po ROSC po pozaszpitalnym zatrzymaniu krążenia powinno się rozważyć natychmiastową angiografię i interwencję przezskórną lub fibrynolizę 316,321. Wydaje się także uzasadnione wykonanie natychmiastowej angiografii i PCI u wybranych pacjentów pomimo braku uniesienia odcinka ST lub uprzednich objawów, takich jak ból w klatce piersiowej. Należy uwzględnić leczenie reperfuzyjne w standardowym postępowaniu po zatrzymaniu krążenia jako strategię poprawiającą rokowanie 317. Leczenie reperfuzyjne nie powinno wykluczać innych metod leczniczych, w tym terapeutycznej hipotermii. Prewencja pierwotna i wtórna Postępowanie prewencyjne u pacjentów z objawami OZW powinno być rozpoczęte zaraz po przyjęciu do szpitala, jak również powinny być kontynuowane już podjęte działania. Środki zapobiegawcze poprawiają rokowanie, zmniejszając częstość ciężkich powikłań sercowych. Prewencja farmakologiczna obejmuje stosowanie beta-blokerów, inhibitorów enzymu konwertującego angiotensynę (ACE) / blokerów receptora angiotensyny (ARB) oraz statyn, a także podstawowe leczenie aspiryną i jeśli są wskazania tienopirydynami. Zabiegi resuscytacyjne u dzieci Podstawowe zabiegi resuscytacyjne u dzieci Kolejność postępowania Ratownicy, którzy nie posiadają szczegółowej wiedzy na temat resuscytacji pacjentów pediatrycznych, a byli uczeni algorytmu BLS dorosłych, mogą zastosować kolejność postępowania jak u osób dorosłych, gdyż rokowanie jest gorsze, jeśli nie zrobiliby nic. Osoby bez wykształcenia medycznego, które chcą nauczyć się resuscytacji pacjentów pediatrycznych ze względu na odpowiedzialność, jaką ponoszą za dzieci (np. nauczyciele, pielęgniarki szkolne, ratownicy wodni), powinni być uczeni, że preferuje się modyfikowanie algorytmu BLS dla osób dorosłych, co oznacza konieczność wykonania pięciu oddechów ratowniczych przed rozpoczęciem uciskania klatki piersiowej, a następnie prowadzenie przez około jedną minutę resuscytacji krążeniowo-oddechowej przed udaniem się po pomoc (patrz algorytm BLS dla osób dorosłych). Podstawowe zabiegi resuscytacyjne u dzieci dla osób z obowiązkiem udzielenia pomocy NIE REAGUJE? Głośno wołaj o pomoc Udrożnij drogi oddechowe i sprawdź oddech NIE ODDYCHA PRAWIDŁOWO? 5 oddechów ratowniczych BRAK OZNAK ŻYCIA? 15 uciśnięć klatki piersiowej 2 oddechy ratownicze 15 uciśnięć Po 1 min RKO zadzwoń pod 112 lub 999 albo wezwij zespół resuscytacyjny Ryc Algorytm podstawowych zabiegów resuscytacyjnych u dzieci dla osób z obowiązkiem interwencji
37 Podsumowanie Komitetu Wykonawczego ERC 39 Poniższa sekwencja jest przeznaczona dla osób z obowiązkiem udzielenia pomocy w sytuacjach nagłych u pacjenta pediatrycznego (zazwyczaj profesjonalne zespoły służb medycznych) (ryc. 1.11). 1. Upewnij się, że jest bezpiecznie zarówno dla ciebie jak i dziecka. 2. Sprawdź reakcję dziecka: delikatnie potrząśnij dzieckiem i zapytaj głośno: Czy wszystko w porządku? 3A. Jeśli dziecko odpowiada lub porusza się: pozostaw dziecko w pozycji, w jakiej je zastałeś (pod warunkiem, że nie jest ona dla niego niebezpieczna) oceń jego stan i w razie potrzeby wezwij pomoc powtarzaj regularnie ocenę stanu ogólnego dziecka 3B. Jeśli dziecko nie reaguje: głośno wołaj o pomoc delikatnie odwróć dziecko na plecy udrożnij drogi oddechowe dziecka poprzez odchylenie głowy i uniesienie bródki. umieść rękę na czole dziecka i delikatnie odchyl jego głowę ku tyłowi w tym samym czasie umieść opuszkę palca (lub palców) pod bródką dziecka i unieś ją. Nie naciskaj na tkanki miękkie pod bródką, bo możesz spowodować niedrożność dróg oddechowych jeśli nadal masz trudności z udrożnieniem dróg oddechowych, spróbuj metody wysunięcia żuchwy: połóż palce wskazujące obydwu rąk za żuchwą dziecka po jej bokach i popchnij ją do przodu. 4. Utrzymując drożność dróg oddechowych, oceń wzrokiem, słuchem i dotykiem, czy występują prawidłowe oddechy poprzez przysunięcie swojej twarzy blisko twarzy dziecka i obserwowanie jego klatki piersiowej: obserwuj ruchy klatki piersiowej słuchaj nad nosem i ustami dziecka szmerów oddechowych poczuj ruch powietrza na swoim policzku. W pierwszych kilku minutach po zatrzymaniu krążenia dziecko może nabierać kilka wolnych, nieregularnych oddechów (gasping). Patrz, słuchaj i staraj się wyczuć oddech nie dłużej niż 10 sekund, zanim podejmiesz decyzję. Jeśli masz jakiekolwiek wątpliwości, czy dziecko oddycha prawidłowo, postępuj tak, jakby oddech był nieprawidłowy: 5A. Jeśli dziecko oddycha prawidłowo: ułóż dziecko w pozycji bezpiecznej (patrz poniżej) wyślij kogoś po pomoc lub sam udaj się po pomoc zadzwoń pod lokalny numer ratunkowy, aby wezwać karetkę sprawdzaj, czy oddech nadal występuje. 5B. Jeśli dziecko nie oddycha lub oddycha nieprawidłowo: delikatnie usuń widoczne ciała obce mogące powodować niedrożność dróg oddechowych wykonaj pięć pierwszych oddechów ratowniczych podczas wykonywania oddechów ratowniczych zwróć uwagę na pojawienie się kaszlu lub odruchów z tylnej ściany gardła w odpowiedzi na twoje działania; obecność lub brak tego typu reakcji stanowi część oceny obecności oznak krążenia; zostaną one opisane w dalszej części rozdziału. Oddechy ratownicze dla dzieci powyżej 1. roku życia: zapewnij odchylenie głowy i uniesienie żuchwy kciukiem i palcem wskazującym ręki leżącej na czole zaciśnij miękkie części nosa rozchyl usta dziecka, ale zapewnij uniesienie bródki nabierz powietrza, obejmij szczelnie swoimi ustami usta dziecka, upewniając się, że nie ma przecieku powietrza wykonaj powolny wydech do ust dziecka trwający ok. 1 1,5 sekundy, obserwując równocześnie unoszenie się klatki piersiowej utrzymując odgięcie głowy i uniesienie żuchwy, odsuń swoje usta od ust poszkodowanego i obserwuj, czy podczas wydechu opada klatka piersiowa ponownie nabierz powietrza i powtórz opisaną sekwencję 5 razy; oceń jakość oddechu, obserwując klatkę piersiową dziecka: powinna się unosić i opadać jak przy normalnym oddechu. Oddechy ratownicze dla niemowląt: umieść głowę w pozycji neutralnej i unieś bródkę nabierz powietrza, obejmij szczelnie swoimi ustami usta i nos dziecka upewniając się, że nie ma przecieku powietrza. Jeśli u starszego niemowlęcia nie można objąć ust i nosa, ratownik może próbować objąć swoimi ustami albo tylko usta, albo tylko nos niemowlęcia (jeśli tylko nos należy zacisnąć usta, aby powietrze nie wydostawało się na zewnątrz) powoli wdmuchuj powietrze do ust i nosa niemowlęcia przez 1 1,5 sekundy, w ilości wystarczającej do widocznego uniesienia się klatki piersiowej utrzymując odchylenie głowy i uniesienie żuchwy, odsuń swoje usta od ust poszkodowanego i obserwuj, czy podczas wydechu opada klatka piersiowa nabierz powietrza i powtórz opisaną sekwencję 5 razy. Zarówno u niemowlęcia jak i dziecka, jeśli wykonanie skutecznego oddechu natrafia na trudność, drogi oddechowe mogą być niedrożne: otwórz usta dziecka i usuń z nich wszelkie widoczne przeszkody; nigdy nie staraj się usunąć ciała obcego na ślepo upewnij się, że głowa jest prawidłowo odchylona, bródka uniesiona, ale także, że szyja nie jest nadmiernie odgięta jeśli odgięcie głowy i uniesienie brody nie powoduje udrożnienia dróg oddechowych, spróbuj metody wysunięcia żuchwy podejmij do 5 prób w celu uzyskania efektywnych oddechów, jeśli nadal jest to nieskuteczne, rozpocznij uciskanie klatki piersiowej. 1
38 40 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 6. Oceń układ krążenia dziecka. Masz nie więcej niż 10 sekund na: poszukiwanie oznak krążenia zalicza się do tego jakikolwiek ruch, kaszel lub prawidłowy oddech (nie oddechy agonalne, które są rzadkie i nieregularne). Jeśli sprawdzasz tętno, upewnij się, że nie zajmie ci to więcej niż 10 sekund. U dziecka powyżej 1. roku życia badaj tętno na tętnicy szyjnej. U niemowlęcia badaj tętno na tętnicy ramiennej na wewnętrznej stronie ramienia. Puls na tętnicy udowej można badać zarówno u niemowląt, jak i u dzieci. Tętno bada się w pachwinie, miejsce to znajduje się w połowie odległości pomiędzy kolcem biodrowym górnym przednim a spojeniem łonowym. 7A. Jeżeli jesteś pewien, że w ciągu 10 sekund stwierdziłeś obecność oznak krążenia: jeśli to konieczne, kontynuuj oddechy ratownicze aż do powrotu spontanicznego oddechu jeśli dziecko nadal jest nieprzytomne, ułóż je w pozycji bezpiecznej powtarzaj regularnie ocenę stanu ogólnego dziecka. 7B. Jeśli brak oznak krążenia, chyba że jesteś PEWIEN, iż możesz wyczuć wyraźne tętno o częstości większej niż 60/min w ciągu 10 sekund: rozpocznij uciskanie klatki piersiowej połącz uciskanie klatki piersiowej z oddechami ratowniczymi. Uciśnięcia klatki piersiowej U wszystkich dzieci uciskaj dolną połowę mostka. Aby uniknąć uciśnięć nadbrzusza, zlokalizuj wyrostek mieczykowaty poprzez znalezienie miejsca, gdzie łuki żebrowe dolnych żeber łączą się ze sobą. Należy uciskać mostek na szerokość jednego palca powyżej tego punktu. Uciśnięcia powinny być wystarczające, aby obniżyć mostek o około jedną trzecią głębokości klatki piersiowej. Nie należy się obawiać, że uciska się za mocno: Uciskaj szybko i mocno. Należy całkowicie zwolnić ucisk i powtarzać tę czynność z częstością co najmniej 100/min (ale nie przekraczając 120/min). Po 15 uciśnięciach należy odchylić głowę, unieść bródkę i wykonać dwa efektywne oddechy. Uciskanie klatki piersiowej i oddechy ratownicze powinno się kontynuować w stosunku 15 : 2. Najkorzystniejsza metoda uciskania klatki piersiowej różni się nieznacznie u dzieci i u niemowląt. Uciśnięcia klatki piersiowej u niemowląt W przypadku uciśnięć klatki piersiowej prowadzonych przez jednego ratownika, zalecane jest wykonanie tej procedury opuszkami dwóch palców. Jeżeli jest dwóch lub więcej ratowników, należy użyć techniki dwóch kciuków i dłoni obejmujących klatkę piersiową niemowlęcia. Należy umieścić kciuki jeden obok drugiego w dolnej połowie mostka (jak powyżej), ułożone końcami w kierunku głowy niemowlęcia. Pozostałe rozpostarte palce obu dłoni obejmują dolną część klatki piersiowej, a końce palców podtrzymują plecy niemowlęcia. W obydwu metodach należy uciskać dolną część mostka tak, aby obniżyć mostek o około jedną trzecią głębokości klatki piersiowej (około 4 cm). Uciśnięcia klatki piersiowej u dzieci powyżej 1. roku życia Należy umieścić nadgarstek jednej ręki na dolnej połowie mostka (jak powyżej). Konieczne jest uniesienie palców, aby upewnić się, że nie uciska się żeber. Należy ustawić się pionowo nad klatką piersiową poszkodowanego, wyprostować ramiona i uciskać tak, aby obniżyć mostek do około jednej trzeciej głębokości klatki piersiowej (około 5 cm). W przypadku większych dzieci lub drobno zbudowanych ratowników łatwiej będzie to osiągnąć przy użyciu dwóch rąk ze splecionymi palcami. 8. Nie przerywaj resuscytacji do momentu: powrotu oznak życia u dziecka (zacznie się budzić, poruszać, otworzy oczy oraz zacznie prawidłowo oddychać lub będzie miało wyczuwalne tętno z częstością powyżej 60 uderzeń/min) przybycia wykwalifikowanej pomocy, która przejmie działania ratownicze wyczerpania własnych sił. Kiedy wezwać pomoc Dla ratowników ważne jest, aby wezwać pomoc tak szybko, jak to możliwe, kiedy tylko dziecko straci przytomność. Gdy jest więcej niż jeden ratownik, jeden z nich rozpoczyna resuscytację, podczas gdy drugi idzie po pomoc. Gdy jest tylko jeden ratownik, prowadzi on resuscytację przez około minutę, zanim uda się po pomoc. Aby zminimalizować czas trwania przerwy w RKO, możliwe jest przeniesienie niemowlęcia lub małego dziecka do miejsca wzywania pomocy. Jedynym wyjątkiem, kiedy nie należy prowadzić RKO przez minutę, zanim uda się po pomoc, jest przypadek, kiedy dziecko nagle straci przytomność i stało się to w obecności jednego ratownika. W tej sytuacji najbardziej prawdopodobną przyczyną zatrzymania krążenia są zaburzenia rytmu serca i dziecko wymaga defibrylacji. Należy natychmiast szukać pomocy, jeśli nikt inny nie może tego zrobić. Pozycja bezpieczna Nieprzytomne dziecko z drożnymi drogami oddechowymi i spontanicznym, prawidłowym oddechem powinno być ułożone w pozycji bezpiecznej. Pozycja bezpieczna stosowana u pacjentów dorosłych jest również odpowiednia dla dzieci. Niedrożność dróg oddechowych spowodowana ciałem obcym Uderzenia w okolicę międzyłopatkową, uciśnięcia klatki piersiowej i nadbrzusza powodują wzrost ciśnienia w klatce piersiowej i mogą spowodować usunięcie ciała obcego z dróg oddechowych. W połowie przypadków, aby usunąć przyczynę niedrożności, trzeba użyć więcej niż jednej techniki 465. Nie ma danych wskazujących na to, który sposób powinien być użyty jako pierwszy, ani w jakim porządku te techniki powinny być stosowane. Jeśli jedna jest nieskuteczna, trzeba spróbować innych zamiennie aż do momentu usunięcia ciała obcego. Algorytm postępowania w przypadku niedrożności dróg oddechowych spowodowanej ciałem obcym został uproszczony i ujednolicony z algorytmem postępowania u osób dorosłych w Wytycznych 2005; nadal jest zalecane stosowanie się do wspomnianej sekwencji (ryc. 1.12).
39 Podsumowanie Komitetu Wykonawczego ERC 41 Leczenie zadławienia u dzieci 1 Ryc Algorytm postępowania w przypadku niedrożności dróg oddechowych spowodowanej ciałem obcym u dzieci W porównaniu z algorytmem stosowanym u dorosłych najbardziej znacząca różnica polega na zakazie stosowania uciśnięć nadbrzusza u niemowląt. Chociaż te uciśnięcia mogą powodować urazy w każdej grupie pacjentów, ryzyko jest szczególnie wysokie w grupie niemowląt i bardzo małych dzieci. Spowodowane jest to poziomym ułożeniem żeber, w wyniku czego narządy górnego piętra jamy brzusznej są bardziej narażone na urazy. Z tego powodu wytyczne dotyczące postępowania w przypadku obecności ciała obcego w drogach oddechowych są różne u niemowląt i u dzieci. Objawy rozpoznawania ciała obcego w drogach oddechowych zostały przedstawione w tabeli 1.2. Zaawansowane zabiegi u dzieci Zapobieganie zatrzymaniu krążenia U dzieci zatrzymanie krążenia jako wtórne do niewydolności oddychania lub krążenia jest znacznie częstsze niż pierwotne zatrzymanie krążenia spowodowane zaburzeniami rytmu Tak zwane uduszenie lub zatrzymanie oddechu jest również znacznie częstsze u młodych dorosłych (np. uraz, utonięcie, zatrucie) 472,473. Przeżywalność po zatrzymaniu krążenia i oddychania u dzieci jest niska, a sprawą nadrzędną jest identyfikacja objawów zapowiadających rozwój niewydolności krążenia lub oddychania, gdyż wczesna i skuteczna interwencja może uratować życie. Kolejność oceny i wykonywanych interwencji u każdego poważnie chorego lub rannego dziecka powinna przebiegać zgodnie z zasadami ABCDE opisanymi wcześniej dla pacjentów dorosłych. Podsumowując, pediatryczne RRT lub MET mogą zmniejszyć ryzyko wystąpienia zatrzymania oddychania i/lub krążenia u dzieci hospitalizowanych poza oddziałami intensywnego nadzoru pediatrycznego 202, Postępowanie w przypadku niewydolności oddechowej i krążeniowej U dzieci istnieje wiele przyczyn niewydolności oddechowej i krążeniowej i mogą one rozwijać się stopniowo lub wystąpić nagle. Zarówno niewydolność oddechowa jak i krążeniowa mogą być na początku kompensowane, ale zwykle, Tabela 1.2. Objawy niedrożności dróg oddechowych spowodowanych ciałem obcym Główne objawy obecności ciała obcego w drogach oddechowych zdarzenie w obecności świadków kaszel/dławienie nagły początek informacja z wywiadu o połknięciu lub zabawie małym przedmiotem Kaszel nieefektywny niemożność mówienia cisza lub bezgłośny kaszel niemożność oddychania sinica postępująca utrata przytomności Kaszel efektywny płacz lub słowna odpowiedź na pytania głośny kaszel może nabrać powietrza przed kaszlem w pełni reagujący
40 42 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 jeżeli nie podejmie się właściwego leczenia, dochodzi do dekompensacji. Nieleczona zdekompensowana niewydolność oddechowa lub krążenia prowadzi do zatrzymania krążenia. Dlatego celem zaawansowanych zabiegów resuscytacyjnych u dzieci jest podjęcie szybkich i skutecznych działań zapobiegających przejściu niewydolności oddechowej i krążeniowej w pełnoobjawowe zatrzymanie krążenia. Drogi oddechowe i oddychanie Udrożnij drogi oddechowe i zapewnij prawidłową wentylację i natlenienie. Podaj tlen w wysokim przepływie. Zapewnij monitorowanie oddechu pacjenta (w pierwszej kolejności pulsoksymetria/spo 2 ). Osiągnięcie prawidłowej wentylacji i natleniania może wymagać zastosowania przyrządów do dróg oddechowych, wentylacji workiem samorozprężalnym (BMV), zastosowaniem maski krtaniowej (LMA) lub, w celu ostatecznego zabezpieczenia drożności dróg oddechowych, intubacji dotchawiczej i wentylacji dodatnimi ciśnieniami. W skrajnych, rzadkich przypadkach może być wymagane chirurgiczne udrożnienie dróg oddechowych. Postępowanie w szybkiej indukcji i intubacji Dziecko w stanie zatrzymania krążenia i w śpiączce nie wymaga sedacji lub analgezji do wykonania intubacji; w innym przypadku intubacja musi być poprzedzona natlenieniem (spokojna wentylacja za pomocą worka samorozprężalnego z maską jest niekiedy wymagana, aby zapobiec hipoksji), szybką sedacją, analgezją i zastosowaniem środków zwiotczających mięśnie, aby zminimalizować ryzyko wystąpienia powikłań lub niepowodzenia intubacji 479. Osoba wykonująca intubację musi mieć doświadczenie i być zaznajomiona z lekami używanymi w trakcie szybkiej indukcji. Zastosowanie uciśnięcia chrząstki pierścieniowatej może zapobiec lub zmniejszyć ryzyko regurgitacji 480,481, lecz może również prowadzić do zniekształcenia dróg oddechowych i spowodować, że laryngoskopia i intubacja będą trudniejsze do wykonania 482. Uciśnięcia chrząstki pierścieniowatej nie należy stosować, jeśli utrudnia intubację albo natlenianie. Ogólne zalecenia dotyczące doboru średnicy wewnętrznej rurki intubacyjnej (ID Internal Diameter) w zależności od wieku zostały przedstawione w tabeli Są to tylko wskazówki; zawsze należy mieć dostępne rurki intubacyjne o jeden rozmiar większy i mniejszy. Rozmiar rurki intubacyjnej określa się również na podstawie długości ciała dziecka wyznaczanego przy użyciu taśmy resuscytacyjnej 489. Rurki intubacyjne bez mankietu uszczelniającego tradycyjnie stosuje się u dzieci do 8. roku życia, jednak rurki z mankietem mogą być przydatne w niektórych okolicznościach, np.: gdy zmniejszona jest podatność płuc, są wysokie opory w drogach oddechowych lub z powodu dużego przecieku powietrza wokół rurki na poziomie głośni 483,490,491. Zastosowanie rurek z mankietem sprawia również, że zwiększa się prawdopodobieństwo wybrania właściwego rozmiaru za pierwszym razem 483,484,492. Zbyt wysokie ciśnienie w mankiecie uszczelniającym może prowadzić do spowodowanego niedokrwieniem uszkodzenia tkanek otaczających krtań i w efekcie doprowadzić do zwężenia na tym poziomie. Należy utrzymywać ciśnienie w mankiecie poniżej 25 cm H 2 O i stale je kontrolować 493. Przemieszczenie, złe umiejscowienie lub zatkanie rurki często występuje u zaintubowanych dzieci i wiąże się ze zwiększonym ryzykiem zgonu 281,494. Żadna z izolowanych metod nie jest w 100% niezawodna w rozróżnieniu intubacji do przełyku od intubacji dotchawiczej Ocena prawidłowego położenia rurki intubacyjnej opiera się na: obserwacji w laryngoskopii bezpośredniej przejścia rurki przez struny głosowe; wykryciu końcowo-wydechowego dwutlenku węgla u dziecka z rytmem perfuzyjnym (może być to również obserwowane przy skutecznej RKO, lecz nie jest do końca wiarygodne); obserwacji symetrycznych ruchów klatki piersiowej podczas wentylacji dodatnimi ciśnieniami; obserwacji pojawienia się pary wodnej w rurce intubacyjnej podczas wydechowej fazy wentylacji; braku rozdęcia żołądka; symetrycznie słyszalnych szmerach oddechowych przy obustronnym osłuchiwaniu w liniach pachowych i szczytach płuc; braku odgłosów obecności powietrza przy osłuchiwaniu żołądka; poprawie lub stabilizacji saturacji na oczekiwanym poziomie (uwaga na opóźnienie sygnału!); normalizacji częstości akcji serca do wartości należnej dla wieku (lub pozostawania w granicach normy) (uwaga na opóźnienie sygnału!). Jeżeli u dziecka doszło do zatrzymania krążenia i nie można wykryć końcowo-wydechowego CO 2 pomimo prawidłowo prowadzonych uciśnięć klatki piersiowej oraz jeżeli są jakiekolwiek wątpliwości, należy potwierdzić położenie rurki intubacyjnej w laryngoskopii bezpośredniej. Oddychanie W początkowej fazie resuscytacji należy stosować najwyższe stężenia tlenu (tzn. 100%). Po przywróceniu krążenia należy zapewnić wystarczającą ilość tlenu pozwalającą utrzymać saturację krwi tętniczej (SaO 2 ) w zakresie wartości 94 98% 498,499. Tabela 1.3. Ogólne zalecenia dla stosowania rurek z lub bez mankietu uszczelniającego (średnica wewnętrzna w mm) Bez mankietu Z mankietem Noworodki wcześniaki Czas trwania ciąży [tygodnie]/10 Nie stosuje się Noworodki urodzone o czasie 3.5 Zazwyczaj się nie stosuje Niemowlęta Dzieci r.ż Dzieci >2. r.ż. Wiek/4 + 4 Wiek/
41 Podsumowanie Komitetu Wykonawczego ERC 43 Osoby z wykształceniem medycznym zwykle nadmiernie wentylują podczas RKO, co może być szkodliwe. Hyperwetylacja powoduje wzrost ciśnienia w klatce piersiowej, spadek przepływu mózgowego i wieńcowego oraz gorszą przeżywalność, co wynika z badań na zwierzętach i z udziałem dorosłych 224,225,286, Choć prawidłowa wentylacja jest celem, który należy osiągnąć podczas resuscytacji, trudne jest określenie dokładnej objętości minutowej, którą należy dostarczyć pacjentowi. Prostą wskazówką może być fakt, że idealna objętość oddechowa powinna spowodować niewielkie uniesienie się klatki piersiowej. Gdy tylko drogi oddechowe zostaną zabezpieczone poprzez intubację, można kontynuować wentylację dodatnimi ciśnieniami o częstości oddechów/min bez przerywania uciskania klatki piersiowej. Po przywróceniu krążenia lub u dziecka z rytmem perfuzyjnym należy wentylować z częstością oddechów/min w celu utrzymania ciśnienia parcjalnego dwutlenku węgla (PaCO 2 ) w granicach normy. Monitorowanie końcowo-wydechowego CO 2 (ETCO 2 ) za pomocą detektora zmieniającego kolor lub kapnometru pozwala potwierdzić prawidłowe położenie rurki intubacyjnej u dzieci ważących powyżej 2 kg i może być przydatne zarówno w warunkach przed- jak i wewnątrzszpitalnych oraz podczas każdego transportu pacjenta pediatrycznego Zmiana koloru lub obecność zapisu fali na ekranie kapnografu po wykonaniu więcej niż czterech oddechów ratowniczych wskazuje na to, że rurka znajduje się w drzewie oskrzelowym zarówno w przypadku rytmu z zachowaną perfuzją, jak i w zatrzymaniu krążenia. Kapnografia nie rozpoznaje intubacji oskrzela. Brak lub niski poziom końcowo-wydechowego CO 2 podczas zatrzymania krążenia może nie wynikać z przemieszczenia się rurki intubacyjnej, ale odzwierciedlać całkowity brak lub niski przepływ krwi w krążeniu płucnym 235, Kapnografia może również dostarczyć informacji na temat efektywności uciśnięć klatki piersiowej oraz być wczesnym wskaźnikiem powrotu spontanicznego krążenia 511,512. Należy podjąć starania, aby poprawić jakość uciśnięć klatki piersiowej jeżeli ETCO 2 pozostaje poniżej 15 mm Hg (2 kpa). Dotychczas brak jest dowodów na wartość progową ETCO 2, która byłaby wskaźnikiem pozwalającym na przerwanie czynności resuscytacyjnych. Użycie elastycznej gumowej gruszki lub aspiracja za pomocą specjalnej strzykawki (detektor przełykowy Oesophageal Detector Device, ODD) może być użyteczną metodą potwierdzającą wtórnie prawidłowe położenie rurki intubacyjnej u dzieci z rytmem perfuzyjnym 513,514. Nie ma żadnych badań naukowych na temat zastosowania ODD u dzieci w zatrzymaniu krążenia. Kliniczna ocena poziomu tlenu w krwi tętniczej (SaO 2 ) jest niepewna, dlatego należy stale monitorować saturację obwodową u dziecka za pomocą pulsoksymetrii (SpO 2 ). Krążenie Zapewnij monitorowanie pracy serca [jako pierwszy pulsoksymetr (SpO 2 ), EKG i nieinwazyjny pomiar ciśnienia tętniczego krwi (NIBP)]. Zapewnij dostęp donaczyniowy. Można go uzyskać poprzez założenie kaniuli do krążenia obwodowego (iv) lub jamy szpikowej (io).jeśli wcześniej został zabezpieczony dostęp centralny, należy go używać. Podaj bolus płynów (20 ml/kg) i/lub leki (np.: inotropowe, wazopresyjne, antyarytmiczne), jeśli są wymagane. Izotoniczne krystaloidy są zalecane we wstępnej resuscytacji płynowej u dzieci niezależnie od typu wstrząsu włącznie ze wstrząsem septycznym Stale badaj i wykonuj ponowną ocenę stanu dziecka, rozpoczynając za każdym razem od sprawdzenia drożności dróg oddechowych, zanim przejdzie się do oceny oddychania i krążenia. Podczas leczenia zastosowanie kapnografii, inwazyjnego monitorowania ciśnienia tętniczego krwi, gazometrii, pomiaru rzutu serca, echokardiografii oraz saturacji krwi żylnej (ScvO 2 ) może pomóc w podejmowaniu decyzji co do dalszego postępowania i leczenia niewydolności oddechowej i/lub krążeniowej. Dostęp donaczyniowy Dostęp dożylny może być trudny do uzyskania podczas resuscytacji niemowlęcia lub dziecka. Jeśli próby uzyskania dostępu dożylnego trwają powyżej 1 minuty, należy założyć dostęp doszpikowy 519,520. Dostępy doszpikowy lub dożylny są zdecydowanie preferowaną drogą podawania leków w stosunku do dostępu dotchawiczego 521. Adrenalina Zalecane dawki adrenaliny u dzieci, dla dawki pierwszej i kolejnych zarówno dożylne, jak i doszpikowe, to 10 μg/kg. Maksymalna pojedyncza dawka wynosi 1 mg. Jeśli są wskazania, kolejne dawki adrenaliny należy podawać co 3 5 minut. Podawanie adrenaliny do rurki intubacyjnej nie jest obecnie zalecane , lecz jeśli używa się tej drogi, dawka adrenaliny powinna być 10-krotnie większa (100 μg/kg). Zaawansowane zabiegi resuscytacyjne w zatrzymaniu krążenia 1. Gdy dziecko nie reaguje i nie ma oznak krążenia (nie oddycha, nie kaszle lub nie porusza się), natychmiast rozpocznij RKO. 2. Zapewnij wentylację workiem samorozprężalnym z maską twarzową i użyciem 100% tlenu. 3. Podłącz monitor. Poproś o defibrylator manualny lub AED, aby jak najszybciej rozpoznać i leczyć rytm defibrylacyjny (do defibrylacji) (ryc. 1.13). A B C Rozpocznij i kontynuuj podstawowe zabiegi resuscytacyjne. Natleniaj i wentyluj pacjenta za pomocą worka samorozprężalnego i maski. Zapewnij wentylację dodatnimi ciśnieniami z wysokim stężeniem tlenu. Wykonaj 5 efektywnych wdechów, a następnie rozpocznij uciskanie klatki piersiowej i wentylację dodatnimi ciśnieniami w stosunku 15 : 2. Unikaj zmęczenia ratownika poprzez częstą zmianę osoby uciskającej klatkę piersiową. Zapewnij monitorowanie rytmu serca. Oceń rytm serca i oznaki życia. (± Sprawdź tętno na dużych tętnicach, ale nie dłużej niż 10 s). 1
42 44 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Zaawansowane zabiegi resuscytacyjne u dzieci Nie reaguje? Brak oddechu lub tylko pojedyncze westchnięcia RKO (5 wstępnych oddechów ratowniczych, potem 15 : 2) Minimalizuj przerwy Wezwij zespół resuscytacyjny (Jeśli pojedynczy ratownik, najpierw 1 min RKO) Oceń rytm (VF/ VT bez tętna) (PEA/asystolia) 1 defibrylacja 4 J/kg Powrót spontanicznego krążenia Natychmiast podejmij RKO przez 2 min Minimalizuj przerwy NATYCHMIASTOWA OPIEKA PORESUSCYTACYJNA Zastosuj schemat ABCDE Kontroluj wentylację i oksygenację Badania Lecz przyczynę zatrzymania krążenia Kontrola temperatury Terapeutyczna hipotermia? Natychmiast podejmij RKO przez 2 min Minimalizuj przerwy PODCZAS RKO Zapewnij wysokiej jakości uciśnięcia klatki piersiowej: częstość, głębokość, właściwe odkształcenie Zaplanuj działanie, zanim przerwiesz RKO Podaj tlen Dostęp donaczyniowy (dożylny, doszpikowy) Podaj adrenalinę co 3 5 min Rozważ zaawansowane drogi oddechowe i kapnografię Nie przerywaj uciskania klatki piersiowej po zabezpieczeniu dróg oddechowych Lecz odwracalne przyczyny ODWRACALNE PRZYCZYNY Hipoksja Hipowolemia Hipo-/hiperkaliemia/zaburzenia metaboliczne Hipotermia Odma prężna Zatrucia Tamponada osierdzia Zaburzenia zatorowo-zakrzepowe Ryc Algorytm zaawansowanych zabiegów resuscytacyjnych u dzieci Rytmy nie do defibrylacji asystolia, aktywność elektryczna bez tętna (PEA) Podaj adrenalinę dożylnie lub doszpikowo w dawce 10 μg/kg i powtarzaj tą dawkę co 3 5 minut. Rozpoznaj i lecz odwracalne przyczyny zatrzymania krążenia (4 H i 4 T). Rytmy do defibrylacji VF/VT bez tętna Natychmiast wykonaj defibrylację (4 J/kg): Naładuj defibrylator, podczas gdy drugi ratownik prowadzi uciśnięcia klatki piersiowej. Gdy defibrylator jest naładowany, przerwij uciskanie klatki piersiowej i upewnij się, że nikt nie dotyka pacjenta. Minimalizuj czas pomiędzy przerwaniem uciśnięć klatki piersiowej a dostarczeniem wyładowania nawet opóźnienie 5 10 sekund zmniejsza szansę na skuteczną defibrylację 71,110. Wykonaj jedną defibrylację.
43 Podsumowanie Komitetu Wykonawczego ERC 45 Tak szybko, jak to możliwe, powróć do RKO bez ponownej oceny rytmu. Po 2 minutach przez krótki okres czasu sprawdź zapis rytmu na monitorze. Jeśli nadal występuje VF/VT, wykonaj drugą defibrylację (4 J/kg). Natychmiast rozpocznij RKO przez 2 minuty bez ponownej oceny rytmu. Przerwij krótko na ocenę rytmu; jeśli nadal występuje VF/VT, wykonaj trzecią defibrylację energią 4 J/kg. Podaj adrenalinę w dawce 10 μg/kg i amiodaron w dawce 5 mg/kg po wykonaniu trzeciej defibrylacji, równocześnie z rozpoczęciem RKO. Podawaj adrenalinę co drugi cykl (tzn. co 3 5 minut podczas RKO). Podaj drugą dawkę amiodaronu 5 mg/kg, jeśli nadal występuje VF/VT po piątej defibrylacji 526. Jeśli u dziecka nadal występuje VF/VT, kontynuuj wykonywanie defibrylacji wartością 4 J/kg na zmianę z 2 minutami RKO. Jeśli widoczne są oznaki życia, oceń rytm na monitorze w celu poszukiwania zorganizowanej aktywności elektrycznej serca i jeśli jest obecna, sprawdź oznaki krążenia i tętno na dużych tętnicach oraz oceń wydolność hemodynamiczną dziecka (ciśnienie tętnicze krwi, tętno na naczyniach obwodowych, nawrót kapilarny). Rozpoznaj i lecz odwracalne przyczyny zatrzymania krążenia (4 H, 4 T), pamiętając, że pierwsze dwa H (hipoksja i hipowolemia) są najbardziej powszechną przyczyną zatrzymania krążenia u dzieci w stanie zagrożenia życia lub u dzieci z urazem. Jeśli defibrylacja była skuteczna, ale VF/VT powróciło, podejmij ponownie RKO, podaj ponownie amiodaron w dawce, która poprzednio była skuteczna. Rozpocznij wlew ciągły amiodaronu. Echokardiografia może być użyteczna do identyfikacji potencjalnie odwracalnych przyczyń zatrzymania krążenia u dzieci. Można szybko uwidocznić aktywność mięśnia sercowego 527, jak również rozpoznać tamponadę worka osierdziowego 268. Musi być jednak dostępny właściwie przeszkolony sonografista, należy również zachować równowagę pomiędzy wykonywaniem echokardiografii a jakością uciskania klatki piersiowej. Zaburzenia rytmu Zaburzenia rytmu u niestabilnych pacjentów Należy zbadać oznaki życia i tętno na dużych tętnicach u każdego dziecka z zaburzeniami rytmu. Jeżeli brak jest oznak życia, należy rozpocząć leczenie zatrzymania krążenia. Jeśli zaś obecne są oznaki życia i tętno na dużych tętnicach, konieczna jest ocena stanu hemodynamicznego pacjenta. Gdy tylko stwierdzi się upośledzenie krążenia, należy postępować następująco: 1. Udrożnij drogi oddechowe. 2. Podaj tlen i w razie konieczności wspomagaj oddychanie. 3. Podłącz monitor EKG lub defibrylator i oceń zapis rytmu serca. 4. Oceń, czy rytm jest za wolny, czy za szybki w stosunku do wieku dziecka. 5. Oceń, czy rytm jest miarowy, czy niemiarowy. 6. Oceń szerokość zespołów QRS (wąskie: <0,08 s; poszerzone: >0,08 s). 7. Leczenie zależeć będzie od stanu hemodynamicznego dziecka. Bradykardia jest zwykle spowodowana niedotlenieniem, kwasicą i/lub ciężką hipotensją; w rezultacie może przejść w zatrzymanie krążenia. Należy podać 100-procentowy tlen i, jeżeli to konieczne, wentylować dodatnimi ciśnieniami każde dziecko z objawami bradykardii i niewydolnością krążenia. Jeżeli u dziecka z objawami złej perfuzji częstość rytmu serca wynosi <60/min i nie przyspiesza pomimo wentylacji oraz tlenoterapii, należy rozpocząć uciskanie klatki piersiowej i podać adrenalinę. Jeżeli bradykardia jest spowodowana pobudzeniem nerwu błędnego (jak np. podczas wprowadzania sondy do żołądka), może okazać się skuteczne podanie atropiny. Stymulacja mięśnia sercowego (zarówno przezżylna, jak i przezskórna) jest na ogół nieskuteczna w trakcie resuscytacji. Jej zastosowanie można rozważyć w przypadkach bloku AV lub dysfunkcji węzła zatokowego nie reagującej na tlenoterapię, wentylację, uciskanie klatki piersiowej i inne leki. Stymulacja jest nieskuteczna w asystolii oraz zaburzeniach rytmu spowodowanych niedotlenieniem i niedokrwieniem 528. Jeżeli rytm widoczny na monitorze jest prawdopodobnie częstoskurczem nadkomorowym (SVT) u hemodynamicznie stabilnych dzieci, można wykonać stymulację nerwu błędnego (próba Valsalvy lub odruch na nurkowanie). Manewry te można także wykonać u niestabilnych pacjentów pod warunkiem, że nie opóźniają farmakologicznej (np. adenozyna) lub elektrycznej kardiowersji 529. Jeżeli stan dziecka jest niestabilny z obniżonym poziomem świadomości, należy natychmiast wykonać kardiowersję. Kardiowersja elektryczna (zsynchronizowana z załamkiem R) jest także wskazana u dziecka, u którego brak jest dostępu donaczyniowego lub u którego adenozyna była nieskuteczna w przywróceniu rytmu zatokowego. Pierwsza dawka energii dla kardiowersji w przypadku SVT wynosi 0,5 1 J/kg, a druga 2 J/kg. U dzieci częstoskurcz z szerokimi zespołami QRS występuje rzadko i częściej jest pochodzenia nadkomorowego niż komorowego 530. Jednakże u hemodynamicznie niestabilnych dzieci taki częstoskurcz musi być traktowany jak VT, dopóki nie udowodni się, że jest inaczej. Kardiowersja jest leczeniem z wyboru niestabilnych pacjentów, u których występuje VT z zachowanym tętnem. Należy rozważyć zastosowanie leków antyarytmicznych, jeżeli 2. kardiowersja jest nieskuteczna lub VT nawraca. Zaburzenia rytmu u stabilnych pacjentów Należy skontaktować się ze specjalistą podczas zabezpieczania drożności dróg oddechowych, oddychania i krążenia, a przed rozpoczęciem leczenia. W zależności od wywiadu, stanu klinicznego oraz zapisu EKG dziecko ze stabilnym częstoskurczem z szerokimi zespołami QRS może być leczone jak SVT, poprzez wykonanie stymulacji nerwu błędnego i podanie adenozyny. W sytuacji gdy okaże się to nieskuteczne lub rozpoznanie VT będzie potwierdzone w zapisie EKG, jako opcję leczenia można rozważyć podanie amiodaronu. 1
44 46 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Sytuacje szczególne Dysfunkcje kanałów jonowych Jeśli u dziecka lub młodego dorosłego wystąpi z nieznanych przyczyn nagłe zatrzymanie krążenia, należy uzyskać pełną informację dotyczącą przeszłości chorobowej dziecka, wywiad rodzinny (włączając epizody utraty przytomności, drgawek, niewyjaśnionych wypadków/utonięć czy nagłej śmierci), a także obejrzeć wszystkie wcześniejsze zapisy EKG, jeśli są one dostępne. Wszystkie niemowlęta, dzieci i młodzi dorośli, którzy zmarli nagłą, niespodziewaną śmiercią, powinni w miarę możliwości zostać poddani pełnej sekcji zwłok, przeprowadzonej przez patomorfologa doświadczonego w patologii układu sercowo-naczyniowego Należy rozważyć zabezpieczenie i genetyczną analizę tkanek w celu wykrycia dysfunkcji kanałów jonowych. Rodziny tych pacjentów, u których podczas autopsji nie udało się określić przyczyny śmierci, należy skierować do ośrodków specjalizujących się w rozpoznawaniu i leczeniu zaburzeń rytmu serca. Pojedyncza komora serca po pierwszym etapie leczenia Częstość zatrzymań krążenia u niemowląt z pojedynczą komorą serca po pierwszym etapie leczenia wynosi około 20%, a 33% z nich przeżywa taki epizod do momentu wypisu ze szpitala 541. Nie ma dowodów wskazujących, że protokoły resuscytacji inne niż standardowe powinny być stosowane. Rozpoznanie stanu zagrażającego zatrzymaniem krążenia jest trudne, ale może być ułatwione poprzez monitorowanie wysycenia krwi tlenem w żyle głównej górnej (ScvO 2 ) lub spektroskopię (przy użyciu pasma bliskiej podczerwieni) krążenia mózgowego oraz trzewnego Leczenie wysokiego naczyniowego oporu systemowego antagonistami receptorów alfa-adrenergicznych może poprawić systemowe dostarczanie tlenu do tkanek 545, ograniczyć częstość epizodów sercowo-naczyniowych 546 oraz poprawić przeżywalność 547. Pojedyncza komora serca po operacji typu Fontan U dzieci będących w stanie zagrażającym zatrzymaniem krążenia po operacji kardiochirurgicznej typu Fontan lub hemi-fontan może przynieść korzyści: zwiększenie oksygenacji oraz zwiększenie rzutu serca, uzyskane za pomocą wentylacji ujemnymi ciśnieniami 548,549. Pozaustrojowe natlenianie (ECMO) może być użyteczne u dzieci z niewydolnym krążeniem typu Fontan, nie ma natomiast rekomendacji za lub przeciw stosowaniu ECMO u pacjentów z krążeniem typu hemi-fontan jako postępowanie ratunkowe podczas resuscytacji 550. Nadciśnienie płucne U dzieci z nadciśnieniem płucnym istnieje zwiększone ryzyko zatrzymania krążenia 551,552. U tych pacjentów należy przestrzegać standardowego algorytmu resuscytacji, kładąc szczególny nacisk na utrzymanie wysokiego FiO 2 oraz zasadowicy/hiperwentylacji, gdyż mogą one być równie skuteczne, jak zastosowanie tlenku azotu w celu redukcji oporu w krążeniu płucnym 553. Resuscytacja ma większe szanse powodzenia u pacjentów z odwracalną przyczyną zatrzymania krążenia, jeśli są oni leczeni epoprostenolem stosowanym dożylnie lub tlenkiem azotu stosowanym wziewnie 554. Jeśli stosowane rutynowo leki obniżające ciśnienie płucne zostały odstawione, należy je włączyć z powrotem i rozważyć podanie epoprostenolu w aerozolu lub inhalację tlenkiem azotu 555. Zwiększyć przeżywalność może także zastosowanie urządzeń wspomagających funkcję skurczową prawej komory Opieka poresuscytacyjna Zasady opieki poresuscytacyjnej oraz leczenia zespołu poresuscytacyjnego u dzieci są podobne do tych u dorosłych. Kontrola temperatury Hipotermia jest częstym zjawiskiem po resuscytacji krążeniowo-oddechowej u dzieci 350. Obniżenie temperatury głębokiej (32 34 C) może przynieść korzyści, podczas gdy gorączka może wpływać niekorzystnie na uszkodzony mózg. Zastosowanie łagodnej hipotermii jest dopusz - czal ną i bezpieczną procedurą u dorosłych 355,356 i noworodków Natomiast, choć może to poprawiać wyniki neurologiczne u dzieci, dane pochodzące z badań klinicznych ani nie wspierają, ani nie odradzają zastosowania hipotermii terapeutycznej w przypadku zatrzymania krążenia w tej grupie wiekowej 566. W przypadku dzieci, u których przywrócono spontaniczne krążenie, a pozostających w śpiączce, korzystne może być obniżenie temperatury głębokiej ciała do C na okres co najmniej 24 godzin. Dzieci, u których resuscytacja była skuteczna, ale nadal pozostają w hipotermii, nie należy ogrzewać, chyba że temperatura głęboka jest poniżej 32 C. Po okresie łagodnej hipotermii dziecko należy ogrzewać powoli, około 0,25 0,5 C na godzinę. Powyższe wytyczne oparte są na badaniach klinicznych dotyczących zastosowania hipotermii terapeutycznej u noworodków i dorosłych. W momencie opracowywania tych zaleceń trwają prospektywne, wieloośrodkowe badania nad użyciem hipotermii terapeutycznej po poza- i wewnątrzszpitalnym zatrzymaniu krążenia u dzieci ( NCT i NCT ). Gorączka często pojawia się po resuscytacji krążeniowo-oddechowej i jej wystąpienie wiąże się ze złym rokowaniem neurologicznym 346,348,349, a ryzyko takich powikłań rośnie wraz ze wzrostem temperatury o każdy stopień powyżej 37 C 349. Istnieje ograniczona liczba badań eksperymentalnych sugerujących, że zastosowanie leków przeciwgorączkowych i/lub fizyczne schładzanie zmniejsza uszkodzenie komórek nerwowych 567,568. Ponieważ leki przeciwgorączkowe są uznawane za bezpieczne, należy je stosować celem agresywnego leczenia gorączki. Kontrola glikemii U dorosłych i dzieci w stanie zagrożenia życia zarówno hiper-, jak i hipoglikemia mogą wpływać niekorzystnie na wynik leczenia i dlatego należy ich unikać, ale ścisła kontrola poziomu glukozy również może być szkodliwa. Pomimo że nie ma wystarczającej ilości dowodów na poparcie któregokolwiek sposobu postępowania dotyczącego kontroli glikemii, u dzieci po przywróceniu spontanicznego krążenia 3,569,570 zaleca się monitorowanie poziomu glukozy we krwi oraz unikanie hipoglikemii w takim samym stopniu jak przedłużającej się hiperglikemii.
45 Podsumowanie Komitetu Wykonawczego ERC 47 DO ROZWAŻENIA NA KAŻDYM ETAPIE: CZY POTRZEBUJESZ POMOCY? Zabiegi resuscytacyjne u noworodka Osusz Usuń mokre ręczniki i okryj Włącz zegar lub rejestruj czas Oceń (napięcie), oddychanie, czynność serca Jeśli westchnięcia (gasping) lub brak oddychania, Udrożnij drogi oddechowe Wykonaj 5 oddechów upowietrznij płuca Rozważ monitorowanie SpO 2 Oceń ponownie Jeśli czynność serca nie wzrasta, poszukuj ruchów klatki piersiowej Jeśli klatka piersiowa nie unosi się, Ponownie sprawdź ułożenie głowy Rozważ udrożnienie dróg oddechowych przez 2 osoby lub inne sposoby zapewnienia drożności dróg oddechowych Spróbuj ponownie upowietrznić płuca Rozważ monitorowanie SpO 2 Oceń odpowiedź Jeśli czynność serca nie wzrasta, poszukuj ruchów klatki piersiowej Kiedy klatka piersiowa unosi się, Jeśli czynność serca niebadalna lub wolna (<60), rozpocznij uciskanie klatki piersiowej 3 uciśnięcia na 1 oddech Oceniaj czynność serca co 30 sek Jeśli czynność serca niebadalna lub wolna (<60), Rozważ dostęp dożylny i leki Poród 30 sek 60 sek Zadowalająca* przed-przewodowa SpO 2 2 min: 60% 3 min: 70% 4 min: 80% 5 min: 85% 10 min: 90% * / /peds Ryc Algorytm NLS Resuscytacja noworodków bezpośrednio po urodzeniu Przygotowanie Relatywnie mała grupa noworodków wymaga jakichkolwiek zabiegów resuscytacyjnych w momencie narodzin. Wśród tych, które rzeczywiście ich potrzebują, znakomita większość będzie wymagać tylko pomocy w upowietrznieniu płuc. Tylko niewielka grupa, oprócz upowietrznienia płuc, będzie wymagać dodatkowo krótkiego okresu uciskania klatki piersiowej. Spośród dzieci urodzonych w Szwecji w ciągu jednego roku tylko 10 na 1000 (1%) o masie ciała równej lub wyższej niż 2,5 kg wymagało resuscytacji w trakcie porodu 571. Wśród tych dzieci 8 na 1000 odpowiedziało pozytywnie na wentylację przy użyciu maski, a tylko 2 na 1000 wymagało intubacji. W tym samym badaniu starano się określić częstość występowania niespodziewanej resuscytacji po urodzeniu i stwierdzono, że w przypadku dzieci z grupy niskiego ryzyka, tj. urodzonych po 32. tygodniu ciąży, po przebiegającym prawidłowo porodzie, tylko 2 na 1000 (0,2%) wymagało resuscytacji bezpośrednio po urodzeniu. Wśród nich 90% odpowiedziało pozytywnie na
46 48 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 wentylację przy użyciu maski, a tylko pozostałe 10% wymagało intubacji w związku z brakiem odpowiedzi na tę procedurę (ryc. 1.14). Resuscytacja lub specjalistyczna pomoc może być bardziej potrzebna noworodkom, u których stwierdzono znaczące zaburzenia dobrostanu płodu w trakcie porodu, a także tym urodzonym przed 35. tygodniem ciąży, po porodzie pośladkowym lub mnogim. Pomimo że często w trakcie porodu istnieje możliwość przewidzenia potrzeby resuscytacji lub stabilizacji stanu dziecka, nie zawsze jest to wykonywane. Dlatego personel przeszkolony w resuscytacji noworodka powinien być łatwo osiągalny przy każdym porodzie i, jeśli pojawi się potrzeba interwencji, opieka nad dzieckiem należy do jego obowiązków. W optymalnych warunkach osoba doświadczona w intubacji noworodka powinna towarzyszyć przy porodzie o wysokim prawdopodobieństwie konieczności resuscytacji noworodka. Powinny być opracowane lokalne wytyczne, oparte na aktualnej praktyce i audycie klinicznym, precyzujące, kto powinien sprawować tego rodzaju opiekę okołoporodową. Kluczowe jest, aby w instytucjach, gdzie odbywają się porody, powstały programy edukacyjne dotyczące standardów i umiejętności wymaganych do resuscytacji noworodków. Porody planowane w domu Zalecenia co do osób, które powinny asystować przy porodzie zaplanowanym w domu, w różnych krajach są różne, ale podjęta przez lekarza i położną decyzja o przeprowadzeniu porodu w domu nie powinna wpływać na standardy wstępnej resuscytacji po porodzie. Na pewno resuscytacja noworodka w domu wiąże się z ograniczeniami, które wynikają z braku dostępności zaawansowanej pomocy medycznej i musi to być jasno wytłumaczone matce jeszcze w okresie przygotowań do porodu w domu. Najlepiej byłoby, aby w każdym porodzie domowym uczestniczyły dwie przeszkolone osoby, z których co najmniej jedna posiada umiejętności i doświadczenie w prowadzeniu wentylacji workiem samorozprężalnym z maską oraz uciskaniu klatki piersiowej noworodków. Sprzęt i środowisko W odróżnieniu od resuscytacji krążeniowo-oddechowej u osób dorosłych resuscytacja noworodków po porodzie jest często zdarzeniem przewidywalnym. Dlatego możliwe jest przygotowanie odpowiednich warunków i sprzętu przed urodzeniem się dziecka. Resuscytację najlepiej prowadzić w ciepłym, dobrze oświetlonym, nienarażonym na przeciągi miejscu, z płaską powierzchnią przeznaczoną do reanimacji umieszczoną pod promiennikiem ciepła oraz z natychmiastowo dostępnym sprzętem niezbędnym do resuscytacji. Całe wyposażenie musi być regularnie sprawdzane. Jeżeli do porodu dojdzie w miejscu do tego nieprzeznaczonym, minimalny zestaw sprzętu obejmuje przyrząd do bezpiecznego upowietrznienia płuc we właściwym dla noworodka rozmiarze, ciepłe i suche ręczniki i koce, sterylne narzędzie do przecięcia pępowiny oraz rękawiczki dla całego zespołu. Pomocne może być także posiadanie urządzenia do odsysania wraz z cewnikiem we właściwym rozmiarze oraz szpatułki (lub laryngoskopu) do oceny jamy ustnej i gardła. Niespodziewane porody poza szpitalem często wymagają pomocy pogotowia, które powinno być przygotowane na taką ewentualność. Kontrola temperatury Nagie, mokre noworodki nie mają możliwości utrzymania prawidłowej temperatury ciała w pomieszczeniu, w którym temperatura jest komfortowa dla osób dorosłych. Noworodki urodzone w zamartwicy są szczególnie narażone na utratę temperatury 572. Narażenie noworodka na stres związany z niską temperaturą otoczenia powoduje spadek ciśnienia parcjalnego tlenu w krwi tętniczej 573 i nasila kwasicę metaboliczną 574. Należy zapobiegać utracie ciepła: Chronić noworodka przed przeciągiem. Utrzymywać ciepło w sali porodowej. Dla noworodków urodzonych przed 28. tygodniem ciąży temperatura pomieszczenia powinna wynosić 26 C 575, 576. Osuszyć nowo narodzone dziecko tuż po porodzie. Należy okryć głowę i ciało dziecka, z wyjątkiem twarzy, ciepłym ręcznikiem w celu zapobieżenia dalszej utracie ciepła. Alternatywnie można położyć nagie dziecko bezpośrednio na skórze matki i przykryć oboje ręcznikiem. Jeżeli dziecko wymaga resuscytacji, należy je położyć na ciepłej powierzchni pod wcześniej włączonym promiennikiem ciepła. W przypadku skrajnego wcześniactwa (szczególnie przed 28. tygodniem ciąży) osuszenie i zawinięcie mogą być niewystarczające. Bardziej efektywną metodą utrzymania właściwej temperatury u takich noworodków jest owinięcie głowy i ciała dziecka (z wyjątkiem twarzy) plastikową folią, bez wcześniejszego osuszania, a następnie umieszczenie tak okrytego noworodka pod promiennikiem ciepła. Ocena wstępna Skala Apgar została zaproponowana jako prosta, powszechnie stosowana, jasna klasyfikacja lub narzędzie oceny noworodków, stosowana w celu stworzenia podstawy dla dyskusji i porównania rezultatów praktyk położniczych, sposobów uśmierzania bólu porodowego u matki oraz wyniku resuscytacji 577. Nie została ona opracowana w celu identyfikacji noworodków wymagających resuscytacji 578. Jednak pewne jej elementy składowe, a dokładniej częstość oddechów, częstość pracy serca oraz napięcie mięśniowe, jeśli ocenione szybko, mogą pomóc w identyfikacji noworodków potrzebujących resuscytacji 577. Co więcej, powtarzana ocena, zwłaszcza czynności serca i w mniejszym stopniu oddechu, może wskazywać, czy dziecko reaguje na leczenie lub czy dalsze działania są konieczne. Oddychanie Należy sprawdzić, czy dziecko oddycha. Jeżeli tak, należy ocenić częstość i głębokość oraz symetrię oddechów wraz z ewentualną obecnością nieprawidłowych objawów, takich jak gasping (wolne, nieregularne oddechy) lub postękiwanie. Częstość pracy serca Najlepszym sposobem oceny częstości pracy serca jest osłuchiwanie okolicy koniuszka za pomocą stetoskopu. Bada-
47 Podsumowanie Komitetu Wykonawczego ERC 49 nie tętna u podstawy pępowiny jest często skuteczne, ale może być mylące. Tętnienie pępowiny jest wiarygodnym objawem tylko wówczas, gdy jego częstość jest wyższa niż 100 uderzeń na minutę 579. U dzieci wymagających resuscytacji i/lub ciągłego wspomagania wentylacji dokładna ocena częstości pracy serca może być uzyskana za pomocą pulsoksymetru 580. Kolor skóry Kolor skóry jest niewiarygodnym sposobem oceny oksygenacji 581. Powinna ona być oceniana, jeśli jest to możliwe, za pomocą pulsoksymetrii. Zdrowy noworodek rodzi się siny, ale w ciągu 30 sekund od rozpoczęcia efektywnego oddychania kolor skóry zmienia się na różowy. Sinica obwodowa jest częsta i sama w sobie nie jest objawem niedotlenienia. Utrzymująca się bladość skóry pomimo wentylacji może wskazywać na znaczną kwasicę lub rzadziej hipowolemię. Pomimo że kolor skóry jest słabym wyznacznikiem natlenienia, nie może zostać zignorowany: jeśli u dziecka utrzymuje się sinica, należy ocenić saturację za pomocą pulsoksymetrii. Napięcie mięśni Istnieje duże prawdopodobieństwo, że bardzo wiotkie dziecko jest nieprzytomne i będzie wymagać wspomagania wentylacji. Stymulacja przez dotyk Osuszanie dziecka zwykle zapewnia wystarczającą stymulację do zainicjowania efektywnego oddychania. Należy unikać gwałtowniejszych metod stymulacji. Jeżeli noworodek nie podejmie spontanicznego i wydolnego oddechu po krótkim okresie stymulacji, konieczne będzie zastosowanie bardziej zaawansowanych czynności. Klasyfikacja oparta na ocenie wstępnej Opierając się na ocenie wstępnej, dziecko może być zakwalifikowane do jednej z trzech grup: 1. Wydolny oddech lub płacz Prawidłowe napięcie mięśniowe Czynność serca powyżej 100/min Dziecko to nie wymaga innych interwencji niż osuszenie, owinięcie w ciepły ręcznik i, jeśli to możliwe, przekazanie matce. Położone na skórę matki i przykryte będzie utrzymywać ciepło dzięki bezpośredniemu kontaktowi. Może być przystawione do piersi. 2. Oddech niewydolny lub jego brak Prawidłowe lub obniżone napięcie mięśniowe Czynność serca poniżej 100/min Należy osuszyć i okryć dziecko. Stan noworodka może poprawić się po upowietrznieniu płuc, ale jeśli nie skutkuje to odpowiednim wzrostem częstości pracy serca, może wymagać uciśnięć klatki piersiowej. 3. Oddech niewydolny lub jego brak Wiotkie Wolna lub niebadalna czynność serca Często występująca bladość sugerująca upośledzoną perfuzję Należy osuszyć i okryć dziecko. Noworodek będzie następnie wymagał natychmiastowego zabezpieczenia dróg oddechowych, upowietrznienia płuc oraz wentylacji. Po skutecznym wykonaniu tych procedur dziecko może również wymagać uciśnięć klatki piersiowej i możliwe, że także podania leków. Pozostaje nieliczna grupa dzieci, u których pomimo prawidłowego oddychania i właściwej czynności serca utrzymuje się hipoksemia. Do tej grupy zalicza się noworodki z następującymi możliwymi zaburzeniami: przepuklina przeponowa, niedobór surfaktantu, wrodzone zapalenie płuc, odma opłucnowa oraz wrodzona sinicza wada serca. Resuscytacja noworodka Resuscytację noworodka należy rozpocząć, jeśli w czasie oceny stwierdzono brak regularnego i prawidłowego oddechu lub częstość pracy serca wynosi mniej niż 100/min. Udrożnienie dróg oddechowych i upowietrznienie płuc zazwyczaj okazują się wystarczające. Co więcej, bardziej złożone interwencje będą daremne, dopóki te dwa pierwsze kroki nie zostaną skutecznie wykonane. Drożność dróg oddechowych Dziecko powinno być położone na plecach z głową w pozycji neutralnej. Koc lub ręcznik o grubości 2 cm położony pod ramionami dziecka może być pomocny w utrzymaniu głowy we właściwej pozycji. U wiotkich dzieci zastosowanie rękoczynu wysunięcia żuchwy lub założenie rurki ustno-gardłowej o właściwym rozmiarze może pomóc w udrożnieniu dróg oddechowych. Odsysanie należy zastosować tylko wówczas, gdy drogi oddechowe są niedrożne. Zbyt intensywne odsysanie gardła może jednak spowodować opóźnienie w rozpoczęciu samodzielnego oddychania, być przyczyną skurczu krtani i wywołać odruchową bradykardię poprzez stymulację nerwu błędnego 582. Obecność gęstej smółki u urodzonego w zamartwicy dziecka jest jedynym wskazaniem do rozważenia natychmiastowego odsysania jamy ustno-gardłowej. Jeśli wykonuje się odsysanie, najlepiej robić to pod kontrolą wzroku. Należy podłączyć cewnik do odsysania o rozmiarze FG lub cewnik typu Yankauer do próżni, nie przekraczając ciśnienia ssania 100 mm Hg. Oddychanie Po wstępnym zaopatrzeniu bezpośrednio po porodzie, jeśli próby samodzielnego oddychania są niewystarczające lub nie występują, priorytetem jest upowietrznienie płuc. U donoszonych noworodków należy rozpocząć wentylację powietrzem. Pierwszym wskaźnikiem właściwej wentylacji jest natychmiastowy wzrost częstości pracy serca. Jeśli czynność serca nie ulegnie poprawie, należy ocenić ruchy klatki piersiowej. Podczas wykonywania każdego z wstępnych wdechów należy utrzymywać dodatnie ciśnienie przez 2 3 sekundy. Pomoże to w rozprężeniu płuc. Większość dzieci wymagających resuscytacji bezpośrednio po urodzeniu reaguje szybkim wzrostem czynności serca w ciągu 30-sekundowego upowietrznienia płuc. Jeśli czynność serca wzrasta, ale dziecko nadal nie oddycha wydolnie, należy kontynuować wentylację z częstością około 30 oddechów na minutę do czasu pojawienia się prawidłowego, spontanicznego oddechu. Na jeden wdech należy przeznaczyć około jednej sekundy. 1
48 50 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Dowodem na właściwą wentylację jest zwykle szybki wzrost częstości pracy serca lub utrzymywanie się jej na poziomie powyżej 100/min. Jeśli dziecko nie zareaguje w ten sposób, najczęstszą przyczyną jest niewłaściwe udrożnienie dróg oddechowych lub nieprawidłowa wentylacja. Bez prawidłowego upowietrznienia płuc uciskanie klatki piersiowej będzie nieskuteczne, dlatego niezbędne jest upowietrznienie płuc przed przystąpieniem do wspomagania układu krążenia. Osoby przeszkolone mogą zapewnić drożność dróg oddechowych poprzez intubację dotchawiczą, ale wymaga to praktyki i doświadczenia. Jeśli nie posiada się tej umiejętności, a częstość pracy serca dziecka ulega obniżeniu, należy ponownie ocenić drożność dróg oddechowych i prowadzić wentylację, jednocześnie wzywając osobę posiadającą umiejętność intubacji. Należy kontynuować wspomaganie wentylacji, dopóki dziecko nie rozpocznie regularnie i prawidłowo oddychać. Wspomaganie układu krążenia Wspomaganie układu krążenia poprzez uciskanie klatki piersiowej jest skuteczne tylko wtedy, gdy wcześniej udało się rozprężyć płuca dziecka. Jeżeli pomimo prawidłowej wentylacji częstość pracy serca pozostaje mniejsza niż 60 uderzeń/min, należy rozpocząć uciśnięcia klatki piersiowej. Najbardziej skuteczna technika uciskania klatki piersiowej polega na umieszczeniu nad dolną jedną trzecią mostka, tuż poniżej linii międzysutkowej, obok siebie dwóch kciuków. Pozostałymi palcami obu dłoni należy objąć klatkę piersiową i podtrzymywać plecy dziecka Alternatywnie miejsce uciskania klatki piersiowej może być wyznaczone poprzez identyfikację wyrostka mieczykowatego i ułożenie kciuków na mostku w odległości równej szerokości jednego palca powyżej tego punktu. Mostek powinien być uciskany na głębokość odpowiadającą około jednej trzeciej wymiaru przedniotylnego klatki piersiowej, pozwalając na jej relaksację do wyjściowego kształtu pomiędzy uciśnięciami 587. Należy wykonywać te czynności w stosunku trzech uciśnięć do jednej wentylacji, dążąc do uzyskania łącznie około 120 czynności na minutę (tj. około 90 uciśnięć i 30 oddechów). Ocena częstości pracy serca powinna zostać wykonana po około 30 sekundach, a następnie powtarzana co 30 sekund. Gdy częstość pracy serca wzrośnie powyżej 60 uderzeń/min, należy przerwać uciskanie klatki piersiowej. Leki Rzadko istnieją wskazania do podania leków podczas resuscytacji noworodka. Bradykardia występująca po porodzie jest zwykle spowodowana niewystarczającym rozprężeniem płuc lub ciężką hipoksją, a najważniejszym sposobem jej leczenia jest zapewnienie właściwej wentylacji. Jeśli jednak częstość pracy serca utrzymuje się poniżej 60 uderzeń/ min, pomimo właściwej wentylacji i uciskania klatki piersiowej, zasadne jest rozważenie podania leków. Najlepszą drogą podawania leków jest cewnik wprowadzony do żyły pępowinowej. Adrenalina Pomimo braku danych pochodzących z obserwacji klinicznych u ludzi wydaje się uzasadnione stosowanie adrenaliny w sytuacji, kiedy właściwa wentylacja i uciskanie klatki piersiowej nie spowodowały przyspieszenia częstości pracy serca powyżej 60 uderzeń/min. Jeśli stosuje się adrenalinę, to należy ją podać dożylnie w dawce μg/kg tak szybko, jak to tylko możliwe. Nie zaleca się podawania tego leku dotchawiczo, ale jeżeli wykorzystuje się tę drogę podania, jest wysoce prawdopodobne, że wymagane będą dawki μg/kg. Brak jest danych dotyczących bezpieczeństwa i skuteczności tak wysokich dawek adrenaliny podawanych drogą dotchawiczą. Nie należy podawać tak wysokich dawek adrenaliny dożylnie. Wodorowęglan Brak jest wystarczającej ilości danych, by zalecić rutynowe podawanie wodorowęglanu w resuscytacji noworodków. Hiperosmolarność i generowanie dwutlenku węgla towarzyszące stosowaniu wodorowęglanu sodu mogą mieć niekorzystny wpływ na czynność mięśnia sercowego i mózgu. Odradza się stosowanie wodorowęglanu sodu podczas krótkotrwałej resuscytacji. Jeżeli stosuje się ten lek w przypadku przedłużającego się, niereagującego na inne leczenie zatrzymania krążenia, należy wcześniej zapewnić właściwą wentylację i krążenie poprzez wykonywanie RKO. Dawka 1 2 mmol/kg podawana dożylnie w powolnym wstrzyknięciu może być zastosowana pod warunkiem uzyskania adekwatnej wentylacji i perfuzji. Płyny Jeżeli podejrzewa się u noworodka utratę krwi lub obserwuje się objawy wstrząsu (blada skóra, zła perfuzja, słabo wyczuwalne tętno), a dziecko nie reaguje właściwie na wykonane dotychczas zabiegi resuscytacyjne, należy rozważyć podanie płynów 588. Sytuacja taka jest bardzo rzadka. W przypadku braku odpowiedniej krwi (tj. ubogoleukocytarnej, napromienianej krwi grupy 0 Rh ujemny) w celu przywrócenia objętości wewnątrznaczyniowej z wyboru należy stosować izotoniczne roztwory krystaloidów, a nie albumin. Wstępny bolus powinien wynosić 10 ml/kg. Jeśli przyniesie skutek, może wymagać powtórzenia w celu utrzymania osiągniętej poprawy. Przerwanie resuscytacji Lokalne i narodowe komitety powinny określić wskazania do przerwania resuscytacji. Jeśli u noworodka po urodzeniu nie udaje się stwierdzić obecności pracy serca i pozostaje ona niebadalna przez 10 minut, należy rozważyć zaprzestanie resuscytacji. W przypadkach gdy częstość pracy serca wynosi poniżej 60 uderzeń/min bezpośrednio po urodzeniu i nie wzrasta po 10 lub 15 minutach nieprzerwanej i prawidłowo prowadzonej resuscytacji, podjęcie decyzji o zaprzestaniu resuscytacji jest mniej oczywiste. W tych sytuacjach dane dotyczące wyników odległych leczenia pacjentów są niewystarczające, aby określić ścisłe wytyczne, czy zaprzestać lub kontynuować resuscytację. Komunikacja z rodzicami Ważne jest, aby zespół opiekujący się noworodkiem informował rodziców o stanie dziecka. W trakcie porodu należy stosować rutynowe lokalne postępowanie i, jeśli jest to
49 Podsumowanie Komitetu Wykonawczego ERC 51 możliwe, należy jak najszybciej przekazać dziecko matce. Jeżeli konieczna jest resuscytacja, rodzice powinni być poinformowani o rozpoczętych zabiegach oraz celu ich wykonywania. Należy dokładnie prowadzić dokumentację dotyczącą przeprowadzonych rozmów i podjętych decyzji, przed porodem w historii choroby matki oraz w dokumentacji dziecka po porodzie. Zatrzymanie krążenia w sytuacjach szczególnych Zaburzenia elektrolitowe Zaburzenia rytmu zagrażające życiu wynikają najczęściej z nieprawidłowego poziomu jonów potasu, zwykle hiperkaliemii. Nieco rzadziej ich przyczyną są zaburzenia poziomu jonów wapnia i magnezu w surowicy. W niektórych przypadkach leczenie zagrażających życiu zaburzeń elektrolitowych powinno być rozpoczęte przed otrzymaniem wyników badań laboratoryjnych. Istnieje mało, lub w niektórych przypadkach w ogóle brak jest danych, opartych na badaniach naukowych, dotyczących leczenia zaburzeń elektrolitowych podczas zatrzymania krążenia. Wytyczne dotyczące takiego postępowania są oparte na sposobach leczenia pacjenta, u którego nie doszło do zatrzymania krążenia. Nowe wytyczne nie zmieniły się znacznie w stosunku do wytycznych Zatrucia Zatrucia rzadko są przyczyną zatrzymania krążenia, ale pozostają główną przyczyną zgonów wśród osób w wieku poniżej 40. roku życia 590. Najczęstszą przyczyną przyjęć do szpitala i konsultacji telefonicznych prowadzonych przez ośrodki toksykologiczne są zatrucia lekami, substancjami psychoaktywnymi lub używanymi w gospodarstwach domowych. Toksyczność leków może wynikać także z ich nieprawidłowego dawkowania, interakcji między różnymi preparatami lub podania niewłaściwego leku. Przypadkowe zatrucia najczęściej zdarzają się u dzieci. Otrucia są stosunkowo rzadkie. Wypadki w zakładach przemysłowych, działania wojenne lub ataki terrorystyczne mogą być również przyczyną narażenia na substancje szkodliwe. Zapobieganie zatrzymaniu krążenia Należy ocenić i leczyć pacjenta, używając schematu ABCDE (Airway, Breathing, Circulation, Disability, Exposure). Utrata przytomności prowadząca wtórnie do niedrożności dróg oddechowych i zatrzymania oddechu jest najczęstszą przyczyną zgonów w grupie pacjentów, którzy przyjęli leki w celach samobójczych 591. Po zatruciu lekami działającymi depresyjnie na ośrodkowy układ nerwowy może wystąpić aspiracja treści pokarmowej. Wczesna intubacja nieprzytomnego pacjenta przez wykwalifikowaną osobę może zmniejszyć ryzyko aspiracji. Spadek ciśnienia wywołany działaniem leków zwykle odpowiada na płynoterapię, ale w niektórych przypadkach konieczne jest zastosowanie leków o działaniu wazopresyjnym (np. wlew noradrenaliny). Długotrwająca śpiączka, z ułożeniem ciała w jednej pozycji może przyczynić się do wystąpienia odleżyn i rabdomiolizy. Należy zbadać poziom elektrolitów (szczególnie potasu), poziom glikemii i wykonać gazometrię krwi tętniczej. Monitorowanie temperatury ciała jest konieczne z powodu zaburzonej termoregulacji. Zarówno hipotermia jak i hipertermia (hiperpyreksja) mogą być objawem zatrucia niektórymi lekami. Należy zachować próbki krwi i moczu do dalszych badań. Pacjenci z ciężkim zatruciem powinni być leczeni w warunkach intensywnej terapii. Takie działania jak dekontaminacja, zwiększenie eliminacji substancji toksycznej, użycie odtrutek mogą być wskazane, ale są zwykle interwencjami drugoplanowymi 592. Nadużycie alkoholu często jest skojarzone z przyjęciem innych substancji w celach samobójczych. Modyfikacje BLS/ALS Zadbaj szczególnie o swoje bezpieczeństwo w przypadku podejrzanych okoliczności zdarzenia lub gdy doszło do niespodziewanego zatrzymania krążenia. Szczególnie istotne jest to w przypadku jednoczasowej utraty przytomności więcej niż jednej osoby. Unikaj prowadzenia wentylacji usta usta w przypadku zatrucia takimi środkami chemicznymi, jak: cyjanki, siarkowodór, fosforany organiczne oraz substancje żrące. W leczeniu zagrażających życiu zaburzeń rytmu zaleca się wykonanie kardiowersji zgodnie z algorytmem leczenia zaburzeń rytmu serca (zob. rozdział 4. Zaawansowane zabiegi resuscytacyjne u osób dorosłych) 6. Należy również leczyć zaburzenia elektrolitowe i równowagi kwasowo-zasadowej. Spróbuj zidentyfikować truciznę(y). Użytecznych informacji może udzielić rodzina, przyjaciele i personel pogotowia ratunkowego. Badanie fizykalne pacjenta może pomóc w rozpoznaniu trucizny i dostarczyć takich wskazówek, jak: zapach, ślady po wkłuciach igieł, nieprawidłowości w badaniu źrenic czy ślady świadczące o użyciu substancji żrącej w jamie ustnej. Zbadaj temperaturę ciała pacjenta. Zarówno hipo- jak i hipertermia mogą wystąpić po przedawkowaniu pewnych leków (zob. rozdział 8d i 8e). Przygotuj się na prowadzenie resuscytacji przez dłuższy czas, szczególnie u młodych osób, część trucizn może ulec zmetabolizowaniu lub wydaleniu w czasie przedłużonych czynności resuscytacyjnych. Odmienne postępowanie, które może być skuteczne u pacjentów z ciężkim zatruciem, obejmuje: użycie wyższych niż standardowe dawek leków, niestandardowe protokoły leczenia, przedłużoną resuscytację krążeniowo-oddechową. Skontaktuj się z regionalnymi lub krajowymi ośrodkami leczenia zatruć w celu zdobycia informacji o sposobie leczenia pacjenta. The International Programme on Chemical Safety (IPCS) umieszcza listę ośrodków leczenia zatruć na stronie internetowej: int/ipcs/poisons/centre/en/ (zawiera także kontakt do ośrodków w Polsce przyp. tłum.). Dostępna on-line baza danych toksykologicznych i informacji o niebezpiecznych związkach chemicznych: W Polsce strony: cm-uj.krakow.pl oraz 1
50 52 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Tonięcie Światowa Organizacja Zdrowia (WHO) ocenia, że każdego roku z powodu tonięcia umiera na całym świecie osób, a w Europie jest to jedna z najczęstszych przyczyn zgonu, do którego dochodzi w wyniku wypadku. Po epizodzie tonięcia czas trwania niedotlenienia jest krytycznym czynnikiem wpływającym na rokowanie. Z tego powodu natlenienie, wentylacja i perfuzja powinny być przywrócone tak szybko, jak to tylko możliwe. Natychmiastowe rozpoczęcie resuscytacji na miejscu zdarzenia jest kluczowym działaniem umożliwiającym przeżycie z przywróceniem funkcji neurologicznych po epizodzie tonięcia. Sytuacja taka wymaga rozpoczęcia resuscytacji przez świadków zdarzenia i natychmiastowej aktywacji systemu ratownictwa medycznego. Rokowanie jest zazwyczaj dobre w przypadku pacjentów, którzy w chwili przybycia do szpitala mają zachowany oddech i krążenie. W porównaniu z pierwotnie kardiologicznymi zatrzymaniami krążenia obserwacje dotyczące epizodów tonięcia są ograniczone i istnieje potrzeba dalszych badań w tym zakresie 593. Dokładne wytyczne postępowania są opisane w rozdziale 8 Wytycznych ERC i są one przeznaczone dla pracowników ochrony zdrowia oraz określonych grup osób niezwiązanych zawodowo z medycyną, które mogą mieć do czynienia z ofiarami tonięcia, np. ratownicy wodni 10. Hipotermia przypadkowa Hipotermię przypadkową stwierdzamy, gdy temperatura głęboka ciała w sposób niezamierzony spada poniżej 35 C. Hipotermię dzielimy na łagodną (35 32 C), umiarkowaną (32 28 C) oraz ciężką (poniżej 28 C) 594. U pacjenta w hipotermii stwierdzanie zgonu jedynie na podstawie braku oznak życia jest zbyt mało wiarygodne. W warunkach przedszpitalnych należy rozważyć niepodejmowanie resuscytacji jedynie wówczas, gdy przyczyna zatrzymania krążenia nie budzi wątpliwości i jest spowodowana śmiertelnym urazem, chorobą terminalną, przedłużonym zatrzymaniem oddechu lub gdy nie ma możliwości uciskania klatki piersiowej (incompressible chest). Wszystkie zasady zapobiegania zatrzymaniu krążenia, prowadzenia podstawowych oraz zaawansowanych zabiegów resuscytacyjnych dotyczą także pacjentów z hipotermią. Należy wykonywać uciśnięcia klatki piersiowej i wentylację z taką samą częstotliwością jak u pacjentów z prawidłową temperaturą ciała. Hipotermia powoduje jednak zwiększenie sztywności klatki piersiowej, przez co zarówno wentylacja jak i uciśnięcia klatki piersiowej mogą być trudniejsze do wykonania. Serce pacjenta w hipotermii może nie odpowiadać na leki, próby elektrostymulacji czy defibrylację. Metabolizm leków jest zwolniony, prowadząc przy powtarzanych dawkach do potencjalnie toksycznego ich stężenia w osoczu 595. Z tego powodu nie należy podawać adrenaliny i innych leków stosowanych podczas RKO do czasu ogrzania pacjenta powyżej 30 C. Gdy temperatura osiągnie 30 C należy podwoić przerwy pomiędzy dawkami leków w stosunku do przerw stosowanych w normotermii. Gdy zostanie osiągnięta normotermia (>35 C), należy stosować standardowy protokół podawania leków. W miarę obniżania się temperatury głębokiej ciała bradykardia zatokowa przechodzi w migotanie przedsionków, a następnie w VF i ostatecznie w asystolię 596. Jak tylko poszkodowany z zatrzymaniem krążenia przebiegu ciężkiej hipotermią znajdzie się w szpitalu, powinien być aktywnie ogrzewany przy użyciu metod wewnętrznych. Zaburzenia rytmu, poza VF, ustępują spontanicznie wraz ze wzrostem temperatury głębokiej ciała i z reguły nie wymagają natychmiastowego działania. Bradykardia może fizjologicznie występować w ciężkiej hipotermii, lecz stymulacja serca nie jest wskazana, chyba że po ogrzaniu bradykardia utrzymuje się wraz z objawami niestabilności hemodynamicznej. W ciężkiej hipotermi nie została określona temperatura, przy której powinno się podjąć po raz pierwszy próbę defibrylacji oraz jak często należy ją powtarzać. Można stosować AED u tych pacjentów. Jeśli stwierdzi się VF, należy wykonać defibrylację najwyższą możliwą energią, jeśli natomiast VF/VT utrzymuje sie po trzech wyładowaniach, kolejne próby defibrylacji, powinno się wykonać po osiągnięciu temperatury głębokiej ciała powyżej 30 C 597. Używając AED, należy postępować zgodnie z poleceniami urządzenia, równocześnie ogrzewając pacjenta. RKO oraz ogrzewanie mogą wymagać kontynuacji przez kilka godzin, zanim uda się doprowadzić do efektywnej defibrylacji 597. Ogrzewanie możemy podzielić na bierne, czynne zewnętrzne i czynne wewnętrzne. Bierne ogrzewanie jest właściwe u poszkodowanych przytomnych w łagodnej hipotermii, u których wciąż występują dreszcze. Pacjenci w hipotermii, u których występują zaburzenia świadomości powinni być przyjęci do szpitala, gdzie są możliwości zastosowania ogrzewania czynnego wewnętrznego i zewnętrznego. U pacjentów w hipotermii z zatrzymaniem oddychania i krążenia preferowaną metodą czynnego wewnętrznego ogrzewania jest zastosowanie krążenia pozaustrojowego. Zapewnia ono krążenie i natlenienie krwi jednoczasowo umożliwiając wzrost temperatury głębokiej ciała 8 12 C na godzinę 598. W trakcie ogrzewania pacjent powinien otrzymywać duże objętości płynów, gdyż na skutek rozszerzenia naczyń dochodzi do zwiększenia przestrzeni wewnątrznaczyniowej. Podstawową czynnością jest ciągły monitoring hemodynamiczny i podawanie dożylne ciepłych płynów, jak również unikanie hipertermii zarówno w trakcie, jak i po ogrzewaniu. Mimo że brak jest opublikowanych badań, gdy tylko uda się osiągnąć ROSC, należy rozpocząć standardową procedurę opieki poresuscytacyjnej, włączając w to łagodną hipotermię, jeśli są ku temu wskazania. Hipertermia Hipertermia występuje wtedy, kiedy wyczerpują się mechanizmy termoregulacji, w efekcie czego temperatura głęboka podnosi się powyżej górnej granicy wartości prawidłowych utrzymywanych przez mechanizmy homeostazy ustroju. Hipertermia może rozwinąć się w wyniku działania czynników zewnętrznych (środowiskowych) lub wtórnie z powodu nadmiernej produkcji ciepła przez organizm. Do hipertermii związanej z działaniem czynników środowiskowych dochodzi wówczas, gdy ciepło (zwykle dzięki promieniowaniu) jest absorbowane przez organizm szybciej, niż może być eliminowane dzięki mechanizmom termoregulacji. Hipertermia może się manifestować w szeregu coraz poważniejszych stanów klinicznych, od objawów przegrzania (heat stress) poprzez wyczerpanie cieplne i udar cieplny
51 Podsumowanie Komitetu Wykonawczego ERC 53 (Heat Stroke HS) do zespołu niewydolności wielonarządowej, a niekiedy nawet zatrzymania krążenia 599. Udar cieplny powstaje w wyniku rozwinięcia się systemowej odpowiedzi zapalnej spowodowanej wzrostem temperatury głębokiej powyżej 40,6 C. Towarzyszą temu zaburzenia stanu świadomości i objawy niewydolności narządów o różnym stopniu zaawansowania. Rozpoznaje się 2 postaci udaru cieplnego. Klasyczna postać udaru cieplnego nie jest związana z wysiłkiem i występuje w wyniku narażenia na wysoką temperaturą otoczenia. Tę postać często można obserwować u osób starszych podczas fali upałów 600. Postać udaru cieplnego związana z wysiłkiem fizycznym częściej występuje u zdrowych, młodych osób. Rozwija się ona w wyniku wykonywania intensywnego wysiłku fizycznego przy wysokiej temperaturze otoczenia i/lub wysokiej wilgotności powietrza 601. Śmiertelność w przebiegu udaru cieplnego wynosi od 10 do 50% 602. Podstawą leczenia jest zabezpieczenie i optymalizacja ABCDE i szybkie chłodzenie pacjenta Chłodzenie należy rozpocząć jeszcze przed przybyciem do szpitala. Celem jest jak najszybsze obniżenie temperatury głębokiej ciała do ok. 39 C. Pacjenci z ciężkim udarem cieplnym powinni być leczeni w warunkach intensywnego nadzoru. Brak badań klinicznych dotyczących postępowania w zatrzymaniu krążenia u pacjentów w hipertermii. Jeżeli dojdzie do zatrzymania krążenia, należy postępować zgodnie z wytycznymi dla podstawowych i zaawansowanych zabiegów resuscytacyjnych oraz rozpocząć ochładzanie pacjenta. Należy stosować techniki chłodzenia podobne do indukcji hipotermii leczniczej. Nie ma badań opisujących wpływ hipertermii na próg defibrylacji, dlatego należy wykonywać defibrylację zgodnie z aktualnymi wytycznymi, równocześnie chłodząc pacjenta. Badania na zwierzętach pokazują, że efektywność takiej resuscytacji jest znacznie gorsza niż przy zatrzymaniu krążenia w normotermii 606, 607. Ryzyko wystąpienia powikłań neurologicznych rośnie wraz ze wzrostem temperatury głębokiej o każdy stopień powyżej 37 C 349. Astma Objawy astmy na świecie dotyczą od 1% do 18% populacji z częstszym występowaniem w niektórych krajach Europy (Wielka Brytania, Irlandia i Skandynawia) 608. Roczna umieralność z powodu astmy została określona na Istnieją już krajowe i międzynarodowe wytyczne postępowania w astmie 608,609. Wytyczne te skupiają się na leczeniu pacjentów z zagrażającą życiu astmą i zatrzymaniem krążenia w przebiegu tej choroby. Przyczyny zatrzymania krążenia w przebiegu astmy Zatrzymanie krążenia u chorych na astmę jest często końcowym etapem po okresie ciężkiego niedotlenienia; sporadycznie może mieć nagły charakter. Zatrzymanie krążenia w przebiegu astmy jest związane z: ciężkim skurczem oskrzeli i zamknięciem ich światła wydzieliną śluzową, co prowadzi do asfiksji (ten stan jest przyczyną zdecydowanej większości zgonów w przebiegu astmy); zaburzeniami rytmu spowodowanymi niedotlenieniem (które jest najczęstszą przyczyną arytmii w przebiegu astmy) 610 ; zaburzenia rytmu mogą także być wynikiem działania leków stymulujących (np. agonistów receptorów beta-adrenergicznych, aminofiliny) lub zaburzeń elektrolitowych; dynamicznie postępującą hiperinflacją pęcherzyków płucnych, np. auto-peep, która może się pojawić u wentylowanych mechanicznie astmatyków. Auto-PEEP jest spowodowany pułapką powietrzną i gromadzeniem się powietrza (powietrze podczas wdechu dostaje się do pęcherzyków płucnych, ale nie może się z nich wydostać). Ciśnienie w pęcherzykach płucnych wzrasta stopniowo, redukując powrót krwi żylnej i ciśnienie tętnicze krwi; odmą prężną (często obustronną). Kluczowe interwencje zapobiegające wystąpieniu zatrzymania krążenia Pacjent z objawami ciężkiego napadu astmy wymaga agresywnego leczenia, aby zapobiec pogorszeniu jego stanu. Ocenę i leczenie pacjenta należy opierać na schemacie ABCDE. U pacjentów z SaO 2 <92% lub z cechami zagrażającej życiu astmy istnieje ryzyko hiperkapnii i wymagają oni oznaczenia gazometrii krwi tętniczej. Tego rodzaju pacjenci wysokiego ryzyka powinni być leczeni przez doświadczonych lekarzy w warunkach intensywnej terapii. Wybór leków i kolejności leczenia będzie różnić się w zależności od lokalnej praktyki, a zostało ono opisane w rozdziale 8f Wytycznych resuscytacji 10. Leczenie zatrzymania krążenia w przebiegu astmy BLS należy prowadzić zgodnie ze standardowymi wytycznymi. Wentylacja będzie trudna z powodu zwiększonego oporu w drogach oddechowych; należy unikać rozdęcia żołądka. Modyfikacje w standardowych wytycznych ALS obejmują rozważenie potrzeby wczesnej intubacji tchawicy. Bardzo wysoki opór w drogach oddechowych oznacza, że u tych pacjentów istnieje znaczące ryzyko rozdęcia żołądka i hipowentylacji płuc podczas prowadzenia wentylacji bez wcześniejszej intubacji. W trakcie zatrzymania krążenia ryzyko to jest jeszcze wyższe, gdyż wtedy ciśnienie otwarcia dolnego zwieracza przełyku jest niższe niż fizjologiczne 611. Częstość oddechów 8 10 na minutę oraz objętość oddechowa wymagana do prawidłowego unoszenia się klatki piersiowej podczas RKO nie powinny powodować dynamicznej hiperinflacji płuc (pułapki powietrznej). Objętość oddechowa zależy od czasu trwania i przepływu podczas wdechu. Opróżnianie płuc zależy od czasu trwania i przepływu podczas wydechu. U pacjentów z ciężką astmą, wentylowanych mechanicznie, wydłużenie czasu wydechu (osiągane poprzez zmniejszenie częstości wentylacji) dostarcza tylko umiarkowanych korzyści w redukcji pułapki powietrznej, gdy stosowana jest pojemność minutowa mniejsza niż 10 l/min 612. W pojedynczych przypadkach klinicznych opisywano sytuację, kiedy po rozłączeniu rurki intubacyjnej wystąpił niespodziewany powrót spontanicznego krążenia u pacjentów podejrzewanych o wystąpienie pułapki powietrznej Jeżeli w trakcie resuscytacji podejrzewa się nadmierne rozdęcie płuc spowodowane zjawiskiem pułapki powietrznej, okresowe rozłączenie rurki intubacyjnej i prowadzenie przez 1
52 54 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 chwilę tylko uciśnięć klatki piersiowej może ograniczyć to zjawisko. Jakkolwiek nieliczne dowody potwierdzają skuteczność tej metody, raczej nie może ona zaszkodzić w tak krytycznej sytuacji 15. Hiperinflacja płuc prowadzi do wzrostu impedancji klatki piersiowej 618. Jeżeli pierwsze defibrylacje są nieskuteczne, należy rozważyć użycie wyższych wartości energii 14. Brak jest wystarczających dowodów potwierdzających skuteczność prowadzenia bezpośredniego masażu serca u pacjentów z zatrzymaniem krążenia spowodowanym ciężkim napadem astmy. W trakcie resuscytacji pacjenta chorego na astmę zawsze należy myśleć o odwracalnych przyczynach zatrzymania krążenia (4 H, 4 T). Odma prężna może być trudna do rozpoznania w trakcie zatrzymania krążenia, może na to wskazywać asymetria ruchów klatki piersiowej w trakcie wentylacji, przesunięcie tchawicy i wystąpienie rozedmy podskórnej. Badanie ultrasonograficzne jamy opłucnowej wykonane przez doświadczoną osobę jest szybszą i bardziej czułą metodą potwierdzającą obecność odmy prężnej niż RTG klatki piersiowej 619. W przypadku NZK u chorych z astmą zawsze należy brać pod uwagę obecność powietrza w obu jamach opłucnowych. Pozaustrojowe metody wspomagania układu krążenia (Extracorporeal Life Support ECLS) mogą zapewnić zarówno perfuzję narządową, jak i wymianę gazową w sytuacji niereagującej na leczenie niewydolności oddechowej i krążeniowej. Opisano kilka przypadków skutecznego leczenia przy zastosowaniu ECLS zatrzymania krążenia u pacjentów dorosłych spowodowanego ostrym napadem astmy 620,621, jednakże rola ECLS w wyżej wspomnianych okolicznościach nigdy nie była analizowana w badaniach z grupą kontrolną. Anafilaksja Anafilaksja jest ciężką, zagrażającą życiu, uogólnioną lub układową reakcją nadwrażliwości. Charakteryzuje ją gwałtowny rozwój zagrażających życiu problemów związanych z drożnością dróg oddechowych i/lub oddychaniem, i/lub krążeniem, połączonych zwykle ze zmianami skórnymi i w obrębie błon śluzowych 622,623. Anafilaksja na ogół obejmuje uwolnienie mediatorów zapalnych z mastocytów i/lub bazofili, wyzwolone reakcją antygenu z komórkami wiążącymi immunoglobulinę E (IgE). Do uwolnienia mediatorów może także dojść bez udziału IgE lub w wyniku działań mechanizmów nieimmunologicznych. Uwolnienie histaminy i innych mediatorów zapalnych jest odpowiedzialne za rozkurcz naczyń, obrzęk i zwiększoną przepuszczalność naczyń włosowatych. Rozpoznanie anafilaksji jest prawdopodobne, jeśli u pacjenta, który jest eksponowany na czynnik wyzwalający (alergen), rozwija się nagle (zwykle w ciągu kilku minut) choroba z szybko narastającymi, zagrażającymi życiu objawami niedrożności dróg oddechowych i/lub niewydolności oddechowej i/lub krążenia, zwykle z towarzyszącymi zmianami skórnymi i zmianami błon śluzowych. Reakcja ta jest zwykle niespodziewana. Do rozpoznania i leczenia anafilaksji należy używać schematu badania ABCDE. Adrenalina powinna być podana wszystkim pacjentom z objawami zagrożenia życia. Podanie domięśniowe (im) adrenaliny jest najlepsze dla większości osób, które używają adrenaliny w leczeniu anafilaksji. Należy użyć następujących dawek: >12 lat i dorośli: 500 μg im >6 12 lat: 300 μg im >6 m-cy 6 lat: 150 μg im <6 m-cy: 150 μg im Dożylna podaż adrenaliny powinna być wykonywana jedynie przez osoby mające doświadczenie kliniczne w stosowaniu i miareczkowaniu leków wazopresyjnych (np. anestezjolog, lekarz ratunkowy, lekarz intensywnej terapii). U osób dorosłych adrenalinę należy rozcieńczyć i podawać w powtarzanych bolusach po 50 μg do uzyskania pożądanego działania. Od początku leczenia należy zapewnić maksymalne osiągalne stężenie tlenu, stosując maskę twarzową z rezerwuarem 427. Należy szybko przetoczyć bolus płynów dożylnie (20 ml/kg) w przypadku dzieci lub ml w przypadku osób dorosłych, obserwować reakcję i podać kolejny bolus, jeżeli to jest wskazane. Inne leki (steroidy, leki antyhistaminowe itp.) stosowane w leczeniu zagrażającego życiu napadu astmy zostały opisane w rozdziale 8g. Jeżeli nastąpi zatrzymanie krążenia, resuscytację krążeniowooddechową (RKO) należy rozpocząć bezzwłocznie i prowadzić ją zgodnie z aktualnymi wytycznymi. Konieczne może okazać się przedłużenie czasu prowadzenia RKO. Ratownicy powinni się upewnić, czy pomoc została wezwana, gdyż zasadnicze znaczenie ma wczesne wdrożenie zaawansowanych zabiegów resuscytacyjnych (ALS). Oznaczenie tryptazy uwolnionej z mastocytów może pomóc w potwierdzeniu rozpoznania reakcji anafilaktycznej. Optymalnie należy pobrać trzy próbki, pierwszą jak najszybciej po rozpoczęciu leczenia, drugą 1 2 godziny od pojawienia objawów i trzecią po 24 godzinach lub w okresie rekonwalescencji. Wszyscy pacjenci z rozpoznaną reakcją anafilaktyczną powinni zostać skierowani do specjalistycznej kliniki alergologicznej, aby zidentyfikować przyczynę, zmniejszyć ryzyko wystąpienia reakcji anafilaktycznej w przyszłości i przygotować ich do samodzielnego radzenia sobie z tą chorobą. Zatrzymanie krążenia w następstwie zabiegów kardiochirurgicznych Zatrzymanie krążenia w następstwie dużych zabiegów kardiochirurgicznych występuje dość często, bezpośrednio po zabiegu opisuje sie jego częstość na poziomie 0,7 2,9% Jest ono zwykle związane z załamaniem mechanizmów fizjologicznych 633, choć może również nagle wystąpić u pacjentów stabilnych 630. Z reguły istnieją konkretne przyczyny takiego zatrzymania krążenia, takie jak: tamponada worka osierdziowego, hipowolemia, niedokrwienie mięśnia sercowego, odma prężna czy dysfunkcja stymulatora rytmu. Wszystkie te przyczyny są potencjalnie odwracalne i jeśli są leczone odpowiednio wcześnie, zatrzymanie krążenia po zabiegach kardiochirurgicznych cechuje się wysoką przeżywalnością. Kluczem do efektywnej resuscytacji tych pacjentów jest rozpoznanie konieczności wykonania ratunkowego, ponownego otwarcia klatki piersiowej, zwłaszcza
53 Podsumowanie Komitetu Wykonawczego ERC 55 w kontekście tamponady czy krwawienia, kiedy zewnętrzne uciśnięcia klatki piersiowej mogą być nieefektywne. Rozpoczęcie RKO Jak najszybciej należy rozpocząć uciśnięcia klatki piersiowej u wszystkich pacjentów, którzy stracili przytomność i u których nie stwierdza się rzutu serca. Konieczne jest rozważenie potencjalnie odwracalnych przyczyn zatrzymania krążenia: hipoksja sprawdź położenie rurki intubacyjnej, rozpocznij wentylację 100-procentowym tlenem; odma prężna wykonaj badanie fizykalne, USG klatki piersiowej; hipowolemia, dysfunkcja rozrusznika. W asystolii powstałej w wyniku awarii stymulatora można odwlec w czasie uciśnięcia klatki piersiowej do momentu chirurgicznego założenia tymczasowej elektrody endokawitarnej, aby jak najszybciej ponownie włączyć stymulację (DDD o częstotliwości 100/min przy maksymalnej ampitudzie). Efektywność uciśnięć klatki piersiowej może być oceniana przez obserwację zapisu linii tętniczej, należy starać się osiągnąć ciśnienie skurczowe krwi tętniczej min 80 mm Hg, przy częstotliwości uciśnięć 100/min. Defibrylacja Istnieją obawy, że uciśnięcia klatki piersiowej mogą uszkodzić mostek lub serce Na oddziałach intensywnej terapii kardiochirurgicznej w zauważonym i monitorowanym zatrzymaniu krążenia w mechanizmie VF/VT należy wykonać jak najszybciej serię do trzech defibrylacji. Nieefektywne trzy próby defibrylacji w zatrzymaniu krążenia po zabiegu kardiochirurgicznym są wskazaniem do wykonania otwarcia klatki piersiowej w trybie natychmiastowym. Jeżeli otwarto klatkę piersiową, kolejne próby defibrylacji powinny być wykonywane zgodnie z uniwersalnym algorytmem, z zastosowaniem łyżek do bezpośredniej defibrylacji i energią 20 J. Leki w sytuacji zagrożenia życia Adrenalina powinna być podawana bardzo ostrożnie w dawkach podzielonych aż do uzyskania efektu (dawki dożylne u osób dorosłych to 100 μg lub mniej). Amiodaron w dawce 300 mg powinien być podany po trzeciej nieskutecznej defibrylacji, jego podanie nie powinno opóźniać ponownego otwarcia klatki piersiowej. Ponowne otwarcie klatki piersiowej w trybie natychmiastowym Jeżeli wszystkie inne odwracalne przyczyny zatrzymania krążenia zostały wykluczone, jest to procedura będąca integralną częścią resuscytacji po zabiegu kardiochirurgicznym. Nie należy opóźniać ponownego otwarcia klatki piersiowej, jeżeli zabezpieczono drogi oddechowe i wdrożono wentylację, a także nieskuteczne okazały się trzy próby defibrylacji VF/VT. Ponowne otwarcie klatki piersiowej w trybie natychmiastowym jest również wskazane w przypadku asystolii i PEA, jeśli wdrożone leczenie jest nieskuteczne. Defibrylacja bezpośrednia Defibrylacja bezpośrednia, przy użyciu łyżek przyłożonych bezpośrednio do komór serca, wymaga znacznie mniejszych energii niż defibrylacja zewnętrzna. 20 J jest najczęściej stosowaną energią w zatrzymaniu krążenia, jednak 5 J będzie wystarczające dla pacjentów podłączonych do krążenia pozaustrojowego. Kontynuując uciśnięcia serca łyżkami do defibrylacji podczas ładowania defibrylatora i dostarczając energię w trakcie trwania fazy relaksacji, można poprawić skuteczność wyładowania 638,639. Zatrzymanie krążenia spowodowane urazem Zatrzymanie krążenia spowodowane urazem związane jest z bardzo wysoką śmiertelnością. Ogólną przeżywalność ocenia się na około 5,6% (pomiędzy 0 17%) (tabela 8.4) Z niejasnych przyczyn odsetek przeżywalności w ciągu ostatnich 5 lat uległ poprawie w stosunku do przytaczanego uprzednio. Wśród pacjentów, którzy przeżyli urazowe zatrzymanie krążenia (Traumatic Cardiorespiratory Arrest TCRA) i na temat których dostępne są dane, pomyślny wynik neurologiczny stwierdza się tylko u 1,6%. Wstrząśnienie serca Wstrząśnieniem serca określa się sytuację, w której doszło lub niemal doszło do zatrzymania krążenia spowodowanego tępym urazem klatki piersiowej w okolicy serca Uderzenie, do którego dochodzi w fazie ranliwej cyklu mięśnia sercowego, może spowodować zagrażające życiu zaburzenia rytmu (zwykle VF). Do wstrząśnienia serca często dochodzi podczas uprawiania sportów (zwykle baseball) lub w czasie rekreacji, a poszkodowanymi są zwykle młodzi mężczyźni (średni wiek 14 lat). Przeżywalność w przypadku wstrząśnienia serca oceniana jest na około 15% i wzrasta do 25%, jeżeli zabiegi resuscytacyjne zostaną podjęte w ciągu 3 minut 651. Oznaki życia i początkowa aktywność elektryczna serca Nie ma pewnych rokowniczo objawów świadczących o szansach przeżycia pacjenta z urazowym zatrzymaniem krążenia. W jednym z badań stwierdzono, że obecność reakcji źrenic na światło oraz rytmu zatokowego znacząco koreluje z większą szansą przeżycia 652. W badaniu dotyczącym pacjentów z urazem penetrującym reagujące na światło źrenice, aktywność oddechowa i rytm zatokowy korelowały z przeżywalnością, ale często były niewiarygodne 646. Trzy badania potwierdziły brak przeżycia pacjentów, u których stwierdzono w zapisie rytm agonalny lub asystolię 642,646,653. W innym badaniu stwierdzono brak przeżyć pacjentów z PEA w przebiegu tępego urazu 654. Opierając się na tych badaniach American College of Surgeons i National Association of EMS Physicians opracowały wytyczne dotyczące sytuacji, w których nie należy podejmować resuscytacji 655. Leczenie Przeżywalność w urazowym zatrzymaniu krążenia jest ściśle powiązana z czasem trwania fazy przedszpitalnej oraz resuscytacji krążeniowo-oddechowej 644, Na miejscu zdarzenia powinno się podejmować tylko procedury ratujące życie, a jeśli u pacjenta stwierdza się oznaki życia, należy go natychmiast przewieźć do najbliższego właściwego szpitala. W wybranych przypadkach można rozważyć wykonanie torakotomii na miejscu zdarzenia 661,662. Nie wolno opóźniać działań poprzez wykonywanie procedur o nieudowodnionym wpływie na przeżywalność, takich jak 1
54 56 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 unieruchomienie kręgosłupa szyjnego 663. Należy leczyć odwracalne przyczyny zatrzymania krążenia: hipoksemia (natlenowanie, wentylacja), krwotok, który można zatamować uciskiem (ucisk, opatrunki uciskowe, opaski uciskowe, nowoczesne środki hemostatyczne), krwotok, którego nie można zatamować uciskiem (szyny, dożylna płynoterapia), odma prężna (odbarczenie), tamponada osierdzia (natychmiastowa torakotomia). Uciskanie klatki piersiowej może być nieskuteczne u pacjentów z zatrzymaniem krążenia w przebiegu hipowolemii, ale większość osób, które przeżyły uraz, nie mają hipowolemii i w tej podgrupie standardowe zaawansowane zabiegi resuscytacyjne mogą okazać się ratującymi życie. Standardowa RKO nie powinna opóźnić leczenia odwracalnych przyczyn zatrzymania krążenia (np. torakotomia w przypadku tamponady osierdzia). Torakotomia ratunkowa Wykonanie torakotomii ratunkowej może być konieczne u niektórych pacjentów z zatrzymaniem krążenia współistniejącym z urazem penetrującym, jeśli lekarze będący na miejscu zdarzenia posiadają odpowiednie umiejętności. Torakotomię w warunkach oddziału ratunkowego najlepiej stosować u pacjentów z penetrującymi ranami serca, którzy trafili do centrum urazowego krótko po urazie, a u których obserwuje się oznaki życia lub aktywność elektryczną mięśnia sercowego (szacowana przeżywalność około 31%) 664. W przypadku urazów tępych torakotomia w warunkach oddziału ratunkowego powinna być ograniczona do pacjentów z oznakami życia w chwili przyjazdu i zauważonym zatrzymaniem krążenia (szacowana przeżywalność około 1,6%). Ultrasonografia Ultrasonografia jest skutecznym narzędziem w ocenie poszkodowanych urazowych w stanach zagrożenia życia. Umożliwia pewne stwierdzenie obecności krwi w jamie otrzewnej, opłucnej i odmy opłucnej oraz tamponady osierdzia. Rozpoznania te mogą być postawione w ciągu kilku minut, nawet w okresie przedszpitalnym 665. Dostępne są obecnie aparaty USG umożliwiające diagnostykę w warunkach pomocy przedszpitalnej. Ich znaczenie nie zostało dotychczas udowodnione 666. Zatrzymanie krążenia w przebiegu ciąży Zgony związane z ciążą w krajach rozwiniętych są stosunkowo rzadkie, ich częstość wynosi około 1 na porodów 667. Jeżeli u ciężarnej obserwuje się zaburzenia sercowo-naczyniowe, trzeba zawsze także myśleć o płodzie. Opracowując wytyczne dotyczące resuscytacji pacjentek w ciąży, opierano się głównie na opisanych w literaturze naukowej seriach przypadków klinicznych, ekstrapolacji danych z zatrzymań krążenia u kobiet niebędących w ciąży, badaniach na manekinach oraz opiniach ekspertów opartych na fizjologii ciąży oraz zmianach, jakie zachodzą w czasie fizjologicznego porodu. Większość prac naukowych dotyczy krajów rozwiniętych, podczas gdy do zatrzymań krążenia znacznie częściej dochodzi w krajach rozwijających się. W roku 2008 zanotowano na świecie przypadków śmierci u matek (śmierć w trakcie ciąży, podczas porodu lub w okresie 42 dni po porodzie) 668. Przyczyny zatrzymania krążenia u kobiety ciężarnej obejmują: chorobę serca, zatorowość płucną, zaburzenia psychiczne, chorobę nadciśnieniową rozwijającą się w przebiegu ciąży, sepsę, krwotok, zator wodami płodowymi, ciążę pozamaciczną 669. Do zatrzymania krążenia u kobiety ciężarnej może także dojść z tych samych powodów, niezwiązanych z ciążą, co u każdej kobiety w podobnym wieku. Modyfikacje wytycznych BLS Powyżej 20. tygodnia ciąży powiększona macica może uciskać żyłę główną dolną i aortę, powodując zmniejszenie powrotu żylnego i rzutu serca. Efektem tego może być poprzedzający zatrzymanie krążenia spadek ciśnienia lub wstrząs, co u pacjentek w krytycznym stanie może przyśpieszyć wystąpienie zatrzymania krążenia 670,671. Podczas resuscytacji zmniejszenie powrotu żylnego i rzutu serca spowodowane przez powiększoną macicę ogranicza skuteczność wykonywanych uciśnięć klatki piersiowej. Kluczowe elementy BLS u kobiety ciężarnej są następujące: Wczesne wezwanie pomocy specjalisty (włącznie z położnikiem i neonatologiem). Rozpoczęcie podstawowych zabiegów resuscytacyjnych zgodnie ze standardowymi wytycznymi, zapewnienie dobrej jakości uciśnięć klatki piersiowej z minimalizowaniem przerw podczas resuscytacji. Ręczne przesunięcie macicy na lewą stronę w celu zniwelowania nacisku na żyłę główną dolną. Jeśli to możliwe, dodatkowe przechylenie kobiety ciężarnej na lewy bok, jednak nieznany jest optymalny kąt nachylenia. Celem jest utrzymanie kąta pomiędzy 15 a 30 stopni. Niezbędne jest, aby zastosowany kąt przechylenia umożliwiał prowadzenie dobrej jakości uciśnięć klatki piersiowej i jeśli to konieczne, wykonanie cesarskiego cięcia w celu wydobycia płodu (patrz niżej). Modyfikacje zaawansowanych zabiegów resuscytacyjnych U ciężarnych pacjentek napięcie dolnego zwieracza przełyku jest niższe, czego efektem jest wzrost ryzyka aspiracji treści pokarmowej do płuc. Wczesna intubacja dotchawicza z właściwie wykonanym uciskiem na chrząstkę pierścieniowatą zmniejsza to ryzyko. Intubacja ułatwia także prowadzenie wentylacji u pacjentek ze zwiększonym ciśnieniem wewnątrz jamy brzusznej. Może okazać się konieczne użycie rurki intubacyjnej o średnicy 0,5 1 mm mniejszej od normalnie stosowanej u pacjentki niebędącej w ciąży. Wynika to z faktu, iż drogi oddechowe kobiety ciężarnej ulegają zwężeniu z powodu obrzęku 672. Opór klatki piersiowej w czasie ciąży nie zmienia się, co sugeruje zastosowanie standardowych energii w celu wykonania defibrylacji 673. W trakcie prowadzenia resuscytacji ratownicy powinni podjąć próbę identyfikacji typowych odwracalnych przyczyn zatrzymania krążenia związanych z ciążą. Pomocne jest wykorzystanie w tym celu schematu 4 H i 4 T. U pacjentek w ciąży występują te same czynniki ryzyka zatrzymania krążenia, co u innych osób w tej samej grupie wiekowej (np. anafilaksja, zatrucie lekami, urazy). Należy rozważyć
55 Podsumowanie Komitetu Wykonawczego ERC 57 wykonanie przez doświadczonego ultrasonografistę badania USG jamy brzusznej w celu stwierdzenia ciąży i ewentualnej identyfikacji przyczyny zatrzymania krążenia w jej przebiegu. Badanie to nie powinno jednak opóźniać właściwego leczenia. Postępowanie w przypadku nieskuteczności natychmiastowo podjętej resuscytacji U kobiety ciężarnej w momencie zatrzymania krążenia należy rozważyć natychmiastowe wykonanie histerotomii lub cięcia cesarskiego. W niektórych przypadkach szybkie podjęcie resuscytacji może przywrócić rytm perfuzyjny i jeśli są to początkowe tygodnie ciąży, umożliwić kontynuowanie ciąży aż do terminu porodu. Kiedy wstępne działania resuscytacyjne zawiodą, wydobycie płodu może zwiększyć szansę skutecznej resuscytacji zarówno dziecka jak i matki W przypadku wieku płodu <20. tygodnia ciąży nie ma konieczności wykonania cięcia cesarskiego, ponieważ takiej wielkości macica raczej nie powoduje znaczącego ograniczenia rzutu serca u matki. W przypadku wieku płodu około tygodnia ciąży należy wykonać ratunkową histerotomię, aby umożliwić skuteczną resuscytację matki, a nie przeżycie wydobytego dziecka, gdyż jest to mało prawdopodobne w tym wieku ciążowym. W przypadku wieku płodu równym lub większym od tygodnia ciąży, należy wykonać ratunkową histerotomię w celu ratowania życia zarówno matki, jak i płodu. Najwyższą przeżywalność w przypadku płodów w wieku powyżej tygodnia ciąży można uzyskać, jeżeli wydobycie dziecka nastąpi w ciągu 5 minut od chwili zatrzymania krążenia u matki. Wymaga to rozpoczęcia wykonywania histerotomii w ciągu około 4 minut od chwili zatrzymania krążenia. Porażenie prądem Urazy spowodowane porażeniem prądem są stosunkowo rzadkie i odpowiadają za 0,54 przypadków zgonów na osób rocznie. Mogą one jednak potencjalnie prowadzić do wielonarządowych obrażeń z wysoką chorobowością i śmiertelnością. Do większości porażeń prądem wśród dorosłych dochodzi w pracy i są one związane z narażeniem na energię elektryczną o wysokim napięciu. Wśród dzieci ryzyko to głównie związane jest z domową instalacją elektryczną i prądem o niższym napięciu (220 V w Europie, Australii i Azji, 110 V w USA i Kanadzie) 677. Porażenie piorunem jest rzadkim przypadkiem i odpowiada za 1000 zgonów rocznie na całym świecie 678. Urazy spowodowane porażeniem prądem powstają w wyniku bezpośredniego działania energii elektrycznej na błony komórkowe i mięśniówkę gładką naczyń. Zatrzymanie oddechu może być spowodowane porażeniem ośrodka oddechowego lub mięśni oddechowych. Jeżeli prąd zmienny przepłynie przez miokardium będące w fazie ranliwej (analogicznie do zjawiska R na T), może wywołać migotanie komór (VF) 679. Prąd elektryczny może także odpowiadać za niedokrwienie mięśnia sercowego spowodowane skurczem naczyń wieńcowych. Asystolia może wystąpić jako pierwotny mechanizm zatrzymania krążenia lub wtórnie do asfiksji spowodowanej zatrzymaniem oddechu. Porażenie piorunem jest wyładowaniem energii elektrycznej o napięciu dochodzącym do 300 kv, którego czas trwania wynosi kilka milisekund. U osób, które przeżyły moment porażenia piorunem, może dochodzić do wyrzutu dużej ilości amin katecholowych lub pobudzenia układu współczulnego, co prowadzi do nadciśnienia, tachykardii, niespecyficznych zmian w EKG (obejmujących wydłużenie odstępu QT i przejściowe odwrócenia załamka T) oraz martwicy mięśnia sercowego. Śmiertelność spowodowana porażeniem piorunem dochodzi do 30%, a u 70% pacjentów, którzy przeżyli, stwierdza się znacząco zwiększoną chorobowość Resuscytacja Należy upewnić się, że wszystkie źródła prądu są wyłączone, a do poszkodowanego nie należy podchodzić, dopóki nie jest bezpiecznie. Należy bezzwłocznie rozpocząć standardowe podstawowe i zaawansowane zabiegi resuscytacyjne. Udrożnienie dróg oddechowych może być trudne, jeżeli doszło do oparzenia elektrycznego twarzy lub szyi. W takich sytuacjach konieczne jest wczesne wykonanie intubacji dotchawiczej, ponieważ narastający szybko obrzęk tkanek miękkich może doprowadzić do niedrożności dróg oddechowych. W wyniku porażenia prądem może dojść do urazów głowy i kręgosłupa. Należy unieruchomić pacjenta do momentu przeprowadzenia badania. Porażenie mięśni, zwłaszcza wywołane działaniem prądu o wysokim napięciu, może trwać nawet kilka godzin 681. W tym okresie konieczne jest wspomaganie wentylacji. VF jest najczęstszym mechanizmem zatrzymania krążenia, do którego dochodzi w wyniku porażenia prądem zmiennym o wysokim napięciu. Leczenie polega na szybkim wykonaniu defibrylacji. Asystolia występuje częściej po porażeniu prądem stałym. W przypadku zaburzeń rytmu należy stosować standardowe protokoły postępowania. Należy usunąć tlące się ubrania i buty, aby zapobiec dalszym urazom termicznym. Intensywna płynoterapia jest niezbędna w przypadkach znacznego uszkodzenia tkanek. Należy utrzymać prawidłową diurezę w celu umożliwienia usunięcia z organizmu mioglobiny, potasu i innych substancji pochodzących ze zniszczonych tkanek 683. Należy rozważyć wczesną interwencję chirurgiczną u pacjentów z ciężkimi oparzeniami. W przypadku podejrzenia urazu głowy lub kręgosłupa konieczne jest zapewnienie unieruchomienia pacjenta 684,685. Należy przeprowadzić ponowne badanie pacjenta w celu wykluczenia urazów spowodowanych skurczem tężcowym mięśni szkieletowych lub odrzuceniem poszkodowanego od źródła prądu 685,686. Porażenie prądem może spowodować ciężki uraz głębiej położonych tkanek miękkich przy jednoczesnym stosunkowo niewielkim uszkodzeniu skóry. Ponieważ prąd przemieszcza się wzdłuż pęczków naczyniowo- 1
56 58 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 -nerwowych, należy uważnie obserwować pacjenta pod kątem wystąpienia wczesnych objawów zespołu przedziałowego (compartment syndrome), a w przypadku jego pojawienia się wykonać wcześnie fasciotomię. Zasady edukacji w resuscytacji Przeżywalność w nagłym zatrzymaniu krążenia zależy od jakości dowodów naukowych leżących u podstaw wytycznych, efektywności nauczania i środków przeznaczonych na implementację wytycznych 687. Dodatkowym czynnikiem jest chęć wdrażania wytycznych do praktyki klinicznej i wpływ czynnika ludzkiego na przekształcanie teorii w praktykę 688. Implementacja Wytycznych 2010 ma większe szanse powodzenia pod warunkiem starannego planowania i całościowej strategii wprowadzania, obejmującej także edukację. Jako przyczyny w opóźnieniu wdrażania Wytycznych 2005 uważa się opóźnienia w dostarczaniu materiałów edukacyjnych i umożliwianiu personelowi udziału w szkoleniach Kluczowe zalecenia edukacyjne Kluczowe kwestie zidentyfikowane przez zespół ds. edukacji, implementacji i zespołów ILCOR podczas procesu oceny dowodów naukowych Wytycznych 2010 są następujące 19 : Metody nauczania powinny podlegać ocenie w celu upewnienia się, że ich zastosowanie pozwala niezawodnie spełnić postawione zadania. Celem jest upewnienie się, czy osoby uczestniczące w szkoleniu przyswajają i zapamiętują wiedzę oraz praktyczne umiejętności w stopniu, który pozwoli im działać prawidłowo w trakcie rzeczywistych zatrzymań krążenia i wpłynie na poprawę wyników końcowych. Krótkie kursy samokształcące video czy komputerowe z minimalnym udziałem lub bez udziału instruktora, połączone z praktycznym ćwiczeniem umiejętności, mogą stanowić efektywną alternatywę dla opartych na pracy instruktora kursów podstawowych zabiegów resuscytacyjnych (resuscytacja krążeniowo-oddechowa [RKO] i automatyczna defibrylacja zewnętrzna [AED]). Idealnie byłoby przeszkolić wszystkich obywateli z zakresu typowej RKO, obejmującej uciśnięcia klatki piersiowej i wentylację. W niektórych okolicznościach dopuszczalne jest nauczanie RKO z wyłącznym uciskaniem klatki piersiowej (np. okazyjne, krótkie szkolenia). Osoby przeszkolone w zakresie wykonywania RKO z wyłącznym uciskaniem klatki piersiowej należy zachęcać do uczenia się typowej RKO. Wiedza i umiejętności z zakresu podstawowych i zaawansowanych zabiegów resuscytacyjnych zanikają w krótkim czasie 3 6 miesięcy. Częste powtarzanie oceny pomoże zidentyfikować te osoby, które wymagają szkoleń przypominających w celu utrzymania wiedzy i umiejętności. Urządzenia, dające instrukcje lub informacje zwrotne o jakości wykonywanej RKO, poprawiają przyswajanie i zapamiętywanie wiedzy z tego zakresu i powinny być stosowane podczas szkoleń zarówno osób niezwiązanych zawodowo z medycyną, jak i personelu medycznego. Zwiększony nacisk na dodatkowe, pozatechniczne umiejętności (Non-technical Skills NTS), jak kierowanie zespołem, praca zespołu, podział obowiązków i umiejętność prawidłowego komunikowania się, pomoże poprawić jakość wykonywania RKO i opiekę nad pacjentem. Należy przeprowadzać odprawy dla zespołów, których celem jest planowanie przebiegu resuscytacji (briefing), oraz spotkania, w trakcie których omawiane są czynności wykonywane podczas symulowanych bądź rzeczywistych resuscytacji (debriefing). Spotkania takie mają na celu pomoc w poprawie zarówno pracy całych zespołów, jak i umiejętności ich poszczególnych członków. Badania na temat wpływu szkoleń z zakresu resuscytacji na wyniki leczenia pacjentów są ograniczone. Chociaż badania z wykorzystaniem manekinów są przydatne, należy zachęcać do badań oceniających wpływ metod nauczania na rzeczywiste wyniki leczenia pacjentów. Kogo i jak szkolić W sytuacji idealnej wszyscy obywatele powinni posiadać wiedzę z zakresu RKO. Nie ma dowodów naukowych przemawiających za lub przeciw szkoleniom osób z populacji wysokiego ryzyka. Jednakże szkolenie może zmniejszyć lęk u pacjenta i członków jego rodziny, poprawić emocjonalną adaptację i spowodować, że ktoś będzie w stanie rozpocząć RKO 19. Populacja wymagająca szkoleń obejmuje osoby bez wykształcenia medycznego, pełniące jednak funkcje społeczne nakładające na nie obowiązek udzielania pomocy (np. ratownicy WOPR, osoby udzielające pierwszej pomocy w zakładach pracy), jak również personel medyczny różnych szczebli systemu ochrony zdrowia pracujący w przychodniach, pomocy doraźnej, ogólnych oddziałach szpitalnych czy oddziałach intensywnej terapii. Szkolenia powinny być dostosowane do potrzeb różnych grup osób szkolących się, a styl nauczania powinien zapewnić przyswajanie oraz zapamiętywanie wiedzy i umiejętności praktycznych. Osoby często wykonujące RKO (będące niejako ekspertami w tej dziedzinie) powinny znać aktualne wytyczne i umieć efektywnie je zastosowywać, działając w zespole wielospecjalistycznym. Takim osobom potrzebne jest bardziej kompleksowe szkolenie, obejmujące zarówno merytoryczne, jak i pozamerytoryczne umiejętności (np. praca w zespole, kierowanie zespołem, efektywna komunikacja) 691,692. Poziomy kształcenia zostały arbitralnie podzielone na podstawowy i zaawansowany, chociaż tak naprawdę stanowią one kontinuum. Poziom podstawowy i szkolenia z zakresu użycia AED RKO prowadzona przez świadków zdarzenia i wczesna defibrylacja ratują życie. Wiele czynników zmniejsza chęć świadków zdarzenia do podejmowania RKO, między innymi panika, strach przed zakażeniem, możliwość wyrządzenia krzywdy osobie poszkodowanej lub strach przed nieprawidłowo wykonywaną RKO Szkolenia osób niezwiązanych zawodowo z medycyną zwiększają ich chęć podejmowania RKO 696, , Szkolenie z zakresu RKO i wykonywanie RKO podczas zatrzymania krążenia jest w większości przypadków bezpieczne. Osoby zamie-
57 Podsumowanie Komitetu Wykonawczego ERC 59 rzające odbyć szkolenie z RKO powinny być informowane o charakterze i zakresie aktywności fizycznej wymaganej w programie szkolenia. Osoby uczące się, u których podczas szkolenia wystąpią znaczące objawy (np. ból w klatce piersiowej, silna duszność), powinny je przerwać. Ratownicy, u których wystąpią znaczące objawy podczas RKO, powinni rozważyć zaprzestanie resuscytacji (dodatkowe informacje o ryzyku dla ratownika znajdują się w wytycznych BLS) 4. Program kursu podstawowych zabiegów resuscytacyjnych i AED Program kursu BLS-AED powinien być dostosowany do docelowej grupy odbiorców i możliwie prosty. Program ten powinien obejmować następujące kluczowe elementy 13,19 : Czynniki ryzyka związane ze środowiskiem i poszkodowanym w trakcie wykonywania RKO. Rozpoznanie zatrzymania krążenia na podstawie oceny przytomności, udrożnienia dróg oddechowych i oceny oddechu 4,13. Rozpoznanie westchnięć (gasping) lub nieprawidłowych oddechów jako oznak zatrzymania krążenia u nieprzytomnej, niereagującej osoby 69,715. Dobrej jakości uciśnięcia klatki piersiowej (włączając częstość, głębokość, pełną relaksację klatki piersiowej i minimalizowanie przerw w uciskaniu) oraz oddechy ratownicze. Zwrotna informacja i instrukcje (również z odpowiednich urządzeń) powinny być stosowane w celu lepszego przyswajania i zapamiętywania umiejętności praktycznych podczas szkoleń z zakresu podstawowych zabiegów resuscytacyjnych 716. Wszystkie kursy BLS i AED powinny mieć na celu nauczanie standardowej RKO, włączając oddechy ratownicze/wentylację. W niektórych szczególnych sytuacjach nauczanie RKO z wyłącznym uciskaniem klatki piersiowej ma potencjalną przewagę nad nauczeniem standardowego RKO 694,699,702,707,708,711,717,718. Zalecane podejście do nauczania RKO opisano poniżej. Nauczanie standardowej RKO w porównaniu z wykonywaniem RKO z wyłącznym uciskaniem klatki piersiowej Istnieją kontrowersje, jakich umiejętności z zakresu RKO powinno się uczyć różne grupy ratowników. Uczenie RKO z wyłącznym uciskaniem klatki piersiowej jest prostsze i szybsze, szczególnie gdy szkolenie dotyczy dużej liczby osób, które prawdopodobnie nie będą miały dostępu do szkoleń z zakresu standardowej RKO. W wielu sytuacjach RKO obejmująca uciśnięcia klatki piersiowej i oddechy ratownicze jest lepsza, np. u dzieci 84 w zatrzymaniach krążenia w asfiksji lub kiedy RKO, wykonywana przez przypadkowego świadka, trwa dłużej niż kilka minut 13. Stąd zalecane jest uproszczone podejście do nauczania w oparciu o następujące zasady edukacyjne: Optymalnie wszyscy obywatele powinni być uczeni umiejętności standardowej RKO (uciśnięcia i wentylacja w stosunku 30 : 2). Jeżeli szkolenie odbywa się w ograniczonym czasie lub w szczególnych okolicznościach (np. telefoniczne instruowanie świadka zdarzenia przez dyspozytora pogotowia, zdarzenia masowe, kampanie publiczne, wideo na portalach internetowych, np. YouTube, osoby, które nie chcą być szkolone), powinno koncentrować się na wykonywaniu RKO z wyłącznym uciskaniem klatki piersiowej. Osoby przeszkolone w wykonywaniu RKO z wyłącznym uciskaniem klatki piersiowej w trakcie kolejnego szkolenia powinny uczyć się zarówno uciśnięć klatki piersiowej, jak i wentylacji. Optymalnie takie osoby powinno się szkolić w wykonywaniu RKO z wyłącznym uciskaniem klatki piersiowej, a następnie zaoferować szkolenie obejmujące uciskanie klatki piersiowej i wentylacje podczas tej samej sesji. Osoby niezwiązane zawodowo z medycyną, ale mające obowiązek udzielania pomocy, takie jak policjanci, strażacy, pracownicy ochrony, osoby opiekujące się dziećmi, powinny uczyć się wykonywania uciśnięć klatki piersiowej i wentylacji. W przypadku dzieci należy zachęcać ratowników, aby zastosowali jakąkolwiek znaną sobie sekwencję uciśnięć klatki piersiowej i wentylacji stosowaną u dorosłych, ponieważ wyniki końcowe są gorsze, jeśli nie podejmuje się RKO w ogóle. Osoby niebędące specjalistami, które chcą się szkolić z zakresu resuscytacji dzieci z racji odpowiedzialności za ich zdrowie (np. rodzice, nauczyciele, pielęgniarki szkolne, ratownicy itp.), powinni być uczeni, że zaleca się modyfikację podstawowych zabiegów resuscytacyjnych stosowanych u dorosłych tzn. wykonanie najpierw pięciu oddechów ratowniczych, a następnie prowadzenie RKO przez około jedną minutę przed udaniem się po pomoc, jeżeli nie ma nikogo, kto mógłby ją wcześniej wezwać. Głębokość uciśnięć klatki piersiowej u dzieci stanowi co najmniej 1/3 przednio-tylnego wymiaru klatki piersiowej 8. Uczenie obywateli prowadzenia RKO powinno być szeroko promowane. Jednakże brak przeszkolenia nie powinien stanowić przeszkody w wykonywaniu RKO z wyłącznym uciskaniem klatki piersiowej, które najlepiej wykonywać z telefonicznym instruktażem dyspozytora. Metody kształcenia z zakresu BLS i AED Istnienie wiele metod stosowanych w trakcie uczenia podstawowych zabiegów resuscytacyjnych i AED. Najczęściej stosowaną metodą są tradycyjne kursy, prowadzone przez instruktorów 719. Porównanie metod nauczania podstawowych zabiegów resuscytacyjnych i AED osób niezwiązanych zawodowo z medycyną oraz personelu medycznego wykazało, że dobrze opracowane programy samokształcenia (np. video, DVD, komputerowe) z minimalnym udziałem lub bez udziału instruktora mogą stanowić skuteczną alternatywę kursów prowadzonych przez instruktora Jest konieczne, aby program kursów zawierał zajęcia praktyczne z uciśnięć klatki piersiowej i zastosowania AED. W trakcie szkoleń dla laików i pracowników ochrony zdrowia można rozważyć użycie urządzeń dających informacje zwrotną lub instrukcje głosowe w czasie RKO
58 60 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 Czas trwania i częstotliwość powtarzania kursów podstawowych zabiegów resuscytacyjnych i AED prowadzonych przez instruktorów Nie określono optymalnego czasu trwania kursów podstawowych zabiegów resuscytacyjnych i AED prowadzonych przez instruktorów. Prawdopodobnie będzie on różny w zależności od charakterystyki uczestników (np. laicy czy pracownicy ochrony zdrowia; wiek), programu, stosunku ilości instruktorów do uczestników, czasu przeznaczonego na ćwiczenia praktyczne i sposobu oceny końcowej. Większość badań wykazała, że praktyczne umiejętności z zakresu RKO, takie jak wzywanie pomocy, uciskanie klatki piersiowej i wentylacja, zanikają w czasie od 3 do 6 miesięcy od odbycia szkolenia 722, 725, Umiejętności związane z zastosowaniem AED są zachowywane dłużej niż te potrzebne do prowadzenia wyłącznie podstawowych zabiegów resuscytacyjnych 736, 741, 742. Szkolenia zaawansowane Program kursów zaawansowanych Kursy na poziomie zaawansowanym są zwykle przeznaczone dla pracowników ochrony zdrowia. Program kursu powinien być dostosowany do indywidualnych potrzeb osób szkolących się, obejmować różne przypadki kliniczne oraz uwzględniać rolę, jaką mogą pełnić szkolący się pracownicy ochrony zdrowia w czasie zatrzymania krążenia. Szkolenie zespołów i umiejętność rozpoznawania rytmów serca będą konieczne, by zminimalizować przerwy w uciśnięciach klatki piersiowej podczas stosowania strategii defibrylacji manualnej wg Wytycznych 2010, która zakłada ładowanie łyżek podczas wykonywania uciśnięć klatki piersiowej 117, 743. Kluczowymi elementami programów nauczania zaawansowanych zabiegów resuscytacyjnych powinny być: Prewencja zatrzymania krążenia 192, 744. Dobrej jakości uciśnięcia klatki piersiowej z uwzględnieniem prawidłowej częstości, głębokości, pełnej relaksacji klatki piersiowej i minimalizacji przerw oraz wentylacja z wykorzystaniem podstawowych umiejętności (np. maska kieszonkowa, worek samorozprężalny z maską twarzową). Defibrylacja z uwzględnieniem ładowania w trakcie wykonywania uciśnięć klatki piersiowej w przypadku manualnych defibrylatorów. Algorytmy zaawansowanych zabiegów resuscytacyjnych. Umiejętności pozatechniczne (np. kierowanie zespołem, praca w zespole, komunikacja). Metody kształcenia w trakcie szkoleń zaawansowanych Można zastosować różne metody, aby przygotować uczestników, zanim wezmą udział w szkoleniu (takie jak przeczytanie podręcznika, pre-test i e-learning) Symulacja i realistyczne techniki szkolenia Szkolenia oparte na symulacji są kluczową częścią nauczania resuscytacji. Istnieje jednak wiele wariantów sposobów, w jaki można i jak stosuje się symulację w nauczaniu resuscytacji 754. Brak spójnej definicji utrudnia porównanie badań dotyczących różnego typu szkoleń symulacyjnych (np. symulacja z wysokim [high fidelity] w porównaniu z niskim stopniem realizmu [low fidelity]). Odstępy czasowe między szkoleniami z zaawansowanych zabiegów resuscytacyjnych Wiedza i umiejętności praktyczne po wstępnym szkoleniu z zakresu resuscytacji szybko zanikają. Aby utrzymać wiedzę i umiejętności niezmienione, potrzebne są szkolenia przypominające, jednakże ich optymalna częstotliwość nie została określona. Większość badań wskazuje, że wiedza i umiejętności z zakresu zaawansowanych zabiegów resuscytacyjnych zanikają, jeżeli są oceniane po 3 do 6 miesiącach od szkolenia 737, , dwa badania sugerowały okres 7 do 12 miesięcy 763,764, a jedno 18 miesięcy 765. Etyczne zagadnienia resuscytacji i problemy końca życia Wiele czynników i okoliczności trzeba wziąć pod uwagę, decydując o podjęciu lub niepodejmowaniu resuscytacji, gdyż musimy być pewni, że pacjent jest traktowany z godnością. Decyzje te są skomplikowane oraz kompleksowe i muszą uwzględniać uwarunkowania indywidualne, międzynarodowe, lokalne, kulturowe, prawne, tradycyjne, religijne, socjalne i ekonomiczne 766. Wytyczne resuscytacji 2010 omawiają następujące zagadnienia związane z etyką i decyzjami końca życia: Kluczowe zasady etyczne. Nagłe zatrzymanie krążenia w perspektywie globalnej. Wyniki odległe leczenia i prognozowanie wyników leczenia. Kiedy rozpoczynać i kiedy kończyć resuscytację. Wyrażenie woli (advance directives) i niepodejmowanie resuscytacji (DNAR). Obecność rodziny w czasie resuscytacji. Donacja i pobieranie organów do przeszczepu. Badania w dziedzinie resuscytacji i świadoma zgoda. Badania i szkolenie na zwłokach. Bibliografia 1. Nolan J. European Resuscitation Council Guidelines for resuscitation Section 1. Introduction. Resuscitation 2005;67(Suppl. 1):S Nolan JP, Hazinski MF, Billi JE, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 1. Executive Summary. Resuscitation; doi: /j.res uscitation , in press. 3. Nolan JP, Neumar RW, Adrie C, et al. Post-cardiac arrest syndrome: epidemiology, pathophysiology, treatment, and prognostication. A Scientific Statement from the International Liaison Committee on Resuscitation; the American Heart Association Emergency Cardiovascular Care Committee; the Council on Cardiovascular Surgery and Anesthesia; the Council on Cardiopulmonary, Perioperative, and Critical Care; the Council on Clinical Cardiology; the Council on Stroke. Resuscitation 2008;79: Koster RW, Baubin MA, Caballero A, et al. European Resuscitation Council Guidelines for Resuscitation Section 2. Adult basic life support and use of automated external defibrillators. Resuscitation 2010;81: Deakin CD, Nolan JP, Sunde K, Koster RW. European Resuscitation Council Guidelines for Resuscitation Section 3. Electrical therapies: automated external defibrillators, defibrillation, cardioversion and pacing. Resuscitation 2010;81: Deakin CD, Nolan JP, Soar J, et al. European Resuscitation Council Guidelines for Resuscitation Section 4. Adult advanced life support. Resuscitation 2010;81:
59 Podsumowanie Komitetu Wykonawczego ERC Arntz HR, Bossaert L, Danchin N, Nikolaou N. European Resuscitation Council Guidelines for Resuscitation Section 5. Initial management of acute coronary syndromes. Resuscitation 2010;81: Biarent D, Bingham R, Eich C, et al. European Resuscitation Council Guidelines for Resuscitation Section 6. Paediatric life support. Resuscitation 2010;81: Wyllie J, Richmond S. European Resuscitation Council Guidelines for Resuscitation Section 7. Resuscitation of babies at birth. Resuscitation 2010;81: Soar J, Perkins GD, Abbas G, et al. European Resuscitation Council Guidelines for Resuscitation Section 8. Cardiac arrest in special circumstances: electrolyte abnormalities, poisoning, drowning, accidental hypothermia, hyperthermia, asthma, anaphylaxis, cardiac surgery, trauma, pregnancy, electrocution. Resuscitation 2010;81: Soar J, Monsieurs KG, Ballance J, et al. European Resuscitation Council Guidelines for Resuscitation. Section 9. Principles of education in resuscitation. Resuscitation 2010;81: Lippert FK, Raffay V, Georgiou M, Steen PA, Bossaert L. European Resuscitation Council Guidelines for Resuscitation Section 10. The ethics of resuscitation and end-of-life decisions. Resuscitation 2010;81: Koster RW, Sayre MR, Botha M, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 5. Adult basic life support. Resuscitation; doi: /j.resuscitation , in press. 14. Sunde K, Jacobs I, Deakin CD, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 6. Defibrillation. Resuscitation; doi: /j.resuscitat ion , in press. 15. Deakin CD, Morrison LJ, Morley PT, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 8. Advanced life support. Resuscitation; doi: /j.resuscitation , in press. 16. Bossaert L, O Connor RE, Arntz H-R, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 9. Acute coronary syndromes. Resuscitation; doi: /j.resuscitation , in press. 17. de Caen AR, Kleinman ME, Chameides L, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 10. Pediatric basic and advanced life support. Resuscitation; doi: /j.resuscitation , in press. 18. Wyllie J, Perlman JM, Kattwinkel J, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 11. Neonatal resuscitation. Resuscitation; doi: /j.resuscitation , in press. 19. Soar J, Mancini ME, Bhanji F, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 12. Education, implementation, and teams. Resuscitation; doi: /j.resuscitation , in press. 20. Murray CJ, Lopez AD. Mortality by cause for eight regions of the world: global burden of disease study. Lancet 1997;349: Sans S, Kesteloot H, Kromhout D. The burden of cardiovascular diseases mortality in Europe. Task force of the European Society of Cardiology on cardiovascular mortality and morbidity statistics in Europe. Eur Heart J 1997;18: Zheng ZJ, Croft JB, Giles WH, Mensah GA. Sudden cardiac death in the United States, 1989 to Circulation 2001;104: a. Atwood C, Eisenberg MS, Herlitz J, Rea TD. Incidence of EMS-treated out-ofhospital cardiac arrest in Europe. Resuscitation 2005;67: Nichol G, Thomas E, Callaway CW, et al. Regional variation in out-of-hospital cardiac arrest incidence and outcome. JAMA 2008;300: Hollenberg J, Herlitz J, Lindqvist J, et al. Improved survival after out-of-hospital cardiac arrest is associated with an increase in proportion of emergency crew witnessed cases and bystander cardiopulmonary resuscitation. Circulation 2008;118: Iwami T, Nichol G, Hiraide A, et al. Continuous improvements in chain of survival increased survival after out-of-hospital cardiac arrests: a large-scale population-based study. Circulation 2009;119: Cobb LA, Fahrenbruch CE, Olsufka M, Copass MK. Changing incidence of out-of-hospital ventricular fibrillation, JAMA 2002;288: Rea TD, Pearce RM, Raghunathan TE, et al. Incidence of out-of-hospital cardiac arrest. Am J Cardiol 2004;93: Vaillancourt C, Verma A, Trickett J, et al. Evaluating the effectiveness of dispatch-assisted cardiopulmonary resuscitation instructions. Acad Emerg Med 2007;14: Agarwal DA, Hess EP, Atkinson EJ, White RD. Ventricular fibrillation in Rochester, Minnesota: experience over 18 years. Resuscitation 2009;80: Ringh M, Herlitz J, Hollenberg J, Rosenqvist M, Svensson L. Out of hospital cardiac arrest outside home in Sweden, change in characteristics, outcome and availability for public access defibrillation. Scand J Trauma Resusc Emerg Med 2009;17: Cummins R, Thies W. Automated external defibrillators and the Advanced Cardiac Life Support Program: a new initiative from the American Heart Association. Am J Emerg Med 1991;9: Waalewijn RA, Nijpels MA, Tijssen JG, Koster RW. Prevention of deterioration of ventricular fibrillation by basic life support during out-of-hospital cardiac arrest. Resuscitation 2002;54: Weisfeldt ML, Sitlani CM, Ornato JP, et al. Survival after application of automatic external defibrillators before arrival of the emergency medical system: evaluation in the resuscitation outcomes consortium population of 21 million. J Am Coll Cardiol 2010;55: van Alem AP, Vrenken RH, de Vos R, Tijssen JG, Koster RW. Use of automated external defibrillator by first responders in out of hospital cardiac arrest: prospective controlled trial. BMJ 2003;327: Sandroni C, Nolan J, Cavallaro F, Antonelli M. In-hospital cardiac arrest: incidence, prognosis and possible measures to improve survival. Intensive Care Med 2007;33: Meaney PA, Nadkarni VM, Kern KB, Indik JH, Halperin HR, Berg RA. Rhythms and outcomes of adult in-hospital cardiac arrest. Crit Care Med 2010;38: Proceedings of the 2005 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care science with Treatment Recommendations. Resuscitation 2005;67: International Liaison Committee on Resuscitation. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Circulation 2005;112(Suppl. III):III Morley PT, Atkins DL, Billi JE, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 3. Evidence evaluation process. Resuscitation; doi: /j.resuscitation , in press. 40. Billi JE, Zideman DA, Eigel B, Nolan JP, Montgomery WH, Nadkarni VM. Con.ict of interest management before, during, and after the 2005 International Consensus Conference on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Resuscitation 2005;67: Shuster M, Billi JE, Bossaert L, et al. International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Part 4. Con.ict of interest management before, during, and after the 2010 International Consensus Conference on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Resuscitation; doi: /j.resuscitation , in press. 42. Valenzuela TD, Roe DJ, Cretin S, Spaite DW, Larsen MP. Estimating effectiveness of cardiac arrest interventions: a logistic regression survival model. Circulation 1997;96: Holmberg M, Holmberg S, Herlitz J. Factors modifying the effect of bystander cardiopulmonary resuscitation on survival in out-of-hospital cardiac arrest patients in Sweden. Eur Heart J 2001;22: Holmberg M, Holmberg S, Herlitz J, Gardelov B. Survival after cardiac arrest outside hospital in Sweden. Swedish Cardiac Arrest Registry. Resuscitation 1998;36: Waalewijn RA, Tijssen JG, Koster RW. Bystander initiated actions in out-ofhospital cardiopulmonary resuscitation: results from the Amsterdam Resuscitation Study (ARREST). Resuscitation 2001;50: SOS-KANTO Study Group. Cardiopulmonary resuscitation by bystanders with chest compression only (SOS-KANTO): an observational study. Lancet 2007;369: Iwami T, Kawamura T, Hiraide A, et al. Effectiveness of bystander-initiated cardiac-only resuscitation for patients with out-of-hospital cardiac arrest. Circulation 2007;116: Weaver WD, Hill D, Fahrenbruch CE, et al. Use of the automatic external defibrillator in the management of out-of-hospital cardiac arrest. N Engl J Med 1988;319: Auble TE, Menegazzi JJ, Paris PM. Effect of out-of-hospital defibrillation by basic life support providers on cardiac arrest mortality: a metaanalysis. Ann Emerg Med 1995;25: Stiell IG, Wells GA, Field BJ, et al. Improved out-of-hospital cardiac arrest survival through the inexpensive optimization of an existing defibrillation program: OPALS study phase II. Ontario Prehospital Advanced Life Support. JAMA 1999;281: Stiell IG, Wells GA, DeMaio VJ, et al. Modifiable factors associated with improved cardiac arrest survival in a multicenter basic life support/defibrillation system: OPALS Study Phase I results. Ontario Prehospital Advanced Life Support. Ann Emerg Med 1999;33: Caffrey S. Feasibility of public access to defibrillation. Curr Opin Crit Care 2002;8: O Rourke MF, Donaldson E, Geddes JS. An airline cardiac arrest program. Circulation 1997;96: Page RL, Hamdan MH, McKenas DK. Defibrillation aboard a commercial aircraft. Circulation 1998;97: Valenzuela TD, Roe DJ, Nichol G, Clark LL, Spaite DW, Hardman RG. Outcomes of rapid defibrillation by security officers after cardiac arrest in casinos. N Engl J Med 2000;343: Waalewijn RA, de Vos R, Tijssen JG, Koster RW. Survival models for out-of hospital cardiopulmonary resuscitation from the perspectives of the bystander, the first responder, and the paramedic. Resuscitation 2001;51: Engdahl J, Abrahamsson P, Bang A, Lindqvist J, Karlsson T, Herlitz J. Is hospital care of major importance for outcome after out-of-hospital cardiac arrest? Experience acquired from patients with out-of-hospital cardiac arrest resuscitated by the same Emergency Medical Service and admitted to one of two hospitals over a 16-year period in the municipality of Goteborg. Resuscitation 2000;43:
60 62 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger Langhelle A, Tyvold SS, Lexow K, Hapnes SA, Sunde K, Steen PA. In-hospital factors associated with improved outcome after out-of-hospital cardiac arrest. A comparison between four regions in Norway. Resuscitation 2003;56: Carr BG, Goyal M, Band RA, et al. A national analysis of the relationship between hospital factors and post-cardiac arrest mortality. Intensive Care Med 2009;35: Liu JM, Yang Q, Pirrallo RG, Klein JP, Aufderheide TP. Hospital variability of out-of-hospital cardiac arrest survival. Prehosp Emerg Care 2008;12: Carr BG, Kahn JM, Merchant RM, Kramer AA, Neumar RW. Inter-hospital variability in post-cardiac arrest mortality. Resuscitation 2009;80: Herlitz J, Engdahl J, Svensson L, Angquist KA, Silfverstolpe J, Holmberg S. Major differences in 1-month survival between hospitals in Sweden among initial survivors of out-of-hospital cardiac arrest. Resuscitation 2006;70: Keenan SP, Dodek P, Martin C, Priestap F, Norena M, Wong H. Variation in length of intensive care unit stay after cardiac arrest: where you are is as important as who you are. Crit Care Med 2007;35: Bahr J, Klingler H, Panzer W, Rode H, Kettler D. Skills of lay people in checking the carotid pulse. Resuscitation 1997;35: Nyman J, Sihvonen M. Cardiopulmonary resuscitation skills in nurses and nursing students. Resuscitation 2000;47: Tibballs J, Russell P. Reliability of pulse palpation by healthcare personnel to diagnose paediatric cardiac arrest. Resuscitation 2009;80: Ruppert M, Reith MW, Widmann JH, et al. Checking for breathing: evaluation of the diagnostic capability of emergency medical services personnel, physicians, medical students, and medical laypersons. Ann Emerg Med 1999;34: Perkins GD, Stephenson B, Hulme J, Monsieurs KG. Birmingham assessment of breathing study (BABS). Resuscitation 2005;64: Bobrow BJ, Zuercher M, Ewy GA, et al. Gasping during cardiac arrest in humans is frequent and associated with improved survival. Circulation 2008;118: Taylor RB, Brown CG, Bridges T, Werman HA, Ashton J, Hamlin RL. A model for regional blood flow measurements during cardiopulmonary resuscitation in a swine model. Resuscitation 1988;16: Eftestol T, Sunde K, Steen PA. Effects of interrupting precordial compressions on the calculated probability of defibrillation success during out-of-hospital cardiac arrest. Circulation 2002;105: Aufderheide TP, Pirrallo RG, Yannopoulos D, et al. Incomplete chest wall decompression: a clinical evaluation of CPR performance by EMS personnel and assessment of alternative manual chest compression decompression techniques. Resuscitation 2005;64: Yannopoulos D, McKnite S, Aufderheide TP, et al. Effects of incomplete chest wall decompression during cardiopulmonary resuscitation on coronary and cerebral perfusion pressures in a porcine model of cardiac arrest. Resuscitation 2005;64: Ornato JP, Hallagan LF, McMahan SB, Peeples EH, Rostafinski AG. Attitudes of BCLS instructors about mouth-to-mouth resuscitation during the AIDS epidemic. Ann Emerg Med 1990;19: Hew P, Brenner B, Kaufman J. Reluctance of paramedics and emergency medical technicians to perform mouth-to-mouth resuscitation. J Emerg Med 1997;15: Chandra NC, Gruben KG, Tsitlik JE, et al. Observations of ventilation during resuscitation in a canine model. Circulation 1994;90: Kern KB, Hilwig RW, Berg RA, Sanders AB, Ewy GA. Importance of continuous chest compressions during cardiopulmonary resuscitation: improved outcome during a simulated single lay-rescuer scenario. Circulation 2002;105: Geddes LA, Rundell A, Otlewski M, Pargett M. How much lung ventilation is obtained with only chest-compression CPR? Cardiovasc Eng 2008;8: Berg RA, Kern KB, Hilwig RW, et al. Assisted ventilation does not improve outcome in a porcine model of single-rescuer bystander cardiopulmonary resuscitation. Circulation 1997;95: Berg RA, Kern KB, Hilwig RW, Ewy GA. Assisted ventilation during bystander CPR in a swine acute myocardial infarction model does not improve outcome. Circulation 1997;96: Turner I, Turner S, Armstrong V. Does the compression to ventilation ratio affect the quality of CPR: a simulation study. Resuscitation 2002;52: Dorph E, Wik L, Stromme TA, Eriksen M, Steen PA. Oxygen delivery and return of spontaneous circulation with ventilation: compression ratio 2:30 versus chest compressions only CPR in pigs. Resuscitation 2004;60: Bohm K, Rosenqvist M, Herlitz J, Hollenberg J, Svensson L. Survival is similar after standard treatment and chest compression only in out-of-hospital bystander cardiopulmonary resuscitation. Circulation 2007;116: Kitamura T, Iwami T, Kawamura T, et al. Conventional and chest-compression only cardiopulmonary resuscitation by bystanders for children who have out-of-hospital cardiac arrests: a prospective, nationwide, population-based cohort study. Lancet Kitamura T, Iwami T, Kawamura T, Nagao K, Tanaka H, Hiraide A. Bystanderinitiated rescue breathing for out-of-hospital cardiac arrests of noncardiac origin. Circulation 2010;122: Peberdy MA, Ottingham LV, Groh WJ, et al. Adverse events associated with lay emergency response programs: the public access defibrillation trial experience. Resuscitation 2006;70: Sugerman NT, Edelson DP, Leary M, et al. Rescuer fatigue during actual inhospital cardiopulmonary resuscitation with audiovisual feedback: a prospective multicenter study. Resuscitation 2009;80: Hallstrom AP, Ornato JP, Weisfeldt M, et al. Public-access defibrillation and survival after out-of-hospital cardiac arrest. N Engl J Med 2004;351: Hoke RS, Heinroth K, Trappe HJ, Werdan K. Is external defibrillation an electric threat for bystanders? Resuscitation 2009;80: Dickinson CL, Hall CR, Soar J. Accidental shock to rescuer during successful defibrillation of ventricular fibrillation a case of human involuntary automaticity. Resuscitation 2008;76: Cydulka RK, Connor PJ, Myers TF, Pavza G, Parker M. Prevention of oral bacterial flora transmission by using mouth-to-mask ventilation during CPR. J Emerg Med 1991;9: Blenkharn JI, Buckingham SE, Zideman DA. Prevention of transmission of infection during mouth-to-mouth resuscitation. Resuscitation 1990;19: Turner S, Turner I, Chapman D, et al. A comparative study of the 1992 and 1997 recovery positions for use in the UK. Resuscitation 1998;39: Handley AJ. Recovery position. Resuscitation 1993;26: Anon. Guidelines 2000 for cardiopulmonary resuscitation and emergency cardiovascular care an international consensus on science. Resuscitation 2000;46: Fingerhut LA, Cox CS, Warner M. International comparative analysis of injury mortality. Findings from the ICE on injury statistics. International Collaborative Effort on Injury Statistics. Adv Data 1998: White RD, Bunch TJ, Hankins DG. Evolution of a community-wide early defibrillation programme experience over 13 years using police/fire personnel and paramedics as responders. Resuscitation 2005;65: Mosesso Jr VN, Davis EA, Auble TE, Paris PM, Yealy DM. Use of automated external defibrillators by police officers for treatment of out-of-hospital cardiac arrest. Ann Emerg Med 1998;32: The Public Access Defibrillation Trial Investigators. Public-access defibrillation and survival after out-of-hospital cardiac arrest. N Engl J Med 2004;351: Kitamura T, Iwami T, Kawamura T, Nagao K, Tanaka H, Hiraide A. Nationwide public-access defibrillation in Japan. N Engl J Med 2010;362: Bardy GH, Lee KL, Mark DB, et al. Home use of automated external defibrillators for sudden cardiac arrest. N Engl J Med 2008;358: Zafari AM, Zarter SK, Heggen V, et al. A program encouraging early defibrillation results in improved in-hospital resuscitation efficacy. J Am Coll Cardiol 2004;44: Destro A, Marzaloni M, Sermasi S, Rossi F. Automatic external defibrillators in the hospital as well? Resuscitation 1996;31: Spearpoint KG, Gruber PC, Brett SJ. Impact of the Immediate Life Support course on the incidence and outcome of in-hospital cardiac arrest calls: an observational study over 6 years. Resuscitation 2009;80: Cummins RO, Eisenberg MS, Litwin PE, Graves JR, Hearne TR, Hallstrom AP. Automatic external defibrillators used by emergency medical technicians: a controlled clinical trial. JAMA 1987;257: Stults KR, Brown DD, Kerber RE. Efficacy of an automated external defibrillator in the management of out-of-hospital cardiac arrest: validation of the diagnostic algorithm and initial clinical experience in a rural environment. Circulation 1986;73: Kramer-Johansen J, Edelson DP, Abella BS, Becker LB, Wik L, Steen PA. Pauses in chest compression and inappropriate shocks: a comparison of manual and semi-automatic defibrillation attempts. Resuscitation 2007;73: Pytte M, Pedersen TE, Ottem J, Rokvam AS, Sunde K. Comparison of handsoff time during CPR with manual and semi-automatic defibrillation in a manikin model. Resuscitation 2007;73: Forcina MS, Farhat AY, O Neil WW, Haines Defi Cardiac arrest survival after implementation of automated external defibrillator technology in the in-hospital setting. Crit Care Med 2009;37: Edelson DP, Abella BS, Kramer-Johansen J, et al. Effects of compression depth and pre-shock pauses predict defibrillation failure during cardiac arrest. Resuscitation 2006;71: Yu T, Weil MH, Tang W, et al. Adverse outcomes of interrupted precordial compression during automated defibrillation. Circulation 2002;106: Gundersen K, Kvaloy JT, Kramer-Johansen J, Steen PA, Eftestol T. Development of the probability of return of spontaneous circulation in intervals without chest compressions during out-of-hospital cardiac arrest: an observational study. BMC Med 2009;7: Lloyd MS, Heeke B, Walter PF, Langberg JJ. Hands-on defibrillation: an analysis of electrical current flow through rescuers in direct contact with patients during biphasic external defibrillation. Circulation 2008;117: Bojar RM, Payne DD, Rastegar H, Diehl JT, Cleveland RJ. Use of self-adhesive external defibrillator pads for complex cardiac surgical procedures. Ann Thorac Surg 1988;46: Bradbury N, Hyde D, Nolan J. Reliability of ECG monitoring with a gel pad/ paddle combination after defibrillation. Resuscitation 2000;44: Brown J, Rogers J, Soar J. Cardiac arrest during surgery and ventilation in the prone position: a case report and systematic review. Resuscitation 2001;50: Perkins GD, Davies RP, Soar J, Thickett DR. The impact of manual defibrillation technique on no-flow time during simulated cardiopulmonary resuscitation. Resuscitation 2007;73: Wilson RF, Sirna S, White CW, Kerber RE. Defibrillation of high-risk patients during coronary angiography using self-adhesive, preapplied electrode pads. Am J Cardiol 1987;60:380 2.
61 Podsumowanie Komitetu Wykonawczego ERC Stults KR, Brown DD, Cooley F, Kerber RE. Self-adhesive monitor/defibrillation pads improve prehospital defibrillation success. Ann Emerg Med 1987;16: Callaway CW, Sherman LD, Mosesso Jr VN, Dietrich TJ, Holt E, Clarkson MC. Scaling exponent predicts defibrillation success for out-of-hospital ventricular fibrillation cardiac arrest. Circulation 2001;103: Eftestol T, Sunde K, Aase SO, Husoy JH, Steen PA. Predicting outcome of defibrillation by spectral characterization and nonparametric classification of ventricular fibrillation in patients with out-of-hospital cardiac arrest. Circulation 2000;102: Eftestol T, Wik L, Sunde K, Steen PA. Effects of cardiopulmonary resuscitation on predictors of ventricular fibrillation defibrillation success during out-ofhospital cardiac arrest. Circulation 2004;110: Weaver WD, Cobb LA, Dennis D, Ray R, Hallstrom AP, Copass MK. Amplitude of ventricular fibrillation waveform and outcome after cardiac arrest. Ann Intern Med 1985;102: Brown CG, Dzwonczyk R. Signal analysis of the human electrocardiogram during ventricular fibrillation: frequency and amplitude parameters as predictors of successful countershock. Ann Emerg Med 1996;27: Callaham M, Braun O, Valentine W, Clark DM, Zegans C. Prehospital cardiac arrest treated by urban first-responders: profile of patient response and prediction of outcome by ventricular fibrillation waveform. Ann Emerg Med 1993;22: Strohmenger HU, Lindner KH, Brown CG. Analysis of the ventricular fibrillation ECG signal amplitude and frequency parameters as predictors of countershock success in humans. Chest 1997;111: Strohmenger HU, Eftestol T, Sunde K, et al. The predictive value of ventricular fibrillation electrocardiogram signal frequency and amplitude variables in patients with out-of-hospital cardiac arrest. Anesth Analg 2001;93: Podbregar M, Kovacic M, Podbregar-Mars A, Brezocnik M. Predicting defibrillation success by genetic programming in patients with out-of-hospital cardiac arrest. Resuscitation 2003;57: Menegazzi JJ, Callaway CW, Sherman LD, et al. Ventricular fibrillation scaling exponent can guide timing of defibrillation and other therapies. Circulation 2004;109: Povoas HP, Weil MH, Tang W, Bisera J, Klouche K, Barbatsis A. Predicting the success of defibrillation by electrocardiographic analysis. Resuscitation 2002;53: Noc M, Weil MH, Tang W, Sun S, Pernat A, Bisera J. Electrocardiographic prediction of the success of cardiac resuscitation. Crit Care Med 1999;27: Strohmenger HU, Lindner KH, Keller A, Lindner IM, Pfenninger EG. Spectral analysis of ventricular fibrillation and closed-chest cardiopulmonary resuscitation. Resuscitation 1996;33: Noc M, Weil MH, Gazmuri RJ, Sun S, Biscera J, Tang W. Ventricular fibrillation voltage as a monitor of the effectiveness of cardiopulmonary resuscitation. J Lab Clin Med 1994;124: Lightfoot CB, Nremt P, Callaway CW, et al. Dynamic nature of electrocardiographic waveform predicts rescue shock outcome in porcine ventricular fibrillation. Ann Emerg Med 2003;42: Marn-Pernat A, Weil MH, Tang W, Pernat A, Bisera J. Optimizing timing of ventricular defibrillation. Crit Care Med 2001;29: Hamprecht FA, Achleitner U, Krismer AC, et al. Fibrillation power, an alternative method of ECG spectral analysis for prediction of countershock success in a porcine model of ventricular fibrillation. Resuscitation 2001;50: Amann A, Achleitner U, Antretter H, et al. Analysing ventricular fibrillation ECG-signals and predicting defibrillation success during cardiopulmonary resuscitation employing N(alpha)-histograms. Resuscitation 2001;50: Brown CG, Grif.th RF, Van Ligten P, et al. Median frequency a new parameter for predicting defibrillation success rate. Ann Emerg Med 1991;20: Amann A, Rheinberger K, Achleitner U, et al. The prediction of defibrillation outcome using a new combination of mean frequency and amplitude inporcine models of cardiac arrest. Anesth Analg 2002;95: [table of contents] Deakin CD, Nolan JP. European Resuscitation Council guidelines for resuscitation Section 3. Electrical therapies: automated external defibrillators, defibrillation, cardioversion and pacing. Resuscitation 2005; 67(Suppl. 1):S Cobb LA, Fahrenbruch CE, Walsh TR, et al. Influence of cardiopulmonary resuscitation prior to defibrillation in patients with out-of-hospital ventricular fibrillation. JAMA 1999;281: Wik L, Hansen TB, Fylling F, et al. Delaying defibrillation to give basic cardiopulmonary resuscitation to patients with out-of-hospital ventricular fibrillation: a randomized trial. JAMA 2003;289: Baker PW, Conway J, Cotton C, et al. Defibrillation or cardiopulmonary resuscitation first for patients with out-of-hospital cardiac arrests found by paramedics to be in ventricular fibrillation? A randomised control trial. Resuscitation 2008;79: Jacobs IG, Finn JC, Oxer HF, Jelinek GA. CPR before defibrillation in out-ofhospital cardiac arrest: a randomized trial. Emerg Med Australas 2005;17: Hayakawa M, Gando S, Okamoto H, Asai Y, Uegaki S, Makise H. Shortening of cardiopulmonary resuscitation time before the defibrillation worsens the outcome in out-of-hospital VF patients. Am J Emerg Med 2009;27: Bradley SM, Gabriel EE, Aufderheide TP, et al. Survival Increases with CPR by Emergency Medical Services before defibrillation of out-of-hospital ventricular fibrillation or ventricular tachycardia: observations from the resuscitation outcomes consortium. Resuscitation 2010;81: Christenson J, Andrusiek D, Everson-Stewart S, et al. Chest compression fraction determines survival in patients with out-of-hospital ventricular fibrillation. Circulation 2009;120: Olasveengen TM, Vik E, Kuzovlev A, Sunde K. Effect of implementation of new resuscitation guidelines on quality of cardiopulmonary resuscitation and survival. Resuscitation 2009;80: Bobrow BJ, Clark LL, Ewy GA, et al. Minimally interrupted cardiac resuscitation by emergency medical services for out-of-hospital cardiac arrest. JAMA 2008;299: Rea TD, Helbock M, Perry S, et al. Increasing use of cardiopulmonary resuscitation during out-of-hospital ventricular fibrillation arrest: survival implications of guideline changes. Circulation 2006;114: Steinmetz J, Barnung S, Nielsen SL, Risom M, Rasmussen LS. Improved survival after an out-of-hospital cardiac arrest using new guidelines. Acta Anaesthesiol Scand 2008;52: Jost D, Degrange H, Verret C, et al. DEFI 2005: a randomized controlled trial of the effect of automated external defibrillator cardiopulmonary resuscitation protocol on outcome from out-of-hospital cardiac arrest. Circulation 2010;121: van Alem AP, Chapman FW, Lank P, Hart AA, Koster RW. A prospective, randomised and blinded comparison of first shock success of monophasic and biphasic waveforms in out-of-hospital cardiac arrest. Resuscitation 2003;58: Carpenter J, Rea TD, Murray JA, Kudenchuk PJ, Eisenberg MS. Defibrillation waveform and post-shock rhythm in out-of-hospital ventricular fibrillation cardiac arrest. Resuscitation 2003;59: Morrison LJ, Dorian P, Long J, et al. Out-of-hospital cardiac arrest rectilinear biphasic to monophasic damped sine defibrillation waveforms with advanced life support intervention trial (ORBIT). Resuscitation 2005;66: Mittal S, Ayati S, Stein KM, et al. Transthoracic cardioversion of atrial fibrillation: comparison of rectilinear biphasic versus damped sine wave monophasic shocks. Circulation 2000;101: Page RL, Kerber RE, Russell JK, et al. Biphasic versus monophasic shock waveform for conversion of atrial fibrillation: the results of an international randomized, double-blind multicenter trial. J Am Coll Cardiol 2002;39: Koster RW, Dorian P, Chapman FW, Schmitt PW, O Grady SG, Walker RG. A randomized trial comparing monophasic and biphasic waveform shocks for external cardioversion of atrial fibrillation. Am Heart J 2004;147:e Ambler JJ, Deakin CD. A randomized controlled trial of efficacy and ST change following use of the Welch-Allyn MRL PIC biphasic waveform versus damped sine monophasic waveform for external DC cardioversion. Resuscitation 2006;71: Martens PR, Russell JK, Wolcke B, et al. Optimal response to cardiac arrest study: defibrillation waveform effects. Resuscitation 2001;49: Gliner BE, Jorgenson DB, Poole JE, et al. Treatment of out-of-hospital cardiac arrest with a low-energy impedance-compensating biphasic waveform automatic external defibrillator. The LIFE Investigators. Biomed Instrum Technol 1998;32: White RD, Blackwell TH, Russell JK, Snyder DE, Jorgenson DB. Transthoracic impedance does not affect defibrillation, resuscitation or survival in patients with out-of-hospital cardiac arrest treated with a non-escalating biphasic waveform defibrillator. Resuscitation 2005;64: Stiell IG, Walker RG, Nesbitt LP, et al. BIPHASIC trial: a randomized comparison of fixed lower versus escalating higher energy levels for defibrillation in outof-hospital cardiac arrest. Circulation 2007;115: Walsh SJ, McClelland AJ, Owens CG, et al. Efficacy of distinct energy delivery protocols comparing two biphasic defibrillators for cardiac arrest. Am J Cardiol 2004;94: Higgins SL, Herre JM, Epstein AE, et al. A comparison of biphasic and monophasic shocks for external defibrillation. Physio-control biphasic investigators. Prehosp Emerg Care 2000;4: Berg RA, Samson RA, Berg MD, et al. Better outcome after pediatric defibrillation dosage than adult dosage in a swine model of pediatric ventricular fibrillation. J Am Coll Cardiol 2005;45: Killingsworth CR, Melnick SB, Chapman FW, et al. Defibrillation threshold and cardiac responses using an external biphasic defibrillator with pediatric and adult adhesive patches in pediatric-sized piglets. Resuscitation 2002;55: Tang W, Weil MH, Sun S, et al. The effects of biphasic waveform design on postresuscitation myocardial function. J Am Coll Cardiol 2004;43: Xie J, Weil MH, Sun S, et al. High-energy defibrillation increases the severity of postresuscitation myocardial dysfunction. Circulation 1997;96: Lown B. Electrical reversion of cardiac arrhythmias. Br Heart J 1967;29: Boodhoo L, Mitchell AR, Bordoli G, Lloyd G, Patel N, Sulke N. DC cardioversion of persistent atrial fibrillation: a comparison of two protocols. Int J Cardiol 2007;114: Boos C, Thomas MD, Jones A, Clarke E, Wilbourne G, More RS. Higher energy monophasic DC cardioversion for persistent atrial fibrillation: is it time to start at 360 joules? Ann Noninvasive Electrocardiol 2003;8: Glover BM, Walsh SJ, McCann CJ, et al. Biphasic energy selection for transthoracic cardioversion of atrial fibrillation. The BEST AF Trial. Heart 2008;94: Rashba EJ, Gold MR, Crawford FA, Leman RB, Peters RW, Shorofsky SR. Efficacy of transthoracic cardioversion of atrial fibrillation using a biphasic, trun- 1
62 64 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger 1 cated exponential shock waveform at variable initial shock energies. Am J Cardiol 2004;94: Pinski SL, Sgarbossa EB, Ching E, Trohman RG. A comparison of 50-J versus 100-J shocks for direct-current cardioversion of atrial flutter. Am Heart J 1999;137: Alatawi F, Gurevitz O, White R. Prospective, randomized comparison of two biphasic waveforms for the efficacy and safety of transthoracic biphasic cardioversion of atrial fibrillation. Heart Rhythm 2005;2: Kerber RE, Martins JB, Kienzle MG, et al. Energy, current, and success in defibrillation and cardioversion: clinical studies using anautomated impedancebased method of energy adjustment. Circulation 1988;77: Kerber RE, Kienzle MG, Olshansky B, et al. Ventricular tachycardia rate and morphology determine energy and current requirements for transthoracic cardioversion. Circulation 1992;85: Stockwell B, Bellis G, Morton G, et al. Electrical injury during hands on defibrillation a potential risk of internal cardioverter defibrillators? Resuscitation 2009;80: Nolan J, Soar J, Eikeland H. The chain of survival. Resuscitation 2006;71: Gwinnutt CL, Columb M, Harris R. Outcome after cardiac arrest in adults in UK hospitals: effect of the 1997 guidelines. Resuscitation 2000;47: Peberdy MA, Kaye W, Ornato JP, et al. Cardiopulmonary resuscitation of adults in the hospital: a report of cardiac arrests from the National Registry of Cardiopulmonary Resuscitation. Resuscitation 2003;58: Smith GB. In-hospital cardiac arrest: is it time for an in-hospital chain of prevention? Resuscitation National Confidential Enquiry into Patient Outcome and Death. An acute problem? London: NCEPOD; Hodgetts TJ, Kenward G, Vlackonikolis I, et al. Incidence, location and reasons for avoidable in-hospital cardiac arrest in a district general hospital. Resuscitation 2002;54: Kause J, Smith G, Prytherch D, Parr M, Flabouris A, Hillman K. A comparison of antecedents to cardiac arrests, deaths and emergency intensive care admissions in Australia and New Zealand, and the United Kingdom the ACADEMIA study. Resuscitation 2004;62: Castagna J, Weil MH, Shubin H. Factors determining survival in patients with cardiac arrest. Chest 1974;65: Herlitz J, Bang A, Aune S, Ekstrom L, Lundstrom G, Holmberg S. Characteristics and outcome among patients suffering in-hospital cardiac arrest in monitored and non-monitored areas. Resuscitation 2001;48: Campello G, Granja C, Carvalho F, Dias C, Azevedo LF, Costa-Pereira A. Immediate and long-term impact of medical emergency teams on cardiac arrest prevalence and mortality: a plea for periodic basic life-support training programs. Crit Care Med 2009;37: Bellomo R, Goldsmith D, Uchino S, et al. A prospective before-and-after trial of a medical emergency team. Med J Aust 2003;179: Bellomo R, Goldsmith D, Uchino S, et al. Prospective controlled trial of effect of medical emergency team on postoperative morbidity and mortality rates. Crit Care Med 2004;32: DeVita MA, Smith GB, Adam SK, et al. Identifying the hospitalised patient in crisis a consensus conference on the afferent limb of rapid response systems. Resuscitation 2010;81: Goldhill DR, Worthington L, Mulcahy A, Tarling M, Sumner A. The patientatrisk team: identifying and managing seriously ill ward patients. Anaesthesia 1999;54: Hodgetts TJ, Kenward G, Vlachonikolis IG, Payne S, Castle N. The identification of risk factors for cardiac arrest and formulation of activation criteria to alert a medical emergency team. Resuscitation 2002;54: Subbe CP, Davies RG, Williams E, Rutherford P, Gemmell L. Effect of introducing the modified early warning score on clinical outcomes, cardio-pulmonary arrests and intensive care utilisation in acute medical admissions. Anaesthesia 2003;58: Armitage M, Eddleston J, Stokes T. Recognising and responding to acute illness in adults in hospital: summary of NICE guidance. BMJ 2007;335: Hillman K, Chen J, Cretikos M, et al. Introduction of the medical emergency team (MET) system: a cluster-randomised controlled trial. Lancet 2005;365: Lee A, Bishop G, Hillman KM, Daffurn K. The Medical Emergency Team. Anaesth Intensive Care 1995;23: Devita MA, Bellomo R, Hillman K, et al. Findings of the first consensus conference on medical emergency teams. Crit Care Med 2006;34: Ball C, Kirkby M, Williams S. Effect of the critical care outreach team on patient survival to discharge from hospital and readmission to critical care: nonrandomised population based study. BMJ 2003;327: Critical care outreach 2003: progress in developing services. The National Outreach Report. London, UK: Department of Health and National Health Service Modernisation Agency; Chan PS, Jain R, Nallmothu BK, Berg RA, Sasson C. Rapid response teams: a systematic review and meta-analysis. Arch Intern Med 2010;170: Parr MJ, Hadfield JH, Flabouris A, Bishop G, Hillman K. The Medical Emergency Team: 12 month analysis of reasons for activation, immediate outcome and not-for-resuscitation orders. Resuscitation 2001;50: Smith GB. Increased do not attempt resuscitation decision making in hospitals with a medical emergency teams system cause and effect? Resuscitation 2008;79: Chen J, Flabouris A, Bellomo R, Hillman K, Finfer S. The Medical Emergency Team System and not-for-resuscitation orders: results from the MERIT study. Resuscitation 2008;79: Jones DA, McIntyre T, Baldwin I, Mercer I, Kattula A, Bellomo R. The medical emergency team and end-of-life care: a pilot study. Crit Care Resusc 2007;9: Excellence NIfHaC. NICE clinical guideline 50 acutely ill patients in hospital: recognition of and response to acute illness in adults in hospital. London: National Institute for Health and Clinical Excellence; Marshall S, Harrison J, Flanagan B. The teaching of a structured tool improves the clarity and content of interprofessional clinical communication. Qual Saf Health Care 2009;18: Muller D, Agrawal R, Arntz HR. How sudden is sudden cardiac death? Circulation 2006;114: Amital H, Glikson M, Burstein M, et al. Clinical characteristics of unexpected death among young enlisted military personnel: results of a three-decade retrospective surveillance. Chest 2004;126: Basso C, Maron BJ, Corrado D, Thiene G. Clinical profile of congenital coronary artery anomalies with origin from the wrong aortic sinus leading to sudden death in young competitive athletes. J Am Coll Cardiol 2000;35: Corrado D, Basso C, Thiene G. Sudden cardiac death in young people with apparently normal heart. Cardiovasc Res 2001;50: Drory Y, Turetz Y, Hiss Y, et al. Sudden unexpected death in persons less than 40 years of age. Am J Cardiol 1991;68: Kramer MR, Drori Y, Lev B. Sudden death in young soldiers. High incidence of syncope prior to death. Chest 1988;93: Quigley F, Greene M, O Connor D, Kelly F. A survey of the causes of sudden cardiac death in the under 35-year-age group. Ir Med J 2005;98: Wisten A, Forsberg H, Krantz P, Messner T. Sudden cardiac death in year olds in Sweden during J Intern Med 2002;252: Wisten A, Messner T. Young Swedish patients with sudden cardiac death have a lifestyle very similar to a control population. Scand Cardiovasc J 2005;39: Wisten A, Messner T. Symptoms preceding sudden cardiac death in the young are common but often misinterpreted. Scand Cardiovasc J 2005;39: Morrison LJ, Visentin LM, Kiss A, et al. Validation of a rule for termination of resuscitation in out-of-hospital cardiac arrest. N Engl J Med 2006;355: Gabbott D, Smith G, Mitchell S, et al. Cardiopulmonary resuscitation standards for clinical practice and training in the UK. Resuscitation 2005;64: Dyson E, Smith GB. Common faults in resuscitation equipment guidelines for checking equipment and drugs used in adult cardiopulmonary resuscitation. Resuscitation 2002;55: Perkins GD, Roberts C, Gao F. Delays in defibrillation: influence of different monitoring techniques. Br J Anaesth 2002;89: Featherstone P, Chalmers T, Smith GB. RSVP: a system for communication of deterioration in hospital patients. Br J Nurs 2008;17: Abella BS, Alvarado JP, Myklebust H, et al. Quality of cardiopulmonary resuscitation during in-hospital cardiac arrest. JAMA 2005;293: Abella BS, Sandbo N, Vassilatos P, et al. Chest compression rates during cardiopulmonary resuscitation are suboptimal: a prospective study during in-hospital cardiac arrest. Circulation 2005;111: Stiell IG, Wells GA, Field B, et al. Advanced cardiac life support in out-of-hospital cardiac arrest. N Engl J Med 2004;351: Olasveengen TM, Sunde K, Brunborg C, Thowsen J, Steen PA, Wik L. Intravenous drug administration during out-of-hospital cardiac arrest: a randomized trial. JAMA 2009;302: Herlitz J, Ekstrom L, Wennerblom B, Axelsson A, Bang A, Holmberg S. Adrenaline in out-of-hospital ventricular fibrillation. Does it make any difference? Resuscitation 1995;29: Holmberg M, Holmberg S, Herlitz J. Low chance of survival among patients requiring adrenaline (epinephrine) or intubation after out-of-hospital cardiac arrest in Sweden. Resuscitation 2002;54: Sunde K, Eftestol T, Askenberg C, Steen PA. Quality assessment of defibrillation and advanced life support using data from the medical control module of the defibrillator. Resuscitation 1999;41: Rea TD, Shah S, Kudenchuk PJ, Copass MK, Cobb LA. Automated external defibrillators: to what extent does the algorithm delay CPR? Ann Emerg Med 2005;46: van Alem AP, Sanou BT, Koster RW. Interruption of cardiopulmonary resuscitation with the use of the automated external defibrillator in out-of-hospital cardiac arrest. Ann Emerg Med 2003;42: Pytte M, Kramer-Johansen J, Eilevstjonn J, et al. Haemodynamic effects of adrenaline (epinephrine) depend on chest compression quality during cardiopulmonary resuscitation in pigs. Resuscitation 2006;71: Prengel AW, Lindner KH, Ensinger H, Grunert A. Plasma catecholamine concentrations after successful resuscitation in patients. Crit Care Med 1992; 20: Bhende MS, Thompson AE. Evaluation of an end-tidal CO 2 detector during pediatric cardiopulmonary resuscitation. Pediatrics 1995;95: Sehra R, Underwood K, Checchia P. End tidal CO 2 is a quantitative measure of cardiac arrest. Pacing Clin Electrophysiol 2003;26: Amir O, Schliamser JE, Nemer S, Arie M. Ineffectiveness of precordial thump for cardioversion of malignant ventricular tachyarrhythmias. Pacing Clin Electrophysiol 2007;30: Haman L, Parizek P, Vojacek J. Precordial thump efficacy in termination of induced ventricular arrhythmias. Resuscitation 2009;80:14 6.
63 Podsumowanie Komitetu Wykonawczego ERC Pellis T, Kette F, Lovisa D, et al. Utility of pre-cordial thump for treatment of out of hospital cardiac arrest: a prospective study. Resuscitation 2009;80: Kohl P, King AM, Boulin C. Antiarrhythmic effects of acute mechanical stimulation. In: Kohl P, Sachs F, Franz MR, editors. Cardiac mechano-electric feedback and arrhythmias: form pipette to patient. Philadelphia: Elsevier Saunders; p Caldwell G, Millar G, Quinn E, Vincent R, Chamberlain DA. Simple mechanical methods for cardioversion:defence of the precordial thumpand cough version. BMJ (Clin Res Ed) 1985;291: Wenzel V, Lindner KH, Augenstein S, et al. Intraosseous vasopressin improves coronary perfusion pressure rapidly during cardiopulmonary resuscitation in pigs. Crit Care Med 1999;27: Shavit I, Hoffmann Y, Galbraith R, Waisman Y. Comparison of two mechanical intraosseous infusion devices: a pilot, randomized crossover trial. Resuscitation 2009;80: Kudenchuk PJ, Cobb LA, Copass MK, et al. Amiodarone for resuscitation after out-of-hospital cardiac arrest due to ventricular fibrillation. N Engl J Med 1999;341: Dorian P, Cass D, Schwartz B, Cooper R, Gelaznikas R, Barr A. Amiodarone as compared with lidocaine for shock-resistant ventricular fibrillation. N Engl J Med 2002;346: Thel MC, Armstrong AL, McNulty SE, Califf RM, O Connor CM. Randomised trial of magnesium in in-hospital cardiac arrest. Duke Internal Medicine Housestaff. Lancet 1997;350: Allegra J, Lavery R, Cody R, et al. Magnesium sulfate in the treatment of refractory ventricular fibrillation in the prehospital setting. Resuscitation 2001;49: Fatovich D, Prentice D, Dobb G. Magnesium in in-hospital cardiac arrest. Lancet 1998;351: Hassan TB, Jagger C, Barnett DB. A randomised trial to investigate the efficacy of magnesium sulphate for refractory ventricular fibrillation. Emerg Med J 2002;19: Miller B, Craddock L, Hoffenberg S, et al. Pilot study of intravenous magnesium sulfate in refractory cardiac arrest: safety data and recommendations for future studies. Resuscitation 1995;30: Stiell IG, Wells GA, Hebert PC, Laupacis A, Weitzman BN. Association of drug therapy with survival in cardiac arrest: limited role of advanced cardiac life support drugs. Acad Emerg Med 1995;2: Engdahl J, Bang A, Lindqvist J, Herlitz J. Can we define patients with no and those with some chance of survival when found in asystole out of hospital? Am J Cardiol 2000;86: Engdahl J, Bang A, Lindqvist J, Herlitz J. Factors affecting short- and long-term prognosis among 1069 patients with out-of-hospital cardiac arrest and pulse-less electrical activity. Resuscitation 2001;51: Dumot JA, Burval DJ, Sprung J, et al. Outcome of adult cardiopulmonary resuscitations at a tertiary referral center including results of limited resuscitations. Arch Intern Med 2001;161: Tortolani AJ, Risucci DA, Powell SR, Dixon R. In-hospital cardiopulmonary resuscitation during asystole. Therapeutic factors associated with 24-hour survival. Chest 1989;96: Coon GA, Clinton JE, Ruiz E. Use of atropine for brady-asystolic prehospital cardiac arrest. Ann Emerg Med 1981;10: Bottiger BW, Arntz HR, Chamberlain DA, et al. Thrombolysis during resuscitation for out-of-hospital cardiac arrest. N Engl J Med 2008;359: Böttiger BW, Martin E. Thrombolytic therapy during cardiopulmonary resuscitation and the role of coagulation activation after cardiac arrest. Curr Opin Crit Care 2001;7: Spöhr F, Böttiger BW. Safety of thrombolysis during cardiopulmonary resuscitation. Drug Saf 2003;26: Soar J, Foster J, Breitkreutz R. Fluid infusion during CPR and after ROSC is it safe? Resuscitation 2009;80: Price S, Uddin S, Quinn T. Echocardiography in cardiac arrest. Curr Opin Crit Care 2010;16: Memtsoudis SG, Rosenberger P, Loffler M, et al. The usefulness of ransesophageal echocardiography during intraoperative cardiac arrest in non cardiac surgery. Anesth Analg 2006;102: Comess KA, DeRook FA, Russell ML, Tognazzi-Evans TA, Beach KW. The incidence of pulmonary embolism in unexplained sudden cardiac arrest with pulseless electrical activity. Am J Med 2000;109: Niendorff DF, Rassias AJ, Palac R, Beach ML, Costa S, Greenberg M. Rapid cardiac ultrasound of inpatients suffering PEA arrest performed by nonexpert sonographers. Resuscitation 2005;67: Tayal VS, Kline JA. Emergency echocardiography to detect pericardial effusion in patients in PEA and near-pea states. Resuscitation 2003;59: van der Wouw PA, Koster RW, Delemarre BJ, de Vos R, Lampe-Schoenmaeckers AJ, Lie KI. Diagnostic accuracy of transesophageal echocardiography during cardiopulmonary resuscitation. J Am Coll Cardiol 1997;30: Hernandez C, Shuler K, Hannan H, Sonyika C, Likourezos A, Marshall J. C.A.U.S.E.: cardiac arrest ultra-sound exam a better approach to managing patients in primary non-arrhythmogenic cardiac arrest. Resuscitation 2008;76: Steiger HV, Rimbach K, Muller E, Breitkreutz R. Focused emergency echocardiography: lifesaving tool for a 14-year-old girl suffering out-of-hospital pulseless electrical activity arrest because of cardiac tamponadefi Eur J Emerg Med 2009;16: Breitkreutz R, Walcher F, Seeger FH. Focused echocardiographic evaluation in resuscitation management: concept of an advanced life support-conformed algorithm. Crit Care Med 2007;35:S Blaivas M, Fox JC. Outcome in cardiac arrest patients found to have cardiac standstill on the bedside emergency department echocardiogram. Acad Emerg Med 2001;8: Salen P, O Connor R, Sierzenski P, et al. Can cardiac sonography and capnography be used independently and in combination to predict resuscitation outcomes? Acad Emerg Med 2001;8: Salen P, Melniker L, Chooljian C, et al. Does the presence or absence of sonographically identified cardiac activity predict resuscitation outcome sofcardiac arrest patients? Am J Emerg Med 2005;23: Balan IS, Fiskum G, Hazelton J, Cotto-Cumba C, Rosenthal RE. Oximetryguided reoxygenation improves neurological outcome after experimental cardiac arrest. Stroke 2006;37: Kilgannon JH, Jones AE, Shapiro NI, et al. Association between arterial hyperoxia following resuscitation from cardiac arrest and in-hospital mortality. JAMA 2010;303: Nolan JP, Soar J. Airway techniques and ventilation strategies. Curr Opin Crit Care 2008;14: Grmec S. Comparison of three different methods to con.rm tracheal tube placement in emergency intubation. Intensive Care Med 2002;28: Lyon RM, Ferris JD, Young DM, McKeown DW, Oglesby AJ, Robertson C. Field intubation of cardiac arrest patients: a dying art? Emerg Med J 2010;27: Jones JH, Murphy MP, Dickson RL, Somerville GG, Brizendine EJ. Emergency physician-verified out-of-hospital intubation: miss rates by paramedics. Acad Emerg Med 2004;11: Pelucio M, Halligan L, Dhindsa H. Out-of-hospital experience with the syringe esophageal detector device. Acad Emerg Med 1997;4: Jemmett ME, Kendal KM, Fourre MW, Burton JH. Unrecognized misplacement of endotracheal tubes in a mixed urban to rural emergency medical services setting. Acad Emerg Med 2003;10: Katz SH, Falk JL. Misplaced endotracheal tubes by paramedics in an urban emergency medical services system. Ann Emerg Med 2001;37: Wang HE, Simeone SJ, Weaver MD, Callaway CW. Interruptions in cardiopulmonary resuscitation from paramedic endotracheal intubation. Ann Emerg Med 2009;54:645 52, e Gatward JJ, Thomas MJ, Nolan JP, Cook TM. Effect of chest compressions on the time taken to insert airway devices in a manikin. Br J Anaesth 2008;100: Li J. Capnography alone is imperfect for endotracheal tube placement con.rmation during emergency intubation. J Emerg Med 2001;20: Delguercio LR, Feins NR, Cohn JD, Coomaraswamy RP, Wollman SB, State D. Comparison of blood flow during external and internal cardiac massage in man. Circulation 1965;31(Suppl. 1): Wik L, Kramer-Johansen J, Myklebust H, et al. Quality of cardiopulmonary resuscitation during out-of-hospital cardiac arrest. JAMA 2005;293: Kramer-Johansen J, Myklebust H, Wik L, et al. Quality of out-of-hospital cardiopulmonary resuscitation with real time automated feedback: a prospective interventional study. Resuscitation 2006;71: Sutton RM, Maltese MR, Niles D, et al. Quantitative analysis of chest compression interruptions during in-hospital resuscitation of older children and adolescents. Resuscitation 2009;80: Sutton RM, Niles D, Nysaether J, et al. Quantitative analysis of CPR quality during in-hospital resuscitation of older children and adolescents. Pediatrics 2009;124: Cabrini L, Beccaria P, Landoni G, et al. Impact of impedance threshold devices on cardiopulmonary resuscitation: a systematic review and meta-analysis of randomized controlled studies. Crit Care Med 2008;36: Steen S, Liao Q, Pierre L, Paskevicius A, Sjoberg T. Evaluation of LUCAS, a new device for automatic mechanical compression and active decompression resuscitation. Resuscitation 2002;55: Rubertsson S, Karlsten R. Increased cortical cerebral blood flow with LUCAS; a new device for mechanical chest compressions compared to standard external compressions during experimental cardiopulmonary resuscitation. Resuscitation 2005;65: Timerman S, Cardoso LF, Ramires JA, Halperin H. Improved hemodynamic performance with a novel chest compression device during treatment of in-hospital cardiac arrest. Resuscitation 2004;61: Halperin H, Berger R, Chandra N, et al. Cardiopulmonary resuscitation with a hydraulic-pneumatic band. Crit Care Med 2000;28:N Halperin HR, Paradis N, Ornato JP, et al. Cardiopulmonary resuscitation with a novel chest compression device in a porcine model of cardiac arrest: improved hemodynamics and mechanisms. J Am Coll Cardiol 2004;44: Hallstrom A, Rea TD, Sayre MR, et al. Manual chest compression vs use of an automated chest compression device during resuscitation following out-of-hospital cardiac arrest: a randomized trial. JAMA 2006;295: Ong ME, Ornato JP, Edwards DP, et al. Use of an automated, load-distributing band chest compression device for out-of-hospital cardiac arrest resuscitation. JAMA 2006;295: Larsen AI, Hjornevik AS, Ellingsen CL, Nilsen DW. Cardiac arrest with continuous mechanical chest compression during percutaneous coronary intervention. A report on the use of the LUCAS device. Resuscitation 2007;75:
64 66 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger Wagner H, Terkelsen CJ, Friberg H, et al. Cardiac arrest in the catheterisation laboratory: a 5-year experience of using mechanical chest compressions to facilitate PCI during prolonged resuscitation efforts. Resuscitation 2010;81: Wirth S, Korner M, Treitl M, et al. Computed tomography during cardiopulmonary resuscitation using automated chest compression devices an initial study. Eur Radiol 2009;19: Holmstrom P, Boyd J, Sorsa M, Kuisma M. A case of hypothermic cardiac arrest treated with an external chest compression device (LUCAS) during transport to re-warming. Resuscitation 2005;67: Wik L, Kiil S. Use of an automatic mechanical chest compression device (LUCAS) as a bridge to establishing cardiopulmonary bypass for a patient with hypothermic cardiac arrest. Resuscitation 2005;66: Olasveengen TM, Wik L, Steen PA. Quality of cardiopulmonary resuscitation before and during transport in out-of-hospital cardiac arrest. Resuscitation 2008;76: Sunde K, Wik L, Steen PA. Quality of mechanical, manual standard and active compression decompression CPR on the arrest site and during transport in a manikin model. Resuscitation 1997;34: Laver S, Farrow C, Turner D, Nolan J. Mode of death after admission to an intensive care unit following cardiac arrest. Intensive Care Med 2004;30 : Laurent I, Monchi M, Chiche JD, et al. Reversible myocardial dysfunction in survivors of out-of-hospital cardiac arrest. J Am Coll Cardiol 2002;40: Ruiz-Bailen M, Aguayo de Hoyos E, Ruiz-Navarro S, et al. Reversible myocardial dysfunction after cardiopulmonary resuscitation. Resuscitation 2005;66: Cerchiari EL, Safar P, Klein E, Diven W. Visceral, hematologic and bacteriologic changes and neurologic outcome after cardiac arrest in dogs. The visceral post-resuscitation syndrome. Resuscitation 1993;25: Adrie C, Monchi M, Laurent I, et al. Coagulopathy after successful cardiopulmonary resuscitation following cardiac arrest: implication of the protein C anticoagulant pathway. J Am Coll Cardiol 2005;46: Adrie C, Adib-Conquy M, Laurent I, et al. Successful cardiopulmonary resuscitation after cardiac arrest as a sepsis-like syndrome. Circulation 2002;106: Adrie C, Laurent I, Monchi M, Cariou A, Dhainaou JF, Spaulding C. Postresuscitation disease after cardiac arrest: a sepsis-like syndrome? Curr Opin Crit Care 2004;10: Zwemer CF, Whitesall SE, D Alecy LG. Cardiopulmonary-cerebral resuscitation with 100% oxygen exacerbates neurological dysfunction following nine minutes of normothermic cardiac arrest in dogs. Resuscitation 1994;27: Richards EM, Fiskum G, Rosenthal RE, Hopkins I, McKenna MC. Hyperoxic reperfusion after global ischemia decreases hippocampal energy metabolism. Stroke 2007;38: Vereczki V, Martin E, Rosenthal RE, Hof PR, Hoffman GE, Fiskum G. Normoxic resuscitation after cardiac arrest protects against hippocampaloxidative stress, metabolic dysfunction, and neuronal death. J Cereb Blood Flow Metab 2006;26: Liu Y, Rosenthal RE, Haywood Y, Miljkovic-Lolic M, Vanderhoek JY, Fiskum G. Normoxic ventilation after cardiac arrest reduces oxidation of brain lipids and improves neurological outcome. Stroke 1998;29: Spaulding CM, Joly LM, Rosenberg A, et al. Immediate coronary angiography in survivors of out-of-hospital cardiac arrest. N Engl J Med 1997;336: Sunde K, Pytte M, Jacobsen D, et al. Implementation of a standardised treatment protocol for post resuscitation care after out-of-hospital cardiac arrest. Resuscitation 2007;73: Bendz B, Eritsland J, Nakstad AR, et al. Long-term prognosis after out-of-hospital cardiac arrest and primary percutaneous coronary intervention. Resuscitation 2004;63: Keelan PC, Bunch TJ, White RD, Packer DL, Holmes Jr DR. Early direct coronary angioplasty in survivors of out-of-hospital cardiac arrest. Am J Cardiol 2003;91: A Quintero-Moran B, Moreno R, Villarreal S, et al. Percutaneous coronary intervention for cardiac arrest secondary to ST-elevation acute myocardial infarction. Influence of immediate paramedical/medical assistance on clinical outcome. J Invasive Cardiol 2006;18: Garot P, Lefevre T, Eltchaninoff H, et al. Six-month outcome of emergency percutaneous coronary intervention in resuscitated patients after cardiac arrest complicating ST-elevation myocardial infarction. Circulation 2007;115: Nagao K, Hayashi N, Kanmatsuse K, et al. Cardiopulmonary cerebral resuscitation using emergency cardiopulmonary bypass, coronary reperfusion therapy and mild hypothermia in patients with cardiac arrest outside the hospital. J Am Coll Cardiol 2000;36: Knafelj R, Radsel P, Ploj T, Noc M. Primary percutaneous coronary intervention and mild induced hypothermia in comatose survivors of ventricular fibrillation with ST-elevation acute myocardial infarction. Resuscitation 2007;74: Nielsen N, Hovdenes J, Nilsson F, et al. Outcome, timing and adverse events in therapeutic hypothermia after out-of-hospital cardiac arrest. Acta Anaesthesiol Scand 2009;53: Hovdenes J, Laake JH, Aaberge L, Haugaa H, Bugge JF. Therapeutic hypothermia after out-of-hospital cardiac arrest: experiences with patients treated with percutaneous coronary intervention and cardiogenic shock. Acta Anaesthesiol Scand 2007;51: Wolfrum S, Pierau C, Radke PW, Schunkert H, Kurowski V. Mild therapeutic hypothermia in patients after out-of-hospital cardiac arrest due to acute ST-segment elevation myocardial infarction undergoing immediate percutaneous coronary intervention. Crit Care Med 2008;36: Snyder BD, Hauser WA, Loewenson RB, Leppik IE, Ramirez-Lassepas M, Gum-nit RJ. Neurologic prognosis after cardiopulmonary arrest. III. Seizure activity. Neurology 1980;30: Levy DE, Caronna JJ, Singer BH, Lapinski RH, Frydman H, Plum F. Predicting outcome from hypoxic-ischemic coma. JAMA 1985;253: Krumholz A, Stern BJ, Weiss HD. Outcome from coma after cardiopulmonary resuscitation: relation to seizures and myoclonus. Neurology 1988;38: Zandbergen EG, Hijdra A, Koelman JH, et al. Prediction of poor outcome within the first 3 days of postanoxic coma. Neurology 2006;66: Ingvar M. Cerebral blood flow and metabolic rate during seizures. Relationship to epileptic brain damage. Ann N Y Acad Sci 1986;462: Nolan JP, Laver SR, Welch CA, Harrison DA, Gupta V, Rowan K. Outcome following admission to UK intensive care units after cardiac arrest: a secondary analysis of the ICNARC Case Mix Programme Database. Anaesthesia 2007;62: Losert H, Sterz F, Roine RO, et al. Strict normoglycaemic blood glucose levels in the therapeutic management of patients within 12 h after cardiac arrest might not be necessary. Resuscitation Skrifvars MB, Saarinen K, Ikola K, Kuisma M. Improved survival after inhospital cardiac arrest outside critical care areas. Acta Anaesthesiol Scand 2005;49: Mullner M, Sterz F, Binder M, Schreiber W, Deimel A, Laggner AN. Blood glucose concentration after cardiopulmonary resuscitation influences functional neurological recovery in human cardiac arrest survivors. J Cereb Blood Flow Metab 1997;17: Calle PA, Buylaert WA, Vanhaute OA. Glycemia in the post-resuscitation period. The Cerebral Resuscitation Study Group. Resuscitation 1989;17(Suppl.): S181 8 [discussion S99 S206] Longstreth Jr WT, Diehr P, Inui TS. Prediction of awakening after out-of-hospital cardiac arrest. N Engl J Med 1983;308: Longstreth Jr WT, Inui TS. High blood glucose level on hospital admission and poor neurological recovery after cardiac arrest. Ann Neurol 1984;15: Finfer S, Chittock DR, Su SY, et al. Intensive versus conventional glucose control in critically ill patients. N Engl J Med 2009;360: Preiser JC, Devos P, Ruiz-Santana S, et al. A prospective randomised multicentre controlled trial on tight glucose control by intensive insulin therapy in adult intensive care units: the Glucontrol study. Intensive Care Med 2009;35: Griesdale DE, de Souza RJ, van Dam RM, et al. Intensive insulin therapy and mortality among critically ill patients: a meta-analysis including NICE-SUGAR study data. CMAJ 2009;180: Wiener RS, Wiener DC, Larson RJ. Benefits and risks of tight glucose control in critically ill adults: a meta-analysis. JAMA 2008;300: Krinsley JS, Grover A. Severe hypoglycemia in critically ill patients: risk factors and outcomes. Crit Care Med 2007;35: Meyfroidt G, Keenan DM, Wang X, Wouters PJ, Veldhuis JD, Van den Berghe G. Dynamic characteristics of blood glucose time series during the course of critical illness: effects of intensive insulin therapy and relative association with mortality. Crit Care Med 2010;38: Padkin A. Glucose control after cardiac arrest. Resuscitation 2009;80: Takino M, Okada Y. Hyperthermia following cardiopulmonary resuscitation. Intensive Care Med 1991;17: Hickey RW, Kochanek PM, Ferimer H, Alexander HL, Garman RH, Graham SH. Induced hyperthermia exacerbates neurologic neuronal histologic damage after asphyxial cardiac arrest in rats. Crit Care Med 2003;31: Takasu A, Saitoh D, Kaneko N, Sakamoto T, Okada Y. Hyperthermia: is it an ominous sign after cardiac arrest? Resuscitation 2001;49: Zeiner A, Holzer M, Sterz F, et al. Hyperthermia after cardiac arrest is associated with an unfavorable neurologic outcome. Arch Intern Med 2001;161: Hickey RW, Kochanek PM, Ferimer H, Graham SH, Safar P. Hypothermia and hyperthermia in children after resuscitation from cardiac arrest. Pediatrics 2000;106: Diringer MN, Reaven NL, Funk SE, Uman GC. Elevated body temperature independently contributes to increased length of stay in neurologic intensive care unit patients. Crit Care Med 2004;32: Gunn AJ, Thoresen M. Hypothermic neuroprotection. Neuro Rx 2006;3: Froehler MT, Geocadin RG. Hypothermia for neuroprotection after cardiac arrest: mechanisms, clinical trials and patient care. J Neurol Sci 2007;261: McCullough JN, Zhang N, Reich DL, et al. Cerebral metabolic suppression during hypothermic circulatory arrest in humans. Ann Thorac Surg 1999;67: [discussion ] Mild therapeutic hypothermia to improve the neurologic outcome after cardiac arrest. N Engl J Med 2002;346: Bernard SA, Gray TW, Buist MD, et al. Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia. N Engl J Med 2002;346: Bernard SA, Jones BM, Horne MK. Clinical trial of induced hypothermia in comatose survivors of out-of-hospital cardiac arrest. Ann Emerg Med 1997;30: Oddo M, Schaller MD, Feihl F, Ribordy V, Liaudet L. From evidence to clinical practice: effective implementation of therapeutic hypothermia to improve patient outcome after cardiac arrest. Crit Care Med 2006;34:
65 Podsumowanie Komitetu Wykonawczego ERC Busch M, Soreide E, Lossius HM, Lexow K, Dickstein K. Rapid implementation of therapeutic hypothermia in comatose out-of-hospital cardiac arrest survivors. Acta Anaesthesiol Scand 2006;50: Storm C, Steffen I, Schefold JC, et al. Mild therapeutic hypothermia shortens intensive care unit stay of survivors after out-of-hospital cardiac arrest compared to historical controls. Crit Care 2008;12:R Don CW, Longstreth Jr WT, Maynard C, et al. Active surface cooling protocol to induce mild therapeutic hypothermia after out-of-hospital cardiac arrest: a retrospective before-and-after comparison in a single hospital. Crit Care Med 2009;37: Arrich J. Clinical application of mild therapeutic hypothermia after cardiac arrest. Crit Care Med 2007;35: Holzer M, Mullner M, Sterz F, et al. Efficacy and safety of endovascular cooling after cardiac arrest: cohort study and Bayesian approach. Stroke 2006;37: Polderman KH, Herold I. Therapeutic hypothermia and controlled normothermia in the intensive care unit: practical considerations, side effects, and cooling methods. Crit Care Med 2009;37: Kuboyama K, Safar P, Radovsky A, et al. Delay in cooling negates the beneficial effect of mild resuscitative cerebral hypothermia after cardia arrest in dogs: a prospective, randomized study. Crit Care Med 1993;21: Edgren E, Hedstrand U, Nordin M, Rydin E, Ronquist G. Prediction of outcome after cardiac arrest. Crit Care Med 1987;15: Young GB, Doig G, Ragazzoni A. Anoxic-ischemic encephalopathy: clinical and electrophysiological associations with outcome. Neurocrit Care 2005;2: Al Thenayan E, Savard M, Sharpe M, Norton L, Young B. Predictors of poor neurologic outcome after induced mild hypothermia following cardiac arrest. Neurology 2008;71: Wijdicks EF, Parisi JE, Sharbrough FW. Prognostic value of myoclonus status in comatose survivors of cardiac arrest. Ann Neurol 1994;35: Thomke F, Marx JJ, Sauer O, et al. Observations on comatose survivors of cardiopulmonary resuscitation with generalized myoclonus. BMC Neurol 2005;5: Arnoldus EP, Lammers GJ. Postanoxic coma: good recovery despite myoclonus status. Ann Neurol 1995;38: Celesia GG, Grigg MM, Ross E. Generalized status myoclonicus in acute anoxic and toxic-metabolic encephalopathies. Arch Neurol 1988;45: Morris HR, Howard RS, Brown P. Early myoclonic status and outcome after cardiorespiratory arrest. J Neurol Neurosurg Psychiatry 1998;64: Datta S, Hart GK, Opdam H, Gutteridge G, Archer J. Post-hypoxic myoclonic status: the prognosis is not always hopeless. Crit Care Resusc 2009;11: English WA, Giffin NJ, Nolan JP. Myoclonus after cardiac arrest: pitfalls in diagnosis and prognosis. Anaesthesia 2009;64: Wijdicks EF, Hijdra A, Young GB, Bassetti CL, Wiebe S. Practice parameter: prediction of outcome in comatose survivors after cardiopulmonary resuscitation (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2006;67: Tiainen M, Kovala TT, Takkunen OS, Roine RO. Somatosensory and brainstem auditory evoked potential sincardiac arrest patients treated with hypothermia. Crit Care Med 2005;33: Rossetti AO, Oddo M, Liaudet L, Kaplan PW. Predictors of awakening from post anoxic status epilepticus after therapeutic hypothermia. Neurology 2009;72: Rossetti AO, Logroscino G, Liaudet L, et al. Status epilepticus: an independent outcome predictor after cerebral anoxia. Neurology 2007;69: Fieux F, Losser MR, Bourgeois E, et al. Kidney retrieval after sudden out of hospital refractory cardiac arrest: a cohort of uncontrolled non heart beating donors. Crit Care 2009;13:R Kootstra G. Statement on non-heart-beating donor programs. Transplant Proc 1995;27: Vermeer F, Oude Ophuis AJ, vd Berg EJ, et al. Prospective randomised comparison between thrombolysis, rescue PTCA, and primary PTCA in patients with extensive myocardial infarction admitted to a hospital without PTCA facilities: a safety and feasibility study. Heart 1999;82: Widimsky P, Groch L, Zelizko M, Aschermann M, Bednar F, Suryapranata H. Multicentre randomized trial comparing transport to primary angioplasty vs immediate thrombolysis vs combined strategy for patients with acutemyocardial infarction presenting to a community hospital without a catheterization laboratory. The PRAGUE study. Eur Heart J 2000;21: Widimsky P, Budesinsky T, Vorac D, et al. Long distance transport for primary angioplasty vs immediate thrombolysis in acute myocardial infarction. Final results of the randomized national multicentre trial PRAGUE-2. Eur Heart J 2003;24: LeMay MR, So DY, Dionne R, et al. A city wide protocol for primary PCI in ST-segment elevation myocardial infarction.n Engl J Med 2008;358: Abernathy 3rd JH, McGwin Jr G, Acker 3rd JE, Rue 3rd LW. Impact of a voluntary trauma system on mortality, length of stay, and cost at a level I trauma center. Am Surg 2002;68: Clemmer TP, Orme Jr JF, Thomas FO, Brooks KA. Outcome of critically injured patients treated at Level I trauma centers versus full-service community hospitals. Crit Care Med 1985;13: Culica D, Aday LA, Rohrer JE. Regionalized trauma care system in Texas: implications for redesigning trauma systems. Med Sci Monit 2007;13:SR Hannan EL, Farrell LS, Cooper A, Henry M, Simon B, Simon R. Physiologic trauma triage criteria in adult trauma patients: are they effective in saving lives by transporting patients to trauma centers? J Am Coll Surg 2005;200: Harrington DT, Connolly M, Biffl WL, Majercik SD, Cioffi WG. Transfer times to definitive care facilities are too long: a consequence of an immature trauma system. Ann Surg 2005;241:961 6 [discussion 6 8] Liberman M, Mulder DS, Lavoie A, Sampalis JS. Implementation of a trauma care system: evolution through evaluation. J Trauma 2004;56: MacKenzie EJ, Rivara FP, Jurkovich GJ, et al. A national evaluation of the effect of trauma-center care on mortality. N Engl J Med 2006;354: Mann NC, Cahn RM, Mullins RJ, Brand DM, Jurkovich GJ. Survival among injured geriatric patients during construction of a statewide trauma system. J Trauma 2001;50: Mullins RJ, Veum-Stone J, Hedges JR, et al. Influence of a statewide trauma system on location of hospitalization and outcome of injured patients. J Trauma 1996;40: [discussion 45 46] Mullins RJ, Mann NC, Hedges JR, Worrall W, Jurkovich GJ. Preferential benefit of implementation of a statewide trauma system in one of two adjacent states. J Trauma 1998;44: [discussion 17] Mullins RJ, Veum-Stone J, Helfand M, et al. Outcome of hospitalized injured patients after institution of a trauma system in an urban area. JAMA 1994;271: Mullner R, Goldberg J. An evaluation of the Illinois trauma system. Med Care 1978;16: Mullner R, Goldberg J. Toward an outcome-oriented medical geography: an evaluation of the Illinois trauma/emergency medical services system. Soc Sci Med 1978;12: Nathens AB, Jurkovich GJ, Rivara FP, Maier RV. Effectiveness of state trauma systems in reducing injury-related mortality: a national evaluation. J Trauma 2000;48:25 30 [discussion 1] Nathens AB, Maier RV, Brundage SI, Jurkovich GJ, Grossman DC. The effect of interfacility transfer on outcome in an urban trauma system. J Trauma 2003;55: Nicholl J, Turner J. Effectiveness of a regional trauma system in reducing mortality from major trauma: before and after study. BMJ 1997;315: Potoka DA, Schall LC, Gardner MJ, Stafford PW, Peitzman AB, Ford HR. Impact of pediatric trauma centers on mortality in a statewide system. J Trauma 2000;49: Sampalis JS, Lavoie A, Boukas S, et al. Trauma center designation: initial impact on trauma-related mortality. J Trauma 1995;39:232 7 [discussion 7 9] Sampalis JS, Denis R, Frechette P, Brown R, Fleiszer D, Mulder D. Direct transport to tertiary trauma centers versus transfer from lower level facilities: impact on mortality and morbidity among patients with major trauma. J Trauma 1997;43: [discussion 95 96] Nichol G, Aufderheide TP, Eigel B, et al. Regional systems of care for out-ofhospital cardiac arrest: a policy statement from the American Heart Association. Circulation 2010;121: Nichol G, Soar J. Regional cardiac resuscitation systems of care. Curr Opin Crit Care 2010;16: Soar J, Packham S. Cardiac arrest centres make sense. Resuscitation 2010;81: Tunstall-Pedoe H, Vanuzzo D, Hobbs M, et al. Estimation of contribution of changes in coronary care to improving survival, event rates, and coronary heart disease mortality across the WHO MONICA Project populations. Lancet 2000;355: Fox KA, Cokkinos DV, Deckers J, Keil U, Maggioni A, Steg G. The ENACT study: a pan-european survey of acute coronary syndromes. European Network for Acute Coronary Treatment. Eur Heart J 2000;21: Goodman SG, Huang W, Yan AT, et al. The expanded global registry of acute coronary events: baseline characteristics, management practices, and hospital outcomes of patients with acute coronary syndromes. Am Heart J 2009;158: , e1 e Lowel H, Meisinger C, Heier M, et al. Sex specific trends of sudden cardiac death and acute myocardial infarction: results of the population-based KORA/ MONICA-Augsburg register 1985 to Dtsch Med Wochenschr 2002;127: Thygesen K, Alpert JS, White HD. Universal definition of myocardial infarction. Eur Heart J 2007;28: Van de Werf F, Bax J, Betriu A, et al. Management of acute myocardial infarction in patients presenting with persistent ST-segment elevation: the Task Force on the Management of ST-Segment Elevation Acute Myocardial Infarction of the European Society of Cardiology. Eur Heart J 2008;29: Antman EM, Anbe DT, Armstrong PW, et al. ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 1999 Guidelines for the Management of Patients With Acute Myocardial Infarction). Circulation 2004;110: Douglas PS, Ginsburg GS. The evaluation of chest pain in women. N Engl J Med 1996;334: Solomon CG, Lee TH, Cook EF, et al. Comparison of clinical presentation of acute myocardial infarction in patients older than 65 years of age to younger patients: the Multicenter Chest Pain Study experience. Am J Cardiol 1989;63: Ioannidis JP, Salem D, Chew PW, Lau J. Accuracy and clinical effect of out-ofhospital electrocardiography in the diagnosis of acute cardiac ischemia: a metaanalysis. Ann Emerg Med 2001;37:
66 68 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger Kudenchuk PJ, Ho MT, Weaver WD, et al. Accuracy of computer-interpreted electrocardiography in selecting patients for thrombolytic therapy. MITI Project Investigators. J Am Coll Cardiol 1991;17: Dhruva VN, Abdelhadi SI, Anis A, et al. ST-Segment Analysis Using Wireless Technology in Acute Myocardial Infarction (STAT-MI) trial. J Am Coll Cardiol 2007;50: Antman EM, Tanasijevic MJ, Thompson B, et al. Cardiac-specific troponin I levels to predict the risk of mortality in patients with acute coronary syndromes. N Engl J Med 1996;335: Hess EP, Thiruganasambandamoorthy V, Wells GA, et al. Diagnostic accuracy of clinical prediction rules to exclude acute coronary syndrome in the emergency department setting: a systematic review. CJEM 2008;10: Ramakrishna G, Milavetz JJ, Zinsmeister AR, et al. Effect of exercise treadmill testing and stress imaging on the triage of patients with chest pain: CHEER substudy. Mayo Clin Proc 2005;80: Kearney PM, Baigent C, Godwin J, Halls H, Emberson JR, Patrono C. Do selective cyclo-oxygenase-2 inhibitors and traditional non-steroidal anti-inflammatory drugs increase the risk of atherothrombosis? Meta-analysis of randomised trials. BMJ 2006;332: Rawles JM, Kenmure AC. Controlled trial of oxygen in uncomplicated myocardial infarction. BMJ 1976;1: Wijesinghe M, Perrin K, Ranchord A, Simmonds M, Weatherall M, Beasley R. Routine use of oxygen in the treatment of myocardial infarction: systematic review. Heart 2009;95: Cabello JB, Burls A, Emparanza JI, Bayliss S, Quinn T. Oxygen therapy for acute myocardial infarction. Cochrane Database Syst Rev 2010;6:CD O Driscoll BR, Howard LS, Davison AG. BTS guideline for emergency oxygen use in adult patients. Thorax 2008;63(Suppl. 6):vi Freimark D, Matetzky S, Leor J, et al. Timing of aspirin administration as a determinant of survival of patients with acute myocardial infarction treated with thrombolysis. Am J Cardiol 2002;89: Barbash IM, Freimark D, Gottlieb S, et al. Outcome of myocardial infarction in patients treated with aspirin is enhanced by pre-hospital administration. Cardiology 2002;98: Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001;345: Mehta SR, Yusuf S, Peters RJ, et al. Effects of pretreatment with clopidogrel and aspirin followed by long-term therapy in patients undergoing percutaneous coronary intervention: the PCI-CURE study. Lancet 2001;358: TIMI-11B Investigators, Antman EM, McCabe CH, et al. Enoxaparin prevents death and cardiac ischemic events in unstable angina/non-q-wave myocardial infarction. Results of the thrombolysis in myocardial infarction (TIMI) 11B trial. Circulation 1999;100: Cohen M, Demers C, Gurfinkel EP, et al. A comparison of low-molecular-weight heparin with unfractionated heparin for unstable coronary artery disease. Efficacy and safety of subcutaneous enoxaparin in non-q-wave coronary events study group. N Engl J Med 1997;337: Yusuf S, Mehta SR, Chrolavicius S, et al. Comparison of fondaparinux and enoxaparin in acute coronary syndromes. N Engl J Med 2006;354: Mehta SR, Boden WE, Eikelboom JW, et al. Antithrombotic therapy with fondaparinux in relation to interventional management strategy in patients with ST-and non-st-segment elevation acute coronary syndromes: an individual patient-level combined analysis of the Fifth and Sixth Organization to Assess Strategies in Ischemic Syndromes (OASIS 5 and 6) randomized trials. Circulation 2008;118: Lincoff AM, Bittl JA, Harrington RA, et al. Bivalirudin and provisional glycoprotein IIb/IIIa blockade compared with heparin and planned glycoprotein IIb/ IIIa blockade during percutaneous coronary intervention: REPLACE-2 randomized trial. JAMA 2003;289: Efficacy and safety of tenecteplase in combination with enoxaparin, abciximab, or unfractionated heparin: the ASSENT-3 randomised trial in acute myocardial infarction. Lancet 2001;358: Eikelboom JW, Quinlan DJ, Mehta SR, Turpie AG, Menown IB, Yusuf S. Unfractionated and low-molecular-weight heparin as adjuncts to thrombolysis in aspirin-treated patients with ST-elevation acute myocardialin farction: a metaanalysis of the randomized trials. Circulation 2005;112: Wallentin L, Goldstein P, Armstrong PW, et al. Efficacy and safety of tenecteplase in combination with the low-molecular-weight heparin enoxaparin or unfractionated heparin in the prehospital setting: the Assessment of the Safety and Efficacy of a New Thrombolytic Regimen (ASSENT)-3 PLUS randomized trial in acute myocardial infarction. Circulation 2003;108: Zeymer U, Gitt A, Junger C, et al. Efficacy and safety of enoxaparin in unselected patients with ST-segment elevation myocardial infarction. Thromb Haemost 2008;99: Zeymer U, Gitt A, Zahn R, et al. Efficacy and safety of enoxaparin in combination with and without GP IIb/IIIa inhibitors in unselected patients with ST segment elevation myocardial infarction treated with primary percutaneous coronary intervention. EuroIntervention 2009;4: Bassand JP, Hamm CW, Ardissino D, et al. Guidelines for the diagnosis and treatment of non-st-segment elevation acute coronary syndromes. Eur Heart J 2007;28: Anderson JL, Adams CD, Antman EM, et al. ACC/AHA 2007 guidelines for the management of patients with unstable angina/non ST-elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines for the Management of Patients With Unstable Angina/Non ST-Elevation Myocardial Infarction): developed in collaboration with the American College of Emergency Physicians, the Society for Cardiovascular Angiography and Interventions, and the Society of Thoracic Surgeons: endorsed by the American Association of Cardiovascular and Pulmonary Rehabilitation and the Society for Academic Emergency Medicine. Circulation 2007;116: e Kushner FG, Hand M, Smith SCJJr, et al Focused Updates: ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction (updating the 2004 Guideline and 2007 Focused Update) and ACC/ AHA/SCAI Guidelines on Percutaneous Coronary Intervention (updating the 2005 Guideline and 2007 Focused Update): a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation 2009;120: Erratum in: Circulation. 010 March 30;121(12):e257. Dosage error in article text Boersma E, Maas AC, Deckers JW, Simoons ML. Early thrombolytic treatment in acute myocardial infarction: reappraisal of the golden hour. Lancet 1996;348: Prehospital thrombolytic therapy in patients with suspected acute myocardial infarction. The European Myocardial Infarction Project Group. N Engl J Med 1993;329: Weaver WD, Cerqueira M, Hallstrom AP, et al. Prehospital-initiated vs hospital-initiated thrombolytic therapy. The Myocardial Infarction Triage and Intervention Trial. JAMA 1993;270: Feasibility, safety, and efficacy of domiciliary thrombolysis by general practitioners: Grampian region early anistreplase trial. GREAT Group. BMJ 1992;305: Welsh RC, Travers A, Senaratne M, Williams R, Armstrong PW. Feasibility and applicability of paramedic-based prehospital fibrinolysis in a large North American center. Am Heart J 2006;152: Pedley DK, Bissett K, Connolly EM, et al. Prospective observational cohort study of time saved by prehospital thrombolysis for ST elevation myocardial infarction delivered by paramedics. BMJ 2003;327: Grijseels EW, Bouten MJ, Lenderink T, et al. Pre-hospital thrombolytic therapy with either alteplase or streptokinase. Practical applications, complications and long-term results in 529 patients. Eur Heart J 1995;16: Morrison LJ, Verbeek PR, McDonald AC, Sawadsky BV, Cook DJ. Mortality and prehospital thrombolysis for acute myocardial infarction: a meta-analysis. JAMA 2000;283: Keeley EC, Boura JA, Grines CL. Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review of 23 randomised trials. Lancet 2003;361: Dalby M, Bouzamondo A, Lechat P, Montalescot G. Transfer for primary angioplasty versus immediate thrombolysis in acute myocardial infarction: a metaanalysis. Circulation 2003;108: Steg PG, Bonnefoy E, Chabaud S, et al. Impact of time to treatment on mortality after prehospital fibrinolysis or primary angioplasty: data from the CAPTIM randomized clinical trial. Circulation 2003;108: Bonnefoy E, Steg PG, Boutitie F, et al. Comparison of primary angioplasty and pre-hospital fibrinolysis in acutemyocardial infarction (CAPTIM) trial: a 5-year follow-up. Eur Heart J 2009;30: Kalla K, Christ G, Karnik R, et al. Implementation of guidelines improves the standard of care: the Viennese registry on reperfusion strategies in ST-elevation myocardial infarction (Vienna STEMI registry). Circulation 2006;113: Primary versus tenecteplase-facilitated percutaneous coronary intervention in patients with ST-segment elevation acute myocardial infarction (ASSENT-4 PCI): randomised trial. Lancet 2006;367: Pinto DS, Kirtane AJ, Nallamothu BK, et al. Hospital delays in reperfusion for ST-elevation myocardial infarction: implications when selecting a reperfusion strategy. Circulation 2006;114: Keeley EC, Boura JA, Grines CL. Comparison of primary and facilitated percutaneous coronary interventions for ST-elevation myocardial infarction: quantitative review of randomised trials. Lancet 2006;367: Herrmann HC, Lu J, Brodie BR, et al. Benefit of facilitated percutaneous coronary intervention in high-risk ST-segment elevation myocardial infarction patients presenting to nonpercutaneous coronary intervention hospitals. JACC Cardiovasc Interv 2009;2: Gershlick AH, Stephens-Lloyd A, Hughes S, et al. Rescue angioplasty after failed thrombolytic therapy for acute myocardial infarction. N Engl J Med 2005;353: Danchin N, Coste P, Ferrieres J, et al. Comparison of thrombolysis followed by broad use of percutaneous coronary intervention with primary percutaneous coronary intervention for ST-segment-elevation acute myocardial infarction: data from the french registry on acute ST-elevation myocardial infarction (FAST-MI). Circulation 2008;118: Cantor WJ, Fitchett D, Borgundvaag B, et al. Routine early angioplasty after fibrinolysis for acute myocardial infarction. N Engl J Med 2009;360: Redding JS. The choking controversy: critique of evidence on the Heimlich maneuver. Crit Care Med 1979;7: Kuisma M, Suominen P, Korpela R. Paediatric out-of-hospital cardiac arrests epidemiology and outcome. Resuscitation 1995;30:
67 Podsumowanie Komitetu Wykonawczego ERC Sirbaugh PE, Pepe PE, Shook JE, et al. A prospective, population-based study of the demographics, epidemiology, management, and outcome of out-of-hospital pediatric cardiopulmonary arrest. Ann Emerg Med 1999;33: Hickey RW, Cohen DM, Strausbaugh S, Dietrich AM. Pediatric patients requiring CPR in the prehospital setting. Ann Emerg Med 1995;25: Young KD, Seidel JS. Pediatric cardiopulmonary resuscitation: a collective review. Ann Emerg Med 1999;33: Reis AG, Nadkarni V, Perondi MB, Grisi S, Berg RA. A prospective investigation into the epidemiology of in-hospital pediatric cardiopulmonary resuscitation using the international Utstein reporting style. Pediatrics 2002;109: Young KD, Gausche-Hill M, McClung CD, Lewis RJ. A prospective, population-based study of the epidemiology and outcome of out-of-hospital pediatric cardiopulmonary arrest. Pediatrics 2004;114: Richman PB, Nashed AH. The etiology of cardiac arrest in children and young adults: special considerations for ED management. Am J Emerg Med 1999;17: Engdahl J, Bang A, Karlson BW, Lindqvist J, Herlitz J. Characteristics and outcome among patients suffering from out of hospital cardiac arrest of noncardiac aetiology. Resuscitation 2003;57: Tibballs J, Kinney S. Reduction of hospital mortality and of preventable cardiac arrest and death on introduction of a pediatric medical emergency team. Pediatr Crit Care Med 2009;10: Hunt EA, Zimmer KP, Rinke ML, et al. Transition from a traditional code team to a medical emergency team and categorization of cardiopulmonary arrests in a children s center. Arch Pediatr Adolesc Med 2008;162: Sharek PJ, Parast LM, Leong K, et al. Effect of a rapid response team on hospital-wide mortality and code rates outside the ICU in a Children s Hospital. JAMA 2007;298: Brilli RJ, Gibson R, Luria JW, et al. Implementation of a medical emergency team in a large pediatric teaching hospital prevents respiratory and cardiopulmonary arrests outside the intensive care unit. Pediatr Crit Care Med 2007;8: [quiz 47] Tibballs J, Kinney S, Duke T, Oakley E, Hennessy M. Reduction of paediatric inpatient cardiac arrest and death with a medical emergency team: preliminary results. Arch Dis Child 2005;90: Sagarin MJ, Chiang V, Sakles JC, et al. Rapid sequence intubation for pediatric emergency airway management. Pediatr Emerg Care 2002;18: Moynihan RJ, Brock-Utne JG, Archer JH, Feld LH, Kreitzman TR. The effect of cricoid pressure on preventing gastric insuf.ation in infants and children. Anesthesiology 1993;78: Salem MR, Joseph NJ, Heyman HJ, Belani B, Paulissian R, Ferrara TP. Cricoid compression is effective in obliterating the esophageal lumen in the presence of a nasogastric tube. Anesthesiology 1985;63: Walker RW, Ravi R, Haylett K. Effect of cricoid force on airway calibre in children: a bronchoscopic assessment. Br J Anaesth 2010;104: Khine HH, Corddry DH, Kettrick RG, et al. Comparison of cuffed and uncuffed endotracheal tubes in young children during general anesthesia. Anesthesiology 1997;86: [discussion 27A] Weiss M, Dullenkopf A, Fischer JE, Keller C, Gerber AC. Prospective randomized controlled multi-centre trial of cuffed or uncuffed endotracheal tubes in small children. Br J Anaesth 2009;103: Duracher C, Schmautz E, Martinon C, Faivre J, Carli P, Orliaguet G. Evaluation of cuffed tracheal tube size predicted using the Khine formula in children. Paediatr Anaesth 2008;18: Dullenkopf A, Kretschmar O, Knirsch W, et al. Comparison of tracheal tube cuff diameters with internal transverse diameters of the trachea in children. Acta Anaesthesiol Scand 2006;50: Dullenkopf A, Gerber AC, Weiss M. Fit and seal characteristics of a new paediatric tracheal tube with high volume-low pressure polyurethane cuff. Acta Anaesthesiol Scand 2005;49: Salgo B, Schmitz A, Henze G, et al. Evaluation of a new recommendation for improved cuffed tracheal tube size selection in infants and small children. Acta Anaesthesiol Scand 2006;50: Luten RC, Wears RL, Broselow J, et al. Length-based endotracheal tube and emergency equipment in pediatrics. Ann Emerg Med 1992;21: Deakers TW, Reynolds G, Stretton M, Newth CJ. Cuffed endotracheal tubes in pediatric intensive care. J Pediatr 1994;125: Newth CJ, Rachman B, Patel N, Hammer J. The use of cuffed versus uncuffed endotracheal tubes in pediatric intensive care. J Pediatr 2004;144: Dorsey DP, Bowman SM, Klein MB, Archer D, Sharar SR. Perioperative use of cuffed endotracheal tubes is advantageous in young pediatric burn patients. Burns Mhanna MJ, Zamel YB, Tichy CM, Super DM. The air leak test around the endotracheal tube, as a predictor of postextubation stridor, is age dependent in children. Crit Care Med 2002;30 : Gausche M, Lewis RJ, Stratton SJ, et al. Effect of out-of-hospital pediatric endotracheal intubation on survival and neurological outcome: a controlled clinical trial. JAMA 2000;283: Kelly JJ, Eynon CA, Kaplan JL, de Garavilla L, Dalsey WC. Use of tube condensation as an indicator of endotracheal tube placement. Ann Emerg Med 1998;31: Andersen KH, Hald A. Assessing the position of the tracheal tube: the reliability of different methods. Anaesthesia 1989;44: Andersen KH, Schultz-Lebahn T. Oesophageal intubation can be undetected by auscultation of the chest. Acta Anaesthesiol Scand 1994;38: Van de Louw A, Cracco C, Cerf C, et al. Accuracy of pulse oximetry in the intensive care unit. Intensive Care Med 2001;27: Seguin P, Le Rouzo A, Tanguy M, Guillou YM, Feuillu A, Malledant Y. Evidence for the need of bedside accuracy of pulse oximetry in an intensive care unit. Crit Care Med 2000;28: Aufderheide TP, Sigurdsson G, Pirrallo RG, et al. Hyperventilation-induced hypotension during cardiopulmonary resuscitation. Circulation 2004;109: Aufderheide TP, Lurie KG. Death by hyperventilation: a common and lifethreatening problem during cardiopulmonary resuscitation. Crit Care Med 2004;32:S Borke WB, Munkeby BH, Morkrid L, Thaulow E, Saugstad OD. Resuscitation with 100% O(2) does not protect the myocardium in hypoxic newborn piglets. Arch Dis Child Fetal Neonatal Ed 2004;89:F O Neill JF, Deakin CD. Do we hyperventilate cardiac arrest patients? Resuscitation 2007;73: Bhende MS, Thompson AE, Orr RA. Utility of an end-tidal carbon dioxide detector during stabilization and transport of critically ill children. Pediatrics 1992;89: Bhende MS, LaCovey DC. End-tidal carbon dioxide monitoring in the prehospital setting. Prehosp Emerg Care 2001;5: Ornato JP, Shipley JB, Racht EM, et al. Multicenter study of a portable, handsize, colorimetric end-tidal carbon dioxide detection device. Ann Emerg Med 1992;21: Gonzalez del Rey JA, Poirier MP, Digiulio GA. Evaluation of an ambubag valve with a self-contained, colorimetric end-tidal CO 2 system in the detection of airway mishaps: an animal trial. Pediatr Emerg Care 2000;16: Bhende MS, Karasic DG, Karasic RB. End-tidal carbondioxide changes during cardiopulmonary resuscitation after experimental asphyxial cardiac arrest. Am J Emerg Med 1996;14: DeBehnke DJ, Hilander SJ, Dobler DW, Wickman LL, Swart GL. The hemodynamic and arterial blood gas response to asphyxiation: a canine model of pulseless electrical activity. Resuscitation 1995;30: Ornato JP, Garnett AR, Glauser FL. Relationship between cardiac output and the end-tidal carbon dioxide tension. Ann Emerg Med 1990;19: Mauer D, Schneider T, Elich D, Dick W. Carbon dioxide levels during pre-hospital active compression decompression versus standard cardiopulmonary resuscitation. Resuscitation 1998;39: Kolar M, Krizmaric M, Klemen P, Grmec S. Partial pressure of end-tidal carbon dioxide successful predicts cardiopulmonary resuscitation in the field: a prospective observational study. Crit Care 2008;12:R Sharieff GQ, Rodarte A, Wilton N, Bleyle D. The self-inflating bulb as an airway adjunct: is it reliable in children weighing less than 20 kilograms? Acad Emerg Med 2003;10: Sharieff GQ, Rodarte A, Wilton N, Silva PD, Bleyle D. The self-inflating bulb as an esophageal detector device in children weighing more than twenty kilograms: a comparison of two techniques. Ann Emerg Med 2003;41: Dung NM, Day NPJ, Tam DTH, et al. Fluid replacement in dengue shock syndrome: a randomized, double-blind comparison of four intravenous-fluid regimens. Clin Infect Dis 1999;29: Ngo NT, Cao XT, Kneen R, et al. Acute management of dengue shock syndrome: a randomized double-blind comparison of 4 intravenous fluid regimens in the first hour. Clin Infect Dis 2001;32: Wills BA, Nguyen MD, Ha TL, et al. Comparison of three fluid solutions for resuscitation in dengue shock syndrome. N Engl J Med 2005;353: Upadhyay M, Singhi S, Murlidharan J, Kaur N, Majumdar S. Randomized evaluation of fluid resuscitation with crystalloid (saline) and colloid (polymer from degraded gelatin in saline) in pediatric septic shock. Indian Pediatr 2005;42: Lillis KA, Jaffe DM. Prehospital intravenous access in children. Ann Emerg Med 1992;21: Kanter RK, Zimmerman JJ, Strauss RH, Stoeckel KA. Pediatric emergency intravenous access. Evaluation of a protocol. Am J Dis Child 1986;140: Kleinman ME, Oh W, Stonestreet BS. Comparison of intravenous and endotracheal epinephrine during cardiopulmonary resuscitation in newborn piglets. Crit Care Med 1999;27: Roberts JR, Greenburg MI, Knaub M, Baskin SI. Comparison of the pharmacological effects of epinephrine administered by the intravenous and endotracheal routes. JACEP 1978;7: Zaritsky A. Pediatric resuscitation pharmacology. Members of the medications in pediatric resuscitation panel. Ann Emerg Med 1993;22: Manisterski Y, Vaknin Z, Ben-Abraham R, et al. Endotracheal epinephrine: a call for larger doses. Anesth Analg 2002;95: [table of contents] Efrati O, Ben-Abraham R, Barak A, et al. Endobronchial adrenaline: should it be reconsidered? Dose response and haemodynamic effect in dogs. Resuscitation 2003;59: Saul JP, Scott WA, Brown S, et al. Intravenous amiodarone for incessant tachyarrhythmias in children: a randomized, double-blind, antiarrhythmic drug trial. Circulation 2005;112: Tsung JW, Blaivas M. Feasibility of correlating the pulse check with focused point-of-care echocardiography during pediatric cardiac arrest: a case series. Resuscitation 2008;77: Cummins RO, Graves JR, Larsen MP, et al. Out-of-hospital transcutaneous pacing by emergency medical technicians in patients with asystolic cardiac arrest. N Engl J Med 1993;328:
68 70 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger Sreeram N, Wren C. Supraventricular tachycardia in infants: response to initial treatment. Arch Dis Child 1990;65: Benson Jr D, Smith W, Dunnigan A, Sterba R, Gallagher J. Mechanisms of regular wide QRS tachycardia in infants and children. Am J Cardiol 1982;49: Ackerman MJ, Siu BL, Sturner WQ, et al. Postmortem molecular analysis of SCN5A defects in sudden infant death syndrome. JAMA 2001;286: Arnestad M, Crotti L, Rognum TO, et al. Prevalence of long-qt syndrome gene variants in sudden infant death syndrome. Circulation 2007;115: Cronk LB, Ye B, Kaku T, et al. Novel mechanism for sudden infant death syndrome: persistent late sodium current secondary to mutations in caveolin-3. Heart Rhythm 2007;4: Millat G, Kugener B, Chevalier P, et al. Contribution of long-qt syndrome genetic variants in sudden infant death syndrome. Pediatr Cardiol 2009;30: Otagiri T, Kijima K, Osawa M, et al. Cardiac ion channel gene mutations in sudden infant death syndrome. Pediatr Res 2008;64: Plant LD, Bowers PN, Liu Q, et al. A common cardiac sodium channel variant associated with sudden infant death in African Americans. SCN5A S1103Y. J Clin Invest 2006;116: Tester DJ, Dura M, Carturan E, et al. A mechanism for sudden infant death syndrome (SIDS): stress-induced leak via ryanodine receptors. Heart Rhythm 2007;4: Albert CM, Nam EG, Rimm EB, et al. Cardiac sodium channel gene variants and sudden cardiac death in women. Circulation 2008;117: Chugh SS, Senashova O, Watts A, et al. Postmortem molecular screening in unexplained sudden death. J Am Coll Cardiol 2004;43: Tester DJ, Spoon DB, Valdivia HH, Makielski JC, Ackerman MJ. Targeted mutational analysis of the RyR2-encoded cardiac ryanodine receptor in sudden unexplained death: a molecular autopsy of 49 medical examiner/coroner s cases. Mayo Clin Proc 2004;79: Graham EM, Forbus GA, Bradley SM, Shirali GS, Atz AM. Incidence and outcome of cardiopulmonary resuscitation in patients with shunted single ventricle: advantage of right ventricle to pulmonary artery shunt. J Thorac Cardiovasc Surg 2006;131:e Charpie JR, Dekeon MK, Goldberg CS, Mosca RS, Bove EL, Kulik TJ. Postoperative hemodynamics after Norwood palliation for hypoplastic left heart syndrome. Am J Cardiol 2001;87: Hoffman GM, Mussatto KA, Brosig CL, et al. Systemic venous oxygen saturation after the Norwood procedure and childhood neurodevelopmental outcome. J Thorac Cardiovasc Surg 2005;130: Johnson BA, Hoffman GM, Tweddell JS, et al. Near-infrared spectroscopy in neonates before palliation of hypoplastic left heart syndrome. Ann Thorac Surg 2009;87:571 7 [discussion 7 9] Hoffman GM, Tweddell JS, Ghanayem NS, et al. Alteration of the critical arteriovenous oxygen saturation relationship by sustained afterload reduction after the Norwood procedure. J Thorac Cardiovasc Surg 2004;127: De Oliveira NC, Van Arsdell GS. Practical use of alpha blockade strategy in the management of hypoplastic left heart syndrome following stage one palliation with a Blalock-Taussig shunt. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu 2004;7: Tweddell JS, Hoffman GM, Mussatto KA, et al. Improved survival of patients undergoing palliation of hypoplastic left heart syndrome: lessons learned from 115 consecutive patients. Circulation 2002;106:I Shekerdemian LS, Shore DF, Lincoln C, Bush A, Redington AN. Negativepressure ventilation improves cardiac output after right heart surgery. Circulation 1996;94:II Shekerdemian LS, Bush A, Shore DF, Lincoln C, Redington AN. Cardiopulmonary interactions after Fontan operations: augmentation of cardiac output using negative pressure ventilation. Circulation 1997;96: Booth KL, Roth SJ, Thiagarajan RR, Almodovar MC, del Nido PJ, Laussen PC. Extracorporeal membrane oxygenation support of the Fontan and bidirectional Glenn circulations. Ann Thorac Surg 2004;77: Polderman FN, Cohen J, Blom NA, et al. Sudden unexpected death in children with a previously diagnosed cardiovascular disorder. Int J Cardiol 2004;95: Sanatani S, Wilson G, Smith CR, Hamilton RM, Williams WG, Adatia I. Sudden unexpected death in children with heart disease. Congenit Heart Dis 2006;1: Morris K, Beghetti M, Petros A, Adatia I, Bohn D. Comparison of hyperventilation and inhaled nitric oxide for pulmonary hypertension after repair of congenital heart disease. Crit Care Med 2000;28: Hoeper MM, Galie N, Murali S, et al. Outcome after cardiopulmonary resuscitation in patients with pulmonary arterial hypertension. Am J Respir Crit Care Med 2002;165: Rimensberger PC, Spahr-Schopfer I, Berner M, et al. Inhaled nitric oxide versus aerosolized iloprostin secondary pulmonary hypertension in children with congenital heart disease: vasodilator capacity and cellular mechanisms. Circulation 2001;103: Liu KS, Tsai FC, Huang YK, et al. Extracorporeal life support: a simple and effective weapon for postcardiotomy right ventricular failure. Artif Organs 2009;33: Dhillon R, Pearson GA, Firmin RK, Chan KC, Leanage R. Extracorporeal membrane oxygenation and the treatment of critical pulmonary hypertension in congenital heart disease. Eur J Cardiothorac Surg 1995;9: Arpesella G, Loforte A, Mikus E, Mikus PM. Extracorporeal membrane oxygenation for primary allograft failure. Transplant Proc 2008;40: Strueber M, Hoeper MM, Fischer S, et al. Bridge to thoracic organ transplantation in patients with pulmonary arterial hypertension using a pumpless lung assist device. Am J Transplant 2009;9: Gluckman PD, Wyatt JS, Azzopardi D, et al. Selective head cooling with mild systemic hypothermia after neonatal encephalopathy: multicentre randomised trial. Lancet 2005;365: Battin MR, Penrice J, Gunn TR, Gunn AJ. Treatment of term infants with head cooling and mild systemic hypothermia (35.0 degrees C and 34.5 degrees C) after perinatal asphyxia. Pediatrics 2003;111: Compagnoni G, Pogliani L, Lista G, Castoldi F, Fontana P, Mosca F. Hypothermia reduces neurological damage in asphyxiated newborn infants. Biol Neonate 2002;82: Gunn AJ, Gunn TR, Gunning MI, Williams CE, Gluckman PD. Neuroprotection with prolonged head cooling started before postischemic seizures in fetal sheep. Pediatrics 1998;102: Debillon T, Daoud P, Durand P, et al. Whole-body cooling after perinatal asphyxia: a pilot study in term neonates. Dev Med Child Neurol 2003;45: Shankaran S, Laptook AR, Ehrenkranz RA, et al. Whole-body hypothermia for neo nates with hypoxic-ischemic encephalopathy. N Engl J Med 2005;353: Doherty DR, Parshuram CS, Gaboury I, et al. Hypothermia therapy after pediatric cardiac arrest. Circulation 2009;119: Coimbra C, Boris-Moller F, Drake M, Wieloch T. Diminished neuronal damage in the rat brain by late treatment with the antipyretic drug dipyrone or cooling following cerebral ischemia. Acta Neuropathol 1996;92: Coimbra C, Drake M, Boris-Moller F, Wieloch T. Long-lasting neuroprotective effect of postischemic hypothermia and treatment with an anti-inflammatory/ antipyretic drug. Evidence for chronic encephalopathic processes following ischemia. Stroke 1996;27: Losert H, Sterz F, Roine RO, et al. Strict normoglycaemic blood glucose levels in the therapeutic management of patients within 12 h after cardiac arrest might not be necessary. Resuscitation 2008;76: Oksanen T, Skrifvars MB, Varpula T, et al. Strict versus moderate glucose control after resuscitation from ventricular fibrillation. Intensive Care Med 2007;33: Palme-Kilander C. Methods of resuscitation in low-apgar-score newborn infants a national survey. Acta Paediatr 1992;81: Dahm LS, James LS. Newborn temperature and calculated heat loss in the delivery room. Pediatrics 1972;49: Stephenson J, Du J, Oliver TK. The effect of cooling on blood gas tensions in newborn infants. J Pediatr 1970;76: Gandy GM, Adamsons Jr K, Cunningham N, Silverman WA, James LS. Thermal environment and acid base homeostasis in human infants during the first few hours of life. J Clin Invest 1964;43: Kent AL, Williams J. Increasing ambient operating theatre temperature and wrapping in polyethylene improves admission temperature in premature infants. J Paediatr Child Health 2008;44: Knobel RB, Wimmer Jr JE, Holbert D. Heat loss prevention for preterm infants in the delivery room. J Perinatol 2005;25: Apgar V. A proposal for a new method of evaluation of the newborn infant. Curr Res Anesth Analg 1953: Chamberlain G, Banks J. Assessment of the Apgar score. Lancet 1974;2: Owen CJ, Wyllie JP. Determination of heart rate in the baby at birth. Resuscitation 2004;60: Kamlin CO, Dawson JA, O Donnell CP, et al. Accuracy of pulse oximetry measurement of heart rate of newborn infants in the delivery room. J Pediatr 2008;152: O Donnell CP, Kamlin CO, Davis PG, Carlin JB, Morley CJ. Clinical assessment of infant colour at delivery. Arch Dis Child Fetal Neonatal Ed 2007;92: F Cordero Jr L, Hon EH. Neonatal bradycardia following nasopharyngeal stimulation. J Pediatr 1971;78: Houri PK, Frank LR, Menegazzi JJ, Taylor R. A randomized, controlled trial of two-thumb vs two-finger chest compression in a swine infant model of cardiac arrest [see comment]. Prehosp Emerg Care 1997;1: David R. Closed chest cardiac massage in the newborn infant. Pediatrics 1988;81: Menegazzi JJ, Auble TE, Nicklas KA, Hosack GM, Rack L, Goode JS. Twothumb versus two-finger chest compression during CRP in a swine infant model of cardiac arrest. Ann Emerg Med 1993;22: Thaler MM, Stobie GH. An improved technique of external caridac compression in infants and young children. N Engl J Med 1963;269: Meyer A, Nadkarni V, Pollock A, et al. Evaluation of the Neonatal Resuscitation Program s recommended chest compression depth using computerized tomography imaging. Resuscitation 2010;81: Wyckoff MH, Perlman JM, Laptook AR. Use of volume expansion during delivery room resuscitation in near-term and term infants. Pediatrics 2005;115: Soar J, Deakin CD, Nolan JP, et al. European Resuscitation Council guidelines for resuscitation Section 7. Cardiac arrest in special circumstances. Resuscitation 2005;67(Suppl. 1):S Bronstein AC, Spyker DA, Cantilena Jr LR, Green JL, Rumack BH, Giffin SL Annual Report of the American Association of Poison Control Centers National Poison Data System (NPDS): 26th Annual Report. Clin Toxicol (Phila) 2009;47:
69 Podsumowanie Komitetu Wykonawczego ERC Yanagawa Y, Sakamoto T, Okada Y. Recovery from a psychotropic drug overdose tends to depend on the time from ingestion to arrival, the Glasgow Coma Scale, and a sign of circulatory insufficiency on arrival. Am J Emerg Med 2007;25: Zimmerman JL. Poisonings and overdoses in the intensive care unit: general and specific management issues. Crit Care Med 2003;31: Warner DS, Bierens JJ, Beerman SB, Katz LM. Drowning: a cry for help. Anesthesiology 2009;110: Danzl D. Accidental hypothermia. In: Auerbach P, editor. Wilderness medicine. St. Louis: Mosby; p Paal P, Beikircher W, Brugger H. Avalanche emergencies. Review of the current situation. Anaesthesist 2006;55: Mattu A, Brady WJ, Perron AD. Electrocardiographic manifestations of hypothermia. Am J Emerg Med 2002;20: Ujhelyi MR, Sims JJ, Dubin SA, Vender J, Miller AW. Defibrillation energy requirements and electrical heterogeneity during total body hypothermia. Crit Care Med 2001;29: Walpoth BH, Walpoth-Aslan BN, Mattle HP, et al. Outcome of survivors of accidental deep hypothermia and circulatory arrest treated with extracorporeal blood warming. N Engl J Med 1997;337: Bouchama A, Knochel JP. Heat stroke. N Engl J Med 2002;346: Bouchama A. The 2003 European heat wave. Intensive Care Med 2004;30: Coris EE, Ramirez AM, Van Durme DJ. Heat illness in athletes: the dangerous combination of heat, humidity and exercise. Sports Med 2004;34: Grogan H, Hopkins PM. Heat stroke: implications for critical care and anaesthesia. Br J Anaesth 2002;88: Hadad E, Weinbroum AA, Ben-Abraham R. Drug-induced hyperthermia and muscle rigidity: a practical approach. Eur J Emerg Med 2003;10: Halloran LL, Bernard DW. Management of drug-induced hyperthermia. Curr Opin Pediatr 2004;16: Bouchama A, Dehbi M, Chaves-Carballo E. Cooling and hemodynamic management in heatstroke: practical recommendations. Crit Care 2007;11:R Eshel G, Safar P, Sassano J, Stezoski W. Hyperthermia-induced cardiac arrest in dogs and monkeys. Resuscitation 1990;20: Eshel G, Safar P, Radovsky A, Stezoski SW. Hyperthermia-induced cardiac arrest in monkeys: limited efficacy of standard CPR. Aviat Space Environ Med 1997;68: Masoli M, Fabian D, Holt S, Beasley R. The global burden of asthma: executive summary of the GINA Dissemination Committee report. Allergy 2004;59: Global Strategy for Asthma Management and Prevention 2009 [accessed ] Williams TJ, Tuxen DV, Scheinkestel CD, Czarny D, Bowes G. Risk factors for morbidity in mechanically ventilated patients with acute severe asthma. Am Rev Respir Dis 1992;146: Bowman FP, Menegazzi JJ, Check BD, Duckett TM. Lower esophageal sphincter pressure during prolonged cardiac arrest and resuscitation. Ann Emerg Med 1995;26: Leatherman JW, McArthur C, Shapiro RS. Effect of prolongation of expiratory time on dynamic hyperinflation in mechanically ventilated patients with severe asthma. Crit Care Med 2004;32: Lapinsky SE, Leung RS. Auto-PEEP and electromechanical dissociation. N Engl J Med 1996;335: Rogers PL, Schlichtig R, Miro A, Pinsky M. Auto-PEEP during CPR. An occult cause of electromechanical dissociation? Chest 1991;99: Rosengarten PL, Tuxen DV, Dziukas L, Scheinkestel C, Merrett K, Bowes G. Circulatory arrest induced by intermittent positive pressure ventilation in a patient with severe asthma. Anaesth Intensive Care 1991;19: Sprung J, Hunter K, Barnas GM, Bourke DL. Abdominal distention is not always a sign of esophageal intubation: cardiac arrest due to auto-peep. Anesth Analg 1994;78: Harrison R. Chest compression first aid for respiratory arrest due to acute asphyxic asthma. Emerg Med J 2010;27: Deakin CD, McLaren RM, Petley GW, Clewlow F, Dalrymple-Hay MJ. Effects of positive end-expiratory pressure on transthoracic impedance implications for defibrillation. Resuscitation 1998;37: Galbois A, Ait-Oufella H, Baudel JL, et al. Pleural ultrasound compared to chest radiographic detection of pneumothorax resolution after drainage. Chest Mabuchi N, Takasu H, Ito S, et al. Successful extracorporeal lung assist (ECLA) for a patient with severe asthma and cardiac arrest. Clin Intensive Care 1991;2: Martin GB, Rivers EP, Paradis NA, Goetting MG, Morris DC, Nowak RM. Emergency department cardiopulmonary bypass in the treatment of human cardiac arrest. Chest 1998;113: Soar J, Pumphrey R, Cant A, et al. Emergency treatment of anaphylactic reactions guidelines for healthcare providers. Resuscitation 2008;77: Soar J. Emergency treatment of anaphylaxis in adults: concise guidance. Clin Med 2009;9: Charalambous CP, Zipitis CS, Keenan DJ. Chest reexploration in the intensive care unit after cardiac surgery: a safe alternative to returning to the operating theater. Ann Thorac Surg 2006;81: McKowen RL, Magovern GJ, Liebler GA, Park SB, Burkholder JA, Maher TD. Infectious complications and cost-effectiveness of open resuscitation in the surgical intensive care unit after cardiac surgery. Ann Thorac Surg 1985;40: Pottle A, Bullock I, Thomas J, Scott L. Survival to discharge following Open Chest Cardiac Compression (OCCC). A 4-year retrospective audit in a cardiothoracic specialist centre Royal Brompton and Harefield NHS Trust, United Kingdom. Resuscitation 2002;52: Mackay JH, Powell SJ, Osgathorp J, Rozario CJ. Six-year prospective audit of chest reopening after cardiac arrest. Eur J Cardiothorac Surg 2002;22: Birdi I, Chaudhuri N, Lenthall K, Reddy S, Nashef SA. Emergency reinstitution of cardiopulmonary bypass following cardiac surgery: outcome justifies the cost. Eur J Cardiothorac Surg 2000;17: el-banayosy A, Brehm C, Kizner L, et al. Cardiopulmonary resuscitation after cardiac surgery: a two-year study. J Cardiothorac Vasc Anesth 1998;12: Anthi A, Tzelepis GE, Alivizatos P, Michalis A, Palatianos GM, Geroulanos S. Unexpected cardiac arrest after cardiac surgery: incidence, predisposing causes, and outcome of open chest cardiopulmonary resuscitation. Chest 1998;113: Wahba A, Gotz W, Birnbaum Defi Outcome of cardiopulmonary resuscitation following open heart surgery. Scand Cardiovasc J 1997;31: Kaiser GC, Naunheim KS, Fiore AC, et al. Reoperation in the intensive care unit. Ann Thorac Surg 1990;49:903 7 [discussion 8] Rhodes JF, Blaufox AD, Seiden HS, et al. Cardiac arrest in infants after congenital heart surgery. Circulation 1999;100:II Kempen PM, Allgood R. Right ventricular rupture during closed-chest cardiopulmonary resuscitation after pneumonectomy with pericardiotomy: a case report. Crit Care Med 1999;27: Bohrer H, Gust R, Bottiger BW. Cardiopulmonary resuscitation after cardiac surgery. J Cardiothorac Vasc Anesth 1995;9: Klintschar M, Darok M, Radner H. Massive injury to the heart after attempted active compression decompression cardiopulmonary resuscitation. Int J Legal Med 1998;111: Fosse E, Lindberg H. Left ventricular rupture following external chest compression. Acta Anaesthesiol Scand 1996;40: Li Y, Wang H, Cho JH, et al. Defibrillation delivered during the upstroke phase of manual chest compression improves shock success. Crit Care Med 2010;38: Li Y, Yu T, Ristagno G, et al. The optimal phasic relationship between synchronized shock and mechanical chest compressions. Resuscitation 2010;81: Rosemurgy AS, Norris PA, Olson SM, Hurst JM, Albrink MH. Prehospital traumatic cardiac arrest: the cost of futility. J Trauma 1993;35: Shimazu S, Shatney CH. Outcomes of trauma patients with no vital signs on hospital admission. J Trauma 1983;23: Battistella FD, Nugent W, Owings JT, Anderson JT. Field triage of the pulseless trauma patient. Arch Surg 1999;134: Stockinger ZT, McSwain Jr NE. Additional evidence in support of withholding or terminating cardiopulmonary resuscitation for trauma patients in the field. J Am Coll Surg 2004;198: Fulton RL, Voigt WJ, Hilakos AS. Confusion surrounding the treatment of traumatic cardiac arrest. J Am Coll Surg 1995;181: Pasquale MD, Rhodes M, Cipolle MD, Hanley T, Wasser T. Defining dead on arrival : impact on a level I trauma center. J Trauma 1996;41: Stratton SJ, Brickett K, Crammer T. Prehospital pulseless, unconscious penetrating trauma victims: field assessments associated with survival. J Trauma 1998;45: Maron BJ, Estes 3rd NA. Commotio cordis. N Engl J Med 2010;362: Maron BJ, Gohman TE, Kyle SB, Estes 3rd NA, Link MS. Clinical profile and spectrum of commotio cordis. JAMA 2002;287: Maron BJ, Estes 3rd NA, Link MS. Task Force 11: commotio cordis. J Am Coll Cardiol 2005;45: Nesbitt AD, Cooper PJ, Kohl P. Rediscovering commotio cordis. Lancet 2001;357: Link MS, Estes M, Maron BJ. Sudden death caused by chest wall trauma (commotio cordis). In: Kohl P, Sachs F, Franz MR, editors. Cardiac mechano-electric feedback and arrhythmias: from pipette to patient. Philadelphia: Elsevier Saunders; p Cera SM, Mostafa G, Sing RF, Sarafin JL, Matthews BD, Heniford BT. Physiologic predictors of survival in post-traumatic arrest. Am Surg 2003;69: Esposito TJ, Jurkovich GJ, Rice CL, Maier RV, Copass MK, Ashbaugh DG. Reappraisal of emergency room thoracotomy in a changing environment. J Trauma 1991;31:881 5 [discussion 5 7] Martin SK, Shatney CH, Sherck JP, et al. Blunt trauma patients with pre-hospital pulseless electrical activity (PEA): poor ending assured. J Trauma 2002;53: [discussion 80 81] Domeier RM, McSwain Jr NE, Hopson LR, et al. Guidelines for withholding or termination of resuscitation in prehospital traumatic cardiopulmonary arrest. J Am Coll Surg 2003;196: Gervin AS, Fischer RP. The importance of prompt transport of salvage of patients with penetrating heart wounds. J Trauma 1982;22: Branney SW, Moore EE, Feldhaus KM, Wolfe RE. Critical analysis of two decades of experience with postinjury emergency department thoracotomy in a regional trauma center. J Trauma 1998;45:87 94 [discussion 5] Durham III LA, Richardson RJ, Wall Jr MJ, Pepe PE, Mattox KL. Emergency center thoracotomy: impact of prehospital resuscitation. J Trauma 1992;32: Frezza EE, Mezghebe H. Is 30 minutes the golden period to perform emergency room thoratomy (ERT) in penetrating chest injuries? J Cardiovasc Surg (Torino) 1999;40: Powell DW, Moore EE, Cothren CC, et al. Is emergency department resuscitative thoracotomy futile care for the critically injured patient requiring prehospital cardiopulmonary resuscitation? J Am Coll Surg 2004;199:
70 72 J.P. Nolan, J. Soar, D.A. Zideman, D. Biarent, L.L. Bossaert, Ch. Deakin, R.W. Koster, J. Wyllie, B. Böttiger Coats TJ, Keogh S, Clark H, Neal M. Prehospital resuscitative thoracotomy for cardiac arrest after penetrating trauma: rationale and case series. J Trauma 2001;50: Wise D, Davies G, Coats T, Lockey D, Hyde J, Good A. Emergency thoracotomy: how to do it. Emerg Med J 2005;22: Kwan I, Bunn F, Roberts I. Spinal immobilisation for trauma patients. Cochrane Database Syst Rev 2001:CD Practice management guidelines for emergency department thoracotomy. Working Group, Ad Hoc Subcommittee on Outcomes, American College of Surgeons-Committee on Trauma. J Am Coll Surg 2001;193: Walcher F, Kortum S, Kirschning T, Weihgold N, Marzi I. Optimized management of polytraumatized patients by prehospital ultrasound. Unfallchirurg 2002;105: Kirschning T, Brenner F, Stier M, Weber CF, Walcher F. Pre-hospital emergency sonography of trauma patients. Anaesthesist 2009;58: Department of Health, Welsh Office, Scottish Office Department of Health, Department of Health and Social Services, Northern Ireland. Why mothers die. Report on confidential enquiries into maternal deaths in the United Kingdom, London: The Stationery Office; Hogan MC, Foreman KJ, Naghavi M, et al. Maternal mortality for 181 countries, : a systematic analysis of progress towards Millennium Development Goal 5. Lancet 2010;375: Lewis G. The Confidential Enquiry into Maternal and Child Health (CEMACH). Saving Mothers Lives: reviewing maternal deaths to make motherhood safer The Seventh Report of the Confidential Enquiries into Maternal Deaths in the United Kingdom. London: CEMACH; Page-Rodriguez A, Gonzalez-Sanchez JA. Perimortem cesarean section of twin pregnancy: case report and review of the literature. Acad Emerg Med 1999;6: Cardosi RJ, Porter KB. Cesarean delivery of twins during maternal cardiopulmonary arrest. Obstet Gynecol 1998;92: Johnson MD, Luppi CJ, Over DC. Cardiopulmonary resuscitation. In: Gambling DR, Douglas MJ, editors. Obstetric anesthesia and uncommon disorders. Philadelphia: W.B. Saunders; p Nanson J, Elcock D, Williams M, Deakin CD. Do physiological changes in pregnancy change defibrillation energy requirements? Br J Anaesth 2001;87: Katz VL, Dotters DJ, Droegemueller W. Perimortem cesarean delivery. Obstet Gynecol 1986;68: American Heart Association in collaboration with International Liaison Committee on Resuscitation. Guidelines 2000 for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation 2000;102(Suppl.):I Chapter 4; Part 6: cardiac arrest associated with pregnancy. Cummins R, Hazinski M, Field J, editors. ACLS the reference textbook. Dallas: American Heart Association; p Budnick LD. Bathtub-related electrocutions in the United States, 1979 to JAMA 1984;252: Lightning-associated deaths United States, MMWR Morb Mortal Wkly Rep 1998;47: Geddes LA, Bourland JD, Ford G. The mechanism underlying sudden death from electric shock. Med Instrum 1986;20: Cooper MA. Lightning injuries: prognostic signs for death. Ann Emerg Med 1980;9: Kleinschmidt-DeMasters BK. Neuropathology of lightning-strike injuries. Semin Neurol 1995;15: Stewart CE. When lightning strikes. Emerg Med Serv 2000;29:57 67 [quiz 103] Cooper MA. Emergent care of lightning and electrical injuries. Semin Neurol 1995;15: Duclos PJ, Sanderson LM. An epidemiological description of lightning-related deaths in the United States. Int J Epidemiol 1990;19: Epperly TD, Stewart JR. The physical effects of lightning injury. J Fam Pract 1989;29: Whitcomb D, Martinez JA, Daberkow D. Lightning injuries. South Med J 2002;95: Chamberlain DA, Hazinski MF. Education in resuscitation. Resuscitation 2003;59: Yeung J, Perkins GD. Timing of drug administration during CPR and the role of simulation. Resuscitation 2010;81: Berdowski J, Schmohl A, Tijssen JG, Koster RW. Time needed for a regional emergency medical system to implement resuscitation Guidelines 2005 The Netherlands experience. Resuscitation 2009;80: Bigham BL, Koprowicz K, Aufderheide TP, et al. Delayed Prehospital Implementation of the 2005 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiac Care. Prehosp Emerg Care Andersen PO, Jensen MK, Lippert A, Ostergaard D. Identifying non-technical skills and barriers for improvement of team work in cardiac arrest teams. Resuscitation 2010;81: Flin R, Patey R, Glavin R, Maran N. Anaesthetists non-technical skills. Br J Anaesth Axelsson A, Thoren A, Holmberg S, Herlitz J. Attitudes of trained Swedish lay rescuers toward CPR performance in an emergency: a survey of 1012 recently trained CPR rescuers. Resuscitation 2000;44: Hubble MW, Bachman M, Price R, Martin N, Huie D. Willingness of high school students to perform cardiopulmonary resuscitation and automated external defibrillation. Prehosp Emerg Care 2003;7: Swor RA, Jackson RE, Compton S, et al. Cardiac arrest in private locations: different strategies are needed to improve outcome. Resuscitation 2003;58: Swor R, Khan I, Domeier R, Honeycutt L, Chu K, Compton S. CPR training and CPR performance: do CPR-trained bystanders perform CPR? Acad Emerg Med 2006;13: Vaillancourt C, Stiell IG, Wells GA. Understanding and improving low bystander CPR rates: a systematic review of the literature. CJEM 2008;10: Boucek CD, Phrampus P, Lutz J, Dongilli T, Bircher NG. Willingness to perform mouth-to-mouth ventilation by health care providers: a survey. Resuscitation 2009;80: Caves ND, Irwin MG. Attitudes to basic life support among medical students following the 2003 SARS outbreak in Hong Kong. Resuscitation 2006;68: Coons SJ, Guy MC. Performing bystander CPR for sudden cardiac arrest: behavioral intentions among the general adult population in Arizona. Resuscitation 2009;80: Dwyer T. Psychological factors inhibit family members confidence to initiate CPR. Prehosp Emerg Care 2008;12: Jelinek GA, Gennat H, Celenza T, O Brien D, Jacobs I, Lynch D. Community attitudes towards performing cardiopulmonary resuscitation in Western Australia. Resuscitation 2001;51: Johnston TC, Clark MJ, Dingle GA, FitzGerald G. Factors influencing Queenslanders willingness to perform bystander cardiopulmonary resuscitation. Resuscitation 2003;56: Kuramoto N, Morimoto T, Kubota Y, et al. Public perception of and willingness to perform bystander CPR in Japan. Resuscitation 2008;79: Omi W, Taniguchi T, Kaburaki T, et al. The attitudes of Japanese high school students toward cardiopulmonary resuscitation. Resuscitation 2008;78: Riegel B, Mosesso VN, Birnbaum A, et al. Stress reactions and perceived difficulties of lay responders to a medical emergency. Resuscitation 2006;70: Shibata K, Taniguchi T, Yoshida M, Yamamoto K. Obstacles to bystander cardiopulmonary resuscitation in Japan. Resuscitation 2000;44: Taniguchi T, Omi W, Inaba H. Attitudes toward the performance of bystander cardiopulmonary resuscitation in Japan. Resuscitation 2007;75: Moser DK, Dracup K, Doering LV. Effect of cardiopulmonary resuscitation training for parents of high-risk neonates on perceived anxiety, control, and burden. Heart Lung 1999;28: Axelsson A, Herlitz J, Ekstrom L, Holmberg S. Bystander-initiated cardiopulmonary resuscitation out-of-hospital. A first description of the bystanders and their experiences. Resuscitation 1996;33: Donohoe RT, Haefeli K, Moore F. Public perceptions and experiences of myocardial infarction, cardiac arrest and CPR in London. Resuscitation 2006;71: Hamasu S, Morimoto T, Kuramoto N, et al. Effects of BLS training on factors associated with attitude toward CPR in college students. Resuscitation 2009;80: Parnell MM, Pearson J, Galletly DC, Larsen PD. Knowledge of and attitudes towards resuscitation in New Zealand high-school students. Emerg Med J 2006;23: Swor R, Compton S, Farr L, et al. Perceived self-efficacy in performing and willingness to learn cardiopulmonary resuscitation in an elderly population in a suburban community. Am J Crit Care 2003;12: Perkins GD, Walker G, Christensen K, Hulme J, Monsieurs KG. Teaching recognition of agonal breathing improves accuracy of diagnosing cardiac arrest. Resuscitation 2006;70: Yeung J, Meeks R, Edelson D, Gao F, Soar J, Perkins GD. The use of CPR feedback/prompt devices during training and CPR performance: a systematic review. Resuscitation 2009;80: Lam KK, Lau FL, Chan WK, Wong WN. Effect of severe acute respiratory syndrome on bystander willingness to perform cardiopulmonary resuscitation (CPR) is compression-only preferred to standard CPR? Prehosp Disaster Med 2007;22: Locke CJ, Berg RA, Sanders AB, et al. Bystander cardiopulmonary resuscitation. Concerns about mouth-to-mouth contact. Arch Intern Med 1995;155: Hoke RS, Chamberlain DA, Handley AJ. A reference automated external defibrillator provider course for Europe. Resuscitation 2006;69: Lynch B, Einspruch EL, Nichol G, Becker LB, Aufderheide TP, Idris A. Effectiveness of a 30-min CPR self-instruction program for lay responders: a controlled randomized study. Resuscitation 2005;67: Todd KH, Braslow A, Brennan RT, et al. Randomized, controlled trial of video self-instruction versus traditional CPR training. Ann Emerg Med 1998;31: Einspruch EL, Lynch B, Aufderheide TP, Nichol G, Becker L. Retention of CPR skills learned in a traditional AHA Heartsaver course versus 30-min video self-training: a controlled randomized study. Resuscitation 2007;74: Todd KH, Heron SL, Thompson M, Dennis R, O Connor J, Kellermann AL. Simple CPR: a randomized, controlled trial of video self-instructional cardiopulmonary resuscitation training in an African American church congregation. Ann Emerg Med 1999;34: Reder S, Cummings P, Quan L. Comparison of three instructional methods for teaching cardiopulmonary resuscitation and use of an automatic external defibrillator to high school students. Resuscitation 2006;69:
71 Podsumowanie Komitetu Wykonawczego ERC Roppolo LP, Pepe PE, Campbell L, et al. Prospective, randomized trial of the effectiveness and retention of 30-min layperson training for cardiopulmonary resuscitation and automated external defibrillators: The American Airlines Study. Resuscitation 2007;74: Batcheller AM, Brennan RT, Braslow A, Urrutia A, Kaye W. Cardiopulmonary resuscitation performance of subjects over forty is better following half-hour video self-instruction compared to traditional four-hour classroom training. Resuscitation 2000;43: Braslow A, Brennan RT, Newman MM, Bircher NG, Batcheller AM, Kaye W. CPR training without an instructor: development and evaluation of a video selfinstructional system for effective performance of cardiopulmonary resuscitation. Resuscitation 1997;34: Isbye DL, Rasmussen LS, Lippert FK, Rudolph SF, Ringsted CV. Laypersons may learn basic life support in 24 min using a personal resuscitation manikin. Resuscitation 2006;69: Moule P, Albarran JW, Bessant E, Brownfield C, Pollock J. A non-randomized comparison of e-learning and classroom delivery of basic life support with automated external defibrillator use: a pilot study. Int J Nurs Pract 2008;14: Liberman M, Golberg N, Mulder D, Sampalis J. Teaching cardiopulmonary resuscitation to CEGEP students in Quebec a pilot project. Resuscitation 2000;47: Jones I, Handley AJ, Whitfield R, Newcombe R, Chamberlain D. A preliminary feasibility study of a short DVD-based distance-learning package for basic life support. Resuscitation 2007;75: Brannon TS, White LA, Kilcrease JN, Richard LD, Spillers JG, Phelps CL. Use of instructional video to prepare parents for learning infant cardiopulmonary resuscitation. Proc (Bayl Univ Med Cent) 2009;22: de Vries W, Turner N, Monsieurs K, Bierens J, Koster R. Comparison of instructor-led automated external defibrillation training and three alternative DVDbased training methods. Resuscitation 2010;81: Perkins GD, Mancini ME. Resuscitation training for healthcare workers. Resuscitation 2009;80: Spooner BB, Fallaha JF, Kocierz L, Smith CM, Smith SC, Perkins GD. An evaluation of objective feedback in basic life support (BLS) training. Resuscitation 2007;73: Andresen D, Arntz HR, Gra.ing W, et al. Public access resuscitation program including defibrillator training for laypersons: a randomized trial to evaluate the impact of training course duration. Resuscitation 2008;76: Smith KK, Gilcreast D, Pierce K. Evaluation of staff s retention of ACLS and BLS skills. Resuscitation 2008;78: Woollard M, Whitfeild R, Smith A, et al. Skill acquisition and retention in automated external defibrillator (AED) use and CPR by lay responders: a prospective study. Resuscitation 2004;60: Berden HJ, Willems FF, Hendrick JM, Pijls NH, Knape JT. How frequently should basic cardiopulmonary resuscitation training be repeated to maintain adequate skills? BMJ 1993;306: Woollard M, Whit.eld R, Newcombe RG, Colquhoun M, Vetter N, Chamberlain D. Optimal refresher training intervals for AED and CPR skills: a randomised controlled trial. Resuscitation 2006;71: Riegel B, Nafziger SD, McBurnie MA, et al. How well are cardiopulmonary resuscitation and automated external defibrillator skills retained over time? Results from the Public Access Defibrillation (PAD) trial. Acad Emerg Med 2006;13: Beckers SK, Fries M, Bickenbach J, et al. Retention of skills in medical students following minimal theoretical instructions on semi and fully automated external defibrillators. Resuscitation 2007;72: Perkins GD, Lockey AS. Defibrillation-safety versus efficacy. Resuscitation 2008;79: Perkins GD, Barrett H, Bullock I, et al. The Acute Care Undergraduate TEaching (ACUTE) Initiative: consensus development of core competencies in acute care for undergraduates in the United Kingdom. Intensive Care Med 2005;31: Schwid HA, Rooke GA, Ross BK, Sivarajan M. Use of a computerized advanced cardiac life support simulator improves retention of advanced cardiac life support guidelines better than a textbook review. Crit Care Med 1999;27: Polglase RF, Parish DC, Buckley RL, Smith RW, Joiner TA. Problem-based ACLS instruction: a model approach for undergraduate emergency medical education. Ann Emerg Med 1989;18: Clark LJ, Watson J, Cobbe SM, Reeve W, Swann IJ, Macfarlane PW. CPR 98: a practical multimedia computer-based guide to cardiopulmonary resuscitation for medical students. Resuscitation 2000;44: Hudson JN. Computer-aided learning in the real world of medical education: does the quality of interaction with the computer affect student learning? Med Educ 2004;38: Jang KS, Hwang SY, Park SJ, Kim YM, Kim MJ. Effects of a web-based teaching method on undergraduate nursing students learning of electrocardiography. J Nurs Educ 2005;44: Kim JH, Kim WO, Min KT, Yang JY, Nam YT. Learning by computer simulation does not lead to better test performance than textbook study in the diagnosis and treatment of dysrhythmias. J Clin Anesth 2002;14: Leong SL, Baldwin CD, Adelman AM. Integrating web-based computer cases into a required clerkship: development and evaluation. Acad Med 2003;78: Rosser JC, Herman B, Risucci DA, Murayama M, Rosser LE, Merrell RC. Effectiveness of a CD-ROM multimedia tutorial in transferring cognitive knowledge essential for laparoscopic skill training. Am J Surg 2000;179: Papadimitriou L, Xanthos T, Bassiakou E, Stroumpoulis K, Barouxis D, Iacovidou N. Distribution of pre-course BLS/AED manuals does not influence skill acquisition and retention in lay rescuers: a randomised study. Resuscitation 2010;81: Perkins GD. Simulation in resuscitation training. Resuscitation 2007;73: Duran R, Aladag N, Vatansever U, Kucukugurluoglu Y, Sut N, Acunas B. Proficiency and knowledge gained and retained by pediatric residents after neonatal resuscitation course. Pediatr Int 2008;50: Anthonypillai F. Retention of advanced cardiopulmonary resuscitation knowledge by intensive care trained nurses. Intensive Crit Care Nurs 1992;8: Boonmak P, Boonmak S, Srichaipanha S, Poomsawat S. Knowledge and skill after brief ACLS training. J Med Assoc Thai 2004;87: Kaye W, Wynne G, Marteau T, et al. An advanced resuscitation training course for preregistration house officers. J R Coll Physicians Lond 1990;24: Semeraro F, Signore L, Cerchiari EL. Retention of CPR performance in anaesthetists. Resuscitation 2006;68: Skidmore MB, Urquhart H. Retention of skills in neonatal resuscitation. Paediatr Child Health 2001;6: Trevisanuto D, Ferrarese P, Cavicchioli P, Fasson A, Zanardo V, Zacchello F. Knowledge gained by pediatric residents after neonatal resuscitation program courses. Paediatr Anaesth 2005;15: Young R, King L. An evaluation of knowledge and skill retention following an in-house advanced life support course. Nurs Crit Care 2000;5: Grant EC, Marczinski CA, Menon K. Using pediatric advanced life support in pediatric residency training: does the curriculum need resuscitation? Pediatr Crit Care Med 2007;8: O Steen DS, Kee CC, Minick MP. The retention of advanced cardiac life support knowledge among registered nurses. J Nurs Staff Dev 1996;12: Hammond F, Saba M, Simes T, Cross R. Advanced life support: retention of registered nurses knowledge 18 months after initial training. Aust Crit Care 2000;13: Baskett PJ, Lim A. The varying ethical attitudes towards resuscitation in Europe. Resuscitation 2004;62:
72 Publikacja przygotowana przez Europejską Radę Resuscytacji (ERC) przy współpracy z Polską Radą Resuscytacji (PRR). Tekst tłumaczony przez Polską Radę Resuscytacji. Wiedza i praktyka w zakresie resuscytacji krążeniowo-oddechowej to stale zmieniająca się dziedzina medycyny. W miarę rozwoju wiedzy oraz postępu w nauce i doświadczeniu klinicznym zmienia się w sposób ciągły również praktyka medycz na oraz sposób stosowania leków. Czytelnik tego podręcznika jest zobowiązany do zapoznania się z aktualnymi wiado mościami na temat przedstawionych sposobów postępowania i farmakoterapii ze szczególnym uwzględnieniem informacji producentów na temat dawek, czasu i drogi podawania oraz efektów ubocznych stosowanych leków. Na każdej z osób praktykujących medycynę resuscytacji spoczywa osobista odpowiedzialność za stosowane metody lecznicze, których uży cie powinno być oparte na gruntownej wiedzy i umiejętnościach praktycznych z zachowaniem niezbędnych warunków bez pieczeństwa własnego i pacjenta. Wydawcy oraz redaktorzy niniejszego opracowania nie ponoszą odpowiedzialności za szkody, które mogłyby być w jakikolwiek sposób związane z materiałem zawartym w tej książce. Bibliografia do wszystkich rozdziałów została w całości powtórzona za wydaniem oryginalnym. REDAKTOR NAUKOWY WYDANIA POLSKIEGO prof. dr hab. Janusz Andres TŁUMACZENIE Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Elżbieta Dobrowolska, Edyta Drab, Bartosz Frączek, Anna Jarosz, Piotr Kolęda, Paweł Krawczyk, Rafał Surmacz, Jurij Szymański, Grzegorz Zając KOREKTA MERYTORYCZNA Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Bartosz Frączek, Paweł Krawczyk ADIUSTACJA I KOREKTA WYDAWNICZA Danuta Ambrożewicz PROJEKT OKŁADKI Polska Rada Resuscytacji wg plakatu V Międzynarodowego Kongresu Polskiej Rady Resuscytacji autorstwa Mieczysława Górowskiego Publikację wydano ze środków Polskiej Rady Resuscytacji. Copyright by European Resuscitation Council (ERC), 2010 Copyright for the Polish edition by Polska Rada Resuscytacji, Kraków 2010 Copyright for the Polish translation by Polska Rada Resuscytacji, Kraków 2010 Wszystkie prawa zastrzeżone. Żadna część poniższej publikacji nie może być kopiowana i przechowywana w jakimkol wiek mechanicznym systemie kopiowania danych, włączając fotokopie, kserokopie, nagrania i inne, bez uprzedniej pisem nej zgody PRR (dotyczy terenu Rzeczpospolitej Polskiej). Wszystkie prośby o możliwość wykorzystania materiałów zawartych w tej publikacji należy kierować do ERC. ISBN KOORDYNATOR STRONY ORAZ WERSJI ELEKTRONICZNEJ Wytycznych resuscytacji 2010 Wiesław Pyrczak prc@prc.krakow.pl ADRES DO KORESPONDENCJI ADRES DO KORESPONDENCJI W POLSCE ERC Secretariat VZW Polska Rada Resuscytacji Drie Eikenstraat 661 ul. Radziwiłłowska 4, Kraków BE-2650 EDEGEM tel fax Belgium biuro@prc.krakow.pl tel fax Koordynator kursów info@erc.edu Tomasz Galewicz kursy@prc.krakow.pl SKŁAD I PRZYGOTOWANIE DO DRUKU FALL ul. Garczyńskiego 2, Kraków tel ; fall@fall.pl
73 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 2 Rudolph W. Koster a, *, Michael A. Baubin b, Leo L. Bossaert c, Antonio Caballero d, Pascal Cassan e, Maaret Castrén f, Cristina Granja g, Anthony J. Handley h, Koenraad G. Monsieurs i, Gavin D. Perkins j, Violetta Raffay k, Claudio Sandroni l a Department of Cardiology, Academic Medical Center, Amsterdam, The Netherlands b Department of Anaesthesiology and Critical Care Medicine, University Hospital Innsbruck, Innsbruck, Austria c Department of Critical Care, University of Antwerp, Antwerp, Belgium d Department of Emergency Medicine, Hospital Universitario Virgen del Rocío, Sevilla, Spain e European Reference Centre for First Aid Education, French Red Cross, Paris, France f Department of Clinical Science and Education, Karolinska Institute, Stockholm, Sweden g Department of Emergency and Intensive Medicine, Hospital Pedro Hispano, Matosinhos, Portugal h Colchester Hospital University NHS Foundation Trust, Colchester, UK i Emergency Medicine, Ghent University Hospital, Ghent, Belgium j Department of Critical Care and Resuscitation, University of Warwick, Warwick Medical School, Warwick, UK k Emergency Medicine, Municipal Institute for Emergency Medicine Novi Sad, Novi Sad, AP Vojvodina, Serbia l Department of Anaesthesiology and Intensive Care, Catholic University School of Medicine, Policlinico Universitario Agostino Gemelli, Rome, Italy Podstawowe zabiegi resuscytacyjne (Basic Life Support BLS) obejmują bezprzyrządowe (za wyjątkiem środków ochrony osobistej) utrzymywanie drożności dróg oddechowych oraz podtrzymywanie oddychania i krążenia 1. Rozdział ten zawiera wytyczne dotyczące prowadzenia BLS u osób dorosłych oraz użycia automatycznego defibrylatora zewnętrznego (Automated External Defibrillator AED). Ponadto omawia rozpoznawanie NZK, pozycję bezpieczną i sposób postępowania w zadławieniu (niedrożność dróg oddechowych spowodowana ciałem obcym). Wytyczne zastosowania defibrylatorów manualnych oraz rozpoczęcia resuscytacji na terenie szpitala zawarto w rozdziale 3 i 4 2, 3. Podsumowanie zmian w stosunku do Wytycznych 2005 Wiele z zaleceń zawartych w Wytycznych ERC 2005 pozostaje niezmienionych, czy to z powodu braku publikacji nowych badań, czy też w związku z tym, iż nowe doniesienia zaledwie wzmocniły już istniejące rekomendacje. Przykładami takich zaleceń są ogólna postać algorytmu BLS i AED, sposób, w jaki rozpoznaje się konieczność rozpoczęcia resuscytacji krążeniowo-oddechowej (RKO), użycie AED (włączając w to protokół wykonywania defibrylacji), stosunek uciśnięć klatki piersiowej do wentylacji 30 : 2 oraz rozpoznanie i postępowanie w przypadku zadławienia. Z drugiej strony, od 2005 roku zostały opublikowane wyniki badań, które spowodowały konieczność wprowadzenia zmian w niektórych składowych Wytycznych Poniżej przedstawiono zmiany w Wytycznych dotyczących podstawowych zabiegów resuscytacyjnych (Basic Life Support BLS) w porównaniu z Wytycznymi 2005: * Corresponding author. r.w.koster@amc.nl (R.W. Koster). Dyspozytor powinien być przeszkolony w zakresie zbierania informacji od osób wzywających pomocy zgodnie z precyzyjnym protokołem. Informacje te powinny być ukierunkowane na rozpoznawanie stanu nieprzytomności i jakości oddychania poszkodowanego. Stwierdzenie braku oddechu lub niewłaściwego toru oddechowego w zestawieniu z brakiem przytomności powinny skutkować wdrożeniem właściwego protokołu związanego z podejrzeniem zatrzymania krążenia. Podkreślana jest waga rozpoznania pojedynczych westchnięć (gasping) jako objawu zatrzymania krążenia zarówno w trakcie szkoleń, jak i podczas zbierania informacji przez dyspozytora. Osoby udzielające pomocy, niezależnie od stopnia przeszkolenia, powinny wykonywać uciśnięcia klatki piersiowej u poszkodowanych z zatrzymaniem krążenia. Kluczową interwencją, na które Wytyczne nadal kładą nacisk, jest wysoka jakość wykonywanych uciśnięć klatki piersiowej. Celem powinno być osiągnięcie głębokości przynajmniej 5 cm i częstości przynajmniej 100 uciśnięć na minutę. Należy przy tym pamiętać, by klatka piersiowa powróciła w pełni do pierwotnego kształtu oraz by minimalizować przerwy w uciskaniu klatki piersiowej. Osoby przeszkolone powinny ponadto wykonywać wentylację w sekwencji 30 uciśnięć do 2 oddechów. Osoby nieprzeszkolone zachęca się do prowadzenia RKO na podstawie telefonicznego instruktażu z zaleceniem nieprzerwanego wykonywania wyłącznie uciśnięć klatki piersiowej. W celu utrzymania wysokiej jakości RKO zachęca się do stosowania metod przyrządowych pozwalających na uzyskanie przez ratowników natychmiastowej informacji zwrotnej. Tak zarejestrowane dane mogą być użyte w celu monitorowania jakości wykonywanej RKO, jak również dostarczają ratownikom medycznym informacji zwrotnej przydatnej w trakcie sesji debriefingowych.
74 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 75 Jeśli ratownicy używają AED, analiza rytmu serca i wykonanie defibrylacji nie powinny być opóźniane poprzez wcześniejsze prowadzenie RKO przez określony czas. Jednakże RKO należy prowadzić minimalizując przerwy w uciśnięciach klatki piersiowej zarówno przed naklejeniem elektrod AED, jak i w trakcie jego używania. Zachęca się do dalszego rozwoju programów AED istnieje potrzeba dalszego rozpowszechniania automatycznych defibrylatorów zewnętrznych zarówno w miejscach publicznych, jak i w obszarach mieszkalnych. Wprowadzenie Nagłe zatrzymanie krążenia (NZK) jest główną przyczyną śmierci w Europie. W zależności od tego jak jest definiowane, NZK rozpoznaje się u osób w skali roku 4, 5. Podczas wstępnej analizy rytmu serca w około 25 30% przypadków NZK stwierdza się migotanie komór (VF). Odsetek ten uległ zmniejszeniu w ciągu ostatnich 20 lat Prawdopodobnie znacznie większa liczba osób z NZK w momencie utraty przytomności ma VF lub szybki częstoskurcz komorowy (Ventricular Tachycardia VT), ale do chwili wykonania przez personel pogotowia pierwszej analizy rytmu, zmienia się on w gorzej rokującą asystolię 11, 12. Jeżeli ocena rytmu nastąpi tuż po utracie przytomności, w szczególności za pomocą znajdującego się na miejscu AED, odsetek pacjentów z VF może wynieść nawet od 59% 13 do 65% 14. Wielu poszkodowanych z NZK może przeżyć, o ile świadkowie zdarzenia zareagują natychmiast, kiedy VF jest jeszcze obecne. Skuteczna resuscytacja jest znacznie mniej prawdopodobna, jeśli rytm serca zmieni się w gorzej rokującą asystolię. Zalecane leczenie zatrzymania krążenia w mechanizmie VF polega na natychmiastowym podjęciu przez świadków zdarzenia RKO (uciśnięcia klatki piersiowej w połączeniu z oddechami ratowniczymi) oraz szybkiej defibrylacji elektrycznej. Większość zatrzymań krążenia pierwotnie niekardiogennych ma przyczynę oddechową, tak jak w przypadku tonięcia (w tej grupie znajduje się wiele dzieci) czy asfiksji. W wielu regionach świata utonięcie jest jedną z głównych przyczyn zgonów (patrz: W tych przypadkach oddechy ratownicze mają krytyczne znaczenie dla powodzenia resuscytacji. Łańcuch przeżycia Koncepcja łańcucha przeżycia podsumowuje czynności niezbędne do skutecznej resuscytacji (ryc. 2.1). Większość z jego ogniw odnosi się zarówno do poszkodowanych, u których do zatrzymania krążenia doszło w mechanizmie pierwotnie kardiogennym, jak i na skutek asfiksji Wczesne rozpoznanie zatrzymania krążenia Obejmuje rozpoznanie bólu w klatce piersiowej spowodowanego chorobą serca, rozpoznanie zatrzymania krążenia, powiadomienie służb ratowniczych (np. telefon pod numer 112 lub krajowy numer ratunkowy 999 przyp. tłum.). Szczególnie ważne jest rozpoznanie bólu stenokardialnego, ponieważ prawdopodobieństwo zatrzymania krążenia w wyniku ostrego niedotlenienia mięśnia sercowego, w pierwszej godzinie od wystąpienia objawów, wynosi co najmniej 21% 33% 16,17. Jeżeli telefoniczne wezwanie służb ratowniczych nastąpi przed utratą przytomności przez poszkodowanego, czas od tego momentu do przyjazdu karetki jest znacznie krótszy, a co za tym idzie szansa na przeżycie pacjenta powinna być wyższa Wczesne podjęcie RKO przez świadków zdarzenia Natychmiastowa RKO może podwoić, a nawet potroić szanse przeżycia osób, u których doszło do NZK w mechanizmie VF Prowadzenie RKO z wyłącznym uciskaniem klatki piersiowej jest lepsze niż nieprowadzenie RKO w ogóle 22,23. Jeżeli osoba wzywająca pomocy nie jest przeszkolona w prowadzeniu RKO, dyspozytor powinien stanowczo zachęcać ją do prowadzenia RKO z wyłącznym uciskaniem klatki piersiowej do momentu przyjazdu służb ratowniczych Wczesna defibrylacja RKO w połączeniu z defibrylacją w czasie 3 5 minut od utraty przytomności może skutkować przeżywalnością nawet do 49 75% Każda minuta opóźnienia defibrylacji zmniejsza prawdopodobieństwo przeżycia do wypisu ze szpitala o 10 12% 19, Wczesne podjęcie zaawansowanych zabiegów resuscytacyjnych i standaryzowana opieka poresuscytacyjna Jakość leczenia w okresie po resuscytacji wpływa na ostateczny wynik leczenia Terapeutyczna hipotermia jest obecnie dobrze udokumentowaną 2 Ryc Łańcuch przeżycia
75 76 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni 2 metodą leczenia, która znacząco poprawia przeżycie z dobrym neurologicznym wynikiem końcowym W większości obszarów średni czas od momentu wezwania pomocy do przybycia służb ratowniczych (czas reakcji) wynosi 5 8 minut 13,14 lub 11 minut do wykonania pierwszej defibrylacji 43. W tym okresie przeżycie poszkodowanego zależy od świadków zdarzenia, którzy rozpoczną BLS i użyją AED do wykonania defibrylacji. Osoby, u których wystąpiło NZK, wymagają natychmiastowej RKO. Zapewnia ona niewielki, ale istotny przepływ krwi przez serce i mózg. Ponadto zwiększa prawdopodobieństwo skutecznej defibrylacji w przypadku VF i tym samym umożliwia powrót prawidłowego rytmu i rzutu serca. Uciskanie klatki piersiowej jest szczególnie ważne, gdy defibrylacji nie można przeprowadzić w ciągu kilku pierwszych minut od utraty przytomności 44. Jeżeli serce jest wciąż żywotne, bezpośrednio po defibrylacji jego naturalny rozrusznik podejmie zorganizowaną czynność elektryczną z podtrzymaną aktywnością skurczową. W ciągu pierwszych minut po skutecznej defibrylacji migotania komór rytm serca może być wolny, a siła skurczów słaba. W takiej sytuacji wykonywanie uciśnięć klatki piersiowej jest niezbędne do momentu powrotu prawidłowej pracy serca 45. Ratownicy bez wykształcenia medycznego mogą być szkoleni w zakresie użycia AED, których dostępność w miejscach publicznych wzrasta. AED wydaje komendy głosowe w celu kierowania postępowaniem ratownika, analizuje rytm serca, a gdy wykryje VF lub szybki częstoskurcz komorowy (VT), instruuje ratownika, jak wykonać defibrylację. AED są niezwykle dokładne i zalecają defibrylację jedynie w przypadku VF (lub szybkiego VT) 46. Zasady działania i obsługi AED zostały omówione w rozdziale 3. Wiele badań wykazało zarówno poprawę przeżywalności, gdy RKO została natychmiast rozpoczęta, jak również szkodliwe następstwa opóźnienia defibrylacji. Z każdą minutą opóźnienia defibrylacji szanse na przeżycie pacjenta w przypadku zauważonego VF zmniejszają się o 10% 12% 19,36. Jeżeli świadkowie zdarzenia podejmą RKO, szanse przeżycia pacjenta maleją wolniej, średnio o 3 4% z każdą minutą 12,36,47. Podsumowując, prowadzenie RKO przez świadków zdarzenia zwiększa 2- lub 3-krotnie szanse przeżycia w zauważonym zatrzymaniu krążenia 19,47,48. BLS u osób dorosłych kolejność postępowania W poniższym rozdziale termin poszkodowany odnosi się zarówno do kobiet, jak i mężczyzn. Podstawowe zabiegi resuscytacyjne polegają na wykonaniu następującej sekwencji działań (ryc. 2.2). 1. Upewnij się, że ty, poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni. 2. Sprawdź reakcję poszkodowanego (ryc. 2.3): delikatnie potrząśnij za ramiona i głośno zapytaj: Czy wszystko w porządku? 3a. Jeżeli reaguje: zostaw poszkodowanego w pozycji, w której go zastałeś, o ile nie zagraża mu żadne niebezpieczeństwo, Podstawowe zabiegi resuscytacyjne u osób dorosłych Głośno wołaj o pomoc Udrożnij drogi oddechowe i sprawdź oddech NIE ODDYCHA PRAWIDŁOWO? Ryc Algorytm BLS u dorosłych sekwencja postępowania dowiedz się jak najwięcej o stanie poszkodowanego i wezwij pomoc, jeśli będzie potrzebna, regularnie oceniaj jego stan. 3b. Jeżeli nie reaguje: głośno zawołaj o pomoc (ryc. 2.4) odwróć poszkodowanego na plecy, a następnie udrożnij jego drogi oddechowe, wykonując odgięcie głowy i uniesienie żuchwy (ryc. 2.5), umieść jedną rękę na czole poszkodowanego i delikatnie odegnij jego głowę, opuszki palców drugiej ręki umieść na żuchwie poszkodowanego, a następnie unieś ją w celu udrożnienia dróg oddechowych. 4. Utrzymując drożność dróg oddechowych wzrokiem, słuchem i dotykiem oceń oddech (ryc. 2.6): oceń wzrokiem ruchy klatki piersiowej, nasłuchuj przy ustach poszkodowanego szmerów oddechowych, staraj się wyczuć ruch powietrza na swoim policzku, zadecyduj, czy oddech jest prawidłowy, nieprawidłowy czy nieobecny.
76 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 77 2 Ryc Sprawdź, czy poszkodowany reaguje Ryc Wołaj o pomoc W pierwszych minutach zatrzymania krążenia poszkodowany może słabo oddychać lub wydawać nieregularne, wolne i głośne westchnięcia (gasping). Nie należy ich mylić z prawidłowym oddechem. Na ocenę prawidłowego oddechu za pomocą wzroku, słuchu i dotyku przeznacz nie więcej niż 10 sekund. W przypadku jakichkolwiek wątpliwości dotyczących prawidłowego oddechu działaj tak, jakby był nieprawidłowy. 5a. Jeżeli oddech jest prawidłowy: ułóż poszkodowanego w pozycji bezpiecznej (patrz poniżej), wyślij kogoś lub sam udaj się po pomoc zadzwoń pod numer 112 lub krajowy numer ratunkowy (999 przyp. tłum.), aby wezwać karetkę pogotowia, regularnie oceniaj, czy oddech nadal jest prawidłowy. 5b. Jeżeli oddech poszkodowanego jest nieprawidłowy lub nieobecny: poproś kogoś o wezwanie pomocy oraz przyniesienie AED, jeśli jest dostępne. Jeżeli jesteś sam, użyj telefonu komórkowego w celu wezwania pogotowia ratunkowego. Pozostaw poszkodowanego tylko wtedy, gdy nie ma innej możliwości wezwania pomocy. rozpocznij uciskanie klatki piersiowej poszkodowanego zgodnie z poniższym opisem: uklęknij obok poszkodowanego, ułóż nadgarstek jednej ręki na środku jego klatki piersiowej (dolna połowa mostka poszkodowanego) (ryc. 2.7) ułóż nadgarstek drugiej dłoni na grzbiecie dłoni leżącej na klatce piersiowej poszkodowanego (ryc. 2.8), Ryc Odgięcie głowy i uniesienie żuchwy spleć palce obu dłoni i upewnij się, że nacisk nie będzie kierowany na żebra poszkodowanego. Utrzymuj ramiona wyprostowane (ryc. 2.9). Nie uciskaj górnej części brzucha ani dolnego końca mostka, ustaw ramiona prostopadle do klatki piersiowej poszkodowanego i uciskaj mostek na głębokość nie mniejszą niż 5 cm (ale nie przekraczaj 6 cm) (ryc. 2.10),
77 78 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni 2 Ryc Wzrokiem, słuchem i dotykiem poszukaj prawidłowego oddechu po każdym uciśnięciu zwolnij nacisk na klatkę piersiową, nie odrywając rąk od mostka. Powtarzaj uciśnięcia z częstotliwością co najmniej 100/min (nie przekraczając 120/min), okresy uciskania i zwalniania ucisku na mostek powinny być równe. 6a. Połącz uciskanie klatki piersiowej z oddechami ratowniczymi: po wykonaniu 30 uciśnięć klatki piersiowej ponownie udrożnij drogi oddechowe poszkodowanego, odchylając jego głowę i unosząc żuchwę (ryc. 2.5), zaciśnij skrzydełka nosa poszkodowanego, używając palca wskazującego i kciuka dłoni umieszczonej na jego czole, pozostaw usta poszkodowanego lekko otwarte, jednocześnie utrzymując uniesienie żuchwy, weź normalny wdech i obejmij szczelnie usta poszkodowanego swoimi ustami, upewniając się, że nie ma przecieku powietrza, wdmuchuj powietrze do ust poszkodowanego przez około 1 sekundę (jak przy normalnym oddychaniu) i ze stałą szybkością, obserwując jednocześnie, czy klatka piersiowa się unosi (ryc. 2.11) jest to skuteczny oddech ratowniczy, utrzymując odgięcie głowy i uniesienie żuchwy, odsuń swoje usta od ust poszkodowanego i obserwuj, czy podczas wydechu opada jego klatka piersiowa (ryc. 2.12), ponownie nabierz powietrza i wdmuchnij je do ust poszkodowanego, dążąc do wykonania całkowitej liczby dwóch skutecznych oddechów ratowniczych. Dwa oddechy ratownicze nie powinny w sumie trwać dłużej niż 5 sekund. Następnie bez opóźnienia ponownie ułóż dłonie w prawidłowej pozycji na mostku poszkodowanego i wykonaj kolejnych 30 uciśnięć klatki piersiowej, kontynuuj uciskanie klatki piersiowej i oddechy ratownicze w stosunku 30 : 2, przerwij swoje działania w celu sprawdzenia stanu poszkodowanego tylko wtedy, gdy zacznie reagować: poruszy się, otworzy oczy i zacznie prawidłowo oddychać. W innym przypadku nie przerywaj resuscytacji. Jeżeli pierwszy oddech ratowniczy nie spowoduje uniesienia się klatki piersiowej, jak przy prawidłowym oddychaniu, przed podjęciem kolejnej próby wykonaj następujące czynności: sprawdź jamę ustną poszkodowanego i usuń wszystkie ciała obce, potwierdź właściwe odchylenie głowy i uniesienie żuchwy, Ryc Ułóż nadgarstek jednej ręki na środku klatki piersiowej poszkodowanego Ryc Nadgarstek drugiej ręki ułóż na już położonym
78 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 79 2 Ryc Spleć palce obu rąk. Wyprostuj ramiona Ryc Uciskaj mostek na głębokość przynajmniej 5 cm nie podejmuj więcej niż dwóch prób wentylacji przed każdorazowym podjęciem uciskania klatki piersiowej. Jeżeli na miejscu zdarzenia jest więcej niż jeden ratownik, powinni się oni zmieniać podczas prowadzenia RKO co 2 minuty, aby zapobiec zmęczeniu. Podczas zmian należy minimalizować przerwy w uciśnięciach klatki piersiowej. W tym celu oraz aby wykonywać dokładnie 30 uciśnięć z prawidłową częstością, pomocne może być głośne liczenie. Doświadczeni ratownicy mogą prowadzić RKO w dwie osoby i wówczas powinni zmieniać się rolami/miejscami co dwie minuty. 6b. RKO z wyłącznym uciskaniem klatki piersiowej może być zastosowana, jeżeli: ratownik nie posiada przeszkolenia lub nie chce wykonywać oddechów ratowniczych, jeżeli prowadzone jest RKO z wyłącznym uciskaniem klatki piersiowej, powinno ono być wyko- Ryc Powoli wdmuchuj powietrze do ust, obserwując unoszenie się klatki piersiowej poszkodowanego Ryc Odsuń swoje usta od ust poszkodowanego i obserwuj czy opada klatka piersiowa
79 80 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni 2 nywane bez przerw, z częstotliwością co najmniej 100/min (nie przekraczając 120/min). 7. Nie przerywaj resuscytacji do momentu: przybycia wykwalifikowanych służb medycznych i przejęcia przez nie działania lub gdy poszkodowany zacznie reagować: poruszy się, otworzy oczy i zacznie prawidłowo oddychać, lub wyczerpania własnych sił. Udrażnianie dróg oddechowych Ratownikom bez wykształcenia medycznego nie zaleca się stosowania rękoczynu wysunięcia żuchwy, ponieważ jest trudny do nauczenia i wykonania i może spowodować ruch kręgosłupa szyjnego 49. Dlatego powinni udrażniać drogi oddechowe za pomocą odgięcia głowy i uniesienia żuchwy, zarówno w przypadku poszkodowanych urazowych, jak i nieurazowych. Rozpoznanie zatrzymania krążenia i oddychania Sprawdzanie tętna na tętnicy szyjnej (lub innej tętnicy) nie jest dokładną metodą potwierdzania obecności lub braku krążenia i dotyczy to zarówno ratowników bez wykształcenia medycznego, jak i personelu medycznego Nie ma też jednak dowodów, żeby stwierdzenie ruchu, oddechu czy kaszlu (oznak zachowanego krążenia) miało przewagę diagnostyczną. Zarówno personel medyczny, jak i ratownicy bez wykształcenia medycznego mają trudności z określeniem obecności prawidłowego oddechu lub jego braku u nieprzytomnego poszkodowanego 53,54. Może to wynikać z niedrożności dróg oddechowych bądź wykonywania przez poszkodowanego tylko pojedynczych (agonalnych) westchnięć. Świadkowie zdarzenia, zapytani przez dyspozytora podczas zgłoszenia telefonicznego, czy poszkodowany oddycha, często błędnie interpretują agonalne westchnięcia jako prawidłowy oddech. W wyniku tej błędnej informacji świadkowie zdarzenia mogą nie podjąć RKO u poszkodowanego z zatrzymaniem krążenia 55. Agonalne westchnięcia (gasping) w ciągu pierwszych minut zatrzymania krążenia występują u blisko 40% poszkodowanych i wiążą się z większą przeżywalnością, jeżeli zostaną rozpoznane jako objaw NZK 56. Świadkowie opisują agonalny oddech jako słabe oddechy, ciężki oddech z wysiłkiem lub głośne, przerywane westchnięcia 57. Dlatego ratowników bez wykształcenia medycznego należy uczyć, że RKO należy rozpocząć wtedy, gdy poszkodowany jest nieprzytomny (nie reaguje) i nie oddycha prawidłowo. W trakcie szkolenia należy podkreślać, iż agonalne westchnięcia często występują w pierwszych minutach NZK. Stanowią wskazanie do natychmiastowego rozpoczęcia RKO i nie należy ich mylić z prawidłowym oddechem. Podczas rozmowy z dyspozytorem pogotowia ratunkowego kluczowe znaczenie ma właściwe opisanie poszkodowanego. Dla dyspozytora ważne jest, że osoba wzywająca pomocy widzi poszkodowanego, ale w niewielkiej ilości przypadków osoba ta może nie znajdować się na miejscu zdarzenia 58. Informacja dotycząca oddechu poszkodowanego jest najważniejsza, ale opisy oddechu przez osoby wzywające pomocy znacząco się różnią. Jeżeli charakter oddechu poszkodowanego nie zostanie opisany przez osobę wzywającą pomocy lub dyspozytor o to nie zapyta, szansa na rozpoznanie zatrzymania krążenia jest znacznie mniejsza niż w sytuacji, gdy oddech zostanie opisany jako nieprawidłowy lub nieobecny 59. Jeżeli osoba wzywająca pomocy opisze poszkodowanego jako nieprzytomnego bez oddechu lub z nieprawidłowym oddechem, dyspozytor pogotowia ratunkowego zawsze zareaguje jak w przypadku zatrzymania krążenia i żaden przypadek NZK nie zostanie pominięty 60. Rozpoznanie zatrzymania krążenia, którego pierwszym objawem są drgawki, jest znacznie bardziej prawdopodobne, jeżeli potwierdzi się brak epizodów drgawkowych w przeszłości chorobowej poszkodowanego 59,61. Pytanie o regularność oddechów może również pomóc w rozpoznaniu zatrzymania krążenia wśród zgłoszeń dotyczących drgawek u poszkodowanych. Doświadczenie dyspozytora może w znaczący sposób wpłynąć na przeżywalność: jeżeli odbiera on rocznie tylko kilka zgłoszeń o zatrzymaniu krążenia, przeżywalność jest znacznie niższa niż w przypadku, gdy liczba takich zgłoszeń przekracza dziewięć w skali roku (22% vs. 39%) 58. Dokładność rozpoznania zatrzymania krążenia przez dyspozytorów waha się od 50% do 80%. Jeżeli dyspozytor rozpozna zatrzymanie krążenia, przeżycie po NZK jest bardziej prawdopodobne, ponieważ podjęte zostaną odpowiednie działania (np. RKO prowadzone dzięki telefonicznemu instruktażowi czy odpowiednie zgłoszenie dla karetki pogotowia) 25, 60. Początkowe oddechy ratownicze W zatrzymaniu krążenia pierwotnie kardiogennym (do którego nie doszło wskutek asfiksji), krew tętnicza nie krąży i pozostaje wysycona tlenem przez kilka minut 62. Jeśli w ciągu tych kilku minut rozpocznie się RKO, zawartość tlenu we krwi pozostaje wystarczająca, a dostarczanie go do mięśnia sercowego i mózgu jest ograniczone bardziej przez zmniejszony rzut serca aniżeli przez brak tlenu w płucach i krwi tętniczej. Z tego powodu wentylacja w początkowej fazie NZK jest mniej istotna niż uciskanie klatki piersiowej 63,64. U osób dorosłych wymagających RKO zakłada się a priori chorobę serca jako pierwotną przyczynę zatrzymania krążenia. W celu podkreślenia priorytetu uciśnięć klatki piersiowej zaleca się, aby rozpoczynać RKO od uciskania klatki piersiowej, a nie od wykonywania początkowych oddechów ratowniczych. Nie należy tracić czasu na poszukiwanie ciał obcych w jamie ustnej, chyba że próby oddechów ratowniczych nie spowodują uniesienia się klatki piersiowej. Wentylacja Celem wentylacji w trakcie RKO jest utrzymanie właściwej oksygenacji i eliminacja CO 2. Jednakże optymalna objętość oddechowa, częstość oddechów, jak i stężenie tlenu w mieszaninie oddechowej niezbędne dla osiągnięcia tego celu nie są w pełni poznane. Aktualne zalecenia bazują na następujących faktach naukowych: 1. W trakcie RKO przepływ krwi przez płuca jest znacznie zmniejszony, dlatego właściwy stosunek wentylacji do perfuzji może być utrzymywany przy objętości oddechowej i częstości oddechu mniejszych niż prawidłowe Hiperwentylacja jest szkodliwa, ponieważ zwiększa ciśnienie w klatce piersiowej, co obniża powrót krwi żyl-
80 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 81 nej do serca i zmniejsza jego rzut. W konsekwencji zmniejsza się szansa przeżycia Przerwy w uciskaniu klatki piersiowej (np. w celu oceny rytmu serca lub badania tętna) drastycznie obniżają przeżywalność Jeżeli drogi oddechowe nie są zabezpieczone, objętość oddechowa 1 l powoduje znacznie większe rozdęcie żołądka niż objętość 500 ml Niska wentylacja minutowa (objętość oddechowa i częstość oddechów mniejsza niż prawidłowa) może zapewniać skuteczne natlenienie i wentylację w trakcie RKO W trakcie RKO u dorosłych zaleca się stosowanie objętości oddechowej ok ml (6 7 ml/kg). W związku z powyższym aktualnie zaleca się, aby ratownicy wykonywali każdy oddech ratowniczy w ciągu około 1 sekundy objętością wystarczającą do spowodowania widocznego uniesienia się klatki piersiowej, ale unikając szybkich i mocnych wdechów. Czas konieczny do wykonania dwóch oddechów ratowniczych nie powinien przekraczać 5 sekund. To zalecenie dotyczy wszystkich form wentylacji w trakcie RKO, zarówno usta usta, jak i za pomocą worka samorozprężalnego z maską twarzową, niezależnie od podaży tlenu. Wentylacja metodą usta nos jest dopuszczalną alternatywą dla wentylacji usta usta 73. Można ją rozważyć, gdy usta poszkodowanego są poważnie uszkodzone lub nie można ich otworzyć, gdy ratownik wykonuje wentylację u poszkodowanego znajdującego się w wodzie, lub kiedy trudno osiągnąć szczelność techniką usta usta. Nie ma publikacji naukowych na temat bezpieczeństwa, skuteczności i możliwości wykonywania wentylacji metodą usta tracheostomia, ale można ją zastosować u poszkodowanych z rurką tracheotomijną lub tracheostomią, którzy wymagają oddechów ratowniczych. Prowadzenie wentylacji za pomocą worka samorozprężalnego z maską twarzową wymaga doświadczenia i pewnych umiejętności 74,75. Metoda ta może być stosowana przez właściwie przeszkolonych i doświadczonych ratowników, prowadzących RKO we dwie osoby. Uciskanie klatki piersiowej Uciskanie klatki piersiowej wytwarza przepływ krwi poprzez zwiększenie ciśnienia wewnątrz klatki piersiowej i bezpośrednie ściskanie serca. Mimo że prawidłowo wykonane uciśnięcia klatki piersiowej generują szczytowe, skurczowe ciśnienie tętnicze rzędu mm Hg, ciśnienie rozkurczowe pozostaje niskie i średnie ciśnienie w tętnicy szyjnej rzadko przekracza 40 mm Hg 76. Uciskanie klatki piersiowej generuje niewielki, ale krytycznie ważny przepływ krwi przez mózg i mięsień sercowy i zwiększa prawdopodobieństwo skutecznej defibrylacji. Od czasu opublikowania Wytycznych 2005 badania z użyciem urządzeń podpowiadających/dających informację zwrotną podczas RKO u poszkodowanych z zatrzymaniem krążenia dostarczyły nowych danych, które uzupełniły dotychczasowe badania na zwierzętach i fantomach Na ich podstawie powstały poniższe zalecenia: 1. Za każdym razem, kiedy podejmuje się uciskanie klatki piersiowej, ratownik powinien niezwłocznie ułożyć ręce na środku klatki piersiowej. 2. Należy uciskać klatkę piersiową z częstotliwością co najmniej 100/min. 3. Trzeba zwracać uwagę, aby uciśnięcia osiągały pełną głębokość, co najmniej 5 cm (u osób dorosłych). 4. Po każdym uciśnięciu należy pozwolić, aby klatka piersiowa całkowicie wracała do pozycji wyjściowej, tzn. nie należy się opierać na klatce piersiowej w czasie trwania fazy relaksacji. 5. Fazy nacisku i relaksacji powinny trwać tyle samo. 6. Należy minimalizować przerwy w uciśnięciach tak, aby wykonać co najmniej 60 uciśnięć w ciągu każdej minuty. 7. Podczas uciskania klatki piersiowej nie należy polegać na wyczuwaniu tętna na tętnicy szyjnej lub innej jako wskaźnika efektywnego przepływu tętniczego 50, 82. Ułożenie rąk Ratownik wykonujący uciśnięcia klatki piersiowej u osoby dorosłej powinien ułożyć dłonie na dolnej połowie mostka. Zaleca się, aby uczyć tego ułożenia w sposób uproszczony, na przykład słowami: ułóż nadgarstek swojej dłoni na środku klatki piersiowej, a na nim drugą dłoń. Ten opis powinien być uzupełniony pokazem ułożenia dłoni na manekinie na dolnej połowie mostka. Wykorzystanie linii międzysutkowej jako wyznacznika miejsca ułożenia dłoni nie jest wiarygodne 83,84. Częstotliwość uciśnięć klatki piersiowej Istnieje dodatnia korelacja pomiędzy rzeczywistą ilością uciśnięć klatki piersiowej wykonywanych w ciągu minuty a szansą skutecznej resuscytacji 81. Chociaż częstotliwość uciśnięć klatki piersiowej (szybkość, z jaką wykonuje się serię 30 uciśnięć) powinna wynosić co najmniej 100/min, rzeczywista liczba uciśnięć wykonanych w ciągu jednej minuty RKO jest mniejsza z powodu przerw koniecznych do wykonania oddechów ratowniczych, analizy rytmu przez AED itp. W jednym z badań dotyczących pozaszpitalnych zatrzymań krążenia zarejestrowana częstotliwość uciśnięć klatki piersiowej wykonywanych przez ratowników wynosiła /min, ale rzeczywista średnia liczba uciśnięć na minutę była zredukowana do 64 w wyniku licznych przerw 79. W ciągu każdej minuty powinno być wykonanych co najmniej 60 uciśnięć. Głębokość uciśnięć klatki piersiowej Obawa przed spowodowaniem urazu, zmęczenie oraz ograniczona siła mięśni często powodują, że ratownik uciska klatkę piersiową płycej, niż jest to zalecane. Badania naukowe dowodzą, że w porównaniu z grupą pacjentów, w której wykonywano uciśnięcia na głębokość 4 cm lub mniej, uciśnięcia wynoszące co najmniej 5 cm zwiększają szansę na powrót spontanicznego krążenia (ROSC) oraz wiążą się z większym odsetkiem pacjentów przyjmowanych do szpitala z przywróconym krążeniem po NZK 77,78. Nie ma bezpośrednich dowodów świadczących o tym, że obrażenia klatki piersiowej są związane z głębokością uciśnięć. Brak także badań umożliwiających ustalenie maksymalnej głębokości uciśnięć. Za- 2
81 82 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni 2 leca się jednak, aby nawet u dobrze zbudowanych osób dorosłych głębokość uciśnięć nie przekraczała 6 cm. Jeśli to tylko możliwe, RKO powinna być prowadzona na twardej powierzchni. Materace wypełniane powietrzem powinno się rutynowo opróżniać w trakcie RKO 85. Brak dowodów przemawiających za, jak i przeciwko użyciu sztywnej deski podkładanej pod plecy 86,87, ale jeśli się ją stosuje, należy zadbać, aby podczas jej podkładania unikać przerw w uciśnięciach klatki piersiowej oraz aby nie doszło do utraty dostępu donaczyniowego lub przemieszczenia rurki intubacyjnej. Faza relaksacji podczas uciskania klatki piersiowej Pełna relaksacja po uciśnięciu pozwala na lepszy powrót krwi żylnej do klatki piersiowej i może zwiększyć efektywność RKO 88,89. Do tej pory nie ustalono jednak optymalnej metody osiągnięcia tego celu tak, aby nie wpływała ona negatywnie na inne aspekty techniczne uciskania klatki piersiowej, na przykład głębokość uciśnięć. Informacja zwrotna dotycząca techniki uciskania klatki piersiowej W celu uzyskania zalecanej głębokości i częstotliwości uciśnięć ratownicy mogą być wspomagani przez urządzenia dające wskazówki i informację zwrotną o jakości uciśnięć. Urządzenia takie mogą być oddzielnym sprzętem, być elementem AED lub manualnego defibrylatora. Zastosowanie tego typu urządzeń może być korzystne jako jednego z elementów strategii mającej na celu poprawę jakości RKO. Ratownicy muszą być świadomi, że dokładność urządzeń mierzących głębokość uciśnięć klatki piersiowej może być różna i zależy od twardości podłoża, na którym prowadzi się resuscytację (np. podłoga/materac) urządzenia mogą zawyżać głębokość uciśnięć 87. Konieczne są dalsze badania, aby określić, czy tego typu urządzenia zwiększają przeżywalność. Stosunek uciśnięć klatki piersiowej do wentylacji Badania na zwierzętach przemawiają za zwiększeniem stosunku uciśnięć i wentylacji powyżej 15 : Modele matematyczne sugerują, że sekwencja 30 : 2 stanowi najlepszy kompromis pomiędzy przepływem krwi a dostarczaniem tlenu 93,94. Stosunek 30 uciśnięć do 2 oddechów ratowniczych był zalecany przez Wytyczne 2005 dla pojedynczego ratownika prowadzącego resuscytację u osób dorosłych i dzieci poza szpitalem. Wyjątek dotyczył przeszkolonego personelu medycznego, który u dzieci powinien stosować sekwencję 15 : 2. Wytyczne te zmniejszyły liczbę przerw w uciskaniu klatki piersiowej oraz czas bez przepływu 95,96, a także zmniejszyły prawdopodobieństwo hiperwentylacji 66,97. Brak jednak bezpośrednich dowodów świadczących o wzroście przeżywalności w rezultacie wprowadzonych zmian. Podobnie nie ma nowych danych, które sugerowałyby zmianę zalecanego stosunku uciśnięć do wentylacji (30 : 2). RKO z wyłącznym uciskaniem klatki piersiowej Niektórzy ratownicy medyczni, jak również ratownicy bez wykształcenia medycznego przyznają, że niechętnie podejmują wentylację usta usta, zwłaszcza u nieznanych osób z NZK 98,99. Doświadczenia na zwierzętach pokazały, iż w pierwszych minutach zatrzymania krążenia, którego przyczyną nie była asfiksja, samo uciskanie klatki piersiowej może być tak samo efektywne jak połączenie uciśnięć z wentylacją 63,100. Jeżeli drogi oddechowe są udrożnione, pojedyncze westchnienia (gasping) oraz bierne odkształcanie klatki piersiowej podczas jej uciskania mogą powodować niewielką wymianę powietrza, ale może się ona ograniczać wyłącznie do wentylacji przestrzeni martwej 56, Badania na zwierzętach i modele matematyczne wykazały, że podczas uciskania klatki piersiowej bez wykonywania oddechów ratowniczych znajdujące się we krwi tętniczej rezerwy tlenu wyczerpują się po 2 4 minutach 92,104. Przeżywalność dorosłych z NZK, do którego nie doszło w wyniku asfiksji, jest znacząco wyższa, gdy podjęto RKO z wyłącznym uciskaniem klatki piersiowej, niż w grupie, w której nie podjęto RKO w ogóle 22,23. Kilka badań dotyczących zatrzymań krążenia u ludzi sugeruje równorzędność uciskania klatki piersiowej jako jedynego elementu RKO w porównaniu z resuscytacją polegającą na połączeniu uciśnięć klatki piersiowej z wentylacją, ale żadne z nich nie wyklucza możliwości, że metoda ta jest gorsza od pełnej RKO 23,105. Jedno badanie sugeruje wyższość RKO z wyłącznym uciskaniem klatki piersiowej 22. Wszystkie te badania posiadają znaczące ograniczenia, ponieważ opierają się na retrospektywnej analizie danych, gdzie przebieg RKO nie był kontrolowany i nie obejmował prowadzenia resuscytacji zgodnie z Wytycznymi 2005 (stosunek uciśnięć do wentylacji 30 : 2). Wyłączne uciskanie klatki piersiowej może być skuteczne tylko w pierwszych kilku minutach po utracie przytomności. Profesjonalnej pomocy należy się spodziewać średnio po 8 minutach lub nawet później od wezwania pomocy. W takiej sytuacji wyłączne uciskanie klatki piersiowej może być w wielu przypadkach niewystarczające. U dzieci i osób dorosłych z zatrzymaniem krążenia z przyczyn niekardiogennych (np. tonięcie, uduszenie) RKO z wyłącznym uciskaniem klatki piersiowej nie jest tak skuteczne jak konwencjonalna RKO 106, 107. RKO polegająca na połączeniu uciśnięć klatki piersiowej z oddechami ratowniczymi jest zatem metodą z wyboru zarówno dla personelu medycznego, jak i przeszkolonych ratowników bez wykształcenia medycznego. Inne osoby udzielające pomocy powinny być zachęcane do prowadzenia RKO z wyłącznym uciskaniem klatki piersiowej w sytuacji, gdy nie mogą lub nie chcą podejmować oddechów ratowniczych lub kiedy wykonują resuscytację instruowani telefonicznie przez dyspozytora pogotowia ratunkowego 26, 27. RKO w ciasnych przestrzeniach W ograniczonej przestrzeni można rozważyć prowadzenie resuscytacji zza głowy pacjenta (gdy RKO prowadzi jeden ratownik) lub w rozkroku nad pacjentem (gdy jest dwóch ratowników) 108, 109. Zagrożenia dla poszkodowanego w trakcie wykonywania RKO Wielu ratowników nie podejmuje RKO w obawie, że wykonywanie uciśnięć klatki piersiowej u poszkodowanego, u którego nie doszło do zatrzymania krążenia, doprowadzi do ciężkich powikłań. W badaniach, gdzie resuscytację
82 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 83 prowadzili świadkowie zdarzenia instruowani telefonicznie przez dyspozytora, wśród poszkodowanych bez zatrzymania krążenia, którym uciskano klatkę piersiową, 12% odczuwało dyskomfort w klatce piersiowej, a tylko 2% doznała złamania żeber; u żadnego z poszkodowanych nie doszło do urazu narządów wewnętrznych 110. U osób, które w rzeczywistości nie mają zatrzymania krążenia, resuscytacja prowadzona przez świadków zdarzenia niezmiernie rzadko prowadzi do ciężkich obrażeń. Ratownicy nie powinni więc rezygnować z podejmowania RKO w obawie o spowodowanie obrażeń u poszkodowanego. Zagrożenia dla ratowników w trakcie ćwiczeń i w trakcie prowadzenia resuscytacji Wysiłek fizyczny Badania obserwacyjne podczas ćwiczeń lub rzeczywistej resuscytacji opisują rzadkie przypadki skurczów mięśniowych, bólów pleców, duszności i hiperwentylacji oraz pojedyncze przypadki wystąpienia odmy, bólu w klatce piersiowej, zawału mięśnia sercowego czy uszkodzeń nerwów 111,112. Częstość występowania takich zdarzeń jest bardzo mała i w większości przypadków zarówno ćwiczenia, jak i rzeczywista resuscytacja są bezpieczne 113. Osoby planujące udział w szkoleniu z zakresu resuscytacji powinny zostać poinformowane o charakterze i stopniu aktywności fizycznej wymaganej podczas ćwiczeń. Osobom szkolącym się oraz ratownikom, u których podczas wykonywania RKO pojawiły się niepokojące objawy (takie jak: ból w klatce piersiowej, silna duszność), należy doradzić przerwanie prowadzenia resuscytacji. Zmęczenie ratownika Kilka badań prowadzonych na fantomach wykazało, że głębokość uciśnięć klatki piersiowej może zacząć spadać nawet już po dwóch minutach prowadzenia resuscytacji. Badania prowadzone w warunkach wewnątrzszpitalnych wykazały spadek średniej głębokości uciśnięć po czasie 1,5 do 3 minut od rozpoczęcia RKO, nawet w sytuacji, kiedy ratownik stosował urządzenie dające natychmiastową (w czasie rzeczywistym) informację zwrotną o jakości uciśnięć 114. Dlatego ratownicy powinni się zmieniać co dwie minuty, aby zapobiec spadkowi jakości uciśnięć klatki piersiowej, który wynika ze zmęczenia ratownika. Zmiana ratowników nie powinna powodować przerw w uciśnięciach klatki piersiowej. Zagrożenia w czasie defibrylacji Duże randomizowane badanie nad programem publicznego dostępu do defibrylacji wykazało, że AED mogą być używane bezpiecznie zarówno przez osoby bez wykształcenia medycznego, jak i służby paramedyczne, docierające jako pierwsze na miejsce zdarzenia 115. Systematyczny przegląd dostępnych źródeł wykazał osiem prac opisujących w sumie 29 przypadków powikłań związanych z wykonywaniem defibrylacji 116. Obejmowały one przypadkowe lub zamierzone użycie defibrylatora niezgodnie z jego przeznaczeniem, nieprawidłową pracę urządzenia i przypadkowe wyładowanie w trakcie ćwiczeń lub konserwacji urządzenia. Cztery publikacje opisują pojedyncze przypadki porażenia ratownika przez wyładowanie z wszczepialnego kardiowertera-defibrylatora (ICD), w jednym z nich spowodowało to uszkodzenie nerwu obwodowego. Nie ma doniesień mówiących o urazach ratowników w wyniku wykonywania defibrylacji w wilgotnym otoczeniu. Urazy, do których dochodzi u ratowników podczas defibrylacji, są niezwykle rzadkie. Niemniej jednak ratownik nie powinien kontynuować uciśnięć klatki piersiowej podczas dostarczania wyładowania. Poszkodowanych nie należy także dotykać w przypadku wykonywania wyładowania przez ICD. Należy unikać bezpośredniego kontaktu pomiędzy ratownikiem a poszkodowanym podczas defibrylacji wykonywanej w wilgotnym otoczeniu. Reakcje psychologiczne W jednym dużym prospektywnym badaniu dotyczącym programu publicznego dostępu do defibrylacji opisano kilka niekorzystnych reakcji psychologicznych związanych z wykonywaniem RKO i użyciem AED 113. W dwóch dużych, opartych na ankietach badaniach retrospektywnych nad prowadzeniem RKO przez świadków zdarzenia prawie wszyscy respondenci opisywali swoje działania jako pozytywne doświadczenie 117,118. Rzadkie przypadki niekorzystnych reakcji psychologicznych u ratowników wykonujących RKO powinny być właściwie rozpoznane i leczone. Przenoszenie chorób zakaźnych Opisano tylko kilka przypadków, w których prowadzenie RKO wiązało się z transmisją zakażenia, m.in. Salmonella infantis, Staphylococcus aureus, wirusem SARS (Severe Acute Respiratory Syndrome), Meningococcal meningitis, Helicobacter pylori, wirusem Herpes simplex, postacią skórną gruźlicy, zapaleniem jamy ustnej lub tchawicy, Shigella i Streptococcus pyogenes. Odnotowano jeden przypadek zakażenia wirusem herpes simplex podczas ćwiczeń RKO. Analiza dostępnych danych wykazała, że przy braku działań związanych z dużym ryzykiem zakażenia, takich jak kaniulacja naczynia, zarówno w trakcie rzeczywistej resuscytacji, jak i podczas ćwiczeń, nie odnotowano transmisji wirusem zapalenia wątroby typu B i C, wirusem ludzkiego niedoboru odporności (HIV) czy cytomegalowirusem 119. Ryzyko zakażenia w trakcie ćwiczeń czy rzeczywistej resuscytacji jest niezmiernie niskie. Stosowanie rękawiczek w trakcie wykonywania RKO jest zasadne, ale resuscytacja nie może być niepodejmowana lub opóźniana, jeśli rękawiczki nie są dostępne. Ratownicy powinni zastosować odpowiednie środki ostrożności, jeżeli wiedzą, że poszkodowany ma poważną infekcję (np. HIV, gruźlica, WZW B, wirus SARS). Zabezpieczenia w trakcie wentylacji Nie ma badań przeprowadzonych w trakcie rzeczywistej resuscytacji, których celem byłaby ocena bezpieczeństwa, efektywności i możliwości wykorzystania zabezpieczeń stosowanych w trakcie resuscytacji (takich jak chusty twarzowe czy maski kieszonkowe), których zadaniem jest zapobieżenie kontaktowi pomiędzy ratownikiem a poszkodowanym w trakcie wykonywania oddechów ratowniczych. 2
83 84 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni 2 Ryc Kończynę górną poszkodowanego bliższą tobie ułóż w zgięciu w stawie łokciowym, po zgięciu łokcia dłoń powinna być skierowana ku górze Ryc Przełóż dalsze ramię ratowanego w poprzek jego klatki piersiowej, a grzbiet jego ręki przytrzymaj przy jego policzku Dwa badania przeprowadzone w kontrolowanych warunkach laboratoryjnych wykazały skuteczność takich narzędzi w zmniejszaniu ryzyka zakażenia 120,121. Ponieważ ryzyko zakażenia jest bardzo niskie, prowadzenie oddechów ratowniczych bez tego typu narzędzi jest uzasadnione. Jeżeli wiadomo, że poszkodowany ma poważną infekcję (np. HIV, gruźlica, WZW B, wirus SARS), zaleca się stosowanie zabezpieczeń w trakcie wentylacji. Pozycja bezpieczna Istnieje kilka wariantów pozycji bezpiecznej, każdy z nich ma swoje zalety. Nie ma pozycji idealnej dla wszystkich poszkodowanych 122,123. Pozycja powinna być stabilna, jak najbliższa ułożeniu na boku, powinna umożliwiać podparcie głowy i nie uciskać na klatkę piersiową, by nie utrudniać oddechu 124. ERC zaleca następująca sekwencję postępowania w celu ułożenia poszkodowanego w pozycji bezpiecznej: Uklęknij przy poszkodowanym i upewnij się, że obie jego nogi są wyprostowane. Rękę bliższą tobie ułóż pod kątem prostym w stosunku do ciała i zegnij w łokciu tak, aby dłoń ręki była skierowana do góry (ryc. 2.13). Dalszą rękę przełóż w poprzek klatki piersiowej i przytrzymaj stroną grzbietową przy bliższym tobie policzku poszkodowanego (ryc. 2.14). Drugą ręką chwyć za dalszą kończynę dolną poszkodowanego tuż powyżej kolana i podciągnij ją ku górze, nie odrywając stopy od podłoża (ryc. 2.15). Przytrzymując dłoń dociśniętą do policzka, pociągnij za dalszą kończynę dolną tak, by poszkodowany obrócił się na bok w twoim kierunku. Ułóż kończynę, za którą przetaczałeś poszkodowanego w taki sposób, aby staw kolanowy i biodrowy były zgięte pod kątem prostym. Odegnij głowę ratowanego ku tyłowi, by upewnić się, że drogi oddechowe są drożne. Jeśli jest to konieczne, ułóż rękę poszkodowanego pod policzkiem tak, by utrzymać głowę w odgięciu, twarzą zwróconą do podłoża (ryc. 2.16), aby umożliwić wydostawanie się treści płynnej z ust. Regularnie sprawdzaj oddech. Jeżeli poszkodowany musi być ułożony w tej pozycji dłużej niż 30 minut, po tym czasie odwróć go na drugi bok, aby zwolnić ucisk na leżące niżej ramię. Ciało obce w drogach oddechowych (zadławienie) Niedrożność dróg oddechowych spowodowana ciałem obcym (Foreign-Body Airway Obstruction FBAO) jest rzadką, potencjalnie uleczalną przyczyną przypadkowej śmierci 125. Większość epizodów zadławienia związana jest z jedzeniem i obecnością świadków, co daje możliwość podjęcia szybkiej interwencji, kiedy poszkodowany jest jeszcze w kontakcie. Rozpoznanie Ponieważ rozpoznanie niedrożności dróg oddechowych jest kluczem do sukcesu w postępowaniu, bardzo ważne jest, aby nie pomylić tej nagłej sytuacji z omdleniem, zawałem Tabela 2.1. Różnicowanie ciężkiej i łagodnej niedrożności dróg oddechowych spowodowanej ciałem obcym (FBAO) a Objaw Łagodna niedrożność Ciężka niedrożność Czy się zadławiłeś? Inne objawy Tak Może mówić, kaszleć, oddychać Nie może mówić, może kiwać głową Nie może oddychać / świsty oddechowe / ciche próby kaszlu / nieprzytomny a Ogólne objawy FBAO: objawy występują podczas jedzenia; poszkodowany może trzymać się za szyję.
84 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 85 2 Ryc Drugą ręką uchwyć dalszą kończynę dolną poszkodowanego tuż ponad kolanem i pociągnij ją ku górze, nie odrywając stopy od podłoża serca, drgawkami lub innymi stanami, które mogą powodować nagłe zaburzenia oddechowe, sinicę lub utratę świadomości. Ciało obce może spowodować łagodną lub ciężką niedrożność dróg oddechowych. Objawy pozwalające na różnicowanie łagodnej i ciężkiej niedrożności zostały omówione w tabeli 2.1. Ważne jest zapytanie przytomnego poszkodowanego: Czy się zadławiłeś?. Postępowanie w FBAO (zadławieniu) u dorosłych Postępowanie to jest także właściwe dla dzieci powyżej 1. roku życia (ryc. 2.17). 1. Jeżeli poszkodowany ma objawy łagodnej niedrożności dróg oddechowych: zachęcaj go do kaszlu i nie rób nic więcej. 2. Jeżeli poszkodowany ma objawy ciężkiej niedrożności i jest przytomny: Ryc Pozycja bezpieczna. Odegnij głowę poszkodowanego ku tyłowi, aby zapewnić drożność dróg oddechowych. Twarz powinna być skierowana ku dołowi, aby zapewnić swobodny wypływ wydzieliny zastosuj do 5 uderzeń w okolicę międzyłopatkową zgodnie z zasadami: stań z boku i nieco za poszkodowanym, podłóż jedną dłoń na klatce piersiowej poszkodowanego i pochyl go do przodu tak, aby przemieszczone ciało obce mogło przedostać się do ust, a nie przesuwało się w głąb dróg oddechowych, wykonaj do 5 energicznych uderzeń nadgarstkiem drugiej ręki w okolicę międzyłopatkową; Jeżeli 5 uderzeń w okolicę międzyłopatkową nie spowoduje usunięcia ciała obcego, zastosuj 5 uciśnięć nadbrzusza zgodnie z zasadami: stań za poszkodowanym i obejmij go ramionami na wysokości nadbrzusza, pochyl go do przodu, Postępowanie w zadławieniu u dorosłych poszkodowanego i wystąpienia nieefektywnego kaszlu Ryc Algorytm postępowania w zadławieniu u dorosłych
85 86 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni 2 zaciśnij pięść i umieść ją pomiędzy pępkiem i wyrostkiem mieczykowatym, wolną ręką złap za zaciśniętą pięść i silnie pociągnij do wewnątrz i ku górze, powtórz tę czynność do 5 razy. Jeżeli te czynności nie spowodują usunięcia ciała obcego z dróg oddechowych, kontynuuj uderzenia w okolicę międzyłopatkową w połączeniu z uciśnięciami nadbrzusza. 3. Jeżeli poszkodowany straci przytomność: bezpiecznie ułóż go na ziemi, natychmiast wezwij pogotowie, rozpocznij RKO, zaczynając od uciśnięć klatki piersiowej. Łagodna niedrożność dróg oddechowych spowodowana ciałem obcym Kaszel generuje wysokie ciśnienie w drogach oddechowych i może usunąć ciało obce. Agresywne leczenie poprzez uderzenia w okolicę międzyłopatkową, uciśnięcia nadbrzusza i uciskanie klatki piersiowej może być przyczyną poważnych komplikacji, a nawet nasilić objawy niedrożności dróg oddechowych. Takie czynności powinny być zarezerwowane dla poszkodowanych z objawami ciężkiej niedrożności dróg oddechowych. U poszkodowanych z łagodną niedrożnością w każdej chwili może się rozwinąć ciężka niedrożność i dlatego należy ich obserwować do czasu, aż ich stan się poprawi. Ciężka niedrożność dróg oddechowych spowodowana ciałem obcym Dane kliniczne na temat zadławienia mają w dużej mierze charakter retrospektywny i dotyczą opisów pojedynczych przypadków. Opisy przypadków przytomnych dorosłych i dzieci powyżej 1. roku życia z całkowitą FBAO wykazały skuteczność uderzeń czy klepania w plecy oraz uciśnięć nadbrzusza lub klatki piersiowej 126. W około 50% przypadków niedrożności dróg oddechowych potrzebne było zastosowanie co najmniej dwóch z tych technik 127. Prawdopodobieństwo sukcesu wzrasta przy połączeniu uderzeń lub klepania w plecy z uciśnięciami nadbrzusza i klatki piersiowej 126. Randomizowane badanie na zwłokach 128 oraz dwa prospektywne badania, w których uczestniczyli znieczuleni ogólnie ochotnicy 129,130, wykazały, że uciśnięcia klatki piersiowej generują wyższe ciśnienia w drogach oddechowych, niż uciśnięcia nadbrzusza. Ponieważ uciśnięcia klatki piersiowej stosowane w FBAO są praktycznie identyczne jak uciśnięcia w trakcie resuscytacji, ratownicy powinni być nauczani rozpoczynania RKO, jeśli poszkodowany, u którego podejrzewa się lub stwierdza FBAO, traci przytomność. Celem uciśnięć klatki piersiowej jest przede wszystkim usunięcie niedrożności dróg oddechowych u leżącego, nieprzytomnego poszkodowanego, a tylko wtórnie wspomaganie krążenia. Dlatego uciśnięcia klatki piersiowej należy wykonywać nawet wtedy, gdy ratownik z wykształceniem medycznym wyczuwa u poszkodowanego tętno. Jeżeli nie uda się usunąć przyczyny niedrożności, dochodzi do postępującej bradykardii i asystolii. W trakcie RKO u osoby zadławionej, za każdym razem kiedy drogi oddechowe są udrażniane, należy szybko sprawdzić jamę ustną poszkodowanego, czy nie ma w niej ciała obcego, które mogło się tu przemieścić. W pozostałych przypadkach RKO rutynowe badanie zawartości ust w poszukiwaniu ciał obcych nie jest konieczne. Próba usunięcia ciała obcego na ślepo Nie ma badań oceniających rutynowe oczyszczanie palcem jamy ustnej poszkodowanego, gdy ciało obce nie jest widoczne Zanotowano natomiast 4 przypadki urazu u poszkodowanego 131, 134 lub ratownika na skutek takich działań 126. Dlatego należy unikać oczyszczania jamy ustnej na ślepo, a ciała obce powinno się usuwać tylko wtedy, gdy się je widzi. Dalsza opieka i przekazanie poszkodowanego personelowi medycznemu Po skutecznym leczeniu FBAO ciało obce może pozostać w górnej lub dolnej części dróg oddechowych i być przyczyną późniejszych komplikacji. Poszkodowani z uporczywym kaszlem, utrudnionym połykaniem lub uczuciem ciała obcego w drogach oddechowych powinni być skierowani na konsultację medyczną. Uciśnięcia nadbrzusza i klatki piersiowej mogą potencjalnie powodować poważne obrażenia wewnętrzne, dlatego wszyscy, u których były one stosowane, powinni być zbadani przez lekarza. Resuscytacja dzieci (patrz także rozdział 6) 134a i ofiar tonięcia (patrz także rozdział 8c) 134b U poszkodowanych z NZK z przyczyn kardiogennych, u których prowadzi się RKO z wyłącznym uciskaniem klatki piersiowej, rezerwy tlenu wyczerpują się po około 2 4 minutach od rozpoczęcia resuscytacji 92,104. Po tym czasie szczególnie istotne jest włączenie do RKO wentylacji. W przypadku NZK z powodu asfiksji od samego początku resuscytacji ważne jest połączenie uciśnięć klatki piersiowej i wentylacji. Poprzednie wytyczne próbowały podkreślić tę różnicę w patofizjologii i w przypadku poszkodowanych ze zidentyfikowaną asfiksją (tonięcie, toksyny) oraz u dzieci zalecały, aby ratownik (jeśli jest sam) prowadził RKO przez jedną minutę, zanim zostawi poszkodowanego, aby udać się po pomoc. Jednakże zdecydowana większość pozaszpitalnych epizodów NZK dotyczy osób dorosłych i, pomimo że w ciągu ostatnich lat częstość występowania VF jako pierwszego rejestrowanego rytmu w NZK spadła, nadal jest ono główną przyczyną NZK u osób dorosłych (59%), dokumentowaną we wczesnej fazie NZK przy użyciu AED 13. U dzieci do zatrzymania krążenia w mechanizmie VF dochodzi znacznie rzadziej (około 7%) 135. Wspomniane dodatkowe rekomendacje spowodowały rozbudowanie wytycznych, chociaż dotyczą jedynie niewielkiej grupy poszkodowanych. Należy być świadomym, że u wielu dzieci resuscytacja nie jest podejmowana, ponieważ potencjalni ratownicy boją się, że wyrządzą krzywdę, gdyż nie są przeszkoleni specyficznie w resuscytacji dzieci. Lęk jest nieuzasadniony, gdyż o wiele lepiej stosować u dzieci BLS według algorytmu dla dorosłych, niż nie robić nic. W celu uproszczenia nauczania i utrwalania wiedzy osoby bez wykształcenia medycznego powinno się nauczać, że sekwencja BLS dla dorosłych
86 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 87 może być stosowana także u dzieci, które są nieprzytomne i nie oddychają lub oddychają nieprawidłowo. Poniższe niewielkie modyfikacje w sekwencji postępowania u osób dorosłych spowodują, że algorytm ten stanie się jeszcze bardziej odpowiedni dla dzieci. Zanim rozpoczniesz uciśnięcia klatki piersiowej (sekwencja BLS u osób dorosłych, 5b), wykonaj 5 początkowych oddechów ratowniczych. Jeżeli działasz sam, prowadź RKO przez 1 minutę, zanim udasz się po pomoc. Uciskaj mostek na głębokość jednej trzeciej wymiaru przednio-tylnego klatki piersiowej; u niemowląt poniżej 1. roku życia używaj do tego dwóch palców; aby osiągnąć właściwą głębokość u dzieci powyżej 1. roku życia, używaj jednej lub obu rąk. Te same zmiany dotyczące 5 początkowych oddechów ratowniczych i prowadzenia RKO przez minutę przed wezwaniem pomocy, jeśli ratownik jest sam, mogą zwiększyć przeżywalność u ofiar tonięcia, ale takich modyfikacji powinno się uczyć wyłącznie te osoby, które mają zawodowy obowiązek udzielenia pomocy potencjalnym ofiarom tonięcia (np. ratowników wodnych). Łatwo rozpoznać tonięcie, ale przypadki zatrzymania krążenia wskutek urazu lub zatrucia mogą okazać się trudne do zidentyfikowania dla osób bez wykształcenia medycznego. Dlatego u takich poszkodowanych postępowanie powinno odbywać się zgodnie ze standardowym algorytmem BLS. Użycie automatycznego defibrylatora zewnętrznego Postępowanie z użyciem AED Rozdział 3 omawia wytyczne dotyczące defibrylacji wykonywanej za pomocą AED i klasycznego defibrylatora. AED są bezpieczne i skuteczne także w rękach osób bez wykształcenia medycznego i umożliwiają wykonanie defibrylacji na wiele minut przed dotarciem specjalistycznej pomocy. Ratownicy powinni kontynuować RKO i starać się minimalizować przerwy w uciśnięciach klatki piersiowej podczas naklejania elektrod i używania AED. Powinni się skoncentrować na stosowaniu się do głosowych zaleceń AED bez opóźnienia. Dotyczy to szczególnie natychmiastowego podjęcia RKO, gdy tylko AED to zaleci. Standardowe AED są odpowiednie dla dzieci powyżej 8. roku życia. U dzieci pomiędzy 1. a 8. rokiem życia, jeśli to możliwe, należy używać elektrod pediatrycznych razem z przystawką zmniejszającą energię defibrylacji lub możli- 2 reagować: poruszać się, otwierać oczy, oddychać prawidłowo Ryc Algorytm postępowania z użyciem AED
87 88 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni 2 wością włączenia trybu pediatrycznego. Jeżeli takie urządzenie nie jest dostępne, należy zastosować standardowe AED. Nie zaleca się stosowania AED u dzieci poniżej 1. roku życia. Istnieją jednak opisy kilku przypadków, w których użyto AED u dzieci poniżej 1. roku życia 136,137. Częstość występowania rytmów do defibrylacji u niemowląt jest bardzo niska za wyjątkiem sytuacji, kiedy przyczyną zatrzymania krążenia jest choroba serca 135,138,139. W tych rzadkich przypadkach, jeżeli AED jest jedynym dostępnym defibrylatorem, należy rozważyć jego użycie (najlepiej z przystawką zmniejszającą dawkę energii). Sekwencja użycia AED (ryc. 2.18) 1. Upewnij się, że ty, poszkodowany i pozostali świadkowie zdarzenia jesteście bezpieczni. 2. Postępuj zgodnie ze schematem BLS dla osób dorosłych (punkty 1 do 5). jeśli poszkodowany nie reaguje i nie oddycha prawidłowo, poproś kogoś o wezwanie pomocy oraz przyniesienie AED, jeśli jest dostępny, jeżeli jesteś sam, użyj telefonu komórkowego w celu wezwania pogotowia ratunkowego pozostaw poszkodowanego tylko w sytuacji, jeżeli nie ma innej możliwości wezwania pomocy. 3. Rozpocznij RKO zgodnie z wytycznymi BLS dla dorosłych. Jeżeli jesteś sam, a AED jest w pobliżu, rozpocznij od jego podłączenia. 4. Gdy tylko pojawi się AED: włącz go i naklej elektrody na odsłoniętą klatkę piersiową poszkodowanego (ryc. 2.19), jeśli ratowników jest więcej niż jeden, RKO powinna być prowadzona podczas naklejania elektrod, postępuj zgodnie z poleceniami głosowymi/wizualnymi bez opóźnienia, upewnij się, że nikt nie dotyka poszkodowanego, gdy AED przeprowadza analizę rytmu (ryc. 2.20). 5a. Jeżeli wyładowanie jest zalecane: upewnij się, że nikt nie dotyka poszkodowanego (ryc. 2.21), naciśnij przycisk defibrylacji zgodnie z poleceniem (w pełni zautomatyzowany AED dostarczy wyładowanie samoczynnie), natychmiast rozpocznij RKO 30 : 2 (ryc. 2.22) kontynuuj postępowanie zgodnie z dalszymi poleceniami głosowymi/wizualnymi. 5b. Jeżeli wyładowanie nie jest zalecane: niezwłocznie podejmij RKO, stosując sekwencję 30 uciśnięć do 2 wdechów ratowniczych, kontynuuj postępowanie zgodnie z dalszymi poleceniami głosowymi/wizualnymi. 6. Kontynuuj postępowanie zgodnie z poleceniami AED do chwili, gdy: przybędzie wykwalifikowana pomoc i przejmie działania, poszkodowany zacznie reagować: poruszy się, otworzy oczy i zacznie prawidłowo oddychać, ulegniesz wyczerpaniu. RKO przed defibrylacją Natychmiastowa defibrylacja, tak szybko, gdy tylko dostępny jest AED, zawsze była kluczowym elementem wytycznych i nauczania. Przypisuje się jej największy wpływ na przeżycie w migotaniu komór. Ta koncepcja została podważona, ponieważ istniały dowody sugerujące, iż uciskanie klatki piersiowej przed defibrylacją może zwiększyć szanse Ryc Naklejanie elektrod samoprzylepnych. Umieść pierwszą elektrodę w linii pachowej środkowej tuż poniżej dołu pachowego. Drugą elektrodę należy przykleić tuż pod prawym obojczykiem Ryc Podczas analizy rytmu przez AED nie wolno dotykać poszkodowanego
88 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 89 przeżycia w sytuacji, gdy czas od wezwania służb ratowniczych do ich przybycia przekraczał 5 minut 140, 141. Dwa ostatnio przeprowadzone badania kliniczne 142, 143 i jedno badanie na zwierzętach 144 nie potwierdziły zwiększenia przeżywalności. Z tego powodu obecnie nie zaleca się rutynowego prowadzenia RKO przez określony czas przed wykonaniem analizy rytmu i defibrylacji. Wysokiej jakości RKO musi być jednak kontynuowana w czasie naklejania elektrod i uruchamiania defibrylatora. Ogromny nacisk kładzie się na jak najszybsze podjęcie i minimalne przerywanie uciśnięć klatki piersiowej. Niektóre zespoły ratownictwa medycznego wprowadziły standardową procedurę prowadzenia uciśnięć klatki piersiowej przez ustalony czas przed wykonaniem defibrylacji; ze względu na brak przekonujących danych potwierdzających bądź negujących tę strategię, zasadne wydaje się kontynuowanie tej praktyki. Polecenia głosowe W wielu miejscach algorytm zaleca: postępuj zgodnie z poleceniami głosowymi/wizualnymi. Polecenia głosowe mogą być programowane i zaleca się, aby były zgodne z sekwencją wyładowań i czasem prowadzenia RKO określonym w rozdziale 2. Polecenia te powinny uwzględniać co najmniej: 1. Tylko pojedyncze wyładowania, gdy rozpoznany zostanie rytm do defibrylacji. 2. Niepodejmowanie analizy rytmu, oceny oddechu lub tętna po wyładowaniu. 3. Polecenie natychmiastowego podjęcia RKO po wyładowaniu (prowadzenie uciśnięć klatki piersiowej po powrocie spontanicznego krążenia nie jest szkodliwe) minuty RKO przed ponowną informacją o analizie rytmu. Sekwencja wyładowań i poziomy energii omówiono w rozdziale 3 2. W pełni zautomatyzowane AED W pełni zautomatyzowane AED dostarczą wyładowanie bez pomocy ratownika, gdy tylko wykryją rytm do defibrylacji. Pojedyncze badanie z użyciem manekinów pokazało, że nieprzeszkoleni studenci pielęgniarstwa rzadziej popełniali błędy dotyczące bezpieczeństwa, kiedy używali w pełni zautomatyzowanych AED, niż AED półautomatycznych 145. Nie ma żadnych danych z badań z udziałem ludzi, które określałyby, czy powyższe wyniki można odnieść do praktyki klinicznej. Programy publicznego dostępu do defibrylacji Należy rozważyć wdrażanie programów wczesnej defibrylacji z użyciem AED w warunkach pozaszpitalnych. Dotyczy to miejsc publicznych, takich jak lotniska 32, obiekty sportowe, biura, kasyna 35 i samoloty 33, gdzie do zatrzymania krążenia dochodzi zwykle w obecności świadków, a przeszkoleni ratownicy docierają szybko na miejsce zdarzenia. Programy AED z udziałem ratowników bez wykształcenia medycznego, z bardzo krótkim czasem dotarcia do poszkodowanego, oraz niekontrolowane badania, gdzie pierwszej pomocy udzielała policja 146, 147, zarejestrowały przeżywalność NZK sięgającą 49 74%. Sukces tych programów zależy od ilości przeszkolonych ratowników i dostępności AED. Dotychczas nie wykorzystano pełnego potencjału AED, ponieważ w większości przypadków używa się ich w miej- 2 Ryc Przed naciśnięciem przycisku wyładowania upewnij się, że nikt nie dotyka poszkodowanego Ryc Zaraz po wyładowaniu AED poinformuje cię o konieczności rozpoczęcia RKO. RKO należy podjąć natychmiast, wykonując naprzemiennie 30 uciśnięć klatki piersiowej i 2 oddechy ratownicze
89 90 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni 2 scach publicznych, a 60 80% NZK ma miejsce w domu. Programy publicznego dostępu do defibrylacji (PAD) oraz programy AED z udziałem kwalifikowanej pierwszej pomocy mogą zwiększyć liczbę osób, u których świadkowie zdarzenia podejmą RKO i wykonają wczesną defibrylację, i w związku z tym mogą zwiększyć przeżywalność w pozaszpitalnych zatrzymaniach krążenia 148. Ostatnie ogólnokrajowe badania w Japonii i USA 13, 43 wykazały, że gdy AED było dostępne, wykonywano defibrylację znacznie wcześniej, co zwiększało szansę przeżycia poszkodowanego. Jednakże defibrylację z użyciem AED wykonywano jedynie w 3,7% ( Japonia) i 5% (USA) zatrzymań krążenia w mechanizmie VF. Badanie japońskie wykazało wyraźnie, że stosunek liczby AED dostępnych na kilometr kwadratowy terenu był odwrotnie proporcjonalny do czasu pomiędzy utratą przytomności a wykonaniem pierwszej defibrylacji i wprost proporcjonalny do przeżywalności zatrzymań krążenia. W obu badaniach AED było używane znacznie częściej w miejscach publicznych aniżeli w obszarach mieszkalnych. Wysyłanie na miejsce zdarzenia służb kwalifikowanej pierwszej pomocy policji czy straży pożarnej (first responder programme) wydłuży czas rozpoczęcia resuscytacji, ale umożliwi objęcie programem całej populacji. Podczas wdrażania programów AED społeczność i osoby odpowiedzialne za organizację programu powinny rozważyć szereg zagadnień, takich jak: lokalizacja AED w strategicznych miejscach, stworzenie zespołu odpowiedzialnego za monitorowanie i utrzymanie sprawności urządzeń, programy szkoleń i szkoleń przypominających dla osób, które najprawdopodobniej będą używać AED, selekcja grupy ochotników zaangażowanych w udzielanie pierwszej pomocy z użyciem AED u poszkodowanych z zatrzymaniem krążenia 149. Problem logistyczny związany z organizacją programu kwalifikowanej pierwszej pomocy polega na tym, że powinny one przybyć na miejsce zdarzenia nie tylko wcześniej od pogotowia ratunkowego, ale być w stanie w czasie 5 6 minut od zgłoszenia telefonicznego wykonać defibrylację w elektrycznej lub krążeniowej fazie zatrzymania krążenia 44. Dłuższa zwłoka zmniejsza przeżywalność 36, 47 : zyskanie na czasie kilku minut nie będzie miało znaczenia, jeśli służby kwalifikowanej pierwszej pomocy przybędą na miejsce zdarzenia po 10 minutach od zgłoszenia lub nie dotrą tam przed pogotowiem ratunkowym 151. Programy kwalifikowanej pierwszej pomocy mogą tylko nieznacznie zredukować czas dotarcia, ale ponieważ obejmą swym zasięgiem większą liczbę poszkodowanych z obszarów mieszkalnych, mogą przynieść więcej korzyści niż programy PAD, które mają wpływ na znacznie mniejszą liczbę poszkodowanych z zatrzymaniem krążenia 152, 153. Programy publicznego dostępu do AED w obszarach mieszkalnych nie były dotychczas obiektem badań. Natomiast nie udowodniono korzyści z udostępniania AED indywidualnym osobom do użytku w domu, nawet jeśli występowało u nich zwiększone ryzyko zatrzymania krążenia 154. Ryc Uniwersalny symbol ILCOR, informujący o dostępności AED. Niniejszemu symbolowi mogą towarzyszyć strzałki wskazujące miejsce, w którym znajduje się AED Uniwersalne oznakowanie miejsc z dostępem do AED Gdy dojdzie do utraty przytomności i należy szybko odnaleźć AED, ważne jest, aby oznakowanie lokalizacji i najkrótszej drogi do AED było proste i przejrzyste. ILCOR opracował oznakowanie rozpoznawane na całym świecie i zalecane w celu identyfikacji lokalizacji AED (ryc. 2.23). Więcej informacji o wyglądzie i zastosowaniu uniwersalnego znaku AED można znaleźć na stronach: oraz Bibliografia 1. Recommended guidelines for uniform reporting of data from out-of-hospital cardiac arrest: the Utstein style. Prepared by a Task Force of Representatives from the European Resuscitation Council, American Heart Association, Heart and Stroke Foundation of Canada, Australian Resuscitation Council. Resuscitation 1991;22: Deakin CD, Nolan JP, Sunde K, Koster RW. European Resuscitation Council Guidelines for Resuscitation Section 3. Electrical therapies: automated external defibrillators, defibrillation, cardioversion and pacing. Resuscitation 2010;81: Deakin CD, Nolan JP, Soar J, et al. European Resuscitation Council Guidelines for Resuscitation Section 4. Adult advanced life support. Resuscitation 2010;81: Sans S, Kesteloot H, Kromhout D. The burden of cardiovascular diseases mortality in Europe. Task Force of the European Society of Cardiology on Cardiovascular Mortality and Morbidity Statistics in Europe. Eur Heart J 1997;18: Atwood C, Eisenberg MS, Herlitz J, Rea TD. Incidence of EMS-treated out-of- -hospital cardiac arrest in Europe. Resuscitation 2005;67: Cobb LA, Fahrenbruch CE, Olsufka M, Copass MK. Changing incidence of out-of-hospital ventricular fibrillation, JAMA 2002;288: Rea TD, Pearce RM, Raghunathan TE, et al. Incidence of out-of-hospital cardiac arrest. Am J Cardiol 2004;93: Vaillancourt C, Verma A, Trickett J, et al. Evaluating the effectiveness of dispatch-assisted cardiopulmonary resuscitation instructions. Acad Emerg Med 2007;14: Agarwal DA, Hess EP, Atkinson EJ, White RD. Ventricular fibrillation in Rochester, Minnesota: experience over 18 years. Resuscitation 2009;80: Ringh M, Herlitz J, Hollenberg J, Rosenqvist M, Svensson L. Out of hospital cardiac arrest outside home in Sweden, change in characteristics, outcome and availability for public access defibrillation. Scand J Trauma Resusc Emerg Med 2009;17: Cummins R, Thies W. Automated external defibrillators and the Advanced Cardiac Life Support Program: a new initiative from the American Heart Association. Am J Emerg Med 1991;9: Waalewijn RA, Nijpels MA, Tijssen JG, Koster RW. Prevention of deterioration of ventricular fibrillation by basic life support during out-of-hospital cardiac arrest. Resuscitation 2002;54: Weisfeldt ML, Sitlani CM, Ornato JP, et al. Survival after application of automatic external defibrillators before arrival of the emergency medical system: evaluation in the resuscitation outcomes consortium population of 21 million. J Am Coll Cardiol 2010;55: van Alem AP, Vrenken RH, de Vos R, Tijssen JG, Koster RW. Use of automated external defibrillator by first responders in out-of-hospital cardiac arrest: prospective controlled trial. BMJ 2003;327:1312.
90 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) Nolan J, Soar J, Eikeland H. The chain of survival. Resuscitation 2006;71: Muller D, Agrawal R, Arntz HR. How sudden is sudden cardiac death? Circulation 2006;114: Lowel H, Lewis M, Hormann A. Prognostic significance of prehospital phase in acute myocardial infarct. Results of the Augsburg Myocardial Infarct Registry, Dtsch Med Wochenschr 1991;116: Waalewijn RA, Tijssen JG, Koster RW. Bystander initiated actions in out-of- -hospital cardiopulmonary resuscitation: results from the Amsterdam Resuscitation Study (ARREST). Resuscitation 2001;50: Valenzuela TD, Roe DJ, Cretin S, Spaite DW, Larsen MP. Estimating effectiveness of cardiac arrest interventions: a logistic regression survival model. Circulation 1997;96: Holmberg M, Holmberg S, Herlitz J. Factors modifying the effect of bystander cardiopulmonary resuscitation on survival in out-of-hospital cardiac arrest patients in Sweden. Eur Heart J 2001;22: Holmberg M, Holmberg S, Herlitz J, Gardelov B. Survival after cardiac arrest outside hospital in Sweden. Swedish Cardiac Arrest Registry. Resuscitation 1998;36: SOS-KANTO Study Group. Cardiopulmonary resuscitation by bystanders with chest compression only (SOS-KANTO): an observational study. Lancet 2007;369: Iwami T, Kawamura T, Hiraide A, et al. Effectiveness of bystander-initiated cardiac-only resuscitation for patients with out-of-hospital cardiac arrest. Circulation 2007;116: Rea TD, Eisenberg MS, Culley LL, Becker L. Dispatcher-assisted cardiopulmonary resuscitation and survival in cardiac arrest. Circulation 2001;104: Kuisma M, Boyd J, Vayrynen T, Repo J, Nousila-Wiik M, Holmstrom P. Emergency call processing and survival from out-of-hospital ventricular fibrillation. Resuscitation 2005;67: Rea TD, Fahrenbruch C, Culley L, et al. CPR with chest compresssions alone or with rescue breathing. N Engl J Med 2010;363: Svensson L, Bohm K, Castren M, et al. Compression-only CPR or standard CPR in out-of-hospital cardiac arrest. N Engl J Med 2010;363: Weaver WD, Hill D, Fahrenbruch CE, et al. Use of the automatic external defibrillator in the management of out-of-hospital cardiac arrest. N Engl J Med 1988;319: Auble TE, Menegazzi JJ, Paris PM. Effect of out-of-hospital defibrillation by basic life support providers on cardiac arrest mortality: a metaanalysis. Ann Emerg Med 1995;25: Stiell IG, Wells GA, Field BJ, et al. Improved out-of-hospital cardiac arrest survival through the inexpensive optimization of an existing defibrillation program: OPALS study phase II. Ontario prehospital advanced life support. JAMA 1999;281: Stiell IG, Wells GA, DeMaio VJ, et al. Modifiable factors associated with improved cardiac arrest survival in a multicenter basic life support/defibrillation system: OPALS Study Phase I results. Ontario prehospital advanced life support. Ann Emerg Med 1999;33: Caffrey S. Feasibility of public access to defibrillation. Curr Opin Crit Care 2002;8: O Rourke MF, Donaldson E, Geddes JS. An airline cardiac arrest program. Circulation 1997;96: Page RL, Hamdan MH, McKenas DK. Defibrillation aboard a commercial aircraft. Circulation 1998;97: Valenzuela TD, Roe DJ, Nichol G, Clark LL, Spaite DW, Hardman RG. Outcomes of rapid defibrillation by security officers after cardiac arrest in casinos. N Engl J Med 2000;343: Waalewijn RA, de Vos R, Tijssen JG, Koster RW. Survival models for out-of- -hospital cardiopulmonary resuscitation from the perspectives of the bystander, the first responder, and the paramedic. Resuscitation 2001;51: Carr BG, Kahn JM, Merchant RM, Kramer AA, Neumar RW. Inter-hospital variability in post-cardiac arrest mortality. Resuscitation 2009;80: Neumar RW, Nolan JP, Adrie C, et al. Post-cardiac arrest syndrome: epidemiology, pathophysiology, treatment, and prognostication. A consensus statement from the International Liaison Committee on Resuscitation (American Heart Association, Australian and New Zealand Council on Resuscitation, European Resuscitation Council, Heart and Stroke Foundation of Canada, InterAmerican Heart Foundation, Resuscitation Council of Asia, and the Resuscitation Council of Southern Africa); the American Heart Association Emergency Cardiovascular Care Committee; the Council on Cardiovascular Surgery and Anesthesia; the Council on Cardiopulmonary, Perioperative, and Critical Care; the Council on Clinical Cardiology; and the Stroke Council. Circulation 2008;118: Sunde K, Pytte M, Jacobsen D, et al. Implementation of a standardised treatment protocol for post resuscitation care after out-of-hospital cardiac arrest. Resuscitation 2007;73: Bernard SA, Gray TW, Buist MD, et al. Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia. N Engl J Med 2002;346: Mild therapeutic hypothermia to improve the neurologic outcome after cardiac arrest. N Engl J Med 2002;346: Arrich J, Holzer M, Herkner H, Mullner M. Hypothermia for neuroprotection in adults after cardiopulmonary resuscitation. Cochrane Database Syst Rev CD Kitamura T, Iwami T, Kawamura T, Nagao K, Tanaka H, Hiraide A. Nationwide public-access defibrillation in Japan. N Engl J Med 2010;362: Weisfeldt ML, Becker LB. Resuscitation after cardiac arrest: a 3-phase time-sensitive model. JAMA 2002;288: White RD, Russell JK. Refibrillation, resuscitation and survival in out-of-hospital sudden cardiac arrest victims treated with biphasic automated external defibrillators. Resuscitation 2002;55: Kerber RE, Becker LB, Bourland JD, et al. Automatic external defibrillators for public access defibrillation: recommendations for specifying and reporting arrhythmia analysis algorithm performance, incorporating new waveforms, and enhancing safety. A statement for health professionals from the American Heart Association Task Force on Automatic External Defibrillation, Subcommittee on AED Safety and Efficacy. Circulation 1997;95: Larsen MP, Eisenberg MS, Cummins RO, Hallstrom AP. Predicting survival from out-of-hospital cardiac arrest: a graphic model. Ann Emerg Med 1993;22: Holmberg M, Holmberg S, Herlitz J. Effect of bystander cardiopulmonary resuscitation in out-of-hospital cardiac arrest patients in Sweden. Resuscitation 2000;47: Aprahamian C, Thompson BM, Finger WA, Darin JC. Experimental cervical spine injury model: evaluation of airway management and splinting techniques. Ann Emerg Med 1984;13: Bahr J, Klingler H, Panzer W, Rode H, Kettler D. Skills of lay people in checking the carotid pulse. Resuscitation 1997;35: Nyman J, Sihvonen M. Cardiopulmonary resuscitation skills in nurses and nursing students. Resuscitation 2000;47: Tibballs J, Russell P. Reliability of pulse palpation by healthcare personnel to diagnose paediatric cardiac arrest. Resuscitation 2009;80: Ruppert M, Reith MW, Widmann JH, et al. Checking for breathing: evaluation of the diagnostic capability of emergency medical services personnel, physicians, medical students, and medical laypersons. Ann Emerg Med 1999;34: Perkins GD, Stephenson B, Hulme J, Monsieurs KG. Birmingham assessment of breathing study (BABS). Resuscitation 2005;64: Hauff SR, Rea TD, Culley LL, Kerry F, Becker L, Eisenberg MS. Factors impeding dispatcher-assisted telephone cardiopulmonary resuscitation. Ann Emerg Med 2003;42: Bobrow BJ, Zuercher M, Ewy GA, et al. Gasping during cardiac arrest in humans is frequent and associated with improved survival. Circulation 2008;118: Clark JJ, Larsen MP, Culley LL, Graves JR, Eisenberg MS. Incidence of agonal respirations in sudden cardiac arrest. Ann Emerg Med 1992;21: Karlsten R, Elowsson P. Who calls for the ambulance: implications for decision support. A descriptive study from a Swedish dispatch centre. Eur J Emerg Med 2004;11: Nurmi J, Pettila V, Biber B, Kuisma M, Komulainen R, Castren M. Effect of protocol compliance to cardiac arrest identification by emergency medical dispatchers. Resuscitation 2006;70: Berdowski J, Beekhuis F, Zwinderman AH, Tijssen JG, Koster RW. Importance of the first link: description and recognition of an out-of-hospital cardiac arrest in an emergency call. Circulation 2009;119: Clawson J, Olola C, Heward A, Patterson B. Cardiac arrest predictability in seizure patients based on emergency medical dispatcher identification of previous seizure or epilepsy history. Resuscitation 2007;75: Mithoefer JC, Mead G, Hughes JM, Iliff LD, Campbell EJ. A method of distinguishing death due to cardiac arrest from asphyxia. Lancet 1967;2: Kern KB, Hilwig RW, Berg RA, Sanders AB, Ewy GA. Importance of continuous chest compressions during cardiopulmonary resuscitation: improved outcome during a simulated single lay-rescuer scenario. Circulation 2002;105: Bobrow BJ, Clark LL, Ewy GA, et al. Minimally interrupted cardiac resuscitation by emergency medical services for out-of-hospital cardiac arrest. JAMA 2008;299: Taylor RB, Brown CG, Bridges T, Werman HA, Ashton J, Hamlin RL. A model for regional blood flow measurements during cardiopulmonary resuscitation in a swine model. Resuscitation 1988;16: Aufderheide TP, Sigurdsson G, Pirrallo RG, et al. Hyperventilation-induced hypotension during cardiopulmonary resuscitation. Circulation 2004;109: Eftestol T, Sunde K, Steen PA. Effects of interrupting precordial compressions on the calculated probability of defibrillation success during out-of-hospital cardiac arrest. Circulation 2002;105: Wenzel V, Idris AH, Banner MJ, Kubilis PS, Williams JLJ. Influence of tidal volume on the distribution of gas between the lungs and stomach in the nonintubated patient receiving positive-pressure ventilation. Crit Care Med 1998;26: Idris A, Gabrielli A, Caruso L. Smaller tidal volume is safe and effective for bagvalve-ventilation, but not for mouth-to-mouth ventilation: an animal model for basic life support. Circulation 1999;100:I Idris A, Wenzel V, Banner MJ, Melker RJ. Smaller tidal volumes minimize gastric inflation during CPR with an unprotected airway. Circulation 1995;92(Suppl.):I Dorph E, Wik L, Steen PA. Arterial blood gases with 700 ml tidal volumes during out-of-hospital CPR. Resuscitation 2004;61: Winkler M, Mauritz W, Hackl W, et al. Effects of half the tidal volume during cardiopulmonary resuscitation on acid base balance and haemodynamics in pigs. Eur J Emerg Med 1998;5: Ruben H. The immediate treatment of respiratory failure. Br J Anaesth 1964;36:
91 92 R.W. Koster, M.A. Baubin, L.L. Bossaert, A. Caballero, P. Cassan, M. Castrén, C. Granja, A.J. Handley, K.G. Monsieurs, G.D. Perkins, V. Raffay, C. Sandroni Elam JO. Bag-valve-mask O 2 ventilation. In: Safar P, Elam JO, editors. Advances in cardiopulmonary resuscitation: the Wolf Creek conference on cardiopulmonary resuscitation. New York, NY: Springer-Verlag, Inc.; p Dailey RH. The airway: emergency management. St. Louis, MO: Mosby Year Book; Paradis NA, Martin GB, Goetting MG, et al. Simultaneous aortic, jugular bulb, and right atrial pressures during cardiopulmonary resuscitation in humans. Insights into mechanisms. Circulation 1989;80: Kramer-Johansen J, Myklebust H, Wik L, et al. Quality of out-of-hospital cardiopulmonary resuscitation with real time automated feedback: a prospective interventional study. Resuscitation 2006;71: Edelson DP, Abella BS, Kramer-Johansen J, et al. Effects of compression depth and pre-shock pauses predict defibrillation failure during cardiac arrest. Resuscitation 2006;71: Wik L, Kramer-Johansen J, Myklebust H, et al. Quality of cardiopulmonary resuscitation during out-of-hospital cardiac arrest. JAMA 2005;293: Abella BS, Alvarado JP, Myklebust H, et al. Quality of cardiopulmonary resuscitation during in-hospital cardiac arrest. JAMA 2005;293: Christenson J, Andrusiek D, Everson-Stewart S, et al. Chest compression fraction determines survival in patients with out-of-hospital ventricular fibrillation. Circulation 2009;120: Ochoa FJ, Ramalle-Gomara E, Carpintero JM, Garcia A, Saralegui I. Competence of health professionals to check the carotid pulse. Resuscitation 1998;37: Shin J, Rhee JE, Kim K. Is the inter-nipple line the correct hand position for effective chest compression in adult cardiopulmonary resuscitation? Resuscitation 2007;75: Kusunoki S, Tanigawa K, Kondo T, Kawamoto M, Yuge O. Safety of the inter-nipple line hand position landmark for chest compression. Resuscitation 2009;80: Delvaux AB, Trombley MT, Rivet CJ, et al. Design and development of a cardiopulmonary resuscitation mattress. J Intensive Care Med 2009;24: Perkins GD, Smith CM, Augre C, et al. Effects of a backboard, bed height, and operator position on compression depth during simulated resuscitation. Intensive Care Med 2006;32: Perkins GD, Kocierz L, Smith SC, McCulloch RA, Davies RP. Compression feedback devices over estimate chest compression depth when performed on a bed. Resuscitation 2009;80: Aufderheide TP, Pirrallo RG, Yannopoulos D, et al. Incomplete chest wall decompression: a clinical evaluation of CPR performance by EMS personnel and assessment of alternative manual chest compression decompression techniques. Resuscitation 2005;64: Yannopoulos D, McKnite S, Aufderheide TP, et al. Effects of incomplete chest wall decompression during cardiopulmonary resuscitation on coronary and cerebral perfusion pressures in a porcine model of cardiac arrest. Resuscitation 2005;64: Sanders AB, Kern KB, Berg RA, Hilwig RW, Heidenrich J, Ewy GA. Survival and neurologic outcome after cardiopulmonary resuscitation with four different chest compression ventilation ratios. Ann Emerg Med 2002;40: Dorph E, Wik L, Stromme TA, Eriksen M, Steen PA. Quality of CPR with three different ventilation:compression ratios. Resuscitation 2003;58: Dorph E, Wik L, Stromme TA, Eriksen M, Steen PA. Oxygen delivery and return of spontaneous circulation with ventilation:compression ratio 2:30 versus chest compressions only CPR in pigs. Resuscitation 2004;60: Babbs CF, Kern KB. Optimum compression to ventilation ratios in CPR under realistic, practical conditions: a physiological and mathematical analysis. Resuscitation 2002;54: Fenici P, Idris AH, Lurie KG, Ursella S, Gabrielli A. What is the optimal chest compression ventilation ratio? Curr Opin Crit Care 2005;11: Sayre MR, Cantrell SA, White LJ, Hiestand BC, Keseg DP, Koser S. Impact of the 2005 American Heart Association cardiopulmonary resuscitation and emergency cardio vascular care guidelines on out-of-hospital cardiac arrest survival. Prehosp Emerg Care 2009;13: Olasveengen TM, Vik E, Kuzovlev A, Sunde K. Effect of implementation of new resuscitation guidelines on quality of cardiopulmonary resuscitation and survival. Resuscitation 2009;80: Aufderheide TP, Lurie KG. Death by hyperventilation: a common and lifethreatening problem during cardiopulmonary resuscitation. Crit Care Med 2004;32:S Ornato JP, Hallagan LF, McMahan SB, Peeples EH, Rostafinski AG. Attitudes of BCLS instructors about mouth-to-mouth resuscitation during the AIDS epidemic. Ann Emerg Med 1990;19: Hew P, Brenner B, Kaufman J. Reluctance of paramedics and emergency medical technicians to perform mouth-to-mouth resuscitation. J Emerg Med 1997;15: Chandra NC, Gruben KG, Tsitlik JE, et al. Observations of ventilation during resuscitation in a canine model. Circulation 1994;90: Geddes LA, Rundell A, Otlewski M, Pargett M. How much lung ventilation is obtained with only chest-compression CPR? Cardiovasc Eng 2008;8: Berg RA, Kern KB, Hilwig RW, et al. Assisted ventilation does not improve outcome in a porcine model of single-rescuer bystander cardiopulmonary resuscitation. Circulation 1997;95: Berg RA, Kern KB, Hilwig RW, Ewy GA. Assisted ventilation during bystander CPR in a swine acute myocardial infarction model does not improve outcome. Circulation 1997;96: Turner I, Turner S, Armstrong V. Does the compression to ventilation ratio affect the quality of CPR: a simulation study. Resuscitation 2002;52: Bohm K, Rosenqvist M, Herlitz J, Hollenberg J, Svensson L. Survival is similar after standard treatment and chest compression only in out-of-hospital bystander cardiopulmonary resuscitation. Circulation 2007;116: Kitamura T, Iwami T, Kawamura T, Nagao K, Tanaka H, Hiraide A. Bystanderinitiated rescue breathing for out-of-hospital cardiac arrests of noncardiac origin. Circulation 2010;122: Kitamura T, Iwami T, Kawamura T, et al. Conventional and chest-compression only cardiopulmonary resuscitation by bystanders for children who have out-of- -hospital cardiac arrests: a prospective, nationwide, population-based cohort study. Lancet 2010;375: Handley AJ, Handley JA. Performing chest compressions in a confined space. Resuscitation 2004;61: Perkins GD, Stephenson BT, Smith CM, Gao F. A comparison between over-thehead and standard cardiopulmonary resuscitation. Resuscitation 2004;61: White L, Rogers J, Bloomingdale M, et al. Dispatcher-assisted cardiopulmonary resuscitation: risks for patients not in cardiac arrest. Circulation 2010;121: Cheung W, Gullick J, Thanakrishnan G, et al. Injuries occurring in hospital staff attending medical emergency team (MET) calls a prospective, observational study. Resuscitation 2009;80: Sullivan F, Avstreih D. Pneumothorax during CPR training: case report and review of the CPR literature. Prehosp Disaster Med 2000;15: Peberdy MA, Ottingham LV, Groh WJ, et al. Adverse events associated with lay emergency response programs: the public access defibrillation trial experience. Resuscitation 2006;70: Sugerman NT, Edelson DP, Leary M, et al. Rescuer fatigue during actual inhospital cardiopulmonary resuscitation with audiovisual feedback: a prospective multicenter study. Resuscitation 2009;80: Hallstrom AP, Ornato JP, Weisfeldt M, et al. Public-access defibrillation and survival after out-of-hospital cardiac arrest. N Engl J Med 2004;351: Hoke RS, Heinroth K, Trappe HJ, Werdan K. Is external defibrillation an electric threat for bystanders? Resuscitation 2009;80: Axelsson A, Herlitz J, Karlsson T, et al. Factors surrounding cardiopulmonary resuscitation influencing bystanders psychological reactions. Resuscitation 1998;37: Axelsson A, Herlitz J, Ekstrom L, Holmberg S. Bystander-initiated cardiopulmonary resuscitation out-of-hospital. A first description of the bystanders and their experiences. Resuscitation 1996;33: Mejicano GC, Maki DG. Infections acquired during cardiopulmonary resuscitation: estimating the risk and defining strategies for prevention. Ann Intern Med 1998;129: Cydulka RK, Connor PJ, Myers TF, Pavza G, Parker M. Prevention of oral bacterial flora transmission by using mouth-to-mask ventilation during CPR. J Emerg Med 1991;9: Blenkharn JI, Buckingham SE, Zideman DA. Prevention of transmission of infection during mouth-to-mouth resuscitation. Resuscitation 1990;19: Turner S, Turner I, Chapman D, et al. A comparative study of the 1992 and 1997 recovery positions for use in the UK. Resuscitation 1998;39: Handley AJ. Recovery Position. Resuscitation 1993;26: Anonymous. Guidelines 2000 for Cardiopulmonary resuscitation and emergency cardiovascular care an international consensus on science. Resuscitation 2000;46: Fingerhut LA, Cox CS, Warner M. International comparative analysis of injury mortality. Findings from the ICE on injury statistics. International Collaborative Effort on Injury Statistics. Adv Data 1998: Proceedings of the 2005 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Resuscitation 2005;67: Redding JS. The choking controversy: critique of evidence on the Heimlich maneuver. Crit Care Med 1979;7: Langhelle A, Sunde K, Wik L, Steen PA. Airway pressure with chest compressions versus Heimlich manoeuvre in recently dead adults with complete airway obstruction. Resuscitation 2000;44: Guildner CW, Williams D, Subitch T. Airway obstructed by foreign material: the Heimlich maneuver. JACEP 1976;5: Ruben H, Macnaughton FI. The treatment of food-choking. Practitioner 1978;221: Hartrey R, Bingham RM. Pharyngeal trauma as a result of blind finger sweeps in the choking child. J Accid Emerg Med 1995;12: Elam JO, Ruben AM, Greene DG. Resuscitation of drowning victims. JAMA 1960;174: Ruben HM, Elam JO, Ruben AM, Greene DG. Investigation of upper airway problems in resuscitation, 1: studies of pharyngeal x-rays and performance by laymen. Anesthesiology 1961;22: Kabbani M, Goodwin SR. Traumatic epiglottis following blind finger sweep to remove a pharyngeal foreign body. Clin Pediatr (Phila) 1995;34: a. European Resuscitation Council Guidelines for Resuscitation 2010: Section 6: Paediatric life support. Resuscitation 2010; 81: b. European Resuscitation Council Guidelines for Resuscitation 2010: Section 8: Cardiac arrest in special circumstances. Resuscitation 2010; 81: Atkins DL, Everson-Stewart S, Sears GK, et al. Epidemiology and outcomes from out-of-hospital cardiac arrest in children: the Resuscitation Outcomes Consortium Epistry-Cardiac Arrest. Circulation 2009;119:
92 Podstawowe zabiegi resuscytacyjne u osób dorosłych oraz zastosowanie automatycznych defibrylatorów zewnętrznych (AED) 136. Bar-Cohen Y, Walsh EP, Love BA, Cecchin F. First appropriate use of automated external defibrillator in an infant. Resuscitation 2005;67: Divekar A, Soni R. Successful parental use of an automated external defibrillator for an infant with long-qt syndrome. Pediatrics 2006;118:e Rodriguez-Nunez A, Lopez-Herce J, Garcia C, Dominguez P, Carrillo A, Bellon JM. Pediatric defibrillation after cardiac arrest: initial response and outcome. Crit Care 2006;10:R Samson RA, Nadkarni VM, Meaney PA, Carey SM, Berg MD, Berg RA. Out-comes of in-hospital ventricular fibrillation in children. N Engl J Med 2006;354: Cobb LA, Fahrenbruch CE, Walsh TR, et al. Influence of cardiopulmonary resuscitation prior to defibrillation in patients with out-of-hospital ventricular fibrillation. JAMA 1999;281: Wik L, Hansen TB, Fylling F, et al. Delaying defibrillation to give basic cardiopulmonary resuscitation to patients with out-of-hospital ventricular fibrillation: a randomized trial. JAMA 2003;289: Jacobs IG, Finn JC, Oxer HF, Jelinek GA. CPR before defibrillation in out-of- -hospital cardiac arrest: a randomized trial. Emerg Med Australas 2005;17: Baker PW, Conway J, Cotton C, et al. Defibrillation or cardiopulmonary resuscitation first for patients with out-of-hospital cardiac arrests found by paramedics to be in ventricular fibrillation? A randomised control trial. Resuscitation 2008;79: Indik JH, Hilwig RW, Zuercher M, Kern KB, Berg MD, Berg RA. Preshock cardiopulmonary resuscitation worsens outcome from circulatory phase ventricular fibrillation with acute coronary artery obstruction in swine. Circ Arrhythm Electrophysiol 2009;2: Monsieurs KG, Vogels C, Bossaert LL, Meert P, Calle PA. A study comparing the usability of fully automatic versus semi-automatic defibrillation by untrained nursing students. Resuscitation 2005;64: White RD, Bunch TJ, Hankins DG. Evolution of a community-wide early defibrillation programme experience over 13 years using police/fire personnel and paramedics as responders. Resuscitation 2005;65: Mosesso Jr VN, Davis EA, Auble TE, Paris PM, Yealy DM. Use of automated external defibrillators by police officers for treatment of out-of-hospital cardiac arrest. Ann Emerg Med 1998;32: The public access defibrillation trial investigators. Public-access defibrillation and survival after out-of-hospital cardiac arrest. N Engl J Med 2004;351: Priori SG, Bossaert LL, Chamberlain DA, et al. Policy statement: ESC ERC recommendations for the use of automated external defibrillators (AEDs) in Europe. Resuscitation 2004;60: Groh WJ, Newman MM, Beal PE, Fineberg NS, Zipes DP. Limited response to cardiac arrest by police equipped with automated external defibrillators: lack of survival benefit in suburban and rural Indiana the police as responder automated defibrillation evaluation (PARADE). Acad Emerg Med 2001;8: Sayre MR, Swor R, Pepe PE, Overton J. Current issues in cardiopulmonary resuscitation. Prehosp Emerg Care 2003;7: Nichol G, Hallstrom AP, Ornato JP, et al. Potential cost-effectiveness of public access defibrillation in the United States. Circulation 1998;97: Nichol G, Valenzuela T, Roe D, Clark L, Huszti E, Wells GA. Cost effectiveness of defibrillation by targeted responders in public settings. Circulation 2003;108: Bardy GH, Lee KL, Mark DB, et al. Home use of automated external defibrillators for sudden cardiac arrest. N Engl J Med 2008;358:
93 Publikacja przygotowana przez Europejską Radę Resuscytacji (ERC) przy współpracy z Polską Radą Resuscytacji (PRR). Tekst tłumaczony przez Polską Radę Resuscytacji. Wiedza i praktyka w zakresie resuscytacji krążeniowo-oddechowej to stale zmieniająca się dziedzina medycyny. W miarę rozwoju wiedzy oraz postępu w nauce i doświadczeniu klinicznym zmienia się w sposób ciągły również praktyka medycz na oraz sposób stosowania leków. Czytelnik tego podręcznika jest zobowiązany do zapoznania się z aktualnymi wiado mościami na temat przedstawionych sposobów postępowania i farmakoterapii ze szczególnym uwzględnieniem informacji producentów na temat dawek, czasu i drogi podawania oraz efektów ubocznych stosowanych leków. Na każdej z osób praktykujących medycynę resuscytacji spoczywa osobista odpowiedzialność za stosowane metody lecznicze, których uży cie powinno być oparte na gruntownej wiedzy i umiejętnościach praktycznych z zachowaniem niezbędnych warunków bez pieczeństwa własnego i pacjenta. Wydawcy oraz redaktorzy niniejszego opracowania nie ponoszą odpowiedzialności za szkody, które mogłyby być w jakikolwiek sposób związane z materiałem zawartym w tej książce. Bibliografia do wszystkich rozdziałów została w całości powtórzona za wydaniem oryginalnym. REDAKTOR NAUKOWY WYDANIA POLSKIEGO prof. dr hab. Janusz Andres TŁUMACZENIE Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Elżbieta Dobrowolska, Edyta Drab, Bartosz Frączek, Anna Jarosz, Piotr Kolęda, Paweł Krawczyk, Rafał Surmacz, Jurij Szymański, Grzegorz Zając KOREKTA MERYTORYCZNA Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Bartosz Frączek, Paweł Krawczyk ADIUSTACJA I KOREKTA WYDAWNICZA Danuta Ambrożewicz PROJEKT OKŁADKI Polska Rada Resuscytacji wg plakatu V Międzynarodowego Kongresu Polskiej Rady Resuscytacji autorstwa Mieczysława Górowskiego Publikację wydano ze środków Polskiej Rady Resuscytacji. Copyright by European Resuscitation Council (ERC), 2010 Copyright for the Polish edition by Polska Rada Resuscytacji, Kraków 2010 Copyright for the Polish translation by Polska Rada Resuscytacji, Kraków 2010 Wszystkie prawa zastrzeżone. Żadna część poniższej publikacji nie może być kopiowana i przechowywana w jakimkol wiek mechanicznym systemie kopiowania danych, włączając fotokopie, kserokopie, nagrania i inne, bez uprzedniej pisem nej zgody PRR (dotyczy terenu Rzeczpospolitej Polskiej). Wszystkie prośby o możliwość wykorzystania materiałów zawartych w tej publikacji należy kierować do ERC. ISBN KOORDYNATOR STRONY ORAZ WERSJI ELEKTRONICZNEJ Wytycznych resuscytacji 2010 Wiesław Pyrczak prc@prc.krakow.pl ADRES DO KORESPONDENCJI ADRES DO KORESPONDENCJI W POLSCE ERC Secretariat VZW Polska Rada Resuscytacji Drie Eikenstraat 661 ul. Radziwiłłowska 4, Kraków BE-2650 EDEGEM tel fax Belgium biuro@prc.krakow.pl tel fax Koordynator kursów info@erc.edu Tomasz Galewicz kursy@prc.krakow.pl SKŁAD I PRZYGOTOWANIE DO DRUKU FALL ul. Garczyńskiego 2, Kraków tel ; fall@fall.pl
94 Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja 3 Charles D. Deakin a,*, Jerry P. Nolan b, Kjetil Sunde c, Rudolph W. Koster d a Southampton University Hospital NHS Trust, Southampton, UK b Royal United Hospital, Bath, UK c Oslo University Hospital Ulleval, Oslo, Norway d Department of Cardiology, Academic Medical Center, Amsterdam, The Netherlands Podsumowanie zmian od czasu Wytycznych 2005 Poniżej zestawiono najbardziej istotne zmiany dotyczące elektroterapii w Wytycznych resuscytacji 2010 Europejskiej Rady Resuscytacji (ERC): Wytyczne zwiększają nacisk na wczesne podjęcie i unikanie przerw w uciśnięciach klatki piersiowej. Znacznie większy nacisk został położony na unikanie przerw zarówno przed-, jak i po defibrylacji. Zaleca się kontynuowanie uciśnięć klatki piersiowej podczas ładowania defibrylatora. Zaleca się również natychmiastowe podjęcie uciśnięć klatki piersiowej po defibrylacji; w połączeniu z kontynuacją uciśnięć podczas ładowania defibrylatora, wykonanie defibrylacji powinno być możliwe z przerwą w uciśnięciach klatki piersiowej nie dłuższą niż 5 sek. Bezpieczeństwo ratownika pozostaje najważniejsze, jednak wytyczne podkreślają, iż ryzyko porażenia ratownika w czasie defibrylacji jest bardzo małe, szczególnie jeśli nosi on rękawiczki. Aktualnie uwaga skupia się na szybkiej ocenie bezpieczeństwa, aby skrócić czas przerwy przed defibrylacją. Podczas leczenia pozaszpitalnego zatrzymania krążenia zespół ratownictwa medycznego powinien prowadzić dobrej jakości RKO w trakcie oczekiwania na defibrylator, podłączania go i ładowania. Nie zaleca się rutynowego prowadzenia RKO przez określony okres czasu (np. 2 czy 3 minuty) przed analizą rytmu i defibrylacją. W przypadku niektórych systemów pomocy doraźnej, które wprowadziły procedurę wykonywania RKO przez określony czas przed defibrylacją, ze względu na brak przekonujących danych potwierdzających bądź negujących jej skuteczność rozsądne wydaje się kontynuowanie tej praktyki. Można rozważyć zastosowanie serii do trzech wyładowań z rzędu, jeśli VF/VT wystąpi podczas cewnikowania serca lub we wczesnym okresie po operacjach kardiochirurgicznych. Strategię potrójnej defibrylacji można również wdrożyć we wczesnej fazie leczenia zauważonego zatrzymania krążenia w mechanizmie VF/VT, jeżeli pacjent jest już podłączony do defibrylatora manualnego. * Corresponding author. charlesdeakin@doctors.org.uk (C.D. Deakin). Pasty lub kleje do defibrylacji mogą się rozlać pomiędzy łyżkami defibrylatora, stwarzając ryzyko powstania łuku elektrycznego i nie powinny być stosowane. Wprowadzenie W rozdziale tym przedstawiono wytyczne dotyczące zastosowania AED oraz defibrylatorów manualnych. W porównaniu z Wytycznymi ERC 2005 wprowadzono niewiele zmian. Zarówno personel medyczny, jak i osoby bez wykształcenia medycznego mogą używać AED jako integralnej części podstawowych zabiegów resuscytacyjnych. Defibrylacja manualna pozostaje elementem leczenia w trakcie zaawansowanych zabiegów resuscytacyjnych (ALS). W niniejszym rozdziale omówiono także zsynchronizowaną kardiowersję i elektrostymulację, opcje dostępne w wielu defibrylatorach. Defibrylacja polega na przejściu przez mięsień sercowy prądu elektrycznego o wystarczającej energii, aby wywołać depolaryzację krytycznej masy mięśnia sercowego i przywrócić skoordynowaną aktywność elektryczną. Defibrylacja jest definiowana jako zakończenie migotania lub dokładniej brak VF/VT w ciągu 5 sekund od wyładowania. Jednakże celem defibrylacji jest przywrócenie zorganizowanego rytmu i spontanicznego krążenia. Technologia defibrylatorów szybko się rozwija. Interakcja pomiędzy AED i ratownikami odbywa się za pośrednictwem poleceń głosowych, a postęp techniczny umożliwi w przyszłości wydawanie bardziej specyficznych instrukcji za ich pomocą. Rosnące możliwości analizy rytmu przez defibrylator w trakcie RKO są ważnym udoskonaleniem i umożliwiają ocenę rytmu bez przerywania uciśnięć klatki piersiowej. W przyszłości analiza kształtu fali przez defibrylator może umożliwić obliczenie optymalnego czasu dostarczenia wyładowania. Najistotniejsze ogniwo łańcucha przeżycia Defibrylacja jest kluczowym ogniwem łańcucha przeżycia i jedną z nielicznych interwencji, dla których udowodniono, że poprawiają wyniki leczenia w zatrzymaniu krążenia w mechanizmie VF/VT. Poprzednie wytyczne, opublikowane w 2005 roku, słusznie podkreślają znaczenie wczesnej defibrylacji, wykonywanej z jak najmniejszym opóźnieniem 1,2.
95 Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja 95 Prawdopodobieństwo skutecznej defibrylacji i w konsekwencji szanse na przeżycie do wypisu ze szpitala zmniejszają się gwałtownie wraz z upływem czasu 3,4. Dlatego możliwość wykonania wczesnej defibrylacji jest jednym z najważniejszych czynników decydujących o przeżyciu w zatrzymaniu krążenia. Z każdą minutą opóźnienia defibrylacji, jeśli świadkowie zdarzenia nie podejmą RKO, szanse przeżycia VF spadają o 10 12% 4,5. Systemy ratownictwa medycznego zwykle nie są w stanie zapewnić wykonania defibrylacji w ciągu pierwszych kilku minut od momentu ich powiadomienia. Dlatego też rozpowszechniono wykonywanie szybkiej defibrylacji za pomocą AED przez przeszkolonych świadków zdarzenia. W przypadku systemów ratownictwa medycznego, które skróciły czas od zatrzymania krążenia do defibrylacji wykonywanej przez przeszkolonych świadków zdarzenia, zanotowano znaczną poprawę wskaźnika przeżycia do wypisu ze szpitala 6 9, w niektórych przypadkach nawet do 75%, jeżeli defibrylację wykonywano w ciągu 3 minut od chwili zatrzymania krążenia 10. Koncepcję tę rozszerzono na wewnątrzszpitalne zatrzymania krążenia, gdzie przeszkolony personel medyczny (inny niż lekarze) wykonuje defibrylację za pomocą AED, zanim przybędzie zespół resuscytacyjny 11. Jeżeli świadkowie zdarzenia podejmą RKO, tempo obniżania szans na przeżycie jest wolniejsze i waha się od 3 do 4% na każdą minutę od chwili utraty przytomności do defibrylacji 3,4,12. RKO wykonywane przez świadków zdarzenia może podwoić 3,4,13 lub potroić 14 szanse przeżycia w przypadku zauważonego, pozaszpitalnego zatrzymania krążenia. Instruktaż wykonywania resuscytacji podawany przez dyspozytora przed przybyciem wyszkolonych ratowników zwiększa zarówno częstość podejmowania, jak i jakość RKO wykonywanego przez świadków zdarzenia 15,16, a dalszą poprawę mogłyby przynieść instrukcje wideo w telefonach komórkowych 17,18. Wszystkie osoby spośród personelu medycznego, które mają obowiązek podjęcia RKO, powinny być szkolone, wyposażone i zachęcane do podejmowania defibrylacji i RKO. Należy zapewnić możliwość wczesnej defibrylacji w szpitalach, placówkach ochrony zdrowia i miejscach publicznych, w których gromadzą się duże liczby osób (zob. rozdział 2) 19. Aby poprawić skuteczność wczesnej defibrylacji, osoby, które uczą się obsługi AED, powinny być również szkolone w wykonywaniu dobrej jakości RKO przed przybyciem zespołów resuscytacyjnych. Automatyczne defibrylatory zewnętrzne AED są wysoce specjalistycznymi, niezawodnymi, skomputeryzowanymi urządzeniami, które za pomocą poleceń głosowych i wizualnych prowadzą zarówno osoby z wykształceniem medycznym, jak i bez niego przez procedurę bezpiecznej defibrylacji w zatrzymaniu krążenia. Niektóre AED posiadają instrukcje wykonywania defibrylacji, a także optymalnego prowadzenia uciśnięć klatki piersiowej. Użycie AED przez świadków zdarzenia lub ratowników niemających wykształcenia medycznego zostało omówione w rozdziale Wielokrotnie zdarza się, że AED użyte do pierwszej defibrylacji jest natychmiast po przybyciu ZRM wymieniane na defibrylator manualny. Jeśli taka zamiana nie uwzględnia cyklu pracy AED, może doprowadzć do opóźnienia wykonania defibrylacji i w efekcie pogorszyć wynik resuscytacji 20. Dlatego ZRM powinien zostawić AED podłączone podczas zabezpieczania drożności dróg oddechowych i wykonywania wkłucia dożylnego. Wymiana AED na defibrylator manualny powinna nastąpić po kolejnej analizie rytmu i defibrylacji, jeśli była wskazana. Aktualnie każdy producent używa specyficznych dla swojego sprzętu łączników elektrod z defibrylatorami, co w przypadku wymiany urządzeń zmusza również do odklejenia elektrod i zastąpienia ich nowymi, kompatybilnymi z używanym defibrylatorem. Zachęca się producentów do współpracy i stworzenia uniwersalnego łącznika, który pasowałby do wszystkich defibrylatorów, co zawocuje znaczącą korzyścią dla pacjenta i ograniczy niepotrzebne wydatki. Zastosowanie AED w szpitalu Do czasu konferencji 2010 Consensus on CPR Science nie opublikowano żadnych randomizowanych badań porównujących wewnątrzszpitalne użycie AED z defibrylatorami manualnymi. Dwa badania niższego stopnia referencyjności oceniające wewnątrzszpitalne nagłe zatrzymania krążenia w rytmach do defibrylacji u osób dorosłych wykazały wyższą przeżywalność do wypisu ze szpitala, gdy używane były AED w porównaniu z wyłącznym użyciem defibrylatorów manualnych 21,22. Jedno badanie retrospektywne 23 wykazało brak poprawy przeżywalności do wypisu ze szpitala w wewnątrzszpitalnym zatrzymaniu krążenia, gdy używane było AED w porównaniu z defibrylacją manualną. W tym badaniu w grupie pacjentów, u których stosowano AED, odnotowano niższą przeżywalność do wypisu ze szpitala, gdy początkowym rytmem była asystolia lub czynność elektryczna bez tętna, w porównaniu z grupą pacjentów, u których stosowano defibrylatory manualne (15% vs. 23%; p = 0,04). Badania na manekinach wykazały, że użycie AED istotnie zwiększyło prawdopodobieństwo wykonania 3 wyładowań, ale wydłużyło czas wykonania procedury w porównaniu z defibrylatorem manualnym 24. Dla porównania, badając zatrzymanie krążenia w warunkach symulowanych okazało się, iż użycie elektrod samoprzylepnych i w pełni zautomatyzowanych defibrylatorów skraca czas do defibrylacji w porównaniu z defibrylatorami klasycznymi 25. Opóźnienie defibrylacji może nastąpić, gdy do NZK dochodzi u niemonitorowanych pacjentów w oddziałach szpitalnych i przychodniach 26. W takich miejscach może upłynąć kilka minut do czasu przybycia zespołu resuscytacyjnego z defibrylatorem i wykonania defibrylacji. Pomimo ograniczonej liczby dowodów naukowych AED powinny być uznane przez szpitale za metodę ułatwiającą wykonanie wczesnej defibrylacji (cel: czas krótszy niż 3 minuty od utraty przytomności), w szczególności w miejscach, gdzie personel nie posiada umiejętności rozpoznawania rytmów lub rzadko używa defibrylatorów. W takich placówkach należy wprowadzić efektywny system szkoleń i ich recertyfikacji oraz przeszkolić odpowiednią liczbę pracowników, aby umożliwić osiągnięcie celu, jakim jest wykonanie pierwszej defibrylacji w ciągu 3 minut od utraty przytomności na terenie całego szpitala 11. Placówki powinny również rejestrować czas upływający od chwili utraty przytomności do pierwszej defibrylacji oraz monitorować odległe wyniki resuscytacji. 3
96 96 Ch.D. Deakin, J.P. Nolan, K. Sunde, R.W. Koster 3 Porównanie defibrylacji manualnej i trybu półautomatycznego Wiele AED posiada zarówno tryb manualny, jak i półautomatyczny, jednak niewiele badań porównało te dwie opcje. Wykazano, że użycie trybu półautomatycznego skraca czas do wykonania pierwszej defibrylacji, zarówno w zastosowaniu wewnątrzszpitalnym 27, jak i pozaszpitalnym 28, zwiększa częstość konwersji VF 28 oraz zmniejsza ilość wyładowań bez wskazań 29. Równocześnie użycie trybu półautomatycznego skraca czas wykonywania uciśnięć klatki piersiowej 29,30, głównie ze względu na dłuższy czas konieczny na automatyczną ocenę rytmu przed defibrylacją. Mimo tych odmienności żadne badanie nie wykazało różnicy w osiągnięciu powrotu spontanicznego krążenia (ROSC), przeżywalności czy częstości wypisów ze szpitala 23,27,28. Właściwy tryb defibrylacji, który zapewniałby najlepszy odległy wynik resuscytacji, będzie zależeć od organizacji systemu, umiejętności, wyszkolenia oraz zdolności rozpoznawania rytmów przez ratowników. Krótsza przerwa przeddefibrylacyjna, jak i krótszy całkowity czas bez uciśnięć klatki piersiowej zwiększa perfuzję życiowo ważnych narządów oraz prawdopodobieństwo osiągnięcia ROSC Używając defibrylatorów manualnych (głównie z elektrodami samoprzylepnymi), jak i niektórych AED, możliwe jest wykonywanie uciśnięć klatki piersiowej podczas ładowania urządzenia, co skraca czas przerwy przeddefibrylacyjnej poniżej 5 sekund. Wyszkoleni ratownicy mogą wykonywać defibrylację w trybie manualnym, wymaga to jednak częstego szkolenia zespołowego, jak i umiejętności rozpoznawania EKG. Automatyczna analiza rytmu AED posiada mikroprocesory analizujące różne cechy EKG, włączając w to częstotliwość i amplitudę. Rozwijająca się technologia powinna wkrótce umożliwić AED dostarczanie informacji na temat częstotliwości i głębokości uciskania klatki piersiowej w trakcie RKO, co pozwoli na poprawę jakości wykonywania BLS przez wszystkich ratowników 34,35. Automatyczne defibrylatory zewnętrzne zostały gruntownie sprawdzone w zakresie prawidłowości rozpoznawania rytmów serca na podstawie zapisanych w ich pamięci danych w wielu badaniach u dorosłych 36,37 i dzieci 38,39. Zapewniają one bardzo dokładną analizę rytmu. AED nie są przeznaczone do wykonywania zsynchronizowanych wyładowań, zalecają natomiast wykonywanie defibrylacji w VT, jeżeli częstość, morfologia i czas trwania załamka R przekraczają zaprogramowane wartości. Większość AED wymaga przerwania uciśnięć klatki piersiowej (hands-off period) w czasie analizy rytmu. Choć długość tej pauzy może być różna, to jednak w znaczący sposób przerywa uciśnięcia klatki piersiowej 40 i jest istotnym czynnikiem wpływającym niekorzystnie na wynik odległy resuscytacji 41. Producenci powinni zrobić wszystko, co w ich mocy, by w urządzeniach maksymalnie skrócić czas analizy, co zapewni minimalizację przerw w uciskaniu klatki piersiowej. Postępowanie przed defibrylacją Skracanie przerwy przeddefibrylacyjnej Czas pomiędzy przerwaniem uciśnięć klatki piersiowej a wykonaniem defibrylacji (przerwa przeddefibrylacyjna) musi być absolutnie skrócony do minimum; nawet 5 10 sekundowa przerwa zmniejsza szanse na skuteczność defibrylacji 31,32,42. Przerwa przeddefibrylacyjna może być z łatwością skrócona poniżej 5 sekund poprzez kontynuację uciśnięć w trakcie ładowania defibrylatora oraz pod warunkiem wydajnej pracy zespołu pod kierownictwem efektywnie komunikującego się lidera. Ocena bezpieczeństwa, tak by nikt nie dotykał poszkodowanego podczas defibrylacji, powinna być wykonana szybko i skutecznie. Ryzyko przypadkowego porażenia jest również zminimalizowane, jeśli wszyscy ratownicy mają ubrane rękawiczki 43. Przerwa po defibrylacji powinna być zminimalizowana przez jak najszybsze podjęcie uciśnięć klatki piersiowej po defibrylacji (patrz poniżej). Procedura defibrylacji powinna być wykonana tak, aby przerwa w uciskaniu klatki piersiowej wyniosła nie więcej niż 5 sekund. Bezpieczne użycie tlenu podczas defibrylacji W atmosferze wzbogaconej tlenem iskrzenie wskutek niedokładnego przyłożenia łyżek może stać się przyczyną zapłonu Istnieją doniesienia o pożarach wywołanych w ten właśnie sposób, a większość z nich skończyła się poważnym oparzeniem pacjenta. Nie ma udokumentowanych przypadków wywołania pożaru przez iskrzenie, gdy używano elektrod samoprzylepnych. W dwóch badaniach przeprowadzonych na manekinach stwierdzono, że w strefie defibrylacji stężenie tlenu nie wzrasta, jeśli urządzenia do wentylacji (worek samorozprężalny, worek oddechowy, respirator) są podłączone do rurki intubacyjnej bądź źródło tlenu zostało odsunięte na co najmniej 1 m poza usta pacjenta 50,51. Jedno badanie opisuje, że gdy tlen jest dostarczany w przestrzeniach zamkniętych bez właściwego przewietrzania, stężenie tlenu wzrasta, a czas jego usuwania z otoczenia wydłuża się 52. Ryzyko zapłonu w trakcie defibrylacji może być zminimalizowane przez zachowanie następujących środków ostrożności: Zdejmij pacjentowi maskę tlenową lub wąsy tlenowe i odsuń je na odległość co najmniej 1 metra od jego klatki piersiowej. Pozostaw worek samorozprężalny, jeśli jest podłączony do rurki intubacyjnej lub innych nadgłośniowych przyrządów służących do udrażniania dróg oddechowych. Alternatywnie rozłącz worek samorozprężalny od rurki intubacyjnej lub innych nadgłośniowych przyrządów służących do udrażniania dróg oddechowych i odsuń na odległość co najmniej 1 metra od klatki piersiowej pacjenta w trakcie wykonywania defibrylacji. Jeżeli pacjent jest podłączony do respiratora, na przykład na sali operacyjnej lub na oddziale intensywnej terapii, pozostaw zamknięty układ oddechowy respiratora podłączony do rurki intubacyjnej, o ile uciskanie klatki piersiowej nie przeszkadza w dostarczaniu odpowiedniej objętości oddechowej. Gdyby tak się działo, zastąp pracę respiratora wentylacją za pomocą worka samorozprężalnego, który można pozostawić połączony z układem lub rozłączyć i odsunąć na odległość co najmniej 1 metra. Jeśli rury respiratora są odłączone, upewnij się, że znajdują się co najmniej 1 metr od pacjenta lub, co bezpieczniej-
97 Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja 97 sze, wyłącz respirator. Nowoczesne respiratory po rozszczelnieniu układu generują masywny strumień tlenu. W czasie normalnego użytkowania na oddziale intensywnej terapii, kiedy respirator jest podłączony do rurki intubacyjnej, tlen z respiratora jest wydalany przez główny zawór z dala od strefy defibrylacji. Pacjenci na oddziałach intensywnej terapii mogą być zależni od wentylacji dodatnim ciśnieniem końcowowydechowym (Positive End Expiratory Pressure PEEP), która pozwala utrzymać odpowiedni poziom utlenowania. Podczas kardiowersji, gdy spontaniczne krążenie potencjalnie umożliwia utrzymanie utlenowania krwi, właściwe jest, aby podczas dostarczania wyładowania pacjent w stanie krytycznym pozostawał podłączony do respiratora. Minimalizuj ryzyko iskrzenia w trakcie defibrylacji. Mniej prawdopodobne jest powstanie iskry przy użyciu elektrod samoprzylepnych, niż kiedy używa się tradycyjnych łyżek. Niektóre wczesne wersje urządzenia do uciskania klatki piersiowej LUCAS są napędzane tlenem i podczas pracy wyrzucają nadmiar gazu ponad klatkę piersiową pacjenta. Zostało stwierdzone, że używając tego typu urządzeń, powstaje wysokie stężenie tlenu nad klatką piersiową pacjenta, szczególnie w zamkniętych przestrzeniach, jak tylny przedział karetki. Dlatego podczas defibrylacji należy szczególnie uważać, gdy używany jest model napędzany tlenem 52. Technika umieszczania łyżek i elektrod na klatce piersiowej Optymalna technika defibrylacji ma na celu dostarczenie prądu do mięśnia sercowego objętego migotaniem, pokonując minimalny opór klatki piersiowej. Opór przezklatkowy znacząco waha się w zależności od masy ciała pacjenta i wynosi około Ω u dorosłych 53,54. Techniki opisane poniżej mają zapewnić umieszczenie zewnętrznych elektrod (klasycznych lub samoprzylepnych) w optymalnej pozycji, która umożliwi minimalizację oporu przezklatkowego. Usuwanie owłosienia z klatki piersiowej U pacjentów z owłosioną klatką piersiową pod elektrodą zostaje uwięziona warstwa powietrza, która powoduje niedostateczny kontakt elektrody ze skórą. Zwiększa to opór, zmniejsza skuteczność defibrylacji, stwarza ryzyko powstania łuku elektrycznego (iskrzenia) pomiędzy elektrodą a skórą i pomiędzy elektrodami oraz zwiększa prawdopodobieństwo oparzenia klatki piersiowej pacjenta. Konieczne może być szybkie ogolenie miejsca przyłożenia elektrod, ale nie powinno się opóźniać defibrylacji, jeżeli golarka nie jest natychmiast dostępna. Golenie klatki piersiowej zmniejsza nieznacznie opór przezklatkowy i zaleca się je przy wykonywaniu planowej kardiowersji defibrylatorem jednofazowym 55. Natomiast efektywność fali dwufazowej z kompensacją oporu może nie być wrażliwa na zwiększony opór elektryczny klatki piersiowej 56. Siła przyłożenia łyżek Jeśli używa się łyżek, należy je mocno przycisnąć do ściany klatki piersiowej. Zmniejsza to opór, przez zapewnienie lepszego kontaktu elektrody ze skórą, i zmniejsza objętość klatki piersiowej 57. Osoba obsługująca defibrylator powinna zawsze mocno naciskać na łyżki, optymalnie siłą 8 kg u osób dorosłych i 5 kg u dzieci w wieku 1 8 lat, o ile defibrylacja jest wykonywana przy użyciu łyżek dla dorosłych 58. Siłę 8 kg mogą wygenerować wyłącznie najsilniejsi członkowie zespołu resuscytacyjnego, dlatego zaleca się, aby właśnie oni obsługiwali defibrylator w czasie resuscytacji. W przeciwieństwie do elektrod samoprzylepnych, powierzchnię klasycznych łyżek stanowi warstwa metalu i z tego powodu, w celu poprawienia przewodnictwa elektrycznego, wskazane jest umieszczenie pomiędzy metalem a skórą pacjenta materiału przewodzącego. Używanie metalowych łyżek bez materiału przewodzącego zwiększa znacznie opór klatki piersiowej, podnosząc ryzyko powstania łuku elektrycznego i pogłębienia oparzeń skóry na skutek defibrylacji. Ułożenie elektrod Nie prowadzono dotychczas badań klinicznych, oceniających ułożenie elektrod jako czynnika wpływającego na ROSC lub przeżycie w zatrzymaniu krążenia w mechanizmie VF/VT. Przepływ prądu przez mięsień sercowy w trakcie wyładowania będzie największy, jeśli pomiędzy elektrodami znajdzie się okolica serca objęta migotaniem, np. komory w przypadku VF/VT, a przedsionki w przypadku migotania przedsionków (Atrial Fibrillation AF). Dlatego optymalne ułożenie elektrod może nie być takie samo w przypadku leczenia arytmii komorowych i arytmii przedsionkowych. Coraz więcej pacjentów posiada wszczepialne rozruszniki serca lub kardiowertery-defibrylatory (Implantable Cardioverter Defibrillator ICD). Takim pacjentom zaleca się noszenie bransoletek informacyjnych, gdyż wszczepione urządzenia mogą ulec uszkodzeniu w trakcie defibrylacji, jeśli pomiędzy elektrodami umieszczonymi dokładnie nad nimi przebiegnie impuls elektryczny 59,60. Dlatego należy umieścić łyżki defibrylatora w odległości od urządzenia (co najmniej 8 cm) 59 bądź zastosować alternatywne ułożenie elektrod (przednio-boczne, przednio-tylne), jak opisano poniżej. Plastry zawierające leki mogą utrudniać dobry kontakt elektrod defibrylatora ze skórą, powodując powstanie łuku elektrycznego lub oparzeń, jeśli elektrody w trakcie defibrylacji są przyłożone dokładnie nad plastrem 61,62. Należy usunąć plastry z lekami i przetrzeć powierzchnię skóry, zanim przyłoży się elektrody. Ułożenie elektrod podczas zatrzymania krążenia i w arytmiach komorowych Elektrody (zarówno klasyczne, jak i samoprzylepne) należy umieścić w miejscu typowym pozycja mostkowo-koniuszkowa. Prawą elektrodę (mostkową) należy umieścić po prawej stronie mostka, poniżej obojczyka, a koniuszkową w linii środkowopachowej, w przybliżeniu na wysokości odprowadzenia V6 EKG lub kobiecej piersi, ale nie nad tkanką gruczołu piersiowego. Ważne jest, aby ta elektroda była ułożona wystarczająco bocznie. Inne akceptowane ułożenia łyżek obejmują: Obie elektrody na bocznych ścianach klatki piersiowej, po prawej i lewej stronie (bi-axillary). 3
98 98 Ch.D. Deakin, J.P. Nolan, K. Sunde, R.W. Koster 3 Jedna elektroda w standardowej koniuszkowej pozycji, a druga w górnej części pleców po prawej stronie. Jedna elektroda z przodu nad lewą okolicą przedsercową, druga elektroda z tyłu w stosunku do serca, tuż poniżej lewej łopatki. Nie ma znaczenia która elektroda (koniuszek mostek) znajdzie się w której pozycji. Wykazano zmniejszenie oporu klatki piersiowej, jeżeli elektroda koniuszkowa nie jest układana na piersi u kobiet 63. Asymetrycznie ukształtowana elektroda koniuszkowa ma mniejszy opór, kiedy ułożona jest podłużnie, a nie poprzecznie 64. Ułożenie elektrod w arytmiach przedsionkowych Migotanie przedsionków podtrzymywane jest poprzez mechanizm pętli re-entry zakotwiczonej w lewym przedsionku. Ponieważ lewy przedsionek jest położony z tyłu klatki piersiowej, ułożenie elektrod powodujące przepływ prądu ku tyłowi może być teoretycznie skuteczniejsze w arytmiach przedsionkowych. Mimo że niektóre badania wykazały większą skuteczność przednio-tylnego ułożenia elektrod w porównaniu z typowym przednio-koniuszkowym w kardiowersji migotania przedsionków 65,66, większość badań nie wykazała jakiejkolwiek przewagi żadnego specyficznego ułożenia elektrod 67,68. Stosując energię dwufazową z kompensacją oporu, skuteczność kardiowersji w mniejszym stopniu zależy od sposobu ułożenia elektrod 56. Wszystkie poniższe ułożenia elektrod wydają się bezpieczne i skuteczne przy kardiowersji przedsionkowych zaburzeń rytmu: Pozycja typowa przednio-koniuszkowa Pozycja przednio-tylna (jedna elektroda z przodu w lewej okolicy przedsercowej, druga elektroda z tyłu w stosunku do serca, tuż poniżej lewej łopatki). Faza oddechowa Opór klatki piersiowej zmienia się w trakcie oddychania i osiąga najmniejsze wartości na końcu wydechu. Jeśli to możliwe, defibrylacja powinna być wykonana w tej fazie oddychania. Dodatnie ciśnienie końcowowydechowe (PEEP) zwiększa opór i powinno być zminimalizowane w trakcie defibrylacji. Auto-PEEP (pułapka powietrzna) bywa szczególnie wysoki w astmie, co może powodować konieczność użycia większych niż zwykle energii defibrylacji 69. Rozmiar elektrod Association for the Advancement of Medical Instrumentation wydaje rekomendacje dotyczące minimalnego rozmiaru poszczególnych elektrod i zaleca, aby suma ich powierzchni nie była mniejsza niż 150 cm Większe elektrody mają mniejszy opór, ale nadmiernie duże elektrody mogą prowadzić do zmniejszenia przepływu prądu przez mięsień sercowy 71. Do defibrylacji u dorosłych używa się z dobrym skutkiem tak elektrod klasycznych, jak i samoprzylepnych o średnicy 8 12 cm. Skuteczność defibrylacji może być większa w przypadku elektrod o średnicy 12 cm niż tych o rozmiarze 8 cm 54,72. Standardowy AED może być stosowany u dzieci powyżej 8. roku życia. U dzieci pomiędzy 1. i 8. rokiem życia należy używać elektrod pediatrycznych, z urządzeniem redukującym dostarczaną energię lub wykorzystywać tryb pediatryczny, o ile jest dostępny. Jeżeli nie ma takiej możliwości, stosuje się urządzenie niezmodyfikowane, dbając, aby duże elektrody nie zachodziły na siebie. Nie zaleca się użycia AED w przypadku dzieci poniżej 1. roku życia. Materiał przewodzący W przypadku stosowania elektrod klasycznych należy używać jednorazowych podkładek żelowych, by zmniejszyć opór na granicy elektroda skóra. Pasty i żele do defibrylacji mogą się rozlać pomiędzy elektrodami, wywołując potencjalne ryzyko iskrzenia i dlatego nie powinny być używane. Nie należy jednak używać łyżek bez podkładek żelowych, ponieważ zwiększony w ten sposób opór elektryczny klatki piersiowej zmniejsza skuteczność defibrylacji i zwiększa ciężkość oparzeń skóry oraz ryzyko powstania łuku elektrycznego, co może doprowadzić do pożaru lub wybuchu. Porównanie elektrod samoprzylepnych i klasycznych łyżek Używanie elektrod samoprzylepnych do rutynowego monitorowania oraz defibrylacji jest w praktyce korzystniejsze w porównaniu z łyżkami klasycznymi Ponieważ są one bezpieczne i efektywne, preferuje się ich użycie zamiast klasycznych łyżek do defibrylacji 72. Szczególną uwagę powinno się zwrócić na stosowanie elektrod samoprzylepnych w sytuacjach, kiedy ryzyko zatrzymania krążenia jest wysokie oraz kiedy dostęp do pacjenta jest utrudniony. Mają one podobny do klasycznych łyżek opór 71 (a co za tym idzie skuteczność) 78,79 i umożliwiają osobie przeprowadzającej defibrylację wykonanie wyładowania z zachowaniem bezpiecznej odległości od pacjenta, bez potrzeby pochylania się nad nim (co ma miejsce w wypadku łyżek). W porównaniu ze standardowymi elektrodami EKG zarówno elektrody samoprzylepne, jaki i łyżki zapewniają szybsze wykonanie pierwszego wyładowania, jeśli używa się ich do wstępnego monitorowania rytmu. Porównując z łyżkami, elektrody samoprzylepne są szybsze 80. Kiedy używane są podkładki żelowe pod łyżki, zawarty w nich żel elektrolitowy zostaje spolaryzowany w trakcie defibrylacji, co powoduje, że po defibrylacji pogarsza się jego przewodnictwo. Jeśli używa się ich do monitorowania rytmu, można obserwować rzekomą asystolię, trwającą około 3 4 minuty; zjawiska tego nie obserwuje się, gdy używa się elektrod samoprzylepnych 74,81. Gdy wykorzystuje się łyżki z podkładkami żelowymi, diagnozę asystolii należy potwierdzać, używając raczej niezależnych elektrod EKG, aniżeli łyżek. Analiza kształtu fali migotania Możliwe jest, z różną wiarygodnością, przewidywanie skuteczności defibrylacji na podstawie analizy kształtu fali migotania Jeśli w badaniach prospektywnych uda się ustalić optymalny do wykonania defibrylacji kształt fali migotania i moment wykonania wyładowania, możliwe stanie się zapobieganie nieskutecznym wyładowaniom wysoką energią, a tym samym zminimalizowanie uszkodzenia miokardium. Ta technologia jest ciągle badana, lecz jej dotychczasowa czułość i swoistość są niewystarczające, by wprowadzić analizę fali VF do praktyki klinicznej.
99 Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja 99 Wstępne postępowanie: RKO czy defibrylacja? Przeprowadzono kilka badań, których celem było stwierdzenie, czy RKO wykonywane przed defibrylacją przynosi skutki pozytywne, zwłaszcza u pacjentów, u których doszło do niezauważonego zatrzymania krążenia, bądź u pacjentów z wydłużonym czasem od utraty przytomności do rozpoczęcia resuscytacji. Analiza dostępnych danych naukowych podjęta w celu stworzenia Wytycznych 2005 określała, iż u pacjentów z przedłużonym okresem od utraty przytomności (>5 minut) rozsądnym jest podjęcie przez ZRM 2 minut RKO (np. około 5 cykli 30 : 2) przed defibrylacją 1. Te wytyczne oparto na badaniach klinicznych, które wykazały, że u pacjentów dorosłych z pozaszpitalnym zatrzymaniem krążenia w mechanizmie VF lub VT, u których czas do rozpoczęcia resuscytacji przekraczał 4 5 minut, okres 1,5 3 minut RKO prowadzonej przez ratowników lub lekarzy przed wykonaniem defibrylacji zwiększał, w porównaniu z natychmiastową defibrylacją, częstość ROSC, przeżywalność do wypisu ze szpitala 102,103, a także przeżywalność jednoroczną 103. W niektórych badaniach na zwierzętach stwierdzono, iż RKO przed defibrylacją poprawia hemodynamikę i przeżywalność , jeśli VF trwało co najmniej 5 minut. Ostatnio opublikowana praca doświadczalna oparta na świńskim modelu niedokrwienia prowadzącego do zatrzymania krążenia wykazała spadek przeżywalności, gdy przed defibrylacją prowadzono RKO 107. Z drugiej strony dwa kontrolowane, randomizowane badania wykazały brak poprawy ROSC czy przeżywalności do wypisu ze szpitala u pacjentów po pozaszpitalnym zatrzymaniu krążenia w mechanizmie VF i VT, gdy ZRM wykonywał 1,5 3 minut RKO przed defibrylacją, bez względu na czas dotarcia do poszkodowanego 108,109. Cztery inne badania również nie wykazały znaczącej poprawy ROSC lub przeżywalności do wypisu ze szpitala przy rozpoczynaniu resuscytacji od uciskania klatki piersiowej i wentylacji 102,103,110,111, aczkolwiek jedno z nich wykazało lepszy wynik neurologiczny w 30. dniu, jak i rok po zatrzymaniu krążenia 110. Dokładny czas trwania utraty przytomności jest często trudny do określenia, istnieją jednak dowody, że wykonywanie dobrej jakości uciśnięć klatki piersiowej w trakcie podłączania i ładowania defibrylatora zwiększa prawdopodobieństwo przeżycia 112. Dlatego w każdym przypadku niezauważonego zatrzymania krążenia ZRM powinien prowadzić dobrej jakości uciśnięcia klatki piersiowej podczas dostarczania, podłączania i ładowania defibrylatora, jednak niezalecany jest jakikolwiek rutynowy czas wykonywania RKO przed analizą rytmu i defibrylacją (np. 2 czy 3 minuty). Niektóre zespoły ratownictwa medycznego wypracowały standardową procedurę prowadzenia uciśnięć klatki piersiowej przez ustalony czas przed wykonaniem defibrylacji; ze względu na brak przekonujących danych potwierdzających bądź negujących tę strategię, zasadne wydaje się kontynuowanie tej praktyki. W szpitalach, w których dostępne są AED (również dla ratowników bez wykształcenia medycznego), oraz w sytuacjach, kiedy do zatrzymania krążenia doszło w obecności ZRM, należy wykonać defibrylację najszybciej, jak tylko defibrylator będzie dostępny. Uciśnięcia klatki piersiowej powinny być wykonywane do momentu poprzedzającego wyładowanie (zob. rozdział 4. Zaawansowane zabiegi resuscytacyjne u osób dorosłych) 113. Aktualne wytyczne kładą ogromny nacisk na jak najszybsze podjęcie i nieprzerwane wykonywanie uciśnięć klatki piersiowej w NZK. W praktyce bardzo trudno określić, kiedy dokładnie doszło do utraty przytomności i dlatego w każdym przypadku resuscytację należy rozpoczynać najszybciej, jak to tylko możliwe. Ratownik wykonujący uciśnięcia klatki piersiowej powinien przerywać je wyłącznie na wykonanie wentylacji, analizę rytmu serca i wyładowanie, a uciśnięcia powinny być podjęte ponownie, gdy tylko wyładowanie zostanie wykonane. Gdy jest obecnych dwóch ratowników, osoba obsługująca AED powinna go podłączać w trakcie prowadzenia RKO przez drugą osobę. RKO można przerwać wyłącznie wtedy, kiedy jest to konieczne do oceny rytmu i dostarczenia wyładowania. Ratownik obsługujący AED powinien być przygotowany do jak najszybszego wykonania defibrylacji, gdy tylko analiza rytmu zostanie zakończona, upewniając się jednocześnie, że żaden ratownik nie dotyka poszkodowanego. Wykonanie defibrylacji Porównanie pojedynczej defibrylacji z sekwencją trzech defibrylacji Główną zmianą w Wytycznych 2005 było zalecenie pojedynczego wyładowania zamiast trzech następujących po sobie wyładowań. Było tak, ponieważ badania na zwierzętach wykazały związek stosunkowo niewielkich przerw w uciskaniu klatki piersiowej (w celu wykonania oddechów ratowniczych 114,115 lub analizy rytmu 33 ) z dysfunkcją mięśnia sercowego po resuscytacji oraz spadkiem przeżycia. Przerwy w prowadzeniu uciśnięć klatki piersiowej zmniejszają również szanse na konwersję migotania komór w inny rytm 32. Analiza RKO wykonywanej w czasie pozaszpitalnego 34,116 oraz wewnątrzszpitalnego 35 zatrzymania krążenia wykazała, że znaczące przerwy w uciskaniu klatki piersiowej są powszechne i w efekcie uciśnięcia klatki piersiowej stanowią nie więcej niż do 76% 35 całkowitego czasu RKO. Biorąc pod uwagę skuteczność pierwszego wyładowania energii dwufazowej, przekraczającą 90% , brak powodzenia w konwersji migotania komór sugeruje potrzebę raczej prowadzenia RKO przez pewien okres niż kolejnego wyładowania. Nawet jeśli defibrylacja jest skuteczna w przywróceniu rytmu, który może dać tętno, bardzo rzadko jest ono wyczuwalne zaraz po defibrylacji, a czas stracony na próby jego znalezienia stanowi kolejne zagrożenie dla mięśnia sercowego, jeśli nie został przywrócony rytm z perfuzją 40. Przeprowadzone badania wykazały, że całkowity czas bez wykonywania uciśnięć klatki piersiowej jest znacznie krótszy przy stosowaniu pojedynczych wyładowań 121, a niektóre 41,122,123, jednak nie wszystkie 121,124, sugerują znaczną poprawę przeżywalności przy stosowaniu strategii pojedynczego wyładowania. Niestety, wszystkie badania z wyjątkiem jednego 134 były oparte na ograniczonych i wielokrotnie zmienianych protokołach, co spowodowało trudności w przypisaniu obserwowanych wyników do przeżywalności. Gdy defibrylacja jest wskazana, należy wykonać pojedynczą defibrylację i jak najszybciej podjąć uciśnięcia klatki 3
100 100 Ch.D. Deakin, J.P. Nolan, K. Sunde, R.W. Koster 3 Ryc Fala jednofazowa o kształcie tłumionej sinusoidy (Monophasic Damped Sinusoidal MDS) Ryc Fala dwufazowa rektalinearna (Rectilinear Biphasic RLB) piersiowej. Nie powinno się opóźniać rozpoczęcia RKO, poświęcając czas na ocenę rytmu czy sprawdzanie tętna bezpośrednio po defibrylacji. Należy kontynuować RKO (30 uciśnięć : 2 wdechy) przez 2 minuty aż do kolejnej analizy rytmu i wykonania kolejnej defibrylacji (jeśli wskazana) (zob. rozdział 4. Zaawansowane zabiegi resuscytacyjne u osób dorosłych) 113. Ta strategia wykonywania pojedynczych defibrylacji dotyczy zarówno defibrylatorów jedno-, jak i dwufazowych. Należy rozważyć wykonanie do trzech wyładowań z rzędu przed rozpoczęciem uciśnięć klatki piersiowej, jeśli VF/VT wystąpi podczas cewnikowania serca lub we wczesnym okresie pooperacyjnym w zabiegach kardiochirurgicznych (gdy uciśnięcia klatki piersiowej mogłyby uszkodzić szwy naczyniowe) (zob. rozdział 8. dot. sytuacji szczególnych) 125. Ta strategia potrójnej defibrylacji może być również rozważona przy zauważonym zatrzymaniu krążenia w VF/ VT u pacjentów podłączonych już do defibrylatora manualnego. Mimo że nie ma danych potwierdzających skuteczność tej strategii w wymienionych sytuacjach, mało prawdopodobne jest, by uciśnięcia klatki piersiowej poprawiły i tak bardzo wysoką szansę na powrót spontanicznego krążenia, gdy wykonuje się defibrylację w fazie elektrycznej, natychmiast po pojawieniu się VF. Ryc Fala dwufazowa ścięta wykładniczo (Biphasic Truncated Exponential BTE) Kształty fal energii defibrylacji Defibrylatory dostarczające impuls jednofazowy były standardem postępowania do lat dziewięćdziesiątych. Defibrylatory jednofazowe dostarczają prąd jednobiegunowy (czyli płynący w jednym kierunku) (ryc. 3.1). Defibrylatory jednofazowe były szczególnie wrażliwe na zmiany kształtu fali energii zależne od oporu elektrycznego klatki piersiowej. Pacjenci drobnej budowy ciała, z minimalnym oporem klatki piersiowej otrzymywali relatywnie większą dawkę energii przepływającej przez mięsień sercowy niż więksi pacjenci, u których nie dość, że dawka energii była mniejsza, to jeszcze wydłużała się długość fali, co obniżało jej skuteczność. Defibrylatory jednofazowe zostały już wycofane z produkcji i pomimo że wiele z nich pozostanie w użytku przez kilka lat, są zastępowane przez defibrylatory dwufazowe. Defibrylatory dwufazowe dostarczają impuls prądu, który płynie w kierunku wartości dodatnich przez określony czas, by następnie odwrócić się i płynąć w kierunku wartości ujemnych w czasie pozostałych milisekund wyładowania. Istnieją dwa główne typy fali dwufazowej: fala dwufazowa ścięta wykładniczo (Biphasic Truncated Exponential BTE) (ryc. 3.2) oraz fala dwufazowa rektalinearna (Rectilinear Biphasic RLB) (ryc. 3.3). Defibrylatory dwufazowe kompensują w szerokim zakresie opór klatki piersiowej poprzez elektroniczne dostosowywanie wielkości i czasu trwania impulsu elektrycznego, by zapewnić dostarczenie optymalnego prądu do mięśnia sercowego, niezależnie od budowy ciała pacjenta. Ostatnio opisano falę dwufazową o pulsującym kształcie, gdzie prąd szybko oscyluje pomiędzy wartością zero a wartościami dodatnimi, by następnie odwrócić się w kierunku wartości ujemnych. Ten kształt fali jest również używany w praktyce klinicznej. Skuteczność tej fali może być podobna do pozostałych fal dwufazowych, jednak żadne badanie kliniczne nad tą falą nie zostało przeprowadzone z użyciem urządzeń kompensujących opór klatki piersiowej 126,127. Występuje również kilka innych kształtów fal dwufazowych, nie wykazano jednak żadnych dowodów klinicznych wyższości jednego kształtu fali nad innymi. Wszystkie defibrylatory manualne oraz AED, które umożliwiają ręczny wybór energii, powinny posiadać odpowiednie oznaczenia informujące o rodzaju i kształcie fali prądu (jednofazowy/dwufazowy) oraz o zalecanych energiach defibrylacji w przypadku VF/VT.
101 Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja 101 Porównanie defibrylacji jednofazowej i dwufazowej Fale dwufazowe efektywniej leczą komorowe zaburzenia rytmu przy niższych wartościach energii, wykazują większą skuteczność pierwszego wyładowania w porównaniu z falą jednofazową oraz większą skuteczność pierwszej defibrylacji dla długotrwającego VF/VT Jednak żadne randomizowane badanie nie wykazało przewagi którejkolwiek z fal, kiedy oceniano stopień ubytków neurologicznych przy wypisie ze szpitala. Niektóre badania 119, , choć nie wszystkie 134, sugerują poprawę krótkoterminowych wyników po zatrzymaniu krążenia w mechanizmie VF w porównaniu z defibrylacją jednofazową. Fale dwufazowe mają przewagę nad falami jednofazowymi podczas planowej kardiowersji migotania przedsionków, wykazują większą ogólną skuteczność przy użyciu niższej energii, zmniejszając przez to ciężkość oparzeń skóry , dlatego są falą z wyboru dla tej procedury. Porównanie defibrylacji dwufazowej i wielofazowej Testowane na zwierzętach są również różne fale wielofazowe (trójfazowe, czterofazowe, wielofazowe). Dane z tych badań sugerują, że używając fal wielofazowych można zastosować niższą energię, co pozwala zmniejszyć podefibrylacyjne uszkodzenie mięśnia sercowego Dane te są ograniczone ze względu na krótki czas trwania VF w przeprowadzonych badaniach (ok. 30 sekund) oraz brak badań potwierdzających skuteczność tej techniki w warunkach klinicznych. Na dzień dzisiejszy brak jest badań na ludziach porównujących fale wielofazowe z dwufazowymi zastosowanymi do defibrylacji oraz żaden z dostępnych defibrylatorów nie wykorzystuje fal wielofazowych. Poziomy energii Defibrylacja wymaga dostarczenia wystarczającej energii elektrycznej przez krytyczną masę mięśnia sercowego, aby przerwać migotanie komór i umożliwić przywrócenie spontanicznej, zsynchronizowanej czynności elektrycznej serca w formie zorganizowanego rytmu. Optymalna energia defibrylacji to taka, która spowoduje defibrylację, jednocześnie wywołując najmniejsze możliwe uszkodzenie mięśnia sercowego 142. Wybór właściwego poziomu energii zmniejszy również ilość koniecznych wyładowań, co ograniczy uszkodzenie mięśnia sercowego 143. Nie są znane optymalne wartości energii zarówno defibrylacji jednofazowej, jak i dwufazowej. Zalecenia określające wartości energii są oparte na podstawie konsensusu wynikającego z dokładnego przeglądu aktualnego piśmiennictwa. Poziomy energii dla defibrylacji są wybierane, ale w rzeczywistości jedynie prąd przepływający przez mięsień sercowy odpowiada za jej skuteczność. Ten prąd koreluje z efektywną defibrylacją i kardiowersją 144. Optymalny prąd defibrylacji przy zastosowaniu fali jednofazowej mieści się w przedziale amperów. Z pośrednich dowodów naukowych, uzyskanych na podstawie pomiarów wykonywanych podczas kardiowersji migotania przedsionków wynika, że prąd defibrylacji przy zastosowaniu fali dwufazowej mieści się w przedziale amperów 137. Rozwój technologii może spowodować, że defibrylatory będą w stanie dostarczyć wyładowanie z uzyskaniem odpowiedniego natężenia prądu przepływającego przez klatkę piersiową jest to strategia, która potencjalnie prowadzi do zwiększenia skuteczności defibrylacji. W celu ustalenia optymalnych wartości tego prądu należy przeprowadzić badania nad jego maksymalną amplitudą natężenia, średnim natężeniem i czasem trwania fazy, jak również zachęcać producentów do prowadzenia działań umożliwiających zamianę defibrylacji opartej na wartości energii na defibrylację opartą na wartości natężenia prądu. Pierwsza defibrylacja Defibrylatory jednofazowe Od czasu Wytycznych 2005 nie opublikowano nowych badań nad optymalnym poziomem energii dla fal jednofazowych. Skuteczność pierwszej defibrylacji przy zastosowaniu fali jednofazowej w sytuacji, gdy od utraty przytomności do rozpoczęcia resuscytacji upływa dużo czasu, określa się jako 54 63% dla 200 J fali jednofazowej ściętej wykładniczo (MTE) 129,145 oraz 77 91% przy użyciu 200 J fali jednofazowej o kształcie tłumionej sinusoidy (MDS) ,145. Z powodu mniejszej skuteczności tego rodzaju fali zalecana energia pierwszego wyładowania, przy użyciu defibrylatora jednofazowego wynosi 360 J. Pomimo że wyższe wartości energii niosą ze sobą większe ryzyko uszkodzenia mięśnia sercowego, najważniejsza jest korzyść wynikająca z wczesnego przywrócenia rytmu perfuzyjnego. Blok przedsionkowo-komorowy występuje częściej po zastosowaniu wysokich wartości energii jednofazowej, lecz jest zazwyczaj przejściowy i wykazano, że nie wpływa na przeżycie do wypisu ze szpitala 146. Tylko jedno z 27 badań na zwierzętach wykazało niekorzystny wpływ defibrylacji wysokimi energiami 147. Defibrylatory dwufazowe Stosunkowo mało badań zostało opublikowanych przez ostatnie pięć lat, by możliwe stało się udoskonalenie Wytycznych 2005 w tym zakresie. Nie ma dowodów naukowych na potwierdzenie tezy, iż jeden rodzaj dwufazowej fali lub defibrylatora jest skuteczniejszy niż inny. Wykazano skuteczność pierwszego wyładowania o kształcie fali BTE i o energii J na poziomie 86 98% 128,129,145,148,149. Skuteczność pierwszego wyładowania impulsem o kształcie fali RLB i energii 120 J wynosi do 85% (dane nieopublikowane, pochodzące z przekazu ustnego) 130. Skuteczność pierwszego wyładowania dla nowej pulsującej fali dwufazowej przy 130 J wynosi 90% 126. Dwa badania sugerują równorzędność niższej i wyższej dwufazowej energii początkowej defibrylacji 150,151. Mimo że badania na ludziach nie wykazały uszkodzeń (podwyższenie biomarkerów, zmiany w EKG, zmiany frakcji wyrzutowej) spowodowanych którąkolwiek z fal dwufazowych do energii 360 J 150,152, niektóre badania na zwierzętach jednak sugerują potencjalne ryzyko uszkodzenia wraz ze wzrostem energii Energia pierwszego wyładowania nie powinna być niższa niż 120 J dla fali RLB oraz 150 J dla fali BTE. Najlepiej, jeśli energia każdej fali dwufazowej dla pierwszej defibrylacji wynosi przynajmniej 150 J. Producenci powinni podawać skuteczną wartość energii na panelu defibrylatora dwufazowego; starsze defibrylatory 3
102 102 Ch.D. Deakin, J.P. Nolan, K. Sunde, R.W. Koster 3 jednofazowe również powinny być w czytelny sposób oznakowane. Jeśli ratownik nie wie, jaka jest zalecana energia dla danego urządzenia, powinien użyć najwyższej możliwej. Druga i kolejne defibrylacje Wytyczne 2005 zalecały, by do defibrylacji używać stałej lub stopniowo zwiększanej energii. Przeprowadzone w oparciu o te zalecenia badania wykazały, że chociaż wzrastające energie zmniejszają ilość wyładowań koniecznych do przywrócenia zorganizowanego rytmu i mogą być konieczne dla uzyskania skutecznej defibrylacji 157,158, częstość ROSC lub przeżywalność do wypisu ze szpitala nie różni się znacząco w porównaniu ze strategią o stałej wartości energii defibrylacji 150,151. Przeciwnie, stała wartość energii stosowana trzykrotnie wykazała wysoką częstość kardiowersji (>90%), lecz zbyt mała ilość opisanych przypadków nie wyklucza znaczącego spadku częstości ROSC przy nawracającym VF 159. Kilka badań prowadzonych w szpitalach, w których używano strategii wzrastającej energii do kardiowersji, wykazało wiekszą skuteczność (porównując do powtarzanych wyładowań stałą energią) przy leczeniu zaburzeń rytmu u pacjentów bez zatrzymania krążenia, wykorzystując zarówno defibrylatory jedno-, jak i dwufazowe 135,137, Defibrylatory jednofazowe Jeśli pierwsze wyładowanie energią 360 J jest nieskuteczne, kolejne wyładowania powinny być wykonywane również energią 360 J. Defibrylatory dwufazowe Nie ma dowodów popierających strategię stosowania stałych czy wzrastających energii. Obydwie strategie są akceptowalne, jeśli jednak pierwsze wyładowanie było nieskuteczne, a defibrylator jest przystosowany do wyładowań z większą energią, rozsądnym jest wykonanie kolejnych defibrylacji wyższą energią. Nawracające migotanie komór Gdy rytm do defibrylacji powraca po skutecznej defibrylacji i osiągnięciu ROSC, należy wykonać następne wyładowanie energią, która poprzednio była skuteczna. Inne zagadnienia związane z defibrylacją Defibrylacja u dzieci Zatrzymanie krążenia u dzieci występuje rzadziej. Najczęstsze przyczyny VF u dzieci to urazy, wrodzona choroba serca, wydłużony odstęp QT, przedawkowanie leków i hipotermia W porównaniu z zatrzymaniem krążenia u dorosłych migotanie komór występuje stosunkowo rzadko, stanowiąc 7 15% zatrzymań krążenia u dzieci i młodocianych Natychmiastowa defibrylacja takich pacjentów może poprawić odległe wyniki resuscytacji 171,172. Optymalny poziom energii, kształt fali i sekwencja wyładowań są nieznane, lecz, podobnie jak u dorosłych, wyładowania dwufazowe wydają się co najmniej tak samo efektywne, a powodują mniej uszkodzeń niż wyładowania jednofazowe Górna granica bezpiecznej energii defibrylacji jest nieznana, ale wyładowania o energii przewyższającej uprzednio zalecane maksimum 4 J/kg (do 9 J/kg) powodowały skuteczną defibrylację bez znaczących efektów niepożądanych 38,176,177. Zalecana wartość energii dla klasycznych defibrylatorów jednofazowych wynosi 4 J/kg dla pierwszego i kolejnych wyładowań. Ten sam poziom energii jest zalecany dla klasycznych defibrylatorów dwufazowych 178. Podobnie jak u dorosłych, jeżeli rytm do defibrylacji nawraca, do następnego wyładowania należy zastosować energię, która poprzednio była skuteczna. Używając AED do defibrylacji u dzieci powyżej 8. roku życia, stosuje się standardowe elektrody i dopuszczalne jest wykorzystanie standardowych ustawień energii. U dzieci w przedziale 1 8 lat zaleca się stosowanie specjalnych elektrod dziecięcych oraz przystawek zmniejszających energię do poziomu zalecanego dla defibrylatorów manualnych. Jeśli takie AED nie jest dostępne, należy użyć urządzenia ze standardowymi elektrodami. Użycie AED nie jest zalecane dla dzieci poniżej 1. roku życia, opisano jednak kilka przypadków użycia AED u dzieci w tym wieku 179,180. Możliwość wystąpienia rytmów defibrylacyjnych u noworodków jest bardzo niska, chyba że występuje choroba serca 167,181,182. W tych rzadkich przypadkach, jeśli AED jest jedynym dostępnym defibrylatorem, należy rozważyć jego użycie (najlepiej z przystawką zmniejszającą energię defibrylacji). Kardiowersja Gdy kardiowersja jest wykonywana w przedsionkowych czy komorowych zaburzeniach rytmu, konieczne jest zsynchronizowanie wyładowania z załamkiem R elektrokardiogramu, a nie z załamkiem T, ponieważ dostarczenie wyładowania w trakcie refrakcji względnej cyklu serca może doprowadzić do migotania komór 183. W przypadku VT synchronizacja może być utrudniona z powodu szerokich zespołów QRS oraz różnych form arytmii komorowych. Należy kontrolować znacznik synchronizacji, by być pewnym właściwego rozpoznania załamka R. W razie konieczności należy zmienić odprowadzenie lub/i cechę zapisu. Jeśli synchronizacja nie zadziała, u pacjenta z niestabilnym VT należy wykonać niezsynchronizowane wyładowanie, aby uniknąć opóźnienia w przywróceniu rytmu zatokowego. Migotanie komór oraz VT bez tętna wymagają wyładowań niezsynchronizowanych. Przytomni pacjenci przed wykonaniem próby zsynchronizowanej kardiowersji powinni zostać znieczuleni lub poddani sedacji. Migotanie przedsionków Omówiono już optymalne ułożenie elektrod, jednak zarówno przednio-boczne, jak i przednio-tylne ułożenie elektrod jest akceptowalne. Fale dwufazowe są skuteczniejsze od jednofazowych w kardiowersji AF oraz powodują mniejsze oparzenia skóry 184. Dlatego, jeśli to możliwe, preferuje się użycie defibrylatorów dwufazowych zamiast defibrylatorów jednofazowych. Różnice pomiędzy falami dwufazowymi nie zostały określone. Fale jednofazowe Badania nad kardiowersją elektryczną stosowaną w AF wykazały, iż wyładowania o energii 360 J i kształcie fali
103 Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja 103 MDS były bardziej skuteczne niż wyładowania 100 J lub 200 J MDS 185. Mimo że pierwsze wyładowanie o energii 360 J zmniejsza całkowitą ilość energii wymaganą do kardiowersji 185, należy brać pod uwagę fakt, iż może spowodować większe uszkodzenia mięśnia sercowego oraz mocniejsze oparzenia skóry niż przy użyciu wyładowań o mniejszej energii. Zaleca się rozpoczynanie kardiowersji migotania przedsionków od energii 200 J i jej stopniowe zwiększanie, jeśli to konieczne. Fale dwufazowe Konieczne jest przeprowadzenie większej ilości badań, zanim zostaną opracowane szczegółowe zalecenia dotyczące optymalnej energii dwufazowej. Rozpoczynanie kardiowersji od wyższych wartości energii nie wykazało lepszych rezultatów w porównaniu z niższymi 135, Na podstawie obecnych danych do pierwszego wyładowania zaleca się użycie energii na poziomie J i jej zwiększenie w razie konieczności. Trzepotanie przedsionków i napadowy częstoskurcz nadkomorowy Trzepotanie przedsionków oraz napadowy częstoskurcz nadkomorowy (Supraventricular Tachycardia SVT) wymagają ogólnie mniejszych poziomów energii do kardiowersji niż migotanie przedsionków 190. Zaleca się wykonanie pierwszego wyładowania energią 100 J jednofazową lub J dwufazową. Kolejne wyładowania powinny być wykonywane zwiększanymi stopniowo energiami 144. Częstoskurcz komorowy Energia konieczna do kardiowersji VT zależy od charakterystyki morfologicznej oraz częstości arytmii 192. VT z tętnem poddaje się dobrze leczeniu początkową energią jednofazową 200 J. W przypadku energii dwufazowej zaleca się użycie dla pierwszego wyładowania energii J. Jeśli pierwsze wyładowanie nie spowoduje przywrócenia rytmu zatokowego, rozważ wykonanie kolejnych zwiększanymi stopniowo energiami 192. Stymulacja Stymulację należy rozważyć w przypadku leczenia pacjentów z objawową bradykardią, oporną na leki antycholinergiczne lub inne sposoby leczenia (zob. rozdział 4. Zaawansowane zabiegi resuscytacyjne u osób dorosłych) 113. Natychmiastowa stymulacja jest wskazana zwłaszcza wtedy, gdy blok występuje na poziomie lub poniżej pęczka Hisa. Jeśli stymulacja przezskórna jest nieskuteczna, należy rozważyć stymulację elektrodą endokawitarną. Zawsze, jeśli postawiona jest diagnoza asystolii, należy uważnie sprawdzić EKG w poszukiwaniu załamków P, ponieważ ten rodzaj asystolii może odpowiedzieć na stymulację serca. Użycie elektrod nasierdziowych do stymulacji mięśnia sercowego po zabiegach kardiochiruricznych jest skuteczne i omówione dalej. Nie należy podejmować prób stymulacji w asystolii, jeśli załamki P są nieobecne; nie powoduje to poprawy ani krótkoterminowego, ani długoterminowego przeżycia w szpitalu lub poza nim U pacjentów niestabilnych, przytomnych z bradyarytmią można zastosować stymulację mechaniczną (percussion pacing) w oczekiwaniu na podłączenie stymulatora, choć jej skuteczność nie jest do tej pory określona. Wszczepialne kardiowertery-defibrylatory Wszczepialne kardiowerterty-defibrylatory (Implantable Cardioverter Defibrillators ICD) stają się coraz bardziej popularne i chętnie stosowane ze względu na starzenie się społeczeństwa. Są one stosowane w przypadku przebycia lub ryzyka zagrażających życiu zaburzeń rytmu poddających się leczeniu kardiowersją lub defibrylacją. Umieszcza się je z reguły pod mięśniem piersiowym poniżej lewego obojczyka (podobnie jak stymulatory, od których trudno je odróżnić na pierwszy rzut oka). W prawej komorze serca zostaje umieszczona elektroda, przez którą dostarczany jest impuls o energii około 40 J, jeżeli urządzenie wykryje rytm wymagający wyładowania. Wykrywając VF/VT, urządzenie wykona maksymalnie osiem wyładowań, może jednak rozpocząć procedurę od początku, jeżeli wykryje ponowne pojawienie się VF/VT. W przypadku uszkodzenia elektrody kardiowertera-defibrylatora pacjent może odczuwać powtarzające się defibrylacje w związku z zakłóceniami elektrycznymi, które odbierane są jako rytm do defibrylacji. W takich przypadkch pacjenci są z reguły przytomni, a w EKG obserwujemy względnie prawidłową częstość serca. Umieszczenie nad ICD magnesu zablokuje wtedy funkcję defibrylacji. Wyładowanie ICD może spowodować skurcz mięśni piersiowych, ponadto opisano przypadki porażenia prądem ratowników udzielających pomocy 202. Ze względu na niską energię wyładowania ICD są bezpieczne dla ratowników, rozsądne jednak jest użycie rękawiczek i minimalizowanie kontaktu z pacjentem podczas wyładowania. Po każdej wykonanej defibrylacji ICD, a także wszczepiony rozrusznik serca powinny być ponownie sprawdzone zarówno pod względem funkcjonowania samego urządzenia, jak i ustawień progu defibrylacji lub stymulacji. Piki stymulacji generowane przez urządzenie zaprogramowane na stymulację jednobiegunową mogą zaburzać pracę oprogramowania AED oraz dezorientować zespół ratowniczy, co może uniemożliwić rozpoznanie VF 203. Algorytmy diagnostyczne nowoczesnych AED są niewrażliwe na występowanie pików stymulacji. Bibliografia 1. Deakin CD, Nolan JP. European Resuscitation Council guidelines for resuscitation Section 3. Electrical therapies: automated external defibrillators, defibrillation, cardioversion and pacing. Resuscitation 2005;67(Suppl. 1):S Proceedings of the 2005 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Resuscitation 2005;67: Larsen MP, Eisenberg MS, Cummins RO, Hallstrom AP. Predicting survival from out-of-hospital cardiac arrest: a graphic model. Ann Emerg Med 1993;22: Valenzuela TD, Roe DJ, Cretin S, Spaite DW, Larsen MP. Estimating effectiveness of cardiac arrest interventions: a logistic regression survival model. Circulation 1997;96: Waalewijn RA, de Vos R, Tijssen JG, Koster RW. Survival models for out-of- -hospital cardiopulmonary resuscitation from the perspectives of the bystander, the first responder, and the paramedic. Resuscitation 2001;51: Weisfeldt ML, Sitlani CM, Ornato JP, et al. Survival after application of automatic external defibrillators before arrival of the emergency medical system: eval- 3
104 104 Ch.D. Deakin, J.P. Nolan, K. Sunde, R.W. Koster 3 uation in the resuscitation outcomes consortium population of 21 million. J Am Coll Cardiol 2010;55: Myerburg RJ, Fenster J, Velez M, et al. Impact of community-wide police car deployment of automated external defibrillators on survival from out-of-hospital cardiac arrest. Circulation 2002;106: Capucci A, Aschieri D, Piepoli MF, Bardy GH, Iconomu E, Arvedi M. Tripling survival from sudden cardiac arrest via early defibrillation without traditional education in cardiopulmonary resuscitation. Circulation 2002;106: van Alem AP, Vrenken RH, de Vos R, Tijssen JG, Koster RW. Use of automated external defibrillator by first responders in out of hospital cardiac arrest: prospective controlled trial. BMJ 2003;327: Valenzuela TD, Bjerke HS, Clark LL, et al. Rapid defibrillation by nontraditional responders: the Casino Project. Acad Emerg Med 1998;5: Spearpoint KG, Gruber PC, Brett SJ. Impact of the Immediate Life Support course on the incidence and outcome of in-hospital cardiac arrest calls: an observational study over 6 years. Resuscitation 2009;80: Waalewijn RA, Tijssen JG, Koster RW. Bystander initiated actions in out-of- -hospital cardiopulmonary resuscitation: results from the Amsterdam Resuscitation Study (ARREST). Resuscitation 2001;50: Swor RA, Jackson RE, Cynar M, et al. Bystander CPR, ventricular fibrillation, and survival in witnessed, unmonitored out-of-hospital cardiac arrest. Ann Emerg Med 1995;25: Holmberg M, Holmberg S, Herlitz J. Effect of bystander cardiopulmonary resuscitation in out-of-hospital cardiac arrest patients in Sweden. Resuscitation 2000;47: Vaillancourt C, Verma A, Trickett J, et al. Evaluating the effectiveness of dispatch-assisted cardiopulmonary resuscitation instructions. Acad Emerg Med 2007;14: O Neill JF, Deakin CD. Evaluation of telephone CPR advice for adult cardiac arrest patients. Resuscitation 2007;74: Yang CW, Wang HC, Chiang WC, et al. Interactive video instruction improves the quality of dispatcher-assisted chest compression-only cardiopulmonary resuscitation in simulated cardiac arrests. Crit Care Med 2009;37: Yang CW, Wang HC, Chiang WC, et al. Impact of adding video communication to dispatch instructions on the quality of rescue breathing in simulated cardiac arrests a randomized controlled study. Resuscitation 2008;78: Koster RW, Baubin MA, Caballero A, et al. European Resuscitation Council Guidelines for Resuscitation Section 2. Adult basic life support and use of automated external defibrillators. Resuscitation 2010;81: Berdowski J, Schulten RJ, Tijssen JG, van Alem AP, Koster RW. Delaying a shock after take over from the automated external defibrillator by paramedics is associated with decreased survival. Resuscitation 2010;81: Zafari AM, Zarter SK, Heggen V, et al. A program encouraging early defibrillation results in improved in-hospital resuscitation efficacy. J Am Coll Cardiol 2004;44: Destro A, Marzaloni M, Sermasi S, Rossi F. Automatic external defibrillators in the hospital as well? Resuscitation 1996;31: Forcina MS, Farhat AY, O Neil WW, Haines Defi Cardiac arrest survival after implementation of automated external defibrillator technology in the in-hospital setting. Crit Care Med 2009;37: Domanovits H, Meron G, Sterz F, et al. Successful automatic external defibrillator operation by people trained only in basic life support in a simulated cardiac arrest situation. Resuscitation 1998;39: Cusnir H, Tongia R, Sheka KP, et al. In hospital cardiac arrest: a role for automatic defibrillation. Resuscitation 2004;63: Chan PS, Krumholz HM, Nichol G, Nallamothu BK. Delayed time to defibrillation after in-hospital cardiac arrest. N Engl J Med 2008;358: Cummins RO, Eisenberg MS, Litwin PE, Graves JR, Hearne TR, Hallstrom AP. Automatic external defibrillators used by emergency medical technicians: a controlled clinical trial. JAMA 1987;257: Stults KR, Brown DD, Kerber RE. Efficacy of an automated external defibrillator in the management of out-of-hospital cardiac arrest: validation of the diagnostic algorithm and initial clinical experience in a rural environment. Circulation 1986;73: Kramer-Johansen J, Edelson DP, Abella BS, Becker LB, Wik L, Steen PA. Pauses in chest compression and inappropriate shocks: a comparison of manual and semi-automatic defibrillation attempts. Resuscitation 2007;73: Pytte M, Pedersen TE, Ottem J, Rokvam AS, Sunde K. Comparison of hands- -off time during CPR with manual and semi-automatic defibrillation in a manikin model. Resuscitation 2007;73: Edelson DP, Abella BS, Kramer-Johansen J, et al. Effects of compression depth and pre-shock pauses predict defibrillation failure during cardiac arrest. Resuscitation 2006;71: Eftestol T, Sunde K, Steen PA. Effects of interrupting precordial compressions on the calculated probability of defibrillation success during out-of-hospital cardiac arrest. Circulation 2002;105: Yu T, Weil MH, Tang W, et al. Adverse outcomes of interrupted precordial compression during automated defibrillation. Circulation 2002;106: Wik L, Kramer-Johansen J, Myklebust H, et al. Quality of cardiopulmonary resuscitation during out-of-hospital cardiac arrest. JAMA 2005;293: Abella BS, Alvarado JP, Myklebust H, et al. Quality of cardiopulmonary resuscitation during in-hospital cardiac arrest. JAMA 2005;293: Kerber RE, Becker LB, Bourland JD, et al. Automatic external defibrillators for public access defibrillation: recommendations for specifying and reporting arrhythmia analysis algorithm performance, incorporating new waveforms, and enhancing safety. A statement for health professionals from the American Heart Association Task Force on Automatic External Defibrillation, Subcommittee on AED Safety and Efficacy. Circulation 1997;95: Dickey W, Dalzell GW, Anderson JM, Adgey AA. The accuracy of decisionmaking of a semi-automatic defibrillator during cardiac arrest. Eur Heart J 1992;13: Atkinson E, Mikysa B, Conway JA, et al. Specificity and sensitivity of automated external defibrillator rhythm analysis in infants and children. Ann Emerg Med 2003;42: Cecchin F, Jorgenson DB, Berul CI, et al. Is arrhythmia detection by automatic external defibrillator accurate for children? Sensitivity and specificity of an automatic external defibrillator algorithm in 696 pediatric arrhythmias. Circulation 2001;103: van Alem AP, Sanou BT, Koster RW. Interruption of cardiopulmonary resuscitation with the use of the automated external defibrillator in out-of-hospital cardiac arrest. Ann Emerg Med 2003;42: Rea TD, Helbock M, Perry S, et al. Increasing use of cardiopulmonary resuscitation during out-of-hospital ventricular fibrillation arrest: survival implications of guideline changes. Circulation 2006;114: Gundersen K, Kvaloy JT, Kramer-Johansen J, Steen PA, Eftestol T. Development of the probability of return of spontaneous circulation in intervals without chest compressions during out-of-hospital cardiac arrest: an observational study. BMC Med 2009;7: Lloyd MS, Heeke B, Walter PF, Langberg JJ. Hands-on defibrillation: an analysis of electrical current flow through rescuers in direct contact with patients during biphasic external defibrillation. Circulation 2008;117: Miller PH. Potential fire hazard in defibrillation. JAMA 1972;221: Hummel III RS, Ornato JP, Weinberg SM, Clarke AM. Spark-generating properties of electrode gels used during defibrillation. A potential fire hazard. JAMA 1988;260: ECRI. Defibrillation in oxygen-enriched environments [hazard]. Health Devices 1987;16: Lefever J, Smith A. Risk of fire when using defibrillation in an oxygen enriched atmosphere. Med Devices Agency Safety Notices 1995;3: Ward ME. Risk of fires when using defibrillators in an oxygen enriched atmosphere. Resuscitation 1996;31: Theodorou AA, Gutierrez JA, Berg RA. Fire attributable to a defibrillation attempt in a neonate. Pediatrics 2003;112: Robertshaw H, McAnulty G. Ambient oxygen concentrations during simulated cardiopulmonary resuscitation. Anaesthesia 1998;53: Cantello E, Davy TE, Koenig KL. The question of removing a ventilation bag before defibrillation. J Accid Emerg Med 1998;15: Deakin CD, Paul V, Fall E, Petley GW, Thompson F. Ambient oxygen concentrations resulting from use of the Lund University Cardiopulmonary Assist System (LUCAS) device during simulated cardiopulmonary resuscitation. Resuscitation 2007;74: Kerber RE, Kouba C, Martins J, et al. Advance prediction of transthoracic impedance in human defibrillation and cardioversion: importance of impedance in determining the success of low-energy shocks. Circulation 1984;70: Kerber RE, Grayzel J, Hoyt R, Marcus M, Kennedy J. Transthoracic resistance in human defibrillation. Influence of body weight, chest size,serial shocks, paddle size and paddle contact pressure. Circulation 1981;63: Sado DM, Deakin CD, Petley GW, Clewlow F. Comparison of the effects of removal of chest hair with not doing so before external defibrillation on transthoracic impedance. Am J Cardiol 2004;93: Walsh SJ, McCarty D, McClelland AJ, et al. Impedance compensated biphasic waveforms for transthoracic cardioversion of atrial fibrillation: a multi-centre comparison of antero-apical and antero-posterior pad positions. Eur Heart J 2005;26: Deakin CD, Sado DM, Petley GW, Clewlow F. Differential contribution of skin impedance and thoracic volume to transthoracic impedance during external defibrillation. Resuscitation 2004;60: Deakin C, Sado D, Petley G, Clewlow F. Determining the optimal paddle force for external defibrillation. Am J Cardiol 2002;90: Manegold JC, Israel CW, Ehrlich JR, et al. External cardioversion of atrial fibrillation in patients with implanted pacemaker or cardioverter-defibrillator systems: a randomized comparison of monophasic and biphasic shock energy application. Eur Heart J 2007;28: Alferness CA. Pacemaker damage due to external countershock in patients with implanted cardiac pacemakers. Pacing Clin Electrophysiol 1982;5: Panacek EA, Munger MA, Rutherford WF, Gardner SF. Report of nitropatch explosions complicating defibrillation. Am J Emerg Med 1992;10: Wrenn K. The hazards of defibrillation through nitroglycerin patches. Ann Emerg Med 1990;19: Pagan-Carlo LA, Spencer KT, Robertson CE, Dengler A, Birkett C, Kerber RE. Transthoracic defibrillation: importance of avoiding electrode placement directly on the female breast. J Am Coll Cardiol 1996;27: Deakin CD, Sado DM, Petley GW, Clewlow F. Is the orientation of the apical defibrillation paddle of importance during manual external defibrillation? Resuscitation 2003;56: Kirchhof P, Eckardt L, Loh P, et al. Anterior-posterior versus anterior-lateral electrode positions for external cardioversion of atrial fibrillation: a randomised trial. Lancet 2002;360:
105 Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja Botto GL, Politi A, Bonini W, Broffoni T, Bonatti R. External cardioversion of atrial fibrillation: role of paddle position on technical efficacy and energy requirements. Heart 1999;82: Alp NJ, Rahman S, Bell JA, Shahi M. Randomised comparison of antero-lateral versus antero-posterior paddle positions for DC cardioversion of persistent atrial fibrillation. Int J Cardiol 2000;75: Mathew TP, Moore A, McIntyre M, et al. Randomised comparison of electrode positions for cardioversion of atrial fibrillation. Heart 1999;81: Deakin CD, McLaren RM, Petley GW, Clewlow F, Dalrymple-Hay MJ. Effects of positive end-expiratory pressure on transthoracic impedance implications for defibrillation. Resuscitation 1998;37: American National Standard: automatic external defibrillators and remote controlled defibrillators (DF39). Arlington, Virgina: Association for the Advancement of Medical Instrumentation; Deakin CD, McLaren RM, Petley GW, Clewlow F, Dalrymple-Hay MJ. A comparison of transthoracic impedance using standard defibrillation paddles and self-adhesive defibrillation pads. Resuscitation 1998;39: Stults KR, Brown DD, Cooley F, Kerber RE. Self-adhesive monitor/defibrillation pads improve prehospital defibrillation success. Ann Emerg Med 1987;16: Bojar RM, Payne DD, Rastegar H, Diehl JT, Cleveland RJ. Use of self-adhesive external defibrillator pads for complex cardiac surgical procedures. Ann Thorac Surg 1988;46: Bradbury N, Hyde D, Nolan J. Reliability of ECG monitoring with a gel pad/ paddle combination after defibrillation. Resuscitation 2000;44: Brown J, Rogers J, Soar J. Cardiac arrest during surgery and ventilation in the prone position: a case report and systematic review. Resuscitation 2001;50: Perkins GD, Davies RP, Soar J, Thickett DR. The impact of manual defibrillation technique on no-flow time during simulated cardiopulmonary resuscitation. Resuscitation 2007;73: Wilson RF, Sirna S, White CW, Kerber RE. Defibrillation of high-risk patients during coronary angiography using self-adhesive, preapplied electrode pads. Am J Cardiol 1987;60: Kerber RE, Martins JB, Kelly KJ, et al. Self-adhesive preapplied electrode pads for defibrillation and cardioversion. J Am Coll Cardiol 1984;3: Kerber RE, Martins JB, Ferguson DW, et al. Experimental evaluation and initial clinical application of new self-adhesive defibrillation electrodes. Int J Cardiol 1985;8: Perkins GD, Roberts C, Gao F. Delays in defibrillation: influence of different monitoring techniques. Br J Anaesth 2002;89: Chamberlain D. Gel pads should not be used for monitoring ECG after defibrillation. Resuscitation 2000;43: Callaway CW, Sherman LD, Mosesso Jr VN, Dietrich TJ, Holt E, Clarkson MC. Scaling exponent predicts defibrillation success for out-of-hospital ventricular fibrillation cardiac arrest. Circulation 2001;103: Eftestol T, Sunde K, Aase SO, Husoy JH, Steen PA. Predicting outcome of defibrillation by spectral characterization and nonparametric classification of ventricular fibrillation in patients with out-of-hospital cardiac arrest. Circulation 2000;102: Eftestol T, Wik L, Sunde K, Steen PA. Effects of cardiopulmonary resuscitation on predictors of ventricular fibrillation defibrillation success during out-of-hospital cardiac arrest. Circulation 2004;110: Weaver WD, Cobb LA, Dennis D, Ray R, Hallstrom AP, Copass MK. Amplitude of ventricular fibrillation waveform and outcome after cardiac arrest. Ann Intern Med 1985;102: Brown CG, Dzwonczyk R. Signal analysis of the human electrocardiogram during ventricular fibrillation: frequency and amplitude parameters as predictors of successful countershock. Ann Emerg Med 1996;27: Callaham M, Braun O, Valentine W, Clark DM, Zegans C. Prehospital cardiac arrest treated by urban first-responders: profile of patient response and prediction of outcome by ventricular fibrillation waveform. Ann Emerg Med 1993;22: Strohmenger HU, Lindner KH, Brown CG. Analysis of the ventricular fibrillation ECG signal amplitude and frequency parameters as predictors of countershock success in humans. Chest 1997;111: Strohmenger HU, Eftestol T, Sunde K, et al. The predictive value of ventricular fibrillation electrocardiogram signal frequency and amplitude variables in patients with out-of-hospital cardiac arrest. Anesth Analg 2001;93: Podbregar M, Kovacic M, Podbregar-Mars A, Brezocnik M. Predicting defibrillation success by genetic programming in patients with out-of-hospital cardiac arrest. Resuscitation 2003;57: Menegazzi JJ, Callaway CW, Sherman LD, et al. Ventricular fibrillation scaling exponent can guide timing of defibrillation and other therapies. Circulation 2004;109: Povoas HP, Weil MH, Tang W, Bisera J, Klouche K, Barbatsis A. Predicting the success of defibrillation by electrocardiographic analysis. Resuscitation 2002;53: Noc M, Weil MH, Tang W, Sun S, Pernat A, Bisera J. Electrocardiographic prediction of the success of cardiac resuscitation. Crit Care Med 1999;27: Strohmenger HU, Lindner KH, Keller A, Lindner IM, Pfenninger EG. Spectral analysis of ventricular fibrillation and closed-chest cardiopulmonary resuscitation. Resuscitation 1996;33: Noc M, Weil MH, Gazmuri RJ, Sun S, Biscera J, Tang W. Ventricular fibrillation voltage as a monitor of the effectiveness of cardiopulmonary resuscitation. J Lab Clin Med 1994;124: Lightfoot CB, Nremt P, Callaway CW, et al. Dynamic nature of electrocardiographic waveform predicts rescue shock outcome in porcine ventricular fibrillation. Ann Emerg Med 2003;42: Marn-Pernat A, Weil MH, Tang W, Pernat A, Bisera J. Optimizing timing of ventricular defibrillation. Crit Care Med 2001;29: Hamprecht FA, Achleitner U, Krismer AC, et al. Fibrillation power, an alternative method of ECG spectral analysis for prediction of countershock success in a porcine model of ventricular fibrillation. Resuscitation 2001;50: Amann A, Achleitner U, Antretter H, et al. Analysing ventricular fibrillation ECG-signals and predicting defibrillation success during cardiopulmonary resuscitation employing N(alpha)-histograms. Resuscitation 2001;50: Brown CG, Grif.th RF, Van Ligten P, et al. Median frequency a new parameter for predicting defibrillation success rate. Ann Emerg Med 1991;20: Amann A, Rheinberger K, Achleitner U, et al. The prediction of defibrillation outcome using a new combination of mean frequency and amplitude in porcine models of cardiac arrest. Anesth Analg 2002;95:716 22, table of contents Cobb LA, Fahrenbruch CE, Walsh TR, et al. Influence of cardiopulmonary resuscitation prior to defibrillation in patients with out-of-hospital ventricular fibrillation. JAMA 1999;281: Wik L, Hansen TB, Fylling F, et al. Delaying defibrillation to give basic cardiopulmonary resuscitation to patients with out-of-hospital ventricular fibrillation: a randomized trial. JAMA 2003;289: Berg RA, Hilwig RW, Kern KB, Ewy GA. Precountershock cardiopulmonary resuscitation improves ventricular fibrillation median frequency and myocardial readiness for successful defibrillation from prolonged ventricular fibrillation: a randomized, controlled swine study. Ann Emerg Med 2002;40: Berg RA, Hilwig RW, Ewy GA, Kern KB. Precountershock cardiopulmonary resuscitation improves initial response to defibrillation from prolonged ventricular fibrillation: a randomized, controlled swine study. Crit Care Med 2004;32: Kolarova J, Ayoub IM, Yi Z, Gazmuri RJ. Optimal timing for electrical defibrillation after prolonged untreated ventricular fibrillation. Crit Care Med 2003;31: Indik JH, Hilwig RW, Zuercher M, Kern KB, Berg MD, Berg RA. Preshock cardiopulmonary resuscitation worsens outcome from circulatory phase ventricular fibrillation with acute coronary artery obstruction in swine. Circ Arrhythm Electrophysiol 2009;2: Baker PW, Conway J, Cotton C, et al. Defibrillation or cardiopulmonary resuscitation first for patients with out-of-hospital cardiac arrests found by paramedics to be in ventricular fibrillation? A randomised control trial. Resuscitation 2008;79: Jacobs IG, Finn JC, Oxer HF, Jelinek GA. CPR before defibrillation in out-of- -hospital cardiac arrest: a randomized trial. Emerg Med Aust 2005;17: Hayakawa M, Gando S, Okamoto H, Asai Y, Uegaki S, Makise H. Shortening of cardiopulmonary resuscitation time before the defibrillation worsens the outcome in out-of-hospital VF patients. Am J Emerg Med 2009;27: Bradley SM, Gabriel EE, Aufderheide TP, et al. Survival Increases with CPR by Emergency Medical Services before defibrillation of out-of-hospital ventricular fibrillation or ventricular tachycardia: observations from the Resuscitation Outcomes Consortium. Resuscitation 2010;81: Christenson J, Andrusiek D, Everson-Stewart S, et al. Chest compression fraction determines survival in patients with out-of-hospital ventricular fibrillation. Circulation 2009;120: Deakin CD, Nolan JP, Soar J, et al. European Resuscitation Council Guidelines for Resuscitation Section 4. Adult advanced life support. Resuscitation 2010;81: Berg RA, Sanders AB, Kern KB, et al. Adverse hemodynamic effects of interrupting chest compressions for rescue breathing during cardiopulmonary resuscitation for ventricular fibrillation cardiac arrest. Circulation 2001;104: Kern KB, Hilwig RW, Berg RA, Sanders AB, Ewy GA. Importance of continuous chest compressions during cardiopulmonary resuscitation:improved outcome during a simulated single lay-rescuer scenario. Circulation 2002;105: Valenzuela TD, Kern KB, Clark LL, et al. Interruptions of chest compressions during emergency medical systems resuscitation. Circulation 2005;112: Bain AC, Swerdlow CD, Love CJ, et al. Multicenter study of principles-based waveforms for external defibrillation. Ann Emerg Med 2001;37: Poole JE, White RD, Kanz KG, et al. Low-energy impedance-compensating biphasic waveforms terminate ventricular fibrillation at high rates in victims of out-of-hospital cardiac arrest. LIFE Investigators. J Cardiovasc Electrophysiol 1997;8: Schneider T, Martens PR, Paschen H, et al. Multicenter, randomized, controlled trial of 150-J biphasic shocks compared with 200-to 360-J monophasic shocks in the resuscitation of out-of-hospital cardiac arrest victims. Optimized Response to Cardiac Arrest (ORCA) Investigators. Circulation 2000;102: Rea TD, Shah S, Kudenchuk PJ, Copass MK, Cobb LA. Automated external defibrillators: to what extent does the algorithm delay CPR? Ann Emerg Med 2005;46: Olasveengen TM, Vik E, Kuzovlev A, Sunde K. Effect of implementation of new resuscitation guidelines on quality of cardiopulmonary resuscitation and survival. Resuscitation 2009;80: Bobrow BJ, Clark LL, Ewy GA, et al. Minimally interrupted cardiac resuscitation by emergency medical services for out-of-hospital cardiac arrest. JAMA 2008;299:
106 106 Ch.D. Deakin, J.P. Nolan, K. Sunde, R.W. Koster Steinmetz J, Barnung S, Nielsen SL, Risom M, Rasmussen LS. Improved survival after an out-of-hospital cardiac arrest using new guidelines. Acta Anaesthesiol Scand 2008;52: Jost D, Degrange H, Verret C, et al. DEFI 2005: a randomized controlled trial of the effect of automated external defibrillator cardiopulmonary resuscitation protocol on outcome from out-of-hospital cardiac arrest. Circulation 2010;121: Soar J, Perkins GD, Abbas G, et al. European Resuscitation Council Guidelines for Resuscitation Section 8. Cardiac arrest in special circumstances: electrolyte abnormalities, poisoning, drowning, accidental hypothermia, hyperthermia, asthma, anaphylaxis, cardiac surgery, trauma, pregnancy, electrocution. Resuscitation 2010;81: Didon JP, Fontaine G, White RD, Jekova I, Schmid JJ, Cansell A. Clinical experience with a low-energy pulsed biphasic waveform in out-of-hospital cardiac arrest. Resuscitation 2008;76: Li Y, Wang H, Cho JH, et al. Comparison of efficacy of pulsed biphasic waveform and rectilinear biphasic waveform in a short ventricular fibrillation pig model. Resuscitation 2009;80: van Alem AP, Chapman FW, Lank P, Hart AA, Koster RW. A prospective, randomised and blinded comparison of first shock success of monophasic and biphasic waveforms in out-of-hospital cardiac arrest. Resuscitation 2003;58: Carpenter J, Rea TD, Murray JA, Kudenchuk PJ, Eisenberg MS. Defibrillation waveform and post-shock rhythm in out-of-hospital ventricular fibrillation cardiac arrest. Resuscitation 2003;59: Morrison LJ, Dorian P, Long J, et al. Out-of-hospital cardiac arrest rectilinear biphasic to monophasic damped sine defibrillation waveforms with advanced life support intervention trial (ORBIT). Resuscitation 2005;66: Gliner BE, White RD. Electrocardiographic evaluation of defibrillation shocks delivered to out-of-hospital sudden cardiac arrest patients. Resuscitation 1999;41: Freeman K, Hendey GW, Shalit M, Stroh G. Biphasic defibrillation does not improve outcomes compared to monophasic defibrillation in out-of-hospital cardiac arrest. Prehosp Emerg Care 2008;12: Hess EP, Atkinson EJ, White RD. Increased prevalence of sustained return of spontaneous circulation following transition to biphasic waveform defibrillation. Resuscitation 2008;77: Kudenchuk PJ, Cobb LA, Copass MK, Olsufka M, Maynard C, Nichol G. Transthoracic incremental monophasic versus biphasic defibrillation by emergency responders (TIMBER): a randomized comparison of monophasic with biphasic waveform ascending energy defibrillation for the resuscitation of out-of-hospital cardiac arrest due to ventricular fibrillation. Circulation 2006;114: Mittal S, Ayati S, Stein KM, et al. Transthoracic cardioversion of atrial fibrillation: comparison of rectilinear biphasic versus damped sine wave monophasic shocks. Circulation 2000;101: Page RL, Kerber RE, Russell JK, et al. Biphasic versus monophasic shock waveform for conversion of atrial fibrillation: the results of an international randomized, double-blind multicenter trial. J Am Coll Cardiol 2002;39: Koster RW, Dorian P, Chapman FW, Schmitt PW, O Grady SG, Walker RG. A randomized trial comparing monophasic and biphasic waveform shocks for external cardioversion of atrial fibrillation. Am Heart J 2004;147:e Ambler JJ, Deakin CD. A randomized controlled trial of efficacy and ST change following use of the Welch-Allyn MRL PIC biphasic waveform versus damped sine monophasic waveform for external DC cardioversion. Resuscitation 2006;71: Pagan-Carlo LA, Allan JJ, Spencer KT, Birkett CL, Myers R, Kerber RE. Encircling overlapping multipulse shock waveforms for transthoracic defibrillation. J Am Coll Cardiol 1998;32: Zhang Y, Ramabadran RS, Boddicker KA, et al. Triphasic waveforms are superior to biphasic waveforms for transthoracic defibrillation: experimental studies. J Am Coll Cardiol 2003;42: Zhang Y, Rhee B, Davies LR, et al. Quadriphasic waveforms are superior to triphasic waveforms for transthoracic defibrillation in a cardiac arrest swine model with high impedance. Resuscitation 2006;68: Kerber RE. External defibrillation: new technologies. Ann Emerg Med 1984;13: Joglar JA, Kessler DJ, Welch PJ, et al. Effects of repeated electrical defibrillations on cardiac troponin I levels. Am J Cardiol 1999;83: A Kerber RE, Martins JB, Kienzle MG, et al. Energy, current, and success in defibrillation and cardioversion: clinical studies using an automated impedancebased method of energy adjustment. Circulation 1988;77: Martens PR, Russell JK, Wolcke B, et al. Optimal Response to Cardiac Arrest study: defibrillation waveform effects. Resuscitation 2001;49: Weaver WD, Cobb LA, Copass MK, Hallstrom AP. Ventricular defibrillation: a comparative trial using 175-Jand 320-J shocks. N Engl J Med 1982;307: Tang W, Weil MH, Sun S, et al. The effects of biphasic and conventional monophasic defibrillation on postresuscitation myocardial function. J Am Coll Cardiol 1999;34: Gliner BE, Jorgenson DB, Poole JE, et al. Treatment of out-of-hospital cardiac arrest with a low-energy impedance-compensating biphasic waveform automatic external defibrillator. The LIFE Investigators. Biomed Instrum Technol 1998;32: White RD, Blackwell TH, Russell JK, Snyder DE, Jorgenson DB. Transthoracic impedance does not affect defibrillation, resuscitation or survival in patients with out-of-hospital cardiac arrest treated with a non-escalating biphasic waveform defibrillator. Resuscitation 2005;64: Stiell IG, Walker RG, Nesbitt LP, et al. BIPHASIC Trial: a randomized comparison of fixed lower versus escalating higher energy levels for defibrillation in out-of-hospital cardiac arrest. Circulation 2007;115: Walsh SJ, McClelland AJ, Owens CG, et al. Efficacy of distinct energy delivery protocols comparing two biphasic defibrillators for cardiac arrest. Am J Cardiol 2004;94: Higgins SL, Herre JM, Epstein AE, et al. A comparison of biphasic and monophasic shocks for external defibrillation. Physio-Control Biphasic Investigators. Prehosp Emerg Care 2000;4: Berg RA, Samson RA, Berg MD, et al. Better outcome after pediatric defibrillation dosage than adult dosage in a swine model of pediatric ventricular fibrillation. J Am Coll Cardiol 2005;45: Killingsworth CR, Melnick SB, Chapman FW, et al. Defibrillation threshold and cardiac responses using an external biphasic defibrillator with pediatric and adult adhesive patches in pediatric-sized piglets. Resuscitation 2002;55: Tang W, Weil MH, Sun S, et al. The effects of biphasic waveform design on postresuscitation myocardial function. J Am Coll Cardiol 2004;43: Xie J, Weil MH, Sun S, et al. High-energy defibrillation increases the severity of postresuscitation myocardial dysfunction. Circulation 1997;96: Koster RW, Walker RG, Chapman FW. Recurrent ventricular fibrillation during advanced life support care of patients with prehospital cardiac arrest. Resuscitation 2008;78: Walker RG, Koster RW, Sun C, et al. Defibrillation probability and impedance change between shocks during resuscitation from out-of-hospital cardiac arrest. Resuscitation 2009;80: Hess EP, Russell JK, Liu PY, White RD. A high peak current 150-J fixed-energy defibrillation protocol treats recurrent ventricular fibrillation (VF) as effectively as initial VF. Resuscitation 2008;79: Deakin CD, Ambler JJ. Post-shock myocardial stunning: a prospective randomised double-blind comparison of monophasic and biphasic waveforms. Resuscitation 2006;68: Khaykin Y, Newman D, Kowalewski M, Korley V, Dorian P. Biphasic versus monophasic cardioversion in shock-resistant atrial fibrillation. J Cardiovasc Electrophysiol 2003;14: Kmec J. Comparison the effectiveness of damped sine wave monophasic and rectilinear biphasic shocks in patients with persistent atrial fibrillation. Kardiologia 2006;15: Kosior DA, Szulec M, Torbicki A, Opolski G, Rabczenko D. A decrease of enlarged left atrium following cardioversion of atrial fibrillation predicts the longterm maintenance of sinus rhythm. Kardiol Pol 2005;62: Kuisma M, Suominen P, Korpela R. Paediatric out-of-hospital cardiac arrests: epidemiology and outcome. Resuscitation 1995;30: Sirbaugh PE, Pepe PE, Shook JE, et al. A prospective, population-based study of the demographics, epidemiology, management, and outcome of out-of-hospital pediatric cardiopulmonary arrest. Ann Emerg Med 1999;33: Hickey RW, Cohen DM, Strausbaugh S, Dietrich AM. Pediatric patients requiring CPR in the prehospital setting. Ann Emerg Med 1995;25: Atkins DL, Everson-Stewart S, Sears GK, et al. Epidemiology and outcomes from out-of-hospital cardiac arrest in children: the Resuscitation Outcomes Consortium Epistry-Cardiac Arrest. Circulation 2009;119: Appleton GO, Cummins RO, Larson MP, Graves JR. CPR and the single rescuer: at what age should you call first rather than call fast? Ann Emerg Med 1995;25: Ronco R, King W, Donley DK, Tilden SJ, Outcome. cost at a children s hospital following resuscitation for out-of-hospital cardiopulmonary arrest. Arch Pediatr Adolesc Med 1995;149: Losek JD, Hennes H, Glaeser P, Hendley G, Nelson DB. Prehospital care of the pulseless, nonbreathing pediatric patient. Am J Emerg Med 1987;5: Mogayzel C, Quan L, Graves JR, Tiedeman D, Fahrenbruch C, Herndon P. Out-of-hospital ventricular fibrillation in children and adolescents: causes and outcomes. Ann Emerg Med 1995;25: Safranek DJ, Eisenberg MS, Larsen MP. The epidemiology of cardiac arrest in young adults. Ann Emerg Med 1992;21: Berg RA, Chapman FW, Berg MD, et al. Attenuated adult biphasic shocks compared with weight-based monophasic shocks in a swine model of prolonged pediatric ventricular fibrillation. Resuscitation 2004;61: Tang W, Weil MH, Jorgenson D, et al. Fixed-energy biphasic waveform defibrillation in a pediatric model of cardiac arrest and resuscitation. Crit Care Med 2002;30 : Clark CB, Zhang Y, Davies LR, Karlsson G, Kerber RE. Pediatric transthoracic defibrillation: biphasic versus monophasic waveforms in an experimental model. Resuscitation 2001;51: Gurnett CA, Atkins DL. Successful use of a biphasic waveform automated external defibrillator in a high-risk child. Am J Cardiol 2000;86: Atkins DL, Jorgenson DB. Attenuated pediatric electrode pads for automated external defibrillator use in children. Resuscitation 2005;66: Gutgesell HP, Tacker WA, Geddes LA, Davis S, Lie JT, McNamara DG. Energy dose for ventricular defibrillation of children. Pediatrics 1976;58: Bar-Cohen Y, Walsh EP, Love BA, Cecchin F. First appropriate use of automated external defibrillator in an infant. Resuscitation 2005;67: Divekar A, Soni R. Successful parental use of an automated external defibrillator for an infant with long-qt syndrome. Pediatrics 2006;118:e526 9.
107 Elektroterapia: automatyczne defibrylatory zewnętrzne, defibrylacja, kardiowersja i stymulacja 181. Rodriguez-Nunez A, Lopez-Herce J, Garcia C, Dominguez P, Carrillo A, Bellon JM. Pediatric defibrillation after cardiac arrest: initial response and outcome. Crit Care 2006;10:R Samson RA, Nadkarni VM, Meaney PA, Carey SM, Berg MD, Berg RA. Outcomes of in-hospital ventricular fibrillation in children. N Engl J Med 2006;354: Lown B. Electrical reversion of cardiac arrhythmias. Br Heart J 1967;29: Ambler JJ, Deakin CD. A randomised controlled trial of the effect of biphasic or monophasic waveform on the incidence and severity of cutaneous burns following external direct current cardioversion. Resuscitation 2006;71: Joglar JA, Hamdan MH, Ramaswamy K, et al. Initial energy for elective external cardioversion of persistent atrial fibrillation. Am J Cardiol 2000;86: Boodhoo L, Mitchell AR, Bordoli G, Lloyd G, Patel N, Sulke N. DC cardioversion of persistent atrial fibrillation: a comparison of two protocols. Int J Cardiol 2007;114: Boos C, Thomas MD, Jones A, Clarke E, Wilbourne G, More RS. Higher energy monophasic DC cardioversion for persistent atrial fibrillation: is it time to start at 360 joules? Ann Noninvasive Electrocardiol 2003;8: Glover BM, Walsh SJ, McCann CJ, et al. Biphasic energy selection for transthoracic cardioversion of atrial fibrillation. The BEST AF Trial. Heart 2008;94: Rashba EJ, Gold MR, Crawford FA, Leman RB, Peters RW, Shorofsky SR. Efficacy of transthoracic cardioversion of atrial fibrillation using a biphasic, truncated exponential shock waveform at variable initial shock energies. Am J Cardiol 2004;94: Pinski SL, Sgarbossa EB, Ching E, Trohman RG. A comparison of 50-J versus 100-J shocks for direct-current cardioversion of atrial flutter. Am Heart J 1999;137: Alatawi F, Gurevitz O, White R. Prospective, randomized comparison of two biphasic waveforms for the efficacy and safety of transthoracic biphasic cardioversion of atrial fibrillation. Heart Rhythm 2005;2: Kerber RE, Kienzle MG, Olshansky B, et al. Ventricular tachycardia rate and morphology determine energy and current requirements for transthoracic cardioversion. Circulation 1992;85: Hedges JR, Syverud SA, Dalsey WC, Feero S, Easter R, Shultz B. Prehospital trial of emergency transcutaneous cardiac pacing. Circulation 1987;76: Barthell E, Troiano P, Olson D, Stueven HA, Hendley G. Prehospital external cardiac pacing: a prospective, controlled clinical trial. Ann Emerg Med 1988;17: Cummins RO, Graves JR, Larsen MP, et al. Out-of-hospital transcutaneous pacing by emergency medical technicians in patients with asystolic cardiac arrest. N Engl J Med 1993;328: Ornato JP, Peberdy MA. The mystery of bradyasystole during cardiac arrest. Ann Emerg Med 1996;27: Niemann JT, Adomian GE, Garner D, Rosborough JP. Endocardial and transcutaneous cardiac pacing, calcium chloride, and epinephrine in postcountershock asystole and bradycardias. Crit Care Med 1985;13: Quan L, Graves JR, Kinder DR, Horan S, Cummins RO. Transcutaneous cardiac pacing in the treatment of out-of-hospital pediatric cardiac arrests. Ann Emerg Med 1992;21: Dalsey WC, Syverud SA, Hedges JR. Emergency department use of transcutaneous pacing for cardiac arrests. Crit Care Med 1985;13: Knowlton AA, Falk RH. External cardiac pacing during in-hospital cardiac arrest. Am J Cardiol 1986;57: Ornato JP, Carveth WL, Windle JR. Pacemaker insertion for prehospital bradyasystolic cardiac arrest. Ann Emerg Med 1984;13: Stockwell B, Bellis G, Morton G, et al. Electrical injury during hands on defibrillation A potential risk of internal cardioverter defibrillators? Resuscitation 2009;80: Monsieurs KG, Conraads VM, Goethals MP, Snoeck JP, Bossaert LL. Semiautomatic external defibrillation and implanted cardiac pacemakers: understanding the interactions during resuscitation. Resuscitation 1995;30:
108 Publikacja przygotowana przez Europejską Radę Resuscytacji (ERC) przy współpracy z Polską Radą Resuscytacji (PRR). Tekst tłumaczony przez Polską Radę Resuscytacji. Wiedza i praktyka w zakresie resuscytacji krążeniowo-oddechowej to stale zmieniająca się dziedzina medycyny. W miarę rozwoju wiedzy oraz postępu w nauce i doświadczeniu klinicznym zmienia się w sposób ciągły również praktyka medycz na oraz sposób stosowania leków. Czytelnik tego podręcznika jest zobowiązany do zapoznania się z aktualnymi wiado mościami na temat przedstawionych sposobów postępowania i farmakoterapii ze szczególnym uwzględnieniem informacji producentów na temat dawek, czasu i drogi podawania oraz efektów ubocznych stosowanych leków. Na każdej z osób praktykujących medycynę resuscytacji spoczywa osobista odpowiedzialność za stosowane metody lecznicze, których uży cie powinno być oparte na gruntownej wiedzy i umiejętnościach praktycznych z zachowaniem niezbędnych warunków bez pieczeństwa własnego i pacjenta. Wydawcy oraz redaktorzy niniejszego opracowania nie ponoszą odpowiedzialności za szkody, które mogłyby być w jakikolwiek sposób związane z materiałem zawartym w tej książce. Bibliografia do wszystkich rozdziałów została w całości powtórzona za wydaniem oryginalnym. REDAKTOR NAUKOWY WYDANIA POLSKIEGO prof. dr hab. Janusz Andres TŁUMACZENIE Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Elżbieta Dobrowolska, Edyta Drab, Bartosz Frączek, Anna Jarosz, Piotr Kolęda, Paweł Krawczyk, Rafał Surmacz, Jurij Szymański, Grzegorz Zając KOREKTA MERYTORYCZNA Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Bartosz Frączek, Paweł Krawczyk ADIUSTACJA I KOREKTA WYDAWNICZA Danuta Ambrożewicz PROJEKT OKŁADKI Polska Rada Resuscytacji wg plakatu V Międzynarodowego Kongresu Polskiej Rady Resuscytacji autorstwa Mieczysława Górowskiego Publikację wydano ze środków Polskiej Rady Resuscytacji. Copyright by European Resuscitation Council (ERC), 2010 Copyright for the Polish edition by Polska Rada Resuscytacji, Kraków 2010 Copyright for the Polish translation by Polska Rada Resuscytacji, Kraków 2010 Wszystkie prawa zastrzeżone. Żadna część poniższej publikacji nie może być kopiowana i przechowywana w jakimkol wiek mechanicznym systemie kopiowania danych, włączając fotokopie, kserokopie, nagrania i inne, bez uprzedniej pisem nej zgody PRR (dotyczy terenu Rzeczpospolitej Polskiej). Wszystkie prośby o możliwość wykorzystania materiałów zawartych w tej publikacji należy kierować do ERC. ISBN KOORDYNATOR STRONY ORAZ WERSJI ELEKTRONICZNEJ Wytycznych resuscytacji 2010 Wiesław Pyrczak prc@prc.krakow.pl ADRES DO KORESPONDENCJI ADRES DO KORESPONDENCJI W POLSCE ERC Secretariat VZW Polska Rada Resuscytacji Drie Eikenstraat 661 ul. Radziwiłłowska 4, Kraków BE-2650 EDEGEM tel fax Belgium biuro@prc.krakow.pl tel fax Koordynator kursów info@erc.edu Tomasz Galewicz kursy@prc.krakow.pl SKŁAD I PRZYGOTOWANIE DO DRUKU FALL ul. Garczyńskiego 2, Kraków tel ; fall@fall.pl
109 Zaawansowane zabiegi resuscytacyjne 4 u osób dorosłych Charles D. Deakin a,1, Jerry P. Nolan b,*,1, Jasmeet Soar c, Kjetil Sunde d, Rudolph W. Koster e, Gary B. Smith f, Gavin D. Perkins f a Cardiothoracic Anaesthesia, Southampton General Hospital, Southampton, UK b Anaesthesia and Intensive Care Medicine, Royal United Hospital, Bath, UK c Anaesthesia and Intensive Care Medicine, Southmead Hospital, Bristol, UK d Surgical Intensive Care Unit, Oslo University Hospital Ulleval, Oslo, Norway e Department of Cardiology, Academic Medical Center, Amsterdam, The Netherlands f Critical Care and Resuscitation, University of Warwick, Warwick Medical School, Warwick, UK Podsumowanie zmian od Wytycznych 2005 * Corresponding author. jerry.nolan@btinternet.com ( J.P. Nolan). 1 These individuals contributed equally to this manuscript and are equal first co-authors. Najważniejsze zmiany w Wytycznych 2010 dotyczące zaawansowanych zabiegów resuscytacyjnych (Advanced Life Support ALS) u osób dorosłych obejmują: Zwiększony nacisk na znaczenie wysokiej jakości i minimalizowania przerw w uciśnięciach klatki piersiowej podczas wszystkich interwencji ALS. Uciśnięcia klatki piersiowej przerywa się na krótko, jedynie by umożliwić istotne interwencje. Zwiększony nacisk na zastosowanie systemu obserwuj i reaguj ( track and trigger systems ), by uchwycić pogorszenie się stanu zdrowia pacjenta i umożliwić wdrożenie leczenia w celu prewencji wewnątrzszpitalnego zatrzymania krążenia. Zwiększenie świadomości niepokojących objawów związanych z ryzykiem nagłej śmierci sercowej poza szpitalem. Usunięcie zalecenia dotyczącego zdefiniowanego okresu RKO przed defibrylacją w przebiegu niezauważonego przez służby ratownicze pozaszpitalnego zatrzymania krążenia. Kontynuację uciśnięć klatki piersiowej podczas ładowania defibrylatora pozwoli to zminimalizować przerwę przed defibrylacją. Mniejsze znaczenie uderzenia przedsercowego. Zastosowanie do trzech pod rząd defibrylacji w przypadku migotania komór/częstoskurczu komorowego bez tętna (VF/VT) występujących podczas cewnikowania serca lub we wczesnym okresie pooperacyjnym w kardiochirurgii. Nie zaleca się już podawania leków przez rurkę intubacyjną jeżeli nie można zapewnić dostępu dożylnego, leki należy podawać doszpikowo (intraosseous io). W leczeniu zatrzymania krążenia w mechanizmie VF/ VT 1 mg adrenaliny należy podać po trzeciej defibrylacji, po ponownym podjęciu uciśnięć klatki piersiowej, a następnie co 3 5 minut (co drugą pętlę RKO). Amiodaron w dawce 300 mg jest podawany także po trzeciej defibrylacji. Nie zaleca się już rutynowego stosowania atropiny w leczeniu asystolii lub aktywności elektrycznej bez tętna (Pulseless Electrical Activity PEA). Zmniejszony nacisk na wczesną intubację, z wyjątkiem sytuacji, gdy wykonywana jest przez dobrze wyszkolone osoby, z minimalną przerwą w uciśnięciach klatki piersiowej. Zwiększony nacisk na zastosowanie kapnografii w celu potwierdzenia i ciągłego monitorowania położenia rurki dotchawiczej, jakości RKO oraz umożliwienia wczesnego rozpoznania powrotu spontanicznego krążenia (Return of Spontaneous Circulation ROSC). Zwrócenie uwagi na potencjalne znaczenie obrazowania ultrasonograficznego podczas ALS. Rozpoznanie potencjalnej szkodliwości hiperoksemii po ROSC. Po powrocie spontanicznego krążenia, jeśli można wiarygodnie monitorować saturację krwi tętniczej (SaO 2 ) (za pomocą pulsoksymetrii i/lub gazometrii krwi tętniczej), wdechowe stężenie tlenu należy miareczkować tak, by osiągnąć SaO %. Zwiększony nacisk i uszczegółowienie leczenia zespołu objawów występujących po zatrzymaniu krążenia syndrom poresuscytacyjny (SP) (post-cardiac arrest syndrome). Rozpoznanie, że wdrożenie kompleksowego, przejrzystego protokołu leczenia pacjentów po zatrzymaniu krążenia może zwiększyć przeżywalność po ROSC. Zwiększony nacisk na zastosowanie pierwotnej przezskórnej interwencji wieńcowej u określonej grupy pacjentów z zachowanym krążeniem po ROSC (włączając pacjentów w stanie śpiączki). Rewizję zaleceń dotyczących kontroli poziomu glikemii: u osób dorosłych po ROSC powinno się wdrożyć leczenie, gdy poziom glukozy we krwi jest >10 mmol/l (>180 mg/dl). Jednocześnie powinno się unikać hipoglikemii. Zastosowanie terapeutycznej hipotermii u pacjentów pozostających w stanie śpiączki po zatrzymaniu krążenia zarówno w rytmach nie do defibrylacji, jak i w rytmach do defibrylacji. Zauważa się niższy poziom dowodów naukowych w przypadku zastosowania hipotermii w grupie pacjentów z zatrzymaniem krążenia w rytmach nie do defibrylacji.
110 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 109 Stwierdzenie, że wiele akceptowanych dotychczas czynników przewidujących niekorzystny wynik leczenia pacjentów pozostających w stanie śpiączki po NZK jest niewiarygodnych, szczególnie gdy zastosowano terapeutyczną hipotermię. 4a Zapobieganie wewnątrzszpitalnemu zatrzymaniu krążenia Wczesne rozpoznanie pogorszenia stanu pacjenta i prewencja zatrzymania krążenia stanowią pierwsze ogniwo łańcucha przeżycia 1. W przypadku wewnątrzszpitalnego zatrzymania krążenia mniej niż 20% pacjentów przeżyje do momentu wypisania ze szpitala 2-4. Prewencja wewnątrzszpitalnego zatrzymania krążenia wymaga edukacji personelu medycznego, monitorowania pacjentów, rozpoznania pogorszenia stanu pacjenta oraz stworzenia systemu wzywania pomocy i skutecznej odpowiedzi na jej wezwanie 5. Problem Zatrzymanie krążenia występujące u pacjentów przebywających na oddziałach bez monitorowania nie jest zwykle ani zdarzeniem nagłym czy nieprzewidywalnym, ani spowodowanym przyczynami pierwotnie kardiologicznymi 6. W tej grupie pacjentów występuje zwykle wolne i postępujące pogorszenie stanu ogólnego, włączając w to hipoksemię i hipotensję, które pozostają niezauważone przez personel medyczny lub są rozpoznane, ale nieadekwatnie leczone 7-9. U wielu z tych pacjentów dochodzi do niemonitorowanego zatrzymania krążenia, a leżący u jego podstaw rytm jest zwykle nie do defibrylacji 3,10. W takim przypadku przeżywalność pacjentów do wypisania ze szpitala jest niska 2,4,10. W dokumentacji medycznej pacjentów, u których doszło do NZK albo którzy nieoczekiwanie wymagali przyjęcia na Oddział Intensywnej Terapii (OIT), często znajdują się dowody świadczące o braku rozpoznania lub braku leczenia pojawiających się zaburzeń oddychania i krążenia 6,8, Badanie ACADEMIA wykazało takie dane w przypadku 79% zatrzymań krążenia, 55% zgonów i 54% nieoczekiwanych przyjęć na OIT 8. Wczesne i skuteczne leczenie ciężko chorych pacjentów może zapobiec niektórym zatrzymaniom krążenia, zgonom i nieprzewidzianym przyjęciom na OIT. Kilka badań pokazuje, że tylko jedna trzecia spośród pacjentów, u których błędnie rozpoznano NZK, w rezultacie umiera Istota niedostatecznego rozpoznania i leczenia pacjentów z pogorszeniem stanu zdrowia Niedostateczna opieka często obejmuje: rzadką, późną lub niekompletną ocenę podstawowych parametrów życiowych; brak wiedzy dotyczącej prawidłowych ich wartości; niedostatecznie dobre zaprojektowanie kart obserwacji; niska czułość i swoistość systemów obserwuj i reaguj ( track and trigger ); zbyt mała ilość personelu medycznego a przez to brak możliwości zaawansowanego monitorowania pacjentów, lepszej nad nimi opieki Częstym problemem jest nieskuteczne leczenie zaburzeń drożności dróg oddechowych, oddychania i krążenia, niewłaściwe zastosowanie tlenoterapii, słaba komunikacja, brak pracy zespołowej, niewystarczające wdrażanie protokołów ograniczających leczenie 7,14,29. Edukacja dotycząca postępowania w stanach nagłych Liczne badania wykazały, że zarówno personelowi lekarskiemu, jak i pielęgniarskiemu brakuje wiedzy i umiejętności dotyczących postępowania w sytuacjach nagłych 30. Dotyczy to np. tlenoterapii 31, równowagi płynowo-elektrolitowej 32, terapii przeciwbólowej 33, zagadnień związanych ze zgodą na procedury medyczne 34, pulsoksymetrii 35,36 czy dawek leków 37. Studia medyczne niedostatecznie przygotowują młodych lekarzy do pracy, niewystarczajaco uczą podstawowych zagadnień związanych z patofizjologią i medycyną, stanów nagłych 38. Jest potrzeba zwrócenia uwagi na szkolenia dotyczące stanów nagłych zarówno studentów medycyny, jak i młodych lekarzy 39,40. Nie ma, niestety, danych przekonujących, że umiejętności i wiedza starszego personelu medycznego w tym zakresie są lepsze 41,42. Często brakuje pewności i umiejętności podejmowania decyzji w stanach nagłych, a usystematyzowany sposób oceny krytycznie chorych pacjentów jest rzadko stosowany 43. Edukacja personelu medycznego jest istotnym elementem implementacji systemu zapobiegania zatrzymaniu krążenia 44. Nie ma jednak randomizowanych badań z grupą kontrolną określających wpływ poszczególnych interwencji edukacyjnych na poprawę wyników leczenia pacjentów, takich jak: wcześniejsze rozpoznanie lub leczenie pacjenta zagrożonego zatrzymaniem krążenia lub oddychania. W badaniu australijskim praktycznie cała poprawa, czyli zmniejszenie częstości występowania wewnątrzszpitalnego zatrzymania krążenia, nastąpiła w fazie edukacji w związku z implementacją zespołów resuscytacyjnych (MET) 45,46. W badaniach pochodzących z australijskich i amerykańskich szpitali, gdzie już działały zespoły szybkiego reagowania, wprowadzenie edukacji dotyczącej określonych kryteriów wzywania tych zespołów doprowadziło do zwiększenia liczby uzasadnionych przyjęć na OIT oraz zmniejszenia liczby zatrzymań krążenia na innych oddziałach Badanie ze Zjednoczonego Królestwa wykazało, że w dwóch szpitalach po wprowadzeniu ustandaryzowanego programu nauczania zmniejszyła się ilość wezwań do zatrzymania krążenia, przy wzroście wezwań do pacjentów zagrożonych jego wystąpieniem. Towarzyszyło temu zmniejszenie liczby rzeczywistych zatrzymań krążenia oraz zwiększenie ilości ROSC, jak i przeżywalności do wypisu ze szpitala 50,51. Monitorowanie i rozpoznawanie pacjenta w ciężkim stanie Objawy kliniczne w stanach nagłych, niezależnie od przyczyny wyjściowej, są podobne, ponieważ odzwierciedlają niewydolność układu oddechowego, krążenia i nerwowego. Zaburzenia procesów fizjologicznych są częste u pacjentów oddziałów ogólnych 52, ale mimo to pomiary i rejestracja ważnych zmian w tym zakresie zdarza się znacznie rzadziej, niż jest to pożądane 6,8,13,16,24,53,54. W celu ułatwienia wczesnego wykrycia ciężkiego schorzenia, u każdego pacjenta powinno się zaplanować schemat monitorowania podstawowych parametrów życiowych okre- 4
111 110 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 ślający, jakie parametry i jak często powinny być oceniane 26. Aktualnie w wielu szpitalach, w celu identyfikacji pacjentów wymagających poszerzonego monitorowania, leczenia lub konsultacji specjalistycznej, stosowane są skale wczesnego ostrzegania (Early Warning Scores EWS) lub kryteria wezwania zespołu resuscytacyjnego (strategia track and trigger ) 13,24, Systemy te zostały wprowadzone, by zwiększyć częstości przeprowadzania oceny podstawowych parametrów życiowych u pacjentów 54,58,59. Kryteria wezwania lub systemy obserwuj i reaguj obejmują obserwację pojedynczych lub kilku parametrów, skale sumujące punkty dotyczące poszczególnych zmiennych lub kombinacje powyższych 60. Sumaryczny, zbalansowany system obserwuj i reaguj oferuje stopniowe podnoszenie poziomu opieki, podczas gdy systemy oparte na ocenie pojedynczych parametrów wyzwalają działanie wszystko albo nic. W większości przypadków brak jest przekonujących danych wskazujących, że poszczególne systemy posiadają akceptowalną dokładność pozwalającą na zastosowanie ich w założonych celach. Ich niska czułość oznacza, że znaczna liczba pacjentów zagrożonych wystąpieniem zatrzymania krążenia może zostać przeoczona 61,62. W celu identyfikacji pacjentów zagrożonych poważnym ryzykiem pogorszenia stanu zdrowia, wystąpieniem zatrzymania krążenia lub zgonu, szpitale powinny stosować walidowane dla określonej populacji pacjentów systemy zarówno podczas ich przyjęcia, jak i pobytu w szpitalu. Zmiany dotyczące fizjologicznych parametrów oceniane pojedynczo lub sumarycznie mogą, ze zmienną czułością i swoistością, służyć przewidywaniu wystąpienia zatrzymania krążenia 9,13,15,63,64, zgonu w szpitalu 22,23,65-82 i nieplanowanych przyjęć na OIT 15,80,83. Różniące się pomiędzy szpitalami kryteria przyjęcia pacjentów na OIT czynią nieplanowane przyjęcia na OIT mniej użytecznym punktem końcowym badań. Jak można się spodziewać, większa ilość nieprawidłowych parametrów zwiększa prawdopodobieństwo zgonu 11,15,20,63,77, Najlepsze zestawienie tych zmiennych i ich wartości odcięcia pozwalające na wczesne prognozowanie jest nieznane. Najlepsze wartości prognostyczne osiągają sumaryczne, zbalansowane systemy oceny zawierające następujące parametry: czynność serca (Heart Rate HR), ilość oddechów (Respiratory Rate RR), skurczowe ciśnienie krwi (Systolic Blood Pressure SBP), skalę AVPU (Alert, Vocalizing, Pain, Unresponsive), temperaturę, wiek, wysycenie tlenem 22,61. Spośród pojedynczych parametrów stosowanych w systemach obserwuj i reaguj punkty odcięcia dla HR <35 i >140/min, RR <6 i >32/min oraz SBP <80 mm Hg osiągają najlepsze wartości prognostyczne 23. Wzięcie pod uwagę wieku pacjenta poprawia wartości prognostyczne zarówno sumarycznych, jak i opartych na jednym parametrze systemów oceny 77. Sumaryczne, zbalansowane systemy oceny wydają się posiadać relatywnie stały porządek przedstawianych wartości (rank order of performance) 92. Nowo skonstruowane sumaryczne, zbalansowane systemy oceny lepiej różnicują pacjentów, prognozując 24- -godzinną śmiertelność przy użyciu skal wczesnego ostrzegania (Early Warning Score EWS) 92. Właściwie zaprojektowana karta oceny podstawowych czynności życiowych czy zastosowanie odpowiedniej technologii mogą mieć istotną rolę w wykrywaniu pogorszenia stanu pacjenta i wymagają dalszych badań 21,93,94. Wzywanie pomocy Tradycyjną reakcją na zatrzymanie krążenie jest aktywacja personelu szpitalnego (zespół resuscytacyjny), który zajmuje się pacjentem po wystąpieniu zatrzymania krążenia. Zespół ten wprowadzony został, by poprawić przeżywalność w zatrzymaniu krążenia w okolicznościach, kiedy żadne specjalne zespoły, działające w tym celu, nie istniały 95. Obecnie kwestionuje się rolę zespołu resuscytacyjnego. W jednym małym badaniu do wypisu ze szpitala przeżyli jedynie pacjenci, u których do powrotu spontanicznego krążenia doszło przed przybyciem zespołu resuscytacyjnego 96. Po zestawieniu tego ze słabym wynikiem leczenia wewnątrzszpitalnego zatrzymania krążenia, obecnie nacisk kładzie się na wczesne rozpoznanie i leczenie krytycznie chorych pacjentów w celu prewencji zatrzymania krążenia. Personelowi pielęgniarskiemu lub młodym lekarzom często trudno jest poprosić o pomoc lub wdrożyć zaawansowane leczenie z powodu ryzyka zostania skrytykowanym. Szpitale powinny stworzyć warunki, w których cały personel jest upoważniony do wezwania pomocy, jak również jest przeszkolony w zakresie stosowania specjalnych narzędzi zapewniających skuteczną komunikację, takich jak: RSVP (Reason-Story-Vital Signs-Plan) 97 lub SBAR (Situation- -Background-Assessment-Recommendation) 98. Postępowanie z pacjentem w ciężkim stanie Pacjetów w ciężkim stanie lub tym stanem zagrożonych zazwyczaj leczy zespół resuscytacyjny (Medical Emergency Team MET), zespół szybkiego reagowania (Rapid Response Team RRT) lub konsultacyjny zespół intensywnej terapii (Critical Care Outreach Team CCOT) Zespoły te współistnieją lub zamieniły tradycyjne zespoły resuscytacyjne, typowo leczące pacjentów, u których już doszło do zatrzymania krążenia; zespoły MET/RRT zwykle składają się z personelu lekarskiego i pielęgniarskiego pracującego na oddziałach intensywnej terapii i oddziałach ogólnych. Zespoły te reagują w przypadku stwierdzenia konkretnych kryteriów wezwania. Zespoły CCOT, popularne w Zjednoczonym Królestwie, są zwykle złożone z personelu pielęgniarskiego działającego pojedynczo lub w zespołach 60. Działanie to przybiera różne formy począwszy od jednej pielęgniarki po wielodyscyplinarne zespoły dostępne przez 24 godziny 7 dni w tygodniu. Wezwania zespołów MET/RRT/COOT może dokonać każda osoba z personelu zajmującego się pacjentem. W niektórych szpitalach zachęca się, by, jeśli to konieczne, zespół mógł być wezwany również przez rodzinę lub przyjaciół pacjenta Interwencje wykonywane przez zespół często obejmują proste czynności, takie jak rozpoczęcie tlenoterapii czy dożylna podaż płynów Jakkolwiek analiza post hoc badania MERIT sugeruje, że prawie wszystkie wezwania zespołu resuscytacyjnego wymagały interwencji o zaawansowanym charakterze 110. Opisywane są całodobowe strategie działania zespołów resuscytacyjnych, co może sugerować, że identyfikacja i reagowanie na nagłe zdarzenia mogą nie być jednolite w ciągu doby 111,112. Analiza efektu wdrożenia systemów MET/RRT/ CCOT na wynik leczenia pacjentów jest trudna z powo-
112 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 111 du złożonej natury podejmowanych interwencji. W czasie trwania wielu badań nad działaniem zespołów szybkiego reagowania prowadzono międzynarodowe inicjatywy ukierunkowane na poprawę innych aspektów dotyczących bezpieczeństwa pacjenta, np. zakażeń wewnątrzszpitalnych, wczesnego leczenia sepsy i lepszego postępowania medycznego, które mogły mieć potencjalny wpływ na stan zdrowia pacjentów oraz korzystny efekt na redukcję występowania wewnątrzszpitalnych zatrzymań krążenia i zgonów. Dodatkowo zwiększenie nacisku na poprawę opieki paliatywnej oraz niepodejmowanie decyzji o rozpoczynaniu resuscytacji (Do Not Attempt Resuscitation DNAR) może mieć także wpływ na ilość wezwań dotyczących zatrzymania krążenia. Dostępne obecnie badania naukowe nie uwzględniają wspomnianych czynników zaburzających. Pomimo to liczne badania jednoośrodkowe donoszą o zmniejszeniu liczby zatrzymań krążenia po implementacji systemów RRT/MET 45,47,107,111, Jakkolwiek badanie MERIT, dobrze skonstruowane klastrowo randomizowane z grupą kontrolną, skupiające 23 szpitale 24, nie wykazało zmniejszenia występowania zatrzymania krążenia po wprowadzeniu MET, analizując wyniki w grupach wyodrębnionych zgodnie z zaplanowanym leczeniem. W badaniu, obejmującym 6-miesięczny okres wdrożenia MET na oddziałach ogólnych, nie udało się wykazać różnicy pomiędzy szpitalami wdrażającymi interwencje a grupą kontrolną w redukcji łącznego wyniku leczenia, na który składały się (a) wystąpienie zatrzymania krążenia bez wcześniejszych zaleceń niepodejmowania resuscytacji (Not For Resuscitation NFR), (b) nieplanowanych przyjęć na OIT oraz (c) niespodziewanych zgonów (bez występujących wcześniej decyzji NFR). Obydwie grupy, kontrolna i stosująca zespoły MET, zademonstrowały poprawę wyników leczenia w zestawieniu z wartościami sprzed wdrożenia interwencji. Analiza post hoc badania MERIT wykazała zmniejszenie występowania zatrzymania krążenia i niespodziewanych zgonów, co wiązało się ze zwiększoną liczbą wezwań MET 126. Kilka innych badań także nie wykazało redukcji w ilości zatrzymań krążenia związanych z wprowadzeniem systemów RRT/MET 105,106,108,109, Badanie przeprowadzone w jednym ośrodku, gdzie stosowano EWS, wykazało zwiększenie częstości epizodów zatrzymania krążenia wśród pacjentów z wyższą punktacją EWS w porównaniu z grupą podobnie ocenianą w EWS przed wprowadzeniem tej interwencji 56. Ostatnie metaanalizy wykazały, że wdrożenie systemów RRT/MET było związane z redukcją zatrzymań krążenia występujących poza OIT, lecz nie wykazano zmniejszenia śmiertelności wewnątrzszpitalnej 131. Właściwe umieszczenie pacjentów W warunkach idealnych najciężej chorych pacjentów powinno się przyjmować na oddziały zapewniające najlepszy nadzór, opiekę pielęgniarską oraz najwyższy poziom wspomagania życiowo ważnych narządów. Tak się często dzieje, chociaż niektórzy pacjenci zostają skierowani niewłaściwie 132. Organizacje międzynarodowe przygotowały definicje różnych poziomów leczenia i opracowały kryteria przyjęcia i wypisu dla oddziałów wzmożonego nadzoru i oddziałów intensywnej terapii 133,134. Obsada personalna Liczebność personelu w szpitalu jest zwykle najniższa w nocy i w weekendy. Może to wpływać na jakość monitorowania pacjentów, leczenie i wyniki końcowe. Dane pochodzące z US National Registry of CPR Investigators wykazały, że wyniki leczenia wewnątrzszpitalnego zatrzymania krążenia mającego miejsce w nocy lub podczas weekendu są gorsze 135. Przyjęcia na oddziały ogólne po godzinie albo do szpitala w weekendy 137 wiążą się z wyższą śmiertelnością. Ryzyko zgonu w szpitalu w przypadku pacjentów wypisywanych z OIT na oddziały ogólne w nocy jest wyższe niż dla tych, którzy są wypisywani w dzień albo na oddziały wzmożonego nadzoru 138,139. Kilka badań wykazało, że zwiększona liczba personelu pielęgniarskiego wiąże się ze spadkiem ilości zatrzymań krążenia, niepowodzeń w jego leczeniu, jak również częstości występowania zapalenia płuc, wstrząsu i zgonu 25, 140, 141. Decyzje dotyczące resuscytacji Decyzje o podjęciu, kontynuowaniu, zakończeniu resuscytacji są oparte na równowadze pomiędzy ryzykiem, korzyścią i ciężarem podjęcia tej decyzji dla pacjenta, jego rodziny i członków zespołu leczącego. Istnieją okoliczności, kiedy resuscytacja nie jest właściwa i nie powinna być podejmowana. Należy rozważyć decyzję o niepodejmowaniu resuscytacji (DNAR), jeżeli pacjent: nie życzy sobie podejmowania RKO, nie przeżyje zatrzymania krążenia nawet, gdy resuscytacja zostanie podjęta. Personel szpitalny często nie rozważa, czy przystępowanie do resuscytacji jest właściwe, a podejmowanie zabiegów resuscytacyjnych w nierokujących przypadkach (uporczywa terapia) jest powszechne 142. Nawet jeśli jest oczywiste, że dojdzie do NZK czy zgonu, rzadko podejmowane są decyzje dotyczące wskazań do resuscytacji u danego pacjenta 8. W wielu krajach europejskich nie ma formalnych regulacji dotyczących protokołu DNAR, a praktyka konsultowania decyzji z pacjentami jest różna 143,144. Postęp w zakresie wiedzy i umiejętności w resuscytacji, a także podejmowanie decyzji o nieprzystępowaniu do resuscytacji powinny poprawić jakość dostępnej opieki nad pacjentami i zapobiec daremnym próbom resuscytacji (zob. rozdział 10) 145. Zespoły resuscytacyjne mogą istotnie ułatwić podejmowanie decyzji dotyczących problemów końca życia i niepodejmowania resuscytacji (DNAR) 142, Wytyczne dotyczące zapobiegania wewnątrzszpitalnemu zatrzymaniu krążenia Szpitale powinny wprowadzić system opieki obejmujący: (a) szkolenie personelu medycznego dotyczące objawów świadczących o pogarszaniu się stanu ogólnego pacjenta i zasadności wdrożenia szybkiego działania w celu jego poprawy, (b) właściwe i regularne monitorowanie podstawowych parametrów życiowych pacjenta, (c) przejrzyste wytyczne (np. poprzez kryteria wezwania lub skale wczesnego ostrzegania), by pomóc personelowi medycznemu we wczesnym rozpoznaniu pogorszenia stanu pacjenta, (d) prosty, jednolity system wzywania pomocy oraz (e) właściwą i zastosowaną o czasie odpowiedź na wezwanie pomocy 5. Poniższe 4
113 112 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 strategie mogą zapobiec możliwym do uniknięcia wewnątrzszpitalnym zatrzymaniom krążenia: 1. Opiekę nad pacjentami krytycznie chorymi lub zagrożonymi pogorszeniem się stanu zdrowia należy prowadzić na właściwych oddziałach, gdzie jej poziom jest dostosowany do ciężkości stanu chorego. 2. Krytycznie chorzy pacjenci potrzebują regularnej obserwacji: każdy pacjent powinien posiadać udokumentowany plan monitorowania, definiujący, jak często i jakie parametry życiowe powinny być monitorowane w zależności od ciężkości stanu pacjenta, prawdopodobieństwa pogorszenia jego stanu i wystąpienia zatrzymania krążenia. Ostatnio zaleca się monitorowanie prostych fizjologicznych zmiennych, obejmujących tętno, ciśnienie tętnicze, częstość oddychania, poziom świadomości, temperaturę i saturację (SpO 2 ) 26, W celu identyfikacji pacjentów w krytycznym stanie i/lub zagrożonych pogorszeniem stanu ogólnego oraz zatrzymaniem krążenia należy zastosować system obserwuj i reaguj (track and trigger) (kryteria wezwania lub systemy wczesnego ostrzegania). 4. Należy stosować system karty pacjenta umożliwiający regularne pomiary i dokumentowanie wartości podstawowych parametrów życiowych oraz skal wczesnego ostrzegania jeśli są używane. 5. Należy opracować jasne i swoiste reguły postępowania klinicznego w odpowiedzi na nieprawidłowości parametrów fizjologicznych pacjenta, oparte na systemie obserwuj i reaguj. Powinny one zawierać zalecenia dotyczące dalszego leczenia i określać zakres obowiązków personelu lekarskiego i pielęgniarskiego. 6. W szpitalu powinien obowiązywać jasno określony schemat postępowania w stanach nagłych. Może to być wezwanie zespołu konsultującego lub zespołu resuscytacyjnego (np. MET, RRT), zdolnego do adekwatnego w czasie działania w odpowiedzi na nagłe pogorszenie stanu ogólnego identyfikowanego za pomocą systemu obserwuj i reaguj lub innych wskaźników. Zespół musi być dostępny 24 godziny na dobę i posiadać w swoim składzie osoby z odpowiednimi umiejętnościami postępowania w stanach nagłych. 7. Należy przeszkolić cały personel medyczny w zakresie rozpoznawania, monitorowania i postępowania z pacjentami w stanie ciężkim. Dotyczy to również działań podejmowanych podczas oczekiwania na bardziej doświadczoną pomoc. Należy upewnić się, że personel zna swoją rolę, działając w systemie szybkiej odpowiedzi. 8. Szpitale muszą umożliwić personelowi wszystkich dyscyplin wezwanie pomocy, gdy rozpoznają pacjenta zagrożonego pogorszeniem stanu zdrowia lub wystąpieniem zatrzymania krążenia. Personel powinien być przeszkolony w użyciu uporządkowanych narzędzi komunikacyjnych w celu skutecznego przekazania informacji pomiędzy lekarzami, pielęgniarkami i innymi pracownikami ochrony zdrowia. 9. Należy rozpoznać pacjentów, u których zatrzymanie krążenia i oddychania jest przewidywalnym zdarzeniem związanym z końcem życia i u których podejmowanie RKO jest niewłaściwe, a także zidentyfikować pacjentów, którzy nie życzą sobie wdrożenia RKO. Szpitale powinny posiadać strategię dotyczącą DNAR, opartą na krajowych wytycznych, zrozumiałą dla całego personelu medycznego. 10. Należy zapewnić audyt przypadków zatrzymania krążenia, fałszywych rozpoznań zatrzymania krążenia, nieoczekiwanych zgonów i nieplanowanych przyjęć na OIT, w oparciu o dostępne bazy danych. Audytem powinny zostać również objęte zdarzenia poprzedzające zatrzymanie krążenia oraz wdrożone postępowanie. Zapobieganie pozaszpitalnej nagłej śmierci sercowej Choroba wieńcowa jest najczęstszą przyczyną nagłej śmierci sercowej (Sudden Cardiac Death SCD). Przyczynami większości pozostałych epizodów SCD są kardiomiopatia niezwiązana z niedokrwieniem oraz wady zastawkowe. Niewielki odsetek SCD jest spowodowany wrodzonymi zaburzeniami (np. zespół Brugadów, kardiomiopatia przerostowa) lub wrodzonymi chorobami serca. Większość przypadków SCD jest poprzedzona wywiadem dotyczącym choroby serca i objawami ostrzegającymi, najczęściej bólem w klatce piersiowej, około godziny przed zatrzymaniem krążenia 150. U pacjentów z rozpoznaną chorobą serca utrata przytomności (z obecnością lub bez objawów prodromalnych szczególnie, gdy występowały ostatnio lub nawracają) jest niezależnym czynnikiem ryzyka dla zwiększonego ryzyka zgonu Ból w klatce piersiowej pojawiający się wyłącznie przy wysiłku oraz uczucie kołatania serca związane wyłącznie z utratą przytomności są związane z kardiomiopatią przerostową, nieprawidłowościami naczyń wieńcowych, zespołem Wolffa Parkinsona White a i arytmogenną kardiomiopatią prawej komory. Zdrowe dotychczas dzieci lub młodzi dorośli, dotknięci SCD, mogli także wykazywać objawy niepokojące (np. zasłabnięcie/utrata przytomności, ból w klatce piersiowej i kołatanie serca), które powinny były zaalarmować pracowników ochrony zdrowia i skłonić do poszukiwania opinii eksperta w celu zapobieżenia zatrzymaniu krążenia Dzieci i młodych dorosłych, prezentujących charakterystyczne objawy utraty przytomności z towarzyszącymi zaburzeniami rytmu, należy poddać specjalistycznej ocenie kardiologicznej, która powinna obejmować wykonanie EKG, a w większości przypadków także echokardiografii oraz testu wysiłkowego. Charakterystyczne cechy dla utraty przytomności wywołanej zaburzeniami rytmu obejmują: zasłabnięcie w ułożeniu na wznak, podczas lub po wysiłku, bez lub z krótko występującymi objawami prodromalnymi, nawracające epizody oraz (w pojedynczych przypadkach) dodatni wywiad rodzinny w kierunku nagłych zgonów. Dodatkowo dolegliwości bólowe o charakterze nieopłucnowym, kołatanie serca związane z utratą przytomności, drgawki (oporne na leczenie, występujące nocą, wywoływane wysiłkiem, utratą przytomności lub hałasem), tonięcie osoby umiejącej pływać wszystkie powinny wzbudzać podejrzenie zwiększonego ryzyka. Systematyczna ocena przeprowadzona w klinice specjalizującej się w opiece nad oso-
114 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 113 bami zagrożonymi SCD jest zalecana członkom rodzin osób, które zmarły w młodym wieku z powodu SCD oraz tym ze znanym zaburzeniem zwiększającym ryzyko wystąpienia SCD 151, Rodzinny wywiad dotyczący utraty przytomności lub SCD oraz związanego z tym kołatania serca, jak również utrata przytomności w ułożeniu na wznak, utrata przytomności związana z wysiłkiem i stresem emocjonalnym są bardziej powszechne u pacjentów z zespołem wydłużonego QT (Long QT Syndrome LQTS) 176. U osób starszych 177,178 brak nudności i wymiotów przed utratą przytomności oraz nieprawidłowości w zapisie EKG są niezależnymi czynnikami zwiastującymi utratę przytomności z powodu arytmii. Niewytłumaczalne utonięcia oraz utonięcia dobrze pływających osób mogą być spowodowane LQTS lub katecholaminergicznym, wielokształtnym częstoskurczem komorowym (Catecholaminergic Polymorphic Ventricular Tachycardia CPVT) 179. Istnieje związek pomiędzy LQTS i fenotypem drgawek 180,181. Opublikowane zostały wytyczne zalecające badania przesiewowe w grupie sportowców wyczynowych, w celu identyfikacji osób zagrożonych wystąpieniem nagłego zgonu b Resuscytacja przedszpitalna Personel systemu ratownictwa medycznego Systemy ratownictwa medycznego w Europie różnią się między sobą zarówno w strukturze, jak i w działaniu. Niektóre kraje rozwinęły przedszpitalne systemy oparte niemal wyłącznie na ratownikach i technikach medycznych (Emergency Medical Technician EMT), podczas gdy w innych krajach w mniejszym lub większym stopniu zatrudniani są lekarze. Obecność lekarzy podczas resuscytacji dorosłych w porównaniu do resuscytacji przeprowadzanych przez ratowników wiąże się z większą zgodnością działania z wytycznymi 183,184, ponadto lekarze w niektórych systemach skuteczniej wykonują zaawansowane zabiegi resuscytacyjne 183, Porównania w obrębie jednego systemu ratownictwa uwidaczniają sprzeczne dane, tzn. niektóre badania wykazują poprawę przeżywalności do wypisu ze szpitala, gdy lekarz jest członkiem zespołu resuscytacyjnego , inne wykazują brak różnic zarówno w krótko, jak i długoterminowych wynikach leczenia 183,189,191, , a jedno wykazało nawet niższą przeżywalność zatrzymania krążenia, gdy lekarz był częścią zespołu resuscytacyjnego 199. Badania porównujące wyniki resuscytacji pomiędzy systemami zatrudniającymi lekarzy i inny personel medyczny są trudne do interpretacji z powodu skrajnie wysokiej zmienności w systemach, niezależnie od składu personelu medycznego 200. Chociaż niektóre badania dokumentują wyższą przeżywalność zatrzymania krążenia w systemie, w którym pracują doświadczeni lekarze 186,188, , w zestawieniu z zespołami nielekarskimi 201,202,204,205, to inne badania nie wykazały różnic pomiędzy systemami niezależnie od składu zespołu 206,207. Istnieją również doniesienia o dobrze zorganizowanych systemach opartych na wyszkolonych ratownikach bez lekarza, w których osiągana jest wysoka przeżywalność 200. Biorąc powyższe pod uwagę, włączenie bądź wyłączenie lekarzy z personelu medycznego działającego w systemach ratownictwa w przedszpitalnych zatrzymaniach krążenia będzie zależało głównie od lokalnego protokołu. Zasady kończenia resuscytacji Jedno wysokiej jakości, prospektywne badanie wykazało, że wprowadzenie zasady kończenia resuscytacji w oparciu o przyjęte kryteria na poziomie podstawowych zabiegów resuscytacyjnych prowadzonych przez techników medycznych (defibrillation only EMT) jest związane z wysokim prawdopodobieństwem zgonu 208. Zasada ta zaleca zakończenie resuscytacji w sytuacji braku ROSC, braku defibrylacji i w sytuacji, kiedy zatrzymanie krążenia nie wystąpiło w obecności zespołu pogotowia ratunkowego. Spośród 776 pacjentów z zatrzymaniem krążenia, u których zgodnie z powyższą zasadą zalecano zakończenie resuscytacji, przeżyły 4 osoby (0,5% [95% CI 0,2 0,9]). Wdrożenie tej zasady mogłoby zmniejszyć liczbę transportów o około 2/3. Cztery badania wykazały możliwość rozpowszechnienia tej zasady Dodatkowe badania wykazały związek daremnie podejmowanych interwencji z takimi zmiennymi, jak: brak ROSC na miejscu zdarzenia, wystąpienie rytmu nie do defibrylacji, niezauważone zatrzymanie krążenia, brak RKO wykonywanej przez świadków zdarzenia, czas od wezwania do interwencji, demografia pacjentów Dwa wewnątrzszpitalne badania i jedno obejmujące działania w oddziale ratunkowym wykazały ograniczoną wiarygodność zasad kończenia resuscytacji w tych warunkach Prospektywnie sprawdzona (walidowana) zasada kończenia resuscytacji, taka jak zakończenie działań resuscytacyjnych na poziomie podstawowych zabiegów resuscytacyjnych, może być zastosowana jako pomocne wskazanie w celu podjęcia decyzji o zakończeniu przedszpitalnej RKO u osób dorosłych. Wymaga to jednak jej prospektywnego sprawdzenia (walidacji) w systemach ratownictwa medycznego (analogicznie jak zaproponowane wyżej jej wdrożenie). Wprowadzanie jasnych zasad działania osób na różnych poziomach systemu ochrony zdrowia, włączając w to pomoc wewnątrzszpitalną, może być przydatne w ograniczeniu zmienności podejmowanych decyzji, jakkolwiek zasady te powinny być prospektywnie walidowane przed ich implementacją. Najpierw RKO czy defibrylacja? Są dowody wskazujące, że wykonywanie uciskania klatki piersiowej w czasie przygotowania i ładowania defibrylatora poprawia prawdopodobieństwo przeżycia 222. Pracownicy pogotowia ratunkowego powinni wykonywać wysokiej jakości RKO w czasie, kiedy defibrylator jest przygotowywany i ładowany oraz przyklejane są elektrody, ale rutynowe stosowanie RKO przez określony czas (np. 2 3 minuty) przed analizą rytmu czy defibrylacją nie jest rekomendowane. Ponieważ niektóre systemy ratownictwa już w pełni implementowały określony czas wykonywania RKO przed defibrylacją, przy braku dowodów popierających czy zaprzeczających tej teorii zasadne jest w ich sytuacji utrzymanie tej praktyki (zob. rozdział 3)
115 114 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 4c Resuscytacja wewnątrzszpitalna Podział postępowania w przypadku wystąpienia zatrzymania krążenia w szpitalu na podstawowe i zaawansowane zabiegi resuscytacyjne jest arbitralny, gdyż prowadzenie resuscytacji jest procesem ciągłym i opiera się na zdrowym rozsądku. Społeczeństwo oczekuje, że personel medyczny podejmie i prawidłowo wykona resuscytację krążeniowo-oddechową. W przypadku wszystkich wewnątrzszpitalnych zatrzymań krążenia należy upewnić się, że: Zatrzymanie krążenia i oddychania zostanie natychmiast rozpoznane. Pomoc jest osiągalna pod standardowym numerem telefonu. Natychmiast rozpocznie się RKO z wykorzystaniem przyrządów do udrażniania dróg oddechowych, jeśli będą wskazane, oraz jak najszybszym wykonaniem defibrylacji na pewno w ciągu 3 minut. Dokładna kolejność działania w przebiegu zatrzymania krążenia w szpitalu będzie zależała od wielu czynników, włączając w to: lokalizację (oddział szpitalny/poza oddziałem; oddział prowadzący monitorowanie/nieprowadzący monitorowania); stopień wyszkolenia osób rozpoczynających resuscytację; liczbę osób udzielających pomocy; dostępny sprzęt; sposób organizacji działań w szpitalu w odpowiedzi na zatrzymanie krążenia i inne stany naglące (np. MET, RRT). Lokalizacja U monitorowanych pacjentów rozpoznanie zatrzymania krążenia zwykle jest natychmiastowe. U pacjentów na oddziałach ogólnych może dochodzić do stopniowego pogarszania się stanu ogólnego i niezauważonego zatrzymania krążenia 6,8. Najkorzystniej jest, gdy wszyscy pacjenci z ryzykiem NZK są leczeni na oddziałach prowadzących monitorowanie, gdzie sprzęt do prowadzenia zabiegów resuscytacyjnych jest natychmiast dostępny. Szkolenie osób rozpoczynających resuscytację Każda osoba personelu medycznego powinna umieć rozpoznać zatrzymanie krążenia, wezwać pomoc i rozpocząć RKO. Personel powinien wykonywać czynności, w zakresie których został przeszkolony, i tak np. osoby pracujące na OIT lub na oddziałach ratunkowych będą miały większe doświadczenie i umiejętności w prowadzeniu resuscytacji niż osoby, które nie są systematycznie zaangażowane w resuscytację w codziennej praktyce. Personel szpitalny biorący udział w resuscytacji może mieć zróżnicowane umiejętności udrażniania dróg oddechowych, prowadzenia wentylacji czy przywracania krążenia. Ratownicy powinni wykonywać tylko te czynności, w zakresie których są przeszkoleni i kompetentni. Liczba osób udzielających pomocy Działający w pojedynkę ratownik, podejmujący resuscytację, musi wezwać pomoc. Jeśli obecne są inne osoby z personelu, kilka czynności może być wykonywanych równocześnie. Dostępny sprzęt We wszystkich miejscach klinicznych szpitala powinien być natychmiast dostępny sprzęt i leki umożliwiające prowadzenie resuscytacji. W idealnych warunkach sprzęt do RKO, włączając w to defibrylator, oraz leki i sposób ich rozmieszczenia powinny być ujednolicone w całym szpitalu 224,225. Zespół resuscytacyjny Zespół resuscytacyjny może być tradycyjnym zespołem reagującym na wezwanie jedynie w sytuacji rozpoznania zatrzymania krążenia. Alternatywnie szpitale mogą stosować strategie rozpoznawania pacjentów, u których istnieje ryzyko wystąpienia zatrzymania krążenia i wzywać zespół (np. MET lub RRT) przed wystąpieniem zatrzymania krążenia. Termin zespół resuscytacyjny odnosi się do całej grupy różnych zespołów funkcjonujących w szpitalach. Zatrzymanie krążenia w szpitalu rzadko jest nagłe lub nieoczekiwane. Działania zmierzające do rozpoznania pacjentów, u których występuje ryzyko zatrzymania krążenia, mogą umożliwić prewencję NZK, albo też zapobiec podejmowaniu daremnych resuscytacji pacjentów, u których podjęcie resuscytacji nie przyniesie korzyści. Natychmiastowe działania w przypadku utraty przytomności pacjenta w szpitalu Algorytm wstępnego postępowania w przypadku zatrzymania krążenia w szpitalu ilustruje ryc Zapewnij bezpieczeństwo własne i personelu. Oceń stan świadomości pacjenta. Jeżeli osoba z wykształceniem medycznym widzi pacjenta tracącego przytomność albo znajduje pacjenta nieprzytomnego w szpitalu, powinna najpierw głośno zawołać o pomoc, a potem ocenić, czy pacjent reaguje: delikatnie potrzasnąć za ramiona i głośno zapytać: Czy wszystko w porządku?. Jeżeli inne osoby z personelu medycznego są w pobliżu, istnieje możliwość podjęcia działań równolegle. Pacjent przytomny Potrzebna jest niezwłoczna ocena medyczna pacjenta. W zależności od przyjętych w danym szpitalu procedur może ona być wykonana przez zespół resuscytacyjny (np. MET, RRT). Podczas oczekiwania na zespół należy podać pacjentowi tlen, podłączyć monitor i uzyskać dostęp dożylny. Pacjent nieprzytomny Dokładna kolejność działań będzie zależała od przeszkolenia personelu i jego doświadczenia w zakresie oceny oddychania i krążenia. Nawet przeszkolony personel może mieć trudności z wiarygodną oceną oddechu i tętna podczas potwierdzenia zatrzymania krążenia Oddech agonalny (tzw. gasping, pojedyncze westchnięcia, wolny, głośny oddech z wysiłkiem) występuje często na początku zatrzymania krążenia, natomiast nie powinien być niewłaściwie interpretowany jako oznaka życia, tzn. zachowanego krążenia Oddech agonalny może także wystąpić podczas uciskania klatki piersiowej, jako wyraz poprawy perfuzji mózgowej, nie jest to jednak wyznacznik ROSC.
116 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 115 Resuscytacyja wewnątrzszpitalna Pacjent nieprzytomny/w ciężkim stanie Zawołaj o POMOC i oceń stan pacjenta Nie Oznaki życia? Tak Wezwij zespół resuscytacyjny RKO 30 : 2 używając sprzętu do udrażniania dróg oddechowych i stosując tlen Przyklej elektrody/podłącz monitor Oceń ABCDE Rozpoznaj i lecz przyczyny Tlen, monitorowanie, dostęp dożylny Wezwij zespół resuscytacyjny, jeśli wskazane 4 Zaawansowane zabiegi resuscytacyjne, gdy przybędzie zespół resuscytacyjny Przekaż pacjenta zespołowi resuscytacyjnemu Ryc Algorytm postępowania w wewnątrzszpitalnym zatrzymaniu krążenia Głośno zawołaj o pomoc (jeśli dotychczas tego nie zrobiłeś). Odwróć pacjenta na plecy i udrożnij drogi oddechowe: Udrożnij drogi oddechowe i ocen oddech: Udrożnij drogi oddechowe, stosując odgięcie głowy i uniesienie żuchwy. Sprawdź jamę ustną; jeżeli widoczne jest ciało obce czy resztki pokarmu, podejmij próbę ich usunięcia wygarniając palcem, używając kleszczyków lub ssaka, w zależności od potrzeby. Jeżeli podejrzewasz obrażenia szyi, staraj się udrożnić drogi oddechowe, stosując wysunięcie żuchwy; pamiętaj, że utrzymanie drożności dróg oddechowych i właściwej wentylacji jest priorytetem w opiece nad pacjentem z podejrzeniem uszkodzenia kręgosłupa; jeżeli wysunięcie żuchwy nie wystarcza, odegnij głowę w stopniu umożliwiającym udrożnienie dróg oddechowych; jeśli jest wystarczająca liczba ratowników, zastosuj ręczną stabilizację szyi i głowy, aby zminimalizować ruchy głową. Działania ukierunkowane na ochronę szyjnego odcinka kręgosłupa nie mogą upośledzać utlenowania i wentylacji. Utrzymując drożność dróg oddechowych, oceń wzrokiem, słuchem i dotykiem, czy oddech jest prawidłowy (pojedyncze westchnięcia oraz oddechy wolne, głośne z wysiłkiem nie są prawidłowe): Oceń wzrokiem poruszanie się klatki piersiowej. Słuchaj szmeru oddechowego przy ustach pacjenta. Staraj się wyczuć na policzku ruch powietrza. Oceń, czy poszkodowany oddycha prawidłowo, przy pomocy wzroku, słuchu i dotyku nie dłużej niż 10 sekund. Oceń oznaki krążenia: Pewna ocena tętna może być trudna; jeżeli nie ma oznak życia (zachowana jest świadomość, pacjent porusza się, oddycha prawidłowo, kaszle), rozpocznij i prowadź resuscytację krążeniowo-oddechową, dopóki nie przybędzie bardziej doświadczona pomoc albo nie pojawią się u pacjenta oznaki życia. Osoby doświadczone w ocenie klinicznej pacjenta powinny badać tętno na tętnicy szyjnej i równocześnie poszukiwać oznak życia nie dłużej niż 10 sekund. Jeżeli nie stwierdza się oznak życia albo są co do tego wątpliwości, należy natychmiast rozpocząć RKO; mało prawdopodobnym jest, by uciskanie klatki piersiowej pacjenta z zachowanym krążeniem (bijącym sercem) spowodowało szkody 240 ; opóźnienia w rozpoznaniu zatrzymania krążenia i podjęciu resuscytacji wpływają niekorzystnie na przeżycie i należy ich unikać.
117 116 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 Jeżeli tętno albo oznaki życia są zachowane, należy dokonać medycznej oceny pacjenta. W zależności od obowiązujących w szpitalu procedur może to być np. badanie przez zespół resuscytacyjny. Podczas oczekiwania na zespół należy podać pacjentowi tlen, podłączyć monitor i uzyskać dostęp dożylny. Gdy jest dostępny wiarygodny sposób monitorowania wysycenia tlenem krwi tętniczej (np. pulsoksymetria), należy miareczkować wdechowe stężenie tlenu tak, by osiągnąć SpO 2 w zakresie 94 98%. Jeżeli pacjent nie oddycha, ale ma zachowane tętno (zatrzymanie oddychania), należy prowadzić wentylację płuc i oceniać krążenie co każde 10 oddechów. Rozpoczęcie resuscytacji krążeniowo-oddechowej w szpitalu Podczas gdy jedna osoba rozpoczyna RKO, pozostałe wzywają zespół resuscytacyjny, gromadzą potrzebny sprzęt i defibrylator. Jeżeli obecna jest tylko jedna osoba, oznacza to konieczność pozostawienia pacjenta. Wykonaj 30 uciśnięć klatki piersiowej, a po nich 2 oddechy. Minimalizuj przerwy i zapewnij wysokiej jakości uciskanie klatki piersiowej. Właściwe uciskanie klatki piersiowej dłuższy czas jest męczące; zapewniając tylko minimalne przerwy, staraj się zmieniać osoby wykonującej uciśnięcia co 2 minuty. Utrzymuj drożność dróg oddechowych i prowadź wentylację płuc, stosując najwłaściwszy, natychmiast dostępny sprzęt. Zwykle do dyspozycji jest maska kieszonkowa jej użycie może być uzupełnione rurką ustno-gardłową. Alternatywnie, w zależności od lokalnych zaleceń można zastosować nadgłośniowe urządzenia do udrożnienia dróg oddechowych (Supraglottic Airway Device SAD), worek samorozprężalny lub worek samorozprężalny z maską twarzową. Intubację tchawicy powinny wykonywać tylko osoby przeszkolone, kompetentne i doświadczone w tym zakresie. Rutynowo powinien być dostępny kapnograf z możliwością pokazywania krzywej w celu potwierdzenia właściwego położenia rurki intubacyjnej (w przypadku zachowanego rzutu serca) i późniejszego monitorowania zaintubowanego pacjenta. Wdech wykonuj przez jedną sekundę i podaj objętość, która spowoduje prawidłowe uniesienie klatki piersiowej. Tak szybko, jak to możliwe, podaj tlen. Od momentu intubacji tchawicy lub zastosowania SAD wykonuj uciśnięcia klatki piersiowej nieprzerwanie (z wyjątkiem defibrylacji i oceny tętna, gdy są wskazane), z częstością przynajmniej 100/min i wentyluj płuca z częstością ok. 10 oddechów/min. Unikaj hiperwentylacji (zbyt dużej zarówno częstości oddechów, jak i objętości oddechowej), która może pogorszyć wynik leczenia. Respiratory, zapewniając właściwą częstość i objętość oddechową, uwalniają ratownika, dając mu możliwość podjęcia innych działań. Jeżeli sprzęt do udrażniania dróg oddechowych i wentylacji jest niedostępny, rozważ prowadzenie wentylacji usta usta. Jeżeli są przeciwwskazania kliniczne do kontaktu usta usta albo nie chcesz lub nie możesz jej prowadzić, wykonuj uciśnięcia klatki piersiowej dopóki nie przybędzie pomoc lub dostępny będzie sprzęt do udrażniania dróg oddechowych. Gdy dostępny będzie defibrylator, przyłóż łyżki do klatki piersiowej pacjenta i oceń rytm. Jeżeli są dostępne elektrody samoprzylepne, naklej je, nie przerywając uciśnięć klatki piersiowej. Zastosowanie samoprzylepnych elektrod lub wykonanie szybkiej oceny rytmu za pomocą łyżek quick look umożliwia szybszą ocenę rytmu w porównaniu z zastosowaniem elektrod EKG 241. Przerwa na ocenę rytmu powinna być krótka. Używając defibrylatora manualnego, jeśli jest obecny rytm do defibrylacji VF/VT, naładuj defibrylator, podczas gdy drugi ratownik kontynuuje uciśnięcia klatki piersiowej. Gdy defibrylator jest naładowany, przerwij uciskanie klatki piersiowej, potwierdź, że nikt nie dotyka pacjenta, i wykonaj defibrylację. W przypadku użycia AED stosuj się do audio-wizualnych zaleceń urządzenia. Natychmiast po defibrylacji podejmij uciskanie klatki piersiowej. Minimalizuj przerwy w uciskaniu klatki piersiowej. Kiedy używa się defibrylatora manualnego, możliwe jest zredukowanie przerwy pomiędzy zaprzestaniem uciśnięć i ponownym ich podjęciem poniżej 5 sekund. Kontynuuj zabiegi resuscytacyjne do czasu przybycia zespołu resuscytacyjnego lub do momentu pojawienia się oznak życia u pacjenta. Jeśli używasz AED, stosuj się do zaleceń głosowych. Jeżeli stosujesz klasyczny defibrylator, postępuj zgodnie z uniwersalnym algorytmem zaawansowanych zabiegów resuscytacyjnych (rozdział 4d). Po rozpoczęciu resuscytacji, jeśli jest wystarczająco dużo personelu, przygotuj wkłucia dożylne i leki, które z dużym prawdopodobieństwem zostaną użyte przez zespół resuscytacyjny (np. adrenalina). Wyznacz jedną osobę odpowiedzialną za przekazanie informacji kierownikowi zespołu resuscytacyjnego. Zastosuj uporządkowane narzędzie do przekazania informacji o pacjencie (np. SBAR, RSVP) 97,98. Zlokalizuj i przygotuj dokumentację pacjenta. Jakość uciśnięć klatki piersiowej podczas resuscytacji w szpitalu jest często niezadowalająca 242,243. Waga nieprzerywanego uciskania klatki piersiowej nie może być przeceniona. Nawet krótkie przerwy w uciśnięciach klatki piersiowej mają katastrofalny wpływ na wynik leczenia i dlatego ciągłe, skuteczne uciskanie klatki piersiowej musi być zapewnione i utrzymane w trakcie działań resuscytacyjnych. Uciskanie klatki piersiowej powinno być rozpoczęte z chwilą podjęcia resuscytacji i kontynuowane nieprzerwanie, za wyjątkiem krótkich przerw w celu wykonania istotnych interwencji (np. ocena tętna). Kierownik zespołu powinien kontrolować jakość prowadzonych zabiegów resuscytacyjnych i jeżeli jest ona niewystarczająca zmieniać ratowników. Ciągłe monitorowanie ETCO 2 może być zastosowane w celu oceny jakości RKO. Chociaż optymalna wartość docelowa ETCO 2 podczas RKO nie została określona, to wartość poniżej 10 mm Hg (1,4 kpa) jest związana z niepowodzeniem w osiągnięciu ROSC i może
118 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 117 wskazywać, że jakość uciśnięć klatki piersiowej powinna być poprawiona. Jeżeli jest to możliwe, osoby wykonujące uciskanie klatki piersiowej powinny zmieniać się co 2 minuty, nie powodując jednak dłuższych przerw w uciskaniu klatki piersiowej. 4d Algorytm zaawansowanych zabiegów resuscytacyjnych ALS Wprowadzenie Rytmy serca związane z zatrzymaniem krążenia dzieli się na dwie grupy: rytmy do defibrylacji (migotanie komór/ częstoskurcz komorowy bez tętna VF/VT) i nie do defibrylacji (asystolia i aktywność elektryczna bez tętna, Pulseless Electrical Activity PEA). Zasadniczą różnicą w leczeniu tych dwóch grup jest konieczność wykonania defibrylacji u pacjentów z VF/VT. Później podjęte czynności, tzn. prowadzenie z minimalnymi przerwami dobrej jakości uciskania klatki piersiowej, zapewnienie drożności dróg oddechowych i wentylacji, uzyskanie dostępu dożylnego, podaż adrenaliny oraz identyfikację i leczenie potencjalnie odwracalnych przyczyn zatrzymania krążenia, są wspólne dla obu grup. Chociaż algorytm postępowania w zatrzymaniu krążenia (ryc. 4.2) jest możliwy do zastosowania w przypadku każdego zatrzymania krążenia, to dodatkowe interwencje mogą być wskazane w sytuacji wystąpienia zatrzymania krążenia w przebiegu szczególnych okoliczności (zob. rozdział 8). Do interwencji, które bezsprzecznie wpływają na poprawę przeżycia po zatrzymaniu krążenia, należą natychmiastowe i skuteczne podjęcie przez świadków zdarzenia podstawowych zabiegów resuscytacyjnych, prowadzenie nieprzerwanych, wysokiej jakości uciśnięć klatki piersiowej oraz wczesna defibrylacja w przypadku VF/VT. Wykazano, że zastosowanie adrenaliny zwiększa ilość ROSC, ale nie wykazano, by jakikolwiek stosowany w resuscytacji lek czy zaawansowany sprzęt do udrażniania dróg oddechowych zwiększał przeżywalność do momentu wypisania ze szpitala po zatrzymaniu krążenia Dlatego też leki i zaawansowany sprzęt do udrażniania dróg oddechowych, mimo że należą do interwencji ALS, mają drugorzędne znaczenie w zestawieniu z wczesną defibrylacją i prowadzeniem nieprzerwanych, wysokiej jakości uciśnięć klatki piersiowej. Jak w poprzednich wytycznych, algorytm ALS wyróżnia rytmy do defibrylacji i rytmy nie do defibrylacji. Każda pętla algorytmu jest podobna, całe 2 minuty powinna być wykonywana RKO, aż do oceny rytmu i, jeżeli wskazane, oceny tętna. Adrenalina 1 mg podawana jest co 3 5 minut, dopóki nie osiągnie się ROSC, a czas podawania pierwszej dawki adrenaliny opisano poniżej. W przypadku wystąpienia VF/VT pojedyncza dawka amiodaronu jest wskazana po wykonaniu trzech nieskutecznych defibrylacji. Rytmy do defibrylacji (migotanie komór/ częstoskurcz komorowy bez tętna VF/VT) VF/VT jest pierwszym monitorowanym rytmem w około 25% zatrzymań krążenia, zarówno w szpitalu 4, jak i poza szpitalem VF/VT występuje również w 25% na pewnym etapie w czasie resuscytacji, kiedy pierwotnie udokumentowanym rytmem była asystolia lub PEA 4. Po potwierdzeniu zatrzymania krążenia należy wezwać pomoc (włączając w to dostarczenie defibrylatora) i rozpocząć RKO, zaczynając od uciśnięć klatki piersiowej w sekwencji 30 uciśnięć : 2 wdechy. Jak tylko zostanie dostarczony defibrylator, należy kontynuować uciskanie klatki piersiowej, jednoczasowo przyklejając elektrody samoprzylepne lub nakładając łyżki na klatkę piersiową. Kolejno należy ocenić rytm i leczyć zgodnie z algorytmem ALS. Gdy potwierdzone zostanie VF/VT, naładuj defibrylator, podczas gdy drugi ratownik wykonuje uciśnięcia klatki piersiowej. Gdy defibrylator jest naładowany, należy przerwać uciskanie klatki piersiowej i szybko ocenić, czy żaden z ratowników nie dotyka pacjenta, a następnie wykonać jedno wyładowanie (360 J dla defibrylatorów jednofazowych lub J dla dwufazowych). Należy minimalizować opóźnienie pomiędzy zaprzestaniem uciskania klatki piersiowej a defibrylacją (przerwy przed defibrylacją). Nawet 5 10 sekund opóźnienia zmniejszy szansę na skuteczną defibrylację 251,252. Bezpośrednio po wyładowaniu, bez ponownej oceny rytmu czy badania tętna, podejmij zabiegi resuscytacyjne (CV 30 : 2), rozpoczynając od uciśnięć klatki piersiowej. Nawet wtedy, gdy defibrylacja się powiedzie i przywróci rytm perfuzyjny, potrzeba czasu, by pojawiło się krążenie 253, a stwierdzenie pulsu bezpośrednio po defibrylacji jest bardzo rzadkie 254. Ponadto opóźnienie wywołane oceną tętna w sytuacji, gdy rytm perfuzyjny nie został przywrócony, będzie negatywnie oddziaływać na mięsień sercowy 255. Kontynuuj RKO przez 2 minuty, a następnie przerwij ją na krótko, aby sprawdzić rytm na monitorze. Jeżeli nadal utrzymuje się VF/VT, wykonaj drugie wyładowanie (360 J dla defibrylatorów jednofazowych lub J dla dwufazowych). Bezpośrednio po wyładowaniu, bez ponownej oceny rytmu czy badania tętna, podejmij RKO (CV 30 : 2) rozpoczynając od uciśnięć klatki piersiowej. Kontynuuj RKO przez 2 minuty, potem przerwij na krótko zabiegi resuscytacyjne, aby ocenić rytm. Gdy nadal utrzymuje się VF/VT, wykonaj trzecie wyładowanie (360 J dla defibrylatorów jednofazowych lub J dla dwufazowych). Niezwłocznie po nim powróć do RKO (CV 30 : 2) bez ponownej oceny rytmu czy tętna, rozpoczynając od uciśnięć klatki piersiowej. Jeśli udało się uzyskać dostęp dożylny lub doszpikowy, podaj 1 mg adrenaliny i 300 mg amiodaronu, jak tylko rozpocznie się na nowo uciskanie klatki piersiowej. Jeśli nie uda się uzyskać ROSC, wykonując trzecią defibrylację, adrenalina poprawi przepływ krwi w miokardium i może zwiększyć szanse na skuteczną defibrylację z kolejną próbą. W badaniach na zwierzętach szczytowe stężenie adrenaliny w osoczu oznaczane było na 90 sekund po obwodowym podaniu leku 256. Jeśli dojdzie do ROSC po trzeciej defibrylacji, to jest możliwe, że bolus adrenaliny doprowadzi do tachykardii i nadciśnienia i może spowodować nawrót VF. Należy wspomnieć, że naturalnie występujący poziom adrenaliny w osoczu, 4
119 118 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins Zaawansowane zabiegi resuscytacyjne Nie reaguje? Brak oddechu lub tylko pojedyncze westchnięcia Wezwij zespół resuscytacyjny RKO 30 : 2 Minimalizuj przerwy 4 (VF/VT bez tętna) Oceń rytm (PEA/asystolia) Powrót spontanicznego krążenia Natychmiast podejmij RKO przez 2 min Minimalizuj przerwy NATYCHMIASTOWA OPIEKA PORESUSCYTACYJNA Zastosuj schemat ABCDE Kontroluj wentylację i oksygenację Wykonaj 12-odprowadzeniowe EKG Lecz przyczynę zatrzymania krążenia Kontroluj temperaturę/zastosuj terapeutyczną hipotermię Natychmiast podejmij RKO przez 2 min Minimalizuj przerwy PODCZAS RKO Zapewnij wysokiej jakości uciśnięcia klatki piersiowej: częstość, głębokość, właściwe odkształcenie Zaplanuj działanie, zanim przerwiesz RKO Podaj tlen Rozważ zaawansowane drogi oddechowe i kapnografię Nie przerywaj uciskania klatki piersiowej po zabezpieczeniu dróg oddechowych Dostęp donaczyniowy (dożylny, doszpikowy) Podaj adrenalinę co 3 5 min Lecz odwracalne przyczyny ODWRACALNE PRZYCZYNY Hipoksja Hipowolemia Hipo-/hiperkaliemia/zaburzenia metaboliczne Hipotermia Zaburzenia zatorowo-zakrzepowe Tamponada osierdzia Zatrucia Odma prężna Ryc Algorytm zaawansowanych zabiegów resuscytacyjnych ALS oceniany bezpośrednio po ROSC, jest wysoki 257 i jak dotąd nie analizowano dodatkowego ryzyka związanego z egzogenną podażą adrenaliny. Przerwanie uciskania klatki piersiowej w trakcie trwania pętli RKO, by zbadać rytm mogący dawać perfuzję, jest także prawdopodobnie szkodliwe. Zastosowanie wykresu kapnografii może pomóc zidentyfikować ROSC bez potrzeby przerywania uciskania klatki piersiowej i może być pomocne w uniknięciu podania bolusa adrenaliny po osiągnięciu ROSC. Dwa prospektywne badania przeprowadzone z udziałem pacjentów wykazały, że powrotowi spontanicznego krążenia towarzyszy znaczący wzrost ETCO 2 258,259. Po każdym 2-minutowym cyklu RKO, jeśli rytm zmienia się w asystolię lub PEA, zastosuj postępowanie jak w rytmach nie do defibrylacji patrz niżej. Jeżeli obecny jest rytm nie do defibrylacji i jest on uporządkowany (zespoły QRS są regularne lub wąskie), należy ocenić tętno. Ocena rytmu powinna być krótka, a ocena tętna wykonywana tylko wtedy, gdy jest obecny uporządkowany rytm. Jeżeli jest jakakolwiek wątpliwość dotycząca obecności tętna w przypadku stwierdzenia uporząd-
120 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 119 kowanego rytmu serca, należy podjąć ponownie RKO. Jeżeli doszło do ROSC, rozpocznij opiekę poresuscytacyjną. Podczas leczenia VF/VT personel medyczny prowadzący resuscytację musi ćwiczyć skuteczną koordynację dotyczącą wykonywania RKO i defibrylacji. Gdy VF utrzymuje się dłużej niż kilka minut, zapasy tlenu i substancji odżywczych w mięśniu sercowym wyczerpują się. Krótki okres uciskania klatki piersiowej dostarczy tlen i substraty energetyczne oraz zwiększy prawdopodobieństwo przywrócenia rytmu z perfuzją po defibrylacji 260. Analiza krzywej VF pod kątem przewidywania skuteczności defibrylacji wskazuje, że im krótszy jest okres między uciśnięciami klatki piersiowej a wyładowaniem energii, tym większe jest prawdopodobieństwo, że defibrylacja będzie skuteczna 260,261. Skrócenie nawet o kilka sekund przerwy między uciśnięciami a wyładowaniem może zwiększyć prawdopodobieństwo skutecznej defibrylacji 251,252. Niezależnie od rytmu towarzyszącemu zatrzymaniu krążenia kolejne dawki 1 mg adrenaliny należy podawać co 3 5 minut do momentu ROSC. W praktyce polega to na podawaniu 1 mg adrenaliny co dwie pętle algorytmu. Jeżeli dojdzie do powrotu oznak życia w trakcie RKO (celowe ruchy, prawidłowy oddech, kaszel), należy ocenić rytm. W przypadku stwierdzenia uporządkowanego rytmu serca należy ocenić tętno. Gdy jest obecne, kontynuuj opiekę poresuscytacyjną i/lub leczenie zaburzeń rytmu występujących w okresie około zatrzymania krążenia. W przypadku braku tętna kontynuuj RKO. Wykonywanie RKO w sekwencji CV 30 : 2 jest męczące. Należy zmieniać osobę wykonującą uciśnięcia klatki piersiowej co 2 minuty, pamiętając o minimalizowaniu przerw w uciśnięciach. Zauważone, monitorowane VF/VT bez tętna, występujące w pracowniach kardiologii inwazyjnej lub po zabiegach kardiochirurgicznych Jeżeli u pacjenta wystąpi zauważone i monitorowane zatrzymanie krążenia podczas cewnikowania serca lub we wczesnym okresie po zabiegach kardiochirurgicznych, należy: Potwierdzić zatrzymanie krążenia i wezwać pomoc. Wykonać do trzech pod rząd defibrylacji, jeżeli pierwotnym rytmem jest VF/VT. Bezpośrednio po wykonaniu trzeciej defibrylacji należy rozpocząć uciśnięcia klatki piersiowej i kontynuować RKO przez 2 minuty. Strategia trzech wyładowań może być również zastosowana jako wstępne postępowanie w zauważonym zatrzymaniu krążenia w mechanizmie VT/VT, gdy pacjent jest już podłączony do defibrylatora manualnego. Chociaż brak jest danych popierających strategię trzech kolejnych wyładowań w jakiejkolwiek z wymienionych sytuacji, jest mało prawdopodobne, by uciśnięcia klatki piersiowej mogły poprawić obecne wtedy warunki dające szansę na skuteczną defibrylację, zwłaszcza jeśli nastąpi ona wcześnie w elektrycznej fazie zatrzymania krążenia, natychmiast po wystąpieniu VF (zob. rozdział 3) 223. Uderzenie przedsercowe Pojedyncze uderzenie przedsercowe ma bardzo małą skuteczność kardiowersji rytmu do defibrylacji i powodzenie tej procedury jest możliwe tylko wtedy, gdy wykonuje się ją w ciągu pierwszych kilku sekund od wystąpienia rytmu do defibrylacji 265. Bardziej prawdopodobna jest konwersja VT bez tętna niż VF. Wykonanie uderzenia przedsercowego nie może opóźniać wezwania pomocy czy dostarczenia defibrylatora. Jest to więc terapia właściwa wyłącznie w sytuacji, gdy kilka osób personelu medycznego jest obecnych przy pacjencie, u którego zauważono monitorowane zatrzymanie krążenia, a defibrylator nie jest natychmiast dostępny (zob. rozdział 3) 223,266. W praktyce jest to możliwe jedynie w miejscach o wzmożonym nadzorze, takich jak oddział ratunkowy lub OIT 264. Uderzenie przedsercowe powinno być wykonane natychmiast po potwierdzeniu zatrzymania krążenia wyłącznie przez przeszkolony w tym zakresie personel medyczny. Należy uderzyć w dolną połowę mostka z wysokości około 20 cm łokciową stroną mocno zaciśniętej pięści, potem cofnąć ją szybko, aby bodziec miał charakter impulsu. Bardzo mało jest doniesień dotyczących przekształcenia rytmu perfuzyjnego w rytm nieperfuzyjny przy zastosowaniu uderzenia przedsercowego 267. Drogi oddechowe i wentylacja Podczas leczenia uporczywego VF zapewnij dobrą jakość uciśnięć klatki piersiowej pomiędzy kolejnymi defibrylacjami. Rozważ odwracalne przyczyny (4 H i 4 T) i lecz je, gdy występują. Sprawdź położenie łyżek/elektrod, ich kontakt ze skórą, zapewnij dobre przewodzenie impulsu (np. podkładki żelowe). Intubacja tchawicy jest najpewniejszym sposobem udrożnienia dróg oddechowych, ale powinna być wykonana tylko przez personel stosownie przeszkolony i posiadający regularnie odnawiane doświadczenie w tym zakresie. Osoby te powinny próbować wykonywać laryngoskopię i intubację bez przerywania uciśnięć klatki piersiowej. Krótka przerwa w uciskaniu klatki piersiowej może być potrzebna na wprowadzenie rurki między struny głosowe, ale nie powinno to trwać dłużej niż 10 sekund. Alternatywnie, ażeby uniknąć jakichkolwiek przerw w uciskaniu klatki piersiowej, intubację można odroczyć do czasu powrotu spontanicznego krążenia. Żadne badanie nie wykazało, że intubacja poprawia przeżywalność w zatrzymaniu krążenia. Po intubacji potwierdź właściwe położenie rurki i odpowiednio ją umocuj. Prowadź wentylację z częstością 10 oddechów na minutę, unikaj hiperwentylacji. Od momentu intubacji tchawicy prowadź uciskanie klatki piersiowej z częstością 100/min, bez przerw na wentylację. Przerwy w uciskaniu klatki piersiowej powodują znaczny spadek ciśnienia perfuzji wieńcowej. Po wznowieniu uciśnięć, zanim wyjściowe ciśnienie perfuzji wieńcowej zostanie ponownie osiągnięte, występuje pewne opóźnienie, dlatego uciśnięcia klatki piersiowej prowadzone bez przerw na wentylację (czy wykonanie innej czynności) skutkują generowaniem znacznie wyższego średniego ciśnienia perfuzji wieńcowej. Jeśli nie ma osób przeszkolonych w zakresie intubacji, alternatywę stanowią nadgłośniowe sprzęty do udrażniania dróg oddechowych (np. maska krtaniowa, zob. rozdział 4e). Od chwili udrożnienia dróg oddechowych jednym z powyższych przyrządów należy podjąć próbę uciskania klatki pier- 4
121 120 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 siowej bez przerw na wentylację. Jeśli pojawi się nadmierny przeciek powietrza upośledzający wentylację, uciśnięcia klatki piersiowej należy prowadzić z przerwami na oddechy, utrzymując stosunek CV 30 : 2. Dostęp dożylny i leki Podaż leków do żyły obwodowej w porównaniu z podażą do żyły centralnej Zapewnij dostęp do żyły, jeśli dotychczas nie został wykonany. Pomimo że szczytowe stężenie leków jest wyższe, a czas dotarcia do krążenia centralnego krótszy, gdy leki wstrzykuje się do cewnika umieszczonego w żyle centralnej w porównaniu z żyłą obwodową 268, założenie centralnego dostępu dożylnego wymaga przerwania zabiegów resuscytacyjnych i jest obarczone ryzykiem powikłań. Kaniulacja żyły obwodowej jest szybsza, prostsza do wykonania i bezpieczniejsza. W ślad za lekiem podanym obwodowo musi być wstrzyknięte co najmniej 20 ml płynu, a kończyna uniesiona na sekund tak, aby ułatwić dostarczenie leku do krążenia centralnego. Dostęp doszpikowy Jeżeli uzyskanie dostępu do żyły jest trudne albo niemożliwe, rozważ drogę doszpikową (intraosseous io). Pomimo że zwykle rozważana jako alternatywa dostępu donaczyniowego u dzieci, u dorosłych jest obecnie uznawana za skuteczną drogę podawania leków 269. Leki podane doszpikowo osiągają pożądane stężenie w osoczu w czasie porównywalnym z lekami wstrzykniętymi przez cewnik umieszczony w żyle centralnej 270. Dostępne ostatnio mechaniczne urządzenia do uzyskiwania dostępu doszpikowego ułatwiają wykonanie tej procedury 271. Dostęp dotchawiczy Stężenie, jakie osiągnie w surowicy lek podany dotchawiczo, jest nieprzewidywalne, a optymalna dawka dotchawicza większości leków jest nieznana. Podczas RKO równoważna dawka adrenaliny podana dotchawiczo jest 3 10 razy wyższa niż dawka dożylna 272,273. Niektóre badania na zwierzętach sugerują, że niższy poziom adrenaliny, osiągany, gdy lek jest podawany dotchawiczo, może wywoływać przejściowy efekt β-adrenergiczny, który spowoduje hipotensję i obniżenie ciśnienia perfuzji wieńcowej W obliczu całkowicie nieprzewidywalnych stężeń osoczowych leków podawanych dotchawiczo, przy zwiększonej dostępności właściwego sprzętu do dostępu doszpikowego, droga dotchawicza nie jest już zalecana. Podawanie leków z wykorzystaniem nadgłośniowych urządzeń udrażniających drogi oddechowe jest jeszcze mniej wiarygodne i nie powinno być stosowane 278. Adrenalina Pomimo powszechnego stosowania adrenaliny podczas resuscytacji oraz kilku badań z użyciem wazopresyny nie ma żadnego badania z grupą kontrolną, gdzie stosowano placebo, które wskazywałoby, że rutynowa podaż jakiegokolwiek wazopresora na jakimkolwiek etapie zatrzymania krążenia u ludzi zwiększa prawdopodobieństwo przeżycia do wypisu ze szpitala bez ubytków neurologicznych. Dotychczas zgromadzone dowody są niewystarczające dla poparcia lub zanegowania rutynowego stosowania określonych leków lub sekwencji ich podawania. Pomimo braku danych pochodzących z badań u ludzi nadal zaleca się stosowanie adrenaliny, głównie w oparciu o dane pochodzące z badań nad zwierzętami oraz raportowanej zwiększonej krótkoterminowej przeżywalności u ludzi 245,246. Działanie alfa-adrenergiczne adrenaliny powoduje skurcz naczyń krwionośnych, co zwiększa ciśnienie perfuzyjne w mięśniu sercowym oraz mózgu. Wyższy wieńcowy przepływ krwi zwiększa częstotliwość i amplitudę fali migotania komór i powinien zwiększyć szanse na przywrócenie krążenia podczas próby defibrylacji 260,279,280. Pomimo że adrenalina poprawia przeżywalność krótkoterminową, dane pochodzące z badań u zwierząt wskazują, iż powoduje ona zaburzenia w mikrokrążeniu 281,282 oraz dysfunkcję mięśnia sercowego występującą po zatrzymaniu krążenia 283,284, co łącznie może mieć wpływ na przeżywalność długoterminową. Nie jest znana optymalna dawka adrenaliny i nie ma danych popierających stosowanie powtarzanych dawek. Mało jest danych dotyczących farmakokinetyki adrenaliny podczas RKO. Nie jest również znany optymalny czas trwania RKO, jak również ilość defibrylacji, które należy przeprowadzić przed podaniem leków. Bazując na konsensusie ekspertów, w rytmach VF/VT bez tętna adrenalinę należy podać po trzeciej defibrylacji, gdy wznowione zostaną uciśnięcia klatki piersiowej, a następnie powtarzać dawkę adrenaliny co 3 do 5 minut podczas zatrzymania krążenia (co drugi cykl). W celu podawania leków nie należy przerywać RKO. Leki antyarytmiczne Nie ma żadnych dowodów na to, że rutynowa podaż jakiegokolwiek leku antyarytmicznego podczas zatrzymania krążenia u ludzi zwiększa przeżywalność do wypisu ze szpitala. W porównaniu z placebo 285 i lidokainą 286 zastosowanie amiodaronu w opornym na defibrylację VF poprawia krótkoterminowe wyniki przeżywalności do przyjęcia do szpitala. W badaniach tych terapia antyarytmiczna była stosowana, jeśli VF/VT utrzymywało się pomimo wykonania przynajmniej trzech defibrylacji; jednakże obserwacje te były przeprowadzane przy stosowaniu konwencjonalnej strategii trzech wyładowań pod rząd. Nie ma żadnych danych o zastosowaniu amiodaronu w opornych na defibrylację VF/VT, gdy używana jest strategia pojedynczych wyładowań. Bazując na konsensusie ekspertów, należy podać bolus 300 mg amiodaronu, jeśli VF/VT utrzymuje się po trzech defibrylacjach. Kolejna dawka 150 mg może być podana w przypadku nawracających lub utrzymujących się epizodów VF/ VT, z następowym wlewem 900 mg w ciągu 24 godzin. Jeśli amiodaron nie jest dostępny, alternatywę stanowi lidokaina w dawce 1 mg/kg, ale nie należy jej podawać, jeśli wcześniej zastosowano amiodaron. Magnez Rutynowe zastosowanie magnezu podczas zatrzymania krążenia nie poprawia przeżywalności i nie jest rekomendowane, chyba że podejrzewa się obecność torsades de pointes (patrz zaburzenia rytmu około zatrzymania krążenia).
122 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 121 Wodorowęglan sodu Rutynowa podaż wodorowęglanu sodu podczas zatrzymania krążenia i RKO lub po powrocie spontanicznego krążenia nie jest zalecana. Należy podać 50 mmol wodorowęglanu sodu, jeśli zatrzymanie krążenia jest związane z hiperkaliemią lub przedawkowaniem trójcyklicznych leków przeciwdepresyjnych. Dawkę należy powtórzyć w zależności od stanu klinicznego pacjenta oraz wyników kolejnych badań gazometrycznych. Podczas zatrzymania krążenia wartości gazometrii krwi tętniczej nie odzwierciedlają warunków równowagi kwasowo-zasadowej obecnej w tkankach 292, ph tkankowe będzie niższe niż to mierzone w krwi tętniczej. Jeśli założony jest cewnik w żyle centralnej, analiza gazometrii krwi żylnej centralnej dostarczy dokładniejszych informacji dotyczących równowagi kwasowo-zasadowej, niż gazometria krwi tętniczej. Utrzymujące się migotanie komór/częstoskurcz komorowy bez tętna Jeśli VF/VT utrzymuje się, należy rozważyć zmianę ułożenia elektrod samoprzylepnych/łyżek defibrylatora (zob. rozdział 3) 223. Należy rozważyć wszystkie potencjalnie odwracalne przyczyny (patrz niżej) oraz leczyć te zidentyfikowane. Utrzymujące się VF/VT może być wskazaniem do przezskórnej interwencji wieńcowej (Percutaneous Coronary Intervention PCI) lub do trombolizy w tych przypadkach mechaniczne urządzenia do prowadzenia RKO mogą być pomocne w utrzymaniu wysokiej jakości RKO wykonywanej przez dłuższy czas 293. Czas trwania resuscytacji w każdym indywidualnym przypadku jest kwestią wynikającą zarówno z klinicznej oceny, biorąc pod uwagę okoliczności wystąpienia zatrzymania krążenia, jak i perspektywy pomyślnego rezultatu. Jeśli uznano za słuszne rozpoczęcie resuscytacji, zwykle uważa się, że należy ją kontynuować przynajmniej dopóki pacjent pozostaje w VF/VT. Rytmy nie do defibrylacji (PEA i asystolia) Aktywność elektryczna bez tętna (PEA) jest definiowana jako zatrzymanie krążenia przebiegające z obecnością elektrycznej aktywności, która normalne wiązałaby się z obecnością wyczuwalnego tętna. U takich pacjentów często występują pewne mechaniczne skurcze mięśnia sercowego, ale są one zbyt słabe, aby generować wyczuwalne tętno lub oznaczalne ciśnienie tętnicze krwi sytuacja taka jest czasem opisywana jako pseudo-pea (patrz niżej). PEA jest często spowodowana odwracalnymi przyczynami i może być leczona, jeśli zostaną one wykryte i skorygowane. Przeżycie po zatrzymaniu krążenia w mechanizmie asystolii lub PEA jest mało prawdopodobne, chyba że rozpozna się i skutecznie wyleczy jego odwracalną przyczynę. Jeśli pierwszym monitorowanym rytmem jest PEA lub asystolia, należy rozpocząć RKO 30 : 2 oraz podać 1 mg adrenaliny tak szybko, jak tylko osiągnie się dostęp dożylny. Jeśli na monitorze obecna jest asystolia, należy bez przerywania RKO sprawdzić, czy elektrody są prawidłowo podłączone. W momencie gdy zabezpieczy się drogi oddechowe technikami zaawansowanymi, należy kontynuować uciśnięcia klatki piersiowej bez przerw na wentylację. Po dwóch minutach RKO należy ponownie ocenić rytm. Jeśli utrzymuje się asystolia, należy natychmiast powrócić do RKO. Jeśli obecny jest uporządkowany rytm, należy ocenić tętno. Jeśli brak tętna (lub gdy są jakiekolwiek wątpliwości co do jego obecności), należy kontynuować RKO. Jeśli tylko uzyska się dostęp donaczyniowy, należy podawać 1 mg adrenaliny (iv/ io) co drugą pętlę RKO (tj. co około 3 5 minut). Jeśli tętno jest obecne, należy rozpocząć opiekę poresuscytacyjną. Jeśli podczas wykonywania RKO powrócą oznaki życia, należy sprawdzić rytm i spróbować wyczuć tętno. Zawsze, gdy zostanie postawiona diagnoza asystolii, należy dokładnie ocenić EKG pod kątem obecności załamków P, ponieważ ten rytm może odpowiedzieć na stymulację serca. Stymulacja prawdziwej asystolii nie przynosi korzyści. Jeśli są wątpliwości, czy rytm jest asystolią, czy niskonapięciowym VF, nie należy wykonywać defibrylacji, ale zamiast tego kontynuować uciśnięcia klatki piersiowej i wentylację. Defibrylacja niskonapęciowego VF, które jest trudne do odróżnienia od asystolii, nie będzie skuteczna w przywróceniu rytmu perfuzyjnego. Kontynuacja dobrej jakości RKO może poprawić amplitudę i częstotliwość VF oraz zwiększyć szansę na skuteczną defibrylację przywracającą rytm perfuzyjny. Próby defibrylacji przypuszczalnego niskonapięciowego VF wskutek powtarzanych wyładowań zwiększają uszkodzenie mięśnia sercowego poprzez bezpośrednie działanie prądu, jak i z powodu przerywania przepływu wieńcowego. Podczas leczenia asystolii lub PEA po 2-minutowej pętli RKO, jeśli rytm zmieni się w VF, należy stosować się do algorytmu dla rytmów do defibrylacji. W przeciwnym razie należy kontynuować RKO oraz podawać adrenalinę co 3 5 minut każdorazowo po wykonaniu oceny i stwierdzeniu braku tętna. Jeśli VF zostanie zauważone na monitorze podczas 2-minutowej pętli RKO, należy ją dokończyć, zanim dokona się formalnej oceny rytmu i defibrylacji ta strategia pozwoli na minimalizowanie przerw w uciśnięciach klatki piersiowej. Potencjalnie odwracalne przyczyny zatrzymania krążenia Podczas każdego zatrzymania krążenia muszą być rozważone potencjalne przyczyny oraz czynniki obciążające, dla których istnieje określone leczenie. Dla ułatwienia zapamiętania podzielono je na dwie grupy po cztery, według ich początkowych liter (w języku angielskim): H lub T. Więcej szczegółów na ich temat zawiera rozdział Zastosowanie obrazowania ultrasonograficznego podczas zaawansowanych zabiegów resuscytacyjnych Kilka badań analizowało zastosowanie ultrasonografii podczas zatrzymania krążenia do wykrywania potencjalnie odwracalnych przyczyn. Pomimo że żadne z tych badań nie wykazało poprawy wyników leczenia przy zastosowaniu tej techniki obrazowania, nie ma żadnych wątpliwości, że echokardiografia umożliwia wykrycie potencjalnie odwracalnych przyczyn zatrzymania krążenia (np. tamponady worka osierdziowego, zatoru płucnego, niedokrwienia [odcinkowe zaburzenia kurczliwości mięśnia sercowego], rozwarstwienie aorty, hipowolemia, odma opłucnowa) Ultrasonografia, jeśli jest dostępna dla przeszkolonego w tym zakresie klini- 4
123 122 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 cysty, może być pomocna w rozpoznaniu i leczeniu potencjalnie odwracalnych przyczyn zatrzymania krążenia. Włączenie ultrasonografii do zaawansowanych zabiegów resuscytacyjnych wymaga odpowiedniego przećwiczenia, tak aby przerwy w uciśnięciach klatki piersiowej były jak najkrótsze. Zaleca się ułożenie głowicy pod wyrostkiem mieczykowatym 295,301,303. Przyłożenie głowicy tuż przed przerwaniem uciśnięć klatki piersiowej w celu planowanej oceny rytmu, umożliwia dobrze wyszkolonemu ultrasonografiście uzyskanie wymaganej projekcji w ciągu 10 sekund. Brak ruchów serca stwierdzonych za pomocą ultrasonografii wykonywanej podczas resuscytacji pacjentów z zatrzymaniem krążenia jest związane z wysokim prawdopodobieństwem śmierci Jakkolwiek brak jest informacji na temat czułości i swoistości tej metody. Cztery H Należy minimalizować ryzyko hipoksji poprzez zapewnienie prawidłowej wentylacji płuc pacjenta 100-procentowym tlenem podczas RKO. Należy upewnić się, że klatka piersiowa unosi się prawidłowo oraz szmery oddechowe słyszalne są obustronnie. Stosując techniki opisane w rozdziale 4e, należy dokładnie sprawdzić, czy rurka nie znajduje się omyłkowo w oskrzelu lub przełyku. Aktywność elektryczna bez tętna spowodowana hipowolemią zwykle jest następstwem ciężkiego krwotoku. Może być on spowodowany urazem (zob. rozdział 8h) 294, krwawieniem z przewodu pokarmowego lub pęknięciem tętniaka aorty. Objętość wewnątrznaczyniową należy szybko przywrócić, podając ogrzane płyny, w połączeniu z pilną operacją, mającą na celu zatrzymanie krwawienia. Hiperkaliemia, hipokaliemia, hipokalcemia, kwasica i inne zaburzenia metaboliczne wykrywane są testami biochemicznymi lub sugerowane w oparciu o wywiad, np. niewydolność nerek (zob. rozdział 8a) 294. Diagnostyczne może być 12-odprowadzieniowe EKG. Dożylnie podawany chlorek wapnia jest wskazany w hiperkaliemii, hipokalcemii oraz przedawkowaniu blokerów kanałów wapniowych. Należy podejrzewać hipotermię w każdym przypadku tonięcia (zob. rozdział 8c i 8d) 294. Należy wtedy stosować termometry z możliwością oceny niskich wartości temperatury. Cztery T Odma prężna może być pierwotną przyczyną PEA oraz być skutkiem prób założenia cewnika do żyły centralnej. Rozpoznaje się ją na podstawie objawów klinicznych. Odmę prężną należy natychmiast odbarczyć poprzez torakocentezę igłową, a następnie założyć dren do klatki piersiowej. W sytuacji ciężkiego urazu bardziej wiarygodną metodą odbarczenia, w przypadku podejrzenia odmy prężnej, jest wykonanie obustronnej torakostomii. Tamponada serca jest trudna do rozpoznania, ponieważ jej typowe objawy w postaci poszerzonych żył szyjnych oraz hipotensji są zazwyczaj maskowane przez zatrzymanie krążenia. Zatrzymanie krążenia po urazie penetrującym klatki piersiowej z dużym prawdopodobieństwem sugeruje obecność tamponady i jest wskazaniem do nakłucia worka osierdziowego lub torakotomii ratunkowej (zob. rozdział 8h) 294. Coraz większe zastosowanie ultrasonografii sprawia, że diagnoza tamponady osierdzia jest bardziej wiarygodna. Przy braku specyficznego wywiadu przypadkowe lub zamierzone spożycie substancji leczniczych czy trujących może być ujawione tylko za pomocą testów laboratoryjnych (zob. rozdział 8b) 294. Jeśli są dostępne, należy podawać specyficzne antidotum, ale zazwyczaj leczenie jest objawowe i polega na stosowaniu standardowych protokołów ALS. Najczęstszą przyczyną zatorowo-zakrzepowej lub mechanicznej przeszkody w układzie krążenia jest masywny zator płuc. Jeśli jest on możliwą przyczyną zatrzymania krążenia, należy rozważyć natychmiastową podaż leków trombolitycznych (rozdział 4f ) e Drożność dróg oddechowych i wentylacja Wstęp Pacjenci wymagający resuscytacji zwykle mają niedrożne drogi oddechowe, zazwyczaj wtórnie do utraty przytomności, ale czasem może to być pierwotna przyczyna zatrzymania krążenia i oddechu. Kluczowa jest natychmiastowa ocena, z kontrolą dróg oddechowych i wentylacji płuc. Pomoże to zapobiec wtórnemu, wynikającemu z hipoksji, uszkodzeniu mózgu i innych życiowo ważnych narządów. Bez prawidłowego natlenienia przywrócenie spontanicznego rzutu serca może być niemożliwe. Powyższe zasady mogą nie dotyczyć zauważonego zatrzymania krążenia, gdy dostępny jest defibrylator; w takim przypadku priorytetem jest natychmiastowa defibrylacja. Niedrożność dróg oddechowych Przyczyny niedrożności dróg oddechowych Niedrożność dróg oddechowych może być częściowa lub całkowita. Może ona wystąpić na każdym poziomie, od nosa i jamy ustnej w dół do tchawicy. U nieprzytomnych pacjentów najczęstszym miejscem, gdzie dochodzi do niedrożności dróg oddechowych jest podniebienie miękkie i nagłośnia 308,309. Niedrożność może być również spowodowana przez wymiociny lub krew (zarzucanie treści pokarmowej lub uraz) lub przez ciała obce. Brak drożności na poziomie krtani może być skutkiem obrzęku spowodowanego oparzeniem, zapaleniem lub anafilaksją. Drażnienie górnych dróg oddechowych może spowodować skurcz krtani. Zatkanie dróg oddechowych poniżej krtani występuje znacznie rzadziej. Może do tego dojść w następstwie zwiększenia wydzieliny w oskrzelach, obrzęku błony śluzowej, skurczu oskrzeli, obrzęku płuc czy aspiracji treści żołądkowej. Rozpoznanie niedrożności dróg oddechowych Niedrożność dróg oddechowych może być ledwie uchwytna i łagodna, dlatego często pozostaje niezauważona przez pracowników ochrony zdrowia, nie mówiąc o osobach bez wykształcenia medycznego. Ocena wzrokiem, słuchem i dotykiem stanowi prostą, usystematyzowaną metodę wykrywania niedrożności dróg oddechowych. Oceń wzrokiem ruchy klatki piersiowej i nadbrzusza. Staraj się wysłuchać i wyczuć przepływ powietrza przy ustach i nosie.
124 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 123 W przypadku częściowej niedrożności dróg oddechowych droga przepływu powietrza jest ograniczona, a oddech zwykle głośny. Niedrożność na poziomie krtani lub powyżej powoduje stridor wdechowy. Świsty wydechowe świadczą o niedrożności na poziomie dolnych dróg oddechowych, które mają tendencję do zapadania się, upośledzając drożność podczas wydechu. Inne charakterystyczne dźwięki to np.: bulgotanie wywołane obecnością płynnej lub półpłynnej treści w głównych drogach oddechowych, chrapanie, które powstaje, gdy podniebienie miękkie lub nagłośnia częściowo zamykają gardło, pianie, świadczące o kurczu głośni. U pacjenta, który wykonuje próby oddechu, całkowita niedrożność dróg oddechowych powoduje paradoksalne ruchy klatki piersiowej i brzucha, często opisywane jako falowanie. Podczas gdy pacjent wykonuje próbę wdechu, klatka piersiowa zapada się, a brzuch unosi; przeciwnie dzieje się podczas wydechu. Kontrastuje to z normalnym torem oddychania, polegającym na synchronicznych ruchach brzucha do góry i na zewnątrz (spychanego w dół przez przeponę) wraz z unoszeniem ściany klatki piersiowej. Gdy drogi oddechowe są niedrożne, uruchomione zostają dodatkowe mięśnie oddechowe, wraz ze skurczami mięśni szyi i obręczy barkowej, które pomagają w ruchach klatki piersiowej. Aby rozpoznać paradoksalne ruchy oddechowe, które mogą przypominać normalny oddech, należy dokładnie zbadać szyję, klatkę piersiową i brzuch. W skład badania musi wejść osłuchiwanie, ponieważ brak szmerów oddechowych jest niezawodnym potwierdzeniem całkowitej niedrożności dróg oddechowych. Każde głośne oddychanie wskazuje na częściową niedrożność dróg oddechowych. W czasie bezdechu, kiedy spontaniczne ruchy oddechowe są nieobecne, całkowitą niedrożność rozpoznaje się, gdy nie można wypełnić powietrzem płuc podczas próby wentylacji dodatnim ciśnieniem. Jeżeli drożność dróg oddechowych nie zostanie przywrócona w ciągu kilku minut, może dojść do uszkodzenia mózgu i innych ważnych dla życia narządów, doprowadzając do zatrzymania krążenia. Podstawowe zabiegi udrażniające drogi oddechowe Po stwierdzeniu niedrożności dróg oddechowych, niezależnie od stopnia jej zaawansowania, trzeba natychmiast wdrożyć działania przywracające i utrzymujące ich drożność. Aby poprawić drożność dróg oddechowych, gdy jest ona upośledzona przez język lub inne struktury górnych dróg oddechowych, stosuje się 3 rękoczyny: odgięcie głowy, uniesienie żuchwy i wysunięcie żuchwy. Odgięcie głowy i uniesienie żuchwy Ratownik kładzie rękę na czole pacjenta i delikatnie odgina głowę ku tyłowi. Opuszki palców drugiej ręki umieszcza na bródce pacjenta i delikatnie unosi ją, rozciągając struktury przedniej części szyi (ryc. 4.3) Wysunięcie żuchwy Wysunięcie żuchwy jest alternatywnym rękoczynem pozwalającym przemieścić żuchwę do przodu i znieść niedrożność spowodowaną przez zapadające się podniebienie miękkie i nagłośnię. Ratownik za pomocą palca wskazują- Ryc Odgięcie głowy i uniesienie żuchwy a) b) Ryc Wysunięcie żuchwy 4
125 124 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 cego i pozostałych palców umieszczonych za kątem żuchwy, wywiera na nią nacisk ku górze i przodowi. Używając kciuków, przemieszcza bródkę ku dołowi i delikatnie otwiera usta (ryc. 4.4). Te proste metody ułożeniowe są skuteczne w większości przypadków niedrożności spowodowanej spadkiem napięcia w obrębie tkanek miękkich. Jeżeli nie można przywrócić drożności dróg oddechowych, należy poszukiwać innej przyczyny. Widoczne w jamie ustnej ciała obce o stałej konsystencji należy wygarnąć palcem lub ewakuować za pomocą kleszczyków lub ssania. Należy usunąć złamane albo przemieszczone protezy zębowe. Protezy dobrze umocowane należy zostawić, ponieważ pomagają one zachować kontury jamy ustnej, a tym samym umożliwiają utrzymanie właściwej szczelności podczas wentylacji. Udrażnianie dróg oddechowych u pacjentów z podejrzeniem urazu szyjnego odcinka rdzenia kręgowego Jeżeli podejrzewa się obrażenia kręgosłupa (np. po upadku z wysokości, urazie głowy lub szyi, skoku do płytkiej wody), należy w czasie resuscytacji utrzymywać głowę, szyję, klatkę piersiową i okolicę lędźwiową w pozycji neutralnej. Nadmierne odgięcie głowy może pogłębić obrażenia i uszkodzić szyjny rdzeń kręgowy , jakkolwiek tego rodzaju powikłania nie zostały udokumentowane i względne ryzyko pozostaje nieznane. Jeśli istnieje podejrzenie uszkodzenia rdzenia w odcinku szyjnym kręgosłupa, udrożnienie górnych dróg oddechowych należy zapewnić poprzez uniesienie lub wysunięcie żuchwy w połączeniu z wykonywaną przez osobę asystującą ręczną stabilizacją w osi (Manual In-Line Stabilisation MILS) głowy i szyi 321,322. Gdy zagrażająca życiu niedrożność dróg oddechowych utrzymuje się nadal, mimo prawidłowo wykonanego uniesienia lub wysunięcia żuchwy, należy stopniowo odginać głowę do momentu uzyskania drożności. Zapewnienie drożności dróg oddechowych jest czynnością priorytetową w stosunku do potencjalnego uszkodzenia rdzenia kręgowego w odcinku szyjnym. Proste przyrządy do udrażniania dróg oddechowych Pomimo braku opublikowanych danych na temat zastosowania rurki nosowo-gardłowej i ustno-gardłowej podczas RKO, często pomagają one, a czasem są niezbędne do utrzymania drożności dróg oddechowych, szczególnie gdy resuscytacja się przedłuża. Aby utrzymać drogi oddechowe w osi, należy zachować odpowiednie ułożenie głowy i szyi. Zastosowanie u osób nieprzytomnych rurki ustno-gardłowej i nosowo-gardłowej zapobiega przemieszczaniu się ku tyłowi podniebienia miękkiego i języka, ale odgięcie głowy i wysunięcie żuchwy może być również wymagane. Rurka ustno-gardłowa Rurki ustno-gardłowe są dostępne w rozmiarach odpowiednich dla noworodków i osób dorosłych. Przybliżony rozmiar potrzebnej rurki uzyskuje się, dobierając jej długość do odległości w linii pionowej pomiędzy siekaczami pacjenta a kątem żuchwy. Najczęściej stosuje się rozmiar 2, 3 i 4 odpowiednio dla dorosłych o drobnej, średniej i masywnej budowie ciała. Ryc Założenie rurki ustno-gardłowej Jeżeli zachowane są odruchy z tylnej ściany gardła oraz odruchy krtaniowe, wprowadzenie rurki ustno-gardłowej może spowodować wymioty albo kurcz głośni. Dlatego prób założenia należy dokonywać tylko u nieprzytomnych pacjentów (ryc. 4.5). Rurka ustno-gardłowa może być niedrożna w następujących trzech okolicznościach 323 : część języka może zamykać koniec rurki, koniec rurki może utknąć w zachyłku, nagłośnia może zamykać rurkę. Rurka nosowo-gardłowa Pacjenci, którzy nie są głęboko nieprzytomni, tolerują rurkę nosowo-gardłową lepiej niż rurkę ustno-gardłową. Rurka nosowo-gardłowa może uratować życie pacjenta w przypadku szczękościsku czy urazów twarzoczaszki, gdy założenie rurki ustno-gardłowej jest niemożliwe. Niezamierzone wprowadzenie rurki nosowo-gardłowej do jamy czaszki przez szczelinę złamania w podstawie czaszki, jest możliwe, ale niezmiernie rzadkie 324,325. W przypadku gdy rozpoznaje się lub podejrzewa złamanie podstawy czaszki, zaleca się użycie rurki ustno-gardłowej, jeżeli jednak nie udaje się jej założyć, a drogi oddechowe są niedrożne, delikatnie wprowadzona rurka nosowo-gardłowa może uratować życie (tj. korzyści mogą znacznie przewyższać ryzyko). Rozmiary rurek są określone w milimetrach ich wewnętrznej średnicy, a ich długość wzrasta proporcjonalnie do średnicy. Tradycyjny sposób dobierania rozmiaru rurki nosowo-gardłowej (pomiar w stosunku do wielkości małego palca albo nozdrzy przednich) nie koreluje z anatomią dróg oddechowych i jest niewiarygodny 326. Dla dorosłych odpowiednie są rozmiary 6 i 7 mm. Zakładanie rurki może spowodować uszkodzenie śluzówki wyścielającej jamę nosową i w rezultacie krwawienie nawet w 30% przypadków 327. Jeśli rurka jest zbyt długa, może wywołać odruchy z tylnej ściany gardła i krtani i spowodować kurcz krtani lub wymioty.
126 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 125 Tlen Podczas RKO tlen należy stosować zawsze, gdy jest dostępny. Nie ma danych wskazujących optymalną saturację krwi tętniczej tlenem (SaO 2 ) podczas RKO. Są dane z badań na zwierzętach 328 oraz pewne dane z obserwacji klinicznych, wykazujące związek pomiędzy wysoką wartością SaO 2 po ROSC a gorszym wynikiem leczenia 329. Podając tlen przez standardową maskę tlenową można uzyskać stężenie tlenu do 50%, pod warunkiem że przepływ tlenu jest wystarczająco wysoki. Maska z rezerwuarem (bez oddechu zwrotnego) pozwala uzyskać stężenie tlenu w mieszaninie wdechowej do 85% przy przepływie l/min. Początkowo należy stosować możliwie najwyższe stężenie tlenu. Gdy tylko saturacja krwi tętniczej może być mierzona w sposób wiarygodny za pomocą pulsoksymetru (SpO 2 ) lub gazometrii krwi tętniczej, należy miareczkować wdechowe stężenia tlenu tak, aby osiągnąć saturację krwi tętniczej w zakresie 94 98%. Odsysanie Do usuwania płynnej treści (krew, ślina, treść żołądkowa) z górnych dróg oddechowych należy używać sztywnego cewnika do odsysania o szerokim świetle (Yankauer). Jeżeli pacjent ma zachowane odruchy z tylnej ściany gardła, odsysanie musi być przeprowadzane ostrożnie; drażnienie gardła może sprowokować wymioty. Wentylacja U każdego pacjenta, który nie oddycha lub którego spontaniczny oddech jest niewydolny, należy możliwie szybko rozpocząć sztuczną wentylację. Wentylacja powietrzem wydechowym ratownika (oddechy ratownicze) jest efektywna, ale stężenie tlenu w powietrzu wydychanym przez ratownika wynosi zaledwie 16 17%, dlatego tak szybko, jak to możliwe, trzeba ją zastąpić wentylacją z zastosowaniem powietrza wzbogaconego w tlen. Szeroko stosowana jest maska kieszonkowa, która jest podobna do maski anestezjologicznej i umożliwia wentylację metodą usta maska. Jest ona wyposażona w jednokierunkową zastawkę, która kieruje wydychane przez pacjenta powietrze z dala od ratownika. Maska jest przezroczysta, co umożliwia zauważenie pojawienia się wymiocin czy krwi u pacjenta. Niektóre maski są wyposażone w łącznik do podawania tlenu. Gdy stosuje się maski bez łącznika, suplementacja tlenu może się odbywać poprzez umieszczenie cewnika z tlenem pod maską, przy zapewnieniu prawidłowej szczelności. Aby maksymalnie zwiększyć szczelność z twarzą pacjenta, należy stosować technikę z użyciem dwóch rąk (ryc. 4.6). Jeżeli objętość oddechowa lub przepływ wdechowy są zbyt duże, generowane jest wysokie ciśnienie w drogach oddechowych, co predysponuje do rozdęcia żołądka i zwiększa ryzyko regurgitacji i aspiracji treści żołądkowej do płuc. Ryzyko rozdęcia żołądka zwiększają: nieprawidłowe ułożenie głowy i szyi i niedrożne drogi oddechowe, niewydolność zwieracza przełyku (występuje u wszystkich pacjentów z zatrzymaniem krążenia), wysokie ciśnienie wdechowe. Z drugiej strony, jeżeli przepływ wdechowy będzie zbyt mały, wydłuży to wdech i czas przeznaczony na uciskanie Ryc Wentylacja metodą usta maska klatki piersiowej ulega skróceniu. Na każdy wdech należy przeznaczyć około sekundy, a dostarczana objętość powinna wywołać prawidłowe uniesienie klatki piersiowej. Pozwala to osiągnąć kompromis pomiędzy dostarczeniem odpowiedniej objętości oddechowej przy minimalnym ryzyku rozdęcia żołądka a odpowiednią ilością czasu przeznaczoną na uciskanie klatki piersiowej. Gdy drogi oddechowe podczas RKO nie są zabezpieczone, należy wykonywać 2 oddechy po każdych 30 uciśnięciach klatki piersiowej. Worek samorozprężalny Worek samorozprężalny można połączyć z maską twarzową, rurką dotchawiczą lub nadgłośniowymi przyrządami do udrażniania dróg oddechowych (Supraglottic Airway Device SAD). Bez suplementacji tlenem worek samorozprężalny pozwala na wentylację płuc pacjenta powietrzem atmosferycznym (21% tlenu). Zastosowanie rezerwuaru i zwiększenie przepływu tlenu do około 10 l/min pozwala zwiększyć wdechowe stężenie tlenu do około 85%. Pomimo że worek samorozprężalny umożliwia wentylację wysokimi stężeniami tlenu, jego stosowanie przez jedną osobę wymaga odpowiednich umiejętności. Jeśli używa się go z maską twarzową, często trudno uzyskać szczelność pomiędzy maską a twarzą pacjenta i równocześnie utrzymywać, jedną ręką, drożność dróg oddechowych, podczas gdy druga ręka ściska worek 330. Każdy większy przeciek powietrza spowoduje hipowentylację, a gdy drogi oddechowe nie są drożne, powietrze może zostać wtłoczone do żołądka 331,332. Jeszcze bardziej zredukuje to wentylację i znacząco zwiększy ryzyko regurgitacji i aspiracji 333. Ucisk na chrząstkę pierścieniowatą może zmniejszyć to ryzyko 334,335, ale wymaga to udziału przeszkolonej osoby. Nieprawidłowo wykonany ucisk na chrząstkę pierścieniowatą może utrudnić wentylację płuc pacjenta 334, Zalecaną techniką wentylacji workiem i maską twarzową jest wentylacja wykonywana przez dwie osoby (ryc. 4.7). Jedna osoba obydwoma rękami utrzymuje położenie maski 4
127 126 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 Ryc Technika wentylacji za pomocą worka samorozprężalnego z maską twarzową wykonywana przez dwie osoby i wysuwa żuchwę, a asystująca uciska worek. Ten sposób pozwala uzyskać lepszą szczelność maski oraz efektywniejszą i bezpieczniejszą wentylację płuc pacjenta. Od momentu intubacji lub założenia nadgłośniowego przyrządu do udrażniania dróg oddechowych należy wentylować płuca z częstością 10 oddechów/min oraz kontynuować uciśnięcia klatki piersiowej bez przerw na wentylację. Szczelność nadgłośniowych przyrządów udrażniających wokół krtani prawdopodobnie będzie niewystarczająca, aby zapobiec w pełni przeciekowi powietrza, gdy wentylacja jest prowadzona z równoczesnymi uciśnięciami klatki piersiowej. Umiarkowany przeciek powietrza jest akceptowalny, zwłaszcza że większość tego powietrza wydostaje się na zewnątrz przez usta pacjenta. Jeżeli występuje duży przeciek upośledzający wentylację płuc pacjenta, należy przerywać uciskanie klatki piersiowej, tak aby ją umożliwić i utrzymywać sekwencję uciśnięć do wentylacji 30 : 2. Wentylacja mechaniczna Zaledwie kilka badań dotyczy wybranych aspektów wentylacji w trakcie zaawansowanych zabiegów resuscytacyjnych. Istnieją dane wskazujące, że częstość wentylacji prowadzonej przez personel medyczny w trakcie zatrzymania krążenia jest zbyt wysoka 242,340,341, chociaż inne badania wykazują prowadzenie wentylacji z prawidłową częstością 245,342,343. Automatyczne respiratory lub urządzenia do prowadzenia resuscytacji zapewniają stały przepływ gazów do pacjenta w czasie wdechu. Objętość, która zostanie dostarczona, zależy od czasu trwania wdechu (dłuższy okres pozwala uzyskać większą objętość oddechową). Ponieważ w czasie wdechu rośnie ciśnienie w drogach oddechowych, często urządzenia te są limitowane ciśnieniowo, aby zabezpieczyć płuca przed barotraumą. Automatyczne respiratory można stosować zarówno z maską twarzową, jak i innymi przyrządami do udrażniania dróg oddechowych (np. rurką dotchawiczą, SAD). Respiratory te należy początkowo ustawić tak, aby dostarczały objętość oddechową 6 7 ml/kg z częstością 10 oddechów/min. Niektóre respiratory mają na panelu sterowania oznaczenia umożliwiające łatwe i szybkie dostosowanie parametrów do wielkości pacjenta, inne dają możliwość wyszukanych wariantów wentylacji. Jeżeli pacjent ma zachowane spontaniczne krążenie, poprawność ustawionych parametrów ocenia się analizując gazometrię krwi tętniczej. W porównaniu z innymi metodami wentylacji stosowanie automatycznych respiratorów niesie wiele korzyści: U niezaintubowanych pacjentów ratownik ma obie ręce wolne, aby utrzymywać drożność dróg oddechowych i maskę. Jedną ręką można uciskać chrząstkę pierścieniowatą, podczas gdy druga szczelnie utrzymuje maskę na twarzy. U pacjentów zaintubowanych ratownik może wykonywać inne czynności 344. Po wstępnym ustawieniu respiratory pozwalają uzyskać stałą objętość oddechową, częstość oddechów oraz wentylację minutową i dlatego mogą pomóc uniknąć nadmiernej wentylacji. Za pomocą automatycznych respiratorów można utrzymywać niższe niż w czasie ręcznej wentylacji szczytowe ciśnienia wdechowe, co zmniejsza ciśnienie w klatce piersiowej i umożliwia poprawę powrotu żylnego, a tym samym rzutu serca. Badania symulowanych zatrzymań krążenia z wykorzystaniem manekinów oraz badania z udziałem strażaków, którzy prowadzili wentylację płuc u pacjentów poddanych znieczuleniu ogólnemu, wykazały znamienne zmniejszenie występowania rozdęcia żołądka, gdy stosowano inicjowany ręcznie, ograniczany przepływem, zasilany tlenem respirator wraz z maską, w porównaniu z zastosowaniem worka samorozprężalnego i maski 345,346. Jednak wpływ stosowania automatycznych respiratorów na rozdęcie żołądka u ludzi z zatrzymaniem krążenia nie został zbadany i nie ma żadnych danych wykazujących ich wyraźne korzyści w zestawieniu z wentylacją workiem samorozprężalnym z maską. Bierne dostarczanie tlenu Przy zachowanej drożności dróg oddechowych, wyłączne uciskanie klatki piersiowej związane jest z pewnego stopnia wentylacją płuc 347. Tlen może być dostarczany biernie, zarówno poprzez zaadaptowaną rurkę dotchawiczą (Boussignac tube) 348,349 lub poprzez połączenie rurki ustno-gardłowej ze standardową maską tlenową z rezerwuarem bezzwrotnym 350. Mimo że jedno badanie wykazało większą przeżywalność bez ubytków neurologicznych po pozaszpitalnym nagłym zatrzymaniu krążenia w mechanizmie VF przy użyciu biernego dostarczania tlenu (rurka ustno-gardłowa z maską tlenową) w porównaniu do wentylacji przy użyciu maski i worka, była to analiza retrospektywna i występuje w niej wiele elementów zaburzających wyniki badań 350. Brak jest wystarczającej ilości danych potwierdzających lub negujących poprawę odległych wyników leczenia przy użyciu biernego dostarczania tlenu podczas RKO w porównaniu z dostarczaniem tlenu z wykorzystaniem wentylacji dodatnimi ciśnieniami. Do czasu udostępnienia dalszych danych, bier-
128 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 127 Ryc Założenie maski krtaniowej ne dostarczanie tlenu bez wentylacji nie jest zalecane do rutynowego stosowania podczas RKO. Alternatywne przyrządy do udrażniania dróg oddechowych Intubacja dotchawicza jest powszechnie uważana za optymalną metodę zabezpieczania dróg oddechowych podczas zatrzymania krążenia. Są jednak dowody, że bez wystarczającego przeszkolenia i doświadczenia, częstość powikłań, takich jak nierozpoznana intubacja przełyku (6 17% w kilku badaniach z udziałem ratowników medycznych) i przemieszczenie rurki, jest niedopuszczalnie wysoka 355. Przedłużające się próby intubacji są szkodliwe. Przerwanie uciskania klatki piersiowej na czas intubacji upośledza przepływ wieńcowy i mózgowy. Do udrażniania dróg oddechowych w czasie RKO rozważono wykorzystanie kilku alternatywnych przyrządów. Opublikowano wyniki badań dotyczących zastosowania podczas RKO Combitube, klasycznej maski krtaniowej (clma), rurki krtaniowej (LT) oraz I-gel, ale siła statystyczna żadnego z tych badań nie była na tyle duża, aby można było analizować przeżywalność jako pierwotny punkt końcowy. Większość badaczy oceniała natomiast skuteczność dotyczącą zakładania i wentylacji za pomocą tych przyrządów. Nadgłośniowe przyrządy do udrażniania dróg oddechowych (SAD) są łatwiejsze do założenia niż rurka dotchawicza i w przeciwieństwie do intubacji mogą w większości przypadków być wprowadzone bez przerywania uciśnięć klatki piersiowej 356. Nie ma żadnych danych popierających rutynowe stosowanie któregokolwiek sposobu zabezpieczenia drożności dróg oddechowych podczas zatrzymania krążenia. O tym, która z technik będzie najlepsza, decydują określone okoliczności zatrzymania krążenia i kompetencje ratownika. Maska krtaniowa Maska krtaniowa (ryc. 4.8) jest szybciej i łatwiej zakładana niż rurka dotchawicza Użycie oryginalnej LMA (classic Laryngeal Mask Airway clma), która jest wielokrotnego użytku, zostało zbadane podczas RKO, ale żadne z tych badań nie porównywało jej bezpośrednio do rurki intubacyjnej. Różnorodne LMA jednokrotnego użytku są stosowane podczas RKO, ale różnią się one od klasycznej LMA i nie ma opublikowanych danych o ich wykorzystaniu w takich okolicznościach 365. Opisywana skuteczność wentylacji podczas RKO przy użyciu LMA jest bardzo wysoka dla badań wewnątrzszpitalnych (86 100%) , ale ogólnie mniej skuteczne (71 90%) jest użycie LMA w pozaszpitalnym zatrzymaniu krążenia. Przyczyna niezadawalających wyników zastosowania LMA w pozaszpitalnych zatrzymaniach krążenia pozostaje niejasna. Wykonywana przez niedoświadczony personel wentylacja płuc u znieczulonych pacjentów jest bardziej efektywna i prostsza przy użyciu LMA, niż worka samorozprężalnego z maską twarzową 330. Jeśli możliwe jest założenie LMA bez opóźnienia, preferowane jest unikanie wentylacji workiem samorozprężalnym z maską. W porównaniu z wentylacją workiem samorozprężalnym i maską, zastosowanie worka samorozprężalnego i LMA podczas zatrzymania krążenia zmniejsza częstość występowania regurgitacji 333. W jednym badaniu wykazano podobne wyniki gazometrii krwi tętniczej u pacjentów skutecznie zresuscytowanych po poza szpitalnym zatrzymaniu krążenia, gdzie stosowano zarówno maski krtaniowe, jak i worki z maską twarzową 373. W porównaniu z intubacją tchawicy, zauważalną wadą LMA jest zwiększone ryzyko aspiracji i niemożność zapewnienia adekwatnej wentylacji u pacjentów z niską podatnością płuc i/lub klatki piersiowej. Nie ma żadnych danych stwierdzających, czy prowadzenie skutecznej wentylacji przez LMA bez przerywania uciśnięć klatki piersiowej jest możliwe, czy nie. Zapewnienie adekwatnej wentylacji płuc podczas ciągłego uciskania klatki piersiowej może stanowić jedną z głównych korzyści intubacji. Istnieje zadziwiająco mało doniesień na temat zachłyśnięcia płuc w badaniach nad zastosowaniem LMA w czasie RKO. Combitube Combitube jest rurką o podwójnym świetle, wprowadzaną na ślepo wzdłuż krzywizny języka i umożliwiającą wentylację, jeśli trafi ona do przełyku. Przeprowadzono wiele badań dotyczących zastosowania Combitube w czasie RKO i skuteczną wentylację osiągnięto u 79 98% pacjentów 371, Dwa randomizowane badania porównujące zastosowanie Combitube i intubacji dotchawiczej w pozaszpitalnym zatrzymaniu krążenia nie wykazały różnic w przeżywalności 380,381. Zastosowanie Combitube zanika i w wielu rejonach świata jest ona zastępowana przez inne przyrządy, takie jak rurka krtaniowa. Rurka krtaniowa Rurka krtaniowa (Laryngeal Tube LT) została wprowadzona w 2001 roku (ryc. 4.9). W Stanach Zjednoczonych jest znana pod nazwą King LT. U znieczulonych pacjentów założenie LT jest łatwiejsze w porównaniu z klasyczną 4
129 128 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 Ryc Rurka krtaniowa 2010 ERC Ryc I-gel 2010 ERC LMA oraz ProSeal LMA 382,383. Już po dwóch godzinach ćwiczeń pielęgniarki skutecznie zakładały rurkę krtaniową oraz osiągnęły wentylację w 24 na 30 przypadków (80%) pozaszpitalnego zatrzymania krążenia 384. Dostępne są jednorazowe rurki krtaniowe (LT-D), które zostały skutecznie założone przez ratowników z wykształceniem medycznym w 92 przypadkach pozaszpitalnego zatrzymania krążenia (w 85 w pierwszej próbie, w 7 w drugiej) 385. W badaniach nad RKO na manekinach użycie LT-D znamiennie zmniejszyło czas bez przepływu w porównaniu z zastosowaniem rurki dotchawiczej 386. I-gel Mankiet maski I-gel jest wytworzony z termoplastycznego żelu elastomerowego, który nie wymaga wypełniania powietrzem. Trzon I-gel zawiera wbudowane zabezpieczenie przed przygryzieniem oraz wąski przewód do wprowadzenia sondy żołądkowej (ryc. 4.10). I-gel jest bardzo łatwy do założenia, wymaga to tylko niewielkiej praktyki, oraz umożliwia osiągnięcie ciśnienia szczelności na poziomie krtani na poziomie cm H 2 O 387,388. W dwóch badaniach na manekinach założenie I-gel przebiegało zdecydowanie szybciej w porównaniu do kilku innych przyrządów do udrażniania dróg oddechowych 356,389. Łatwość założenia I-gel i korzystne ciśnienie szczelności na poziomie krtani czynią z tego urządzenia teoretycznie bardzo atrakcyjny do zastosowania sprzęt do zaopatrzenia dróg oddechowych podczas resuscytacji, możliwy do użycia przez osoby z brakiem doświadczenia w intubacji dotchawiczej. Istnieją doniesienia o użyciu I-gel podczas zatrzymania krążenia, ale oczekiwane są dalsze badania dotyczące zastosowania I-gel w tych okolicznościach 390,391. Inne przyrządy do udrażniania dróg oddechowych Maska krtaniowa typu ProSeal Maskę krtaniową typu ProSeal (ProSeal LMA) poddano licznym badaniom z udziałem pacjentów znieczulanych ogólnie, ale nie ma badań dotyczących jej zastosowania w czasie RKO. Maska ta posiada kilka atrybutów, które teoretycznie sprawiają, że bardziej nadaje się do wykorzystania w czasie RKO niż klasyczna LMA: lepsza szczelność wokół krtani, umożliwiająca wentylację przy wyższych ciśnieniach w drogach oddechowych 392 ; wbudowany port żołądkowy, umożliwiający odsysanie zarzuconej do górnej części przełyku płynnej treści żołądkowej oraz pozwalający na wprowadzenie zgłębnika do żołądka i drenowanie płynnej treści żołądkowej; wbudowane wzmocnienie chroniące przed przygryzieniem. ProSeal LMA jest nieco trudniej założyć niż klasyczną LMA oraz jest stosunkowo droga. Wersją jednorazową ProSeal LMA jest SupremeLMA. Badania na znieczulonych pacjentach wskazują, że jest ona stosunkowo łatwa do założenia oraz umożliwia osiągnięcie ciśnień szczelności na poziomie krtani cm H 2 O Oczekuje się danych dotyczących zastosowania maski Supreme podczas zatrzymania krążenia. Intubacyjna maska krtaniowa Intubacyjna maska krtaniowa (Intubating Laryngeal Mask Airway ILMA) jest stosunkowo łatwa do założenia 396,397, ale już wprowadzenie przez nią na ślepo rurki intubacyjnej zwykle wymaga dłuższego przeszkolenia 398. Jedno badanie udokumentowało zastosowanie ILMA przez lekarzy udzielających pomocy przedszpitalnej po nieudanej intubacji za pomocą laryngoskopii bezpośredniej w 24 incydentach zatrzymania krążenia we Francji 399.
130 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 129 Intubacja tchawicy Nie ma wystarczających dowodów przemawiających za lub przeciw jakijkolwiek technice udrażniania dróg oddechowych i wentylacji w zatrzymaniu krążenia i oddychania u dorosłych. Mimo to intubacja tchawicy jest postrzegana jako optymalna metoda zapewnienia oraz utrzymania drożnych i zabezpieczonych dróg oddechowych. Powinna być stosowana tylko wtedy, gdy dostępny jest przeszkolony personel, posiadający wysokie umiejętności i pewność w tej procedurze. Aktualny systematyczny przegląd randomizowanych badań porównujących intubację dotchawiczą z alternatywnym udrażnianiem dróg oddechowych u ciężko chorych lub urazowych pacjentów wyodrębnił tylko trzy badania 400. Dwa dotyczyły porównania Combitube i intubacji dotchawiczej w pozaszpitalnym zatrzymaniu krążenia 380,381, które nie ujawniły różnic w przeżywalności. Trzecie randomizowane badanie dotyczyło porównania przedszpitalnie wykonywanej intubacji tchawicy w zestawieniu z wentylacją przy pomocy worka z maską u dzieci wymagających udrożnienia dróg oddechowych w przebiegu zatrzymania krążenia, pierwotnych zaburzeń oddychania lub wskutek ciężkich urazów 401. Nie zaobserwowano korzyści wynikających z intubacji dotchawiczej; przeciwnie, u dzieci wymagających udrożnienia dróg oddechowych, przydzielonych do grupy z intubacją, zaobserwowano niższą przeżywalność niż w grupie z wentylacją workiem z maską. Badanie OPALS (Ontario Prehospital Advanced Life Support) nie udokumentowało zwiększenia przeżywalności do wypisu ze szpitala, gdy do schematu BLS-AED dołączono umiejętność intubacji dotchawiczej i dożylną podaż leków stosowanych w resuscytacji 244. Korzyści związane z intubacją tchawicy w porównaniu z wentylacją workiem samorozprężalnym z maską twarzową obejmują: zapewnienie wentylacji bez przerywania uciśnięć klatki piersiowej 402 ; umożliwienie skutecznej wentylacji, zwłaszcza gdy podatność płuc i/lub klatki piersiowej jest mała; minimalizację rozdęcia żołądka i przez to także ryzyka regurgitacji; zabezpieczenie przed aspiracją treści żołądkowej do płuc, a także uwolnienie rąk ratownika do innych zadań. Wentylacja workiem samorozprężalnym i maską twarzową częściej spowoduje rozdęcie żołądka, teoretycznie zwiększając ryzyko regurgitacji i aspiracji. Nie ma jednak żadnych wiarygodnych danych wykazujących, że aspiracja zdarza się częściej w czasie zatrzymania krążenia u pacjentów wentylowanych workiem samorozprężalnym i maską twarzową w porównaniu z tymi wentylowanymi przez rurkę dotchawiczą. Zauważalne wady intubacji w porównaniu z wentylacją z użyciem worka samorozprężalnego i maski twarzowej obejmują: ryzyko nierozpoznania nieprawidłowego położenia rurki dotchawiczej, które u pacjentów z pozaszpitalnym zatrzymaniem krążenia występuje od 0,5% do 17% i wynosi u lekarzy medycyny ratunkowej 0,5% 403, a u ratowników medycznych 2,4% 404, 6% 351,352, 9% 353, 17% 354, przedłużony okres bez uciskania klatki piersiowej podczas prób intubacji. W badaniu dotyczącym przedszpitalnej intubacji wykonywanej przez ratowników z wykształceniem medycznym w czasie 100 zatrzymań krążenia całkowity czas trwania przerw w RKO związany z próbami intubacji tchawicy wynosił 110 sekund (IQR s; zakres s), a w 25% przerwy były dłuższe niż 3 minuty 405. Próby intubacji tchawicy były odpowiedzialne za prawie 25% wszystkich przerw w RKO, stosunkowo wysoką częstość niepowodzeń. Częstość powodzenia intubacji koreluje z doświadczeniem w jej wykonywaniu, zdobytym przez danego ratownika medycznego 406. Częstość niepowodzeń intubacji wynosi aż do 50% w systemach pomocy przedszpitalnej z małą ilością pacjentów, gdy osoby udzielające pomocy nie wykonują intubacji często 407,408. Personel ochrony zdrowia, który podejmuje próbę pozaszpitalnej intubacji, powinien brać udział w uporządkowanym, monitorowanym programie szkoleniowym, opartym na zrozumiałych kryteriach nabywania umiejętności, umożliwiającym ich odnawianie w regularny sposób. Ratownicy muszą rozważyć ryzyko i korzyści wynikające z intubacji i zestawić to z koniecznością prowadzenia efektywnych uciśnięć klatki piersiowej. Próby intubacji mogą wymagać pewnych przerw w uciskaniu klatki piersiowej, ale od momentu, gdy drogi oddechowe zostaną zabezpieczone przez rurkę dotchawiczą, przerwy na wentylacje nie będą konieczne. Personel posiadający umiejętności w zakresie zaawansowanych technik udrażniania dróg oddechowych powinien być w stanie wykonać laryngoskopię bez przerywania uciśnięć klatki piersiowej. Krótka przerwa może być wymagana w celu wsunięcia rurki między struny głosowe. Alternatywnie, aby uniknąć jakichkolwiek przerw w uciskaniu klatki piersiowej, można odroczyć próby intubacji do czasu powrotu spontanicznego krążenia 350,409. Żadna próba intubacji nie powinna powodować przerwania uciśnięć klatki piersiowej na dłużej niż 10 sekund, a jeśli intubacja nie jest osiągalna w tym czasie, należy podjąć wentylację workiem samorozprężalnym i maską. Po intubacji należy potwierdzić właściwe położenie rurki i odpowiednio ją zabezpieczyć. Potwierdzenie właściwego położenia rurki dotchawiczej Nierozpoznana intubacja przełyku jest najpoważniejszym powikłaniem w trakcie prób intubacji tchawicy. Rutynowe stosowanie pierwotnych i wtórnych technik potwierdzających prawidłowe położenie rurki dotchawiczej powinno zmniejszyć takie ryzyko. Ocena kliniczna Do pierwotnej oceny należy obserwacja symetrycznego poruszania się klatki piersiowej, osłuchiwanie pól płucnych obustronnie w liniach pachowych (szmery oddechowe powinny być symetryczne i dobrze słyszalne) i osłuchiwanie nadbrzusza (brak szmerów). Kliniczne objawy prawidłowego umieszczenia rurki (skraplanie pary w rurce, unoszenie się klatki piersiowej, szmer oddechowy w trakcie osłuchiwania płuc i brak odgłosów świadczących o wdmuchiwaniu powietrza do żołądka) nie są całkowicie wiarygodne. Opisywana czułość (proporcja intubacji tchawicy prawidłowo rozpoznanych) oraz swoistość (proporcja intubacji przełyku prawidłowo rozpoznanych) oceny klinicznej są różne: czułość %; swoistość % 403, Wtórne potwierdzenie położenia rurki dotchawiczej na podstawie wydychanego dwutlenku węgla albo detektora 4
131 130 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 przełykowego powinno zmniejszyć ryzyko nierozpoznanej intubacji przełyku, ale wiarygodność dostępnych przyrządów zasadniczo się różni. Ponadto żadna z wtórnych technik potwierdzających położenie rurki nie pozwala rozróżnić, czy rurka jest umieszczona prawidłowo w tchawicy, czy głębiej w głównym oskrzelu. Nie ma właściwych danych, aby wyłonić optymalną metodę potwierdzającą położenie rurki w czasie zatrzymania krążenia i wszystkie przyrządy należy traktować jako pomocnicze do innych technik potwierdzających 414. Nie ma też żadnych danych oceniających ich zdolność do monitorowania położenia rurki po wstępnym potwierdzeniu jej lokalizacji. Detektor przełykowy Detektor przełykowy wytwarza siłę ssącą na tchawiczym końcu rurki intubacyjnej poprzez podciąganie tłoka dużej strzykawki albo rozprężanie zgniecionej elastycznej gruszki. Powietrze z dolnych dróg oddechowych jest łatwe do zaaspirowania, gdy rurka znajduje się w tchawicy o sztywnym, chrzęstnym rusztowaniu. Jeśli rurka znajdzie się w przełyku, powietrza nie udaje się zaaspirować, ponieważ ściany przełyku zapadają się podczas prób aspiracji. Ocena za pomocą detektora przełykowego może być myląca u pacjentów z chorobliwą otyłością, w zaawansowanej ciąży, w ciężkiej astmie lub z obfitą wydzieliną w tchawicy. W tych warunkach tchawica może się zapadać podczas prób aspiracji 352,410, Zastosowanie strzykawkowego detektora przełykowego w identyfikacji położenia rurki intubacyjnej zostało opisane w pięciu badaniach dotyczących zatrzymania krążenia 352, : czułość wynosiła %, a swoistość %. Zastosowanie detektora gruszkowego w rozpoznawaniu położenia rurki zostało opisane w trzech badaniach dotyczących zatrzymania krążenia 410,415,421 : czułość wyniosła 71 75%, a swoistość %. Detektory dwutlenku węgla Detektor dwutlenku węgla (CO 2 ) pozwala mierzyć stężenie wydychanego z płuc dwutlenku węgla. Obecność dwutlenku węgla w powietrzu wydechowym po wykonaniu 6 oddechów wskazuje na umieszczenie rurki w tchawicy lub głównym oskrzelu 403. Potwierdzenie prawidłowego położenia rurki powyżej rozwidlenia tchawicy wymaga osłuchiwania klatki piersiowej obustronnie w liniach pachowych środkowych. Mówiąc ogólnie, wyróżnia się trzy rodzaje detektorów dwutlenku węgla: 1. Detektory kolorymetryczne końcowo-wydechowego dwutlenku węgla (end-tidal carbon dioxide ETCO 2 ) jednorazowego użytku, w których do wykrywania CO 2 stosuje się papierek lakmusowy i które generalnie dokonują odczytu fioletu (ETCO 2 <0,5%), brązu (ETCO 2 0,5 2%) i żółci (ETCO 2 >2%). W większości badań położenie rurki uważa się za zweryfikowane, gdy kolor brązowy utrzymuje się po kilku oddechach. Osiem badań dotyczących pacjentów z zatrzymaniem krążenia wykazało czułość detekcji położenia tchawiczego rurki intubacyjnej wynoszącą % oraz swoistość % przy identyfikacji położenia rurki poza tchawicą 258, 414,420, Mimo że detektory kolorymetryczne całkiem dobrze identyfikują położenie rurki intubacyjnej u pacjentów z dobrą perfuzją, to w przypadku zatrzymania krążenia przyrządy te są mniej dokładne niż ocena kliniczna, ponieważ przepływ krwi przez płuca może być tak niski, że ilość wydychanego dwutlenku węgla będzie niewystarczająca. Ponadto, jeśli rurka dotchawicza znajduje się w przełyku, wykonanie sześciu oddechów może doprowadzić do rozdęcia żołądka, wymiotów i aspiracji. 2. Elektroniczne przyrządy cyfrowe bez zapisu krzywej mierzą ETCO 2, stosując spektrometr podczerwieni, wyświetlają wyniki w postaci liczbowej. Nie generują one fali graficznej cyklu oddechowego na kapnografie. Pięć badań z zastosowaniem tych urządzeń użytych w celu identyfikacji położenia rurki dotchawiczej u pacjentów z zatrzymaniem krążenia wykazało ich % czułość i 100% swoistość 403,412,414,418,422, Detektory ETCO 2 z wyświetlaczem graficznej fali (kapnografy) są najbardziej wiarygodne w weryfikacji położenia rurki dotchawiczej podczas zatrzymania krążenia. Dwa badania dotyczące zastosowania kapnografii (graficzna fala ETCO 2 ) w weryfikacji położenia rurki dotchawiczej u osób z zatrzymaniem krążenia wykazały 100% czułość i 100% swoistość w identyfikacji prawidłowego położenia rurki 403,428. Trzy badania z całkowitą liczbą 194 dotchawiczych i 22 doprzełykowych intubacji wykazały zbiorczo 64% czułość i 100% swoistość w identyfikacji prawidłowego położenia rurki dotchawiczej za pomocą kapnografii u osób z pozaszpitalnym zatrzymaniem krążenia 410,415,421. Jednak w badaniach tych intubacja była wykonywana dopiero po przybyciu do szpitala (średni czas do wykonania intubacji wynosił ponad 30 minut) i u wielu z badanych osób z zatrzymaniem krążenia resuscytacja i czas transportu były przedłużone. W oparciu o dostępne dane należy stwierdzić, że dokładność kolorymetrycznych detektorów CO 2, detektorów przełykowych oraz kapnometrów bez zapisu krzywej nie jest większa od precyzji oceny towarzyszącej osłuchiwaniu i bezpośredniej ocenie wzrokowej w potwierdzaniu położenia rurki w tchawicy u osób z zatrzymaniem krążenia. Kapnografia z zapisem krzywej jest najbardziej czułym i swoistym sposobem potwierdzenia położenia i ciągłego monitorowania lokalizacji rurki dotchawiczej u osób z zatrzymaniem krążenia. Ten sposób oceny powinien stanowić uzupełnienie oceny klinicznej (osłuchiwanie i wzrokowe potwierdzenie obecności rurki między strunami głosowymi). Kapnografia z zapisem fali nie pozwala na rozróżnienie położenia rurki pomiędzy tchawicą a oskrzelem głównym kluczowe jest dokładne osłuchanie. Dostępne, przenośne monitory umożliwiające za pomocą kapnografii wstępne potwierdzenie, jak również ciągły monitoring położenia rurki intubacyjnej, są odpowiednie do zastosowania niezależnie od lokalizacji zdarzenia: pozaszpitalnie, w oddziale ratunkowym czy w różnych lokalizacjach szpitalnych, gdzie wykonywana jest intubacja. W przypadku braku tego typu urządzeń zastosowanie nadgłośniowych przyrządów udrażniających drogi oddechowe może być preferowane, gdy zaistnieje potrzeba użycia zaawansowanych technik udrażniających.
132 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 131 Opór klatki piersiowej Zmiany w oporze klatki piersiowej podczas wentylacji przełyku są mniejsze niż podczas wentylacji płuc Zmiany dotyczące oporu klatki piersiowej mogą być wykorzystywane do wykrywania wentylacji 432 i intubacji przełyku 402,433 podczas zatrzymania krążenia. Możliwe jest wykorzystanie tej technologii do pomiaru objętości oddechowej podczas RKO. Rola oporu klatki piersiowej jako narzędzia do wykrywania położenia rurki dotchawiczej i adekwatnej wentylacji podczas RKO jest poddawana dalszym badaniom. Na razie nie jest na tyle opracowana, by można ją było stosować rutynowo w praktyce klinicznej. Ucisk na chrząstkę pierścieniowatą U pacjentów bez zatrzymania krążenia ucisk na chrząstkę pierścieniowatą może w pewnym stopniu zabezpieczać drogi oddechowe przed aspiracją, ale może również upośledzić wentylację i zaburzać intubację. Rola ucisku na chrząstkę pierścieniowatą podczas zatrzymania krążenia nie została zbadana. Jej zastosowanie podczas wentylacji maską z workiem samorozprężalnym zmniejsza rozdęcie żołądka 334,335,434,435. Badania z udziałem znieczulonych pacjentów wskazują, że ucisk na chrząstkę pierścieniowatą u wielu z nich upośledza wentylację, zwiększa szczytowe ciśnienie wdechowe i powoduje całkowite zamknięcie dróg oddechowych w prawie 50% przypadków w zależności od siły nacisku na chrząstkę pierścieniowatą (w zakresie rekomendowanego skutecznego ciśnienia) , 436,437. Nie zaleca się rutynowego stosowania ucisku na chrząstkę pierścieniowatą w zatrzymaniu krążenia. Gdy jest używany podczas zatrzymania krążenia, a utrudnia wentylację lub intubację, nacisk powinien być odpowiednio dostosowany zmniejszony lub zwolniony. Zabezpieczenie rurki dotchawiczej Przypadkowe przemieszczenie się rurki dotchawiczej może zdarzyć się zawsze, ale jest bardziej prawdopodobne w czasie resuscytacji i transportu. Nie została jeszcze określona najskuteczniejsza metoda zabezpieczania rurki intubacyjnej. Należy stosować zwykłe plastry lub tasiemki, albo specjalnie do tego celu przeznaczone urządzenia mocujące. Konikotomia W sporadycznych przypadkach wentylacja nieoddychającego pacjenta workiem samorozprężalnym z maską będzie niemożliwa, jak również niemożliwe będzie wprowadzenie rurki dotchawiczej lub alternatywnych przyrządów do udrażniania dróg oddechowych. Może to wystąpić u pacjentów z rozległymi obrażeniami twarzy lub niedrożnością na poziomie krtani spowodowaną obrzękiem lub ciałem obcym. W tych okolicznościach dostarczenie tlenu za pomocą nakłucia igłą albo przecięcia błony pierścienno-tarczowej może być procedurą ratującą życie. W sytuacji nagłej tracheotomia jest przeciwwskazana, ponieważ jest czasochłonna, niebezpieczna, a także wymaga odpowiednich umiejętności chirurgicznych i sprzętu. Konikotomia umożliwia dostęp do dróg oddechowych i wentylację płuc pacjenta do czasu wykonania semi-elektywnej intubacji czy tracheotomii. Konikopunkcja jest procedurą tymczasową, zapewniającą jedynie przez krótki czas możliwość dostarczania tlenu. Do jej przeprowadzenia potrzebna jest kaniula o szerokim świetle, która się nie zagina, oraz źródło tlenu pod wysokim ciśnieniem. Technika ta niesie ze sobą ryzyko barotraumy i może być szczególnie nieskuteczna u pacjentów z urazem klatki piersiowej. Możliwość niepowodzenia w jej zastosowaniu wynika również z zaginania się kaniuli (zapadania się jej światła). Nie jest to metoda właściwa do użycia u pacjentów w czasie transportu. 4f Wspomaganie krążenia Leki i płyny w zatrzymaniu krążenia Rozdział ten omawia: leki stosowane w zatrzymaniu krążenia, leki antyarytmiczne i inne leki stosowane w okresie około zatrzymania krążenia, a także płyny i drogi podawania leków. Dołożono wszelkich starań, aby informacje podane w wytycznych były możliwie dokładne, jednakże to producenci leków dostarczają najbardziej aktualnych danych. Leki stosowane podczas leczenia zatrzymania krążenia Podczas natychmiastowego leczenia zatrzymania krążenia wskazane jest zastosowanie tylko kilku leków, a dane naukowe przemawiające za ich stosowaniem są ograniczone. Podaż leków należy rozważać tylko po wykonaniu uprzedniej defibrylacji (jeśli jest wskazana) i gdy podjęto już uciskanie klatki piersiowej i wentylację. Dowody naukowe dotyczące optymalnego czasu, kolejności podania oraz dawek leków są ograniczone. Istnieją trzy grupy leków właściwych do zastosowania w leczeniu zatrzymania krążenia i te leki poddano analizie podczas 2010 Consensus Conference. Są to: wazopresory, leki antyarytmiczne i inne leki. Poddano przeglądowi i dyskusji również inne, niż optymalna droga dożylna, drogi podania leków. Wazopresory Pomimo wciąż szerokiego zastosowania adrenaliny i wzrastającego, w niektórych krajach, stosowania wazopresyny podczas resuscytacji, nie opublikowano dotychczas badań z grupą kontrolną, gdzie stosowano placebo, które udowodniłyby, że rutynowe stosowanie któregokolwiek wazopresora podczas zatrzymania krążenia u ludzi zwiększa przeżycie do czasu wypisu ze szpitala, chociaż wykazano poprawę przeżycia krótkoterminowego 245,246. Głównym celem RKO jest zapewnienie przepływu krwi przez ważne dla życia narządy do czasu, aż przywrócone zostanie spontaniczne krążenie. Pomimo braku danych dotyczących zatrzymania krążenia u ludzi, nadal zaleca się stosowanie wazopresorów w celu zwiększenia perfuzji mózgowej i wieńcowej podczas RKO. Porównanie adrenaliny (epinefryny) i wazopresyny Adrenalina to sympatykomimetyk, który od 40 lat jest lekiem pierwszego rzutu w leczeniu zatrzymania krążenia 438. Jej działanie wynika z α-adrenergicznego, naczynioskurczo- 4
133 132 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 wego wpływu na krążenie systemowe, co zwiększa ciśnienie perfuzji wieńcowej i mózgowej. Co prawda β-adrenergiczne działanie adrenaliny (inotropowe i chronotropowe) może zwiększać przepływ wieńcowy i mózgowy, jednak równoczesny wzrost zużycia tlenu przez mięsień sercowy, wywoływanie ektopowych arytmii komorowych (szczególnie gdy mięsień sercowy jest zakwaszony) i przejściowa hipoksemia w następstwie przecieku płucnego, zaburzenia dotyczące mikrokrążenia 281 oraz dysfunkcja mięśnia sercowego występująca po zatrzymaniu krążenia 283,284 mogą zniwelować ten korzystny efekt. Ten potencjalnie niekorzystny efekt działania adrenaliny wywierany za pośrednictwem receptorów β spowodował poszukiwanie innych wazopresorów. Wazopresyna jest fizjologicznie występującym hormonem o działaniu antydiuretycznym. W bardzo dużych dawkach silnie obkurcza naczynia za pośrednictwem stymulacji receptorów V1 w mięśniach gładkich. Trzy randomizowane badania z grupą kontrolną oraz jedna metaanaliza 442 wykazały brak różnicy w wynikach końcowych (ROSC, przeżycie do wypisu ze szpitala lub powikłania neurologiczne) w grupie pacjentów otrzymujących odpowiednio wazopresynę lub adrenalinę jako wazopresor pierwszego rzutu w leczeniu zatrzymania krążenia. Dwa niedawno opublikowane badania porównujące stosowanie adrenaliny w monoterapii lub w skojarzeniu z wazopresyną także nie wykazały istotnych różnic w zakresie powrotu spontanicznego krążenia, przeżycia do wypisu ze szpitala lub występowania powikłań neurologicznych 443,444. Brak jest innych, w porównaniu z adrenaliną, alternatywnych leków wazopresyjnych, które stosowane podczas resuscytacji zwiększałyby przeżywalność po zatrzymaniu krążenia. Uczestnicy 2010 Consensus Conference, wykorzystując dostępne wyniki badań, szczegółowo analizowali zalecenia terapeutyczne. Pomimo braku danych świadczących o poprawie przeżycia długoterminowego, adrenalina pozostaje standardowym wazopresorem w zatrzymaniu krążenia. Uzgodniono, że aktualnie nie ma wystarczających dowodów naukowych, aby zalecać lub odrzucać stosowanie jakiegokolwiek innego leku wazopresyjnego w zatrzymaniu krążenia, niezależnie od jego rytmu, jako alternatywy dla adrenaliny lub łącznie z nią, w celu zwiększenia przeżywalności lub zmniejszenia powikłań neurologicznych. Obecnie przyjęta praktyka czyni adrenalinę podstawowym wazopresorem w leczeniu zatrzymania krążenia, niezależnie od jego mechanizmu. Mimo ograniczonej liczby dowodów przemawiających za korzyściami płynącymi ze stosowania adrenaliny, w niektórych badaniach wykazano poprawę przeżycia krótkoterminowego 245,246, co stanowi podstawę do jej dalszego stosowania, i chociaż brak jest dowodów klinicznych, w Wytycznych 2010 utrzymano rekomendacje dotyczące dawki i czasu podania adrenaliny. Adrenalina Wskazania Adrenalina jest pierwszym lekiem podawanym w zatrzymaniu krążenia niezależnie od jego przyczyny. Jest włączona w algorytm ALS, który zaleca jej użycie co 3 5 minut RKO (co drugą pętlę). Adrenalina jest lekiem preferowanym w leczeniu anafilaksji (zob. rozdział 8g) 294. Adrenalina jest lekiem drugiego rzutu w leczeniu wstrząsu kardiogennego. Dawkowanie Podczas zatrzymania krążenia wstępna dawka iv/io adrenaliny wynosi 1 mg. Brak jest badań raportujących poprawę przeżycia wynikającą ze stosowania wysokich dawek adrenaliny w przebiegu opornego na leczenie zatrzymania krążenia. W niektórych przypadkach w okresie po resuscytacji może zaistnieć potrzeba podawania adrenaliny we wlewie ciągłym. Po przywróceniu spontanicznego krążenia nawet małe dawki adrenaliny ( μg) mogą wywoływać tachykardię, niedokrwienie mięśnia sercowego, VT i VF. Od momentu przywrócenia rytmu dającego perfuzję, jeśli podanie adrenaliny uważa się za niezbędne, należy ostrożnie miareczkować dawkę do momentu uzyskania właściwego ciśnienia tętniczego. Dożylne dawki 50 μg są zwykle wystarczające u większości pacjentów z hipotensją. Szczególnej ostrożności wymaga stosowanie adrenaliny u pacjentów, u których zatrzymanie krążenia związane jest z nadużyciem kokainy lub innych środków sympatykomimetycznych. Zastosowanie Adrenalina jest dostępna najczęściej w dwóch rozcieńczeniach: 1 : (10 ml tego roztworu zawiera 1 mg adrenaliny), 1 : 1000 (1 ml tego roztworu zawiera 1 mg adrenaliny). Obydwa te roztwory są rutynowo stosowane w Europie. Leki antyarytmiczne Podobnie jak w przypadku wazopresorów, dowody naukowe na to, że stosowanie leków antyarytmicznych w zatrzymaniu krążenia przynosi korzyści, są ograniczone. Żaden z leków antyarytmicznych podawanych w czasie zatrzymania krążenia u ludzi nie wpłynął na poprawę przeżycia do wypisu ze szpitala, chociaż wykazano, że amiodaron zwiększa przeżycie do czasu przyjęcia do szpitala 285,286. Pomimo braku danych dotyczących odległych wyników leczenia u ludzi, analiza dowodów naukowych przemawia za stosowaniem leków antyarytmicznych w leczeniu arytmii występujących podczas zatrzymaniem krążenia. Amiodaron Amiodaron jest lekiem antyarytmicznym stabilizującym błony, który wydłuża czas trwania potencjału czynnościowego i okres refrakcji w kardiomiocytach przedsionków i komór. Dochodzi do zwolnienia przewodnictwa przedsionkowo-komorowego, a podobny efekt obserwuje się również w obrębie dodatkowych dróg przewodzenia. Amiodaron ma umiarkowane działanie inotropowo ujemne i powoduje rozszerzenie naczyń obwodowych poprzez niekompetycyjne blokowanie receptorów α. Hipotensja, która zdarza się podczas dożylnego podawania amiodaronu, zależy od szybkości wlewu i powodowana jest w większym stopniu przez rozpuszczalnik (Polysorbate 80 i alkohol benzylowy) uwalniający histaminę, niż przez sam lek 445. Zastosowanie wodne-
134 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 133 go preparatu amiodaronu, relatywnie pozbawionego tego rodzaju działań niepożądanych, zostało ostatnio zatwierdzone do użycia w Stanach Zjednoczonych 446, 447. W opornym na defibrylację VF amiodaron podany po 3 wstępnych wyładowaniach, w porównaniu z placebo 285 lub lidokainą 286, poprawia krótkoterminowe wyniki leczenia w postaci wzrostu przeżycia do przyjęcia do szpitala. Amiodaron wydaje się też poprawiać odpowiedź na defibrylację po zastosowaniu u ludzi lub zwierząt z VF lub niestabilnym hemodynamicznie VT Nie ma dowodów naukowych dotyczących optymalnego czasu, w którym amiodaron powinien być podany, gdy stosuje się strategię pojedynczych wyładowań. W badaniach klinicznych przeprowadzonych dotychczas amiodaron podawano, gdy VF/VT bez tętna utrzymywało się po wykonaniu co najmniej 3 defibrylacji. Z tego względu, wobec braku jakichkolwiek innych danych zaleca się podanie 300 mg amiodaronu, jeżeli VF/VT utrzymuje się po 3 wyładowaniach. Wskazania Amiodaron jest wskazany w następujących przypadkach: Oporne na leczenie VF/VT bez tętna. Hemodynamicznie stabilny VT i inne oporne tachyarytmie (zob. rozdział 4g). Dawkowanie Jeśli VF/VT utrzymuje się po 3 defibrylacjach, należy rozważyć dawkę wstępną amiodaronu 300 mg dożylnie, rozcieńczonego 5% glukozą (lub innym odpowiednim rozpuszczalnikiem) do objętości 20 ml (lub z ampułkostrzykawki). W przypadku utrzymującego się VT/VF należy podać kolejną dawkę amiodaronu wynoszącą 150 mg. Amiodaron podany do żyły obwodowej może spowodować zakrzepowe zapalenie żył. Gdy pacjent ma założony dostęp do żyły centralnej, lek należy podać tą drogą, jeżeli nie do dużej żyły obwodowej lub jamy szpikowej, a następnie obficie przepłukać. Szczegółowe informacje dotyczące zastosowania amiodaronu w leczeniu innych zaburzeń rytmu przedstawiono w rozdziale 4g. Kliniczne aspekty zastosowania Amiodaron może wywierać paradoksalne działanie arytmogenne, szczególnie jeśli jest stosowany równocześnie z innymi lekami wydłużającymi odstęp QT. Jednakże działanie to obserwuje się rzadziej niż w przypadku innych leków antyarytmicznych, gdy są stosowane w podobnych okolicznościach. Głównym, ostrym objawem ubocznym podaży amiodaronu jest hipotensja i bradykardia. Można im zapobiec, zmniejszając szybkość wlewu albo podając płyny i/lub leki o działaniu inotropowym. Działania uboczne związane z przewlekłym przyjmowaniem preparatów doustnych (zaburzenia czynności tarczycy, mikrozłogi w rogówce, neuropatia obwodowa, nacieki w płucach, wątrobie) nie mają znaczenia w doraźnym zastosowaniu w nagłych sytuacjach. Lidokaina Do czasu opublikowania Wytycznych 2000 ILCOR była lekiem z wyboru. Badania porównawcze z amiodaronem 286 spowodowały przesunięcie jej z tej pozycji i lidokaina obecnie jest zalecana tylko wtedy, gdy amiodaron jest niedostępny. Amiodaron powinien być dostępny w sytuacji leczenia przez personel medyczny we wszystkich szpitalnych oraz poza szpitalnych nagłych zatrzymaniach krążenia. Lidokaina jest lekiem antyarytmicznym stabilizującym błony, który działa przez wydłużenie okresu refrakcji miocytów. Powoduje ona zmniejszenie automatyzmu komór, a jej działanie znieczulające miejscowo hamuje ich ektopową aktywność. Lidokaina hamuje aktywność zdepolaryzowanych, arytmogennych tkanek, podczas gdy minimalnie wpływa na aktywność elektryczną tkanek prawidłowych. Dlatego jest skuteczna w hamowaniu arytmii z depolaryzacją (np. niedokrwienie, zatrucie digoksyną), a stosunkowo mało skuteczna w zwalczaniu arytmii związanych z normalną polaryzacją komórek (np. migotanie/trzepotanie przedsionków). Lidokaina podnosi próg migotania komór. Zatrucie lidokainą powoduje parestezje, senność, splątanie oraz zrywania mięśniowe, które mogą narastać do wystąpienia drgawek. Powszechnie uważa się, że bezpieczna dawka lidokainy nie może przekraczać 3 mg/kg w ciągu 1. godziny. Gdy pojawią się objawy zatrucia, należy natychmiast przerwać wlew leku i leczyć drgawki, jeśli wystąpią. Lidokaina powoduje depresję funkcji miokardium, ale w znacznie mniejszym stopniu niż amiodaron. Zjawisko to jest zwykle przejściowe i może być leczone podażą płynów i wazopresorów. Wskazania Lidokaina jest wskazana w opornym na leczenie VF/ VT (gdy amiodaron nie jest dostępny). Dawkowanie W przypadku VF/VT opornych na trzykrotną defibrylację, gdy amiodaron nie jest dostępny, należy rozważyć wstępną dawkę 100 mg lidokainy (1 1,5 mg/kg). W razie potrzeby można dodatkowo podać bolus 50 mg. Całkowita dawka nie powinna przekroczyć 3 mg/kg w czasie pierwszej godziny leczenia. Kliniczne aspekty zastosowania Lidokaina jest metabolizowana w wątrobie i okres jej półtrwania jest przedłużony przy obniżeniu przepływu krwi przez wątrobę np. w przypadku niskiego rzutu serca, chorób wątroby czy w podeszłym wieku. W czasie zatrzymania krążenia nie funkcjonują prawidłowe mechanizmy klirensu, stąd po pojedynczej dawce leku jego stężenie w osoczu może być wysokie. Po 24 godzinach ciągłego wlewu osoczowy okres półtrwania znamiennie się wydłuża. W tej sytuacji należy redukować dawki i regularnie analizować wskazania do kontynuacji terapii. Lidokaina jest mniej skuteczna w obecności hipokaliemii i hipomagnezemii, wobec czego jak najszybciej należy wyrównywać te zaburzenia. Magnez Magnez jest ważnym składnikiem wielu układów enzymatycznych, w szczególności tych, które są związane z generowaniem ATP przez mięśnie. Odgrywa on ważną rolę w procesach transmisji neurochemicznej, gdyż zmniejsza uwalnianie acetylocholiny i obniża wrażliwość płytki nerwowo-mięśnio- 4
135 134 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 wej. Magnez poprawia skurczową odpowiedź ogłuszonego miokardium i zmniejsza obszar zawału poprzez mechanizm, który nie jest jeszcze do końca wyjaśniony 451. Prawidłowe stężenie magnezu w osoczu wynosi 0,8 1,0 mmol/l. Hipomagnezemia jest często skojarzona z hipokaliemią i może wpływać na występowanie zaburzeń rytmu i zatrzymania krążenia. Hipomagnezemia zwiększa wychwyt digoksyny przez mięsień sercowy i obniża aktywność komórkowej Na + /K + ATP-azy. U pacjentów z hipomagnezemią, hipokaliemią lub przy współistnieniu tych zaburzeń, digoksyna nawet w stężeniach terapeutycznych może wywierać działanie kardiotoksyczne. Niedobór magnezu jest nierzadko spotykany u pacjentów hospitalizowanych i często współistnieje z innymi zaburzeniami elektrolitowymi, szczególnie hipokaliemią, hipofosfatemią, hiponatremią i hipokalcemią. Mimo że pozytywne skutki wynikające z podawania magnezu w stanach jego niedoboru są znane, to nie udowodniono korzyści z rutynowego podawania magnezu podczas zatrzymania krążenia. Badania dotyczące dorosłych pacjentów przeprowadzane w warunkach poza- i wewnątrzszpitalnych ,452 nie wykazały zwiększenia częstości ROSC po rutynowym podaniu magnezu w trakcie RKO. Wskazania Siarczan magnezu jest wskazany w następujących przypadkach: Tachyarytmie komorowe lub nadkomorowe związane z hipomagnezemią Torsades de pointes Zatrucie digoksyną. Dawkowanie Należy podać dawkę początkową 2 g dożylnie (4 ml [8 mmol] 50% siarczanu magnezu) do naczynia obwodowego, w czasie 1 2 minut. Można ją powtórzyć po minutach. Preparaty zawierające roztwór siarczanu magnezu różną się między sobą w krajach europejskich. Kliniczne aspekty zastosowania Pacjenci z hipokaliemią mają często hipomagnezemię. Jeżeli wystąpi tachyarytmia komorowa, dożylna podaż magnezu jest skutecznym i bezpiecznym sposobem leczenia. Rola magnezu w ostrym zawale mięśnia sercowego ciągle budzi wątpliwości. Magnez jest wydalany przez nerki, lecz nawet w niewydolności nerek objawy niepożądane związane z hipermagnezemią należą do rzadkości. Magnez hamuje skurcze mięśni gładkich, co powoduje wazodylatację i zależną od dawki hipotensję. Zwykle jest to efekt przejściowy, dobrze odpowiadający na przetaczanie płynów i wazopresory. Inne leki Brak jest dowodów, że rutynowe stosowanie innych leków (np. atropiny, prokainamidu, bretylium, wapnia i hormonów) podczas zatrzymania krążenia u ludzi powoduje wzrost przeżywalności do wypisu ze szpitala. Zalecenia dotyczące stosowania tych leków opierają się na ograniczonej ilości badań klinicznych, aktualnym rozumieniu farmakodynamicznych właściwości tych leków oraz patofizjologii zatrzymania krążenia. Atropina Atropina antagonizuje działanie parasympatycznego neurotransmitera acetylocholiny na receptory muskarynowe. Dzięki temu blokuje wpływ nerwu błędnego zarówno na węzeł zatokowo-przedsionkowy (sinoatrial SA), jak i przedsionkowo-komorowy (atrioventricular AV), zwiększając automatyzm węzła zatokowego i ułatwiając przewodzenie w węźle AV. Występowanie objawów ubocznych po podaniu atropiny (zaburzenia widzenia, suchość w jamie ustnej, retencja moczu) zależy od dawki i nie ma znaczenia w trakcie zatrzymania krążenia. Po podaniu dożylnym może dochodzić do ostrych stanów splątania, szczególnie u osób w podeszłym wieku. Poszerzenie źrenic obecne po zatrzymaniu krążenia nie powinno być traktowane wyłącznie jako następstwo podania atropiny. Asystolia podczas zatrzymania krążenia wynika zwykle z pierwotnej patologii mięśnia sercowego, a nie nadmiernego napięcia nerwu błędnego i nie ma żadnych badań dowodzących, że rutynowe stosowanie atropiny jest korzystne w leczeniu asystolii lub PEA. W kilku ostatnio przeprowadzonych badaniach nie udowodniono jakichkolwiek korzyści ze stosowania atropiny w pozaszpitalnych i wewnątrzszpitalnych zatrzymaniach krążenia 244, Nie zaleca się już rutynowego stosowania atropiny w leczeniu asystolii lub PEA. Atropina jest zalecana w następujących przypadkach: Bradykardia zatokowa, przedsionkowa lub węzłowa, powodująca niestabilność hemodynamiczną (zob. rozdział 4g). Wapń Wapń odgrywa życiowo ważną rolę w procesach komórkowych leżących u podstawy aktywności skurczowej mięśnia sercowego. Brak danych potwierdzających korzystne działanie wapnia w większości przypadków zatrzymania krążenia 453, , przeciwnie niektóre badania wykazały możliwość wystąpienia działań niepożądanych po rutynowym podaniu wapnia podczas leczenia zatrzymania krążenia (niezależnie od mechanizmu) 464,465. Wysokie stężenie wapnia w osoczu osiągane po podaniu w iniekcji dożylnej może mieć niekorzystny wpływ na niedokrwiony mięsień sercowy i nasilić uszkodzenie mózgu. Wapń należy podawać podczas resuscytacji tylko wtedy, gdy istnieją konkretne wskazania, np. w przypadku aktywności elektrycznej bez tętna spowodowanej przez: Hiperkaliemię Hipokalcemię Zatrucie blokerami kanału wapniowego. Początkową dawkę 10 ml 10% chlorku wapnia (6,8 mmol Ca 2+ ) można w razie potrzeby powtórzyć. Wapń może zwolnić czynność serca i wywołać arytmię. W zatrzymaniu krążenia można podać go dożylnie w postaci szybkiego wstrzyknięcia. Jeśli krążenie jest zachowane, zaleca się wolniejsze podawanie. Nie należy podawać roztworów wapnia i wodorowęglanu sodu równocześnie przez to samo wkłucie. Bufory Zatrzymanie krążenia powoduje mieszaną kwasicę oddechową i metaboliczną w następstwie ustania wymiany ga-
136 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 135 zowej w płucach i przejścia metabolizmu komórek na tor beztlenowy. Najlepszym sposobem leczenia kwasicy wywołanej zatrzymaniem krążenia jest uciskanie klatki piersiowej, pewne dodatkowe korzyści przynosi wentylacja. Podczas zatrzymania krążenia wartości gazometrii krwi tętniczej mogą być mylące i wykazywać niewielki związek ze stanem równowagi kwasowo-zasadowej tkanek 292. Analiza krwi z żyły centralnej pozwala lepiej ocenić ph tkanek (zob. rozdział 4d). Z wodorowęglanu sodu uwalniania się dwutlenek węgla, który szybko dyfunduje do komórek, w efekcie dochodzi do: Nasilenia kwasicy wewnątrzkomórkowej Działania inotropowo ujemnego na niedokrwiony mięsień sercowy Obciążenia dużym, osmotycznie aktywny ładunkiem sodu już niewydolnego krążenia i mózgu Przesunięcia w lewo krzywej dysocjacji hemoglobina tlen, co dodatkowo utrudnia uwalnianie tlenu w tkankach. Łagodna kwasica prowadzi do rozszerzenia łożyska naczyniowego i może zwiększyć przepływ krwi przez mózg. Z tego względu pełna korekta ph krwi tętniczej może teoretycznie zmniejszyć mózgowy przepływ krwi w szczególnie krytycznym momencie. Ponieważ jon dwuwęglanowy jest wydalany jako dwutlenek węgla przez płuca, należy zwiększyć wentylację. W kilku badaniach na zwierzętach oraz obserwacjach klinicznych poddano analizie zastosowanie buforów w czasie zatrzymania krążenia. Badania kliniczne z użyciem Tribonate 467 lub wodorowęglanu sodu jako buforów nie wykazały żadnych zalet płynących z ich zastosowania Tylko w dwóch badaniach stwierdzono kliniczną korzyść, sugerując, że w systemach ratownictwa medycznego, gdzie stosowano wodorowęglan na wcześniejszym etapie leczenia, częściej osiągnięto znamiennie wyższą liczbę ROSC i zwiększono przeżywalność do wypisu ze szpitala wraz ze zmniejszeniem liczby powikłań neurologicznych 473,474. Ogólnie biorąc, badania na zwierzętach nie przyniosły konkluzji, ale niektóre z nich wykazały korzyści z podania wodorowęglanów w przypadku kardiotoksycznego (hipotensja, arytmie) działania wynikającego z zatrucia trójcyklicznymi lekami antydepresyjnymi i innymi blokerami szybkich kanałów sodowych (rozdział 8b) 294,475. Nie jest zalecane rutynowe stosowanie wodorowęglanu sodu podczas zatrzymania krążenia i RKO lub po powrocie spontanicznego krążenia. Należy rozważyć zastosowanie wodorowęglanu sodu w przypadku: Zagrażającej życiu hiperkaliemii Zatrzymania krążenia w przebiegu hiperkaliemii Zatrucia trójcyklicznymi lekami przeciwdepresyjnymi. Podaje się 50 mmol (50 ml roztworu 8,4%) wodorowęglanu sodu dożylnie. Dawkę powtarza się w zależności od potrzeby, na podstawie badania równowagi kwasowo-zasadowej (tętniczej lub z żyły głównej czy aspiratu szpiku kostnego przy dostępie io). Wynaczynienie stężonego roztworu wodorowęglanu sodu do tkanki podskórnej może doprowadzić do jej poważnego uszkodzenia. Roztworu wodorowęglanu sodu nie wolno mieszać z solami wapnia, ponieważ powoduje to wytrącanie się węglanu wapnia. Fibrynoliza w trakcie RKO Formowanie się skrzepliny jest częstą przyczyną zatrzymania krążenia. Jest to zwykle spowodowane niedokrwieniem mięśnia sercowego wywołanym przez skrzeplinę zwężającą światło naczynia wieńcowego, ale niekiedy przyczyną jest przemieszczenie skrzepliny powstałej w naczyniach żylnych skutkując zatorowością płucną. Przeprowadzono kilka badań mających na celu ocenę użycia leków fibrynolitycznych w celu rozpuszczenia skrzepliny w tętnicy wieńcowej i płucnej. Wykazano również korzystny wpływ fibrynolityków na krążenie mózgowe w badaniach dotyczących zatrzymania krążenia u zwierząt 476,477, a doniesienia kliniczne wykazały mniejszą ilość encefalopatii anoksemicznych po zastosowaniu trombolityków podczas RKO 478. Kilka badań poświęcono ocenie zastosowania trombolityków w czasie zatrzymania krążenia niezwiązanego z urazem i opornego na standardowe postępowanie 307, W kilku z nich zaobserwowano nieznamienny statystycznie wzrost przeżywalności do wypisania ze szpitala 307,481 i zwiększenie przeżywalności w OIT 478. Spośród kilku doniesień serie przypadków klinicznych na temat stosowania trombolityków opisano 3 przypadki przeżycia do wypisu ze szpitala. Dotyczyły one opornych na standardowe leczenie zatrzymań krążenia w mechanizmie VF lub PEA 485. Przeciwne wyniki otrzymano w 2 dużych badaniach 486,487, w których nie wykazano znaczących korzyści ze stosowania fibrynolizy w przypadkach pozaszpitalnego zatrzymania krążenia, opornego na wstępne leczenie. Wyniki stosowania leków fibrynolitycznych u pacjentów z zatrzymaniem krążenia i podejrzeniem zatoru tętnicy płucnej są zróżnicowane. Metaanaliza dotycząca pacjentów z zatrzymaniem krążenia z powodu zatoru tętnicy płucnej wykazała, iż stosowanie leków fibrynolitycznych zwiększa ilość ROSC, poprawia przeżywalność do wypisu ze szpitala oraz neurologiczne wyniki leczenia 488. Kilka innych badań wykazało wzrost ROSC i liczby przyjęć do szpitala lub oddziału intensywnej terapii, lecz bez wpływu na przeżycie bez istotnych powikłań neurologicznych do wypisania ze szpitala 307, , 483, 484, Mimo że przeprowadzone badania kliniczne z relatywnie małą liczebnością grupy badanej 307,479,481,490 oraz analiza serii przypadków klinicznych 478, 485, nie wykazały wzrostu ilości powikłań krwotocznych w przebiegu stosowania trombolityków podczas RKO w zatrzymaniu krążenia niezwiązanym z urazem, to w niedawno opublikowanym dużym badaniu 487 i metaanalizie 488 wykazano zwiększone ryzyko wystąpienia krwawienia śródczaszkowego w przypadku pacjentów leczonych rutynowo fibrynolizą w przebiegu zatrzymania krążenia niezwiązanego z urazem. Skuteczna terapia fibrynolityczna podczas RKO wiąże się zwykle z korzystnym rokowaniem neurologicznym 488,490,491. Fibrynoliza nie powinna być rutynowo stosowana w leczeniu zatrzymania krążenia. Należy rozważyć tego typu terapię, gdy istnieje podejrzenie lub udowodniono ostry zator tętnicy płucnej. Po zastosowaniu trombolizy w zatrzymaniu krążenia wynikającym z ostrej zatorowości płucnej przeżycie połączone z dobrym efektem neurologicznym było opisywane w przypadkach wymagających ponad 60-minutowej RKO. Po podaniu leków fibrynolitycznych w wyżej 4
137 136 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 opisanych okolicznościach przed zakończeniem czynności resuscytacyjnych należy rozważyć prowadzenie przynajmniej minutowej resuscytacji 496,497. Śmiertelność w grupie pacjentów z zatrzymaniem krążenia, których poddano embolektomii chirurgicznej jest wysoka. Z tego powodu powinno unikać się wykonywania tego zabiegu u osób wymagających RKO. U pacjentów niebędących kandydatami do terapii fibrynolitycznej należy rozważyć mechaniczną tromboembolektomię przezskórną. Trwająca RKO nie jest przeciwwskazaniem do stosowania fibrynolizy. Dożylna płynoterapia Hipowolemia jest jedną z potencjalnie odwracalnych przyczyn zatrzymania krążenia. W przypadku podejrzenia hipowolemii należy szybko przetaczać płyny. Nie wykazano korzyści ze stosowania koloidów we wstępnej fazie resuscytacji, należy więc używać roztworu soli fizjologicznej lub roztworu Hartmanna (izotoniczny roztwór elektrolitowy buforowany mleczanem przyp. tłum.). Należy unikać stosowania roztworów glukozy, która szybko przemieszcza się poza łożysko naczyniowe i powoduje hiperglikemię, co może pogorszyć rokowania dotyczące powikłań neurologicznych po zatrzymaniu krążenia Rutynowa płynoterapia podczas zatrzymania krążenia jest kontrowersyjna. Nie ma dostępnych danych dotyczących porównania rutynowego podawania płynów, z postępowaniem bez płynoterapii u pacjentów z zatrzymaniem krążenia w przebiegu normowolemii. W dwóch badaniach na zwierzętach 506,507 wykazano, że wzrost ciśnienia w prawym przedsionku w odpowiedzi na podawanie normotermicznych płynów podczas RKO powoduje zmniejszenie ciśnienia perfuzji naczyń wieńcowych. W innym badaniu z udziałem zwierząt 508 ciśnienie perfuzji naczyń wieńcowych wzrastało po podaniu adrenaliny w trakcie RKO, ale nie obserwowano dalszego wzrostu po podaniu płynów. Badania kliniczne z udziałem małej grupy pacjentów nie wykazały korzyści ze stosowania roztworów hipertonicznych 509 lub płynów schłodzonych 510, 511. W jednym badaniu z udziałem zwierząt wykazano, że podaż hipertonicznego roztworu chlorku sodu zwiększała przepływ mózgowy podczas RKO 512. Należy zapewnić normowolemię, ale wobec braku hipowolemii podaż nadmiernej ilości płynów może być szkodliwa 513. Wskazane jest stosowanie płynów w celu przyspieszenia dotarcia do krążenia centralnego leków podanych obwodowo. Alternatywne drogi podawania leków Dostęp doszpikowy Jeśli w ciągu dwóch pierwszych minut resuscytacji nie uda się uzyskać dostępu dożylnego, należy rozważyć uzyskanie dostępu do jamy szpikowej (io). Dostęp doszpikowy był tradycyjne stosowany u dzieci z powodu trudności z dostępem dożylnym. Został on obecnie uznany za bezpieczny i skuteczny dostęp donaczyniowy także w grupie pacjentów dorosłych 271, Miejsca dostępu zlokalizowane na kości piszczelowej i ramiennej są łatwo osiągalne i zapewniają porównywalną szybkość przetaczania płynów 514. Doszpikowa podaż leków stosowanych w trakcie resuscytacji pozwala osiągnąć ich odpowiednie stężenia w osoczu. Kilka badań wykazało, że dostęp doszpikowy pozwala bezpiecznie i skutecznie prowadzić resuscytację płynową i podaż leków 269, Leki podawane przez rurkę dotchawiczą Leki stosowane w resuscytacji mogą być również podawane przez rurkę dotchawiczą, ale osoczowe stężenie leków dostarczonych tą drogą jest zmienne i znacznie niższe od stężenia osiąganego poprzez podanie dożylne lub doszpikowe, szczególnie w przypadku adrenaliny. Ponadto relatywnie duża objętość płynów podanych dotchawiczo pogarsza wymianę gazową. W związku z łatwością uzyskania dostępu doszpikowego i brakiem skuteczności leków podawanych dotchawiczo, podaż leków drogą dotchawiczą nie jest już więcej zalecana. Techniki i urządzenia do prowadzenia RKO Standardowo wykonywana, manualna RKO w najlepszym wypadku generuje jedynie 30% prawidłowej perfuzji wieńcowej i mózgowej 525. Istnieje kilka technik i urządzeń stosowanych w czasie RKO, które mogą w wybranych przypadkach poprawić hemodynamikę i krótkoterminową przeżywalność, pod warunkiem że zostaną zastosowane przez właściwie przeszkolony personel. Powodzenie danej techniki lub urządzenia zależy od edukacji i wyszkolenia ratowników oraz dostępności zasobów, również ludzkich. W określonych grupach ratowników te nowatorskie techniki i urządzenia mogą być lepsze od standardowej RKO. Trzeba zwrócić jednak uwagę, że urządzenie lub technika zapewniająca dobrej jakości RKO, kiedy używane są przez wysoce wykwalifikowany personel lub w warunkach testowych, mogą skutkować niską jakością i częstymi przerwami w RKO, gdy zostaną użyte w niekontrolowanych warunkach klinicznych 526. Pomimo braku rekomendacji dla rutynowego użycia jakiegokolwiek urządzenia wspomagającego krążenie zamiast manualnej RKO, niektóre z nich są stosowane rutynowo zarówno w szpitalach, jak i poza nimi. Jeżeli dobrze wyszkoleni ratownicy stosują urządzenia do prowadzenia RKO, rozważnym jest, by było to prowadzone pod nadzorem, aby zapewnić, że zastosowanie urządzenia nie wpływa negatywnie na przeżycie pacjentów. Chociaż manualne wykonywanie uciskania klatki piersiowej jest często bardzo niskiej jakości , nie wykazano, by którekolwiek z urządzeń było jednoznacznie lepsze od tej techniki. Bezpośredni masaż serca Stosowanie RKO przy otwartej klatce piersiowej daje lepsze ciśnienie perfuzji wieńcowej niż standardowa RKO 530. Metoda ta może być wskazana u pacjentów z zatrzymaniem krążenia w wyniku urazu, we wczesnej fazie po operacji kardiochirurgicznej 531,532 (zob. rozdział 8i) 294 lub gdy klatka piersiowa czy jama brzuszna (dostęp przezprzeponowy) są już otwarte w trakcie operacji, np. u pacjenta z mnogimi obrażeniami ciała. Naprzemienne uciskanie jamy brzusznej podczas RKO Technika naprzemiennego uciskania jamy brzusznej (IAC-CPR Interposed Abdominal Compression) polega na uciskaniu nadbrzusza podczas fazy relaksacji uciskania
138 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 137 klatki piersiowej 533,534. Powoduje to poprawę powrotu żylnego podczas RKO 535, 536 oraz zwiększa ilość ROSC i krótkoterminową przeżywalność 537,538. W dwóch badaniach wykazano poprawę przeżywalności do wypisu ze szpitala przy stosowaniu IAC-CPR w porównaniu ze standardową RKO w wewnątrzszpitalnych zatrzymaniach krążenia 537,538, ale inne badanie nie wykazało tej korzyści 539. RKO z zastosowaniem aktywnej kompresji dekompresji (ACD-CPR) Aktywna kompresja dekompresja (ACD-CPR Active Compression-Decompression) polega na stosowaniu urządzenia trzymanego w rękach ratownika, wyposażonego w przyssawkę pomagającą unieść aktywnie przednią ścianę klatki piersiowej podczas fazy relaksacji uciskania klatki piersiowej. Obniżenie ciśnienia wewnątrz klatki piersiowej w fazie dekompresji zwiększa powrót żylny, powodując zwiększenie rzutu serca i następowo ciśnienia perfuzji w naczyniach wieńcowych i mózgowych w trakcie fazy kompresji Wyniki stosowania ACD-CPR są różne, w niektórych badaniach klinicznych wykazano poprawę parametrów hemodynamicznych w porównaniu ze standardową RKO 541, , w innych zaś nie 546. W 3 randomizowanych badaniach 545,547,548 użycie ACD-CPR poprawiło odległą przeżywalność po pozaszpitalnym zatrzymaniu krążenia, w 5 innych badaniach tego typu nie wykazano żadnej różnicy w przeżywalności Skuteczność ACD-CPR może być w dużym stopniu zależna od jakości i czasu trwania szkolenia w obsłudze sprzętu 554. Metaanaliza 10 badań dotyczących pozaszpitalnego zatrzymania krążenia i 2 badań opisujących wewnątrzszpitalne epizody nie wykazała wpływu ani na krótko-, ani na długoterminową przeżywalność przy stosowaniu ACD- -CPR, porównując z konwencjonalną RKO 205. Dwa doniesienia opierające się na badaniach pośmiertnych pacjentów wykazały więcej przypadków złamania żeber i mostka po zastosowaniu ACD-CPR 555,556, ale inne badanie nie wykazało różnic między grupami 557. Zastawka oporowa (Impedance Threshold Device ITD) ITD jest to zastawka oporowa, która ogranicza możliwość wejścia powietrza do klatki piersiowej podczas fazy relaksacji pomiędzy uciśnięciami. Zmniejsza to ciśnienie wewnątrz klatki piersiowej, zwiększając powrót krwi żylnej do serca. Uważa się, że jednoczesne stosowanie tego urządzenia i ACD-CPR u pacjenta zaintubowanego pozwala uzyskać efekt synergiczny, polegający na poprawie powrotu żylnego podczas fazy aktywnej dekompresji. ITD używano także w trakcie standardowo prowadzonej RKO u pacjentów zaintubowanych lub wentylowanych za pomocą maski twarzowej 561. Jeżeli ratownik jest w stanie utrzymać dobrą szczelność maski, to możliwe jest uzyskanie ujemnego ciśnienia wewnątrz klatki piersiowej o wartościach porównywalnych z tymi, jakie uzyskuje się przy zastosowaniu intubacji dotchawiczej 561. Większość , ale nie wszystkie z badań przeprowadzonych na zwierzętach wykazała poprawę wskaźników hemodynamicznych lub wyników leczenia podczas RKO z użyciem ITD. Z kolei kilka randomizowanych badań dało różniące się wyniki. W dwóch badaniach analizujących pozaszpitalne zatrzymanie krążenia ACD-CPR stosowane w połączeniu z ITD poprawiło 24-godzinne przeżycie oraz przeżywalność do przyjęcia do oddziału intensywnej terapii w porównaniu ze standardowo wykonywaną RKO 560,574, ale te badania pozostają w sprzeczności z innymi, w których nie wykazano poprawy w ROSC i przeżywalności 24- godzinnej 558,561. Aktualna metaanaliza wykazała poprawę ROSC oraz wzrost przeżycia krótkoterminowego u dorosłych pacjentów z pozaszpitalnym zatrzymaniem krążenia resuscytowanych za pomocą ITD, ale nie wykazano poprawy przeżywalności do wypisu ze szpitala oraz przeżywalności z dobrym efektem neurologicznym 575. Wobec braku danych wskazujących, że ITD zwiększa przeżywalność do wypisu ze szpitala, jej rutynowe użycie w zatrzymaniu krążenia nie jest zalecane. RKO przy użyciu mechanicznego tłoka Mechaniczny tłok używany do prowadzenia RKO to urządzenie uciskające mostek, zamontowane na desce, zasilane sprężonym gazem. W kilku badaniach na zwierzętach 576 zastosowanie tego urządzenia poprawiło zarówno końcowowydechowe stężenie dwutlenku węgla, rzut serca, mózgowy przepływ krwi, średnie ciśnienie tętnicze krwi, jak i krótkoterminowe przeżycie z dobrym efektem neurologicznym. W badaniach u ludzi, wykazano także poprawę końcowowydechowego stężenia dwutlenku węgla oraz średniego ciśnienia tętniczego krwi w porównaniu ze standardową RKO W jednym badaniu wykazano, że zastosowanie mechanicznego tłoka w porównaniu ze standardową RKO zwiększa częstość przerw podczas RKO wynikających z zakładania i zdejmowania przyrządu podczas transportu pacjentów z pozaszpitalnym zatrzymaniem krążenia 580. Lund University Cardiac Arrest System (LUCAS) CPR Lund University Cardiac Arrest System jest zasilanym gazem urządzeniem uciskającym mostek. Zawiera ono w sobie przyssawkę do aktywnej dekompresji. W badaniach na zwierzętach udowodniono poprawę parametrów hemodynamicznych i krótkoterminowe przeżycie podczas RKO przy użyciu LUCAS w porównaniu ze standardową RKO 581,582. Nie ma opublikowanych badań z randomizacją dotyczących ludzi, porównujących standardową RKO z RKO przy użyciu LUCAS. Badanie przeprowadzone w grupie pacjentów, u których doszło do pozaszpitalnego zatrzymania krążenia w obecności świadków i u których stosowano urządzenie LUCAS, nie udowodniło przewagi takiego postępowania (ROSC, przeżycie do przyjęcia do szpitala lub przeżycie do wypisu ze szpitala) w porównaniu ze standardową RKO 583. Serie przypadków klinicznych opisujące łącznie 200 pacjentów wykazywały zróżnicowaną skuteczność wynikającą z zastosowania przyrządu LUCAS po okresie standardowej, niezakończonej sukcesem RKO 347,581, W jednej serii przypadków wykorzystano przyrząd LUCAS w czasie jednoczesnego wykonywania PCI 293. Jedenastu spośród 43 pacjentów przeżyło do wypisu ze szpitala bez ubytków neurologicznych. Opublikowano kilka innych raportów poświęconych zastosowaniu LUCAS podczas PCI 585,587,588. W jednym badaniu przeprowadzanym pośmiertnie wykazano podobny 4
139 138 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 profil obrażeń po stosowaniu LUCAS jak po standardowej RKO 589. Wcześniejsze wersje LUCAS napędzane tlenem o wysokim przepływie (LUCAS 1) nie powinny być stosowane w ciasnych pomieszczeniach, gdyż wykonywanie defibrylacji w środowisku o wysokim stężeniu tlenu grozi pożarem 590. Load-Distributing Band CPR (AutoPulse) Load-Distributing Band (LDB) jest okrężnym urządzeniem uciskającym klatkę piersiową, składającym się z pneumatycznie zasilanego pasa ściskającego i deski. Choć stosowanie LDB CPR poprawia parametry hemodynamiczne , wyniki badań klinicznych pozostają sprzeczne. Jedno wieloośrodkowe badanie z randomizacją, przeprowadzone z udziałem ponad 1000 dorosłych pacjentów z pozaszpitalnym zatrzymaniem krążenia, leczonych przez personel pogotowia ratunkowego i resuscytowanych za pomocą LDB CPR, nie wykazało poprawy przeżycia 4-godzinnego oraz zanotowało gorsze neurologiczne wyniki leczenia 594. Jednakże analiza post hoc tego badania ujawniła znaczącą różnorodność między ośrodkami uczestniczącymi w badaniu 598. Dalsze badanie wykazało niższy iloraz szans 30-dniowego przeżycia (OR 0,4), choć analiza podgrup wykazała wzrost ilości ROSC u pacjentów leczonych za pomocą LDB CPR 595. W innym badaniach z udziałem ludzi, bez randomizacji, wykazano wzrost ROSC 596, 597, wzrost przeżycia do wypisu ze szpitala po pozaszpitalnym zatrzymaniu krążenia 597 oraz poprawę parametrów hemodynamicznych u pacjentów z nieskuteczną RKO w warunkach wewnątrzszpitalnych 591. Wyniki zarówno badań klinicznych 594,598, jak i symulacyjnych 599 sugerują, że jakość, a co za tym idzie skuteczność działania urządzenia są zależne od czynników związanych z miejscem prowadzenia RKO. Miejsce LUCAS i AutoPulse w leczeniu zatrzymania krążenia Obecnie prowadzone są dwa duże wieloośrodkowe badania prospektywne z randomizacją, mające na celu ocenę skuteczności urządzeń AutoPulse i LUCAS. Wyniki tych badań są oczekiwane z zainteresowaniem. W warunkach szpitalnych urządzenia mechaniczne okazały się skuteczne w leczeniu pacjentów poddawanych PCI 293,585 oraz TK 600, a także podczas przedłużonych prób resuscytacji (np. w przypadku hipotermii 601,602, zatrucia, podczas trombolizy u pacjentów z zatorem tętnicy płucnej czy przedłużonego transportu itp.), czyli w sytuacjach, gdzie zmęczenie ratownika może zmniejszyć skuteczność manualnego uciskania klatki piersiowej. W warunkach przedszpitalnych urządzenia te mogą odgrywać ważną rolę w sytuacjach, gdy konieczne jest wydobywanie pacjentów, resuscytacja prowadzona jest w ograniczonych przestrzeniach, wymagane jest przewiezienie pacjenta; co często uniemożliwia skuteczne uciskanie klatki piersiowej przez ratownika. Podczas transportu do szpitala jakość manualnie wykonywanej RKO jest często niezadowalająca. Przyrządowa RKO pozwala na utrzymanie dobrej jakości resuscytacji podczas transportu karetką do szpitala 343,603. Zaletą urządzeń mechanicznych jest możliwość wykonania defibrylacji bez przerw w uciskaniu klatki piersiowej. Rola opisanych urządzeń we wszystkich sytuacjach klinicznych wymaga dalszej oceny. 4g Zaburzenia rytmu towarzyszące zatrzymaniu krążenia Prawidłowe rozpoznanie i leczenie zaburzeń rytmu u pacjentów w stanie krytycznym może zapobiec wystąpieniu lub nawrotowi zatrzymania krążenia po skutecznej wstępnej resuscytacji. Algorytmy postępowania opisane w tym rozdziale skonstruowano w sposób umożliwiający osobom po szkoleniu ALS, niekoniecznie specjalistom, skuteczne i bezpieczne leczenie pacjenta w stanie zagrożenia życia. Z tego powodu starano się je przedstawić w sposób jak najprostszy. Jeżeli życie pacjenta nie jest bezpośrednio zagrożone, sposoby postępowania są różne, włączając w to podaż leków (doustnie lub parenteralnie), w stosowaniu których osoba nie będąca specjalistą może mieć mniejsze doświadczenie. W tej sytuacji istnieje możliwość poszukania pomocy kardiologa lub doświadczonego w danej dziedzinie lekarza. Wyczerpujące informacje dotyczące zaburzeń rytmu można znaleźć na stronie Podstawowe zasady leczenia Ocena wstępna i leczenie pacjenta z zaburzeniem rytmu powinno przebiegać zgodnie ze schematem ABCDE. W skład kluczowych elementów tego procesu wchodzą ocena objawów niepokojących, podanie tlenu w dużym przepływie, uzyskanie dostępu dożylnego oraz wdrożenie monitorowania (EKG, pomiar ciśnienia tętniczego, SpO 2 ). Jeżeli tylko jest to możliwe, należy wykonać 12-odprowadzeniowe EKG. Pomoże to dokładnie ocenić rytm przed leczeniem bądź retrospektywnie. Należy wyrównywać wszelkie zaburzenia elektrolitowe (np. K +, Mg 2+, Ca 2+ ). Planując leczenie, należy rozważyć przyczynę i okoliczności wystąpienia arytmii. W ocenie i leczeniu wszystkich zaburzeń rytmu brane są pod uwagę dwa czynniki: stan pacjenta (stabilny czy niestabilny) oraz charakter arytmii. Leki antyarytmiczne charakteryzują się powolnym początkiem działania i są mniej skuteczne niż kardiowersja elektryczna w uzyskiwaniu rytmu zatokowego u pacjentów z tachykardią. Z tego względu leki te powinny być rezerwowane wyłącznie dla pacjentów bez objawów niepokojących, a kardiowersja elektryczna dla pacjentów niestabilnych, wykazujących objawy niepokojące. Objawy niepokojące W przypadku większości zaburzeń rytmu obecność lub brak niepokojących objawów determinuje właściwy sposób leczenia. Poniżej wymienione objawy wskazują pacjentów, u których niestabilność hemodynamiczna powodowana jest arytmią: 1. Wstrząs objawiający się bladością powłok, nadmierną potliwością, zimną i lepką skórą kończyn (zwiększona aktywność układu sympatycznego), zaburzonym stanem świadomości (zmniejszony przepływ mózgowy) i hipotensją (np. skurczowe ciśnienie krwi <90 mm Hg). 2. Omdlenie/utrata przytomności w następstwie zredukowanego przepływu mózgowego.
140 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Niewydolność krążenia zaburzenia rytmu, redukując przepływ wieńcowy, upośledzają pracę mięśnia sercowego. W ostrych epizodach może się to objawiać obrzękiem płuc (niewydolność lewej komory) i/lub nadmiernie wypełnionymi żyłami szyjnymi i powiększeniem wątroby (niewydolność prawej komory). 4. Niedokrwienie mięśnia sercowego występuje, gdy zużycie tlenu w sercu przewyższa jego dostarczanie. Niedokrwienie mięśnia sercowego może manifestować się jako ból w klatce piersiowej (dusznica) lub przebiegać bez bólu, jako izolowana zmiana w 12-odprowadzeniowym EKG (ciche niedokrwienie). Obecność niedokrwienia jest szczególnie ważna, gdy pacjent ma wyjściowo chorobę niedokrwienną lub wadę strukturalną serca. W tych przypadkach może pociągnąć to za sobą dalsze, zagrażające życiu komplikacje z zatrzymaniem krążenia włącznie. Możliwości terapii Po rozpoznaniu rytmu oraz stwierdzeniu obecności lub braku objawów niepokojących natychmiastowe postępowanie obejmuje dwie opcje terapeutyczne: 1. Elektryczna (kardiowersja, stymulacja serca). 2. Farmakologiczna (leki antyarytmiczne i inne). Częstoskurcze Jeżeli pacjent jest niestabilny Jeżeli pacjent jest niestabilny, pogarsza się jego stan i występują jakiekolwiek objawy niepokojące lub symptomy opisane powyżej, będące następstwem tachykardii, należy natychmiast wykonać kardiowersję (ryc. 4.11). U pacjentów bez obciążeń kardiologicznych rzadko występują niepokojące objawy, gdy czynność komór jest <150/ min. U osób z upośledzoną funkcją mięśnia sercowego lub istotnymi schorzeniami towarzyszącymi niepożądane objawy i niestabilność mogą się rozwinąć już przy niższej czynności serca. Jeżeli kardiowersja nie przywróci rytmu zatokowego i pacjent nadal pozostaje niestabilny, należy podać dożylnie 300 mg amiodaronu w ciągu minut i ponowić próbę elektrycznej kardiowersji. Po wysycającej dawce można kontynuować wlew tego leku 900 mg przez 24 godziny. Wykonywanie kolejnych kardiowersji nie jest zalecane w przypadku nawracających (w ciągu godzin, dni) napadowych (samoustępujących) epizodów migotania przedsionków. Tego rodzaju zaburzenia rytmu są względnie częste u krytycznie chorych pacjentów, u których są stale obecne czynniki wywołujące arytmię (np. zaburzenia metaboliczne, sepsa). Kardiowersja w tym przypadku nie zapobiega ponownemu wystąpieniu arytmii. Jeżeli występują kolejne epizody, należy je leczyć farmakologicznie. Zsynchronizowana kardiowersja elektryczna Jeżeli elektryczna kardiowersja jest używana do leczenia przedsionkowych lub komorowych tachyarytmii, wyładowanie musi być zsynchronizowane z załamkiem R, a nie z załamkiem T zapisu EKG 604. Unikanie dostarczenia energii podczas okresu refrakcji względnej minimalizuje ryzyko indukcji migotania komór. Przed wykonaniem kardiowersji u przytomnych pacjentów należy zastosować sedację lub wykonać znieczulenie ogólne. Leczenie częstoskurczu z szerokimi zespołami QRS i migotania przedsionków należy rozpocząć od energii 200 J dla defibrylatorów jednofazowych lub J dla dwufazowych. Przy braku efektu należy zwiększać energię (zob. rozdział 3) 223. Trzepotanie przedsionków i napadowy częstoskurcz nadkomorowy często można skutecznie leczyć wyładowaniami o niższych energiach, rozpoczynając od 100 J dla defibrylatorów jednofazowych lub J dla dwufazowych. Jeżeli pacjent jest stabilny Jeżeli pacjent, u którego występuje częstoskurcz, jest stabilny (nie ma żadnych niepokojących objawów powodowanych tachykardią) i nie pogarsza się jego stan, istnieje możliwość wdrożenia leczenia farmakologicznego. Należy ocenić rytm za pomocą 12-odprowadzeniowego EKG i oszacować czas trwania zespołu QRS. Jeżeli przekracza on 0,12 sekundy (3 małe kwadraty na standardowym papierze do EKG), rozpoznaje się częstoskurcz z szerokimi zespołami QRS. Jeśli czas ten jest krótszy niż 0,12 sekundy, rozpoznaje się częstoskurcz z wąskimi zespołami QRS. Wszystkie metody leczenia antyarytmicznego, tj. manewry fizykalne, leki lub kardiowersja elektryczna, mogą mieć działanie proarytmiczne, należy więc mieć na uwadze, że pogorszenie się stanu klinicznego pacjenta może raczej wynikać z zastosowanej terapii niż z braku jej rezultatu. Użycie wielu leków antyarytmicznych lub zastosowanie dużych dawek jednego leku może powodować depresję mięśnia sercowego i hipotensję. Skutkiem może być pogorszenie rytmu serca. Przed zastosowaniem leków antyarytmicznych w skojarzeniu lub pojedynczego leku w powtarzanej, wysokiej dawce należy zasięgnąć porady specjalisty. Częstoskurcz z szerokimi zespołami QRS Częstoskurcze z szerokimi zespołami QRS mają z reguły pochodzenie komorowe 605. Istnieje jednak możliwość, że częstoskurcz z szerokimi zespołami QRS jest pochodzenia nadkomorowego z aberracją przewodnictwa. U niestabilnych pacjentów w okresie około zatrzymania krążenia należy przyjąć, że ten rytm jest pochodzenia komorowego. W przypadku pacjentów stabilnych kolejny krok to ocena miarowości rytmu. Miarowy częstoskurcz z szerokimi zespołami QRS Miarowy częstoskurcz z szerokimi zespołami QRS jest najczęściej tachykardią komorową lub nadkomorową tachykardią z blokiem odnogi pęczka Hisa. W przypadku trudności ze zidentyfikowaniem źródła arytmii należy podać adenozynę dożylnie (stosując strategię opisaną poniżej). Takie postępowanie zwiększa szansę powrotu rytmu zatokowego i ułatwia rozpoznanie rytmu 606. Stabilna tachykardia komorowa może być leczona amiodaronem podanym dożylnie w dawce 300 mg przez minut, a następnie we wlewie 900 mg przez 24 godziny. Przed wdrożeniem alternatywnego leczenia, obejmującego prokainamid, nifekalant lub sotalol, należy zasięgnąć porady specjalisty. 4
141 140 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 Oceń, stosując schemat ABCDE Podaj tlen, zapewnij dostęp dożylny Monitoruj EKG, ciśnienie krwi, SpO 2, wykonaj 12-odprowadzeniowe EKG Rozpoznaj i lecz odwracalne przyczyny (np. zaburzenia elektrolitowe) Oceń, czy występują objawy niepokojące 1. Wstrząs 2. Omdlenie 3. Niedokrwienie mięśnia sercowego 4. Niewydolność serca Kardiowersja* Do 3 prób Postępowanie w przypadku tachykardii (z tętnem) Czy zespoły QRS są wąskie (<0,12 sek)? Stabilny Niestabilny Wąskie Szerokie Amiodaron 300 mg iv w ciągu min i kolejna kardiowersja; następnie: Amiodaron 900 mg w ciągu 24 h Niemiarowy Wąskie Czy rytm jest miarowy? Miarowy Miarowe Szerokie Czy zespoły QRS są miarowe? Niemiarowe * Kardiowersja powinna być zawsze wykonywana po zastosowaniu sedacji lub znieczulenia ogólnego. Niemiarowy częstoskurcz z wąskimi QRS Prawdopodobnie migotanie przedsionków Kontroluj rytm komór: ß-bloker lub diltiazem Rozważ digoksynę lub amiodaron przy objawach niewydolności serca Włącz leki p/zakrzepowe, gdy >48 h Zastosuj stymulację nerwu błędnego Adenozyna 6 mg iv, szybki bolus; jeżeli nieskuteczna, podaj 12 mg; jeżeli nieskuteczna, podaj kolejne 12 mg Stale monitoruj rytm sreca Poproś o pomoc specjalistę Poproś o pomoc specjalistę Nie Przywrócono rytm zatokowy? Tak Jeżeli częstoskurcz komorowy (lub nie masz pewności): Amiodaron 300 mg iv w ciągu min, następnie 900 mg w ciągu 24 h Możliwe przyczyny: AF z blokiem odnogi lecz jak częstoskurcz z wąskimi QRS AF w zespole preekscytacji rozważ amiodaron (np. torsades de pointes podaj magnez 2 g w ciągu 10 min) Prawdopodobnie trzepotanie przedsionków Kontroluj rytm serca (np. β-bloker) Prawdopodobnie PSVT w mechanizmie re-entry: Wykonaj 12-odprowadzeniowe EKG przy rytmie zatokowym Jeśli nawraca, podaj ponownie Jeśli wcześniej stwierdzono SVT z blokiem odnogi: Podaj adenozynę jak dla miarowych częstoskurczów z wąskimi QRS adenozynę i rozważ profilaktyczne leczenie antyarytmiczne Ryc Algorytm postępowania w przypadku tachykardii
142 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 141 Niemiarowy częstoskurcz z szerokimi zespołami QRS Niemiarowy częstoskurcz z szerokimi zespołami QRS jest najczęściej migotaniem przedsionków (atrial fibrillation AF) z towarzyszącym blokiem odnogi pęczka Hisa. Inną prawdopodobną przyczyną może być AF z towarzyszącym zespołem preekscytacji (np. u pacjentów z zespołem Wolffa Parkinsona White a WPW). Istnieje więcej możliwych prezentacji zmian morfologicznych dotyczących zespołów QRS niż AF z blokiem odnogi pęczka Hisa. Trzecią możliwością jest polimorficzny VT (np. torsades de pointes). Taki rytm rzadko występuje bez niepokojących objawów. Podczas oceny i leczenia niemiarowego VT należy szukać pomocy specjalisty. W przypadku rozpoznania AF z blokiem odnogi pęczka Hisa należy postępować zgodnie z algorytmem leczenia AF (patrz dalej). Przy podejrzeniu obecności AF z zespołem preekscytacji (lub trzepotania przedsionków) należy unikać stosowania adenozyny, digoksyny, werapamilu i diltiazemu. Leki te blokują przewodnictwo w węźle przedsionkowo-komorowym i mogą nasilić przewodzenie drogą dodatkową, co może wywołać tachykardię o ciężkim przebiegu. W tym przypadku najbezpieczniejszym sposobem postępowania jest elektryczna kardiowersja. Leczenie torsades de pointes trzeba rozpocząć od zaprzestania podaży leków wydłużających odstęp QT. Należy wyrównać zaburzenia elektrolitowe, szczególnie hipokaliemię. Należy podać 2 g siarczanu magnezu dożylnie w ciągu 10 minut 607, 608. Zalecana jest konsultacja specjalistyczna, ponieważ, aby zapobiec nawrotowi częstoskurczu, mogą być wskazane inne metody postępowania (np. overdrive pacing). W przypadku wystąpienia objawów niepokojących, co zdarza się często, należy natychmiast wykonać kardiowersję, a przy braku tętna defibrylację zgodnie z algorytmem zatrzymania krążenia. Częstoskurcz z wąskimi zespołami QRS Pierwszym krokiem w ocenie częstoskurczu z wąskimi zespołami QRS jest ocena jego miarowości. Najczęstszymi postaciami częstoskurczu z wąskimi zespołami QRS są: tachykardia zatokowa, częstoskurcz z węzła przedsionkowo-komorowego z towarzyszącym zjawiskiem re-entry (AV Nodal Re-entry Tachycardia AVNRT, najczęstszy typ częstoskurczu nadkomorowego [Supraventricular Tachykardia SVT]), częstoskurcz przedsionkowo-komorowy ze zjawiskiem re-entry (AV Re-entry Tachycardia AVRT), który towarzyszy zespołowi WPW, trzepotanie przedsionków z regularnym blokiem przedsionkowo-komorowym (zwykle 2 : 1). Niemiarowy częstoskurcz z wąskimi zespołami QRS najczęściej jest AF lub czasami trzepotaniem przedsionków ze zmiennym blokiem przedsionkowo-komorowym ( variable block ). Miarowy częstoskurcz z wąskimi zespołami QRS Tachykardia zatokowa Tachykardia zatokowa jest częstą fizjologiczną odpowiedzią organizmu między innymi na wysiłek fizyczny lub niepokój. W przebiegu choroby stan ten może wywoływać wiele bodźców, takich jak: ból, gorączka, anemia, utrata krwi, niewydolność krążenia. Leczenie powinno być przyczynowe, gdyż inne próby zwolnienia rytmu pogorszą stan chorego. AVNRT i AVRT (napadowy SVT) AVNRT jest najczęstszą postacią napadowego SVT. Występuje on często u osób bez innych schorzeń mięśnia sercowego i stosunkowo rzadko w okresie około zatrzymania krążenia 609. W zapisie EKG obecny jest częstoskurcz z wąskimi zespołami QRS, często bez widocznej aktywności przedsionków. Częstość tego rytmu przekracza zwykle typową częstość dla rytmu zatokowego w spoczynku (60 120/ min). Przebieg zaburzenia jest zazwyczaj łagodny, chyba że towarzyszy mu dodatkowo strukturalne uszkodzenie serca lub choroba niedokrwienna. Tachykardia przedsionkowo-komorowa ze zjawiskiem re-entry (AVRT) występuje u pacjentów z zespołem WPW i z reguły przebiega również łagodnie, jeżeli nie współtowarzyszy temu inna strukturalna choroba serca. Częstym typem AVRT jest regularna tachykardia z wąskimi zespołami QRS bez widocznej aktywności przedsionków w zapisie EKG. Trzepotanie przedsionków z regularnym blokiem przedsionkowo-komorowym (często blok 2 : 1) Trzepotanie przedsionków z regularnym blokiem przedsionkowo-komorowym (często 2 : 1) generuje częstoskurcz z wąskimi zespołami QRS, gdzie trudne może być jednoznaczne stwierdzenie aktywności przedsionków czy fali trzepotania. W konsekwencji może ono być początkowo trudne do odróżnienia od AVNRT i AVRT. Kiedy trzepotaniu przedsionków z blokiem 2 : 1 lub nawet 1 : 1 towarzyszy blok odnogi pęczka Hisa, generowany częstoskurcz z szerokimi zespołami QRS może być trudny do odróżnienia od VT. Leczenie tego rytmu jako VT najczęściej będzie skuteczne lub doprowadzi do zwolnienia czynności komór i umożliwi właściwą identyfikację rytmu. Najbardziej typowy obraz trzepotania przedsionków to rytm z częstością przedsionków około 300/min, a więc przy obecności bloku 2 : 1 będzie obecna tachykardia około 150/min. Znacznie szybsze rytmy rzadko są wywoływane przez trzepotanie przedsionków z blokiem 2 : 1. Leczenie miarowego częstoskurczu z wąskimi zespołami QRS W przypadku niestabilnego pacjenta, u którego rozwinęły się objawy niewydolności związane z arytmią, należy wykonać kardiowersję elektryczną. Uzasadnione jest podanie niestabilnym pacjentom adenozyny w czasie, gdy przygotowuje się kardiowersję, jakkolwiek nie należy opóźniać jej wykonania, jeśli adenozyna nie przyniesie pożądanego efektu. Kiedy pacjent jest stabilny, należy postępować w poniżej przedstawiony sposób. Należy rozpocząć stymulacją nerwu błędnego 609 : masaż zatoki tętnicy szyjnej i próba Valsalvy są skuteczne w jednej czwartej przypadków napadowego SVT. Masaż zatoki tętnicy szyjnej powoduje stymulację baroreceptorów, co zwiększa napięcie nerwu błędnego 4
143 142 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 i zmniejsza aktywność układu sympatycznego, prowadząc w konsekwencji do zwolnienia przewodnictwa w węźle AV. Masaż zatoki tętnicy szyjnej polega na zastosowaniu ucisku na tętnicę szyjną na wysokości chrząstki pierścieniowatej i wykonaniu okrężnych ruchów masujących przez około 5 sekund. W przypadku braku reakcji należy wykonać manewr po przeciwnej stronie. W przypadku obecności szmeru nad tętnicą szyjną należy unikać masażu zatoki. Pęknięcie blaszki miażdżycowej w tej okolicy może spowodować zator i w konsekwencji zawał mózgu. Próba Valsalvy (nasilony wydech przy zamkniętej głośni) w ułożeniu na plecach może być najbardziej efektywną techniką. Praktycznym sposobem jej wykonania, unikając przedłużonego wyjaśniania procedury, może być poproszenie pacjenta o próbę nadmuchania strzykawki 20 ml tak, aby przesunął się tłok. Należy wykonywać zapis EKG (preferowany zapis wieloodprowadzeniowy) podczas każdej próby stymulacji nerwu błędnego. U pacjentów z trzepotaniem przedsionków dojdzie często do zwolnienia czynności komór i uwidoczni się fala trzepotania. Jeżeli arytmia nadal się utrzymuje i nie jest to trzepotanie przedsionków, należy podać adenozynę. Dawka 6 mg powinna być podana jako szybki, dożylny bolus. Podczas każdorazowej podaży leku zalecane jest wykonanie zapisu EKG (preferowany zapis wieloodprowadzeniowy). Jeżeli dojdzie tylko do przejściowego zwolnienia czynności komór, należy poszukać aktywności przedsionków: trzepotania przedsionków lub innego częstoskurczu przedsionkowego, i odpowiednio je leczyć. W przypadku braku odpowiedzi na 6 mg adenozyny należy podać kolejny bolus 12 mg, gdy nadal brak reakcji jeszcze jedną dawkę 12 mg. Strategia ta pozwala zakończyć 90 95% nadkomorowych zaburzeń rytmu 610. Pozytywne efekty stymulacji nerwu błędnego lub użycia adenozyny wskazują na to, że był to najprawdopodobniej epizod AVNRT lub AVRT. Takich pacjentów należy nadal monitorować pod kątem dalszych zaburzeń rytmu. Nawroty arytmii zaleca się leczyć stosując adenozynę lub dłużej działające leki blokujące przewodnictwo przedsionkowo-komorowe (np. diltiazem lub werapamil). Jeżeli są przeciwwskazania do stosowania adenozyny lub jest ona nieskuteczna (bez potwierdzenia, że mamy do czynienia z trzepotaniem przedsionków), należy podać bloker kanału wapniowego (np. werapamil lub diltiazem). Niemiarowy częstoskurcz z wąskimi zespołami QRS Niemiarowy częstoskurcz z wąskimi zespołami QRS najczęściej jest AF z niekontrolowaną odpowiedzią komór lub, rzadziej, trzepotaniem przedsionków ze zmiennym blokiem przedsionkowo-komorowym. Należy dokonać zapisu 12-odprowadzeniowego EKG celem identyfikacji rytmu. Gdy pacjent jest niestabilny, z objawami niewydolności wywołanymi arytmią, należy wykonać kardiowersję elektryczną, tak jak to opisano powyżej. Europejskie Towarzystwo Kardiologiczne przedstawiło szczegółowe wytyczne postępowania w przypadku AF 611. Kiedy brak jest objawów niewydolności, zalecane postępowanie obejmuje: farmakologiczną kontrolę częstości rytmu, umiarowienie przy użyciu leków (farmakologiczna kardiowersja), umiarowienie przez elektryczną kardiowersję, leczenie zapobiegające powikłaniom (np. antykoagulacja). Aby wdrożyć najbardziej korzystne dla danego pacjenta leczenie, należy uzyskać opinię specjalisty. Im dłużej u pacjenta występuje AF, tym większe jest prawdopodobieństwo powstania skrzepliny w przedsionku. U pacjentów, u których epizod AF trwa powyżej 48 godzin, nie powinno się stosować kardiowersji (zarówno elektrycznej, jak i farmakologicznej), dopóki nie wdroży się pełnego leczenia antykoagulacyjnego lub nie wykluczy przezprzełykowym badaniem echokardiograficznym obecności skrzepliny w przedsionku. Gdy stan kliniczny pacjenta z AF wymaga wykonania kardiowersji, a czas trwania AF jest dłuższy niż 48 godzin (lub czas jego trwania jest nieznany), należy podać początkową dawkę heparyny dożylnie w postaci bolusa, a następnie we wlewie ciągłym tak, aby osiągnąć wartość APTT 1,5 do 2 razy większą od wartości przyjętych za prawidłowe. Należy kontynuować podawanie leków przeciwzakrzepowych przez przynajmniej 4 tygodnie 611. Jeśli celem jest kontrola częstości rytmu, lekami z wyboru są beta-blokery 612,613 i diltiazem 614,615. Digoksynę i amiodaron można stosować u pacjentów z niewydolnością serca. Używany był również w tym celu siarczan magnezu, choć dane potwierdzające zasadność takiego postępowania są ograniczone 616,617. Gdy czas trwania epizodu AF jest krótszy niż 48 godzin i za właściwe uznano kontrolę nad rytmem, można zastosować kardiowersję farmakologiczną. Należy zasięgnąć opinii specjalisty i rozważyć podanie ibutilidu, flekainidu lub dofetilidu. Można także podać amiodaron (300 mg dożylnie przez min, a następnie we wlewie 900 mg przez 24 godz.), choć jego skuteczność jest mniejsza. Jednym ze sposobów postępowania u tych pacjentów jest elektryczna kardiowersja, bardziej skuteczna niż kardiowersja farmakologiczna. W przypadku pacjentów z AF i współistniejącym zespołem WPW, stwierdzonym lub podejrzewanym, zalecana jest konsultacja specjalistyczna. U pacjentów z zespołem preekscytacji i towarzyszącym AF lub trzepotaniem przedsionków należy unikać stosowania adenozyny, diltiazemu, werapamilu lub digoksyny, ponieważ leki te mogą, blokując przewodnictwo przedsionkowo-komorowe, względnie nasilić zjawisko preekscytacji. Bradykardia Bradykardię definiowana jest jako czynność serca <60/ min. Bradykardia może być wywołana przyczynami sercowymi (np. zawał mięśnia sercowego, niedokrwienie mięśnia sercowego, zespół chorego węzła), pozasercowymi (np. reakcja wazowagalna, hipotermia, hipoglikemia, niedoczynność tarczycy, wzrost ciśnienia śródczaszkowego) lub zatru-
144 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 143 ciem lekami (np. digoksyna, beta-blokery, blokery kanałów wapniowych). Bradykardia jest spowodowana zmniejszoną aktywnością węzła zatokowo-przedsionkowego lub zaburzeniami przewodnictwa przedsionkowo-komorowego. Zmniejszoną aktywność węzła zatokowo-przedsionkowego obserwujemy w bradykardii zatokowej (wywołanej zwiększonym napięciem nerwu błędnego), zespole chorego węzła i zahamowaniu zatokowym. Bloki przedsionkowo-komorowe można podzielić na I, II i III stopień. Mogą one być zarówno skutkiem działania wielu leków, zaburzeń elektrolitowych, jak również zmian strukturalnych w sercu związanych z zawałem lub zapaleniem mięśnia sercowego. Blok przedsionkowo-komorowy I stopnia jest definiowany jako wydłużenie odstępu PQ (>0,20 s) i zwykle jest bezobjawowy. Blok przedsionkowo-komorowy II stopnia podzielono na blok typu Mobitz I i Mobitz II. W przypadku bloku typu Mobitz I zaburzenie przewodnictwa występuje w węźle przedsionkowo-komorowym. Zwykle ma to charakter przejściowy i bezobjawowy. W bloku typu Mobitz II zaburzenie przewodnictwa jest najczęściej zlokalizowane poniżej węzła przedsionkowo-komorowego i dotyczy pęczka Hisa lub jego gałęzi. Blok tego typu często jest objawowy, potencjalnie może się rozwinąć całkowity blok serca. Blok III stopnia jest definiowany jako rozkojarzenie przedsionkowo-komorowe. Może ono być przejściowe lub trwałe, w zależności od wywołującej go przyczyny. Ocena wstępna Należy ocenić stan pacjenta z bradykardią w oparciu o schemat ABCDE. Należy rozważyć potencjalne przyczyny wywołujące bradykardię, poszukiwać objawów niepokojących, rozpoznać podczas wstępnej oceny odwracalne przyczyny bradykardii i rozpocząć ich leczenie. W przypadku istnienia objawów niepokojących należy wdrożyć leczenie bradykardii. Leczenie wstępne opiera się na podawaniu leków oraz stymulacji zarezerwowanej wyłącznie dla pacjentów, u których nie uzyskano odpowiedzi na leczenie farmakologiczne lub pacjentów z czynnikami ryzyka wystąpienia asystolii (ryc. 4.12). Leczenie farmakologiczne W przypadku obecności objawów niepokojących należy podać atropinę 500 μg dożylnie i, jeżeli to konieczne, powtarzać tę dawkę co 3 5 minut do całkowitej dawki 3 mg. Dawki atropiny poniżej 500 μg paradoksalnie mogą jeszcze zwolnić rytm serca 618. U zdrowych ochotników dawka 3 mg wywołuje maksymalne przyspieszenie czynności serca będącego w spoczynku 619. W przypadku ostrego niedokrwienia lub zawału mięśnia sercowego należy rozważnie używać atropiny, gdyż przyspieszenie czynności serca może nasilić niedokrwienie i zwiększyć obszar zawału. W przypadku braku odpowiedzi na leczenie atropiną należy rozważyć leki drugiego rzutu. Należą do nich izoprenalina (dawka początkowa 5μg/min), adrenalina (2 10μg/ min) oraz dopamina (2 10μg/kg/min). W przypadku gdy bradykardia jest wywołana zawałem ściany dolnej mięśnia sercowego, występuje po przeszczepie serca lub w przebiegu urazu rdzenia kręgowego, należy rozważyć stosowanie teofiliny ( mg w powolnym wlewie dożylnym). Jeżeli potencjalną przyczyną bradykardii są β-blokery lub blokery kanału wapniowego, wskazane jest podanie dożylne glukagonu. Nie należy podawać atropiny u pacjentów po przeszczepie serca, gdyż paradoksalnie może to wywołać zaawansowany blok przedsionkowo-komorowy lub nawet zahamowanie zatokowe 620. Stymulacja Jeżeli nie ma odpowiedzi na leczenie atropiną lub jest mało prawdopodobne, że atropina będzie skuteczna, należy natychmiast wdrożyć stymulację przezskórną. Stymulacja przezskórna może powodować ból, a przechwycenie mechaniczne może nie zostać osiągnięte. Należy potwierdzić skuteczność przechwycenia mechanicznego i ponownie ocenić stan pacjenta. W celu kontroli bólu należy zastosować sedację i analgezję. Należy poszukiwać przyczyny bradyarytmii. W przypadku braku reakcji po podaniu atropiny i gdy niedostępna jest natychmiastowo stymulacja przezskórna, można, oczekując na sprzęt do stymulacji elektrycznej, zastosować mechaniczną stymulację pięścią Należy rytmicznie uderzać zamkniętą pięścią w okolicę dolnej części lewego brzegu mostka, starając się uzyskać fizjologiczną częstość stymulacji 50 70/min. Należy zasięgnąć porady specjalisty w celu oceny wskazań do czasowej stymulacji endokawitarnej. Należy ją rozważyć w przypadku wystąpienia asystolii w wywiadzie, bloku przedsionkowo-komorowym II stopnia typu Möbitz II, całkowitego bloku serca (III stopnia) (szczególnie z szerokimi zespołami QRS lub wstępną częstością rytmu <40/min) lub w przypadku występowania zatrzymania czynności komór powyżej 3 sekund. Leki antyarytmiczne Adenozyna Adenozyna jest naturalnie występującym nukleotydem purynowym. Zwalnia ona przewodnictwo przez węzeł przedsionkowo-komorowy, lecz ma niewielki wpływ na pozostałe komórki mięśnia sercowego i drogi przewodzenia. Jest wysoce skuteczna w leczeniu napadowych SVT powodowanych pętlami re-entry, włączając w to AVNRT. W innych częstoskurczach z wąskimi zespołami QRS adenozyna, poprzez zwolnienie czynności komór, pozwala na uwidocznienie wyjściowego rytmu przedsionków. Ma ona wyjątkowo krótki czas połowiczego rozpadu, wynoszący sekund, dlatego też jest podawana w postaci bolusa równolegle z szybkim wlewem dożylnym lub poprzedza szybkie wstrzyknięcie roztworu soli fizjologicznej. Najmniejsza skuteczna dawka to 6 mg (niektóre źródła nie rekomendują takiej dawki wstępnej), jeżeli nie jest skuteczna, można dwukrotnie powtórzyć dawki po 12 mg co 1 2 minut. Powinno się poinformować pacjenta o przejściowych, nieprzyjemnych skutkach ubocznych podania tego leku, szczególnie o nudnościach, uderzeniach gorąca, dyskomforcie w klatce piersiowej 624. W kilku krajach europejskich adenozyna nie jest dostępna, alternatywą jest trójfosforan adenozyny (ATP). Jeżeli i ten preparat jest nieosiągalny, 4
145 144 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins Postępowanie w przypadku bradykardii Oceń, stosując schemat ABCDE Podaj tlen, zapewnij dostęp dożylny Monitoruj EKG, ciśnienie krwi, SpO 2, wykonaj 12-odprowadzeniowe EKG Rozpoznaj i lecz odwracalne przyczyny (np. zaburzenia elektrolitowe) Tak Oceń, czy występują objawy niepokojące: 1. Wstrząs 2. Omdlenie 3. Niedokrwienie mięśnia sercowego 4. Niewydolność serca Nie Atropina 500 μg iv 4 Pozytywna odpowiedź? Nie W międzyczasie: Atropina 500 μg iv powtarzaj do max dawki 3 mg Izoprenalina 5 μg/min Adrenalina 2 10 μg/min Alternatywne leki* LUB Stymulacja przezskórna Tak Tak Ryzyko asystolii? Ostatnio przebyty epizod asystolii Blok AV Mobitz II Całkowity blok serca z szerokimi zespołami QRS Pauzy komorowe >3 sek Nie Poproś o pomoc specjalistę Podejmij działania w celu założenia stymulacji wewnętrznej Obserwuj * Alternatywne leki: Aminofilina Dopamina Glukagon (przy przedawkowaniu β-blokerów lub blokerów kanałów wapniowych) Glycopyrolate można stosować zamiast atropiny Ryc Algorytm postępowania w przypadku bradykardii prawdopodobnie werapamil będzie najlepszym wyborem. Teofilina i jej pochodne blokują działanie adenozyny. U pacjentów otrzymujących dipyridamol lub karbamazepinę, jak również po przeszczepie mięśnia sercowego, zastosowanie adenozyny może być niebezpieczne ze względu na znaczne nasilenie efektu jej działania. W tej grupie pacjentów lub przy podaży leku do żyły centralnej należy zmniejszyć początkową dawkę do 3 mg. W przypadku obecności zespołu WPW blokada węzła przedsionkowo-komorowego może ułatwiać przewodnictwo przez istniejącą dodatkową drogę, co w częstoskurczach nadkomorowych doprowadzi do niebezpiecznego przyspieszenia czynności komór. Ponadto rzadko występującą reakcją na podanie adenozyny w przebiegu WPW jest wyzwolenie AF z niebezpiecznie szybką czynnością komór. Amiodaron Amiodaron podany dożylnie wpływa na kanały sodowe, potasowe i wapniowe, jak również posiada właściwości blokujące receptory α- i β-adrenergiczne. Wskazaniami do dożylnego podania amiodaronu są: Kontrola stabilnego hemodynamicznie monomorficznego VT, polimorficznego VT oraz tachykardii z szerokimi zespołami QRS niewiadomego pochodzenia, Napadowe SVT oporne na działanie adenozyny, stymulację nerwu błędnego czy blokadę przewodnictwa przedsionkowo-komorowego, Kontrola szybkiej czynności komór w przebiegu arytmii przedsionkowych współistniejących z dodatkową drogą przewodzenia, Nieefektywna kardiowersja elektryczna.
146 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 145 Należy podać 300 mg amiodaronu dożylnie przez minut w zależności od warunków i stanu hemodynamicznego pacjenta. Po tej dawce wysycającej powinno się wdrożyć wlew dożylny 900 mg przez 24 godziny. Dodatkowo, w razie potrzeby można powtórzyć wlew 150 mg w przypadku nawracających lub opornych na leczenie arytmii. Maksymalna, zalecana przez producenta dawka wynosi 2 g na dobę (zalecana dawka dobowa w różnych krajach jest inna). U pacjentów ze znanym ciężkim upośledzeniem funkcji serca dożylnie podawany amiodaron jest lekiem preferowanym w przedsionkowych i komorowych zaburzeniach rytmu. Głównymi skutkami ubocznymi terapii amiodaronem są hipotensja i bradykardia, czemu można zapobiec zmniejszając szybkość wlewu. Spadki ciśnienia związane z podażą amiodaronu spowodowane są wazoaktywnym rozpuszczalnikiem (Polisorbate 80 i alkohol benzylowy). Nowy, wodny roztwór amiodaronu nie zawiera tych substancji i jego efekt hipotensyjny jest porównywalny z lidokainą 446. Z uwagi na występujące po podaży obwodowej zakrzepowe zapalenie żył amiodaron powinno się podawać wykorzystując dostęp centralny. W sytuacjach nagłych amiodaron może być podany do dużej żyły obwodowej. Blokery kanału wapniowego: werapamil i diltiazem Werapamil i diltiazem to blokery kanału wapniowego zwalniające przewodnictwo i wydłużające okres refrakcji w węźle przedsionkowo-komorowym. Dożylna postać diltiazemu nie jest zarejestrowana w niektórych krajach. Działanie tych leków powoduje wygaszenie arytmii wynikających ze zjawiska re-entry, jak również pozwala na kontrolę czynności komór w przebiegu różnych tachyarytmii przedsionkowych. Wskazania do ich zastosowania obejmują: Stabilny, regularny częstoskurcz z wąskimi zespołami QRS bez reakcji na podanie adenozyny i stymulację nerwu błędnego, Kontrolę rytmu komór u pacjentów z AF lub trzepotaniem przedsionków z zachowaną funkcją komór, gdy czas trwania arytmii jest mniejszy niż 48 godz. Dawka wstępna werapamilu wynosi 2,5 5 mg podane dożylnie w ciągu 2 minut. Przy braku efektu i gdy nie występują objawy uboczne podania leku, należy powtórzyć dawkę 5 10 mg co minut do maksymalnej dawki 20 mg. Werapamil powinno się podawać tylko w przypadku napadowego częstoskurczu z wąskimi zespołami QRS lub w arytmiach o potwierdzonym nadkomorowym pochodzeniu. Podanie blokerów kanału wapniowego pacjentowi z częstoskurczem komorowym może spowodować zapaść krążeniową. Diltiazem w dawce 250 μg/kg z ewentualną drugą dawką 350 μg/kg jest równie skuteczny jak werapamil. Werapamil oraz, w mniejszym stopniu, diltiazem mogą zmniejszać kurczliwość mięśnia sercowego i krytycznie redukować rzut serca u pacjentów z ciężką dysfunkcją lewej komory. Z powodów przedstawionych w akapicie dotyczącym adenozyny patrz wyżej blokery kanału wapniowego uważane są za szkodliwe u pacjentów z AF lub trzepotaniem przedsionków w przebiegu zespołu preekscytacji (WPW). β-blokery Leki blokujące receptor β: atenolol, metoprolol, labetalol (posiadający właściwości blokujące receptor α i β), propranolol i esmolol zmniejszają efekt krążących katecholamin, częstość skurczów serca i obniżają ciśnienie krwi. Mają one także działanie kardioprotekcyjne u pacjentów z OZW. Użycie β-blokerów jest wskazane w przypadku następujących częstoskurczów: Regularny częstoskurcz z wąskimi zespołami QRS, niepoddający się kontroli za pomocą stymulacji nerwu błędnego ani za pomocą użycia adenozyny u pacjentów z zachowaną funkcją komór, AF i trzepotanie przedsionków w celu kontroli czynności komór przy ich zachowanej funkcji. Dożylna dawka atenololu (β1) wynosi 5 mg podane przez 5 minut. Można ją powtórzyć w razie potrzeby po 10 minutach. Metoprolol (β1) jest podawany w dawkach 2 5 mg co 5 minut do całkowitej dawki 15 mg. Propranolol (β1 i β2 efekt) 100 μg/kg podaje się powoli w trzech równych dawkach w odstępach 2 3 minutowych. Podawany dożylnie esmolol jest krótko działającym lekiem (czas półtrwania 2 9 min), blokującym selektywnie receptory β1. Dawka wysycająca podana dożylnie przez minutę wynosi 500 μg/kg. Następnie stosuje się wlew ciągły μg/kg/min. Efekty uboczne działania β-blokerów obejmują bradykardię, zwolnienie przewodnictwa przedsionkowo-komorowego, hipotensję. Przeciwwskazaniami do stosowania β-blokerów są blok serca II i III stopnia, hipotensja, ciężka zastoinowa niewydolność krążenia oraz choroby płuc z towarzyszącym skurczem oskrzeli. Magnez Magnez jest lekiem pierwszego rzutu w leczeniu polimorficznego częstoskurczu komorowego. Może być podany także w celu kontroli czynności komór w migotaniu przedsionków 617, Należy podawać 2 g siarczanu magnezu (8 mmol) przez 10 minut. Dawka ta może być powtórzona w razie konieczności. 4h Opieka poresuscytacyjna Wstęp Przywrócenie spontanicznego krążenia (ROSC) jest tylko pierwszym krokiem w kierunku osiągnięcia celu, jakim jest powrót do stanu zdrowia sprzed zatrzymania krążenia. Zespół objawów występujący po zatrzymaniu krążenia, obejmujący szereg złożonych procesów patofizjologicznych zachodzących na skutek uogólnionego niedokrwienia oraz reperfuzji po skutecznej resuscytacji nazwano syndromem poresuscytacyjnym (SP) 628. Wielu spośród tych pacjentów będzie wymagać wspomagania pracy wielu narządów, a leczenie stosowane w okresie poresuscytacyjnym ma znaczący wpływ na odległe wyniki dotyczące funkcjonowania układu nerwowego 184, Faza poresuscytacyjna rozpoczyna się w miejscu, gdzie udaje się osiągnąć ROSC. Po stabilizacji pacjent jest przekazywany na właściwy oddział o wzmożonym nadzorze (np. oddział intensywnej terapii, oddział intensywnej opieki kardiologicznej) celem dalszego monito- 4
147 146 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 rowania i leczenia. Około 25 56% pacjentów przyjętych na oddziały intensywnej terapii przeżyje do wypisu ze szpitala, liczba ta zależeć będzie od systemu i jakości opieki realizowanej w danym ośrodku 498,629,632, Znakomita większość pacjentów, którzy są wypisywani ze szpitala, charakteryzuje się dobrym stanem neurologicznym, aczkolwiek u wielu z nich rozpoznaje się zaburzenia funkcji poznawczych 639. Syndrom poresuscytacyjny W skład syndromu poresuscytacyjnego wchodzi uszkodzenie mózgu, dysfunkcja mięśnia sercowego, systemowa rekcja na niedokrwienie/reperfuzję oraz będące przyczyną wystąpienia zatrzymania krążenia wciąż obecne procesy patologiczne 628. Ciężkość występowania tych objawów różni się w zależności od czasu trwania i przyczyny zatrzymania krążenia. W przypadku krótkotrwałego zatrzymania krążenia, mogą one zupełnie nie wystąpić. Uszkodzenie móz gu po zatrzymaniu krążenia objawia się występowaniem śpiączki, drgawek, mioklonii, zróżnicowanych zaburzeń poznawczych oraz śmiercią mózgu. Wśród pacjentów, którzy przeżyli do przyjęcia na OIT, ale zmarli podczas hospitalizacji, uszkodzenie mózgu było przyczyną śmierci u 68% pacjentów z pozaszpitalnym zatrzymaniem krążenia oraz u 23% pacjentów po wewnątrzszpitalnym zatrzymaniu krążenia 245,640. Uszkodzenie mózgu po zatrzymaniu krążenia może być nasilone przez zaburzenia dotyczące mikrokrążenia, upośledzenie autoregulacji przepływu mózgowego, hiperkarbię, hiperoksję, gorączkę, hiperglikemię i drgawki. Znaczna dysfunkcja mięśnia sercowego występuje często po zatrzymaniu krążenia, ale typowo ustępuje po 2 3 dniach 641,642. Globalne niedokrwienie/reperfuzja występująca podczas zatrzymania krążenia aktywuje układ immunologiczny i krzepnięcia, co sprzyja wystąpieniu niewydolności wielonarządowej i zwiększonej podatności na zakażenia 643,644. Zatem syndrom poresuscytacyjny posiada wiele cech wspólnych z sepsą, w tym deficyt objętości wewnątrznaczyniowej i wazodylatację 645,646. Drogi oddechowe i oddychanie Pacjenci, u których doszło do krótkotrwałego zatrzymania krążenia i zastosowane właściwe leczenie przyniosło natychmiastowy rezultat, mogą szybko odzyskać prawidłowe funkcje CSN. Ci pacjenci nie wymagają intubacji dotchawiczej i wentylacji, lecz powinno im się podać tlen przez maskę twarzową. Hipoksemia i hiperkarbia mogą zwiększać prawdopodobieństwo kolejnego zatrzymania krążenia, jak również wtórnego uszkodzenia mózgu. W kilku badaniach z udziałem zwierząt wykazano, że hiperoksemia wywołuje stres oksydacyjny oraz powoduje uszkodzenie neuronów dotkniętych niedokrwieniem W jednym badaniu na zwierzętach wykazano, że modyfikacja FiO 2 w celu osiągnięcia saturacji krwi tętniczej do poziomu 94 96% w ciągu pierwszej godziny od ROSC (tzw. reoksygenacja kontrolowana) wiązała się z uzyskaniem mniejszej ilości powikłań neurologicznych w porównaniu do stosowania 100-procentowego tlenu 328. Niedawno opublikowane badanie typu registry study z udziałem ponad 6000 pacjentów potwierdziło wyniki obserwacji na zwierzętach i wykazało, że hiperoksemia po resuscytacji wiąże się z gorszymi wynikami leczenia w porównaniu zarówno do normo- jak i hipoksemii 329. W praktyce klinicznej, jak tylko uzyska się dostęp do wiarygodnych metod monitorowania saturacji krwi tętniczej (analiza gazometryczna i/lub pulsoksymetria), najbardziej praktyczne wydaje się miareczkowanie stężenia tlenu w podawanej mieszaninie oddechowej, aż do osiągnięcia saturacji krwi tętniczej w granicach 94 98%. Należy rozważyć intubację dotchawiczą, sedację i kontrolowaną wentylację u każdego pacjenta z obniżoną aktywnością CSN. Należy potwierdzić właściwe położenie rurki intubacyjnej powyżej rozwidlenia tchawicy. Hipokarbia powoduje skurcz naczyń mózgowych i zmniejszenie przepływu mózgowego 651. Po zatrzymaniu krążenia hipokapnia wywołana hiperwentylacją powoduje niedokrwienie mózgu Nie ma danych określających docelowy poziom PaCO 2 po resuscytacji, lecz jest wskazane prowadzenie odpowiedniej wentylacji w celu osiągnięcia normokarbii. Należy monitorować zarówno końcowo-wydechowy poziom PCO 2, jak i gazometrię krwi tętniczej. Korzystne jest odbarczenie żołądka za pomocą zgłębnika. Rozdęcie żołądka powodowane przez wentylację usta usta lub użycie worka samorozprężalnego z maską powoduje zmniejszenie ruchomości przepony i upośledza wentylację. Należy stosować odpowiednie dawki leków sedujących w celu redukcji zużycia tlenu. Może wystąpić konieczność podania bolusowych dawek leków zwiotczających mięśnie, szczególnie w przypadku stosowania hipotermii terapeutycznej (patrz niżej). Należy jednak unikać podawania tych leków w postaci ciągłych wlewów, ich działanie może wtedy maskować wystąpienie drgawek. Należy wykonać zdjęcie radiologiczne klatki piersiowej, by ocenić położenie rurki dotchawiczej, cewników w naczyniach centralnych, ocenić w kierunku obecności obrzęku płuc czy powikłań resuscytacji, takich jak na przykład odma związana ze złamaniem żeber. Krążenie U większości pacjentów z pozaszpitalnym zatrzymaniem krążenia stwierdza się chorobę wieńcową 656,657. Ostre zmiany dotyczące blaszki miażdżycowej w naczyniach wieńcowych obecne są u 40 86% pacjentów, którzy przeżyli zatrzymanie krążenia oraz opisywane w 15 64% badań sekcyjnych 658. Pacjenci po przywróceniu krążenia, u których stwierdza się zawał mięśnia sercowego z uniesieniem odcinka ST (STEMI), powinni mieć wykonaną wczesną angiografię naczyń wieńcowych oraz PCI. Ponieważ ból w klatce piersiowej i/lub uniesienie odcinka ST są złymi czynnikami, wskazującymi na ostrą okluzję naczyń wieńcowych w tej grupie pacjentów 659, interwencje te należy rozważyć u wszystkich pacjentów po przywróceniu krążenia, u których podejrzewa się chorobę wieńcową 629,633, Wyniki wielu badań wskazują, że równoczesne stosowanie hipotermii terapeutycznej i PCI jest możliwe do przeprowadzenia i bezpieczne u pacjentów po resuscytacji, u których zatrzymanie krążenia było spowodowane ostrym zawałem mięśnia sercowego 629, 633, 638, 665,666. Dysfunkcja mięśnia sercowego po zatrzymaniu krążenia prowadzi do niestabilności hemodynamicznej, co objawia się występowaniem hipotensji, niskim wskaźnikiem sercowym oraz zaburzeniami rytmu 641. Wcześnie wykonane badanie echokardiograficzne umożliwia oszacowanie stop-
148 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 147 nia dysfunkcji mięśnia sercowego 642. W warunkach OIT ciągły inwazyjny pomiar ciśnienia tętniczego krwi jest niezbędny. Terapia z wykorzystaniem płynów, leków inotropowych i wazopresyjnych może być oparta na analizie parametrów takich, jak ciśnienie tętnicze, częstość rytmu serca, diureza, osoczowy klirens mleczanu, saturacja krwi żylnej centralnej. Techniki nieinwazyjnego pomiaru rzutu serca mogą być pomocne w prowadzeniu terapii, lecz nie udowodniono, aby ich stosowanie wpływało na odległe jego wyniki leczenia. Jeśli płynoterapia i stosowanie leków wazoaktywnych nie jest skuteczne w stabilizacji układu krążenia, należy rozważyć kontrapulsację wewnątrzaortalną 629,638. Przetoczenie względnie dużej objętości płynów jest nadzwyczaj dobrze tolerowane przez pacjentów z syndromem poresuscytacyjnym 513,629,630,641. Mimo że leczenie ukierunkowane na cel (goal directed therapy) znalazło zastosowanie w leczeniu sepsy 667 i zostało również zaproponowane jako strategia postępowania u pacjentów po zatrzymaniu krążenia 630, jak dotąd brak jest randomizowanych badań, popierających jego rutynowe stosowanie w tym przypadku. Jest bardzo mało randomizowanych badań oceniających wpływ ciśnienia krwi na wyniki leczenia pacjentów po zatrzymaniu krążenia. Jedno z nich nie wykazało różnic w stanie neurologicznym pomiędzy grupą pacjentów ze średnim ciśnieniem krwi >100 mm Hg w porównaniu z grupą ze średnim ciśnieniem 100 mm Hg w 5 minut po ROSC, jakkolwiek dobry efekt neurologiczny wiązał się z wyższym ciśnieniem krwi w ciągu 2 pierwszych godzin po ROSC 668. W jednym badaniu, w oparciu o rejestr ponad 6000 pacjentów po zatrzymaniu, występowanie hipotensji (ciśnienie skurczowe <90 mm Hg) przy przyjęciu do OIT wiązało się z gorszym rokowaniem 668a. Dobre wyniki końcowe osiągnięto w badaniach z udziałem pacjentów przyjętych do szpitala po pozaszpitalnym zatrzymaniu krążenia, u których docelowa wartość średniego ciśnienia krwi była nie mniejsza niż mm Hg 629 i nie większa niż mm Hg 632, 669. Wobec braku ostatecznych danych należy dążyć do osiągnięcia średniego ciśnienia tętniczego pozwalającego na uzyskanie odpowiedniej diurezy (1 ml/kg/h) i prawidłowego lub malejącego osoczowego poziomu mleczanu, biorąc pod uwagę wartość ciśnienia tętniczego krwi prawidłową dla danego pacjenta, przyczynę wywołującą zatrzymanie krążenia oraz ciężkość dysfunkcji mięśnia sercowego 628. Należy pamiętać, że hipotermia może zwiększać diurezę i upośledzać klirens mleczanów. Natychmiast po wystąpieniu zatrzymania krążenia dochodzi zwykle do przejściowej hiperkaliemii. Następowe uwolnienie endogennych katecholamin powoduje wewnątrzkomórkowy transport potasu i w konsekwencji hipokaliemię. Hipokaliemia może predysponować do wystąpienia komorowych zaburzeń rytmu. Należy stosować suplementację potasu celem utrzymania w surowicy poziomu 4 4,5 mmol/l. Ocena neurologiczna (optymalizacja powrotu funkcji neurologicznych) Perfuzja mózgowa Natychmiast po ROSC dochodzi do przejściowego przekrwienia mózgu 670. Po zatrzymaniu krążenia wynikającym z asfiksji i uzyskaniu ROSC obserwuje się przejściowy obrzęk mózgu, któremu rzadko towarzyszy klinicznie istotny wzrost ciśnienia śródczaszkowego 671,672. Po przywróceniu krążenia na pewien czas upośledzona jest autoregulacja przepływu mózgowego, co powoduje, że przepływ mózgowy uzależniony jest od mózgowego ciśnienia perfuzji, a nie jest związany z aktywnością neuronalną 673,674. Należy więc, jak wcześniej wspomniano, utrzymywać średnie ciśnienie krwi na poziomie normalnego ciśnienia krwi danego pacjenta. Sedacja Pomimo powszechnego stosowania sedacji i wentylacji pacjentów na przynajmniej 24 godziny po ROSC, nie ma jednoznacznych danych uzasadniających takie postępowanie, jak również stosowanie leków zwiotczających u pacjentów po zatrzymaniu krążenia. U pacjentów poddanych terapeutycznej hipotermii należy stosować sedację i sztuczną wentylację, których długość trwania zależy od czasu jej stosowania. Nie ma danych określających, czy rodzaj sedacji wpływa na wyniki leczenia, ale najczęściej stosowana jest kombinacja opioidu i leku nasennego. Krótko działające leki (np. propofol, alfentanyl, remifentanyl) dają możliwość wcześniejszej oceny neurologicznej. Odpowiednia sedacja zmniejsza zużycie tlenu. Podczas leczenia hipotermią optymalna sedacja pozwala także zmniejszyć lub zapobiec występowaniu dreszczy, co z kolei skraca czas osiągnięcia temperatury docelowej. W monitorowaniu takich pacjentów pomocne jest wykorzystanie dostępnych skal oceny głębokości sedacji (np. Richmond lub Ramsay) 675, 676. Kontrola drgawek Drgawki i/lub mioklonie występują w 5 15% przypadków dorosłych pacjentów po ROSC i około 10 40% przypadków spośród tych, którzy pozostają w stanie śpiączki 498, Drgawki mogą spowodować aż trzykrotne zwiększenie metabolizmu mózgowego 681 i uszkodzenie CSN, dlatego powinny być szybko i skutecznie kontrolowane za pomocą benzodiazepin, fenytoiny, walproinianu sodu, propofolu lub barbituranów. Mioklonie są przeważnie trudne do leczenia, a fenytoina jest wtedy często nieskuteczna. Klonazepam jest najbardziej skutecznym lekiem przeciwdrgawkowym, choć równie skuteczne mogą być: walproinian sodu, levetiracetam i propofol 682. Należy wdrożyć terapię podtrzymującą natychmiast po wykluczeniu potencjalnej przyczyny drgawek (np. krwawienia śródczaszkowego, zaburzeń elektrolitowych). Żadne z prowadzonych badań nie analizowało bezpośrednio zagadnienia profilaktycznego stosowania leków przeciwdrgawkowych u dorosłych pacjentów po zatrzymaniu krążenia. Kontrola poziomu glukozy Istnieje silny związek pomiędzy wysokim poziomem glikemii u pacjentów po resuscytacji a niekorzystnym neurologicznym rokowaniem ,504,634,683,684. Chociaż w jednym randomizowanym badaniu z udziałem grupy kontrolnej przeprowadzonym w warunkach oddziału intensywnej terapii kardiochirurgicznej wykazano, że ścisła kontrola glikemii (4,4 6,1 mmol/l lub mg/dl) przy użyciu insuliny redukuje wewnątrzszpitalną śmiertelność u krytycznie 4
149 148 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 chorych, dorosłych pacjentów 685, w innym badaniu nie uzyskano podobnych wyników 686. W jednym badaniu randomizowanym z udziałem osób z pozaszpitalnym zatrzymaniem krążenia w mechanizmie migotania komór i skutecznej resuscytacji ścisła kontrola glikemii w przedziale mg/ dl (4 6 mmol/l) nie wiązała się ze zwiększonym przeżyciem w porównaniu do grupy z umiarkowaną kontrolą glikemii mg/dl (6 8 mmol/l) i charakteryzowała się zwiększonym ryzykiem wystąpienia hipoglikemii u tych pacjentów 687. Duże badanie z randomizacją wykazało, że intensywna kontrola glikemii (4,5 6,0 mmol/l) w porównaniu do kontroli konwencjonalnej (10 mmol/l i mniej) u pacjentów w OIT wiąże się ze zwiększoną 90-dniową śmiertelnością w grupie z intensywną kontrolą glikemii 688. Inne niedawno opublikowane badanie oraz 2 metaanalizy badań porównujących ścisłą i konwencjonalną kontrolę glikemii u ciężko chorych pacjentów wykazały brak istotnej różnicy w śmiertelności, podczas gdy intensywna kontrola glikemii wiązała się ze znacznym zwiększeniem ryzyka wystąpienia hipoglikemii Ciężka hipoglikemia wiąże się ze zwiększoną śmiertelnością w grupie ciężko chorych pacjentów 692. Pacjenci w stanie śpiączki są szczególnie zagrożeni wystąpieniem nierozpoznanej hipoglikemii. Udowodniono, że niezależnie od zakresu wartości docelowych wahania poziomu glikemii wiążą się ze śmiertelnością 693. W oparciu o powyższe dane poziom glikemii po ROSC powinien być utrzymywany 10 mmol/l (180 mg/dl) 694. Należy unikać hipoglikemii. Nie należy stosować intensywnej kontroli glikemii u dorosłych pacjentów po zatrzymaniu krążenia i ROSC z uwagi na zwiększone ryzyko wystąpienia hipoglikemii w tej grupie chorych. Kontrola temperatury Leczenie hiperpyreksji Okres hipertermii (hiperpyreksji) występuje często w ciągu pierwszych 48 godzin po zatrzymaniu krążenia Kilkanaście badań wykazało związek pomiędzy wystąpieniem gorączki po zatrzymaniu krążenia i złymi wynikami końcowego leczenia 498,695, Nie przeprowadzono żadnych randomizowanych badań z grupą kontrolną porównujących wyniki leczenia pacjentów, u których leczono pyreksję (definiowaną jako temperatura ciała 37,6 C) w porównaniu z pacjentami po zatrzymaniu krążenia, u których nie kontrolowano gorączki. Pomimo że nie udowodniono wpływu temperatury na końcowe wyniki leczenia, wydaje się, iż rozsądne jest leczenie jakiegokolwiek epizodu hipertermii występującego po zatrzymaniu krążenia, stosując leki przeciwgorączkowe lub aktywne chłodzenie. Terapeutyczna hipotermia W oparciu o wyniki badań z udziałem zwierząt i ludzi uważa się, że umiarkowana hipotermia ma działanie neuroprotekcyjne i poprawia wyniki końcowe po okresie uogólnionej hipoksji-niedokrwieniu mózgu 701,702. Schłodzenie hamuje liczne szlaki prowadzące do opóźnionej śmierci komórki, w tym do apoptozy (zaprogramowanej śmierci komórki). Hipotermia powoduje zmniejszenie wskaźnika mózgowego metabolizmu tlenu (CMRO 2 ) o około 6% na każdy 1 C obniżonej temperatury 703, a to z kolei może hamować uwalnianie aminokwasów pobudzających i powstawanie wolnych rodników 701. Hipotermia blokuje wewnątrzkomórkowe konsekwencje ekspozycji na substancje toksyczne (wysokie stężenie jonów wapnia i glutaminianu) i redukuje odpowiedź zapalną związaną z syndromem poresuscytacyjnym. Którzy pacjenci po zatrzymaniu krążenia powinni być schładzani? Wszystkie badania poświęcone hipotermii terapeutycznej po zatrzymaniu krążenia dotyczyły jedynie pacjentów w stanie śpiączki. Istnieją silne dowody na poparcie stosowania indukowanej hipotermii u pacjentów w stanie śpiączki po pozaszpitalnym zatrzymaniu krążenia w mechaniz mie VF. Jedno badanie kliniczne z randomizacją 704 i jedno badanie z pseudorandomizacją 669 wykazały poprawę neurologicznych wyników leczenia przy wypisie ze szpitala lub po upływie 6 miesięcy u dorosłych pacjentów w stanie śpiączki po resuscytacji z powodu pozaszpitalnego zatrzymania krążenia (VF). Schładzanie było inicjowane w kilka minut lub godzin po ROSC, a następnie utrzymywano temperaturę na poziomie C przez godzin. W dwóch badaniach z udziałem historycznych grup kontrolnych wykazano poprawę neurologicznych wyników leczenia u pacjentów pozostających w stanie śpiączki po epizodzie NZK w mechanizmie VF, u których zastosowano hipotermię terapeutyczną Ekstrapolacja tych wyników na zatrzymania krążenia wywołane innymi przyczynami (inne rytmy, wewnątrzszpitalne, pacjenci pediatryczni) wydaje się rozsądna, ale oparta na danych o niższej wiarygodności. Jedno małe, randomizowane badanie udokumentowało redukcję poziomu mleczanów i ekstrakcji tlenu u pozostających w stanie śpiączki pacjentów z ROSC po zatrzymaniu krążenia w mechanizmie PEA lub asystolii, u których stosowano hełm chłodzący 708. W sześciu badaniach z udziałem historycznych grup kontrolnych wykazano korzyść ze stosowania hipotermii terapeutycznej u pacjentów ze śpiączką, po epizodzie pozaszpitalnego zatrzymania krążenia niezależnie od jego mechanizmu 629,632, Dwa badania kliniczne bez randomizacji z grupą kontrolną wykazały możliwą korzyść ze stosowania hipotermii po epizodzie zatrzymania krążenia w innych pierwotnych rytmach, w warunkach zarówno wewnątrz- jak i pozaszpitalnych 713,714. Jak schładzać? Praktyczne stosowanie hipotermii leczniczej zostało podzielone na trzy fazy: indukcja, podtrzymanie i ponowne ogrzanie 715. Do rozpoczęcia schładzania mogą być stosowane techniki zewnętrzne i/lub wewnętrzne. Wlew 30 ml/kg roztworu soli fizjologicznej lub roztworu Hartmanna o temperaturze 4 C obniża głęboką temperaturę ciała o 1,5 C 629,633,638,706,707,711, Technika ta może być wdrażana już w warunkach przedszpitalnych 511, W skład innych metod indukowania i/lub podtrzymywania hipotermii wchodzą: Worki z lodem i/lub mokre ręczniki są tanie, jakkolwiek metody te są czasochłonne dla personelu pielęgniarskiego, ich stosowanie może wiązać się z występowaniem większych wahań temperatury i nie
150 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 149 zapewniają odpowiedniej kontroli w trakcie ogrzewania 633,638,669,705,709,710,725,726, Schłodzone płyny nie mogą być stosowane do podtrzymywania hipotermii 719, lecz dodanie zwykłych worków z lodem może pozwolić na odpowiednią kontrolę temperatury 725 Chłodzące koce lub podkłady 727, Donosowe systemy chłodzące 740a Koce z obiegiem zimnej wody lub powietrza 629,630,632,706, 707,712,713,727, Żelowe podkłady z obiegiem wody 629,711,720,721,727,738,743,745 Wewnątrznaczyniowy wymiennik ciepła, umieszczany w żyle udowej lub podobojczykowej 629,630,713,714,718,724, 727,732,733,742, Krążenie pozaustrojowe 749. W większości przypadków schłodzenie pacjentów po ROSC nie stanowi większego problemu, ponieważ w ciągu pierwszej godziny po zatrzymaniu krążenia normalnie występuje obniżenie temperatury ciała 498,698. Stosowanie leków zwiotczających i sedacji (zapobieganie występowaniu dreszczy) ułatwia wstępne schładzanie pacjentów 750. Można rozważyć stosowanie siarczanu magnezu, naturalnie występującego antagonisty receptora NMDA, by w niewielkim stopniu obniżyć próg drżeniowy 715,751. W fazie podtrzymania schładzania preferowane są metody umożliwiające skuteczną kontrolę temperatury, unikając zmienności jej poziomu. Można to osiągnąć, stosując techniki zewnętrzne lub wewnętrzne, dające ciągłą informację zwrotną, co pozwala uzyskać temperaturę docelową. Temperatura jest zwykle monitorowana za pomocą termistora umieszczonego w pęcherzu moczowym i/lub przełyku 715. Do tej pory nie opublikowano danych wskazujących, by zastosowanie jakiejkolwiek szczególnej techniki chłodzenia, w porównaniu z innymi, wpływało na poprawę przeżywalności, jakkolwiek urządzenia wewnątrznaczyniowe umożliwiają bardziej precyzyjną kontrolę temperatury w porównaniu z technikami zewnętrznymi 727. Podczas fazy ogrzewania, podobnie jak w fazie chłodzenia, stężenia elektrolitów w osoczu, skuteczna objętość wewnątrznaczyniowa i wskaźnik metaboliczny mogą ulegać gwałtownym zmianom. Z tego powodu ogrzewanie musi następować stopniowo. Optymalny wskaźnik nie jest znany, ale uzgodniono, że powinien wynosić około 0,25 0,5 C w ciągu godziny 713. Kiedy schładzać? Badania na zwierzętach wskazują, że wcześniejsze zastosowanie schładzania po ROSC wiąże się z lepszymi wynikami leczenia 752. W zasadzie wdrażanie schładzania podczas zatrzymania krążenia może okazać się najbardziej korzystne badania na zwierzętach wskazują, że może to ułatwiać osiągnięcie ROSC 753,754. Kilka badań klinicznych wykazało, że hipotermia może być wdrożona już w warunkach przedszpitalnych 510,728,729,731,740,740a, ale jak dotąd nie wykazano, że szybkość osiągnięcia temperatury docelowej skutkuje lepszymi wynikami leczenia u ludzi. W jednym badaniu opartym na rejestrze przypadków klinicznych dotyczącym 986 pacjentów w stanie śpiączki po zatrzymaniu krążenia zasugerowano, że czas do wdrożenia schładzania nie wiązał się z poprawą neurologicznego wyniku leczenia ocenianego po wypisie ze szpitala 665. W serii przypadków obejmujących 49 pacjentów w stanie śpiączki po pozaszpitalnym zatrzymaniu krążenia i schładzanych metodą wewnątrznaczyniową wykazano, że czas do osiągnięcia temperatury docelowej nie był niezależnym czynnikiem predykcyjnym związanym z neurologicznym wynikiem leczenia 748. Efekty fizjologiczne i powikłania związane ze stosowaniem hipotermii Poniżej przedstawiono dobrze poznane fizjologiczne efekty stosowania hipotermii, które należy szczególnie wziąć pod uwagę w trakcie leczenia 715 : Drżenia zwiększają metabolizm i produkcję ciepła. Powyżej przedstawiono strategie umożliwiające ograniczenie ich występowania. Umiarkowana hipotermia zwiększa systemowy opór naczyniowy i wywołuje zaburzenia rytmu (zwykle bradykardię) 714. Hipotermia prowadzi do zwiększenia diurezy i zaburzeń dotyczących poziomu elektrolitów, takich jak hipofosfatemia, hipokaliemia, hipomagnezemia i hipokalcemia 715,755. Hipotermia zmniejsza wrażliwość na insulinę, jej wydzielanie i powoduje hiperglikemię 669, która wymaga leczenia insuliną (patrz kontrola glikemii). Umiarkowana hipotermia zaburza proces krzepnięcia i sprzyja krwawieniom, choć nie znalazło to odzwierciedlenia w licznych badaniach klinicznych 629,704. W jednym badaniu opartym na rejestrze pacjentów wykazano zwiększoną częstość występowania niewielkich krwawień związanych z wykonywaniem angiografii naczyń wieńcowych podczas stosowanej hipotermii terapeutycznej, ale połączenie tych interwencji było najlepszym czynnikiem prognostycznym związanym z wystąpieniem dobrych wyników leczenia 665. Hipotermia może zaburzać czynność układu odpornościowego i zwiększać ilość zakażeń 715,734,736. Podczas hipotermii stężenie amylazy w surowicy jest często zwiększone, ale znaczenie tego zjawiska pozostaje niejasne. Klirens leków sedujących i zwiotczających mięśnie w temperaturze 34 C ulega zmniejszeniu do 30% 756. Przeciwwskazania do stosowania hipotermii Ogólnie znane przeciwwskazania do stosowania hipotermii terapeutycznej, niemające jednak uniwersalnego zastosowania, obejmują: ciężkie zakażenia układowe, potwierdzoną niewydolność wielonarządową oraz istniejącą wyjściowo koagulopatię (terapia fibrynolityczna nie jest przeciwwskazaniem do stosowania hipotermii terapeutycznej). Inne metody leczenia Nie wykazano, aby stosowanie leków neuroprotekcyjnych (koenzym Q10 737, tiopental 757, glikokortykosteroidy 758,759, nimodypina 760,761, lidoflazyna 762 lub diazepam 452 ) w monoterapii lub w skojarzeniu z hipotermią terapeutyczną zwiększało przeżycie z dobrym wynikiem neurologicznym u pacjentów po zatrzymaniu krążenia. W chwili obecnej nie ma wystarczającej ilości danych uzasadniających ru- 4
151 150 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 tynowe stosowanie hemofiltracji wysokoobjętościowej 763 w celu poprawy neurologicznego wyniku leczenia u pacjentów z ROSC. Prognozowanie/rokowanie Przyczyną dwóch trzecich zgonów pacjentów z pozaszpitalnym zatrzymaniem krążenia, którzy zmarli po przyjęciu na OIT, było uszkodzenie neurologiczne, niezależnie od tego, czy zastosowano hipotermię terapeutyczną 245, czy nie 640. W przypadku wewnątrzszpitalnych zatrzymań krążenia przyczyna ta odpowiadała za jedną czwartą zgonów pacjentów przyjętych na OIT. Poszukiwane są metody, jakie można zastosować u indywidualnych pacjentów w celu prognozowania neurologicznych wyników leczenia bezpośrednio po ROSC. Wiele badań koncentruje się na prognozowaniu wystąpienia niekorzystnych odległych wyników leczenia (stan wegetatywny lub zgon) w oparciu o badanie kliniczne lub testy laboratoryjne wskazujące na istnienie nieodwracalnego uszkodzenia mózgu. Mają one na celu pomóc klinicystom w podjęciu decyzji o zaprzestaniu uporczywej terapii. Warunkiem zastosowania tych testów prognostycznych powinna być 100-procentowa swoistość oraz wskaźnik wyników fałszywie dodatnich (False Positive Rate FPR) na poziomie zero, tj. możliwość identyfikacji pacjentów, którzy ostatecznie uzyskają dobre długoterminowe wyniki leczenia pomimo przewidywania złego rokowania. Prognozowanie wyników leczenia u pacjentów po NZK jest kontrowersyjne z uwagi na: (1) wiele badań jest niewłaściwie zaplanowanych z powodu dążenia do uzyskania założonych wyników (rzadko wystarczająco długo kontynuuje się leczenie u dobrze rokujących pacjentów, aby umożliwić uzyskanie prawdziwej oceny wskaźnika wyników fałszywie dodatnich dla każdego czynnika prognostycznego); (2) w wielu badaniach bierze udział tak nieliczna grupa pacjentów, że nawet gdy FPR wnosi 0%, górna granica 95% przedziału ufności może być wysoka; oraz (3) większość badań dotyczących prognozowania wyników leczenia przeprowadzono jeszcze przed wprowadzeniem hipotermii terapeutycznej i istnieją dowody, że wdrożenie tej terapii czyni oceniane testy mniej wiarygodnymi. Testy kliniczne Nie ma neurologicznych objawów, za pomocą których można wiarygodnie przewidzieć niekorzystny wynik leczenia (Cerebral Performance Category [CPC]: 3, 4 lub zgon) w ciągu pierwszych 24 godzin po zatrzymaniu krążenia. U pacjentów dorosłych pozostających w stanie śpiączki po zatrzymaniu krążenia, którzy nie byli leczeni za pomocą hipotermii terapeutycznej i wykluczono u nich czynniki wpływające na wiarygodną ocenę (takie jak hipotensja, leki uspakajające lub zwiotczające), brak zarówno reakcji źrenic na światło, jak i odruchów rogówkowych w okresie 72 godzin uważa się za wiarygodne czynniki prognostyczne niepomyślnego wyniku leczenia (FPR 0%, 95% CI 0 9%) 680. Mniej wiarygodne jest stwierdzenie braku odruchów przedsionkowo-ocznych w okresie 24 godzin (FPR 0%, 95% CI 0 14%) 764,765 oraz odpowiedzi motorycznej ocenianej wg skali GCS równej lub niższej od 2 72 godzin (FPR 5%, 95% CI 2 9%) 680. Inne objawy kliniczne, w tym mioklonie, nie są uważane za czynniki predykcyjne niepomyślnego rokowania. Obecność stanu mioklonicznego u pacjentów dorosłych silnie wiąże się ze złym rokowaniem 679,680, , jakkolwiek opisywano rzadkie przypadki dobrych neurologicznych wyników leczenia w tej grupie pacjentów, co powoduje, że postawienie właściwej diagnozy w tych przypadkach jest problematyczne Markery biochemiczne Wzrost poziomu neurono-specyficznej enolazy (NSE) w surowicy wiąże się ze złym rokowaniem u pacjentów w stanie śpiączki po zatrzymaniu krążenia 680,748, Mimo że w różnych badaniach raportowano występowanie specyficznych wartości odcięcia dla wskaźnika wyników fałszywie dodatnich wynoszącego 0%, to jego kliniczne zastosowanie jest ograniczone z uwagi na opisywane zróżnicowanie wartości odcięcia dla FPR 0%. Wzrost stężenia białka S100 wiąże się ze złym rokowaniem u pacjentów w stanie śpiączki po zatrzymaniu krążenia 680, ,782,784,785,787,788,791, Pozostałe markery osoczowe, takie jak: BNP 799, vwf 800, ICAM-1 800, prokalcytonina 794, IL-1ra, RANTES, stnfrii, IL-6, IL-8 i IL mierzone po uzyskaniu ROSC, wiążą się ze złym rokowaniem po zatrzymaniu krążenia. Jednak w innych badaniach nie udowodniono związku pomiędzy wynikami leczenia a osoczowym poziomem IL-8 793, prokalcytoniny oraz strem Gorsze rokowanie u pacjentów w stanie śpiączki po NZK jest również związane ze zwiększonym poziomem CK 802,803 oraz CKBB w płynie mózgowo-rdzeniowym 774,775,777,789, Jakkolwiek jedno badanie nie wykazało związku pomiędzy wynikami leczenia a poziomem CKBB w płynie mózgowo- -rdzeniowym 808. Wyniki leczenia są także związane ze zwiększonym poziomem innych markerów w płynie mózgowo-rdzeniowym, takich jak NSE 775,784,789, S , LDH,GOT 777,803, neurofilament 809, fosfataza kwaśna i mleczany 803. Nie wykazano, aby poziom beta-d-n-acetyloglukozaminidazy oraz pirogronianu, oceniany w płynie mózgowo rdzeniowym, wiązał się z rokowaniem u pacjentów po zatrzymaniu krążenia 803. Podsumowywując, nie udowodniono, aby izolowana ocena biomarkerów osoczowych i obecnych w płynie mózgowo-rdzeniowym była przydatnym narzędziem rokowniczym u pacjentów w stanie śpiączki po zatrzymaniu krążenia bez względu na to, czy zastosowano hipotermię terapeutyczną czy nie. Czynnikami ograniczającymi przydatność tych parametrów jest niska liczebność badanej populacji pacjentów i/lub brak jednolitych wartości odcięcia dla prognozowania złych wyników leczenia. Badania elektrofizjologiczne Żadne z badań elektrofizjologicznych nie pozwala w sposób wiarygodny przewidzieć wyników leczenia u pacjentów w śpiączce w ciągu pierwszych 24 godzin po zatrzymaniu krążenia. W przypadku pomiaru somatosensorycznych potencjałów wywołanych obustronny brak odpowiedzi korowej N20 na stymulację nerwu pośrodkowego u pacjentów w śpiączce po zatrzymaniu krążenia, nieleczonych za pomocą hipotermii terapeutycznej, wiąże się jednoznacznie ze złym rokowaniem (zgon lub CPC 3 lub 4) z FPR równym
152 Zaawansowane zabiegi resuscytacyjne u osób dorosłych 151 0,7% (95% CI: 0,1 3,7) 774. Wobec braku zdarzeń zakłócających, takich jak stosowanie leków sedujących, hipotensja, hipotermia lub hipoksemia, zasadne jest traktowanie nieprzetworzonego zapisu EEG (szczególnie, gdy rozpoznawane jest uogólnione hamowanie aktywności korowej do poziomu poniżej 20 μv, obecność wyładowań typu burst suppression z obrazem uogólnionej aktywności padaczkowej lub rozsiane wyładowania złożone występujące okresowo i towarzyszące płaskiemu zapisowi), otrzymanego w okresie od 24 do 72 godzin od uzyskania ROSC, jako metodę pomocniczą w ocenie złego rokowania (FPR 3%, 95% CI: 0,9 11%), jeśli dotyczy to pacjentów w stanie śpiączki po zatrzymaniu krążenia, którzy nie byli leczeni za pomocą hipotermii 774. Brak jest właściwych dowodów, by popierać rutynowe stosowanie innych badań elektrofizjologicznych (np. nieprawidłowe słuchowe potencjały wywołane z pnia mózgu) w prognozowaniu złych wyników leczenia u pacjentów po zatrzymaniu krążenia 606. Badania obrazowe Badano wiele metod obrazowania pod kątem ich przydatności w ocenie rokowania wyników leczenia u dorosłych pacjentów po zatrzymaniu krążenia. W tym gronie znalazły się MRI, TK, SPECT, angiografia naczyń mózgowych, Doppler przezczaszkowy, badania z zakresu medycyny nuklearnej, NIRS (Near Infra-red Spectroscopy) 606. Nie opublikowano dotąd badań pierwszego lub drugiego poziomu dowodów naukowych, które potwierdzałyby zasadność stosowania którejkolwiek z powyższych metod w prognozowaniu wyników leczenia u pacjentów w stanie śpiączki po zatrzymaniu krążenia. Podsumowując, uwzględnionych badań obrazowych nie uznano za przydatne z uwagi na ich wykonanie u nielicznej grupy pacjentów, w różnych okresach leczenia (wiele z nich wykonano pod koniec okresu leczenia), brak możliwości porównania ze standaryzowaną metodą prognozowania i wczesnym zaprzestaniem leczenia. Pomimo ogromnego potencjału metod neuroobrazowania, pozostaje wciąż do udowodnienia ich rola w procesie niezależnego i dokładnego prognozowania wyników leczenia u pacjentów w stanie śpiączki po zatrzymaniu krążenia. Ich rutynowe stosowanie nie jest zalecane. Wpływ hipotermii terapeutycznej na prognozowanie/ rokowanie Istnieje niewystarczająca ilość dowodów potwierdzających przydatność stosowania określonego sposobu prognozowania niepomyślnych wyników leczenia u pacjentów po zatrzymaniu krążenia leczonych za pomocą hipotermii terapeutycznej. Do chwili obecnej nie uznano, aby jakikolwiek neurologiczny objaw kliniczny, badanie elektrofizjologiczne, biomarkery lub badanie obrazowe pozwalały w sposób wiarygodny określić neurologiczny wynik leczenia w ciągu pierwszych 24 godzin po zatrzymaniu krążenia. W oparciu o ograniczoną liczbę dostępnych dowodów obustronny brak odpowiedzi korowej N20 na stymulację nerwu pośrodkowego 24 godzin po zatrzymaniu krążenia (FPR 0%, 95% CI: 0 69%) oraz brak zarówno reakcji źrenic na światło, jak i odruchów rogówkowych w okresie 3 dni od zatrzymania krążenia (FPR 0%, 95% CI 0 48%) uważa się za potencjalnie wiarygodne czynniki prognozujące złe rokowanie u pacjentów leczonych za pomocą hipotermii 766,810. Istnieje ograniczona ilość danych wskazujących, że także funkcje motoryczne określone wg skali GCS 2 w okresie 3 dni po ROSC (FPR 14%, 95% CI 3 44%) 766 oraz obecność stanu padaczkowego (FPR 7% [95% CI 1 25%] do 11,5% [95% CI 3 31%]) 811,812 są potencjalnie niewiarygodnymi czynnikami prognozującymi niepomyślne rokowanie u pacjentów leczonych za pomocą hipotermii. W jednym z badań, które objęło 111 pacjentów po NZK leczonych za pomocą hipotermii, próbowano walidować kryteria prognostyczne zaproponowane przez American Academy of Neurology 774,813. Badanie wykazało, że wyniki badania klinicznego przeprowadzonego w ciągu godzin nie były wiarygodnymi czynnikami prognozującymi złe rokowanie, podczas gdy obustronny brak odpowiedzi korowej N20 podczas somatosensorycznych potencjałów wywołanych (FPR 0%, 95% CI: 0 13%) oraz niereaktywny zapis EEG (FPR 0%, 95% CI: 0 13%) uznano za najbardziej wiarygodne. Reguła decyzyjna oparta na powyższych danych wykazała, że obecność dwóch niezależnych czynników prognostycznych (niepełne odruchy z pnia mózgu, wcześnie występujące mioklonie oraz obustronny brak korowych somatosensorycznych potencjałów wywołanych) świadczy o złym rokowaniu neurologicznym u pacjentów leczonych za pomocą hipotermii z FPR 0% (95% CI: 0 14%). Oznaczanie poziomu biomarkerów w osoczu, takich jak NSE, traktuje się jako badanie dodatkowe przy ocenie rokowania u pacjentów leczonych za pomocą hipotermii. Wiarygodność tego badania jest ograniczona z uwagi na małą liczebność badanej grupy oraz brak optymalnej standaryzacji tej metody 814,815. Ze względu na ograniczoną ilość dostępnych dowodów decyzja o zaprzestaniu terapii nie powinna opierać się wyłącznie na wynikach pojedynczych narzędzi prognostycznych. Przeszczepianie narządów Możliwe jest skuteczne przeszczepianie narządów od pacjentów po śmierci sercowej (cardiac death) 816. Ta grupa pacjentów daje niewykorzystywaną możliwość zwiększenia ilości potencjalnych dawców. Pozyskiwanie organów od dawców z niebijącym sercem (non-heart beating donors) jest klasyfikowane jako kontrolowane i niekontrolowane 817. Donacja kontrolowana następuje w wyniku wcześniej zaplanowanego zaprzestania leczenia u pacjentów po śmiertelnych urazach/chorobach. Donacja niekontrolowana dotyczy sytuacji, kiedy dochodzi do pobrania narządów od pacjenta przewiezionego do szpitala i stwierdzeniu zgonu z powodu nieodwracalnego zatrzymania krążenia (brought in dead) lub w trakcie trwania czynności resuscytacyjnych, które nie dają efektu w postaci powrotu spontanicznego krążenia. Funkcjonowanie organu po przeszczepieniu zależy od czasu trwania ciepłego niedokrwienia, tj. od wystąpienia braku rzutu serca do czasu zabezpieczenia narządu. Kiedy przewiduje się opóźnienia w rozpoczęciu zabezpieczania organów, należy rozważyć stosowanie mechanicznych urządzeń do uciskania klatki piersiowej, które zapewnią skuteczne krążenie i perfuzję narządów, podczas gdy podejmowane są konieczne środki prawne umożliwiające pobranie narządów
153 152 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 Centra leczenia pacjentów po zatrzymaniu krążenia Istnieje duża zmienność dotycząca przeżywalności pacjentów w szpitalach zajmujących się leczeniem chorych po zatrzymaniu krążenia 498,631,635,636, Istnieją dowody o niższym poziomie wiarygodności, że OIT przyjmujące rocznie ponad 50 pacjentów po zatrzymaniu krążenia osiągają lepsze wskaźniki dotyczące przeżycia niż OIT przyjmujące rocznie mniej niż 20 pacjentów 636. Inne badanie obserwacyjne wykazało, że nieskorygowana przeżywalność do wypisu ze szpitala była wyższa w przypadku szpitali, w których hospitalizowano rocznie 40 pacjentów po zatrzymaniu krążenia, w porównaniu do szpitali, w których liczba takich pacjentów nie przekraczała 40. Jednak po uwzględnieniu czynników zakłócających, różnica ta stawała się nieistotna 824. Kilka badań z udziałem historycznych grup kontrolnych wykazało poprawę przeżycia po wdrożeniu specjalistycznych pakietów interwencji w zakresie opieki poresuscytacyjnej, które obejmowały hipotermię terapeutyczną oraz przezskórne interwencje wieńcowe 629,632,633. Udowodniono także poprawę przeżywalności u pacjentów z pozaszpitalnym zatrzymaniem krążenia, leczonych w dużych szpitalach posiadających pracownię kardiologii inwazyjnej, w porównaniu do mniejszych ośrodków, w których pracownie te nie są dostępne 631. W kilku badaniach z udziałem dorosłych pacjentów z pozaszpitalnym zatrzymaniem krążenia nie udało się wykazać wpływu długości czasu związanego z transportem do szpitala na przeżycie pacjentów do wypisu, warunkiem było przywrócenie spontanicznego krążenia na miejscu zdarzenia oraz krótki czas transportu (3 11 minut) Na tej podstawie wydaje się, że bezpieczne może być kierowanie pacjentów bezpośrednio do regionalnego centrum leczenia pacjentów po zatrzymaniu krążenia, omijając lokalne szpitale. Istnieją pośrednie dowody mówiące o wpływie regionalnych systemów opieki kardiologicznej na poprawę wyników leczenia u pacjentów po zawale mięśnia sercowego z uniesieniem odcinka ST (STEMI) Z powyższych danych wynika, że specjalistyczne centra i systemy opieki ukierunkowane na leczenie pacjentów po zatrzymaniu krążenia mogą okazać się skuteczne, ale jak do tej pory, nie udało się zgromadzić bezpośrednich dowodów potwierdzających tę hipotezę Bibliografia 1. Nolan J, Soar J, Eikeland H. The chain of survival. Resuscitation 2006;71: Gwinnutt CL, Columb M, Harris R. Outcome after cardiac arrest in adults in UK hospitals: effect of the 1997 guidelines. Resuscitation 2000;47: Peberdy MA, Kaye W, Ornato JP, et al. Cardiopulmonary resuscitation of adults in the hospital: a report of cardiac arrests from the National Registry of Cardiopulmonary Resuscitation. Resuscitation 2003;58: Meaney PA, Nadkarni VM, Kern KB, Indik JH, Halperin HR, Berg RA. Rhythms and outcomes of adult in-hospital cardiac arrest. Crit Care Med 2010;38: Smith GB. In-hospital cardiac arrest: is it time for an in-hospital chain of prevention? Resuscitation National Confidential Enquiry into Patient Outcome and Death. An acute problem? London: NCEPOD; Hodgetts TJ, Kenward G, Vlackonikolis I, et al. Incidence, location and reasons for avoidable in-hospital cardiac arrest in a district general hospital. Resuscitation 2002;54: Kause J, Smith G, Prytherch D, Parr M, Flabouris A, Hillman K. A comparison of antecedents to cardiac arrests, deaths and emergency intensive care admissions in Australia and New Zealand, and the United Kingdom the ACADEMIA study. Resuscitation 2004;62: Castagna J, Weil MH, Shubin H. Factors determining survival in patients with cardiac arrest. Chest 1974;65: Herlitz J, Bang A, Aune S, Ekstrom L, Lundstrom G, Holmberg S. Characteristics and outcome among patients suffering in-hospital cardiac arrest in monitored and non-monitored areas. Resuscitation 2001;48: Buist M, Bernard S, Nguyen TV, Moore G, Anderson J. Association between clinically abnormal observations and subsequent in-hospital mortality: a prospective study. Resuscitation 2004;62: Franklin C, Mathew J. Developing strategies to prevent inhospital cardiac arrest: analyzing responses of physicians and nurses in the hours before the event. Crit Care Med 1994;22: Hodgetts TJ, Kenward G, Vlachonikolis IG, Payne S, Castle N. The identification of risk factors for cardiac arrest and formulation of activation criteria to alert a medical emergency team. Resuscitation 2002;54: McQuillan P, Pilkington S, Allan A, et al. Confidential inquiry into quality of care before admission to intensive care. BMJ 1998;316: Jacques T, Harrison GA, McLaws ML, Kilborn G. Signs of critical conditions and emergency responses (SOCCER): a model for predicting adverse events in the inpatient setting. Resuscitation 2006;69: McGain F, Cretikos MA, Jones D, et al. Documentation of clinical review and vital signs after major surgery. Med J Aust 2008;189: Cashman JN. In-hospital cardiac arrest: what happens to the false arrests? Resuscitation 2002;53: Hein A, Thoren AB, Herlitz J. Characteristics and outcome of false cardiac arrests in hospital. Resuscitation 2006;69: Kenward G, Robinson A, Bradburn S, Steeds R. False cardiac arrests: the right time to turn away? Postgrad Med J 2007;83: Fuhrmann L, Lippert A, Perner A, Ostergaard D. Incidence, staff awareness and mortality of patients at risk on general wards. Resuscitation 2008;77: Chatterjee MT, Moon JC, Murphy R, McCrea D. The OBS chart: an evidence based approach to re-design of the patient observation chart in a district general hospital setting. Postgrad Med J 2005;81: Smith GB, Prytherch DR, Schmidt PE, Featherstone PI. Review and performance evaluation of aggregate weighted track and trigger systems. Resuscitation 2008;77: Smith GB, Prytherch DR, Schmidt PE, Featherstone PI, Higgins B. A review, and performance evaluation, of single-parameter track and trigger systems. Resuscitation 2008;79: Hillman K, Chen J, Cretikos M, et al. Introduction of the medical emergency team (MET) system: a cluster-randomised controlled trial. Lancet 2005;365: Needleman J, Buerhaus P, Mattke S, Stewart M, Zelevinsky K. Nurse-staffing levels and the quality of care in hospitals. N Engl J Med 2002;346: DeVita MA, Smith GB, Adam SK, et al. Identifying the hospitalised patient in crisis a consensus conference on the afferent limb of rapid response systems. Resuscitation 2010;81: Hogan J. Why don t nurses monitor the respiratory rates of patients? Br J Nurs 2006;15: Buist M. The rapid response team paradox: why doesn t anyone call for help? Crit Care Med 2008;36: Andrews T, Waterman H. Packaging: a grounded theory of how to report physiological deterioration effectively. J Adv Nurs 2005;52: Derham C. Achieving comprehensive critical care. Nurs Crit Care 2007;12: Smith GB, Poplett N. Knowledge of aspects of acute care in trainee doctors. Postgrad Med J 2002;78: Meek T. New house officers knowledge of resuscitation, fluid balance and analgesia. Anaesthesia 2000;55: Gould TH, Upton PM, Collins P. A survey of the intended management of acute postoperative pain by newly qualified doctors in the south west region of England in August Anaesthesia 1994;49: Jackson E, Warner J. How much do doctors know about consent and capacity? J R Soc Med 2002;95: Kruger PS, Longden PJ. A study of a hospital staff s knowledge of pulse oximetry. Anaesth Intensive Care 1997;25: Howell M. Pulse oximetry: an audit of nursing and medical staff understanding. Br J Nurs 2002;11: Wheeler DW, Remoundos DD, Whittlestone KD, et al. Doctors confusion over ratios and percentages in drug solutions: the case for standard labelling. JRSoc Med 2004;97: Goldacre MJ, Lambert T, Evans J, Turner G. Preregistration house officers views on whether their experience at medical school prepared them well for their jobs: national questionnaire survey. BMJ 2003;326: Perkins GD, Barrett H, Bullock I, et al. The Acute Care Undergraduate TEaching (ACUTE) Initiative: consensus development of core competencies in acute care for undergraduates in the United Kingdom. Intensive Care Med 2005;31: Smith CM, Perkins GD, Bullock I, Bion JF. Undergraduate training in the care of the acutely ill patient: a literature review. Intensive Care Med 2007;33: Thwaites BC, Shankar S, Niblett D, Saunders J. Can consultants resuscitate? J R Coll Physicians Lond 1992;26: Saravanan P, Soar J. A survey of resuscitation training needs of senior anaesthetists. Resuscitation 2005;64: Featherstone P, Smith GB, Linnell M, Easton S, Osgood VM. Impact of a oneday inter-professional course (ALERTtrade mark) on attitudes and confidence in managing critically ill adult patients. Resuscitation 2005;65:
154 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Campello G, Granja C, Carvalho F, Dias C, Azevedo LF, Costa-Pereira A. Immediate and long-term impact of medical emergency teams on cardiac arrest prevalence and mortality: a plea for periodic basic life-support training programs. Crit Care Med 2009;37: Bellomo R, Goldsmith D, Uchino S, et al. A prospective before-and-after trial of a medical emergency team. Med J Aust 2003;179: Bellomo R, Goldsmith D, Uchino S, et al. Prospective controlled trial of effect of medical emergency team on postoperative morbidity and mortality rates. Crit Care Med 2004;32: DeVita MA, Braithwaite RS, Mahidhara R, Stuart S, Foraida M, Simmons RL. Use of medical emergency team responses to reduce hospital cardiopulmonary arrests. Qual Saf Health Care 2004;13: Foraida MI, DeVita MA, Braithwaite RS, Stuart SA, Brooks MM, Simmons RL. Improving the utilization of medical crisis teams (Condition C) at an urban tertiary care hospital. J Crit Care 2003;18: Green AL, Williams A. An evaluation of an early warning clinical marker referral tool. Intensive Crit Care Nurs 2006;22: Spearpoint KG, Gruber PC, Brett SJ. Impact of the Immediate Life Support course on the incidence and outcome of in-hospital cardiac arrest calls: an observational study over 6 years. Resuscitation 2009;80: Soar J, Perkins GD, Harris S, et al. The immediate life support course. Resuscitation 2003;57: Harrison GA, Jacques TC, Kilborn G, McLaws ML. The prevalence of recordings of the signs of critical conditions and emergency responses in hospital wards the SOCCER study. Resuscitation 2005;65: Hall S, Williams E, Richards S, Subbe C, Gemmell L. Waiting to exhale: critical care outreach and recording of ventilatory frequency. Br J Anaesth 2003;90: McBride J, Knight D, Piper J, Smith G. Long-term effect of introducing an early warning score on respiratory rate charting on general wards. Resuscitation 2005;65: Goldhill DR, Worthington L, Mulcahy A, Tarling M, Sumner A. The patientatrisk team: identifying and managing seriously ill ward patients. Anaesthesia 1999;54: Subbe CP, Davies RG, Williams E, Rutherford P, Gemmell L. Effect of introducing the Modified Early Warning score on clinical outcomes, cardio-pulmonary arrests and intensive care utilisation in acute medical admissions. Anaesthesia 2003;58: Armitage M, Eddleston J, Stokes T. Recognising and responding to acute illness in adults in hospital: summary of NICE guidance. BMJ 2007;335: Chen J, Hillman K, Bellomo R, Flabouris A, Finfer S, Cretikos M. The impact of introducing medical emergency team system on the documentations of vital signs. Resuscitation 2009;80: Odell M, Rechner IJ, Kapila A, et al. The effect of a critical care outreach service and an early warning scoring system on respiratory rate recording on the general wards. Resuscitation 2007;74: Critical care outreach 2003: progress in developing services. The National Outreach Report. London, UK: Department of Health and National Health Service Modernisation Agency; Gao H, McDonnell A, Harrison DA, et al. Systematic review and evaluation of physiological track and trigger warning systems for identifying at-risk patients on the ward. Intensive Care Med 2007;33: Cuthbertson BH. Optimising early warning scoring systems. Resuscitation 2008;77: Cretikos M, Chen J, Hillman K, Bellomo R, Finfer S, Flabouris A. The objective medical emergency team activation criteria: a case control study. Resuscitation 2007;73: Fieselmann J, Hendryx M, Helms C, Wakefield D. Respiratory rate predicts cardiopulmonary arrest for internal medicine patients. J Gen Intern Med 1993;8: Henry OF, Blacher J, Verdavaine J, Duviquet M, Safar ME. Alpha 1-acid glycoprotein is an independent predictor of in-hospital death in the elderly. Age Ageing 2003;32: Barlow G, Nathwani D, Davey P. The CURB65 pneumonia severity score outperforms generic sepsis and early warning scores in predicting mortality in community-acquired pneumonia. Thorax 2007;62: Sleiman I, Morandi A, Sabatini T, et al. Hyperglycemia as a predictor of in-hospital mortality in elderly patients without diabetes mellitus admitted to a sub-intensive care unit. J Am Geriatr Soc 2008;56: Alarcon T, Barcena A, Gonzalez-Montalvo JI, Penalosa C, Salgado A. Factors predictive of outcome on admission to an acute geriatric ward. Age Ageing 1999;28: Goel A, Pinckney RG, Littenberg B. APACHE II predicts long-term survival in COPD patients admitted to a general medical ward. J Gen Intern Med 2003;18: Rowat AM, Dennis MS, Wardlaw JM. Central periodic breathing observed on hospital admission is associated with an adverse prognosis in conscious acute stroke patients. Cerebrovasc Dis 2006;21: Neary WD, Prytherch D, Foy C, Heather BP, Earnshaw JJ. Comparison of different methods of risk stratification in urgent and emergency surgery. Br J Surg 2007;94: Asadollahi K, Hastings IM, Beeching NJ, Gill GV. Laboratory risk factors for hospital mortality in acutely admitted patients. QJM 2007;100: Jones AE, Aborn LS, Kline JA. Severity of emergency department hypotension predicts adverse hospital outcome. Shock 2004;22: Duckitt RW, Buxton-Thomas R, Walker J, et al. Worthing physiological scoring system: derivation and validation of a physiological early-warning system for medical admissions. An observational, population-based single-centre study. Br J Anaesth 2007;98: Kellett J, Deane B. The Simple Clinical Score predicts mortality for 30 days after admission to an acute medical unit. QJM 2006;99: Prytherch DR, Sirl JS, Schmidt P, Featherstone PI, Weaver PC, Smith GB. The use of routine laboratory data to predict in-hospital death in medical admissions. Resuscitation 2005;66: Smith GB, Prytherch DR, Schmidt PE, et al. Should age be included as a component of track and trigger systems used to identify sick adult patients? Resuscitation 2008;78: Olsson T, Terent A, Lind L. Rapid Emergency Medicine score: a new prognostic tool for in-hospital mortality in nonsurgical emergency department patients. J Intern Med 2004;255: Prytherch DR, Sirl JS, Weaver PC, Schmidt P, Higgins B, Sutton GL. Towards a national clinical minimum data set for general surgery. Br J Surg 2003;90: Subbe CP, Kruger M, Rutherford P, Gemmel L. Validation of a modified Early Warning Score in medical admissions. QJM 2001;94: Goodacre S, Turner J, Nicholl J. Prediction of mortality among emergency medical admissions. Emerg Med J 2006;23: Paterson R, MacLeod DC, Thetford D, et al. Prediction of in-hospital mortality and length of stay using an early warning scoring system: clinical audit. Clin Med 2006;6: Cuthbertson BH, Boroujerdi M, McKie L, Aucott L, Prescott G. Can physiological variables and early warning scoring systems allow early recognition of the deteriorating surgical patient? Crit Care Med 2007;35: Goldhill DR, McNarry AF. Physiological abnormalities in early warning scores are related to mortality in adult inpatients. Br J Anaesth 2004;92: Harrison GA, Jacques T, McLaws ML, Kilborn G. Combinations of early signs of critical illness predict in-hospital death-the SOCCER study (signs of critical conditions and emergency responses). Resuscitation 2006;71: Bell MB, Konrad D, Granath F, Ekbom A, Martling CR. Prevalence and sensitivity of MET-criteria in a Scandinavian University Hospital. Resuscitation 2006;70: Gardner-Thorpe J, Love N, Wrightson J, Walsh S, Keeling N. The value of Modified Early Warning Score (MEWS) in surgical in-patients: a prospective observational study. Ann R Coll Surg Engl 2006;88: Quarterman CP, Thomas AN, McKenna M, McNamee R. Use of a patient information system to audit the introduction of modified early warning scoring. J Eval Clin Pract 2005;11: Goldhill DR, McNarry AF, Hadjianastassiou VG, Tekkis PP. The longer patients are in hospital before Intensive Care admission the higher their mortality. Intensive Care Med 2004;30: Goldhill DR, McNarry AF, Mandersloot G, McGinley A. A physiologicallybased early warning score for ward patients: the association between score and outcome. Anaesthesia 2005;60: Boniatti MM, Azzolini N, da Fonseca DL, et al. Prognostic value of the calling criteria in patients receiving a medical emergency team review. Resuscitation 2010;81: Prytherch DR, Smith GB, Schmidt PE, Featherstone PI. ViEWS-Towards a national early warning score for detecting adult inpatient deterioration. Resuscitation 2010;81: Mitchell IA, McKay H, Van Leuvan C, et al. A prospective controlled trial of the effect of a multi-faceted intervention on early recognition and intervention in deteriorating hospital patients. Resuscitation Smith GB, Prytherch DR, Schmidt P, et al. Hospital-wide physiological surveillance-a new approach to the early identification and management of the sick patient. Resuscitation 2006;71: Sandroni C, Ferro G, Santangelo S, et al. In-hospital cardiac arrest: survival depends mainly on the effectiveness of the emergency response. Resuscitation 2004;62: Soar J, McKay U. A revised role for the hospital cardiac arrest team? Resuscitation 1998;38: Featherstone P, Chalmers T, Smith GB. RSVP: a system for communication of deterioration in hospital patients. Br J Nurs 2008;17: Marshall S, Harrison J, Flanagan B. The teaching of a structured tool improves the clarity and content of interprofessional clinical communication. Qual Saf Health Care 2009;18: Lee A, Bishop G, Hillman KM, Daffurn K. The Medical Emergency Team. Anaesth Intensive Care 1995;23: Devita MA, Bellomo R, Hillman K, et al. Findings of the first consensus conference on medical emergency teams. Crit Care Med 2006;34: Ball C, Kirkby M, Williams S. Effect of the critical care outreach team on patient survival to discharge from hospital and readmission to critical care: nonrandomised population based study. BMJ 2003;327: Zenker P, Schlesinger A, Hauck M, et al. Implementation and impact of a rapid response team in a children s hospital. Jt Comm J Qual Patient Saf 2007;33: Dean BS, Decker MJ, Hupp D, Urbach AH, Lewis E, Benes-Stickle J. Condition HELP: a pediatric rapid response team triggered by patients and parents. J Healthc Qual 2008;30 : Ray EM, Smith R, Massie S, et al. Family alert: implementing direct family activation of a pediatric rapid response team. Jt Comm J Qual Patient Saf 2009;35:
155 154 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins Kenward G, Castle N, Hodgetts T, Shaikh L. Evaluation of a medical emergency team one year after implementation. Resuscitation 2004;61: Chan PS, Khalid A, Longmore LS, Berg RA, Kosiborod M, Spertus JA. Hospital-wide code rates and mortality before and after implementation of a rapid response team. JAMA 2008;300: Dacey MJ, Mirza ER, Wilcox V, et al. The effect of a rapid response team on major clinical outcome measures in a community hospital. Crit Care Med 2007;35: Story DA, Shelton AC, Poustie SJ, Colin-Thome NJ, McNicol PL. The effect of critical care outreach on postoperative serious adverse events. Anaesthesia 2004;59: Story DA, Shelton AC, Poustie SJ, Colin-Thome NJ, McIntyre RE, McNicol PL. Effect of an anaesthesia department led critical care outreach and acute pain service on postoperative serious adverse events. Anaesthesia 2006;61: Flabouris A, Chen J, Hillman K, Bellomo R, Finfer S. Timing and interventions of emergency teams during the MERIT study. Resuscitation 2010;81: Jones D, Bellomo R, Bates S, et al. Long term effect of a medical emergency team on cardiac arrests in a teaching hospital. Crit Care 2005;9:R Galhotra S, DeVita MA, Simmons RL, Schmid A. Impact of patient monitoring on the diurnal pattern of medical emergency team activation. Crit Care Med 2006;34: Baxter AD, Cardinal P, Hooper J, Patel R. Medical emergency teams at The Ottawa Hospital: the first two years. Can J Anaesth 2008;55: Benson L, Mitchell C, Link M, Carlson G, Fisher J. Using an advanced practice nursing model for a rapid response team. Jt Comm J Qual Patient Saf 2008;34: Bertaut Y, Campbell A, Goodlett D. Implementing a rapid-response team using a nurse-to-nurse consult approach. J Vasc Nurs 2008;26: Buist MD, Moore GE, Bernard SA, Waxman BP, Anderson JN, Nguyen TV. Effects of a medical emergency team on reduction of incidence of and mortality from unexpected cardiac arrests in hospital: preliminary study. BMJ 2002;324: Buist M, Harrison J, Abaloz E, Van Dyke S. Six year audit of cardiac arrests and medical emergency team calls in an Australian outer metropolitan teaching hospital. BMJ 2007;335: Chamberlain B, Donley K, Maddison J. Patient outcomes using a rapid response team. Clin Nurse Spec 2009;23: Hatler C, Mast D, Bedker D, et al. Implementing a rapid response team to decrease emergencies outside the ICU: one hospital s experience. Medsurg Nurs 2009;18, 84-90, Jones D, Bellomo R, Bates S, et al. Patient monitoring and the timing of cardiac arrests and medical emergency team calls in a teaching hospital. Intensive Care Med 2006;32: Moldenhauer K, Sabel A, Chu ES, Mehler PS. Clinical triggers: an alternative to a rapid response team. Jt Comm J Qual Patient Saf 2009;35: Offner PJ, Heit J, Roberts R. Implementation of a rapid response team decreases cardiac arrest outside of the intensive care unit. J Trauma 2007;62: [discussion 7 8] Gould D. Promoting patient safety: The Rapid Medical Response Team. Perm J 2007;11: Jolley J, Bendyk H, Holaday B, Lombardozzi KA, Harmon C. Rapid response teams: do they make a difference? Dimens Crit Care Nurs 2007;26:253 60, quiz Konrad D, Jaderling G, Bell M, Granath F, Ekbom A, Martling CR. Reducing in-hospital cardiac arrests and hospital mortality by introducing a medical emergency team. Intensive Care Med 2010;36: Chen J, Bellomo R, Flabouris A, Hillman K, Finfer S. The relationship between early emergency team calls and serious adverse events. Crit Care Med 2009;37: Bristow PJ, Hillman KM, Chey T, et al. Rates of in-hospital arrests, deaths and intensive care admissions: the effect of a medical emergency team. Med J Aust 2000;173: King E, Horvath R, Shulkin DJ. Establishing a rapid response team (RRT) in an academic hospital: one year s experience. J Hosp Med 2006;1: McFarlan SJ, Hensley S. Implementation and outcomes of a rapid response team. J Nurs Care Qual 2007;22:307 13, quiz Rothschild JM, Woolf S, Finn KM, et al. A controlled trial of a rapid response system in an academic medical center. Jt Comm J Qual Patient Saf 2008;34, , Chan PS, Jain R, Nallmothu BK, Berg RA, Sasson C. Rapid Response Teams: a systematic review and meta-analysis. Arch Intern Med 2010;170: Leeson-Payne CG, Aitkenhead AR. A prospective study to assess the demand for a high dependency unit. Anaesthesia 1995;50: Guidelines for the utilisation of intensive care units. European Society of Intensive Care Medicine. Intensive Care Med 1994;20: Haupt MT, Bekes CE, Brilli RJ, et al. Guidelines on critical care services and personnel: recommendations based on a system of categorization of three levels of care. Crit Care Med 2003;31: Peberdy MA, Ornato JP, Larkin GL, et al. Survival from in-hospital cardiac arrest during nights and weekends. JAMA 2008;299: Hillson SD, Rich EC, Dowd B, Luxenberg MG. Call nights and patients care: effects on inpatients at one teaching hospital. J Gen Intern Med 1992;7: Bell CM, Redelmeier DA. Mortality among patients admitted to hospitals on weekends as compared with weekdays. N Engl J Med 2001;345: Beck DH, McQuillan P, Smith GB. Waiting for the break of dawn? The effects of discharge time, discharge TISS scores and discharge facility on hospital mortality after intensive care. Intensive Care Med 2002;28: Goldfrad C, Rowan K. Consequences of discharges from intensive care at night. Lancet 2000;355: Tourangeau AE, Cranley LA, Jeffs L. Impact of nursing on hospital patient mortality: a focused review and related policy implications. Qual Saf Health Care 2006;15: Aiken LH, Clarke SP, Sloane DM, Sochalski J, Silber JH. Hospital nurse staffing and patient mortality, nurse burnout, and job dissatisfaction. JAMA 2002;288: Parr MJ, Hadfield JH, Flabouris A, Bishop G, Hillman K. The Medical Emergency Team: 12 month analysis of reasons for activation, immediate outcome and not-for-resuscitation orders. Resuscitation 2001;50: Baskett PJ, Lim A. The varying ethical attitudes towards resuscitation in Europe. Resuscitation 2004;62: Baskett PJ, Steen PA, Bossaert L. European Resuscitation Council guidelines for resuscitation 2005, Section 8. The ethics of resuscitation and end-of-life decisions. Resuscitation 2005;67(Suppl. 1):S Lippert FK, Raffay V, Georgiou M, Steen PA, Bossaert L. European Resuscitation Council Guidelines for Resuscitation 2010, Section 10. The ethics of resuscitation and end-of-life decisions. Resuscitation 2010;81: Smith GB. Increased do not attempt resuscitation decision making in hospitals with a medical emergency teams system-cause and effect? Resuscitation 2008;79: Chen J, Flabouris A, Bellomo R, Hillman K, Finfer S. The Medical Emergency Team System and not-for-resuscitation orders: results from the MERIT study. Resuscitation 2008;79: Jones DA, McIntyre T, Baldwin I, Mercer I, Kattula A, Bellomo R. The medical emergency team and end-of-life care: a pilot study. Crit Care Resusc 2007;9: Excellence NIfHaC. NICE clinical guideline 50 Acutely ill patients in hospital: recognition of and response to acute illness in adults in hospital. London: National Institute for Health and Clinical Excellence; Muller D, Agrawal R, Arntz HR. How sudden is sudden cardiac death? Circulation 2006;114: Nava A, Bauce B, Basso C, et al. Clinical profile and long-term follow-up of 37 families with arrhythmogenic right ventricular cardiomyopathy. J Am Coll Cardiol 2000;36: Brugada J, Brugada R, Brugada P. Determinants of sudden cardiac death in individuals with the electrocardiographic pattern of Brugada syndrome and no previous cardiac arrest. Circulation 2003;108: Elliott PM, Poloniecki J, Dickie S, et al. Sudden death in hypertrophic cardiomyopathy: identification of high risk patients. J Am Coll Cardiol 2000;36: Goldenberg I, Moss AJ, Peterson DR, et al. Risk factors for aborted cardiac arrest and sudden cardiac death in children with the congenital long-qt syndrome. Circulation 2008;117: Hobbs JB, Peterson DR, Moss AJ, et al. Risk of aborted cardiac arrest or sudden cardiac death during adolescence in the long-qt syndrome. JAMA 2006;296: Hulot JS, Jouven X, Empana JP, Frank R, Fontaine G. Natural history and risk stratification of arrhythmogenic right ventricular dysplasia/cardiomyopathy. Circulation 2004;110: Kofflard MJ, Ten Cate FJ, van der Lee C, van Domburg RT. Hypertrophic cardiomyopathy in a large community-based population: clinical outcome and identification of risk factors for sudden cardiac death and clinical deterioration. J Am Coll Cardiol 2003;41: Peters S. Long-term follow-up and risk assessment of arrhythmogenic right ventricular dysplasia/cardiomyopathy: personal experience from different primary and tertiary centres. J Cardiovasc Med (Hagerstown) 2007;8: Priori SG, Napolitano C, Gasparini M, et al. Natural history of Brugada syndrome: insights for risk stratification and management. Circulation 2002;105: Spirito P, Autore C, Rapezzi C, et al. Syncope and risk of sudden death in hypertrophic cardiomyopathy. Circulation 2009;119: Sumitomo N, Harada K, Nagashima M, et al. Catecholaminergic polymorphic ventricular tachycardia: electrocardiographic characteristics and optimal therapeutic strategies to prevent sudden death. Heart 2003;89: Amital H, Glikson M, Burstein M, et al. Clinical characteristics of unexpected death among young enlisted military personnel: results of a three-decade retrospective surveillance. Chest 2004;126: Basso C, Maron BJ, Corrado D, Thiene G. Clinical profile of congenital coronary artery anomalies with origin from the wrong aortic sinus leading to sudden death in young competitive athletes. J Am Coll Cardiol 2000;35: Corrado D, Basso C, Thiene G. Sudden cardiac death in young people with apparently normal heart. Cardiovasc Res 2001;50: Drory Y, Turetz Y, Hiss Y, et al. Sudden unexpected death in persons less than 40 years of age. Am J Cardiol 1991;68: Kramer MR, Drori Y, Lev B. Sudden death in young soldiers. High incidence of syncope prior to death. Chest 1988;93: Quigley F, Greene M, O Connor D, Kelly F. A survey of the causes of sudden cardiac death in the under 35-year-age group. Ir Med J 2005;98: Wisten A, Forsberg H, Krantz P, Messner T. Sudden cardiac death in year olds in Sweden during J Intern Med 2002;252:
156 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Wisten A, Messner T. Young Swedish patients with sudden cardiac death have a lifestyle very similar to a control population. Scand Cardiovasc J 2005;39: Wisten A, Messner T. Symptoms preceding sudden cardiac death in the young are common but often misinterpreted. Scand Cardiovasc J 2005;39: Behr ER, Dalageorgou C, Christiansen M, et al. Sudden arrhythmic death syndrome: familial evaluation identifies inheritable heart disease in the majority of families. Eur Heart J 2008;29: Brothers JA, Stephens P, Gaynor JW, Lorber R, Vricella LA, Paridon SM. Anomalous aortic origin of a coronary artery with an interarterial course: should family screening be routine? J Am Coll Cardiol 2008;51: Gimeno JR, Lacunza J, Garcia-Alberola A, et al. Penetrance and risk profile in inherited cardiac diseases studied in a dedicated screening clinic. Am J Cardiol 2009;104: Tan HL, Hofman N, van Langen IM, van der Wal AC, Wilde AA. Sudden unexplained death: heritability and diagnostic yield of cardiological and genetic examination in surviving relatives. Circulation 2005;112: Moya A, Sutton R, Ammirati F, et al. Guidelines for the diagnosis and management of syncope (version 2009): the Task Force for the Diagnosis and Management of Syncope of the European Society of Cardiology (ESC). Eur Heart J 2009;30 : Colman N, Bakker A, Linzer M, Reitsma JB, Wieling W, Wilde AA. Value of history-taking in syncope patients: in whom to suspect long QT syndrome? Europace 2009;11: Oh JH, Hanusa BH, Kapoor WN. Do symptoms predict cardiac arrhythmias and mortality in patients with syncope? Arch Intern Med 1999;159: Calkins H, Shyr Y, Frumin H, Schork A, Morady F. The value of the clinical history in the differentiation of syncope due to ventricular tachycardia, atrioventricular block, and neurocardiogenic syncope. Am J Med 1995;98: Tester DJ, Kopplin LJ, Creighton W, Burke AP, Ackerman MJ. Pathogenesis of unexplained drowning: new insights from a molecular autopsy. Mayo Clin Proc 2005;80: Johnson JN, Hofman N, Haglund CM, Cascino GD, Wilde AA, Ackerman MJ. Identification of a possible pathogenic link between congenital long QT syndrome and epilepsy. Neurology 2009;72: MacCormick JM, McAlister H, Crawford J, et al. Misdiagnosis of long QT syndrome as epilepsy at first presentation. Ann Emerg Med 2009;54: Chandra N, Papadakis M, Sharma S. Preparticipation screening of young competitive athletes for cardiovascular disorders. Phys Sportsmed 2010;38: Olasveengen TM, Lund-Kordahl I, Steen PA, Sunde K. Out-of hospital advanced life support with or without aphysician: effects on quality of CPR and outcome. Resuscitation 2009;80: Kirves H, Skrifvars MB, Vahakuopus M, Ekstrom K, Martikainen M, Castren M. Adherence to resuscitation guidelines during prehospital care of cardiac arrest patients. Eur J Emerg Med 2007;14: Schneider T, Mauer D, Diehl P, Eberle B, Dick W. Quality of on-site performance in prehospital advanced cardiac life support (ACLS). Resuscitation 1994;27: Arntz HR, Wenzel V, Dissmann R, Marschalk A, Breckwoldt J, Muller D. Out-of-hospital thrombolysis during cardiopulmonary resuscitation in patients with high likelihood of ST-elevation myocardial infarction. Resuscitation 2008;76: Bell A, Lockey D, Coats T, Moore F, Davies G. Physician Response Unit a feasibility study of an initiative to enhance the delivery of pre-hospital emergency medical care. Resuscitation 2006;69: Lossius HM, Soreide E, Hotvedt R, et al. Prehospital advanced life support provided by specially trained physicians: is there a benefit in terms of life years gained? Acta Anaesthesiol Scand 2002;46: Dickinson ET, Schneider RM, Verdile VP. The impact of prehospital physicians on out-of-hospital nonasystolic cardiac arrest. Prehosp Emerg Care 1997;1: Soo LH, Gray D, Young T, Huff N, Skene A, Hampton JR. Resuscitation from out-of-hospital cardiac arrest: is survival dependent on who is available at the scene? Heart 1999;81: Frandsen F, Nielsen JR, Gram L, et al. Evaluation of intensified prehospital treatment in out-of-hospital cardiac arrest: survival and cerebral prognosis. The Odense ambulance study. Cardiology 1991;79: Sipria A, Talvik R, Korgvee A, Sarapuu S, Oopik A. Out-of-hospital resuscitation in Tartu: effect of reorganization of Estonian EMS system. Am J Emerg Med 2000;18: Estner HL, Gunzel C, Ndrepepa G, et al. Outcome after out-of-hospital cardiac arrest in a physician-staffed emergency medical system according to the Utstein style. Am Heart J 2007;153: Eisenburger P, Czappek G, Sterz F, et al. Cardiac arrest patients in an alpine area during a six year period. Resuscitation 2001;51: Gottschalk A, Burmeister MA, Freitag M, Cavus E, Standl T. Influence of early defibrillation on the survival rate and quality of life after CPR in prehospital emergency medical service in a German metropolitan area. Resuscitation 2002;53: Hampton JR, Dowling M, Nicholas C. Comparison of results from a cardiac ambulance manned by medical or non-medical personnel. Lancet 1977;1: Schneider T, Mauer D, Diehl P, et al. Early defibrillation by emergency physicians or emergency medical technicians? A controlled, prospective multicentre study. Resuscitation 1994;27: Soo LH, Gray D, Young T, Skene A, Hampton JR. Influence of ambulance crew s length of experience on the outcome of out-of-hospital cardiac arrest. Eur Heart J 1999;20: Yen ZS, Chen YT, Ko PC, et al. Cost-effectiveness of different advanced life support providers for victims of out-of-hospital cardiac arrests. J Formos Med Assoc 2006;105: Nichol G, Thomas E, Callaway CW, et al. Regional variation in out-of-hospital cardiac arrest incidence and outcome. JAMA 2008;300: Fischer M, Krep H, Wierich D, et al. Comparison of the emergency medical services systems of Birmingham and Bonn: process efficacy and cost effectiveness. Anasthesiol Intensivmed Notfallmed Schmerzther 2003;38: Bottiger BW, Grabner C, Bauer H, et al. Long term outcome after out-of-hospital cardiac arrest with physician staffed emergency medical services: the Utstein style applied to a midsized urban/suburban area. Heart 1999;82: Bjornsson HM, Marelsson S, Magnusson V, Sigurdsson G, Thornorgeirsson G. Prehospital cardiac life support in the Reykjavik area Laeknabladid 2006;92: Mitchell RG, Brady W, Guly UM, Pirrallo RG, Robertson CE. Comparison of two emergency response systems and their effect on survival from out of hospital cardiac arrest. Resuscitation 1997;35: Lafuente-Lafuente C, Melero-Bascones M. Active chest compression decompression for cardiopulmonary resuscitation. Cochrane Database Syst Rev 2004: CD Lewis RP, Stang JM, Fulkerson PK, Sampson KL, Scoles A, Warren JV. Effectiveness of advanced paramedics in a mobile coronary care system. JAMA 1979;241: Silfvast T, Ekstrand A. The effect of experience of on-site physicians on survival from prehospital cardiac arrest. Resuscitation 1996;31: Morrison LJ, Visentin LM, Kiss A, et al. Validation of a rule for termination of resuscitation in out-of-hospital cardiac arrest. N Engl J Med 2006;355: Richman PB, Vadeboncoeur TF, Chikani V, Clark L, Bobrow BJ. Independent evaluation of an out-of-hospital termination of resuscitation (TOR) clinical decision rule. Acad Emerg Med 2008;15: Morrison LJ, Verbeek PR, Zhan C, Kiss A, Allan KS. Validation of a universal prehospital termination of resuscitation clinical prediction rule for advanced and basic life support providers. Resuscitation 2009;80: Sasson C, Hegg AJ, Macy M, Park A, Kellermann A, McNally B. Prehospital termination of resuscitation in cases of refractory out-of-hospital cardiac arrest. JAMA 2008;300: Skrifvars MB, Vayrynen T, Kuisma M, et al. Comparison of Helsinki and European Resuscitation Council do not attempt to resuscitate guidelines, and a termination of resuscitation clinical prediction rule for out-of-hospital cardiac arrest patients found in asystole or pulseless electrical activity. Resuscitation Ong ME, Jaffey J, Stiell I, Nesbitt L. Comparison of termination-of-resuscitation guidelines for basic life support: defibrillator providers in out-of-hospital cardiac arrest. Ann Emerg Med 2006;47: Morrison LJ, Verbeek PR, Vermeulen MJ, et al. Derivation and evaluation of a termination of resuscitation clinical prediction rule for advanced life support providers. Resuscitation 2007;74: Bailey ED, Wydro GC, Cone DC. Termination of resuscitation in the prehospital setting for adult patients suffering nontraumatic cardiac arrest. National Association of EMS Physicians Standards and Clinical Practice Committee. Prehosp Emerg Care 2000;4: Verbeek PR, Vermeulen MJ, Ali FH, Messenger DW, Summers J, Morrison LJ. Derivation of a termination-of-resuscitation guideline for emergency medical technicians using automated external defibrillators. Acad Emerg Med 2002;9: Ong ME, Tan EH, Ng FS, et al. Comparison of termination-of-resuscitation guidelines for out-of-hospital cardiac arrest in Singapore EMS. Resuscitation 2007;75: Pircher IR, Stadlbauer KH, Severing AC, et al. A prediction model for out-of- -hospital cardiopulmonary resuscitation. Anesth Analg 2009;109: van Walraven C, Forster AJ, Parish DC, et al. Validation of a clinical decision aid to discontinue in-hospital cardiac arrest resuscitations. JAMA 2001;285: van Walraven C, Forster AJ, Stiell IG. Derivation of a clinical decision rule for the discontinuation of in-hospital cardiac arrest resuscitations. Arch Intern Med 1999;159: McCullough PA, Thompson RJ, Tobin KJ, Kahn JK, O Neill WW. Validation of a decision support tool for the evaluation of cardiac arrest victims. Clin Cardiol 1998;21: Christenson J, Andrusiek D, Everson-Stewart S, et al. Chest compression fraction determines survival in patients with out-of-hospital ventricular fibrillation. Circulation 2009;120: Deakin CD, Nolan JP, Sunde K, Koster RW. European Resuscitation Council Guidelines for Resuscitation Section 3. Electrical therapies: automated external defibrillators, defibrillation, cardioversion and pacing. Resuscitation 2010;81: Gabbott D, Smith G, Mitchell S, et al. Cardiopulmonary resuscitation standards for clinical practice and training in the UK. Resuscitation 2005;64: Dyson E, Smith GB. Common faults in resuscitation equipment guidelines for checking equipment and drugs used in adult cardiopulmonary resuscitation. Resuscitation 2002;55: Brennan RT, Braslow A. Skill mastery in public CPR classes. Am J Emerg Med 1998;16:
157 156 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins Chamberlain D, Smith A, Woollard M, et al. Trials of teaching methods in basic life support (3): comparison of simulated CPR performance after first training and at 6 months, with a note on the value of re-training. Resuscitation 2002;53: Eberle B, Dick WF, Schneider T, Wisser G, Doetsch S, Tzanova I. Checking the carotid pulse check: diagnostic accuracy of first responders in patients with and without a pulse. Resuscitation 1996;33: Lapostolle F, Le Toumelin P, Agostinucci JM, Catineau J, Adnet F. Basic cardiac life support providers checking the carotid pulse: performance, degree of conviction, and influencing factors. Acad Emerg Med 2004;11: Liberman M, Lavoie A, Mulder D, Sampalis J. Cardiopulmonary resuscitation: errors made by pre-hospital emergency medical personnel. Resuscitation 1999;42: Moule P. Checking the carotid pulse: diagnostic accuracy in students of the healthcare professions. Resuscitation 2000;44: Nyman J, Sihvonen M. Cardiopulmonary resuscitation skills in nurses and nursing students. Resuscitation 2000;47: Perkins GD, Stephenson B, Hulme J, Monsieurs KG. Birmingham assessment of breathing study (BABS). Resuscitation 2005;64: Ruppert M, Reith MW, Widmann JH, et al. Checking for breathing: evaluation of the diagnostic capability of emergency medical services personnel, physicians, medical students, and medical laypersons. Ann Emerg Med 1999;34: Tibballs J, Russell P. Reliability of pulse palpation by healthcare personnel to diagnose paediatric cardiac arrest. Resuscitation 2009;80: Bang A, Herlitz J, Martinell S. Interaction between emergency medical dispatcher and caller in suspected out-of-hospital cardiac arrest calls with focus on agonal breathing. A review of 100 tape recordings of true cardiac arrest cases. Resuscitation 2003;56: Bohm K, Rosenqvist M, Hollenberg J, Biber B, Engerstrom L, Svensson L. Dispatcher-assisted telephone-guided cardiopulmonary resuscitation: an underused lifesaving system. Eur J Emerg Med 2007;14: Bobrow BJ, Zuercher M, Ewy GA, et al. Gasping during cardiac arrest in humans is frequent and associated with improved survival. Circulation 2008;118: Vaillancourt C, Verma A, Trickett J, et al. Evaluating the effectiveness of dispatch-assisted cardiopulmonary resuscitation instructions. Acad Emerg Med 2007;14: White L, Rogers J, Bloomingdale M, et al. Dispatcher-assisted cardiopulmonary resuscitation: risks for patients not in cardiac arrest. Circulation 2010;121: Perkins GD, Roberts C, Gao F. Delays in defibrillation: influence of different monitoring techniques. Br J Anaesth 2002;89: Abella BS, Alvarado JP, Myklebust H, et al. Quality of cardiopulmonary resuscitation during in-hospital cardiac arrest. JAMA 2005;293: Abella BS, Sandbo N, Vassilatos P, et al. Chest compression rates during cardiopulmonary resuscitation are suboptimal: a prospective study during in-hospital cardiac arrest. Circulation 2005;111: Stiell IG, Wells GA, Field B, et al. Advanced cardiac life support in out-of-hospital cardiac arrest. N Engl J Med 2004;351: Olasveengen TM, Sunde K, Brunborg C, Thowsen J, Steen PA, Wik L. Intravenous drug administration during out-of-hospital cardiac arrest: a randomized trial. JAMA 2009;302: Herlitz J, Ekstrom L, Wennerblom B, Axelsson A, Bang A, Holmberg S. Adrenaline in out-of-hospital ventricular fibrillation. Does it make any difference? Resuscitation 1995;29: Holmberg M, Holmberg S, Herlitz J. Low chance of survival among patients requiring adrenaline (epinephrine) or intubation after out-of-hospital cardiac arrest in Sweden. Resuscitation 2002;54: Bradley SM, Gabriel EE, Aufderheide TP, et al. Survival Increases with CPR by Emergency Medical Services before defibrillation of out-of-hospital ventricular fibrillation or ventricular tachycardia: observations from the Resuscitation Outcomes Consortium. Resuscitation 2010;81: Hollenberg J, Herlitz J, Lindqvist J, et al. Improved survival after out-of-hospital cardiac arrest is associated with an increase in proportion of emergency crew witnessed cases and bystander cardiopulmonary resuscitation. Circulation 2008;118: Iwami T, Nichol G, Hiraide A, et al. Continuous improvements in chain of survival increased survival after out-of-hospital cardiac arrests: a large-scale population-based study. Circulation 2009;119: Edelson DP, Abella BS, Kramer-Johansen J, et al. Effects of compression depth and pre-shock pauses predict defibrillation failure during cardiac arrest. Resuscitation 2006;71: Eftestol T, Sunde K, Steen PA. Effects of interrupting precordial compressions on the calculated probability of defibrillation success during out-of-hospital cardiac arrest. Circulation 2002;105: Sunde K, Eftestol T, Askenberg C, Steen PA. Quality assessment of defibrillation and advanced life support using data from the medical control module of the defibrillator. Resuscitation 1999;41: Rea TD, Shah S, Kudenchuk PJ, Copass MK, Cobb LA. Automated external defibrillators: to what extent does the algorithm delay CPR? Ann Emerg Med 2005;46: van Alem AP, Sanou BT, Koster RW. Interruption of cardiopulmonary resuscitation with the use of the automated external defibrillator in out-of-hospital cardiac arrest. Ann Emerg Med 2003;42: Pytte M, Kramer-Johansen J, Eilevstjonn J, et al. Haemodynamic effects of adrenaline (epinephrine) depend on chest compression quality during cardiopulmonary resuscitation in pigs. Resuscitation 2006;71: Prengel AW, Lindner KH, Ensinger H, Grunert A. Plasma catecholamine concentrations after successful resuscitation in patients. Crit Care Med 1992;20: Bhende MS, Thompson AE. Evaluation of an end-tidal CO2 detector during pediatric cardiopulmonary resuscitation. Pediatrics 1995;95: Sehra R, Underwood K, Checchia P. End tidal CO2 is a quantitative measure of cardiac arrest. Pacing Clin Electrophysiol 2003;26: Eftestol T, Wik L, Sunde K, Steen PA. Effects of cardiopulmonary resuscitation on predictors of ventricular fibrillation defibrillation success during out-of-hospital cardiac arrest. Circulation 2004;110: Eftestol T, Sunde K, Aase SO, Husoy JH, Steen PA. Predicting outcome of defibrillation by spectral characterization and nonparametric classification of ventricular fibrillation in patients with out-of-hospital cardiac arrest. Circulation 2000;102: Amir O, Schliamser JE, Nemer S, Arie M. Ineffectiveness of precordial thump for cardioversion of malignant ventricular tachyarrhythmias. Pacing Clin Electrophysiol 2007;30: Haman L, Parizek P, Vojacek J. Precordial thump efficacy in termination of induced ventricular arrhythmias. Resuscitation 2009;80: Pellis T, Kette F, Lovisa D, et al. Utility of pre-cordial thump for treatment of out of hospital cardiac arrest: a prospective study. Resuscitation 2009;80: Kohl P, King AM, Boulin C. Antiarrhythmic effects of acute mechanical stiumulation. In: Kohl P, Sachs F, Franz MR, editors. Cardiac mechano-electric feedback and arrhythmias: form pipette to patient. Philadelphia: Elsevier Saunders; p Caldwell G, Millar G, Quinn E, Vincent R, Chamberlain DA. Simple mechanical methods for cardioversion: defence of the precordial thump and cough version. Br Med J (Clin Res Ed) 1985;291: Krijne R. Rate acceleration of ventricular tachycardia after a precordial chest thump. Am J Cardiol 1984;53: Emerman CL, Pinchak AC, Hancock D, Hagen JF. Effect of injection site on circulation times during cardiac arrest. Crit Care Med 1988;16: Glaeser PW, Hellmich TR, Szewczuga D, Losek JD, Smith DS. Five-year experience in prehospital intraosseous infusions in children and adults. Ann Emerg Med 1993;22: Wenzel V, Lindner KH, Augenstein S, et al. Intraosseous vasopressin improves coronary perfusion pressure rapidly during cardiopulmonary resuscitation in pigs. Crit Care Med 1999;27: Shavit I, Hoffmann Y, Galbraith R, Waisman Y. Comparison of two mechanical intraosseous infusion devices: a pilot, randomized crossover trial. Resuscitation 2009;80: Schuttler J, Bartsch A, Ebeling BJ, et al. Endobronchial administration of adrenaline in preclinical cardiopulmonary resuscitation. Anasth Intensivther Notfallmed 1987;22: Hornchen U, Schuttler J, Stoeckel H, Eichelkraut W, Hahn N. Endobronchial instillation of epinephrine during cardiopulmonary resuscitation. Crit Care Med 1987;15: Vaknin Z, Manisterski Y, Ben-Abraham R, et al. Is endotracheal adrenaline deleterious because of the beta adrenergic effect? Anesth Analg 2001;92: Manisterski Y, Vaknin Z, Ben-Abraham R, et al. Endotracheal epinephrine: a call for larger doses. Anesth Analg 2002;95: , table of contents Efrati O, Ben-Abraham R, Barak A, et al. Endobronchial adrenaline: should it be reconsidered? Dose response and haemodynamic effect in dogs. Resuscitation 2003;59: Elizur A, Ben-Abraham R, Manisterski Y, et al. Tracheal epinephrine or norepinephrine preceded by beta blockade in a dog model. Can beta blockade bestow any benefits? Resuscitation 2003;59: Prengel AW, Rembecki M, Wenzel V, Steinbach G. A comparison of the endotracheal tube and the laryngeal mask airway as a route for endobronchial lidocaine administration. Anesth Analg 2001;92: Berg RA, Hilwig RW, Kern KB, Ewy GA. Precountershock cardiopulmonary resuscitation improves ventricular fibrillation median frequency and myocardial readiness for successful defibrillation from prolonged ventricular fibrillation: a randomized, controlled swine study. Ann Emerg Med 2002;40: Achleitner U, Wenzel V, Strohmenger HU, et al. The beneficial effect of basic life support on ventricular fibrillation mean frequency and coronary perfusion pressure. Resuscitation 2001;51: Fries M, Tang W, Chang YT, Wang J, Castillo C, Weil MH. Microvascular blood flow during cardiopulmonary resuscitation is predictive of outcome. Resuscitation 2006;71: Ristagno G, Tang W, Huang L, et al. Epinephrine reduces cerebral perfusion during cardiopulmonary resuscitation. Crit Care Med 2009;37: Tang W, Weil MH, Sun S, Gazmuri RJ, Bisera J. Progressive myocardial dysfunction after cardiac resuscitation. Crit Care Med 1993;21: Angelos MG, Butke RL, Panchal AR, et al. Cardiovascular response to epinephrine varies with increasing duration of cardiac arrest. Resuscitation 2008;77: Kudenchuk PJ, Cobb LA, Copass MK, et al. Amiodarone for resuscitation after out-of-hospital cardiac arrest due to ventricular fibrillation. N Engl J Med 1999;341: Dorian P, Cass D, Schwartz B, Cooper R, Gelaznikas R, Barr A. Amiodarone as compared with lidocaine for shock-resistant ventricular fibrillation. N Engl J Med 2002;346:
158 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Thel MC, Armstrong AL, McNulty SE, Califf RM, O Connor CM. Randomised trial of magnesium in in-hospital cardiac arrest. Duke Internal Medicine Housestaff. Lancet 1997;350: Allegra J, Lavery R, Cody R, et al. Magnesium sulfate in the treatment of refractory ventricular fibrillation in the prehospital setting. Resuscitation 2001;49: Fatovich D, Prentice D, Dobb G. Magnesium in in-hospital cardiac arrest. Lancet 1998;351: Hassan TB, Jagger C, Barnett DB. A randomised trial to investigate the efficacy of magnesium sulphate for refractory ventricular fibrillation. Emerg Med J 2002;19: Miller B, Craddock L, Hoffenberg S, et al. Pilot study of intravenous magnesium sulfate in refractory cardiac arrest: safety data and recommendations for future studies. Resuscitation 1995;30: Weil MH, Rackow EC, Trevino R, Grundler W, Falk JL, Griffel MI. Difference in acid-base state between venous and arterial blood during cardiopulmonary resuscitation. N Engl J Med 1986;315: Wagner H, Terkelsen CJ, Friberg H, et al. Cardiac arrest in the catheterisation laboratory: a 5-year experience of using mechanical chest compressions to facilitate PCI during prolonged resuscitation efforts. Resuscitation 2010;81: Soar J, Perkins GD, Abbas G, et al. European Resuscitation Council Guidelines for Resuscitation Section 8. Cardiac arrest in special circumstances: electrolyte abnormalities, poisoning, drowning, accidental hypothermia, hyperthermia, asthma, anaphylaxis, cardiac surgery, trauma, pregnancy, electrocution. Resuscitation 2010;81: Price S, Uddin S, Quinn T. Echocardiography in cardiac arrest. Curr Opin Crit Care 2010;16: Memtsoudis SG, Rosenberger P, Loffler M, et al. The usefulness of transesophageal echocardiography during intraoperative cardiac arrest in non cardiac surgery. Anesth Analg 2006;102: Comess KA, DeRook FA, Russell ML, Tognazzi-Evans TA, Beach KW. The incidence of pulmonary embolism in unexplained sudden cardiac arrest with pulseless electrical activity. Am J Med 2000;109: Niendorff DF, Rassias AJ, Palac R, Beach ML, Costa S, Greenberg M. Rapid cardiac ultrasound of inpatients suffering PEA arrest performed by nonexpert sonographers. Resuscitation 2005;67: Tayal VS, Kline JA. Emergency echocardiography to detect pericardial effusion in patients in PEA and near-pea states. Resuscitation 2003;59: van der Wouw PA, Koster RW, Delemarre BJ, de Vos R, Lampe-Schoenmaeckers AJ, Lie KI. Diagnostic accuracy of transesophageal echocardiography during cardiopulmonary resuscitation. J Am Coll Cardiol 1997;30: Hernandez C, Shuler K, Hannan H, Sonyika C, Likourezos A, Marshall J. C.A.U.S.E.: Cardiac arrest ultra-sound exam a better approach to managing patients in primary non-arrhythmogenic cardiac arrest. Resuscitation 2008;76: Steiger HV, Rimbach K, Muller E, Breitkreutz R. Focused emergency echocardiography: lifesaving tool for a 14-year-old girl suffering out-of-hospital pulseless electrical activity arrest because of cardiac tamponadefi Eur J Emerg Med 2009;16: Breitkreutz R, Walcher F, Seeger FH. Focused echocardiographic evaluation in resuscitation management: concept of an advanced life support-conformed algorithm. Crit Care Med 2007;35:S Blaivas M, Fox JC. Outcome in cardiac arrest patients found to have cardiac standstill on the bedside emergency department echocardiogram. Acad Emerg Med 2001;8: Salen P, O Connor R, Sierzenski P, et al. Can cardiac sonography and capnography be used independently and in combination to predict resuscitation outcomes? Acad Emerg Med 2001;8: Salen P, Melniker L, Chooljian C, et al. Does the presence or absence of sonographically identified cardiac activity predict resuscitation outcomes of cardiac arrest patients? Am J Emerg Med 2005;23: Bottiger BW, Bode C, Kern S, et al. Efficacy and safety of thrombolytic therapy after initially unsuccessful cardiopulmonary resuscitation: a prospective clinical trial. Lancet 2001;357: Boidin MP. Airway patency in the unconscious patient. Br J Anaesth 1985;57: Nandi PR, Charlesworth CH, Taylor SJ, Nunn JF, Dore CJ. Effect of general anaesthesia on the pharynx. Br J Anaesth 1991;66: Guildner CW. Resuscitation: opening the airway. A comparative study of techniques for opening an airway obstructed by the tongue. JACEP 1976;5: Safar P, Escarraga LA, Chang F. Upper airway obstruction in the unconscious patient. J Appl Physiol 1959;14: Greene DG, Elam JO, Dobkin AB, Studley CL. Cinefluorographic study of hyperextension of the neck and upper airway patency. JAMA 1961;176: Morikawa S, Safar P, Decarlo J. Influence of the headjaw position upon upper airway patency. Anesthesiology 1961;22: Ruben HM, Elam JO, Ruben AM, Greene DG. Investigation of upper airway problems in resuscitation, 1: studies of pharyngeal x-rays and performance by laymen. Anesthesiology 1961;22: Elam JO, Greene DG, Schneider MA, et al. Head-tilt method of oral resuscitation. JAMA 1960;172: Aprahamian C, Thompson BM, Finger WA, Darin JC. Experimental cervical spine injury model: evaluation of airway management and splinting techniques. Ann Emerg Med 1984;13: Donaldson 3rd WF, Heil BV, Donaldson VP, Silvaggio VJ. The effect of airway maneuvers on the unstable C1 C2 segment. A cadaver study. Spine 1997;22: Donaldson 3rd WF, Towers JD, Doctor A, Brand A, Donaldson VP. A methodology to evaluate motion of the unstable spine during intubation techniques. Spine 1993;18: Hauswald M, Sklar DP, Tandberg D, Garcia JF. Cervical spine movement during airway management: cinefluoroscopic appraisal in human cadavers. Am J Emerg Med 1991;9: Brimacombe J, Keller C, Kunzel KH, Gaber O, Boehler M, Puhringer F. Cervical spine motion during airway management: a cinefluoroscopic study of the posteriorly destabilized third cervical vertebrae in human cadavers. Anesth Analg 2000;91: Majernick TG, Bieniek R, Houston JB, Hughes HG. Cervical spine movement during orotracheal intubation. Ann Emerg Med 1986;15: Lennarson PJ, Smith DW, Sawin PD, Todd MM, Sato Y, Traynelis VC. Cervical spinal motion during intubation: efficacy of stabilization maneuvers in the setting of complete segmental instability. J Neurosurg Spine 2001;94: Marsh AM, Nunn JF, Taylor SJ, Charlesworth CH. Airway obstruction associated with the use of the Guedel airway. Br J Anaesth 1991;67: Schade K, Borzotta A, Michaels A. Intracranial malposition of nasopharyngeal airway. J Trauma 2000;49: Muzzi DA, Losasso TJ, Cucchiara RF. Complication from a nasopharyngeal airway in a patient with a basilar skull fracture. Anesthesiology 1991;74: Roberts K, Porter K. How do you size a nasopharyngeal airway. Resuscitation 2003;56: Stoneham MD. The nasopharyngeal airway. Assessment of position by fibre-optic laryngoscopy. Anaesthesia 1993;48: Balan IS, Fiskum G, Hazelton J, Cotto-Cumba C, Rosenthal RE. Oximetryguided reoxygenation improves neurological outcome after experimental cardiac arrest. Stroke 2006;37: Kilgannon JH, Jones AE, Shapiro NI, et al. Association between arterial hyperoxia following resuscitation from cardiac arrest and in-hospital mortality. JAMA 2010;303: Alexander R, Hodgson P, Lomax D, Bullen C. A comparison of the laryngeal mask airway and Guedel airway, bag and face mask for manual ventilation following formal training. Anaesthesia 1993;48: Doerges V, Sauer C, Ocker H, Wenzel V, Schmucker P. Smaller tidal volumes during cardiopulmonary resuscitation: comparison of adult and paediatric self-inflatable bags with three different ventilatory devices. Resuscitation 1999;43: Ocker H, Wenzel V, Schmucker P, Dorges V. Effectiveness of various airway management techniques in a bench model simulating a cardiac arrest patient. J Emerg Med 2001;20: Stone BJ, Chantler PJ, Baskett PJ. The incidence of regurgitation during cardiopulmonary resuscitation: a comparison between the bag valve mask and laryngeal mask airway. Resuscitation 1998;38: Petito SP, Russell WJ. The prevention of gastric inflation a neglected benefit of cricoid pressure. Anaesth Intensive Care 1988;16: Lawes EG, Campbell I, Mercer D. Inflation pressure, gastric insufflation and rapid sequence induction. Br J Anaesth 1987;59: Hartsilver EL, Vanner RG. Airway obstruction with cricoid pressure. Anaesthesia 2000;55: Allman KG. The effect of cricoid pressure application on airway patency. J Clin Anesth 1995;7: Hocking G, Roberts FL, Thew ME. Airway obstruction with cricoid pressure and lateral tilt. Anaesthesia 2001;56: Mac GPJH, Ball DR. The effect of cricoid pressure on the cricoid cartilage and vocal cords: an endoscopic study in anaesthetised patients. Anaesthesia 2000;55: Aufderheide TP, Sigurdsson G, Pirrallo RG, et al. Hyperventilation-induced hypotension during cardiopulmonary resuscitation. Circulation 2004;109: O Neill JF, Deakin CD. Do we hyperventilate cardiac arrest patients? Resuscitation 2007;73: Olasveengen TM, Vik E, Kuzovlev A, Sunde K. Effect of implementation of new resuscitation guidelines on quality of cardiopulmonary resuscitation and survival. Resuscitation 2009;80: Olasveengen TM, Wik L, Steen PA. Quality of cardiopulmonary resuscitation before and during transport in out-of-hospital cardiac arrest. Resuscitation 2008;76: Weiss SJ, Ernst AA, Jones R, et al. Automatic transport ventilator versus bag valve in the EMS setting: a prospective, randomized trial. South Med J 2005;98: Stallinger A, Wenzel V, Wagner-Berger H, et al. Effects of decreasing inspiratory flow rate during simulated basic life support ventilation of a cardiac arrest patient on lung and stomach tidal volumes. Resuscitation 2002;54: Noordergraaf GJ, van Dun PJ, Kramer BP, et al. Can first responders achieve and maintain normocapnia when sequentially ventilating with a bag-valve device and two oxygen-driven resuscitators? A controlled clinical trial in 104 patients. Eur J Anaesthesiol 2004;21: Deakin CD, O Neill JF, Tabor T. Does compression-only cardiopulmonary resuscitation generate adequate passive ventilation during cardiac arrest? Resuscitation 2007;75: Saissy JM, Boussignac G, Cheptel E, et al. Efficacy of continuous insufflation of oxygen combined with active cardiac compression decompression during out- -of-hospital cardiorespiratory arrest. Anesthesiology 2000;92:
159 158 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins Bertrand C, Hemery F, Carli P, et al. Constant flow insufflation of oxygen as the sole mode of ventilation during out-of-hospital cardiac arrest. Intensive Care Med 2006;32: Bobrow BJ, Ewy GA, Clark L, et al. Passive oxygen insufflation is superior to bag-valve-mask ventilation for witnessed ventricular fibrillation out-of-hospital cardiac arrest. Ann Emerg Med 2009;54, e Jones JH, Murphy MP, Dickson RL, Somerville GG, Brizendine EJ. Emergency physician-verified out-of-hospital intubation: miss rates by paramedics. Acad Emerg Med 2004;11: Pelucio M, Halligan L, Dhindsa H. Out-of-hospital experience with the syringe esophageal detector device. Acad Emerg Med 1997;4: Jemmett ME, Kendal KM, Fourre MW, Burton JH. Unrecognized misplacement of endotracheal tubes in a mixed urban to rural emergency medical services setting. Acad Emerg Med 2003;10: Katz SH, Falk JL. Misplaced endotracheal tubes by paramedics in an urban emergency medical services system. Ann Emerg Med 2001;37: Nolan JP, Soar J. Airway techniques and ventilation strategies. Curr Opin Crit Care 2008;14: Gatward JJ, Thomas MJ, Nolan JP, Cook TM. Effect of chest compressions on the time taken to insert airway devices in a manikin. Br J Anaesth 2008;100: Davies PR, Tighe SQ, Greenslade GL, Evans GH. Laryngeal mask airway and tracheal tube insertion by unskilled personnel. Lancet 1990;336: Flaishon R, Sotman A, Ben-Abraham R, Rudick V, Varssano D, Weinbroum AA. Antichemical protective gear prolongs time to success ful airway management: a randomized, crossover study in humans. Anesthesiology 2004;100: Ho BY, Skinner HJ, Mahajan RP. Gastro-oesophageal reflux during day case gynaecological laparoscopy under positive pressure ventilation: laryngeal mask vs. tracheal intubation. Anaesthesia 1998;53: Reinhart DJ, Simmons G. Comparison of placement of the laryngeal mask airway with endotracheal tube by paramedics and respiratory therapists. Ann Emerg Med 1994;24: Rewari W, Kaul HL. Regurgitation and aspiration during gynaecological laparoscopy: comparison between laryngeal mask airway and tracheal intubation. J Anaesthesiol Clin Pharmacol 1999;15: Pennant JH, Walker MB. Comparison of the endotracheal tube and laryngeal mask in airway management by paramedical personnel. Anesth Analg 1992;74: Maltby JR, Beriault MT, Watson NC, Liepert DJ, Fick GH. LMA-Classicand LMA-ProSeal are effective alternatives to endotracheal intubation for gynecologic laparoscopy. Can J Anaesth 2003;50: Deakin CD, Peters R, Tomlinson P, Cassidy M. Securing the prehospital airway: a comparison of laryngeal mask insertion and endotracheal intubation by UK paramedics. Emerg Med J 2005;22: Cook TM, Hommers C. New airways for resuscitation? Resuscitation 2006; 69: Verghese C, Prior-Willeard PF, Baskett PJ. Immediate management of the airway during cardiopulmonary resuscitation in a hospital without a resident anaesthesiologist. Eur J Emerg Med 1994;1: Kokkinis K. The use of the laryngeal mask airway in CPR. Resuscitation 1994;27: Leach A, Alexander CA, Stone B. The laryngeal mask in cardiopulmonary resuscitation in a district general hospital: a preliminary communication. Resuscitation 1993;25: The use of the laryngeal mask airway by nurses during cardiopulmonary resuscitation: results of a multicentre trial. Anaesthesia 1994;49: Rumball CJ, MacDonald D. The PTL, Combitube, laryngeal mask, and oral airway: a randomized prehospital comparative study of ventilatory device effectiveness and cost-effectiveness in 470 cases of cardiorespiratory arrest. Prehosp Emerg Care 1997;1: Tanigawa K, Shigematsu A. Choice of airway devices for 12,020 cases of nontraumatic cardiac arrest in Japan. Prehosp Emerg Care 1998;2: Grantham H, Phillips G, Gilligan JE. The laryngeal mask in prehospital emergency care 1994;6: Comparison of arterial blood gases of laryngeal mask airway and bag-valvemask ventilation in out-of-hospital cardiac arrests. Circ J 2009;73: Staudinger T, Brugger S, Watschinger B, et al. Emergency intubation with the Combitube: comparison with the endotracheal airway. Ann Emerg Med 1993;22: Lefrancois DP, Dufour DG. Use of the esophageal tracheal combitube by basic emergency medical technicians. Resuscitation 2002;52: Ochs M, Vilke GM, Chan TC, Moats T, Buchanan J. Successful prehospital airway management by EMT-Ds using the combitube. Prehosp Emerg Care 2000;4: Vezina D, Lessard MR, Bussieres J, Topping C, Trepanier CA. Complications associated with the use of the Esophageal-Tracheal Combitube. Can J Anaesth 1998;45: Richards CF. Piriform sinus perforation during Esophageal-Tracheal Combitube placement. J Emerg Med 1998;16: Rumball C, Macdonald D, Barber P, Wong H, Smecher C. Endotracheal intubation and esophageal tracheal Combitube insertion by regular ambulance attendants: a comparative trial. Prehosp Emerg Care 2004;8: Rabitsch W, Schellongowski P, Staudinger T, et al. Comparison of a conventional tracheal airway with the Combitube in an urban emergency medical services system run by physicians. Resuscitation 2003;57: Goldenberg IF, Campion BC, Siebold CM, McBride JW, Long LA. Esophageal gastric tube airway vs endotracheal tube in prehospital cardiopulmonary arrest. Chest 1986;90: Cook TM, McCormick B, Asai T. Randomized comparison of laryngeal tube with classic laryngeal mask airway for anaesthesia with controlled ventilation. Br J Anaesth 2003;91: Cook TM, McKinstry C, Hardy R, Twigg S. Randomized crossover comparison of the ProSeal laryngeal mask airway with the Laryngeal Tube during anaesthesia with controlled ventilation. Br J Anaesth 2003;91: Kette F, Reffo I, Giordani G, et al. The use of laryngeal tube by nurses in out-of- -hospital emergencies: preliminary experience. Resuscitation 2005;66: Wiese CH, Semmel T, Muller JU, Bahr J, Ocker H, Graf BM. The use of the laryngeal tube disposable (LT-D) by paramedics during out-of-hospital resuscitation-an observational study concerning ERC guidelines Resuscitation 2009;80: Wiese CH, Bartels U, Schultens A, et al. Using a Laryngeal Tube Suction-Device (LTS-D) reduces the No Flow Time in a single rescuer Manikin study. J Emerg Med Wharton NM, Gibbison B, Gabbott DA, Haslam GM, Muchatuta N, Cook TM. I-gel insertion by novices in manikins and patients. Anaesthesia 2008; 63: Gatward JJ, Cook TM, Seller C, et al. Evaluation of the size 4 i-gel airway in one hundred non-paralysed patients. Anaesthesia 2008;63: Jackson KM, Cook TM. Evaluation of four airway training manikins as patient simulators for the insertion of eight types of supraglottic airway devices. Anaesthesia 2007;62: Soar J. The I-gel supraglottic airway and resuscitation some initial thoughts. Resuscitation 2007;74: Thomas M, Benger J. Pre-hospital resuscitation using the igel. Resuscitation 2009;80: Cook TM, Nolan JP, Verghese C, et al. Randomized crossover comparison of the proseal with the classic laryngeal mask airway in unparalysed anaesthetized patients. Br J Anaesth 2002;88: Timmermann A, Cremer S, Eich C, et al. Prospective clinical and fiberoptic evaluation of the Supreme laryngeal mask airway. Anesthesiology 2009;110: Cook TM, Gatward JJ, Handel J, et al. Evaluation of the LMA Supreme in 100 non-paralysed patients. Anaesthesia 2009;64: Hosten T, Gurkan Y, Ozdamar D, Tekin M, Toker K, Solak M. A new supraglottic airway device: LMA-supreme, comparison with LMA-Proseal. Acta Anaesthesiol Scand 2009;53: Burgoyne L, Cyna A. Laryngeal mask vs intubating laryngeal mask: insertion and ventilation by inexperienced resuscitators. Anaesth Intensive Care 2001; 29: Choyce A, Avidan MS, Shariff A, Del Aguila M, Radcliffe JJ, Chan T. A comparison of the intubating and standard laryngeal mask airways for airway management by inexperienced personnel. Anaesthesia 2001;56: Baskett PJ, Parr MJ, Nolan JP. The intubating laryngeal mask. Results of a multicentre trial with experience of 500 cases. Anaesthesia 1998;53: Tentillier E, Heydenreich C, Cros AM, Schmitt V, Dindart JM, Thicoipe M. Use of the intubating laryngeal mask airway in emergency pre-hospital difficult intubation. Resuscitation 2008;77: Lecky F, Bryden D, Little R, Tong N, Moulton C. Emergency intubation for acutely ill and injured patients. Cochrane Database Syst Rev 2008:CD Gausche M, Lewis RJ, Stratton SJ, et al. Effect of out-of-hospital pediatric endotracheal intubation on survival and neurological outcome: a controlled clinical trial. JAMA 2000;283: Kramer-Johansen J, Wik L, Steen PA. Advanced cardiac life support before and after tracheal intubation direct measurements of quality. Resuscitation 2006;68: Grmec S. Comparison of three different methods to confirm tracheal tube placement in emergency intubation. Intensive Care Med 2002;28: Lyon RM, Ferris JD, Young DM, McKeown DW, Oglesby AJ, Robertson C. Field intubation of cardiac arrest patients: a dying art? Emerg Med J 2010;27: Wang HE, Simeone SJ, Weaver MD, Callaway CW. Interruptions in cardiopulmonary resuscitation from paramedic endotracheal intubation. Ann Emerg Med 2009;54:645e1 52e Garza AG, Gratton MC, Coontz D, Noble E, Ma OJ. Effect of paramedic experience on orotracheal intubation success rates. J Emerg Med 2003;25: Sayre MR, Sakles JC, Mistler AF, Evans JL, Kramer AT, Pancioli AM. Field trial of endotracheal intubation by basic EMTs. Ann Emerg Med 1998;31: Bradley JS, Billows GL, Olinger ML, Boha SP, Cordell WH, Nelson DR. Prehospital oral endotracheal intubation by rural basic emergency medical technicians. Ann Emerg Med 1998;32: Bobrow BJ, Clark LL, Ewy GA, et al. Minimally interrupted cardiac resuscitation by emergency medical services for out-of-hospital cardiac arrest. JAMA 2008;299: Takeda T, Tanigawa K, Tanaka H, Hayashi Y, Goto E, Tanaka K. The assessment of three methods to identify tracheal tube placement in the emergency setting. Resuscitation 2003: Knapp S, Kofler J, Stoiser B, et al. The assessment of four different methods to verify tracheal tube placement in the critical care setting. Anesth Analg 1999;88: Grmec S, Mally S. Prehospital determination of tracheal tube placement in severe head injury. Emerg Med J 2004;21:
160 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Yao YX, Jiang Z, Lu XH, He JH, Ma XX, Zhu JH. A clinical study of impedance graph in verifying tracheal intubation. Zhonghua Yi Xue Za Zhi 2007;87: Li J. Capnography alone is imperfect for endotracheal tube placement confirmation during emergency intubation. J Emerg Med 2001;20: Tanigawa K, Takeda T, Goto E, Tanaka K. Accuracy and reliability of the selfinflating bulb to verify tracheal intubation in out-of-hospital cardiac arrest patients. Anesthesiology 2000;93: Baraka A, Khoury PJ, Siddik SS, Salem MR, Joseph NJ. Efficacy of the self-inflating bulb in differentiating esophageal from tracheal intubation in the parturient undergoing cesarean section. Anesth Analg 1997;84: Davis DP, Stephen KA, Vilke GM. Inaccuracy in endotracheal tube verification using a Toomey syringe. J Emerg Med 1999;17: Bozeman WP, Hexter D, Liang HK, Kelen GD. Esophageal detector device versus detection of end-tidal carbon dioxide level in emergency intubation. Ann Emerg Med 1996;27: Jenkins WA, Verdile VP, Paris PM. The syringe aspiration technique to verify endotracheal tube position. Am J Emerg Med 1994;12: Schaller RJ, Huff JS, Zahn A. Comparison of a colorimetric end-tidal CO2 detector and an esophageal aspiration device for verifying endotracheal tube placement in the prehospital setting: a six-month experience. Prehosp Disaster Med 1997;12: Tanigawa K, Takeda T, Goto E, Tanaka K. The efficacy of esophageal detector devices in verifying tracheal tube placement: a randomized cross-over study of out-of-hospital cardiac arrest patients. Anesth Analg 2001;92: Anton WR, Gordon RW, Jordan TM, Posner KL, Cheney FW. A disposable end-tidal CO2 detector to verify endotracheal intubation. Ann Emerg Med 1991;20: MacLeod BA, Heller MB, Gerard J, Yealy DM, Menegazzi JJ. Verification of endotracheal tube placement with colorimetric end-tidal CO2 detection. Ann Emerg Med 1991;20: Ornato JP, Shipley JB, Racht EM, et al. Multicenter study of a portable, handsize, colorimetric end-tidal carbon dioxide detection device. Ann Emerg Med 1992;21: Sanders KC, Clum 3rd WB, Nguyen SS, Balasubramaniam S. End-tidal carbon dioxide detection in emergency intubation in four groups of patients. J Emerg Med 1994;12: Varon AJ, Morrina J, Civetta JM. Clinical utility of a colorimetric end-tidal CO 2 detector in cardiopulmonary resuscitation and emergency intubation. J Clin Monit 1991;7: Vukmir RB, Heller MB, Stein KL. Confirmation of endotracheal tube placement: a miniaturized infrared qualitative CO 2 detector. Ann Emerg Med 1991;20: Silvestri S, Ralls GA, Krauss B, et al. The effectiveness of out-of-hospital use of continuous end-tidal carbon dioxide monitoring on the rate of unrecognized misplaced intubation within a regional emergency medical services system. Ann Emerg Med 2005;45: Mehta KH, Turley A, Peyrasse P, Janes J, Hall JE. An assessment of the ability of impedance respirometry distinguish oesophageal from tracheal intubation. Anaesthesia 2002;57: Absolom M, Roberts R, Bahlmann UB, Hall JE, Armstrong T, Turley A. The use of impedance respirometry to confirm tracheal intubation in children. Anaesthesia 2006;61: Kramer-Johansen J, Eilevstjonn J, Olasveengen TM, Tomlinson AE, Dorph E, Steen PA. Transthoracic impedance changes as a tool to detect malpositioned tracheal tubes. Resuscitation 2008;76: Risdal M, Aase SO, Stavland M, Eftestol T. Impedance-based ventilation detection during cardiopulmonary resuscitation. IEEE Trans Biomed Eng 2007;54: Pytte M, Olasveengen TM, Steen PA, Sunde K. Misplaced and dislodged endotracheal tubes may be detected by the defibrillator during cardiopulmonary resuscitation. Acta Anaesthesiol Scand 2007;51: Salem MR, Wong AY, Mani M, Sellick BA. Efficacy of cricoid pressure in preventing gastric inflation during bag-mask ventilation in pediatric patients. Anesthesiology 1974;40: Moynihan RJ, Brock-Utne JG, Archer JH, Feld LH, Kreitzman TR. The effect of cricoid pressure on preventing gastric insufflation in infants and children. Anesthesiology 1993;78: Ho AM, Wong W, Ling E, Chung DC, Tay BA. Airway difficulties caused by improperly applied cricoid pressure. J Emerg Med 2001;20: Shorten GD, Alfille PH, Gliklich RE. Airway obstruction following application of cricoid pressure. J Clin Anesth 1991;3: Proceedings of the guidelines 2000 conference for cardiopulmonary resuscitation and emergency cardiovascularcare: an international consensus on science. Ann Emerg Med 2001;37:S Lindner KH, Dirks B, Strohmenger HU, Prengel AW, Lindner IM, Lurie KG. Randomised comparison of epinephrine and vasopressin in patients with out-of- -hospital ventricular fibrillation. Lancet 1997;349: Wenzel V, Krismer AC, Arntz HR, Sitter H, Stadlbauer KH, Lindner KH. A comparison of vasopressin and epinephrine for out-of-hospital cardiopulmonary resuscitation. N Engl J Med 2004;350: Stiell IG, Hebert PC, Wells GA, et al. Vasopressin versus epinephrine for inhospital cardiac arrest: a randomised controlled trial. Lancet 2001;358: Aung K, Htay T. Vasopressin for cardiac arrest: a systematic review and metaanalysis. Arch Intern Med 2005;165: Callaway CW, Hostler D, Doshi AA, et al. Usefulness of vasopressin administered with epinephrine during out-of-hospital cardiac arrest. Am J Cardiol 2006;98: Gueugniaud PY, David JS, Chanzy E, et al. Vasopressin and epinephrine vs. epinephrine alone in cardiopulmonary resuscitation. N Engl J Med 2008;359: Masini E, Planchenault J, Pezziardi F, Gautier P, Gagnol JP. Histamine-releasing properties of Polysorbate 80 in vitro and in vivo: correlation with its hypotensive action in the dog. Agents Actions 1985;16: Somberg JC, Bailin SJ, Haffajee CI, et al. Intravenous lidocaine versus intravenous amiodarone (in a new aqueous formulation) for incessant ventricular tachycardia. Am J Cardiol 2002;90: Somberg JC, Timar S, Bailin SJ, et al. Lack of a hypotensive effect with rapid administration of a new aqueous formulation of intravenous amiodarone. Am J Cardiol 2004;93: Skrifvars MB, Kuisma M, Boyd J, et al. The use of undiluted amiodarone in the management of out-of-hospital cardiac arrest. Acta Anaesthesiol Scand 2004;48: Petrovic T, Adnet F, Lapandry C. Successful resuscitation of ventricular fibrillation after low-dose amiodarone. Ann Emerg Med 1998;32: Levine JH, Massumi A, Scheinman MM, et al. Intravenous amiodarone for recurrent sustained hypotensive ventricular tachyarrhythmias. Intravenous Amiodarone Multicenter Trial Group. J Am Coll Cardiol 1996;27: Matsusaka T, Hasebe N, Jin YT, Kawabe J, Kikuchi K. Magnesium reduces myocardial infarct size via enhancement of adenosine mechanism in rabbits. Cardiovasc Res 2002;54: Longstreth Jr WT, Fahrenbruch CE, Olsufka M, Walsh TR, Copass MK, Cobb LA. Randomized clinical trial of magnesium, diazepam, or both after out-of-hospital cardiac arrest. Neurology 2002;59: Stiell IG, Wells GA, Hebert PC, Laupacis A, Weitzman BN. Association of drug therapy with survival in cardiac arrest: limited role of advanced cardiac life support drugs. Acad Emerg Med 1995;2: Engdahl J, Bang A, Lindqvist J, Herlitz J. Can we define patients with no and those with some chance of survival when found in asystole out of hospital? Am J Cardiol 2000;86: Engdahl J, Bang A, Lindqvist J, Herlitz J. Factors affecting short-and long-term prognosis among 1069 patients with out-of-hospital cardiac arrest and pulse-less electrical activity. Resuscitation 2001;51: Dumot JA, Burval DJ, Sprung J, et al. Outcome of adult cardiopulmonary resuscitations at a tertiary referral center including results of limited resuscitations. Arch Intern Med 2001;161: Tortolani AJ, Risucci DA, Powell SR, Dixon R. In-hospital cardiopulmonary resuscitation during asystole. Therapeutic factors associated with 24-hour survival. Chest 1989;96: Coon GA, Clinton JE, Ruiz E. Use of atropine for brady-asystolic prehospital cardiac arrest. Ann Emerg Med 1981;10: Harrison EE, Amey BD. The use of calcium in cardiac resuscitation. Am J Emerg Med 1983;1: Stueven HA, Thompson B, Aprahamian C, Tonsfeldt DJ, Kastenson EH. The effectiveness of calcium chloride in refractory electromechanical dissociation. Ann Emerg Med 1985;14: Stueven HA, Thompson B, Aprahamian C, Tonsfeldt DJ, Kastenson EH. Lack of effectiveness of calcium chloride in refractory asystole. Ann Emerg Med 1985;14: Stueven HA, Thompson BM, Aprahamian C, Tonsfeldt DJ. Calcium chloride: reassessment of use in asystole. Ann Emerg Med 1984;13: Gando S, Tedo I, Tujinaga H, Kubota M. Variation in serum ionized calcium on cardiopulmonary resuscitation. J Anesth 1988;2: Stueven H, Thompson BM, Aprahamian C, Darin JC. Use of calcium in prehospital cardiac arrest. Ann Emerg Med 1983;12: van Walraven C, Stiell IG, Wells GA, Hebert PC, Vandemheen K. Do advanced cardiac life support drugs increase resuscitation rates from in-hospital cardiac arrest? The OTAC Study Group. Ann Emerg Med 1998;32: Dybvik T, Strand T, Steen PA. Buffer therapy during out-of-hospital cardiopulmonary resuscitation. Resuscitation 1995;29: Aufderheide TP, Martin DR, Olson DW, et al. Prehospital bicarbonate use in cardiac arrest: a 3-year experience. Am J Emerg Med 1992;10: Delooz H, Lewi PJ. Are inter-center differences in EMS-management and sodium-bicarbonate administration important for the outcome of CPR? The Cerebral Resuscitation Study Group. Resuscitation 1989;17(Suppl.):S Roberts D, Landolfo K, Light R, Dobson K. Early predictors of mortality for hospitalized patients suffering cardiopulmonary arrest. Chest 1990;97: Suljaga-Pechtel K, Goldberg E, Strickon P, Berger M, Skovron ML. Cardiopulmonary resuscitation in a hospitalized population: prospective study of factors associated with outcome. Resuscitation 1984;12: Weil MH, Trevino RP, Rackow EC. Sodium bicarbonate during CPR. Does it help or hinder? Chest 1985;88: Vukmir RB, Katz L. Sodium bicarbonate improves outcome in prolonged prehospital cardiac arrest. Am J Emerg Med 2006;24: Bar-Joseph G, Abramson NS, Kelsey SF, Mashiach T, Craig MT, Safar P. Improved resuscitation outcomein emergency medical systems with increased usage of sodium bicarbonate during cardiopulmonary resuscitation. Acta Anaesthesiol Scand 2005;49: Weaver WD, Eisenberg MS, Martin JS, et al. Myocardial Infarction Triage and Intervention Project, phase I: patient characteristics and feasibility of prehospital initiation of thrombolytic therapy. J Am Coll Cardiol 1990;15:
161 160 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins Sandeman DJ, Alahakoon TI, Bentley SC. Tricyclic poisoning successful management of ventricular fibrillation following massive overdose of imipramine. Anaesth Intensive Care 1997;25: Lin SR. The effect of dextran and streptokinase on cerebral function and blood flow after cardiac arrest. An experimental study on the dog. Neuroradiology 1978;16: Fischer M, Bottiger BW, Popov-Cenic S, Hossmann KA. Thrombolysis using plasminogen activator and heparin reduces cerebral no-reflow after resuscitation from cardiac arrest: an experimental study in the cat. Intensive Care Med 1996;22: Ruiz-Bailen M, Aguayo de Hoyos E, Serrano-Corcoles MC, Diaz-Castellanos MA, Ramos-Cuadra JA, Reina-Toral A. Efficacy of thrombolysis in patients with acute myocardial infarction requiring cardiopulmonary resuscitation. Intensive Care Med 2001;27: Janata K, Holzer M, Kurkciyan I, et al. Major bleeding complications in cardiopulmonary resuscitation: the place of thrombolytic therapy in cardiac arrest due to massive pulmonary embolism. Resuscitation 2003;57: Kurkciyan I, Meron G, Sterz F, et al. Pulmonary embolism as a cause of cardiac arrest: presentation and outcome. Arch Intern Med 2000;160: Lederer W, Lichtenberger C, Pechlaner C, Kroesen G, Baubin M. Recombinant tissue plasminogen activator during cardiopulmonary resuscitation in 108 patients with out-of-hospital cardiac arrest. Resuscitation 2001;50: Bozeman WP, Kleiner DM, Ferguson KL. Empiric tenecteplase is associated with increased return of spontaneous circulation and short term survival in cardiac arrest patients unresponsive to standard interventions. Resuscitation 2006;69: Stadlbauer KH, Krismer AC, Arntz HR, et al. Effects of thrombolysis during out-of-hospital cardiopulmonary resuscitation. Am J Cardiol 2006;97: Fatovich DM, Dobb GJ, Clugston RA. A pilot randomised trial of thrombolysis in cardiac arrest (The TICA trial). Resuscitation 2004;61: Tiffany PA, Schultz M, Stueven H. Bolus thrombolytic infusions during CPR for patients with refractory arrest rhythms: outcome of a case series. Ann Emerg Med 1998;31: Abu-Laban RB, Christenson JM, Innes GD, et al. Tissue plasminogen activator in cardiac arrest with pulseless electrical activity. N Engl J Med 2002; 346: Bottiger BW, Arntz HR, Chamberlain DA, et al. Thrombolysis during resuscitation for out-of-hospital cardiac arrest. N Engl J Med 2008;359: Li X, Fu QL, Jing XL, et al. A meta-analysis of cardiopulmonary resuscitation with and without the administration of thrombolytic agents. Resuscitation 2006;70: Fava M, Loyola S, Bertoni H, Dougnac A. Massive pulmonary embolism: percutaneous mechanical thrombectomy during cardiopulmonary resuscitation. J Vasc Interv Radiol 2005;16: Lederer W, Lichtenberger C, Pechlaner C, Kinzl J, Kroesen G, Baubin M. Longterm survival and neurological outcome of patients who received recombinant tissue plasminogen activator during out-of-hospital cardiac arrest. Resuscitation 2004;61: Zahorec R. Rescue systemic thrombolysis during cardiopulmonary resuscitation. Bratisl Lek Listy 2002;103: Konstantinov IE, Saxena P, Koniuszko MD, Alvarez J, Newman MA. Acute massive pulmonary embolism with cardiopulmonary resuscitation: management and results. Tex Heart Inst J 2007;34:41 5 [discussion 5 6] Scholz KH, Hilmer T, Schuster S, Wojcik J, Kreuzer H, Tebbe U. Thrombolysis in resuscitated patients with pulmonary embolism. Dtsch Med Wochenschr 1990;115: Gramann J, Lange-Braun P, Bodemann T, Hochrein H. Der Einsatz von Thrombolytika in der Reanimation als Ultima ratio zur Überwindung des Herztodes. Intensiv- und Notfallbehandlung 1991;16: Klefisch F, Gareis R, Störck T, Möckel M, Danne O. Praklinische ultima-ratio thrombolyse bei therapierefraktarer kardiopulmonaler reanimation. Intensivmedizin 1995;32: Böttiger BW, Martin E. Thrombolytic therapy during cardiopulmonary resuscitation and the role of coagulation activation after cardiac arrest. Curr Opin Crit Care 2001;7: Spöhr F, Böttiger BW. Safety of thrombolysis during cardiopulmonary resuscitation. Drug Saf 2003;26: Langhelle A, Tyvold SS, Lexow K, Hapnes SA, Sunde K, Steen PA. In-hospital factors associated with improved outcome after out-of-hospital cardiac arrest. A comparison between four regions in Norway. Resuscitation 2003;56: Calle PA, Buylaert WA, Vanhaute OA. Glycemia in the post-resuscitation period. The Cerebral Resuscitation Study Group. Resuscitation 1989;17(Suppl.): S181 8 [discussion S99 206] Longstreth Jr WT, Diehr P, Inui TS. Prediction of awakening after out-of-hospital cardiac arrest. N Engl J Med 1983;308: Longstreth Jr WT, Inui TS. High blood glucose level on hospital admission and poor neurological recovery after cardiac arrest. Ann Neurol 1984;15: Longstreth Jr WT, Copass MK, Dennis LK, Rauch-Matthews ME, Stark MS, Cobb LA. Intravenous glucose after out-of-hospital cardiopulmonary arrest: a community-based randomized trial. Neurology 1993;43: Mackenzie CF. A review of 100 cases of cardiac arrest and the relation of potassium, glucose, and haemoglobin levels to survival. West Indian Med J 1975;24: Mullner M, Sterz F, Binder M, Schreiber W, Deimel A, Laggner AN. Blood glucose concentration after cardiopulmonary resuscitation influences functional neurological recovery in human cardiac arrest survivors. J Cereb Blood Flow Metab 1997;17: Skrifvars MB, Pettila V, Rosenberg PH, Castren M. A multiple logistic regression analysis of in-hospital factors related to survival at six months in patients resuscitated from out-of-hospital ventricular fibrillation. Resuscitation 2003;59: Ditchey RV, Lindenfeld J. Potential adverse effects of volume loading on perfusion of vital organs during closed-chest resuscitation. Circulation 1984;69: Voorhees WD, Ralston SH, Kougias C, Schmitz PM. Fluid loading with whole blood or Ringer s lactate solution during CPR in dogs. Resuscitation 1987;15: Gentile NT, Martin GB, Appleton TJ, Moeggenberg J, Paradis NA, Nowak RM. Effects of arterial and venous volume infusion on coronary perfusion pressures during canine CPR. Resuscitation 1991;22: Bender R, Breil M, Heister U, et al. Hypertonic saline during CPR: feasibility and safety of a new protocol of fluid management during resuscitation. Resuscitation 2007;72: Bruel C, Parienti JJ, Marie W, et al. Mild hypothermia during advanced life support: a preliminary study in out-of-hospital cardiac arrest. Crit Care 2008;12: R Kamarainen A, Virkkunen I, Tenhunen J, Yli-Hankala A, Silfvast T. Prehospital induction of therapeutic hypothermia during CPR: a pilot study. Resuscitation 2008;76: Krep H, Breil M, Sinn D, Hagendorff A, Hoeft A, Fischer M. Effects of hypertonic versus isotonic infusion therapy on regional cerebral blood flow after experimental cardiac arrest cardiopulmonary resuscitation in pigs. Resuscitation 2004;63: Soar J, Foster J, Breitkreutz R. Fluid infusion during CPR and after ROSC is it safe? Resuscitation 2009;80: Ong ME, Chan YH, Oh JJ, Ngo AS. An observational, prospective study comparing tibial and humeral intraosseous access using the EZ-IO. Am J Emerg Med 2009;27: Gerritse BM, Scheffer GJ, Draaisma JM. Prehospital intraosseus access with the bone injection gun by a helicopter-transported emergency medical team. J Trauma 2009;66: Brenner T, Bernhard M, Helm M, et al. Comparison of two intraosseous infusion systems for adult emergency medical use. Resuscitation 2008;78: Frascone RJ, Jensen JP, Kaye K, Salzman JG. Consecutive field trials using two different intraosseous devices. Prehosp Emerg Care 2007;11: Banerjee S, Singhi SC, Singh S, Singh M. The intraosseous route is a suitable alternative to intravenous route for fluid resuscitation in severely dehydrated children. Indian Pediatr 1994;31: Brickman KR, Krupp K, Rega P, Alexander J, Guinness M. Typing and screening of blood from intraosseous access. Ann Emerg Med 1992;21: Fiser RT, Walker WM, Seibert JJ, McCarthy R, Fiser DH. Tibial length following intraosseous infusion: a prospective, radiographic analysis. Pediatr Emerg Care 1997;13: Ummenhofer W, Frei FJ, Urwyler A, Drewe J. Are laboratory values in bone marrow aspirate predictable for venous blood in paediatric patients? Resuscitation 1994;27: Guy J, Haley K, Zuspan SJ. Use of intraosseous infusion in the pediatric trauma patient. J Pediatr Surg 1993;28: Macnab A, Christenson J, Findlay J, et al. A new system for sternal intraosseous infusion in adults. Prehosp Emerg Care 2000;4: Ellemunter H, Simma B, Trawoger R, Maurer H. Intraosseous lines in preterm and full term neonates. Arch Dis Child Fetal Neonatal Ed 1999;80:F Delguercio LR, Feins NR, Cohn JD, Coomaraswamy RP, Wollman SB, State D. Comparison of blood flow during external and internal cardiac massage in man. Circulation 1965;31(Suppl. 1): Wik L, Kramer-Johansen J, Myklebust H, et al. Quality of cardiopulmonary resuscitation during out-of-hospital cardiac arrest. JAMA 2005;293: Kramer-Johansen J, Myklebust H, Wik L, et al. Quality of out-of-hospital cardiopulmonary resuscitation with real time automated feedback: a prospective interventional study. Resuscitation 2006;71: Sutton RM, Maltese MR, Niles D, et al. Quantitative analysis of chest compression interruptions during in-hospital resuscitation of older children and adolescents. Resuscitation 2009;80: Sutton RM, Niles D, Nysaether J, et al. Quantitative analysis of CPR quality during in-hospital resuscitation of older children and adolescents. Pediatrics 2009;124: Boczar ME, Howard MA, Rivers EP, et al. A technique revisited: hemodynamic comparison of closed-and open-chest cardiac massage during human cardiopulmonary resuscitation. Crit Care Med 1995;23: Anthi A, Tzelepis GE, Alivizatos P, Michalis A, Palatianos GM, Geroulanos S. Unexpected cardiac arrest after cardiac surgery: incidence, predisposing causes, and outcome of open chest cardiopulmonary resuscitation. Chest 1998;113: Pottle A, Bullock I, Thomas J, Scott L. Survival to discharge following Open Chest Cardiac Compression (OCCC). A 4-year retrospective audit in a cardiothoracic specialist centre Royal Brompton and Harefield NHS Trust, United Kingdom. Resuscitation 2002;52: Babbs CF. Interposed abdominal compression CPR: a comprehensive evidence based review. Resuscitation 2003;59: Babbs CF, Nadkarni V. Optimizing chest compression to rescue ventilation ratios during one-rescuer CPR by professionals and lay persons: children are not just little adults. Resuscitation 2004;61:
162 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Beyar R, Kishon Y, Kimmel E, Neufeld H, Dinnar U. Intrathoracic and abdominal pressure variations as an efficient method for cardiopulmonary resuscitation: studies in dogs compared with computer model results. Cardiovasc Res 1985;19: Voorhees WD, Niebauer MJ, Babbs CF. Improved oxygen delivery during cardiopulmonary resuscitation with interposed abdominal compressions. Ann Emerg Med 1983;12: Sack JB, Kesselbrenner MB, Bregman D. Survival from in-hospital cardiac arrest with interposed abdominal counterpulsation during cardiopulmonary resuscitation. JAMA 1992;267: Sack JB, Kesselbrenner MB, Jarrad A. Interposed abdominal compression-cardiopulmonary resuscitation and resuscitation outcome during asystole and electromechanical dissociation. Circulation 1992;86: Mateer JR, Stueven HA, Thompson BM, Aprahamian C, Darin JC. Pre-hospital IAC-CPR versus standard CPR: paramedic resuscitation of cardiac arrests. Am J Emerg Med 1985;3: Lindner KH, Pfenninger EG, Lurie KG, Schurmann W, Lindner IM, Ahnefeld FW. Effects of active compression decompression resuscitation on myocardial and cerebral blood flow in pigs. Circulation 1993;88: Shultz JJ, Coffeen P, Sweeney M, et al. Evaluation of standard and active compression decompression CPR in an acute human model of ventricular fibrillation. Circulation 1994;89: Chang MW, Coffeen P, Lurie KG, Shultz J, Bache RJ, White CW. Active compression decompression CPR improves vital organ perfusion in a dog model of ventricular fibrillation. Chest 1994;106: Orliaguet GA, Carli PA, Rozenberg A, Janniere D, Sauval P, Delpech P. Endtidal carbon dioxide during out-of-hospital cardiac arrest resuscitation: comparison of active compression decompression and standard CPR. Ann Emerg Med 1995;25: Guly UM, Mitchell RG, Cook R, Steedman DJ, Robertson CE. Paramedics and technicians are equally successful at managing cardiac arrest outside hospital. BMJ 1995;310: Tucker KJ, Galli F, Savitt MA, Kahsai D, Bresnahan L, Redberg RF. Active compression decompression resuscitation: effect on resuscitation success after in-hospital cardiac arrest. J Am Coll Cardiol 1994;24: Malzer R, Zeiner A, Binder M, et al. Hemodynamic effects of active compression decompression after prolonged CPR. Resuscitation 1996;31: Lurie KG, Shultz JJ, Callaham ML, et al. Evaluation of active compression decompression CPR in victims of out-of-hospital cardiac arrest. JAMA 1994;271: Cohen TJ, Goldner BG, Maccaro PC, et al. A comparison of active compression decompression cardiopulmonary resuscitation with standard cardiopulmonary resuscitation for cardiac arrests occurring in the hospital. N Engl J Med 1993;329: Schwab TM, Callaham ML, Madsen CD, Utecht TA. A randomized clinical trial of active compression decompression CPR vs standard CPR in out-of-hospital cardiac arrest in two cities. JAMA 1995;273: Stiell I, H ebert P, Well G, et al. The Ontario trial of active compression decompression cardiopulmonary resuscitation for in-hospital and prehospital cardiac arrest. JAMA 1996;275: Mauer D, Schneider T, Dick W, Withelm A, Elich D, Mauer M. Active compression decompression resuscitation: a prospective, randomized study in a twotiered EMS system with physicians in the field. Resuscitation 1996;33: Nolan J, Smith G, Evans R, et al. The United Kingdom pre-hospital study of active compression decompression resuscitation. Resuscitation 1998;37: Luiz T, Ellinger K, Denz C. Active compression decompression cardiopulmonary resuscitation does not improve survival in patients with prehospital cardiac arrest in a physician-manned emergency medical system. J Cardiothorac Vasc Anesth 1996;10: Plaisance P, Lurie KG, Vicaut E, et al. A comparison of standard cardiopulmonary resuscitation and active compression decompression resuscitation for out- -of-hospital cardiac arrest. French Active Compression-Decompression Cardiopulmonary Resuscitation Study Group. N Engl J Med 1999;341: Baubin M, Rabl W, Pfeiffer KP, Benzer A, Gilly H. Chest injuries after active compression decompression cardiopulmonary resuscitation (ACD-CPR) in cadavers. Resuscitation 1999;43: Rabl W, Baubin M, Broinger G, Scheithauer R. Serious complications from active compression decompression cardiopulmonary resuscitation. Int J Legal Med 1996;109: Hoke RS, Chamberlain D. Skeletal chest injuries secondary to cardiopulmonary resuscitation. Resuscitation 2004;63: Plaisance P, Lurie KG, Payen D. Inspiratory impedance during active compression decompression cardiopulmonary resuscitation: a randomized evaluation in patients in cardiac arrest. Circulation 2000;101: Plaisance P, Soleil C, Lurie KG, Vicaut E, Ducros L, Payen D. Use of an inspiratory impedance threshold device on a facemask and endotracheal tube to reduce intrathoracic pressures during the decompression phase of active compression decompression cardiopulmonary resuscitation. Crit Care Med 2005;33: Wolcke BB, Mauer DK, Schoefmann MF, et al. Comparison of standard cardiopulmonary resuscitation versus the combination of active compression decompression cardiopulmonary resuscitation and an inspiratory impedance threshold device for out-of-hospital cardiac arrest. Circulation 2003;108: Aufderheide TP, Pirrallo RG, Provo TA, Lurie KG. Clinical evaluation of an inspiratory impedance threshold device during standard cardiopulmonary resuscitation in patients with out-of-hospital cardiac arrest. Crit Care Med 2005;33: Lurie KG, Barnes TA, Zielinski TM, McKnite SH. Evaluation of a prototypic inspiratory impedance threshold valve designed to enhance the efficiency of cardiopulmonary resuscitation. Respir Care 2003;48: Lurie KG, Coffeen P, Shultz J, McKnite S, Detloff B, Mulligan K. Improving active compression decompression cardiopulmonary resuscitation with an inspiratory impedance valve. Circulation 1995;91: Lurie KG, Mulligan KA, McKnite S, Detloff B, Lindstrom P, Lindner KH. Optimizing standard cardiopulmonary resuscitation with an inspiratory impedance threshold valve. Chest 1998;113: Lurie KG, Voelckel WG, Zielinski T, et al. Improving standard cardiopulmonary resuscitation with an inspiratory impedance threshold valve in a porcine model of cardiac arrest. Anesth Analg 2001;93: Lurie KG, Zielinski T, McKnite S, Aufderheide T, Voelckel W. Use of an inspiratory impedance valve improves neurologically intact survival in a porcine model of ventricular fibrillation. Circulation 2002;105: Raedler C, Voelckel WG, Wenzel V, et al. Vasopressor response in a porcine model of hypothermic cardiac arrest is improved with active compression decompression cardiopulmonary resuscitation using the inspiratory impedance threshold valve. Anesth Analg 2002;95: Voelckel WG, Lurie KG, Zielinski T, et al. The effects of positive end-expiratory pressure during active compression decompression cardiopulmonary resuscitation with the inspiratory threshold valve. Anesth Analg 2001;92: Yannopoulos D, Aufderheide TP, Gabrielli A, et al. Clinical and hemodynamic comparison of 15:2 and 30 : 2 compression-to-ventilation ratios for cardiopulmonary resuscitation. Crit Care Med 2006;34: Mader TJ, Kellogg AR, Smith J, et al. A blinded, randomized controlled evaluation of an impedance threshold device during cardiopulmonary resuscitation in swine. Resuscitation 2008;77: Menegazzi JJ, Salcido DD, Menegazzi MT, et al. Effects of an impedance threshold device on hemodynamics and restoration of spontaneous circulation in prolonged porcine ventricular fibrillation. Prehosp Emerg Care 2007;11: Langhelle A, Stromme T, Sunde K, Wik L, Nicolaysen G, Steen PA. Inspiratory impedance threshold valve during CPR. Resuscitation 2002;52: Herff H, Raedler C, Zander R, et al. Use of an inspiratory impedance threshold valve during chest compressions without assisted ventilation may result in hypoxaemia. Resuscitation 2007;72: Plaisance P, Lurie KG, Vicaut E, et al. Evaluation of an impedance threshold device in patients receiving active compression decompression cardiopulmonary resuscitation for out of hospital cardiac arrest. Resuscitation 2004;61: Cabrini L, Beccaria P, Landoni G, et al. Impact of impedance threshold devices on cardiopulmonary resuscitation: a systematic review and meta-analysis of randomized controlled studies. Crit Care Med 2008;36: Wik L, Bircher NG, Safar P. A comparison of prolonged manual and mechanical external chest compression after cardiac arrest in dogs. Resuscitation 1996;32: Dickinson ET, Verdile VP, Schneider RM, Salluzzo RF. Effectiveness of mechanical versus manual chest compressions in out-of-hospital cardiac arrest resuscitation: a pilot study. Am J Emerg Med 1998;16: McDonald JL. Systolic and mean arterial pressures during manual and mechanical CPR in humans. Ann Emerg Med 1982;11: Ward KR, Menegazzi JJ, Zelenak RR, Sullivan RJ, McSwain Jr NE. A comparison of chest compressions between mechanical and manual CPR by monitoring endtidal PCO 2 during human cardiac arrest. Ann Emerg Med 1993; 22: Wang HC, Chiang WC, Chen SY, et al. Video-recording and time-motion analyses of manual versus mechanical cardiopulmonary resuscitation during ambulance transport. Resuscitation 2007;74: Steen S, Liao Q, Pierre L, Paskevicius A, Sjoberg T. Evaluation of LUCAS, a new device for automatic mechanical compression and active decompression resuscitation. Resuscitation 2002;55: Rubertsson S, Karlsten R. Increased cortical cerebral blood flow with LUCAS; a new device for mechanical chest compressions compared to standard external compressions during experimental cardiopulmonary resuscitation. Resuscitation 2005;65: Axelsson C, Nestin J, Svensson L, Axelsson AB, Herlitz J. Clinical consequences of the introduction of mechanical chest compression in the EMS system for treatment of out-of-hospital cardiac arrest a pilot study. Resuscitation 2006;71: Steen S, Sjoberg T, Olsson P, Young M. Treatment of out-of-hospital cardiac arrest with LUCAS, a new device for automatic mechanical compression and active decompression resuscitation. Resuscitation 2005;67: Larsen AI, Hjornevik AS, Ellingsen CL, Nilsen DW. Cardiac arrest with continuous mechanical chest compression during percutaneous coronary intervention. A report on the use of the LUCAS device. Resuscitation 2007;75: Bonnemeier H, Olivecrona G, Simonis G, et al. Automated continuous chest compression for in-hospital cardiopulmonary resuscitation of patients with pulseless electrical activity: a report of five cases. Int J Cardiol 2009;136:e Grogaard HK, Wik L, Eriksen M, Brekke M, Sunde K. Continuous mechanical chest compressions during cardiac arrest to facilitate restoration of coronary circulation with percutaneous coronary intervention. J Am Coll Cardiol 2007;50: Larsen AI, Hjornevik A, Bonarjee V, Barvik S, Melberg T, Nilsen DW. Coronary blood flow and perfusion pressure during coronary angiography in patients 4
163 162 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins 4 with ongoing mechanical chest compression: a report on 6 cases. Resuscitation 2010;81: Smekal D, Johansson J, Huzevka T, Rubertsson S. No difference in autopsy detected injuries in cardiac arrest patients treated with manual chest compressions compared with mechanical compressions with the LUCAS device a pilot study. Resuscitation 2009;80: Deakin CD, PaulV, Fall E, Petley GW, Thompson F. Ambient oxygen concentrations resulting from use of the Lund University Cardiopulmonary Assist System (LUCAS) device during simulated cardiopulmonary resuscitation. Resuscitation 2007;74: Timerman S, Cardoso LF, Ramires JA, Halperin H. Improved hemodynamic performance with a novel chest compression device during treatment of in-hospital cardiac arrest. Resuscitation 2004;61: Halperin H, Berger R, Chandra N, et al. Cardiopulmonary resuscitation with a hydraulic-pneumatic band. Crit Care Med 2000;28:N Halperin HR, Paradis N, Ornato JP, et al. Cardiopulmonary resuscitation with a novel chest compression device in a porcine model of cardiac arrest: improved hemodynamics and mechanisms. J Am Coll Cardiol 2004;44: Hallstrom A, Rea TD, Sayre MR, et al. Manual chest compression vs use of an automated chest compression device during resuscitation following out-of-hospital cardiac arrest: a randomized trial. JAMA 2006;295: Steinmetz J, Barnung S, Nielsen SL, Risom M, Rasmussen LS. Improved survival after an out-of-hospital cardiac arrest using new guidelines. Acta Anaesthesiol Scand 2008;52: Casner M, Andersen D, Isaacs SM. Preliminary report of the impact of a new CPR assist device on the rate of return of spontaneous circulation in out of hospital cardiac arrest. PreHosp Emerg Med 2005;9: Ong ME, Ornato JP, Edwards DP, et al. Use of an automated, load-distributing band chest compression device for out-of-hospital cardiac arrest resuscitation. JAMA 2006;295: Paradis N, Young G, Lemeshow S, Brewer J, Halperin H. Inhomogeneity and temporal effects in AutoPulse Assisted Prehospital International Resuscitation an exception from consent trial terminated early. Am J Emerg Med 2010;28: Tomte O, Sunde K, Lorem T, et al. Advanced life support performance with manual and mechanical chest compressions in a randomized, multicentre manikin study. Resuscitation 2009;80: Wirth S, Korner M, Treitl M, et al. Computed tomography during cardiopulmonary resuscitation using automated chest compression devices an initial study. Eur Radiol 2009;19: Holmstrom P, Boyd J, Sorsa M, Kuisma M. A case of hypothermic cardiac arrest treated with an external chest compression device (LUCAS) during transport to re-warming. Resuscitation 2005;67: Wik L, Kiil S. Use of an automatic mechanical chest compression device (LUCAS) as a bridge to establishing cardiopulmonary bypass for a patient with hypothermic cardiac arrest. Resuscitation 2005;66: Sunde K, Wik L, Steen PA. Quality of mechanical, manual standard and active compression decompression CPR on the arrest site and during transport in a manikin model. Resuscitation 1997;34: Lown B, Amarasingham R, Neuman J. New method for terminating cardiac arrhythmias. Use of synchronized capacitor discharge. JAMA 1962;182: Zipes DP, Camm AJ, Borggrefe M, et al. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death). J Am Coll Cardiol 2006;48:e Deakin CD, Morrison LJ, Morley PT, et al. International consensus on cardiopulmonary resuscitation and emergency cardiovascular care science with treatment recommendations. Part 8: advanced life support. Resuscitation; 2010:81 (Supl. 1):e Manz M, Pfeiffer D, Jung W, Lueritz B. Intravenous treatment with magnesium in recurrent persistent ventricular tachycardia. New Trends Arrhythmias 1991;7: Tzivoni D, Banai S, Schuger C, et al. Treatment of torsade de pointes with magnesium sulfate. Circulation 1988;77: Delacretaz E. Clinical practice. Supraventricular tachycardia. N Engl J Med 2006;354: DiMarco JP, Miles W, Akhtar M, et al. Adenosine for paroxysmal supraventricular tachycardia: dose ranging and comparison with verapamil: assessment in placebo-controlled, multicenter trials. The Adenosine for PSVT Study Group [published correction appears in Ann Intern Med. 1990; 113:996]. Ann Intern Med 1990;113: Fuster V, Ryden LE, Cannom DS, et al. ACC/AHA/ESC 2006 guidelines for the management of patients with atrial fibrillation: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Revise the 2001 Guidelines for the Management of Patients With Atrial Fibrillation): developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. Circulation 2006;114:e Sticherling C, Tada H, Hsu W, et al. Effects of diltiazem and esmolol on cycle length and spontaneous conversion of a trial fibrillation. J Cardiovasc Pharmacol Ther 2002;7: Shettigar UR, Toole JG, Appunn DO. Combined use of esmolol and digoxin in the acute treatment of atrial fibrillation or flutter. Am Heart J 1993;126: Demircan C, Cikriklar HI, Engindeniz Z, et al. Comparison of the effectiveness of intravenous diltiazem and metoprolol in the management of rapid ventricular rate in atrial fibrillation. Emerg Med J 2005;22: Wattanasuwan N, Khan IA, Mehta NJ, et al. Acute ventricular rate control in atrial fibrillation: IV combination of diltiazem and digoxin vs. IV diltiazem alone. Chest 2001;119: Davey MJ, Teubner D. A randomized controlled trial of magnesium sulfate, in addition to usual care, for rate control in atrial fibrillation. Ann Emerg Med 2005;45: Chiladakis JA, Stathopoulos C, Davlouros P, Manolis AS. Intravenous magnesium sulfate versus diltiazem in paroxysmal atrial fibrillation. Int J Cardiol 2001;79: Dauchot P, Gravenstein JS. Effects of atropine on the electrocardiogram in different age groups. Clin Pharmacol Ther 1971;12: Chamberlain DA, Turner P, Sneddon JM. Effects of atropine on heart-rate in healthy man. Lancet 1967;2: Bernheim A, Fatio R, Kiowski W, Weilenmann D, Rickli H, Rocca HP. Atropine often results in complete atrioventricular block or sinus arrest after cardiac transplantation: an unpredictable and dose-independent phenomenon. Transplantation 2004;77: Klumbies A, Paliege R, Volkmann H. Mechanical emergency stimulation in asystole and extreme bradycardia. Z Gesamte Inn Med 1988;43: Zeh E, Rahner E. The manual extrathoracal stimulation of the heart. Technique and effect of the precordial thump (author s transl). Z Kardiol 1978;67: Chan L, Reid C, Taylor B. Effect of three emergency pacing modalities on cardiac output in cardiac arrest due to ventricular asystole. Resuscitation 2002;52: Camm AJ, Garratt CJ. Adenosine and supraventricular tachycardia. N Engl J Med 1991;325: Wang HE, O Connor RE, Megargel RE, et al. The use of diltiazem for treating rapid atrial fibrillation in the out-of-hospital setting. Ann Emerg Med 2001;37: Martinez-Marcos FJ, Garcia-Garmendia JL, Ortega-Carpio A, Fernandez-Gomez JM, Santos JM, Camacho C. Comparison of intravenous flecainide, propafenone, and amiodarone for conversion of acute atrial fibrillation to sinus rhythm. Am J Cardiol 2000;86: Kalus JS, Spencer AP, Tsikouris JP, et al. Impact of prophylactic iv magnesium on the efficacy of ibutilide for conversion of atrial fibrillation or flutter. Am J Health Syst Pharm 2003;60: Nolan JP, Neumar RW, Adrie C, et al. Post-cardiac arrest syndrome: epidemiology, pathophysiology, treatment, and prognostication. A Scientific Statement from the International Liaison Committee on Resuscitation; the American Heart Association Emergency Cardiovascular Care Committee; the Council on Cardiovascular Surgery and Anesthesia; the Councilon Cardiopulmonary, Perioperative, and Critical Care; the Council on Clinical Cardiology; the Council on Stroke. Resuscitation 2008;79: Sunde K, Pytte M, Jacobsen D, et al. Implementation of a standardised treatment protocol for post resuscitation care after out-of-hospital cardiac arrest. Resuscitation 2007;73: Gaieski DF, Band RA, Abella BS, et al. Early goal-directed hemodynamic optimization combined with therapeutic hypothermia in comatose survivors of out- -of-hospital cardiac arrest. Resuscitation 2009;80: Carr BG, Goyal M, Band RA, et al. A national analysis of the relationship between hospital factors and post-cardiac arrest mortality. Intensive Care Med 2009;35: Oddo M, Schaller MD, Feihl F, Ribordy V, Liaudet L. From evidence to clinical practice: effective implementation of therapeutic hypothermia to improve patient outcome after cardiac arrest. Crit Care Med 2006;34: Knafelj R, Radsel P, Ploj T, Noc M. Primary percutaneous coronary intervention and mild induced hypothermia in comatose survivors of ventricular fibrillation with ST-elevation acute myocardial infarction. Resuscitation 2007;74: Nolan JP, Laver SR, Welch CA, Harrison DA, Gupta V, Rowan K. Outcome following admission to UK intensive care units after cardiac arrest: a secondary analysis of the ICNARC Case Mix Programme Database. Anaesthesia 2007;62: Keenan SP, Dodek P, Martin C, Priestap F, Norena M, Wong H. Variation in length of intensive care unit stay after cardiac arrest: where you are is as important as who you are. Crit Care Med 2007;35: Carr BG, Kahn JM, Merchant RM, Kramer AA, Neumar RW. Inter-hospital variability in post-cardiac arrest mortality. Resuscitation 2009;80: Niskanen M, Reinikainen M, Kurola J. Outcome from intensive care after cardiac arrest: comparison between two patient samples treated in and in Finnish ICUs. Acta Anaesthesiol Scand 2007;51: Hovdenes J, Laake JH, Aaberge L, Haugaa H, Bugge JF. Therapeutic hypothermia after out-of-hospital cardiac arrest: experiences with patients treated with percutaneous coronary intervention and cardiogenic shock. Acta Anaesthesiol Scand 2007;51: Soar J, Mancini ME, Bhanji F, et al International consensus on cardiopulmonary resuscitation and emergency cardiovascular care science with treatment recommendations. Part 12: education, implementation, and teams. Resuscitation; 2010:81 (Supl. 1):e Laver S, Farrow C, Turner D, Nolan J. Mode of death after admission to an intensive care unit following cardiac arrest. Intensive Care Med 2004;30 :
164 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Laurent I, Monchi M, Chiche JD, et al. Reversible myocardial dysfunction in survivors of out-of-hospital cardiac arrest. J Am Coll Cardiol 2002;40: Ruiz-Bailen M, Aguayo de Hoyos E, Ruiz-Navarro S, et al. Reversible myocardial dysfunction after cardiopulmonary resuscitation. Resuscitation 2005; 66: Cerchiari EL, Safar P, Klein E, Diven W. Visceral, hematologic and bacteriologic changes and neurologic outcome after cardiac arrest in dogs. The visceral post-resuscitation syndrome. Resuscitation 1993;25: Adrie C, Monchi M, Laurent I, et al. Coagulopathy after successful cardiopulmonary resuscitation following cardiac arrest: implication of the protein C anticoagulant pathway. J Am Coll Cardiol 2005;46: Adrie C, Adib-Conquy M, Laurent I, et al. Successful cardiopulmonary resuscitation after cardiac arrest as a sepsis-like syndrome. Circulation 2002;106: Adrie C, Laurent I, Monchi M, Cariou A, Dhainaou JF, Spaulding C. Postresuscitation disease after cardiac arrest: a sepsis-like syndrome? Curr Opin Crit Care 2004;10: Zwemer CF, Whitesall SE, D Alecy LG. Cardiopulmonary-cerebral resuscitation with 100% oxygen exacerbates neurological dysfunction following nine minutes of normothermic cardiac arrest in dogs. Resuscitation 1994;27: Richards EM, Fiskum G, Rosenthal RE, Hopkins I, McKenna MC. Hyperoxic reperfusion after global ischemia decreases hippocampal energy metabolism. Stroke 2007;38: Vereczki V, Martin E, Rosenthal RE, Hof PR, Hoffman GE, Fiskum G. Normoxic resuscitation after cardiac arrest protects against hippocampal oxidative stress, metabolic dysfunction, and neuronal death. J Cereb Blood Flow Metab 2006;26: Liu Y, Rosenthal RE, Haywood Y, Miljkovic-Lolic M, Vanderhoek JY, Fiskum G. Normoxic ventilation after cardiac arrest reduces oxidation of brain lipids and improves neurological outcome. Stroke 1998;29: Menon DK, Coles JP, Gupta AK, et al. Diffusion limited oxygen delivery following head injury. Crit Care Med 2004;32: Buunk G, van der Hoeven JG, Meinders AE. Cerebrovascular reactivity in comatose patients resuscitated from a cardiac arrest. Stroke 1997;28: Buunk G, van der Hoeven JG, Meinders AE. A comparison of near-infrared spectroscopy and jugular bulb oximetry in comatose patients resuscitated from a cardiac arrest. Anaesthesia 1998;53: Roine RO, Launes J, Nikkinen P, Lindroth L, Kaste M. Regional cerebral blood flow after human cardiac arrest. A hexamethylpropyleneamine oxime single photon emission computed tomographic study. Arch Neurol 1991;48: Beckstead JE, Tweed WA, Lee J, MacKeen WL. Cerebral blood flow and metabolism in man following cardiac arrest. Stroke 1978;9: Zheng ZJ, Croft JB, Giles WH, Mensah GA. Sudden cardiac death in the United States, 1989 to Circulation 2001;104: Pell JP, Sirel JM, Marsden AK, Ford I, Walker NL, Cobbe SM. Presentation, management, and outcome of out of hospital cardiopulmonary arrest: comparison by underlying aetiology. Heart 2003;89: Zipes DP, Wellens HJ. Sudden cardiac death. Circulation 1998;98: Spaulding CM, Joly LM, Rosenberg A, et al. Immediate coronary angiography in survivors of out-of-hospital cardiac arrest. N Engl J Med 1997;336: Bendz B, Eritsland J, Nakstad AR, et al. Long-term prognosis after out-of-hospital cardiac arrest and primary percutaneous coronary intervention. Resuscitation 2004;63: Keelan PC, Bunch TJ, White RD, Packer DL, Holmes Jr DR. Early direct coronary angioplasty in survivors of out-of-hospital cardiac arrest. Am J Cardiol 2003;91: A Quintero-Moran B, Moreno R, Villarreal S, et al. Percutaneous coronary intervention for cardiac arrest secondary to ST-elevation acute myocardial infarction. Influence of immediate paramedical/medical assistance on clinical outcome. J Invasive Cardiol 2006;18: Garot P, Lefevre T, Eltchaninoff H, et al. Six-month outcome of emergency percutaneous coronary intervention in resuscitated patients after cardiac arrest complicating ST-elevation myocardial infarction. Circulation 2007;115: Nagao K, Hayashi N, Kanmatsuse K, et al. Cardiopulmonary cerebral resuscitation using emergency cardiopulmonary bypass, coronary reperfusion therapy and mild hypothermia in patients with cardiac arrest outside the hospital. J Am Coll Cardiol 2000;36: Nielsen N, Hovdenes J, Nilsson F, et al. Outcome, timing and adverse events in therapeutic hypothermia after out-of-hospital cardiac arrest. Acta Anaesthesiol Scand 2009;53: Wolfrum S, Pierau C, Radke PW, Schunkert H, Kurowski V. Mild therapeutic hypothermia in patients after out-of-hospital cardiac arrest due to acute ST-segment elevation myocardial infarction undergoing immediate percutaneous coronary intervention. Crit Care Med 2008;36: Rivers E, Nguyen B, Havstad S, et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med 2001;345: Mullner M, Sterz F, Binder M, et al. Arterial blood pressure after human cardiac arrest and neurological recovery. Stroke 1996;27: a. Trzeciak S, Jones AE, Kilgannon JH, et al. Significance of arterial hypotension after resuscitation from cardiac arrest. Crit Care Med 2009;37: Bernard SA, Gray TW, Buist MD, et al. Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia. N Engl J Med 2002;346: Angelos MG, Ward KR, Hobson J, Beckley PD. Organ blood flow following cardiac arrest in a swine low-flow cardiopulmonary bypass model. Resuscitation 1994;27: Sakabe T, Tateishi A, Miyauchi Y, et al. Intracranial pressure following cardiopulmonary resuscitation. Intensive Care Med 1987;13: Morimoto Y, Kemmotsu O, Kitami K, Matsubara I, Tedo I. Acute brain swelling after out-of-hospital cardiac arrest: pathogenesis and outcome. Crit Care Med 1993;21: Nishizawa H, Kudoh I. Cerebral autoregulation is impaired in patients resuscitated after cardiac arrest. Acta Anaesthesiol Scand 1996;40: Sundgreen C, Larsen FS, Herzog TM, Knudsen GM, Boesgaard S, Aldershvile J. Autoregulation of cerebral blood flow in patients resuscitated from cardiac arrest. Stroke 2001;32: Ely EW, Truman B, Shintani A, et al. Monitoring sedation status over time in ICU patients: reliability and validity of the Richmond Agitation-Sedation Scale (RASS). JAMA 2003;289: De Jonghe B, Cook D, Appere-De-Vecchi C, Guyatt G, Meade M, Outin H. Using and understanding sedation scoring systems: a systematic review. Intensive Care Med 2000;26: Snyder BD, Hauser WA, Loewenson RB, Leppik IE, Ramirez-Lassepas M, Gum-nit RJ. Neurologic prognosis after cardiopulmonary arrest. III: seizure activity. Neurology 1980;30: Levy DE, Caronna JJ, Singer BH, Lapinski RH, Frydman H, Plum F. Predicting outcome from hypoxic ischemic coma. JAMA 1985;253: Krumholz A, Stern BJ, Weiss HD. Outcome from coma after cardiopulmonary resuscitation: relation to seizures and myoclonus. Neurology 1988;38: Zandbergen EG, Hijdra A, Koelman JH, et al. Prediction of poor outcome within the first 3 days of postanoxic coma. Neurology 2006;66: Ingvar M. Cerebral blood flow and metabolic rate during seizures. Relationship to epileptic brain damage. Ann NY Acad Sci 1986;462: Caviness JN, Brown P. Myoclonus: current concepts and recent advances. Lancet Neurol 2004;3: Losert H, Sterz F, Roine RO, et al. Strict normoglycaemic blood glucose levels in the therapeutic management of patients within 12 h after cardiac arrest might not be necessary. Resuscitation Skrifvars MB, Saarinen K, Ikola K, Kuisma M. Improved survival after in-hospital cardiac arrest outside critical care areas. Acta Anaesthesiol Scand 2005;49: van den Berghe G, Wouters P, Weekers F, et al. Intensive insulin therapy in the critically ill patients. N Engl J Med 2001;345: Van den Berghe G, Wilmer A, Hermans G, et al. Intensive insulin therapy in the medical ICU. N Engl J Med 2006;354: Oksanen T, Skrifvars MB, Varpula T, et al. Strict versus moderate glucose control after resuscitation from ventricular fibrillation. Intensive Care Med 2007;33: Finfer S, Chittock DR, Su SY, et al. Intensive versus conventional glucose control in critically ill patients. N Engl J Med 2009;360: Preiser JC, Devos P, Ruiz-Santana S, et al. A prospective randomised multi-centre controlled trial on tight glucose control by intensive insulin therapy in adult intensive care units: the Glucontrol study. Intensive Care Med 2009;35: Griesdale DE, de Souza RJ, van Dam RM, et al. Intensive insulin therapy and mortality among critically ill patients: a meta-analysis including NICE-SUGAR study data. CMAJ 2009;180: Wiener RS, Wiener DC, Larson RJ. Benefits and risks of tight glucose control in critically ill adults: a meta-analysis. JAMA 2008;300: Krinsley JS, Grover A. Severe hypoglycemia in critically ill patients: risk factors and outcomes. Crit Care Med 2007;35: Meyfroidt G, Keenan DM, Wang X, Wouters PJ, Veldhuis JD, Van den Berghe G. Dynamic characteristics of blood glucose time series during the course of critical illness: effects of intensive insulin therapy and relative association with mortality. Crit Care Med 2010;38: Padkin A. Glucose control after cardiac arrest. Resuscitation 2009;80: Takino M, Okada Y. Hyperthermia following cardiopulmonary resuscitation. Intensive Care Med 1991;17: Hickey RW, Kochanek PM, Ferimer H, Alexander HL, Garman RH, Graham SH. Induced hyperthermia exacerbates neurologic neuronal histologic damage after asphyxial cardiac arrest in rats. Crit Care Med 2003;31: Takasu A, Saitoh D, Kaneko N, Sakamoto T, Okada Y. Hyperthermia: is it an ominous sign after cardiac arrest? Resuscitation 2001;49: Zeiner A, Holzer M, Sterz F, et al. Hyperthermia after cardiac arrest is associated with an unfavorable neurologic outcome. Arch Intern Med 2001;161: Hickey RW, Kochanek PM, Ferimer H, Graham SH, Safar P. Hypothermia and hyperthermia in children after resuscitation from cardiac arrest. Pediatrics 2000;106: Diringer MN, Reaven NL, Funk SE, Uman GC. Elevated body temperature independently contributes to increased length of stay in neurologic intensive care unit patients. Crit Care Med 2004;32: Gunn AJ, Thoresen M. Hypothermic neuroprotection. NeuroRx 2006;3: Froehler MT, Geocadin RG. Hypothermia for neuroprotection after cardiac arrest: mechanisms, clinical trials and patient care. J Neurol Sci 2007;261: McCullough JN, Zhang N, Reich DL, et al. Cerebral metabolic suppression during hypothermic circulatory arrest in humans. Ann Thorac Surg 1999;67: [discussion ] Mild therapeutic hypothermia to improve the neurologic outcome after cardiac arrest. N Engl J Med 2002;346: Belliard G, Catez E, Charron C, et al. Efficacy of therapeutic hypothermia after out-of-hospital cardiac arrest due to ventricular fibrillation. Resuscitation 2007;75:
165 164 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins Castrejon S, Cortes M, Salto ML, et al. Improved prognosis after using mild hypothermia to treat cardiorespiratory arrest due to a cardiac cause: comparison with a control group. Rev Esp Cardiol 2009;62: Bro-Jeppesen J, Kjaergaard J, Horsted TI, et al. The impact of therapeutic hypothermia on neurological function and quality of life after cardiac arrest. Resuscitation 2009;80: Hachimi-Idrissi S, Corne L, Ebinger G, Michotte Y, Huyghens L. Mild hypothermia induced by a helmet device: a clinical feasibility study. Resuscitation 2001;51: Bernard SA, Jones BM, Horne MK. Clinical trial of induced hypothermia in comatose survivors of out-of-hospital cardiac arrest. Ann Emerg Med 1997;30: Busch M, Soreide E, Lossius HM, Lexow K, Dickstein K. Rapid implementation of therapeutic hypothermia in comatose out-of-hospital cardiac arrest survivors. Acta Anaesthesiol Scand 2006;50: Storm C, Steffen I, Schefold JC, et al. Mild therapeutic hypothermia shortens intensive care unit stay of survivors after out-of-hospital cardiac arrest compared to historical controls. Crit Care 2008;12:R Don CW, Longstreth Jr WT, Maynard C, et al. Active surface cooling protocol to induce mild therapeutic hypothermia after out-of-hospital cardiac arrest: a retrospective before-and-after comparison in a single hospital. Crit Care Med 2009;37: Arrich J. Clinical application of mild therapeutic hypothermia after cardiac arrest. Crit Care Med 2007;35: Holzer M, Mullner M, Sterz F, et al. Efficacy and safety of endovascular cooling after cardiac arrest: cohort study and Bayesian approach. Stroke 2006;37: Polderman KH, Herold I. Therapeutic hypothermia and controlled normothermia in the intensive care unit: practical considerations, side effects, and cooling methods. Crit Care Med 2009;37: Bernard S, Buist M, Monteiro O, Smith K. Induced hypothermia using large volume, ice-cold intravenous fluid in comatose survivors of out-of-hospital cardiac arrest: a preliminary report. Resuscitation 2003;56: Virkkunen I, Yli-Hankala A, Silfvast T. Induction of therapeutic hypothermia after cardiac arrest in prehospital patients using ice-cold Ringer s solution: a pilot study. Resuscitation 2004;62: Kliegel A, Losert H, Sterz F, et al. Cold simple intravenous infusions preceding special endovascular cooling for faster induction of mild hypothermia after cardiac arrest a feasibility study. Resuscitation 2005;64: Kliegel A, Janata A, Wandaller C, et al. Cold infusions alone are effective for induction of therapeutic hypothermia but do not keep patients cool after cardiac arrest. Resuscitation 2007;73: Kilgannon JH, Roberts BW, Stauss M, et al. Use of a standardized order set for achieving target temperature in the implementation of therapeutic hypothermia after cardiac arrest: a feasibility study. Acad Emerg Med 2008;15: Scott BD, Hogue T, Fixley MS, Adamson PB. Induced hypothermia following out-of-hospital cardiac arrest; initial experience in a community hospital. Clin Cardiol 2006;29: Kim F, Olsufka M, Carlbom D, et al. Pilot study of rapid infusion of 2 L of 4 degrees C normal saline for induction of mild hypothermia in hospitalized, comatose survivors of out-of-hospital cardiac arrest. Circulation 2005;112: Jacobshagen C, Pax A, Unsold BW, et al. Effects of large volume, ice-cold intravenous fluid infusion on respiratory function in cardiac arrest survivors. Resuscitation 2009;80: Spiel AO, Kliegel A, Janata A, et al. Hemostasis in cardiac arrest patients treated with mild hypothermia initiated by cold fluids. Resuscitation 2009;80: Larsson IM, Wallin E, Rubertsson S. Cold saline infusion and ice packs alone are effective in inducing and maintaining therapeutic hypothermia after cardiac arrest. Resuscitation 2010;81: Skulec R, Kovarnik T, Dostalova G, Kolar J, Linhart A. Induction of mild hypothermia in cardiac arrest survivors presenting with cardiogenic shock syndrome. Acta Anaesthesiol Scand 2008;52: Hoedemaekers CW, Ezzahti M, Gerritsen A, van der Hoeven JG. Comparison of cooling methods to induce and maintain normo-and hypothermia in intensive care unit patients: a prospective intervention study. Crit Care 2007;11:R Kim F, Olsufka M, Longstreth Jr WT, et al. Pilot randomized clinical trial of prehospital induction of mild hypothermia in out-of-hospital cardiac arrest patients with a rapid infusion of 4 degrees C normal saline. Circulation 2007;115: Kamarainen A, Virkkunen I, Tenhunen J, Yli-Hankala A, Silfvast T. Prehospital therapeutic hypothermia for comatose survivors of cardiac arrest: a randomized controlled trial. Acta Anaesthesiol Scand 2009;53: Kamarainen A, Virkkunen I, Tenhunen J, Yli-Hankala A, Silfvast T. Induction of therapeutic hypothermia during prehospital CPR using ice-cold intravenous fluid. Resuscitation 2008;79: Hammer L, Vitrat F, Savary D, et al. Immediate prehospital hypothermia protocol in comatose survivors of out-of-hospital cardiac arrest. Am J Emerg Med 2009;27: Aberle J, Kluge S, Prohl J, et al. Hypothermia after CPR through conduction and convection initial experience on an ICU. Intensivmed Notfallmed 2006;43: Feuchtl A, Gockel B, Lawrenz T, Bartelsmeier M, Stellbrink C. Endovascular cooling improves neurological short-term outcome after prehospital cardiac arrest. Intensivmedizin 2007;44: Fries M, Stoppe C, Brucken D, Rossaint R, Kuhlen R. Influence of mild therapeutic hypothermia on the inflammatory response after successful resuscitation from cardiac arrest. J Crit Care 2009;24: Benson DW, Williams Jr GR, Spencer FC, Yates AJ. The use of hypothermia after cardiac arrest. Anesth Analg 1959;38: Yanagawa Y, Ishihara S, Norio H, et al. Preliminary clinical outcome study of mild resuscitative hypothermia after out-of-hospital cardiopulmonary arrest. Resuscitation 1998;39: Damian MS, Ellenberg D, Gildemeister R, et al. Coenzyme Q10 combined with mild hypothermia after cardiac arrest: a preliminary study. Circulation 2004;110: Hay AW, Swann DG, Bell K, Walsh TS, Cook B. Therapeutic hypothermia in comatose patients after out-of-hospital cardiac arrest. Anaesthesia 2008;63: Zeiner A, Holzer M, Sterz F, et al. Mild resuscitative hypothermia to improve neurological outcome after cardiac arrest. A clinical feasibility trial. Hypothermia After Cardiac Arrest (HACA) Study Group. Stroke 2000;31: Uray T, Malzer R. Out-of-hospital surface cooling to induce mild hypothermia in human cardiac arrest: a feasibility trial. Resuscitation 2008;77: a. Castren M, Nordberg P, Svensson L, et al. Intra-arrest transnasal evaporative cooling: a randomized, prehospital, multicenter study (PRINCE: Pre-ROSC IntraNasal Cooling Effectiveness). Circulation 2010;122: Felberg RA, Krieger DW, Chuang R, et al. Hypothermia after cardiac arrest: feasibility and safety of an external cooling protocol. Circulation 2001;104: Flint AC, Hemphill JC, Bonovich DC. Therapeutic hypothermia after cardiac arrest: performance characteristics and safety of surface cooling with or without endovascular cooling. Neurocrit Care 2007;7: Heard KJ, Peberdy MA, Sayre MR, et al. A randomized controlled trial comparing the Arctic Sun to standard cooling for induction of hypothermia after cardiac arrest. Resuscitation 2010;81: Merchant RM, Abella BS, Peberdy MA, et al. Therapeutic hypothermia after cardiac arrest: unintentional overcooling is common using ice packs and conventional cooling blankets. Crit Care Med 2006;34:S Haugk M, Sterz F, Grassberger M, et al. Feasibility and efficacy of a new noninvasive surface cooling device in post-resuscitation intensive care medicine. Resuscitation 2007;75: Al-Senani FM, Graffagnino C, Grotta JC, et al. A prospective, multicenter pilot study to evaluate the feasibility and safety of using the CoolGard System and Icy catheter following cardiac arrest. Resuscitation 2004;62: Pichon N, Amiel JB, Francois B, Dugard A, Etchecopar C, Vignon P. Efficacy of and tolerance to mild induced hypothermia after out-of-hospital cardiac arrest using an endovascular cooling system. Crit Care 2007;11:R Wolff B, Machill K, Schumacher D, Schulzki I, Werner D. Early achievement of mild therapeutic hypothermia and the neurologic outcome after cardiac arrest. Int J Cardiol 2009;133: Nagao K, Kikushima K, Watanabe K, et al. Early induction of hypothermia during cardiac arrest improves neurological outcomes in patients with out-of-hospital cardiac arrest who undergo emergency cardiopulmonary bypass and percutaneous coronary intervention. Circ J 2010;74: Mahmood MA, Zweifier RM. Progress in shivering control. J Neurol Sci 2007;261: Wadhwa A, Sengupta P, Durrani J, et al. Magnesium sulphate only slightly reduces the shivering threshold in humans. Br J Anaesth 2005;94: Kuboyama K, Safar P, Radovsky A, et al. Delay in cooling negates the beneficial effect of mild resuscitative cerebral hypothermia after cardia arrest in dogs: a prospective, randomized study. Crit Care Med 1993;21: Riter HG, Brooks LA, Pretorius AM, Ackermann LW, Kerber RE. Intra-arrest hypothermia: both cold liquid ventilation with perfluorocarbons and cold intravenous saline rapidly achieve hypothermia, but only cold liquid ventilation improves resumption of spontaneous circulation. Resuscitation 2009;80: Staffey KS, Dendi R, Brooks LA, et al. Liquid ventilation with perfluorocarbons facilitates resumption of spontaneous circulation in a swine cardiac arrest model. Resuscitation 2008;78: Polderman KH, Peerdeman SM, Girbes AR. Hypophosphatemia and hypomagnesemia induced by cooling in patients with severe head injury. J Neurosurg 2001;94: Tortorici MA, Kochanek PM, Poloyac SM. Effects of hypothermia on drug disposition, metabolism, and response: a focus of hypothermia-mediated alterations on the cytochrome P450 enzyme system. Crit Care Med 2007;35: Randomized clinical study of thiopental loading in comatose survivors of cardiac arrest. Brain Resuscitation Clinical Trial I Study Group. N Engl J Med 1986;314: Grafton ST, Longstreth Jr WT. Steroids after cardiac arrest: a retrospective study with concurrent, nonrandomized controls. Neurology 1988;38: Mentzelopoulos SD, Zakynthinos SG, Tzou. M, et al. Vasopressin, epinephrine, and corticosteroids for in-hospital cardiac arrest. Arch Intern Med 2009;169: Gueugniaud PY, Gaussorgues P, Garcia-Darennes F, et al. Early effects of nimodipine on intracranial and cerebral perfusion pressures in cerebral anoxia after out-of-hospital cardiac arrest. Resuscitation 1990;20: Roine RO, Kaste M, Kinnunen A, Nikki P, Sarna S, Kajaste S. Nimodipine after resuscitation from out-of-hospital ventricular fibrillation: a placebo-controlled, double-blind, randomized trial. JAMA 1990;264: A randomized clinical study of a calcium-entry blocker (lidoflazine) in the treatment of comatose survivors of cardiac arrest. Brain Resuscitation Clinical Trial II Study Group. N Engl J Med 1991;324:
166 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Laurent I, Adrie C, Vinsonneau C, et al. High-volume hemofiltration after out- -of-hospital cardiac arrest: a randomized study. J Am Coll Cardiol 2005;46: Edgren E, Hedstrand U, Nordin M, Rydin E, Ronquist G. Prediction of outcome after cardiac arrest. Crit Care Med 1987;15: Young GB, Doig G, Ragazzoni A. Anoxic-ischemic encephalopathy: clinical and electrophysiological associations with outcome. Neurocrit Care 2005;2: Al Thenayan E, Savard M, Sharpe M, Norton L, Young B. Predictors of poor neurologic outcome after induced mild hypothermia following cardiac arrest. Neurology 2008;71: Wijdicks EF, Parisi JE, Sharbrough FW. Prognostic value of myoclonus status in comatose survivors of cardiac arrest. Ann Neurol 1994;35: Thomke F, Marx JJ, Sauer O, et al. Observations on comatose survivors of cardiopulmonary resuscitation with generalized myoclonus. BMC Neurol 2005;5: Arnoldus EP, Lammers GJ. Postanoxic coma: good recovery despite myoclonus status. Ann Neurol 1995;38: Celesia GG, Grigg MM, Ross E. Generalized status myoclonicus in acute anoxic and toxic-metabolic encephalopathies. Arch Neurol 1988;45: Morris HR, Howard RS, Brown P. Early myoclonic status and outcome after cardiorespiratory arrest. J Neurol Neurosurg Psychiatry 1998;64: Datta S, Hart GK, Opdam H, Gutteridge G, Archer J. Post-hypoxic myoclonic status: the prognosis is not always hopeless. Crit Care Resusc 2009;11: English WA, Giffin NJ, Nolan JP. Myoclonus after cardiac arrest: pitfalls in diagnosis and prognosis. Anaesthesia 2009;64: Wijdicks EF, Hijdra A, Young GB, Bassetti CL, Wiebe S. Practice parameter: prediction of outcome in comatose survivors after cardiopulmonary resuscitation (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2006;67: Zandbergen EG, de Haan RJ, Hijdra A. Systematic review of prediction of poor outcome in anoxic ischaemic coma with biochemical markers of brain damage. Intensive Care Med 2001;27: Grubb NR, Simpson C, Sherwood R, et al. Prediction of cognitive dysfunction after resuscitation from out-of-hospital cardiac arrest using serum neuron-specific enolase and protein S-100. Heart Martens P. Serum neuron-specific enolase as a prognostic marker for irreversible brain damage in comatose cardiac arrest survivors. Acad Emerg Med 1996;3: Meynaar IA, Straaten HM, van der Wetering J, et al. Serum neuron-specific enolase predicts outcome in post-anoxic coma: a prospective cohort study. Intensive Care Med 2003;29: Rech TH, Vieira SR, Nagel F, Brauner JS, Scalco R. Serum neuron-specific enolase as early predictor of outcome after in-hospital cardiac arrest: a cohort study. Crit Care 2006;10:R Reisinger J, Hollinger K, Lang W, et al. Prediction of neurological outcome after cardiopulmonary resuscitation by serial determination of serum neuron-specific enolase. Eur Heart J 2007;28: Schoerkhuber W, Kittler H, Sterz F, et al. Time course of serum neuron-specific enolase. A predictor of neurological outcome in patients resuscitated from cardiac arrest. Stroke 1999;30: Bottiger BW, Mobes S, Glatzer R, et al. Astroglial protein S-100 is an early and sensitive marker of hypoxic brain damage and outcome after cardiac arrest in humans. Circulation 2001;103: Fogel W, Krieger D, Veith M, et al. Serum neuron-specific enolase as early predictor of outcome after cardiac arrest. Crit Care Med 1997;25: Martens P, Raabe A, Johnsson P. Serum S-100 and neuron-specific enolase for prediction of regaining consciousness after global cerebral ischemia. Stroke 1998;29: Prohl J, Rother J, Kluge S, et al. Prediction of short-term and long-term outcomes after cardiac arrest: a prospective multivariate approach combining biochemical, clinical, electrophysiological, and neuropsychological investigations. Crit Care Med 2007;35: Stelzl T, von Bose MJ, Hogl B, Fuchs HH, Flugel KA. A comparison of the prognostic value of neuron-specific enolase serum levels and somatosensory evoked potentials in 13 reanimated patients. Eur J Emerg Med 1995;2: Tiainen M, Roine RO, Pettila V, Takkunen O. Serum neuron-specific enolase and S-100B protein in cardiac arrest patients treated with hypothermia. Stroke 2003;34: Pfeifer R, Borner A, Krack A, Sigusch HH, Surber R, Figulla HR. Outcome after cardiac arrest: predictive values and limitations of the neuroproteins neuronspecific enolase and protein S-100 and the Glasgow Coma Scale. Resuscitation 2005;65: Roine RO, Somer H, Kaste M, Viinikka L, Karonen SL. Neurological outcome after out-of-hospital cardiac arrest. Prediction by cerebrospinal fluid enzyme analysis. Arch Neurol 1989;46: Zingler VC, Krumm B, Bertsch T, Fassbender K, Pohlmann-Eden B. Early prediction of neurological outcome after cardiopulmonary resuscitation: a multimodal approach combining neurobiochemical and electrophysiological investigations may provide high prognostic certainty in patients after cardiac arrest. Eur Neurol 2003;49: Rosen H, Sunnerhagen KS, Herlitz J, Blomstrand C, Rosengren L. Serum levels of the brain-derived proteins S-100 and NSE predict long-term outcome after cardiac arrest. Resuscitation 2001;49: Dauberschmidt R, Zinsmeyer J, Mrochen H, Meyer M. Changes of neuron-specific enolase concentration in plasma after cardiac arrest and resuscitation. Mol Chem Neuropathol 1991;14: Mussack T, Biberthaler P, Kanz KG, et al. Serum S-100B and interleukin-8 as predictive markers for comparative neurologic outcome analysis of patients after cardiac arrest and severe traumatic brain injury. Crit Care Med 2002;30 : Fries M, Kunz D, Gressner AM, Rossaint R, Kuhlen R. Procalcitonin serum levels after out-of-hospital cardiac arrest. Resuscitation 2003;59: Hachimi-Idrissi S, Van der Auwera M, Schiettecatte J, Ebinger G, Michotte Y, Huyghens L. S-100 protein as early predictor of regaining consciousness after out of hospital cardiac arrest. Resuscitation 2002;53: Piazza O, Cotena S, Esposito G, De Robertis E, Tufano R. S100B is a sensitive but not specific prognostic index in comatose patients after cardiac arrest. Minerva Chir 2005;60: Rosen H, Rosengren L, Herlitz J, Blomstrand C. Increased serum levels of the S-100 protein are associated with hypoxic brain damage after cardiac arrest. Stroke 1998;29: Mussack T, Biberthaler P, Kanz KG, Wiedemann E, Gippner-Steppert C, Jochum M. S-100b, se-selectin, and sp-selectin for evaluation of hypoxic brain damage in patients after cardiopulmonary resuscitation: pilot study. World J Surg 2001;25: [discussion 44] Sodeck GH, Domanovits H, Sterz F, et al. Can brain natriuretic peptide predict outcome after cardiac arrest? An observational study. Resuscitation 2007;74: Geppert A, Zorn G, Delle-Karth G, et al. Plasma concentrations of von Willebrand factor and intracellular adhesion molecule-1 for prediction of outcome after successful cardiopulmonary resuscitation. Crit Care Med 2003;31: Adib-Conquy M, Monchi M, Goulenok C, et al. Increased plasma levels of soluble triggering receptor expressed on myeloid cells 1 and procalcitonin after cardiac surgery and cardiac arrest without infection. Shock 2007;28: Longstreth Jr WT, Clayson KJ, Chandler WL, Sumi SM. Cerebrospinal fluid creatine kinase activity and neurologic recovery after cardiac arrest. Neurology 1984;34: Karkela J, Pasanen M, Kaukinen S, Morsky P, Harmoinen A. Evaluation of hypoxic brain injury with spinal fluid enzymes, lactate, and pyruvate. Crit Care Med 1992;20: Rothstein T, Thomas E, Sumi S. Predicting outcome in hypoxic-ischemic coma. A prospective clinical and electrophysiological study. Electroencephalogr Clin Neurophysiol 1991;79: Sherman AL, Tirschwell DL, Micklesen PJ, Longstreth Jr WT, Robinson LR. Somatosensory potentials. CSF creatine kinase BB activity, and awakening after cardiac arrest. Neurology 2000;54: Longstreth Jr WT, Clayson KJ, Sumi SM. Cerebrospinal fluid and serum creatine kinase BB activity after out-of-hospital cardiac arrest. Neurology 1981;31: Tirschwell DL, Longstreth Jr WT, Rauch-Matthews ME, et al. Cerebrospinal fluid creatine kinase BB isoenzyme activity and neurologic prognosis after cardiac arrest. Neurology 1997;48: Clemmensen P, Strandgaard S, Rasmussen S, Grande P. Cerebrospinal fluid creatine kinase isoenzyme BB levels do not predict the clinical outcome in patients unconscious following cardiac resuscitation. Clin Cardiol 1987;10: Rosen H, Karlsson JE, Rosengren L. CSF levels of neurofilament is a valuable predictor of long-term outcome after cardiac arrest. J Neurol Sci 2004;221: Tiainen M, Kovala TT, Takkunen OS, Roine RO. Somatosensory and brainstem auditory evoked potentials in cardiac arrest patients treated with hypothermia. Crit Care Med 2005;33: Rossetti AO, Oddo M, Liaudet L, Kaplan PW. Predictors of awakening from postanoxic status epilepticus after therapeutic hypothermia. Neurology 2009;72: Rossetti AO, Logroscino G, Liaudet L, et al. Status epilepticus: an independent outcome predictor after cerebral anoxia. Neurology 2007;69: Rossetti AO, Oddo M, Logroscino G, Kaplan PW. Prognostication after cardiac arrest and hypothermia: a prospective study. Ann Neurol 2010;67: Oksanen T, Tiainen M, Skrifvars MB, et al. Predictive power of serum NSE and OHCA score regarding 6-month neurologic outcome after out-ofhospital ventricular fibrillation and therapeutic hypothermia. Resuscitation 2009;80: Rundgren M, Karlsson T, Nielsen N, Cronberg T, Johnsson P, Friberg H. Neuron specific enolase and S-100B as predictors of outcome after cardiac arrest and induced hypothermia. Resuscitation 2009;80: Fieux F, Losser MR, Bourgeois E, et al. Kidney retrieval after sudden out of hospital refractory cardiac arrest: a cohort of uncontrolled non heart beating donors. Crit Care 2009;13:R Kootstra G. Statement on non-heart-beating donor programs. Transplant Proc 1995;27: Fondevila C, Hessheimer AJ, Ruiz A, et al. Liver transplant using donors after unexpected cardiac death: novel preservation protocolandacceptancecriteria. Am J Transplant 2007;7: Morozumi J, Sakurai E, Matsuno N, et al. Successful kidney transplantation from donation after cardiac death using a load-distributing-band chest compression device during long warm ischemic time. Resuscitation 2009;80: Perkins GD, Brace S, Gates S. Mechanical chest-compression devices: current and future roles. Curr Opin Crit Care 2010;16: Engdahl J, Abrahamsson P, Bang A, Lindqvist J, Karlsson T, Herlitz J. Is hospital care of major importance for outcome after out-of-hospital cardiac arrest? Experience acquired from patients with out-of-hospital cardiac arrest resuscitated by the same Emergency Medical Service and admitted to one of two hospitals over a 16- -year period in the municipality of Goteborg. Resuscitation 2000;43:
167 166 Ch.D. Deakin, J.P. Nolan, J. Soar, K. Sunde, R.W. Koster, G.B. Smith, G.D. Perkins Liu JM, Yang Q, Pirrallo RG, Klein JP, Aufderheide TP. Hospital variability of out-of-hospital cardiac arrest survival. Prehosp Emerg Care 2008;12: Herlitz J, Engdahl J, Svensson L, Angquist KA, Silfverstolpe J, Holmberg S. Major differences in 1-month survival between hospitals in Sweden among initial survivors of out-of-hospital cardiac arrest. Resuscitation 2006;70: Callaway CW, Schmicker R, Kampmeyer M, et al. Receiving hospital characteristics associated with survival after out-of-hospital cardiac arrest. Resuscitation Davis DP, Fisher R, Aguilar S, et al. The feasibility of a regional cardiac arrest receiving system. Resuscitation 2007;74: Spaite DW, Bobrow BJ, Vadeboncoeur TF, et al. The impact of prehospital transport interval on survival in out-of-hospital cardiac arrest: implications for regionalization of post-resuscitation care. Resuscitation 2008;79: Spaite DW, Stiell IG, Bobrow BJ, et al. Effect of transport interval on out-of- -hospital cardiac arrest survival in the OPALS Study: implications for triaging patients to specialized cardiac arrest centers. Ann Emerg Med Vermeer F, Oude Ophuis AJ, vd Berg EJ, et al. Prospective randomised comparison between thrombolysis, rescue PTCA, and primary PTCA in patients with extensive myocardial infarction admitted to a hospital without PTCA facilities: a safety and feasibility study. Heart 1999;82: Widimsky P, Groch L, Zelizko M, Aschermann M, Bednar F, Suryapranata H. Multicentre randomized trial comparing transport to primary angioplasty vs immediate thrombolysis vs combined strategy for patients with acute myocardial infarction presenting to a community hospital without a catheterization laboratory The PRAGUE study. Eur Heart J 2000;21: Widimsky P, Budesinsky T, Vorac D, et al. Long distance transport for primary angioplasty vs immediate thrombolysis in acute myocardial infarction. Final results of the randomized national multicentre trial PRAGUE-2. Eur Heart J 2003;24: Le May MR, So DY, Dionne R, et al. A citywide protocol for primary PCI in ST-segment elevation myocardial infarction. N Engl J Med 2008; 358: Abernathy 3rd JH, McGwin Jr G, Acker 3rd JE, Rue 3rd LW. Impact of a voluntary trauma system on mortality, length of stay, and cost at a level I trauma center. Am Surg 2002;68: Clemmer TP, Orme Jr JF, Thomas FO, Brooks KA. Outcome of critically injured patients treated at Level I trauma centers versus full-service community hospitals. Crit Care Med 1985;13: Culica D, Aday LA, Rohrer JE. Regionalized trauma care system in Texas: implications for redesigning trauma systems. Med Sci Monit 2007;13:SR Hannan EL, Farrell LS, Cooper A, Henry M, Simon B, Simon R. Physiologic trauma triage criteria in adult trauma patients: are they effective in saving lives by transporting patients to trauma centers? J Am Coll Surg 2005;200: Harrington DT, Connolly M, Bif. WL, Majercik SD, Ciof. WG. Transfer times to definitive care facilities are too long: a consequence of an immature trauma system. Ann Surg 2005;241:961 6 [discussion 6 8] Liberman M, Mulder DS, Lavoie A, Sampalis JS. Implementation of a trauma care system: evolution through evaluation. J Trauma 2004;56: MacKenzie EJ, Rivara FP, Jurkovich GJ, et al. A national evaluation of the effect of trauma-center care on mortality. N Engl J Med 2006;354: Mann NC, Cahn RM, Mullins RJ, Brand DM, Jurkovich GJ. Survival among injured geriatric patients during construction of a statewide trauma system. J Trauma 2001;50: Mullins RJ, Veum-Stone J, Hedges JR, et al. Influence of a statewide trauma system on location of hospitalization and outcome of injured patients. J Trauma 1996;40: [discussion 45 6] Mullins RJ, Mann NC, Hedges JR, Worrall W, Jurkovich GJ. Preferential benefit of implementation of a statewide trauma system in one of two adjacent states. J Trauma 1998;44: [discussion 17] Mullins RJ, Veum-Stone J, Helfand M, et al. Outcome of hospitalized injured patients after institution of a trauma system in an urban area. JAMA 1994;271: Mullner R, Goldberg J. An evaluation of the Illinois trauma system. Med Care 1978;16: Mullner R, Goldberg J. Toward an outcome-oriented medical geography: an evaluation of the Illinois trauma/emergency medical services system. Soc Sci Med 1978;12: Nathens AB, Jurkovich GJ, Rivara FP, Maier RV. Effectiveness of state trauma systems in reducing injury-related mortality: a national evaluation. J Trauma 2000;48:25 30 [discussion 1] Nathens AB, Maier RV, Brundage SI, Jurkovich GJ, Grossman DC. The effect of interfacility transfer on outcome in an urban trauma system. J Trauma 2003;55: Nicholl J, Turner J. Effectiveness of a regional trauma system in reducing mortality from major trauma: before and after study. BMJ 1997;315: Potoka DA, Schall LC, Gardner MJ, Stafford PW, Peitzman AB, Ford HR. Impact of pediatric trauma centers on mortality in a statewide system. J Trauma 2000;49: Sampalis JS, Lavoie A, Boukas S, et al. Trauma center designation: initial impact on trauma-related mortality. J Trauma 1995;39:232 7 [discussion 7 9] Sampalis JS, Denis R, Frechette P, Brown R, Fleiszer D, Mulder D. Direct transport to tertiary trauma centers versus transfer from lower level facilities: impact on mortality and morbidity among patients with major trauma. J Trauma 1997;43: [discussion 95 6] Nichol G, Aufderheide TP, Eigel B, et al. Regional systems of care for out-of- -hospital cardiac arrest: a policy statement from the American Heart Association. Circulation 2010;121: Nichol G, Soar J. Regional cardiac resuscitation systems of care. Curr Opin Crit Care 2010;16: Soar J, Packham S. Cardiac arrest centres make sense. Resuscitation 2010;81:
168 Publikacja przygotowana przez Europejską Radę Resuscytacji (ERC) przy współpracy z Polską Radą Resuscytacji (PRR). Tekst tłumaczony przez Polską Radę Resuscytacji. Wiedza i praktyka w zakresie resuscytacji krążeniowo-oddechowej to stale zmieniająca się dziedzina medycyny. W miarę rozwoju wiedzy oraz postępu w nauce i doświadczeniu klinicznym zmienia się w sposób ciągły również praktyka medycz na oraz sposób stosowania leków. Czytelnik tego podręcznika jest zobowiązany do zapoznania się z aktualnymi wiado mościami na temat przedstawionych sposobów postępowania i farmakoterapii ze szczególnym uwzględnieniem informacji producentów na temat dawek, czasu i drogi podawania oraz efektów ubocznych stosowanych leków. Na każdej z osób praktykujących medycynę resuscytacji spoczywa osobista odpowiedzialność za stosowane metody lecznicze, których uży cie powinno być oparte na gruntownej wiedzy i umiejętnościach praktycznych z zachowaniem niezbędnych warunków bez pieczeństwa własnego i pacjenta. Wydawcy oraz redaktorzy niniejszego opracowania nie ponoszą odpowiedzialności za szkody, które mogłyby być w jakikolwiek sposób związane z materiałem zawartym w tej książce. Bibliografia do wszystkich rozdziałów została w całości powtórzona za wydaniem oryginalnym. REDAKTOR NAUKOWY WYDANIA POLSKIEGO prof. dr hab. Janusz Andres TŁUMACZENIE Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Elżbieta Dobrowolska, Edyta Drab, Bartosz Frączek, Anna Jarosz, Piotr Kolęda, Paweł Krawczyk, Rafał Surmacz, Jurij Szymański, Grzegorz Zając KOREKTA MERYTORYCZNA Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Bartosz Frączek, Paweł Krawczyk ADIUSTACJA I KOREKTA WYDAWNICZA Danuta Ambrożewicz PROJEKT OKŁADKI Polska Rada Resuscytacji wg plakatu V Międzynarodowego Kongresu Polskiej Rady Resuscytacji autorstwa Mieczysława Górowskiego Publikację wydano ze środków Polskiej Rady Resuscytacji. Copyright by European Resuscitation Council (ERC), 2010 Copyright for the Polish edition by Polska Rada Resuscytacji, Kraków 2010 Copyright for the Polish translation by Polska Rada Resuscytacji, Kraków 2010 Wszystkie prawa zastrzeżone. Żadna część poniższej publikacji nie może być kopiowana i przechowywana w jakimkol wiek mechanicznym systemie kopiowania danych, włączając fotokopie, kserokopie, nagrania i inne, bez uprzedniej pisem nej zgody PRR (dotyczy terenu Rzeczpospolitej Polskiej). Wszystkie prośby o możliwość wykorzystania materiałów zawartych w tej publikacji należy kierować do ERC. ISBN KOORDYNATOR STRONY ORAZ WERSJI ELEKTRONICZNEJ Wytycznych resuscytacji 2010 Wiesław Pyrczak prc@prc.krakow.pl ADRES DO KORESPONDENCJI ADRES DO KORESPONDENCJI W POLSCE ERC Secretariat VZW Polska Rada Resuscytacji Drie Eikenstraat 661 ul. Radziwiłłowska 4, Kraków BE-2650 EDEGEM tel fax Belgium biuro@prc.krakow.pl tel fax Koordynator kursów info@erc.edu Tomasz Galewicz kursy@prc.krakow.pl SKŁAD I PRZYGOTOWANIE DO DRUKU FALL ul. Garczyńskiego 2, Kraków tel ; fall@fall.pl
169 Wstępne postępowanie 5 w ostrych zespołach wieńcowych Hans-Richard Arntz a,1, Leo L. Bossaert b,*,1, Nicolas Danchin c, Nikolaos I. Nikolaou d a Department of Cardiology, Campus Benjamin Franklin, Charite, Berlin, Germany b Department of Critical Care, University of Antwerp, Antwerp, Belgium c Department of Coronary Artery Disease and Intensive Cardiac Care, Hôpital Européen Georges Pompidou, Paris, France d Constantopouleio General Hospital, Athens, Greece Podsumowanie głównych zmian od Wytycznych 2005 Zmiany w postępowaniu w ostrym zespole wieńcowym w stosunku do Wytycznych 2005 obejmują: Definicje Określenie zawał mięśnia sercowego bez uniesienia odcinka ST ostry zespół wieńcowy (NSTEMI-OZW) wprowadzono łącznie dla NSTEMI oraz niestabilnej choroby wieńcowej, ponieważ diagnostyka różnicowa opiera się na markerach biochemicznych, które są oznaczalne dopiero po kilku godzinach, podczas gdy leczenie podejmuje się na podstawie objawów klinicznych przy przyjęciu. Oddziały obserwacji pacjentów z bólem w klatce piersiowej oraz zasady podejmowania decyzji o wczesnym wypisie Wywiad, badanie fizykalne, markery biochemiczne, kryteria EKG oraz skale oceny ryzyka są niewiarygodne w identyfikacji pacjentów, których można bezpiecznie wcześnie wypisać do domu. Zadaniem oddziałów obserwacyjnych dla pacjentów z bólem w klatce piersiowej (CPUs Chest Pain observation Units) jest rozpoznanie na podstawie powtarzanego badania fizykalnego, EKG oraz oznaczania markerów biochemicznych tych pacjentów, którzy wymagają przyjęcia do szpitala celem wykonania zabiegów inwazyjnych. Taka ocena może obejmować również wykonywanie testów prowokacyjnych, a u wybranych pacjentów badań obrazowych, takich jak tomografia komputerowa serca, rezonans magnetyczny etc. Leczenie objawowe Powinno się unikać niesteroidowych leków przeciwzapalnych (NSAIDs). Nitraty nie powinny być stosowane w celach diagnostycznych. Tlenoterapia tylko dla pacjentów z hipoksemią, dusznością oraz zastojem w krążeniu płucnym. Hiperoksemia może być szkodliwa w niepowikłanym zawale. * Corresponding author. leo.bossaert@ua.ac.be (L.L. Bossaert). 1 These individuals contributed equally to this manuscript and are equal first coauthors. Leczenie przyczynowe Zostały opracowane bardziej liberalne wytyczne dla stosowania kwasu acetylosalicylowego (ASA), który może być podany także przez świadków zdarzenia na zlecenie dyspozytorów lub bez ich udziału. Poprawiono zalecenia dotyczące nowego sposobu leczenia przeciwpłytkowego i przeciwkrzepliwego u pacjentów ze STEMI oraz NSTEMI-OZW w oparciu o strategię terapeutyczną. Odradza się podawanie inhibitorów Gp IIb/IIIa przed angiografią/przezskórną interwencją wieńcową (PCI). Strategia reperfuzyjna w STEMI Pierwotna PCI (PPCI) jest preferowaną strategią reperfuzyjną przy założeniu, że jest wykonywana w odpowiednim momencie przez doświadczony zespół. Zespół pogotowia ratunkowego (PR) może ominąć najbliższy szpital, jeśli w innym osiągalne jest wykonanie PPCI bez zbytniej zwłoki. Akceptowane opóźnienie pomiędzy początkiem fibrynolizy a pierwszym napełnieniem balona może się wahać od 45 do 180 minut i zależy od lokalizacji zawału, wieku pacjenta oraz czasu trwania objawów. Ratunkowa PCI powinna być podjęta, jeśli nie powiodła się fibrynoliza. Odradza się stosowanie rutynowej PCI natychmiast po fibrynolizie ( torowana PCI ). Pacjenci po skutecznej fibrynolizie a pozostający w szpitalu, w którym nie przeprowadza się PCI, powinni być przeniesieni do innego ośrodka celem wykonania angiografii i ewentualnej PCI, optymalnie w przeciągu 6 24 godzin po fibrynolizie (podejście farmakologiczno-inwazyjne ). Angiografia i, jeśli to konieczne, PCI mogą być uzasadnione u pacjentów z powrotem spontanicznego krążenia (ROSC) po NZK i mogą być częścią standardowego postępowania po resuscytacji. Aby zrealizować te cele, przydatnym jest stworzenie sieci obejmującej zespoły pogotowia ratunkowego (PR), szpitale niewykonujące PCI oraz szpitale przeprowadzające PCI. Prewencja pierwotna i wtórna Wskazania do stosowania beta-blokerów są bardziej restrykcyjne: nie ma dowodów na skuteczność rutynowego dożylnego podawania beta-blokerów za wyjątkiem
170 168 H.-R. Arntz, L.L. Bossaert, N. Danchin, N.I. Nikolaou 5 szczególnych okoliczności, takich jak leczenie częstoskurczów. W innych przypadkach beta-blokery mogą być wprowadzane w niskich dawkach tylko po ustabilizowaniu stanu pacjenta. Wytyczne dla profilaktycznego stosowania leków antyarytmicznych, inhibitorów enzymu konwertującego angiotensynę (ACE)/blokerów receptora dla angiotensyny (ARB) oraz statyn pozostają niezmienione. Wprowadzenie W wielu krajach europejskich częstość występowania ostrego zawału mięśnia sercowego z uniesieniem odcinka ST (Acute Myocardial Infarction AMI) zmniejsza się 1 ; podczas gdy zwiększa się częstość występowania ostrego zespołu wieńcowego bez uniesienia odcinka ST (NSTEMI-OZW) 2,3. Chociaż dzięki nowoczesnej terapii reperfuzyjnej i poprawie wtórnej profilaktyki udało się znacznie zmniejszyć wewnątrzszpitalną śmiertelność z powodu STEMI, całkowita śmiertelność w ciągu 28 dni pozostaje praktycznie niezmienna, ponieważ dwie trzecie pacjentów umiera przed przyjęciem do szpitala, głównie z powodu ciężkich zaburzeń rytmu wywołanych przez niedokrwienie 4. Dlatego najlepszym sposobem poprawy przeżywalności w przebiegu ostrego niedokrwienia jest zmniejszenie opóźnienia pomiędzy pojawieniem się objawów a pierwszym kontaktem z personelem medycznym oraz rozpoczęcie celowanego leczenia we wczesnej, przedszpitalnej, fazie choroby. Termin ostre zespoły wieńcowe (OZW) zawiera w sobie trzy różne jednostki chorobowe z ostrymi objawami choroby wieńcowej (ryc. 5.1): zawał mięśnia sercowego z uniesieniem odcinka ST (ST Elevation Myocardial Infarction STEMI), zawał mięśnia sercowego bez uniesienia odcinka ST (non-st Elevation Myocardial Infarction NSTEMI) oraz niestabilną dusznicę bolesną (Ustable Angina Pectoris UAP). Zawał mięśnia sercowego bez uniesienia odcinka ST oraz UAP zwykle określa się łącznie mianem NSTEMI-OZW. Częstą przyczyną OZW jest pęknięcie lub erozja blaszki miażdżycowej 5. Zmiany elektrokardiograficzne (brak lub obecność uniesienia odcinka ST) różnicuje STEMI od NSTEMI-OZW. Te ostatnie mogą przebiegać z obniżeniem lub niespecyficznymi zmianami odcinka ST, a nawet prawidłowym zapisem EKG. W przypadku braku uniesienia odcinka ST wzrost stężenia markerów uszkodzenia mięśnia sercowego w surowicy, szczególnie troponin T lub I jako najbardziej specyficznych wskaźników martwicy mięśnia sercowego, wskazuje na obecność NSTEMI. OZW są najczęstszą przyczyną poważnych zaburzeń rytmu serca prowadzących do nagłej śmierci sercowej. Celem terapeutycznym jest leczenie ostrych, zagrażających życiu stanów, takich jak migotanie komór (VF), skrajna bradykardia, jak również utrzymanie funkcji lewej komory oraz zapobieganie wystąpieniu niewydolności krążenia poprzez minimalizację obszaru uszkodzenia mięśnia sercowego. Aktualne wytyczne dotyczą pierwszych godzin od wystąpienia objawów. Postępowanie przedszpitalne i wstępne leczenie w obrębie szpitalnego oddziału ratunkowego (SOR) może się różnić w zależności od lokalnych możliwości, protokołów i uwarunkowań. Dane dotyczące sposobu postępowania przedszpitalnego są zwykle ekstrapolowane z badań nad Ryc Definicje ostrych zespołów wieńcowych (OZW) (STEMI zawał mięśnia sercowego z uniesieniem odcinka ST; NSTEMI zawał mięśnia sercowego bez uniesienia odcinka ST; UAP niestabilna choroba wieńcowa)
171 Wstępne postępowanie w ostrych zespołach wieńcowych 169 wstępnym leczeniem pacjentów zaraz po przyjęciu ich do szpitala; istnieje jedynie kilka wartościowych badań dotyczących oceny postępowania przed przyjęciem pacjenta do szpitala. Wyczerpujące wytyczne dotyczące diagnostyki i leczenia OZW, z uniesieniem lub bez uniesienia odcinka ST, zostały opublikowane przez European Society of Cardiology i American College of Cardiology / American Heart Association. Aktualne rekomendacje pozostają z nimi w zgodzie 6,7. Rozpoznanie i oszacowanie ryzyka w ostrych zespołach wieńcowych Ponieważ wczesne leczenie OZW przynosi największe korzyści, a niedokrwienie mięśnia sercowego jest najczęstszym czynnikiem odpowiedzialnym za wystąpienie nagłej śmierci sercowej, ważnym jest uświadamianie społeczeństwu, jakie objawy są typowe dla OZW. Istnieją jednakże grupy pacjentów, które rzadziej wzywają pomocy medycznej w przypadku wystąpienia objawów OZW. Znaczące opóźnienia w rozpoczęciu leczenia/reperfuzji opisywane są w przypadku kobiet, osób starszych, osób należących do mniejszości etnicznych i rasowych lub do niskiej klasy społeczno-ekonomicznej oraz u osób samotnych 8. Zagrożeni pacjenci i ich rodziny powinni umieć rozpoznać charakterystyczne objawy, takie jak ból w klatce piersiowej promieniujący do innych obszarów górnej połowy ciała, któremu często towarzyszą: duszność, potliwość, nudności, wymioty lub utrata przytomności. Powinni oni także rozumieć potrzebę wczesnego wezwania pogotowia ratunkowego, a najlepiej, by byli oni przeszkoleni w zakresie wykonywania BLS. Dalszego opracowania wymagają strategie mające na celu zwiększanie znajomości różnych objawów OZW oraz poprawy częstości rozpoznawania OZW w szczególnie narażonych grupach pacjentów. Dyspozytorzy Pogotowia Ratunkowego muszą umieć rozpoznawać OZW oraz zadawać odpowiednie pytania. W przypadku podejrzenia OZW powinien interweniować zespół PR wyszkolony w zakresie ALS, posiadający odpowiednie możliwości diagnostyczne i terapeutyczne. Ze względu na dużą pilność ratunkowej rewaskularyzacji u pacjentów ze STEMI oraz zagrożonych wysokim ryzykiem zgonu sercowego, powinno się wdrożyć specjalne systemy opieki, mające na celu poprawę rozpoznania STEMI oraz skrócenie czasu do momentu rozpoczęcia leczenia. Oceniono czułość, swoistość oraz istotność kliniczną różnych sposobów diagnozowania stosowanych w OZW. W celu postawienia rozpoznania należy wziąć pod uwagę wszystkie informacje uzyskane na podstawie badania fizykalnego, EKG, oznaczania biomarkerów oraz badań obrazowych, jednocześnie należy dokonać oceny ryzyka tak, aby można było podjąć optymalne decyzje dotyczące przyjęcia pacjenta do szpitala oraz jego leczenia/reperfuzji. Objawy OZW Typowe objawy towarzyszące OZW to promieniujący ból w klatce piersiowej, duszność oraz wzmożona potliwość, jednakże u pacjentów w podeszłym wieku, kobiet lub u chorujących na cukrzycę mogą wystąpić nietypowy obraz lub objawy niespecyficzne 9,10. Żaden z tych objawów nie może być jedyną podstawą rozpoznania OZW. Zmniejszenie nasilenia bólu w klatce piersiowej po podaniu nitrogliceryny może być mylące i nie jest polecane jako sposób postępowania diagnostycznego 11. U pacjentów ze STEMI objawy mogą być bardziej nasilone oraz trwać dłużej, ale nie jest to wystarczająco wiarygodne do rozróżnienia STEMI oraz NSTEMI-OZW. Wywiad powinien być starannie zebrany już podczas pierwszego kontaktu z personelem medycznym, gdyż może dostarczyć pierwszych wskazówek co do ewentualnego występowania OZW, prowadząc do zaplanowania odpowiednich badań. Wyniki testów mogą ułatwić przeprowadzenie kwalifikacji i podjęcie decyzji terapeutycznych w warunkach przedszpitalnych oraz Szpitalnego Oddziału Ratunkowego (SOR). 12-odprowadzeniowe EKG 12-odprowadzeniowe EKG jest kluczowym badaniem dla oceny OZW. W przypadku STEMI wskazuje ono potrzebę pilnej terapii reperfuzyjnej (np. pierwotnej przezskórnej interwencji wieńcowej lub prowadzonej przedszpitalnie fibrynolizy). Kiedy podejrzewany jest OZW, 12-odprowadzeniowe EKG powinno być wykonane i ocenione najszybciej, jak to jest możliwe, po pierwszym kontakcie pacjenta z personelem medycznym, celem wcześniejszego postawienia rozpoznania oraz przeprowadzenia kwalifikacji pacjenta. EKG wykonane w warunkach przedszpitalnych lub w SOR ma dużą wartość diagnostyczną, jeśli jest interpretowane przez przeszkolony personel medyczny 12. Zapis 12-odprowadzeniowego EKG wykonany w warunkach przedszpitalnych umożliwia wczesne zawiadomienie ośrodka przyjmującego pacjenta oraz przyspiesza decyzje terapeutyczne. Wiele badań potwierdza, że skraca to czas od przyjęcia do szpitala do rozpoczęcia terapii repefuzyjnej o minut 13,14. Przeszkoloni członkowie zespołów ratownictwa medycznego (lekarze specjaliści medycyny ratunkowej, ratownicy medyczni, pielęgniarki) potrafią z wysoką specyficznością i czułością, porównywalną do warunków szpitalnych, rozpoznać STEMI, definiowany jako uniesienie odcinka ST o. 0,1 mv w co najmniej dwóch sąsiadujących odprowadzeniach kończynowych lub >0,2 mv w co najmniej dwóch sąsiadujących odprowadzeniach przedsercowych Z tego powodu ratownicy medyczni oraz pielęgniarki powinni być szkoleni w rozpoznawaniu STEMI bez bezpośredniego wsparcia lekarza tak długo, jak długo zapewnia się ścisłą kontrolę nad jakością takiego działania. Jeśli interpretacja wykonanego przedszpitalnie EKG nie jest możliwa na miejscu, powinno się dokonać interpretacji komputerowej 18,19 lub przesłać zapis EKG (teletransmisja). Wykonanie i przesłanie do szpitala diagnostycznych zapisów EKG trwa zwykle krócej niż 5 minut. W ocenie pacjentów z podejrzeniem OZW interpretacja komputerowa zapisu EKG może zwiększyć swoistość rozpoznania STEMI, szczególnie w przypadku lekarzy niedoświadczonych w interpretacji EKG. Jednakże przydatność interpretacji komputerowej zależy od jakości wykonanego zapisu EKG. W związku z tym nieprawidłowe raporty komputero- 5
172 170 H.-R. Arntz, L.L. Bossaert, N. Danchin, N.I. Nikolaou 5 we mogą zwieść lekarzy niedoświadczonych w ocenie EKG. Z tego powodu interpretacja komputerowa EKG nie powinna zastąpić, a jedynie wspomóc doświadczonego klinicystę. Markery biochemiczne W przypadku charakterystycznego wywiadu brak uniesień odcinka ST w 12-odprowadzeniowym EKG oraz podwyższony poziom markerów martwicy mięśnia sercowego (troponiny T, troponiny I, CK, CK-MB, mioglobiny) świadczy o obecności NSTEMI i pozwala na różnicowanie ze STEMI oraz niestabilną dusznicą bolesną. Preferowanym markerem są specyficzne dla mięśnia sercowego troponiny. Podwyższone poziomy troponiny są szczególnie przydatne w identyfikacji pacjentów z grupy zwiększonego ryzyka niepomyślnego przebiegu choroby 20. Oznaczenie poziomu sercowych markerów biochemicznych powinno być częścią wstępnej oceny wszystkich pacjentów SORu z objawami wskazującymi na niedokrwienie mięśnia sercowego 21. Jednakże opóźnienie wyrzutu biomarkerów z uszkodzonego mięśnia sercowego ogranicza ich znaczenie diagnostyczne w pierwszych 4 6 godzinach od początku wystąpienia objawów 22. U pacjentów przyjętych przed upływem 6 godzin, u których pierwszy wynik troponin był ujemny, należy ponownie oznaczyć poziom wskaźników sercowych po 6 12 godzinach od pojawienia się pierwszych symptomów. Aby móc w pełni wykorzystać wynik oznaczenia biomarkerów, lekarze powinni dokładnie poznać czułość i precyzję oznaczenia oraz lokalne normy laboratoryjne, jak również kinetykę uwalniania i eliminacji tych wskaźników. Zostały już opracowane testy do wykrywania troponin sercowych o wysokiej czułości (ultraczułe), które pomagają zwiększyć czułość rozpoznania zawału u pacjentów z podejrzeniem niedokrwienia mięśnia sercowego 23. Jeśli do oznaczenia troponin nie są dostępne testy o wysokiej czułości, powinno się rozważyć ocenę kilku markerów: CKMB lub mioglobiny w połączeniu z troponiną. Nie ma dowodów na skuteczność oznaczania troponin przy użyciu przenośnych urządzeń diagnostycznych jako wstępnego testu w warunkach przedszpitalnych, mającego na celu ocenę pacjentów z objawami wskazującymi na niedokrwienie mięśnia sercowego 23. W oddziale ratunkowym wykonanie oznaczeń za pomocą przenośnych urządzeń diagnostycznych może pomóc skrócić czas do rozpoczęcia leczenia oraz długość pobytu na oddziale 24. Dopóki nie zostaną przeprowadzone dalsze randomizowane badania kliniczne, oznaczenia żadnych innych markerów osoczowych nie powinny być uważane za postępowanie z wyboru w rozpoznawaniu oraz postępowaniu z pacjentami z objawami OZW 25. Zasady podejmowania decyzji o wczesnym wypisie Podjęto próby połączenia danych z wywiadu, badania fizykalnego oraz powtarzanych zapisów EKG i oznaczeń markerów biochemicznych celem stworzenia zasad klinicznych, które pomogłyby w oddziale ratunkowym zróżnicować pacjentów z podejrzewanym OZW. Jednakże żadna z tych zasad nie jest odpowiednia i wystarczająca do rozpoznania w SOR pacjenta z bólem w klatce piersiowej i podejrzeniem OZW, którego można bezpiecznie wypisać 26. Z tego samego powodu systemy oceny ryzyka pacjentów z OZW, które przetestowano w warunkach szpitalnych (np. Thrombolysis in Myocardial Infarction [TIMI] score, Global Registry of Acute Coronary Events [GRACE] score, Fast Revascularisation in Instability in Coronary Disease [FRISC] score lub kryteria Goldmana), nie powinny być używane do identyfikacji pacjentów niskiego ryzyka, nadających się do wypisu z oddziału ratunkowego. Bardzo niski, krótkoterminowy wskaźnik częstości występowania zdarzeń ma podgrupa pacjentów poniżej 40. roku życia z nietypowymi objawami oraz brakiem istotnych nieprawidłowości w wywiadzie, u których występują prawidłowe powtarzane oznaczenia biomarkerów oraz normalne zapisy 12-odprowadzeniowego EKG. Protokoły obserwacji pacjentów z bólem w klatce piersiowej U pacjentów z podejrzeniem OZW nie można wiarygodnie wykluczyć tej jednostki chorobowej, wykorzystując niecharakterystyczny wywiad oraz badanie fizykalne ze wstępną negatywną oceną EKG oraz markerów biochemicznych. Dlatego, aby postawić rozpoznanie oraz podjąć decyzje terapeutyczne, niezbędna jest trwająca pewien czas obserwacja. Protokoły obserwacji pacjentów z bólem w klatce piersiowej są szybkimi sposobami oceny pacjentów z podejrzewanym OZW. Z założenia powinny one obejmować wywiad i badanie fizykalne, a następnie okres obserwacji, w czasie którego powinny być wykonywane kolejne zapisy EKG oraz oznaczenia markerów sercowych. Po wykluczeniu AMI ocena pacjenta powinna być uzupełniona o nieinwazyjną ocenę anatomiczną choroby naczyń wieńcowych lub testy prowokacyjne dla indukowanego niedokrwienia mięśnia sercowego. Takie protokoły mogą być wykorzystywane do poprawy skuteczności identyfikowania pacjentów wymagających przyjęcia do szpitala lub dalszych testów diagnostycznych, zapewniają jednocześnie bezpieczeństwo pacjentom, skracając czas pobytu w szpitalu oraz obniżając koszty 27. Dla pacjentów oddziału ratunkowego z wywiadem charakterystycznym w kierunku OZW, ale prawidłowymi badaniami wstępnymi, bezpiecznym i skutecznym rozwiązaniem mogą być oddziały obserwacyjne dla pacjentów z bólem w klatce piersiowej. Mogą one przyczynić się do ograniczenia czasu pobytu w szpitalu, ilości przyjęć do szpitala oraz obniżenia kosztów ponoszonych przez służbę zdrowia, a także poprawy skuteczności diagnostycznej oraz jakości życia 28. Nie ma bezpośrednich dowodów wskazujących na to, że oddziały obserwacyjne dla pacjentów z bólem w klatce piersiowej lub protokoły obserwacji zmniejszają częstość niekorzystnych wyników leczenia zdarzeń sercowo-naczyniowych, w szczególności śmiertelności u pacjentów z objawami sugerującymi OZW. Techniki obrazowe Skuteczne badanie przesiewowe pacjentów z podejrzewanym OZW, ale ujemnymi wynikami EKG oraz markerów sercowych pozostaje wyzwaniem. Ocenie zostały poddane nieinwazyjne techniki obrazowe (angiografia TK 29, rezonans magnetyczny serca, scyntygrafia mięśnia sercowego 30
173 Wstępne postępowanie w ostrych zespołach wieńcowych 171 oraz echokardiografia 31 ) jako sposoby badania przesiewowego pacjentów niskiego ryzyka oraz identyfikacji podgrup pacjentów, których można bezpiecznie wypisać do domu. Chociaż nie ma dużych, wieloośrodkowych badań klinicznych, istniejące dowody wskazują na to, że powyższe sposoby diagnostyczne umożliwiają postawienie wczesnego i prawidłowego rozpoznania, a z nim skrócenie długości pobytu w szpitalu oraz zmniejszenie kosztów, bez wzrostu częstości zdarzeń sercowych. Należy zwrócić uwagę na narażenie na promieniowanie jonizujące oraz kontrast jodowy w przypadku stosowania wielorzędowej tomografii komputerowej (MDCT) oraz scyntygrafii mięśnia sercowego. Objawowe leczenie ostrych zespołów wieńcowych Nitraty Triazotan glicerolu jest skutecznym lekiem w przypadku bólu wieńcowego w klatce piersiowej, wywołuje również korzystny efekt hemodynamiczny poprzez poszerzenie łożyska żylnego, rozkurcz tętnic wieńcowych oraz w mniejszym stopniu tętnic obwodowych. Można rozważyć podanie triazotanu glicerolu, gdy skurczowe ciśnienie tętnicze jest wyższe niż 90 mm Hg oraz gdy występują dolegliwości bólowe w klatce piersiowej (ryc. 5.2). Podanie triazotanu glicerolu może być również korzystne w leczeniu ostrego zastoju w krążeniu płucnym. Nie należy stosować nitratów u pacjentów z niskim ciśnieniem krwi (. 90 mm Hg skurczowego ciśnienia krwi), zwłaszcza gdy towarzyszy temu bradykardia oraz u pacjentów z zawałem dolnej ściany mięśnia sercowego i podejrzeniem zawału prawej komory. Użycie nitratów w tych przypadkach może spowodować znaczne obniżenie ciśnienia krwi oraz rzutu serca. Leczenie przeciwbólowe Morfina jest lekiem z wyboru w przypadku zwalczania bólu opornego na działanie nitratów, a dzięki jej działaniu uspokajającemu użycie leków sedatywnych w większości przypadków nie jest konieczne. Jej użycie, jako leku zwiększającego pojemność łożyska żylnego, może przynieść dodatkowe korzyści w przypadku zastoju w krążeniu płucnym. Morfinę należy podawać w dawkach 3 5 mg dożylnie, powtarzanych co kilka minut, aż do ustąpienia bólu. W leczeniu przeciwbólowym powinno się unikać niesteroidowych leków przeciwzapalnych (NSAIDs) ze względu na ich działanie prozakrzepowe 32. Tlen Monitorowanie saturacji krwi tętniczej (SaO 2 ) przy pomocy pulsoksymetru (SpO 2 ) pomaga ocenić potrzebę stoso- 5 # Zgodnie ze stratyfikacją ryzyka * Prasugrel, w dawce wysycającej 60 mg, może być stosowany jako alternatywa dla klopidogrelu u pacjentów ze STEMI oraz planowaną PPCI, jeśli nie mają udaru lub TIA w wywiadzie. W momencie opracowania wytycznych tikagrelor nie został jeszcze zaakceptowany jako alternatywa dla klopidogrelu. Ryc Algorytm leczenia ostrych zespołów wieńcowych (PCI = przezskórna interwencja wieńcowa; UFH = heparyna niefrakcjonowana)
174 172 H.-R. Arntz, L.L. Bossaert, N. Danchin, N.I. Nikolaou 5 wania tlenoterapii. Tylko pacjenci z hipoksją wymagają leczenia tlenem. Niektóre dane wskazują, że tlen w dużych przepływach może być szkodliwy dla pacjentów z niepowikłanym zawałem mięśnia sercowego Należy dążyć do utrzymywania saturacji krwi pomiędzy 94 a 98% lub 88 92%, jeśli pacjent narażony jest na ryzyko niewydolności oddechowej związanej z hiperkapnią 36. Przyczynowe leczenie ostrych zespołów wieńcowych Inhibitory agregacji płytek Ponieważ aktywacja i agregacja płytek są głównymi procesami wyzwalającymi OZW, hamowanie agregacji płytek jest jednym z najważniejszych elementów wstępnego leczenia zespołów wieńcowych i ma znaczenie w prewencji wtórnej. Kwas acetylosalicylowy (ASA) Dane z dużych, randomizowanych badań klinicznych wykazują zmniejszoną śmiertelność u pacjentów przyjętych do szpitala z rozpoznaniem OZW, którym podawano mg kwasu acetylosalicylowego (Acetylsalicylic Acid ASA). Kilka prac sugeruje zmniejszoną śmiertelność, gdy ASA podawano wcześniej 37,38. Dlatego zaleca się jak najwcześniejsze podanie ASA wszystkim pacjentom z podejrzeniem OZW, za wyjątkiem osób z prawdziwą alergią na ten lek. ASA może być podany przez personel medyczny, świadka zdarzenia lub wzięty za poradą dyspozytora pogotowia, zależnie od lokalnych standardów postępowania. Wstępna dawka ASA podana doustnie (do rozgryzienia) wynosi mg. Inne formy ASA (rozpuszczalna, dożylna) mogą być równie skuteczne co rozgryzione tabletki. Inhibitory receptora ADP Tienopirydyny (klopidogrel, prasugrel) oraz cyklo-pentylo-triazolo-pirymidyna, tikagrelor hamują nieodwracalnie receptor ADP, co powoduje dalsze hamowanie agregacji płytek, zainicjowane przez ASA. W przeciwieństwie do klopidogrelu, metabolizm prasugrelu oraz tikagreloru jest niezależny od determinowanej genetycznie zmienności metabolizmu oraz aktywacji leku. Z tego powodu prasugrel oraz tikagrelor prowadzą do silniejszego i pewniejszego hamowania agregacji płytek. Duże randomizowane badanie porównujące klopidogrel w dawce wysycającej 300 mg, a następnie podtrzymującej 75 mg na dobę z prasugrelem (dawka wysycająca 60 mg, a następnie 10 mg dziennie) u pacjentów z OZW wykazało mniejszą ilość poważnych sercowych zdarzeń niepożądanych (Major Adverse Cardiac Events MACE) w grupie prasugrelu; jednakże częstość krwawień była wyższa. Ryzyko krwawienia było znamiennie wyższe u pacjentów z masą ciała poniżej 60 kg oraz w wieku powyżej 75. roku życia 39. Znamiennie wyższe ryzyko krwawienia wewnątrzczaszkowego obserwowane było u pacjentów z przemijającym napadem niedokrwienia (TIA) oraz/lub udarem w wywiadzie. W innym badaniu tikagrelor wykazał wyższość w stosunku do klopidogrelu w odniesieniu do MACE 40. W momencie opracowania wytycznych tikagrelor nie został jeszcze zaakceptowany jako alternatywa dla klopidogrelu. Inhibitory receptora ADP w NSTEMI-OZW Klopidogrel Klopidogrel podany oprócz heparyny i ASA pacjentom z dużym ryzykiem NSTEMI-OZW poprawia wyniki leczenia 41,42. Nawet jeśli nie ma dużego badania klinicznego oceniającego wstępne leczenie klopidogrelem w porównaniu z podaniem leku bezpośrednio przed interwencją wieńcową w dawce wysycającej 300 mg lub 600 mg nie należy odkładać leczenia do czasu przeprowadzenia angiografii/ PCI, gdyż największą ilość zdarzeń sercowych obserwuje się we wczesnej fazie wystąpienia zespołu wieńcowego. U niewyselekcjonowanych pacjentów poddawanych PCI leczenie wstępne wysokimi dawkami klopidogrelu skutkuje lepszymi wynikami leczenia 43. Dlatego też klopidogrel w połączeniu z ASA oraz lekiem przeciwkrzepliwym powinien być podany tak szybko, jak to jest możliwe, wszystkim pacjentom z NSTEMI-OZW. Jeśli wybiera się leczenie zachowawcze, należy podać dawkę wysycającą 300 mg; przy planowanym PCI preferowana może być dawka 600 mg. Prasugrel Pacjentom wysokiego ryzyka NSTEMI-OZW, u których w czasie angiografii planuje się PCI, można podać prasugrel (dawka wysycająca 60 mg) zamiast klopidogrelu, pod warunkiem że zwężenia naczyń wieńcowych nadają się do PCI. Należy wziąć pod uwagę przeciwwskazania (TIA/udar w wywiadzie) oraz stosunek korzyści do ryzyka u pacjentów z dużym ryzykiem krwawienia (waga <60 kg, wiek >75. roku życia). Inhibitory receptora ADP w STEMI Klopidogrel Chociaż nie ma żadnego dużego badania dotyczącego wstępnego stosowania klopidogrelu u pacjentów z objawami STEMI i planowanym PCI, takie postępowanie jest prawdopodobnie korzystne. Ponieważ im większa dawka, tym lepsze jest hamowanie płytek, pacjentom ze STEMI oraz planowaną PCI zaleca się podanie dawki wysycającej 600 mg tak szybko, jak to jest możliwe. Dwa duże randomizowane badania kliniczne porównywały klopidogrel oraz placebo stosowane u pacjentów ze STEMI i leczonych zachowawczo lub fibrynolizą 44,45. Jedno z badań obejmowało pacjentów przed 75. rokiem życia, leczonych fibrynolizą, ASA, lekiem przeciwkrzepliwym oraz dawką wysycającą 300 mg klopidogrelu 45. Leczenie klopidogrelem skutkowało mniejszą ilością zwężeń naczyń wieńcowych, których niedrożność prowadziła do zawału mięśnia sercowego widocznych w angiografii oraz mniejszą ilością powtórnych zawałów, bez wzrostu ryzyka krwawienia. W innym badaniu oceniano pacjentów ze STEMI bez limitu wieku, leczonych zachowawczo lub fibrynolizą. W tym badaniu klopidogrel (bez dawki wysycającej, 75 mg dziennie) w porównaniu z placebo skutkował mniejszą ilością zgonów oraz zmniejszeniem częstości wystąpienia kombinowane-
175 Wstępne postępowanie w ostrych zespołach wieńcowych 173 go punktu końcowego: zgonu i udaru 44. Dlatego pacjenci ze STEMI leczeni fibrynolizą powinni mieć podawany klopidogrel (300 mg w dawce wysycającej przed 75. rokiem życia oraz 75 mg bez dawki wysycającej po 75. roku życia) w połączeniu z ASA oraz lekiem przeciwkrzepliwym. Prasugrel Prasugrel w dawce wysycającej 60 mg można podać w połączeniu z ASA oraz antytrombiną pacjentom z objawami STEMI, u których planuje się PCI. Należy wziąć pod uwagę przeciwwskazania (TIA/udar w wywiadzie), a u pacjentów o masie ciała <60 kg oraz >75. roku życia także stosunek ryzyka krwawienia do spodziewanych korzyści. Nie ma danych na temat leczenia prasugrelem w opiece przedszpitalnej oraz stosowania prasugrelu i jednoczasowej fibrynolizy. Inhibitory glikoproteiny (Gp) IIB/IIIA Blokowanie receptora glikoproteiny (Gp) IIB/IIIA jest wspólnym etapem końcowym hamowania agregacji płytek. Eptifibatyd oraz tirofiban hamują receptor Gp IIB/IIIA w sposób odwracalny, podczas gdy abciksymab prowadzi do nieodwracalnej blokady. Wyniki starszych badań prowadzonych przed erą stentów promują zastosowanie głównie tej klasy leków 46,47. Nowsze badania w większości dokumentują brak ich działania lub pogorszenie wyników leczenia Ponadto w większości badań popierających te leki, jak również w tych obojętnych oraz wykazujących brak ich działania doszło do krwawienia u większej ilości pacjentów leczonych blokerami receptora Gp IIB/IIIA, niż u osób nie otrzymujących takiego leczenia. Obecnie nie ma wystarczających danych popierających rutynowe leczenie wstępne pacjentów ze STEMI lub NSTEMI-OZW inhibitorami Gp IIB/IIIA. U pacjentów wysokiego ryzyka z NSTEMI-OZW akceptuje się wewnątrzszpitalne leczenie wstępne eptifibatydem oraz tirofibanem, podczas gdy abciksymab można podawać tylko w kontekście PCI 47,52. Ze względu na zwiększone ryzyko krwawienia podczas stosowania brokerów Gp IIB/ IIIA w połączeniu z heparynami należy rozważyć nowsze alternatywy leczenia przeciwpłytkowego. Antytrombiny Heparyna niefrakcjonowana (Unfractionated Heparin UFH) jest pośrednim inhibitorem trombiny i w połączeniu z ASA wykorzystuje się ją jako uzupełnienie terapii fibrynolitycznej lub pierwotnej PCI. Stanowi ona istotną część leczenia niestabilnej dusznicy bolesnej lub STEMI. Ograniczeniem stosowania niefrakcjonowanej heparyny jest jej zmienny osobniczo efekt antykoagulacyjny, konieczność podaży dożylnej leku oraz monitorowania aptt. Co więcej, stosowanie heparyny może powodować trombocytopenię. Od czasu opublikowania Wytycznych Europejskiej Rady Resuscytacji w 2005 roku dotyczących ostrych zespołów wieńcowych przeprowadzono duże randomizowane badania testujące kilka alternatywnych antytrombin stosowanych w leczeniu pacjentów z OZW. W porównaniu z heparyną niefrakcjonowaną leki te mają bardziej specyficzną aktywność czynnika Xa (heparyny drobnocząsteczkowe [LMWH Low Molecular Weight Heparins], fondaparynuks) lub są bezpośrednimi inhibitorami trombiny (biwalirudyna). Zasadniczo przy stosowaniu nowszych antytrombin nie ma konieczności monitorowania układu krzepnięcia, jak również istnieje mniejsze ryzyko wystąpienia trombocytopenii. Antytrombiny w NSTEMI-OZW W porównaniu z niefrakcjonowaną heparyną enoksaparyna podana w ciągu pierwszych godzin od epizodu NSTEMI-OZW obniża łącznie całkowitą śmiertelność, częstość zawału mięśnia sercowego oraz potrzebę pilnej rewaskularyzacji 53,54. Choć w przypadku enoksaparyny ilość mniejszych krwawień wzrasta, to w porównaniu z UFH występowanie poważnych powikłań krwotocznych nie jest częstsze. Krwawienie pogarsza rokowanie u pacjentów z OZW 55. Fondaparynuks oraz biwalirudyna powodują mniej krwawień niż UFH W większości badań nad pacjentami z objawami NSTEMI-OZW leki alternatywne dla UFH były podawane dopiero po przyjęciu do szpitala; nie można polegać na wynikach ekstrapolacji tych danych, dla postępowania w środowisku przedszpitalnym lub w SOR. Fondaparynuks oraz enoksaparyna są dobrą alternatywą dla UFH u pacjentów z planowanym leczeniem zachowawczym. Jednakże nie ma wystarczających danych, aby polecić jakąkolwiek inną LMWH niż enoksaparynę. U pacjentów ze zwiększonym ryzykiem krwawienia należy rozważyć podanie fondaparynuksu lub biwalirudyny. Jeśli planuje się leczenie inwazyjne, dobrą alternatywą dla UFH są enoksaparyna lub biwalirudyna. W jednym badaniu zaobserwowano obecność skrzepliny na cewniku wewnątrznaczyniowym u pacjentów poddawanych PCI, którzy otrzymywali fondaparynuks konieczna była dodatkowa dawka UFH 56. W związku z akumulacją enoksaparyny oraz fondaparynuksu u pacjentów z niewydolnością nerek niezbędne jest dostosowanie dawki tych leków; w tej sytuacji dobrą alternatywą są biwalirudyna lub UFH. Zmiana leku przeciwkrzepliwego może prowadzić do wzrostu ryzyka krwawienia, dlatego należy kontynuować raz podany lek za wyjątkiem fondaparynuksu, kiedy u pacjentów poddawanych PCI wymagana jest dodatkowa dawka UFH 60. Antytrombiny w STEMI Antytrombiny u pacjentów, u których planuje się fibrynolizę Enoksaparyna Kilka randomizowanych badań przeprowadzonych u pacjentów ze STEMI poddawanych fibrynolizie udowodniło, że dodatkowe leczenie enoksaparyną zamiast UFH skutkuje lepszymi wynikami klinicznymi (niezależnie od stosowanego leku fibrynolitycznego), a jednocześnie nieznacznie zwiększonym ryzykiem krwawienia u pacjentów starszych ( 75. roku życia) oraz z niską masą ciała (masa ciała <60 kg) Zmniejszone dawki enoksaparyny u starszych oraz u pacjentów z niską masą ciała umożliwiają utrzymanie dobrych wyników leczenia i zmniejszają ryzyko krwawienia 64. Rozsądnym jest również podawanie enoksaparyny zamiast UFH w leczeniu przedszpitalnym. Dawkowanie enoksaparyny: u pacjentów <75. roku życia należy podać wstępny bolus 30 mg iv, a następnie 1 mg/kg sc 5
176 174 H.-R. Arntz, L.L. Bossaert, N. Danchin, N.I. Nikolaou 5 co 12 godzin (pierwsza dawka podskórna zaraz po podaniu bolusa dożylnego). U pacjentów 75. roku podaje się 0,75 mg/kg sc co 12 godzin bez wstępnej dawki dożylnej. Pacjenci z rozpoznaną upośledzoną funkcją nerek (klirens kreatyniny <30 ml/min) mogą otrzymywać 1 mg/kg enoksaparyny podskórnie raz dziennie lub mogą być leczeni UFH. Nie ma wystarczających danych, by zalecać stosowanie innej LMWH. Fondaparynuks W kilku badaniach nad pacjentami ze STEMI wykazano większą lub podobną skuteczność fondaparynuksu w porównaniu z UFH jako dodatkowego leku podawanego przy fibrynolizie 56. Stosowanie fondaparynuksu (dawka początkowa 2,5 mg sc, a następnie 2,5 mg sc raz na dobę) powinno się rozważyć szczególnie w połączeniu z lekami fibrynolitycznymi niespecyficznymi dla fibryny (np. streptokinazą) u pacjentów z osoczowym stężeniem kreatyniny <3 mg/dl (250 μmol/l). Biwalirudyna Nie ma wystarczających danych, aby zalecić stosowanie biwalirudyny zamiast UFH u pacjentów ze STEMI leczonych fibrynolizą. Ponieważ wraz ze zmianą leku przeciwkrzepliwego wzrasta ryzyko krwawienia, powinno się utrzymać środek podany pierwotnie, za wyjątkiem fondaparynuksu, który wymaga podaży dodatkowej UFH, jeśli planuje się zabieg inwazyjny 60. Antytrombiny u pacjentów, u których planuje się pierwotną PCI (PPCI) Istnieje niewiele badań nad stosowaniem leczenia przeciwkrzepliwego w opiece przedszpitalnej lub na oddziale ratunkowym u pacjentów ze STEMI i planowaną PPCI. Dlatego też do czasu udostępnienia wyników toczących się obecnie badań, zalecenia lecznicze dla tych warunków muszą być ekstrapolowane z badań obejmujących postępowanie wewnątrzszpitalne. Enoksaparyna Analizy kilku baz danych oraz mniejszych badań wykazały lepsze lub podobne wyniki, kiedy porównywano enoksaparynę z UFH w czasie aktualnie stosowanej PPCI (np. z szerokim zastosowaniem tienopirydyny oraz/lub blokera receptora Gp IIB/IIIA) 65,66. Z tego powodu enoksaparyna jest bezpieczną i skuteczną alternatywą dla UFH. Nie ma wystarczających danych, by zalecić stosowanie innej niż enoksaparyna LMWH do PPCI u pacjentów ze STEMI. Zamiana UFH na enoksaparynę lub vice versa może prowadzić do zwiększonego ryzyka krwawienia i dlatego powinno się jej unikać 60. Pacjenci z upośledzoną funkcją nerek wymagają odpowiedniego dostosowania dawki leku. Fondaparynuks W porównaniu z UFH fondaparynuks ma podobne wyniki skuteczności, ale mniejszą częstość krwawienia, kiedy podawany jest w kontekście PPCI 56, jednakże ze względu na powstawanie skrzepów na cewnikach wewnątrznaczyniowych wymaga dodatkowego leczenia UFH. Nawet jeśli fondaparynuks zmniejsza ryzyko krwawienia w porównaniu z UFH u pacjentów ze STEMI poddawanych PPCI, stosowanie dwóch leków zamiast podawania wyłącznie UFH nie jest zalecane. Pacjenci z upośledzoną funkcją nerek wymagają odpowiedniego dostosowania dawki leku. Biwalirudyna Dwa duże randomizowane badania wykazały mniejszą częstość krwawienia oraz zmniejszenie krótko i długoterminowej śmiertelności, kiedy porównywano biwalirudynę i UFH wraz z blokerami dla receptora Gp IIB/IIIA u pacjentów ze STEMI i planowaną PCI Kilka innych badań oraz serii przypadków także wskazywało na lepsze lub podobne wyniki oraz mniejszą ilość krwawień przy porównaniu biwalirudyny oraz UFH; dlatego też biwalirudyna jest bezpieczną alternatywą dla UFH. Jednakże w ciągu pierwszych 24 godzin po PCI obserwowano nieznacznie większą częstość zakrzepicy w stencie 67. Strategie oraz systemy opieki medycznej Prowadzono badania nad kilkoma rodzajami strategii, których celem była poprawa przedszpitalnej opieki nad pacjentami z OZW. Wszystkie one mają zasadniczo na celu szybką identyfikację pacjentów ze STEMI, tak aby skrócić opóźnienie w leczeniu reperfuzyjnym. Ponadto opracowano kryteria przeprowadzania kwalifikacji pacjentów i wyodrębnienia chorych wysokiego ryzyka z NSTEMI-OZW, którzy wymagają transportu do ośrodka najwyższego stopnia referencyjności przeprowadzającego PCI w systemie całodobowym. W tym kontekście podczas wstępnej opieki nad pacjentem, obejmującej podstawowe czynności diagnostyczne oraz ocenę 12-odprowadzeniowego EKG, konieczne jest podjęcie kilku dodatkowych decyzji. Te decyzje odnoszą się do: 1. Strategii reperfuzyjnej u pacjentów ze STEMI, np. PPCI lub (przed)szpitalna fibrynoliza. 2. Ominięcia najbliższego, ale nie oferującego PCI szpitala oraz podjęcie kroków mających na celu skrócenie opóźnienia interwencji, jeśli zadecydowano o przeprowadzeniu PPCI. 3. Procedur w warunkach szczególnych, np. u pacjentów skutecznie zresuscytowanych po nieurazowym zatrzymaniu krążenia, pacjentów we wstrząsie lub pacjentów z NSTEMI-OZW, którzy są niestabilni lub mają objawy świadczące o wysokim ryzyku. Terapia reperfuzyjna u pacjentów z objawami STEMI Terapia reperfuzyjna jest najważniejszym osiągnięciem ostatnich 25 lat w leczeniu STEMI. U wszystkich pacjentów z rozpoznanym STEMI terapia reperfuzyjna powinna być rozpoczęta tak szybko, jak to tylko możliwe, bez względu na wybór metody, w czasie nie dłuższym niż 12 godzin od wystąpienia objawów 7, Reperfuzję można uzyskać poprzez fibrynolizę, PPCI lub kombinację obu metod. Korzyści z leczenia reperfuzyjnego zmniejszają się z czasem, który upłynął od wystąpienia objawów. Fibrynoliza jest najbardziej skuteczna, jeżeli terapię rozpocznie się w ciągu pierwszych 2 do 3 godzin od wystąpienia objawów; skuteczność PPCI w mniejszym stopniu zależy od czasu 73.
177 Wstępne postępowanie w ostrych zespołach wieńcowych 175 Fibrynoliza Metaanaliza sześciu badań z udziałem 6434 pacjentów wykazała 17-procentowe zmniejszenie śmiertelności u pacjentów, u których wdrożono leczenie fibrynolityczne przed przyjęciem do szpitala, w porównaniu z fibrynolizą rozpoczętą w szpitalu 74. Efektywne i bezpieczne stosowanie przedszpitalnej fibrynolizy wymaga, aby dostępne były odpowiednie środki do diagnostyki i leczenia STEMI oraz jego powikłań. Optymalnym rozwiązaniem byłaby możliwość konsultacji z doświadczonym lekarzem w szpitalu (np. specjalista medycyny ratunkowej lub kardiolog). Przedszpitalne zastosowanie fibrynolizy skracało czas do rozpoczęcia terapii średnio o 60 minut, a jej wyniki były niezależne od doświadczenia osób prowadzących leczenie. Dlatego w przypadku STEMI lub objawów OZW z podejrzeniem świeżego LBBB w zapisie EKG korzystne jest podawanie fibrynolityków przed przyjęciem do szpitala. Leczenie fibrynolityczne może być bezpiecznie wdrożone przez przeszkolonych ratowników medycznych, pielęgniarki lub lekarzy przy wykorzystaniu odpowiednich protokołów postępowania Skuteczność tego leczenia jest najwyższa w pierwszych 3 godzinach od wystąpienia objawów 74. U pacjentów z objawami OZW i zmianami o charakterze STEMI w zapisie EKG (lub obecnością świeżego LBBB czy potwierdzonym zawałem ściany tylnej), którzy zgłaszają się bezpośrednio na oddział ratunkowy, należy jak najszybciej rozpocząć leczenie fibrynolityczne, chyba że możliwa jest natychmiastowa PPCI. Tabela 5.1. Przeciwwskazania do fibrynolizy* Przeciwwskazania bezwzględne: Przebyty kiedykolwiek udar krwotoczny lub udar o nieznanej etiologii Udar niedokrwienny przebyty w ciągu ostatnich 6 miesięcy Uraz lub nowotwór CSN Przebyty duży uraz/zabieg/uraz głowy (w ciągu ostatnich 3 tygodni) Krwawienie z przewodu pokarmowego w ciągu ostatniego miesiąca Znane zaburzenia układu krzepnięcia Tętniak rozwarstwiający aorty Przeciwwskazania względne: TIA w ciągu ostatnich 6 miesięcy Doustna terapia przeciwzakrzepowa Ciąża i do pierwszego tygodnia połogu Nakłucie w miejscu niepoddającym się uciskowi Resuscytacja urazowa Nadciśnienie oporne na działanie leków (ciśnienie skurczowe >180 mm Hg) Zaawansowana choroba wątroby Infekcyjne zapalenie wsierdzia Czynna choroba wrzodowa * zgodnie z zaleceniami European Society of Cardiology Ryzyko leczenia fibrynolitycznego Personel medyczny stosujący fibrynolizę musi mieć świadomość istniejącego ryzyka oraz przeciwwskazań do jej wdrożenia (tabela 5.1). Pacjenci z rozległym zawałem mięśnia sercowego (np. posiadający rozległe cechy niedokrwienia w zapisie EKG) należą do grupy chorych, u których leczenie fibrynolityczne może przynieść największe korzyści. Korzyści z zastosowania terapii fibrynolitycznej są w przypadku zawału w zakresie ściany dolnej mniejsze niż w zakresie ściany przedniej. Starsi pacjenci mają wyższe bezwzględne ryzyko zgonu, jakkolwiek bezwzględna korzyść z zastosowania fibrynolizy jest porównywalna z wynikami tego sposobu postępowania u młodszych pacjentów. U osób powyżej 75. roku życia istnieje zwiększone ryzyko krwawienia wewnątrzczaszkowego jako powikłania fibrynolizy, co zmniejsza bezwzględną korzyść z takiego leczenia. Ryzyko krwawienia wewnątrzczaszkowego zwiększa się w grupie pacjentów z wartościami skurczowego ciśnienia tętniczego krwi powyżej 180 mm Hg. Tak zaawansowane nadciśnienie tętnicze jest względnym przeciwwskazaniem do stosowania fibrynolizy. Ryzyko krwawienia śródczaszkowego zależy także od prowadzonego leczenia przeciwkrzepliwego i przeciwpłytkowego. Pierwotne przezskórne interwencje wieńcowe Angioplastyka wieńcowa, z implantacją stentu lub bez, stała się leczeniem z wyboru u pacjentów ze STEMI, ponieważ w kilku badaniach i metaanalizach wykazano wyższość tego sposobu postępowania nad fibrynolizą w obniżaniu częstości występowania łącznego punktu końcowego: zgonu, udaru oraz powtórnego zawału 81,82. Tego rodzaju poprawę obserwowano, gdy PPCI było wykonywane przez doświadczone osoby, w dużych ośrodkach, z minimalnym opóźnieniem pomiędzy pierwszym kontaktem z personelem medycznym a pierwszym napełnieniem balonu 83. Z tego powodu PPCI przeprowadzona w dużym ośrodku, w niedługim czasie po pierwszym kontakcie z personelem medycznym, przez doświadczonego operatora, który utrzymuje odpowiednio wysoki poziom wyszkolenia, jest preferowanym sposobem leczenia, a w porównaniu z natychmiast przeprowadzoną fibrynolizą charakteryzuje się mniejszą chorobowością i śmiertelnością. Porównanie fibrynolizy z pierwotną PCI Ograniczeniami pierwotnej PCI są dostępność pracowni hemodynamiki, odpowiednio wyszkolonego personelu oraz opóźnienie czasu do pierwszego napełnienia balonu. Fibrynoliza jest powszechnie dostępną metodą leczenia reperfuzyjnego. Obie strategie lecznicze są dobrze udokumentowane i poddane ocenie w dużych, wieloośrodkowych, randomizowanych badaniach klinicznych, prowadzonych w ciągu kilku ostatnich dekad. W tym czasie obie metody ulegały znacznym zmianom, a w związku z tym dane z badań są niejednorodne. W randomizowanych badaniach porównujących PPCI i leczenie fibrynolityczne średni czas pomiędzy podjęciem decyzji terapeutycznej a rozpoczęciem leczenia dla obu metod wynosił mniej niż 60 minut. Kilka raportów i przeglądów porównujących leczenie fibrynolityczne (w tym przedszpitalne podanie leku) z PPCI wskazywało na lepszą przeżywalność, jeśli fibrynolizę rozpoczęto do 2 godzin od wystąpienia objawów, a następnie przeprowadzono ratunkową lub opóźnioną PCI W przeglądach, które bardziej realistycznie odzwierciedlają codzienną praktykę medyczną, akceptowane opóźnienie związane z przeprowadzeniem PPCI (np. od rozpoznania do napełnienia balonu minus od rozpoznania do podania leku fibrynolitycznego), które nadal zapewnia wyższość PPCI nad fibry- 5
178 176 H.-R. Arntz, L.L. Bossaert, N. Danchin, N.I. Nikolaou 5 nolizą, znacznie się waha i wynosi pomiędzy 45 a >180 minut, zależnie od stanu pacjenta (np. wiek, lokalizacja zawału oraz czas trwania objawów) 87. Ponadto pojedyncze badania wykazały większą korzyść z PPCI niż z fibrynolizy w specyficznych grupach pacjentów, na przykład u pacjentów po zabiegach CABG, z niewydolnością nerek lub z cukrzycą 88,89. Czas niezbędny do rozpoczęcia PCI można znacznie skrócić, jeśli poprawi się system opieki nad pacjentami 13,90-93, na przykład: Wykonując przedszpitalny zapis EKG Przesyłając zapis EKG do przyjmującego szpitala Organizując możliwość telefonicznego postawienia w stan gotowości pracowni hemodynamiki Zapewniając gotowość pracowni do zabiegu w czasie do 20 minut Zapewniając w szpitalu całodobową konsultację specjalisty kardiologa Na bieżąco podając wyniki badań Zapewniając nadzór starszych, doświadczonych lekarzy Zachęcając do zespołowej opieki nad pacjentem. Jeśli w odpowiednim przedziale czasu nie da się przeprowadzić PPCI, należy, niezależnie od potrzeby pilnego przeniesienia pacjenta do innego ośrodka, rozważyć natychmiastową fibrynolizę, o ile nie ma do niej przeciwwskazań. U pacjentów, u których są przeciwwskazania do leczenia fibrynolitycznego, powinno się nadal dążyć do przeprowadzenia PCI, niezależnie od opóźnienia leczenia, zamiast w ogóle rezygnować z terapii reperfuzyjnej. U pacjentów we wstrząsie ze STEMI leczeniem z wyboru jest pierwotna PCI (lub zabieg pomostowania aortalno-wieńcowego). W tych wypadkach fibrynolizę powinno się rozważyć wyłącznie wtedy, gdy ma miejsce znaczące opóźnienie PCI. Kwalifikacja pacjentów oraz przekazywanie ich od innego ośrodka celem wykonania pierwotnej PCI Ryzyko zgonu, ponownego zawału albo udaru jest obniżone, jeżeli pacjenci ze STEMI są natychmiastowo przekazywani z ośrodków o niższej referencyjności do ośrodków mogących wykonać PPCI 82,94,95. W grupie młodszych pacjentów z zawałem ściany przedniej, u których czas od wystąpienia objawów wynosi poniżej 2 3 godzin, nie wyjaśniono, czy więcej korzyści przyniesie przedszpitalna fibrynoliza, czy pierwotne PCI 87. Uzasadnione jest przekazywanie pacjentów ze STEMI celem wykonania pierwotnej PCI wtedy, gdy czas od wystąpienia objawów mieści się w przedziale od 3 12 godzin, a transport jest natychmiast dostępny. Połączenie fibrynolizy i przezskórnej interwencji wieńcowej Aby przywrócić wieńcowy przepływ krwi oraz perfuzję mięśnia sercowego, można w różnych połączeniach stosować fibrynolizę oraz PCI. Istnieje kilka sposobów na połączenie tych dwóch rodzajów terapii. Niestety brak jest jednolitego nazewnictwa dla PCI przeprowadzanej w takich okolicznościach. Torowana PCI określa PCI przeprowadzoną natychmiast po fibrynolizie, podejście farmakologiczno-inwazyjne odnosi się do PCI planowo przeprowadzonej w czasie 3 do 24 godzin po fibrynolizie, a ratunkowa PCI to PCI przeprowadzana po nieudanej próbie leczenia reperfuzyjnego (określanej jako <50% normalizacji uniesienia odcinka ST po 60 do 90 minutach od zakończenia terapii fibrynolitycznej). Te strategie różnią się od standardowego podejścia, w którym angiografię i interwencję wykonuje się w kilka dni po udanej fibrynolizie. Kilka badań i metaanaliz wskazuje na gorsze wyniki leczenia, jeśli rutynowo przeprowadza się PCI zaraz po fibrynolizie lub tak szybko, jak to jest możliwe 48,95. Dlatego nie poleca się przeprowadzania planowo torowanej PCI, nawet jeśli mogą być podgrupy pacjentów, dla których takie postępowanie byłoby korzystne 96. U pacjentów z nieudaną fibrynolizą, rozpoznaną na podstawie objawów klinicznych oraz/lub niedostatecznej normalizacji odcinka ST powinno się niezwłocznie wykonać angiografię oraz PCI 97. W przypadku klinicznie skutecznej fibrynolizy (rozpoznanej na podstawie objawów klinicznych lub normalizacji odcinka ST >50%) zaobserwowano poprawę rokowania, jeśli angiografię wykonano kilka godzin po fibrynolizie (podejście farmakologiczno-inwazyjne). Po zakończonej fibrynolizie ten sposób leczenia wymaga wczesnego przekazania pacjenta do ośrodka wykonującego angiografię i PCI 98,99. Sytuacje szczególne Wstrząs kardiogenny Wstrząs kardiogenny (a szerzej ujmując ciężka niewydolność lewokomorowa) jest jednym z powikłań występujących w przebiegu OZW. Śmiertelność w tych przypadkach wynosi powyżej 50%. Wstrząs kardiogenny w przebiegu STEMI nie stanowi przeciwwskazania do leczenia fibrynolitycznego, jakkolwiek PCI jest postępowaniem z wyboru. Wczesna rewaskularyzacja (PPCI, wczesna PCI po fibrynolizie) jest wskazana u pacjentów, u których wstrząs rozwinął się do 36 godzin od wystąpienia objawów AMI i spełniają oni kryteria jej przeprowadzenia 100. U pacjentów z zawałem dolnej ściany mięśnia sercowego i objawami wstrząsu przy braku zastoju nad polami płucnymi należy podejrzewać zawał prawej komory. Uniesienie odcinka ST 1 mm w odprowadzeniu RV4 jest pomocne w identyfikacji zawału prawej komory. W tej grupie pacjentów śmiertelność wewnątrzszpitalna wynosi do 30% i wielu z nich odnosi dużą korzyść z leczenia reperfuzyjnego. Należy u nich unikać podaży nitratów i innych leków rozszerzających naczynia, a w przypadku niskich wartości ciśnienia stosować płynoterapię. Reperfuzja po skutecznej resuscytacji Choroba niedokrwienna serca jest najczęstszą pozaszpitalną przyczyną zatrzymania krążenia. Wielu z tych pacjentów będzie miało objawy ostrej niedrożności tętnicy wieńcowej z objawami STEMI w zapisie EKG, jednakże zatrzymanie krążenia w przebiegu choroby niedokrwiennej serca może mieć miejsce także w przypadku braku tych zmian. W kilku seriach przypadków pokazano, że możliwe jest wykonanie angiografii i, jeśli to konieczne, PCI u pacjentów ze spontanicznym powrotem krążenia po NZK. U wielu pacjentów możliwe jest uwidocznienie a następnie leczenie zamknięcia lub znacznego zwężenia tętnic wieńcowych. U pacjentów z objawami STEMI w zapisie EKG alternatywą może być fibrynoliza 101. Z tego powodu u pacjen-
179 Wstępne postępowanie w ostrych zespołach wieńcowych 177 tów ze STEMI lub świeżym blokiem lewej odnogi pęczka Hisa (LBBB) w EKG występującymi po ROSC po pozaszpitalnym zatrzymaniu krążenia powinno się rozważyć natychmiastową angiografię i interwencję przezskórną lub fibrynolizę 102,103. Wydaje się także uzasadnione wykonanie natychmiastowej angiografii i PCI u wybranych pacjentów pomimo braku uniesienia odcinka ST lub uprzednich objawów, takich jak ból w klatce piersiowej. Należy uwzględnić leczenie reperfuzyjne w standardowym postępowaniu po zatrzymaniu krążenia, jako strategii poprawiającej rokowanie 104. Leczenie reperfuzyjne nie powinno wykluczać innych metod leczniczych, w tym terapeutycznej hipotermii. Prewencja pierwotna i wtórna Postępowanie prewencyjne u pacjentów z objawami OZW powinno być rozpoczęte zaraz po przyjęciu do szpitala, jak również powinny być kontynuowane już podjęte działania. Środki zapobiegawcze poprawiają rokowanie, zmniejszając częstość ciężkich powikłań sercowych. Prewencja farmakologiczna obejmuje stosowanie beta-blokerów, inhibitorów enzymu konwertującego angiotensynę (ACE)/blokerów receptora dla angiotensyny (ARB) oraz statyn, a także podstawowe leczenie aspiryną i, jeśli są wskazania, tienopirydynami. Beta-blokery Kilka badań, głównie przeprowadzonych przed erą reperfuzji dowodzi, że wczesna terapia beta-blokerami zmniejsza śmiertelność, częstość występowania kolejnych zawałów oraz pęknięcia mięśnia sercowego, jak również incydentów migotania komór czy nadkomorowych zaburzeń rytmu 105. W przypadku przeprowadzenia pierwotnego PCI, dożylne podanie beta-blokerów pacjentom nieprzyjmującym wcześniej tych leków doustnie również obniża śmiertelność. Badania nad beta-blokerami są bardzo niejednorodne, jeśli chodzi o czas rozpoczęcia terapii. Niewiele jest danych na temat podawania tych leków w opiece przedszpitalnej lub w oddziale ratunkowym. Ponadto ostatnie badania wskazują na zwiększone ryzyko rozwoju wstrząsu kardiogennego u pacjentów ze STEMI, nawet jeśli dzięki podawaniu betablokerów zmniejszyła się częstość ciężkich częstoskurczy 106. Nie ma dowodów popierających rutynowe podawanie dożylne beta-blokerów w środowisku przedszpitalnym lub zaraz po przyjęciu do oddziału ratunkowego. Ich stosowanie może być wskazane w sytuacjach szczególnych, takich jak ciężkie nadciśnienie tętnicze lub częstoskurcz, jeśli nie ma żadnych przeciwwskazań. Po ustabilizowaniu stanu pacjenta można rozpocząć leczenie doustnymi beta-blokerami w niskiej dawce. Leki antyarytmiczne Nie ma dowodów na korzystne działanie profilaktyczne leków antyarytmicznych w przebiegu OZW. Migotanie komór (VF) jest przyczyną większości wczesnych zgonów w przebiegu OZW. Częstość występowania VF jest najwyższa w pierwszych godzinach od wystąpienia objawów. Tłumaczy to, dlaczego przeprowadzono tak wiele badań mających na celu ocenę skuteczności profilaktycznego zastosowania leków antyarytmicznych 107. Badano efekt działania leków przeciwarytmicznych (lidokaina, magnez, dizopiramid, meksyletyna, werapamil, sotalol, tokainamid), podanych profilaktycznie pacjentom z OZW. Profilaktyczne podawanie lidokainy zmniejsza częstość występowania VF, lecz może zwiększyć śmiertelność 108. Rutynowe podawanie magnezu u pacjentów z AMI nie obniża śmiertelności. Zapobiegawcze podawanie dizopiramidu, meksyletyny, werapamilu lub innych leków antyarytmicznych w pierwszych godzinach OZW również nie zmniejszyło śmiertelności. Z tego powodu profilaktyczne stosowanie leków antyarytmicznych nie jest zalecane. Inhibitory enzymu konwertującego angiotensynę i blokery receptora dla angiotensyny Doustne inhibitory enzymu konwertującego angiotensynę (ACE) zmniejszają śmiertelność u pacjentów z AMI, niezależnie, czy stosowano terapię reperfuzyjną, czy nie. Korzystny efekt jest najbardziej zaznaczony u pacjentów z zawałem przedniej ściany mięśnia sercowego, towarzyszącym zastojem płucnym lub frakcją wyrzutową <40%. Nie należy podawać inhibitorów ACE, jeżeli skurczowe ciśnienie krwi w chwili przyjęcia jest niższe niż 100 mm Hg lub gdy znane są przeciwwskazania do użycia leku. W przypadku podawania inhibitorów ACE dożylnie w 1. dobie od wystąpienia objawów udokumentowano zwiększoną śmiertelność. Zaleca się zatem podaż doustną inhibitorów ACE w pierwszych 24 godzinach od pojawienia się objawów u pacjentów z AMI, niezależnie od planowanej później terapii reperfuzyjnej. Jest to szczególnie korzystne w przypadku zawału przedniej ściany mięśnia sercowego, zastoju płucnego oraz frakcji wyrzutowej <40%. Nie zaleca się dożylnego podawania inhibitorów ACE w ciągu pierwszych 24 godzin od wystąpienia objawów. W przypadku nietolerancji leków hamujących ACE należy stosować blokery receptora dla angiotensyny 109,110. Statyny Statyny zmniejszają częstość występowania ciężkich powikłań sercowych (major adverse cardiovascular events), jeśli zostaną podane w ciągu kilku dni od wystąpienia OZW 111,112. Rozpoczęcie leczenia statynami powinno się rozważyć w ciągu 24 godzin od pojawienia się objawów OZW, chyba że istnieją przeciwwskazania do ich podawania (należy dążyć do utrzymywania poziomu cholesterolu LDL <80 mg dl -1 [2,1 mmol l -1 ]). Jeżeli u pacjentów prowadzona jest już terapia statynami, nie należy jej przerywać 113. Bibliografia 1. Tunstall-Pedoe H, Vanuzzo D, Hobbs M, et al. Estimation of contribution of changes in coronary care to improving survival, event rates, and coronary heart disease mortality across the WHO MONICA Project populations. Lancet 2000;355: Fox KA, Cokkinos DV, Deckers J, Keil U, Maggioni A, Steg G. The ENACT study: a pan-european survey of acute coronary syndromes. European Network for Acute Coronary Treatment. Eur Heart J 2000;21: Goodman SG, Huang W, Yan AT, et al. The expanded Global Registry of Acute Coronary Events: baseline characteristics, management practices, and hospital outcomes of patients with acute coronary syndromes. Am Heart J 2009;158, e1 5. 5
180 178 H.-R. Arntz, L.L. Bossaert, N. Danchin, N.I. Nikolaou 5 4. Lowel H, Meisinger C, Heier M, et al. Sex specific trends of sudden cardiac death and acute myocardial infarction: results of the population-based KORA/MONICA-Augsburg register 1985 to Dtsch Med Wochenschr 2002;127: Thygesen K, Alpert JS, White HD. Universal definition of myocardial infarction. Eur Heart J 2007;28: Van de Werf F, Bax J, Betriu A, et al. Management of acute myocardial infarction in patients presenting with persistent ST-segment elevation: the task force on the management of ST-segment elevation acute myocardial infarction of the European Society of Cardiology. Eur Heart J 2008;29: Antman EM, Anbe DT, Armstrong PW, et al. ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 1999 Guidelines for the Management of Patients With Acute Myocardial Infarction). Circulation 2004;110: Khraim FM, Carey MG. Predictors of pre-hospital delay among patients with acute myocardial infarction. Patient Educ Couns 2009;75: Douglas PS, Ginsburg GS. The evaluation of chest pain in women. N Engl J Med 1996;334: Solomon CG, Lee TH, Cook EF, et al. Comparison of clinical presentation of acute myocardial infarction in patients older than 65 years of age to younger patients: the Multicenter Chest Pain Study experience. Am J Cardiol 1989;63: Henrikson CA, Howell EE, Bush DE, et al. Chest pain relief by nitroglycerin does not predict active coronary artery disease. Ann Intern Med 2003;139: Ioannidis JP, Salem D, Chew PW, Lau J. Accuracy and clinical effect of out-of- -hospital electrocardiography in the diagnosis of acute cardiac ischemia: a metaanalysis. Ann Emerg Med 2001;37: Terkelsen CJ, Lassen JF, Norgaard BL, et al. Reduction of treatment delay in patients with ST-elevation myocardial infarction: impact of pre-hospital diagnosis and direct referral to primary percutanous coronary intervention. Eur Heart J 2005;26: Brainard AH, Raynovich W, Tandberg D, Bedrick EJ. The prehospital 12- lead electrocardiogram s effect on time to initiation of reperfusion therapy: a systematic review and meta-analysis of existing literature. Am J Emerg Med 2005;23: Swor R, Hegerberg S, McHugh-McNally A, Goldstein M, McEachin CC. Prehospita l12-lead ECG: efficacy or effectiveness? Prehosp Emerg Care 2006;10: Masoudi FA, Magid DJ, Vinson DR, et al. Implications of the failure to identify high-risk electrocardiogram findings for the quality of care of patients with acute myocardial infarction: results of the Emergency Department Quality in Myocardial Infarction (EDQMI) study. Circulation 2006;114: Feldman JA, Brinsfield K, Bernard S, White D, Maciejko T. Real-time paramedic compared with blinded physician identification of ST-segment elevation myocardial infarction: results of an observational study. Am J Emerg Med 2005;23: Kudenchuk PJ, Ho MT, Weaver WD, et al. Accuracy of computer-interpreted electrocardiography in selecting patients for thrombolytic therapy. MITI Project Investigators. J Am Coll Cardiol 1991;17: Dhruva VN, Abdelhadi SI, Anis A, et al. ST-segment analysis using wireless technology in acute myocardial infarction (STAT-MI) trial. J Am Coll Cardiol 2007;50: Antman EM, Tanasijevic MJ, Thompson B, et al. Cardiac-specific troponin I levels to predict the risk of mortality in patients with acute coronary syndromes. N Engl J Med 1996;335: Collinson PO, Gaze DC, Morris F, Morris B, Price A, Goodacre S. Comparison of biomarker strategies for rapid rule out of myocardial infarction in the emergency department using ACC/ESC diagnostic criteria. Ann Clin Biochem 2006;43: Schuchert A, Hamm C, Scholz J, Klimmeck S, Goldmann B, Meinertz T. Prehospital testing for troponin T in patients with suspected acute myocardial infarction. Am Heart J 1999;138: Keller T, Zeller T, Peetz D, et al. Sensitive troponin I assay in early diagnosis of acute myocardial infarction. N Engl J Med 2009;361: Renaud B, Maison P, Ngako A, et al. Impact of point-of-care testing in the emergency department evaluation and treatment of patients with suspected acute coronary syndromes. Acad Emerg Med 2008;15: Mitchell AM, Garvey JL, Kline JA. Multimarker panel to rule out acute coronary syndromes in low-risk patients. Acad Emerg Med 2006;13: Hess EP, Thiruganasambandamoorthy V, Wells GA, et al. Diagnostic accuracy of clinical prediction rules to exclude acute coronary syndrome in the emergency department setting: a systematic review. CJEM 2008;10: Farkouh ME, Smars PA, Reeder GS, et al. A clinical trial of a chest-pain observation unit for patients with unstable angina. Chest Pain Evaluation in the Emergency Room (CHEER) Investigators. N Engl J Med 1998;339: Ramakrishna G, Milavetz JJ, Zinsmeister AR, et al. Effect of exercise treadmill testing and stress imaging on the triage of patients with chest pain: CHEER substudy. Mayo Clin Proc 2005;80: Goldstein JA, Gallagher MJ, O Neill WW, Ross MA, O Neil BJ, Raff GL. A randomized controlled trial of multi-slice coronary computed tomography for evaluation of acute chest pain. J Am Coll Cardiol 2007;49: Forberg JL, Hilmersson CE, Carlsson M, et al. Negative predictive value and potential cost savings of acute nuclear myocardial perfusion imaging in low risk patients with suspected acute coronary syndrome: a prospective single blinded study. BMC Emerg Med 2009;9: Nucifora G, Badano LP, Sarraf-Zadegan N, et al. Comparison of early dobutamine stress echocardiography and exercise electrocardiographic testing for management of patients presenting to the emergency department with chest pain. Am J Cardiol 2007;100: Kearney PM, Baigent C, Godwin J, Halls H, Emberson JR, Patrono C. Do selective cyclo-oxygenase-2 inhibitors and traditional non-steroidal anti-inflammatory drugs increase the risk of atherothrombosis? Meta-analysis of randomised trials. BMJ 2006;332: Rawles JM, Kenmure AC. Controlled trial of oxygen in uncomplicated myocardial infarction. Br Med J 1976;1: Wijesinghe M, Perrin K, Ranchord A, Simmonds M, Weatherall M, Beasley R. Routine use of oxygen in the treatment of myocardial infarction: systematic review. Heart 2009;95: Cabello JB, Burls A, Emparanza JI, Bayliss S, Quinn T. Oxygen therapy for acute myocardial infarction. Cochrane Database Syst Rev 2010;6:CD O Driscoll BR, Howard LS, Davison AG. BTS guideline for emergency oxygen use in adult patients. Thorax 2008;63:vi Freimark D, Matetzky S, Leor J, et al. Timing of aspirin administration as a determinant of survival of patients with acute myocardial infarction treated with thrombolysis. Am J Cardiol 2002;89: Barbash IM, Freimark D, Gottlieb S, et al. Outcome of myocardial infarction in patients treated with aspirin is enhanced by pre-hospital administration. Cardiology 2002;98: Wiviott SD, Braunwald E, McCabe CH, et al. Prasugrel versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2007;357: Wallentin L, Becker RC, Budaj A, et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009;361: Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001;345: Mehta SR, Yusuf S, Peters RJ, et al. Effects of pretreatment with clopidogrel and aspirin followed by long-term therapy in patients undergoing percutaneous coronary intervention: the PCI-CURE study. Lancet 2001;358: Steinhubl SR, Berger PB, Mann JT, 3rd, et al. Early and sustained dual oral antiplatelet therapy following percutaneous coronary intervention: a randomized controlled trial. JAMA 2002;288: Chen ZM, Jiang LX, Chen YP, et al. Addition of clopidogrel to aspirin in 45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet 2005;366: Verheugt FW, Montalescot G, Sabatine MS, et al. Prehospital fibrinolysis with dual antiplatelet therapy in ST-elevation acute myocardial infarction: a substudy of the randomized double blind CLARITY-TIMI 28 trial. J Thromb Thrombolysis 2007;23: Bosch X, Marrugat J. Platelet glycoprotein IIb/IIIa blockers for percutaneous coronary revascularization, and unstable angina and non-st-segment elevation myocardial infarction. Cochrane Database Syst Rev 2001:CD Boersma E, Harrington RA, Moliterno DJ, et al. Platelet glycoprotein IIb/IIIa inhibitors in acute coronary syndromes: a meta-analysis of all major randomised clinical trials. Lancet 2002;359: [erratum appears in Lancet 2002 June 15;359(9323):2120]. 48. Keeley EC, Boura JA, Grines CL. Comparison of primary and facilitated percutaneous coronary interventions for ST-elevation myocardial infarction: quantitative review of randomised trials. Lancet 2006;367: Stone GW, Grines CL, Cox DA, et al. Comparison of angioplasty with stenting, with or without abciximab, in acute myocardial infarction. N Engl J Med 2002;346: van t Hof AW, Ernst N, de Boer MJ, et al. Facilitation of primary coronary angioplasty by early start of a glycoprotein 2b/3a inhibitor: results of the ongoing tirofiban in myocardial infarction evaluation (on-time) trial. Eur Heart J 2004;25: Pannu R, Andraws R. Effects of glycoprotein IIb/IIIa inhibitors in patients undergoing percutaneous coronary intervention after pretreatment with clopi-dogrel: a meta-analysis of randomized trials. Crit Pathw Cardiol 2008; 7: De Luca G, Gibson M, Bellandi F, et al. Early glycoprotein IIb IIIa inhibitors in primary angioplasty (EGYPT) cooperation. An individual patients data metaanalysis. Heart TIMI-11B Investigators, Antman EM, McCabe CH, et al. Enoxaparin prevents death and cardiac ischemic events in unstable angina/non-q-wave myocardial infarction. Results of the thrombolysis in myocardial infarction (TIMI) 11B trial. Circulation 1999;100: Cohen M, Demers C, Gurfinkel EP, et al. A comparison of low-molecularweight heparin with unfractionated heparin for unstable coronary artery disease. Efficacy and Safety of Subcutaneous Enoxaparin in Non-Q-Wave Coronary Events Study Group. N Engl J Med 1997;337: Moscucci M, Fox KA, Cannon CP, et al. Predictors of major bleeding in acute coronary syndromes: the Global Registry of Acute Coronary Events (GRACE). Eur Heart J 2003;24: Yusuf S, Mehta SR, Chrolavicius S, et al. Comparison of fondaparinux and enoxaparin in acute coronary syndromes. N Engl J Med 2006;354:
181 Wstępne postępowanie w ostrych zespołach wieńcowych Mehta SR, Boden WE, Eikelboom JW, et al. Antithrombotic therapy with fondaparinux in relation to interventional management strategy in patients with ST-and non-st-segment elevation acute coronary syndromes: an individual patient-level combined analysis of the Fifth and Sixth Organization to Assess Strategies in Ischemic Syndromes (OASIS 5 and 6) randomized trials. Circulation 2008;118: Lincoff AM, Bittl JA, Harrington RA, et al. Bivalirudin and provisional glycoprotein IIb/IIIa blockade compared with heparin and planned glycoprotein IIb/ IIIa blockade during percutaneous coronary intervention: REPLACE-2 randomized trial. JAMA 2003;289: Stone GW, McLaurin BT, Cox DA, et al. Bivalirudin for patients with acute coronary syndromes. N Engl J Med 2006;355: Ferguson JJ, Califf RM, Antman EM, et al. Enoxaparin vs unfractionated heparin in high-risk patients with non-st-segment elevation acute coronary syndromes managed with an intended early invasive strategy: primary results of the SYNERGY randomized trial. JAMA 2004;292: Efficacy and safety of tenecteplase in combination with enoxaparin, abciximab, or unfractionated heparin: the ASSENT-3 randomised trial in acute myocardial infarction. Lancet 2001;358: Eikelboom JW, Quinlan DJ, Mehta SR, Turpie AG, Menown IB, Yusuf S. Unfractionated and low-molecular-weight heparin as adjuncts to thrombolysis in aspirin-treated patients with ST-elevation acute myocardial infarction: a metaanalysis of the randomized trials. Circulation 2005;112: Wallentin L, Goldstein P, Armstrong PW, et al. Efficacy and safety of tenecteplase in combination with the low-molecular-weight heparin enoxaparin or unfractionated heparin in the prehospital setting: the assessment of the safety and efficacy of a new thrombolytic regimen (ASSENT)-3 PLUS randomized trial in acute myocardial infarction. Circulation 2003;108: Antman EM, Morrow DA, McCabe CH, et al. Enoxaparin versus unfractionated heparin with fibrinolysis for ST-elevation myocardial infarction. N Engl J Med 2006;354: Zeymer U, Gitt A, Junger C, et al. Efficacy and safety of enoxaparin in unselected patients with ST-segment elevation myocardial infarction. Thromb Haemost 2008;99: Zeymer U, Gitt A, Zahn R, et al. Efficacy and safety of enoxaparin in combination with and without GP IIb/IIIa inhibitors in unselected patients with ST segment elevation myocardial infarction treated with primary percutaneous coronary intervention. EuroIntervention 2009;4: White HD, Aylward PE, Frey MJ, et al. Randomized, double-blind comparison of hirulog versus heparin in patients receiving streptokinase and aspirin for acute myocardial infarction (HERO). Hirulog Early Reperfusion/Occlusion (HERO) Trial Investigators. Circulation 1997;96: Stone GW, Witzenbichler B, Guagliumi G, et al. Bivalirudin during primary PCI in acute myocardial infarction. N Engl J Med 2008;358: Madsen JK, Chevalier B, Darius H, et al. Ischaemic events and bleeding in patients undergoing percutaneous coronary intervention with concomitant bivalirudin treatment. EuroIntervention 2008;3: Bassand JP, Hamm CW, Ardissino D, et al. Guidelines for the diagnosis and treatment of non-st-segment elevation acute coronary syndromes. Eur Heart J 2007;28: Anderson JL, Adams CD, Antman EM, et al. ACC/AHA 2007 Guidelines for the Management of Patients With Unstable Angina/Non ST-Elevation Myocardial Infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines for the Management of Patients With Unstable Angina/Non ST-Elevation Myocardial Infarction): developed in collaboration with the American College of Emergency Physicians, the Society for Cardiovascular Angiography and Interventions, and the Society of Thoracic Surgeons: endorsed by the American Association of Cardiovascular and Pulmonary Rehabilitation and the Society for Academic Emergency Medicine. Circulation 2007;116: e Kushner FG, Hand M, Smith SC, Jr., et al., Focused updates: ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction (updating the 2004 Guideline and 2007 Focused Update) and ACC/ AHA/SCAI guidelines on percutaneous coronary intervention (updating the 2005 Guideline and 2007 Focused Update): a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation 2009;120: Erratum in: Circulation. 010 March 30;121(12):e257. Dosage error in article text. 73. Boersma E, Maas AC, Deckers JW, Simoons ML. Early thrombolytic treatment in acute myocardial infarction: reappraisal of the golden hour. Lancet 1996;348: Morrison LJ, Verbeek PR, McDonald AC, Sawadsky BV, Cook DJ. Mortality and prehospital thrombolysis for acute myocardial infarction: a meta-analysis. JAMA 2000;283: Prehospital thrombolytic therapy in patients with suspected acute myocardial infarction. The European Myocardial Infarction Project Group. N Engl J Med 1993;329: Weaver WD, Cerqueira M, Hallstrom AP, et al. Prehospital-initiated vs hospitalinitiated thrombolytic therapy. The myocardial infarction triage and intervention trial. JAMA 1993;270: Feasibility, safety, and efficacy of domiciliary thrombolysis by general practitioners: Grampian region early anistreplase trial. GREAT Group. BMJ 1992;305: Welsh RC, Travers A, Senaratne M, Williams R, Armstrong PW. Feasibility and applicability of paramedic-based prehospital fibrinolysis in a large North American center. Am Heart J 2006;152: Pedley DK, Bissett K, Connolly EM, et al. Prospective observational cohort study of time saved by prehospital thrombolysis for ST elevation myocardial infarction delivered by paramedics. BMJ 2003;327: Grijseels EW, Bouten MJ, Lenderink T, et al. Pre-hospital thrombolytic therapy with either alteplase or streptokinase. Practical applications, complications and long-term results in 529 patients. Eur Heart J 1995;16: Keeley EC, Boura JA, Grines CL. Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review of 23 randomised trials. Lancet 2003;361: Dalby M, Bouzamondo A, Lechat P, Montalescot G. Transfer for primary angioplasty versus immediate thrombolysis in acute myocardial infarction: a metaanalysis. Circulation 2003;108: Magid DJ, Calonge BN, Rumsfeld JS, et al. Relation between hospital primary angioplasty volume and mortality for patients with acute MI treated with primary angioplasty vs thrombolytic therapy. JAMA 2000;284: Steg PG, Bonnefoy E, Chabaud S, et al. Impact of time to treatment on mortality after prehospital fibrinolysis or primary angioplasty: data from the CAPTIM randomized clinical trial. Circulation 2003;108: Bonnefoy E, Steg PG, Boutitie F, et al. Comparison of primary angioplasty and pre-hospital fibrinolysis in acute myocardial infarction (CAPTIM) trial: a 5-year follow-up. Eur Heart J 2009;30: Kalla K, Christ G, Karnik R, et al. Implementation of guidelines improves the standard of care: the Viennese registry on reperfusion strategies in ST-elevation myocardial infarction (Vienna STEMI registry). Circulation 2006;113: Pinto DS, Kirtane AJ, Nallamothu BK, et al. Hospital delays in reperfusion for ST-elevation myocardial infarction: implications when selecting a reperfusion strategy. Circulation 2006;114: Madsen MM, Busk M, Sondergaard HM, et al. Does diabetes mellitus abolish the beneficial effect of primary coronary angioplasty on long-term risk of reinfarction after acute ST-segment elevation myocardial infarction compared with fibrinolysis? (A DANAMI-2 substudy). Am J Cardiol 2005;96: Peterson LR, Chandra NC, French WJ, Rogers WJ, Weaver WD, Tiefenbrunn AJ. Reperfusion therapy in patients with acute myocardial infarction and prior coronary artery bypass graft surgery (National Registry of Myocardial Infarction-2). Am J Cardiol 1999;84: Kereiakes DJ, Gibler WB, Martin LH, Pieper KS, Anderson LC. Relative importance of emergency medical system transport and the prehospital electrocardiogram on reducing hospital time delay to therapy for acute myocardial infarction: a preliminary report from the Cincinnati Heart Project. Am Heart J 1992;123: Le May MR, So DY, Dionne R, et al. A citywide protocol for primary PCI in ST-segment elevation myocardial infarction. N Engl J Med 2008;358: Gross BW, Dauterman KW, Moran MG, et al. An approach to shorten time to infarct artery patency in patients with ST-segment elevation myocardial infarction. Am J Cardiol 2007;99: Bradley EH, Herrin J, Wang Y, et al. Strategies for reducing the door-to-balloon time in acute myocardial infarction. N Engl J Med 2006;355: Widimsky P, Groch L, Zelizko M, Aschermann M, Bednar F, Suryapranata H. Multicentre randomized trial comparing transport to primary angioplasty vs immediate thrombolysis vs combined strategy for patients with acute myocardial infarction presenting to a community hospital without a catheterization laboratory. The PRAGUE study. Eur Heart J 2000;21: Primary versus tenecteplase-facilitated percutaneous coronary intervention in patients with ST-segment elevation acute myocardial infarction (ASSENT-4 PCI): randomised trial. Lancet 2006;367: Herrmann HC, Lu J, Brodie BR, et al. Benefit of facilitated percutaneous coronary intervention in high-risk ST-segment elevation myocardial infarction patients presenting to nonpercutaneous coronary intervention hospitals. JACC Cardiovasc Interv 2009;2: Gershlick AH, Stephens-Lloyd A, Hughes S, et al. Rescue angioplasty after failed thrombolytic therapy for acute myocardial infarction. N Engl J Med 2005;353: Danchin N, Coste P, Ferrieres J, et al. Comparison of thrombolysis followed by broad use of percutaneous coronary intervention with primary percutaneous coronary intervention for ST-segment-elevation acute myocardial infarction: data from the french registry on acute ST-elevation myocardial infarction (FAST- -MI). Circulation 2008;118: Cantor WJ, Fitchett D, Borgundvaag B, et al. Routine early angioplasty after fibrinolysis for acute myocardial infarction. N Engl J Med 2009;360: Hochman JS, Sleeper LA, Webb JG, et al. Early revascularization in acute myocardial infarction complicated by cardiogenic shock. SHOCK Investigators. Should we emergently revascularize occluded coronaries for cardiogenic shock. N Engl J Med 1999;341: Arntz HR, Wenzel V, Dissmann R, Marschalk A, Breckwoldt J, Muller D. Out-of-hospital thrombolysis during cardiopulmonary resuscitation in patients with high likelihood of ST-elevation myocardial infarction. Resuscitation 2008;76: Garot P, Lefevre T, Eltchaninoff H, et al. Six-month outcome of emergency percutaneous coronary intervention in resuscitated patients after cardiac arrest complicating ST-elevation myocardial infarction. Circulation 2007;115:
182 180 H.-R. Arntz, L.L. Bossaert, N. Danchin, N.I. Nikolaou 103. Spaulding CM, Joly LM, Rosenberg A, et al. Immediate coronary angiography in survivors of out-of-hospital cardiac arrest. N Engl J Med 1997;336: Sunde K, Pytte M, Jacobsen D, et al. Implementation of a standardised treatment protocol for post resuscitation care after out-of-hospital cardiac arrest. Resuscitation 2007;73: Yusuf S, Peto R, Lewis J, Collins R, Sleight P. Beta blockade during and after myocardial infarction: an overview of the randomized trials. Prog Cardiovasc Dis 1985;27: Chen ZM, Pan HC, Chen YP, et al. Early intravenous then oral metoprolol in 45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet 2005;366: Teo KK, Yusuf S, Furberg CD. Effects of prophylactic antiarrhythmic drug therapy in acute myocardial infarction. An overview of results from randomized controlled trials. JAMA 1993;270: Hine LK, Laird N, Hewitt P, Chalmers TC. Meta-analytic evidence against prophylactic use of lidocaine in acute myocardial infarction. Arch Intern Med 1989;149: Swedberg K, Held P, Kjekshus J, Rasmussen K, Ryden L, Wedel H. Effects of the early administration of enalapril on mortality in patients with acute myocardial infarction. Results of the Cooperative New Scandinavian Enalapril Survival Study II (CONSENSUS II). N Engl J Med 1992;327: Indications for ACE inhibitors in the early treatment of acute myocardial infarction: systematic overview of individual data from 100,000 patients in randomized trials. ACE Inhibitor Myocardial Infarction Collaborative Group. Circulation 1998;97: Patti G, Pasceri V, Colonna G, et al. Atorvastatin pretreatment improves outcomes in patients with acute coronary syndromes undergoing early percutaneous coronary intervention: results of the ARMYDA-ACS randomized trial. J Am Coll Cardiol 2007;49: Hulten E, Jackson JL, Douglas K, George S, Villines TC. The effect of early, intensive statin therapy on acute coronary syndrome: a meta-analysis of randomized controlled trials. Arch Intern Med 2006;166: Heeschen C, Hamm CW, Laufs U, Snapinn S, Bohm M, White HD. Withdrawal of statins increases event rates in patients with acute coronary syndromes. Circulation 2002;105:
183 Publikacja przygotowana przez Europejską Radę Resuscytacji (ERC) przy współpracy z Polską Radą Resuscytacji (PRR). Tekst tłumaczony przez Polską Radę Resuscytacji. Wiedza i praktyka w zakresie resuscytacji krążeniowo-oddechowej to stale zmieniająca się dziedzina medycyny. W miarę rozwoju wiedzy oraz postępu w nauce i doświadczeniu klinicznym zmienia się w sposób ciągły również praktyka medycz na oraz sposób stosowania leków. Czytelnik tego podręcznika jest zobowiązany do zapoznania się z aktualnymi wiado mościami na temat przedstawionych sposobów postępowania i farmakoterapii ze szczególnym uwzględnieniem informacji producentów na temat dawek, czasu i drogi podawania oraz efektów ubocznych stosowanych leków. Na każdej z osób praktykujących medycynę resuscytacji spoczywa osobista odpowiedzialność za stosowane metody lecznicze, których uży cie powinno być oparte na gruntownej wiedzy i umiejętnościach praktycznych z zachowaniem niezbędnych warunków bez pieczeństwa własnego i pacjenta. Wydawcy oraz redaktorzy niniejszego opracowania nie ponoszą odpowiedzialności za szkody, które mogłyby być w jakikolwiek sposób związane z materiałem zawartym w tej książce. Bibliografia do wszystkich rozdziałów została w całości powtórzona za wydaniem oryginalnym. REDAKTOR NAUKOWY WYDANIA POLSKIEGO prof. dr hab. Janusz Andres TŁUMACZENIE Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Elżbieta Dobrowolska, Edyta Drab, Bartosz Frączek, Anna Jarosz, Piotr Kolęda, Paweł Krawczyk, Rafał Surmacz, Jurij Szymański, Grzegorz Zając KOREKTA MERYTORYCZNA Janusz Andres, Elżbieta Byrska-Maciejasz, Grzegorz Cebula, Marta Dembkowska, Bartosz Frączek, Paweł Krawczyk ADIUSTACJA I KOREKTA WYDAWNICZA Danuta Ambrożewicz PROJEKT OKŁADKI Polska Rada Resuscytacji wg plakatu V Międzynarodowego Kongresu Polskiej Rady Resuscytacji autorstwa Mieczysława Górowskiego Publikację wydano ze środków Polskiej Rady Resuscytacji. Copyright by European Resuscitation Council (ERC), 2010 Copyright for the Polish edition by Polska Rada Resuscytacji, Kraków 2010 Copyright for the Polish translation by Polska Rada Resuscytacji, Kraków 2010 Wszystkie prawa zastrzeżone. Żadna część poniższej publikacji nie może być kopiowana i przechowywana w jakimkol wiek mechanicznym systemie kopiowania danych, włączając fotokopie, kserokopie, nagrania i inne, bez uprzedniej pisem nej zgody PRR (dotyczy terenu Rzeczpospolitej Polskiej). Wszystkie prośby o możliwość wykorzystania materiałów zawartych w tej publikacji należy kierować do ERC. ISBN KOORDYNATOR STRONY ORAZ WERSJI ELEKTRONICZNEJ Wytycznych resuscytacji 2010 Wiesław Pyrczak prc@prc.krakow.pl ADRES DO KORESPONDENCJI ADRES DO KORESPONDENCJI W POLSCE ERC Secretariat VZW Polska Rada Resuscytacji Drie Eikenstraat 661 ul. Radziwiłłowska 4, Kraków BE-2650 EDEGEM tel fax Belgium biuro@prc.krakow.pl tel fax Koordynator kursów info@erc.edu Tomasz Galewicz kursy@prc.krakow.pl SKŁAD I PRZYGOTOWANIE DO DRUKU FALL ul. Garczyńskiego 2, Kraków tel ; fall@fall.pl
184 Zaawansowane zabiegi resuscytacyjne 6 u dzieci Dominique Biarent a, *, Robert Bingham b, Christoph Eich c, Jesús López-Herce d, Ian Maconochie e, Antonio Rodríguez-Núñez f, Thomas Rajka g, David Zideman h a Paediatric Intensive Care, Hôpital Universitaire des Enfants, 15 av JJ Crocq, Brussels, Belgium b Great Ormond Street Hospital for Children, London, UK c Zentrum Anaesthesiologie, Rettungs-und Intensivmedizin, Universitätsmedizin Göttingen, Robert-Koch-Str. 40, D Göttingen, Germany d Pediatric Intensive Care Department, Hospital General Universitario Gregorio Marañón, Complutense University of Madrid, Madrid, Spain e St Mary s Hospital, Imperial College Healthcare NHS Trust, London, UK f University of Santiago de Compostela FEAS, Pediatric Emergency and Critical Care Division, Pediatric Area Hospital Clinico Universitario de Santiago de Compostela, Santiago de Compostela, Spain g Oslo University Hospital, Kirkeveien, Oslo, Norway h Imperial College Healthcare NHS Trust, London, UK Wstęp Poniższe wytyczne dotyczące zabiegów resuscytacyjnych u dzieci oparte są na dwóch głównych regułach: 1) częstość występowania krytycznych stanów zagrożenia życia, szczególnie zatrzymania krążenia oraz urazów u dzieci jest znacznie mniejsza niż u osób dorosłych; 2) większość stanów nagłych u pacjentów pediatrycznych jest początkowo zaopatrywana przez osoby, które nie specjalizują się w resuscytacji dzieci i które mają ograniczone doświadczenie w postępowaniu z dzieckiem w stanie zagrożenia życia. Z tych powodów wytyczne dotyczące zabiegów resuscytacyjnych u dzieci muszą być oparte na najlepszych, dostępnych dowodach naukowych, ale także cechować się prostotą i łatwością zastosowania. Ostatecznie, międzynarodowe wytyczne muszą uznać różne warianty struktur ratownictwa medycznego zarówno narodowe, jak i lokalne, dopuszczając, jeśli zaistnieje taka konieczność, możliwość dostosowania ich do istniejących warunków. Proces powstawania wytycznych Europejska Rada Resuscytacji (ERC) wydała wytyczne dotyczące zabiegów resuscytacyjnych u dzieci (PLS) w 1994, 1998, 2000 i 2005 roku 1 5. Ostatnie dwie publikacje były oparte na International Consensus of Science opracowanym przez International Liaison Committee on Resuscitation (ILCOR) 6-8. Ta metoda została ponownie użyta w latach 2009/2010 i dała w rezultacie Consensus on Science with Treatment Recommendation (CoSTR), który został równocześnie opublikowany w Resuscitation, Circulation i Pediatrics 9,10. Grupa robocza PLS przy ERC pracowała nad wytycznymi ERC PLS opartymi na CoSTR 2010 roku i dodatkowej, uzupełniającej literaturze naukowej. Wytyczne dotyczące resuscytacji noworodków zostały opisane w rozdziale * Corresponding author. dominique.biarent@huderf.be (D. Biarent). Podsumowanie zmian w stosunku do Wytycznych 2005 Wprowadzenie zmian w wytycznych było odpowiedzią na nowe przekonywające dowody naukowe. Celem twórców było także ułatwienie uczenia się i zapamiętywania nowych wytycznych. Tak jak poprzednio, nadal brak jest przekonywających dowodów naukowych dotyczących resuscytacji dzieci. Dlatego też, aby ułatwić i pomóc w rozpowszechnianiu i wdrażaniu wytycznych PLS, zmiany zostały wprowadzone tylko na podstawie nowych, wysokiej jakości dowodów naukowych lub w celu zapewnienia zgodności z wytycznymi stosowanymi u osób dorosłych. Głównym tematem badań pozostaje nadal możliwość zastosowania tych samych wytycznych u dorosłych i dzieci. Główne zmiany w wytycznych dotyczą następujących zagadnień: Rozpoznawanie zatrzymania krążenia Personel medyczny nie jest w stanie w sposób wiarygodny stwierdzić obecność lub brak tętna u niemowląt i u dzieci w czasie krótszym niż 10 sekund 12,13. Dlatego też badanie tętna nie może być jedynym wyznacznikiem określającym zatrzymanie krążenia i konieczność wykonywania uciśnięć klatki piersiowej. Jeśli poszkodowany nie reaguje, nie oddycha prawidłowo i nie ma żadnych oznak życia, ratownicy przedmedyczni powinni rozpocząć RKO. Personel medyczny powinien poszukiwać oznak krążenia oraz jeśli posiada doświadczenie w tej technice, może dodać badanie tętna do metod rozpoznania zatrzymania krążenia i podjęcia decyzji o tym, czy powinno się rozpocząć uciśnięcia klatki piersiowej czy też nie. Decyzję o rozpoczęciu RKO należy podjąć w czasie krótszym niż 10 sekund. W zależności od wieku dziecka tętno można sprawdzać na tętnicy szyjnej (dzieci), ramiennej (niemowlęta) lub udowej (dzieci i niemowlęta) 14,15. Stosunek uciśnięć do wentylacji Stosunek uciśnięć klatki piersiowej do wentylacji (Compression Ventilation CV) stosowany w resuscytacji dzieci powinien zależeć od liczby ratowników obecnych na miejscu zdarzenie (jeden lub więcej) 16. Ratownicy przedme-
185 182 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman 6 dyczni, którzy zazwyczaj uczą się technik resuscytacji wykonywanej przez jedną osobę, powinni być szkoleni w prowadzeniu resuscytacji w stosunku 30 uciśnięć do 2 oddechów ratowniczych. Jest on taki sam jak u osób dorosłych i daje możliwość, że każda osoba przeszkolona w BLS będzie w stanie resuscytować dziecko po przekazaniu tylko niewielkiej ilości dodatkowych informacji. Ratownicy z obowiązkiem udzielenia pomocy powinni być uczeni stosunku 15 : 2, ponieważ skuteczność tej metody została potwierdzona w badaniach na zwierzętach oraz na manekinach Ta ostatnia grupa, w której zwykle znajdują się pracownicy ochrony zdrowia, powinna otrzymać rozszerzone szkolenie ukierunkowane ściśle na resuscytację dzieci. Zatraci się prostotę szkolenia z zakresu resuscytacji, jeśli stosunek uciśnięć do wentylacji będzie uzależniony od tego, czy obecny jest jeden, dwóch czy więcej ratowników. Niemniej jednak osoby z obowiązkiem udzielenia pomocy mogą używać stosunku uciśnięć do wentylacji 30 : 2, jeśli są same, szczególnie gdy nie osiągają wystarczającej liczby uciśnięć na minutę z powodu trudności w naprzemiennym wykonywaniu wentylacji i uciśnięć. Wentylacja pozostaje ważnym elementem RKO w zatrzymaniu krążenia spowodowanym asfiksją 22. Tym niemniej ratownicy, którzy nie są w stanie lub nie chcą prowadzić wentylacji metodą usta usta, powinni być zachęcani do wdrożenia resuscytacji polegającej jedynie na uciskaniu klatki piersiowej. Jakość RKO Technika uciśnięć klatki piersiowej u niemowląt zaleca stosowanie uciśnięć opuszkami dwóch palców w przypadku resuscytacji wykonywanej przez jednego ratownika oraz techniki dwóch kciuków i dłoni obejmujących klatę piersiową niemowlęcia, gdy jest obecnych dwóch lub więcej ratowników U dzieci starszych można stosować uciśnięcia za pomocą jednej lub dwóch rąk w zależności od preferencji ratownika 28. Należy kłaść nacisk na konieczność osiągnięcia odpowiedniej głębokości uciśnięć: co najmniej na jedną trzecią wymiaru przednio-tylnego klatki piersiowej u wszystkich dzieci (tzn. ok. 4 cm u niemowląt i ok. 5 cm u dzieci). Należy również zwrócić uwagę na całkowitą relaksację klatki piersiowej po fazie uciśnięcia. Uciskanie klatki piersiowej powinno być wykonywane z jak najmniejszą liczbą przerw, aby zminimalizować czas bez przepływu krwi. Zarówno dla niemowląt, jak i dla dzieci częstotliwość uciśnięć powinna wynosić co najmniej 100/min, jednak nie więcej niż 120/min. Defibrylacja Automatyczne defibrylatory zewnętrzne Opisane w literaturze fachowej pojedyncze przypadki kliniczne wskazują na fakt, że zastosowanie automatycznych defibrylatorów zewnętrznych (AED) u dzieci powyżej pierwszego roku życia jest skuteczne i bezpieczne 29,30. Automatyczne defibrylatory zewnętrzne potrafią prawidłowo zidentyfikować zaburzenia rytmu u dzieci i jest niezwykle mało prawdopodobne, aby zaleciły wykonanie defibrylacji w przypadku, gdy jest ona niewskazana Tym samym wskazane jest stosowanie AED u dzieci powyżej pierwszego roku życia 34. Niemniej jednak, jeśli istnieje prawdopodobieństwo, że AED będzie użyte u dzieci, osoba kupująca AED powinna sprawdzić, czy funkcjonowanie konkretnego modelu zostało sprawdzone na okoliczność rozpoznawania dziecięcych zaburzeń rytmu. Obecnie wielu producentów dostarcza zaprojektowane specjalnie dla pacjentów pediatrycznych elektrody samoprzylepne lub oprogramowanie, które zapewniają standardową redukcję energii dostarczanej przez urządzenie do wartości J 35 i takie modele są rekomendowane dla dzieci pomiędzy 1. a 8. rokiem życia 36,37. Jeśli brak jest możliwości wykonania defibrylacji zmniejszoną wartością energii lub urządzenie nie ma dostępnej funkcji manualnej redukcji energii, można zastosować AED używane dla osób dorosłych u dzieci powyżej 1. roku życia 38. Dowody wspierające zastosowanie AED u dzieci poniżej 1. roku życia ograniczone są do pojedynczych doniesień klinicznych 39,40. Częstość występowania rytmów do defibrylacji u niemowląt jest bardzo mała, z wyjątkiem sytuacji kiedy przyczyną zatrzymania krążenia jest choroba serca W tych rzadkich sytuacjach stosunek korzyści do możliwych powikłań może się przechylać na stronę korzyści i należy wówczas rozważyć zastosowanie AED (preferowana jest redukcja energii). Defibrylatory manualne Nadal zalecane jest leczenie za pomocą natychmiastowej defibrylacji w przypadku rozpoznania zatrzymania krążenia u dzieci w mechanizmie migotania komór (VF) lub w częstoskurczu komorowym bez tętna (VT). W zaawansowanych zabiegach resuscytacyjnych u osób dorosłych (ALS) zalecane jest wykonanie pojedynczego wyładowania a następnie natychmiastowe podjęcie RKO bez sprawdzania tętna lub zapisu rytmu na monitorze (zob. rozdział 4) Aby zminimalizować czas bez przepływu krwi, uciśnięcia klatki piersiowej powinny być kontynuowane podczas przyłożenia i ładowania łyżek defibrylatora lub elektrod samoprzylepnych (jeśli pozwala na to rozmiar klatki piersiowej dziecka). W momencie gdy defibrylator jest naładowany, uciśnięcia klatki piersiowej należy na krótko przerwać, aby wykonać defibrylację. Nie jest znana optymalna wartość energii defibrylacji u dzieci zapewniająca bezpieczeństwo i skuteczność wyładowania, jednak badania na modelach zwierzęcych oraz doniesienia na podstawie nielicznych serii przypadków klinicznych pokazują, że wartości energii większe od 4 J/kg są odpowiednie dla wykonania skutecznej defibrylacji bez istotnych skutków ubocznych 29,37,48,49. Badania kliniczne dowodzą, że dawka 2 J/kg w większości przypadków jest niewystarczająca 13,42,50. Wyładowanie dwufazowe jest tak samo efektywne jak jednofazowe, a wywołuje mniej podefibrylacyjnych dysfunkcji w miokardium 36,37,49, Dlatego, aby uprościć i ujednolicić postępowanie w BLS i ALS u dorosłych i dzieci, zaleca się stosowanie pojedynczych wyładowań niewzrastającą energią 4 J/kg w przypadku wykonywania defibrylacji u dzieci (preferowane są defibrylatory dwufazowe, lecz jednofazowe są również akceptowalne). Należy używać łyżek defibrylatora w największym rozmiarze lub elektrod samoprzylepnych, które pasują do rozmiaru klatki piersiowej niemowlęcia lub dziecka, w pozycji przednio-bocznej lub przednio-tylnej. Istotne jest, aby łyżki lub elektrody nie dotykały jedna drugiej 13.
186 Zaawansowane zabiegi resuscytacyjne u dzieci 183 Drogi oddechowe Rurki z mankietem uszczelniającym Rurki z mankietem uszczelniającym mogą być bezpiecznie stosowane u niemowląt i małych dzieci. Rozmiar powinien być dobrany na podstawie obowiązującego wzoru. Ucisk chrząstki pierścieniowatej Bezpieczeństwo oraz korzyści wynikające z zastosowania ucisku chrząstki pierścieniowatej w czasie intubacji nie są do końca jasne. Dlatego też ucisk na chrząstkę powinien być modyfikowany lub przerwany, jeśli uniemożliwia wentylację lub wydłuża czas i zmniejsza łatwość wykonania intubacji. Kapnometria Monitorowanie końcowowydechowego dwutlenku węgla (CO 2 ), najlepiej za pomocą kapnografii, jest przydatne w potwierdzeniu prawidłowego położenia rurki intubacyjnej oraz zalecane podczas RKO, ponieważ pomaga ocenić i zoptymalizować jakość prowadzonej resuscytacji. Dobór stężenia tlenu w mieszaninie oddechowej Wobec rosnącej liczby dowodów na potencjalną szkodliwość hiperoksji po zatrzymaniu krążenia należy od momentu przywrócenia spontanicznego krążenia kontrolować wdechowe stężenie, aby zmniejszyć ryzyko hiperoksemii. Systemy wczesnego reagowania Wdrożenie systemów wczesnego reagowania w warunkach oddziałów pediatrycznych może zmniejszyć częstość występowania zatrzymań krążenia i oddychania oraz śmiertelność wewnątrzszpitalną. Nowe zagadnienia Nowe zagadnienia poruszone w Wytycznych 2010 obejmują postępowanie w patologiach kanałów jonowych (tzn. znaczenie wykonywania sekcji oraz w następnej kolejności wykonywanie testów wśród członków rodziny) i niektórych sytuacjach szczególnych: urazach, korekcji serca jednokomorowego przed i po pierwszym etapie, korekcji metodą Fontana, nadciśnieniu płucnym. Terminologia W poniższym tekście rodzaj męski obejmuje także rodzaj żeński oraz nijaki, a termin dziecko odnosi się zarówno do niemowląt, jak i dzieci, chyba że zaznaczono inaczej. Określenie świeżorodek (newly born) odnosi się do noworodka zaraz po urodzeniu. Noworodek oznacza dziecko do 4. tygodnia życia. Niemowlę to dziecko poniżej pierwszego roku życia, a termin dziecko odnosi się do dzieci pomiędzy pierwszym rokiem życia a początkiem okresu pokwitania. Od okresu pokwitania dzieci określa się jako nastolatki, dla których można używać algorytmów stosowanych u osób dorosłych. Ponadto konieczne jest odróżnienie niemowlęcia i starszego dziecka, ponieważ istnieje kilka istotnych różnic w odniesieniu do diagnostyki i wykonywanych interwencji w obu tych grupach. Początek pokwitania, który jest fizjologicznym końcem dzieciństwa, jest najbardziej logiczną górną granicą wieku, poniżej której stosuje się wytyczne dla pacjentów pediatrycznych. Jeśli ratownicy uważają, że osoba poszkodowana jest dzieckiem, powinni stosować algorytmy pediatryczne. Jeżeli zaś ta opinia będzie błędna i poszkodowany okaże się młodym dorosłym, ryzyko związane z podjętą decyzją będzie niewielkie, ponieważ jak pokazały badania nad etiologią zatrzymania krążenia model pediatryczny zatrzymania krążenia obowiązuje aż do wczes nego okresu dojrzałości 54. A. Podstawowe zabiegi resuscytacyjne u dzieci Kolejność postępowania Ratownicy, którzy byli uczeni algorytmu BLS dla osób dorosłych oraz nie mają specjalistycznej wiedzy na temat resuscytacji dzieci, mogą używać sekwencji postępowania jak u osób dorosłych, ponieważ przeżywalność będzie niższa, jeśli nie podejmą żadnych działań. Osoby bez wykształcenia medycznego, które chcą się nauczyć resuscytacji pediatrycznej w związku z tym, że ich praca jest związana z ponoszeniem odpowiedzialności za dzieci (np.: nauczyciele, pielęgniarki szkolne, ratownicy wodni), należy uczyć, iż preferowana jest modyfikacja BLS dla osób dorosłych polegająca na wykonaniu pięciu początkowych oddechów ratowniczych, a następnie prowadzeniu RKO przez około 1 minutę przed udaniem się po pomoc (patrz algorytm BLS dla osób dorosłych). Podstawowe zabiegi resuscytacyjne u dzieci dla osób z obowiązkiem udzielenia pomocy Po 1 min RKO zadzwoń pod 112 lub 999 albo wezwij zespół resuscytacyjny Ryc Algorytm podstawowych zabiegów resuscytacyjnych u dzieci dla osób z obowiązkiem interwencji 6
187 184 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman 6 Poniższa sekwencja powinna być stosowana przez osoby z obowiązkiem udzielenia pomocy w sytuacjach zagrożenia życia u dzieci (zazwyczaj są to członkowie zespołów medycznych) (ryc. 6.1). 1. Upewnij się, że jest bezpiecznie zarówno dla ciebie jak i dla dziecka. 2. Sprawdź reakcję dziecka: delikatnie potrząśnij dzieckiem i zapytaj głośno: Czy wszystko w porządku? 3A. Jeśli dziecko odpowiada lub porusza się: pozostaw dziecko w pozycji, w jakiej je zastałeś (pod warunkiem że jest ona dla niego bezpieczna); oceń jego stan i w razie potrzeby wezwij pomoc; powtarzaj regularnie ocenę stanu ogólnego dziecka. 3B. Jeśli dziecko nie reaguje: głośno wołaj o pomoc; delikatnie odwróć dziecko na plecy; udrożnij drogi oddechowe dziecka poprzez odchylenie głowy do tyłu i uniesienie bródki w następujący sposób: umieść rękę na czole dziecka i delikatnie odchyl jego głowę ku tyłowi; w tym samym czasie umieść opuszki palca (lub palców) pod bródką dziecka i unieś ją. Nie naciskaj na tkanki miękkie pod bródką, bo możesz spowodować niedrożność dróg oddechowych; jeśli wciąż masz trudności z udrożnieniem dróg oddechowych, spróbuj metody wysunięcia żuchwy: połóż palce wskazujące obydwu rąk za żuchwą dziecka po jej bokach i popchnij ją do przodu. Jeżeli podejrzewasz istnienie urazu okolicy szyi, staraj się udrożnić drogi oddechowe, używając jedynie metody wysunięcia żuchwy. Jeśli nadal jest to nieskuteczne, zastosuj niewielkie odchylenie głowy do tyłu, do momentu aż drogi oddechowe zostaną udrożnione. 4. Utrzymujac drożność dróg oddechowych, wzrokiem, słuchem i dotykiem oceń, czy występują prawidłowe oddechy poprzez przysunięcie swojej twarzy blisko twarzy dziecka i obserwowania jego klatki piersiowej: obserwuj ruchy klatki piersiowej; słuchaj nad nosem i ustami dziecka szmerów oddechowych; poczuj ruch powietrza na swoim policzku. W pierwszych kilku minutach po zatrzymaniu krążenia dziecko może nabierać kilka wolnych, nieregularnych oddechów (gasping). Patrz, słuchaj i staraj się wyczuć oddech nie dłużej niż 10 sekund, zanim podejmiesz decyzję. Jeśli masz jakiekolwiek wątpliwości, czy dziecko oddycha prawidłowo, postępuj tak, jakby oddech był nieprawidłowy. 5A. Jeśli dziecko oddycha prawidłowo: ułóż dziecko w pozycji bezpiecznej (patrz dalej); wyślij kogoś lub sam udaj się po pomoc zadzwoń pod lokalny numer ratunkowy aby wezwać karetkę; sprawdzaj, czy oddech nadal występuje. 5B. Jeśli dziecko nie oddycha lub oddycha nieprawidłowo: delikatnie usuń widoczne ciała obce mogące powodować niedrożność dróg oddechowych; wykonaj 5 pierwszych oddechów ratowniczych; podczas wykonywania oddechów ratowniczych zwróć uwagę na pojawienie się kaszlu lub odruchów z tylnej ściany gardła w odpowiedzi na twoje działania; obecność lub brak tego typu reakcji stanowi część oceny obecności oznak krążenia, która zostanie opisana w dalszej części rozdziału. Oddechy ratownicze u dziecka powyżej 1. roku życia (ryc. 6.2): zapewnij odchylenie głowy i uniesienie bródki; kciukiem i palcem wskazującym ręki leżącej na czole zaciśnij miękkie części nosa; rozchyl usta dziecka, ale zapewnij uniesienie bródki; nabierz powietrza, obejmij szczelnie swoimi ustami usta dziecka, upewniając się, że nie ma przecieku powietrza; wykonaj powolny wydech do ust dziecka trwający ok. 1 1,5 sekundy, obserwując równocześnie unoszenie się klatki piersiowej; utrzymując odchylenie głowy i uniesienie bródki odsuń swoje usta od ust poszkodowanego i obserwuj, czy podczas wydechu opada klatka piersiowa; ponownie nabierz powietrze i powtórz opisaną sekwencję pięć razy; oceń jakość oddechu, obserwując klatkę piersiową dziecka: powinna się unosić i opadać jak przy normalnym oddechu. Ryc Wentylacja usta usta dziecko Oddechy ratownicze dla niemowląt (ryc. 6.3): umieść głowę w pozycji neutralnej (kiedy niemowlę leży na plecach, głowa jest zazwyczaj przygięta i może wymagać niewielkiego odchylenia) i unieś bródkę, nabierz powietrza, obejmij szczelnie swoimi ustami usta i nos dziecka upewniając się, że nie ma przecieku powietrza. Jeśli u starszego niemowlęcia nie można objąć ust i nosa, ratownik może próbować objąć swoimi ustami albo usta, albo nos niemowlęcia (jeśli tylko nos należy zacisnąć usta, aby powietrze nie wydostawało się na zewnątrz), powoli wdmuchuj powietrze do ust i nosa niemowlęcia przez 1 1,5 sekundy, w ilości wystarczającej do widocznego uniesienia się klatki piersiowej;
188 Zaawansowane zabiegi resuscytacyjne u dzieci 185 Ryc Wentylacja usta usta nos niemowlę utrzymując odchylenie głowy i uniesienie żuchwy odsuń swoje usta od ust poszkodowanego i obserwuj, czy podczas wydechu opada klatka piersiowa; nabierz powietrza i powtórz opisaną sekwencję 5 razy. Zarówno u niemowlęcia, jak i u dziecka, jeśli wykonanie skutecznego oddechu natrafia na trudność, drogi oddechowe mogą być niedrożne: otwórz usta dziecka i usuń z nich wszelkie widoczne przeszkody; nigdy nie staraj się usunąć ciała obcego na ślepo; upewnij się, że głowa jest prawidłowo odchylona, bródka uniesiona oraz czy szyja nie jest nadmiernie odgięta; jeśli odgięcie głowy i uniesienie brody nie powoduje udrożnienia dróg oddechowych, spróbuj metody wysunięcia żuchwy; podejmij do 5 prób w celu uzyskania efektywnych oddechów, jeśli nadal jest to nieskuteczne, rozpocznij uciskanie klatki piersiowej. 6. Oceń układ krążenia dziecka. Masz nie więcej niż 10 sekund na: poszukiwanie oznak krążenia zalicza się do tego jakikolwiek ruch, kaszel lub prawidłowy oddech (nie oddechy agonalne, które są rzadkie i nieregularne). Jeśli sprawdzasz tętno, upewnij się, że nie zajmie ci to więcej niż 10 sekund. U dziecka powyżej 1. roku życia badaj tętno na tętnicy szyjnej. U niemowlęcia badaj tętno na tętnicy ramiennej, czyli wewnętrznej stronie ramienia. Puls na tętnicy udowej można badać zarówno u niemowląt, jak i u dzieci. Tętno bada się w pachwinie, miejsce to znajduje się w połowie odległości pomiędzy kolcem biodrowym górnym przednim a spojeniem łonowym. 7A. Jeżeli jesteś pewien, że w ciągu 10 sekund stwierdziłeś obecność oznak krążenia: jeśli to konieczne, kontynuuj oddechy ratownicze aż do powrotu spontanicznego oddechu; jeśli dziecko nadal jest nieprzytomne, ułóż je w pozycji bezpiecznej; powtarzaj regularnie ocenę stanu ogólnego dziecka. 7B. Jeśli brak oznak krążenia, chyba że jesteś PEWIEN, że możesz wyczuć wyraźne tętno o częstości większej niż 60/min w ciągu 10 sekund: rozpocznij uciskanie klatki piersiowej; połącz uciskanie klatki piersiowej z oddechami ratowniczymi. Uciśnięcia klatki piersiowej U wszystkich dzieci uciskaj dolną połowę mostka. Aby uniknąć uciśnięć nadbrzusza, zlokalizuj wyrostek mieczykowaty poprzez znalezienie miejsca, gdzie łuki żebrowe dolnych żeber łączą się ze sobą. Należy uciskać mostek na szerokość jednego palca powyżej tego punktu. Uciśnięcia powinny być wystarczające, aby obniżyć mostek o około jedną trzecią głębokości klatki piersiowej. Nie należy się obawiać, że uciska się za mocno: Uciskaj szybko i mocno. Należy całkowicie zwolnić ucisk i powtarzać tę czynność z częstością co najmniej 100/min (ale nie przekraczając 120/min). Po 15 uciśnięciach należy odchylić głowę, unieść bródkę i wykonać dwa efektywne oddechy. Uciskanie klatki piersiowej i oddechy ratownicze powinno się kontynuować w stosunku 15 : 2. Najkorzystniejsza metoda uciskania klatki piersiowej różni się nieznacznie u dzieci i u niemowląt. Uciśnięcia klatki piersiowej u niemowląt (ryc. 6.4) W przypadku uciśnięć klatki piersiowej prowadzonych przez jednego ratownika zalecane jest wykonanie tej procedury opuszkami dwóch palców. Jeżeli jest dwóch lub więcej ratowników, należy użyć techniki dwóch kciuków i dłoni obejmujących klatkę piersiową niemowlęcia. Należy umieścić kciuki jeden obok drugiego w dolnej połowie mostka (jak powyżej), ułożone końcami w kierunku głowy niemowlęcia. Pozostałe rozpostarte palce obu dłoni obejmują dolną część klatki piersiowej, a końce palców podtrzymują plecy niemowlęcia. W obydwu metodach należy uciskać dolną część mostka tak, aby obniżyć mostek o około jedną trzecią głębokości klatki piersiowej. Ryc Uciśnięcia klatki piersiowej niemowlę 6
189 186 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman 6 Ryc Uciśnięcia klatki piersiowej jedną ręką dziecko Uciśnięcia klatki piersiowej u dzieci powyżej 1. roku życia (ryc. 6.5 i 6.6) Należy umieścić nadgarstek jednej ręki w dolnej połowie mostka (jak powyżej). Konieczne jest uniesienie palców aby upewnić się, że nie uciska się żeber. Należy ustawić się pionowo nad klatką piersiową poszkodowanego, wyprostować ramiona i uciskać tak, aby obniżyć mostek o około jedną trzecią głębokości klatki piersiowej. W przypadku większych dzieci lub drobno zbudowanych ratowników łatwiej będzie to osiągnąć przy użyciu dwóch rąk ze splecionymi palcami. 8. Nie przerywaj resuscytacji do czasu: powrotu oznak życia u dziecka (zacznie się budzić, poruszać, otworzy oczy oraz zacznie prawidłowo oddychać lub będzie miało dobrze wyczuwalne tętno z częstością powyżej 60 uderzeń/minutę); przybycia wykwalifikowanej pomocy, która przejmie działania ratownicze; wyczerpania własnych sił. Kiedy wezwać pomoc Dla ratowników ważne jest, aby wezwać pomoc tak szybko, jak to możliwe, kiedy tylko dziecko straci przytomność. Gdy jest więcej niż jeden ratownik, jeden z nich rozpoczyna resuscytację, podczas gdy drugi idzie po pomoc. Gdy jest tylko jeden ratownik, prowadzi on resuscytację przez około 1 minutę, zanim uda się po pomoc. Aby zminimalizować czas trwania przerwy w RKO, możliwe jest przeniesienie niemowlęcia lub małego dziecka do miejsca wzywania pomocy. Jedynym wyjątkiem, kiedy nie należy prowadzić RKO przez minutę zanim uda się po pomoc, jest przypadek, kiedy dziecko nagle straci przytomność i stało się to w obecności jednego ratownika. W tej sytuacji najbardziej prawdopodobną przyczyną zatrzymania krążenia są zaburzenia rytmu serca i dziecko wymaga defibrylacji. Należy natychmiast szukać pomocy, jeśli nikt inny nie może tego zrobić. Pozycja bezpieczna Nieprzytomne dziecko z drożnymi drogami oddechowymi i spontanicznym, prawidłowym oddechem powinno być ułożone na boku w pozycji bezpiecznej. Istnieje kilka wariantów tej pozycji; celem wszystkich jest zapobiegnięcie niedrożności dróg oddechowych oraz zmniejszenie prawdopodobieństwa przedostania się płynów, takich jak ślina, wydzieliny lub wymiociny, do górnych dróg oddechowych. Istotne jest postępowanie według poniższych reguł: Jeśli jest to możliwe, połóż dziecko w pozycji najbardziej zbliżonej do bocznej, z otwartymi ustami umożliwiającymi wydostanie się płynnej treści. Pozycja powinna być stabilna. Niemowlęta mogą potrzebować podparcia za pomocą małej poduszki lub zrolowanego koca położonego za plecami dziecka celem utrzymania go w takiej pozycji, aby zapobiec obróceniu się dziecka na plecy lub na brzuch. Unikaj wywierania ucisku na klatkę piersiową, bo może to utrudnić oddychanie. Obrócenie dziecka na bok z jednej strony na drugą powinno być możliwie łatwe i bezpieczne. Należy uwzględnić prawdopodobne uszkodzenia kręgosłupa w odcinku szyjnym, utrzymując stabilizację ręczną. W regularnych odstępach czasu (tzn. co 30 min) zmieniaj strony, na których pacjent jest ułożony, aby zapobiec przewlekłemu uciskowi na wystające punkty ciała. Pozycja bezpieczna stosowana u dorosłych jest również odpowiednia dla dzieci. Ryc Uciśnięcia klatki piersiowej dwiema rękami dziecko
190 Zaawansowane zabiegi resuscytacyjne u dzieci 187 Niedrożność dróg oddechowych spowodowana ciałem obcym W trakcie 2010 Consensus Conference nie zaprezentowano żadnych nowych dowodów dotyczących tego tematu. Zarówno uderzenia w okolicę międzyłopatkową, jak i uciśnięcia klatki piersiowej lub nadbrzusza powodują wzrost ciśnienia w klatce piersiowej i mogą spowodować usunięcie ciała obcego z dróg oddechowych. W połowie przypadków, aby usunąć przyczynę niedrożności, trzeba użyć więcej niż jednej technik 55. Nie ma danych wskazujących na to, który sposób powinien być użyty jako pierwszy, ani w jakim porządku te techniki powinny być stosowane. Jeśli jedna jest nieskuteczna, trzeba spróbować zamiennie innych aż do momentu usunięcia ciała obcego. Algorytm postępowania w przypadku niedrożności dróg oddechowych spowodowanej ciałem obcym został uproszczony i ujednolicony z algorytmem postępowania u osób dorosłych w Wytycznych 2005, nadal jest zalecane stosowanie się do wspomnianej sekwencji (ryc. 6.7). W porównaniu z algorytmem stosowanym u dorosłych najbardziej znacząca różnica polega na zakazie stosowania uciśnięć nadbrzusza u niemowląt. Chociaż te uciśnięcia mogą powodować urazy w każdej grupie pacjentów, ryzyko jest szczególnie wysokie w grupie niemowląt i bardzo małych dzieci. Spowodowane jest to poziomym ułożeniem żeber, w wyniku czego narządy górnego piętra jamy brzusznej są bardziej narażone na urazy. Z tego powodu wytyczne dotyczące postępowania w przypadku obecności ciała obcego w drogach oddechowych są różne u niemowląt i u dzieci. Rozpoznawanie obecności ciała obcego w drogach oddechowych Gdy ciało obce dostanie się do dróg oddechowych, dziecko natychmiast zareaguje kaszlem, próbując je usunąć. Spontaniczny kaszel jest prawdopodobnie bardziej efektywny i bezpieczniejszy niż jakikolwiek rękoczyn wykonany przez ratownika. Jeśli jednak kaszel jest nieskuteczny lub dziecko nie kaszle, świadczy to o całkowitym zatkaniu dróg oddechowych, co może szybko doprowadzić do uduszenia. Dlatego podjęcie interwencji mających na celu usunięcie ciała obcego jest wymagane tylko wtedy, kiedy kaszel staje się nieefektywny. Należy je wdrożyć w sposób szybki i zdecydowany. Większość przypadków zadławienia u niemowląt i dzieci zdarza się podczas zabawy lub podczas posiłków w obecności opiekunów. A zatem większość tych wypadków zdarza się przy świadkach i interwencje są podjęte, kiedy dziecko jest jeszcze przytomne. Niedrożność z powodu ciała obcego w drogach oddechowych charakteryzuje się nagłym początkiem zaburzeń oddechowych z kaszlem, nudnościami lub stridorem (tabela 6.1). Podobne objawy i symptomy mogą towarzyszyć innym przyczynom niedrożności dróg oddechowych, takim jak zapalenie nagłośni lub podgłośniowe zapalenie krtani. Wymagają one jednak innego postępowania. Zadławienie podejrzewamy wtedy, kiedy początek jest nagły, brak innych objawów choroby oraz w wywiadzie występują wskazówki alarmujące ratownika, np. posiłek lub zabawa małymi przedmiotami tuż przed początkiem objawów. Pomoc w zadławieniu (ryc. 6.7) 1. Bezpieczeństwo i wezwanie pomocy Bezpieczeństwo jest nadrzędne: ratownik nie może narażać siebie na zagrożenie i powinien rozważyć najbezpieczniejszy sposób leczenia zadławionego dziecka. Jeśli dziecko kaszle efektywnie, żadne dodatkowe działania nie są potrzebne. Zachęcaj je do kaszlu i nieustannie obserwuj. Jeśli kaszel jest lub staje się nieefektywny, natychmiast wołaj o pomoc i oceń stan świadomości dziecka. 2. Zadławienie u przytomnego dziecka Jeśli dziecko jest nadal przytomne, ale nie kaszle lub kaszel jest nieefektywny, wykonaj 5 uderzeń w okolicę międzyłopatkową. Jeśli uderzenia w okolicę międzyłopatkową są nieskuteczne, wykonaj uciśnięcia klatki piersiowej u niemowląt, a u dzieci uciśnięcia nadbrzusza. Zabiegi te powodują wytworzenie sztucznego kaszlu, mającego na celu usunięcie ciała obcego poprzez zwiększenie ciśnienia wewnątrz klatki piersiowej. Uderzenia w okolicę międzyłopatkową u niemowląt Ułóż dziecko głową w dół, leżące na brzuchu, aby do usunięcia ciała obcego wykorzystać siłę grawitacji. 6 Tabela 6.1. Objawy niedrożności dróg oddechowych spowodowanych ciałem obcym Główne objawy obecności ciała obcego w drogach oddechowych zdarzenie w obecności świadków kaszel/dławienie nagły początek informacja z wywiadu o połknięciu lub zabawie małym przedmiotem Kaszel nieefektywny niemożność mówienia cisza lub bezgłośny kaszel niemożność oddychania sinica postępująca utrata przytomności Kaszel efektywny płacz lub słowna odpowiedź na pytania głośny kaszel może nabrać powietrza przed kaszlem w pełni reagujący
191 188 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman Leczenie zadławienia u dzieci Ryc Algorytm postępowania w przypadku niedrożności dróg oddechowych spowodowanej ciałem obcym u dzieci 6 Siedzący lub klęczący ratownik powinien być w stanie bezpiecznie podtrzymywać dziecko na swoim kolanie. Podeprzyj głowę niemowlęcia w następujący sposób: kciuk jednej dłoni połóż na kącie żuchwy po jednej stronie, a po drugiej stronie w tym samym miejscu żuchwy jeden lub dwa palce tej samej ręki. Nie uciskaj na miękkie tkanki pod żuchwą, bo to może nasilić niedrożność dróg oddechowych. Wykonaj do 5 mocnych uderzeń w plecy nadgarstkiem jednej ręki w okolicę międzyłopatkową. Celem jest raczej usunięcie niedrożności, a nie wykonanie wszystkich 5 uderzeń. Uderzenia w okolicę międzyłopatkową u dzieci powyżej 1. roku życia Uderzenia w okolicę międzyłopatkową są bardziej efektywne, jeśli dziecko będzie ułożone głową w dół. Małe dziecko, podobnie jak niemowlę, może być ułożone w poprzek kolan ratownika. Jeśli to nie jest możliwe, utrzymuj dziecko nachylone do przodu i wykonaj od tyłu uderzenia w okolicę międzyłopatkową. Jeśli uderzenia w okolice międzyłopatkową są nieskuteczne, a dziecko jest nadal przytomne, wykonaj u niemowląt uciśnięcia klatki piersiowej, a u dzieci uciśnięcia nadbrzusza. Nie wykonuj uciśnięć nadbrzusza (manewru Heimlicha) u niemowląt. Uciśnięcia klatki piersiowej u niemowląt Obróć dziecko na wznak głową skierowaną w dół. Aby to bezpiecznie wykonać, połóż dziecko na wolnym przedramieniu i obejmij ręką jego potylicę. Utrzymuj dziecko leżące głową skierowaną w dół (lub w poprzek) na twoim przedramieniu opartym o udo. Wyznacz miejsce jak do uciskania klatki piersiowej (dolna połowa mostka około szerokość jednego palca powyżej wyrostka mieczykowatego). Wykonaj 5 uciśnięć klatki piersiowej podobnie jak podczas RKO, ale wykonaj je gwałtowniej i z mniejszą częstotliwością. Uciśnięcia nadbrzusza u dzieci powyżej 1. roku życia Stań lub uklęknij za dzieckiem, obejmij jego tułów, umieść swoje ramiona pod ramionami dziecka. Zaciśniętą pięść ułóż pomiędzy pępkiem a wyrostkiem mieczykowatym. Chwyć ją drugą ręką i mocno pociągnij ręce do siebie i ku górze. Powtórz tę czynność do 5 razy. Upewnij się, że nie uciskasz wyrostka mieczykowatego lub dolnych żeber, bo może to doprowadzić do urazu jamy brzusznej. Po wykonaniu uciśnięć klatki piersiowej lub nadbrzusza należy ponownie ocenić stan dziecka. Jeśli przedmiot nie został usunięty i poszkodowany jest wciąż przytomny, konieczne jest wykonywanie sekwencji uderzeń w okolicę międzyłopatkową i uciśnięcia klatki piersiowej (u niemowląt) lub uciśnięcia nadbrzusza (u dzieci). Należy zadzwonić lub wysłać kogoś po pomoc, jeśli ona jeszcze nie dotarła. Na tym etapie działań nie należy zostawiać dziecka samego. Jeśli przedmiot został usunięty, należy ocenić stan kliniczny dziecka. Istnieje możliwość, że małe fragmenty mogły pozostać w drogach oddechowych i spowodować powikłania. W razie jakichkolwiek wątpliwości konieczne jest zasięgnięcie porady medycznej. Uciśnięcia nadbrzusza mogą spowodować powstanie obrażeń wewnętrznych, dlatego każdy poszkodowany leczony w ten sposób powinien być zbadany przez lekarza 5.
192 Zaawansowane zabiegi resuscytacyjne u dzieci Niedrożność dróg oddechowych u nieprzytomnego dziecka Jeśli dziecko z niedrożnymi drogami oddechowymi jest nieprzytomne lub traci przytomność, należy położyć je na twardej, płaskiej powierzchni. Następnie należy zadzwonić lub wysłać kogoś po pomoc, jeżeli ta nadal nie dotarła. Na tym etapie działań nie należy zostawiać dziecka samego. Powinno się postępować w następujący sposób: Udrożnij drogi oddechowe Otwórz usta dziecka i poszukaj widocznych ciał obcych. Jeśli widzisz jakiekolwiek, podejmij jednorazową próbę usunięcia poprzez wygarnięcie palcem, nie usuwaj nic na ślepo ani nie powtarzaj próby wygarnięcia, gdyż może to spowodować wepchnięcie ciała obcego głębiej do krtani i być przyczyną urazu. Oddechy ratownicze Udrożnij drogi oddechowe poprzez odchylenie głowy i wysuniecie bródki, a następnie podejmij próbę wykonania 5 oddechów ratowniczych. Oceń efektywność każdego oddechu, jeśli nie spowoduje on uniesienia się klatki piersiowej, popraw pozycję głowy przed wykonaniem następnej próby. Uciśnięcia klatki piersiowej i RKO Podejmij 5 prób wykonania oddechów ratowniczych, jeżeli nie spowodują one żadnej reakcji (poruszanie się, kaszel, spontaniczny oddech), przejdź do uciśnięć klatki piersiowej bez uprzedniej oceny krążenia. Postępuj zgodnie z algorytmem BLS dla jednego ratownika (patrz powyżej krok 7B) przez około minutę, zanim wezwiesz pogotowie ratunkowe (jeśli nikt tego nie zrobił wcześniej). Kiedy udrażniasz drogi oddechowe w celu wykonania kolejnych oddechów ratowniczych, skontroluj jamę ustną, czy nie widać tam ciała obcego. Jeśli widzisz jakiekolwiek, podejmij próbę usunięcia poprzez jednokrotne wygarnięcie palcem. Jeśli ciało obce się pojawiło i zostało usunięte, sprawdź i udrożnij drogi oddechowe w wyżej opisany sposób oraz wykonaj oddechy ratownicze, jeśli dziecko nadal nie oddycha. Jeśli dziecko zaczyna odzyskiwać przytomność i wykonywać spontaniczne, efektywne oddechy, ułóż je w pozycji bezpiecznej i obserwuj oddychanie oraz stan świadomości do czasu przybycia pogotowia ratunkowego. B. Zaawansowane zabiegi resuscytacyjne u dzieci Zapobieganie wystąpieniu zatrzymania krążenia U dzieci zatrzymanie krążenia jako wtórne do niewydolności krążenia lub oddychania jest znacznie częstsze niż pierwotne zatrzymanie krążenia spowodowane zaburzeniami rytmu Tak zwane uduszenie lub zatrzymanie oddechu jest również znacznie częstsze u młodych dorosłych (np. uraz, utonięcie, zatrucie) 62,63. Przeżywalność po zatrzymaniu krążenia i oddychania u dzieci jest niska, a sprawą nadrzędną jest identyfikacja objawów zapowiadających rozwój niewydolności krążenia lub oddychania, gdyż wczesna i skuteczna interwencja może uratować życie. Kolejność oceny i wykonywanych interwencji u każdego dziecka z poważną chorobą lub obrażeniami ciała przebiega zgodnie z zasadą ABC. A oznacza drogi oddechowe (Airway), Ac drogi oddechowe z równoczesną stabilizacją szyjnego odcinka kręgosłupa u dziecka urazowego (cervical spine). B oznacza oddychanie (Breathing). C oznacza krążenie (Circulation) (wraz z kontrolą krwawień u dziecka z urazem). Interwencje są podejmowane na każdym etapie oceny, jeżeli tylko stwierdzi się nieprawidłowości. Nie można przejść do następnego etapu, jeśli poprzednie zaburzenie nie zostanie w miarę możliwości zaopatrzone i skorygowane. Wzywanie zespołu szybkiego reagowania lub pediatrycznego zespołu resuscytacyjnego może zmniejszyć ryzyko zatrzymania oddechu i/lub krążenia u dzieci hospitalizowanych poza oddziałem intensywnej terapii W tego rodzaju zespole powinien być co najmniej jeden pediatra posiadający specjalistyczną wiedzę oraz jedna wykwalifikowana w opiece pediatrycznej pielęgniarka. Zespół ten powinien być wzywany do oceny dziecka w stanie zagrożenia życia, które jeszcze nie znajduje się na oddziale intensywnej terapii pediatrycznej (Paediatric Intensive Care Unit PICU) lub na pediatrycznym oddziale ratunkowym (Emergency Department ED). Rozpoznawanie niewydolności oddechowej: ocena A i B Ocena dziecka w stanie zagrożenia życia rozpoczyna się od oceny drożności dróg oddechowych (A) i oddychania (B). Zaburzenia w drożności dróg oddechowych i wymianie gazowej w płucach mogą prowadzić do niewydolności oddechowej. Objawy niewydolności oddechowej obejmują: Częstość oddechów wykraczającą poza normalne wartości należne dla wieku dziecka zarówno za szybka, jak i za wolna; Początkowo wzmożony wysiłek oddechowy, który z czasem może być niewystarczający lub osłabiony w sytuacji, kiedy zawiodą mechanizmy kompensacyjne, dodatkowe odgłosy, takie jak: stridor, świsty, charczenie, pochrząkiwanie lub całkowity brak szmerów oddechowych; Zmniejszoną objętością oddechową objawiającą się płytkimi oddechami, zmniejszonym rozprężaniem klatki piersiowej lub osłuchowo zmniejszoną ilością powietrza dostającą się do płuc podczas wdechu; Hipoksemię (bez lub z tlenoterapią), rozpoznawaną na podstawie wystąpienia sinicy lub najlepiej ocenianą za pomocą pulsoksymetru. Tym objawom mogą towarzyszyć dodatkowe zaburzenia w innych narządach i układach dotkniętych niedostateczną wentylacją i podażą tlenu lub też wynikające z prób kompensacji zaburzeń oddechowych w tych narządach. Będzie można je wykryć przy ocenie C krążenia. Są to: Narastająca tachykardia (mechanizm kompensacyjny próbujący zwiększyć dowóz tlenu); Bladość; Bradykardia (objaw ten jest złym prognostycznie wskaźnikiem wyczerpania się mechanizmów kompensacyjnych); 6
193 190 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman 6 Zmiany w stanie świadomości (objaw mówiący o tym, że mechanizmy kompensacyjne zawiodły). Rozpoznawanie niewydolności krążenia: ocena C Niewydolność krążenia (lub wstrząs) jest określana jako niewspółmierność pomiędzy zapotrzebowaniem metabolicznym tkanek a dostarczaniem tlenu i składników odżywczych przez układ krążenia 70. Fizjologiczne mechanizmy kompensacyjne prowadzą do zmian w częstości pracy serca, obwodowym oporze naczyniowym (który zwykle wzrasta jako mechanizm kompensacyjny) oraz do zmian perfuzji tkanek i narządów. Objawy niewydolności krążenia obejmują: Wzrost częstości pracy serca (bradykardia jest złym prognostycznie wskaźnikiem zwiastującym dekompensację); Obniżone ciśnienie systemowe; Spadek perfuzji obwodowej (wydłużony nawrót kapilarny, obniżona temperatura skóry, blada lub marmurkowata skóra); Słabo wyczuwalne tętno lub całkowity brak tętna na obwodzie; Zmniejszona lub zwiększona objętość wewnątrznaczyniowa; Spadek diurezy i kwasica metaboliczna. Objawy mogą dotyczyć także innych układów i narządów, np.: Początkowy wzrost częstości oddechów, jako próba zwiększenia ilości dostarczanego tlenu, później przechodząca w bradypnoe w przypadku zdekompensowanej niewydolności krążenia; Poziom świadomości może się obniżyć z powodu obniżonej perfuzji mózgowej. Rozpoznawanie zatrzymania krążenia Objawy zatrzymania krążenia są następujące: Brak reakcji na ból (śpiączka); Brak oddechu lub oddechy agonalne; Brak krążenia; Bladość lub głęboka sinica. Badanie tętna jako jedynego wyznacznika warunkującego podjęcie decyzji o rozpoczęciu uciskania klatki piersiowej nie jest wiarygodne 71,72. Jeśli podejrzewa się zatrzymanie krążenia oraz brak jest oznak życia, ratownicy (zarówno laicy, jak i profesjonaliści) powinni rozpocząć RKO, chyba że są pewni, że wyczuwają tętno na głównych tętnicach w czasie 10 sekund (u niemowląt na tętnicy ramiennej lub udowej, u dzieci na szyjnej lub udowej). Jeśli są jakiekolwiek wątpliwości, należy rozpocząć RKO Jeżeli obecny jest personel wyszkolony w wykonywaniu echokardiografii, to badanie może pomóc w wykryciu aktywności skurczowej mięśnia sercowego i potencjalnie możliwych do leczenia przyczyn zatrzymania krążenia 76. Jednak należy pamiętać, że wykonanie echokardiografii nie może zakłócać prowadzenia uciśnięć klatki piersiowej. Postępowanie w niewydolności oddechowej i krążeniowej U dzieci istnieje wiele przyczyn niewydolności oddechowej i krążeniowej. Mogą one rozwijać się stopniowo lub wystąpić nagle. Zarówno niewydolność oddechowa, jak i krążeniowa mogą być na początku kompensowane, ale zwykle, jeżeli nie podejmie się właściwego leczenia, dochodzi do dekompensacji. Nieleczona zdekompensowana niewydolność oddechowa lub krążenia prowadzi do zatrzymania krążenia. Dlatego celem zaawansowanych zabiegów resuscytacyjnych u dzieci jest podjęcie szybkich i skutecznych działań zapobiegających przejściu niewydolności oddechowej i krążeniowej w pełnoobjawowe zatrzymanie krążenia. Drogi oddechowe i oddychanie Udrożnij drogi oddechowe,zapewnij prawidłową wentylację i natlenienie. Podaj tlen w wysokim przepływie. Zapewnij monitorowanie oddechu pacjenta (w pierwszej kolejności pulsoksymetria/spo 2 ). Osiągnięcie prawidłowej wentylacji i natleniania może wymagać zastosowania prostych przyrządów do udrażniania dróg oddechowych, wentylacji workiem samorozprężalnym (BMV), zastosowania maski krtaniowej (LMA) lub, w celu ostatecznego zabezpieczenia drożności dróg oddechowych, intubacji dotchawiczej i wentylacji dodatnimi ciśnieniami. W skrajnych, rzadkich przypadkach może być wymagane chirurgiczne udrożnienie dróg oddechowych. Krążenie Podłącz kardiomonitor (w pierwszej kolejności pulsoksymetr (SpO 2 ), elektrokardiograf/ekg i nieinwazyjny pomiar ciśnienia tętniczego krwi (NIBP Noninvasive Blood Pressure). Zapewnij dostęp donaczyniowy. Można go uzyskać poprzez założenie kaniuli do krążenia obwodowego (iv) lub do jamy szpikowej (io). Użyj dostępu centralnego, jeśli wcześniej został zabezpieczony. Podaj bolus płynów (20 ml/kg) i/lub leki (np.: inotropowe, wazopresyjne, antyarytmiczne), jeśli są wskazane. Izotoniczne krystaloidy są zalecane we wstępnej resuscytacji płynowej u dzieci niezależnie od typu wstrząsu włącznie ze wstrząsem septycznym Stale badaj i wykonuj ponowną re-ocenę stanu dziecka, rozpoczynając za każdym razem od sprawdzenia drożności dróg oddechowych, zanim przejdzie się do oceny oddychania i krążenia. Podczas leczenia zastosowanie kapnografii, inwazyjnego monitorowania ciśnienia tętniczego krwi, gazometrii, pomiaru rzutu serca, echokardiografii oraz saturacji krwi żylnej (ScvO 2 ) może pomóc w podejmowaniu decyzji co do dalszego postępowania i leczenia niewydolności oddechowej i/lub krążeniowej. Drogi oddechowe Drogi oddechowe należy udrożnić przy użyciu technik stosowanych w podstawowych zabiegach resuscytacyjnych. Rurka ustno-gardłowa lub nosowo-gardłowa może pomóc utrzymać drożność dróg oddechowych. Rurkę ustno-gardłową należy używać tylko u nieprzytomnego dziecka, u którego nie ma odruchów z tylnej ściany gardła. Ważne jest zastosowanie właściwego rozmiaru (odległość od siekaczy do kąta żuchwy), aby uniknąć wepchnięcia języka głębiej i zamknięcia wejścia do krtani nagłośnią lub bezpośredniego uciśnię-
194 Zaawansowane zabiegi resuscytacyjne u dzieci 191 cia okolicy głośni. Podniebienie miękkie u dzieci może zostać uszkodzone w czasie wprowadzania rurki ustno-gardłowej. Można tego uniknąć, wprowadzając rurkę delikatnie, bez użycia siły. Rurka nosowo-gardłowa jest lepiej tolerowana przez przytomne lub półprzytomne dzieci z zachowanymi odruchami z tylnej ściany gardła, ale nie powinna być użyta, jeśli doszło do złamania podstawy czaszki lub w przypadku koagulopatii. Należy poprawnie odmierzyć głębokość, na jaką zostanie wprowadzona rurka, poprzez pomiar odległości od nozdrza do kąta żuchwy. Konieczna jest jednak ponowna ocena głębokości po wprowadzeniu rurki. Te proste przyrządy do udrażniania dróg oddechowych nie zabezpieczają przed aspiracją wydzieliny, krwi lub zawartości żołądka. Maska krtaniowa (LMA) Pomimo że wentylacja przy użyciu maski i worka samorozprężalnego pozostaje nadal rekomendowaną metodą dla uzyskania kontroli nad drogami oddechowymi i wentylacją u dzieci, maska krtaniowa może być użyta w celu udrożnienia dróg oddechowych przez osoby mające doświadczenie i przeszkolone w jej stosowaniu 81,82. Może być szczególnie przydatna w niedrożności górnych dróg oddechowych spowodowanej nieprawidłowościami w okolicy nagłośniowej lub w sytuacji, gdy wentylacja przy użyciu maski twarzowej staje się niemożliwa. Maska krtaniowa nie zabezpiecza całkowicie dróg oddechowych przed aspiracją wydzieliny, krwi lub zawartości żołądka, dlatego wymagana jest stała i dokładna obserwacja. U małych dzieci, w porównaniu z dorosłymi, użycie maski krtaniowej wiąże się z większym ryzykiem wystąpienia powikłań 83,84. Inne nadgłośniowe przyrządy do zabezpieczenia drożności dróg oddechowych (np. rurka krtaniowa), które z powodzeniem stosuje się w anestezjologii dziecięcej, mogą również być użyte w sytuacjach zagrożenia życia, ale do tej pory jest niewiele danych dotyczących zastosowania tych urządzeń w stanach nagłych u dzieci 85. Intubacja dotchawicza Intubacja dotchawicza jest najbezpieczniejszym i najskuteczniejszym sposobem zabezpieczenia górnych dróg oddechowych, zapobiega rozdęciu żołądka, zabezpiecza przed aspiracją, daje możliwość optymalnej kontroli ciśnienia w drogach oddechowych oraz zapewnia wentylację z dodatnim ciśnieniem końcowo-wydechowym (PEEP). Podczas resuscytacji zalecana jest intubacja przez usta. Ta droga jest szybsza i obarczona mniejszą ilością powikłań niż intubacja przez nos. U przytomnego dziecka niezbędne jest rozważne użycie anestetyków, leków sedujących i zwiotczających, aby uniknąć wielokrotnych prób intubacji lub jej niepowodzenia Anatomia dróg oddechowych u dzieci różni się znacząco od anatomii dróg oddechowych u dorosłych, w związku z tym intubacja dziecka wymaga specjalistycznego treningu i doświadczenia. Należy sprawdzić prawidłowe położenie rurki intubacyjnej poprzez ocenę kliniczną oraz kontrolę końcowo-wydechowego dwutlenku węgla (kapnografia). Rurka intubacyjna musi być zabezpieczona przed przemieszczeniem. Niezbędne jest stałe monitorowanie parametrów życiowych 96. Konieczne jest również zaplanowanie alternatywnej metody udrażniania dróg oddechowych w przypadku niemożności intubacji tchawicy. Obecnie nie ma opartych na badaniach naukowych rekomendacji definiujących zależności pomiędzy rodzajem sprzętu, pacjentem a osobą wykonująca intubację u dzieci w pomocy przedszpitalnej. Intubację u dzieci w pomocy przedszpitalnej można rozważyć w następujących okolicznościach: 1. Drożność dróg oddechowych i/lub oddychanie są poważnie upośledzone lub zagrożone. 2. Rodzaj i czas trwania transportu wymaga wczesnego zabezpieczenia dróg oddechowych (np. transport lotniczy). 3. Jeśli osoba intubująca jest wystarczająco przeszkolona w zabezpieczaniu dróg oddechowych u dzieci, włączając w to użycie leków ułatwiających intubację 97. Technika szybkiej indukcji i intubacji Dziecko w stanie zatrzymania krążenia lub w głębokiej śpiączce nie wymaga sedacji oraz analgezji do wykonania intubacji, w innym przypadku intubacja musi być poprzedzona natlenieniem (spokojna wentylacja za pomocą worka samorozprężalnego z maską jest niekiedy wymagana, aby zapobiec hipoksji), szybką sedacją, analgezją i zastosowaniem środków zwiotczających mięśnie, aby zminimalizować ryzyko wystąpienia powikłań lub niepowodzenia intubacji 98. Osoba wykonująca intubację musi mieć doświadczenie i być zaznajomiona z lekami używanymi w trakcie szybkiej indukcji. Zastosowanie uciśnięcia chrząstki pierścieniowatej może zapobiec lub zmniejszyć ryzyko regurgitacji treści żołądkowej 99,100, lecz może również prowadzić do zniekształcenia dróg oddechowych i spowodować, że laryngoskopia i intubacja będą trudniejsze do wykonania 101. Uciśnięcia chrząstki pierścieniowatej nie należy stosować, jeśli albo intubacja, albo natlenianie są ograniczone. Rozmiary rurek intubacyjnych Ogólne zalecenia dotyczące doboru średnicy wewnętrznej rurki intubacyjnej (ID Internal Diameter) w zależności od wieku zostały przedstawione w tabeli Są to tylko wskazówki, zawsze należy mieć dostępne rurki intubacyjne o jeden rozmiar większy i mniejszy. Rozmiar rurki intubacyjnej określa się również na podstawie długości ciała dziecka wyznaczanego przy użyciu taśmy resuscytacyjnej 108. Porównanie rurek intubacyjnych bez i z mankietem uszczelniającym Rurki intubacyjne bez mankietu uszczelniającego tradycyjnie stosuje się u dzieci do 8. roku życia, natomiast rurki z mankietem mogą być bardziej przydatne w niektórych okolicznościach, np.: gdy zmniejszona jest podatność płuc, są wysokie opory w drogach oddechowych lub z powodu dużego przecieku powietrza wokół rurki na poziomie głośni 102,109,110. Zastosowanie rurek z mankietem sprawia również, że zwiększa się prawdopodobieństwo wybrania właściwego rozmiaru za pierwszym razem 102,103,111. Prawidłowo dobrana rurka z mankietem jest tak samo bezpieczna jak rurka bez mankietu w przypadku niemowląt i dzieci (ale nie u noworodków) pod warunkiem, że zwraca się należytą uwagę na jej umiejscowienie, rozmiar i ciśnienie w mankiecie uszczelniającym 109,110,112. Zbyt wysokie ciśnienie w tym 6
195 192 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman Tabela 6.2. Ogólne zalecenia dla stosowania rurek z lub bez mankietu uszczelniającego (średnica wewnętrzna w mm) Bez mankietu Z mankietem Noworodki wcześniaki Czas trwania ciąży [tygodnie]/10 Nie stosuje się Noworodki urodzone o czasie 3.5 Zazwyczaj się nie stosuje Niemowlęta Dzieci r.ż Dzieci >2. r.ż. Wiek/4 + 4 Wiek/ mankiecie może prowadzić do spowodowanego niedokrwieniem uszkodzenia tkanek otaczających krtań i w efekcie doprowadzić do zwężenia na tym poziomie. Należy utrzymywać ciśnienie w mankiecie poniżej 25 cm H 2 O i stale je kontrolować 112. Potwierdzenie prawidłowego położenia rurki intubacyjnej Przemieszczenie, złe umiejscowienie lub zatkanie rurki często występuje u zaintubowanych dzieci i wiąże się ze zwiększonym ryzykiem zgonu 113,114. Żadna metoda stosowana pojedynczo nie jest w 100% niezawodna w rozróżnieniu intubacji do przełyku od intubacji dotchawiczej Ocena prawidłowego położenia rurki intubacyjnej opiera się na: obserwacji w laryngoskopii bezpośredniej przejścia rurki przez struny głosowe; wykryciu końcowo-wydechowego dwutlenku węgla (dzięki kolorymetrii lub kapnometrii/kapnografii) u dziecka z rytmem perfuzyjnym (można je również obserwować przy skutecznej RKO, lecz nie jest do końca wiarygodne); obserwacji symetrycznych ruchów klatki piersiowej podczas wentylacji dodatnimi ciśnieniami; obserwacji pojawienia się pary wodnej w rurce intubacyjnej podczas wydechowej fazy wentylacji; braku rozdęcia żołądka; symetrycznie słyszalnych szmerach oddechowych przy obustronnym osłuchiwaniu w liniach pachowych i szczytach płuc; braku odgłosów obecności powietrza przy osłuchiwaniu żołądka; poprawie lub stabilizacji saturacji na oczekiwanym poziomie (uwaga na opóźnienie sygnału!); normalizacji częstości pracy serca do wartości należnej dla wieku (lub pozostawania w granicach normy) (uwaga objaw spóźniony!). Jeżeli u dziecka doszło do zatrzymania krążenia i nie można wykryć końcowo-wydechowego CO 2 pomimo prawidłowo prowadzonych uciśnięć klatki piersiowej oraz w razie jakichkolwiek wątpliwości, należy potwierdzić położenie rurki intubacyjnej w laryngoskopii bezpośredniej. Po prawidłowym umieszeniu rurki intubacyjnej i potwierdzeniu położenia należy zabezpieczyć rurkę i ponownie ocenić jej położenie. Należy utrzymywać głowę dziecka w pozycji neutralnej. Przygięcie głowy powoduje wsunięcie się rurki głębiej do tchawicy, podczas gdy jej odgięcie może wysunąć ją z dróg oddechowych 118. Konieczne jest potwierdzenie położenia rurki intubacyjnej w środkowej części tchawicy poprzez wykonanie zdjęcia rentgenowskiego AP klatki piersiowej; koniec rurki intubacyjnej powinien znajdować się na wysokości drugiego lub trzeciego kręgu piersiowego. DOPES jest użytecznym angielskim akronimem obejmującym przyczyny nagłego pogorszenia się stanu zaintubowanego dziecka. D (Displacement) przemieszczenie się rurki intubacyjnej O (Obstruction) zatkanie się rurki intubacyjnej lub układu nawilżacza P E S (Pneumothorax) odma prężna (Equipment) problemy ze sprzętem (źródło gazów, maska twarzowa z workiem samorozprężalnym, respirator itd.) (Stomach) rozdęcie żołądka, które może utrudnić wentylację (w związku z uniesieniem przepony). Oddychanie Tlenoterapia W początkowym etapie resuscytacji należy stosować najwyższe stężenia tlenu (tzn. 100%). Po przywróceniu krążenia należy zapewnić wystarczającą ilość tlenu pozwalającą utrzymać saturację krwi tętniczej (SaO 2 ) w zakresie wartości 94 98% 119,120. Badania przeprowadzone z udziałem noworodków sugerują występowanie pewnych korzyści z zastosowania powietrza podczas resuscytacji (zob. rozdział 7) 11, U starszych dzieci nie ma dowodów na ich istnienie, dlatego należy używać 100-procentowego tlenu w początkowym etapie resuscytacji. Po powrocie spontanicznego krążenia (Return of Spontaneous Circulation ROSC) należy w taki sposób regulować stężenie tlenu w mieszaninie wdechowej (FiO 2 ), aby uzyskać SaO 2 w zakresie wartości 94 98%. Jednakże po inhalacji dymu (zatrucie tlenkiem węgla) oraz w ostrej anemii, do momentu rozwiązania problemu, należy utrzymać wysokie FiO 2, gdyż w takich przypadkach rozpuszczony fizycznie tlen pełni ważną rolę w transporcie tlenu do tkanek. Wentylacja Osoby z wykształceniem medycznym zwykle nadmiernie wentylują podczas RKO, co może być szkodliwe. Hiperwetylacja powoduje wzrost ciśnienia w klatce piersiowej, spadek przepływu mózgowego i wieńcowego oraz gorszą przeżywalność, co potwierdzają badania na zwierzętach i z udziałem dorosłych Choć prawidłowa wentylacja jest celem, który należy osiągnąć podczas resuscytacji, trudne jest określenie dokładnej objętości minutowej, którą należy dostarczyć pacjentowi. Prostą wskazówką może być fakt, że idealna objętość oddechowa powinna spowodować niewielkie uniesienie się klatki piersiowej. Należy używać stosunku
196 Zaawansowane zabiegi resuscytacyjne u dzieci uciśnięć klatki piersiowej do 2 wentylacji, a częstość uciśnięć klatki piersiowej powinna wynosić /min 125. Po przywróceniu krążenia należy prowadzić prawidłową wentylację (częstość/objętość) w oparciu o wiek poszkodowanego i tak szybko, jak to możliwe, o monitorowanie końcowowydechowego CO 2 i wartości gazometrii. Gdy tylko drogi oddechowe zostaną zabezpieczone poprzez intubację, można kontynuować wentylację dodatnimi ciśnieniami z częstością oddechów/min bez przerywania uciskania klatki piersiowej. Należy zwrócić uwagę na konieczność zapewnienia wystarczającej wentylacji płuc podczas uciśnięć klatki piersiowej. Po przywróceniu krążenia lub u dziecka z rytmem perfuzyjnym należy wentylować z częstością oddechów/min w celu utrzymania ciśnienia parcjalnego dwutlenku węgla (PaCO 2 ) w granicach normy. Hiperwetylacja i hipowentylacja są szkodliwe. Wentylacja za pomocą worka samorozprężalnego i maski Wentylacja za pomocą worka samorozprężalnego i maski jest skuteczną i bezpieczną metodą u dzieci wymagających wspomagania wentylacji przez krótki okres, np. w pomocy przedszpitalnej lub w oddziale ratunkowym 114, Ocena efektywności tego rodzaju wentylacji polega na obserwowaniu odpowiedniego uniesienia się klatki piersiowej, monitorowaniu częstości pracy serca, osłuchiwaniu szmerów oddechowych oraz obserwacji wskazań pulsoksymetru (SpO 2 ). Każda osoba z wykształceniem medycznym pracująca z dziećmi musi umieć prowadzić skuteczną wentylację za pomocą maski i worka samorozprężalnego. Przedłużona wentylacja Jeśli wymagana jest przedłużona wentylacja, korzyści wynikające z zabezpieczenia dróg oddechowych prawdopodobnie przeważają nad potencjalnym ryzykiem związanym z intubacją dotchawiczą. W sytuacjach nagłych można stosować zarówno rurki z mankietem uszczelniającym, jak i bez. Monitorowanie oddychania i wentylacji Końcowo-wydechowe CO 2 Monitorowanie końcowo-wydechowego CO 2 (ETCO 2 ) za pomocą detektora zmieniającego kolor lub kapnometru pozwala potwierdzić prawidłowe położenie rurki intubacyjnej u dzieci ważących powyżej 2 kg i może być przydatne zarówno w warunkach przed-, jak i wewnątrzszpitalnych oraz podczas każdego transportu pacjenta pediatrycznego Zmiana koloru lub obecność zapisu fali na ekranie kapnografu po więcej niż czterech wentylacjach wskazuje na to, że rurka jest w drzewie oskrzelowym zarówno w przypadku rytmu z zachowaną perfuzją, jak i w zatrzymaniu krążenia. Prawidłowy wynik kapnografii nie wyklucza intubacji prawego głównego oskrzela. Brak lub niski poziom końcowo-wydechowego CO 2 podczas zatrzymania krążenia może nie wynikać z przemieszczenia się rurki intubacyjnej, ale odzwierciedlać całkowity brak lub niski przepływ krwi w krążeniu płucnym Kapnografia może również dostarczać informacje na temat skuteczności uciśnięć klatki piersiowej oraz być wczesnym wskaźnikiem powrotu spontanicznego krążenia 144,145. Należy poprawić jakość uciśnięć, jeśli wartość ETCO 2 pozostaje poniżej 15 mm Hg (2kPa). Należy zwrócić szczególną uwagę na interpretację wartości ETCO 2 zwłaszcza po podaniu adrenaliny lub innego leku powodującego wazokonstrykcję, co może wpływać na przejściowe obniżenie wartości ETCO , oraz po podaniu wodorowęglanu sodu, co może doprowadzić do przejściowego wzrostu wartości ETCO Dotychczas brak jest dowodów na wartość progową ETCO 2, która byłaby wskaźnikiem pozwalającym na przerwanie czynności resuscytacyjnych. Detektory przełykowe Użycie elastycznej gumowej gruszki lub aspiracja za pomocą specjalnej strzykawki (detektor przełykowy) może być użyteczną metodą potwierdzającą wtórnie prawidłowe położenie rurki u dzieci z rytmem perfuzyjnym 152,153. Nie ma żadnych badań naukowych na temat zastosowania tych urządzeń u dzieci w zatrzymaniu krążenia. Pulsoksymetria Kliniczna ocena poziomu tlenu w krwi tętniczej (SaO 2 ) jest niepewna, dlatego należy stale monitorować saturację obwodową u dziecka za pomocą pulsoksymetrii (SpO 2 ). Pulsoksymetria w niektórych przypadkach może nie być wiarygodna, np. jeśli dziecko jest w stanie niewydolności krążeniowej, podczas zatrzymania krążenia lub przy złej perfuzji obwodowej. Pomimo że pulsoksymetria jest relatywnie prosta do zastosowania, nie jest dobrym wskaźnikiem umożliwiającym rozpoznanie sytuacji, gdzie doszło do przemieszczenia się rurki intubacyjnej. Kapnografia, szybciej niż pulsoksymetria, pozwala wykryć wysunięcie się rurki intubacyjnej 154. Krążenie Dostęp donaczyniowy Dostęp donaczyniowy jest niezbędny do podawania leków i płynów oraz w celu uzyskania próbek krwi. Dostęp dożylny może być trudny do uzyskania podczas resuscytacji niemowlęcia lub dziecka. U dzieci w stanie zagrożenia życia, gdy tylko dostęp dożylny nie jest łatwy do uzyskania, należy wcześnie rozważyć założenie dostępu doszpikowego, zwłaszcza u dzieci z zatrzymaniem krążenia lub w zdekompensowanej niewydolności krążenia W każdym przypadku u dziecka w stanie krytycznym, jeśli próby założenia dostępu dożylnego trwają powyżej jednej minuty, należy uzyskać dostęp doszpikowy 155,158. Dostęp doszpikowy Dostęp doszpikowy jest szybką, bezpieczną i skuteczną drogą do podawania leków, płynów i preparatów krwiopochodnych Początek działania i czas potrzebny do osiągnięcia odpowiedniego stężenia leku w osoczu są podobne do tych uzyskiwanych po podaniu do dostępu centralnego 169,170. Próbki szpiku kostnego mogą być użyte do oznaczenia grupy krwi i próby krzyżowej 171, analiz chemicznych 172,173 oraz wykonania gazometrii (wartości są porównywalne z wartościami gazometrii krwi żylnej, jeśli żaden lek nie został po- 6
197 194 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman 6 dany do jamy szpikowej) 172,174, 175,176. Jednakże próbki mogą zniszczyć analizator parametrów krytycznych i powinny być badane w laboratorium biochemicznym. Po iniekcji każdego leku należy podać bolus soli fizjologicznej, aby zapewnić rozprzestrzenienie się leku w obrębie jamy szpikowej, co umożliwi szybszą jego dystrybucję do krążenia centralnego. Duże bolusy płynów należy podawać pod ciśnieniem (np. wykorzystując zestaw do szybkich przetoczeń lub strzykawkę przyp. tłum.). Dostęp doszpikowy może być utrzymany do czasu uzyskania pewnego dostępu dożylnego. Korzyści z zastosowania półautomatycznych urządzeń do zakładania dostępów doszpikowych wymagają dalszej oceny, ale wstępne doświadczenia w ich stosowaniu pokazują, że są to urządzenia szybkie i skuteczne do uzyskania dostępu do układu krążenia 167,168,177,178. Dostęp dożylny Obwodowy dostęp dożylny zapewnia odpowiednie stężenie leków w osoczu i związaną z tym odpowiedź kliniczną równoważną z dostępem centralnym lub doszpikowym 156,157, Dostępy centralne są pewniejsze i można je dłużej utrzymać, ale w porównaniu z dostępem doszpikowym lub obwodowym dożylnym nie zapewniają żadnych dodatkowych korzyści w postępowaniu resuscytacyjnym 156, Dostęp dotchawiczy Dostępy doszpikowy lub dożylny są zdecydowanie preferowaną drogą podawania leków w stosunku do dostępu dotchawiczego 182. Leki podawane dotchawiczo mają bardzo zmienną absorpcję, ale rekomendowany jest poniższy schemat dawkowania: adrenalina 100 μg/kg lidokaina 2 3 mg/kg atropina 30 μg/kg Nieznana jest optymalna dawka naloksonu. Należy rozcieńczyć lek w 5 ml soli fizjologicznej i po podaniu wykonać pięć wentylacji Nie należy podawać do rurki intubacyjnej leków nierozpuszczalnych w tłuszczach (np. glukoza, wodorowęglany, wapń), ponieważ mogą spowodować uszkodzenie błony śluzowej dróg oddechowych. Płyny i leki Kiedy dziecko ma objawy niewydolności krążenia, a nie ma objawów przeciążenia układu krążenia płynami, wskazane jest odpowiednie wypełnienie łożyska naczyniowego 186. Niezależnie od typu niewydolności krążenia, izotoniczne krystaloidy są rekomendowane jako wstępna resuscytacja płynowa u niemowląt i dzieci. Jeśli ogólnoustrojowa perfuzja jest niewystarczająca, nawet przy prawidłowym ciśnieniu krwi należy podać bolus izotonicznych krystaloidów 20 ml/kg. Po każdym bolusie płynów powinno się ponownie ocenić stan kliniczny dziecka według reguły ABC, aby zadecydować, czy jest potrzebny kolejny bolus płynów lub inny sposób leczenia. Nie ma wystarczających danych klinicznych, aby zalecać stosowanie hipertonicznych roztworów soli we wstrząsie ze współistniejącym urazem głowy lub hipowolemią 187,188. Nie ma również wystarczających danych klinicznych zalecających odroczenie resuscytacji płynowej u dzieci z tępym urazem i niskim ciśnieniem tętniczym krwi 189. Należy unikać roztworów zawierających glukozę, o ile nie stwierdza się hipoglikemii Konieczne jest monitorowanie poziomu glukozy, aby uniknąć hipoglikemii, zwłaszcza że u niemowląt i małych dzieci istnieje skłonność do występowania spadków stężenia glukozy. Adenozyna Adenozyna jest endogennym nukleotydem, który powoduje krótkotrwałą blokadę przewodzenia przedsionkowokomorowego (AV) i utrudnia przewodnictwo przez dodatkowe drogi przewodzenia w mechanizmie re-entry na poziomie węzła przedsionkowo-komorowego. Adenozyna jest zalecana w leczeniu tachykardii nadkomorowych (SVT) 194. Jest bezpieczna w użyciu, ponieważ ma krótki okres półtrwania (10 s), należy ją podać do żył kończyny górnej lub do żył centralnych, aby skrócić czas dotarcia do serca. Adenozynę należy podać szybko w bolusie i natychmiast przepłukać 3 5 ml roztworu soli fizjologicznej 195. Adenozynę należy stosować ostrożnie u pacjentów z astmą, blokiem przedsionkowo-komorowym drugiego lub trzeciego stopnia, zespołem wydłużonego odcinka QT i u pacjentów po przeszczepie serca. Adrenalina (epinefryna) Adrenalina jest endogenną katecholaminą z silną α, β 1 i β 2 aktywnością adrenergiczną. Jest podstawowym lekiem stosowanym w zatrzymaniu krążenia i znajduje ważne miejsce w algorytmach leczenia rytmów nie do defibrylacji i do defibrylacji. Adrenalina powoduje skurcz naczyń, podnosi ciśnienie rozkurczowe i przez to poprawia ciśnienie perfuzyjne w naczyniach wieńcowych, zwiększa kurczliwość mięśnia sercowego, pobudza skurcze spontaniczne, zwiększa amplitudę i częstotliwość migotania komór (VF), tym samym zwiększając prawdopodobieństwo powodzenia defibrylacji. Zalecane dawki adrenaliny u dzieci, dla dawki pierwszej i kolejnych, zarówno dożylne jak i doszpikowe, to 10 μg/kg. Maksymalna pojedyncza dawka wynosi 1 mg. Jeśli są wskazania, kolejne dawki adrenaliny należy podawać co 3 5 minut. Podawanie adrenaliny do rurki intubacyjnej nie jest obecnie zalecane , lecz jeśli używa się tej drogi, dawka adrenaliny powinna być 10-krotnie większa (100 μg/kg). Nie jest zalecane stosowanie rutynowo wyższych dożylnych lub doszpikowych dawek adrenaliny, ponieważ takie działanie nie podnosi przeżywalności ani nie zmniejsza liczby powikłań neurologicznych po zatrzymaniu krążenia Po przywróceniu spontanicznego krążenia może być wymagany ciągły wlew adrenaliny. Jej skuteczność hemodynamiczna zależy od dawki, a w przypadku dzieci występują także znaczące różnice osobnicze w odpowiedzi na lek. Należy miareczkować wlew leku w zależności od oczekiwanego efektu. Szybka infuzja dużej ilości leku może spowodować
198 Zaawansowane zabiegi resuscytacyjne u dzieci 195 nadmierny skurcz naczyń, upośledzać krążenie w kończynach, krążenie krezkowe i nerkowe. Wysokie dawki adrenaliny mogą powodować groźny wzrost ciśnienia i zaburzenia rytmu serca pod postacią częstoskurczu 204. Aby uniknąć uszkodzenia tkanek, należy podawać adrenalinę przez pewny dostęp donaczyniowy (iv lub io). Adrenalina (i inne katecholaminy) mogą być inaktywowane przez roztwory zasadowe i nigdy nie powinny być mieszane z wodorowęglanem sodu 205. Amiodaron Amiodaron jest niekompetencyjnym inhibitorem receptorów adrenergicznych, hamuje przewodzenie w tkance mięśnia sercowego, odpowiadając za zwolnienie przewodnictwa w węźle AV, wydłużenie odstępu QT i okresu refrakcji. Poza leczeniem opornego na defibrylację VF lub VT bez tętna, amiodaron należy podawać powoli (przez min), pod kontrolą ciśnienia tętniczego krwi i monitorowania EKG, aby uniknąć spadku ciśnienia. Ten skutek uboczny występuje rzadziej przy wodnym roztworze leku 206. Inne, rzadziej występujące, ale istotne, skutki uboczne to bradykardia i wielokształtny VT 207. Atropina Atropina zwiększa automatyzm węzła zatokowego i przedsionkowo-komorowego poprzez blokowanie układu parasympatycznego. Może też zwiększać szybkość przewodzenia w węźle AV. Małe dawki (<100 μg) mogą powodować paradoksalną bradykardię 208. W bradykardii z upośledzoną perfuzją, która nie odpowiada na wentylację i natlenianie, lekiem pierwszego rzutu jest adrenalina, nie atropina. Atropinę zaleca się do stosowania w bradykardii spowodowanej zwiększonym napięciem nerwu błędnego lub w zatruciu lekami cholinergicznymi Wapń Wapń jest niezbędny dla funkcjonowania mięśnia sercowego 213,214, ale rutynowe podawanie wapnia nie zwiększa przeżywalności w zatrzymaniu krążenia Wapń jest wskazany w hipokalcemii, przedawkowaniu brokerów kanałów wapniowych, hipermagnezemii i hiperkaliemii Glukoza Badania dotyczące noworodków, dzieci i dorosłych pokazują, że występowanie zarówno hiperglikemii jak i hipoglikemii jest związane ze złym rokowaniem po zatrzymaniu krążenia , ale wątpliwe jest, czy jest to związek przyczynowo-skutkowy 224. Należy sprawdzić poziom glukozy we krwi i dokładnie go monitorować u każdego chorego dziecka lub dziecka z urazem, włączając w to pacjentów po zatrzymaniu krążenia. Podczas RKO nie powinno się podawać płynów zawierających glukozę, chyba że występuje hipoglikemia. Należy unikać hipo- i hiperglikemii po powrocie spontanicznego krążenia. Bardzo precyzyjne kontrolowanie poziomu glukozy u dorosłych nie zwiększa przeżywalności w NZK w porównaniu z grupą, gdzie mniej restrykcyjnie kontrolowano ten poziom 225,226, jednocześnie zwiększa ryzyko hipoglikemii u noworodków, dzieci i dorosłych Magnez Nie ma żadnych dowodów potwierdzających konieczność rutynowego stosowania magnezu podczas zatrzymania krążenia 232. Podanie magnezu jest wskazane w przypadku dziecka z udokumentowaną hipomagnezemią lub z torsades de pointes, niezależnie od przyczyny 233. Wodorowęglan sodu Nie jest zalecane rutynowe stosowanie wodorowęglanu sodu podczas zatrzymania krążenia czy po powrocie spontanicznego krążenia 220,234,235. Po osiągnięciu efektywnej wentylacji i uciskaniu klatki piersiowej oraz po podaniu adrenaliny, podanie wodorowęglanu sodu może być rozważane u dzieci z przedłużającym się zatrzymaniem krążenia i/lub ciężką kwasicą metaboliczną. Można go także wziąć pod uwagę w przypadku niestabilności hemodynamicznej i współistniejącej hiperkaliemii oraz w leczeniu zatrucia trójcyklicznymi lekami antydepresyjnymi. Nadmierna podaż wodorowęglanu sodu może pogorszyć dostarczanie tlenu do tkanek, wywołać hipokaliemię, hipernatremię i hiperosmię oraz inaktywować katecholaminy. Lidokaina U dorosłych lidokaina jest mniej skuteczna od amiodaronu w leczeniu opornego na defibrylację migotania komór lub częstoskurczu komorowego bez tętna 236 i dlatego nie jest zalecana jako lek pierwszego rzutu w leczeniu tych zaburzeń u dzieci. Prokainamid Prokainamid zwalnia wewnątrzprzedsionkowe przewodnictwo oraz wydłuża czas trwania zespołu QRS i odstęp QT. Może być używany w leczeniu tachykardii nadkomorowej (SVT) lub częstoskurczu komorowego 240 opornego na inne leki u dziecka stabilnego hemodynamicznie. Jednakże wyniki badań u dzieci są nieliczne i z tego powodu prokainamid powinien być stosowany ostrożnie 241,242. Prokainamid ma silne działanie naczyniorozszerzające i może powodować hipotensję, dlatego należy go podawać powoli i uważnie monitorować stan pacjenta Wazopresyna terlipresyna Wazopresyna jest endogennym hormonem, który poprzez działanie na specyficzne receptory pośredniczy w skurczu naczyń (poprzez receptory V1) i resorpcji zwrotnej wody w kanalikach nerkowych (poprzez receptory V2) 246. Obecnie brak jest wystarczających dowodów, aby poprzeć lub kwestionować użycie wazopresyny lub terlipresyny jako alternatywę lub w połączeniu z adrenaliną w jakimkolwiek mechanizmie zatrzymania krążenia u dorosłych lub dzieci Na podstawie niektórych badań odnotowano, że terlipresyna (długodziałający analog wazopresyny o zbliżonym działaniu) poprawia hemodynamikę krążenia u dzieci z opornym na leczenie wstrząsem septycznym z wazodilatacją, lecz wpływ tego leku na przeżywalność jest mniej oczywisty ,259,260. Dwie serie pediatrycznych przypadków klinicznych sugerują, że terlipresyna może być skuteczna w opornym na leczenie zatrzymaniu krążenia 258,261. Te leki mogą być używane w opornym na leczenie zatrzymaniu krążenia, po podaniu kilku dawek adrenaliny. 6
199 196 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman 6 Defibrylatory Defibrylatory mogą być obsługiwane automatycznie lub manualnie. Mogą one również dostarczać energię jednofazową lub dwufazową. Defibrylatory manualne są w stanie dostarczyć każdą wymaganą wartość energii, począwszy od właściwej dla noworodków wzwyż. Muszą być one dostępne w szpitalach i innych ośrodkach zajmujących się opieką nad dziećmi z ryzykiem zatrzymania krążenia. Automatyczne defibrylatory zewnętrzne mają fabrycznie ustawione wszystkie parametry pracy, wliczając w to także poziom energii. Rozmiar elektrod samoprzylepnych i łyżek defibrylatora Należy wybrać największe dostępne łyżki w celu zapewnienia dobrego kontaktu ze ścianą klatki piersiowej. Nie jest znany idealny rozmiar łyżek, jakkolwiek podczas użycia należy zachować odpowiedni odstęp pomiędzy nimi 13,262,263. Rekomendowane są następujące rozmiary: 4,5 cm średnicy dla niemowląt i dzieci o wadze poniżej 10 kg, 8 12 cm średnicy dla dzieci o wadze powyżej 10 kg (powyżej 1. roku życia). Aby zmniejszyć impedancję skóry i klatki piersiowej, należy umieścić pomiędzy skórą a łyżkami defibrylatora materiał przewodzący. Skuteczne są podkładki żelowe lub fabryczne elektrody samoprzylepne. Nie należy używać żelu stosowanego w ultrasonografii, gazików lub podkładek nasączonych roztworem soli fizjologicznej lub alkoholem. Położenie łyżek Należy pewnie umieścić łyżki na odsłoniętej klatce piersiowej w pozycji przednio-bocznej. Jedną łyżkę należy umieścić poniżej prawego obojczyka, a drugą pod lewą pachą (ryc. 6.8). Jeśli łyżki są za duże, istnieje niebezpieczeństwo powstania łuku elektrycznego pomiędzy nimi. W takiej sytuacji jedną należy umieścić na plecach poniżej lewej łopatki, a drugą z przodu na lewo od mostka. Takie położenie łyżek określa się jako pozycję przednio-tylną i jest również akceptowalne. Optymalna siła nacisku na łyżki Aby zmniejszyć opór klatki piersiowej podczas defibrylacji, należy naciskać na łyżki z siłą 3 kg dla dzieci poniżej 10 kg i z siłą 5 kg dla większych dzieci 264,265. W praktyce oznacza to, że łyżki powinny być mocno dociśnięte do ściany klatki piersiowej. Wartości energii stosowane u dzieci Nieznana jest idealna wartość energii, jakiej należy użyć, aby wykonać bezpieczną i skuteczną defibrylację. Defibrylacja energią dwufazową jest co najmniej równie skuteczna i powoduje mniejszą dysfunkcję miokardium po defibrylacji, niż defibrylacja energią jednofazową 36,49,51-53,266. Badania na zwierzętach wykazują lepsze wyniki w przypadku wartości energii stosowanych w pediatrii (3 4 J/kg) w porównaniu z niższymi 49 lub stosowanymi u dorosłych 38. Kliniczne badania nad pacjentami pediatrycznymi wykazują, że energia 2 J/kg jest niewystarczająca w większości przypadków 12,38,42. Wartości wyższe niż 4 J/kg (tak duże jak 9 J/kg) zapewniają skuteczną defibrylację u dzieci przy stosunkowo niewielkich efektach ubocznych 29,48. Jeśli używa się defibrylatorów manualnych (preferowane dwufazowe, jednak jednofazowe są również akceptowalne), należy użyć energii 4 J/kg dla pierwszego i kolejnych wyładowań. Jeśli nie jest dostępny defibrylator manualny, należy użyć AED, które rozpoznaje pediatryczne rytmy do defibrylacji 31,32,267. Takie AED powinno być wyposażone w urządzenie redukujące poziom energii do wartości odpowiedniej dla dzieci pomiędzy rokiem życia (50 75 J) 34,37. Jeśli takie AED jest niedostępne, należy użyć standardowego AED, zaprogramowanego na dostarczanie energii używanych u dorosłych. W przypadku dzieci powyżej 8. roku życia należy użyć normalnego AED ze standardowymi elektrodami. Chociaż nie ma wystarczających dowodów, aby poprzeć zastosowanie AED u dzieci poniżej 1. roku życia (preferowane z możliwością zmniejszenia energii), a rekomendacje są ograniczone do kilku przypadków klinicznych 39,40, jest to akceptowalne, jeżeli nie jest dostępna inna opcja leczenia. Zaawansowane zabiegi resuscytacyjne w zatrzymaniu krążenia (ryc. 6.9) Ryc Ułożenie łyżek w celu wykonania defibrylacji dziecko A B C Rozpocznij i kontynuuj resuscytację zgodnie z algorytmem BLS. Zapewnij natlenianie i wentylację za pomocą worka samorozprężalnego z maską. Zapewnij wentylację dodatnimi ciśnieniami z wysokim stężeniem tlenu. Wykonaj 5 efektywnych oddechów ratowniczych, a następnie rozpocznij uciskanie klatki piersiowej i wentylację dodatnimi ciśnieniami w stosunku 15 : 2. Unikaj zmęczenia ratownika poprzez częstą zmianę osoby uciskającej klatkę piersiową. Zapewnij monitorowanie rytmu serca. Oceń rytm serca i oznaki krążenia (± sprawdź tętno na głównych tętnicach, nie dłużej niż 10 s).
200 Zaawansowane zabiegi resuscytacyjne u dzieci 197 Zaawansowane zabiegi resuscytacyjne u dzieci 6 Ryc Algorytm zaawansowanych zabiegów resuscytacyjnych u dzieci Rytmy nie do defibrylacji asystolia, aktywność elektryczna bez tętna (PEA) Podaj adrenalinę w dawce 10 μg/kg dożylnie lub doszpikowo co 3 5 minut. Rozpoznaj i lecz odwracalne przyczyny zatrzymania krążenia (4 H i 4 T) (ryc. 6.10). Rytmy do defibrylacji VF/VT Natychmiast wykonaj defibrylację (4 J/kg ). Naładuj defibrylator, podczas gdy drugi ratownik prowadzi uciśnięcia klatki piersiowej. Gdy defibrylator jest naładowany, przerwij uciskanie klatki piersiowej i upewnij się, że nikt nie dotyka pacjenta. Minimalizuj czas pomiędzy przerwaniem uciśnięć klatki piersiowej a dostarczeniem wyładowania nawet opóźnienie 5 10 sekund zmniejsza szansę na skuteczną defibrylację 268,269. Wykonaj jedną defibrylację.
201 198 D. Biarent, R. Bingham, Ch. Eich, J. López-Herce, I. Maconochie, A. Rodríguez-Núñez, Th. Rajka, D. Zideman Zatrzymanie krążenia: rytm nie do defibrylacji Ryc Algorytm postępowania w przypadku rytmu nie do defibrylacji u dzieci Zatrzymanie krążenia: rytm do defibrylacji 6 Ryc Algorytm postępowania w przypadku rytmu do defibrylacji u dzieci Tak szybko, jak to możliwe, powróć do RKO bez ponownej oceny rytmu. Po 2. minutach przez krótki okres czasu sprawdź zapis rytmu na monitorze. Jeśli nadal występuje VF/VT, wykonaj drugą defibrylację (4 J/kg). Natychmiast rozpocznij RKO przez 2 minuty bez ponownej oceny rytmu. Przerwij na krótko, by ocenić rytm, i jeśli nadal występuje VF/VT, wykonaj trzecią defibrylację energią 4 J/kg. Podaj adrenalinę w dawce 10 μg/kg i amiodaron w dawce 5 mg/kg po wykonaniu trzeciej defibrylacji, równocześnie z rozpoczęciem RKO. Podawaj adrenalinę co drugi cykl (tzn. co 3 5 minut podczas RKO). Podaj drugą dawkę amiodaronu 5 mg/kg 270, jeśli nadal występuje VF/VT po piątej defibrylacji. Jeśli u dziecka nadal występuje VF/VT, kontynuuj wykonywanie defibrylacji wartością 4 J/kg na zmianę z 2 minutami RKO. Jeśli widoczne są oznaki życia, oceń rytm na monitorze w celu poszukiwania zorganizowanej aktywności elektrycznej serca i jeśli jest obecna, sprawdź oznaki krążenia i tętno na dużych tętnicach oraz oceń wydolność hemodynamiczną dziecka (ciśnienie tętnicze krwi, tętno na naczyniach obwodowych, nawrót kapilarny). Rozpoznaj i lecz odwracalne przyczyny zatrzymania krążenia (4 H, 4 T), pamiętając, że pierwsze dwa H (hipoksja i hipowolemia) są najbardziej powszechną przyczyną zatrzymania krążenia u dzieci w stanie zagrożenia życia lub u dzieci z urazem (ryc. 6.11). Jeśli defibrylacja była skuteczna, ale VF/VT bez tętna powróciło, podejmij ponownie RKO, podaj amiodaron i defibryluj kolejny raz energią 4 J/kg. Rozpocznij wlew ciągły amiodaronu. Odwracalne przyczyny zatrzymania krążenia Odwracalne przyczyny zatrzymania krążenia (4 H i 4 T) zostaną pokrótce omówione w tym rozdziale:
Podstawowe zabiegi resuscytacyjne u dorosłych
 1 Podstawowe zabiegi resuscytacyjne u dorosłych Algorytm BLS zaleca: 1. Upewnij się czy poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni. 2. Sprawdź reakcję poszkodowanego (rys. 1): delikatnie
1 Podstawowe zabiegi resuscytacyjne u dorosłych Algorytm BLS zaleca: 1. Upewnij się czy poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni. 2. Sprawdź reakcję poszkodowanego (rys. 1): delikatnie
PODSTAWOWE ZABIEGI RESUSCYTACYJNE U OSÓB DOROSŁYCH ZAWSZE PAMIĘTAJ O SWOIM BEZPIECZEŃSTWIE KURS KWALIFIKOWANEJ PIERWSZEJ POMOCY. Basic Life Support
 KURS KWALIFIKOWANEJ PIERWSZEJ POMOCY Wytyczne 2005 wg Europejskiej Rady ds. Resuscytacji OPRACOWANIE: mgr Dorota Ladowska mgr Sławomir Nawrot Gorzów Wlkp. 2010r. PODSTAWOWE ZABIEGI RESUSCYTACYJNE U OSÓB
KURS KWALIFIKOWANEJ PIERWSZEJ POMOCY Wytyczne 2005 wg Europejskiej Rady ds. Resuscytacji OPRACOWANIE: mgr Dorota Ladowska mgr Sławomir Nawrot Gorzów Wlkp. 2010r. PODSTAWOWE ZABIEGI RESUSCYTACYJNE U OSÓB
RESUSCYTACJA KRĄŻENIOWO ODDECHOWA
 RESUSCYTACJA KRĄŻENIOWO ODDECHOWA Podstawowe zabiegi resuscytacyjne u dorosłych: 1. Upewnij się, czy poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni 2. Sprawdź reakcję poszkodowanego (ryc.1):
RESUSCYTACJA KRĄŻENIOWO ODDECHOWA Podstawowe zabiegi resuscytacyjne u dorosłych: 1. Upewnij się, czy poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni 2. Sprawdź reakcję poszkodowanego (ryc.1):
Jak uczyd wg wytycznych 2010?
 Jak uczyd wg wytycznych 2010? Przeżycia w nagłym zatrzymaniu krążenia zależą od jakości dowodów naukowych leżących u podstaw wytycznych, efektywności nauczania i środków przeznaczonych na implementację
Jak uczyd wg wytycznych 2010? Przeżycia w nagłym zatrzymaniu krążenia zależą od jakości dowodów naukowych leżących u podstaw wytycznych, efektywności nauczania i środków przeznaczonych na implementację
Algorytm BLS sekwencja postępowania
 Algorytm BLS (basic live support) zaleca : 1. Upewnij się, czy poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni. 2. Sprawdź reakcję poszkodowanego, delikatnie potrząśnij za ramiona i głośno zapytaj:
Algorytm BLS (basic live support) zaleca : 1. Upewnij się, czy poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni. 2. Sprawdź reakcję poszkodowanego, delikatnie potrząśnij za ramiona i głośno zapytaj:
Polska Rada Resuscytacji ul. Radziwiłłowska 4, 31-026 Kraków www.prc.krakow.pl
 Polska Rada Resuscytacji ul. Radziwiłłowska 4, 31-026 Kraków www.prc.krakow.pl Podsumowanie głównych zmian w porównaniu z Wytycznymi 2005: Podstawowe zabiegi resuscytacyjne Zmiany w wytycznych dotyczące
Polska Rada Resuscytacji ul. Radziwiłłowska 4, 31-026 Kraków www.prc.krakow.pl Podsumowanie głównych zmian w porównaniu z Wytycznymi 2005: Podstawowe zabiegi resuscytacyjne Zmiany w wytycznych dotyczące
Europejska Rada Resuscytacji. Kurs Podstawowych Zabiegów Resuscytacyjnych i Automatycznej Defibrylacji Zewnętrznej
 Kurs Podstawowych Zabiegów Resuscytacyjnych i Automatycznej Defibrylacji Zewnętrznej CELE Po zakończeniu kursu uczestnik powinien umieć zademonstrować: Jak wykonać ocenę nieprzytomnego poszkodowanego Jak
Kurs Podstawowych Zabiegów Resuscytacyjnych i Automatycznej Defibrylacji Zewnętrznej CELE Po zakończeniu kursu uczestnik powinien umieć zademonstrować: Jak wykonać ocenę nieprzytomnego poszkodowanego Jak
ALGORYTM P-BLS. Podstawowe zabiegi resuscytacyjne u dzieci KURS KWALIFIKOWANEJ PIERWSZEJ POMOCY. P-BLS Paediatric Basic Life Support
 KURS KWALIFIKOWANEJ PIERWSZEJ POMOCY Wytyczne 2005 wg Europejskiej Rady ds. Resuscytacji Podstawowe zabiegi resuscytacyjne u dzieci OPRACOWANIE: mgr Dorota Ladowska mgr Sławomir Nawrot Gorzów Wlkp. 2010r.
KURS KWALIFIKOWANEJ PIERWSZEJ POMOCY Wytyczne 2005 wg Europejskiej Rady ds. Resuscytacji Podstawowe zabiegi resuscytacyjne u dzieci OPRACOWANIE: mgr Dorota Ladowska mgr Sławomir Nawrot Gorzów Wlkp. 2010r.
ZASADY UDZIELANIA PIERWSZEJ POMOCY RESUSCYTACJA KRĄŻENIOWO - ODDECHOWA
 ZASADY UDZIELANIA PIERWSZEJ POMOCY RESUSCYTACJA KRĄŻENIOWO - ODDECHOWA Upewnij się, czy poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni. Sprawdź reakcje poszkodowanego: delikatnie potrząśnij
ZASADY UDZIELANIA PIERWSZEJ POMOCY RESUSCYTACJA KRĄŻENIOWO - ODDECHOWA Upewnij się, czy poszkodowany i wszyscy świadkowie zdarzenia są bezpieczni. Sprawdź reakcje poszkodowanego: delikatnie potrząśnij
Wytyczne resuscytacji krążeniowooddechowej. 2005 (Update 2010)
 Wytyczne resuscytacji krążeniowooddechowej 2005 (Update 2010) II KATEDRA KARDIOLOGII CM UMK 2014 1 Mechanizmy nagłego zatrzymania krążenia (NZK) Migotanie komór szybka chaotyczna depolaryzacja i repolaryzacja
Wytyczne resuscytacji krążeniowooddechowej 2005 (Update 2010) II KATEDRA KARDIOLOGII CM UMK 2014 1 Mechanizmy nagłego zatrzymania krążenia (NZK) Migotanie komór szybka chaotyczna depolaryzacja i repolaryzacja
RESUSCYTACJA KRĄŻENIOWO - ODDECHOWA (RKO) CENTRUM POWIADAMIANIA RATUNKOWEGO W POZNANIU
 RESUSCYTACJA KRĄŻENIOWO - ODDECHOWA (RKO) CENTRUM POWIADAMIANIA RATUNKOWEGO W POZNANIU WIADOMOŚCI PODSTAWOWE Nagłe zatrzymanie krążenia (NZK) jest główną przyczyną śmierci w Europie Dochodzi do 350 700
RESUSCYTACJA KRĄŻENIOWO - ODDECHOWA (RKO) CENTRUM POWIADAMIANIA RATUNKOWEGO W POZNANIU WIADOMOŚCI PODSTAWOWE Nagłe zatrzymanie krążenia (NZK) jest główną przyczyną śmierci w Europie Dochodzi do 350 700
Łańcuch przeżycia 2015-04-23. Wytyczne resuscytacji krążeniowooddechowej. 2005 (Update 2010) Mechanizmy nagłego zatrzymania krążenia (NZK)
 Wytyczne resuscytacji krążeniowooddechowej 2005 (Update 2010) II KATEDRA KARDIOLOGII CM UMK 2014 Mechanizmy nagłego zatrzymania krążenia (NZK) Migotanie komór szybka chaotyczna depolaryzacja i repolaryzacja
Wytyczne resuscytacji krążeniowooddechowej 2005 (Update 2010) II KATEDRA KARDIOLOGII CM UMK 2014 Mechanizmy nagłego zatrzymania krążenia (NZK) Migotanie komór szybka chaotyczna depolaryzacja i repolaryzacja
RESUSCYTACJA DOROSŁEGO
 RESUSCYTACJA DOROSŁEGO W Europie rocznie dochodzi do około 700,000 nagłych zatrzymań krążenia z przyczyn kardiologicznych Przeżycia do wypisu ze szpitala wynoszą obecnie około 5-10% Podjęcie RKO przez
RESUSCYTACJA DOROSŁEGO W Europie rocznie dochodzi do około 700,000 nagłych zatrzymań krążenia z przyczyn kardiologicznych Przeżycia do wypisu ze szpitala wynoszą obecnie około 5-10% Podjęcie RKO przez
Kurs podstawowy RKO/AED. Resuscytacja Krążeniowo- Oddechowa i Automatyczna Defibrylacja Zewnętrzna
 Kurs podstawowy RKO/AED Resuscytacja Krążeniowo- Oddechowa i Automatyczna Defibrylacja Zewnętrzna Cele Po zakończeniu kursu uczestnik powinien umieć zademonstrować: Jak ocenić nieprzytomnego poszkodowanego
Kurs podstawowy RKO/AED Resuscytacja Krążeniowo- Oddechowa i Automatyczna Defibrylacja Zewnętrzna Cele Po zakończeniu kursu uczestnik powinien umieć zademonstrować: Jak ocenić nieprzytomnego poszkodowanego
BEZPIECZNE SERCE ZIELONEJ GÓRY Program Powszechnego Dostępu Do Defibrylacji
 BEZPIECZNE SERCE ZIELONEJ GÓRY Program Powszechnego Dostępu Do Defibrylacji Każdy łańcuch jest tak silny, jak silne jest jego najsłabsze ogniwo Lek. Szymon Michniewicz Specjalista medycyny ratunkowej Dyspozytor
BEZPIECZNE SERCE ZIELONEJ GÓRY Program Powszechnego Dostępu Do Defibrylacji Każdy łańcuch jest tak silny, jak silne jest jego najsłabsze ogniwo Lek. Szymon Michniewicz Specjalista medycyny ratunkowej Dyspozytor
Resuscytacja krążeniowo-oddechowa u osoby dorosłej i dziecka
 Resuscytacja krążeniowo-oddechowa u osoby dorosłej i dziecka dr n. o zdr. Krystyna Ziółkowska Akademia Pomorska w Słupsku Instytut Nauk o Zdrowiu Zakład Ratownictwa Medycznego BLS Basic Life Support Podstawowe
Resuscytacja krążeniowo-oddechowa u osoby dorosłej i dziecka dr n. o zdr. Krystyna Ziółkowska Akademia Pomorska w Słupsku Instytut Nauk o Zdrowiu Zakład Ratownictwa Medycznego BLS Basic Life Support Podstawowe
Wytyczne Resuscytacji 2015 Europejskiej Rady Resuscytacji
 Wytyczne Resuscytacji 2015 Europejskiej Rady Resuscytacji Prof. dr hab. med. Janusz Andres Katedra Anestezjologii i Intensywnej Terapii UJCM w Krakowie Polska Rada Resuscytacji janusz.andres@uj.edu.pl
Wytyczne Resuscytacji 2015 Europejskiej Rady Resuscytacji Prof. dr hab. med. Janusz Andres Katedra Anestezjologii i Intensywnej Terapii UJCM w Krakowie Polska Rada Resuscytacji janusz.andres@uj.edu.pl
Program powszechnego dostępu do wczesnej pomocy medycznej na Lotnisku Chopina
 Program powszechnego dostępu do wczesnej pomocy medycznej na Lotnisku Chopina Zespół Medycyny Ratunkowej Warszawa, 11-02-2009 Skróty używane w prezentacji AED - Automatic External Defibrillator automatyczny
Program powszechnego dostępu do wczesnej pomocy medycznej na Lotnisku Chopina Zespół Medycyny Ratunkowej Warszawa, 11-02-2009 Skróty używane w prezentacji AED - Automatic External Defibrillator automatyczny
Resuscytacja Krążeniowo-Oddechowa i Automatyczna Defibrylacja Zewnętrzna
 Resuscytacja Krążeniowo-Oddechowa i Automatyczna Defibrylacja Zewnętrzna Informacje podstawowe W Europie, co 45 sek. dochodzi do nagłego zatrzymania krążenia, Szczególnie ważnym elementem przed przybyciem
Resuscytacja Krążeniowo-Oddechowa i Automatyczna Defibrylacja Zewnętrzna Informacje podstawowe W Europie, co 45 sek. dochodzi do nagłego zatrzymania krążenia, Szczególnie ważnym elementem przed przybyciem
Wariant A: Na miejscu zdarzenia znajdują się osoby postronne Wariant B: Na miejscu zdarzenia nie ma osób postronnych
 R E S U S C Y T A C J A K R Ą Ż E N I O W O - O D D E C H O W A ALGORYTM RKO U DOROSŁYCH Wariant A: Na miejscu zdarzenia znajdują się osoby postronne Wariant B: Na miejscu zdarzenia nie ma osób postronnych
R E S U S C Y T A C J A K R Ą Ż E N I O W O - O D D E C H O W A ALGORYTM RKO U DOROSŁYCH Wariant A: Na miejscu zdarzenia znajdują się osoby postronne Wariant B: Na miejscu zdarzenia nie ma osób postronnych
5a. JeŜeli oddech jest prawidłowy: - ułóŝ poszkodowanego w pozycji bezpiecznej
 1.2 Resuscytacja krąŝeniowo- oddechowa Resuscytacja krąŝeniowo- oddechowa u dorosłych Obecnie wyróŝnia się 2 algorytmy postępowania w zaleŝności od zaawansowania oraz dostępnych środków: BLS polega na
1.2 Resuscytacja krąŝeniowo- oddechowa Resuscytacja krąŝeniowo- oddechowa u dorosłych Obecnie wyróŝnia się 2 algorytmy postępowania w zaleŝności od zaawansowania oraz dostępnych środków: BLS polega na
Podstawowe zabiegi resuscytacyjne. Zastosowanie AED
 Podstawowe zabiegi resuscytacyjne. Zastosowanie AED Szkolenie zgodne z wytycznymi ERC 2015 PLAN WYKŁADU Nagłe zatrzymanie krążenia (NZK) algorytmy postępowania Aspekty prawne Proces naturalnego umierania
Podstawowe zabiegi resuscytacyjne. Zastosowanie AED Szkolenie zgodne z wytycznymi ERC 2015 PLAN WYKŁADU Nagłe zatrzymanie krążenia (NZK) algorytmy postępowania Aspekty prawne Proces naturalnego umierania
Europejska Rada Resuscytacji. Kurs Podstawowych Zabiegów Resuscytacyjnych i Automatycznej Defibrylacji Zewnętrznej
 Kurs Podstawowych Zabiegów Resuscytacyjnych i Automatycznej Defibrylacji Zewnętrznej CELE Po zakończeniu kursu uczestnik powinien umieć zademonstrować: Jak wykonać ocenę nieprzytomnego poszkodowanego Jak
Kurs Podstawowych Zabiegów Resuscytacyjnych i Automatycznej Defibrylacji Zewnętrznej CELE Po zakończeniu kursu uczestnik powinien umieć zademonstrować: Jak wykonać ocenę nieprzytomnego poszkodowanego Jak
Podsumowanie Komitetu Wykonawczego ERC 1
 Podsumowanie Komitetu Wykonawczego ERC Jerry P. Nolan a, *, Jasmeet Soar b, David A. Zideman c, Dominique Biarent d, Leo L. Bossaert e, Charles Deakin f, Rudolph W. Koster g, Jonathan Wyllie h, Bernd Böttiger
Podsumowanie Komitetu Wykonawczego ERC Jerry P. Nolan a, *, Jasmeet Soar b, David A. Zideman c, Dominique Biarent d, Leo L. Bossaert e, Charles Deakin f, Rudolph W. Koster g, Jonathan Wyllie h, Bernd Böttiger
Udzielanie pierwszej pomocy dzieciom w placówkach oświatowych. Beata Łaziuk Zespół Medycznych Szkół Policealnych w Siedlcach
 Udzielanie pierwszej pomocy dzieciom w placówkach oświatowych Beata Łaziuk Zespół Medycznych Szkół Policealnych w Siedlcach Cele wdrażania pierwszej pomocy Moralny obowiązek ochrony życia Obowiązek prawny
Udzielanie pierwszej pomocy dzieciom w placówkach oświatowych Beata Łaziuk Zespół Medycznych Szkół Policealnych w Siedlcach Cele wdrażania pierwszej pomocy Moralny obowiązek ochrony życia Obowiązek prawny
Skutki przepływu prądu przez ciało człowieka
 Do porażenia prądem dochodzi na skutek przepływu prądu elektrycznego przez ciało człowieka. Poszczególne części ciała mają różny opór elektryczny, który stanowi przeszkodę na drodze prądu i ogranicza jego
Do porażenia prądem dochodzi na skutek przepływu prądu elektrycznego przez ciało człowieka. Poszczególne części ciała mają różny opór elektryczny, który stanowi przeszkodę na drodze prądu i ogranicza jego
Najważniejsze zmiany w Wytycznych Resuscytacji 2010 w stosunku do Wytycznych 2005 Europejskiej Rady Resuscytacji
 Strona1 Załącznik do informacji prasowej Polskiej Rady Resuscytacji z dnia 18 października 2010 r. All you need is flow! ( Wszystko czego potrzebujesz to przepływ! ) Kjetil Sunde, Resuscitation 81, 2010
Strona1 Załącznik do informacji prasowej Polskiej Rady Resuscytacji z dnia 18 października 2010 r. All you need is flow! ( Wszystko czego potrzebujesz to przepływ! ) Kjetil Sunde, Resuscitation 81, 2010
Rozdział 1. Nagły zgon sercowy. Krzysztof Kaczmarek. Definicja. Mechanizmy nagłego zgonu sercowego
 Rozdział 1 Nagły zgon sercowy Krzysztof Kaczmarek Definicja Nagły zgon sercowy lub nagła śmierć sercowa (łac. mors subita cardialis, ang. sudden cardiac death, SCD) są definiowane przez Europejskie Towarzystwo
Rozdział 1 Nagły zgon sercowy Krzysztof Kaczmarek Definicja Nagły zgon sercowy lub nagła śmierć sercowa (łac. mors subita cardialis, ang. sudden cardiac death, SCD) są definiowane przez Europejskie Towarzystwo
Resuscytacja dzieci zmiany w Wytycznych 2010
 Resuscytacja dzieci zmiany w Wytycznych 2010 Nowości 2010 Uproszczenie i ujednolicenie zasad resuscytacji dzieci i osób dorosłych Personel medyczny powinien poszukiwad oznak krążenia oraz JEŚLI POSIADA
Resuscytacja dzieci zmiany w Wytycznych 2010 Nowości 2010 Uproszczenie i ujednolicenie zasad resuscytacji dzieci i osób dorosłych Personel medyczny powinien poszukiwad oznak krążenia oraz JEŚLI POSIADA
Uniwersalny schemat ALS 2010
 Zakład Medycyny Ratunkowej 02-005 Warszawa ul. Lindleya 4 Kierownik Zakładu Dr n. med. Zenon Truszewski Sekretariat: +48225021323 Uniwersalny schemat ALS 2010 Zagadnienia Leczenie pacjentów z NZK: migotanie
Zakład Medycyny Ratunkowej 02-005 Warszawa ul. Lindleya 4 Kierownik Zakładu Dr n. med. Zenon Truszewski Sekretariat: +48225021323 Uniwersalny schemat ALS 2010 Zagadnienia Leczenie pacjentów z NZK: migotanie
KURS Resuscytacja KrąŜeniowo- Oddechowa & Automatyczna Zewnętrzna Defibrylacja. European Resuscitation Council
 KURS Resuscytacja KrąŜeniowo- Oddechowa & Automatyczna Zewnętrzna Defibrylacja Adaptacja z j. angielskiego instruktor Ratownictwa Drogowego PZM Jacek Wacławski ZAŁOśENIA Uczestnicy tego kursu winni po
KURS Resuscytacja KrąŜeniowo- Oddechowa & Automatyczna Zewnętrzna Defibrylacja Adaptacja z j. angielskiego instruktor Ratownictwa Drogowego PZM Jacek Wacławski ZAŁOśENIA Uczestnicy tego kursu winni po
Oceń sytuację, zadbaj o bezpieczeństwo. Jest bezpiecznie. Zbadaj przytomność. Nie reaguje (osoba nieprzytomna)
 R E S U S C Y T A C J A K R Ą Ż E N I O W O - O D D E C H O W A ALGORYTM RKO U DOROSŁYCH Wariant A: Na miejscu zdarzenia nie ma osób postronnych Wariant B: Na miejscu zdarzenia znajdują się osoby postronne
R E S U S C Y T A C J A K R Ą Ż E N I O W O - O D D E C H O W A ALGORYTM RKO U DOROSŁYCH Wariant A: Na miejscu zdarzenia nie ma osób postronnych Wariant B: Na miejscu zdarzenia znajdują się osoby postronne
Pierwsza pomoc w edukacji przedszkolnej i wczesnoszkolnej okiem praktyka. mgr Mariusz Andrzejczak Specjalista ratownictwa medycznego
 Pierwsza pomoc w edukacji przedszkolnej i wczesnoszkolnej okiem praktyka mgr Mariusz Andrzejczak Specjalista ratownictwa medycznego Cel spotkania Celem spotkania jest przekazanie Państwu wiedzy i umiejętności
Pierwsza pomoc w edukacji przedszkolnej i wczesnoszkolnej okiem praktyka mgr Mariusz Andrzejczak Specjalista ratownictwa medycznego Cel spotkania Celem spotkania jest przekazanie Państwu wiedzy i umiejętności
POSTĘPOWANIE PRZY ZATRZYMANIU KRĄŻENIA - RESUSCYTACJA KRĄŻENIOWO-ODDECHOWA (RKO)
 POSTĘPOWANIE PRZY ZATRZYMANIU KRĄŻENIA - RESUSCYTACJA KRĄŻENIOWO-ODDECHOWA (RKO) PRZYCZYNY ZATRZYMANIA KRĄŻENIA zawał serca (oraz inne przyczyny kardiogenne) zatrucia utonięcie hipotermia (wychłodzenie)
POSTĘPOWANIE PRZY ZATRZYMANIU KRĄŻENIA - RESUSCYTACJA KRĄŻENIOWO-ODDECHOWA (RKO) PRZYCZYNY ZATRZYMANIA KRĄŻENIA zawał serca (oraz inne przyczyny kardiogenne) zatrucia utonięcie hipotermia (wychłodzenie)
Szkolenie BLS/AED PIERWSZA POMOC
 Szkolenie BLS/AED PIERWSZA POMOC (Basic Live Support/Automated External Defibrillator) Podstawowe Zabiegi Resuscytacyjne Europejskiej i Polskiej Rady Resuscytacji Dla pracowników instytucji Cele: Ratownik
Szkolenie BLS/AED PIERWSZA POMOC (Basic Live Support/Automated External Defibrillator) Podstawowe Zabiegi Resuscytacyjne Europejskiej i Polskiej Rady Resuscytacji Dla pracowników instytucji Cele: Ratownik
Krakowska Akademia im. Andrzeja Frycza Modrzewskiego. Karta przedmiotu. obowiązuje studentów, którzy rozpoczęli studia w roku akademickim 2012/2013
 Krakowska Akademia im. Andrzeja Frycza Modrzewskiego Karta przedmiotu Wydział Zdrowia i Nauk Medycznych obowiązuje studentów, którzy rozpoczęli studia w roku akademickim 01/013 Kierunek studiów: Ratownictwo
Krakowska Akademia im. Andrzeja Frycza Modrzewskiego Karta przedmiotu Wydział Zdrowia i Nauk Medycznych obowiązuje studentów, którzy rozpoczęli studia w roku akademickim 01/013 Kierunek studiów: Ratownictwo
Przypadki kliniczne EKG
 Przypadki kliniczne EKG Przedrukowano z: Mukherjee D. ECG Cases pocket. Börm Bruckmeier Publishing LLC, Hermosa Beach, CA, 2006: 135 138 (przypadek 31) i 147 150 (przypadek 34) PRZYPADEK NR 1 1.1. Scenariusz
Przypadki kliniczne EKG Przedrukowano z: Mukherjee D. ECG Cases pocket. Börm Bruckmeier Publishing LLC, Hermosa Beach, CA, 2006: 135 138 (przypadek 31) i 147 150 (przypadek 34) PRZYPADEK NR 1 1.1. Scenariusz
Resuscytacja krążeniowo-oddechowa
 Resuscytacja krążeniowo-oddechowa NIE BÓJMY SIĘ UDZIELAĆ PIERWSZEJ POMOCY!!! LEPIEJ ROBIĆ COŚ, NIŻ NIE ROBIĆ NIC I BIERNIE SIĘ PRZYGLĄDAĆ!!! Nie traćmy cennego czasu czekając na przyjazd karetki!!! Czasami
Resuscytacja krążeniowo-oddechowa NIE BÓJMY SIĘ UDZIELAĆ PIERWSZEJ POMOCY!!! LEPIEJ ROBIĆ COŚ, NIŻ NIE ROBIĆ NIC I BIERNIE SIĘ PRZYGLĄDAĆ!!! Nie traćmy cennego czasu czekając na przyjazd karetki!!! Czasami
ZATRZYMANIE KRĄŻENIA KRWI. Szkolenia bhp w firmie Zatrzymanie krążenia krwi 1
 ZATRZYMANIE KRĄŻENIA KRWI Szkolenia bhp w firmie Zatrzymanie krążenia krwi 1 Podstawa prawna Kto człowiekowi znajdującemu się w położeniu grożącym bezpośrednim niebezpieczeństwem utraty życia albo ciężkiego
ZATRZYMANIE KRĄŻENIA KRWI Szkolenia bhp w firmie Zatrzymanie krążenia krwi 1 Podstawa prawna Kto człowiekowi znajdującemu się w położeniu grożącym bezpośrednim niebezpieczeństwem utraty życia albo ciężkiego
Z A D Ł A W I E N I E
 www.scanwork.glt.pl Z A D Ł A W I E N I E CIAŁO OBCE W DROGACH ODDECHOWYCH Szkolenia z pierwszej pomocy WYTYCZNE RESUSCYTACJI 2010 POSTĘPOWANIE U OSÓB DOROSŁYCH I DZIECI POWYŻEJ 1 ROKU ŻYCIA I. ŁAGODNA
www.scanwork.glt.pl Z A D Ł A W I E N I E CIAŁO OBCE W DROGACH ODDECHOWYCH Szkolenia z pierwszej pomocy WYTYCZNE RESUSCYTACJI 2010 POSTĘPOWANIE U OSÓB DOROSŁYCH I DZIECI POWYŻEJ 1 ROKU ŻYCIA I. ŁAGODNA
Resuscytacja noworodka. Dorota i Andrzej Fryc
 Resuscytacja noworodka Dorota i Andrzej Fryc Dlaczego szkolić położne? - Statystyki wewnątrzszpitalne, - Alternatywne miejsca porodu, - Kierunek samodzielność 09:55 2 Źródła zasad dotyczących resuscytacji
Resuscytacja noworodka Dorota i Andrzej Fryc Dlaczego szkolić położne? - Statystyki wewnątrzszpitalne, - Alternatywne miejsca porodu, - Kierunek samodzielność 09:55 2 Źródła zasad dotyczących resuscytacji
CENTRUM KSZTAŁCENIA PODYPLOMOWEGO PIELĘGNIAREK I POŁOŻNYCH
 RAMOWY PROGRAM KURSU SPECJALISTYCZNEGO RESUSCYTACJA KRĄŻENIOWO-ODDECHOWA (Nr 01/11) Program przeznaczony dla pielęgniarek i położnych Warszawa, styczeń 2011r. AUTORZY WSPÓŁPRACUJĄCY Z CENTRUM KSZTAŁCENIA
RAMOWY PROGRAM KURSU SPECJALISTYCZNEGO RESUSCYTACJA KRĄŻENIOWO-ODDECHOWA (Nr 01/11) Program przeznaczony dla pielęgniarek i położnych Warszawa, styczeń 2011r. AUTORZY WSPÓŁPRACUJĄCY Z CENTRUM KSZTAŁCENIA
Organizacja i zasady udzielania pomocy przedlekarskiej:
 Organizacja i zasady udzielania pomocy przedlekarskiej: Materiały szkoleniowe Łańcuch pomocy: ocenić i zabezpieczyć miejsce wypadku, zawsze pamiętać o bezpieczeństwie postronnych, swoim, poszkodowanych
Organizacja i zasady udzielania pomocy przedlekarskiej: Materiały szkoleniowe Łańcuch pomocy: ocenić i zabezpieczyć miejsce wypadku, zawsze pamiętać o bezpieczeństwie postronnych, swoim, poszkodowanych
Podstawowe zabiegi resuscytacyjne u dzieci BLS
 Resuscytacja krąŝeniowo- oddechowa u dzieci Podstawowe zabiegi resuscytacyjne u dzieci BLS Za dzieci naleŝy uznać osobę w wieku poniŝej 8 roku Ŝycia (płci męskiej i płci Ŝeńskiej). 1. Upewnij się, Ŝe jest
Resuscytacja krąŝeniowo- oddechowa u dzieci Podstawowe zabiegi resuscytacyjne u dzieci BLS Za dzieci naleŝy uznać osobę w wieku poniŝej 8 roku Ŝycia (płci męskiej i płci Ŝeńskiej). 1. Upewnij się, Ŝe jest
Przypadki kliniczne EKG
 Przypadki kliniczne EKG Przedrukowano z: Mukherjee D. ECG Cases pocket. Börm Bruckmeier Publishing LLC, Hermosa Beach, CA 2006: 139 142 (przypadek 32); 143 146 (przypadek 33). PRZYPADEK NR 1 1.1. Scenariusz
Przypadki kliniczne EKG Przedrukowano z: Mukherjee D. ECG Cases pocket. Börm Bruckmeier Publishing LLC, Hermosa Beach, CA 2006: 139 142 (przypadek 32); 143 146 (przypadek 33). PRZYPADEK NR 1 1.1. Scenariusz
Kurs podstawowy udzielania pierwszej pomocy
 Kurs podstawowy udzielania pierwszej pomocy Pierwsza pomoc - zespół czynności podejmowanych w celu ratowania osoby w stanie nagłego zagrożenia zdrowotnego wykonywanych przez osobę znajdującą się w miejscu
Kurs podstawowy udzielania pierwszej pomocy Pierwsza pomoc - zespół czynności podejmowanych w celu ratowania osoby w stanie nagłego zagrożenia zdrowotnego wykonywanych przez osobę znajdującą się w miejscu
Ferie w ZST Zimowa Szkoła Pierwszej Pomocy 2009/2010
 Zespół Szkół Technicznych w Mielcu mgr Andrzej Wyzga Ferie w ZST Zimowa Szkoła Pierwszej Pomocy 2009/2010 Program szkolenia młodzieży w zakresie PODSTAW PODTRZYMYWANIA ŻYCIA (BLS) ORAZ AUTOMATYCZNEJ DEFIBRYLACJI
Zespół Szkół Technicznych w Mielcu mgr Andrzej Wyzga Ferie w ZST Zimowa Szkoła Pierwszej Pomocy 2009/2010 Program szkolenia młodzieży w zakresie PODSTAW PODTRZYMYWANIA ŻYCIA (BLS) ORAZ AUTOMATYCZNEJ DEFIBRYLACJI
Ratownictwo XXI wieku
 Zakład Medycyny Ratunkowej 02-005 Warszawa ul. Lindleya 4 Kierownik Zakładu Dr n. med. Zenon Truszewski Sekretariat: +48225021323 Ratownictwo XXI wieku Łańcuch przeżycia Złota godzina Czas upływający
Zakład Medycyny Ratunkowej 02-005 Warszawa ul. Lindleya 4 Kierownik Zakładu Dr n. med. Zenon Truszewski Sekretariat: +48225021323 Ratownictwo XXI wieku Łańcuch przeżycia Złota godzina Czas upływający
PIERWSZA POMOC realizacja programu Ratujemy i uczymy ratować
 PIERWSZA POMOC realizacja programu Ratujemy i uczymy ratować W naszej szkole cyklicznie od 4 lat w klasach III realizowany jest program "Ratujemy i uczymy ratować" przy współpracy Fundacji Wielkiej Orkiestry
PIERWSZA POMOC realizacja programu Ratujemy i uczymy ratować W naszej szkole cyklicznie od 4 lat w klasach III realizowany jest program "Ratujemy i uczymy ratować" przy współpracy Fundacji Wielkiej Orkiestry
Poprawa opieki zdrowotnej nad dziećmi w regionie przygranicznym Litwy i Polski (Interreg V-A Litwa-Polska)
 Projekt LT-PL-1R-042 Poprawa opieki zdrowotnej nad dziećmi w regionie przygranicznym Litwy i Polski (Interreg V-A Litwa-Polska) Workshop wymiana doświadczeń Białystok, Polska, 17.04.2018 17-2-15 Resuscytacja
Projekt LT-PL-1R-042 Poprawa opieki zdrowotnej nad dziećmi w regionie przygranicznym Litwy i Polski (Interreg V-A Litwa-Polska) Workshop wymiana doświadczeń Białystok, Polska, 17.04.2018 17-2-15 Resuscytacja
Podstawowe zabiegi reanimacyjne
 Podstawowe zabiegi reanimacyjne Wskazania do resuscytacji Podmiotem obowiązkowych zabiegów resuscytacyjnych jest umierający człowiek potencjalnie zdolny do życia u którego proces rozpoczął się od jednego
Podstawowe zabiegi reanimacyjne Wskazania do resuscytacji Podmiotem obowiązkowych zabiegów resuscytacyjnych jest umierający człowiek potencjalnie zdolny do życia u którego proces rozpoczął się od jednego
STUDENCKA PRAKTYKA ZAWODOWA
 STUDENCKA PRAKTYKA ZAWODOWA RATOWNICTWO MEDYCZNE STUDIA I STOPNIA STUDIA NIESTACJONARNE SZCZEGÓŁOWY OPIS KSZTAŁCENIA PRAKTYCZNEGO ROK III Rodzaj i czas trwania praktyki Miejsce praktyki Cele ogólne kształcenia
STUDENCKA PRAKTYKA ZAWODOWA RATOWNICTWO MEDYCZNE STUDIA I STOPNIA STUDIA NIESTACJONARNE SZCZEGÓŁOWY OPIS KSZTAŁCENIA PRAKTYCZNEGO ROK III Rodzaj i czas trwania praktyki Miejsce praktyki Cele ogólne kształcenia
ZATRZYMANIE AKCJI SERCA
 MEDICAL SCHOOL Projekt sfinansowany przez program Oceny technologii medycznych Narodowego Instytutu Badań nad Zdrowiem (National Institute for Health Research s Health Technology Assessment programme)
MEDICAL SCHOOL Projekt sfinansowany przez program Oceny technologii medycznych Narodowego Instytutu Badań nad Zdrowiem (National Institute for Health Research s Health Technology Assessment programme)
 www.airliquidemedicalsystems.com REAKCJA NA ZATRZYMANIE KRĄŻENIA I ODDECHU: Aby zapewnić krążenie potrzebna jest właściwa wentylacja Gdy klatka piersiowa pacjenta jest uciskana (CC), wentylacja może niekorzystnie
www.airliquidemedicalsystems.com REAKCJA NA ZATRZYMANIE KRĄŻENIA I ODDECHU: Aby zapewnić krążenie potrzebna jest właściwa wentylacja Gdy klatka piersiowa pacjenta jest uciskana (CC), wentylacja może niekorzystnie
OCENA SYTUACJI Jest to pierwszy krok pierwszej pomocy, który ma znaczenie w dalszych czynnościach u poszkodowanego.
 OCENA SYTUACJI Jest to pierwszy krok pierwszej pomocy, który ma znaczenie w dalszych czynnościach u poszkodowanego. W tym momencie musimy zwrócić uwagę na: - sprawdzenie co się stało, okoliczności,zagrożenie
OCENA SYTUACJI Jest to pierwszy krok pierwszej pomocy, który ma znaczenie w dalszych czynnościach u poszkodowanego. W tym momencie musimy zwrócić uwagę na: - sprawdzenie co się stało, okoliczności,zagrożenie
OCENA ZASTOSOWANIA NADGŁOŚNIOWYCH URZĄDZEŃ DO WENTYLACJI W WARUNKACH RATUNKOWEGO ZABEZPIECZENIA DROŻNOŚCI DRÓG ODDECHOWYCH
 lek. med. Andrzej Bielski OCENA ZASTOSOWANIA NADGŁOŚNIOWYCH URZĄDZEŃ DO WENTYLACJI W WARUNKACH RATUNKOWEGO ZABEZPIECZENIA DROŻNOŚCI DRÓG ODDECHOWYCH Rozprawa na stopień doktora nauk medycznych Streszczenie
lek. med. Andrzej Bielski OCENA ZASTOSOWANIA NADGŁOŚNIOWYCH URZĄDZEŃ DO WENTYLACJI W WARUNKACH RATUNKOWEGO ZABEZPIECZENIA DROŻNOŚCI DRÓG ODDECHOWYCH Rozprawa na stopień doktora nauk medycznych Streszczenie
Resuscytacja krążeniowo-oddechowa w praktyce stomatologicznej
 Rozdział 9 Resuscytacja krążeniowo-oddechowa Tłumaczenie: dr med. Wiesław Jarzynowski WPROWADZENIE Szacuje się, że zatrzymanie krążenia i oddychania stanowi 0,3% nagłych zdarzeń medycznych, do jakich dochodzi
Rozdział 9 Resuscytacja krążeniowo-oddechowa Tłumaczenie: dr med. Wiesław Jarzynowski WPROWADZENIE Szacuje się, że zatrzymanie krążenia i oddychania stanowi 0,3% nagłych zdarzeń medycznych, do jakich dochodzi
PODSTAWOWE ZABIEGI RESUSCYTACYJNE U DOROSŁYCH
 "Kto człowiekowi znajdującemu się w położeniu grożącym bezpośrednim niebezpieczeństwem utraty życia albo ciężkiego uszczerbku na zdrowiu nie udziela pomocy, mogąc jej udzielić bez narażania siebie lub
"Kto człowiekowi znajdującemu się w położeniu grożącym bezpośrednim niebezpieczeństwem utraty życia albo ciężkiego uszczerbku na zdrowiu nie udziela pomocy, mogąc jej udzielić bez narażania siebie lub
Podstawowe zabiegi resuscytacyjne u dzieci
 Podstawowe zabiegi resuscytacyjne u dzieci Pacjent pediatryczny o noworodek od urodzenia do 1. mż. o niemowlę od 1. mż. do 1. rż. o dziecko od 1. rż. do okresu pokwitania Nie jest ważne ścisłe określenie
Podstawowe zabiegi resuscytacyjne u dzieci Pacjent pediatryczny o noworodek od urodzenia do 1. mż. o niemowlę od 1. mż. do 1. rż. o dziecko od 1. rż. do okresu pokwitania Nie jest ważne ścisłe określenie
58 540 Karpacz, ul. Na ŚnieŜkę 7 tel. 075 7528299, fax 075 7528293 +48 509 156 642 e mail: tomek.gorecki@wp.pl
 58540 Karpacz, tel. 075 7528299, fax 075 7528293 +48 509 156 642 e mail: RESUSCITATION ALS Advanced Life Support Provide Course 58540 Karpacz ALS provider 800 zł/osoba Jeśli chcesz zorganizować kurs u
58540 Karpacz, tel. 075 7528299, fax 075 7528293 +48 509 156 642 e mail: RESUSCITATION ALS Advanced Life Support Provide Course 58540 Karpacz ALS provider 800 zł/osoba Jeśli chcesz zorganizować kurs u
Pierwsza pomoc PODSTAWOWE ZABIEGI RESUSCYTACYJNE U DOROSŁYCH. Artykuł pobrano ze strony eioba.pl
 Artykuł pobrano ze strony eioba.pl Pierwsza pomoc Zadaniem osoby udzielającej pierwszej pomocy jest utrzymanie przy życiu poszkodowanego i nie dopuszczenie do powstania dalszych powikłań do chwili przybycia
Artykuł pobrano ze strony eioba.pl Pierwsza pomoc Zadaniem osoby udzielającej pierwszej pomocy jest utrzymanie przy życiu poszkodowanego i nie dopuszczenie do powstania dalszych powikłań do chwili przybycia
W y t yczn ych 2010 Resuscytacji KrążeniowoOddechowej oraz Doraźnego. Postępowania w Zaburzeniach Krążenia opublikowanych przez
 N aj ważn i e j s ze e l e m e n t y W y t yczn ych 2010 Resuscytacji KrążeniowoOddechowej oraz Doraźnego Postępowania w Zaburzeniach Krążenia opublikowanych przez American Heart Association Spis treści
N aj ważn i e j s ze e l e m e n t y W y t yczn ych 2010 Resuscytacji KrążeniowoOddechowej oraz Doraźnego Postępowania w Zaburzeniach Krążenia opublikowanych przez American Heart Association Spis treści
Zaawansowane zabiegi resuscytacyjne
 Zaawansowane zabiegi resuscytacyjne u osób dorosłych Charles D. Deakin a,1, Jerry P. Nolan b,*,1, Jasmeet Soar c, Kjetil Sunde d, Rudolph W. Koster e, Gary B. Smith f, Gavin D. Perkins f a Cardiothoracic
Zaawansowane zabiegi resuscytacyjne u osób dorosłych Charles D. Deakin a,1, Jerry P. Nolan b,*,1, Jasmeet Soar c, Kjetil Sunde d, Rudolph W. Koster e, Gary B. Smith f, Gavin D. Perkins f a Cardiothoracic
Zespół Szkół Technicznych w Mielcu
 Zespół Szkół Technicznych w Mielcu mgr Andrzej Wyzga Ferie w ZST Zimowa Szkoła Pierwszej Pomocy 2012/2013 Program szkolenia młodzieży - PODSTAWOWE ZABIEGI RESUSCYTACYJNE (Basic Life Support BLS) I AUTOMATYCZNA
Zespół Szkół Technicznych w Mielcu mgr Andrzej Wyzga Ferie w ZST Zimowa Szkoła Pierwszej Pomocy 2012/2013 Program szkolenia młodzieży - PODSTAWOWE ZABIEGI RESUSCYTACYJNE (Basic Life Support BLS) I AUTOMATYCZNA
CIAŁO OBCE W DROGACH ODDECHOWYCH (ZADŁAWIENIE)
 CIAŁO OBCE W DROGACH ODDECHOWYCH (ZADŁAWIENIE) Niedrożność dróg oddechowych spowodowana ciałem obcym jest rzadką, potencjalnie uleczalną przyczyną przypadkowej śmierci. Ponieważ rozpoznanie niedrożności
CIAŁO OBCE W DROGACH ODDECHOWYCH (ZADŁAWIENIE) Niedrożność dróg oddechowych spowodowana ciałem obcym jest rzadką, potencjalnie uleczalną przyczyną przypadkowej śmierci. Ponieważ rozpoznanie niedrożności
SĄD OKRĘGOWY W RZESZOWIE ZASADY UDZIELANIA PIERWSZEJ POMOCY
 SĄD OKRĘGOWY W RZESZOWIE ZASADY UDZIELANIA PIERWSZEJ POMOCY Kto człowiekowi znajdującemu się w połoŝeniu groŝącym bezpośrednim niebezpieczeństwem utraty Ŝycia albo cięŝkiego uszczerbku na zdrowiu nie udziela
SĄD OKRĘGOWY W RZESZOWIE ZASADY UDZIELANIA PIERWSZEJ POMOCY Kto człowiekowi znajdującemu się w połoŝeniu groŝącym bezpośrednim niebezpieczeństwem utraty Ŝycia albo cięŝkiego uszczerbku na zdrowiu nie udziela
POSTĘPOWANIE PRZY UTRACIE PRZYTOMNOŚCI
 POSTĘPOWANIE PRZY UTRACIE PRZYTOMNOŚCI (ĆWICZENIE) Wariant A: Na miejscu zdarzenia nie ma osób postronnych Wariant B: Na miejscu zdarzenia znajdują się osoby postronne Oceń sytuację i zadbaj o bezpieczeństwo
POSTĘPOWANIE PRZY UTRACIE PRZYTOMNOŚCI (ĆWICZENIE) Wariant A: Na miejscu zdarzenia nie ma osób postronnych Wariant B: Na miejscu zdarzenia znajdują się osoby postronne Oceń sytuację i zadbaj o bezpieczeństwo
Jak ratować i radzić sobie ze strachem przed podejmowaniem czynności ratowniczych. Zasady udzielania pierwszej pomocy
 Jak ratować i radzić sobie ze strachem przed podejmowaniem czynności ratowniczych Zasady udzielania pierwszej pomocy ASPEKTY UDZIELANIA PIERWSZEJ POMOCY TEORIA PRAKTYKA 1 CELE POZNANIE PIORYTETÓW ZROZUMIENIE
Jak ratować i radzić sobie ze strachem przed podejmowaniem czynności ratowniczych Zasady udzielania pierwszej pomocy ASPEKTY UDZIELANIA PIERWSZEJ POMOCY TEORIA PRAKTYKA 1 CELE POZNANIE PIORYTETÓW ZROZUMIENIE
W y t yczn ych 2010 Resuscytacji KrążeniowoOddechowej oraz Doraźnego. Postępowania w Zaburzeniach Krążenia opublikowanych przez
 N aj ważn i e j s ze e l e m e n t y W y t yczn ych 2010 Resuscytacji KrążeniowoOddechowej oraz Doraźnego Postępowania w Zaburzeniach Krążenia opublikowanych przez American Heart Association Spis treści
N aj ważn i e j s ze e l e m e n t y W y t yczn ych 2010 Resuscytacji KrążeniowoOddechowej oraz Doraźnego Postępowania w Zaburzeniach Krążenia opublikowanych przez American Heart Association Spis treści
PROCEDURA ORGANIZACJI PIERWSZEJ POMOCY W PRZEDSZKOLU MIEJSKIM NR 10 W JAŚLE
 PROCEDURA ORGANIZACJI PIERWSZEJ POMOCY W PRZEDSZKOLU MIEJSKIM NR 10 W JAŚLE Podstawa prawna: Ustawa z dnia 8 września 2006 r. o Państwowym Ratownictwie Medycznym (Dz.U. z 2006 r. Nr 191 poz. 1410 ze zm.),
PROCEDURA ORGANIZACJI PIERWSZEJ POMOCY W PRZEDSZKOLU MIEJSKIM NR 10 W JAŚLE Podstawa prawna: Ustawa z dnia 8 września 2006 r. o Państwowym Ratownictwie Medycznym (Dz.U. z 2006 r. Nr 191 poz. 1410 ze zm.),
OBJAWY. kaszel, ktoś nagle, bez jasnej przyczyny przestaje oddychać, sinieje, traci przytomność.
 ZADŁAWIENIE Ciało obce OBJAWY kaszel, ktoś nagle, bez jasnej przyczyny przestaje oddychać, sinieje, traci przytomność. RÓŻNICOWANIE ZADŁAWIENIA (NIEDROŻNOŚCI) Objawy Czy się zadławiłeś? Inne objawy Łagodna
ZADŁAWIENIE Ciało obce OBJAWY kaszel, ktoś nagle, bez jasnej przyczyny przestaje oddychać, sinieje, traci przytomność. RÓŻNICOWANIE ZADŁAWIENIA (NIEDROŻNOŚCI) Objawy Czy się zadławiłeś? Inne objawy Łagodna
Szkolenia w zakresie Resuscytacji Krążeniowo-Oddechowej w Polsce w oparciu o Kursy Certyfikowane przez Europejską Radę Resuscytacji
 Resuscytacja prof. dr hab. med. Janusz Andres *, lek. med. Edyta Drab **i, lek. med. Grzegorz Cebula i, lek. med. Paweł Krawczyk i, lek. med. Elżbieta Byrska-Maciejasz i Katedra i Zakład Anestezjologii
Resuscytacja prof. dr hab. med. Janusz Andres *, lek. med. Edyta Drab **i, lek. med. Grzegorz Cebula i, lek. med. Paweł Krawczyk i, lek. med. Elżbieta Byrska-Maciejasz i Katedra i Zakład Anestezjologii
Podsumowanie Komitetu Wykonawczego ERC 1
 Podsumowanie Komitetu Wykonawczego ERC Koenraad G. Monsieurs a,b, Jerry P. Nolan c, d, Leo L. Bossaert e, Robert Greif f,g, Ian K. Maconochie h, Nikolaos I. Nikolaou i, Gavin D. Perkins j,p, Jasmeet Soar
Podsumowanie Komitetu Wykonawczego ERC Koenraad G. Monsieurs a,b, Jerry P. Nolan c, d, Leo L. Bossaert e, Robert Greif f,g, Ian K. Maconochie h, Nikolaos I. Nikolaou i, Gavin D. Perkins j,p, Jasmeet Soar
Kurs odbywa się w Zakładzie Medycyny Katastrof i Pomocy Doraźnej KAiIT UJ CM ul. Kopernika 19
 Kurs odbywa się w Zakładzie Medycyny Katastrof i Pomocy Doraźnej KAiIT UJ CM ul. Kopernika 19 SZCZEGÓŁOWY PROGRAM KURSU Tytuł kursu: Ratownictwo medyczne dzień I 19.06.2017 Powitanie uczestników i omówienie
Kurs odbywa się w Zakładzie Medycyny Katastrof i Pomocy Doraźnej KAiIT UJ CM ul. Kopernika 19 SZCZEGÓŁOWY PROGRAM KURSU Tytuł kursu: Ratownictwo medyczne dzień I 19.06.2017 Powitanie uczestników i omówienie
Przegląd najważniejszych informacji W 2015 roku dotyczących Aktualizacji Wytycznych American Heart Association z 2018 roku w zakresie resuscytacji
 Przegląd najważniejszych informacji dotyczących Aktualizacji Wytycznych American Heart Association z 2018 roku w zakresie resuscytacji krążeniowo-oddechowej i doraźnego postępowania w zaburzeniach krążenia:
Przegląd najważniejszych informacji dotyczących Aktualizacji Wytycznych American Heart Association z 2018 roku w zakresie resuscytacji krążeniowo-oddechowej i doraźnego postępowania w zaburzeniach krążenia:
Zmiany w wytycznych resuscytacji krążeniowo-oddechowej oddechowej 2005
 Anna Durka Zmiany w wytycznych resuscytacji krążeniowo-oddechowej oddechowej 2005 Europejska Rada Resuscytacji Polska Rada Resuscytacji Studenckie Koło Naukowe Anestezjologii, Intensywnej Terapii i Medycyny
Anna Durka Zmiany w wytycznych resuscytacji krążeniowo-oddechowej oddechowej 2005 Europejska Rada Resuscytacji Polska Rada Resuscytacji Studenckie Koło Naukowe Anestezjologii, Intensywnej Terapii i Medycyny
Kryteria i sposób stwierdzenia nieodwracalnego zatrzymania krążenia poprzedzającego pobranie narządów do przeszczepienia
 Kryteria i sposób stwierdzenia nieodwracalnego zatrzymania krążenia poprzedzającego pobranie narządów do przeszczepienia Janusz Trzebicki Zrealizowano ze środków finansowych Ministerstwa Zdrowia w ramach
Kryteria i sposób stwierdzenia nieodwracalnego zatrzymania krążenia poprzedzającego pobranie narządów do przeszczepienia Janusz Trzebicki Zrealizowano ze środków finansowych Ministerstwa Zdrowia w ramach
ALS- UNIWERSALNY ALGORYTM POSTĘPOWANIA
 ALS- UNIWERSALNY ALGORYTM POSTĘPOWANIA Cele Wczesne rozpoznawanie pacjentów w stanie zagrożenia życia Znajomość algorytmu zaawansowanych czynności resuscytacyjnych Potencjalnie odwracalne przyczyny NZK
ALS- UNIWERSALNY ALGORYTM POSTĘPOWANIA Cele Wczesne rozpoznawanie pacjentów w stanie zagrożenia życia Znajomość algorytmu zaawansowanych czynności resuscytacyjnych Potencjalnie odwracalne przyczyny NZK
(episode 5) 4-letnia dziewczynka z utratą przytomności po zakrztuszeniu
 (episode 5) 4-letnia dziewczynka z utratą przytomności po zakrztuszeniu Author(s): Paweł Krawczyk Institution(s): Zakład Anestezjologii i Intensywnej Terapii, Jagiellonian University Learning objectives
(episode 5) 4-letnia dziewczynka z utratą przytomności po zakrztuszeniu Author(s): Paweł Krawczyk Institution(s): Zakład Anestezjologii i Intensywnej Terapii, Jagiellonian University Learning objectives
Zespół Szkół Technicznych w Mielcu
 Zespół Szkół Technicznych w Mielcu mgr Andrzej Wyzga Ferie w ZST Zimowa Szkoła Pierwszej Pomocy 2015/2016 Program szkolenia młodzieży - POSTĘPOWANIE W PRZYPADKU ZATRZYMANIA KRĄŻENIA U OSÓB DOROSŁYCH (RESUSCYTACJA
Zespół Szkół Technicznych w Mielcu mgr Andrzej Wyzga Ferie w ZST Zimowa Szkoła Pierwszej Pomocy 2015/2016 Program szkolenia młodzieży - POSTĘPOWANIE W PRZYPADKU ZATRZYMANIA KRĄŻENIA U OSÓB DOROSŁYCH (RESUSCYTACJA
Czy dobrze leczymy w Polsce ostre zespoły wieńcowe?
 Czy dobrze leczymy w Polsce ostre zespoły wieńcowe? co można jeszcze poprawić? Grzegorz Opolski I Katedra i Klinika Kardiologii WUM Porównanie liczby ppci/mln mieszkańców w 37 krajach (dane za 2007 i
Czy dobrze leczymy w Polsce ostre zespoły wieńcowe? co można jeszcze poprawić? Grzegorz Opolski I Katedra i Klinika Kardiologii WUM Porównanie liczby ppci/mln mieszkańców w 37 krajach (dane za 2007 i
Ratowanie życia - reanimacja
 Udzielając pierwszej pomocy powinniśmy wykonywać ją do czasu, aż poszkodowany odzyska oddech lub przybędzie wykwalifikowany ratownik. Jeśli stracimy siły, może nas zastąpić druga osoba. REANIMACJA: 1.
Udzielając pierwszej pomocy powinniśmy wykonywać ją do czasu, aż poszkodowany odzyska oddech lub przybędzie wykwalifikowany ratownik. Jeśli stracimy siły, może nas zastąpić druga osoba. REANIMACJA: 1.
Resuscytacja krążeniowo- -oddechowa u dorosłych. Postępowanie w zadławieniu
 Resuscytacja krążeniowo- -oddechowa u dorosłych. Postępowanie w zadławieniu Jerzy Węgielnik, Andrzej Basiński Katedra i Klinika Medycyny Ratunkowej Akademii Medycznej w Gdańsku STRESZCZENIE Podstawowe
Resuscytacja krążeniowo- -oddechowa u dorosłych. Postępowanie w zadławieniu Jerzy Węgielnik, Andrzej Basiński Katedra i Klinika Medycyny Ratunkowej Akademii Medycznej w Gdańsku STRESZCZENIE Podstawowe
Wytyczne Resuscytacji 2015 ERC
 Wytyczne Resuscytacji 2015 ERC Janusz Andres Katedra Anestezjologii i Intensywnej Terapii UJCM w Krakowie Polska Rada Resuscytacji janusz.andres@uj.edu.pl http://www.cprguidelines.eu/ www.prc.krakow.pl
Wytyczne Resuscytacji 2015 ERC Janusz Andres Katedra Anestezjologii i Intensywnej Terapii UJCM w Krakowie Polska Rada Resuscytacji janusz.andres@uj.edu.pl http://www.cprguidelines.eu/ www.prc.krakow.pl
PIERWSZA POMOC Z ELEMENTAMI PIELĘGNIARSTWA
 Projekt OPERACJA SUKCES unikatowy model kształcenia na Wydziale Lekarskim Uniwersytetu Medycznego w Łodzi odpowiedzią na potrzeby gospodarki opartej na wiedzy współfinansowany ze środków Europejskiego
Projekt OPERACJA SUKCES unikatowy model kształcenia na Wydziale Lekarskim Uniwersytetu Medycznego w Łodzi odpowiedzią na potrzeby gospodarki opartej na wiedzy współfinansowany ze środków Europejskiego
Przywrócenie rytmu zatokowego i jego utrzymanie
 Przywrócenie rytmu zatokowego i jego utrzymanie Jak wspomniano we wcześniejszych artykułach cyklu, strategia postępowania w migotaniu przedsionków (AF) polega albo na kontroli częstości rytmu komór i zapobieganiu
Przywrócenie rytmu zatokowego i jego utrzymanie Jak wspomniano we wcześniejszych artykułach cyklu, strategia postępowania w migotaniu przedsionków (AF) polega albo na kontroli częstości rytmu komór i zapobieganiu
MATERIAŁY SZKOLENIOWE DLA MŁODZIEŻY UCZESTNICZĄCEJ W AKCJI FERIE W ZST ZIMOWA SZKOŁA PIERWSZEJ POMOCY 2010/2011
 Zespół Szkół Technicznych w Mielcu mgr Andrzej Wyzga MATERIAŁY SZKOLENIOWE DLA MŁODZIEŻY UCZESTNICZĄCEJ W AKCJI FERIE W ZST ZIMOWA SZKOŁA PIERWSZEJ POMOCY 2010/2011 SZKOLENIE W ZAKRESIE POSTĘPOWANIA W
Zespół Szkół Technicznych w Mielcu mgr Andrzej Wyzga MATERIAŁY SZKOLENIOWE DLA MŁODZIEŻY UCZESTNICZĄCEJ W AKCJI FERIE W ZST ZIMOWA SZKOŁA PIERWSZEJ POMOCY 2010/2011 SZKOLENIE W ZAKRESIE POSTĘPOWANIA W
PIERWSZA POMOC W PRZYPADKU TONIĘCIA
 PIERWSZA POMOC W PRZYPADKU TONIĘCIA Tonięcie jest jedną z częstszych przyczyn śmierci szczególnie w okresie letnim. Światowa Organizacja Zdrowia (WHO) ocenia, że każdego roku z powodu tonięcia traci życie
PIERWSZA POMOC W PRZYPADKU TONIĘCIA Tonięcie jest jedną z częstszych przyczyn śmierci szczególnie w okresie letnim. Światowa Organizacja Zdrowia (WHO) ocenia, że każdego roku z powodu tonięcia traci życie
Sekwencja założeń taktycznych w ratownictwie medycznym Procedura 1. Przybycie na miejsce zdarzenia
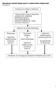 Sekwencja założeń taktycznych w ratownictwie medycznym Procedura 1 Przybycie na miejsce zdarzenia : - zabezpieczenie ratowników - identyfikacja zagrożeń - liczba poszkodowanych - potrzebne dodatkowe siły
Sekwencja założeń taktycznych w ratownictwie medycznym Procedura 1 Przybycie na miejsce zdarzenia : - zabezpieczenie ratowników - identyfikacja zagrożeń - liczba poszkodowanych - potrzebne dodatkowe siły
TARBONUS. 27. Pierwsza pomoc w nagłych wypadkach Organizacja akcji ratunkowej
 27. Pierwsza pomoc w nagłych wypadkach 27.1. Organizacja akcji ratunkowej 27.1.1. Wezwanie pomocy Pamiętajmy, że im wcześniej powiadomimy służby ratunkowe, tym czas oczekiwania na przybycie wykwalifikowanej
27. Pierwsza pomoc w nagłych wypadkach 27.1. Organizacja akcji ratunkowej 27.1.1. Wezwanie pomocy Pamiętajmy, że im wcześniej powiadomimy służby ratunkowe, tym czas oczekiwania na przybycie wykwalifikowanej
NIE BÓJ SIĘ RATOWAĆ śycia INNYM!
 SZKOLENIE Z ZAKRESU PIERWSZEJ POMOCY - ORGANIZACJA SYSTEMU PIERWSZEJ POMOCY w PRZEDSIEBIORSTWIE!,,Los rannego spoczywa w rękach tego, kto załoŝy mu pierwszy opatrunek (płk Nicholas Senn, 1844-1908) mgr
SZKOLENIE Z ZAKRESU PIERWSZEJ POMOCY - ORGANIZACJA SYSTEMU PIERWSZEJ POMOCY w PRZEDSIEBIORSTWIE!,,Los rannego spoczywa w rękach tego, kto załoŝy mu pierwszy opatrunek (płk Nicholas Senn, 1844-1908) mgr
Art. 3 pkt 7 Ustawy o Państwowym Ratownictwie Medycznym z dnia 8 września 2006 r. (Dz.U. z 2016 r. poz. 1868) pierwsza pomoc - zespół czynności
 Art. 3 pkt 7 Ustawy o Państwowym Ratownictwie Medycznym z dnia 8 września 2006 r. (Dz.U. z 2016 r. poz. 1868) pierwsza pomoc - zespół czynności podejmowanych w celu ratowania osoby w stanie nagłego zagrożenia
Art. 3 pkt 7 Ustawy o Państwowym Ratownictwie Medycznym z dnia 8 września 2006 r. (Dz.U. z 2016 r. poz. 1868) pierwsza pomoc - zespół czynności podejmowanych w celu ratowania osoby w stanie nagłego zagrożenia
HIPOTERMIA definicje, rozpoznawanie, postępowanie
 HIPOTERMIA definicje, rozpoznawanie, postępowanie dr med. Maciej Sterliński Szkolenie z zakresu ratownictwa lodowego WOPR Województwa Mazowieckiego Zegrze, 19.02.2006 Główne cele działania zespołów ratowniczych
HIPOTERMIA definicje, rozpoznawanie, postępowanie dr med. Maciej Sterliński Szkolenie z zakresu ratownictwa lodowego WOPR Województwa Mazowieckiego Zegrze, 19.02.2006 Główne cele działania zespołów ratowniczych
Nagłe zatrzymanie krążenia Reanimacja. Dr n.med. Anna Ledakowicz-Polak
 Nagłe zatrzymanie krążenia Reanimacja Dr n.med. Anna Ledakowicz-Polak Cechuje się: Nagłe zatrzymanie krążenia (NZK)- ustanie mechanicznej czynności serca Brakiem reakcji chorego na bodźce Brakiem wyczuwalnego
Nagłe zatrzymanie krążenia Reanimacja Dr n.med. Anna Ledakowicz-Polak Cechuje się: Nagłe zatrzymanie krążenia (NZK)- ustanie mechanicznej czynności serca Brakiem reakcji chorego na bodźce Brakiem wyczuwalnego
Podstawowe zasady udzielania pierwszej pomocy przedmedycznej w Szkole Podstawowej nr 5 im. Adama Mickiewicza w Siemianowicach Śl.
 Podstawowe zasady udzielania pierwszej pomocy przedmedycznej w Szkole Podstawowej nr 5 im. Adama Mickiewicza w Siemianowicach Śl. Bezpieczeństwo podczas udzielania pomocy Po pierwsze - nie szkodzić! Nie
Podstawowe zasady udzielania pierwszej pomocy przedmedycznej w Szkole Podstawowej nr 5 im. Adama Mickiewicza w Siemianowicach Śl. Bezpieczeństwo podczas udzielania pomocy Po pierwsze - nie szkodzić! Nie
Krystian Stachoń Wojciech Rychlik. Oddział Anestezjologii i Intensywnej Terapii z Nadzorem Kardiologicznym SPSZK nr 7 SUM GCM w Katowicach
 Krystian Stachoń Wojciech Rychlik Oddział Anestezjologii i Intensywnej Terapii z Nadzorem Kardiologicznym SPSZK nr 7 SUM GCM w Katowicach Przywrócenie spontanicznego krążenia (ROSC) to tylko pierwszy krok
Krystian Stachoń Wojciech Rychlik Oddział Anestezjologii i Intensywnej Terapii z Nadzorem Kardiologicznym SPSZK nr 7 SUM GCM w Katowicach Przywrócenie spontanicznego krążenia (ROSC) to tylko pierwszy krok
TECHNIKI UDRAŻNIANIA DRÓG ODDECHOWYCH I WENTYLACJI
 TECHNIKI UDRAŻNIANIA DRÓG ODDECHOWYCH I WENTYLACJI Udrażnianie dróg oddechowych i wentylacja Bezprzyrządowe techniki udrażniania dróg oddechowych i wentylacji Przyrządowe techniki udrażniania dróg oddechowych
TECHNIKI UDRAŻNIANIA DRÓG ODDECHOWYCH I WENTYLACJI Udrażnianie dróg oddechowych i wentylacja Bezprzyrządowe techniki udrażniania dróg oddechowych i wentylacji Przyrządowe techniki udrażniania dróg oddechowych
Regulamin zachowania się nad jeziorem, korzystania z łódek oraz udzielanie pierwszej pomocy w przypadku utonięć
 Regulamin zachowania się nad jeziorem, korzystania z łódek oraz udzielanie pierwszej pomocy w przypadku utonięć proszę nie wchodzić do wody poza plażą i wbrew zakazowi opiekuna; nie wolno niszczyć znaków
Regulamin zachowania się nad jeziorem, korzystania z łódek oraz udzielanie pierwszej pomocy w przypadku utonięć proszę nie wchodzić do wody poza plażą i wbrew zakazowi opiekuna; nie wolno niszczyć znaków
Wytyczne resuscytacji 2010 Defibrylacja
 Wytyczne resuscytacji 2010 Defibrylacja Należy minimalizowad przerwy w wysokiej jakości uciśnięciach klatki piersiowej prowadzonych podczas wszystkich interwencji ALS (w tym także defibrylacji). Znacznie
Wytyczne resuscytacji 2010 Defibrylacja Należy minimalizowad przerwy w wysokiej jakości uciśnięciach klatki piersiowej prowadzonych podczas wszystkich interwencji ALS (w tym także defibrylacji). Znacznie
