semestr zimowy 2012/2013
|
|
|
- Edyta Rogowska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Wybrane zagadnienia z fizyki fazy skondensowanej Elektronika molekularna kod przedmiotu: 13.2, EM/II dr Wojciech Kamiński semestr zimowy 2012/2013 Laboratorium dla specjalności fizyka nowych materiałów na kierunku fizyka oraz fizyka materiałów wielofunkcjonalnych i fizyka medyczna na kierunku fizyka techniczna Projekt Rozwój potencjału i oferty edukacyjnej Uniwersytetu Wrocławskiego szansą zwiększenia konkurencyjności Uczelni współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
2 I. PIERWSZE KROKI W SYMULACJI STRUKTUR ATOMOWYCH A. Potrzebne oprogramowanie Oto lista programów, które bedą wykorzystywane na laboratorium z Elektroniki molekularnej : 1. Fireball pakiet programowy do symulacji metodą dynamiki molekularnej. 2. fireball-gui program do wizualizacji i edycji struktur atomowych/molekularnych zapisanych w formacie bas. 3. Gnuplot program do tworzenia wykresów w 2 i 3 wymiarach. 4. Jmol program do wizualizacji i edycji struktur atomowych i molekularnych zapisanych w formacie xyz. 5. NX Client for Windows aplikacja potrzebna do zdalnego uruchamiania programu XCrySDen na stacji roboczej. 6. PuTTY program umożliwiający zdalne połączenie z serwerem przez protokół Telnet lub SSH. 7. WinSCP to graficzny klient SFTP i FTP dla systemu Windows. B. Kilka słów o programie Fireball Pakiet Fireball [1, 2] będzie wykorzystywany do obliczeń struktur atomowych i elektronowych układów atomowych i molekularnych. Program wykonuje obliczenia z pierwszych zasad (ab-initio) wykorzystując teorię funkcjonału gęstości (DFT density-functional theory) w bazie zlokalizowanych orbitali. Elektrony walencyjne opisane są przez zoptymalizowane [3] pseudo-atomowe orbitale (lekko wzbudzone) charakteryzujące się tzw. promieniem obcięcia r c (r c (ψ atomic fireball )(r) r r c = 0). Oddziaływanie elektron-jon jest opisywane przy pomocy zachowujących normę pseudopotencjałów Kleinman a-bylander a. Obliczenia prowadzone są w przybliżeniu lokalnej gęstości (LDA localdensity approximation) dla funcjonału wymienno-korelacyjnego [4]. Program wykorzystuje również standardową metodę superkomórek. Z kolei obliczenia transportu elektronowego są prowadzone w oparciu o metodę SMEAGOL [5] zaimplementowaną w pakiecie Fireball. C. Jak ułatwić sobie pracę z programem? Należy zapamiętać, bądź mieć "pod ręką", najczęściej używane polecenia stosowane do znajdowania szukanych wielkości czy informacji o pracy programu Fireball. Oto lista najbardziej popularnych poleceń: grep ETOT out tail -n 1 grep success out # total energy # gives a list of steps in scf loop 1
3 grep "+++" out grep "+++ Fmax" out grep "+++ Etot" out grep sigma out grep Fermi out tail -n 1 grep "+++ Fmax" out tail -n 1 grep "+++ Etot" out tail -n 1 grep "T_instantaneous" out grep ETOT answer.xyz > ene-temp.dat # history of forces & energy covergence # history of force covergence # history of energy covergence # print values of sigma for all scf steps # Fermi level # last force covergence # last energy covergence # history of inst. temperature in dq method # create a data file containing energy, temp. 2
4 II. PIERWSZE OBLICZENIA MOLEKUŁA BENZENU (C 6 H 6 ) Benzen (C 6 H 6 ) jest węglowodorem aromatycznym, nienasyconym, w którym istnieją sprzężone wiązania wielokrotne, czyli zamknięty układ naprzemiennie położonych wiązań podwójnych i pojedynczych między atomami węgla. 1. Utworzyć odpowiednie zbiory wejściowe: input.bas zawierający położenia atomów, plik input.lvs z wektorami sieci prostej oraz input.kpts zawierający zbiór punktów specjalnych w przestrzeni k. Oto plik input.bas z geometrią molekuły benzenu: 12! total number of atoms ! atom nr coordinate x y z Zbiór input.lvs z wektorami komórki sieci prostej: ! lvs ! lvs ! lvs3 Przykładowy plik input.kpts zawierający zbiór punktów specjalnych w przestrzeni k (tutaj tylko punkt Γ): 1! nr of k-points ! coordinate x y z weight Plik fireball.in sterujący działaniem programu Fireball przykład dla symulacji znajdowania geometrii stanu podstawowego: &OPTION basisfile = input.bas nstepf = 500 iquench = -1 icluster = 1 iqout = 3 dt = 0.5 &END &OUTPUT iwrtxyz = 1 &END 3
5 Rysunek 1: Ewolucja temperatury T (t) (po lewej) i energii całkowitej E tot (t) (po prawej) w funkcji czasu podczas relaksacji geometrii metodą symulowanego wygrzewania. 2. Znaleźć geometrię stanu podstawowego. W tym celu należy przeprowadzić relaksację struktury molekuły dwiema metodami: symulowanego wygrzewania (dynamical quenching) i sprzężonych gradientów (conjugated gradient). Porównać rezultaty otrzymane tymi dwoma algorytmami. Przykładową ewolucję w czasie energii całkowitej E tot (t) i temperatury T (t) przedstawia Rysunek Zwizualizować (np. w programie Jmol) strukturę początkową i końcową oraz jej ewolucję w czasie (dotyczy tylko metody wygrzewania). Rysunek 2: Gęstość stanów: (a) atomu węgla, (b) atomu wodoru i (c) całkowita gęstość stanów molekuły benzenu. 4
6 4. Znaleźć energię całkowitą ETOT dla stanu podstawowego i energię Fermiego E F. 5. Dla geometrii stanu podstawowego i odpowiedającej jej ładunkach policzyć gęstości stanów (DOS density of states). Znaleźć następujące orbitale molekularne (MO molecular orbitals): HOMO-1, HOMO, LUMO, LUMO+1. Określić przerwę energetyczną molekuły. Następnie wykreślić całkowitą gęstość stanów oraz ich projekcję na poszczególne orbitale (PDOS projected density of states) dla wybranego atomu węgla (C) i atomu wodoru (H) patrz Rysunek 2. Dokonać analizy LDOS tj. ocenić z jakich orbitali atomowych (od jakich atomów i z jakiego typu orbitali: s, p x, p y, p z,... ) składają się ww. MO. Rysunek 3: (a) HOMO i (b) LUMO. Przestrzenny rozkład gęstości elektronowej MO molekuły benzenu dla orbitalu: 6. Policzyć wartości własne energii, czyli poziomy energetyczne orbitali molekularnych, a następnie je zwizualizować w programie XCrySDen tj. wykreślić przestrzenne rozkłady gęstości elektronowej (patrz Rysunek 3). Analizę przeprowadzić dla orbitali: HOMO-1, HOMO, LUMO, LUMO+1. Czy któreś z nich są stanami zdegenerowanymi? Uwaga: jeśli którykolwiek z nich jest zdegenerowany konieczne jest wykreślenie przestrzennego rozkładu gęstości elektronowej scałkowanej po zakresie energii w okolicy danego stanu. Ocenić jakiego typu jest to MO: σ, π czy δ. 5
7 III. INNE MOLEKUŁY: ETYLEN (C 2 H 4 ) I PENTAN (C 5 H 12 ) Etylen (C 2 H 4 ) jest najprostszym możliwym alkenem tj. zawiera jedno wiązanie podwójne; w wyniku hybrydyzacji orbitali (sp 2 ) w obu atomach węgla, pomiędzy nimi występuje jedno wiązanie σ i jedno wiązanie π. Z kolei pentan (C 5 H 12 ) jest przedstawicielem węglowodorów nasyconych, zwanych inaczej alkanami (w odróżnieniu od nienasyconych np. alkenów), w których nie występują ani podwójne ani potrójne (tylko pojedyncze) wiązania chemiczne między atomami węgla (orbitale tylko typu σ). Łańcuchy atomów węgla w cząsteczkach alkanów mogą być zarówno proste, jak i rozgałęzione, jednak nie mogą tworzyć zamkniętych pętli, zaś ogólny wzór sumaryczny alkanów ma postać C n H 2n+2. Scharakteryzować w analogiczny sposób jak w poprzednim ćwiczeniu, dwie kolejne molekuły: etylen (C 2 H 4 ) i pentan (C 5 H 12 ), przedstawione schematycznie na Rysunku 4. W tym celu należy przeprowadzić optymalizację geometrii, wyznaczyć strukturę elektronową (DOS, PDOS, określić przerwę energetyczną), dokonać analizy MO (HOMO-1, HOMO, LUMO, LUMO+1) wykreślając ich przestrzenne rozkłady gęstości elektronowej. Rysunek 4: Molekuła etylenu (C 2 H 4 ) po lewej i pentanu (C 5 H 12 ) po prawej. Zadanie to i poprzednie kończy się napisaniem raportu (sprawozdania) w którym nalezy zebrać i przeanalizować wyniki obliczeń przeprowadzonych dla trzech molekuł organicznych: etylenu (C 2 H 4 ), benzenu (C 6 H 6 ) i pentanu (C 5 H 12 ). 6
8 IV. IZOMERIA KONFIGURACYJNA A. Obliczenia konformacji cis i trans dla molekuły azobenzenu 1. Molekuła azobenzenu jest przykładem izomerii konfiguracyjnej tj. posiada dwie formy cis i trans (patrz Rysunek 5). Należy znaleźć geometrię stanu podstawowego tych dwóch izomerów, określić konformację bardziej stabilną oraz wyznaczyć i porównać ich struktury elektronowe. Rysunek 5: Dwie konformacje molekuły azobenzenu: bardziej stabilna forma trans (po lewej) i struktura cis o większej energii po prawej. 2. Przeprowadzić symulację przejścia molekuły azobenzenu ze stanu cis do formy trans (patrz Rysunek 6). W tym celu należy wykorzystać metodę struny elastycznej (NEB nudged elastic band), która jest zaimplementowana w pakiecie Fireball. Określić energię przejścia cis trans. Rysunek 6: Wynik symulacji przejścia z formy cis (po lewej) do koformacji trans (po prawej) uzyskanej metodą NEB. Środkowy panel przedstawia ewolucję energii orbitali HOMO i LUMO dla całej ścieżki reakcji. 7
9 B. Pochodne oligomerów tiofenu 1. W tym zadaniu należy wyznaczyć geometrie pochodnych oligomeów tiofenu z centralną grupą tiadiazolową (dwa atomy N i jeden S) dla dwóch różnych konformacji różniących się pozycją łańcuchów alkilowych (patrz Rysunek 7). Określić konfigurację bardziej stabilną oraz porównać ich struktury elektronowe. Wskazówka: obliczenia można rozpocząć od scharaketryzowania prostszej molekuły tj. bez łańcuchów alkilowych. Rysunek 7: Pochodne oligomeów tiofenu z centralna grupa tiadiazolową (dwa atomy N i jeden S) z dwoma różnymi miejscami łancuchów alkilowych. Źródło: korespondencja prywatna. 2. Kolejnym zadaniem jest określenie stałych sieci dla monowarstw utworzonych z dwóch konformacji tych molekuł (patrz Rysunek 8) i porównanie otrzymanych wyników z danymi doświadczalnymi. Optymalizacja stałych sieci struktur dwuwymiarowych polega na przeprowadzeniu serii obliczeń dla różnych wektorów sieciowych i wybraniu konfiguracji, która odpowiada najmniejszej energii całkowitej. 8
10 Rysunek 8: Dwie różne struktury dwuwymiarowe utworzone z dwóch różnych konformacji molekuł różniących się jedymie pozycją łańcuchów alkilowych. Duża separacja rdzeni czasteczek w przypadku tiadiazolu (ok. 14 Å), odległość ta nie zmiania się niezależnie od pozycji łancuchów alkilowych. Źródło: korespondencja prywatna. 9
11 V. OBLICZENIA DLA OBJĘTOŚCI KRZEM A. Optymalizacja stałej sieci kryształu Si W celu wyznaczenia stałej sieci np. dla struktury objetościowej krzemu musimy znać i utworzyć strukturę komórki elementarnej (patrz Rysunek 9). Krzem krystalizuje w strukturze diamentu tj. strukturze fcc z dwupunktową bazą, co odpowiada następującym położeniom atomów: [0 a, 0 a, 0 a] i [1/4 a, 1/4 a, 1/4 a]. Wtedy nasz zbiór z geometrią input.bas dla a = 1 będzie wyglądać następująco: Rysunek 9: Komórka umowna struktury diamentu. Źródło: [6] co odpowiada wektorom sieci prostej postaci: Punkty specjalne w przestrzeni k (k-points) powinny być wygenerowane przy użyciu osobnego programu, który pozwala na ich redukcję wykorzystując dane o symetrii danej struktury. Oto fragment pliku input.kpts zawierającego 60 puntów specjalnych k:
12 Rachunki przeprowadzamy wykonując serię obliczeń (dla różnych stałych sieci a) bez relaksacji położeń atomów wewnątrz komórki dokonujemy jedynie samouzgodnienia struktury elektronowej. Aby za każdą zmianą stałej sieci a uniknąć generowania trzech nowych plików (input.bas, input.lvs, input.kpts) możemy skorzystać z następującego skryptu, liczącego energię dla serii stałych sieci z zakresu [4, 8; 6, 2] co 0, 2 Å: alat=" " for i in $alat; do echo $i mkdir $i lattice= echo $i " sed "s/aaa/$lattice/g" fireball.sample > fireball.in;./fireball.com > a-$i.out grep "etot/atom" a-$i.out cut -b50-65 mv CHARGES $i/ mv a-$i.out $i/ done Rysunek 10: Standardowe oznaczenia charakterystycznych punktów specjalnych dla pierwszej stefy Brillouina struktury fcc. Źródło: [7]. B. Wyznaczenie modułu ściśliwości objętościowej Si Otrzymane wartości energii całkowitej w funkcji stałej sieci E tot (a) posłużą nam do określenia stałej sieci a odpowiadającej najmniejszej energii oraz modułu ściśliwości objętościowej B 0. W tym celu, korzystamy z osobnego programu, który do naszych punktów dopasowuje krzywą stosując równanie stanu Murnaghana i wylicza równowagową stałą sieci a, moduł ściśliwości objętościowej B 0 oraz jego pochodną B 0. 11
13 C. Obliczenia struktury pasmowej i gestości stanów dla krzemu Dla poprzednio wyznaczonej stałej sieci a obliczyć i wykreślić strukturę pasmową (przykładowa struktura pasmowa dla germanu przedstawiona jest na Rysunku 11). Rysunek 11: Struktura pasmowa germanu. Źródło: [7]. W tym celu należy wyznaczyć punkty specjalne po wybranej drodze wewnątrz pierwszej stefy Brillouina np. LΓX (patrz rysunek 10). Następnie przy "zamrożonych" ładunkach obliczamy dla tak wybranych punktów specjalnych k wartości własne, które są zapisywane do pliku ek.dat. Wynik wykreślamy np. korzystając z poniższego skryptu (dla ośmiu pierwszych, najniższych pasm) dla programu Gnuplot (patrz Rysunek 12): set xrange [0:101] set yrange [-20:10] set xlabel "k-points" set ylabel "Energy [ev]" set unset set size 0.5,1 set multiplot plot ek.dat using 1:2 with lines plot ek.dat using 1:3 with lines plot ek.dat using 1:4 with lines plot ek.dat using 1:5 with lines plot ek.dat using 1:6 with lines plot ek.dat using 1:7 with lines plot ek.dat using 1:8 with lines plot ek.dat using 1:9 with lines Określić rodzaj otrzymanej przerwy energetyczej. Odczytać wartość przerwy energetycznej w punkcie Γ. Wygenerować i dokonać analizy gęstości stanów (m.in. dokonać projekcji gęstości 12
14 Rysunek 12: Struktura pasmowa Si wdłuż ścieżki LΓX (gdzie punkt k = 0 odpowiada punktowi L, k = 51 punktowi Γ zaś k = 101 odpowiada punktowi X). stanów na orbitale s, p x, p y i p z ). 13
15 VI. OBLICZENIA TRANSPORTU ELEKTRONOWEGO W UKŁADACH MOLE- KULARNYCH Istnieje wiele metod do obliczania transportu w nanoukładach bazujących na teorii transportu kwantowego, które można podzielić na dwie główne kategorie: (1) algorytmy stanu stacjonarnego i (2) metody zależne od czasu. Obliczenia transportu elektronowego będą wykonane w oparciu o metodę SMEAGOL (= Spin and Molecular Electronics in Atomically Generated Orbital Landscapes [5]) zaimplementowaną w pakiecie Fireball. Technika ta łączy w sobie metodę niezrównoważonych funkcji Greena z teorią DFT. Jest ona koncepcyjnie prosta, szybka obliczeniowo oraz wszechstonnna w implementacji. Rysunek 13: Typowy układ z dwiema przewodzącymi elektrodami, pomiędzy którymi znajduje się część centralna (extended molecule) w postaci: molekuły, atomowego kontaktu czy bariery potencjału. SMEAGOL pozwala na opis transportu elektronowego w układach z dwiema przewodzącymi elektrodami, pomiędzy którymi znajduje się molekuła, atomowy kontakt czy bariera potencjału. W metodzie tej układ jest modelowany przy pomocy dwóch nieskończonych elektrod i tzw. części centralnej nazywanej extended molecule (EM) co schematycznie przedstawia Rysunek 13. Najlepiej jak EM zawiera kilka warstw elektrod, gdyż zwykle elektrody mają zrekonstruowana powierzchnię. Pełny hamiltonian układu jest przedstawiony na Rysunku 14. Półnieskończone elektrody są opisane przy pomocy macierzy energii własnej, co pozwala uniknąć standardowych problemów, z jakimi się spotykamy w metodach rekurencyjnych. W SMEAGOL zastosowana jest koncepcja tzw. principal layer (PL): czyli najmniejszej komórki, która powtarza się periodycznie wdłuż kierunku transportu, i jest tak skonstruowana że oddziałuje tylko z najbliższymi PL s. A. Schemat obliczeń 1. Podzielić cały układ na trzy części: elektroda/em/elektroda. 2. Wyodrębić z elektrody PL. 3. Znaleźć geometrię stanu postawowego dla PL i EM. Policzyć hamiltonian EM i macierz energii własnej (opisuje elektrody i oddziaływanie z EM). 4. Określić przebieg potencjału w badanym złączu. 14
16 Rysunek 14: Hamiltonian układu w metodzie SMEAGOL. 5. Wykonać rachunki przewodności dla obu polaryzacji. B. Układy dla których należy zbadać transport elektronowy 1. Kryształ krzemu. 2. Molekuła wodoru pomiędzy elektrodami w postaci nanodrutu złożonego z atomów H. Policzyć przewodność tego układu dla różnych położeń molekuły H Molekuła benzenu pomiędzy elektrodami Ag. Należy zbadać właściwości transportu w trzech możliwych konfiguracjach molekuły C 6 H Zaproponować i zbadać układ, który posiada właściwości prostujące (molekularna dioda). 5. Zaproponować i zbadać układ, który będzie posiadać dwa stany, ale tylko jeden z nich będzie przewodzący (molekularny przełącznik). 15
17 VII. PRZYKŁADY PLIKÓW WEJŚCIOWYCH Plik fireball.in dla symulacji relaksacji geometrii tj. do znajdowania stanu podstawowego: &OPTION basisfile = input.bas nstepf = 300 iquench = -1 icluster = 0 iqout = 3 dt = 0.5 sigmatol = 1.0E-8 &END &OUTPUT iwrtxyz = 1 &END Plik fireball.in do generacji gęstości stanów iwrtdos = 1 (wymaga dodatkowego pliku dos.optional) oraz wartości własnych iwrteigen = 1: &OPTION basisfile = input.bas nstepf = 1 iquench = -1 icluster = 0! 0 - for periodic systems 1 - for eg gas phase molecules iqout = 3 dt = 0.5 sigmatol = 1.0E-8! 1.0E-6 1.0E-8 1.0E-12 ifixcharge = 1! 1 - fixed charges &END &OUTPUT iwrtxyz = 1 iwrteigen = 1! writes eigenvalues to a eigen.dat file iwrtefermi = 1! writes occupancies to output file (out) iwrtdos = 1! writes projected DOS on atoms listed in dos.optional &END Dodatkowy plik wejściowy dos.optional wymagany przy obliczeniach gęstości stanów: 1.0! scale factor (leave 1.0) 43 52! list of atoms to analyze DOS 301! number of energy steps ! initial energy, energy step 0! leave untouched ! leave untouched 0.05! imaginary part of Green function (controls energy level smearing) Przykładowy plik fireball.in do generacji przestrzennych gęstości stanów (iwrtewf = 1) oraz wartości własnych (iwrteigen = 1). W tym przykładzie program zapisze przestrzenne gęstości stanów dla czterech wartości własnych (odpowiednio: 118, 119, 120 i 121). Przy całkowaniu gęstości stanów powinniśmy określić parametry ewfewin_min i ewfewin_max przy iewform = 1 i npbands = 0: 16
18 &OPTION basisfile = input.bas nstepf = 1 iquench = -1 icluster = 0! 0 - for periodic systems 1 - for eg gas phase molecules iqout = 3 dt = 0.5 sigmatol = 1.0E-8! 1.0E-6 1.0E-8 1.0E-12 ifixcharge = 1! 1 - fixed charges &END &OUTPUT iwrtxyz = 1 iwrteigen = 1! writes eigenvalues to a eigen.dat file iwrtefermi = 1! writes occupancies to output file (out) iwrtdos = 0! writes projected DOS on atoms listed in dos.optional iwrtewf = 1! writes real space electron density &END &MESH iewform = 1! 1 - eigenvalues 2 - energy range npbands = 4! nr of molecular levels to be plotted 0 if iewform = 2 pbands = ! list of molecular levels to be plotted if iewform = 1 ewfewin_min = -4.80! emin if iewform = 2 ewfewin_max = -4.30! emax if iewform = 2 &END 17
19 [1] J. P. Lewis, K. R. Glaesemann, G. A. Voth, J. Fritsch, A. A. Demkov, J. Ortega, and O. F. Sankey, Phys. Rev. B 64, (2001). [2] P. Jelínek, H. Wang, J. P. Lewis, O. F. Sankey, and J. Ortega, Phys. Rev. B 71, (2005). [3] M. A. Basanta, Y. J. Dappe, P. Jelínek, and J. Ortega, Comput. Mat. Sci. 39, 759 (2007). [4] W. Kohn and L. J. Sham, Phys. Rev. 140, A1133 (1965). [5] G. Rocha and J. Joubert, Phys. Rev. B 73, (2006). [6] N. W. Ashcroft and N. D. Mermin, Solid state physics (Harcourt, 1976). [7] C. Kittel, Introduction to Solid State Physics (John Wiley & Sons, 1996), 7th ed. 18
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450
 Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Wykład V Wiązanie kowalencyjne. Półprzewodniki
 Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
Pasmowa teoria przewodnictwa. Anna Pietnoczka
 Pasmowa teoria przewodnictwa elektrycznego Anna Pietnoczka Wpływ rodzaju wiązań na przewodność próbki: Wiązanie jonowe - izolatory Wiązanie metaliczne - przewodniki Wiązanie kowalencyjne - półprzewodniki
Pasmowa teoria przewodnictwa elektrycznego Anna Pietnoczka Wpływ rodzaju wiązań na przewodność próbki: Wiązanie jonowe - izolatory Wiązanie metaliczne - przewodniki Wiązanie kowalencyjne - półprzewodniki
Ćwiczenie 3. Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe *
 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * 1 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * I. Narysuj etylen a) Wybierz Default
Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * 1 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * I. Narysuj etylen a) Wybierz Default
Przyrządy i układy półprzewodnikowe
 Przyrządy i układy półprzewodnikowe Prof. dr hab. Ewa Popko ewa.popko@pwr.edu.pl www.if.pwr.wroc.pl/~popko p.231a A-1 Zawartość wykładu Wy1, Wy2 Wy3 Wy4 Wy5 Wy6 Wy7 Wy8 Wy9 Wy10 Wy11 Wy12 Wy13 Wy14 Wy15
Przyrządy i układy półprzewodnikowe Prof. dr hab. Ewa Popko ewa.popko@pwr.edu.pl www.if.pwr.wroc.pl/~popko p.231a A-1 Zawartość wykładu Wy1, Wy2 Wy3 Wy4 Wy5 Wy6 Wy7 Wy8 Wy9 Wy10 Wy11 Wy12 Wy13 Wy14 Wy15
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych
 1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
Ćwiczenie 4: Ciepło właściwe monokryształu fcc argonu
 Ćwiczenie 4: Ciepło właściwe monokryształu fcc argonu Tym razem zajmiemy się już problemem bardziej złożonym. Celem ćwiczenia jest wyznaczenie dla monokryształu fcc argonu ciepła właściwego c, tj. ciepła
Ćwiczenie 4: Ciepło właściwe monokryształu fcc argonu Tym razem zajmiemy się już problemem bardziej złożonym. Celem ćwiczenia jest wyznaczenie dla monokryształu fcc argonu ciepła właściwego c, tj. ciepła
Elektryczne własności ciał stałych
 Elektryczne własności ciał stałych Do sklasyfikowania różnych materiałów ze względu na ich własności elektryczne trzeba zdefiniować kilka wielkości Oporność właściwa (albo przewodność) ładunek [C] = 1/
Elektryczne własności ciał stałych Do sklasyfikowania różnych materiałów ze względu na ich własności elektryczne trzeba zdefiniować kilka wielkości Oporność właściwa (albo przewodność) ładunek [C] = 1/
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oarciu o koncecję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncecja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oarciu o koncecję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncecja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
Ćwiczenie 4: Modelowanie reakcji chemicznych. Stan przejściowy.
 Ćwiczenie 4: Modelowanie reakcji chemicznych. Stan przejściowy. Celem ćwiczenia jest wymodelowanie przebiegu reakcji chemicznej podstawienia nukleofilowego zachodzącego zgodnie z mechanizmem SN2. Wprowadzenie:
Ćwiczenie 4: Modelowanie reakcji chemicznych. Stan przejściowy. Celem ćwiczenia jest wymodelowanie przebiegu reakcji chemicznej podstawienia nukleofilowego zachodzącego zgodnie z mechanizmem SN2. Wprowadzenie:
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Absorpcja związana z defektami kryształu
 W rzeczywistych materiałach sieć krystaliczna nie jest idealna występują różnego rodzaju defekty. Podział najważniejszych defektów ze względu na właściwości optyczne: - inny atom w węźle sieci: C A atom
W rzeczywistych materiałach sieć krystaliczna nie jest idealna występują różnego rodzaju defekty. Podział najważniejszych defektów ze względu na właściwości optyczne: - inny atom w węźle sieci: C A atom
Wytwarzanie niskowymiarowych struktur półprzewodnikowych
 Większość struktur niskowymiarowych wytwarzanych jest za pomocą technik epitaksjalnych. Najczęściej wykorzystywane metody wzrostu: - epitaksja z wiązki molekularnej (MBE Molecular Beam Epitaxy) - epitaksja
Większość struktur niskowymiarowych wytwarzanych jest za pomocą technik epitaksjalnych. Najczęściej wykorzystywane metody wzrostu: - epitaksja z wiązki molekularnej (MBE Molecular Beam Epitaxy) - epitaksja
Teoria pasmowa ciał stałych
 Teoria pasmowa ciał stałych Poziomy elektronowe atomów w cząsteczkach ulegają rozszczepieniu. W kryształach zjawisko to prowadzi do wytworzenia się pasm. Klasyfikacja ciał stałych na podstawie struktury
Teoria pasmowa ciał stałych Poziomy elektronowe atomów w cząsteczkach ulegają rozszczepieniu. W kryształach zjawisko to prowadzi do wytworzenia się pasm. Klasyfikacja ciał stałych na podstawie struktury
Przewodność elektryczna ciał stałych. Elektryczne własności ciał stałych Izolatory, metale i półprzewodniki
 Przewodność elektryczna ciał stałych Elektryczne własności ciał stałych Izolatory, metale i półprzewodniki Elektryczne własności ciał stałych Do sklasyfikowania różnych materiałów ze względu na ich własności
Przewodność elektryczna ciał stałych Elektryczne własności ciał stałych Izolatory, metale i półprzewodniki Elektryczne własności ciał stałych Do sklasyfikowania różnych materiałów ze względu na ich własności
Elementy teorii powierzchni metali
 Prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład dla studentów fizyki Rok akademicki 2017/18 (30 godz.) Wykład 1 Plan wykładu Struktura periodyczna kryształów, sieć odwrotna Struktura
Prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład dla studentów fizyki Rok akademicki 2017/18 (30 godz.) Wykład 1 Plan wykładu Struktura periodyczna kryształów, sieć odwrotna Struktura
Wykład 5 XII 2018 Żywienie
 Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
półprzewodniki Plan na dzisiaj Optyka nanostruktur Struktura krystaliczna Dygresja Sebastian Maćkowski
 Plan na dzisiaj Optyka nanostruktur Sebastian Maćkowski Instytut Fizyki Uniwersytet Mikołaja Kopernika Adres poczty elektronicznej: mackowski@fizyka.umk.pl Biuro: 365, telefon: 611-3250 półprzewodniki
Plan na dzisiaj Optyka nanostruktur Sebastian Maćkowski Instytut Fizyki Uniwersytet Mikołaja Kopernika Adres poczty elektronicznej: mackowski@fizyka.umk.pl Biuro: 365, telefon: 611-3250 półprzewodniki
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE 1 Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE 1 Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
Rzędy wiązań chemicznych
 Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Modele kp Studnia kwantowa
 Modele kp Studnia kwantowa Przegląd modeli pozwalających obliczyć strukturę pasmową materiałów półprzewodnikowych. Metoda Fal płaskich Transformata Fouriera Przykładowe wyniki Model Kaine Hamiltonian z
Modele kp Studnia kwantowa Przegląd modeli pozwalających obliczyć strukturę pasmową materiałów półprzewodnikowych. Metoda Fal płaskich Transformata Fouriera Przykładowe wyniki Model Kaine Hamiltonian z
TEORIA PASMOWA CIAŁ STAŁYCH
 TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
Elementy teorii powierzchni metali
 prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Katarzyna Jesionek Zastosowanie symulacji dynamiki cieczy oraz ośrodków sprężystych w symulatorach operacji chirurgicznych.
 Katarzyna Jesionek Zastosowanie symulacji dynamiki cieczy oraz ośrodków sprężystych w symulatorach operacji chirurgicznych. Jedną z metod symulacji dynamiki cieczy jest zastosowanie metody siatkowej Boltzmanna.
Katarzyna Jesionek Zastosowanie symulacji dynamiki cieczy oraz ośrodków sprężystych w symulatorach operacji chirurgicznych. Jedną z metod symulacji dynamiki cieczy jest zastosowanie metody siatkowej Boltzmanna.
Repeta z wykładu nr 3. Detekcja światła. Struktura krystaliczna. Plan na dzisiaj
 Repeta z wykładu nr 3 Detekcja światła Sebastian Maćkowski Instytut Fizyki Uniwersytet Mikołaja Kopernika Adres poczty elektronicznej: mackowski@fizyka.umk.pl Biuro: 365, telefon: 611-3250 Konsultacje:
Repeta z wykładu nr 3 Detekcja światła Sebastian Maćkowski Instytut Fizyki Uniwersytet Mikołaja Kopernika Adres poczty elektronicznej: mackowski@fizyka.umk.pl Biuro: 365, telefon: 611-3250 Konsultacje:
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
MATERIA. = m i liczby całkowite. ciała stałe. - kryształy - ciała bezpostaciowe (amorficzne) - ciecze KRYSZTAŁY. Periodyczność
 MATERIA ciała stałe - kryształy - ciała bezpostaciowe (amorficzne) - ciecze - gazy KRYSZTAŁY Periodyczność Kryształ (idealny) struktura zbudowana z powtarzających się w przestrzeni periodycznie identycznych
MATERIA ciała stałe - kryształy - ciała bezpostaciowe (amorficzne) - ciecze - gazy KRYSZTAŁY Periodyczność Kryształ (idealny) struktura zbudowana z powtarzających się w przestrzeni periodycznie identycznych
Modelowanie molekularne
 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 10 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 10 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
S88 Badanie rzutu kostką sześcienną
 S88 Badanie rzutu kostką sześcienną Andrzej Kapanowski 29 lutego 2012 Streszczenie Celem ćwiczenia jest zbadanie rzutu kostką sześcienną. Dokument ma być pomocą przy przygotowywaniu opracowania z ćwiczenia
S88 Badanie rzutu kostką sześcienną Andrzej Kapanowski 29 lutego 2012 Streszczenie Celem ćwiczenia jest zbadanie rzutu kostką sześcienną. Dokument ma być pomocą przy przygotowywaniu opracowania z ćwiczenia
Modele kp wprowadzenie
 Modele kp wprowadzenie Komórka elementarna i komórka sieci odwrotnej Funkcje falowe elektronu w krysztale Struktura pasmowa Przybliżenie masy efektywnej Naprężenia: potencjał deformacyjny, prawo Hooka
Modele kp wprowadzenie Komórka elementarna i komórka sieci odwrotnej Funkcje falowe elektronu w krysztale Struktura pasmowa Przybliżenie masy efektywnej Naprężenia: potencjał deformacyjny, prawo Hooka
Funkcja rozkładu Fermiego-Diraca w różnych temperaturach
 Funkcja rozkładu Fermiego-Diraca w różnych temperaturach 1 f FD ( E) = E E F exp + 1 kbt Styczna do krzywej w punkcie f FD (E F )=0,5 przecina oś energii i prostą f FD (E)=1 w punktach odległych o k B
Funkcja rozkładu Fermiego-Diraca w różnych temperaturach 1 f FD ( E) = E E F exp + 1 kbt Styczna do krzywej w punkcie f FD (E F )=0,5 przecina oś energii i prostą f FD (E)=1 w punktach odległych o k B
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Rozszczepienie poziomów atomowych
 Rozszczepienie poziomów atomowych Poziomy energetyczne w pojedynczym atomie Gdy zbliżamy atomy chmury elektronowe nachodzą na siebie (inaczej: funkcje falowe elektronów zaczynają się przekrywać) Na skutek
Rozszczepienie poziomów atomowych Poziomy energetyczne w pojedynczym atomie Gdy zbliżamy atomy chmury elektronowe nachodzą na siebie (inaczej: funkcje falowe elektronów zaczynają się przekrywać) Na skutek
Wojewódzki Konkurs Przedmiotowy z chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2010/2011
 Wojewódzki Konkurs Przedmiotowy z chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2010/2011 KOD UCZNIA Etap: Data: Czas pracy: rejonowy 7 lutego 2011r 90 minut Informacje dla ucznia
Wojewódzki Konkurs Przedmiotowy z chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2010/2011 KOD UCZNIA Etap: Data: Czas pracy: rejonowy 7 lutego 2011r 90 minut Informacje dla ucznia
ADF Specyfika metodologii i pliku z danymi
 ADF Specyfika metodologii i pliku z danymi Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii Uniwersytet Jagielloski WCSS Wrocław, Obliczenia w bazie orbitali KS fragmentów Typowe obliczenia:
ADF Specyfika metodologii i pliku z danymi Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii Uniwersytet Jagielloski WCSS Wrocław, Obliczenia w bazie orbitali KS fragmentów Typowe obliczenia:
WYMAGANIA WSTĘPNE W ZAKRESIE WIEDZY, UMIEJĘTNOŚCI I INNYCH KOMPETENCJI 1. Brak
 WYDZIAŁ Podstawowych Problemów Techniki KARTA PRZEDMIOTU Nazwa w języku polskim Podstawy chemii ogólnej Nazwa w języku angielskim General chemistry Język wykładowy polski Kierunek studiów Optyka Specjalność
WYDZIAŁ Podstawowych Problemów Techniki KARTA PRZEDMIOTU Nazwa w języku polskim Podstawy chemii ogólnej Nazwa w języku angielskim General chemistry Język wykładowy polski Kierunek studiów Optyka Specjalność
Modele: kulkowy i czaszowy: wzór półstrukturalny: H 2 C=CH 2. Obecność wiązania podwójnego sygnalizuje końcówka nazwy "-en" Wzór strukturalny:
 Opracowanie: Marek Walnik, 0 Nazewnictwo alkenów Alkeny, zwane też olefinami, to węglowodory, w których cząsteczkach występują wiązania podwójne =. Węglowodory takie, ook alkinów, z potrójnymi wiązaniami,
Opracowanie: Marek Walnik, 0 Nazewnictwo alkenów Alkeny, zwane też olefinami, to węglowodory, w których cząsteczkach występują wiązania podwójne =. Węglowodory takie, ook alkinów, z potrójnymi wiązaniami,
Podstawy chemii. dr hab. Wacław Makowski. Wykład 1: Wprowadzenie
 Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Twórcza szkoła dla twórczego ucznia Projekt współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 SCENARIUSZ LEKCJI PRZEDMIOT: CHEMIA TEMAT: POWTÓRZENIE WIADOMOŚCI O WĘGLU I WĘGLOWODORACH AUTOR SCENARIUSZA: mgr Ewa Gryczman OPRACOWANIE ELEKTRONICZNO GRAFICZNE : mgr Beata Rusin TEMAT LEKCJI Powtórzenie
SCENARIUSZ LEKCJI PRZEDMIOT: CHEMIA TEMAT: POWTÓRZENIE WIADOMOŚCI O WĘGLU I WĘGLOWODORACH AUTOR SCENARIUSZA: mgr Ewa Gryczman OPRACOWANIE ELEKTRONICZNO GRAFICZNE : mgr Beata Rusin TEMAT LEKCJI Powtórzenie
Liczby kwantowe n, l, m l = 0 l =1 l = 2 l = 3
 Liczby kwantowe Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m. Liczby kwantowe nie mogą być dowolne, muszą
Liczby kwantowe Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m. Liczby kwantowe nie mogą być dowolne, muszą
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
Część A wprowadzenie do programu
 Część A wprowadzenie do programu Nieorganiczna baza danych (Inorganic Crystal Structure Database) zawiera wszystkie struktury związków nieorganicznych, ze współrzędnymi atomów, publikowane od roku 1913.
Część A wprowadzenie do programu Nieorganiczna baza danych (Inorganic Crystal Structure Database) zawiera wszystkie struktury związków nieorganicznych, ze współrzędnymi atomów, publikowane od roku 1913.
na dnie (lub w szczycie) pasma pasmo jest paraboliczne, ale masa wyznaczona z krzywizny niekoniecznie = m 0
 Koncepcja masy efektywnej swobodne elektrony k 1 1 E( k) E( k) =, = m m k krzywizna E(k) określa masę cząstek elektrony prawie swobodne - na dnie pasma masa jest dodatnia, ale niekoniecznie = masie swobodnego
Koncepcja masy efektywnej swobodne elektrony k 1 1 E( k) E( k) =, = m m k krzywizna E(k) określa masę cząstek elektrony prawie swobodne - na dnie pasma masa jest dodatnia, ale niekoniecznie = masie swobodnego
Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych
 Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych Justyna Cembrzyńska Zakład Mechaniki Kwantowej Uniwersytet
Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych Justyna Cembrzyńska Zakład Mechaniki Kwantowej Uniwersytet
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
S. Baran - Podstawy fizyki materii skondensowanej Fonony. Fonony
 Fonony Drgania płaszczyzn sieciowych podłużne poprzeczne źródło: Ch. Kittel Wstęp do fizyki..., rozdz. 4, rys. 2, 3, str. 118 Drgania płaszczyzn sieciowych Do opisu drgań sieci krystalicznej wystarczą
Fonony Drgania płaszczyzn sieciowych podłużne poprzeczne źródło: Ch. Kittel Wstęp do fizyki..., rozdz. 4, rys. 2, 3, str. 118 Drgania płaszczyzn sieciowych Do opisu drgań sieci krystalicznej wystarczą
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały
 WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Ćwiczenie 5. Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W
 Ćwiczenie 5 Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W Co powinieneś umieć przed zajęciami Jak obliczyć energię oscylatora harmonicznego, klasycznego i kwantowego?
Ćwiczenie 5 Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W Co powinieneś umieć przed zajęciami Jak obliczyć energię oscylatora harmonicznego, klasycznego i kwantowego?
Spis treści. Metoda VSEPR. Reguły określania struktury cząsteczek. Ustalanie struktury przestrzennej
 Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Kacper Kulczycki. Dynamika molekularna atomów oddziałujących siłami van der Waalsa
 Kacper Kulczycki Dynamika molekularna atomów oddziałujących siłami van der Waalsa Warszawa 2007 Spis treści: Spis treści 1 Wstęp 2 Teoria 2 Algorytm 3 Symulacje 4 Wyniki 24 Wnioski 47 1 Wstęp Ćwiczenie
Kacper Kulczycki Dynamika molekularna atomów oddziałujących siłami van der Waalsa Warszawa 2007 Spis treści: Spis treści 1 Wstęp 2 Teoria 2 Algorytm 3 Symulacje 4 Wyniki 24 Wnioski 47 1 Wstęp Ćwiczenie
 2013 02 27 2 1. Jakie warstwy zostały wyhodowane w celu uzyskania 2DEG? (szkic?) 2. Gdzie było domieszkowanie? Dlaczego jako domieszek użyto w próbce atomy krzemu? 3. Jaki kształt miała próbka? 4. W jaki
2013 02 27 2 1. Jakie warstwy zostały wyhodowane w celu uzyskania 2DEG? (szkic?) 2. Gdzie było domieszkowanie? Dlaczego jako domieszek użyto w próbce atomy krzemu? 3. Jaki kształt miała próbka? 4. W jaki
Wykład VI. Teoria pasmowa ciał stałych
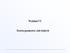 Wykład VI Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Wykład VI Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Fizyka Ciała Stałego
 Wykład III Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć krystaliczną. Amorficzne, brak uporządkowania,
Wykład III Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć krystaliczną. Amorficzne, brak uporządkowania,
Łukasz Januszkiewicz Technika antenowa
 Instrukcja współfinansowana przez Unię Europejską w ramach Europejskiego Funduszu Społecznego w projekcie Innowacyjna dydaktyka bez ograniczeń zintegrowany rozwój Politechniki Łódzkiej zarządzanie Uczelnią,
Instrukcja współfinansowana przez Unię Europejską w ramach Europejskiego Funduszu Społecznego w projekcie Innowacyjna dydaktyka bez ograniczeń zintegrowany rozwój Politechniki Łódzkiej zarządzanie Uczelnią,
S. Baran - Podstawy fizyki materii skondensowanej Pasma energetyczne. Pasma energetyczne
 Pasma energetyczne Niedostatki modelu gazu Fermiego elektronów swobodnych Pomimo wielu sukcesów model nie jest w stanie wyjaśnić następujących zagadnień: 1. różnica między metalami, półmetalami, półprzewodnikami
Pasma energetyczne Niedostatki modelu gazu Fermiego elektronów swobodnych Pomimo wielu sukcesów model nie jest w stanie wyjaśnić następujących zagadnień: 1. różnica między metalami, półmetalami, półprzewodnikami
Identyfikacja płomieniowa tworzyw sztucznych Iloczyny rozpuszczalności trudno rozpuszczalnych związków w wodzie w temperaturze pokojowej
 Jeśli ktoś jest w posiadaniu tablic chemicznych, to bardzo prosilibyśmy, aby nam je nadesłał (na adres któregoś z administratorów, najlepiej w formie pliku *.doc; *.pdf; *.jpg) - na pewno je zamieścimy.
Jeśli ktoś jest w posiadaniu tablic chemicznych, to bardzo prosilibyśmy, aby nam je nadesłał (na adres któregoś z administratorów, najlepiej w formie pliku *.doc; *.pdf; *.jpg) - na pewno je zamieścimy.
Sieci Komputerowe 2 / Ćwiczenia 1
 Tematyka Sieci Komputerowe 2 / Ćwiczenia 1 Opracował: Konrad Kawecki Na ćwiczeniach przeanalizujemy opóźnienia transmisji w sieciach komputerowych. Na podstawie otrzymanych wyników
Tematyka Sieci Komputerowe 2 / Ćwiczenia 1 Opracował: Konrad Kawecki Na ćwiczeniach przeanalizujemy opóźnienia transmisji w sieciach komputerowych. Na podstawie otrzymanych wyników
RJC. Wiązania Chemiczne & Slides 1 to 39
 Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
b) Pierwiastek E tworzy tlenek o wzorze EO 2 i wodorek typu EH 4, a elektrony w jego atomie rozmieszczone są na dwóch powłokach elektronowych
 1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
np. dla elektronów w kryształach; V(x+d) = V(x), d - okres periodyczności = wielkość komórki elementarnej kryształu
 Potencjały eriodyczne n. dla elektronów w kryształach; V(x+d) V(x), d - okres eriodyczności wielkość komórki elementarnej kryształu rzyadek kryształu jednowymiarowego sieci z bazą gdy w komórce elementarnej
Potencjały eriodyczne n. dla elektronów w kryształach; V(x+d) V(x), d - okres eriodyczności wielkość komórki elementarnej kryształu rzyadek kryształu jednowymiarowego sieci z bazą gdy w komórce elementarnej
Dr inż. Zbigniew Szklarski
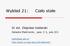 Wykład 1: Ciało stałe Dr inż. Zbigniew Szklarski Katedra Elektroniki, paw. C-1, pok.31 szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Struktura kryształu Ciała stałe o budowie bezpostaciowej
Wykład 1: Ciało stałe Dr inż. Zbigniew Szklarski Katedra Elektroniki, paw. C-1, pok.31 szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Struktura kryształu Ciała stałe o budowie bezpostaciowej
STRUKTURA PASM ENERGETYCZNYCH
 PODSTAWY TEORII PASMOWEJ Struktura pasm energetycznych Teoria wa Struktura wa stałych Półprzewodniki i ich rodzaje Półprzewodniki domieszkowane Rozkład Fermiego - Diraca Złącze p-n (dioda) Politechnika
PODSTAWY TEORII PASMOWEJ Struktura pasm energetycznych Teoria wa Struktura wa stałych Półprzewodniki i ich rodzaje Półprzewodniki domieszkowane Rozkład Fermiego - Diraca Złącze p-n (dioda) Politechnika
Chemia nieorganiczna. Copyright 2000 by Harcourt, Inc. All rights reserved.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych.
 Tematy opisowe 1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych. 2. Dlaczego do kadłubów statków, doków, falochronów i filarów mostów przymocowuje się płyty z
Tematy opisowe 1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych. 2. Dlaczego do kadłubów statków, doków, falochronów i filarów mostów przymocowuje się płyty z
Metody symulacji w nanotechnologii
 Metody symulacji w nanotechnologii Jan Iwaniszewski A. Formalizm operatorowy Załóżmy, że nasz układ kwantowy posiada dyskretny zbiór funkcji własnych ϕ k, k =,,.... Tworzą one bazę w całej przestrzeni
Metody symulacji w nanotechnologii Jan Iwaniszewski A. Formalizm operatorowy Załóżmy, że nasz układ kwantowy posiada dyskretny zbiór funkcji własnych ϕ k, k =,,.... Tworzą one bazę w całej przestrzeni
Analiza obciążeń baneru reklamowego za pomocą oprogramowania ADINA-AUI 8.9 (900 węzłów)
 Politechnika Łódzka Wydział Technologii Materiałowych i Wzornictwa Tekstyliów Katedra Materiałoznawstwa Towaroznawstwa i Metrologii Włókienniczej Analiza obciążeń baneru reklamowego za pomocą oprogramowania
Politechnika Łódzka Wydział Technologii Materiałowych i Wzornictwa Tekstyliów Katedra Materiałoznawstwa Towaroznawstwa i Metrologii Włókienniczej Analiza obciążeń baneru reklamowego za pomocą oprogramowania
Instytut Fizyki Doświadczalnej Wydział Matematyki, Fizyki i Informatyki UNIWERSYTET GDAŃSKI
 Instytut Fizyki Doświadczalnej Wydział Matematyki, Fizyki i Informatyki UNIWERSYTET GDAŃSKI I. Zagadnienia do opracowania. 1. Podstawy teorii pasmowej. 2. Klasyfikacja ciał stałych w oparciu o teorię pasmową.
Instytut Fizyki Doświadczalnej Wydział Matematyki, Fizyki i Informatyki UNIWERSYTET GDAŃSKI I. Zagadnienia do opracowania. 1. Podstawy teorii pasmowej. 2. Klasyfikacja ciał stałych w oparciu o teorię pasmową.
Przejścia promieniste
 Przejście promieniste proces rekombinacji elektronu i dziury (przejście ze stanu o większej energii do stanu o energii mniejszej), w wyniku którego następuje emisja promieniowania. E Długość wyemitowanej
Przejście promieniste proces rekombinacji elektronu i dziury (przejście ze stanu o większej energii do stanu o energii mniejszej), w wyniku którego następuje emisja promieniowania. E Długość wyemitowanej
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
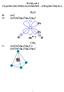 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
Dotyczy to zarówno istniejących już związków, jak i związków, których jeszcze dotąd nie otrzymano.
 Chemia teoretyczna to dział chemii zaliczany do chemii fizycznej, zajmujący się zagadnieniami związanymi z wiedzą chemiczną od strony teoretycznej, tj. bez wykonywania eksperymentów na stole laboratoryjnym.
Chemia teoretyczna to dział chemii zaliczany do chemii fizycznej, zajmujący się zagadnieniami związanymi z wiedzą chemiczną od strony teoretycznej, tj. bez wykonywania eksperymentów na stole laboratoryjnym.
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Wykład III. Teoria pasmowa ciał stałych
 Wykład III Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Wykład III Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Chemia nieorganiczna. Pierwiastki. niemetale Be. 27 Co. 28 Ni. 26 Fe. 29 Cu. 45 Rh. 44 Ru. 47 Ag. 46 Pd. 78 Pt. 76 Os.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
E-E-A-1008-s5 Komputerowa Symulacja Układów Nazwa modułu. Dynamicznych. Elektrotechnika I stopień Ogólno akademicki. Przedmiot kierunkowy
 Załącznik nr 7 do Zarządzenia Rektora nr 10/12 z dnia 21 lutego 2012r. KARTA MODUŁU / KARTA PRZEDMIOTU Kod modułu E-E-A-1008-s5 Komputerowa Symulacja Układów Nazwa modułu Dynamicznych Nazwa modułu w języku
Załącznik nr 7 do Zarządzenia Rektora nr 10/12 z dnia 21 lutego 2012r. KARTA MODUŁU / KARTA PRZEDMIOTU Kod modułu E-E-A-1008-s5 Komputerowa Symulacja Układów Nazwa modułu Dynamicznych Nazwa modułu w języku
Test sprawdzający, wielostopniowy z chemii: Węglowodory
 Test sprawdzający, wielostopniowy z chemii: Węglowodory Typ szkoły: Autor testu: technikum mgr Ewa Jagoda Skonstruowany przeze mnie test zawiera pytania zamknięte czterokrotnego wyboru, w których tylko
Test sprawdzający, wielostopniowy z chemii: Węglowodory Typ szkoły: Autor testu: technikum mgr Ewa Jagoda Skonstruowany przeze mnie test zawiera pytania zamknięte czterokrotnego wyboru, w których tylko
S. Baran - Podstawy fizyki materii skondensowanej Półprzewodniki. Półprzewodniki
 Półprzewodniki Definicja i własności Półprzewodnik materiał, którego przewodnictwo rośnie z temperaturą (opór maleje) i w temperaturze pokojowej wykazuje wartości pośrednie między przewodnictwem metali,
Półprzewodniki Definicja i własności Półprzewodnik materiał, którego przewodnictwo rośnie z temperaturą (opór maleje) i w temperaturze pokojowej wykazuje wartości pośrednie między przewodnictwem metali,
 Klasyfikator liniowy Wstęp Klasyfikator liniowy jest najprostszym możliwym klasyfikatorem. Zakłada on liniową separację liniowy podział dwóch klas między sobą. Przedstawia to poniższy rysunek: 5 4 3 2
Klasyfikator liniowy Wstęp Klasyfikator liniowy jest najprostszym możliwym klasyfikatorem. Zakłada on liniową separację liniowy podział dwóch klas między sobą. Przedstawia to poniższy rysunek: 5 4 3 2
