Do identyfikacji i wyliczania komórek CD34+ w próbkach mobilizowanej krwi ludzkiej i próbkach z leukaferezy.
|
|
|
- Seweryna Milewska
- 8 lat temu
- Przeglądów:
Transkrypt
1 CD34Count Kit Nr kat. K2370 Wydanie 2. Do identyfikacji i wyliczania komórek CD34+ w próbkach mobilizowanej krwi ludzkiej i próbkach z leukaferezy. Zestaw zawiera odczynniki wystarczające do wykonania 50 podwójnych testów. ( ) K2370/PL/JLA/ s 1/14
2 Spis treści Strona Przeznaczenie... 3 Streszczenie i informacje ogólne... 3 Zasady procedury... 3 Odczynniki... 4 Dostarczane materiały... 4 Materiały wymagane, ale niedostarczane... 4 Przygotowanie odczynników... 5 Środki ostroŝności... 5 Przechowywanie... 6 Pobieranie i przygotowanie próbek... 6 Procedura barwienia... 7 Barwienie komórek i dodawanie kulek kontrolnych... 7 Wskazówka, pipetowanie odwrotne z mokrą końcówką... 7 Kontrola jakości... 8 Próbka kontrolna... 8 Kontrola jakości na podstawie czasu... 8 Testy podwójne... 8 Akwizycja danych... 8 Konfiguracja akwizycji dla zestawu CD34Count Kit... 9 Analiza danych Wyniki Przypisanie wartości Ograniczenia metody Rozwiązywanie problemów Urządzenie pomiarowe Piśmiennictwo ( ) K2370/PL/JLA/ s 2/14
3 Przeznaczenie Do diagnostyki in vitro z zastosowaniem cytometrii przepływowej. Zestaw CD34Count Kit jest testem przeznaczonym do diagnostyki in vitro, słuŝącym do identyfikacji i wyliczania CD34-dodatnich (CD34+) krwiotwórczych komórek macierzystych w próbkach mobilizowanej ludzkiej krwi obwodowej i próbkach z leukaferezy. Streszczenie i informacje ogólne Krwiotwórcze komórki progenitorowe (KKP) mogą być mobilizowane ze szpiku kostnego do krwi obwodowej (KO) przy uŝyciu środków cytotoksycznych, cytokin lub kombinacji obu tych metod. Mobilizacja taka umoŝliwia zebranie (metodą aferezy) krwiotwórczych komórek progenitorowych w ilościach wystarczających do przeszczepu (1, 2). W ostatnim dziesięcioleciu wyraźnie wzrosło zainteresowanie wykorzystaniem komórek macierzystych krwi obwodowej (KMKO) do przeszczepów, a w przypadku przeszczepów autologicznych krew obwodowa jest teraz preferowanym źródłem KKP, zastępując w tej roli szpik kostny. Tradycyjnie prognozy co do potencjału regeneracyjnego opierano na bezwzględnej liczbie komórek jednojądrzastych w szpiku w stosunku do masy ciała biorcy. Jednak metoda ta jest niewystarczająca w przypadku próbek KMKO, poniewaŝ charakteryzują się one róŝną zawartością KKP. Pod koniec lat 80. XX w. ostatecznie ustalono, Ŝe niemal cała aktywność komórek zdolnych do tworzenia kolonii oraz potencjał regeneracyjny próbek szpiku lub krwi obwodowej skupia się w niewielkiej populacji komórek zawierających antygen CD34 (3). CD34 to antygen powierzchniowy, który w przypadku komórek krwiotwórczych występuje wyłącznie we wczesnych progenitorach wszystkich linii komórkowych (1, 2). A zatem KKP CD34+ wykazują zdolność do przywracania hematopoezy wielu linii komórkowych u pacjentów z uszkodzeniami szpiku. Wykazano (1, 2), Ŝe liczba komórek CD34+ ustalona metodą cytometrii przepływowej przypadająca na kilogram masy ciała biorcy jest najbardziej uŝytecznym wskaźnikiem zdolności przeszczepionych komórek macierzystych krwi obwodowej (KMKO) do przywracania hematopoezy. Sutherland i in. (5) opracowali dla stowarzyszenia International Society for Hematotherapy and Graft Engineering (ISHAGE, Międzynarodowe Stowarzyszenie Hematoterapii i InŜynierii Przeszczepów) zestaw wytycznych klinicznych upraszczających i standaryzujących zasady wyliczania komórek CD34+. Zestaw CD34Count Kit jest zgodny z tymi wytycznymi i zawiera przeciwciała skierowane przeciwko CD45/FITC oraz przeciwko CD34/RPE, umoŝliwia zatem identyfikację leukocytów (CD45+) oraz weryfikację prawdziwych komórek CD34+ na podstawie słabej fluorescencji CD45 i słabszego rozproszenia bocznego (CD45 dim, SSC low ). Dodanie kulek CytoCount do zawiesiny komórkowej pozwala na określenie stęŝenia komórek CD34+ na jednostkę objętości oryginalnej próbki (tj. bezwzględnej liczby komórek CD34+) w ramach jednego badania metodą cytometrii przepływowej (technika jednoplatformowa) (1-3). W technice jednoplatformowej występuje mniej źródeł zmienności niŝ w powszechnie uŝywanej wcześniej technice dwuplatformowej, a badania wieloośrodkowe wykazały, Ŝe zapewnia ona lepszy współczynnik zmienności, zaś ryzyko wygenerowania błędnych wyników jest niŝsze (4). Dodanie opcjonalnego barwnika DNA, 7-aminoaktynomycyny D (7-AAD), równieŝ wchodzącego w skład zestawu, umoŝliwia wykluczenie martwych komórek z analizy (1, 2). Barwnik 7-AAD dyfunduje wyłącznie do martwych komórek i tylko takie komórki barwi, poniewaŝ ich błona komórkowa nie jest nienaruszona. Zasady procedury Zestaw CD34Count Kit opracowano z myślą o stworzeniu optymalnej metody wyliczania komórek CD34+ zgodnie z wytycznymi ISHAGE dotyczącymi techniki jednoplatformowej (1, 2, 5). Test jest zdublowany i polega na wybarwieniu próbki dwubarwnym odczynnikiem zawierającym przeciwciała przeciwko ludzkiemu CD45/FITC oraz przeciwciała przeciwko ludzkiemu CD34/RPE. Po wybarwieniu próbki erytrocyty są poddawane lizie przy uŝyciu odczynnika na bazie chlorku amonu, zaś jeśli poŝądana jest ocena Ŝywotności komórek, do próbki dodawany jest (opcjonalny) ( ) K2370/PL/JLA/ s 3/14
4 barwnik 7-AAD. Do próbki pełniącej rolę wewnętrznej populacji odniesienia dodawane są fluorescencyjne kulki kontrolne (CytoCount ). W trakcie analizy istnieje moŝliwość ustalenia bezwzględnego stęŝenia komórek CD34+ w próbce; naleŝy w tym celu podzielić liczbę zdarzeń CD34 przez liczbę zdarzeń wywołanych przez kulki fluorescencyjne, a następnie pomnoŝyć przez stęŝenie kulek w materiale CytoCount. W wytycznych ISHAGE wskazane jest uŝycie strategii ograniczeń dwuwartościowych w celu zdefiniowania rzeczywistych komórek progenitorowych wykazujących potencjał regeneracyjny. Realizuje się to poprzez wybarwienie kontrastowe komórek CD34+ przeciwciałem skierowanym przeciwko CD45/FITC, co pozwala na wyeliminowanie z analizy zanieczyszczeń i zdarzeń związanych z barwieniem nieswoistym (1, 2). Co waŝne, rozwiązanie takie pozwala takŝe na rozróŝnienie między KKP, które wykazują stosunkowo słabą ekspresję białka CD45 na powierzchni błony, a limfocytami i monocytami, które wykazują silną ekspresję. Niezłośliwe krwiotwórcze komórki macierzyste CD34+ i prekursory tworzą wyodrębnione zgrupowania na wykresach podobnie jak limfocyty, monocyty i granulocyty, tworzące wyodrębnione zgrupowania na dwuwymiarowych wykresach CD45 / rozproszenie boczne (SSC). Dodanie kulek referencyjnych w znanym stęŝeniu umoŝliwia obliczenie bezwzględnego stęŝenia komórek CD34+ w oryginalnej próbce, tj. określenie liczby komórek CD34+ w µl próbki. Wykluczenie komórek martwych z wyliczenia komórek CD34+ jest opcjonalne; uzyskuje się je poprzez dodanie barwnika DNA, 7-AAD, który umoŝliwia rozróŝnienie komórek Ŝywych od niezdolnych do Ŝycia. Barwnik 7-AAD wzbudza się przy długości fali 488 nm i ma maksimum emisji przy 660 nm. Dodanie barwnika 7-AAD jest szczególnie zalecane podczas analizy próbek z leukaferezy przechowywanych przez czas dłuŝszy niŝ cztery godziny lub rozmroŝonych. Odczynniki Dostarczane materiały Fiolka 1 Fiolka 2 Monoclonal Mouse Anti-Human CD45/FITC, Clone T29/33 + Monoclonal Mouse Anti-Human CD34/RPE, Clone BIRMA-K3 1 ml, gotowy do uŝycia EasyLyse 2 x 5 ml, stęŝony 20x Odczynnik powodujący lizę erytrocytów, na bazie chlorku amonu Fiolka 3 Fiolka 4 7-Aminoactinomycin D (7-AAD) 1 ml (0,01% wagowo-objętościowo), gotowy do uŝycia Do barwienia w celu oceny Ŝywotności CytoCount 17 ml, gotowy do uŝycia po odtworzeniu zawiesiny Kulki kontrolne Materiały wymagane, ale niedostarczane 1. Probówki polistyrenowe 12 x 75 mm. 2. Pipeta skalibrowana do objętości 10 µl i 100 µl. 3. Mieszadło do krwi lub mieszadło rotacyjne do odtwarzania zawiesiny kulek CytoCount. 4. Woda dejonizowana lub destylowana. 5. Mieszadło wirowe. ( ) K2370/PL/JLA/ s 4/14
5 6. Dozownik lub pipetor (2 ml) do odmierzenia 2 ml odczynnika EasyLyse. 7. Bufor fosforanowy (PBS) do ewentualnego rozcieńczenia próbki. 8. Sheat Fluid. 9. Próbki kontrolne CD34+. Przygotowanie odczynników 1. Rozcieńczyć wymaganą ilość odczynnika EasyLyse, fiolka 2, 1+19 wodą dejonizowaną o temperaturze pokojowej. Zamiast tego moŝna wymieszać zawartość jednej buteleczki (5 ml) EasyLyse z 95 ml wody dejonizowanej o temperaturze pokojowej. Odczynnik do lizy nie moŝe być uŝywany z wodą wodociągową. 2. Wyjąć fiolkę 4, CytoCount, z chłodziarki (2 8 C). Upewnić się, Ŝe nakrętka jest szczelnie zamknięta, aby uniknąć wycieku płynu, i dobrze zamieszać, aby w pełni odtworzyć zawiesinę kulek. NaleŜy unikać mieszania za pomocą mieszadła wirowego, poniewaŝ stwarzałoby to ryzyko wprowadzenia pęcherzyków powietrza i w efekcie zmniejszenia rzeczywistej objętości pipetowanej zawiesiny kulek. Zaleca się umieszczenie zawiesiny kulek w mieszadle rotacyjnym na 5 60 minut, aby uniknąć opadnięcia kulek, zanim zawiesina będzie potrzebna. Przed uŝyciem odczynnika CytoCount naleŝy odczekać, aŝ ogrzeje się on do temperatury pokojowej. Środki ostroŝności 1. Odczynniki są przeznaczone dla przeszkolonych UŜytkowników. 2. Fiolka 1, przeciwciała przeciwko ludzkiemu CD45/FITC + przeciwciała przeciwko ludzkiemu CD34/RPE, zawiera materiał pochodzenia zwierzęcego. Podobnie jak w przypadku kaŝdego produktu otrzymywanego z materiału biologicznego, naleŝy stosować odpowiednie procedury postępowania. 3. Nie zamraŝać Ŝadnego z odczynników ani nie wystawiać odczynników na bezpośrednie działanie światła. 4. Fiolka 3, 7-AAD, zawiera barwnik wiąŝący kwasy nukleinowe. StęŜenie barwnika w roztworze wynosi 0,01%, dlatego roztwór nie wymaga oznakowania właściwego dla substancji niebezpiecznych. Nie określono właściwości toksykologicznych tego barwnika. 5. StęŜenie kulek w fiolce 4, CytoCount, jest róŝne w kaŝdej partii. StęŜenie kulek (C) i odchylenie standardowe (S) jest podane na fiolce jako liczba kulek na µl. 6. Fiolki 1, 2, 3 i 4 zawierają azydek sodu (NaN 3 ), substancję chemiczną silnie toksyczną w czystej postaci. Azydek sodu, zastosowany w produkcie w stęŝeniu, które nie jest sklasyfikowane jako niebezpieczne, moŝe reagować z elementami kanalizacji wykonanymi z ołowiu i miedzi, powodując nagromadzenie silnie wybuchowych azydków metali. Po usunięciu spłukać duŝą ilością wody, aby zapobiec nagromadzeniu się azydku metalu w kanalizacji. 7. Fiolka 4, CytoCount, powinna być przechowywana w pozycji pionowej i szczelnie zamknięta, aby zapobiec wyciekowi płynu. Przed uŝyciem kulek CytoCount naleŝy starannie odtworzyć ich zawiesinę. Gwałtowne mieszanie kulek CytoCount w mieszadle wirowym moŝe powodować przedostanie się do płynu pęcherzyków powietrza, a w konsekwencji zmniejszyć faktyczną objętość pipetowanej zawiesiny kulek CytoCount. Zalecane jest delikatne mieszanie (np. w mieszadle rotacyjnym lub mieszadle do probówek). 8. NaleŜy uwaŝać, aby nie rozlać nawet minimalnej ilości odczynnika CytoCount przed odtworzeniem zawiesiny, gdyŝ w przeciwnym razie liczba kulek będzie nieprawidłowa. W razie stwierdzenia wycieku z fiolki 4, CytoCount, w otrzymanym zestawie nie naleŝy uŝywać kulek. NaleŜy skontaktować się z działem technicznym firmy Dako w celu wymiany fiolki 4. ( ) K2370/PL/JLA/ s 5/14
6 9. Kluczowe znaczenie ma uŝywanie tej samej skalibrowanej pipety oraz techniki pipetowania odwrotnego z mokrą końcówką zarówno do próbki, jak i do kulek CytoCount. WaŜne jest dokładne odmierzenie pipetowanej objętości kulek CytoCount oraz próbki. Objętości odczynnika zawierającego przeciwciała oraz odczynnika do lizy nie mają newralgicznego znaczenia przy określaniu bezwzględnej liczby komórek CD34+; istotny jest natomiast stosunek objętości próbki do objętości kulek. 10. Zaleca się ustawienie wartości progowej na FL1 ( nm), poniewaŝ zminimalizuje to ryzyko pominięcia zdarzeń skojarzonych z kulkami CytoCount podczas akwizycji. NaleŜy uwaŝać, by nie wykluczyć Ŝadnych zdarzeń CD34+ w wyniku ustawienia zbyt wysokiego progu FL1. Zob. sekcja Rozwiązywanie problemów. 11. Testy nie wykazały przenoszenia materiału między róŝnymi próbkami. Zaleca się jednak przeprowadzenie walidacji cytometru przepływowego pod kątem efektu przenoszenia materiału między próbkami. Aby uniknąć przenoszenia materiału z próbki o wysokim stęŝeniu komórek CD34+ do próbki o niŝszym stęŝeniu, moŝna między próbkami przepuścić przez cytometr przepływowy bufor fosforanowy. 12. Jeśli uŝywany jest barwnik 7-AAD znakujący komórki martwe, kluczowe znaczenie ma wybranie optymalnych ustawień kompensacji, poniewaŝ sygnał z kanału RPE nakłada się na sygnał z kanału 7-AAD. W najbardziej niekorzystnym przypadku zdarzenia CD34+ będą eliminowane, jeśli wpadną w ograniczenie wykluczające komórki martwe w kanale 7-AAD / rozpraszanie boczne (SSC). 13. Barwnik 7-AAD wzbudza się przy długości fali 488 nm i ma maksimum emisji przy 660 nm (FL3 lub FL4, zaleŝnie od typu cytometru). Z tego względu barwnika nie moŝna uŝywać w systemach z jednym laserem z innymi fluorochromami emitującymi fale o długości >600 nm, takimi jak PerCP lub RPE-Cy Zgłaszano przypadki agregacji kulek kontrolnych (4). Kulki CytoCount charakteryzują się szczególnie małym odsetkiem zlepień (poniŝej 3%), co ułatwia definiowanie ograniczeń. W razie zaobserwowania większej liczby zlepionych kulek CytoCount i powstania wątpliwości co do jakości produktu, naleŝy skontaktować się z działem wsparcia technicznego firmy Dako. Przechowywanie Zestaw naleŝy przechowywać w ciemnym miejscu, w temperaturze 2 8 C. Nie naleŝy uŝywać odczynników po upływie terminu waŝności podanego na opakowaniu zestawu. JeŜeli odczynniki są przechowywane w warunkach innych niŝ podane w ulotce dołączonej do opakowania, UŜytkownik powinien je zweryfikować. EasyLyse, odczynnik w fiolce 2, jest stabilny przez 6 miesięcy od otwarcia fiolki. Po rozcieńczeniu odczynnik do lizy jest stabilny przez 20 dni w temperaturze 2 24 C. Wszystkie odczynniki naleŝy przechowywać w pozycji pionowej. Pobieranie i przygotowanie próbek Krew obwodową naleŝy pobrać aseptycznie, poprzez wkłucie doŝylne, do sterylnej probówki do pobierania krwi K 3 EDTA. Do kaŝdego testu potrzebne jest 200 µl krwi (100 µl na probówkę). Podczas pobierania próbki naleŝy postępować wg instrukcji producenta probówki. Próbki z leukaferezy naleŝy pobierać zgodnie z instrukcjami producenta przyrządu do leukaferezy. Krew ze środkiem zapobiegającym koagulacji naleŝy przechowywać w temperaturze pokojowej (20 do 25 C) do czasu wykonania barwienia. Próbki krwi obwodowej naleŝy wybarwić przed upływem 24 godzin od pobrania. W przypadku próbek z leukaferezy zaleca się przeprowadzenie barwienia równolegle z obróbką produktu leukaferezy. ( ) K2370/PL/JLA/ s 6/14
7 We wszystkich próbkach, które mają być testowane, naleŝy zbadać liczbę leukocytów. Jeśli liczba leukocytów jest wyŝsza niŝ 10 7 /ml, naleŝy rozcieńczyć próbkę buforem fosforanowym do około 10 7 leukocytów/ml. Zapisać współczynnik rozcieńczenia, gdyŝ potrzebny będzie do obliczenia ostatecznej bezwzględnej liczby komórek CD34+ w oryginalnej próbce. Nie uŝywać komórek wstępnie utrwalonych. Procedura barwienia Barwienie komórek i dodawanie kulek kontrolnych 1. Rozcieńczyć oryginalną próbkę buforem fosforanowym do około 10 7 leukocytów na ml. Zanotować dokładny współczynnik rozcieńczenia. W większości przypadków rozcieńczenie będzie konieczne tylko dla próbek z leukaferezy. 2. Na kaŝdej próbce naleŝy wykonać test podwójny. Dlatego dla kaŝdej próbki naleŝy oznaczyć dwie probówki. 3. Za pomocą pipety przenieść po 100 µl próbki do kaŝdej probówki. Zastosować technikę pipetowania odwrotnego (zob. punkt Wskazówka, pipetowanie odwrotne z mokrą końcówką ). 4. Dodać 10 µl odczynnika z fiolki 1 (przeciwciała przeciwko ludzkiemu CD45/FITC + przeciwciała przeciwko ludzkiemu CD34/RPE) do kaŝdej probówki i wymieszać w mieszalniku wirowym. Inkubować probówki przez 30 minut w temperaturze 2 8 C lub przez minut w temperaturze pokojowej (20 25 C). 5. Dodać 2 ml rozcieńczonego odczynnika do lizy (fiolka 2, EasyLyse rozcieńczony 20 x). Natychmiast po dodaniu środka do lizy wymieszać próbkę w mieszadle wirowym. 6. Inkubować w ciemności przez 10 minut w temperaturze pokojowej. 7. Jeśli poŝądane jest określenie Ŝywotności komórek, dodać do kaŝdej próbki 10 µl barwnika z fiolki 3 (7-AAD) i wymieszać. W przeciwnym razie przejść do kroku 8. Przed akwizycją inkubować z barwnikiem 7-AAD przez co najmniej 5 minut. 8. Odtworzyć zawiesinę w fiolce 4 (CytoCount ) za pomocą mieszadła rotacyjnego, zgodnie z opisem w sekcji Przygotowanie odczynników. Dodać 100 µl do próbki wybarwionej i poddanej lizie. Do pipetowania próbki i kulek CytoCount naleŝy uŝywać tej samej skalibrowanej pipety i stosować technikę pipetowania odwrotnego z mokrą końcówką (4) (zob. punkt Wskazówka, pipetowanie odwrotne z mokrą końcówką ). 9. Przed akwizycją przez 3 sekundy delikatnie mieszać kulki z próbką za pomocą mieszadła wirowego, aby uzyskać równomierny rozkład kulek CytoCount w próbce. 10. Akwizycja próbki musi odbyć się przed upływem 45 minut od dodania odczynnika do lizy (krok 5). 11. Przeprowadzić akwizycję zdarzeń skojarzonych z co najmniej leukocytów, 1000 kulek CytoCount i co najmniej 100 komórkami CD34+ (4). Zob. Konfiguracja akwizycji dla zestawu CD34Count Kit. Wskazówka, pipetowanie odwrotne z mokrą końcówką Do dozowania próbki i kulek naleŝy uŝywać tej samej pipety. Do kaŝdego odczynnika uŝywać czystej końcówki pipety. Zastosowanie tej samej techniki do dozowania próbek i kulek zapewni lepszą powtarzalność wyników. Próbka 1. Nacisnąć tłoczek do drugiego oporu, zanurzyć końcówkę w płynie i zassać próbkę. Następnie nacisnąć tłoczek do pierwszego oporu, aby wstrzyknąć próbkę. Końcówka pipety powinna teraz zawierać nadmiar płynu. 2. Powtórzyć ten krok dwukrotnie, trzymając końcówkę pipety zanurzoną w próbce. 3. Końcówka pipety jest teraz gotowa do uŝycia. Nacisnąć tłoczek do drugiego oporu, zanurzyć końcówkę w płynie i zassać próbkę. OstroŜnie wyjąć końcówkę pipety z próbki i delikatnie ( ) K2370/PL/JLA/ s 7/14
8 wytrzeć końcówkę pipety bibułką, aby usunąć nadmiar płynu, uwaŝając przy tym, by nie dotknąć otworu końcówki i przypadkiem nie usunąć próbki z wnętrza końcówki. 4. W miarę moŝliwości utrzymywać pipetę pionowo. Sprawdzić, czy w końcówce nie ma pęcherzyków powietrza. W razie stwierdzenia pęcherzyków wstrzyknąć płyn z powrotem do probówki z próbką i powtórzyć procedurę. 5. Nacisnąć tłoczek do pierwszego oporu, wstrzykując dawkę próbki; po wstrzyknięciu w końcówce pipety powinna być widoczna pozostałość płynu. Nie dotykać ścianek probówki podczas wyjmowania końcówki. Kulki 6. Przygotować pipetę z zawiesiną kulek CytoCount z probówki 4, postępując tak samo, jak z próbką (kroki 1 3). 7. W celu wstrzyknięcia zawiesiny kulek umieścić końcówkę pipety przy ścianie probówki w pobliŝu powierzchni próbki; lekkie nachylenie probówki i pipety ułatwi wykonanie tej czynności. Nacisnąć tłoczek do pierwszego oporu, wstrzykując dawkę zawiesiny; po wstrzyknięciu w końcówce pipety powinna być widoczna pozostałość płynu. 8. W celu pipetowania większej ilości zawiesiny kulek umieścić końcówkę w fiolce CytoCount i zassać więcej zawiesiny, nie wstrzykując resztki płynu pozostałej w końcówce po pierwszym pipetowaniu. 9. Jeśli końcówka nie zetknęła się jeszcze z próbką, naleŝy wstrzyknąć płyn pozostały w końcówce do fiolki CytoCount. Jeśli pozostały płyn będzie wylewany do kanalizacji, odczynnika moŝe nie wystarczyć na 50 testów. Kontrola jakości Próbka kontrolna Zaleca się uwzględnienie w teście dodatniej próbki kontrolnej, co pozwoli na zweryfikowanie poprawności konfiguracji wyliczania komórek CD34+. Zdecydowanie zalecane jest przystąpienie do zewnętrznego programu oceny jakości. Kontrola jakości na podstawie czasu W badaniach jednoplatformowych w charakterze wewnętrznego wskaźnika jakości moŝna wykorzystać czas akwizycji. Badania wykazały, Ŝe w większości cytometrów przepływowych liczba kulek zarejestrowanych w określonym czasie pozostaje zasadniczo stała. Dlatego dla kaŝdej nowej partii kulek uŝytkownik moŝe ustalić przedział liczby kulek o szerokości ± 2 odchylenia standardowe względem średniej liczby rejestrowanej w zadanym czasie. KaŜda próbka, w której liczba zarejestrowanych kulek nie mieści się w tym przedziale, moŝe być skutkiem błędu pipetowania i wymagać ponownego wybarwienia (6). Testy podwójne NaleŜy wykonać podwójny test kaŝdej próbki. RóŜnica wartości uzyskanych z obu egzemplarzy próbki nie powinna przekraczać 15%. Jeśli róŝnica jest większa, test na próbce naleŝy powtórzyć. RóŜnicę między wartościami z dwóch egzemplarzy (X i Y) oblicza się wg poniŝszego wzoru: X-Y (X+Y)/2 x 100% Akwizycja danych NaleŜy skonfigurować cytometr do akwizycji trójbarwnej zgodnie z instrukcjami jego producenta. Konfiguracja powinna obejmować ustawianie lub kontrolę napięcia lampy fotopowielacza (PMT) oraz czułości przyrządu, a takŝe kompensację, jeśli uŝywana będzie kompensacja sprzętowa. Konfigurację akwizycji w cytometrach przepływowych FACSCalibur (Beckton Dickinson) i Coulter XL (Beckman Coulter) przedstawili Sutherland et al. (1) oraz Gratama et al. (2). ( ) K2370/PL/JLA/ s 8/14
9 Konfiguracja akwizycji dla zestawu CD34Count Kit Akwizycja danych moŝe odbywać się z zastosowaniem kompensacji sprzętowej lub bez kompensacji w tym drugim przypadku niezbędna jest kompensacja podczas analizy danych. Informacje na temat ustawień kompensacji moŝna znaleźć w ogólnych wskazówkach dotyczących cytometrii przepływowej. PoniŜszy protokół przeznaczony jest zarówno do akwizycji, jak i do analizy. 1. Wygenerować następujące dwuwymiarowe prezentacje danych (wykresy punktowe) i ustawić regiony zgodnie z ilustracjami: Wykres A: CD45 FITC SSC-H (region 1 i region 5) Wykres B: CD34 RPE SSC-H (region 2) Wykres C: CD45 FITC SSC-H (region 3) Wykres D: FSC-H SSC-H (region 4) Wykres E: 7-AAD SSC-H (region 8) Wykres F: CD45 FITC CD34 RPE (region 6 i region 9) Wykres G: Czas FSC-H z ograniczeniem do zdarzeń CytoCount (region 7) Wykres H: FSC-H SSC-H 2. Utworzyć następujące warunki ograniczeń (bramki; kolor jest opcjonalny): Ograniczenie G7 nosi nazwę Stem Cells (Komórki macierzyste) i dodawane jest do kreatora ograniczeń w celu wyróŝnienia kolorem zdarzeń dodatnich CD34+. Ograniczenie wyróŝniające zdarzenia kolorem jest bardzo przydatne podczas konfiguracji akwizycji oraz analizy. 3. Zastosować ograniczenia do wykresów w następujący sposób: Wykres A: G1 Wykres B: G2 Wykres C: G3 Wykres D: G4 Wykres E: Bez ograniczenia Wykres F: Bez ograniczenia Wykres G: G6 Wykres H: Bez ograniczenia 4. Ustawić wartość progową na FL-1 w taki sposób, by wykluczane były wszystkie zdarzenia CD45-ujemne. Zaleca się ustawienie progu wartości FL-1, poniewaŝ zminimalizuje to ryzyko wykluczenia kulek CytoCount. Ustawienie progu parametru FSC równieŝ moŝe być celowe, naleŝy jednak uwaŝać, by nie wykluczyć Ŝadnych zdarzeń skojarzonych z kulkami. Zob. sekcja Rozwiązywanie problemów. 5. Załadować pierwszą próbkę i wyregulować wzmocnienie fotopowielacza dla parametrów FSC i SSC w taki sposób, by wszystkie populacje na Wykresie H mieściły się na skali. Jeśli ustawiono próg parametru FSC, naleŝy upewnić się, Ŝe zdarzenia CytoCount wypadają nad progiem. ( ) K2370/PL/JLA/ s 9/14
10 6. Wyregulować fotopowielacz dla CD45/FITC. Populacja limfocytów powinna mieścić się w trzeciej dekadzie (Wykres A). Upewnić się, Ŝe nie są wykluczane Ŝadne komórki CD45+ o słabej fluorescencji. W razie wątpliwości naleŝy albo obniŝyć próg FL1, albo zwiększyć wzmocnienie fotopowielacza dla parametru FL1. Po zmianie ustawień fotopowielacza konieczne moŝe być skorygowanie ustawień kompensacji. Wykres A Wykres B Wykres C 7. Wyregulować fotopowielacz dla CD34/RPE. Większość zdarzeń ujemnych powinna przypadać między pierwszą a drugą dekadą (Wykres B). 8. Wyregulować fotopowielacz dla 7-AAD. Większość zdarzeń ujemnych powinna mieścić się w pierwszej dekadzie (Wykres E). 9. Zastosować region 6 z Wykresu F na Wykresie G. Jeśli ustawiono próg parametru FSC, naleŝy na wykresie G sprawdzić, czy ustawienie to nie spowodowało wykluczenia zdarzeń CytoCount (zob. sekcja Rozwiązywanie problemów). Wykres D Wykres E Wykres F 10. Zaleca się zastosowanie ograniczenia wykluczającego na Wykresie H. Ograniczenie to powinno obejmować zdarzenia skojarzone z niskimi wartościami SSC i FSC (Region 9). W trakcie akwizycji zdarzenia wykluczane przez to ograniczenie powinny być odrzucane. Uzyskuje się to poprzez zastosowanie filtru ograniczającego (ograniczenia wykluczającego) do tych zdarzeń lub odrzucanie zdarzeń z regionu R9 w oknie akwizycji. Jeśli w charakterze progu uŝywana jest wartość FSC, ograniczenie wykluczające nie jest istotne. ( ) K2370/PL/JLA/ s 10/14
11 11. Upewnić się, Ŝe podczas akwizycji jako jeden z parametrów rejestrowany jest czas. Wykres G Wykres H Cytometr jest teraz gotowy do rozpoczęcia akwizycji. 12. Przeprowadzić akwizycję co najmniej zdarzeń związanych z leukocytami, 1000 zdarzeń CytoCount oraz 100 zdarzeń CD34+. Kryterium zatrzymania moŝna skojarzyć tylko z jedną z tych liczb. W przypadku próbek o niskim stęŝeniu CD34+ kryterium zatrzymania będzie liczba 100 zdarzeń CD34+, natomiast w przypadku próbek o wysokim stęŝeniu CD34+ kryterium zatrzymania będzie liczba leukocytów. Wskazane jest zarejestrowanie moŝliwe duŝej liczby zdarzeń, gdyŝ pozwoli to z większą dokładnością określić liczbę komórek CD34+. Analiza danych Podczas analizy naleŝy postępować wg tego samego protokołu, co podczas akwizycji. 1. Do danych uzyskanych bez kompensacji sprzętowej zastosować kompensację zgodnie z instrukcjami wyświetlanymi przez oprogramowanie. Szczególnie istotna jest kompensacja zachodzenia kanału RPE na kanał barwnika 7-AAD (zob. Środki ostroŝności). 2. Dla regionu 4 (komórki) naleŝy wyświetlić statystykę przedstawiającą komórki progenitorowe CD34+, a dla regionu 7 (kulki) liczbę kulek. Jeśli potrzebna jest liczba zarejestrowanych Ŝywych komórek CD45-dodatnich, to naleŝy wyświetlić równieŝ statystykę dla regionu 1 (G2). 3. Zaimportować plik danych z akwizycji (plik FCS) i rozmieścić regiony. 4. Na Wykresie D zastosować ograniczenie G5 i umieścić region 4 w taki sposób, by obejmował tylko najmniejsze limfocyty (rysunek 1(a)). 5. Teraz zastosować ograniczenie G4 na Wykresie D, nie zmieniając połoŝenia regionu 4 (rysunek 1(b)). ( ) K2370/PL/JLA/ s 11/14
12 a b Rysunek 1. (a): Region 4 jest umieszczony w taki sposób, by obejmował zdarzenia większe od najmniejszych limfocytów oraz zdarzenia o niskiej wartości SSC. (b): Po ustawieniu regionu 4 na Ŝywych limfocytach do wykresu zastosowano ograniczenie G4, aby uwidocznić zdarzenia spełniające wymogi określone w wytycznych ISHAGE. Wyniki Obliczenie bezwzględnej liczby komórek CD34+ na µl oryginalnej próbki: Bezwzględną liczbę komórek CD34+ naleŝy obliczyć z poniŝszego wzoru: Komórki CD34+ /µl = Zliczona liczba komórek CD34+ (R4) x StęŜenie CytoCount * x Współczynnik rozcieńcz. Zliczona liczba kulek (R7) *Ta wartość (C) podana jest na etykiecie fiolki 4: C= Liczba kulek/µl. W przedstawionym przykładzie (Wykresy od A do H) bezwzględna liczba komórek CD34+ obliczona zostanie z następującego wzoru: 216 x 1006 x 1 = 66 komórek CD34+ /µl 3276 Ostateczny wynik będzie średnią z dwóch testów. Firma Dako zaleca, by test uznawać za waŝny, jeśli róŝnica między tymi dwoma wartościami nie przekracza 15%, w przeciwnym razie próbkę naleŝy przeanalizować ponownie (zob. sekcja Kontrola jakości). Przypisanie wartości StęŜenie kulek (C) i odpowiednie odchylenie standardowe (S) jest podane na etykiecie fiolki 4 jako liczba/µl. Liczba ta ustalana jest za pomocą przyrządu Coulter Particle Counter Z1. Odchylenie standardowe stęŝenia kulek ma niewielki wpływ na łączną niepewność wyniku analizy. Ograniczenia metody 1. Ze względu na zmienność próbek biologicznych wyniki analizy niektórych próbek mogą być nieprawidłowe. Wszystkie wykresy punktowe powinna krytycznie ocenić osoba z doświadczeniem w stosowaniu cytometrii przepływowej. Skutkiem nieprawidłowego, zbyt wysokiego wyniku moŝe być sporządzenie wlewu zawierającego mniej komórek CD34+ niŝ wynosi zalecana ilość graniczna. 2. Wyniki uzyskane przy uŝyciu zestawu CD34Count Kit powinny być interpretowane w kontekście innych informacji klinicznych oraz wyników dodatkowych procedur diagnostycznych. 3. Próbki krwi naleŝy przechowywać w temperaturze pokojowej (20 do 25 C). 4. Nie uŝywać utrwalonych i przechowywanych próbek pochodzących od pacjentów. ( ) K2370/PL/JLA/ s 12/14
13 5. Liczba leukocytów w próbce nie powinna przekraczać 10 7 /ml, a liczba komórek CD34 nie powinna być wyŝsza niŝ 2000 komórek/µl. Rozwiązywanie problemów Problem Niektóre kulki nie są rejestrowane, poniewaŝ ustawiono za wysoką wartość progową FSC-H. Rozwiązanie Ponownie przeanalizować próbkę przy niŝszym progu FSC-H. Zaleca się jednak ustawienie progu parametru FL1. Źle: Na wykresie FSC-H nie są rejestrowane Ŝadne zdarzenia wypadające poniŝej głównej populacji kulek. Niektóre kulki CytoCount zostały wykluczone podczas akwizycji. Część populacji CD34+ została wykluczona, poniewaŝ ustawiono za wysoki próg FL1. Dobrze: Widoczne są kulki mniejsze niŝ główna populacja. Kulki CytoCount nie są wykluczane. Ponownie przeanalizować próbkę przy niŝszym progu FL1. Próbka kontroli jakości poza zakresem. Definiowanie regionów jest utrudnione. Sprawdzić konfigurację cytometru i akwizycji, następnie ponownie przeanalizować próbkę kontroli jakości. Jeśli próbka kontroli jakości nadal nie mieści się w zakresie, skontaktować się ze specjalistą odpowiedzialnym za obsługę techniczną cytometru. Powiększyć wykresy punktowe i przemieścić region. Urządzenie pomiarowe Zestaw CD34Count Kit jest przeznaczony do stosowania w cytometrach przepływowych. Cytometr przepływowy musi być wyposaŝony w sprzęt komputerowy i oprogramowanie oraz w laser 488 nm. Cytometr przepływowy musi umoŝliwiać detekcję fluorescencji o następujących długościach fal: nm (FL1), nm (FL2) i >650 nm (FL3 lub FL4, w zaleŝności od urządzenia). Musi takŝe istnieć moŝliwość detekcji rozpraszania w przód i rozpraszania bocznego. Urządzenie musi umoŝliwiać określenie wartości progowej parametru FL1 albo rozpraszania bocznego. ( ) K2370/PL/JLA/ s 13/14
14 NaleŜy zastosować ustawienia kontroli jakości zalecane przez producenta urządzenia. Konfiguracja powinna obejmować ustawienie lub sprawdzenie napięć fotopowielacza, kompensacji fluorescencji i czułości urządzenia. Piśmiennictwo 1. Sutherland DR, Keeney M, Gratama JW. Enumeration of CD34+ hematopoietic stem and progenitor cells. Current Protocols in Cytometry. New York: John Wiley & Sons; p Gratama JW, Keeney M, Sutherland DR. Enumeration of CD34+ hematopoietic stem and progenitor cells. Current protocols in cytometry. New York: John Wiley & Sons; p Keeney M, Gratama JW, Sutherland DR. Critical role of flow cytometry in evaluating peripheral blood hematopoietic stem cell grafts. Cytometry 2004;58A: Brando B, Barnett D, Janossy G, Mandy F, Autran B, Rothe G, et al. Cytofluorometric methods for assessing absolute numbers of cell subsets in blood (review). Cytometry 2000;42: Sutherland DR, Anderson L, Keeney M, Nayar R, Chin-Yee I. The ISHAGE guidelines for CD34+ cell determination by flow cytometry. J Hematother 1996;5: Bergeron M, Lustyik G, Phaneuf S, Ding T, Nicholson JKA, Janossy G, et al. Stability of currently used cytometers facilitates the identification of pipetting errors and their volumetric operation: time can tell all. Cytometry 2003;52B: Objaśnienie symboli Numer katalogowy Temperatura przechowywania Numer serii Wyrób medyczny do diagnostyki in vitro Sprawdzić w instrukcji stosowania Chronić przed słońcem (patrz sekcja nt. przechowywania) Zawartość wystarcza na <n> testów ZuŜyć przed Producent Producent: Dako Denmark A/S Produktionsvej 42 DK-2600 Glostrup Denmark/ Danemark/ Dänemark Tel Faks ( ) K2370/PL/JLA/ s 14/14
CytoCount Nr kat. S 2366 Wydanie z
 CytoCount Nr kat. S 2366 Wydanie z 03.12.03 Przeznaczenie Wstęp Do badań diagnostycznych in vitro. Produkt CytoCount jest przeznaczony do stosowania w cytometrii przepływowej. CytoCount stanowi zawiesinę
CytoCount Nr kat. S 2366 Wydanie z 03.12.03 Przeznaczenie Wstęp Do badań diagnostycznych in vitro. Produkt CytoCount jest przeznaczony do stosowania w cytometrii przepływowej. CytoCount stanowi zawiesinę
FluoroSpheres Nr kat. K0110
 FluoroSpheres Nr kat. K0110 Wydanie 6 Kulki kalibracyjne do codziennego monitorowania cytometru przepływowego. Zestaw zawiera odczynniki wystarczające do wykonania 40 kalibracji. (108651-004) SSK0110CE_02/PL/2015.12
FluoroSpheres Nr kat. K0110 Wydanie 6 Kulki kalibracyjne do codziennego monitorowania cytometru przepływowego. Zestaw zawiera odczynniki wystarczające do wykonania 40 kalibracji. (108651-004) SSK0110CE_02/PL/2015.12
Komórki macierzyste zastosowania w biotechnologii i medycynie BT Metody identyfikacji i fenotypowania populacji komórek macierzystych
 Metody identyfikacji i fenotypowania populacji komórek macierzystych 1 Wstęp Szpik kostny zawiera hematopoetyczne (HSC) oraz niehematopoetyczne komórki macierzyste (KM). Do niehematopoetycznych KM należą:
Metody identyfikacji i fenotypowania populacji komórek macierzystych 1 Wstęp Szpik kostny zawiera hematopoetyczne (HSC) oraz niehematopoetyczne komórki macierzyste (KM). Do niehematopoetycznych KM należą:
Oznaczanie aktywności cytotoksycznej chemoterapeutyków wobec komórek nowotworowych
 Wydział Chemiczny Politechniki Gdańskiej Katedra Technologii Leków i Biochemii Kultury tkankowe i komórkowe roślin i zwierząt Oznaczanie aktywności cytotoksycznej chemoterapeutyków wobec komórek nowotworowych
Wydział Chemiczny Politechniki Gdańskiej Katedra Technologii Leków i Biochemii Kultury tkankowe i komórkowe roślin i zwierząt Oznaczanie aktywności cytotoksycznej chemoterapeutyków wobec komórek nowotworowych
fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 Sierpień 2018
 Sierpień 2018 fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 EURx Ltd. 80-297 Gdansk Poland ul. Przyrodnikow 3, NIP 957-07-05-191 KRS
Sierpień 2018 fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 EURx Ltd. 80-297 Gdansk Poland ul. Przyrodnikow 3, NIP 957-07-05-191 KRS
Laboratorium z bionanostruktur. Prowadzący: mgr inż. Jan Procek Konsultacje: WT D- 1 8A
 Laboratorium z bionanostruktur Prowadzący: mgr inż. Jan Procek Konsultacje: WT 9.00-10.00 D- 1 8A Regulamin Studenci są dopuszczeni do wykonywania ćwiczenia jeżeli posiadają: Buty na płaskim obcasie, Fartuchy,
Laboratorium z bionanostruktur Prowadzący: mgr inż. Jan Procek Konsultacje: WT 9.00-10.00 D- 1 8A Regulamin Studenci są dopuszczeni do wykonywania ćwiczenia jeżeli posiadają: Buty na płaskim obcasie, Fartuchy,
DETEKCJA W MIKRO- I NANOOBJĘTOŚCIACH. Ćwiczenie nr 3 Detektor optyczny do pomiarów fluorescencyjnych
 DETEKCJA W MIKRO- I NANOOBJĘTOŚCIACH Ćwiczenie nr 3 Detektor optyczny do pomiarów fluorescencyjnych Cel ćwiczenia: Celem ćwiczenia jest zaznajomienie się z zasadą działania i zastosowaniami detektora optycznego
DETEKCJA W MIKRO- I NANOOBJĘTOŚCIACH Ćwiczenie nr 3 Detektor optyczny do pomiarów fluorescencyjnych Cel ćwiczenia: Celem ćwiczenia jest zaznajomienie się z zasadą działania i zastosowaniami detektora optycznego
INSTRUKCJA OBSŁUGI DETEKTOR INDUKCYJNY Z SYGNALIZACJĄ AKUSTYCZNĄ ORAZ OPTYCZNĄ METEK MD-22. # wersja 1.
 INSTRUKCJA OBSŁUGI DETEKTOR INDUKCYJNY Z SYGNALIZACJĄ AKUSTYCZNĄ ORAZ OPTYCZNĄ METEK MD-22 #03259 www.atel.com.pl/produkt.php?hash=03259 wersja 1.1 Wstęp Detektor metali i przewodów pod napięciem słuŝy
INSTRUKCJA OBSŁUGI DETEKTOR INDUKCYJNY Z SYGNALIZACJĄ AKUSTYCZNĄ ORAZ OPTYCZNĄ METEK MD-22 #03259 www.atel.com.pl/produkt.php?hash=03259 wersja 1.1 Wstęp Detektor metali i przewodów pod napięciem słuŝy
Laboratorium z biofizyki
 Laboratorium z biofizyki Regulamin Studenci są dopuszczeni do wykonywania ćwiczenia jeżeli posiadają: Buty na płaskim obcasie, Fartuchy, Rękawiczki bezpudrowe, Zeszyt 16-kartkowy. Zeszyt laboratoryjny
Laboratorium z biofizyki Regulamin Studenci są dopuszczeni do wykonywania ćwiczenia jeżeli posiadają: Buty na płaskim obcasie, Fartuchy, Rękawiczki bezpudrowe, Zeszyt 16-kartkowy. Zeszyt laboratoryjny
1. PRZYGOTOWANIE ROZTWORÓW KOMPLEKSUJĄCYCH
 1. PRZYGOTOWANIE ROZTWORÓW KOMPLEKSUJĄCYCH 1.1. przygotowanie 20 g 20% roztworu KSCN w wodzie destylowanej 1.1.1. odważenie 4 g stałego KSCN w stożkowej kolbie ze szlifem 1.1.2. odważenie 16 g wody destylowanej
1. PRZYGOTOWANIE ROZTWORÓW KOMPLEKSUJĄCYCH 1.1. przygotowanie 20 g 20% roztworu KSCN w wodzie destylowanej 1.1.1. odważenie 4 g stałego KSCN w stożkowej kolbie ze szlifem 1.1.2. odważenie 16 g wody destylowanej
Ćwiczenie: Wyznaczenie dokładności i precyzji pomiaru pipety automatycznej
 Zakład Chemii Oólnej i Analitycznej Ćwiczenie: Wyznaczenie dokładności i precyzji pomiaru pipety automatycznej Sprawdzenie dokładności i precyzji odmierzania objętości za pomocą pipet automatycznych polea
Zakład Chemii Oólnej i Analitycznej Ćwiczenie: Wyznaczenie dokładności i precyzji pomiaru pipety automatycznej Sprawdzenie dokładności i precyzji odmierzania objętości za pomocą pipet automatycznych polea
Pytania i odpowiedzi
 Znak sprawy: DZP 380 6/2013 Pytania i odpowiedzi dotyczące postępowania o udzielenie zamówienia publicznego na dostawę odczynników, krwi kontrolnej oraz niezbędnych akcesoriów do wykonania morfologii 5-DIFF
Znak sprawy: DZP 380 6/2013 Pytania i odpowiedzi dotyczące postępowania o udzielenie zamówienia publicznego na dostawę odczynników, krwi kontrolnej oraz niezbędnych akcesoriów do wykonania morfologii 5-DIFF
KLASYFIKACJI I BUDOWY STATKÓW MORSKICH
 PRZEPISY KLASYFIKACJI I BUDOWY STATKÓW MORSKICH ZMIANY NR 3/2012 do CZĘŚCI IX MATERIAŁY I SPAWANIE 2008 GDAŃSK Zmiany Nr 3/2012 do Części IX Materiały i spawanie 2008, Przepisów klasyfikacji i budowy statków
PRZEPISY KLASYFIKACJI I BUDOWY STATKÓW MORSKICH ZMIANY NR 3/2012 do CZĘŚCI IX MATERIAŁY I SPAWANIE 2008 GDAŃSK Zmiany Nr 3/2012 do Części IX Materiały i spawanie 2008, Przepisów klasyfikacji i budowy statków
Instrukcja ogólna dotycząca postępowania z substancjami niebezpiecznymi
 DOKUMENTACJA ZINTEGROWANEGO SYSTEMU ZARZĄDZANIA OPERATORA GAZOCIĄGÓW PRZESYŁOWYCH GAZ-SYSTEM S.A. Instrukcja ogólna dotycząca postępowania z substancjami niebezpiecznymi Opracował: Zespół ds. Zintegrowanego
DOKUMENTACJA ZINTEGROWANEGO SYSTEMU ZARZĄDZANIA OPERATORA GAZOCIĄGÓW PRZESYŁOWYCH GAZ-SYSTEM S.A. Instrukcja ogólna dotycząca postępowania z substancjami niebezpiecznymi Opracował: Zespół ds. Zintegrowanego
ALGALTOXKIT F Procedura testu
 ALGALTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI A B C D - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI POŻYWEK A (2 fiolki), B, C, D - DESTYLOWANA (lub dejonizowana) WODA 2 A PRZENIEŚĆ
ALGALTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI A B C D - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI POŻYWEK A (2 fiolki), B, C, D - DESTYLOWANA (lub dejonizowana) WODA 2 A PRZENIEŚĆ
POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI. Ćwiczenie 3 ANALIZA TRANSPORTU SUBSTANCJI NISKOCZĄSTECZKOWYCH PRZEZ
 POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 3 ANALIZA TRANSPORTU SUBSTANCJI NISKOCZĄSTECZKOWYCH PRZEZ BŁONĘ KOMÓRKOWĄ I. WSTĘP TEORETYCZNY Każda komórka, zarówno roślinna,
POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 3 ANALIZA TRANSPORTU SUBSTANCJI NISKOCZĄSTECZKOWYCH PRZEZ BŁONĘ KOMÓRKOWĄ I. WSTĘP TEORETYCZNY Każda komórka, zarówno roślinna,
Cyfrowy miernik temperatury
 Cyfrowy miernik temperatury MS6502 INSTRUKCJA OBSŁUGI wersja 1.0 SPIS TREŚCI Wstęp... 3 Bezpieczeństwo uŝytkowania... 3 1. Zawartość opakowania... 3 2. Zasady bezpieczeństwa... 3 3. Środowisko pracy...
Cyfrowy miernik temperatury MS6502 INSTRUKCJA OBSŁUGI wersja 1.0 SPIS TREŚCI Wstęp... 3 Bezpieczeństwo uŝytkowania... 3 1. Zawartość opakowania... 3 2. Zasady bezpieczeństwa... 3 3. Środowisko pracy...
Immunologia komórkowa
 Immunologia komórkowa ocena immunofenotypu komórek Mariusz Kaczmarek Immunofenotyp Definicja I Charakterystyczny zbiór antygenów stanowiących elementy różnych struktur komórki, związany z jej różnicowaniem,
Immunologia komórkowa ocena immunofenotypu komórek Mariusz Kaczmarek Immunofenotyp Definicja I Charakterystyczny zbiór antygenów stanowiących elementy różnych struktur komórki, związany z jej różnicowaniem,
Wprowadzenie do cytometrii przepływowej: metody znakowania komórek
 Fakultet: Cytometria zastosowanie w badaniach biologicznych Wprowadzenie do cytometrii przepływowej: metody znakowania komórek Nadzieja Drela Zakład Immunologii WB UW ndrela@biol.uw.edu.pl Przygotowanie
Fakultet: Cytometria zastosowanie w badaniach biologicznych Wprowadzenie do cytometrii przepływowej: metody znakowania komórek Nadzieja Drela Zakład Immunologii WB UW ndrela@biol.uw.edu.pl Przygotowanie
Ulotka dołączona do opakowania: informacja dla użytkownika. Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych
 Ulotka dołączona do opakowania: informacja dla użytkownika Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
INSTRUKCJA OBSŁUGI MIERNIK MOCY OPTYCZNEJ KINGFISHER
 INSTRUKCJA OBSŁUGI MIERNIK MOCY OPTYCZNEJ KINGFISHER KI3600-Ge KI3600-InGaAS KI3600-Si #04158 #04141 #04160 www.atel.com.pl/produkt.php?hash=04158 wersja 1.0 Wstęp Niedrogi miernik mocy optycznej KI3600-Ge
INSTRUKCJA OBSŁUGI MIERNIK MOCY OPTYCZNEJ KINGFISHER KI3600-Ge KI3600-InGaAS KI3600-Si #04158 #04141 #04160 www.atel.com.pl/produkt.php?hash=04158 wersja 1.0 Wstęp Niedrogi miernik mocy optycznej KI3600-Ge
9.5 Rozliczanie zaopatrzenia w przedmioty ortopedyczne i środki pomocnicze
 Po zakończeniu prac z listą raportów zwrotnych naleŝy kliknąć w przycisk opcji Powrót do listy raportów. Opcja ta spowoduje przywrócenie głównego okna obszaru Sprawozdawczość. 9.5 Rozliczanie zaopatrzenia
Po zakończeniu prac z listą raportów zwrotnych naleŝy kliknąć w przycisk opcji Powrót do listy raportów. Opcja ta spowoduje przywrócenie głównego okna obszaru Sprawozdawczość. 9.5 Rozliczanie zaopatrzenia
Opis przedmiotu zamówienia wraz z wymaganiami technicznymi i zestawieniem parametrów
 Załącznik nr 1 do SIWZ Nazwa i adres Wykonawcy Opis przedmiotu zamówienia wraz z wymaganiami technicznymi i zestawieniem parametrów Przedmiot zamówienia; automatyczny system do diagnostyki molekularnej:
Załącznik nr 1 do SIWZ Nazwa i adres Wykonawcy Opis przedmiotu zamówienia wraz z wymaganiami technicznymi i zestawieniem parametrów Przedmiot zamówienia; automatyczny system do diagnostyki molekularnej:
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
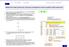 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
Zestaw do wykrywania Chlamydia trachomatis w moczu lub w kulturach komórkowych
 Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
RT31-020, RT , MgCl 2. , random heksamerów X 6
 RT31-020, RT31-100 RT31-020, RT31-100 Zestaw TRANSCRIPTME RNA zawiera wszystkie niezbędne składniki do przeprowadzenia syntezy pierwszej nici cdna na matrycy mrna lub całkowitego RNA. Uzyskany jednoniciowy
RT31-020, RT31-100 RT31-020, RT31-100 Zestaw TRANSCRIPTME RNA zawiera wszystkie niezbędne składniki do przeprowadzenia syntezy pierwszej nici cdna na matrycy mrna lub całkowitego RNA. Uzyskany jednoniciowy
Podstawowe informacje o obsłudze pliku z uprawnieniami licencja.txt
 Podstawowe informacje o obsłudze pliku z uprawnieniami licencja.txt W artykule znajdują się odpowiedzi na najczęściej zadawane pytania związane z plikiem licencja.txt : 1. Jak zapisać plik licencja.txt
Podstawowe informacje o obsłudze pliku z uprawnieniami licencja.txt W artykule znajdują się odpowiedzi na najczęściej zadawane pytania związane z plikiem licencja.txt : 1. Jak zapisać plik licencja.txt
Acusera 24.7 - zarządzanie wynikami kontroli wewnątrzlaboratoryjnej
 Acusera 24.7 - zarządzanie wynikami kontroli wewnątrzlaboratoryjnej II Konferencja Diagnostów Laboratoryjnych Śląski Urząd Wojewódzki w Katowicach 14 września 2015 Acusera 24. 7 - główne funkcje: 1.Prowadzenie
Acusera 24.7 - zarządzanie wynikami kontroli wewnątrzlaboratoryjnej II Konferencja Diagnostów Laboratoryjnych Śląski Urząd Wojewódzki w Katowicach 14 września 2015 Acusera 24. 7 - główne funkcje: 1.Prowadzenie
INSTRUKCJA OBSŁUGI ULTRADŹWIĘKOWY MIERNIK ODLEGŁOŚCI Z WSKAŹNIKIEM LASEROWYM MDM 201 # wersja 1.2
 INSTRUKCJA OBSŁUGI ULTRADŹWIĘKOWY MIERNIK ODLEGŁOŚCI Z WSKAŹNIKIEM LASEROWYM MDM 201 #03941 wersja 1.2 Wstęp Ultradźwiękowy miernik odległości jest to urządzenie umoŝliwiające uŝytkownikowi łatwe dokonanie
INSTRUKCJA OBSŁUGI ULTRADŹWIĘKOWY MIERNIK ODLEGŁOŚCI Z WSKAŹNIKIEM LASEROWYM MDM 201 #03941 wersja 1.2 Wstęp Ultradźwiękowy miernik odległości jest to urządzenie umoŝliwiające uŝytkownikowi łatwe dokonanie
Pobieranie próbek owoców
 Strona 1 z 5 1. Cel i zakres: Pobieranie próbek owoców Celem procedury jest określenie zasad pobierania próbek owoców. Procedura obowiązuje wszystkie osoby odpowiedzialne za wykonywanie tej czynności.
Strona 1 z 5 1. Cel i zakres: Pobieranie próbek owoców Celem procedury jest określenie zasad pobierania próbek owoców. Procedura obowiązuje wszystkie osoby odpowiedzialne za wykonywanie tej czynności.
Program DSA Monitor - funkcje
 Program DSA Monitor - funkcje Program DSA Monitor przeznaczony jest do wczytania i obróbki danych pomiarowych pochodzących z mierników poziomu dźwięku produkcji SONOPAN (DSA-50, DLM-101/102, DD-40/41),
Program DSA Monitor - funkcje Program DSA Monitor przeznaczony jest do wczytania i obróbki danych pomiarowych pochodzących z mierników poziomu dźwięku produkcji SONOPAN (DSA-50, DLM-101/102, DD-40/41),
ODPORNOŚĆ KOROZYJNA STALI 316L W PŁYNACH USTROJOWYCH CZŁOWIEKA
 WyŜsza Szkoła InŜynierii Dentystycznej im. prof. Meissnera w Ustroniu ODPORNOŚĆ KOROZYJNA STALI 316L W PŁYNACH USTROJOWYCH CZŁOWIEKA Magdalena Puda Promotor: Dr inŝ. Jacek Grzegorz Chęcmanowski Cel pracy
WyŜsza Szkoła InŜynierii Dentystycznej im. prof. Meissnera w Ustroniu ODPORNOŚĆ KOROZYJNA STALI 316L W PŁYNACH USTROJOWYCH CZŁOWIEKA Magdalena Puda Promotor: Dr inŝ. Jacek Grzegorz Chęcmanowski Cel pracy
K1. KONDUKTOMETRYCZNE MIARECZKOWANIE STRĄCENIOWE I KOMPLEKSOMETRYCZNE
 K1. KONDUKTOMETRYCZNE MIARECZKOWANIE STRĄCENIOWE I KOMPLEKSOMETRYCZNE Postępowanie analityczne, znane pod nazwą miareczkowania konduktometrycznego, polega na wyznaczeniu punktu końcowego miareczkowania
K1. KONDUKTOMETRYCZNE MIARECZKOWANIE STRĄCENIOWE I KOMPLEKSOMETRYCZNE Postępowanie analityczne, znane pod nazwą miareczkowania konduktometrycznego, polega na wyznaczeniu punktu końcowego miareczkowania
Laboratorium Podstaw Biofizyki
 CEL ĆWICZENIA Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu oraz wyznaczenie równania izotermy Freundlicha. ZAKRES WYMAGANYCH WIADOMOŚCI I UMIEJĘTNOŚCI: widmo absorpcyjne, prawo Lamberta-Beera,
CEL ĆWICZENIA Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu oraz wyznaczenie równania izotermy Freundlicha. ZAKRES WYMAGANYCH WIADOMOŚCI I UMIEJĘTNOŚCI: widmo absorpcyjne, prawo Lamberta-Beera,
Instrukcja uŝycia wyrobu medycznego. GASPERTIN WZDĘCIA 40 mg, kapsułki (Symetykon)
 Instrukcja uŝycia wyrobu medycznego NaleŜy przeczytać uwaŝnie całą instrukcję, poniewaŝ zawiera ona waŝne informacje. Niniejszy wyrób medyczny jest dostępny bez recepty. W celu uzyskania optymalnych rezultatów
Instrukcja uŝycia wyrobu medycznego NaleŜy przeczytać uwaŝnie całą instrukcję, poniewaŝ zawiera ona waŝne informacje. Niniejszy wyrób medyczny jest dostępny bez recepty. W celu uzyskania optymalnych rezultatów
Kontrola owoców na zawartość środków chemicznych
 Strona 1 z 5 1. Cel i zakres: Celem procedury jest określenie zasad kontroli owoców na zawartość. Procedura obowiązuje wszystkie osoby objęte szkoleniem z zakresu higieny pracy z Ŝywnością oraz osoby odpowiedzialne
Strona 1 z 5 1. Cel i zakres: Celem procedury jest określenie zasad kontroli owoców na zawartość. Procedura obowiązuje wszystkie osoby objęte szkoleniem z zakresu higieny pracy z Ŝywnością oraz osoby odpowiedzialne
THAMNOTOXKIT F Procedura testu
 THAMNOTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 LITR) - 5 FIOLEK ZE SKONCENTROWANYMI ROZTWORAMI SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 WLAĆ ZAWARTOŚĆ 5 FIOLEK
THAMNOTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 LITR) - 5 FIOLEK ZE SKONCENTROWANYMI ROZTWORAMI SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 WLAĆ ZAWARTOŚĆ 5 FIOLEK
AmpliTest GMO screening-nos (Real Time PCR)
 AmpliTest GMO screening-nos (Real Time PCR) Zestaw do wykrywania sekwencji DNA terminatora NOS techniką Real Time PCR Nr kat.: GMO03-50 GMO03-100 Wielkość zestawu: 50 reakcji 100 reakcji Objętość pojedynczej
AmpliTest GMO screening-nos (Real Time PCR) Zestaw do wykrywania sekwencji DNA terminatora NOS techniką Real Time PCR Nr kat.: GMO03-50 GMO03-100 Wielkość zestawu: 50 reakcji 100 reakcji Objętość pojedynczej
Załącznik nr 19. Postępowanie z odpadami medycznymi i weterynaryjnymi
 Załącznik nr 19 Postępowanie z odpadami medycznymi i weterynaryjnymi Styczeń 2008 Spis Treści 1 Postępowanie z odpadami medycznymi i weterynaryjnymi w miejscu ich powstania... 3 1.1 Identyfikacja i klasyfikowanie
Załącznik nr 19 Postępowanie z odpadami medycznymi i weterynaryjnymi Styczeń 2008 Spis Treści 1 Postępowanie z odpadami medycznymi i weterynaryjnymi w miejscu ich powstania... 3 1.1 Identyfikacja i klasyfikowanie
Badania mikrobiologiczne wg PN-EN ISO 11737
 Badania mikrobiologiczne wg PN-EN ISO 11737 mgr Agnieszka Wąsowska Specjalistyczne Laboratorium Badawcze ITA-TEST Z-ca Dyrektora ds. Badań Kierownik Zespołu Badań Mikrobiologicznych i Chemicznych Tel.022
Badania mikrobiologiczne wg PN-EN ISO 11737 mgr Agnieszka Wąsowska Specjalistyczne Laboratorium Badawcze ITA-TEST Z-ca Dyrektora ds. Badań Kierownik Zespołu Badań Mikrobiologicznych i Chemicznych Tel.022
WYZNACZANIE STAŁEJ DYSOCJACJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII ABSORPCYJNEJ
 Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
Laboratorium Wirusologiczne
 Laboratorium Wirusologiczne Krzysztof Pyrd Pracownia wirusologiczna: Powstanie i wyposażenie całkowicie nowego laboratorium w ramach Zakładu Mikrobiologii WBBiB Profil: laboratorium molekularno-komórkowe
Laboratorium Wirusologiczne Krzysztof Pyrd Pracownia wirusologiczna: Powstanie i wyposażenie całkowicie nowego laboratorium w ramach Zakładu Mikrobiologii WBBiB Profil: laboratorium molekularno-komórkowe
INSTRUKCJA OBSŁUGI DETEKTOR WIELOFUNKCYJNY METEK
 INSTRUKCJA OBSŁUGI DETEKTOR WIELOFUNKCYJNY METEK MMD-233 #03944 wersja 1.1 Wstęp Detektor wielofunkcyjny MMD-233 jest urządzeniem przeznaczonym do wykrywania metali, przewodów pod napięciem oraz zmiany
INSTRUKCJA OBSŁUGI DETEKTOR WIELOFUNKCYJNY METEK MMD-233 #03944 wersja 1.1 Wstęp Detektor wielofunkcyjny MMD-233 jest urządzeniem przeznaczonym do wykrywania metali, przewodów pod napięciem oraz zmiany
WPŁYW ILOŚCI MODYFIKATORA NA WSPÓŁCZYNNIK RETENCJI W TECHNICE WYSOKOSPRAWNEJ CHROMATOGRAFII CIECZOWEJ
 WPŁYW ILOŚCI MODYFIKATORA NA WSPÓŁCZYNNIK RETENCJI W TECHNICE WYSOKOSPRAWNEJ CHROMATOGRAFII CIECZOWEJ Wprowadzenie Wysokosprawna chromatografia cieczowa (HPLC) jest uniwersalną technika analityczną, stosowaną
WPŁYW ILOŚCI MODYFIKATORA NA WSPÓŁCZYNNIK RETENCJI W TECHNICE WYSOKOSPRAWNEJ CHROMATOGRAFII CIECZOWEJ Wprowadzenie Wysokosprawna chromatografia cieczowa (HPLC) jest uniwersalną technika analityczną, stosowaną
Wpływ ilości modyfikatora na współczynnik retencji w technice wysokosprawnej chromatografii cieczowej
 Wpływ ilości modyfikatora na współczynnik retencji w technice wysokosprawnej chromatografii cieczowej WPROWADZENIE Wysokosprawna chromatografia cieczowa (HPLC) jest uniwersalną techniką analityczną, stosowaną
Wpływ ilości modyfikatora na współczynnik retencji w technice wysokosprawnej chromatografii cieczowej WPROWADZENIE Wysokosprawna chromatografia cieczowa (HPLC) jest uniwersalną techniką analityczną, stosowaną
III zasada dynamiki Newtona
 6COACH 34 III zasada dynamiki Newtona Program: Coach 6 Projekt: na ZMN060c CMA Coach Projects\PTSN Coach 6\ III_zasada_dynamiki\Zestaw.cma Przykład wyników: Zestaw-wyniki.cmr Cel ćwiczenia - Doświadczalna
6COACH 34 III zasada dynamiki Newtona Program: Coach 6 Projekt: na ZMN060c CMA Coach Projects\PTSN Coach 6\ III_zasada_dynamiki\Zestaw.cma Przykład wyników: Zestaw-wyniki.cmr Cel ćwiczenia - Doświadczalna
ĆWICZENIE 4. Oczyszczanie ścieków ze związków fosforu
 ĆWICZENIE 4 Oczyszczanie ścieków ze związków fosforu 1. Wprowadzenie Zbyt wysokie stężenia fosforu w wodach powierzchniowych stojących, spiętrzonych lub wolno płynących prowadzą do zwiększonego przyrostu
ĆWICZENIE 4 Oczyszczanie ścieków ze związków fosforu 1. Wprowadzenie Zbyt wysokie stężenia fosforu w wodach powierzchniowych stojących, spiętrzonych lub wolno płynących prowadzą do zwiększonego przyrostu
PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika
 PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika Spis treści 1. Zawartość 2 1.1 Składniki zestawu 2 2. Opis produktu 2 2.1 Założenia metody 2 2.2 Instrukcja 2 2.3 Specyfikacja
PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika Spis treści 1. Zawartość 2 1.1 Składniki zestawu 2 2. Opis produktu 2 2.1 Założenia metody 2 2.2 Instrukcja 2 2.3 Specyfikacja
CZUJNIK POGODOWY WIATROWY CZUJNIK POGODOWY WIATROWO-SŁONECZNY KOMUNIKACJA POPRZEZ RADIO. WindTec WindTec Lux MODELE INSTRUKCJA
 CZUJNIK POGODOWY WIATROWY CZUJNIK POGODOWY WIATROWO-SŁONECZNY KOMUNIKACJA POPRZEZ RADIO MODELE WindTec WindTec Lux INSTRUKCJA Instrukcja dotyczy dwóch typów czujników pogodowych: - WindTec: czujnik wiatru
CZUJNIK POGODOWY WIATROWY CZUJNIK POGODOWY WIATROWO-SŁONECZNY KOMUNIKACJA POPRZEZ RADIO MODELE WindTec WindTec Lux INSTRUKCJA Instrukcja dotyczy dwóch typów czujników pogodowych: - WindTec: czujnik wiatru
Podstawy obsługi aplikacji Generator Wniosków Płatniczych
 Podstawy obsługi aplikacji Generator Wniosków Płatniczych 1. Instalacja programu Program naleŝy pobrać ze strony www.simik.gov.pl. Instalację naleŝy wykonań z konta posiadającego uprawnienia administratora
Podstawy obsługi aplikacji Generator Wniosków Płatniczych 1. Instalacja programu Program naleŝy pobrać ze strony www.simik.gov.pl. Instalację naleŝy wykonań z konta posiadającego uprawnienia administratora
Wprowadzenie do cytometrii przepływowej: metody znakowania komórek
 Fakultet: Cytometria zastosowanie w badaniach biologicznych Wprowadzenie do cytometrii przepływowej: metody znakowania komórek Nadzieja Drela Zakład Immunologii WB UW ndrela@biol.uw.edu.pl Przygotowanie
Fakultet: Cytometria zastosowanie w badaniach biologicznych Wprowadzenie do cytometrii przepływowej: metody znakowania komórek Nadzieja Drela Zakład Immunologii WB UW ndrela@biol.uw.edu.pl Przygotowanie
Instalacja. Jak skonfigurować Twój e-podpis?
 Page 1 of 7 Instalacja Jak skonfigurować Twój e-podpis? Jak aktywować Twoją kartę i jak uŝywać e-podpisu? JeŜeli odebrałeś juŝ przesyłkę (krok1) zawierającą zestaw Certum i chcesz juŝ teraz uŝywać Twojego
Page 1 of 7 Instalacja Jak skonfigurować Twój e-podpis? Jak aktywować Twoją kartę i jak uŝywać e-podpisu? JeŜeli odebrałeś juŝ przesyłkę (krok1) zawierającą zestaw Certum i chcesz juŝ teraz uŝywać Twojego
SKUTECZNOŚĆ IZOLACJI JAK ZMIERZYĆ ILOŚĆ KWASÓW NUKLEINOWYCH PO IZOLACJI? JAK ZMIERZYĆ ILOŚĆ KWASÓW NUKLEINOWYCH PO IZOLACJI?
 SKUTECZNOŚĆ IZOLACJI Wydajność izolacji- ilość otrzymanego kwasu nukleinowego Efektywność izolacji- jakość otrzymanego kwasu nukleinowego w stosunku do ilości Powtarzalność izolacji- zoptymalizowanie procedury
SKUTECZNOŚĆ IZOLACJI Wydajność izolacji- ilość otrzymanego kwasu nukleinowego Efektywność izolacji- jakość otrzymanego kwasu nukleinowego w stosunku do ilości Powtarzalność izolacji- zoptymalizowanie procedury
Cyfrowy miernik temperatury
 Cyfrowy miernik temperatury MS6500 MS6501 #04010 #04011 INSTRUKCJA OBSŁUGI wersja 1.0 MS6500/MS6501 SPIS TREŚCI Wstęp... 3 Bezpieczeństwo uŝytkowania... 3 1. Zawartość opakowania... 3 2. Zasady bezpieczeństwa...
Cyfrowy miernik temperatury MS6500 MS6501 #04010 #04011 INSTRUKCJA OBSŁUGI wersja 1.0 MS6500/MS6501 SPIS TREŚCI Wstęp... 3 Bezpieczeństwo uŝytkowania... 3 1. Zawartość opakowania... 3 2. Zasady bezpieczeństwa...
Multimetr cyfrowy MAS-345. Instrukcja instalacji i obsługi oprogramowania DMM VIEW Ver 2.0
 Multimetr cyfrowy MAS-345 Instrukcja instalacji i obsługi oprogramowania DMM VIEW Ver 2.0 Do urządzenia MAS-345 została dołączona płyta CD zawierająca oprogramowanie DMM VIEW 2.0, dzięki któremu moŝliwa
Multimetr cyfrowy MAS-345 Instrukcja instalacji i obsługi oprogramowania DMM VIEW Ver 2.0 Do urządzenia MAS-345 została dołączona płyta CD zawierająca oprogramowanie DMM VIEW 2.0, dzięki któremu moŝliwa
OSTRACODTOXKIT F Procedura testu
 OSTRACODTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI SKONCENTROWANYCH SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 PRZELAĆ ZAWARTOŚĆ 5 FIOLEK
OSTRACODTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI SKONCENTROWANYCH SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 PRZELAĆ ZAWARTOŚĆ 5 FIOLEK
Dotyczy zamówienia publicznego ogłoszonego w trybie przetargu nieograniczonego pod nazwą: Dostawa systemów do pozyskiwania osocza bogatopłytkowego
 Piekary Śląskie 28.12.2016 r. Samodzielny Publiczny Wojewódzki Szpital Chirurgii Urazowej im. Dr. Janusza Daaba w Piekarach Śląskich ul. Bytomska 62 41-940 Piekary Śląskie Sekcja d/s zamówień publicznych
Piekary Śląskie 28.12.2016 r. Samodzielny Publiczny Wojewódzki Szpital Chirurgii Urazowej im. Dr. Janusza Daaba w Piekarach Śląskich ul. Bytomska 62 41-940 Piekary Śląskie Sekcja d/s zamówień publicznych
1. Opis. 2. Wymagania sprzętowe:
 1. Opis Aplikacja ARSOFT-WZ2 umożliwia konfigurację, wizualizację i rejestrację danych pomiarowych urządzeń produkcji APAR wyposażonych w interfejs komunikacyjny RS232/485 oraz protokół MODBUS-RTU. Aktualny
1. Opis Aplikacja ARSOFT-WZ2 umożliwia konfigurację, wizualizację i rejestrację danych pomiarowych urządzeń produkcji APAR wyposażonych w interfejs komunikacyjny RS232/485 oraz protokół MODBUS-RTU. Aktualny
KaŜdy z formularzy naleŝy podpiąć do usługi. Nazwa usługi moŝe pokrywać się z nazwą formularza, nie jest to jednak konieczne.
 Dodawanie i poprawa wzorców formularza i wydruku moŝliwa jest przez osoby mające nadane odpowiednie uprawnienia w module Amin (Bazy/ Wzorce formularzy i Bazy/ Wzorce wydruków). Wzorce formularzy i wydruków
Dodawanie i poprawa wzorców formularza i wydruku moŝliwa jest przez osoby mające nadane odpowiednie uprawnienia w module Amin (Bazy/ Wzorce formularzy i Bazy/ Wzorce wydruków). Wzorce formularzy i wydruków
Zestaw do wykrywania Babesia spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych
 Nr kat. PK25N Wersja zestawu: 1.2012 Zestaw do wykrywania spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Zestaw
Nr kat. PK25N Wersja zestawu: 1.2012 Zestaw do wykrywania spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Zestaw
Wprowadzenie. Radio Track 2005 za pomocą oprogramowania. Soft Report Explorer. do analizy danych z badania
 Wprowadzenie do analizy danych z badania Radio Track 2005 za pomocą oprogramowania Soft Report Explorer SMG/KRC Poland Media S.A. Ul. Nowoursynowska 154a 02-797 Warszawa Tel 52 52 000 Fax 54 52 100 www.smgkrc.pl
Wprowadzenie do analizy danych z badania Radio Track 2005 za pomocą oprogramowania Soft Report Explorer SMG/KRC Poland Media S.A. Ul. Nowoursynowska 154a 02-797 Warszawa Tel 52 52 000 Fax 54 52 100 www.smgkrc.pl
Wykresy statystyczne w PyroSim, jako narzędzie do prezentacji i weryfikacji symulacji scenariuszy pożarowych
 Wykresy statystyczne w PyroSim, jako narzędzie do prezentacji i weryfikacji symulacji scenariuszy pożarowych 1. Wstęp: Program PyroSim posiada wiele narzędzi służących do prezentacji i weryfikacji wyników
Wykresy statystyczne w PyroSim, jako narzędzie do prezentacji i weryfikacji symulacji scenariuszy pożarowych 1. Wstęp: Program PyroSim posiada wiele narzędzi służących do prezentacji i weryfikacji wyników
Przykłady analizy płynów z jam ciała na analizatorze XE-5000
 Przykłady analizy płynów z jam ciała na analizatorze XE-5000 Jeśli pacjent ma być leczony szybko i skutecznie, laboratorium musi w krótkim czasie dostarczać wiarygodnych wyników, o ile to możliwe przez
Przykłady analizy płynów z jam ciała na analizatorze XE-5000 Jeśli pacjent ma być leczony szybko i skutecznie, laboratorium musi w krótkim czasie dostarczać wiarygodnych wyników, o ile to możliwe przez
Genomic Mini AX Plant Spin
 Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
QMS Quality in Microbiology Scheme Wydanie 14 Data wydania: czerwiec 2018
 Przyjęcie i przechowywanie Po otrzymaniu materiału do badań należy zapisać datę otrzymania, a następnie przechowywać w lodówce w temperaturze 2-8 º C do momentu przeprowadzenia badania. Materiał do badań
Przyjęcie i przechowywanie Po otrzymaniu materiału do badań należy zapisać datę otrzymania, a następnie przechowywać w lodówce w temperaturze 2-8 º C do momentu przeprowadzenia badania. Materiał do badań
MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ
 MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ Puławy 2013 Opracowanie: Prof. dr hab. Iwona Markowska-Daniel, mgr inż. Kinga Urbaniak,
MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ Puławy 2013 Opracowanie: Prof. dr hab. Iwona Markowska-Daniel, mgr inż. Kinga Urbaniak,
INSTRUKCJA UŻYTKOWANIA
 INSTRUKCJA UŻYTKOWANIA Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny Epower zawiera liofilizowane, standaryzowane ilościowo preparaty mikroorganizmów, które
INSTRUKCJA UŻYTKOWANIA Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny Epower zawiera liofilizowane, standaryzowane ilościowo preparaty mikroorganizmów, które
Zestaw do wykrywania Anaplasma phagocytophilum w kleszczach, krwi i hodowlach komórkowych
 Nr kat. PK24N Wersja zestawu: 1.2016 Zestaw do wykrywania phagocytophilum w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Detekcja
Nr kat. PK24N Wersja zestawu: 1.2016 Zestaw do wykrywania phagocytophilum w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Detekcja
X Y 4,0 3,3 8,0 6,8 12,0 11,0 16,0 15,2 20,0 18,9
 Zadanie W celu sprawdzenia, czy pipeta jest obarczona błędem systematycznym stałym lub zmiennym wykonano szereg pomiarów przy różnych ustawieniach pipety. Wyznacz równanie regresji liniowej, które pozwoli
Zadanie W celu sprawdzenia, czy pipeta jest obarczona błędem systematycznym stałym lub zmiennym wykonano szereg pomiarów przy różnych ustawieniach pipety. Wyznacz równanie regresji liniowej, które pozwoli
INSTRUKCJA STOSOWANIA
 Strona 1 z 6 INSTRUKCJA STOSOWANIA Zawiesiny pasożytów w formalinie PRZEZNACZENIE Zawiesiny pasożytów oferowane przez Microbiologics przeznaczone są do programów zapewnienia jakości tam, gdzie do przeprowadzenia
Strona 1 z 6 INSTRUKCJA STOSOWANIA Zawiesiny pasożytów w formalinie PRZEZNACZENIE Zawiesiny pasożytów oferowane przez Microbiologics przeznaczone są do programów zapewnienia jakości tam, gdzie do przeprowadzenia
Cytology FISH Accessory Kit Nr kat. K 5499
 Cytology FISH Accessory Kit Nr kat. K 5499 Wydanie 2 Do fluorescencyjnej hybrydyzacji in situ (FISH) na próbce cytologicznej. Zestaw zawiera odczynniki wystarczające do wykonania 20 badań. Spis treści
Cytology FISH Accessory Kit Nr kat. K 5499 Wydanie 2 Do fluorescencyjnej hybrydyzacji in situ (FISH) na próbce cytologicznej. Zestaw zawiera odczynniki wystarczające do wykonania 20 badań. Spis treści
Kaucje na opakowania po środkach niebezpiecznych - teoria i praktyka Ŝycia gospodarczego
 Kaucje na opakowania po środkach niebezpiecznych - teoria i praktyka Ŝycia gospodarczego Włodzimierz URBANIAK Wydział Chemii UAM, Poznań Wydział Technologii i InŜynierii Chemicznej UTP, Bydgoszcz Środki
Kaucje na opakowania po środkach niebezpiecznych - teoria i praktyka Ŝycia gospodarczego Włodzimierz URBANIAK Wydział Chemii UAM, Poznań Wydział Technologii i InŜynierii Chemicznej UTP, Bydgoszcz Środki
JAK ZMIERZYĆ ILOŚĆ KWASÓW NUKLEINOWYCH PO IZOLACJI? JAK ZMIERZYĆ ILOŚĆ KWASÓW NUKLEINOWYCH PO IZOLACJI?
 Podstawowe miary masy i objętości stosowane przy oznaczaniu ilości kwasów nukleinowych : 1g (1) 1l (1) 1mg (1g x 10-3 ) 1ml (1l x 10-3 ) 1μg (1g x 10-6 ) 1μl (1l x 10-6 ) 1ng (1g x 10-9 ) 1pg (1g x 10-12
Podstawowe miary masy i objętości stosowane przy oznaczaniu ilości kwasów nukleinowych : 1g (1) 1l (1) 1mg (1g x 10-3 ) 1ml (1l x 10-3 ) 1μg (1g x 10-6 ) 1μl (1l x 10-6 ) 1ng (1g x 10-9 ) 1pg (1g x 10-12
KONSMETAL Zamek elektroniczny NT C496-L250 (RAPTOR)
 KONSMETAL Zamek elektroniczny NT C496-L250 (RAPTOR) Instrukcja obsługi Podstawowe cechy zamka: 1 kod główny (Master) moŝliwość zdefiniowania do 8 kodów uŝytkowników długość kodu otwarcia: 6 cyfr długość
KONSMETAL Zamek elektroniczny NT C496-L250 (RAPTOR) Instrukcja obsługi Podstawowe cechy zamka: 1 kod główny (Master) moŝliwość zdefiniowania do 8 kodów uŝytkowników długość kodu otwarcia: 6 cyfr długość
Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności
 Załącznik nr 4 Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności 1. Zakres i obszar stosowania Metoda służy do urzędowej kontroli zawartości chlorku winylu uwalnianego
Załącznik nr 4 Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności 1. Zakres i obszar stosowania Metoda służy do urzędowej kontroli zawartości chlorku winylu uwalnianego
Miernik poziomu oświetlenia
 Miernik poziomu oświetlenia MS6610 #04013 INSTRUKCJA OBSŁUGI wersja 1.1 VA6610 SPIS TREŚCI Wstęp... 3 Bezpieczeństwo uŝytkowania... 3 1. Zawartość opakowania... 3 2. Zasady bezpieczeństwa... 3 3. Środowisko
Miernik poziomu oświetlenia MS6610 #04013 INSTRUKCJA OBSŁUGI wersja 1.1 VA6610 SPIS TREŚCI Wstęp... 3 Bezpieczeństwo uŝytkowania... 3 1. Zawartość opakowania... 3 2. Zasady bezpieczeństwa... 3 3. Środowisko
9.5 Rozliczanie zaopatrzenia w przedmioty ortopedyczne i środki pomocnicze
 Fragment instrukcji obsługi systemu SZOI przygotowanej przez P.I. Kamsoft - 09.02.2009 r. 9.5 Rozliczanie zaopatrzenia w przedmioty ortopedyczne i środki pomocnicze Obszar Sprawozdawczość/Zaopatrzenie
Fragment instrukcji obsługi systemu SZOI przygotowanej przez P.I. Kamsoft - 09.02.2009 r. 9.5 Rozliczanie zaopatrzenia w przedmioty ortopedyczne i środki pomocnicze Obszar Sprawozdawczość/Zaopatrzenie
OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE
 OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE WPROWADZENIE Przyswajalność pierwiastków przez rośliny zależy od procesów zachodzących między fazą stałą i ciekłą gleby oraz korzeniami roślin. Pod względem stopnia
OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE WPROWADZENIE Przyswajalność pierwiastków przez rośliny zależy od procesów zachodzących między fazą stałą i ciekłą gleby oraz korzeniami roślin. Pod względem stopnia
Genomic Mini AX Milk Spin
 Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Część I. Pomiar drgań własnych pomieszczenia
 LABORATORIUM INśYNIERII DŹWIĘKU 2 ĆWICZENIE NR 10 Część I. Pomiar drgań własnych pomieszczenia I. Układ pomiarowy II. Zadania do wykonania 1. Obliczyć promień krytyczny pomieszczenia, przy załoŝeniu, Ŝe
LABORATORIUM INśYNIERII DŹWIĘKU 2 ĆWICZENIE NR 10 Część I. Pomiar drgań własnych pomieszczenia I. Układ pomiarowy II. Zadania do wykonania 1. Obliczyć promień krytyczny pomieszczenia, przy załoŝeniu, Ŝe
ĆWICZENIE 1: BUFORY 1. Zapoznanie z Regulaminem BHP 2. Oznaczanie ph 2.1. metoda z zastosowaniem papierków wskaźnikowych
 ĆWICZENIE 1: BUFORY 1. Zapoznanie z Regulaminem BHP 2. Oznaczanie ph 2.1. metoda z zastosowaniem papierków wskaźnikowych Zasada metody Wykrywanie stęŝenia jonów wodorowych przy zastosowaniu papierków wskaźnikowych
ĆWICZENIE 1: BUFORY 1. Zapoznanie z Regulaminem BHP 2. Oznaczanie ph 2.1. metoda z zastosowaniem papierków wskaźnikowych Zasada metody Wykrywanie stęŝenia jonów wodorowych przy zastosowaniu papierków wskaźnikowych
Ćwiczenie nr 71: Dyfrakcja światła na szczelinie pojedynczej i podwójnej
 Wydział Imię i nazwisko 1. 2. Rok Grupa Zespół PRACOWNIA Temat: Nr ćwiczenia FIZYCZNA WFiIS AGH Data wykonania Data oddania Zwrot do popr. Data oddania Data zaliczenia OCENA Ćwiczenie nr 71: Dyfrakcja
Wydział Imię i nazwisko 1. 2. Rok Grupa Zespół PRACOWNIA Temat: Nr ćwiczenia FIZYCZNA WFiIS AGH Data wykonania Data oddania Zwrot do popr. Data oddania Data zaliczenia OCENA Ćwiczenie nr 71: Dyfrakcja
KONDUKTOMETRIA. Konduktometria. Przewodnictwo elektrolityczne. Przewodnictwo elektrolityczne zaleŝy od:
 KONDUKTOMETRIA Konduktometria Metoda elektroanalityczna oparta na pomiarze przewodnictwa elektrolitycznego, którego wartość ulega zmianie wraz ze zmianą stęŝenia jonów zawartych w roztworze. Przewodnictwo
KONDUKTOMETRIA Konduktometria Metoda elektroanalityczna oparta na pomiarze przewodnictwa elektrolitycznego, którego wartość ulega zmianie wraz ze zmianą stęŝenia jonów zawartych w roztworze. Przewodnictwo
Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu.
 WSTĘP Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu. Test jest przeznaczony wyłącznie do stosowania ZASADA OZNACZENIA Ten test immunoenzymatyczny
WSTĘP Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu. Test jest przeznaczony wyłącznie do stosowania ZASADA OZNACZENIA Ten test immunoenzymatyczny
Genomic Micro AX Blood Gravity 96-well
 Genomic Micro AX Blood Gravity 96-well Zestaw do izolacji DNA z krwi w formacie płytek na 96 studzienek dedykowany do pracy z pipetą wielokanałową lub automatem typu liquid handler. 960 izolacji Nr kat.
Genomic Micro AX Blood Gravity 96-well Zestaw do izolacji DNA z krwi w formacie płytek na 96 studzienek dedykowany do pracy z pipetą wielokanałową lub automatem typu liquid handler. 960 izolacji Nr kat.
Teoria błędów. Wszystkie wartości wielkości fizycznych obarczone są pewnym błędem.
 Teoria błędów Wskutek niedoskonałości przyrządów, jak również niedoskonałości organów zmysłów wszystkie pomiary są dokonywane z określonym stopniem dokładności. Nie otrzymujemy prawidłowych wartości mierzonej
Teoria błędów Wskutek niedoskonałości przyrządów, jak również niedoskonałości organów zmysłów wszystkie pomiary są dokonywane z określonym stopniem dokładności. Nie otrzymujemy prawidłowych wartości mierzonej
Genomic Mini AX Bacteria+ Spin
 Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
INSTRUKCJA OBSŁUGI TERMOMETR TYPU K. MODELE: 8801 i 8803 WSTĘP
 INSTRUKCJA OBSŁUGI TERMOMETR TYPU K MODELE: 8801 i 8803 WSTĘP Modele 8801 i 8803 są ręcznymi termometrami wyposaŝonymi w trzy i pół cyfrowe wyświetlacze, i są zaprojektowane do podłączenia termopary typu
INSTRUKCJA OBSŁUGI TERMOMETR TYPU K MODELE: 8801 i 8803 WSTĘP Modele 8801 i 8803 są ręcznymi termometrami wyposaŝonymi w trzy i pół cyfrowe wyświetlacze, i są zaprojektowane do podłączenia termopary typu
AmpliTest Babesia spp. (PCR)
 AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
Autodos M1-M2-M3. Automatyczne urządzenie pomiarowo-kontrolne o nowoczesnej konstrukcji, z nową komorą przepływową
 Autodos M1-M2-M3 Automatyczne urządzenie pomiarowo-kontrolne o nowoczesnej konstrukcji, z nową komorą przepływową Pomiar ph, redoks, wolnego chloru i ogólnego chloru Automatyczne dozowanie substancji chemicznych
Autodos M1-M2-M3 Automatyczne urządzenie pomiarowo-kontrolne o nowoczesnej konstrukcji, z nową komorą przepływową Pomiar ph, redoks, wolnego chloru i ogólnego chloru Automatyczne dozowanie substancji chemicznych
LAMPA POLIMERYZACYJNA
 LAMPA POLIMERYZACYJNA DB-686 Latte i Mocha INSTRUKCJA UśYTKOWANIA Wyłączny Dystrybutor: TPH Pol-Intech Sp. z o.o. 93-176 Łódź, ul. ŁomŜyńska 3 tel./fax. +48 42 682 78 75, +48 42 682 16 83 +48 42 684 64
LAMPA POLIMERYZACYJNA DB-686 Latte i Mocha INSTRUKCJA UśYTKOWANIA Wyłączny Dystrybutor: TPH Pol-Intech Sp. z o.o. 93-176 Łódź, ul. ŁomŜyńska 3 tel./fax. +48 42 682 78 75, +48 42 682 16 83 +48 42 684 64
Opis produktu Biotreat. Biologiczne oczyszczanie wody i jej odzyskiwanie do powtórnego uŝycia w myjniach samochodowych
 Opis produktu Biotreat Biologiczne oczyszczanie wody i jej odzyskiwanie do powtórnego uŝycia w myjniach samochodowych Schulstraße 35 Tel.: +49 35795 18662 E-Mail:info@absuts.de 01936 Laußnitz Fax: +49
Opis produktu Biotreat Biologiczne oczyszczanie wody i jej odzyskiwanie do powtórnego uŝycia w myjniach samochodowych Schulstraße 35 Tel.: +49 35795 18662 E-Mail:info@absuts.de 01936 Laußnitz Fax: +49
SPECYFIKACJA ASORTYMENTOWO-CENOWA
 Załącznik nr 1A - NOWY SPECYFIKACJA ASORTYMENTOWO-CENOWA Część nr 3 Załącznik nr 1 1 2 3 4 5 6 7 8 9 10 11 L.p. Przedmiot zamówienia Opis / parametry Nazwa Numer Jedn. Cena jedn. Stawka podatku od towarów
Załącznik nr 1A - NOWY SPECYFIKACJA ASORTYMENTOWO-CENOWA Część nr 3 Załącznik nr 1 1 2 3 4 5 6 7 8 9 10 11 L.p. Przedmiot zamówienia Opis / parametry Nazwa Numer Jedn. Cena jedn. Stawka podatku od towarów
1.2. Zlecenie może być wystawione w formie elektronicznej z zachowaniem wymagań, o których mowa w poz. 1.1.
 Załączniki do rozporządzenia Ministra Zdrowia z dnia 2005 r. (poz. ) Załącznik Nr 1 Podstawowe standardy jakości w czynnościach laboratoryjnej diagnostyki medycznej, ocenie ich jakości i wartości diagnostycznej
Załączniki do rozporządzenia Ministra Zdrowia z dnia 2005 r. (poz. ) Załącznik Nr 1 Podstawowe standardy jakości w czynnościach laboratoryjnej diagnostyki medycznej, ocenie ich jakości i wartości diagnostycznej
KARTA CHARAKTERYSTYKI
 KARTA CHARAKTERYSTYKI Producent: ul. Wiosenna 22 05-092 ŁOMIANKI tel./ fax. (0-81) 749 44 34, 749 44 00 w godzinach: 7 00-15 00 Data sporządzenia karty: 10.09.2007 Data aktualizacji karty: 09.03.2009 1.
KARTA CHARAKTERYSTYKI Producent: ul. Wiosenna 22 05-092 ŁOMIANKI tel./ fax. (0-81) 749 44 34, 749 44 00 w godzinach: 7 00-15 00 Data sporządzenia karty: 10.09.2007 Data aktualizacji karty: 09.03.2009 1.
Cyfrowy miernik temperatury
 Cyfrowy miernik temperatury MS6502 #04012 INSTRUKCJA OBSŁUGI wersja 1.1 MS6502 SPIS TREŚCI Wstęp... 3 Bezpieczeństwo uŝytkowania... 3 1. Zawartość opakowania... 3 2. Zasady bezpieczeństwa... 3 3. Środowisko
Cyfrowy miernik temperatury MS6502 #04012 INSTRUKCJA OBSŁUGI wersja 1.1 MS6502 SPIS TREŚCI Wstęp... 3 Bezpieczeństwo uŝytkowania... 3 1. Zawartość opakowania... 3 2. Zasady bezpieczeństwa... 3 3. Środowisko
INSTRUKCJA OBSŁUGI I INSTALACJI
 INSTRUKCJA OBSŁUGI I INSTALACJI System: Model: Moduł styków bezprądowych (Dry Contact) do termostatu PQDSBNGCM0 UWAGA Przed instalacją wyrobu naleŝy dokładnie przeczytać całą instrukcję. Prace instalacyjne
INSTRUKCJA OBSŁUGI I INSTALACJI System: Model: Moduł styków bezprądowych (Dry Contact) do termostatu PQDSBNGCM0 UWAGA Przed instalacją wyrobu naleŝy dokładnie przeczytać całą instrukcję. Prace instalacyjne
Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej
 Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej Wprowadzenie: Większość lądowych organizmów kręgowych część jonów amonowych NH + 4, produktu rozpadu białek, wykorzystuje w biosyntezie
Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej Wprowadzenie: Większość lądowych organizmów kręgowych część jonów amonowych NH + 4, produktu rozpadu białek, wykorzystuje w biosyntezie
ANALIZA INSTRUMENTALNA
 ANALIZA INSTRUMENTALNA TECHNOLOGIA CHEMICZNA STUDIA NIESTACJONARNE Sala 522 ul. Piotrowo 3 Studenci podzieleni są na cztery zespoły laboratoryjne. Zjazd 5 przeznaczony jest na ewentualne poprawy! Możliwe
ANALIZA INSTRUMENTALNA TECHNOLOGIA CHEMICZNA STUDIA NIESTACJONARNE Sala 522 ul. Piotrowo 3 Studenci podzieleni są na cztery zespoły laboratoryjne. Zjazd 5 przeznaczony jest na ewentualne poprawy! Możliwe
Komunikaty statystyczne medyczne
 Komunikaty statystyczne-medyczne (raporty statystyczne SWX) zawierają informację o usługach medycznych wykonanych przez świadczeniodawcę. Przekazany przez świadczeniodawcę komunikat podlega sprawdzeniu
Komunikaty statystyczne-medyczne (raporty statystyczne SWX) zawierają informację o usługach medycznych wykonanych przez świadczeniodawcę. Przekazany przez świadczeniodawcę komunikat podlega sprawdzeniu
