Alleny i ich zastosowanie w syntezie
|
|
|
- Szymon Wójcik
- 6 lat temu
- Przeglądów:
Transkrypt
1 3. eakcje allenów Instytut Chemii rganicznej PAN. Zespół II Warszawa, 13 lutego 2013
2 3. eakcje allenów 1 1. Wprowadzenie Krótka historia Struktura i właściwości fizyczne allenów Klasyfikacja allenów 2 Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów 3 3. eakcje allenów reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów 4
3 3. eakcje allenów Krótka historia Struktura i właściwości fizyczne allenów Klasyfikacja allenów Krótka historia 1887: Pierwsza synteza allenu (kwas glutynowy), Burton and Pechmann, Chem. Ber. 1887, 145. Potwierdzenie struktury kwasu glutynowego, Jones et al., J. Chem. Soc. 1954, : Wyizolowanie i scharakteryzowanie pierwszego naturalnego allenu, piretrolonu, Staudinger and uzicka, elv. Chim. Acta 1924, : Pierwsze review nt. allenów, Bouis, Ann. Chim. (Paris) 1928, : synteza pierwszego chiralnego allenu, Maitland and Mills, Nature 1935, 994. statnia dekada ( ): Shengming Ma (148 publikacji); Norbert Krause (42 publikacji), Benito Alcaide i Pedro Almendros (33 publikacji) (na podstawie danych z listopada 2012 ze Scifinder-a). CC CC kwas glutynowy Piretrolon
4 1. Wprowadzenie 3. eakcje allenów Krótka historia Struktura i właściwości fizyczne allenów Klasyfikacja allenów orbital LUM orbital M Właściwości spektralne allenów: I: antysymetryczne drgania rozciągające cm 1 (vs. alkene: 1680 cm 1, alkyne 2200 cm 1 ) 1 NM:δ = ppm 13 C NM: δ(c-1, C-3) = ppm; δ(c-2) = ppm.
5 3. eakcje allenów Krótka historia Struktura i właściwości fizyczne allenów Klasyfikacja allenów Klasyfikacja allenów δ δ+ EWG δ EDG M δ δ = alkil, alkenyl, aryl, alkynyl EWG = C 2, CN, S 2,... EDG =, S, N 2, al,... M = Li, Mg, B, Si, Sn, Zn, In, Ti, Cu, Pd - alleny mogą reagować zarówno z nukleofilami jak i elektrofilami - zmiana podstawników może zmienić ich reaktywniość
6 3. eakcje allenów Przegrupowanie prototropowe Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów Me N N K, K2C3 Me, t. wrz. 68% Me N N C K t Bu 84% C Et3N ilosciowo 1. LDA, 2. N4Cl kontr. kinet. MM MM (1)CA 2000, 777;(2)JC 1991, 6264;(3)JCS Perkin T1 1985, 1803;(4)Chem. Eur. J. 1998, 1480.
7 3. eakcje allenów Przegrupowania sigmatropowe Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów X Y Y Y Z [2,3] X X [3,3] X Y Z n-bu SnBu 3 n BuLi 71%, 93% ee przegr. Wittiga n-bu t-bu EtC(Et) 3 EtC 2 Et t-bu E t-bu C 2Et dr = 9:1, 68% ee 1 N 2 C 2Me 2 h 2(S-DSP) 4 1 mol% pentan 2 [h] 1 C 2Me Me 2C 1 2 Ar [Au (I) L]Tf Ar NaB 4 Ar (1)JC 1989, 5854; (2)JACS 2012, 15497; (3)JC 1988, 4736; (4)(a)L 2011, 2618; (b)jacs 2004,
8 3. eakcje allenów Substytucja nukleofilowa Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów 1 1 anti SN2' Nu LG Nu 1 TMS LiCuBr2 S2Ar TMS Br 1 X 1 CuX, MgX, LiX Cu LG LG CuX 1 + X 1 Cu LG X Cu 1 donacja wsteczna: dcu - π C-C dcu - σ C-LG (1)JACS 2001, 1533;
9 3. eakcje allenów Substytucja nukleofilowa c.d. Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów Ac Ac MeMgBr (30 eq) LiBr (30 eq) CuI (30 eq) Ac Ac TF, 0 C, 3.5 h 15 min, 0 C 85% [Cu] n-bu syn : anti: n-bu2culi 60:40 anti n-bu2culi Me2S 6:94 n-bu2cumgbr Me2S 1:99 n-bu syn (1)ACIE 2008, 568; (2)TL 1983, 5587.
10 Addycja do enynów 1. Wprowadzenie 3. eakcje allenów Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów NBn2 N S n-buli (-)-sparteina Me Bn2N N EWG EWG C2Et n Me2CuLi LiI t-buc2 n C2Et Pd(0) (S)-Me-MP (cat)b B PdL* (cat)b PdL* do 63% ee B(cat) C (1)Liebigs Ann. Chem ; (2)TL 1999, 1881; (3)ChemCom 1993, 1468.
11 Eliminacja 1. Wprowadzenie 3. eakcje allenów Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów 1 2 X Y SiMe 3 Br 1. t-buli 1 C 2 Me 3Si Li C Al 3 M 1 2 Al 3 1,2-eliminacja anti Cl 2 Cl Cp 2Ti(P(Et) 3) TiCp Li SiMe' 1. C 2. rozdzial SiMe' Tf2 TASF N 2 C 2Et kat. Fe P 3 P 3 C 2Et 1 2 Et 3N CCl 1 2 C 2Et (1)JACS 1979, 7302; (2)TL 1988, 1355; (3)Synth. 2006, 2577; (4)rg. Biomol. Chem. 2005, 2914; (5)JACS 2007, 1494.
12 Inne metody 1. Wprowadzenie 3. eakcje allenów Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów pochodne metaloorganiczne allenu C n-buli Et 2 : exane 2. C 6 13C 2I 88% 1. n-buli TF 2. Br(C 2) 3Cl Cl karbeny CBr 2 Br Br MeLi SnBu 3 Ti(IV)/(S)-binol 10 mol% + 2 C 2 1 i-prsbet 1 2, DCM Ylidy tytano-fosforowe n C C (ipr)2ticl2 (Me2N)3P=C2 NaMDS n fragmentacja TMS Me Tf TMS TBAF 52% Me (1)(a)TL 1985, 271; (b)t 1979, 353; (2)JACS 1997, 3429; (3)JC 1975, 585; (4)JACS 2012,
13 3. eakcje allenów Wykorzystanie propargilosilanów Przegrupowanie prototropowe Przegrupowania sigmatropowe Substytucja nukleofilowa Addycja do enynów Eliminacja Inne metody Wykorzystanie propargilosilanów SiMe TMSTf Et 2, -78 C 3-6h 2 1 (1)TL 2005, 6861.
14 3. eakcje allenów związki allenylometaliczne związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów 1 2 M 1 M E E 2 E E 1 2 E S E 2 1 S E 2' 2 E gólna zasada (może ulec zmianie w zależności od podstawników 1, 2 i/lub obecności metali, użytego elektrofila): - allen jest stabilniejszy niż związek propargilowy - reakcja zarówno według mechanizmu: S E 2 (Li, Mg...) jak i: S E 2 (Sn, B, In, Zn...) - synteza: wymiana metal-halogen / deprotonowanie w pozycji propargilowej (Li), oksydatywna addycja w warunkach Barbiera (Mg, Zn, In...), transmetalacja (Li, Mg to Cu, Sn, B, Si, Zn, Ti...) lub uwodornienie katalizowane palladem (B, Si) - niektóre związki alleno- i propargilometaliczne mogą być wydzielone (M = B, Si, Sn) Nie będę omawiał: - alleny jako alkeny (np: reakcja Dielsa-Aldera, sprzęganie) - alleny jako enony, α,β-nienasycone estry...(np. addycja 1,4 w allenach podstawionych grupą akceptorową)
15 3. eakcje allenów związki allenylometaliczne c.d. związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów Piv Ms + Pd(Ac)2, P3 Et 2Zn, TF NBoc Piv NBoc 78%, dr > 95:5 Piv [Pd] Piv Me MsZn transmetalacja Me Cy NCBz Me In I Cl, AgP* 10 mol% toluen, cpme Bpin NCbz NCbz + Cy Cy 75%, 88% ee 18%, 25% ee (1)L 2005, 1593; (2)ACIE 2011,
16 cykloaddycje 1. Wprowadzenie 3. eakcje allenów związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów cykloaddycja [2+2] fotochemiczna cykloaddycja [2+2] termiczna 125 C hν δ- δ- 31.2% 62.5% hν SM(π*) LUM δ- δ+ SM(π*) LUM 6.3% NAc hν NAc - δ- (1)ChemCom 1975, 277; (2)T 1975, 1655.
17 3. eakcje allenów eakcje wolnorodnikowe związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów 1 2 α 1 α β α 2 kontrola termodynamiczna β 2 1 CC 6 4CF 3 i-pr 1. hν / 55 C CD / NMC 2. CD / C65S hν, 46% CD: 1,4-cykloheksadien NMC: N-metylokarbazol 1. Bu 3Sn, Et 3B, 2 Br Br 2. TMS3Si, Et3B, 2 73%, dr = 9:1 (1)JACS 1993, 7926; (2)TA 2003, 3005.
18 3. eakcje allenów związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów Addycja do allenów katalizowana Palladem 1 2 Pd (II) X karbopalladowanie 1 PdX π-kompleks Nu - 1 Nu TsN Pd(Ac)2, P3 TsN + I In, DMF, 80 C [In] addycja kwasów aryloborowych do allenów TsN 93% I N Ts + N Pd(Ac)2, P3 N K2C3, Me 110 C N Ts PdX 1 1 Pd (0) /Pd (II) PdX ArB()2 1 Ar I + Pd(0) C, K2C3 N C2Me Me 45 C PdX 60%, 1:1 N C 2Me + ()2B Me Me Pd (II) 5 mol% Et3N dioksan : 2 80 C 68% Me Me (1)ChemCom 2001, 964; (2)TL 2000, 7129; (3)JC 2002, 4376; (4)L 2009, 1441.
19 3. eakcje allenów związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów dane obliczeniowe (CuI, AgI, AuI): To znaczy, że: - ligandy etylenowe są nieznacznie silniej wiązane przez metal przejściowy - na siłę wiązania składa się: oddziaływanie σ (55-70%) oraz wiązanie π-zwrotne (20-33% energii wiązania kowalencyjnego) - reakcje z udziałem alkinów (allenów) w porównaniu do olefin mają charakter procesów kinetycznych - wiązania podwójne oddziałujące z metalem przejściowym stają się bardziej elektrofilowe Furstner and Davies, Angew. Chem. Int. Ed. 2007, alleny w przeciwieństwie do alkenów (i alkinów): - alkiny i alkeny przykoordynowywują do metalu przejściowego η 2, - alleny mogą η 2 ale mają też kilka sposobów koordynacji η 1
20 3. eakcje allenów Aktywacja miękkimi kwasami Lewisa c.d. związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów Me Me' L Au Br Me L Au [TM] + α γ β Me' Nu - TM = Au, Pt, Ag, Pd [Au] (I) Br PEt3Au (I) Cl Me, t. pok. Me L Au 1 [Au] (I) Br Me' Me' L Au Me Me' 2 2 Pd (II) X 1 PdX kompleks π Br Au (III) Cl 3 Me, t. pok. Br [Au] (III) Me L Au Br Br [Au] (III) AgA* dppm(aucl)2 () 3PAuCl / AgTf (5 mol%) DCM, t. pok. A*- [Au] + oddzialywanie z chiralnym przeciwjonem 91%, 97% ee AgTf [Ag] AuCl3 [Au] 55% P = 2,4,6-i-PrC63 (1)M 2010, 4207; (2)JACS 2008, 6940; (3)JACS 2006, 9066; (4)Science 2007, 496; (5)ASC 2008, 547; (6)(a)JACS 2009, 6348; (b)jacs 2009,
21 3. eakcje allenów Cykloaddycje katalizowane fosfinami związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów Et2C + Piv P3 (10 mol% Me, 110 C 63% Et2C Piv P23 P 2 3 Piv
22 3. eakcje allenów związki allenylometaliczne reakcje cykloaddycji eakcje wolnorodnikowe Addycja do allenów katalizowana Palladem Aktywacja miękkimi kwasami Lewisa Cykloaddycje katalizowane fosfinami Karbonylowanie i rakcja Pausona-Khanda allenów Karbonylowanie i rakcja Pausona-Khanda allenów NTs u(c)4 C TsN u(c) 4 TsN M TsN u(c)3 3 C M 1 2 M TsN 3 (C)3 u (1)L 2003, 3491.
23 3. eakcje allenów Literatura przegrupowania prototropowe: CA 2000, 777 JC 1991, 6264 JCS Perkin T1 1985, 1803 Chem. Eur. J. 1998, 1480 przegrupowania sigmatropowe: JC 1989, 5854; JACS 2012, 15497; JC 1988, 4736; L 2011, 2618; JACS 2004, 15978; L 2002, Substytucja nukleofilowa: ACIE 2008, 568; JACS 2001, 1533; TL 1983, 5587; Chem. Lett. 2000, 1360; JC 1995, 796. Addycja do enynów: Liebigs Ann. Chem ; TL 1999, 1881; ChemCom 1993, 1468; JACS 1979, eliminacje: TL 1988, 1355; Synth. 2006, 2577; rg. Biomol. Chem. 2005, 2914; JACS 2007, Inne metody: TL 1985, 271; T 1979, 353; JACS 1997, 3429; JC 1975, 585; JACS 2012, związki allenylometaliczne: L 2005, 1593; ACIE 2011, cykloaddycje: ChemCom 1975, 277; T 1975, reakcje wolnorodnikowe: JACS 1993, 7926; TA 2003, Karbopalladowanie: ChemCom 2001, 964; TL 2000, 7129; JC 2002, addycja ArB()2: L 2009, kwasy Lewisa: M 2010, 4207; JACS 2008, 6940; JACS 2006, 9066; Science 2007, 496; ASC 2008, 547; JACS 2009, 6348; JACS 2009, Pauson-Khand: L 2003, 3491.
24 3. eakcje allenów Dziękuję za uwagę!
STEREOCHEMIA ORGANICZNA
 STEECEMIA GANICZNA Sławomir Jarosz Wykład 6 Typowe energie (ev) i współczynniki orbitalne X LUM 1.5 1.0 C 0 Z +3.0 M -10.5-9.1 C -10.9 Z -9.0 X Typowe energie (ev) i współczynniki orbitalne X LUM 1.0 +0.5
STEECEMIA GANICZNA Sławomir Jarosz Wykład 6 Typowe energie (ev) i współczynniki orbitalne X LUM 1.5 1.0 C 0 Z +3.0 M -10.5-9.1 C -10.9 Z -9.0 X Typowe energie (ev) i współczynniki orbitalne X LUM 1.0 +0.5
Metody syntezy fosfonianów. Marta Sowińska Zespół XII
 Metody syntezy fosfonianów Marta Sowińska Zespół XII Fosfoniany aktywność biologiczna przeciwgrzybicza antybakteryjna antywirusowa leki na nadciśnienie antynowotworowa przeciwmalaryczna =, Me leki na osteoporozę
Metody syntezy fosfonianów Marta Sowińska Zespół XII Fosfoniany aktywność biologiczna przeciwgrzybicza antybakteryjna antywirusowa leki na nadciśnienie antynowotworowa przeciwmalaryczna =, Me leki na osteoporozę
Otrzymywanie -aminokwasów
 trzymywanie -aminokwasów Przykłady -aminokwasów o znaczeniu praktycznym Cl Cl 2 C 2 Melaphalan (lek przeciwnowotworowy) 2 C 2 Levodopa (stosowana w chorobie Parkinsona) 1 1 2 2 3 C środowisko wodne reakcja
trzymywanie -aminokwasów Przykłady -aminokwasów o znaczeniu praktycznym Cl Cl 2 C 2 Melaphalan (lek przeciwnowotworowy) 2 C 2 Levodopa (stosowana w chorobie Parkinsona) 1 1 2 2 3 C środowisko wodne reakcja
STEREOCHEMIA ORGANICZNA Wykład 6
 STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne 1.5 1.0 0 +3.0 1.0 +0.5-0.5 +2.5-10.5-9.1-10.9-9.0-9.1-8.2-9.5-8.5 Me x (-8.5 ev) (+2.5 ev) x+n y (~0 ev) y+m (-10.9 ev) Me x x+n
STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne 1.5 1.0 0 +3.0 1.0 +0.5-0.5 +2.5-10.5-9.1-10.9-9.0-9.1-8.2-9.5-8.5 Me x (-8.5 ev) (+2.5 ev) x+n y (~0 ev) y+m (-10.9 ev) Me x x+n
STEREOCHEMIA ORGANICZNA
 STERECEMIA RGANICZNA Sławomir Jarosz Wykład 5 Reguły Baldwina exo B (-) A B A (-) endo B (-) A B A (-) J. E. Baldwin, J. Chem. Soc., Chem. Commun. 1976, 734. J. E. Baldwin, J. Cutting, W. Dupont, L. Kruse,
STERECEMIA RGANICZNA Sławomir Jarosz Wykład 5 Reguły Baldwina exo B (-) A B A (-) endo B (-) A B A (-) J. E. Baldwin, J. Chem. Soc., Chem. Commun. 1976, 734. J. E. Baldwin, J. Cutting, W. Dupont, L. Kruse,
Organokataliza mechanizmy, katalizatory, reakcje. Maria Rogozińska Zespół VI
 rganokataliza mechanizmy, katalizatory, reakcje Maria ogozińska Zespół VI rganokataliza Katalizowanie reakcji chemicznych małymi cząsteczkami organicznymi, zbudowanymi z węgla, wodoru, fosforu, azotu,
rganokataliza mechanizmy, katalizatory, reakcje Maria ogozińska Zespół VI rganokataliza Katalizowanie reakcji chemicznych małymi cząsteczkami organicznymi, zbudowanymi z węgla, wodoru, fosforu, azotu,
wykład monograficzny O niektórych sposobach udoskonalania procesów katalizowanych metalami i ich związkami
 wykład monograficzny niektórych sposobach udoskonalania procesów katalizowanych metalami i ich związkami rocesy katalizowane kompleksami metali Wybrane przykłady ydroodsiarczanie ropy naftowej e, Mo ydroformylacja
wykład monograficzny niektórych sposobach udoskonalania procesów katalizowanych metalami i ich związkami rocesy katalizowane kompleksami metali Wybrane przykłady ydroodsiarczanie ropy naftowej e, Mo ydroformylacja
CHIRALNE KWASY FOSFOROWE WŁAŚCIWOŚCI I ZASTOSOWANIE. Anna Kozioł Zespół II
 CHIRALNE KWASY FSFRWE WŁAŚCIWŚCI I ZASTSWANIE Anna Kozioł Zespół II STATNIE ZASTSWANIA KWASÓW W FSFRWYCH PARTYCH NA BINLU KWASY BRØNSTEDA JAK KATALIZATRY Model aktywacji kwasami Brønsteda Rozwój enancjoselektywnych,
CHIRALNE KWASY FSFRWE WŁAŚCIWŚCI I ZASTSWANIE Anna Kozioł Zespół II STATNIE ZASTSWANIA KWASÓW W FSFRWYCH PARTYCH NA BINLU KWASY BRØNSTEDA JAK KATALIZATRY Model aktywacji kwasami Brønsteda Rozwój enancjoselektywnych,
Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady
 Synteza i wykorzystanie -aminoketonów (zasad Mannicha) Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady i-pr Falicain środek zneczulający 2 Tramadol środek przeciwbólowy snervan choroba
Synteza i wykorzystanie -aminoketonów (zasad Mannicha) Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady i-pr Falicain środek zneczulający 2 Tramadol środek przeciwbólowy snervan choroba
Halogenki alkilowe RX
 alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
copyright (c) IChO PAN 2
 MECHACHEMIA W SYTEZIE RGAICZEJ Michał Michalak SPSBY IICJWAIA REAKCJI CHEMICZYCH MECHACHEMIA - DEFIICJA RYS HISTRYCZY HgS + Cu Hg + CuS cynober AgCl + Zn (Cu, Sn, Fe) Ag + MCl 1820 r. kowelin Matthew Carey
MECHACHEMIA W SYTEZIE RGAICZEJ Michał Michalak SPSBY IICJWAIA REAKCJI CHEMICZYCH MECHACHEMIA - DEFIICJA RYS HISTRYCZY HgS + Cu Hg + CuS cynober AgCl + Zn (Cu, Sn, Fe) Ag + MCl 1820 r. kowelin Matthew Carey
Sharpless epoxydation of allylic alcohols
 Wykład 6 Sharpless epoxydation of allylic alcohols H H D-(-)-Diethyl tartarate.. : : 3 2 : Ọ. : 1 H (CH 3 ) 3 CH, Ti(iPr) 4 CH 2 Cl 2-20 o C 2 1 H 3 -(+)-Diethyl tartarate H H Green Chemistry Asymmetric
Wykład 6 Sharpless epoxydation of allylic alcohols H H D-(-)-Diethyl tartarate.. : : 3 2 : Ọ. : 1 H (CH 3 ) 3 CH, Ti(iPr) 4 CH 2 Cl 2-20 o C 2 1 H 3 -(+)-Diethyl tartarate H H Green Chemistry Asymmetric
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
b. Rozdział mieszaniny racemicznej na CHIRALNEJ kolumnie (Y. Okamoto, T. Ikai, Chem. Soc. Rev., 2008, 37, )
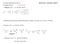 Jak otrzymać związki optycznie czynne??? ławomir Jarosz stereochemia- wykład VII Ze związków chiralnych 1. ozdział racematu a. Klasyczny : A (rac) 50% A() 50%A() b. ozdział mieszaniny racemicznej na CIAEJ
Jak otrzymać związki optycznie czynne??? ławomir Jarosz stereochemia- wykład VII Ze związków chiralnych 1. ozdział racematu a. Klasyczny : A (rac) 50% A() 50%A() b. ozdział mieszaniny racemicznej na CIAEJ
Slajd 1. Reakcje alkinów
 Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Reakcje Cykloaddycji w Syntezie Organicznej
 Reakcje Cykloaddycji w Syntezie rganicznej PDSTAWWE REAKCJE CYKLADDYCJI [4+ 2] + Y X Z + [3+ 2] Y X Z Y X Z [2+ 2] + REAKCJ DIELSA-ALDERA Zorientowanie reagentów: Analiza orbitali granicznych (FM) Donor
Reakcje Cykloaddycji w Syntezie rganicznej PDSTAWWE REAKCJE CYKLADDYCJI [4+ 2] + Y X Z + [3+ 2] Y X Z Y X Z [2+ 2] + REAKCJ DIELSA-ALDERA Zorientowanie reagentów: Analiza orbitali granicznych (FM) Donor
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Przemysłowe procesy katalityczne część II Kataliza kompleksami metali
 Przemysłowe procesy katalityczne część II Kataliza kompleksami metali Studia II stopnia Semestr I Wymiar: 7 godzin Prowadzący: dr hab. inż. Włodzimierz Buchowicz Zakład Chemii Organicznej Gmach Chemii,
Przemysłowe procesy katalityczne część II Kataliza kompleksami metali Studia II stopnia Semestr I Wymiar: 7 godzin Prowadzący: dr hab. inż. Włodzimierz Buchowicz Zakład Chemii Organicznej Gmach Chemii,
Reakcje aldehydów i ketonów. grupa karbonylowa Z = H, aldehyd Z = R (czyli at. C), keton
 30-33. Reakcje aldehydów i ketonów grupa karbonylowa Z =, aldehyd Z = R (czyli at. C), keton Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 15.1. Nazewnictwo Aldehyd
30-33. Reakcje aldehydów i ketonów grupa karbonylowa Z =, aldehyd Z = R (czyli at. C), keton Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 15.1. Nazewnictwo Aldehyd
PIERWIASTKI W UKŁADZIE OKRESOWYM
 PIERWIASTKI W UKŁADZIE OKRESOWYM 1 Układ okresowy Co można odczytać z układu okresowego? - konfigurację elektronową - podział na bloki - podział na grupy i okresy - podział na metale i niemetale - trendy
PIERWIASTKI W UKŁADZIE OKRESOWYM 1 Układ okresowy Co można odczytać z układu okresowego? - konfigurację elektronową - podział na bloki - podział na grupy i okresy - podział na metale i niemetale - trendy
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
10. Eliminacja halogenków alkili
 10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
W poprzednim cyklu wykładów :
 hemia metaloorganiczna 2 W poprzednim cyklu wykładów : Udzielam zgody na korzystanie z tego dokumentu na zasadach określonych w licencji GNU FDL (http://pl.wikipedia.org/wiki/gnu_fdl) Definicja: hemia
hemia metaloorganiczna 2 W poprzednim cyklu wykładów : Udzielam zgody na korzystanie z tego dokumentu na zasadach określonych w licencji GNU FDL (http://pl.wikipedia.org/wiki/gnu_fdl) Definicja: hemia
Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej
 Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej Zespół VI Opiekun: dr hab. Jacek Młynarski, prof. nadzw. Oskar Popik Wstęp Początki organokatalizy Pierwszy przykład organokatalitycznej
Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej Zespół VI Opiekun: dr hab. Jacek Młynarski, prof. nadzw. Oskar Popik Wstęp Początki organokatalizy Pierwszy przykład organokatalitycznej
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
ul. Umultowska 89b, Collegium Chemicum, Poznań tel ; fax
 Wydział Chemii Zakład Chemii Analitycznej Plazma kontra plazma: optyczna spektrometria emisyjna w badaniach środowiska Przemysław Niedzielski ul. Umultowska 89b, Collegium Chemicum, 61-614 Poznań tel.
Wydział Chemii Zakład Chemii Analitycznej Plazma kontra plazma: optyczna spektrometria emisyjna w badaniach środowiska Przemysław Niedzielski ul. Umultowska 89b, Collegium Chemicum, 61-614 Poznań tel.
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
Kierunek i poziom studiów: Biotechnologia, pierwszy. Nazwa wariantu modułu (opcjonalnie): nie dotyczy
 Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
20 i 21. Eliminacja halogenków alkili
 20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
Wiązania. w świetle teorii kwantów fenomenologicznie
 Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
WYKŁAD 6. Zalecana literatura
 Zalecana literatura WYKŁAD 6 1. Johnson, D. S.; Li, J. J. The art of drug synthesis, John Wiley & Sons, Inc., oboken, ew Jersey, 2007. 2. Torrence P. F. Antiviral drug discovery for emerging diseases and
Zalecana literatura WYKŁAD 6 1. Johnson, D. S.; Li, J. J. The art of drug synthesis, John Wiley & Sons, Inc., oboken, ew Jersey, 2007. 2. Torrence P. F. Antiviral drug discovery for emerging diseases and
Wykład 19 XII 2018 Żywienie
 Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Kartkówka nr 1 Imię i Nazwisko:.. Nr albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1.
 Kartkówka nr 1 Imię i azwisko:.. r albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1. b) 3 C 3 c) 1 i 3 d) 2 i 2) Wskaż indywiduum chemiczne, w którym suma ładunków
Kartkówka nr 1 Imię i azwisko:.. r albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1. b) 3 C 3 c) 1 i 3 d) 2 i 2) Wskaż indywiduum chemiczne, w którym suma ładunków
RJC Y R R Y R R R H R H. Slides 1 to 24
 JC eakcje Eliminacji (E1 & E2) B δ B δ B Slides 1 to 24 JC eakcje Eliminacji Dwa mechanizmy są moŝliwe wtedy, kiedy zasada (B - ) atakuje halogenek alkilowy z atomem w pozycji α; ; zachodząca reakcja eliminacji
JC eakcje Eliminacji (E1 & E2) B δ B δ B Slides 1 to 24 JC eakcje Eliminacji Dwa mechanizmy są moŝliwe wtedy, kiedy zasada (B - ) atakuje halogenek alkilowy z atomem w pozycji α; ; zachodząca reakcja eliminacji
Chemia nieorganiczna. Copyright 2000 by Harcourt, Inc. All rights reserved.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
Teoria VSEPR. Jak przewidywac strukturę cząsteczki?
 Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Zarys Chemii Organicznej
 Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Układy pięcioczłonowe z jednym heteroatomem
 WYKŁAD 7 Układy pięcioczłonowe z jednym heteroatomem Furan 1-Pirol Tiofen Benzofuran 1-Indol Benzo[b]tiofen Tetrahydrofuran Pirolidyna Tiolan 1 1. Muskaryna (I, muscarine) Alkaloid pochodzenia naturalnego
WYKŁAD 7 Układy pięcioczłonowe z jednym heteroatomem Furan 1-Pirol Tiofen Benzofuran 1-Indol Benzo[b]tiofen Tetrahydrofuran Pirolidyna Tiolan 1 1. Muskaryna (I, muscarine) Alkaloid pochodzenia naturalnego
Chemia nieorganiczna. Pierwiastki. niemetale Be. 27 Co. 28 Ni. 26 Fe. 29 Cu. 45 Rh. 44 Ru. 47 Ag. 46 Pd. 78 Pt. 76 Os.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu. F Br H 3 C
 alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
Związki kompleksowe pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor?
 pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? 1 1 1 H 3 Li 11 Na 19 K 37 Rb 55 Cs 87 Fr 4 Be 12 Mg 20 Ca 38 Sr 56 Ba 88 Ra Układ okresowy 2 13 14 15 16
pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? 1 1 1 H 3 Li 11 Na 19 K 37 Rb 55 Cs 87 Fr 4 Be 12 Mg 20 Ca 38 Sr 56 Ba 88 Ra Układ okresowy 2 13 14 15 16
Związki kompleksowe. pigmenty i barwniki. co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? Pierwiastki
 pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? 1 07_117 Układ okresowy Pierwiastki 1 1 H 3 Li 11 Na 19 K 37 Rb 55 Cs 87 Fr metale niemetale 2 13 14 15 16
pigmenty i barwniki co to są związki kompleksowe? jaka jest ich budowa? skąd się bierze kolor? 1 07_117 Układ okresowy Pierwiastki 1 1 H 3 Li 11 Na 19 K 37 Rb 55 Cs 87 Fr metale niemetale 2 13 14 15 16
UKŁAD OKRESOWY PIERWIASTKÓW
 UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
STEREOCHEMIA ORGANICZNA Wykład 6
 STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne Reakcja Dielsa Aldera - Regioselektywność w reakcjach DA LUM M 1.5-10.5 M 1.0-9.1 LUM 0-10.9 +3.0-9.0 Me M (-8.5 ev) LUM (+2.5 ev)
STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne Reakcja Dielsa Aldera - Regioselektywność w reakcjach DA LUM M 1.5-10.5 M 1.0-9.1 LUM 0-10.9 +3.0-9.0 Me M (-8.5 ev) LUM (+2.5 ev)
węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny)
 DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH
 ZAAWANSWANE METDY USTALANIA BUDWY ZWIĄZKÓW RGANICZNYC Witold Danikiewicz Instytut Chemii rganicznej PAN ul. Kasprzaka /52, 0-22 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli jak powiązać
ZAAWANSWANE METDY USTALANIA BUDWY ZWIĄZKÓW RGANICZNYC Witold Danikiewicz Instytut Chemii rganicznej PAN ul. Kasprzaka /52, 0-22 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli jak powiązać
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Kataliza metaloorganiczna w procesach o dużym znaczeniu przemysłowym
 Kataliza metaloorganiczna w procesach o dużym znaczeniu przemysłowym Olbrzymia większość reakcji realizowanych w ramach tzw. wielkiej chemii jest katalizowana związkami metaloorganicznymi. 1. eakcje z
Kataliza metaloorganiczna w procesach o dużym znaczeniu przemysłowym Olbrzymia większość reakcji realizowanych w ramach tzw. wielkiej chemii jest katalizowana związkami metaloorganicznymi. 1. eakcje z
MECHANIZMY FRAGMENTACJI ZWIĄZKÓW ORGANICZNYCH. Copyright 2003 Witold Danikiewicz
 MECANIZMY FAGMENTACJI ZWIĄZKÓW GANICZNYC Copyright 2003 Cechy charakterystyczne zjawiska fragmentacji jonów proces jednocząsteczkowy; szybkość fragmentacji jest mała w porównaniu z szybkością rozpraszania
MECANIZMY FAGMENTACJI ZWIĄZKÓW GANICZNYC Copyright 2003 Cechy charakterystyczne zjawiska fragmentacji jonów proces jednocząsteczkowy; szybkość fragmentacji jest mała w porównaniu z szybkością rozpraszania
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
X / \ Y Y Y Z / \ W W ... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Chemia nieorganiczna. Pierwiastki. niemetale Be. 27 Co. 28 Ni. 26 Fe. 29 Cu. 45 Rh. 44 Ru. 47 Ag. 46 Pd. 78 Pt. 76 Os.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by arcourt,
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by arcourt,
RJC A-B A + B. Slides 1 to 27
 Reakcje Rodnikowe rodniki substytucja addycja polimeryzacje A-B A + B Slides 1 to 27 Reakcje Organiczne... powstawanie i rozrywanie wiązań kowalencyjnych. Addycja A + B AB Podstawienie AB + C A + BC Eliminacja
Reakcje Rodnikowe rodniki substytucja addycja polimeryzacje A-B A + B Slides 1 to 27 Reakcje Organiczne... powstawanie i rozrywanie wiązań kowalencyjnych. Addycja A + B AB Podstawienie AB + C A + BC Eliminacja
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
Materiały dodatkowe - węglowodory
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe - węglowodory Alkany 1. Hybrydyzacja atomu węgla Mnogość związków, jakie mogą powstać z udziałem atomów węgla,
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe - węglowodory Alkany 1. Hybrydyzacja atomu węgla Mnogość związków, jakie mogą powstać z udziałem atomów węgla,
Plan prezentacji. Wprowadzenie Metody Wyniki Wnioski Podziękowania. Yaghi et al. Nature 2003, 423, 705 2
 Molecular Modeling of Hydrogen Storage. M+ H2 and M+ Benzene vs. Metal Organic Frameworks (MOF) P. Groch1, M. Stachów1, T. Kupka1 oraz L. Stobiński2 1Uniwersytet Opolski, Wydział Chemii, 45-052 Opole 2Instytut
Molecular Modeling of Hydrogen Storage. M+ H2 and M+ Benzene vs. Metal Organic Frameworks (MOF) P. Groch1, M. Stachów1, T. Kupka1 oraz L. Stobiński2 1Uniwersytet Opolski, Wydział Chemii, 45-052 Opole 2Instytut
Konwersatorium 1. Zagadnienia na konwersatorium
 Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
8. Delokalizacja elektronów i reaktywność dienów sprzężonych
 8. Delokalizacja elektronów i reaktywność dienów sprzężonych 1 8.1. Definicja elektronów zdelokalizowanych Zlokalizowane elektrony rozmieszczone w określonym obszarze cząsteczki, są uwspólnione pomiędzy
8. Delokalizacja elektronów i reaktywność dienów sprzężonych 1 8.1. Definicja elektronów zdelokalizowanych Zlokalizowane elektrony rozmieszczone w określonym obszarze cząsteczki, są uwspólnione pomiędzy
Reaktywność związków metaloorganicznych w stosunku do alkoholi
 eaktywność związków metaloorganicznych w stosunku do alkoholi n M + 'H n-1 M ' M H ' -H -H n X y M + 'H n-1 X y M X=halogen ' X n M + X,Y-H n-1 M + H Y X,Y= H H 2, H eaktywność związków metaloorganicznych
eaktywność związków metaloorganicznych w stosunku do alkoholi n M + 'H n-1 M ' M H ' -H -H n X y M + 'H n-1 X y M X=halogen ' X n M + X,Y-H n-1 M + H Y X,Y= H H 2, H eaktywność związków metaloorganicznych
Źródła światła w AAS. Seminarium Analityczne MS Spektrum Zakopane Jacek Sowiński MS Spektrum
 Źródła światła w AAS Seminarium Analityczne MS Spektrum Zakopane 2013 Jacek Sowiński MS Spektrum js@msspektrum.pl www.msspektrum.pl Lampy HCL Standardowa Super-Lampa 3V 10V specyf. Lampy HCL 1,5 cala
Źródła światła w AAS Seminarium Analityczne MS Spektrum Zakopane 2013 Jacek Sowiński MS Spektrum js@msspektrum.pl www.msspektrum.pl Lampy HCL Standardowa Super-Lampa 3V 10V specyf. Lampy HCL 1,5 cala
spektroskopia elektronowa (UV-vis)
 spektroskopia elektronowa (UV-vis) rodzaje przejść elektronowych Energia σ* π* 3 n 3 π σ σ σ* daleki nadfiolet (λ max < 200 nm) π π* bliski nadfiolet jednostki energii atomowa jednostka energii = energia
spektroskopia elektronowa (UV-vis) rodzaje przejść elektronowych Energia σ* π* 3 n 3 π σ σ σ* daleki nadfiolet (λ max < 200 nm) π π* bliski nadfiolet jednostki energii atomowa jednostka energii = energia
STEREOCHEMIA ORGANICZNA
 STERECEMIA RGANICZNA Sławomir Jarosz Wykład 6 Jak otrzymać związki optycznie czynne??? 1. Ze związków chiralnych a. Klasyczny : A (rac) b. Rozdział mieszaniny racemicznej na CIRALNEJ kolumnie (Y. kamoto,
STERECEMIA RGANICZNA Sławomir Jarosz Wykład 6 Jak otrzymać związki optycznie czynne??? 1. Ze związków chiralnych a. Klasyczny : A (rac) b. Rozdział mieszaniny racemicznej na CIRALNEJ kolumnie (Y. kamoto,
Synteza Nanoproszków Metody Chemiczne II
 Synteza Nanoproszków Metody Chemiczne II Bottom Up Metody chemiczne Wytrącanie, współstrącanie, Mikroemulsja, Metoda hydrotermalna, Metoda solwotermalna, Zol-żel, Synteza fotochemiczna, Synteza sonochemiczna,
Synteza Nanoproszków Metody Chemiczne II Bottom Up Metody chemiczne Wytrącanie, współstrącanie, Mikroemulsja, Metoda hydrotermalna, Metoda solwotermalna, Zol-żel, Synteza fotochemiczna, Synteza sonochemiczna,
Syntezy stereoselektywne
 Syntezy stereoselektywne a b d d a b e d a b d e a b d podstawienie addycja enancjomery z substratów achiralnych diastereoizomery z substratów chiralnych : S : a b : S a b S : a b a C b C C d d a C b C
Syntezy stereoselektywne a b d d a b e d a b d e a b d podstawienie addycja enancjomery z substratów achiralnych diastereoizomery z substratów chiralnych : S : a b : S a b S : a b a C b C C d d a C b C
ALKENY WĘGLOWODORY NIENASYCONE
 Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami
 Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami I. Otrzymywanie halogenowęglowodorów 1. Reakcje halogenacji (substytucji rodnikowej halogenów (Cl, ) na
Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami I. Otrzymywanie halogenowęglowodorów 1. Reakcje halogenacji (substytucji rodnikowej halogenów (Cl, ) na
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania
 Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
Wojewódzki Konkurs Przedmiotowy. dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2013/2014
 Wojewódzki Konkurs Przedmiotowy z Chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2013/2014 KOD UCZNIA Etap: Data: Czas pracy: Rejonowy 17 stycznia 2014 90 minut Informacje dla ucznia
Wojewódzki Konkurs Przedmiotowy z Chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2013/2014 KOD UCZNIA Etap: Data: Czas pracy: Rejonowy 17 stycznia 2014 90 minut Informacje dla ucznia
PL B1. UNIWERSYTET IM. ADAMA MICKIEWICZA W POZNANIU, Poznań, PL BUP 24/17
 RZECZPOSPOLITA POLSKA (2) OPIS PATENTOWY (9) PL () 229709 (3) B (2) Numer zgłoszenia: 49663 (5) Int.Cl. C07F 7/30 (2006.0) Urząd Patentowy Rzeczypospolitej Polskiej (22) Data zgłoszenia: 05.2.206 (54)
RZECZPOSPOLITA POLSKA (2) OPIS PATENTOWY (9) PL () 229709 (3) B (2) Numer zgłoszenia: 49663 (5) Int.Cl. C07F 7/30 (2006.0) Urząd Patentowy Rzeczypospolitej Polskiej (22) Data zgłoszenia: 05.2.206 (54)
Alkeny C n H 2n. podstawiony penten CH 3 CH 2 CH 3 CH 2 CH 2 C CH 2
 Alkeny n 2n Nazewnictwo: 1. Znajdź najdłuższy łańcuch węglowy zawierający wiązanie podwójne i nazwij odpowiednio związek, kończąc nazwę przyrostkiem -en 3 2 3 2 2 2 3 2 3 2 2 2 3 2 2 3 2 2 podstawiony
Alkeny n 2n Nazewnictwo: 1. Znajdź najdłuższy łańcuch węglowy zawierający wiązanie podwójne i nazwij odpowiednio związek, kończąc nazwę przyrostkiem -en 3 2 3 2 2 2 3 2 3 2 2 2 3 2 2 3 2 2 podstawiony
Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku
 Streszczenie pracy doktorskiej Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku mgr Agata Dudek Promotor: prof. dr hab. Jacek Młynarski Praca została wykonana w Zespole Stereokotrolowanej
Streszczenie pracy doktorskiej Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku mgr Agata Dudek Promotor: prof. dr hab. Jacek Młynarski Praca została wykonana w Zespole Stereokotrolowanej
Nazwa przedmiotu (w języku. CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot
 Nazwa pola Komentarz Nazwa (w języku CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot CBMiM PAN Liczba punktów ECTS 5 Sposób zaliczenia Egzamin Język wykładowy
Nazwa pola Komentarz Nazwa (w języku CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot CBMiM PAN Liczba punktów ECTS 5 Sposób zaliczenia Egzamin Język wykładowy
Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna (0310-CH-S1-026) Nazwa wariantu modułu (opcjonalnie):
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Heteroatomowe analogi cyklopropenonu
 RACE AUKWE Akademii im. Jana Długosza w Częstochowie eria: CEMIA I CRA ŚRDWIKA 2008, XII, 83-89 Adrian Zając a,b Józef Drabowicz a,b a Instytut Chemii i chrony Środowiska, Akademia im. Jana Długosza, 42
RACE AUKWE Akademii im. Jana Długosza w Częstochowie eria: CEMIA I CRA ŚRDWIKA 2008, XII, 83-89 Adrian Zając a,b Józef Drabowicz a,b a Instytut Chemii i chrony Środowiska, Akademia im. Jana Długosza, 42
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Mechanizm dehydratacji alkoholi
 Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Struktura elektronowa
 Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
KOLOKWIUM II - ROZWIĄZANIA Chemia organiczna B,
 KLKWIUM II - RZWIĄZANIA Chemia organiczna B, 0..008 Zad.. (0 p.) Przedstaw mechanizmy następujących reakcji. W punktach a-c należy posłużyć się wzorami przestrzennymi lub krzesłowymi. a) (R)--fenylobutan--ol
KLKWIUM II - RZWIĄZANIA Chemia organiczna B, 0..008 Zad.. (0 p.) Przedstaw mechanizmy następujących reakcji. W punktach a-c należy posłużyć się wzorami przestrzennymi lub krzesłowymi. a) (R)--fenylobutan--ol
PODSTAWY CHEMII ANALITYCZNEJ. Miareczkowanie kompleksometryczne
 PODSTAWY CHEMII ANALITYCZNEJ Miareczkowanie kompleksometryczne CYJANKI / ARGENTOMETRIA VOLHARD Miareczkowanie 1: znany nadmiar Ag + (środowisko obojętne!!) Ag + + CN - AgCN Oddzielić osad AgCN!! CN - +
PODSTAWY CHEMII ANALITYCZNEJ Miareczkowanie kompleksometryczne CYJANKI / ARGENTOMETRIA VOLHARD Miareczkowanie 1: znany nadmiar Ag + (środowisko obojętne!!) Ag + + CN - AgCN Oddzielić osad AgCN!! CN - +
 Ę Ę Ę ż Ę Ę Ł Ż Ż ż Ę ż Ę Ż ź Ż Ź Ż Ł Ł Ż Ż Ż Ą Ą Ą ż Ż Ę Ę Ę Ą Ę ż ż Ę ż ź Ą Ć Ł Ż Ę ź Ś Ż Ż Ś Ł Ę Ę Ó Ł Ę Ę Ń Ę Ż Ż Ą ź Ż Ż Ż Ą Ę Ż Ł Ż ź Ż ź Ń Ą Ę Ę Ó Ę ż Ż ż ż ż Ł Ł Ą Ó ż Ż Ż Ę ż Ę Ż Ż Ż ź ż Ż Ż
Ę Ę Ę ż Ę Ę Ł Ż Ż ż Ę ż Ę Ż ź Ż Ź Ż Ł Ł Ż Ż Ż Ą Ą Ą ż Ż Ę Ę Ę Ą Ę ż ż Ę ż ź Ą Ć Ł Ż Ę ź Ś Ż Ż Ś Ł Ę Ę Ó Ł Ę Ę Ń Ę Ż Ż Ą ź Ż Ż Ż Ą Ę Ż Ł Ż ź Ż ź Ń Ą Ę Ę Ó Ę ż Ż ż ż ż Ł Ł Ą Ó ż Ż Ż Ę ż Ę Ż Ż Ż ź ż Ż Ż
Elektrochemia - szereg elektrochemiczny metali. Zadania
 Elektrochemia - szereg elektrochemiczny metali Zadania Czym jest szereg elektrochemiczny metali? Szereg elektrochemiczny metali jest to zestawienie metali według wzrastających potencjałów normalnych. Wartości
Elektrochemia - szereg elektrochemiczny metali Zadania Czym jest szereg elektrochemiczny metali? Szereg elektrochemiczny metali jest to zestawienie metali według wzrastających potencjałów normalnych. Wartości
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA
 Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
10. Alkeny wiadomości wstępne
 0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
