Reumatoidalne zapalenie stawów (RZS) jest przewlekłą
|
|
|
- Bogna Komorowska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Tocilizumab pierwsze przeciwciało monoklonalne blokujące receptor interleukiny 6 w leczeniu reumatoidalnego zapalenia stawów Maria Jarecka 1, Piotr Borowicz 2 1 Dział Informacji Naukowej i Medycznej Instytutu Biotechnologii i Antybiotyków w Warszawie 2 Instytut Biotechnologii i Antybiotyków w Warszawie Adres do korespondencji: Maria Jarecka, Instytut Biotechnologii i Antybiotyków, Warszawa, ul. Starościńska 5, e mail: jareckam@iba.waw.pl Reumatoidalne zapalenie stawów (RZS) jest przewlekłą chorobą zapalną o podłożu autoimmunizacyjnym, w przebiegu której rozwija się zapalenie błony maziowej i postępuje proces destrukcji chrząstki i stawów. W patogenezie reumatoidalnego zapalenia stawów istotną rolę przypisuje się cytokinom. Kontrolują one wszystkie fazy odpowiedzi immunologicznej oraz wpływają na proces zapalny. Ze względu na właściwości dzielimy je na cytokiny prozapalne i przeciwzapalne, jakkolwiek, w zależności od typu odpowiedzi immunologicznej lub fazy procesu zapalnego, mogą wykazywać właściwości charakterystyczne dla obu grup. W chorobach reumatycznych nadmierne wytwarzanie wielu cytokin oraz niedobór cytokin immunoregulacyjnych sprzyjają progresji odpowiedzi zapalnej w fazę przewlekłą, rozwojowi zjawisk autoimmunizacyjnych i procesom destrukcyjnym. Prozapalnymi cytokinami, które odgrywają kluczową rolę w patogenezie RZS są: czynnik martwicy nowotworów (TNF-α), interleukina 1 (IL-1) oraz interleukina 6 (IL-6). Wprowadzone w ciągu ostatnich lat leki ingerujące w poziom cytokin, w tym preparaty uzyskane drogą rekombinacji DNA i technik przeciwciał monoklonalnych z zastosowaniem inżynierii genetycznej stały się obecnie alternatywą w leczeniu wielu chorób zapalnych o podłożu autoimmunologicznym, a przede wszystkim zajęły istotną pozycję w terapii reumatoidalnego zapalenia stawów. Interleukina 6 ogólna charakterystyka Jedną z cytokin, której przypisuje się istotną rolę w patogenezie reumatoidalnego zapalenia stawów jest interleukina 6. Interleukina 6 jest glikozylowanym Tocilizumab the first monoclonal antibodies blocking IL-6 receptor in the treatment of rheumatoid arthritis Interleukin-6 (IL-6) is a pleiotropic cytokine involved in the pathogenesis of rheumatoid arthritis (RA) and other autoimmune diseases. IL-6 regulates immune response and inflammation. Tocilizumab, a humanized anti-il-6 receptor monoclonal antibody, binds both soluble and membrane expressed IL-6R, inhibiting IL-6-mediated biological activity. In patients with moderate to severe active RA responding inadequately or who are intolerant to disease-modifying antirheumatic drugs (DMARD) or tumor necrosis factor (TNF) antagonists, tocilizumab,administered either as monotherapy or in combination with conventional DMARDs is effective and generally safe option for the treatment of rheumatoid arthritis. Keywords: Tocilizumab, interleukin-6, rheumatoid arthritis. Farm Pol, 2010, 66(3): polipeptydem zbudowanym ze 184 aminokwasów o ciężarze cząsteczkowym kda i tworzącym 4 długie helisy α połączone pętlami. Interleukina 6 należy do grupy cytokin, które oddziałują na komórki poprzez receptory zbudowane z różnych łańcuchów α (80 kda) oraz identycznego łańcucha β o ciężarze cząsteczkowym 130 kda. Łańcuch α wiąże swoiście daną cytokinę, a łańcuch β przekazuje sygnał aktywacyjny do wnętrza komórki. Interleukina 6 jest cytokiną prozapalną, wykazującą zdolność do wielokierunkowego działania. Najważniejszym jej zadaniem jest udział w odpowiedzi immunologicznej, krwiotworzeniu oraz reakcjach zapalnych. Wytwarzana jest przez różne rodzaje komórek: limfocyty T i B, monocyty, makrofagi, fibroblasty, komórki śródbłonka, keranocyty, osteoblasty, 193
2 W patogenezie reumatoidalnego zapalenia stawów istotną rolę przypisuje się cytokinom. Kontrolują one wszystkie fazy odpowiedzi immunologicznej oraz wpływają na proces zapalny. Ze względu na właściwości dzielimy je na cytokiny prozapalne i przeciwzapalne, jakkolwiek, w zależności od typu odpowiedzi immunologicznej lub fazy procesu zapalnego, mogą wykazywać właściwości charakterystyczne dla obu grup. chondrocyty oraz komórki owodni. Głównym czynnikiem stymulującym wytwarzanie IL-6 jest interleukina 1 oraz interferony, czynniki martwicy nowotworów, lipopolisacharydy i wirusy. Działając wielokierunkowo wywiera różnorodne efekty biologiczne. Działa przede wszystkim na limfocyty B, jako czynnik stymulujący ich końcowe różnicowanie w kierunku komórek uwalniających immunoglobuliny różnych klas, a ponadto wpływa na limfocyty T poprzez pobudzanie do produkcji IL-2 i syntezy jej receptora. Wraz z IL-1 aktywuje limfocyty T rozpoznające antygeny oraz stymuluje powstawanie i różnicowanie limfocytów cytotoksycznych. Wykazano także stymulujący wpływ interleukiny 6 na aktywację limfocytów T przez monocyty. Synergistycznie z IL-3 interleukina 6 pobudza krwiotworzenie [1, 2]. Interleukina 6 odgrywa istotną i różnorodną funkcję w rozwoju chorób zapalnych i infekcyjnych. W stanach zapalnych stężenie IL-6 w surowicy chorego może zwiększyć się nawet 100-krotnie, stąd uważana jest za wczesny i czuły, ale niespecyficzny wskaźnik reakcji zapalnych toczących się w organizmie. W ostrym zapaleniu ogranicza reakcje zapalne, natomiast w zapaleniu przewlekłym działa prozapalnie. Zwiększone stężenia IL-6 wykryto w różnych przewlekłych chorobach zapalnych, takich jak: RZS, zesztywniające zapalenie stawów, młodzieńcze idiopatyczne zapalenie stawów, toczeń rumieniowaty układowy, łuszczyca, a także w innych chorobach o podłożu immunologicznym chorobie Crohna i chorobie Castelmana. Interleukina 6, odgrywająca kluczową rolę w patogenezie reumatoidalnego zapalenia stawów, pobudza proliferację fibroblastów błony maziowej, nasila ekspresję VRGF (czynnik wzrostu śródbłonka naczyniowego) i neoangiogenezę, indukuje ekspresję czynników hamujących apoptozę komórek, stymuluje napływ komórek zapalnych i wpływa na destrukcję kości [3, 4, 5, 6]. Wykazano, że IL-6 syntetyzowana jest przez różne komórki w zmienionych zapalnie stawach: fibroblasty, synowiocyty, limfocyty i monocyty oraz komórki śródbłonka. Jest głównym mediatorem miejscowego i ogólnoustrojowego procesu zapalnego w RZS. U osób chorych na RZS obserwuje się zwiększone stężenia IL-6 zarówno w surowicy, jak i w płynie stawowym, przy czym stężenie IL-6 w płynie stawowym przewyższa stężenie w surowicy, co świadczy o lokalnej syntezie tej cytokiny. Nadprodukcja tej cytokiny jest ściśle związana z objawami patologicznymi RZS, a zwyżki jej stężenia w surowicy i płynie stawowym towarzyszą zwiększeniu aktywności choroby i radiologicznych cech uszkodzenia stawów. Poza działaniem miejscowym interleukina 6 odpowiada za objawy ogólnoustrojowe RZS, takie jak: wystąpienie gorączki, wtórną amyloidazę i anemię, czy syntezę białek ostrej fazy w wątrobie, zwłaszcza białka CRP [2, 3, 7]. Tocilizumab Tocilizumab (RoActemra ) jest rekombinowanym humanizowanym przeciwciałem monoklonalnym skierowanym przeciwko receptorowi dla interleukiny 6, wytwarzanym w komórkach jajnika chomika chińskiego (CHO) z zastosowaniem technologii inżynierii genetycznej. Tocilizumab wiąże się swoiście zarówno z rozpuszczalnym (sil-6r), jak i związanym z błoną komórkową (mil-6r) receptorem dla IL-6, blokując przekazywanie sygnału do komórki docelowej, co prowadzi do zahamowania prozapalnej aktywności interleukiny 6. Jest pierwszym na świecie i dotychczas jedynym w swojej klasie lekiem hamującym biologiczne działanie IL-6. Tocilizumab, w skojarzeniu z metotreksatem, wskazany jest w leczeniu dorosłych pacjentów z czynnym reumatoidalnym zapaleniem stawów o nasileniu umiarkowanym do ciężkiego, u których stwierdzono niewystarczającą odpowiedź na leczenie lub nietolerancję dotychczasowego leczenia jednym lub kilkoma lekami modyfikującymi przebieg choroby (LMPCh) lub inhibitorami TNFα. Tocilizumab może być podawany w monoterapii w przypadku nietolerancji metotreksatu lub u pacjentów, u których kontynuacja leczenia metotreksatem nie jest wskazana [8]. Przegląd badań klinicznych W ciągu ostatnich lat opublikowano szereg prac, w tym przeglądowych [3, 4, 9, 10, 11] oceniających skuteczność i bezpieczeństwo działania tocilizumabu u chorych z czynną postacią reumatoidalnego zapalenia stawów. Były to wieloośrodkowe, randomizowane badania kliniczne II i III fazy prowadzone metodą podwójnie ślepej próby z kontrolą placebo. Objęci badaniami chorzy wykazywali niewystarczającą odpowiedź kliniczną lub nietolerancję na stosowane dotychczas leczenie przeciwreumatyczne, jednym lub wieloma lekami z grupy LMPCh lub grupy inhibitorów TNFα. W randomizowanym, prowadzonym metodą podwójnie ślepej próby i kontrolowanym placebo europejskim badaniu II fazy CHARISMA [12] wzięło udział 359 pacjentów z czynnym RZS i niewystarczającą odpowiedzią na leczenie metotreksatem. Chorych randomizowano do następujących grup: tocilizumab w dawkach 2, 4 lub lub podawany we wlewie i.v. 1 raz na 4 tygodnie w monoterapii lub terapii skojarzonej z metotreksatem w dawce 194
3 10 25 mg/tydzień oraz placebo z metotreksatem. Głównym punktem końcowym był odsetek chorych, którzy uzyskali odpowiedź na leczenie według kryteriów ACR20 w 16 tygodniu badania. Odpowiedź ACR20 osiągnięto u 61% i 63% pacjentów otrzymujących odpowiednio 4 mg i tocilizumabu w monoterapii i u 63% i 74% pacjentów, którzy otrzymali powyższe dawki tocilizumabu w połączeniu z metotreksatem oraz u 41% chorych z grupy placebo i metotreksat. Tocilizumab był na ogół dobrze tolerowany. Do najczęściej występujących działań niepożądanych należały zakażenia, zaburzenia dotyczące układu mięśniowo-szkieletowego, zaburzenia ze strony przewodu pokarmowego, wysypka skórna, świąd i rumień. U 30 pacjentów wystąpiło 35 ciężkich zdarzeń niepożądanych, przy czym częstość ich występowania była największa w grupie chorych otrzymujących tocilizumab w monoterapii, w dawce 2 mg/kg m.c., a najmniejsza w grupie pacjentów leczonych tocilizumabem, w dawce 4 mg/kg m.c., w skojarzeniu z metotreksatem. Obserwowano, zależny od dawki wzrost poziomu enzymów wątrobowych aminotransferazy alaninowej i w mniejszym stopniu asparginianowej oraz stężenia cholesterolu całkowitego, HDL i trójglicerydów. Ponadto notowano przejściowe, zależne od dawki obniżenie liczby neutrofili. W wieloośrodkowym badaniu III fazy SATORI [13] prowadzonym w Japonii oceniano skuteczność i bezpieczeństwo działania tocilizumabu podawanego w monoterapii u 125 pacjentów z czynną postacią RZS, którzy nie odpowiedzieli wystarczająco na niską (8 mg/tydzień) dawkę metotreksatu. Chorych randomizowano do grupy otrzymującej tocilizumab w dawce co 4 tygodnie bądź metotreksat w dawce 8 mg/tydzień (grupa kontrolna). Pierwszorzędowym punktem końcowym był odsetek pacjentów, u których uzyskano odpowiedź na leczenie według kryterium ACR20 po 24 tygodniach, a dodatkowe punkty końcowe stanowiły ACR50 i ACR70, DAS28 i poprawa wg kryteriów EULAR. W 24 tygodniu badania wskaźnik ACR20 osiągnięto u 80,3% chorych leczonych tocilizumabem w porównaniu z 25.0% pacjentów z grupy kontrolnej. Większość działań niepożądanych była łagodna do umiarkowanych. Występowały one częściej w grupie chorych otrzymujących tocilizumab, z czego najczęstszymi były: zapalenie jamy nosowej i gardła (18% vs 10.9%), zapalenie jamy ustnej (11.5% vs 0). Ciężkie zdarzenia niepożądane wystąpiły u 4.7% chorych z grupy kontrolnej i u 6.6% pacjentów leczonych tocilizumabem. W grupie tocilizumabu notowano częstsze zmiany metabolizmu lipidów, takie jak: wzrost stężenia cholesterolu całkowitego (36% chorych), trójglicerydów (19.7% chorych) oraz cholesterolu LDL (27.9% chorych), które w trakcie badania ulegały stabilizacji w górnym zakresie wartości prawidłowych. Z kolei, większy odsetek pacjentów w grupie chorych otrzymujących metotreksat w porównaniu z leczonymi tocilizumabem miało podwyższoną aktywność AST (8% vs 3%), ALT (11% vs 5%) i stężenie bilirubiny całkowitej (2% vs 0%). Wartości te nie miały tendencji zwyżkowej i w grupie tocilizumabu uległy stabilizacji w 16 tygodniu badania. Badanie III fazy SAMURAI [14] przeprowadzono w 28 ośrodkach w Japonii. Objęto nim 302 chorych z czynnym RZS trwającym średnio 2,3 lat, punktacji w skali DAS 28 6,5, wartości CRP 48 mg/l i średniej całkowitej punktacji w skali Sharpa 29,4. Pacjentom podawano tocilizumab w dawce co 4 tygodnie (n=157) lub konwencjonalne leki z grupy LMPCh, do których należał metotreksat w monoterapii lub w skojarzeniu z innym lekiem (n=145). Po 52 tygodniach oceniano skuteczność tocilizumabu w hamowaniu postępu strukturalnego uszkodzenia stawów na podstawie zdjęć rentgenowskich rąk i stóp, ocenianych metodą Sharpa w modyfikacji van der Tocilizumab jest Heijde. U chorych otrzymujących tocilizumab stwierdzono znacznie mniej- humanizowanym rekombinowanym szą progresję zmian radiologicznych przeciwciałem w porównaniu z pacjentami leczonymi klasycznymi LMPCh zarówno skierowanym przeciwko monoklonalnym w całkowitym wskaźniku Sharpa (2.3 receptorowi dla interleukiny vs 6.1), jak i w zmniejszeniu liczby 6, wytwarzanym nadżerek i zwężeń szpar stawowych. w komórkach jajnika Poważne działania niepożądane wystąpiły u 18% chorych leczonych toci- (CHO) z zastosowaniem chomika chińskiego lizumabem i u 13% pacjentów z grupy technologii inżynierii LMPCh. W grupie tocilizumabu najczęściej występowały: zapalenie jamy wiąże się swoiście zarówno genetycznej. Tocilizumab nosowej i gardła, wysypka, biegunka z rozpuszczalnym (sili ból głowy; w grupie LMPCh: zapalenie jamy nosowej i gardła, biegun- z błoną komórkową (mil- 6R), jak i związanym ka i zapalenie jamy ustnej. Większość 6R) receptorem dla IL-6, z nich miała charakter łagodny lub blokując przekazywanie umiarkowany. sygnału do komórki W badaniu III fazy AMBITION [15], docelowej, co prowadzi do trwającym 24 tygodnie, oceniano skuteczność i bezpieczeństwo działania aktywności interleukiny 6. zahamowania prozapalnej tocilizumabu podawanego w monoterapii, w porównaniu z monoterapią i dotychczas jedynym Jest pierwszym na świecie metotreksatem u chorych z czynnym w swojej klasie lekiem RZS i prawidłową odpowiedzią na hamującym biologiczne wcześniejsze leczenie metotreksatem działanie IL-6. lub lekiem biologicznym. W badaniu wzięło udział 673 pacjentów (nieleczonych metotreksatem w ciągu ostatnich 6 miesięcy), którym podawano tocilizumab w dawce co 4 tygodnie lub metotreksat raz na tydzień w dawce dobieranej indywidualnie, od 7,5 mg do maksymalnie 20 mg/tydzień przez 8 tygodni. Odsetek pacjentów, którzy po 24 tygodniach badania osiągnęli poprawę ACR20, ACR50 i ACR70 był znacząco wyższy w grupie leczonej tocilizumabem w porównaniu z grupą 195
4 Tabela 1. Tocilizumab: odsetek odpowiedzi ACR20, 50 i 70 w wybranych badaniach klinicznych Tydzień 1 Badanie I AMBITION MTX 2 + MTX Badanie II LITHE MTX + MTX Badanie III OPTION MTX + MTX Badanie IV RADIATE MTX + LMPCh 3 Badanie V TOWARD LMPCh N=286 N=284 N=398 N=393 N=205 N=204 N=170 N=158 N=803 N=413 ACR % 53% 56% 27% 59% 27% 50% 10% 61% 25% 52 56% 25% ACR % 34% 32% 10% 44% 11% 29% 4% 38% 9% 52 36% 10% ACR % 15% 13% 2% 22% 2% 12% 1% 21% 3% 52 20% 4% 1 tocilizumab; 2 MTX metotreksat; 3 LMPCh lek przeciwreumatyczny modyfikujący przebieg choroby; 4 Odsetek chorych, którzy uzyskują 20% (ACR20), 50% (ACR50), 70% (ACR70) poprawę, zgodnie z siedmioma klinicznymi i laboratoryjnymi parametrami aktywności choroby opracowanym przez American College of Rheumatology (ACR) Wyniki opublikowanych do tej pory badań klinicznych potwierdziły skuteczność i bezpieczeństwo stosowania tocilizumabu, podawanego w monoterapii lub w skojarzeniu z klasycznymi LMPCh, w leczeniu reumatoidalnego zapalenia stawów u chorych z niedostateczną odpowiedzią na terapie konwencjanalne LMPCh bądź niereagujących na inhibitory TNFα. Wykazano większą efektywność tego przeciwciała, w porównaniu z metotreksatem i innymi LMPCh, zarówno w zmniejszaniu aktywności RZS, jak i w hamowaniu zmian strukturalnych stawów oraz w poprawie sprawności funkcjonalnej i jakości życia pacjentów. otrzymującą metotreksat (odpowiednio 70% vs 53%, 44% vs 34% oraz 28% vs 15%). Podobnie odsetek pacjentów, u których stwierdzono remisję (DAS28<2,6) był istotnie wyższy wśród chorych otrzymujących tocilizumab (33,6%) w porównaniu z grupą otrzymującą metotreksat (12,1%), (tabela 1). U osób leczonych tocilizumabem od 2 tygodnia leczenia obserwowano normalizację średniego stężenia CRP i hemoglobiny. Częstość występowania ciężkich objawów niepożądanych i groźnych zakażeń wynosiła w przypadku tocilizumabu odpowiednio 3,8% i 1,4%, a w przypadku metotreksatu 2,8% i 0,7%. U pacjentów leczonych tocilizumabem częściej stwierdzano neutropenię (3,1% vs 0,4%) i podwyższony poziom całkowitego cholesterolu (13,2% vs 0,4%), natomiast zwiększenie stężenia aminotransferaz występowało rzadziej w porównaniu z grupą otrzymującą metotreksat (1,0% vs 2,5%). W badaniu III fazy LITHE [16] wzięło udział 1190 pacjentów ze 137 ośrodków w 15 krajach świata, włączając Stany Zjednoczone. Chorych, u których stwierdzono niedostateczną odpowiedź kliniczną na metotreksat, randomizowano do grupy otrzymującej 4 mg/kg m.c. (n=399) lub (n=398) tocilizumabu dożylnie co 4 tygodnie w połączeniu z metotreksatem (stała dawka od 10 do 25 mg na tydzień), albo do grupy (n=393) przyjmującej placebo z metotreksatem. Odsetki chorych, którzy po 52 tygodniach osiągnęli poprawę rzędu ACR 20, 50 i 70 były odpowiednio następujące: 56, 36 i 20 (dawka ) i 47, 29 i 16 (dawka 4 mg/kg m.c.) oraz 25, 10 i 4 w grupie otrzymującej sam metotreksat. Remisję kliniczną określoną jako DAS28<2,6, mierzoną po 52 tygodniach leczenia, uzyskało 47% i 30% otrzymujących odpowiednio i 4 mg/kg m.c. tocilizumabu i zaledwie 8% chorych z grupy kontrolnej (tabela 2). Ponadto w badaniu oceniano radiologicznie stopień postępu zmian stawowych i wyrażono jako zmianę w zmodyfikowanej całkowitej skali Sharpa i jej składowych liczbie nadżerek i zwężeń szpar stawowych. Zahamowanie niszczenia struktury stawu wykazano na podstawie istotnie mniejszej progresji radiologicznej u chorych otrzymujących tocilizumab z metotreksatem, w porównaniu z pacjentami leczonymi samym metotreksatem. W randomizowanym badaniu III fazy (OPTION) [17] prowadzonym metodą podwójnie ślepej próby i kontrolowanym placebo oceniano skuteczność tocilizumabu podawanego w skojarzeniu z metotreksatem, w porównaniu z działaniem metotreksatu u chorych z umiarkowaną lub ciężką postacią RZS i nieadekwatną odpowiedzią kliniczną na metotreksat. Badanie przeprowadzono w 73 ośrodkach na terenie 17 krajów z udziałem 623 pacjentów, których przydzielono do grup otrzymujących 4 mg/kg m.c. (n=214) i (n=205) tocilizumabu dożylnie co 4 tygodnie lub placebo (n=204) w skojarzeniu z metotreksatem w stałej dawce (od 10 do 25 mg na tydzień). Po 24 tygodniach u chorych leczonych tocilizumabem w dawce stwierdzono 196
5 Tabela 2. Kliniczna remisja DAS28<2.6 Badanie CHARISMA tocilizumab tocilizumab + metotreksat placebo + metotreksat po 16 tygodniach 17% 34% 8% Badanie SATORI tocilizumab metotreksat po 6 miesiącach 43,1% 1,6% Badanie SAMURAI tocilizumab LMPCh po 52 tygodniach 59% 3% Badanie AMBITION tocilizumab metotreksat po 24 tygodniach 33,6% 12,1% Badanie LITHE tocilizumab + metotreksat tocilizumab 4 mg/kg m.c. + metotreksat placebo + metotreksat po 52 tygodniach 47% 30% 8% Badanie OPTION tocilizumab + metotreksat tocilizumab 4 mg/kg m.c. + metotreksat metotreksat czy placebo po 24 tygodniach 27% 13% 1% Badanie RADIATE tocilizumab + metotreksat tocilizumab 4 mg/kg m.c. + metotreksat placebo + metotreksat po 24 tygodniach 51,2% 15,2% 4,9% Badanie TOWARD tocilizumab + LMPCh placebo + LMPCh po 24 tygodniach 30% 3% istotnie statystycznie większą częstość odpowiedzi na leczenie ACR 20, 50 i 70 w porównaniu do grupy kontrolnej. Wskaźniki ACR 20, 50 i 70 po 6 miesiącach wynosiły odpowiednio 59%, 44% i 22% dla dawki tocilizumabu, 48%, 31% i 12% dla dawki tocilizumabu 4 mg/kg m.c. oraz 26%, 11% i 2% w grupie placebo. Po 24 tygodniach uzyskano znacząco lepsze odpowiedzi we wszystkich głównych parametrach oceny zarówno w opinii lekarza, pacjenta, jak i w wynikach badań laboratoryjnych u chorych leczonych obydwoma dawkami tocilizumabu, w porównaniu z grupą kontrolną. Stężenie czynnika reumatoidalnego zmniejszyło się bardziej znacząco u chorych leczonych tocilizumabem w porównaniu z grupą placebo, a surowicze stężenia IgG i IgM były stabilne we wszystkich 3 grupach przez cały okres badania. U pacjentów otrzymujących tocilizumab uzyskano istotnie większą poprawę sprawności funkcjonalnej mierzonej punktacją HAQ oraz zmniejszenie poczucia zmęczenia i poprawę jakości życia, w porównaniu z grupą kontrolną. Co najmniej jedno zdarzenie niepożądane zgłosiła większa liczba pacjentów otrzymujących tocilizumab niż pacjenci otrzymujący placebo: 69% w grupie stosującej dawkę, 71% w grupie stosującej dawkę 4 mg/kg m.c. i 63% w grupie placebo. Wśród zdarzeń niepożądanych występujących z częstością 5% lub więcej dowolne zakażenie lub infekcję pasożytniczą notowano u 32%, 31% i 27% chorych leczonych odpowiednio dawkami i 4 mg/kg m.c. oraz otrzymujących placebo. Najczęściej obserwowano infekcje górnych dróg oddechowych. Największe różnice względem grupy placebo stwierdzono w przypadku zaburzeń dotyczących skóry i tkanki podskórnej (18% vs 13% vs 7%). W trakcie badania nie notowano aktywacji utajonego zakażenia Mycobacterium tuberculosis. Przejściowy wzrost stężenia aminotransferaz wątrobowych, wzrost stężenia lipidów lub przejściowy spadek bezwzględnej liczby neutrofili zgłaszano częściej wśród chorych leczonych tocilizumabem niż w grupie placebo. Częstość występowania ciężkich zdarzeń niepożądanych była zbliżona we wszystkich trzech grupach (około 6%). Większość tych zdarzeń wystąpiła tylko raz, a 11 spośród 41 ciężkich zdarzeń niepożądanych wymagało przerwania leczenia. W badaniu III fazy (RADIATE) [18] oceniano skuteczność i bezpieczeństwo działania tocilizumabu u 499 chorych z niedostateczną odpowiedzią kliniczną lub nietolerancją jednego lub więcej leków z grupy inhibitorów TNF. Pacjentom podawano tocilizumab w dawce 4 mg/kg m.c. i lub placebo raz na cztery tygodnie przez 6 miesięcy, w skojarzeniu ze stałymi dawkami metotreksatu (od 10 do 25 mg na tydzień). Po 24 tygodniach odpowiedzi ACR20 uzyskano u 50,0%, 30,4% i 10,1% pacjentów otrzymujących odpowiednio 8,0 i 4,0 mg/kg m.c. tocilizumabu oraz placebo. Zaobserwowano istotną poprawę w zakresie funkcjonowania fizycznego, ocenianą na podstawie średniej różnicy w stosunku do wartości wyjściowej, mierzonej kwestionariuszem HAQ po zastosowaniu tocilizumabu w dawce 8,0 i 4,0 mg/kg m.c. odpowiednio ( 0,39 vs 0,31), w porównaniu z grupą kontrolną otrzymującą placebo ( 0,05). Ogólna częstość występowania zdarzeń niepożądanych o nasileniu łagodnym lub umiarkowanym była podobna we wszystkich 3 grupach badanych chorych. Ciężkie zdarzenia niepożądane występowały częściej u chorych otrzymujących placebo (11,3%) w porównaniu z otrzymującymi 8,0 mg/kg m.c. (6,3%) i 4,0 mg/kg m.c. (7,4%) tocilizumabu. Z kolei zakażenia, zaburzenia ze strony przewodu pokarmowego oraz skóry i tkanki podskórnej obserwowano częściej 197
6 u pacjentów leczonych tocilizumabem w porównaniu z grupą kontrolną. Wieloośrodkowe (n=130), prowadzone w 18 krajach badanie kliniczne III fazy TOWARD [19] prowadzone było metodą podwójnie ślepej próby z randomizacją i kontrolowaną placebo. Dotyczyło ono 1220 pacjentów z umiarkowanym lub ciężkim reumatoidalnym zapaleniem stawów, trwającym 6 miesięcy i z niewystarczającą odpowiedzią na stosowane dotychczas leczenie, obejmujące jeden lub więcej leków z grupy LMPCh. Pacjenci, randomizowani w stosunku 2:1, otrzymywali tocilizumab (n=805) w dawce lub placebo (n=415), raz na 4 tygodnie przez 6 miesięcy w skojarzeniu z lekami z grupy LMPCh w stałych dawkach. Pierwszorzędowym punktem końcowym badania był odsetek pacjentów, którzy uzyskali odpowiedź na leczenie zgodnie z kryteriami ACR dla poprawy o 20% (ACR20) w 24 tygodniu badania. Drugorzędowymi punktami były ACR50 i ACR70 w 24 tygodniu oraz czas do uzys kania poprawy ACR 20/50/70. W 24 tygodniu odpowiedź ACR20 stwierdzono w grupie otrzymującej tocilizumab i grupie kontrolnej, odpowiednio u 60,8% i 24,5% pacjentów, ACR50 u 37,6% i 9,0% pacjentów oraz ACR70 u 20,5% i 2,9% badanych chorych. Ciężkie objawy niepożądane notowano u 6,7% chorych otrzymujących tocilizumab i u 4,3% chorych otrzymujących placebo. Ogólnie częstość występowania zakażeń związana z podawaniem tocilizumabu lub placebo wynosiła odpowiednio 37,4% i 31,6%. Zakażenia, których częstość występowania była większa w grupie leczonej tocilizumabem w porównaniu z grupą kontrolną, obejmowały zakażenia górnych dróg oddechowych (9% vs 7%), inne zakażenia dróg oddechowych (12% vs 10%) oraz zakażenia skóry i tkanki podskórnej (5% vs 3%). Większość pacjentów, u których wystąpiły zakażenia, kontynuowała leczenie. Częstość występowania ciężkich zakażeń wynosiła 3% w grupie tocilizumabu oraz 2% w grupie kontrolnej. Częstość występowania zaburzeń ze strony przewodu pokarmowego (20,8% vs 14.7%), skóry i tkanki podskórnej (16.6% vs 7.0%) oraz układu nerwowego (11,6% vs 8.7%) była wyższa w grupie otrzymującej tocilizumab, w porównaniu z grupą kontrolną. Wśród chorych leczonych tocilizumabem, częściej niż w grupie otrzymującej placebo, obserwowano przejściowe zwiększenie aktywności enzymów wątrobowych, któremu nie towarzyszyło klinicznie jawne zapalenie wątroby, zmniejszenie liczby neutrofili (bez związku z gorączką lub zakażeniami) oraz zwiększenie stężenia lipidów, w tym całkowitego cholesterolu, którego stężenie uległo normalizacji po podaniu statyn. Wyniki opublikowanych do tej pory badań klinicznych potwierdziły skuteczność i bezpieczeństwo stosowania tocilizumabu, podawanego w monoterapii lub w skojarzeniu z klasycznymi LMPCh, w leczeniu reumatoidalnego zapalenia stawów u chorych z niedostateczną odpowiedzią na terapie konwencjanalne LMPCh bądź niereagujących na inhibitory TNFα. Wykazano większą efektywność tego przeciwciała, w porównaniu z metotreksatem i innymi LMPCh, zarówno w zmniejszaniu aktywności RZS, jak i w hamowaniu zmian strukturalnych stawów oraz w poprawie sprawności funkcjonalnej i jakości życia pacjentów. Ponadto wykazano, że tocilizumab obok szybkiej poprawy klinicznej pozytywnie wpływa na poprawę parametrów laboratoryjnych, niekiedy obserwowaną już w drugim tygodniu leczenia. Przedstawione badania kliniczne wykazały korzystny profil bezpieczeństwa tocilizumabu stosowanego u chorych z wczesną lub długotrwającą postacią reumatoidalnego zapalenia stawów. Tocilizumab został zarejestrowany w Unii Europejskiej w styczniu 2009 roku. Otrzymano: Zaakceptowano: Piśmiennictwo 1. Łukaszewicz M., Mroczko B., Szmitkowski M.: Znaczenie kliniczne interleukiny 6 (IL-6) jako czynnika rokowniczego w chorobie nowotworowej. Pol. Arch. Med. Wewn. 2007, 117(5 6): Kontny E., Maśliński W.: Interleukina 6 znaczenie biologiczne i rola w patogenezie reumatoidalnego zapalenia stawów. Reumatologia, 2009, 47(1): Szmyrka-Kaczmarek M., Wiland P.: Tocilizumab inhibitor receptora interleukiny 6 nowa opcja terapeutyczna w leczeniu reumatoidalnego zapalenia stawów. Reumatologia, 2009, 47(2): Tuchocka A., Puszczewicz M.: Rola tocilizumabu w leczeniu reumatoidalnego zapalenia stawów na tle znaczenia patogenetycznego interleukiny 6 w rozwoju choroby. Reumatologia, 2008, 46(3): Leczenie biologiczne chorób reumatycznych. Red. Wiland P.: Termedia Wyd. Med., Poznań, Immunologia. Praca zbiorowa pod red. Jakóbisiaka M.: Wyd. Naukowe PWN, Warszawa, Cronstein B.N.: Interleukin-6 a key mediator of systemic and local symptoms in rheumatoid arthritis. Bull. NYU Hosp. Jt Dis. 2007, 65(Suppl. 1): S11 S EMEA charakterystyka produktu leczniczego. 9. Kalanethee P.-P.: Tocilizumab: blockade of interleukin-6 signaling pathway as a therapeutic strategy for inflammatory disorders. Drugs of Today 2006, 42(9): Oldfield V., Dhillon S., Plosker G.L.: Tocilizumab. A review of its use in the management of rheumatoid arthritis. Drugs, 2009, 69(5): da Silva A.F., Corte-Real S., Goncalves J.: Recombinant antibodies as therapeutic agents. Pathways for modeling new biodrugs. Biodrugs 2008, 22(5): Maini R.N., Taylor P.C., Szechinski J., Pavelka K., Broll J., Balint G., Emery P., Raemen F., Petersen J., Smolen J., Thomson D., Kishimoto T., for the CHARISMA Study Group: Double-blind randomized controlled clinical trial of the interleukin-6 receptor antagonist, tocilizumab, in european patients with rheumatoid arthritis who had an incomplete response to methotrexate. Arthritis & Rheumatism 2006, 54(9): Nishimoto N., Miyasaka N., Yamamoto K., Kawai S., Takeuchi T., Azuma J., Kishimoto T.: Study of active controlled tocilizumab monotherapy for rheumatoid arthritis patients with an inadequate response to methotrexate (SATORI): significant reduction in disease activity and serum vascular endothelial growth factor by IL-6 receptor inhibition therapy. Mod. Rheumatol. 2009, 19: Nishimoto N., Hashimoto J., Miyasaka N., Yamamoto K., kawai S., Takeuchi T., Murata N., van der Heijde D., Kishimoto T.: Study of active controlled monotherapy used for rheumatoid arthritis, an IL-6 inhibitor (SAMURAI): evidence of clinical and radiographic benefit from an x ray reader-blinded randomised controlled trial of tocilizumab. Ann. Rheum. Dis. 2007, 66: Jones G., Sebba A., Gu J., Lowenstein M.B., Calvo A., Gomez-Reino J.J., Siri DA, Tomsic M., Alecock E., Woodworth T., Genovese M.C.: 198
7 Comparison of toccilizumab monotherapy versus methotrexate monotherapy in patients with moderate to severe rheumatoid arthritis: The AMBITION study. Ann. Rheum. Dis. 2009, Mar Kremer J.M., Fleischmann R.M., Halland A.-M., et al.: Tocilizumab inhibits structural joint damage in rheumatoid arthritis patients with inadequate response to methotrexate: The LITHE Study. ACR/ARHP Annual Scientific Meeting, San Francisco, October 2008, Abstract L14 (LITHE). 17. Smolen J.S., Beaulieu A., Rubbert-Roth A., Ramos-Remus C., Rovensky J., Alecock E., Woodworth T., Alten R., for the OPTION Investigators: Effect of interleukin-6 receptor inhibition with tocilizumab in patients with rheumatoid arthritis (OPTION study): a double-blind, placebo-controlled, randomised trial. Lancet 2008, 371: Emery P., Keystone E., Tony H.P., Cantaagrel A., van Vollenhoven R., Sanchez A., Alecock E., Lee J., Kremer J.: Il-6 receptor inhibition with tocilizumab improves treatment outcomes in patients with rheumatoid arthritis refractory to anti-tumour necrosis factor biologicals: results from a 24-week multicentre randomised placebo-controlled trial. Ann. Rheum. Dis. 2008, 67: Genovese M.C., McKay J.D., Nasonov E.L., Mysler E.F., da Silva N.A., Alecock E., Woodworth T., Gomez-Reino J.J.: Interleukin-6 receptor inhibition with tocilizumab reduces disease activity in rheumatoid arthritis with inadequate response to disease-modifying antirheumatic drugs. The tocilizumab in combination with traditional disease-modifying antirheumatic drug therapy study. Arthritis & Rheumatism 2008, 58(1):
Długoterminowa skuteczność golimumabu u pacjentów z zapalnymi spondyloartropatiami wtorek, 03 lutego :06
 Skuteczność leczenia zapalnych chorób reumatycznych poprawiła się istotnie w ostatnich latach. Złożyło się na to wiele czynników, do których można zaliczyć wczesną diagnostykę i szybkie rozpoczynanie odpowiedniej
Skuteczność leczenia zapalnych chorób reumatycznych poprawiła się istotnie w ostatnich latach. Złożyło się na to wiele czynników, do których można zaliczyć wczesną diagnostykę i szybkie rozpoczynanie odpowiedniej
Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
Leczenie łuszczycowego zapalenia stawów biologicznymi lekami modyfikującymi
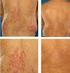 PRACA POGLĄDOWA Forum Reumatol. 2015, tom 1, nr 1, 25 29 Copyright 2015 Via Medica ISSN 2450 3088 Marcin Milchert, Marek Brzosko www.fr.viamedica.pl Klinika Reumatologii i Chorób Wewnętrznych, Pomorski
PRACA POGLĄDOWA Forum Reumatol. 2015, tom 1, nr 1, 25 29 Copyright 2015 Via Medica ISSN 2450 3088 Marcin Milchert, Marek Brzosko www.fr.viamedica.pl Klinika Reumatologii i Chorób Wewnętrznych, Pomorski
Simponi jest lekiem o działaniu przeciwzapalnym. Preparat stosuje się w leczeniu następujących chorób u osób dorosłych:
 EMA/411054/2015 EMEA/H/C/000992 Streszczenie EPAR dla ogółu społeczeństwa golimumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
EMA/411054/2015 EMEA/H/C/000992 Streszczenie EPAR dla ogółu społeczeństwa golimumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO
 Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO A. Kryteria kwalifikacji ŚWIADCZENIOBIORCY 1. Pacjent jest kwalifikowany
Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO A. Kryteria kwalifikacji ŚWIADCZENIOBIORCY 1. Pacjent jest kwalifikowany
"Ścieżka leczenia chorych na RZS w Polsce"
 "Ścieżka leczenia chorych na RZS w Polsce" Jakie bolączki często dotykają chorych na RZS w Polsce? Długi proces diagnozy i oczekiwania na wizytę u specjalisty reumatologa Małe możliwości diagnostyczne
"Ścieżka leczenia chorych na RZS w Polsce" Jakie bolączki często dotykają chorych na RZS w Polsce? Długi proces diagnozy i oczekiwania na wizytę u specjalisty reumatologa Małe możliwości diagnostyczne
LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06)
 Dziennik Urzędowy Ministra Zdrowia 614 Poz. 56 Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 614 Poz. 56 Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY
Konsensus dotyczący stosowania rituksymabu w leczeniu chorych na reumatoidalne zapalenie stawów
 Standardy leczenia/standards of treatment Reumatologia 2007; 45, 3: 115 119 Konsensus dotyczący stosowania rituksymabu w leczeniu chorych na reumatoidalne zapalenie stawów The consensus on rituximab administration
Standardy leczenia/standards of treatment Reumatologia 2007; 45, 3: 115 119 Konsensus dotyczący stosowania rituksymabu w leczeniu chorych na reumatoidalne zapalenie stawów The consensus on rituximab administration
Lek BI w porównaniu z lekiem Humira u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą
 Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Promotor: prof. dr hab. Katarzyna Bogunia-Kubik Promotor pomocniczy: dr inż. Agnieszka Chrobak
 INSTYTUT IMMUNOLOGII I TERAPII DOŚWIADCZALNEJ IM. LUDWIKA HIRSZFELDA WE WROCŁAWIU POLSKA AKADEMIA NAUK mgr Milena Iwaszko Rola polimorfizmu receptorów z rodziny CD94/NKG2 oraz cząsteczki HLA-E w patogenezie
INSTYTUT IMMUNOLOGII I TERAPII DOŚWIADCZALNEJ IM. LUDWIKA HIRSZFELDA WE WROCŁAWIU POLSKA AKADEMIA NAUK mgr Milena Iwaszko Rola polimorfizmu receptorów z rodziny CD94/NKG2 oraz cząsteczki HLA-E w patogenezie
PRZEGLĄD AKTUALNYCH NAJWAŻNIEJSZYCH WYDARZEŃ W REUMATOLOGII
 PRZEGLĄD AKTUALNYCH NAJWAŻNIEJSZYCH WYDARZEŃ W REUMATOLOGII Prof. dr hab. n med. Małgorzata Wisłowska Klinika Chorób Wewnętrznych i Reumatologii Centralnego Szpitala Klinicznego MSWiA Cytokiny Hematopoetyczne
PRZEGLĄD AKTUALNYCH NAJWAŻNIEJSZYCH WYDARZEŃ W REUMATOLOGII Prof. dr hab. n med. Małgorzata Wisłowska Klinika Chorób Wewnętrznych i Reumatologii Centralnego Szpitala Klinicznego MSWiA Cytokiny Hematopoetyczne
Zalecenia postępowania diagnostyczno-terapeutycznego Reumatologia 2016; supl. 1: DOI: /reum
 Zalecenia postępowania diagnostyczno-terapeutycznego Reumatologia 2016; supl. 1: 134 135 DOI: 10.5114/reum.2016.60016 Postępowanie okołooperacyjne w aloplastyce stawu biodrowego i kolanowego u chorych
Zalecenia postępowania diagnostyczno-terapeutycznego Reumatologia 2016; supl. 1: 134 135 DOI: 10.5114/reum.2016.60016 Postępowanie okołooperacyjne w aloplastyce stawu biodrowego i kolanowego u chorych
Porównanie zmian w programie lekowym B.33 w części dotyczącej MIZS przed i po 1 maja 2016
 Porównanie zmian w programie lekowym B.33 w części dotyczącej MIZS przed i po 1 maja 2016 OBOWIĄZUJE od 1 maja 2016 zmiany oznaczono kolorem 1. Kryteria kwalifikacji: 1. Kryteria kwalifikacji: Przed 1
Porównanie zmian w programie lekowym B.33 w części dotyczącej MIZS przed i po 1 maja 2016 OBOWIĄZUJE od 1 maja 2016 zmiany oznaczono kolorem 1. Kryteria kwalifikacji: 1. Kryteria kwalifikacji: Przed 1
NZJ- a problemy stawowe. Małgorzata Sochocka-Bykowska Wojewódzki Zespół Reumatologiczny w Sopocie
 NZJ- a problemy stawowe Małgorzata Sochocka-Bykowska Wojewódzki Zespół Reumatologiczny w Sopocie Przewlekłe nieswoiste zapalenia jelit charakteryzujące się występowaniem częstych powikłań jelitowych i
NZJ- a problemy stawowe Małgorzata Sochocka-Bykowska Wojewódzki Zespół Reumatologiczny w Sopocie Przewlekłe nieswoiste zapalenia jelit charakteryzujące się występowaniem częstych powikłań jelitowych i
LECZENIE BIOLOGICZNE CHORÓB
 LECZENIE BIOLOGICZNE CHORÓB REUMATYCZNYCH U PACJENTÓW 65+ Włodzimierz Samborski Katedra Reumatologii i Rehabilitacji Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu LECZENIE BIOLOGICZNE CHORÓB REUMATYCZNYCH
LECZENIE BIOLOGICZNE CHORÓB REUMATYCZNYCH U PACJENTÓW 65+ Włodzimierz Samborski Katedra Reumatologii i Rehabilitacji Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu LECZENIE BIOLOGICZNE CHORÓB REUMATYCZNYCH
1. NAZWA PRODUKTU LECZNICZEGO. RoActemra 162 mg roztwór do wstrzykiwań w ampułko-strzykawce. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 1. NAZWA PRODUKTU LECZNICZEGO RoActemra 162 mg roztwór do wstrzykiwań w ampułko-strzykawce. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda ampułko-strzykawka zawiera 162 mg tocilizumabu w 0,9 ml. Tocilizumab jest
1. NAZWA PRODUKTU LECZNICZEGO RoActemra 162 mg roztwór do wstrzykiwań w ampułko-strzykawce. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda ampułko-strzykawka zawiera 162 mg tocilizumabu w 0,9 ml. Tocilizumab jest
Leczenie Farmakologiczne
 www.printo.it/pediatric-rheumatology/pl/intro Leczenie Farmakologiczne Wersja 2016 13. Leki biologiczne W ciągu ostatnich lat pojawiły się nowe perspektywy leczenia dzięki nowym lekom określanym jako leki
www.printo.it/pediatric-rheumatology/pl/intro Leczenie Farmakologiczne Wersja 2016 13. Leki biologiczne W ciągu ostatnich lat pojawiły się nowe perspektywy leczenia dzięki nowym lekom określanym jako leki
UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA.
 UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA Małgorzata Biskup Czynniki ryzyka sercowo-naczyniowego u chorych na reumatoidalne zapalenie
UNIWERSYTET MEDYCZNY W LUBLINIE KATEDRA I KLINIKA REUMATOLOGII I UKŁADOWYCH CHORÓB TKANKI ŁĄCZNEJ PRACA DOKTORSKA Małgorzata Biskup Czynniki ryzyka sercowo-naczyniowego u chorych na reumatoidalne zapalenie
USG Power Doppler jest użytecznym narzędziem pozwalającym na uwidocznienie wzmożonego przepływu naczyniowego w synovium będącego skutkiem zapalenia.
 STRESZCZENIE Serologiczne markery angiogenezy u dzieci chorych na młodzieńcze idiopatyczne zapalenie stawów - korelacja z obrazem klinicznym i ultrasonograficznym MIZS to najczęstsza przewlekła artropatia
STRESZCZENIE Serologiczne markery angiogenezy u dzieci chorych na młodzieńcze idiopatyczne zapalenie stawów - korelacja z obrazem klinicznym i ultrasonograficznym MIZS to najczęstsza przewlekła artropatia
Leczenie biologiczne co to znaczy?
 Leczenie biologiczne co to znaczy? lek med. Anna Bochenek Centrum Badawcze Współczesnej Terapii C B W T 26 Październik 2006 W oparciu o materiały źródłowe edukacyjnego Grantu, prezentowanego na DDW 2006
Leczenie biologiczne co to znaczy? lek med. Anna Bochenek Centrum Badawcze Współczesnej Terapii C B W T 26 Październik 2006 W oparciu o materiały źródłowe edukacyjnego Grantu, prezentowanego na DDW 2006
Keytruda (pembrolizumab)
 EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0)
 Załącznik B.47. LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) Kwalifikacja do programu ŚWIADCZENIOBIORCY A. Kryteria kwalifikacji do leczenia ustekinumabem albo adalimumabem w ramach
Załącznik B.47. LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) Kwalifikacja do programu ŚWIADCZENIOBIORCY A. Kryteria kwalifikacji do leczenia ustekinumabem albo adalimumabem w ramach
LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD 10: L40.0)
 Załącznik B.47. LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD 10: L40.0) ŚWIADCZENIOBIORCY Kwalifikacja do programu A. Kryteria kwalifikacji do leczenia ustekinumabem w ramach programu 1.Do programu
Załącznik B.47. LECZENIE CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD 10: L40.0) ŚWIADCZENIOBIORCY Kwalifikacja do programu A. Kryteria kwalifikacji do leczenia ustekinumabem w ramach programu 1.Do programu
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO RoActemra 20 mg/ml koncentrat do sporządzania roztworu do infuzji. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml koncentratu zawiera
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO RoActemra 20 mg/ml koncentrat do sporządzania roztworu do infuzji. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml koncentratu zawiera
LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
 Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1)
Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1)
Czynniki wpływające na długość remisji po zakończeniu leczenia tocylizumabem u chorych na reumatoidalne zapalenie stawów
 Forum Reumatol. 2018, tom 4, nr 3, 158 162 Copyright 2018 Via Medica ISSN 2450 3088 DOI: 10.5603/FR.2018.0003 PRACA POGLĄDOWA www.fr.viamedica.pl Katarzyna Nowacka, Anna Wawryn-Ozdowy, Wojciech Romanowski
Forum Reumatol. 2018, tom 4, nr 3, 158 162 Copyright 2018 Via Medica ISSN 2450 3088 DOI: 10.5603/FR.2018.0003 PRACA POGLĄDOWA www.fr.viamedica.pl Katarzyna Nowacka, Anna Wawryn-Ozdowy, Wojciech Romanowski
LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
 Dziennik Urzędowy Ministra Zdrowia 570 Poz. 56 Załącznika B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
Dziennik Urzędowy Ministra Zdrowia 570 Poz. 56 Załącznika B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0)
 Załącznik B.47. LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) A. Kryteria kwalifikacjiś WIADCZENIOBIORCY 1. Pacjent jest kwalifikowany do programu przez Zespół Koordynacyjny
Załącznik B.47. LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) A. Kryteria kwalifikacjiś WIADCZENIOBIORCY 1. Pacjent jest kwalifikowany do programu przez Zespół Koordynacyjny
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 93/2011 Prezesa Agencji Oceny Technologii Medycznych z dnia 19 grudnia 2011 r. w sprawie zasadności zakwalifikowania świadczenia opieki
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 93/2011 Prezesa Agencji Oceny Technologii Medycznych z dnia 19 grudnia 2011 r. w sprawie zasadności zakwalifikowania świadczenia opieki
LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
 Dziennik Urzędowy Ministra Zdrowia 706 Poz. 71 Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
Dziennik Urzędowy Ministra Zdrowia 706 Poz. 71 Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
Leczenie biologiczne w nieswoistych zapaleniach jelit - Dlaczego? Co? Kiedy? VI Małopolskie Dni Edukacji w Nieswoistych Zapaleniach Jelit
 Leczenie biologiczne w nieswoistych zapaleniach jelit - Dlaczego? Co? Kiedy? VI Małopolskie Dni Edukacji w Nieswoistych Zapaleniach Jelit Co to są nieswoiste zapalenia jelit? Grupa chorób w których dochodzi
Leczenie biologiczne w nieswoistych zapaleniach jelit - Dlaczego? Co? Kiedy? VI Małopolskie Dni Edukacji w Nieswoistych Zapaleniach Jelit Co to są nieswoiste zapalenia jelit? Grupa chorób w których dochodzi
LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Dziennik Urzędowy Ministra Zdrowia 615 Poz. 27 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Dziennik Urzędowy Ministra Zdrowia 615 Poz. 27 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Aneks II Zmiany w drukach informacyjnych produktów leczniczych zarejestrowanych w procedurze narodowej
 Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną immunoglobulinę anty-t limfocytarną pochodzenia króliczego stosowaną u ludzi [rabbit anti-human thymocyte] (proszek
Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną immunoglobulinę anty-t limfocytarną pochodzenia króliczego stosowaną u ludzi [rabbit anti-human thymocyte] (proszek
Produkt RoActemra, w skojarzeniu z metotreksatem (MTX), jest wskazany:
 1. NAZWA PRODUKTU LECZNICZEGO RoActemra 162 mg roztwór do wstrzykiwań w ampułko-strzykawce. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda ampułko-strzykawka zawiera 162 mg tocilizumabu w 0,9 ml. Tocilizumab jest
1. NAZWA PRODUKTU LECZNICZEGO RoActemra 162 mg roztwór do wstrzykiwań w ampułko-strzykawce. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda ampułko-strzykawka zawiera 162 mg tocilizumabu w 0,9 ml. Tocilizumab jest
Rekombinowane leki biologiczne w terapii reumatoidalnego zapalenia stawów
 Rekombinowane leki biologiczne w terapii reumatoidalnego zapalenia stawów Maria Jarecka 1, Piotr Borowicz 2 1 Kierownik Działu Informacji Naukowej i Medycznej Instytutu Biotechnologii i Antybiotyków w
Rekombinowane leki biologiczne w terapii reumatoidalnego zapalenia stawów Maria Jarecka 1, Piotr Borowicz 2 1 Kierownik Działu Informacji Naukowej i Medycznej Instytutu Biotechnologii i Antybiotyków w
CZY PACJENTA Z REUMATOIDALNYM ZAPALENIEM STAWÓW MOŻNA LECZYĆ DWOMA LEKAMI BIOLOGICZNYMI JEDNOCZEŚNIE?
 ANNALES ACADEMIAE MEDICAE STETINENSIS ROCZNIKI POMORSKIEJ AKADEMII MEDYCZNEJ W SZCZECINIE 2010, 56, 1, 15 20 PIOTR LESZCZYŃSKI, KATARZYNA PAWLAK-BUŚ CZY PACJENTA Z REUMATOIDALNYM ZAPALENIEM STAWÓW MOŻNA
ANNALES ACADEMIAE MEDICAE STETINENSIS ROCZNIKI POMORSKIEJ AKADEMII MEDYCZNEJ W SZCZECINIE 2010, 56, 1, 15 20 PIOTR LESZCZYŃSKI, KATARZYNA PAWLAK-BUŚ CZY PACJENTA Z REUMATOIDALNYM ZAPALENIEM STAWÓW MOŻNA
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 12 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4,
Załącznik nr 12 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4,
LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Załącznik B.36. LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW ŚWIADCZENIOBIORCY W PROGRAMIE
Załącznik B.36. LECZENIE CIĘŻKIEJ, AKTYWNEJ POSTACI ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45) ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW ŚWIADCZENIOBIORCY W PROGRAMIE
LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Dziennik Urzędowy Ministra Zdrowia 732 Poz. 71 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Dziennik Urzędowy Ministra Zdrowia 732 Poz. 71 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie. Osoby należące do fachowego
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie. Osoby należące do fachowego
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Metotreksat - mity i fakty. Co o stosowaniu tego leku mówią badania środa, 02 lipca :47
 Metotreksat - podstawowy lek stosowany zgodnie z zaleceniami EULAR w pierwszej linii leczenia reumatoidalnego zapalenia stawów (RZS) - nie posiada ulotki przygotowanej dla pacjentów reumatoidalnych. Część
Metotreksat - podstawowy lek stosowany zgodnie z zaleceniami EULAR w pierwszej linii leczenia reumatoidalnego zapalenia stawów (RZS) - nie posiada ulotki przygotowanej dla pacjentów reumatoidalnych. Część
Dlaczego potrzebne było badanie?
 Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z łagodną postacią choroby Alzheimera oraz trudności z funkcjonowaniem psychicznym Jest to podsumowanie badania klinicznego
Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z łagodną postacią choroby Alzheimera oraz trudności z funkcjonowaniem psychicznym Jest to podsumowanie badania klinicznego
Produkt RoActemra, w skojarzeniu z metotreksatem (MTX), jest wskazany:
 1. NAZWA PRODUKTU LECZNICZEGO RoActemra 162 mg roztwór do wstrzykiwań w ampułko-strzykawce. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda ampułko-strzykawka zawiera 162 mg tocilizumabu w 0,9 ml. Tocilizumab jest
1. NAZWA PRODUKTU LECZNICZEGO RoActemra 162 mg roztwór do wstrzykiwań w ampułko-strzykawce. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda ampułko-strzykawka zawiera 162 mg tocilizumabu w 0,9 ml. Tocilizumab jest
LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
 Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) I. LEKI BIOLOGICZNE A. Kryteria kwalifikacji ŚWIADCZENIOBIORCY
Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) I. LEKI BIOLOGICZNE A. Kryteria kwalifikacji ŚWIADCZENIOBIORCY
CHOROBY REUMATYCZNE A OBNIŻENIE GĘSTOŚCI MINERALNEJ KOŚCI
 CHOROBY REUMATYCZNE A OBNIŻENIE GĘSTOŚCI MINERALNEJ KOŚCI Katarzyna Pawlak-Buś Katedra i Klinika Reumatologii i Rehabilitacji Uniwersytetu Medycznego w Poznaniu ECHA ASBMR 2018 WIELOCZYNNIKOWY CHARAKTER
CHOROBY REUMATYCZNE A OBNIŻENIE GĘSTOŚCI MINERALNEJ KOŚCI Katarzyna Pawlak-Buś Katedra i Klinika Reumatologii i Rehabilitacji Uniwersytetu Medycznego w Poznaniu ECHA ASBMR 2018 WIELOCZYNNIKOWY CHARAKTER
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte na kryteriach
(ICD-10 M 05, M 06, M 08)
 B.33. (ICD10 M 05, M 06, M 08) I. LEKI BIOLOGICZNE A. Kryteria kwalifikacji IADCZENIOBIORCY 1. Dawkowanie W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1. Badania przy kwalifikacji (leczenie
B.33. (ICD10 M 05, M 06, M 08) I. LEKI BIOLOGICZNE A. Kryteria kwalifikacji IADCZENIOBIORCY 1. Dawkowanie W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU 1. Badania przy kwalifikacji (leczenie
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie. Osoby należące do fachowego
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie. Osoby należące do fachowego
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Konsultacyjna Stanowisko Rady Konsultacyjnej nr 94/2011 z dnia 7 listopada 2011 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych/zmiany sposobu lub poziomu
Agencja Oceny Technologii Medycznych Rada Konsultacyjna Stanowisko Rady Konsultacyjnej nr 94/2011 z dnia 7 listopada 2011 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych/zmiany sposobu lub poziomu
Porównanie skuteczności leków adiuwantowych. w neuropatycznym bólu nowotworowym1
 Porównanie skuteczności leków adiuwantowych w neuropatycznym bólu nowotworowym1 Badanie1 New Delhi Cel Metoda Porównanie pregabaliny z amitryptyliną* i gabapentyną pod względem skuteczności klinicznej
Porównanie skuteczności leków adiuwantowych w neuropatycznym bólu nowotworowym1 Badanie1 New Delhi Cel Metoda Porównanie pregabaliny z amitryptyliną* i gabapentyną pod względem skuteczności klinicznej
LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
 Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) 1. Kryteria kwalifikacji: WIADCZENIOBIORCY 1)
Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) 1. Kryteria kwalifikacji: WIADCZENIOBIORCY 1)
Aneks III. Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa.
 Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa. Niniejszy dokument stanowi streszczenie Europejskiego Publicznego Sprawozdania Oceniajc ego (EPAR). Wyja nia, jak Komitet ds. Produktów Leczniczych
Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa. Niniejszy dokument stanowi streszczenie Europejskiego Publicznego Sprawozdania Oceniajc ego (EPAR). Wyja nia, jak Komitet ds. Produktów Leczniczych
 W badaniu 4S (ang. Scandinavian Simvastatin Survivat Study), oceniano wpływ symwastatyny na całkowitą śmiertelność u 4444 pacjentów z chorobą wieńcową i z wyjściowym stężeniem cholesterolu całkowitego
W badaniu 4S (ang. Scandinavian Simvastatin Survivat Study), oceniano wpływ symwastatyny na całkowitą śmiertelność u 4444 pacjentów z chorobą wieńcową i z wyjściowym stężeniem cholesterolu całkowitego
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cosentyx 150 mg proszek do sporządzania roztworu do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda fiolka z proszkiem zawiera
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cosentyx 150 mg proszek do sporządzania roztworu do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda fiolka z proszkiem zawiera
Efficacy and safety of TNF blockers in ankylosing spondylitis in randomized, controlled trials and prolonged open label studies
 Artykuł przeglądowy/review paper Reumatologia 2008; 46, 6: 361 366 Skuteczność i bezpieczeństwo inhibitorów TNF w leczeniu zesztywniającego zapalenia stawów kręgosłupa w świetle badań klinicznych z randomizacją
Artykuł przeglądowy/review paper Reumatologia 2008; 46, 6: 361 366 Skuteczność i bezpieczeństwo inhibitorów TNF w leczeniu zesztywniającego zapalenia stawów kręgosłupa w świetle badań klinicznych z randomizacją
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków
 Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie. Osoby należące do fachowego
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie. Osoby należące do fachowego
ostrym reumatoidalnym zapaleniem stawów (choroba powodująca stan zapalny stawów), gdzie produkt MabThera podaje się dożylnie z metotreksatem;
 EMA/614203/2010 EMEA/H/C/000165 Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/614203/2010 EMEA/H/C/000165 Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
Aneks II. Niniejsza Charakterystyka Produktu Leczniczego oraz ulotka dla pacjenta stanowią wynik procedury arbitrażowej.
 Aneks II Zmiany dotyczące odpowiednich punktów Charakterystyki Produktu Leczniczego oraz ulotki dla pacjenta przedstawione przez Europejską Agencję Leków (EMA) Niniejsza Charakterystyka Produktu Leczniczego
Aneks II Zmiany dotyczące odpowiednich punktów Charakterystyki Produktu Leczniczego oraz ulotki dla pacjenta przedstawione przez Europejską Agencję Leków (EMA) Niniejsza Charakterystyka Produktu Leczniczego
czerniak (nowotwór skóry), który rozprzestrzenił się lub którego nie można usunąć chirurgicznie;
 EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Rejestry w reumatologii Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób Wewnętrznych, Uniwersytet Medyczny im. Piastów Śląskich we
 Rejestry w reumatologii Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób Wewnętrznych, Uniwersytet Medyczny im. Piastów Śląskich we Wrocławiu Warszawa 8.10. 2014 1 Rejestry chorych leczonych
Rejestry w reumatologii Prof. dr hab. Piotr Wiland Katedra i Klinika Reumatologii i Chorób Wewnętrznych, Uniwersytet Medyczny im. Piastów Śląskich we Wrocławiu Warszawa 8.10. 2014 1 Rejestry chorych leczonych
Aktualne zasady diagnostyki i leczenia chorób zapalnych jelit
 Instytut Pomnik Centrum Zdrowia Dziecka Odział Gastroenterologii, Hepatologii, Zaburzeń Odżywiania i Pediatrii Al. Dzieci Polskich 20, 04-730, Warszawa Aktualne zasady diagnostyki i leczenia chorób zapalnych
Instytut Pomnik Centrum Zdrowia Dziecka Odział Gastroenterologii, Hepatologii, Zaburzeń Odżywiania i Pediatrii Al. Dzieci Polskich 20, 04-730, Warszawa Aktualne zasady diagnostyki i leczenia chorób zapalnych
SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE 1. Dawkowanie. 1.1 Adalimumab należy podawać w dawce 40 mg, we wstrzyknięciu podskórnym co dwa tygodnie
 Załącznik nr 1 13. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW (RZS) I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW (MIZS) O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) I. LEKI BIOLOGICZNE A. Kryteria
Załącznik nr 1 13. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW (RZS) I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW (MIZS) O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) I. LEKI BIOLOGICZNE A. Kryteria
Orthogen GmbH. Department of Radiology and Microtherapy University of Witten/Herdecke, Germany
 Orthogen GmbH Biologiczne podstawy stosowania metody Irap IL-1 IL-1 IL-1Ra Podstawy działania Irap IL-1 Ra! TGF-β! PDGF! IGF! HGF! Przygotowywanie autologicznej kondycjonowanej surowicy (ACS) proces Irap
Orthogen GmbH Biologiczne podstawy stosowania metody Irap IL-1 IL-1 IL-1Ra Podstawy działania Irap IL-1 Ra! TGF-β! PDGF! IGF! HGF! Przygotowywanie autologicznej kondycjonowanej surowicy (ACS) proces Irap
ANEKS I. Strona 1 z 5
 ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC WETERYNARYJNYCH PRODUKTÓW LECZNICZYCH, GATUNKI ZWIERZĄT, DROGA PODANIA, PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH
ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC WETERYNARYJNYCH PRODUKTÓW LECZNICZYCH, GATUNKI ZWIERZĄT, DROGA PODANIA, PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH
LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0)
 Załącznik B.47. LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) A. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1. Podczas pierwszej kwalifikacji do programu oraz gdy jest to
Załącznik B.47. LECZENIE UMIARKOWANEJ I CIĘŻKIEJ POSTACI ŁUSZCZYCY PLACKOWATEJ (ICD-10 L 40.0) A. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1. Podczas pierwszej kwalifikacji do programu oraz gdy jest to
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY ZAKRES ŚWIADCZENIA GWARANTOWANEGO SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W RAMACH PROGRAMU
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie. Osoby należące do fachowego
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie. Osoby należące do fachowego
Metotreksat fakty i mity. Prof. dr hab. med. Witold Tłustochowicz Klinika Chorób Wewnętrznych i Reumatologii CSK MON WIM Warszawa Kielce 29.01.2015.
 Metotreksat fakty i mity Prof. dr hab. med. Witold Tłustochowicz Klinika Chorób Wewnętrznych i Reumatologii CSK MON WIM Warszawa Kielce 29.01.2015. Międzynarodowe rekomendacje leczenia MTX Jak działa metotreksat?
Metotreksat fakty i mity Prof. dr hab. med. Witold Tłustochowicz Klinika Chorób Wewnętrznych i Reumatologii CSK MON WIM Warszawa Kielce 29.01.2015. Międzynarodowe rekomendacje leczenia MTX Jak działa metotreksat?
LECZENIE CHOROBY GAUCHERA ICD-10 E
 załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
załącznik nr 19 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHOROBY GAUCHERA ICD-10 E 75 Zaburzenia przemian sfingolipidów i inne zaburzenia spichrzania
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
Załącznik nr 40 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku
 Załącznik nr 40 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW (RZS) I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW
Załącznik nr 40 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW (RZS) I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW
Załącznik Nr 3 do Zarządzenia NR 15/2008/ DGL Prezesa NFZ z dnia 18 lutego 2008 r.. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW INFLIXIMABEM
 Nazwa programu: LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW INFLIXIMABEM ICD-10 M 05 (Serododatnie reumatoidalne zapalenie stawów) M 06 (Seroujemne reumatoidalne zapalenie stawów) Dziedzina medycyny: Reumatologia
Nazwa programu: LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW INFLIXIMABEM ICD-10 M 05 (Serododatnie reumatoidalne zapalenie stawów) M 06 (Seroujemne reumatoidalne zapalenie stawów) Dziedzina medycyny: Reumatologia
Dlaczego potrzebne było badanie?
 Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z chorobą Alzheimera we wczesnym stadium Jest to podsumowanie badania klinicznego przeprowadzonego z udziałem pacjentów
Badanie mające na celu zbadanie czy lek BI 409306 polepsza sprawność umysłową u osób z chorobą Alzheimera we wczesnym stadium Jest to podsumowanie badania klinicznego przeprowadzonego z udziałem pacjentów
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
Terapeutyczne Programy Zdrowotne 2009 Leczenie nowotworów podścieliska przewodu pokarmowego (GIST) Załącznik nr 9
 Załącznik nr 9 Nazwa programu: do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) ICD 10 grupa rozpoznań obejmująca nowotwory
Załącznik nr 9 Nazwa programu: do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) ICD 10 grupa rozpoznań obejmująca nowotwory
Mgr inż. Aneta Binkowska
 Mgr inż. Aneta Binkowska Znaczenie wybranych wskaźników immunologicznych w ocenie ryzyka ciężkich powikłań septycznych u chorych po rozległych urazach. Streszczenie Wprowadzenie Według Światowej Organizacji
Mgr inż. Aneta Binkowska Znaczenie wybranych wskaźników immunologicznych w ocenie ryzyka ciężkich powikłań septycznych u chorych po rozległych urazach. Streszczenie Wprowadzenie Według Światowej Organizacji
zaawansowanym rakiem nerkowokomórkowym, rodzajem raka nerki, u pacjentów, którzy byli wcześniej leczeni lekami przeciwnowotworowymi;
 EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie postaci rzutowej stwardnienia rozsianego oparte
Reumatoidalne zapalenie stawów. Dlaczego pacjent nie może polubić choroby, a lekarz musi być agresywny?
 +. Dlaczego pacjent nie może polubić choroby, a lekarz musi być agresywny? Maria Rell-Bakalarska Interdyscyplinarna Akademia Medycyny Praktycznej Ivey Hayes RZS (1986 Definicja Przewlekła, immunologicznie
+. Dlaczego pacjent nie może polubić choroby, a lekarz musi być agresywny? Maria Rell-Bakalarska Interdyscyplinarna Akademia Medycyny Praktycznej Ivey Hayes RZS (1986 Definicja Przewlekła, immunologicznie
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) ŚWIADCZENIOBIORCY 1.Kryteria kwalifikacji 1.1 Leczenia interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Pełny wykaz substancji pomocniczych, patrz punkt 6.1 Charakterystyki Produktu Leczniczego (ChPL).
 Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka szpikowa
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka szpikowa
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Dziennik Urzędowy Ministra Zdrowia 624 Poz. 71 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dziennik Urzędowy Ministra Zdrowia 624 Poz. 71 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dlaczego tak późno trafiamy do reumatologa?
 Dlaczego tak późno trafiamy do reumatologa? Wyniki najnowszego badania Narodowego Instytutu Geriatrii, Reumatologii i Rehabilitacji im. prof. dr hab. med. Eleonory Reicher. Wczesne rozpoznanie Ustalenie
Dlaczego tak późno trafiamy do reumatologa? Wyniki najnowszego badania Narodowego Instytutu Geriatrii, Reumatologii i Rehabilitacji im. prof. dr hab. med. Eleonory Reicher. Wczesne rozpoznanie Ustalenie
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 765 Poz. 42 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 765 Poz. 42 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) wiek od 12 roku życia; 2) rozpoznanie postaci rzutowej stwardnienia
LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20)
 Dziennik Urzędowy Ministra Zdrowia 511 Poz. 42 Załącznik B.4. LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie zaawansowanego
Dziennik Urzędowy Ministra Zdrowia 511 Poz. 42 Załącznik B.4. LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie zaawansowanego
LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35)
 Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
Dziennik Urzędowy Ministra Zdrowia 589 Poz. 86 Załącznik B.29. LECZENIE STWARDNIENIA ROZSIANEGO (ICD-10 G 35) 1. Kryteria kwalifikacji: ŚWIADCZENIOBIORCY 1.1. Leczenie interferonem beta: 1) rozpoznanie
LECZENIE ŁUSZCZYCOWEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ŁZS) (ICD-10 L 40.5, M 07.1, M 07.2, M 07.3)
 Załącznik B.35. LECZENIE ŁUSZCZYCOWEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ŁZS) (ICD-10 L 40.5, M 07.1, M 07.2, M 07.3) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji:
Załącznik B.35. LECZENIE ŁUSZCZYCOWEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ŁZS) (ICD-10 L 40.5, M 07.1, M 07.2, M 07.3) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji:
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Dziennik Urzędowy Ministra Zdrowia 618 Poz. 51 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dziennik Urzędowy Ministra Zdrowia 618 Poz. 51 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
