Zarządzanie przez jakość w Medycznym Laboratorium Diagnostycznym. Dokumentacja Systemu Zarządzania Jakością. mgr Dorota Skubała Wstęp
|
|
|
- Konrad Jastrzębski
- 8 lat temu
- Przeglądów:
Transkrypt
1 Zarządzanie przez jakość w Medycznym Laboratorium Diagnostycznym. Dokumentacja Systemu Zarządzania Jakością. mgr Dorota Skubała Wojewódzki Szpital Chirurgii Urazowej Piekary Śląskie Wstęp Próby zdefiniowania pojęcia jakości pojawiły się już w czasach starożytnych. Platon definiował jakość jako pewien stopień doskonałości. Pojęcie jakości ewoluowało w czasie. W latach 50-tych mówiło się o jakości produktu, w latach 80-tych o jakości przedsiębiorstwa, w latach 90-tych wraz z serią norm ISO 9000 zdefiniowano jakość w odniesieniu do wymagań klienta. W związku z tym jakość rozumieć należy jako spełnienie oczekiwań lub wymagań (w tym wymagań prawnych) i osiągnięcia zadowolenia klienta. Jakość w laboratorium to wypadkowa wszystkich etapów pracy, które mają wpływ na niepewność wyniku badania i nie może być ograniczona wyłącznie do prowadzenia i monitorowania wewnętrznej kontroli jakości badań. Etap przedanalityczny, analityczny i poanalityczny muszą być planowane, nadzorowane, oceniane i doskonalone. Aby skutecznie realizować koncepcję jakości w Medycznym Laboratorium Diagnostycznym, należy zbudować, otrzymywać i doskonalić system zarządzania jakością, wykorzystując go jako narzędzie zarządzania nowoczesnym laboratorium. Podstawowe pojęcia Jakość wg normy ISO 8402 to ogół cech i właściwości wyrobu lub usługi, które decydują o zdolności wyrobu lub usługi do zaspokajania ustalonych i wymaganych potrzeb, natomiast zgodnie z ISO 9001 to stopień, w jakim zbiór inherentnych właściwości spełnia wymagania (inherentny - tkwiący w czymś w istocie, strukturze, zasadniczym charakterze czegoś, w naturze, w ustalonych obyczajach; nieodłączny od). System zarządzania jakością to struktura organizacyjna, procedury, procesy i wszystkie inne niezbędne elementy potrzebne do realizacji procesu zarządzania jakością. Zasady zarządzania jakością tzw filary jakości to: 1. Orientacja na klienta ostatecznie klient decyduje o jakości produktu 2. Przywództwo system musi mieć lidera, z przywództwa rodzi się zaangażowanie 3. Zaangażowanie ludzi motywacja, zrozumienie, wiedza i umiejętność jej wykorzystania 4. Podejście procesowe metoda podziału organizacji na poszczególne obszary, aby było łatwiej nimi zarządzać 5. Podejście systemowe gwarancja równowagi, stabilności działań 6. Ciągłe doskonalenie rozumiane jako element zarządczy 7. Podejmowanie decyzji na podstawie faktów gwarancja odtwarzalności działań 8. Wzajemnie korzystne relacje z dostawcami Proces zbiór działań wzajemnie powiązanych lub wzajemnie oddziałujących, które przekształcają wejścia w wyjścia. Rodzaje procesów: proces główny ( to proces dla którego funkcjonuje organizacja) w MLD jest to usługa laboratoryjna procesy zarządcze procesy pomocnicze (wspomagają realizację procesu głównego) Kompleksowe Zarządzanie Jakością (Total Quality Management TQM) to kultura zarządzania laboratorium wykorzystująca umiejętność pracy zespołowej dla realizacji celów jakościowych wyznaczonych przez Naczelne Kierownictwo. Jest to rozwiązanie indywidualne dla danego laboratorium. Nie ma rozwiązań uniwersalnych, nie
2 ma uniwersalnej dokumentacji, każde laboratorium jest unikalne i musi dopasować system zarządzania jakością do wymagań aktów normatywnych i prawnych, zaleceń i rekomendacji oraz wymagań i potrzeb klienta laboratorium. Normy ISO w MLD; Certyfikacja i akredytacja Normą podstawową jest norma ISO 9001, jest ona podstawą do certyfikacji. Normy techniczne to: PN-EN ISO norma dla laboratoriów badawczych (bez względu na profil) i PN-EN ISO norma dla laboratoriów medycznych. Obie normy techniczne to podstawa do akredytacji laboratoriów. Certyfikacja to potwierdzenie przez niezależną jednostkę certyfikującą na drodze sprawdzenia (auditu) zgodności systemu zarządzania jakością z normą międzynarodową. Certyfikat jest potwierdzeniem,że laboratorium, które go posiada ma system zarządzania jakością zgodny z normą na którą jest wystawiony certyfikat. Laboratorium poddaje się corocznym auditom zewnętrznym, w trakcie których niezależni auditorzy weryfikują utrzymywanie i doskonalenie systemu zarządzania jakością. Akredytacja to formalne uznanie,że laboratorium posiada kompetencje do wykonania określonego badania (zakres akredytacji sprecyzowany w certyfikacie akredytacyjnym). Akredytacja dotyczy jedynie badań, które są wyszczególnione w certyfikacie akredytacyjnym. Certyfikacja i akredytacja są działaniami dobrowolnymi. Etapy budowania Systemu Zarządzania Jakością 1. Określenie Celów jakościowych i Polityki Jakości przez Naczelne Kierownictwo, oraz zapewnienie środków na realizację. Polityka Jakości zgodnie z pkt 5.3 normy musi zawierać zobowiązanie do spełnienia wymagań i ciągłego doskonalenia skuteczności systemu, oraz tworzyć ramy do formułowania i przeglądów celów jakościowych. Powinna być odpowiednia do celu istnienia organizacji (laboratorium), zakomunikowana całemu personelowi, zrozumiała i okresowo przeglądana oraz weryfikowana. 2. Powołanie przedstawiciela Naczelnego Kierownictwa do tworzenia, wdrożenia, utrzymania i doskonalenia SZJ. Musi to być osoba związana z MLD, merytorycznie kompetentna oraz przeszkolona w zakresie SZJ (Asystent ds SZJ w MLD lub Pełnomocnik ds SZJ zgodnie z normą ISO 9001). 3. Zidentyfikowanie i opisanie procesów przebiegających w MLD, oraz powiązań między procesami, wyznaczenie osób odpowiedzialnych za poszczególne procesy (liderzy procesów) i ustalenie niezbędnych i użytecznych mierników procesów wraz z określeniem częstości ich wyliczania i wartości uznanych za kryterium sukcesu. 4. Opisanie przebiegających procesów, wraz z mapą procesów (graficzne przedstawienie przebiegu, powiązań, odpowiedzialności) 5. Ustalenie szaty graficznej dokumentów systemu, hierarchii dokumentacji 6. Powołanie zespołów do opracowania poszczególnych dokumentów SZJ, ustalenie terminarza budowania SZJ, powierzenie zadań Dokumentacja SZJ wymagania PN-EN ISO 9001:2009 i wymagania prawne dla MLD Norma PN-EN ISO 9001:2009 pkt 1.2 precyzuje,że wymagania zawarte w tej normie są ogólne i przeznaczone do stosowania przez wszystkie organizacje, bez względu na ich rodzaj, wielkość i dostarczany wyrób. Tak więc, MLD może stosować w/w normę jako podstawę SZJ. Hierarchia dokumentacji SZJ: 1. Księga Jakości wraz z udokumentowaną Polityką Jakości i celami jakościowymi 2. Udokumentowane Procedury Ogólne wymagane przez normę ISO Dokumenty wymagane przez normę lub niezbędne do zapewnienia skutecznego planowania, przebiegu i nadzorowania procesów (Instrukcje stanowiskowe, formularze)
3 4. Zapisy wymagane przez normę lub niezbędne do zapewnienia skutecznego planowania, przebiegu i nadzorowania procesów (dowody spełnienia wymagań, w tym wymagań normy i wymagań prawnych dla MLD) Dokumentacja może być opracowana w formie papierowej, elektronicznej lub z wykorzystaniem obu tych form. Niezależnie od formy w jakiej prowadzona jest dokumentacja systemowa należy zapewnić wymagany przez normę nadzór nad dokumentami, zapisami i aktami prawnymi. Księga Jakości musi zawierać zakres SZJ (zakres odnosi się do procesu głównego), wyłączenia jeśli takie zastosowano (tylko z pkt.7 normy) wraz z uzasadnieniem ich zastosowania, mapę procesów. Księga Jakości jest dokumentem wewnętrznym jak też może być udostępniana na zewnątrz, klientom laboratorium jest więc wizytówką laboratorium. Procedury ogólne opisują przebieg poszczególnych procesów i definiują odpowiedzialności. Norma PN-EN ISO 9001:2009 wymaga ustanowienia, udokumentowania i utrzymywania 6 procedur ogólnych: 1. Nadzór nad dokumentami (pkt normy) 2. Nadzór nad zapisami (pkt normy) 3. Audit wewnętrzny (pkt normy) 4. Nadzór nad wyrobem niezgodnym (pkt. 8.3 normy) 5. Działania korygujące (pkt normy) 6. Działania zapobiegawcze (pkt normy) Ze względu na charakter MLD niezbędne dla udokumentowania wszystkich procesów przebiegających w laboratorium jest uzupełnienie wymaganych przez normę 6 procedur o procedury opisujące: 1. Realizację usługi laboratoryjnej (proces główny) 2. Gospodarkę środkami badawczymi i materiałami 3. Kierowanie do badań i pobieranie materiałów do badań 4. Nadzór nad jakością badań 5. Formułowanie, zatwierdzanie i wydawanie sprawozdań z badań 6. Nadzór nad aparaturą pomiarową i wyposażeniem pomocniczym Instrukcje stanowiskowe (instrukcje pracy) nie są wymagane literalnie przez normę, jednak ze względu na charakter procesu głównego w MLD oraz wymagania prawne dla MLD- Rozporządzenie MZ w sprawie standardów jakości badań niezbędne staje się udokumentowanie wszystkich elementów wymaganych przez przepisy prawa. Zapisy są wymagane przez normę i przez przepisy prawa, stanowią dowód spełnienia wymagań, oraz dostarczają dowodów na funkcjonowanie SZJ w laboratorium. Cały proces diagnostyczny przebiegający w MLD musi być w pełni odtwarzalny (od pobrania do wydania sprawozdania z badań). Zapisy muszą się charakteryzować identyfikowalnością (kto, kiedy sporządził), muszą być czytelne, kompletne, zrozumiałe, niezmienialne i wiarygodne(autoryzowane). Należy stosować formularze i rejestry ułatwiające spełnienie powyższych wymagań. Specyfika MLD a norma ISO 9001 Klient to pacjent od którego pobrano materiał do badań / lekarz zlecający badanie. W zakres obsługi klienta w MLD wchodzi pobieranie i transportowanie materiałów do badań. Ten obszar jest określony prawnie Rozp. MZ w sprawie wykazu zabiegów i czynności polegających na pobraniu od pacjenta materiału do badań laboratoryjnych oraz Rozp. MZ w sprawie standardów jakości badań dla MLD i MLM. W zakres obsługi klienta wchodzi umocowany prawnie obowiązek udzielania przez specjalistę konsultacji merytorycznej, dotyczącej wyników badań i ich interpretacji klinicznej Ustawa o diagnostyce laboratoryjnej.
4 Wyrób = usługa laboratoryjna (od pobrania do wydania sprawozdania z badań). Usługa laboratoryjna musi spełniać wymagania klienta oraz być zgodna z wiedzą fachową, zaleceniami, rekomendacjami i wymaganiami prawnymi dla MLD. Produkt = sprawozdanie z badań (wynik lub zbiór wyników poszczególnych oznaczeń opatrzony niezbędnym komentarzem). Kryteria oceny sprawozdania z badań: TAT czas od zlecenia / pobrania materiału do badań do wydania sprawozdania z badań Wartość merytoryczna sprawozdania z badań (niezbędne komentarze, możliwość konsultacji ze specjalistą) Dostępność do badań (panel badań, częstość wykonywania, dostępność informacji dla klienta) Cena badania (realność ceny) Organizacja pracy, zarządzanie MLD Dopasowanie metodyki badania do celu badania Kompetencje merytoryczne i techniczne laboratorium (kompetencje personelu i dostępne wyposażenie pomiarowe i pomocnicze) Wiarygodność wyniku (sprawny i udokumentowany system sterowania jakością badań) Dążenie do wyeliminowania potencjalnych źródeł błędów uszczelnienie i monitorowanie wszystkich procesów Zrozumienie wymagań klienta w odniesieniu do wymagań prawnych i merytorycznych. Wynik badania (produkt) musi być : Poprawny Odtwarzalny Porównywalny / reprezentatywny Przydatny do danego przypadku klinicznego Poparty rzetelną, udokumentowaną kontrolą jakości Autoryzowany przez upoważnioną osobę Dostarczony we właściwym czasie i za sensowną cenę Miernikiem jakości wyniku jest jego użyteczność kliniczna. Etapy wdrażania SZJ w MLD Po etapie budowania SZJ, opisanym powyżej rozpoczyna się następny etap wdrażania SZJ w MLD. Za wdrażanie odpowiedzialny jest przedstawiciel Naczelnego Kierownictwa ds SZJ. 1. Szkolenie personelu w zakresie wymagań normy PN-EN ISO Szkolenie kandydatów na auditorów wewnętrznych 3. Szkolenie personelu w zakresie wdrażanych dokumentów SZJ 4. Powierzenie zadań w zakresie SZJ 5. Przeprowadzenie auditów wewnętrznych obejmujących swoim zakresem wszystkie procesy przebiegające w MLD 6. Rozpatrzenie wniosków poauditowych, wdrożenie działań korygujących i zapobiegawczych, ocena działań 7. Przeprowadzenie przeglądu SZJ, formułowanie wniosku o stopniu dojrzałości systemu 8. Decyzja o przystąpieniu do certyfikacji lub decyzja o utrzymaniu SZJ bez certyfikowania (decyzja Naczelnego Kierownictwa)
5 Etapy utrzymania i doskonalenia SZJ Podejście procesowe wymagane przez normę ISO 9001 oparte jest na tzw Kole Deminga zwanym inaczej zasadą PDCA planuj (Plan) zrób (Do) sprawdź (Check) działaj (Act) Można to przełożyć na 4 etapy działania: Planowanie jakości Sterowanie jakością Zapewnienie jakości Doskonalenie jakości Te etapy następują bezpośrednio po sobie w trakcie utrzymania i doskonalenia wdrożonego SZJ. Planowanie jakości w MLD 1. Szacowanie potrzeb klienta badanie rynku, rozmowy ze zleceniodawcami, pomoc w ustaleniu optymalnego panelu badań 2. Dostosowanie się do wymagań klienta (zaplanowanie usługi laboratoryjnej spełniającej wymagania klienta) 3. Zapewnienie odpowiednich metod badawczych, wyposażenia, personelu o odpowiednich kwalifikacjach i w ilości wystarczającej do bezpiecznej realizacji 4. Zapewnienie aktualnej, czytelnej i użytecznej dokumentacji SZJ 5. Walidacja (tam gdzie to niezbędne) wykazanie przez dostarczenie obiektywnych danych, że metoda / urządzenie są przydatne do określonego celu. Walidacji nie wymagają metodyki stosowane zgodnie z zaleceniami producenta testów/aparatury, stosowane przez MLD bez modyfikacji własnych. 6. Zaplanowanie i wdrożenie kontroli jakości wewnętrznej / zewnętrznej dla całego panelu badań oferowanego przez MLD, z odpowiednią częstotliwością 7. Okresowa ocena podwykonawców (jeśli MLD korzysta z usług zewnętrznych) 8. Wyznaczenie a następnie okresowa weryfikacja celów jakościowych i zapewnienie środków na ich realizację Sterowanie jakością w MLD 1. Prawidłowo zaplanowana, stosowana i oceniana kontrola jakości metod - wewnątrzlaboratoryjna 2. Stosowanie odpowiednich materiałów kontrolnych 3. Poddawanie się ocenie zewnętrznej badania biegłości miedzylaboratoryjne 4. Zapewnienie personelu posiadającego doświadczenie i kwalifikacje do podejmowania działań z zakresu sterowania jakością badań 5. Ocena obszaru sterowania jakością u podwykonawcy(jeśli MLD korzysta z usług zewnętrznych mających wpływ na jakość badań) 6. W Medycznym Laboratorium Mikrobiologicznym (MLM) większość stosowanych metod to metody jakościowe, których charakter nie pozwala na ścisłe metrologiczne i statystyczne oszacowanie niepewności pomiaru. Zadaniem MLM jest dokładne oszacowanie wszystkich składników niepewności i ich oszacowanie na podstawie wiedzy personelu i wiarygodnych danych literaturowych, czy danych z walidacji. Kluczowe jest zapewnienie personelu o odpowiednich kwalifikacjach i w ilości odpowiedniej do bezpiecznego wykonywania badań. Materiałami kontrolnymi są szczepy wzorcowe, które muszą pochodzić z uznanych kultur, a szczególnym nadzorem należy objąć pasażowanie i przechowywanie materiałów kontrolnych. W przypadku metod ilościowych obowiązuje dokument PCA: EA-04/16. Zapewnienie jakości w MLD 1. Należy tworzyć i odpowiednio przechowywać zapisy (dowody) z kontroli jakości wszystkich metod badawczych. 2. Należy udokumentować sprawne działania korygujące, zapobiegawcze i naprawcze 3. Należy udokumentować postępowanie z niezgodnościami i reklamacjami
6 4. Należy udokumentować nadzór nad wyposażeniem pomiarowym i pomocniczym 5. Należy udokumentować kompetencje i zakresy uprawnień personelu fachowego i prowadzić okresową ocenę pracowników 6. Przebieg procesu diagnostycznego (od pobrania do wydania sprawozdania z badań ) musi być udokumentowany i w pełni odtwarzalny. 7. Wszystkie w/w zapisy muszą posiadać cechy wymagane przez normę ISO 9001 Doskonalenie jakości w MLD 1. Sprawne identyfikowanie niezgodności lub potencjalnych niezgodności oraz udokumentowane sprawne i skuteczne działania korygujące / zapobiegawcze / naprawcze 2. Sprawne postępowanie z reklamacjami (zarówno składanymi do MLD przez klienta jak i składanymi przez MLD u dostawców i podwykonawców) 3. Badanie satysfakcji klienta (pacjenta/lekarza), wyciąganie wniosków, dostosowanie do wymagań klientów 4. Stały nadzór liderów nad podległymi im procesami, monitorowanie zadanych mierników 5. System szkoleń, ocena szkoleń, planowanie szkoleń zgodnie z potrzebami, podnoszenie kwalifikacji zawodowych 6. Ocena realizacji celów jakościowych, coroczna weryfikacja celów jakościowych i polityki jakości w trakcie przeglądu zarządzania Stan na dzień dzisiejszy Każde MLD powinno posiadać minimum w zakresie: Wyznaczony, powołany i przeszkolony przedstawiciel Naczelnego Kierownictwa ds SZJ w MLD. Organizacja pracy opisana struktura MLD, zadania, podział obowiązków, uprawnienia, kompetencje, zakresy uprawnień. Zaleca się stosowanie oceny pracowników. Obsługa klienta wyznaczone i przeszkolone osoby do pobierania materiałów biologicznych (zakresy uprawnień), opracowany zestaw procedur pobierania i transportowania materiałów do badań. Udokumentowany i sprawnie działający sposób postępowania z reklamacjami. Badanie satysfakcji klienta. Wyposażenie dokumentacja techniczna wyposażenia pomiarowego i pomocniczego aktualna i kompletna; udokumentowane metody badawcze; udokumentowany nadzór nad przechowywaniem odczynników. Kontrola jakości badań udokumentowana wewnętrzna i zewnętrzna kontrola jakości dla całego panelu badań, udokumentowane działania korygujące i zapobiegawcze, udokumentowane omówienie wniosków po kontroli z personelem fachowym. Najczęstsze problemy MLD w trakcie budowania i wdrażania SZJ brak motywacji do budowania SZJ złe pojmowanie istoty SZJ i nieumiejętność wykorzystania systemu jako narzędzia do efektywnego zarządzania brak personelu przeszkolonego do działań w zakresie SZJ słaba kondycja finansowa jednostki macierzystej, co za tym idzie problemy kadrowe, wyposażeniowe, organizacyjne; brak wsparcia ze strony Naczelnego Kierownictwa; brak środków na realizację celów niewłaściwe rozłożenie odpowiedzialności za jakość odpowiedzialność złożona w ręce jednej osoby lub grupy osób, co powoduje brak identyfikacji personelu z działaniami skierowanie wysiłków na skopiowanie systemów działających w innych MLD każde MLD jest inne, nie ma jednej uniwersalnej dokumentacji ani jednego uniwersalnego sposobu budowania SZJ. Każde MLD musi wypracować własne rozwiązania
7 brak kompletnej dokumentacji, nieumiejętność koordynowania działań na etapie budowania i wdrażania SZJ istniejąca dokumentacja jest nieużyteczna - sztuka dla sztuki brak zapisów lub zapisy są niekompletne albo nie są tworzone na bieżąco brak konsekwencji, działania jakościowe pozorowane, nastawienie na przetrwanie od auditu do auditu brak systemu kontroli i oceny oraz monitorowania traktowanie certyfikacji jako celu ostatecznego a nie etapu w dążeniu do celu Korzyści z wdrożenia i certyfikowania SZJ w MLD usystematyzowanie i opisanie każdego etapu toku diagnostycznego uporządkowanie innych obszarów działania MLD poza tokiem diagnostycznym poprawa jakości zarządzania MLD zmiana podejścia do klienta zmniejszenie kosztów (po okresie budowania i wdrożenia SZJ) poprawa jakości skutkuje wzrostem zadowolenia klienta i zaufania kontrahentów wzrost pozycji MLD na rynku usług diagnostycznych lepsza pozycja marketingowa MLD w konkursach ofert i przetargach łatwiejsze nawiązywanie współpracy z kontrahentami uznającymi certyfikat ISO na zasadzie domniemania jakości pomiędzy firmami poprawa organizacji, warunków i bezpieczeństwa pracy komfort wykonywania obowiązków służbowych system szkoleń i stałe podnoszenie kwalifikacji lepsze wykorzystanie potencjału każdego z pracowników spokój, pewność wyniku, pełna odtwarzalność całego toku diagnostycznego Podsumowanie Filozofia kompleksowego zarządzania jakością (TQM) jest obecnie uważana za najbardziej efektywny sposób prowadzenia działalności produkcyjnej i usługowej. Bez wprowadzenia tego stylu zarządzania Medyczne Laboratoria Diagnostyczne nie będą w stanie skutecznie i uczciwie konkurować na rynku usług diagnostycznych. Często w rozmowach diagnostów można usłyszeć opinie,że to konkurencja wymusza na nas pewne działania. Wobec tego niech konkurencja spowoduje,że zbudujemy System Zarządzania Jakością w MLD, użyjemy go do skutecznego i efektywnego zarządzania, przestaniemy postrzegać jakość w laboratorium wyłącznie przez pryzmat wewnętrznej kontroli jakości, wykorzystamy potencjał i wiedzę personelu fachowego dla osiągnięcia zadowolenia klienta. Niech jakość stanie się kulturą działania MLD, która pozwoli na świadczenie usług diagnostycznych na wymaganym przez klienta poziomie jakości, przy zaangażowaniu każdego pracownika oraz wysiłku całego zespołu skierowanemu na osiągniecie długotrwałego sukcesu i ciągłe doskonalenie.
8 Literatura: 1. PN-EN ISO 9001: PN ISO 8402 : Ustawa z dnia 27 lipca 2001 o diagnostyce laboratoryjnej Dz.U Rozp.MZ z dnia 3 listopada 2004 w sprawie wykazu zabiegów i czynności polegających na pobraniu materiału do badań laboratoryjnych Dz.U. Nr 247, poz Rozp.MZ z dnia 23 marca 2006 w sprawie standardów jakości dla medycznych laboratoriów diagnostycznych i mikrobiologicznych Dz.U Rozp. MZ z dnia 21 stycznia 2009 zmieniające rozporządzenie w sprawie standardów jakości dla medycznych laboratoriów diagnostycznych i mikrobiologicznych Dz.U z dnia 11 lutego 2009 r. 7. A.Blikle, Doktryna Jakości. Rzecz o skutecznym zarządzaniu, Wawak S., Zarządzanie jakością. Teoria i praktyka, Ćwiklicki M., Obora H., Metody TQM w zarządzaniu firmą, praktyczne przykłady zastosowań 10. Łańcucki J., Podstawy kompleksowego zarządzania jakością TQM, 2006
Akredytacja laboratoriów wg PN-EN ISO/IEC 17025:2005
 Akredytacja laboratoriów wg PN-EN ISO/IEC 17025:2005 Marek Misztal ENERGOPOMIAR Sp. z o.o. Biuro Systemów Zarządzania i Ocen Nowe Brzesko, 26 września 2006 r. Czy systemy zarządzania są nadal dobrowolne?
Akredytacja laboratoriów wg PN-EN ISO/IEC 17025:2005 Marek Misztal ENERGOPOMIAR Sp. z o.o. Biuro Systemów Zarządzania i Ocen Nowe Brzesko, 26 września 2006 r. Czy systemy zarządzania są nadal dobrowolne?
Normy ISO serii 9000. www.greber.com.pl. Normy ISO serii 9000. Tomasz Greber (www.greber.com.pl) dr inż. Tomasz Greber. www.greber.com.
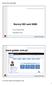 Normy ISO serii 9000 dr inż. Tomasz Greber www.greber.com.pl www.greber.com.pl 1 Droga do jakości ISO 9001 Organizacja tradycyjna TQM/PNJ KAIZEN Organizacja jakościowa SIX SIGMA Ewolucja systemów jakości
Normy ISO serii 9000 dr inż. Tomasz Greber www.greber.com.pl www.greber.com.pl 1 Droga do jakości ISO 9001 Organizacja tradycyjna TQM/PNJ KAIZEN Organizacja jakościowa SIX SIGMA Ewolucja systemów jakości
Norma to dokument przyjęty na zasadzie konsensu i zatwierdzony do powszechnego stosowania przez
 KONCEPCJA SYSTEMU JAKOŚCI zgodnie z wymaganiami norm ISO serii 9000 dr Lesław Lisak Co to jest norma? Norma to dokument przyjęty na zasadzie konsensu i zatwierdzony do powszechnego stosowania przez upoważnioną
KONCEPCJA SYSTEMU JAKOŚCI zgodnie z wymaganiami norm ISO serii 9000 dr Lesław Lisak Co to jest norma? Norma to dokument przyjęty na zasadzie konsensu i zatwierdzony do powszechnego stosowania przez upoważnioną
KLIENCI KIENCI. Wprowadzenie normy ZADOWOLE NIE WYRÓB. Pomiary analiza i doskonalenie. Odpowiedzialnoś ć kierownictwa. Zarządzanie zasobami
 SYSTEM ZARZĄDZANIA JAKOŚCIĄ ISO Jakość samą w sobie trudno jest zdefiniować, tak naprawdę pod tym pojęciem kryje się wszystko to co ma związek z pewnymi cechami - wyrobu lub usługi - mającymi wpływ na
SYSTEM ZARZĄDZANIA JAKOŚCIĄ ISO Jakość samą w sobie trudno jest zdefiniować, tak naprawdę pod tym pojęciem kryje się wszystko to co ma związek z pewnymi cechami - wyrobu lub usługi - mającymi wpływ na
Audit techniczny w laboratorium ASA. Czyli przygotowanie do auditu technicznego jednostki akredytujacej lub auditu wewnetrznego
 Audit techniczny w laboratorium ASA Czyli przygotowanie do auditu technicznego jednostki akredytujacej lub auditu wewnetrznego 2008 Pkt. 4.4 normy Przegląd zapytań, ofert i umów - procedura przeglądu zleceń
Audit techniczny w laboratorium ASA Czyli przygotowanie do auditu technicznego jednostki akredytujacej lub auditu wewnetrznego 2008 Pkt. 4.4 normy Przegląd zapytań, ofert i umów - procedura przeglądu zleceń
Budowanie skutecznych systemów zarządzania opartych na normach ISO
 UKatalog Szkoleń: Budowanie skutecznych systemów zarządzania opartych na normach ISO UBlok I Podejście procesowe: Zarządzanie procesowe (2 dni) Definicje procesu, zarządzanie procesami, podział i identyfikowanie
UKatalog Szkoleń: Budowanie skutecznych systemów zarządzania opartych na normach ISO UBlok I Podejście procesowe: Zarządzanie procesowe (2 dni) Definicje procesu, zarządzanie procesami, podział i identyfikowanie
ISO 9001:2015 przegląd wymagań
 ISO 9001:2015 przegląd wymagań dr Inż. Tomasz Greber (www.greber.com.pl) Normy systemowe - historia MIL-Q-9858 (1959 r.) ANSI-N 45-2 (1971 r.) BS 4891 (1972 r.) PN-N 18001 ISO 14001 BS 5750 (1979 r.) EN
ISO 9001:2015 przegląd wymagań dr Inż. Tomasz Greber (www.greber.com.pl) Normy systemowe - historia MIL-Q-9858 (1959 r.) ANSI-N 45-2 (1971 r.) BS 4891 (1972 r.) PN-N 18001 ISO 14001 BS 5750 (1979 r.) EN
Audyt techniczny w laboratorium widziane okiem audytora. Piotr Pasławski 2008
 Audyt techniczny w laboratorium widziane okiem audytora Piotr Pasławski 2008 Odniesienie do wymagań normy PN-EN ISO/IEC 17025:2005 Pkt. 4.4 normy Przegląd zapytań, ofert i umów - procedura przeglądu zleceń
Audyt techniczny w laboratorium widziane okiem audytora Piotr Pasławski 2008 Odniesienie do wymagań normy PN-EN ISO/IEC 17025:2005 Pkt. 4.4 normy Przegląd zapytań, ofert i umów - procedura przeglądu zleceń
Etapy wdraŝania Systemu Zarządzania Jakością zgodnego z ISO 9001:2008
 1 2 Etapy wdraŝania Systemu Zarządzania Jakością zgodnego z ISO 9001:2008 Etapy wdraŝania Systemu Zarządzania Jakością zgodnego z ISO 9001:2008 3 Agenda 4 Jaki powinien być System Zarządzania wg norm serii
1 2 Etapy wdraŝania Systemu Zarządzania Jakością zgodnego z ISO 9001:2008 Etapy wdraŝania Systemu Zarządzania Jakością zgodnego z ISO 9001:2008 3 Agenda 4 Jaki powinien być System Zarządzania wg norm serii
Zarządzanie jakością. Opis kierunku. Co zyskujesz? Dla kogo? - Kierunek - studia podyplomowe
 1 Zarządzanie jakością - Kierunek - studia podyplomowe Niestacjonarne 2 semestry OD PAŹDZIERNIKA Opis kierunku Podyplomowe studia zarządzania jakością organizowane są we współpracy z firmą TÜV Akademia
1 Zarządzanie jakością - Kierunek - studia podyplomowe Niestacjonarne 2 semestry OD PAŹDZIERNIKA Opis kierunku Podyplomowe studia zarządzania jakością organizowane są we współpracy z firmą TÜV Akademia
System zarządzania. zgodny z modelem w/g norm serii ISO 9000
 System zarządzania zgodny z modelem w/g norm serii ISO 9000 Normalizacja Normy ISO publikowane są przez Międzynarodową Organizację Normalizacyjną z siedzibą w Genewie, a następnie adaptowane i wprowadzane
System zarządzania zgodny z modelem w/g norm serii ISO 9000 Normalizacja Normy ISO publikowane są przez Międzynarodową Organizację Normalizacyjną z siedzibą w Genewie, a następnie adaptowane i wprowadzane
UDOKUMENTOWANE INFORMACJE ISO 9001:2015
 UDOKUMENTOWANE INFORMACJE ISO 9001:2015 4.3 Ustalenie systemu zarządzania jakością Zakres systemu zarządzania jakości organizacji powinien być dostępny i utrzymany w formie udokumentowanej informacji.
UDOKUMENTOWANE INFORMACJE ISO 9001:2015 4.3 Ustalenie systemu zarządzania jakością Zakres systemu zarządzania jakości organizacji powinien być dostępny i utrzymany w formie udokumentowanej informacji.
ISO 9000/9001. Jarosław Kuchta Jakość Oprogramowania
 ISO 9000/9001 Jarosław Kuchta Jakość Oprogramowania Co to jest ISO International Organization for Standardization największa międzynarodowa organizacja opracowująca standardy 13700 standardów zrzesza narodowe
ISO 9000/9001 Jarosław Kuchta Jakość Oprogramowania Co to jest ISO International Organization for Standardization największa międzynarodowa organizacja opracowująca standardy 13700 standardów zrzesza narodowe
Księga Zintegrowanego Systemu Zarządzania ZINTEGROWANY SYSTEM ZARZĄDZANIA
 Strona: 1 z 5 1. Opis systemu zintegrowanego systemu zarządzania 1.1. Postanowienia ogólne i zakres obowiązywania W Samodzielnym Zespole Publicznych Zakładów Lecznictwa Otwartego Warszawa Ochota jest ustanowiony,
Strona: 1 z 5 1. Opis systemu zintegrowanego systemu zarządzania 1.1. Postanowienia ogólne i zakres obowiązywania W Samodzielnym Zespole Publicznych Zakładów Lecznictwa Otwartego Warszawa Ochota jest ustanowiony,
1
 Wprowadzenie 0.1 Postanowienia ogólne Wprowadzenie 0.1 Postanowienia ogólne Wprowadzenie 0.1 Postanowienia ogólne 0.2 Podejście procesowe 0.2 Zasady zarządzania jakością 0.2 Zasady zarządzania jakością
Wprowadzenie 0.1 Postanowienia ogólne Wprowadzenie 0.1 Postanowienia ogólne Wprowadzenie 0.1 Postanowienia ogólne 0.2 Podejście procesowe 0.2 Zasady zarządzania jakością 0.2 Zasady zarządzania jakością
SYSTEMY ZARZĄDZANIA. cykl wykładów dr Paweł Szudra
 SYSTEMY ZARZĄDZANIA cykl wykładów dr Paweł Szudra LITERATURA Brilman J., Nowoczesne koncepcje i metody zarządzania. PWE, 2006. Grudzewski W., Hejduk I., Projektowanie systemów zarządzania. Wydawnictwo
SYSTEMY ZARZĄDZANIA cykl wykładów dr Paweł Szudra LITERATURA Brilman J., Nowoczesne koncepcje i metody zarządzania. PWE, 2006. Grudzewski W., Hejduk I., Projektowanie systemów zarządzania. Wydawnictwo
WYMAGANIA DLA ZAKŁADOWEJ KONTROLI PRODUKCJI
 Instytut Odlewnictwa Biuro Certyfikacji i Normalizacji u l. Z a k o p i a ń s k a 7 3 30-418 Kraków, Polska tel. +48 (12) 26 18 442 fax. +48 (12) 26 60 870 bcw@iod.krakow.pl w w w.i o d.k r ak ow. p l
Instytut Odlewnictwa Biuro Certyfikacji i Normalizacji u l. Z a k o p i a ń s k a 7 3 30-418 Kraków, Polska tel. +48 (12) 26 18 442 fax. +48 (12) 26 60 870 bcw@iod.krakow.pl w w w.i o d.k r ak ow. p l
Procedura auditów wewnętrznych i działań korygujących
 1/14 TYTUŁ PROCEURY Opracował: Zatwierdził: Pełnomocnik ds. SZJ Mariusz Oliwa 18 marca 2010r.... podpis Starosta Bolesławiecki Cezary Przybylski... podpis PROCEURA OBOWIĄZUJE O NIA: 25 czerwca 2010r. 18
1/14 TYTUŁ PROCEURY Opracował: Zatwierdził: Pełnomocnik ds. SZJ Mariusz Oliwa 18 marca 2010r.... podpis Starosta Bolesławiecki Cezary Przybylski... podpis PROCEURA OBOWIĄZUJE O NIA: 25 czerwca 2010r. 18
Systemy zarządzania jakością w ochronie radiologicznej
 DOZYMETRIA Systemy zarządzania jakością w ochronie radiologicznej Jakub Ośko System zarządzania jakością zespół systematycznie planowanych i wykonywanych działań, koniecznych dla wystarczającego zapewnienia,
DOZYMETRIA Systemy zarządzania jakością w ochronie radiologicznej Jakub Ośko System zarządzania jakością zespół systematycznie planowanych i wykonywanych działań, koniecznych dla wystarczającego zapewnienia,
Powody wdraŝania i korzyści z funkcjonowania Systemu Zarządzania Jakością wg ISO 9001. Mariola Witek
 Powody wdraŝania i korzyści z funkcjonowania Systemu Zarządzania Jakością wg ISO 9001 Mariola Witek Przedmiot wykładu 1.Rozwój systemów zarządzania jakością (SZJ) 2.Potrzeba posiadania formalnych SZJ 3.Korzyści
Powody wdraŝania i korzyści z funkcjonowania Systemu Zarządzania Jakością wg ISO 9001 Mariola Witek Przedmiot wykładu 1.Rozwój systemów zarządzania jakością (SZJ) 2.Potrzeba posiadania formalnych SZJ 3.Korzyści
Team Prevent Poland Sp. z o.o. Graficzna prezentacja struktury ISO 9001:2015 i IATF 16949:2016
 Graficzna prezentacja struktury ISO 9001:2015 i 16949:2016 Struktura ISO 9001:2015 ISO 9001:2015 4. Kontekst organizacji 5. Przywództwo 6. Planowanie 7. Wsparcie 8. Działania operacyjne 9. Ocena efektów
Graficzna prezentacja struktury ISO 9001:2015 i 16949:2016 Struktura ISO 9001:2015 ISO 9001:2015 4. Kontekst organizacji 5. Przywództwo 6. Planowanie 7. Wsparcie 8. Działania operacyjne 9. Ocena efektów
Metodyka wdrożenia. System Jakości ISO 9001
 Metodyka wdrożenia System Jakości ISO 9001 Metodyka wdrożenia Proponowana przez nas metodyka wdrażania systemu zarządzania jakością według normy ISO 9001 bazuje na naszych wieloletnich doświadczeniach
Metodyka wdrożenia System Jakości ISO 9001 Metodyka wdrożenia Proponowana przez nas metodyka wdrażania systemu zarządzania jakością według normy ISO 9001 bazuje na naszych wieloletnich doświadczeniach
Audyt wewnętrzny jako metoda oceny Systemu Zarządzania Jakością. Piotr Lewandowski Łódź, r.
 Audyt wewnętrzny jako metoda oceny Systemu Zarządzania Jakością Piotr Lewandowski Łódź, 28.06.2017 r. 2 Audit - definicja Audit - systematyczny, niezależny i udokumentowany proces uzyskiwania zapisów,
Audyt wewnętrzny jako metoda oceny Systemu Zarządzania Jakością Piotr Lewandowski Łódź, 28.06.2017 r. 2 Audit - definicja Audit - systematyczny, niezależny i udokumentowany proces uzyskiwania zapisów,
URZĄD MIEJSKI W GOSTYNIU PREZENTACJA SYSTEMU PN EN ISO 9001:2001 KSIĘGA JAKOŚCI ELEMENTY SYSTEMU ZARZĄDZANIA JAKOŚCI DOKUMENTACJA SYSTEMU
 1 URZĄD MIEJSKI W GOSTYNIU PREZENTACJA SYSTEMU PN EN ISO 9001:2001 ELEMENTY SYSTEMU ZARZĄDZANIA JAKOŚCIĄ STRUKTURA ORGANIZACYJNA PODZIAŁ ODPOWIEDZIALNOŚCI I UPRAWNIEŃ PROCESY ZASOBY UMOŻLIWIAJĄCE WDROŻENIA
1 URZĄD MIEJSKI W GOSTYNIU PREZENTACJA SYSTEMU PN EN ISO 9001:2001 ELEMENTY SYSTEMU ZARZĄDZANIA JAKOŚCIĄ STRUKTURA ORGANIZACYJNA PODZIAŁ ODPOWIEDZIALNOŚCI I UPRAWNIEŃ PROCESY ZASOBY UMOŻLIWIAJĄCE WDROŻENIA
System Zarządzania Jakością ISO 9001:2008
 System Zarządzania Jakością ISO 9001:2008 Każda firma ma w sobie wielką zdolność działania. Kierownictwo musi tylko znaleźć sposób, by ten potencjał wykorzystać w dojściu do postawionego przed firmą celu
System Zarządzania Jakością ISO 9001:2008 Każda firma ma w sobie wielką zdolność działania. Kierownictwo musi tylko znaleźć sposób, by ten potencjał wykorzystać w dojściu do postawionego przed firmą celu
Korzyści wynikające z wdrożenia systemu zarządzania jakością w usługach medycznych.
 Norma PN-EN ISO 9001:2009 System Zarządzania Jakością w usługach medycznych Korzyści wynikające z wdrożenia systemu zarządzania jakością w usługach medycznych. www.isomed.pl Grzegorz Dobrakowski Uwarunkowania
Norma PN-EN ISO 9001:2009 System Zarządzania Jakością w usługach medycznych Korzyści wynikające z wdrożenia systemu zarządzania jakością w usługach medycznych. www.isomed.pl Grzegorz Dobrakowski Uwarunkowania
OFERTA Zespółu ds. Zapewnienia Jakości ZPBE ENERGOPOMIAR-ELEKTRYKA SP. Z O.O. GLIWICE
 OFERTA Zespółu ds. Zapewnienia Jakości ZPBE ENERGOPOMIAR-ELEKTRYKA SP. Z O.O. GLIWICE NASZA OFERTA Usługi w zakresie systemu zarządzania zgodnego z wymaganiami normy PN-EN ISO/IEC 17025:2005: - wdrażanie
OFERTA Zespółu ds. Zapewnienia Jakości ZPBE ENERGOPOMIAR-ELEKTRYKA SP. Z O.O. GLIWICE NASZA OFERTA Usługi w zakresie systemu zarządzania zgodnego z wymaganiami normy PN-EN ISO/IEC 17025:2005: - wdrażanie
Najczęściej popełniane błędy w procesie walidacji metod badawczych
 Najczęściej popełniane błędy w procesie walidacji metod badawczych Maria Szafran Główny Specjalista Działu Akredytacji Laboratoriów Badawczych Polskie Centrum Akredytacji Metody badań proces wdrożenia
Najczęściej popełniane błędy w procesie walidacji metod badawczych Maria Szafran Główny Specjalista Działu Akredytacji Laboratoriów Badawczych Polskie Centrum Akredytacji Metody badań proces wdrożenia
Zmiany w standardzie ISO dr inż. Ilona Błaszczyk Politechnika Łódzka
 Zmiany w standardzie ISO 9001 dr inż. Ilona Błaszczyk Politechnika Łódzka 1 W prezentacji przedstawiono zmiany w normie ISO 9001 w oparciu o projekt komitetu. 2 3 4 5 6 Zmiany w zakresie terminów używanych
Zmiany w standardzie ISO 9001 dr inż. Ilona Błaszczyk Politechnika Łódzka 1 W prezentacji przedstawiono zmiany w normie ISO 9001 w oparciu o projekt komitetu. 2 3 4 5 6 Zmiany w zakresie terminów używanych
Praktyczne aspekty realizacji auditów wewnętrznych w laboratoriach podejście procesowe.
 Praktyczne aspekty realizacji auditów wewnętrznych w laboratoriach podejście procesowe. 1 Opracowała: Katarzyna Rajczakowska Warszawa dnia 16.11.2016 r. Audit wewnętrzny - definicje norma PN-EN ISO 9000:2015-10
Praktyczne aspekty realizacji auditów wewnętrznych w laboratoriach podejście procesowe. 1 Opracowała: Katarzyna Rajczakowska Warszawa dnia 16.11.2016 r. Audit wewnętrzny - definicje norma PN-EN ISO 9000:2015-10
Certyfikacja systemu zarządzania jakością w laboratorium
 INSTYTUT MATERIAŁÓW BUDOWLANYCH I TECHNOLOGII BETONU STANDARD CERTYFIKACJI SQ-2010/LB-001 Certyfikacja systemu zarządzania jakością w laboratorium Copyright by IMBiTB Wszelkie prawa autorskie zastrzeżone
INSTYTUT MATERIAŁÓW BUDOWLANYCH I TECHNOLOGII BETONU STANDARD CERTYFIKACJI SQ-2010/LB-001 Certyfikacja systemu zarządzania jakością w laboratorium Copyright by IMBiTB Wszelkie prawa autorskie zastrzeżone
Księga Jakości. Zawsze w zgodzie z prawem, uczciwie, dla dobra klienta
 Księga Jakości Zawsze w zgodzie z prawem, uczciwie, dla dobra klienta Wydanie nr 2 z dnia 25.02.2013r. Organizacja: Starostwo Powiatowe w Skarżysku-Kamiennej Adres: ul. Konarskiego 20 Tel: 41 39 53 011
Księga Jakości Zawsze w zgodzie z prawem, uczciwie, dla dobra klienta Wydanie nr 2 z dnia 25.02.2013r. Organizacja: Starostwo Powiatowe w Skarżysku-Kamiennej Adres: ul. Konarskiego 20 Tel: 41 39 53 011
RAPORT Z AUDITU NADZORU
 Klient - Nazwa Organizacji INFORMACJE PODSTAWOWE PZM WIMET ZBIGNIEW WIŚNIEWSKI SP. J. Adres 05-420 Józefów, ul. Krucza 2 Oddziały objęte zakresem certyfikacji 05-420 Józefów, ul. Krucza 2 Telefon 48 (22)
Klient - Nazwa Organizacji INFORMACJE PODSTAWOWE PZM WIMET ZBIGNIEW WIŚNIEWSKI SP. J. Adres 05-420 Józefów, ul. Krucza 2 Oddziały objęte zakresem certyfikacji 05-420 Józefów, ul. Krucza 2 Telefon 48 (22)
ZINTEGROWANY SYSTEM ZARZĄDZANIA DOKUMENT NADZOROWANY W WERSJI ELEKTRONICZNEJ Wydanie 07 Urząd Miasta Płocka. Księga środowiskowa
 Strona 1 1. Księga Środowiskowa Księga Środowiskowa to podstawowy dokument opisujący strukturę i funkcjonowanie wdrożonego w Urzędzie Systemu Zarządzania Środowiskowego zgodnego z wymaganiami normy PN-EN
Strona 1 1. Księga Środowiskowa Księga Środowiskowa to podstawowy dokument opisujący strukturę i funkcjonowanie wdrożonego w Urzędzie Systemu Zarządzania Środowiskowego zgodnego z wymaganiami normy PN-EN
PCD ZKP PROGRAM CERTYFIKACJI SYSTEMU ZAKŁADOWEJ KONTROLI PRODUKCJI
 Załącznik nr 3 do KS ZAKŁAD CERTYFIKACJI ul. Kupiecka 4, 03-042 Warszawa tel. (22) 811 02 81; e-mail: certyfikacja@icimb.pl; www.icimb.pl PCD ZKP PROGRAM CERTYFIKACJI SYSTEMU ZAKŁADOWEJ KONTROLI PRODUKCJI
Załącznik nr 3 do KS ZAKŁAD CERTYFIKACJI ul. Kupiecka 4, 03-042 Warszawa tel. (22) 811 02 81; e-mail: certyfikacja@icimb.pl; www.icimb.pl PCD ZKP PROGRAM CERTYFIKACJI SYSTEMU ZAKŁADOWEJ KONTROLI PRODUKCJI
Standard ISO 9001:2015
 Standard ISO 9001:2015 dr inż. Ilona Błaszczyk Politechnika Łódzka XXXIII Seminarium Naukowe Aktualne zagadnienia dotyczące jakości w przemyśle cukrowniczym Łódź 27-28.06.2017 1 Struktura normy ISO 9001:2015
Standard ISO 9001:2015 dr inż. Ilona Błaszczyk Politechnika Łódzka XXXIII Seminarium Naukowe Aktualne zagadnienia dotyczące jakości w przemyśle cukrowniczym Łódź 27-28.06.2017 1 Struktura normy ISO 9001:2015
ZARZĄDZANIE RYZYKIEM W LABORATORIUM BADAWCZYM W ASPEKCIE NOWELIZACJI NORMY PN-EN ISO/ IEC 17025:
 ZARZĄDZANIE RYZYKIEM W LABORATORIUM BADAWCZYM W ASPEKCIE NOWELIZACJI NORMY PN-EN ISO/ IEC 17025:2018-02 DR INŻ. AGNIESZKA WIŚNIEWSKA DOCTUS SZKOLENIA I DORADZTWO e-mail: biuro@doctus.edu.pl tel. +48 514
ZARZĄDZANIE RYZYKIEM W LABORATORIUM BADAWCZYM W ASPEKCIE NOWELIZACJI NORMY PN-EN ISO/ IEC 17025:2018-02 DR INŻ. AGNIESZKA WIŚNIEWSKA DOCTUS SZKOLENIA I DORADZTWO e-mail: biuro@doctus.edu.pl tel. +48 514
Zarządzenie Nr W ojewody Dolnośląskiego z dnia sierpnia 2016 r.
 Zarządzenie Nr W ojewody Dolnośląskiego z dnia sierpnia 2016 r. w sprawie utrzymania, doskonalenia oraz określenia zakresu odpowiedzialności Zintegrowanego Systemu Zarządzania w Dolnośląskim Urzędzie W
Zarządzenie Nr W ojewody Dolnośląskiego z dnia sierpnia 2016 r. w sprawie utrzymania, doskonalenia oraz określenia zakresu odpowiedzialności Zintegrowanego Systemu Zarządzania w Dolnośląskim Urzędzie W
Zarządzanie jakością wg norm serii ISO 9000:2000 cz.1 system, kierownictwo i zasoby
 Jakub Wierciak Zagadnienia jakości i niezawodności w projektowaniu Zarządzanie jakością wg norm serii ISO 9000:2000 cz.1 system, kierownictwo i zasoby System zarządzania jakością (ISO 9000:2000) System
Jakub Wierciak Zagadnienia jakości i niezawodności w projektowaniu Zarządzanie jakością wg norm serii ISO 9000:2000 cz.1 system, kierownictwo i zasoby System zarządzania jakością (ISO 9000:2000) System
Proces certyfikacji ISO 14001:2015
 ISO 14001:2015 Informacje o systemie W chwili obecnej szeroko pojęta ochrona środowiska stanowi istotny czynnik rozwoju gospodarczego krajów europejskich. Coraz większa liczba przedsiębiorców obniża koszty
ISO 14001:2015 Informacje o systemie W chwili obecnej szeroko pojęta ochrona środowiska stanowi istotny czynnik rozwoju gospodarczego krajów europejskich. Coraz większa liczba przedsiębiorców obniża koszty
Księga Zintegrowanego Systemu Zarządzania ODPOWIEDZIALNOŚĆ KIEROWNICTWA
 Strona: 1 z 6 1. Zaangażowanie kierownictwa Najwyższe kierownictwo SZPZLO Warszawa Ochota przejęło pełną odpowiedzialność za rozwój i ciągłe doskonalenie ustanowionego i wdrożonego zintegrowanego systemu
Strona: 1 z 6 1. Zaangażowanie kierownictwa Najwyższe kierownictwo SZPZLO Warszawa Ochota przejęło pełną odpowiedzialność za rozwój i ciągłe doskonalenie ustanowionego i wdrożonego zintegrowanego systemu
Zespół ds. Zapewnienia Jakości ZPBE ENERGOPOMIAR-ELEKTRYKA SP. Z O.O. GLIWICE
 Zespół ds. Zapewnienia Jakości ZPBE ENERGOPOMIAR-ELEKTRYKA SP. Z O.O. GLIWICE NASZA OFERTA Usługi w zakresie systemu zarządzania zgodnego z wymaganiami normy PN-EN ISO/IEC 17025:2018-02 - wdrażanie systemu
Zespół ds. Zapewnienia Jakości ZPBE ENERGOPOMIAR-ELEKTRYKA SP. Z O.O. GLIWICE NASZA OFERTA Usługi w zakresie systemu zarządzania zgodnego z wymaganiami normy PN-EN ISO/IEC 17025:2018-02 - wdrażanie systemu
WZKP Zakładowa kontrola produkcji Wymagania
 02-676 Warszawa ul. Postępu 9 tel. (22) 549 97 04; e-mail: certyfikacja@icimb.pl; www.icimb.pl Wymagania Zatwierdzam Dyrektor dr hab. inż. Adam Witek, prof. Strona 2/6 1. Wstęp 2. Wymagania ogólne 3. Dokumentacja
02-676 Warszawa ul. Postępu 9 tel. (22) 549 97 04; e-mail: certyfikacja@icimb.pl; www.icimb.pl Wymagania Zatwierdzam Dyrektor dr hab. inż. Adam Witek, prof. Strona 2/6 1. Wstęp 2. Wymagania ogólne 3. Dokumentacja
Ćwiczenie 1. System jakości w laboratorium oceny żywności
 Ćwiczenie 1. System jakości w laboratorium oceny żywności Powszechnie przyjmuje się, że każde laboratorium, które chce reprezentować wiarygodne dane musi wdrożyć odpowiednie procedury zapewnienia jakości.
Ćwiczenie 1. System jakości w laboratorium oceny żywności Powszechnie przyjmuje się, że każde laboratorium, które chce reprezentować wiarygodne dane musi wdrożyć odpowiednie procedury zapewnienia jakości.
EUROPEJSKI.* * NARODOWA STRATEGIA SPÓJNOŚCI FUNDUSZ SPOŁECZNY * **
 1 * 1 UNZA EUROPEJSKA KAPITAŁ LUDZKI.* * FUNDUSZ SPOŁECZNY * ** administracji samorządowej", Poddziałanie 5.2.1 Modernizacja zarządzania w administracji samorządowej" W PIHZ l.dane Klienta: RAPORT Z AUDITU
1 * 1 UNZA EUROPEJSKA KAPITAŁ LUDZKI.* * FUNDUSZ SPOŁECZNY * ** administracji samorządowej", Poddziałanie 5.2.1 Modernizacja zarządzania w administracji samorządowej" W PIHZ l.dane Klienta: RAPORT Z AUDITU
Charakterystyka systemu zarządzania jakością zgodnego z wymaganiami normy ISO serii 9000
 Charakterystyka systemu zarządzania jakością zgodnego z wymaganiami normy ISO serii 9000 Normy ISO serii 9000 Zostały uznane za podstawę wyznaczania standardów zarządzania jakością Opublikowane po raz
Charakterystyka systemu zarządzania jakością zgodnego z wymaganiami normy ISO serii 9000 Normy ISO serii 9000 Zostały uznane za podstawę wyznaczania standardów zarządzania jakością Opublikowane po raz
SYSTEMY ZARZĄDZANIA ŚRODOWISKOWEGO
 Auditor wewnętrzny Systemu Zarządzania Środowiskowego 26 27.11.2012 Szczecin SYSTEMY ZARZĄDZANIA ŚRODOWISKOWEGO 1 Co to jest System Zarządzania Środowiskowego (SZŚ)? 2 Zarządzanie: - sposób realizacji
Auditor wewnętrzny Systemu Zarządzania Środowiskowego 26 27.11.2012 Szczecin SYSTEMY ZARZĄDZANIA ŚRODOWISKOWEGO 1 Co to jest System Zarządzania Środowiskowego (SZŚ)? 2 Zarządzanie: - sposób realizacji
SZKOLENIA I WARSZTATY
 SZKOLENIA I WARSZTATY wg. Norm ISO : 9001, ISO 14001, PN-N-18001/OHSAS, ISO/IEC 27001, ISO 22000, ISO 50001, ISO 22301 1. Pełnomocnik Systemu Zarządzania/ Przedstawiciel Najwyższego Kierownictwa - nowa
SZKOLENIA I WARSZTATY wg. Norm ISO : 9001, ISO 14001, PN-N-18001/OHSAS, ISO/IEC 27001, ISO 22000, ISO 50001, ISO 22301 1. Pełnomocnik Systemu Zarządzania/ Przedstawiciel Najwyższego Kierownictwa - nowa
Zarządzanie Jakością. System jakości jako narzędzie zarządzania przedsiębiorstwem. Dr Mariusz Maciejczak
 Zarządzanie Jakością System jakości jako narzędzie zarządzania przedsiębiorstwem Dr Mariusz Maciejczak SYSTEM System to zespół powiązanych ze sobą elementów, które stanowią pewną całość. Istotną cechą
Zarządzanie Jakością System jakości jako narzędzie zarządzania przedsiębiorstwem Dr Mariusz Maciejczak SYSTEM System to zespół powiązanych ze sobą elementów, które stanowią pewną całość. Istotną cechą
System zarządzania laboratorium
 Biuro Zarządzania Jakością, Środowiskiem i BHP Sp. z o.o. przy wsparciu merytorycznym Politechniki Warszawskiej zaprasza wszystkich chętnych do udziału w cyklu szkoleń System zarządzania laboratorium Oferowany
Biuro Zarządzania Jakością, Środowiskiem i BHP Sp. z o.o. przy wsparciu merytorycznym Politechniki Warszawskiej zaprasza wszystkich chętnych do udziału w cyklu szkoleń System zarządzania laboratorium Oferowany
System Zarządzania Jakością Prawo atomowe oraz inne wymagania prawne / ISO 9001
 System Zarządzania Jakością Prawo atomowe oraz inne wymagania prawne / ISO 9001 RAZEM czy OSOBNO? Auditor wiodący Beata Kiercz maj 2015 SYSTEM ZARZĄDZANIA JAKOŚCIĄ NARZĘDZIE BIZNESOWE oparte na: ścisłym
System Zarządzania Jakością Prawo atomowe oraz inne wymagania prawne / ISO 9001 RAZEM czy OSOBNO? Auditor wiodący Beata Kiercz maj 2015 SYSTEM ZARZĄDZANIA JAKOŚCIĄ NARZĘDZIE BIZNESOWE oparte na: ścisłym
KSIĘGA JAKOŚCI 8. POMIARY, ANALIZA, DOSKONALENIE
 1/5. 2/5..1. Postanowienia ogólne. Urząd Miejski planuje i wdraża działania dotyczące pomiarów i monitorowania kierując się potrzebami Klientów oraz zapewnieniem poprawnego działania Systemu Zarządzania
1/5. 2/5..1. Postanowienia ogólne. Urząd Miejski planuje i wdraża działania dotyczące pomiarów i monitorowania kierując się potrzebami Klientów oraz zapewnieniem poprawnego działania Systemu Zarządzania
Rektora Państwowej Wyższej Szkoły Zawodowej w Koninie z dnia 9 listopada 2011 roku
 ZARZĄDZENIE Nr 84/2011 Rektora Państwowej Wyższej Szkoły Zawodowej w Koninie z dnia 9 listopada 2011 roku zmieniające zasady organizacji studiów podyplomowych Zarządzanie jakością Na podstawie 7 Regulaminu
ZARZĄDZENIE Nr 84/2011 Rektora Państwowej Wyższej Szkoły Zawodowej w Koninie z dnia 9 listopada 2011 roku zmieniające zasady organizacji studiów podyplomowych Zarządzanie jakością Na podstawie 7 Regulaminu
System. zarządzania jakością. Pojęcie systemu. Model SZJ wg ISO 9001:2008. Koszty jakości. Podsumowanie. [Słownik języka polskiego, PWN, 1979] System
![System. zarządzania jakością. Pojęcie systemu. Model SZJ wg ISO 9001:2008. Koszty jakości. Podsumowanie. [Słownik języka polskiego, PWN, 1979] System System. zarządzania jakością. Pojęcie systemu. Model SZJ wg ISO 9001:2008. Koszty jakości. Podsumowanie. [Słownik języka polskiego, PWN, 1979] System](/thumbs/53/30829885.jpg) Zarządzanie - wykład 3 Jakość produktu Pojęcie i zasady Zarządzanie. Planowanie w zarządzaniu Kontrola w zarządzaniu Metody i narzędzia projakościowe Wykład 03/07 Model SZJ Doskonalenie w zarządzaniu 2
Zarządzanie - wykład 3 Jakość produktu Pojęcie i zasady Zarządzanie. Planowanie w zarządzaniu Kontrola w zarządzaniu Metody i narzędzia projakościowe Wykład 03/07 Model SZJ Doskonalenie w zarządzaniu 2
Program szkoleń - Zarządzanie Jakoscią
 20 11 - Zarządzanie Jakoscią SZKOLENIA OGÓLNE WARUNKI SZKOLEO kod: QA_Q1 - System Zarządzania Jakością wymagania normy ISO 9001: 2008 kod: QA_Q2 - System Zarządzania Jakością w organizacji ochrony zdrowia
20 11 - Zarządzanie Jakoscią SZKOLENIA OGÓLNE WARUNKI SZKOLEO kod: QA_Q1 - System Zarządzania Jakością wymagania normy ISO 9001: 2008 kod: QA_Q2 - System Zarządzania Jakością w organizacji ochrony zdrowia
Dobre praktyki integracji systemów zarządzania w administracji rządowej, na przykładzie Ministerstwa Gospodarki. Warszawa, 25 lutego 2015 r.
 Dobre praktyki integracji systemów zarządzania w administracji rządowej, na przykładzie Ministerstwa Gospodarki Warszawa, 25 lutego 2015 r. 2 W celu zapewnienia, jak również ciągłego doskonalenia jakości,
Dobre praktyki integracji systemów zarządzania w administracji rządowej, na przykładzie Ministerstwa Gospodarki Warszawa, 25 lutego 2015 r. 2 W celu zapewnienia, jak również ciągłego doskonalenia jakości,
JAK SKUTECZNIE PRZEPROWADZAĆ AUDITY
 Klub Polskich Laboratoriów Badawczych POLLAB JAK SKUTECZNIE PRZEPROWADZAĆ AUDITY Anna Pastuszewska - Paruch Definicje Audit systematyczny, niezależny i udokumentowany proces uzyskiwania dowodów z auditu
Klub Polskich Laboratoriów Badawczych POLLAB JAK SKUTECZNIE PRZEPROWADZAĆ AUDITY Anna Pastuszewska - Paruch Definicje Audit systematyczny, niezależny i udokumentowany proces uzyskiwania dowodów z auditu
SYSTEM ZARZĄDZANIA JAKOŚCIĄ
 Strona: 2 z 7 NAZWA PROCESU Istota / cel procesu System Zarządzania Jakością. Planowane, systematyczne i obiektywne badanie zgodności i skuteczności procesów realizowanych w ramach ustanowionego systemu
Strona: 2 z 7 NAZWA PROCESU Istota / cel procesu System Zarządzania Jakością. Planowane, systematyczne i obiektywne badanie zgodności i skuteczności procesów realizowanych w ramach ustanowionego systemu
SYSTEMY ZARZĄDZANIA JAKOŚCIĄ WEDŁUG
 Wykład 10. SYSTEMY ZARZĄDZANIA JAKOŚCIĄ WEDŁUG NORM ISO 9000 1 1. Rodzina norm ISO 9000: Normy ISO 9000 są od 1987r., a trzecia rodzina norm ISO 9000 z 2000 r. (doskonalona w kolejnych latach) składa się
Wykład 10. SYSTEMY ZARZĄDZANIA JAKOŚCIĄ WEDŁUG NORM ISO 9000 1 1. Rodzina norm ISO 9000: Normy ISO 9000 są od 1987r., a trzecia rodzina norm ISO 9000 z 2000 r. (doskonalona w kolejnych latach) składa się
Konferencja Cukrownicza Katarzyna Mokrosińska
 Konferencja Cukrownicza 22-23.06.2010 Weryfikacja SZJ / HACCP Różne aspekty auditów wewnętrznych 2 Systemy zarządzania Utrzymywanie i rozwój systemów zarządzania w firmach, wymaga ich systematycznej weryfikacji
Konferencja Cukrownicza 22-23.06.2010 Weryfikacja SZJ / HACCP Różne aspekty auditów wewnętrznych 2 Systemy zarządzania Utrzymywanie i rozwój systemów zarządzania w firmach, wymaga ich systematycznej weryfikacji
DCT/ISO/SC/1.01 Księga Jakości DCT Gdańsk S.A. Informacja dla Klientów 2014-04-29
 DCT/ISO/SC/1.01 Księga Jakości DCT Gdańsk S.A. Informacja dla Klientów 2014-04-29 2 ELEMENTY KSIĘGI JAKOŚCI 1. Terminologia 2. Informacja o Firmie 3. Podejście procesowe 4. Zakres Systemu Zarządzania Jakością
DCT/ISO/SC/1.01 Księga Jakości DCT Gdańsk S.A. Informacja dla Klientów 2014-04-29 2 ELEMENTY KSIĘGI JAKOŚCI 1. Terminologia 2. Informacja o Firmie 3. Podejście procesowe 4. Zakres Systemu Zarządzania Jakością
Historia norm ISO serii 9000
 Historia norm ISO serii 9000 15.XII.2000 Nowelizacja norm ISO serii 9000 1996 Normy PN-ISO serii 9000 1994 Aktualizacja norm ISO serii 9000 1993 Normy PN-EN serii 29000 1987 Normy ISO serii 9000 1979 Brytyjska
Historia norm ISO serii 9000 15.XII.2000 Nowelizacja norm ISO serii 9000 1996 Normy PN-ISO serii 9000 1994 Aktualizacja norm ISO serii 9000 1993 Normy PN-EN serii 29000 1987 Normy ISO serii 9000 1979 Brytyjska
DOSKONALENIE SYSTEMU JAKOŚCI Z WYKORZYSTANIEM MODELU PDCA
 Koncepcje zarządzania jakością. Doświadczenia i perspektywy., red. Sikora T., Uniwersytet Ekonomiczny w Krakowie, Kraków 2008, ss. 17-22 Urszula Balon Uniwersytet Ekonomiczny w Krakowie DOSKONALENIE SYSTEMU
Koncepcje zarządzania jakością. Doświadczenia i perspektywy., red. Sikora T., Uniwersytet Ekonomiczny w Krakowie, Kraków 2008, ss. 17-22 Urszula Balon Uniwersytet Ekonomiczny w Krakowie DOSKONALENIE SYSTEMU
Zarządzanie bezpieczeństwem informacji przegląd aktualnych standardów i metodyk
 Zarządzanie bezpieczeństwem informacji przegląd aktualnych standardów i metodyk dr T Bartosz Kalinowski 17 19 września 2008, Wisła IV Sympozjum Klubu Paragraf 34 1 Informacja a system zarządzania Informacja
Zarządzanie bezpieczeństwem informacji przegląd aktualnych standardów i metodyk dr T Bartosz Kalinowski 17 19 września 2008, Wisła IV Sympozjum Klubu Paragraf 34 1 Informacja a system zarządzania Informacja
OCHRONA RADIOLOGICZNA PACJENTA. System Zarządzania Jakością
 OCHRONA RADIOLOGICZNA PACJENTA System Zarządzania Jakością SZJ SYSTEM - zbiór wzajemnie powiązanych ze sobą elementów, których suma jest czymś więcej niż suma oddzielnych jego elementów - wspólne zadanie
OCHRONA RADIOLOGICZNA PACJENTA System Zarządzania Jakością SZJ SYSTEM - zbiór wzajemnie powiązanych ze sobą elementów, których suma jest czymś więcej niż suma oddzielnych jego elementów - wspólne zadanie
Zmiany i nowe wymagania w normie ISO 9001:2008
 FORUM WYMIANY DOŚWIADCZEŃ DLA KONSULTANTÓW 19-20 listopada 2007r. Zmiany i nowe wymagania w normie ISO 9001:2008 Grzegorz Grabka Dyrektor Działu Certyfikacji Systemów, Auditor Senior TÜV CERT 1 Zmiany
FORUM WYMIANY DOŚWIADCZEŃ DLA KONSULTANTÓW 19-20 listopada 2007r. Zmiany i nowe wymagania w normie ISO 9001:2008 Grzegorz Grabka Dyrektor Działu Certyfikacji Systemów, Auditor Senior TÜV CERT 1 Zmiany
KARTA PROCESU VII.00.00/02 SYSTEM ZARZĄDZANIA JAKOŚCIĄ. LIDERZY PROCESU SEKRETARZ WOJEWÓDZTWA PEŁNOMOCNIK ds. SYSTEMU ZARZĄDZANIA JAKOŚCIĄ
 URZĄD MARSZAŁKOWSKI WOJEWÓDZTWA KUJAWSKO-POMORSKIEGO PN-EN ISO 9001:2009 Załącznik 7 do Zarządzenia Nr 46/2010 Marszałka Województwa Kujawsko-Pomorskiego z dnia 19 listopada 2010 roku KARTA PROCESU SYSTEM
URZĄD MARSZAŁKOWSKI WOJEWÓDZTWA KUJAWSKO-POMORSKIEGO PN-EN ISO 9001:2009 Załącznik 7 do Zarządzenia Nr 46/2010 Marszałka Województwa Kujawsko-Pomorskiego z dnia 19 listopada 2010 roku KARTA PROCESU SYSTEM
Instytut Spawalnictwa w Gliwicach Ośrodek Certyfikacji
 1 Wymagania ogólne Wytwórca powinien ustanowić, dokumentować i utrzymywać system ZKP, aby zapewnić, że wyroby wprowadzone na rynek są zgodne z określoną i przedstawioną charakterystyką. System ZKP powinien
1 Wymagania ogólne Wytwórca powinien ustanowić, dokumentować i utrzymywać system ZKP, aby zapewnić, że wyroby wprowadzone na rynek są zgodne z określoną i przedstawioną charakterystyką. System ZKP powinien
ETAPY WDRAŻANIA SYSTEMÓW ZARZĄDZANIA JAKOŚCIĄ
 ETAPY WDRAŻANIA SYSTEMÓW ZARZĄDZANIA JAKOŚCIĄ Standardowe etapy wdrażania systemu zarzadzania jakością ETAP I: Audit wstępny zapoznanie się z organizacją ETAP II: Szkolenie dla Kierownictwa i grupy wdrożeniowej
ETAPY WDRAŻANIA SYSTEMÓW ZARZĄDZANIA JAKOŚCIĄ Standardowe etapy wdrażania systemu zarzadzania jakością ETAP I: Audit wstępny zapoznanie się z organizacją ETAP II: Szkolenie dla Kierownictwa i grupy wdrożeniowej
PEŁNOMOCNIK I AUDYTOR WEWNĘTRZNY ZINTEGROWANEGO SYSTEMU ZARZĄDZANIA JAKOŚCIĄ I ŚRODOWISKOWEGO wg ISO 9001 oraz ISO 14001
 INFORMACJE SZCZEGÓŁOWE NA TEMAT SZKOLENIA OTWARTEGO: PEŁNOMOCNIK I AUDYTOR WEWNĘTRZNY ZINTEGROWANEGO SYSTEMU ZARZĄDZANIA JAKOŚCIĄ I ŚRODOWISKOWEGO wg ISO 9001 oraz ISO 14001 S t r o n a 2 z 5 Serdecznie
INFORMACJE SZCZEGÓŁOWE NA TEMAT SZKOLENIA OTWARTEGO: PEŁNOMOCNIK I AUDYTOR WEWNĘTRZNY ZINTEGROWANEGO SYSTEMU ZARZĄDZANIA JAKOŚCIĄ I ŚRODOWISKOWEGO wg ISO 9001 oraz ISO 14001 S t r o n a 2 z 5 Serdecznie
Zarządzenie Nr 14/2009 Burmistrza Miasta Czeladź. z dnia 28 stycznia 2009. w sprawie: wprowadzenia procedury nadzoru nad dokumentami i zapisami.
 Zarządzenie Nr 14/2009 Burmistrza Miasta Czeladź z dnia 28 stycznia 2009 w sprawie: wprowadzenia procedury nadzoru nad dokumentami i zapisami. Na podstawie art. 31 oraz art. 33 ust.1, 3 i 5 ustawy z dnia
Zarządzenie Nr 14/2009 Burmistrza Miasta Czeladź z dnia 28 stycznia 2009 w sprawie: wprowadzenia procedury nadzoru nad dokumentami i zapisami. Na podstawie art. 31 oraz art. 33 ust.1, 3 i 5 ustawy z dnia
DEKLARACJA POLITYKI JAKOŚCI
 INSTYTUT TECHNOLOGICZNO-PRZYRODNICZY W FALENTACH ODDZIAŁ W WARSZAWIE JEDNOSTKA CERTYFIKUJĄCA WYROBY ul. Rakowiecka 32, 02-532 Warszawa tel/fax:+48 (22) 542 11 84; tel: (22) 542-11-61; 542-11-79 e-mail:
INSTYTUT TECHNOLOGICZNO-PRZYRODNICZY W FALENTACH ODDZIAŁ W WARSZAWIE JEDNOSTKA CERTYFIKUJĄCA WYROBY ul. Rakowiecka 32, 02-532 Warszawa tel/fax:+48 (22) 542 11 84; tel: (22) 542-11-61; 542-11-79 e-mail:
UCHWAŁA Nr 12/2011 Rady Wydziału Społeczno-Technicznego Państwowej Wyższej Szkoły Zawodowej w Koninie z dnia 18 października 2011 r.
 UCHWAŁA Nr 12/2011 Rady Wydziału Społeczno-Technicznego Państwowej Wyższej Szkoły Zawodowej w Koninie z dnia 18 października 2011 r. zmieniająca uchwałę w sprawie uchwalenia planów studiów podyplomowych
UCHWAŁA Nr 12/2011 Rady Wydziału Społeczno-Technicznego Państwowej Wyższej Szkoły Zawodowej w Koninie z dnia 18 października 2011 r. zmieniająca uchwałę w sprawie uchwalenia planów studiów podyplomowych
Zarządzenie Nr 458/2009 Prezydenta Miasta Kalisza z dnia 21 października 2009 r.
 Zarządzenie Nr 458/2009 Prezydenta Miasta Kalisza z dnia 21 października 2009 r. w sprawie wprowadzenia procedury wewnętrznych auditów Systemu Zarządzania Jakością (NS-01). Na podstawie art. 33 ust. 1
Zarządzenie Nr 458/2009 Prezydenta Miasta Kalisza z dnia 21 października 2009 r. w sprawie wprowadzenia procedury wewnętrznych auditów Systemu Zarządzania Jakością (NS-01). Na podstawie art. 33 ust. 1
Matryca efektów kształcenia dla programu studiów podyplomowych ZARZĄDZANIE I SYSTEMY ZARZĄDZANIA JAKOŚCIĄ
 Podstawy firmą Marketingowe aspekty jakością Podstawy prawa gospodarczego w SZJ Zarządzanie Jakością (TQM) Zarządzanie logistyczne w SZJ Wymagania norm ISO serii 9000 Dokumentacja w SZJ Metody i Techniki
Podstawy firmą Marketingowe aspekty jakością Podstawy prawa gospodarczego w SZJ Zarządzanie Jakością (TQM) Zarządzanie logistyczne w SZJ Wymagania norm ISO serii 9000 Dokumentacja w SZJ Metody i Techniki
Wymagania wobec dostawców: jakościowe, środowiskowe, bhp i etyczne
 VI Konferencja nt. systemów zarządzania w energetyce Nowe Czarnowo Świnoujście, 21-23 X 2008 Wymagania wobec dostawców: jakościowe, środowiskowe, bhp i etyczne Grzegorz Ścibisz Łańcuch dostaw DOSTAWCA
VI Konferencja nt. systemów zarządzania w energetyce Nowe Czarnowo Świnoujście, 21-23 X 2008 Wymagania wobec dostawców: jakościowe, środowiskowe, bhp i etyczne Grzegorz Ścibisz Łańcuch dostaw DOSTAWCA
NS-01 Procedura auditów wewnętrznych systemu zarządzania jakością
 Załącznik nr 1 do zarządzenia Burmistrza Miasta Środa Wielkopolska Nr 19/2010 z dnia 22 lutego 2010 r. NS-01 Procedura auditów wewnętrznych systemu zarządzania jakością 1. Cel procedury Celem procedury
Załącznik nr 1 do zarządzenia Burmistrza Miasta Środa Wielkopolska Nr 19/2010 z dnia 22 lutego 2010 r. NS-01 Procedura auditów wewnętrznych systemu zarządzania jakością 1. Cel procedury Celem procedury
KSIĘGA JAKOŚCI POMIARY, ANALIZA I DOSKONALENIE
 Wydanie: 4 z dnia 09.06.2009r zmiana: 0 Strona 1 z 13 8.1 Postanowienia ogólne W Szpitalu Miejskim w Elblągu zostały zaplanowane i wdroŝone procesy monitorowania i pomiarów oraz analizy danych i doskonalenia
Wydanie: 4 z dnia 09.06.2009r zmiana: 0 Strona 1 z 13 8.1 Postanowienia ogólne W Szpitalu Miejskim w Elblągu zostały zaplanowane i wdroŝone procesy monitorowania i pomiarów oraz analizy danych i doskonalenia
Zmiany wymagań normy ISO 14001
 Zmiany wymagań normy ISO 14001 Międzynarodowa Organizacja Normalizacyjna (ISO) opublikowała 15 listopada br. zweryfikowane i poprawione wersje norm ISO 14001 i ISO 14004. Od tego dnia są one wersjami obowiązującymi.
Zmiany wymagań normy ISO 14001 Międzynarodowa Organizacja Normalizacyjna (ISO) opublikowała 15 listopada br. zweryfikowane i poprawione wersje norm ISO 14001 i ISO 14004. Od tego dnia są one wersjami obowiązującymi.
KSIĘGA JAKOŚCI SYSTEM ZARZĄDZANIA JAKOŚCIĄ. 4.1 Wymagania ogólne i zakres obowiązywania systemu zarządzania jakością.
 Wydanie: 4 z dnia 09.06.2009r zmiana: 0 Strona 1 z 6 4.1 Wymagania ogólne i zakres obowiązywania systemu zarządzania jakością. W Szpitalu Miejskim w Elblągu został ustanowiony, udokumentowany, wdroŝony
Wydanie: 4 z dnia 09.06.2009r zmiana: 0 Strona 1 z 6 4.1 Wymagania ogólne i zakres obowiązywania systemu zarządzania jakością. W Szpitalu Miejskim w Elblągu został ustanowiony, udokumentowany, wdroŝony
Akredytacja metod badawczych jako podstawa potwierdzenia kompetencji wykonywania badań w laboratoriach
 Anna Krawczuk WROCŁAWSKIE CENTRUM BADAŃ EIT+ Akredytacja metod badawczych jako podstawa potwierdzenia kompetencji wykonywania badań w laboratoriach WROCŁAWSKIE CENTRUM BADAŃ EIT+ AKREDYTACJA DEFINICJA
Anna Krawczuk WROCŁAWSKIE CENTRUM BADAŃ EIT+ Akredytacja metod badawczych jako podstawa potwierdzenia kompetencji wykonywania badań w laboratoriach WROCŁAWSKIE CENTRUM BADAŃ EIT+ AKREDYTACJA DEFINICJA
System zarządzania laboratorium
 Biuro Zarządzania Jakością, Środowiskiem i BHP Sp. z o.o. przy wsparciu merytorycznym Politechniki Warszawskiej zaprasza wszystkich chętnych do udziału w cyklu szkoleń System zarządzania laboratorium Oferowany
Biuro Zarządzania Jakością, Środowiskiem i BHP Sp. z o.o. przy wsparciu merytorycznym Politechniki Warszawskiej zaprasza wszystkich chętnych do udziału w cyklu szkoleń System zarządzania laboratorium Oferowany
Skrót wymagań normy ISO 9001/2:1994, PN-ISO 9001/2:1996
 Skrót wymagań normy ISO 9001/2:1994, PN-ISO 9001/2:1996 (pojęcie wyrób dotyczy też usług, w tym, o charakterze badań) 4.1. Odpowiedzialność kierownictwa. 4.1.1. Polityka Jakości (krótki dokument sygnowany
Skrót wymagań normy ISO 9001/2:1994, PN-ISO 9001/2:1996 (pojęcie wyrób dotyczy też usług, w tym, o charakterze badań) 4.1. Odpowiedzialność kierownictwa. 4.1.1. Polityka Jakości (krótki dokument sygnowany
POLITYKA JAKOŚCI. Polityka jakości to formalna i ogólna deklaracja firmy, jak zamierza traktować sprawy zarządzania jakością.
 POLITYKA JAKOŚCI Polityka jakości jest zestawem nadrzędnych celów, zamiarów oraz orientacji organizacji na jakość. Stanowi ona dowód na to, że przedsiębiorca wie, czego chce i kieruje swoim przedsiębiorstwem
POLITYKA JAKOŚCI Polityka jakości jest zestawem nadrzędnych celów, zamiarów oraz orientacji organizacji na jakość. Stanowi ona dowód na to, że przedsiębiorca wie, czego chce i kieruje swoim przedsiębiorstwem
1.2. Zlecenie może być wystawione w formie elektronicznej z zachowaniem wymagań, o których mowa w poz. 1.1.
 Załączniki do rozporządzenia Ministra Zdrowia z dnia 2005 r. (poz. ) Załącznik Nr 1 Podstawowe standardy jakości w czynnościach laboratoryjnej diagnostyki medycznej, ocenie ich jakości i wartości diagnostycznej
Załączniki do rozporządzenia Ministra Zdrowia z dnia 2005 r. (poz. ) Załącznik Nr 1 Podstawowe standardy jakości w czynnościach laboratoryjnej diagnostyki medycznej, ocenie ich jakości i wartości diagnostycznej
Elastyczny zakres akredytacji
 Elastyczny zakres akredytacji podejście praktyczne na przykładzie laboratoriów Centrum Badań Jakości sp. z o.o. w Lubinie Katarzyna Rajczakowska Warszawa, grudzień 2010 r. Elastyczny zakres w dokumentach
Elastyczny zakres akredytacji podejście praktyczne na przykładzie laboratoriów Centrum Badań Jakości sp. z o.o. w Lubinie Katarzyna Rajczakowska Warszawa, grudzień 2010 r. Elastyczny zakres w dokumentach
Dokumentacja systemu zarządzania bezpieczeństwem pracy i ochroną zdrowia
 Dokumentacja systemu zarządzania bezpieczeństwem pracy i ochroną zdrowia Dariusz Smoliński Część 1 Prezentacja dostępna na: http://sites.google.com/site/dariuszromualdsmolinski/home/politechnika-gdanska
Dokumentacja systemu zarządzania bezpieczeństwem pracy i ochroną zdrowia Dariusz Smoliński Część 1 Prezentacja dostępna na: http://sites.google.com/site/dariuszromualdsmolinski/home/politechnika-gdanska
Systemy zarządzania jakością
 Systemy zarządzania jakością cechy, funkcje, etapy wdrażania systemu Prezentacja na spotkanie 3 System zarządzania jakością - czym jest a czym nie jest? System zarządzania jakością jest: zbiorem reguł,
Systemy zarządzania jakością cechy, funkcje, etapy wdrażania systemu Prezentacja na spotkanie 3 System zarządzania jakością - czym jest a czym nie jest? System zarządzania jakością jest: zbiorem reguł,
ISO 14000 w przedsiębiorstwie
 ISO 14000 w przedsiębiorstwie Rodzina norm ISO 14000 TC 207 ZARZADZANIE ŚRODOWISKOWE SC1 System zarządzania środowiskowego SC2 Audity środowiskowe SC3 Ekoetykietowanie SC4 Ocena wyników ekologicznych SC5
ISO 14000 w przedsiębiorstwie Rodzina norm ISO 14000 TC 207 ZARZADZANIE ŚRODOWISKOWE SC1 System zarządzania środowiskowego SC2 Audity środowiskowe SC3 Ekoetykietowanie SC4 Ocena wyników ekologicznych SC5
Szkolenie Stowarzyszenia Polskie Forum ISO 14000 Zmiany w normie ISO 14001 i ich konsekwencje dla organizacji Warszawa, 16.04.2015
 Wykorzystanie elementów systemu EMAS w SZŚ według ISO 14001:2015 dr hab. inż. Alina Matuszak-Flejszman, prof. nadzw. UEP Agenda Elementy SZŚ według EMAS (Rozporządzenie UE 1221/2009) i odpowiadające im
Wykorzystanie elementów systemu EMAS w SZŚ według ISO 14001:2015 dr hab. inż. Alina Matuszak-Flejszman, prof. nadzw. UEP Agenda Elementy SZŚ według EMAS (Rozporządzenie UE 1221/2009) i odpowiadające im
Pełnomocnik, Audytor SZJ ISO 9001:2008
 Pełnomocnik, Audytor SZJ ISO Informacje o usłudze Numer usługi 2016/07/06/8177/12401 Cena netto 1 617,89 zł Cena brutto 1 990,00 zł Cena netto za godzinę 67,41 zł Cena brutto za godzinę 82,92 Usługa z
Pełnomocnik, Audytor SZJ ISO Informacje o usłudze Numer usługi 2016/07/06/8177/12401 Cena netto 1 617,89 zł Cena brutto 1 990,00 zł Cena netto za godzinę 67,41 zł Cena brutto za godzinę 82,92 Usługa z
Ryzyko w świetle nowych norm ISO 9001:2015 i 14001:2015
 Ryzyko w świetle nowych norm ISO 9001:2015 i 14001:2015 Rafał Śmiłowski_04.2016 Harmonogram zmian 2 Najważniejsze zmiany oraz obszary Przywództwo Większy nacisk na top menedżerów do udziału w systemie
Ryzyko w świetle nowych norm ISO 9001:2015 i 14001:2015 Rafał Śmiłowski_04.2016 Harmonogram zmian 2 Najważniejsze zmiany oraz obszary Przywództwo Większy nacisk na top menedżerów do udziału w systemie
Zakład Certyfikacji 03-042 Warszawa, ul. Kupiecka 4 Sekcja Ceramiki i Szkła ul. Postępu 9 02-676 Warszawa PROGRAM CERTYFIKACJI
 Zakład Certyfikacji 03-042 Warszawa, ul. Kupiecka 4 Sekcja Ceramiki i Szkła ul. Postępu 9 02-676 Warszawa PC-04 PROGRAM CERTYFIKACJA ZGODNOŚCI WYROBU Z KRYTERIAMI TECHNICZNYMI certyfikacja dobrowolna Warszawa,
Zakład Certyfikacji 03-042 Warszawa, ul. Kupiecka 4 Sekcja Ceramiki i Szkła ul. Postępu 9 02-676 Warszawa PC-04 PROGRAM CERTYFIKACJA ZGODNOŚCI WYROBU Z KRYTERIAMI TECHNICZNYMI certyfikacja dobrowolna Warszawa,
Poznań 23 listopada 2016 r. A u t o r : dr inż. Ludwik Królas
 Ośrodek Kwalifikacji Jakości Wyrobów SIMPTEST Sp. z o.o. Sp. k. ul. Przemysłowa 34 A, 61-579 Poznań, tel. 61-833-68-78 biuro@simptest.poznan.pl www.simptest.poznan.pl 1 Seminarium nt. Zarządzanie ryzykiem
Ośrodek Kwalifikacji Jakości Wyrobów SIMPTEST Sp. z o.o. Sp. k. ul. Przemysłowa 34 A, 61-579 Poznań, tel. 61-833-68-78 biuro@simptest.poznan.pl www.simptest.poznan.pl 1 Seminarium nt. Zarządzanie ryzykiem
ZAKŁADOWA ADOWA KONTROLA PRODUKCJI W ŚWIETLE WYMAGAŃ CPR
 ZAKŁADOWA ADOWA KONTROLA PRODUKCJI W ŚWIETLE WYMAGAŃ CPR Alicja Papier Warszawa, kwiecień 2014 Wprowadzanie wyrobów w budowlanych wg CPR Wszystkie podmioty gospodarcze w łańcuchu dostaw i dystrybucji powinny
ZAKŁADOWA ADOWA KONTROLA PRODUKCJI W ŚWIETLE WYMAGAŃ CPR Alicja Papier Warszawa, kwiecień 2014 Wprowadzanie wyrobów w budowlanych wg CPR Wszystkie podmioty gospodarcze w łańcuchu dostaw i dystrybucji powinny
Opis procedury certyfikacyjnej Program certyfikacji systemów zarządzania
 to inaczej mówiąc skrócony opis procedury systemów realizowanej przez Jednostkę Certyfikującą Systemy Zarządzania TÜV NORD Polska Sp. z o.o. (dalej zwaną Jednostką Certyfikującą) w oparciu o wymagania
to inaczej mówiąc skrócony opis procedury systemów realizowanej przez Jednostkę Certyfikującą Systemy Zarządzania TÜV NORD Polska Sp. z o.o. (dalej zwaną Jednostką Certyfikującą) w oparciu o wymagania
Spis treści. Przedmowa... 11. Rozdział I. Systemowe zarządzanie jakością... 15
 Przedmowa... 11 Rozdział I. Systemowe zarządzanie jakością... 15 1. Charakterystyka zarządzania jakością... 15 1.1. Zarządzanie a kierowanie... 15 1.2. Cel i obiekt zarządzania... 16 1.3. Definiowanie
Przedmowa... 11 Rozdział I. Systemowe zarządzanie jakością... 15 1. Charakterystyka zarządzania jakością... 15 1.1. Zarządzanie a kierowanie... 15 1.2. Cel i obiekt zarządzania... 16 1.3. Definiowanie
Postępowanie z usługą niezgodną. Działania korygujące i zapobiegawcze.
 ostępowanie z usługą niezgodną. Strona: 2 z 6 1. Cel działania. Celem procedury jest zapewnienie, że istnieją i funkcjonują mechanizmy identyfikowania niezgodności oraz ich nadzorowania, podejmowania działań
ostępowanie z usługą niezgodną. Strona: 2 z 6 1. Cel działania. Celem procedury jest zapewnienie, że istnieją i funkcjonują mechanizmy identyfikowania niezgodności oraz ich nadzorowania, podejmowania działań
