Przewodnik do ćwiczeń z Genetyki II rok Ochrona Środowiska Studia Stacjonarne
|
|
|
- Sylwester Adamczyk
- 8 lat temu
- Przeglądów:
Transkrypt
1 Wydział Ochrony Środowiska i Rybactwa UWM w Olsztynie Przewodnik do ćwiczeń z Genetyki II rok Ochrona Środowiska Studia Stacjonarne Sławomir Ciesielski Małgorzata Jankun Darek Kaczmarczyk Mirosław Łuczyński Paweł Woźnicki Olsztyn 2006
2 Ćwiczenie 1 Ćwiczenia z przedmiotu Genetyka Państwo studenci przychodzą na zajęcia przygotowani teoretycznie oraz wyposażeni w przybory do pisania, kalkulator oraz w przypadku ćwiczeń laboratoryjnych w białe fartuchy, dopuszczalna jest nieusprawiedliwiona nieobecność na jednym ćwiczeniu (konieczne jest zaliczenie tego ćwiczenia podczas konsultacji) oraz dwie nieobecności usprawiedliwione (możliwe jest zaliczenie tych ćwiczeń podczas konsultacji), podczas każdego ćwiczenia odbywa się sprawdzian z wiadomości dotyczących poprzedniego i bieżącego ćwiczenia, ocena z ćwiczeń to średnia ocena z wszystkich sprawdzianów (pisemnych i ustnych) pomniejszona o 0,5 za każde ćwiczenie nie zaliczone, przedmiot kończy się egzaminem, a zaliczenie ćwiczeń musi zakończyć się przed letnią sesją egzaminacyjną. Kierownik przedmiotu: Prof. dr hab. Mirosław Łuczyński, prof. zw. Katedra Biotechnologii w Ochronie Środowiska ul. Słoneczna 45G telefon oraz faks: (+48) mirekl@uwm.edu.pl Prowadzący ćwiczenia: dr inż. Sławomir Ciesielski Katedra Biotechnologii w Ochronie Środowiska ul. Słoneczna 45G telefon : (+48) slavcm@uwm.edu.pl
3 Ćwiczenie 1 Szczegółowv program ćwiczeń z przedmiotu GENETYKA dla studentów II roku kierunku Ochrona Środowiska Ćwiczenie 1. Wprowadzenie: regulamin ćwiczeń i zasady zaliczania, plan ćwiczeń, literatura do ćwiczeń z przedmiotu. Podstawy dziedziczenia: I i II prawo Mendla. Rozwiązywanie zadań. Ćwiczenie 2. Genetyka muszki owocowej (Drosophila melanogaster). Wykorzystanie programu komputerowego DrosophiLab (sala komputerowa). Ćwiczenie 3. Podstawy hodowli Drosophila melanogaster, usypianie much, rozdzielanie według płci oraz poszczególnych fenotypów przy użyciu lupy, wyprowadzanie much ze stanu narkozy do stanu aktywności. Geny autosomalne i sprzężone z płcią. Wykonanie odpowiednich krzyżówek w celu uzyskania odpowiedzi na postawione pytania. Zakładanie hodowli Drosophila melanogaster (wybór osobników o odpowiednim fenotypie i płci) (laboratorium) Ćwiczenie 4. Efektywna liczebność populacji i współczynnik inbredu rozwiązywanie zadań rachunkowych. Ćwiczenie 5: a. Analiza wyników krzyżówek z ćwiczenia 3. b. Genotyp a środowisko: wpływ zagęszczenia populacji na masę ciała Drosophila melanogaster- zakładanie hodowli muszki owocowej (dwa różne zagęszczenia populacji) (laboratorium). Ćwiczenie 6. Prawo Hardy'ego-Weinberga. Symulowanie losowego łączenia się gamet w populacji panmiktycznej. Ćwiczenie 7. Wpływ zagęszczenia populacji na masę ciała Drosophila melanogasterzamknięcie doświadczenia (usypianie much i ważenie próby, określenie średniej masy much w każdym zagęszczeniu) analiza wyników przy pomocy testu t- Studenta i wnioski (laboratorium). Ćwiczenie 8. Modele doboru naturalnego w populacjach - symulacje komputerowe dotyczące zmian frekwencji alleli w populacji pod wpływem doboru naturalnego (sala komputerowa). Ćwiczenie 9. Allele wielokrotne na przykładzie systemu grup krwi ABO u człowieka. Czynnik Rh a konflikt serologiczny. Rozwiązywanie zadań rachunkowych: obliczanie frekwencji alleli w populacji na podstawie częstości poszczególnych grup krwi. Ćwiczenie 10. Frekwencja genów w populacji. Wpływ mutacji i migracji na frekwencje genów. Ćwiczenie 11. Kolokwium. Ćwiczenie 12. Badanie zróżnicowanie genetycznego zbiorowisk mikroorganizmów metodami molekularnymi. Wykorzystanie metody RISA (Ribosomal Intergenic Sequnce Analysis) w badaniu zmienności mikroorganizmów w osadzie czynnym (laboratorium). Ćwiczenie 13. Metody obliczania dystansu genetycznego. Analiza wyników RISA (sala komputerowa). Ćwiczenie 14. Niepełna dominacja i addycja dwóch loci genowych. Określanie, czy badana populacja znajduje się w równowadze Hardy'ego-Weinberga. (test χ 2 ). Ćwiczenie 15. Efekt plejotropowy genu. Geny letalne i subletalne na przykładzie dziedziczenia kształtu płetw mieczyka Xiphophorus helleri - rozwiązywanie zadań, teoretyczne przykłady krzyżówek pomiędzy osobnikami o różnych fenotypach.
4 Ćwiczenie 1 Ćwiczenie 1. Podstawy dziedziczenia. Prawa Mendla I prawo Mendla Prawo czystości gamet: podczas tworzenia gamet u organizmów diploidalnych allele oddzielają się i w gametach występują pojedynczo Rodzice P AA x aa Gamety G A a Pokolenie 1. F1 Aa x Aa Gamety G A, a A,a Pokolenie 2. F2 Szachownica genetyczna (Punneta) A a A AA Aa a Aa aa Dominacia zupełna i niezupełna Czarna barwa nasion u fasoli dominuje nad białą. Po skrzyżowaniu roślin o czarnych nasionach z roślinami białonasiennymi otrzymano tylko czarne nasiona. Jaką barwę nasion będzie miało potomstwo roślin otrzymanych w wyniku krzyżowania dwóch czamonasiennych osobników F1? Żółta barwa nasion grochu dominuje nad barwą zieloną. Rośliny homozygotyczne o żółtej barwie nasion skrzyżowano z roślinami o nasionach zielonych, następnie rośliny z pokolenia F1 powtórnie skrzyżowano z: a) zielononasienną formą rodzicielską b) żółtonasienną formą rodzicielską Proszę podać genotypy i fenotypy potomstwa uzyskane po krzyżowaniu a i b. Skrzyżowano roślinę lwiej paszczy o kwiatach czerwonych z rośliną o kwiatach białych. W pokoleniu F1 wszystkie rośliny miały kwiaty różowe. Jak będzie wyglądało pokolenie F2 (powstałe ze skrzyżowania dwu różowokwiatowych roślin z pokolenia F1)? Molinezja (Poecilia sphenops) wykazuje polimońizm genetyczny pod względem kształtu płetw. W locus L odpowiedzialnym za kształt płetw molinezji znajdują się 2 allele L i l. Niepełna dominacja L nad I sprawia, że 3 genotypom odpowiadają 3 fenotypy przedstawione na rysunku:
5 Ćwiczenie 1 fenotyp genotyp A II B LI C LL Skrzyżowano molinezję o fenotypie A z osobnikiem o fenotypie C. W pokoleniu F1 wszystkie ryby miały fenotyp B. Jakie będą proporcje fenotypów w pokoleniu F2? Normalne ubarwienie u karpia dominuje nad ubarwieniem błękitnym. Skrzyżowano rybę normalnie ubarwioną z błękitną. W pokoleniu F1 wszystkie karpie były normalnie ubarwione. Jakich fenotypów można spodziewać się w pokoleniu F2? Jak sprawdzić, czy normalnie ubarwiony karp jest homozygotą czy heterozygotą? Skrzyżowano pstrąga tęczowego o ubarwieniu złocistym z osobnikiem o ubarwieniu normalnym. W pokoleniu F1 otrzymano 100% ryb o ubarwieniu pośrednim (tzw palomino). Jakie będą proporcje fenotypów w pokoleniu F2?
6 Ćwiczenie 1 II prawo Mendla Prawo niezależnego dziedziczenia cech: cechy warunkowane przez różne pary genów dziedziczą się niezależnie i mogą tworzyć dowolne połączenia u osobników potomnych. P AABB x aabb G AB ab F1 AaBb x AaBb G AB, ab, ab, Ab AB, ab, ab, Ab F2 AB ab ab Ab AB AABB AaBB AaBb AABb ab AaBB aabb aabb AaBb ab AaBb aabb aabb Aabb Ab AABb AaBb Aabb AAbb Długa sierść kotów perskich jest uwarunkowana genem recesywnym (p) w stosunku do allelu krótkiej sierści kotów syjamskich (P), zaś czarne umaszczenie persów uwarunkowane jest allelem dominującym (B) w stosunku do genu kawowego umaszczenia syjamczyków (b). Podaj możliwe genotypy syjamczyków i persów. Skrzyżowano homozygotycznego persa z homozygotycznymsyjamczykiem. Jak będzie wyglądało pokolenie F1 i F2? Brązowa barwa oczu człowieka (B), dominuje nad niebieską (b), praworęczność nad leworęcznością. Brązowooki, praworęczny mężczyzna poślubia niebieskooką, praworęczną kobietę. Ich pierwsze dziecko jest niebieskookie i leworęczne. Jeśli urodzą się inne dzieci, jakie cechy ( z wymienionych) ujawnią się? Wyjaśnij genotypy rodziców i dzieci.
7 Ćwiczenie 1 Wiadomości wymagane na tym ćwiczeniu można odnaleźć w następujących podręcznikach: 1. W. Gajewski. Genetyka ogólna i molekularna. PWN Warszawa, 1980, str B. Rodkiewicz i G. Kerszman. Zarys genetyki. PWN Warszawa, str J. Maciejowski i J. Zięba. Genetyka i ogólna hodowla zwierząt. Tom 1. PWN Warszawa, 1972 str B. Nowicki. Genetyka i metody doskonalenia zwierząt. PWR i L Warszawa, str P.C. Winter, G.I. Hickey, H.L. Fletcher. Krótkie wykłady, genetyka. PWN Warszawa, str Książki dostępne w Bibliotece UMW
8 Ćwiczenie 2 Ćwiczenie 2. Genetyka muszki owocowej (Drosophila melanogaster). Wykorzystanie programu komputerowego DrosophiLab. DrosophiLab (autor programu: Hannes Jensen) I Konstrukcja prostego eksperymentu Przewodnik ten pozwala na przeprowadzenie prostego eksperymentu, w którym analizowane będzie dziedziczenie pojedynczego genu (vg vestigial vings) odpowiedzialnego za mutację polegającą na redukcji skrzydeł u D. melanogaster. Do eksperymentu wybieramy rodziców, którzy są heterozygotami pod względem tego genu. Jako, że rodzice nie wykazują żadnej obecności tej mutacji możemy się spodziewać, iż 25% pokolenia potomnego (F1) będzie posiadało zredukowane skrzydła (co ilustruje poniższy diagram) Krok 1. Uruchom program DrosophiLab i wybierz File> New Experiment. Wpisz nazwę eksperymentu mutacja vg a nazwę generacji zostaw bez zmian P1. Kliknij na ikonę Male (samiec) i w oknie dialogowym wybierz vgmale.fly. Zrób te same czynności wybierając samicę (Female vgfemale.fly). Kliknij prawym przyciskiem myszy na białe pole opisane jako Counting jar (naczynie do zliczania muszek) i wybierz Add jar (dodaj naczynie) wpisując jednocześnie nazwę naczynia forma dzika. Dodaj jeszcze jedno naczynie i nazwij je jako forma vg. Kliknij OK żeby przejść do drugiego kroku.
9 Ćwiczenie 2 Krok 2. Kolejny etap to rozpoczęcie eksperymentu z wybranymi rodzicami. Osobniki te ukazane są w formie małych ikon oznaczonych jako P1. Aby obejrzeć wybrane muszki należy przeciągnąć je przy pomocy myszki na pole oznaczone Microscope. Oglądane osobniki można powiększyć poprzez przeciągnięcie w dół suwaka znajdującego się po prawej stronie pola obserwacyjnego. Ponadto, oglądane muszki można obrócić w dowolnym kierunku przytrzymując klawisz ctrl na klawiaturze. Aby usunąć muszkę spod mikroskopu należy kliknąć Empty microscope. Należy zwrócić uwagę, iż obydwie muszki posiadają normalne skrzydła. Aby zatwierdzić muszkę jako rodzica kliknąć na set as parent. Wybór muszki na rodzica jest potwierdzany przez różowe zabarwienie ikony muszki. Z górnego paska dialogowego wybierz Experiment>New generation. Wprowadź liczbę potomstwa Number of offspring (tym razem niech to będzie 20) i upewnij się, że poniżej
10 Ćwiczenie 2 zaznaczona jest opcja Icons (ikony). Inne możliwości pokazania wyników to Tabela (Table) lub wykres (Chart). Przejdź do kolejnego kroku poprzez kliknięcie OK. Krok 3. Potomstwo wybranych rodziców (w formie małych ikon) powinno znajdować się w oknie oznaczonym jako F1. Każdą potomną muszkę przeciągnij przy pomocy myszki pod mikroskop i sprawdź czy posiada ona normalne skrzydła czy też zredukowane. Muszki z normalnymi skrzydłami bezpośrednio spod mikroskopu przeciągnij do naczynia forma dzika natomiast muszki ze zredukowanymi skrzydłami przenieś do naczynia forma vg. Ile jest much z efektem mutacji vg a ile powinno być? II Eksperyment. Dziedziczenie cech recesywnych. Krok 1. Utwórz muszki o podanym poniżej genotypie przy pomocy Edytora Chromosomów: Tools>Chromosome Editor.
11 Ćwiczenie 2 Samiec (zaznacz opcję Male!): (w+) (vg+/vg+), zapisz (File>Save) w katalogu Flies (C:/Program Files\Drosohilab/Flies) jako dzikisamiec.fly. Samica (zaznacz opcję Female!): (w/w) (vg/vg), zapisz jako bialookasamica.fly. Krok 2. Utwórz nowy eksperyment (File>New Experiment) i wybierz samca (dzikisamiec.fly) i samicę (bialookasamica.fly). Potwierdź poprzez kliknięcie OK. Krok 3. Sprawdź pod mikroskopem czy wybrałeś odpowiednie osobniki, jeśli tak to zatwierdź je jako rodziców. Kontynuuj pracę Experiment>New generation, wpisz liczbę osobników potomnych (100), zaznacz format wyniku jako ikony (opcja Icone) i kliknij OK. Krok 4. Przeanalizuj wyniki, dodaj trzy naczynia do liczenia muszek (Experiment>Add counting jar), i nazwij je kolejno: biale oczy, czerwone oczy bez skrzydel. Ile osobników ma czerwone oczy (forma dzika), ile osobników ma białe oczy a ile powstało osobników ze zredukowanymi skrzydłami? Wyjaśnij otrzymane wyniki. Jakie genotypy i jakie fenotypy powinny posiadać osobniki potomne? Krok 5. Wybierz po jednym osobniku z czerwonymi oczami (forma dzika) oraz białymi oczami, wskaż je jako osobniki rodzicielskie. Utwórz pokolenie F2 (Experiment>New Generation). Wpisz liczbę osobników potomnych (100), wyniki utwórz w formie tabeli (opcja Table). Jakich genotypów i jakich fenotypów możemy się spodziewać? Jaki jest empiryczny stosunek otrzymanych fenotypów? w (white eyes) białe oczy rb (ruby eyes) rubinowe oczy t (tan body) żółtobrązowe ciało B (bar eyes) ograniczona wielkość oczu
12 Ćwiczenie 2 al (aristaless antena) urzęsione czułki Cy (curly wings) podwinięte skrzydła b (black body) czarne ciało p (purple eyes) purpurowe oczy vg (vestigial vings) zredukowane skrzydła L (lobe eyes) oczy ograniczone c (curved wings) zakrzywione skrzydła jv (javelin bristles) odstające rzęski se (sepia eyes) oczy w kolorze sepii th (thread arista) nitkowate czułki cu (curly wings) podwinięte skrzydła, jednocześnie czarne ciało sr (striped body) prążkowane ciało ci (cubitus interruptus veins) największe skrzydła poprzerywane, mniejsze w zaniku sv (shaven bristles) rzęski krótkie lub w zaniku
13 Ćwiczenie 3 Ćwiczenie 3. Geny autosomalne i sprzężone z płcią. Drosophila melanogaster jako obiekt badań genetycznych Przygotowanie hodowli Do próbówki wsypać 1 g IDM (Instant Drosophila Medium)(3,5-3,7ml objętości). Dodać 4 ml wody destylowanej. UWAGA! Ścianki próbówki muszą pozostać suche. Wszystkie naczynia muszą być całkowicie suche. Oznakuj probówki swoimi inicjałami, datą i zaznacz, jakie muchy tam hodujesz (gdzie Mel oznacza Drosophila melanogaster - czyli muszka owocowa): Mel + (dzikie), Mel Vg (bezskrzydłe), Mel W (białookie), Mel W/Vg (białookie, bezskrzydle). Jeżeli wykonujesz krzyżówki zaznacz także płeć. Usypianie much przy użyciu anestetyku Fly Nap. Preparat Fly Nap to nowoczesny anestetyk stosowany do usypiania much. W przeciwieństwie wcześniej stosowanych środków jak: CO 2, chloroform, jest on nieszkodliwy dla owadów. Jego użycie nie wpływa na przeżywalność larw, poczwarek i osobników dorosłych. Muchy uśpione preparatem Fly Nap pozostają w stanie narkozy przez okres 1-1,5 godziny. Jego prawidłowe zastosowanie uzależnione jest jednak od przestrzegania poniższej instrukcji. Przy usypianiu much anestetykiem Fly Nap można także skorzystać z rysunku zamieszczonego na sąsiedniej stronie. 1. Przygotować: a. butelkę z preparatem Fly Nap i dozownik do preparatu Fly Nap, b. czarne pudełko na dozownik Fly Nap, c. płytkę szklaną (szalka Petriego), d. próbówki z rozrobioną pożywką wraz z korkiem, e. pędzelek.
14 Ćwiczenie 3 2. Odkręcić butelkę z preparatem Fly Nap i umocz końcówkę dozownika Fly Nap w preparacie. Po umoczeniu końcówki dozownika DOKŁADNIE ZAKRĘCIĆ butelkę! 3. Strząsnąć delikatnie muchy na dno próbówki. 4. Odsunąć częściowo korek próbówki i umieść dozownik poniżej korka (czynność tą trzeba wykonać szybko aby muchy nie uciekły z próbówki). 5. Ułożyć próbówkę z dozownikiem na stole w pozycji horyzontalnej. 6. Pozostawić dozownik Fly Nap pod korkiem próbówki na czas 8-iu minut. 7. Gdy muchy przestaną się ruszać usunąć jednocześnie korek i dozownik Fly Nap. Następnie dozownik umieścić w czarnym pudełku. 8. Wysypać muchy na szalkę Petriego. 9. Z pośród much znajdujących się w szalce wybrać interesujące nas osobniki. Selekcję much dokonujemy przy użyciu pędzelka. 10. Przy użyciu pędzelka przenieść wyselekcjonowane osobniki do nowej próbówki. 11. Zatkać próbówkę i pozostawić ją w pozycji horyzontalnej.
15 Ćwiczenie 3
16 Ćwiczenie 3 Odróżnianie płci u Drosophila melcmogaster 1. Samice są nieco większe od samców. 2. Samice maja, prążkowany odwłok, szeroki i zaostrzony na końcu do składania jaj (Rys. 1). 3. Koniec odwłoka samca jest okrągły i prawie czarny w porównaniu do prążków samicy (Rys.2). U młodych muszek me widać tak wyraźnej różnicy. 4. U samców na pierwszej parze odnóży znajdują. się tzw. sex combs - szereg gęstych czarnych szczecinek (Rys.3).
17 Ćwiczenie 3 Bierzemy pod uwagę dwie cechy muszki owocowej wykazujące zmienność barwa oczu - biała (w) lub czerwona (+) skrzydła - normalne (+) lub zredukowane (vg). Należy określić, które z tych cech sa dominujące, a które recesywne oraz ktore są autosomalne, a które sprzężone z płcią. W tym celu każda podgrupa wykona 2 różne krzyżówki miedzy osobnikami z różnych linii hodowlanych muszki. Przy analizowaniu wyników należy uwzględnić fakt, iż niektóre samice mogły zostać zapłodnione już w hodowli macierzystej, (jeżeli przebywały w niej dłużej niż 8 godzin od momentu opuszczenia poczwarki). Część potomstwa takiej samicy ( z jaj złożonych najwcześniej) nie będzie rezultatem założonej przez nas krzyżówki. Tej części potomstwa nie uwzględniamy w naszej analizie. W każdej podgrupie (połowa grupy) zakładane są dwie uzupełniające się krzyżówki: bialooka bezskrzydła samica (Mel w/vg) z samcem o fenotypie dzikim (Mel +) (czerwone oczy i normalne skrzydła) oraz krzyżówka odwrotna. Trzecia hodowla będzie założona wyłącznie z muszek dzikich w liczbie: 3 samce i 3 samice. Hodowla ta posłuży podgrupie jako materiał do założenia następnego doświadczenia (wpływ zagęszczenia populacji na masę ciała much). Wypełnij tabelę wpisując fenotypy osobników w odpowiednie kratki! Obie cechy Vg autosomalne W Vg sprzężone z płcią Obie cechy autosomalne sprzężone z płcią W autosomalne sprzężone z płcia Obie mutacje 100% białookie i dominujące bezskrzydłe muchy obu płci Vg dominujące W recesywne Vg recesywne W dominujące Obie mutacje samice uskrzydlone i recesywne czerwonookie, samce bezskrzydłe i czerwonookie
18 Ćwiczenie 4 Ćwiczenie 4. Efektywna wielkość populacji i współczynnik inbredu rozwiązywanie zadań. Efektywna wielkość populacji: N e = 4N m N f / N m +N f N m - liczba samców, N f - liczba samic Współczynnik inbredu: F t = 1-(1-1/2N e ) t F - współczynnik inbredu t - liczba pokoleń N e - efektywna wielkość populacji zmiana częstości w pokoleniu t AA p o 2 Aa 2p o q o aa q o 2 +P o q o F t -2p o q o F t +P o q o F t Im wyższa wartość współczynnika inbredu tym szybciej wzrasta nadwyżka homozygot w populacji. Inbred nie ma wpływu na frekwencje alleli A i a, natomiast ma znaczny wpływ na frekwencje poszczególnych genotypów AA, Aa, i aa. 1) Oblicz efektywną wielkość populacji, w której jest: a) 150 samic i 50 samców, b) 180 samic i 20 samców, c) 280 samic i 20 samców, d) 380 samic i 20 samców, e) 170 samic i 30 samców. 2) Oblicz efektywną wielkość populacji złożonej z 10 kur i 1 koguta. 3) Efektywna wielkość pewnej populacji wynosi 20. Frekwencje alleli A i a wynoszą odpowiednio 0,6 i 0,4.
19 Ćwiczenie 4 Oblicz współczynnik inbredu oraz frekwencje genotypów w tej populacji w dziesiątym pokoleniu. Oblicz to samo dla populacji liczącej 1000 samic i 1000 samców.
20 Ćwiczenie 5 Ćwiczenie 5. Analiza wyników krzyżówek z ćwiczenia 3. Wpływ zagęszczenia populacji na masę ciała muszki owocowej (Drosophila melanogaster). A. Analiza wyników krzyżówek z ćwiczenia 3. a) Geny autosomalne i sprzężone z płcią. Analiza wyników doświadczenia 1. Usypiamy muchy i rozdzielamy według płci. 2. Analizujemy fenotyp uzyskanych w pokoleniu F1 samców i samic. 3. Ustalamy, do której z rubryk tabeli z ćwiczenia 3 pasują otrzymane wyniki. 4. Wyciągamy wnioski na temat mechanizmu dziedziczenia badanych dwu cech u muszki owocowej. B. Genotyp a środowisko. Wpływ zagęszczenia populacji na masę ciała muszki owocowej (Drosophila melanogaster). Założenie doświadczenia Każda podgrupa zakłada 3 hodowle ( o wyższym lub niższym zagęszczeniu much): 2 samce + 2 samice (3 hodowle w całej grupie) (zagęszczenie 1) 6 samców + 6 samic (3 hodowle w całej grupie) (zagęszczenie 2) Po 48h muchy rodzicielskie zostaną usunięte z próbówek przez osobę prowadząca ćwiczenia. Wszystkie muchy potomne uzyskane po 2 tygodniach będą należały do pokolenia F1.
21 Ćwiczenie 6 Ćwiczenie 6. Model Hardy ego-weinberga. Svmulowanie losoweao kojarzenia gamet w populacii panmiktvcznei. Stosowanie testu χ 2 (chi 2 ) do określenia. czy obserwacie potwierdzaja spodziewania H-W Proces analizy zmienności genetycznej składa się: - ze zbadania jednego lub więcej typów markerów genetycznych, - ilościowego wyrażenia frekwencji fenotypów, - wywnioskowania na tej podstawie frekwencji genotypów kodujących zbadane fenotypy. Następnie potrzebny jest określony model, który powiąże ze sobą frekwencje genotypów z frekwencjami alleli i umożliwi wyciagnięcie wniosków na temat procesów, oddziałujących na badaną populację. Użyteczność modelu polega na tym, iż pozwala on zidentyfikować kluczowe obserwacje (lub eksperymenty) które należy poczynić, aby lepiej zrozumieć stan obecny populacji oraz zaradzić ewentualnym kłopotom. Najpowszechniej stosowanym modelem, wiążącym frekwencje genotypów z frekwencjami alleli, jest model opracowany niezależnie przez G.H. Hardy'ego (1908) oraz W. Weinberga (1908). Model Hardy'ego-Weinberga opiera się na kilku ważnych założeniach: - liczebność populacji jest wielka i stała w kolejnych pokoleniach, - kojarzenie się osobników jest losowe (populacja jest panmiktyczna, albo bardzo dobrze wymieszana), - organizmy są diploidalne, - pokolenia nie zazębiają się, - rozród odbywa się drogą płciową, - wpływy mutacji, migracji i selekcji sązaniedbywalne. W przypadku autosomalnych (tych, które nie są ulokowane na chromosomach płci) loci genowych o dwóch allelach, model Hardy'ego-Weinberga przyjmuje postać: (p + q) 2 = p 2 + 2pq + q 2 = 1 gdzie p to frekwencja częstszego allelu A podczas gdy q jest frekwencją rzadziej występującego allelu a, natomiast p +q = 1. Proporcje genotypów będą odpowiadały rozwinięciu dwumianu (p + q) 2. AA Aa aa
22 Ćwiczenie 6 p 2 2pq q 2 Model Hardy'ego-Weinberga zakłada, że jeśli zostaną spełnione ww. założenia, to frekwencje alleli i genotypów w populacji nie będą się zmieniały z pokolenia na pokolenie. Zgodnie z tym założeniem, model może być stosowany do przewidywania frekwencji genotypów na podstawie obecnej frekwencji alleli. Zastosowania modelu Hardy'ego-Weinberga dostarczają podstawy do oceny sił ewolucyjnych, wpływających na wachlarz genotypów w populacji. Jeśli stwierdzamy że obserwowane frekwencje genotypów są inne niż frekwencje przewidywane przez model, można stawiać hipotezy co do przyczyn tych odchyleń. Idąc dalej, można zaplanować nowe obserwacje lub eksperymenty, których celem będzie wyjaśnienie procesów, które spowodowały różnice między obserwowanymi i przewidywanymi frekwencjami alleli w populacji. Rozumowanie takie opiera się na przypuszczeniu, iż w rezultacie rozmaitych mechanizmów ekologicznych jedno lub więcej założeń modelu nie jest spełnione w przypadku obserwowanej populacji. Jednym z założeń modelu Hardy'ego-Weinberga jest losowe kojarzenie się osobników w procesie rozrodu. To założenie często nie jest spełniane wskutek najrozmaitszych zachowań rozrodczych. Wybiórcze krzyżowanie się osobników to wybór partnera rozrodczego na podstawie jego fenotypu. Dodatnie krzyżowanie wybiórcze występuje wtedy. gdy osobniki krzyżują się z podobnymi do siebie częściej niż gdyby było to wyłącznie dziełem przypadku. Inbreeding to krzyżowanie się ze sobą osobników spokrewnionych, co stanowi szczególny przypadek pozytywnego krzyżowania się wybiórczego. Negatywne wybiórcze kojarzenie się występuje wówczas, gdy częściej niż wynikałoby to z przypadku osobniki krzyżują się z partnerami niepodobnymi do siebie fenotypowo jak w przypadku "korzyści rzadkich samców" [rare-male advantage] Drosophila). Genetyczny podział populacji gatunku jest również odmianą krzyżowania wybiórczego, w którym na pulę genową gatunku składają się pule genowe grupy subpopulacji (stad), których osobniki krzyżują się panmiktycznie w ramach subpopulacji (stad). W niektórych przypadkach wpływ doboru naturalnego na frekwencje genotypów nie jest zaniedbywalny. Dobrze znanym przykładem u człowieka jest korzystne dostosowanie heterozygot w locus B-hemoglobiny, kiedy to genotyp +s (odporny na malarię, nie anemiczny) jest lepiej dostosowany niż ++ (podatny na malarię) i genotyp ss (cierpi na anemię związaną z sierpowatością erytrocytów). Złamanie założeń prawa Hardy'ego-Weinberga może wyniknąć z rozmaitych innych
23 Ćwiczenie 6 mechanizmów ekologicznych. W rzeczywistości, model Hardy'ego-Weinberga jest dość odporny na niewielkie odstępstwa od jego założeń, co czyni go użytecznym w zastosowaniach praktycznych. Trzeba jednak zaznaczyć, iż jeśli obserwowane frekwencje genotypowe spełniają oczekiwania Hardy'ego-Weinberga, to nie musi to koniecznie oznaczać że wszystkie założenia modelu są spełnione. Symulowanie losowego kojarzenia gamet w populacji panmiktvcznej. Stosowanie testu χ 2 (chi 2 ) do określenia. czy obserwacie potwierdzaja spodziewania H-W Populację określamy jako pamniktyczną, jeżeli kojarzenia należących do niej osobników zachodzą całkowicie losowo. Rozkład genotypów w populacji zależy od wielu czynników. W najprostszym przypadku może on być losowy i bezpośrednio wynikać z frekwencji występujących w tej populacji alleli. Załóżmy, że populacja spełnia następujące warunki: 1. organizmy są diploidalne, 2. rozmnażają się płciowo, 3. pokolenia nie zachodzą na siebie, 4. osobniki kojarzą się losowo (populacja jest panmiktyczna), 5. populacja jest bardzo duża, 6. nie ma migracji, 7. nie ma mutacji, 8. dobór naturalny nie wpływa na badany locus. Populacja będzie spełniała te warunki także wtedy, gdy czynniki wymienione w pkt. 6, 7 i 8 będą się równoważyć. W takich warunkach proporcje genotypów, dla locus o dwu allelach A i a, których frekwencje wynoszą odpowiednio p i q, (przy czym p + q = 1), będą odpowiadały rozwinięciu dwumianu (p + q) 2. Powyższe stwierdzenie jest zwane prawem Hardy'ego i Weinberga. Prawo to mówi, że jeśli zostaną spełnione założenia 1-8, to frekwencje alleli i genotypów w populacji nie będą się zmieniały z pokolenia na pokolenie; dla dwu alleli frekwencje genotypów będą odpowiadały rozwinięciu dwumianu (p + q) 2. Każdy ze studentów losuje dwie. "gamety" z locus A i dwie z locus B. Następnie każdy odczytuje swój "genotyp". Jakie są liczebności poszczególnych genotypów w locus A a jakie w
24 Ćwiczenie 6 locus B? Jakie są oczekiwane liczebności tych genotypów z równania Hardy'ego i Weinberga? Czy frekwencje obserwowane odpowiadają oczekiwanym - sprawdzenie za pomocą testu chi-kwadrat. Test χ 2 stosuje się do określania, czy obserwowane liczby osobników o danych genotypach są takie same, jakich spodziewalibyśmy się na podstawie H-W (to znaczy, czy spełniają oczekiwania H-W, otrzymane wartości z obu (obserwowane i oczekiwane) kolumn podstawiamy do wzoru i obliczamy według modelu (Obs - Exp) 2 χ 2 =Σ Exp gdzie: Obs to liczba obserwowanych osobników o określonym fenotypie Exp to liczba oczekiwanych osobników o określonym fenotypie suma (Σ) będzie zawierała 3 składniki - odpowiednio dla trzech genotypów w każdym z badanych loci genowych (oddzielnie M, Aa i aa oraz BB, Bb i bb). Liczba stopni swobody, związana z tą wielkością χ 2, równa się liczbie klas danych (w tym przykładzie trzy klasy, czyli liczby AA, Aa oraz aa) minus jeden, minus liczba parametrów oszacowanych na podstawie danych (w tym przykładzie jeden parametr, p, oszacowano na podstawie danych), czyli = 1. Zauważmy, że stopień swobody nie jest pomniejszany z powodu oszacowania na podstawie danych wielkości parametru q, gdyż kiedy już oszacowaliśmy p. wówczas q można otrzymać z zależności q = 1 - p. Przy jednym stopniu swobody otrzymana wyżej wartość χ 2 jest wysoce istotna (P < 0,01). Wartość krytyczna statystyki χ 2 na poziomie istotności a = 0,05 wynosi w tym przypadku 3,84 Obliczanie frekwencji alleli w locus przy pełnej dominacji. Rozpatrujemy dwie cechy: 1. barwa oczu: brązowe. piwne lub zielone - genotyp M lub Aa niebieskie lub szare - genotyp aa 2. ucho: wolny koniec - genotyp BB lub Sb, przyrośnięty koniec - genotyp bb.
25 Ćwiczenie 6 Każdy ze studentów określa genotyp sąsiada (na podstawie jego fenotypu) jako Ax lub aa oraz Bx lub bb.(gdzie x oznacza dowolny allel z danego locus). Zauważmy. że tylko homozygoty recesywne są wyróżnialne (dotyczy to obu badanych /oci genowych). Obliczamy udział homozygot recesywnych (dla każdej cechy oddzielnie) w całej grupie studenckiej. Dodajemy również w miarę możliwości wyniki z grup poprzednich, aby zwiększyć liczebność próby i zminimalizować błąd statystyczny. Przykładowo, jeżeli liczba homozygot w locus A wynosiła 5 na 20 osób, to frekwencja homozygot recesywnych w próbie wyniosi 5/20 czyli Z równania Hardy'ego i Weinberga wiemy. że frekwencja homozygot recesywnych w populacji wynosi q 2, a zatem frekwencja allelu recesywnego q = q 2 = 0,5. Frekwencja allelu dominującego wynosi zaś p = 1-q = 0,5 Mamy już frekwencje alleli A i a (p i q) oraz B i b (p 1 i q 1 ). Możemy teraz obliczyć, jaki procent w populacji stanowią heterozygoty - nosiciele cech recesywnych. Obliczamy to ze wzoru: liczba heterozygot Aa = 2pq liczba heterozygot Bb = 2p 1 q 1. Każdy ze studentów, szczególnie potencjalnych heterozygot w badanych loci przypomni sobie jak wyglądają wspomniane cechy u jego rodziców i rodzeństwa, a następnie wyciągnie wnioski co do swojego genotypu w loci A i B.
26 Ćwiczenie 7 Ćwiczenie 7. Genotyp a środowisko. Wpływ zagęszczenia populacji na masę ciała muszki owocowej (Drosophila melanogaster). Analiza statystyczna wyników doświadczenia. Po 2 tygodniach w każdej grupie doświadczalnej oddzielnie: -muchy usypiamy i rozdzielamy według płci, -liczymy samce i samice, -ważymy oddzielnie samce i samice w ramach grupy doświadczalnej, -obliczmy średnia masę w próbie samców i samic dzieląc całkowitą masę próby przez liczbę much w próbie. Jeżeli średnia masa muchy będzie mniejsza niż 0,5 mg lub większa niż 2 mg, powtórzyć ważenie. Zanotować uzyskane dane w zeszycie. Wszystkie obliczenia prowadzimy oddzielnie dla samców i samic, ponieważ średnia masa samców jest o około 20% niższa niż samic. ZADANIE Porównaj testem t-studenta masę ciała samic z najmniejszego i największego zagęszczenia. podgrupa zagęszczenie 2+2 zagęszczenie 6+6 samce samice samce samice Wartość statystyki t obliczoną przez nas porównujemy z krytyczna wartością z tabeli,,poziom istotności dla testu dwustronnego dla poziomu istotności 0,05. Liczba stopni swobody df=n 1 +N 2-2, gdzie N 1 i N 2 to liczby powtórzeń, odpowiednio dla zagęszczenia 1 (2+2) i 2 (6+6)
27 Ćwiczenie 7 X X 1 2 t = S x X 1, X 2 - średnie arytmetyczne Sx - błąd standardowy Błąd standardowy obliczamy ze wzoru: S 1 S x = + N 1 S N 2 2 gdzie S 1 i S 2 to wariancje, odpowiednio dla zagęszczenia 1 (2+2) oraz 2 (6+6). Aby obliczyć Sx musimy mieć najpierw S 1 i S 2 (wariancje). Obliczamy je ze wzoru: S 2 X ( X) = N 1 2 / N Gdy obliczymy wariancję S 1 i S 2, wstawiamy je do wzoru na błąd standardowy (N 1 i N 2 są liczbami powtórzeń w każdym zagęszczeniu). Obliczamy każdą wariancję oddzielnie wstawiając dla S 1 odpowiednio X 1 i N 1 a dla S 2 - X 2 oraz N 2. Gdy obliczymy Sx, wstawiamy do wzoru na t i obliczamy wartość statystyki t. Znajdujemy w tabeli wartość krytyczna.: Liczba stopni swobody df = N 1 + N 2-2. Poziom istotności dla testu dwustronnego α = 0,05 Następnie możemy zweryfikować hipotezę zerowa, która brzmi: HO =,,Brak jest istotnych różnic pomiędzy średnimi masami ciała muszek owocowych hodowanych w różnych zagęszczeniach". Jeżeli obliczona przez nas wartość statystyki t jest niższa od wartości krytycznej, to: Nie ma podstaw do odrzucenia hipotezy zerowej. Jeżeli obliczona wartość t jest wyższa od krytycznej to: Hipotezę zerowa należy odrzucić na rzecz hipotezy alternatywnej, która brzmi:,,występują istotne różnice pomiędzy średnimi masami ciała muszek owocowych hodowanych w różnych zagęszczeniach".
28 Ćwiczenie 8 Ćwiczenie 8. Modele doboru naturalnego w populacjach - symulacje komputerowe dotyczące zmian frekwencji alleli w populacji pod wpływem doboru naturalnego. Współczynnik reprodukcji (R): R=FxP, gdzie F oznacza liczbę potomków przypadających na jednego osobnika rodzicielskiego a P to prawdopodobieństwo przeżycia potomka do wieku reprodukcyjnego. Wartość przystosowawcza genotypu: jest to stosunek współczynnika reprodukcji danego genotypu do współczynnika reprodukcji najkorzystniejszego genoypu: W = R/Rmax. Dobór przeciw homozygotom recesywnym: (np. melanizm przemysłowy Biston betularia na obszarach zanieczyszczonych). W AA = W Aa = 1, W aa = 1-s q = -pq 2 s/1-sq 2 p,q frekwencje alleli A i a q zmiana frekwencji allelu a Dobór przeciw homozygotom dominującym i heterozygotom: (np. forma nie-melanistyczna motyla Biston betularia na obszarach nie zanieczyszczonych) W AA = W Aa = 1-s, W aa = 1 q = -pq 2 s/1-ps(1+q) Dobór przeciw obu homozygotom: (np. anemia sierpowata u człowieka na obszarach malarycznych) W Aa = 1, W AA = 1 s AA, W aa = 1 - s aa Dobór przeciw heterozygotom: W Aa = 1, W AA = 1 + s AA, Waa = 1 + s aa q = pq(qsaa-ps AA )/1+p 2 s AA +q 2 s aa q=0 punkt równowagi nietrwałej, przy niewielkim odchyleniu występuje tendencja do jego pogłębienia (dodatnie sprzężenie zwrotne). Dwa punkty równowagi trwałej: q=1, p=0 oraz q=0, p=1.
29 Ćwiczenie 9 Ćwiczenie 9. Allele wielokrotne na przykładzie sytemu grup krwi ABO u człowieka. Czynnik RH a konflikt serologiczny. Rozwiązywanie zadań rachunkowych: obliczanie frekwencji alleli w populacji na podstawie częstości poszczególnych grup krwi. A. Allele wielokrotne na przykładzie sytemu grup krwi ABO u człowieka. Czynnik RH a konflikt serologiczny. Mechanizm dziedziczenia grup krwi u człowieka Dziedziczenie grup krwi w systemie ABO u człowieka zależy od występowania kombinacji dwu z trzech alleli w jednym locus genowym. Dwa allele I A oraz I B są dominujące wobec trzeciego allelu i. Pomiędzy dominującymi allelami IA i IB występuje zjawisko kodominacji (współdominacji). Polega to na jednoczesnej ekspresji obu tych alleli w heterozygocie. Produktem ekspresji allelu I A jest antygen A obecny w błonie komórkowej erytrocytu. Produktem ekspresji allelu I B jest antygen B. Allel recesywny i jest odpowiedzialny za brak antygenu w błonie komórkowej erytrocytu. Osoby z grupa krwi A posiadają antygen A w błonie komórkowej erytrocytu, oraz przeciwciała (izoaglutyniny) anty-b, skierowane przeciw antygenowi B. Osoby z grupa krwi B posiadają antygen B oraz izoaglutyniny anty-a. Osoby z grupa AB posiadają oba antygeny w błonie erytrocytu i żadnych izoaglutynin w osoczu. Osoby z grupa krwi 0 posiadają izoaglutyniny anty-a i anty-b w osoczu, nie posiadają natomiast żadnych antygenów w błonie erytrocytu. Osoby z grupa krwi A mogą mieć genotypy: I A I A oraz I A i osoby z grupa B: I B I B oraz I B i osoby z grupa AB - tylko I A I B a osoby z grupa 0 tylko ii. W ten sposób sześć różnych genotypów ( 3 homo- i 3 heterozygotyczne) daje w efekcie 4 fenotypy. Dzieje się tak na skutek pełnej dominacji alleli IA oraz IB nad allelem i w odpowiednich genotypach heterozygotycznych. W genotypie heterozygotycznym IAIB występuje zjawisko kodominacji (jednoczesne występowanie obu antygenów w błonie erytrocytu. Występowanie czynnika Rh zależy od układu zależy pary alleli jednym locus genowym. W tym locus występują dwa allele: D oraz d. Występuje pełna dominacja D nad d. Genotypy DD i Dd będą wiec miały wspólny fenotyp (Rh+), natomiast homozygota recesywna dd będzie miała fenotyp Rh-(brak czynnika Rh). Występowanie konfliktu serologicznego wiąże się z odpowiedzią immunologiczną organizmu matki o fenotypie Rh- przeciwko krwinkom czerwonym dziecka o fenotypie Rh+. W takiej sytuacji następuje indukcja syntezy specyficznych przeciwciał skierowanych przeciwko czynnikowi Rh w erytrocytach dziecka,
30 Ćwiczenie 9 gdyż czynnik ten jest rozpoznawany w organizmie matki jako obcy antygen). Wzrost koncentracji tych przeciwciał we krwi matki przebiega stopniowo w trakcie całej ciąży, ale pierwsze dziecko rodzi się zwykle bez większych komplikacji. Poziom przeciwciał przeciw czynnikowi Rh we krwi matki o genotypie dd po przebytej ciąży jest już podwyższony (organizm nabył odporność" na oby antygen - czynnik Rh, podobnie jak to ma miejsce w przypadku wytwarzania się odporność naturalnej po przebytej chorobie). Przy kolejnej ciąży dojdzie do szybkiego dalszego wzrostu koncentracji przeciwciał i w rezultacie nastąpi odpowiedz immunologiczna organizmu matki, polegająca na niszczeniu krwinek dziecka posiadającego czynnik Rh w błonie erytrocytu (genotyp Dd). Osoby z grupą krwi Rh- stanowią 15% całej populacji, natomiast osoby z grupą krwi Rh+ stanowią 85% populacji.
31 Ćwiczenie 10 Ćwiczenie 10. Frekwencja genów w populacji. Wpływ mutacji i migracji na frekwencje genów. Gdy gen ma dwa allele kodujące trzy fenotypy, a każdy genotyp koduje unikalny fenotyp (dominacja niekompletna albo addytywne działanie genów), łatwo określić frekwencje alleli genu w populacji. Frekwencja allelu to: liczba ryb o fenotypie liczba ryb 2 homozygotycznym + o fenotypie kodowanym przez allel heterozygotyczny f (allelu ) = (liczba ryb w populacji) Liczba ryb o fenotypie homozygotycznym jest mnożona przez dwa gdyż każda ryba ma dwie kopie allelu danego rodzaju; heterozygoty mają tylko po jednym allelu tego rodzaju. Liczba ryb w populacji jest mnożona przez dwa gdyż każda ryba jest organizmem diploidalnym i ma dwa allele w każdym locus. Na przykład jeśli hodowca pstrągów znajduje ryby złociste oraz "palomino" i chce wiedzieć, jakie są frekwencje alleli G i G' w hodowanej populacji, powinien policzyć ile jest ryb o każdym fenotypie, zsumować allele i obliczyć ich frekwencje (w procentach). Rozważmy przykład, w którym liczby ryb o poszczególnych fenotypach (i przyporządkowanych im genotypach) były następujące: Fenotyp Genotyp Liczba normalnie ubarwione GG... złociste G G... palomino GG... Każdy normalnie ubarwiony pstrąg ma dwa allele G, każdy pstrąg palomino ma jeden allel G, pstrągi złociste nie mają alleli G. Ogólna liczba alleli w locus G jest równa podwojonej
32 Ćwiczenie 10 liczbie wszystkich ryb w populacji (normalnie ubarwionych + złocistych + palomino). Czyli: liczba alleli G f(g) = = całkowita liczba alleli w locus G 2 (... normalnie ubarwionych) +... palomino... alleli G = = =... 2 (... pstrągów tęczowych razem)... wszystkich alleli Podobnie można obliczyć frekwencję alleli G', która w tym przykładzie wynosi Należy zauważyć iż f(g) + f(g ) = = 1,0. Frekwencja genów i genotypów w populacji. Geny autosomalne. Dominacja kompletna (całkowita). Przy założeniu, że rozpatrujemy 1 locus, w populacji osobników diploidalnych mogą wystąpić: Genotypy O liczebności O frekwencii AA D D/N=d Aa H H/N=h aa R RIN=r razem N 1 Frekwencję danego genotypu w określonej populacji definiuje się jako stosunek liczby osobników posiadających dany genotyp do ogólnej liczby osobników w danej populacji. Dla populacji nieokreślonej lecz o bardzo dużej liczebności, wygodniej jest określać frekwencję jako prawdopodobieństwo występowania danego genotypu w populacji, albo jako prawdopodobieństwo, że wybrany przypadkowo osobnik będzie miał dany genotyp. Przykład: W populacji stwierdzono 300 osobników homozygot dominujących (AA), 500 heterozygot(aa) i 200 homozygot recesywnych (aa). Frekwenqe poszczególnych genotypów będą miały wartości następujące: d(m)=300/1000=0,3; h (Aa)=500/1 000=0,5; r(aa)=200/1000=0,2
33 Ćwiczenie 10 Ważne jest poznanie frekwencji nie tylko genotypów ale i genów, gdyż to właśnie geny się dziedziczą a nie genotypy. Frekwencję genu rozumie się jako względną częstość występowania, proporcję loci zajętych przez dany gen w populacji do wszystkich loei, które dany gen mógłby zajmować. Inaczej można frekwencję genu zdefiniować jako prawdopodobieństwo występowania danego allelu (genu) w populacji. Jeśli przez "p" oznaczymy frekwencję allelu dominującego genu A, przez q oznaczymy frekwencję allelu recesywnego tego genu oznaczonego jako a, wtedy: p+q=1 2D+H 2R+H gdzie: p = ; q = N 2N Allele A oraz a kodominują daną cechę fenotypową. to znaczy że na podstawie fenotypów możemy odróżnić od siebie osobniki o genotypach AA, Aa oraz aa. Frekwencja częstszych homozygot AA wynosi p 2, frekwencja heterozygot Aa wynosi 2pq, a frekwencja rzadszych homozygot aa wynosi q 2, co między innymi wynika z poniższego rozumowania. Jeśli w populacji ryb rozważamy jeden locus genowy, w którym segregują dwa allele: A oraz a, wówczas w czasie rozrodu krzyżują się ze sobą haploidalne gamety, jaja I plemniki, które są nosicielami albo allelu A albo allelu a. Wyrzucone do wody gamety łączą się losowo ze sobą w zygoty o trzech możliwych genotypach: AA,.Aa oraz aa, co można określić na podstawie poniższej szachownicy genetycznej: A a A AA Aa a Aa aa Jeśli allel A występuje w badanej populacji ryb z frekwencją p, podczas gdy allel a
34 Ćwiczenie 10 występuje z frekwencją q, wówczas frekwencje zygot o poszczególnych genotypach (AA, Aa oraz aa) można obliczyć również posługując się szachownicą genetyczną, w której polach w miejsce nazw alleli (A, a) oraz genotypów (AA, Aa, aa) wstawimy obserwowane w populacji frekwencje alleli (p, q) oraz wyliczone prawdopodobieństwa, iż powstaną,zygoty o poszczególnych genotypach (prawdopodobieństwo że powstaną zygoty o genotypie AA = p x p = p 2 ; Aa = p x q + q x p = 2pq; aa = q x q = q 2. p q p pp=p 2 pq q pq qq=q 2 Gdy między allelami występuje dominacja całkowita, frekwencję alleli trzeba obliczać metodą pierwiastka kwadratowego, gdyż w takim przypadku trzy genotypy kodują dwa fenotypy. Ponieważ fenotyp heterozygotyczny jest niemożliwy do odróżnienia od dominującego fenotypu homozygotycznego, nie można obliczyć frekwencji alleli poprzez ich zwykłe policzenie (nie wiadomo które ryby w populacji o dominującym fenotypie mają dwa, a które mają jeden allel dominujący). Tylko genotyp recesywny jest tym, który można rozpoznać na podstawie kodowanego przez niego fenotypu. Ponieważ frekwencja recesywnego fenotypu to kwadrat frekwencji allelu recesywnego, pierwiastek kwadratowy z frekwencji fenotypu recesywnego to frekwencja recesywnego allelu w populacji. Frekwencję allelu dominującego oblicza się odejmując od jedności frekwencję allelu recesywnego.
35 Ćwiczenie 11 Ćwiczenie 11. Kolokwium. Na kolokwium obowiązują wiadomości z ćwiczeń 1 10.
36 Ćwiczenie 12 Ćwiczenie 12. Badanie zróżnicowanie genetycznego zbiorowisk mikroorganizmów metodami molekularnymi. Wykorzystanie metody RISA (Ribosomal Intergenic Sequnce Analysis) w badaniu zmienności mikroorganizmów w osadzie czynnym. Elektroforeza jest standardową techniką umożliwiającą rozdział, identyfikację, wizualizację i oczyszczanie DNA i RNA. Możliwość wykorzystania tej metody wynika z właściwości fizyko-chemicznych kwasów nukleinowych, których grupa fosforanowa decyduje o ujemnym ładunku elektrycznym tych cząsteczek. Oznacza to, że migrują one w polu elektrycznym w kierunku dodatniej elektrody. Rodzaj substratu z jakiego sporządza się żel elektroforetyczny ma decydujący wpływ na jakość rozdziału analizowanych cząsteczek. Najczęściej używa się dwóch rodzajów żelu: agarozowego oraz poliakrylamidowego. Agaroza otrzymywana jest z alg morskich i dostępna jest w postaci proszku, który jest rozpuszczany w buforze, w odpowiedniej koncentracji (Tabela xx). Żel poliakrylamidowy wykorzystywany jest generalnie do rozdziału małych fragmentów DNA i RNA gdyż porowatość tego rodzaju żelu jest znacznie mniejsza. Żel poliakrylamidowy tworzy się przez polimeryzację monomerów akrylamidowych w długie łańcuchy, które z kolei łączone są kowalencyjnie przez N,N'-metyleno-bisakrylamid. W praktyce wykorzystuje się mieszaniny poliakrylamidów, zawierające różny stosunek wagowy akrylamidu do N,N'-metyleno-bisakrylamidu w zależności od tego jakiego rodzaju elektroforezę przeprowadzamy. Polimeryzacja tego rodzaju żelu zapoczątkowywana jest przez wolne rodniki wprowadzane wraz z nadsiarczanem amonu (APS) i które stabilizowane są przez TEMED. Reakcja polimeryzacji trwa od 15 do 60 minut i zależy głównie od stężenia nadsiarczanu amonu i TEMED-u, temperatury otoczenia i wielkości żelu. Elektroforezie poddany zostanie amplifikowany metodą PCR fragment DNA zlokalizowany między genami kodującymi 16S i 23 S rrna (RIS Ribosomal Intergenic Sequence). Odcinek ten charakteryzuje się znaczną różnicą długości u różnych gatunków a nawet szczepów bakterii i może posiadać długość od 100 do 1500 par zasad.
37 Ćwiczenie 12 16S rrna RIS 23S rrna Wykonanie elektroforezy poliakrylamidowej DNA Uwaga: Akrylamid jest bardzo szkodliwą substancją. Zachować ostrożność: nosić rękawice i gogle ochronne. Unikać kontaktu ze skórą. 1. Przygotować żel posługując się Tabelą xx, APS oraz TEMED należy dodać bezpośrednio przed wylaniem żelu. W zależności od używanego aparatu należy przygotować od kilku do kilkudziesięciu mililitrów żelu. 2. Starannie umyte i odtłuszczone szklany płyty złożyć w ten sposób aby znajdowała się między nimi wąska szczelina, do której zostanie wlany żel. 3. Napełnić szczelinę między szybami w taki sposób aby nie dostały się pęcherzyki powietrza, umieścić grzebień. 4. Po polimeryzacji żelu (15-60 minut) wyjąć grzebień i umięścić szyby wraz z żelem w aparacie do elektroforezy. Napełnić aparat buforem (1x TBE lub TAE) i przy pomocy pipety Paustera przepłukać studzienki, wymywając resztki mocznika. 5. Do próbek DNA dodać taką samą objetość buforu obciążającego (0,25% błekitu bromofenolowego, 0,25% ksylenu cyjanu, 40% sacharozy w wodzie) i nałożyć próby do studzienek. 6. Elektroforezę prowadzić tak długo aż niebieski barwnik zawędruję do dolnego końca żelu. 7. Po zakończeniu elektroforezy rozmontować aparat i barwić żel przy pomocy bromku etydyny, SYBRgreen, SYBRgold lub azotanu srebra. 8. Uruchomić zasilacz i nastawić odpowiednią wartość napięcia prądu (5V/cm).
38 Ćwiczenie 12 Tabela xx. Ilości komponentów (ml) w zależności od koncentracji żelu poliakrylamidowego Komponent Stężenie żelu 3,5% 5,0% 8,0% 12,0% 15,0% 20,0% 30% roztwór poliakrylamidu 11,6 16,6 26,6 40,0 50,0 66,6 10x bufor TBE 10,0 10,0 10,0 10,0 10,0 10,0 dh 2 O 77,7 72,7 62,7 49,3 39,3 22,7 10% APS 0,7 0,7 0,7 0,7 0,7 0,7 TEMED 0,005 0,005 0,005 0,005 0,005 0,005
39 Ćwiczenie 13 Ćwiczenie 13. Dystans genetyczny. Analiza prążków RISA. 1. Na podstawie uzyskanego zdjęcia sporządź matrycę zero-jedynkową; obecność prążka oznacz przez 1 natomiast jego brak przez 0. Cyframi arabskimi opisano numer ścieżki jednoznaczny z numerem badanej próby Uzyskaną matrycę przekształć w plik tekstowy o nazwie RISA (risa.txt) według podanego poniżej schematu (6 - liczba ścieżek-prób; 11 liczba analizowanych pozycji) 6 11 proba proba proba proba proba proba Plik zapisz w katalogu RISASTAT. W tym samym katalogu znajdź plik wykonawczy risastat i uruchom program. Otwórz plik risa.txt (File>open binary file). Oblicz dystans genetyczny (Calculate>Distance matrix). Wskaż metodę, według której obliczany będzie dystans (zaznacz opcję Dice) i zatwierdź OK. 4. Aby utworzyć diagram pokazujący dystans genetyczny między analizowanymi próbami Analyze>Cluster analysis i zaznacz opcję UPGMA i Bootstrap z 1000 powtórzeń. Uzyskany diagram można zapisać (File>Save cluster analysis) i otworzyć w programie graficznym analizującym drzewa filogenetyczne (np. Treewiev). Aby zobaczyć obliczony dystans między próbami należy kliknąć na View i Show distance matrix.
40 Ćwiczenie 13 Dystans genetyczny obliczony został za pomocą Dice (Nei i Li, 1979) według wzoru: 2Nxy GDyx= Nx+Ny gdzie, Nxy jest liczbą fragmentów (prążków) obecnych na ścieżkach x i y, Nx jest liczbą prążków na ścieżce x a Ny jest to liczba fragmentów na ścieżce y.
41 Ćwiczenie 14. Niepełna dominacja i addycja dwóch loci genowych. Prawo Hardy'ego-Weinberga dla dwu loci genowych Molinezja (Poecilia sphenops) wykazuje polimorfizm genetyczny pod względem ubarwienia ciała oraz kształtu płetw. W locus L odpowiedzialnym za kształt płetw molinezji znajdują się 2 allele L i l. Niepełna dominacja L nad 1 sprawia, ze 3 genotypom odpowiadają 3 fenotypy przedstawione narysunku: fenotyp A genotyp ll B Ll C LL Frekwencje poszczególnych alleli (p i q) w populacji obliczamy korzystając z danych doświadczalnych (obserwowane częstości fenotypów). W przypadku cechy kształtu płetw: P = f(l); q = r(l) gdzie f to frekwencja allelu. p = n LL +1/ 2 N n Ll gdzie n LL, n Ll to liczba osobników o odpowiednim genotypie i odpowiadającym mu fenotypie, N to liczba badanych osobników. Frekwencję allelu recesywnego (q) oblicza się z zależności p + q = 1 Równanie Hardy-Weinberga dla pary alleli w pojedynczym locus przyjmuje postać (p+q) 2 =1, co po rozwinięciu daje: p 2 + 2pq + q 2 = 1
42 gdzie p = frekwencja allelu A natomiast q = frekwencja allelu a Trzy wyrażenia z lewej strony równania odpowiadają oczekiwanym proporcjom poszczególnych (3) fenotypów molinezji w badanej populacji (odpowiednio: p 2 homozygot LL, 2pq heterozygot i q 2 homozygot ll). Po pomnożeniu każdego z tych wyrażeń przez N (liczba badanych osobników) otrzymamy odpowiednio oczekiwane liczby osobników każdego fenotypu wynikające z równania Hardy-Weinberga, ktore zapisujemy w prawej kolumnie. W lewej kolumnie zapisujemy rzeczywiste (obserwowane) liczby osobników o określonych fenotypach. Następnie otrzymane wartości z obu kolumn podstawiamy do wzoru i obliczmy według modelu χ 2 (chi-kwadrat). χ = ( Obs Exp Exp 2 2 ) gdzie: Obs to liczba obserwowanych osobników o określonym fenotypie Exp to liczba oczekiwanych osobników o określonym fenotypie (w tym przypadku suma Z będzie zawierała 3 składniki) Wartość krytyczna statystyki y1 na poziomie istotności a = 0,05 wynosi w tym przypadku 3,84 (liczba stopni swobody: K - l - s = = 1) P + q= 1 stad p -zmienna niezależna: p + (1 - p) = 1, albo q -zmienna niezależna: q + (1-q) = 1 Jeżeli obliczona wartość statystyki przekroczy wartość krytyczną (3,84) to istnieją podstawy do odrzucenia hipotezy zerowej (ze populacja molinezji znajduje się w równowadze Hardy- Weiberga) na rzecz hipotezy alternatywnej. W takim przypadku należy zastanowić się nad przyczynami takiej struktury genetycznej populacji. Jakie czynniki mogły to wywołać Za ubarwienie ciała odpowiadają dwie pary alleli w dwu loci genowych. Fenotyp każdego osobnika jest sumą oddziaływania alleli zlokalizowanych w locus M i N. Takie współoddziaływanie dwóch lub więcej loci genowych nazywamy addycją. W każdym z dwu loci (M i N) występują u Poecilia sphenops po 2 allele, odpowiednio: M i m oraz N i n. Dominujące allele M i N warunkują melanistyczne (czarne) ubarwienie ryb, natomiast allele recesywne m i n (allele dzikie) warunkują srebrnoszare ubarwienie ciała ryb. Fenotyp każdego osobnika zależy od liczby alleli dominujących (M i N) w obu loci genowych odpowiedzialnych za barwę ciała (liczba ta może wynosić 0,1, 2, 3 lub 4). 9 możliwych kombinacji genotypów daje w efekcie 5 fenotypów:
a) Zapisz genotyp tego mężczyzny... oraz zaznacz poniżej (A, B, C lub D), jaki procent gamet tego mężczyzny będzie miało genotyp ax b.
 W tomie 2 zbioru zadań z biologii z powodu nieprawidłowego wprowadzenia komendy przenoszenia spójników i przyimków do następnej linii wystąpiła zamiana samotnych dużych liter (A, I, W, U) na małe litery.
W tomie 2 zbioru zadań z biologii z powodu nieprawidłowego wprowadzenia komendy przenoszenia spójników i przyimków do następnej linii wystąpiła zamiana samotnych dużych liter (A, I, W, U) na małe litery.
ZARZĄDZANIE POPULACJAMI ZWIERZĄT
 ZARZĄDZANIE POPULACJAMI ZWIERZĄT Ćwiczenia 1 mgr Magda Kaczmarek-Okrój magda_kaczmarek_okroj@sggw.pl 1 ZAGADNIENIA struktura genetyczna populacji obliczanie frekwencji genotypów obliczanie frekwencji alleli
ZARZĄDZANIE POPULACJAMI ZWIERZĄT Ćwiczenia 1 mgr Magda Kaczmarek-Okrój magda_kaczmarek_okroj@sggw.pl 1 ZAGADNIENIA struktura genetyczna populacji obliczanie frekwencji genotypów obliczanie frekwencji alleli
GENETYKA POPULACJI. Ćwiczenia 4 Biologia I MGR
 GEETYKA POPULACJI Ćwiczenia 4 Biologia I MGR Ad. Ćwiczenia Liczba możliwych genotypów w locus wieloallelicznym Geny sprzężone z płcią Prawo Hardy ego-weinberga p +pq+q = p+q= m( m ) p P Q Q P p AA Aa wszystkich_
GEETYKA POPULACJI Ćwiczenia 4 Biologia I MGR Ad. Ćwiczenia Liczba możliwych genotypów w locus wieloallelicznym Geny sprzężone z płcią Prawo Hardy ego-weinberga p +pq+q = p+q= m( m ) p P Q Q P p AA Aa wszystkich_
ZARZĄDZANIE POPULACJAMI ZWIERZĄT 1. RÓWNOWAGA GENETYCZNA POPULACJI. Prowadzący: dr Wioleta Drobik Katedra Genetyki i Ogólnej Hodowli Zwierząt
 ZARZĄDZANIE POPULACJAMI ZWIERZĄT 1. RÓWNOWAGA GENETYCZNA POPULACJI Fot. W. Wołkow Prowadzący: dr Wioleta Drobik Katedra Genetyki i Ogólnej Hodowli Zwierząt POPULACJA Zbiór organizmów żywych, które łączy
ZARZĄDZANIE POPULACJAMI ZWIERZĄT 1. RÓWNOWAGA GENETYCZNA POPULACJI Fot. W. Wołkow Prowadzący: dr Wioleta Drobik Katedra Genetyki i Ogólnej Hodowli Zwierząt POPULACJA Zbiór organizmów żywych, które łączy
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Program wykładu 1. Jakie
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Program wykładu 1. Jakie
[ IMIĘ I NAZWISKO:. KLASA NR.. ] Zadania genetyczne
![[ IMIĘ I NAZWISKO:. KLASA NR.. ] Zadania genetyczne [ IMIĘ I NAZWISKO:. KLASA NR.. ] Zadania genetyczne](/thumbs/27/11944087.jpg) Zadanie 1. (2 pkt). Ciemnooki mężczyzna, którego ojciec miał oczy piwne a matka niebieskie, poślubił ciemnooką kobietę. Syn tej pary jest niebieskooki. Przyjmując oznaczenia: allel dominujący (barwnik
Zadanie 1. (2 pkt). Ciemnooki mężczyzna, którego ojciec miał oczy piwne a matka niebieskie, poślubił ciemnooką kobietę. Syn tej pary jest niebieskooki. Przyjmując oznaczenia: allel dominujący (barwnik
GENETYKA POPULACJI. Ćwiczenia 1 Biologia I MGR /
 GENETYKA POPULACJI Ćwiczenia 1 Biologia I MGR 1 ZAGADNIENIA struktura genetyczna populacji obliczanie frekwencji genotypów obliczanie frekwencji alleli przewidywanie struktury następnego pokolenia przy
GENETYKA POPULACJI Ćwiczenia 1 Biologia I MGR 1 ZAGADNIENIA struktura genetyczna populacji obliczanie frekwencji genotypów obliczanie frekwencji alleli przewidywanie struktury następnego pokolenia przy
Dziedziczenie cech sprzężonych, crossing-over i mapy chromosomów
 Dziedziczenie cech sprzężonych, crossing-over i mapy chromosomów Zadanie 1. Komórka zawiera 3 pary chromosomów, mieszczących 5 par genów. Pary genów A, a i B, b sprzężone są w układzie cis. Pary C, c i
Dziedziczenie cech sprzężonych, crossing-over i mapy chromosomów Zadanie 1. Komórka zawiera 3 pary chromosomów, mieszczących 5 par genów. Pary genów A, a i B, b sprzężone są w układzie cis. Pary C, c i
Zmienność. środa, 23 listopada 11
 Zmienność http://ggoralski.com Zmienność Zmienność - rodzaje Zmienność obserwuje się zarówno między poszczególnymi osobnikami jak i między populacjami. Różnice te mogą mieć jednak różne podłoże. Mogą one
Zmienność http://ggoralski.com Zmienność Zmienność - rodzaje Zmienność obserwuje się zarówno między poszczególnymi osobnikami jak i między populacjami. Różnice te mogą mieć jednak różne podłoże. Mogą one
Metabolizm i biochemia
 Metabolizm i biochemia Zad. 14 ( 3p.) b) W odpowiedziach powinno być że jest to cykl anaboliczny. Zad. 16 ( 3p.) b) Cysteina jest aminokwasem endogennym, który teoretycznie nie musi być dostarczany z pokarmem.
Metabolizm i biochemia Zad. 14 ( 3p.) b) W odpowiedziach powinno być że jest to cykl anaboliczny. Zad. 16 ( 3p.) b) Cysteina jest aminokwasem endogennym, który teoretycznie nie musi być dostarczany z pokarmem.
Imię i nazwisko...kl...
 Gimnazjum nr 4 im. Ojca Świętego Jana Pawła II we Wrocławiu SPRAWDZIAN GENETYKA GR. A Imię i nazwisko...kl.... 1. Nauka o regułach i mechanizmach dziedziczenia to: (0-1pkt) a) cytologia b) biochemia c)
Gimnazjum nr 4 im. Ojca Świętego Jana Pawła II we Wrocławiu SPRAWDZIAN GENETYKA GR. A Imię i nazwisko...kl.... 1. Nauka o regułach i mechanizmach dziedziczenia to: (0-1pkt) a) cytologia b) biochemia c)
Biologia molekularna z genetyką
 Biologia molekularna z genetyką P. Golik i M. Koper Konwersatorium 2: Analiza genetyczna eukariontów Drosophilla melanogaster Makrokierunek: Bioinformatyka i Biologia Systemów; 2016 Opracowano na podstawie
Biologia molekularna z genetyką P. Golik i M. Koper Konwersatorium 2: Analiza genetyczna eukariontów Drosophilla melanogaster Makrokierunek: Bioinformatyka i Biologia Systemów; 2016 Opracowano na podstawie
Bliskie Spotkanie z Biologią. Genetyka populacji
 Bliskie Spotkanie z Biologią Genetyka populacji Plan wykładu 1) Częstości alleli i genotypów w populacji 2) Prawo Hardy ego-weinberga 3) Dryf genetyczny 4) Efekt założyciela i efekt wąskiego gardła 5)
Bliskie Spotkanie z Biologią Genetyka populacji Plan wykładu 1) Częstości alleli i genotypów w populacji 2) Prawo Hardy ego-weinberga 3) Dryf genetyczny 4) Efekt założyciela i efekt wąskiego gardła 5)
PORÓWNYWANIE POPULACJI POD WZGLĘDEM STRUKTURY
 PORÓWNYWANIE POPULACJI POD WZGLĘDEM STRUKTURY obliczanie dystansu dzielącego grupy (subpopulacje) wyrażonego za pomocą indeksu F Wrighta (fixation index) w modelu jednego locus 1 Ćwiczenia III Mgr Kaczmarek-Okrój
PORÓWNYWANIE POPULACJI POD WZGLĘDEM STRUKTURY obliczanie dystansu dzielącego grupy (subpopulacje) wyrażonego za pomocą indeksu F Wrighta (fixation index) w modelu jednego locus 1 Ćwiczenia III Mgr Kaczmarek-Okrój
PODSTAWY GENETYKI. Prowadzący wykład: prof. dr hab. Jarosław Burczyk
 PODSTAWY GENETYKI Prawa Mendla (jako punkt wyjścia) Epistaza (interakcje między genami) Sprzężenia genetyczne i mapowanie genów Sprzężenie z płcią Analiza rodowodów Prowadzący wykład: prof. dr hab. Jarosław
PODSTAWY GENETYKI Prawa Mendla (jako punkt wyjścia) Epistaza (interakcje między genami) Sprzężenia genetyczne i mapowanie genów Sprzężenie z płcią Analiza rodowodów Prowadzący wykład: prof. dr hab. Jarosław
Zadania maturalne z biologii - 7
 Koło Biologiczne Liceum Ogólnokształcące nr II w Gliwicach 2015-2016 Zadania maturalne z biologii - 7 Zadania: Zad.1 (Jesika Stępień, Natalia Świetlak, Daniela Schwedka 3D) Przeczytaj tekst i na jego podstawie
Koło Biologiczne Liceum Ogólnokształcące nr II w Gliwicach 2015-2016 Zadania maturalne z biologii - 7 Zadania: Zad.1 (Jesika Stępień, Natalia Świetlak, Daniela Schwedka 3D) Przeczytaj tekst i na jego podstawie
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ gamety matczyne Genetyka
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ gamety matczyne Genetyka
1 Podstawowe pojęcia z zakresu genetyki. 2 Podstawowy model dziedziczenia
 Rachunek Prawdopodobieństwa MAP8 Wydział Matematyki, Matematyka Stosowana Projekt - zastosowania rachunku prawdopodobieństwa w genetyce Opracowanie: Antonina Urbaniak Podstawowe pojęcia z zakresu genetyki
Rachunek Prawdopodobieństwa MAP8 Wydział Matematyki, Matematyka Stosowana Projekt - zastosowania rachunku prawdopodobieństwa w genetyce Opracowanie: Antonina Urbaniak Podstawowe pojęcia z zakresu genetyki
1 Genetykapopulacyjna
 1 Genetykapopulacyjna Genetyka populacyjna zajmuje się badaniem częstości występowania poszczególnych alleli oraz genotypów w populacji. Bada także zmiany tych częstości spowodowane doborem naturalnym
1 Genetykapopulacyjna Genetyka populacyjna zajmuje się badaniem częstości występowania poszczególnych alleli oraz genotypów w populacji. Bada także zmiany tych częstości spowodowane doborem naturalnym
GENETYKA POPULACJI. Fot. W. Wołkow
 GENETYKA POPULACJI Fot. W. Wołkow GENETYKA POPULACJI Nauka która respektując zasady dziedziczenia z zakresu genetyki klasycznej bada mechanizmy dziedziczenia w odniesieniu do populacji Struktura genetyczna:
GENETYKA POPULACJI Fot. W. Wołkow GENETYKA POPULACJI Nauka która respektując zasady dziedziczenia z zakresu genetyki klasycznej bada mechanizmy dziedziczenia w odniesieniu do populacji Struktura genetyczna:
2. CZYNNIKI ZABURZAJĄCE RÓWNOWAGĘ GENETYCZNĄ
 ZARZĄDZANIE POPULACJAMI ZWIERZĄT 2. CZYNNIKI ZABURZAJĄCE RÓWNOWAGĘ GENETYCZNĄ POPULACJI Fot. W. Wołkow Prowadzący: dr Wioleta Drobik Katedra Genetyki i Ogólnej Hodowli Zwierząt MIGRACJE Zmiana frekwencji
ZARZĄDZANIE POPULACJAMI ZWIERZĄT 2. CZYNNIKI ZABURZAJĄCE RÓWNOWAGĘ GENETYCZNĄ POPULACJI Fot. W. Wołkow Prowadzący: dr Wioleta Drobik Katedra Genetyki i Ogólnej Hodowli Zwierząt MIGRACJE Zmiana frekwencji
Podstawy genetyki. ESPZiWP 2010
 Podstawy genetyki ESPZiWP 2010 Genetyka - nauka o dziedziczności i zmienności organizmów, wyjaśniająca prawa rządzące podobieństwami i różnicami pomiędzy osobnikami spokrewnionymi przez wspólnego przodka
Podstawy genetyki ESPZiWP 2010 Genetyka - nauka o dziedziczności i zmienności organizmów, wyjaśniająca prawa rządzące podobieństwami i różnicami pomiędzy osobnikami spokrewnionymi przez wspólnego przodka
Prawdopodobeństwo, test χ 2
 Prawdopodobeństwo, test χ 2 Autor: Grzegorz Góralski ggoralski.com Co to jest prawdopodobieństwo? Prawdopodobieństwo = Liczba interesujących nas zdarzeń Liczba wszystkich zdarzeń Jakie jest prawdopodobieństwo
Prawdopodobeństwo, test χ 2 Autor: Grzegorz Góralski ggoralski.com Co to jest prawdopodobieństwo? Prawdopodobieństwo = Liczba interesujących nas zdarzeń Liczba wszystkich zdarzeń Jakie jest prawdopodobieństwo
Ekologia molekularna. wykład 3
 Ekologia molekularna wykład 3 Dziedziczenie mendlowskie Grzegorz Mendel 1822-1884 Darwin + Mendel = Ronald Fisher 1890-1962 wykład 3/2 Prawo Hardy'ego-Weinberga A A gamety możliwe genotypy potomstwa genotyp
Ekologia molekularna wykład 3 Dziedziczenie mendlowskie Grzegorz Mendel 1822-1884 Darwin + Mendel = Ronald Fisher 1890-1962 wykład 3/2 Prawo Hardy'ego-Weinberga A A gamety możliwe genotypy potomstwa genotyp
Pamiętając o komplementarności zasad azotowych, dopisz sekwencję nukleotydów brakującej nici DNA. A C C G T G C C A A T C G A...
 1. Zadanie (0 2 p. ) Porównaj mitozę i mejozę, wpisując do tabeli podane określenia oraz cyfry. ta sama co w komórce macierzystej, o połowę mniejsza niż w komórce macierzystej, gamety, komórki budujące
1. Zadanie (0 2 p. ) Porównaj mitozę i mejozę, wpisując do tabeli podane określenia oraz cyfry. ta sama co w komórce macierzystej, o połowę mniejsza niż w komórce macierzystej, gamety, komórki budujące
Zadania z genetyki. Jacek Grzebyta. 21.XII.2005 version Powered by Λ. L A TEX 4 Unicode
 Zadania z genetyki Jacek Grzebyta 21.XII.2005 version 0.9.1 Powered by Λ L A TEX 4 Unicode Geny sprzężone 1. Po skrzyżowaniu dwóch roślin pomidora otrzymano wyłącznie rośliny o owocach gładkich, liściach
Zadania z genetyki Jacek Grzebyta 21.XII.2005 version 0.9.1 Powered by Λ L A TEX 4 Unicode Geny sprzężone 1. Po skrzyżowaniu dwóch roślin pomidora otrzymano wyłącznie rośliny o owocach gładkich, liściach
BLISKIE SPOTKANIA Z BIOLOGIĄ
 BLISKIE SPOTKANIA Z BIOLOGIĄ Instytutu Biologii Eksperymentalnej Instytut Biologii Środowiska Katedra Biologii Ewolucyjnej UNIWERSYTET KAZIMIERZA WIELKIEGO Wykłady Środy, 15.45, Aula Biblioteki UKW Czas
BLISKIE SPOTKANIA Z BIOLOGIĄ Instytutu Biologii Eksperymentalnej Instytut Biologii Środowiska Katedra Biologii Ewolucyjnej UNIWERSYTET KAZIMIERZA WIELKIEGO Wykłady Środy, 15.45, Aula Biblioteki UKW Czas
Wykład 11: Dane jakościowe. Rozkład χ 2. Test zgodności chi-kwadrat
 Wykład 11: Dane jakościowe Obserwacje klasyfikujemy do klas Zliczamy liczbę obserwacji w każdej klasie Jeżeli są tylko dwie klasy, to jedną z nich możemy nazwać sukcesem, a drugą porażką. Generalnie, liczba
Wykład 11: Dane jakościowe Obserwacje klasyfikujemy do klas Zliczamy liczbę obserwacji w każdej klasie Jeżeli są tylko dwie klasy, to jedną z nich możemy nazwać sukcesem, a drugą porażką. Generalnie, liczba
GENETYCZNE PODSTAWY ZMIENNOŚCI ORGANIZMÓW ZASADY DZIEDZICZENIA CECH PODSTAWY GENETYKI POPULACYJNEJ
 GENETYCZNE PODSTAWY ZMIENNOŚCI ORGANIZMÓW ZASADY DZIEDZICZENIA CECH PODSTAWY GENETYKI POPULACYJNEJ ZMIENNOŚĆ - występowanie dziedzicznych i niedziedzicznych różnic między osobnikami należącymi do tej samej
GENETYCZNE PODSTAWY ZMIENNOŚCI ORGANIZMÓW ZASADY DZIEDZICZENIA CECH PODSTAWY GENETYKI POPULACYJNEJ ZMIENNOŚĆ - występowanie dziedzicznych i niedziedzicznych różnic między osobnikami należącymi do tej samej
Biologia medyczna, lekarski Ćwiczenie ; Ćwiczenie 19
 Ćwiczenie 19 Fenotyp sportowca. Geny warunkujące fenotyp sportowca. Testy DNA w ocenie predyspozycji sportowych i ich aspekty etyczne. Genetyka cech ilościowych. Prof. dr hab. Roman Zieliński 1. "Fenotyp
Ćwiczenie 19 Fenotyp sportowca. Geny warunkujące fenotyp sportowca. Testy DNA w ocenie predyspozycji sportowych i ich aspekty etyczne. Genetyka cech ilościowych. Prof. dr hab. Roman Zieliński 1. "Fenotyp
Ćwiczenie 3/4. Prawa Mendla: zadania, analiza rodowodów Sprzężenia i odległość genetyczna. Kariotypy i chromosomopatie. Prof. dr hab.
 Ćwiczenie 3/4 Prawa Mendla: zadania, analiza rodowodów Sprzężenia i odległość genetyczna. Kariotypy i chromosomopatie Prof. dr hab. Roman Zieliński 1 Prawa Mendla 1.1. Pytania i zagadnienia 1.1.1. Przypomnij
Ćwiczenie 3/4 Prawa Mendla: zadania, analiza rodowodów Sprzężenia i odległość genetyczna. Kariotypy i chromosomopatie Prof. dr hab. Roman Zieliński 1 Prawa Mendla 1.1. Pytania i zagadnienia 1.1.1. Przypomnij
Zadania do cz. I. ggoralski.com. Autor: Grzegorz Góralski. środa, 9 listopada 11
 Zadania do cz. I Autor: Grzegorz Góralski ggoralski.com Zadanie 1 Rozpatrujemy dwa geny u zwierzęcia. Allel A jest dominujący i koduje brązową barwę oczu, allel recesywny a determinuje barwę czerwoną.
Zadania do cz. I Autor: Grzegorz Góralski ggoralski.com Zadanie 1 Rozpatrujemy dwa geny u zwierzęcia. Allel A jest dominujący i koduje brązową barwę oczu, allel recesywny a determinuje barwę czerwoną.
2. Rozdział materiału genetycznego w czasie podziałów komórkowych - mitozy i mejozy
 Program ćwiczeń z przedmiotu BIOLOGIA MOLEKULARNA I GENETYKA, część I (GENETYKA) dla kierunku Lekarskiego, rok I 2017/2018 Ćwiczenie nr 1 (09-10.10.2017) Temat: Wprowadzenie 1. Omówienie regulaminu zajęć
Program ćwiczeń z przedmiotu BIOLOGIA MOLEKULARNA I GENETYKA, część I (GENETYKA) dla kierunku Lekarskiego, rok I 2017/2018 Ćwiczenie nr 1 (09-10.10.2017) Temat: Wprowadzenie 1. Omówienie regulaminu zajęć
Składniki jądrowego genomu człowieka
 Składniki jądrowego genomu człowieka Genom człowieka 3 000 Mpz (3x10 9, 100 cm) Geny i sekwencje związane z genami (900 Mpz, 30% g. jądrowego) DNA pozagenowy (2100 Mpz, 70%) DNA kodujący (90 Mpz ~ ok.
Składniki jądrowego genomu człowieka Genom człowieka 3 000 Mpz (3x10 9, 100 cm) Geny i sekwencje związane z genami (900 Mpz, 30% g. jądrowego) DNA pozagenowy (2100 Mpz, 70%) DNA kodujący (90 Mpz ~ ok.
( x) Równanie regresji liniowej ma postać. By obliczyć współczynniki a i b należy posłużyć się następującymi wzorami 1 : Gdzie:
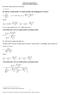 ma postać y = ax + b Równanie regresji liniowej By obliczyć współczynniki a i b należy posłużyć się następującymi wzorami 1 : xy b = a = b lub x Gdzie: xy = też a = x = ( b ) i to dane empiryczne, a ilość
ma postać y = ax + b Równanie regresji liniowej By obliczyć współczynniki a i b należy posłużyć się następującymi wzorami 1 : xy b = a = b lub x Gdzie: xy = też a = x = ( b ) i to dane empiryczne, a ilość
Selekcja, dobór hodowlany. ESPZiWP
 Selekcja, dobór hodowlany ESPZiWP Celem pracy hodowlanej jest genetyczne doskonalenie zwierząt w wyznaczonym kierunku. Trudno jest doskonalić zwierzęta już urodzone, ale można doskonalić populację w ten
Selekcja, dobór hodowlany ESPZiWP Celem pracy hodowlanej jest genetyczne doskonalenie zwierząt w wyznaczonym kierunku. Trudno jest doskonalić zwierzęta już urodzone, ale można doskonalić populację w ten
Program ćwiczeń z przedmiotu BIOLOGIA MOLEKULARNA I GENETYKA, część I dla kierunku Lekarskiego, rok I 2015/2016. Ćwiczenie nr 1 (06-07.10.
 Program ćwiczeń z przedmiotu BIOLOGIA MOLEKULARNA I GENETYKA, część I dla kierunku Lekarskiego, rok I 2015/2016 Ćwiczenie nr 1 (06-07.10.2015) Temat: Wprowadzenie 1. Omówienie regulaminu zajęć Temat: Wprowadzenie
Program ćwiczeń z przedmiotu BIOLOGIA MOLEKULARNA I GENETYKA, część I dla kierunku Lekarskiego, rok I 2015/2016 Ćwiczenie nr 1 (06-07.10.2015) Temat: Wprowadzenie 1. Omówienie regulaminu zajęć Temat: Wprowadzenie
Anna Szewczyk. Wydział Geodezji Górniczej i InŜynierii środowiska AGH
 Anna Szewczyk Wydział Geodezji Górniczej i InŜynierii środowiska AGH Zastosowania biblioteki Genetics programu R The genetics Package Tytuł: Populacja genetyczna Wersja:1.2.0 Data utworzenia: 2005-11-09
Anna Szewczyk Wydział Geodezji Górniczej i InŜynierii środowiska AGH Zastosowania biblioteki Genetics programu R The genetics Package Tytuł: Populacja genetyczna Wersja:1.2.0 Data utworzenia: 2005-11-09
Dorota Fopp-Bayat Mirosław Łuczyński Małgorzata Jankun. Rola genetyki populacyjnej w zachowaniu bioróżnorodności ryb
 1 Dorota Fopp-Bayat Mirosław Łuczyński Małgorzata Jankun Rola genetyki populacyjnej w zachowaniu bioróżnorodności ryb 2 Publikację przygotowano w ramach projektu Ichtiologiczna bioróżnorodność jezior wypracowanie
1 Dorota Fopp-Bayat Mirosław Łuczyński Małgorzata Jankun Rola genetyki populacyjnej w zachowaniu bioróżnorodności ryb 2 Publikację przygotowano w ramach projektu Ichtiologiczna bioróżnorodność jezior wypracowanie
Napisz, który z przedstawionych schematycznie rodzajów replikacji (A, B czy C) ilustruje replikację semikonserwatywną. Wyjaśnij, na czym polega ten
 Napisz, który z przedstawionych schematycznie rodzajów replikacji (A, B czy C) ilustruje replikację semikonserwatywną. Wyjaśnij, na czym polega ten proces. Na schemacie przedstawiono etapy przekazywania
Napisz, który z przedstawionych schematycznie rodzajów replikacji (A, B czy C) ilustruje replikację semikonserwatywną. Wyjaśnij, na czym polega ten proces. Na schemacie przedstawiono etapy przekazywania
GENETYKA. Genetyka. Dziedziczność przekazywanie cech rodziców potomstwu Zmienność występowanie różnic pomiędzy różnymi osobnikami tego samego gatunku
 GENETYKA Genetyka Nauka o dziedziczności i zmienności organizmów, wyjaśniająca prawa rządzące podobieństwami i różnicami pomiędzy osobnikami spokrewnionymi przez wspólnego przodka Dziedziczność przekazywanie
GENETYKA Genetyka Nauka o dziedziczności i zmienności organizmów, wyjaśniająca prawa rządzące podobieństwami i różnicami pomiędzy osobnikami spokrewnionymi przez wspólnego przodka Dziedziczność przekazywanie
Temat 6: Genetyczne uwarunkowania płci. Cechy sprzężone z płcią.
 Temat 6: Genetyczne uwarunkowania płci. Cechy sprzężone z płcią. 1. Kariotyp człowieka. 2. Determinacja płci u człowieka. 3. Warunkowanie płci u innych organizmów. 4. Cechy związane z płcią. 5. Cechy sprzężone
Temat 6: Genetyczne uwarunkowania płci. Cechy sprzężone z płcią. 1. Kariotyp człowieka. 2. Determinacja płci u człowieka. 3. Warunkowanie płci u innych organizmów. 4. Cechy związane z płcią. 5. Cechy sprzężone
GIMNAZJUM SPRAWDZIANY SUKCES W NAUCE
 GIMNAZJUM SPRAWDZIANY BIOLOGIA klasa III SUKCES W NAUCE II GENETYKA CZŁOWIEKA Zadanie 1. Cechy organizmu są warunkowane przez allele dominujące i recesywne. Uzupełnij tabelę, wykorzystując poniższe określenia,
GIMNAZJUM SPRAWDZIANY BIOLOGIA klasa III SUKCES W NAUCE II GENETYKA CZŁOWIEKA Zadanie 1. Cechy organizmu są warunkowane przez allele dominujące i recesywne. Uzupełnij tabelę, wykorzystując poniższe określenia,
Wykład 3 Hipotezy statystyczne
 Wykład 3 Hipotezy statystyczne Hipotezą statystyczną nazywamy każde przypuszczenie dotyczące nieznanego rozkładu obserwowanej zmiennej losowej (cechy populacji generalnej) Hipoteza zerowa (H 0 ) jest hipoteza
Wykład 3 Hipotezy statystyczne Hipotezą statystyczną nazywamy każde przypuszczenie dotyczące nieznanego rozkładu obserwowanej zmiennej losowej (cechy populacji generalnej) Hipoteza zerowa (H 0 ) jest hipoteza
Genetyka populacyjna. Populacja
 Genetyka populacyjna Populacja 1 Populacja Populacja jest to zbiór osobników jednego gatunku żyjących na danym terytorium w danym czasie. Genetykę populacyjną interesuje tzw. populacja panmiktyczna (mendlowska),
Genetyka populacyjna Populacja 1 Populacja Populacja jest to zbiór osobników jednego gatunku żyjących na danym terytorium w danym czasie. Genetykę populacyjną interesuje tzw. populacja panmiktyczna (mendlowska),
PRAWO CZYSTOŚCI GAMET (I Prawo Mendla) RELACJE MIĘDZY ALLELAMI TEGO SAMEGO GENU
 A A a a A a PRAWO CZYSTOŚCI GAMET (I Prawo Mendla) Osobnik diploidalny wytwarza haploidalne gamety, do których w sposób losowy trafiają po jednym chromosomie z pary (po jednym alleleu z pary), zatem osobnik
A A a a A a PRAWO CZYSTOŚCI GAMET (I Prawo Mendla) Osobnik diploidalny wytwarza haploidalne gamety, do których w sposób losowy trafiają po jednym chromosomie z pary (po jednym alleleu z pary), zatem osobnik
Genetyka Populacji http://ggoralski.com
 Genetyka Populacji http://ggoralski.com Frekwencje genotypów i alleli Frekwencja genotypów Frekwencje genotypów i alleli Zadania P AA = 250/500 = 0,5 P Aa = 100/500 = 0,2 P aa = 150/500 = 0,3 = 1 Frekwencje
Genetyka Populacji http://ggoralski.com Frekwencje genotypów i alleli Frekwencja genotypów Frekwencje genotypów i alleli Zadania P AA = 250/500 = 0,5 P Aa = 100/500 = 0,2 P aa = 150/500 = 0,3 = 1 Frekwencje
Testowanie hipotez statystycznych. Wnioskowanie statystyczne
 Testowanie hipotez statystycznych Wnioskowanie statystyczne Hipoteza statystyczna to dowolne przypuszczenie co do rozkładu populacji generalnej (jego postaci funkcyjnej lub wartości parametrów). Hipotezy
Testowanie hipotez statystycznych Wnioskowanie statystyczne Hipoteza statystyczna to dowolne przypuszczenie co do rozkładu populacji generalnej (jego postaci funkcyjnej lub wartości parametrów). Hipotezy
WSTĘP. Copyright 2011, Joanna Szyda
 BIOINFORMATYKA 1. Wykład wstępny 2. Struktury danych w badaniach bioinformatycznych 3. Bazy danych: projektowanie i struktura 4. Bazy danych: projektowanie i struktura 5. Równowaga Hardyego-Weinberga,
BIOINFORMATYKA 1. Wykład wstępny 2. Struktury danych w badaniach bioinformatycznych 3. Bazy danych: projektowanie i struktura 4. Bazy danych: projektowanie i struktura 5. Równowaga Hardyego-Weinberga,
Plan wykładów z genetyki ogólnej
 Plan wykładów z genetyki ogólnej 01 Metody genetyki klasycznej 02 Metody analizy DNA 03 Metody analizy genomu 04 Genomy prokariontów 05 Genomy eukariontów 06 Zmienność genomów w populacjach 07 Genomy a
Plan wykładów z genetyki ogólnej 01 Metody genetyki klasycznej 02 Metody analizy DNA 03 Metody analizy genomu 04 Genomy prokariontów 05 Genomy eukariontów 06 Zmienność genomów w populacjach 07 Genomy a
Wykład 14 Test chi-kwadrat zgodności
 Wykład 14 Test chi-kwadrat zgodności Obserwacje klasyfikujemy do jakościowych klas Zliczamy liczbę obserwacji w każdej klasie Jeżeli są tylko dwie klasy, to liczba obserwacji w pierszej klasie ma rozkład
Wykład 14 Test chi-kwadrat zgodności Obserwacje klasyfikujemy do jakościowych klas Zliczamy liczbę obserwacji w każdej klasie Jeżeli są tylko dwie klasy, to liczba obserwacji w pierszej klasie ma rozkład
dr hab. Dariusz Piwczyński, prof. nadzw. UTP
 dr hab. Dariusz Piwczyński, prof. nadzw. UTP Cechy jakościowe są to cechy, których jednoznaczne i oczywiste scharakteryzowanie za pomocą liczb jest niemożliwe lub bardzo utrudnione. nominalna porządek
dr hab. Dariusz Piwczyński, prof. nadzw. UTP Cechy jakościowe są to cechy, których jednoznaczne i oczywiste scharakteryzowanie za pomocą liczb jest niemożliwe lub bardzo utrudnione. nominalna porządek
b) Niech: - wśród trzech wylosowanych opakowań jest co najwyżej jedno o dawce 15 mg. Wówczas:
 ROZWIĄZANIA I ODPOWIEDZI Zadanie A1. Można założyć, że przy losowaniu trzech kul jednocześnie kolejność ich wylosowania nie jest istotna. A więc: Ω = 20 3. a) Niech: - wśród trzech wylosowanych opakowań
ROZWIĄZANIA I ODPOWIEDZI Zadanie A1. Można założyć, że przy losowaniu trzech kul jednocześnie kolejność ich wylosowania nie jest istotna. A więc: Ω = 20 3. a) Niech: - wśród trzech wylosowanych opakowań
ZARZĄDZANIE POPULACJAMI ZWIERZĄT DRYF GENETYCZNY EFEKTYWNA WIELKOŚĆ POPULACJI PRZYROST INBREDU
 ZARZĄDZANIE POPULACJAMI ZWIERZĄT DRYF GENETYCZNY EFEKTYWNA WIELKOŚĆ POPULACJI PRZYROST INBREDU DRYF GENETYCZNY ) Każdy żywy organizm wytwarza więcej gamet, niż zdolne jest przetrwać (Darwin). 2) Przypadek
ZARZĄDZANIE POPULACJAMI ZWIERZĄT DRYF GENETYCZNY EFEKTYWNA WIELKOŚĆ POPULACJI PRZYROST INBREDU DRYF GENETYCZNY ) Każdy żywy organizm wytwarza więcej gamet, niż zdolne jest przetrwać (Darwin). 2) Przypadek
Podstawy genetyki populacji. Genetyka mendlowska i ewolucja
 Podstawy genetyki populacji Genetyka mendlowska i ewolucja Syntetyczna teoria ewolucji } Pierwsza synteza: połączenie teorii ewolucji Darwina z genetyką mendlowską na poziomie populacji } W naturalnych
Podstawy genetyki populacji Genetyka mendlowska i ewolucja Syntetyczna teoria ewolucji } Pierwsza synteza: połączenie teorii ewolucji Darwina z genetyką mendlowską na poziomie populacji } W naturalnych
ALGORYTMICZNA I STATYSTYCZNA ANALIZA DANYCH
 1 ALGORYTMICZNA I STATYSTYCZNA ANALIZA DANYCH WFAiS UJ, Informatyka Stosowana II stopień studiów 2 Wnioskowanie statystyczne dla zmiennych numerycznych Porównywanie dwóch średnich Boot-strapping Analiza
1 ALGORYTMICZNA I STATYSTYCZNA ANALIZA DANYCH WFAiS UJ, Informatyka Stosowana II stopień studiów 2 Wnioskowanie statystyczne dla zmiennych numerycznych Porównywanie dwóch średnich Boot-strapping Analiza
DOBÓR. Kojarzenie, depresja inbredowa, krzyżowanie, heterozja
 DOBÓR Kojarzenie, depresja inbredowa, krzyżowanie, heterozja SELEKCJA grupa osobników obu płci, która ma zostać rodzicami następnego pokolenia DOBÓR OSOBNIKÓW DO KOJARZEŃ POSTĘP HODOWLANY następne pokolenie
DOBÓR Kojarzenie, depresja inbredowa, krzyżowanie, heterozja SELEKCJA grupa osobników obu płci, która ma zostać rodzicami następnego pokolenia DOBÓR OSOBNIKÓW DO KOJARZEŃ POSTĘP HODOWLANY następne pokolenie
Zestaw 1 Genetyka. Zadanie 2.(1pkt) Schemat przedstawia rodowód genetyczny pewnej rodziny. Kółko oznacza kobietę, kwadrat oznacza mężczyznę.
 Zestaw 1 Genetyka Zadanie 1. (3pkt) Praworęczność i leworęczność są cechami dziedzicznymi, przy czym tendencja do używania prawej ręki jest cechą dominującą. Gen warunkujący tę cechę jest zlokalizowany
Zestaw 1 Genetyka Zadanie 1. (3pkt) Praworęczność i leworęczność są cechami dziedzicznymi, przy czym tendencja do używania prawej ręki jest cechą dominującą. Gen warunkujący tę cechę jest zlokalizowany
CECHY ILOŚCIOWE PARAMETRY GENETYCZNE
 CECHY ILOŚCIOWE PARAMETRY GENETYCZNE Zarządzanie populacjami zwierząt, ćwiczenia V Dr Wioleta Drobik Rodzaje cech Jakościowe o prostym dziedziczeniu uwarunkowane zwykle przez kilka genów Słaba podatność
CECHY ILOŚCIOWE PARAMETRY GENETYCZNE Zarządzanie populacjami zwierząt, ćwiczenia V Dr Wioleta Drobik Rodzaje cech Jakościowe o prostym dziedziczeniu uwarunkowane zwykle przez kilka genów Słaba podatność
Konspekt do zajęć z przedmiotu Genetyka dla kierunku Położnictwo dr Anna Skorczyk-Werner Katedra i Zakład Genetyki Medycznej
 Seminarium 1 część 1 Konspekt do zajęć z przedmiotu Genetyka dla kierunku Położnictwo dr Anna Skorczyk-Werner Katedra i Zakład Genetyki Medycznej Genom człowieka Genomem nazywamy całkowitą ilość DNA jaka
Seminarium 1 część 1 Konspekt do zajęć z przedmiotu Genetyka dla kierunku Położnictwo dr Anna Skorczyk-Werner Katedra i Zakład Genetyki Medycznej Genom człowieka Genomem nazywamy całkowitą ilość DNA jaka
Testowanie hipotez statystycznych.
 Bioinformatyka Wykład 9 Wrocław, 5 grudnia 2011 Temat. Test zgodności χ 2 Pearsona. Statystyka χ 2 Pearsona Rozpatrzmy ciąg niezależnych zmiennych losowych X 1,..., X n o jednakowym dyskretnym rozkładzie
Bioinformatyka Wykład 9 Wrocław, 5 grudnia 2011 Temat. Test zgodności χ 2 Pearsona. Statystyka χ 2 Pearsona Rozpatrzmy ciąg niezależnych zmiennych losowych X 1,..., X n o jednakowym dyskretnym rozkładzie
Konkurs szkolny Mistrz genetyki etap II
 onkurs szkolny istrz genetyki etap II 1.W D pewnego pierwotniaka tymina stanowi 28 % wszystkich zasad azotowych. blicz i zapisz, jaka jest zawartość procentowa każdej z pozostałych zasad w D tego pierwotniaka.
onkurs szkolny istrz genetyki etap II 1.W D pewnego pierwotniaka tymina stanowi 28 % wszystkich zasad azotowych. blicz i zapisz, jaka jest zawartość procentowa każdej z pozostałych zasad w D tego pierwotniaka.
6. Uzupełnij zdanie, wstawiajac w odpowiednie miejsce wyrażenie ujawni się lub nie ujawni się :
 ID Testu: 9S6C1A4 Imię i nazwisko ucznia Klasa Data 1. Allelami nazywamy A. takie same formy jednego genu. B. różne formy różnych genów. C. takie same formy różnych genów. D. różne formy jednego genu.
ID Testu: 9S6C1A4 Imię i nazwisko ucznia Klasa Data 1. Allelami nazywamy A. takie same formy jednego genu. B. różne formy różnych genów. C. takie same formy różnych genów. D. różne formy jednego genu.
GENETYKA POPULACJI. Ćwiczenia 3 Biologia I MGR
 GENETYKA POPULACJI Ćwiczenia 3 Biologia I MGR Heterozygotyczność Rozpatrując różnorodność genetyczną w populacjach o układzie hierarchicznym zauważamy, że najwyższy poziom heterozygotyczności zawsze występuje
GENETYKA POPULACJI Ćwiczenia 3 Biologia I MGR Heterozygotyczność Rozpatrując różnorodność genetyczną w populacjach o układzie hierarchicznym zauważamy, że najwyższy poziom heterozygotyczności zawsze występuje
2. CZYNNIKI ZABURZAJĄCE RÓWNOWAGĘ GENETYCZNĄ
 ZARZĄDZANIE POPULACJAMI ZWIERZĄT 2. CZYNNIKI ZABURZAJĄCE RÓWNOWAGĘ GENETYCZNĄ POPULACJI Fot. W. Wołkow Prowadzący: dr Wioleta Drobik-Czwarno; mgr Magdalena Kaczmarek-Okrój Katedra Genetyki i Ogólnej Hodowli
ZARZĄDZANIE POPULACJAMI ZWIERZĄT 2. CZYNNIKI ZABURZAJĄCE RÓWNOWAGĘ GENETYCZNĄ POPULACJI Fot. W. Wołkow Prowadzący: dr Wioleta Drobik-Czwarno; mgr Magdalena Kaczmarek-Okrój Katedra Genetyki i Ogólnej Hodowli
Ćwiczenie 16/17. Szacowanie częstości mutacji punktowych. Mutacje chromosomowe strukturalne. Mutacje chromosomowe liczbowe.
 Ćwiczenie 16/17 Szacowanie częstości mutacji punktowych. Mutacje chromosomowe strukturalne. Mutacje chromosomowe liczbowe. Prof. dr hab. Roman Zieliński 1. Szacowanie częstości mutacji punktowych 1.1.
Ćwiczenie 16/17 Szacowanie częstości mutacji punktowych. Mutacje chromosomowe strukturalne. Mutacje chromosomowe liczbowe. Prof. dr hab. Roman Zieliński 1. Szacowanie częstości mutacji punktowych 1.1.
I. Genetyka. Dział programu Lp. Temat konieczny podstawowy rozszerzający
 I. Genetyka 1. Czym jest genetyka? wymienia cechy gatunkowe i indywidualne podanych organizmów wyjaśnia, że jego podobieństwo do rodziców jest wynikiem dziedziczenia cech definiuje pojęcia genetyka oraz
I. Genetyka 1. Czym jest genetyka? wymienia cechy gatunkowe i indywidualne podanych organizmów wyjaśnia, że jego podobieństwo do rodziców jest wynikiem dziedziczenia cech definiuje pojęcia genetyka oraz
Ćwiczenie 3. Amplifikacja genu ccr5 Homo sapiens wykrywanie delecji Δ32pz warunkującej oporność na wirusa HIV
 Ćwiczenie 3. Amplifikacja genu ccr5 Homo sapiens wykrywanie delecji Δ32pz warunkującej oporność na wirusa HIV Cel ćwiczenia Określenie podatności na zakażenie wirusem HIV poprzez detekcję homo lub heterozygotyczności
Ćwiczenie 3. Amplifikacja genu ccr5 Homo sapiens wykrywanie delecji Δ32pz warunkującej oporność na wirusa HIV Cel ćwiczenia Określenie podatności na zakażenie wirusem HIV poprzez detekcję homo lub heterozygotyczności
Zadania ze statystyki, cz.6
 Zadania ze statystyki, cz.6 Zad.1 Proszę wskazać, jaką część pola pod krzywą normalną wyznaczają wartości Z rozkładu dystrybuanty rozkładu normalnego: - Z > 1,25 - Z > 2,23 - Z < -1,23 - Z > -1,16 - Z
Zadania ze statystyki, cz.6 Zad.1 Proszę wskazać, jaką część pola pod krzywą normalną wyznaczają wartości Z rozkładu dystrybuanty rozkładu normalnego: - Z > 1,25 - Z > 2,23 - Z < -1,23 - Z > -1,16 - Z
Statystyka matematyczna dla leśników
 Statystyka matematyczna dla leśników Wydział Leśny Kierunek leśnictwo Studia Stacjonarne I Stopnia Rok akademicki 03/04 Wykład 5 Testy statystyczne Ogólne zasady testowania hipotez statystycznych, rodzaje
Statystyka matematyczna dla leśników Wydział Leśny Kierunek leśnictwo Studia Stacjonarne I Stopnia Rok akademicki 03/04 Wykład 5 Testy statystyczne Ogólne zasady testowania hipotez statystycznych, rodzaje
ocena dopuszczająca ocena dostateczna ocena dobra ocena bardzo dobra Dział VII. EKOLOGIA NAUKA O ŚRODOWISKU
 Dział VII. EKOLOGIA NAUKA O ŚRODOWISKU wyróżnia elementy żywe i nieożywione w obserwowanym ekosystemie oblicza zagęszczenie wybranej rośliny na badanym terenie określa znaczenie wiedzy ekologicznej w życiu
Dział VII. EKOLOGIA NAUKA O ŚRODOWISKU wyróżnia elementy żywe i nieożywione w obserwowanym ekosystemie oblicza zagęszczenie wybranej rośliny na badanym terenie określa znaczenie wiedzy ekologicznej w życiu
Wszystkie wyniki w postaci ułamków należy podawać z dokładnością do czterech miejsc po przecinku!
 Pracownia statystyczno-filogenetyczna Liczba punktów (wypełnia KGOB) / 30 PESEL Imię i nazwisko Grupa Nr Czas: 90 min. Łączna liczba punktów do zdobycia: 30 Czerwona Niebieska Zielona Żółta Zaznacz znakiem
Pracownia statystyczno-filogenetyczna Liczba punktów (wypełnia KGOB) / 30 PESEL Imię i nazwisko Grupa Nr Czas: 90 min. Łączna liczba punktów do zdobycia: 30 Czerwona Niebieska Zielona Żółta Zaznacz znakiem
Genetyka populacji. Ćwiczenia 7
 Genetyka populacji Ćwiczenia 7 Rodowody wraz z wynikami kontroli użytkowości stanowią podstawową informację potrzebną do doskonalenia zwierząt C F X S D C F C F S D strzałka oznacza przepływ genów między
Genetyka populacji Ćwiczenia 7 Rodowody wraz z wynikami kontroli użytkowości stanowią podstawową informację potrzebną do doskonalenia zwierząt C F X S D C F C F S D strzałka oznacza przepływ genów między
Współdziałanie alleliczne
 Współdziałanie alleliczne Zadanie 1. U ludzi umieszczanie lewego kciuka na prawym (L na P) podczas splatania dłoni jest cechą dominującą uwarunkowaną obecnością genu F. Cecha dziedziczy się według typu
Współdziałanie alleliczne Zadanie 1. U ludzi umieszczanie lewego kciuka na prawym (L na P) podczas splatania dłoni jest cechą dominującą uwarunkowaną obecnością genu F. Cecha dziedziczy się według typu
Wydział Matematyki. Testy zgodności. Wykład 03
 Wydział Matematyki Testy zgodności Wykład 03 Testy zgodności W testach zgodności badamy postać rozkładu teoretycznego zmiennej losowej skokowej lub ciągłej. Weryfikują one stawiane przez badaczy hipotezy
Wydział Matematyki Testy zgodności Wykład 03 Testy zgodności W testach zgodności badamy postać rozkładu teoretycznego zmiennej losowej skokowej lub ciągłej. Weryfikują one stawiane przez badaczy hipotezy
forma studiów Studia pierwszego stopnia - stacjonarne sposób ustalania Na ocenę końcową modułu składa się średnia ważona z 2 elementów:
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Biotechnologia, poziom I Sylabus modułu: Podstawy genetyki (1BT_22) 1. Informacje ogólne koordynator modułu dr Damian Gruszka rok akademicki
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Biotechnologia, poziom I Sylabus modułu: Podstawy genetyki (1BT_22) 1. Informacje ogólne koordynator modułu dr Damian Gruszka rok akademicki
Testy nieparametryczne
 Testy nieparametryczne Testy nieparametryczne możemy stosować, gdy nie są spełnione założenia wymagane dla testów parametrycznych. Stosujemy je również, gdy dane można uporządkować według określonych kryteriów
Testy nieparametryczne Testy nieparametryczne możemy stosować, gdy nie są spełnione założenia wymagane dla testów parametrycznych. Stosujemy je również, gdy dane można uporządkować według określonych kryteriów
Genetyka populacyjna
 Genetyka populacyjna analizuje strukturę genetyczną całych populacji oraz wyniki kojarzeń wewnątrz populacji lub pomiędzy różnymi populacjami, opiera się na modelach matematycznych Prawo równowagi Hardy
Genetyka populacyjna analizuje strukturę genetyczną całych populacji oraz wyniki kojarzeń wewnątrz populacji lub pomiędzy różnymi populacjami, opiera się na modelach matematycznych Prawo równowagi Hardy
Pytanie: Kiedy do testowania hipotezy stosujemy rozkład normalny?
 Pytanie: Kiedy do testowania hipotezy stosujemy rozkład normalny? Gdy: badana cecha jest mierzalna (tzn. posiada rozkład ciągły); badana cecha posiada rozkład normalny; dysponujemy pojedynczym wynikiem;
Pytanie: Kiedy do testowania hipotezy stosujemy rozkład normalny? Gdy: badana cecha jest mierzalna (tzn. posiada rozkład ciągły); badana cecha posiada rozkład normalny; dysponujemy pojedynczym wynikiem;
PDF created with FinePrint pdffactory Pro trial version http://www.fineprint.com
 Analiza korelacji i regresji KORELACJA zależność liniowa Obserwujemy parę cech ilościowych (X,Y). Doświadczenie jest tak pomyślane, aby obserwowane pary cech X i Y (tzn i ta para x i i y i dla różnych
Analiza korelacji i regresji KORELACJA zależność liniowa Obserwujemy parę cech ilościowych (X,Y). Doświadczenie jest tak pomyślane, aby obserwowane pary cech X i Y (tzn i ta para x i i y i dla różnych
Zarządzanie populacjami zwierząt. Parametry genetyczne cech
 Zarządzanie populacjami zwierząt Parametry genetyczne cech Teoria ścieżki zależność przyczynowo-skutkowa X p 01 Z Y p 02 p 01 2 + p 02 2 = 1 współczynniki ścieżek miary związku między przyczyną a skutkiem
Zarządzanie populacjami zwierząt Parametry genetyczne cech Teoria ścieżki zależność przyczynowo-skutkowa X p 01 Z Y p 02 p 01 2 + p 02 2 = 1 współczynniki ścieżek miary związku między przyczyną a skutkiem
WNIOSKOWANIE STATYSTYCZNE
 STATYSTYKA WNIOSKOWANIE STATYSTYCZNE ESTYMACJA oszacowanie z pewną dokładnością wartości opisującej rozkład badanej cechy statystycznej. WERYFIKACJA HIPOTEZ sprawdzanie słuszności przypuszczeń dotyczących
STATYSTYKA WNIOSKOWANIE STATYSTYCZNE ESTYMACJA oszacowanie z pewną dokładnością wartości opisującej rozkład badanej cechy statystycznej. WERYFIKACJA HIPOTEZ sprawdzanie słuszności przypuszczeń dotyczących
Genetyka ekologiczna i populacyjna W8
 Genetyka ekologiczna i populacyjna W8 Genetyka populacji: Treść wykładów Zmienność genetyczna i środowiskowa Mutacje i rekombinacje Kojarzenie krewniacze Częstość genów i genotypów w populacji i prawdopodobieństwo
Genetyka ekologiczna i populacyjna W8 Genetyka populacji: Treść wykładów Zmienność genetyczna i środowiskowa Mutacje i rekombinacje Kojarzenie krewniacze Częstość genów i genotypów w populacji i prawdopodobieństwo
Dane dotyczące wartości zmiennej (cechy) wprowadzamy w jednej kolumnie. W przypadku większej liczby zmiennych wprowadzamy każdą w oddzielnej kolumnie.
 STATISTICA INSTRUKCJA - 1 I. Wprowadzanie danych Podstawowe / Nowy / Arkusz Dane dotyczące wartości zmiennej (cechy) wprowadzamy w jednej kolumnie. W przypadku większej liczby zmiennych wprowadzamy każdą
STATISTICA INSTRUKCJA - 1 I. Wprowadzanie danych Podstawowe / Nowy / Arkusz Dane dotyczące wartości zmiennej (cechy) wprowadzamy w jednej kolumnie. W przypadku większej liczby zmiennych wprowadzamy każdą
Genetyka SYLABUS A. Informacje ogólne
 Genetyka A. Informacje ogólne Elementy sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język Rodzaj Rok studiów /semestr Wymagania
Genetyka A. Informacje ogólne Elementy sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język Rodzaj Rok studiów /semestr Wymagania
Szacowanie wartości hodowlanej. Zarządzanie populacjami
 Szacowanie wartości hodowlanej Zarządzanie populacjami wartość hodowlana = wartość cechy? Tak! Przy h 2 =1 ? wybitny ojciec = wybitne dzieci Tak, gdy cecha wysokoodziedziczalna. Wartość hodowlana genetycznie
Szacowanie wartości hodowlanej Zarządzanie populacjami wartość hodowlana = wartość cechy? Tak! Przy h 2 =1 ? wybitny ojciec = wybitne dzieci Tak, gdy cecha wysokoodziedziczalna. Wartość hodowlana genetycznie
Depresja inbredowa i heterozja
 Depresja inbredowa i heterozja Charles Darwin Dlaczego rośliny chronią się przed samozapyleniem? Doświadczenie na 57 gatunkach roślin! Samozapłodnienie obniża wigor i płodność większości z 57 gatunków
Depresja inbredowa i heterozja Charles Darwin Dlaczego rośliny chronią się przed samozapyleniem? Doświadczenie na 57 gatunkach roślin! Samozapłodnienie obniża wigor i płodność większości z 57 gatunków
Statystyczna analiza danych w programie STATISTICA (wykład 2) Dariusz Gozdowski
 Statystyczna analiza danych w programie STATISTICA (wykład ) Dariusz Gozdowski Katedra Doświadczalnictwa i Bioinformatyki Wydział Rolnictwa i Biologii SGGW Weryfikacja (testowanie) hipotez statystycznych
Statystyczna analiza danych w programie STATISTICA (wykład ) Dariusz Gozdowski Katedra Doświadczalnictwa i Bioinformatyki Wydział Rolnictwa i Biologii SGGW Weryfikacja (testowanie) hipotez statystycznych
Algorytmy genetyczne. Paweł Cieśla. 8 stycznia 2009
 Algorytmy genetyczne Paweł Cieśla 8 stycznia 2009 Genetyka - nauka o dziedziczeniu cech pomiędzy pokoleniami. Geny są czynnikami, które decydują o wyglądzie, zachowaniu, rozmnażaniu każdego żywego organizmu.
Algorytmy genetyczne Paweł Cieśla 8 stycznia 2009 Genetyka - nauka o dziedziczeniu cech pomiędzy pokoleniami. Geny są czynnikami, które decydują o wyglądzie, zachowaniu, rozmnażaniu każdego żywego organizmu.
Zawartość. Zawartość
 Opr. dr inż. Grzegorz Biesok. Wer. 2.05 2011 Zawartość Zawartość 1. Rozkład normalny... 3 2. Rozkład normalny standardowy... 5 3. Obliczanie prawdopodobieństw dla zmiennych o rozkładzie norm. z parametrami
Opr. dr inż. Grzegorz Biesok. Wer. 2.05 2011 Zawartość Zawartość 1. Rozkład normalny... 3 2. Rozkład normalny standardowy... 5 3. Obliczanie prawdopodobieństw dla zmiennych o rozkładzie norm. z parametrami
Statystyka. Rozkład prawdopodobieństwa Testowanie hipotez. Wykład III ( )
 Statystyka Rozkład prawdopodobieństwa Testowanie hipotez Wykład III (04.01.2016) Rozkład t-studenta Rozkład T jest rozkładem pomocniczym we wnioskowaniu statystycznym; stosuje się go wyznaczenia przedziału
Statystyka Rozkład prawdopodobieństwa Testowanie hipotez Wykład III (04.01.2016) Rozkład t-studenta Rozkład T jest rozkładem pomocniczym we wnioskowaniu statystycznym; stosuje się go wyznaczenia przedziału
ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO
 ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO CZĘŚĆ TEORETYCZNA Metody badań i cechy w oparciu o które przeprowadzana jest klasyfikacja i identyfikacja mikroorganizmówh Struktura
ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO CZĘŚĆ TEORETYCZNA Metody badań i cechy w oparciu o które przeprowadzana jest klasyfikacja i identyfikacja mikroorganizmówh Struktura
166 Wstęp do statystyki matematycznej
 166 Wstęp do statystyki matematycznej Etap trzeci realizacji procesu analizy danych statystycznych w zasadzie powinien rozwiązać nasz zasadniczy problem związany z identyfikacją cechy populacji generalnej
166 Wstęp do statystyki matematycznej Etap trzeci realizacji procesu analizy danych statystycznych w zasadzie powinien rozwiązać nasz zasadniczy problem związany z identyfikacją cechy populacji generalnej
Podkowiańska Wyższa Szkoła Medyczna im. Z. i J. Łyko. Syllabus przedmiotowy 2017/ /22 r.
 Podkowiańska Wyższa Szkoła Medyczna im Z i J Łyko Syllabus przedmiotowy 017/18 01/ r Wydział Fizjoterapii Kierunek studiów Fizjoterapia Specjalność ----------- Forma studiów Stacjonarne Stopień studiów
Podkowiańska Wyższa Szkoła Medyczna im Z i J Łyko Syllabus przedmiotowy 017/18 01/ r Wydział Fizjoterapii Kierunek studiów Fizjoterapia Specjalność ----------- Forma studiów Stacjonarne Stopień studiów
Ekologia molekularna. wykład 4
 Ekologia molekularna wykład 4 Zróżnicowanie między populacjami Przyczyny odchyleń od HWE Czynniki demograficzne nielosowe kojarzenie wsobność (inbred) struktura genetyczna populacji (subpopulacje) migracje
Ekologia molekularna wykład 4 Zróżnicowanie między populacjami Przyczyny odchyleń od HWE Czynniki demograficzne nielosowe kojarzenie wsobność (inbred) struktura genetyczna populacji (subpopulacje) migracje
Analiza wariancji. dr Janusz Górczyński
 Analiza wariancji dr Janusz Górczyński Wprowadzenie Powiedzmy, że badamy pewną populację π, w której cecha Y ma rozkład N o średniej m i odchyleniu standardowym σ. Powiedzmy dalej, że istnieje pewien czynnik
Analiza wariancji dr Janusz Górczyński Wprowadzenie Powiedzmy, że badamy pewną populację π, w której cecha Y ma rozkład N o średniej m i odchyleniu standardowym σ. Powiedzmy dalej, że istnieje pewien czynnik
Dziedziczenie poligenowe
 Dziedziczenie poligenowe Dziedziczenie cech ilościowych Dziedziczenie wieloczynnikowe Na wartość cechy wpływa Komponenta genetyczna - wspólne oddziaływanie wielu (najczęściej jest to liczba nieznana) genów,
Dziedziczenie poligenowe Dziedziczenie cech ilościowych Dziedziczenie wieloczynnikowe Na wartość cechy wpływa Komponenta genetyczna - wspólne oddziaływanie wielu (najczęściej jest to liczba nieznana) genów,
STATYSTYKA I DOŚWIADCZALNICTWO. Wykład 2
 STATYSTYKA I DOŚWIADCZALNICTWO Wykład Parametry przedziałowe rozkładów ciągłych określane na podstawie próby (przedziały ufności) Przedział ufności dla średniej s X t( α;n 1),X + t( α;n 1) n s n t (α;
STATYSTYKA I DOŚWIADCZALNICTWO Wykład Parametry przedziałowe rozkładów ciągłych określane na podstawie próby (przedziały ufności) Przedział ufności dla średniej s X t( α;n 1),X + t( α;n 1) n s n t (α;
46 Olimpiada Biologiczna
 46 Olimpiada Biologiczna Pracownia statystyczno-filogenetyczna Łukasz Banasiak i Jakub Baczyński 22 kwietnia 2017 r. Statystyka i filogenetyka / 30 Liczba punktów (wypełnia KGOB) PESEL Imię i nazwisko
46 Olimpiada Biologiczna Pracownia statystyczno-filogenetyczna Łukasz Banasiak i Jakub Baczyński 22 kwietnia 2017 r. Statystyka i filogenetyka / 30 Liczba punktów (wypełnia KGOB) PESEL Imię i nazwisko
Ekologia wyk. 1. wiedza z zakresu zarówno matematyki, biologii, fizyki, chemii, rozumienia modeli matematycznych
 Ekologia wyk. 1 wiedza z zakresu zarówno matematyki, biologii, fizyki, chemii, rozumienia modeli matematycznych Ochrona środowiska Ekologia jako dziedzina nauki jest nauką o zależnościach decydujących
Ekologia wyk. 1 wiedza z zakresu zarówno matematyki, biologii, fizyki, chemii, rozumienia modeli matematycznych Ochrona środowiska Ekologia jako dziedzina nauki jest nauką o zależnościach decydujących
